Спосіб одержання сполук 5-алкокси-4-гідроксиметилпіразолу та сполуки 5-алкокси-4-гідроксиметилпіразолу
Формула / Реферат
1. Спосіб одержання сполуки 5-алкокси-4-гідроксиметилпіразолу, представленої загальною формулою (3)
 , (3)
, (3)
де R1 являє собою алкільну групу, арильну групу, яка може мати замісник, або гетероарильну групу, яка може мати замісник, R2 являє собою електроноакцепторну групу, R3 являє собою алкільну групу, яка може мати замісник, циклоалкільну групу, яка може мати замісник, циклоалкілалкільну групу, яка може мати замісник, алкенільну групу, яка може мати замісник, або алкінільну групу, яка може мати замісник, що включає реакцію сполуки піразолу, представленої загальною формулою (1)
 , (1)
, (1)
де R1 і R2 визначені вище, зі сполукою, представленою загальною формулою (2)
L-R3, (2)
де L являє собою відхідну групу, а R3 визначений вище, у присутності основи і формальдегіду.
2. Спосіб одержання сполуки 5-алкокси-4-гідроксиметилпіразолу за п. 1, у якому відхідна група, представлена L, являє собою атом галогену, алкілсульфонілоксигрупу, галогеналкілсульфонілоксигрупу або бензолсульфонілоксигрупу, яка може мати замісник.
3. Спосіб одержання сполуки 5-алкокси-4-гідроксиметилпіразолу за п. 1 або 2, у якому електроноакцепторна група, представлена R2, являє собою галогеналкільну групу, ціаногрупу або алкоксикарбонільну групу.
4. Спосіб одержання сполуки 5-алкокси-4-гідроксиметилпіразолу за п. 1 або 2, у якому електроноакцепторна група, представлена R2, являє собою (від моно- до трифтор)метильну групу.
5. Спосіб одержання сполуки 5-алкокси-4-гідроксиметилпіразолу за п. 1 або 2, у якому електроноакцепторна група, представлена R2, являє собою трифторметильну групу.
6. Спосіб одержання сполуки 5-алкокси-4-гідроксиметилпіразолу за п. 1 або 2, у якому електроноакцепторна група, представлена R2, являє собою ціаногрупу.
7. Спосіб одержання сполуки 5-алкокси-4-гідроксиметилпіразолу за п. 1 або 2, у якому електроноакцепторна група, представлена R2, являє собою (С1-С6алкокси)карбонільну групу.
8. Спосіб одержання сполуки 5-алкокси-4-гідроксиметилпіразолу за п. 1 або 2, у якому електроноакцепторна група, представлена R2, являє собою етоксикарбонільну групу.
9. Спосіб одержання сполуки 5-алкокси-4-гідроксиметилпіразолу за будь-яким з пп. 1-8, у якому відхідна група, представлена L, являє собою атом галогену.
10. Спосіб одержання сполуки 5-алкокси-4-гідроксиметилпіразолу за будь-яким з пп. 1-9, у якому відхідна група, представлена L, являє собою атом галогену, а R3 являє собою галогеналкільну групу.
11. Спосіб одержання сполуки 5-алкокси-4-гідроксиметилпіразолу за будь-яким з пп. 1-8, у якому відхідна група, представлена L, являє собою атом хлору, а R3 являє собою дифторметильну групу.
12. Спосіб одержання сполуки 5-алкокси-4-гідроксиметилпіразолу за п. 1, у якому R1 являє собою метильну групу, електроноакцепторна група, представлена R2, являє собою трифторметильну групу, а сполука, представлена загальною формулою (2), являє собою хлор(від моно- до тригалогензаміщений)метан.
13. Спосіб одержання сполуки 5-алкокси-4-гідроксиметилпіразолу за п. 1, у якому R1 являє собою метильну групу, електроноакцепторна група, представлена R2, являє собою трифторметильну групу, а сполука, представлена загальною формулою (2), являє собою хлордифторметан.
14. Сполука 5-алкокси-4-гідроксиметилпіразолу, представлена загальною формулою (4)
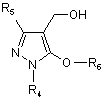 , (4)
, (4)
де R4 являє собою С1-С6алкільну групу, арильну групу, яка може мати замісник, або гетероарильну групу, яка може мати замісник, R5 являє собою С1-С6галогеналкільну групу, ціаногрупу або (С1-С6алкокси)карбонільну групу, a R6 являє собою С1-С6алкільну групу, що є незаміщеною або заміщеною галогеном, фенільною групою, ціаногрупою або (С1-С6алкокси)карбонільною групою, С3-С8циклоалкільну групу, що є незаміщеною або заміщеною галогеном, фенільною групою, ціаногрупою або (С1-С6алкокси)карбонільною групою, C2-С6алкенільну групу, що є незаміщеною або заміщеною галогеном, фенільною групою, ціаногрупою або (С1-С6алкокси)карбонільною групою, або С2-С6алкінільну групу, що є незаміщеною або заміщеною галогеном, фенільною групою, ціаногрупою або (С2-С6алкокси)карбонільною групою.
15. Сполука 5-алкокси-4-гідроксиметилпіразолу за п. 14, де R5 являє собою (від моно- до трифтор)метильну групу.
16. Сполука 5-алкокси-4-гідроксиметилпіразолу за п. 14, де R5 являє собою трифторметильну групу.
17. Сполука 5-алкокси-4-гідроксиметилпіразолу за п. 14, де R5 являє собою ціаногрупу.
18. Сполука 5-алкокси-4-гідроксиметилпіразолу за п. 14, де R5 являє собою (С1-С6алкокси)карбонільну групу.
19. Сполука 5-алкокси-4-гідроксиметилпіразолу за п. 14, де R5 являє собою етоксикарбонільну групу.
20. Сполука 5-алкокси-4-гідроксиметилпіразолу за п. 14, де R4 являє собою метильну групу, R5 являє собою трифторметильну групу, а R6 являє собою (від моно- до тригалогензаміщену)метильну групу.
21. Сполука 5-алкокси-4-гідроксиметилпіразолу за п. 14, де R4 являє собою метильну групу, R5 являє собою трифторметильну групу, а R6 являє собою дифторметильну групу.
Текст
1. Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу, представленої загальною формулою (3) R2 OH C2 2 (19) 1 3 90940 4 собою метильну групу, електроноакцепторна грузаміщеною галогеном, фенільною групою, ціаногпа, представлена R2, являє собою трифторметирупою або (С1-С6алкокси)карбонільною групою, C2льну групу, а сполука, представлена загальною С6алкенільну групу, що є незаміщеною або заміформулою (2), являє собою хлор(від моно- до трищеною галогеном, фенільною групою, ціаногрупою галогензаміщений)метан. або (С1-С6алкокси)карбонільною групою, або С213. Спосіб одержання сполуки 5-алкокси-4С6алкінільну групу, що є незаміщеною або заміщегідроксиметилпіразолу за п. 1, у якому R1 являє ною галогеном, фенільною групою, ціаногрупою собою метильну групу, електроноакцепторна груабо (С2-С6алкокси)карбонільною групою. па, представлена R2, являє собою трифтормети15. Сполука 5-алкокси-4-гідроксиметилпіразолу за льну групу, а сполука, представлена загальною п. 14, де R5 являє собою (від моно- до триформулою (2), являє собою хлордифторметан. фтор)метильну групу. 14. Сполука 5-алкокси-4-гідроксиметилпіразолу, 16. Сполука 5-алкокси-4-гідроксиметилпіразолу за представлена загальною формулою (4) п. 14, де R5 являє собою трифторметильну групу. 17. Сполука 5-алкокси-4-гідроксиметилпіразолу за R5 OH п. 14, де R5 являє собою ціаногрупу. 18. Сполука 5-алкокси-4-гідроксиметилпіразолу за п. 14, де R5 являє собою (С1(4) N С6алкокси)карбонільну групу. O R6 N 19. Сполука 5-алкокси-4-гідроксиметилпіразолу за R4 п. 14, де R5 являє собою етоксикарбонільну групу. , 20. Сполука 5-алкокси-4-гідроксиметилпіразолу за де R4 являє собою С1-С6алкільну групу, арильну п. 14, де R4 являє собою метильну групу, R5 являє групу, яка може мати замісник, або гетероарильну собою трифторметильну групу, а R6 являє собою групу, яка може мати замісник, R5 являє собою С1(від моно- до тригалогензаміщену)метильну групу. С6галогеналкільну групу, ціаногрупу або (С121. Сполука 5-алкокси-4-гідроксиметилпіразолу за С6алкокси)карбонільну групу, a R6 являє собою С1п. 14, де R4 являє собою метильну групу, R5 являє С6алкільну групу, що є незаміщеною або заміщесобою трифторметильну групу, а R6 являє собою ною галогеном, фенільною групою, ціаногрупою дифторметильну групу. або (С1-С6алкокси)карбонільною групою, С3С8циклоалкільну групу, що є незаміщеною або Даний винахід стосується способу одержання сполуки 5-алкокси-4-гідроксиметилпіразолу, який застосовний як проміжний продукт для виробництва медичного і сільськогосподарського хімічного продукту, а також нової сполуки 5-алкокси-4гідроксиметилпіразолу, яку одержують за допомогою зазначеного способу. Сполука 5-алкокси-4-гідроксиметилпіразолу, одержувана за допомогою даного винаходу, застосовна як проміжний продукт для виробництва медичного і сільськогосподарського хімічного продукту. Невідомі способи виробництва сполуки 5алкокси-4-гідроксиметилпіразолу зі сполуки 5гідроксипіразолу в одну стадію. Відомий спосіб відновлення 5-алкокси-4формілпіразолу для одержання сполуки 5-алкокси4-гідроксиметилпіразолу (дивися патентну літературу 1). У даному способі, однак, оскільки для того, щоб одержати сполуку 5-алкокси-4гідроксиметилпіразолу як вихідний матеріал застосовують сполуку 5-гідроксипіразолу, необхідні тристадійні реакції; тому при виробництві передбачуваного продукту виробничий процес і робота були складними, був потрібний тривалий час, а загальний вихід передбачуваного продукту не був задовільним. Патентна література 1: WO 2004-099157 Існує потреба в розробці способу одержання сполуки 5-алкокси-4-гідроксиметилпіразолу, позбавленого вищезгаданих недоліків попереднього рівня техніки, із простими виробничим процесом і роботою і вигідного за часом і виходом. Беручи до уваги вищевказану ситуацію, даний винахідник провів посилене дослідження способу виробництва сполуки 5-алкокси-4гідроксиметилпіразолу. У результаті було виявлено, що сполука 5-алкокси-4-гідроксиметилпіразолу, представлена загальною формулою (3), показаною далі, утворюється шляхом реакції сполуки піразолу, представленої загальною формулою (1), показаною далі, зі сполукою, представленою загальною формулою (2), показаною далі, у присутності основи і формальдегіду. Дане відкриття привело до доробки даного винаходу. Спосіб даного винаходу уможливлює одержання сполуки 5-алкокси-4-гідроксиметилпіразолу, представленої загальною формулою (3), за одну стадію. Даний спосіб простий у виробничому процесі і роботі, вигідний за часом і виходом передбачуваного продукту при виробництві в промисловому масштабі і надзвичайно корисний як промисловий спосіб виробництва сполуки 5алкокси-4-гідроксиметилпіразолу. Даний винахід нижче описаний докладно. Даний винахід вирішує вищевказану задачу шляхом надання винаходів з [1] по [21], показаних нижче. [1] Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу, представленої загальною формулою (3) 5 90940 (де R1 являє собою алкільну групу, арильну групу, яка може мати замісник, або гетероарильну групу, яка може мати замісник, R2 являє собою електроноакцепторну групу, R3 являє собою алкільну групу, яка може мати замісник, циклоалкільну групу, яка може мати замісник, циклоалкілалкільну групу, яка може мати замісник, алкенільну групу, яка може мати замісник, або алкінільну групу, яка може мати замісник), що включає реакцію сполуки піразолу, представленої загальною формулою (1) (де R1 і R2 визначені вище), зі сполукою, представленою загальною формулою (2) L-R3 (2) (де L являє собою відхідну групу, a R3 визначений вище), у присутності основи і формальдегіду. [2] Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу відповідно до [1], у якому відхідна група, представлена L, являє собою атом галогену, алкілсульфонілоксигрупу, галогеналкілсульфонілоксигрупу або бензолсульфонілоксигрупу, яка може мати замісник. [3] Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу відповідно до [1] або [2], у якому електроноакцепторна група, представлена R2, являє собою галогеналкільну групу, ціаногрупу або алкоксикарбонільну групу. [4] Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу відповідно до [1] або [2], у якому електроноакцепторна група, представлена R2, являє собою (від моно- до трифтор)метильну групу. [5] Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу відповідно до [1] або [2], у якому електроноакцепторна група, представлена R2, являє собою трифторметильну групу. [6] Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу відповідно до [1] або [2], у якому електроноакцепторна група, представлена R2, являє собою ціаногрупу. [7] Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу відповідно до [1] або [2], у якому електроноакцепторна група, представлена R2, являє собою (С1-С6алкокси)карбонільну групу. [8] Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу відповідно до [1] або [2], у якому електроноакцепторна група, представлена R2, являє собою етоксикарбонільну групу. [9] Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу відповідно до будь-якого пункту від [1] до [8], у якому відхідна група, представлена L, являє собою атом галогену. 6 [10] Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу відповідно до будь-якого пункту від [1] до [9], у якому відхідна група, представлена L, являє собою атом галогену, a R3 являє собою галогеналкільну групу. [11] Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу відповідно до будь-якого пункту від [1] до [8], у якому відхідна група, представлена L, являє собою атом хлору, a R3 являє собою дифторметильну групу. [12] Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу відповідно до [1], у якому R1 являє собою метильну групу, електроноакцепторна група, представлена R2, являє собою трифторметильну групу, а сполука, представлена загальною формулою (2), являє собою хлор(від моно- до тригалогензаміщений)метан. [13] Спосіб одержання сполуки 5-алкокси-4гідроксиметилпіразолу відповідно до [1], у якому R1 являє собою метильну групу, електроноакцепторна група, представлена R2, являє собою трифторметильну групу, а сполука, представлена загальною формулою (2), являє собою хлордифторметан. [14] Сполука 5-алкокси-4гідроксиметилпіразолу, представлена загальною формулою (4) [де R4 являє собою С1-С6 алкільну групу, арильну групу, яка може мати замісник, або гетероарильну групу, яка може мати замісник, R5 являє собою С1-С6 галогеналкільну групу, ціаногрупу або (С1-С6 алкокси)карбонільну групу, a R6 являє собою С1-С6 алкільну групу, що є незаміщеною або заміщеною галогеном, фенільною групою, ціаногрупою або (С1-С6 алкокси)карбонільною групою, С3-С8 циклоалкільну групу, що є незаміщеною або заміщеною галогеном, фенільною групою, ціаногрупою або (С1-С6 алкокси)карбонільною групою, С2-С6 алкенільну групу, що є незаміщеною або заміщеною галогеном, фенільною групою, ціаногрупою або (С1-С6 алкокси)карбонільною групою, або С2-С6 алкінільну групу, що є незаміщеною або заміщеною галогеном, фенільною групою, ціаногрупою або (С1-С6 алкокси)карбонільною групою]. [15] Сполука 5-алкокси-4гідроксиметилпіразолу відповідно до [14], де R5 являє собою (від моно- до трифтор)метильну групу. [16] Сполука 5-алкокси-4гідроксиметилпіразолу відповідно до [14],де R5 являє собою трифторметильну групу. [17] Сполука 5-алкокси-4гідроксиметилпіразолу відповідно до [14], де R5 являє собою ціаногрупу. [18] Сполука 5-алкокси-4гідроксиметилпіразолу відповідно до [14], де R5 являє собою (С1-С6 алкокси)карбонільну групу. 7 90940 8 [19] Сполука 5-алкокси-4льна група, н-пропільна група, ізопропільна група, гідроксиметилпіразолу відповідно до [14], де R5 н-бутильна група, втор-бутильна група, третявляє собою етоксикарбонільну групу. бутильна група, н-пентильна група, н-гексильна [20] Сполука 5-алкокси-4група і тому подібні; гідроксиметилпіразолу відповідно до [14], де R4 моноциклічні або конденсовані арильні групи, являє собою метильну групу, R5 являє собою тритакі як фенільна група, нафтильна група і тому фторметильну групу, a R6 являє собою (від моноподібні [арильні групи можуть мати, кожна щонайдо тригалогензаміщену)метильну групу. менше один замісник, вибраний з атомів галогенів [21] Сполука 5-алкокси-4(наприклад, брому, хлору, фтору і йоду), С1-С6 гідроксиметилпіразолу відповідно до [14], де R4 алкільних груп з нерозгалуженим ланцюгом або з являє собою метильну групу, R5 являє собою трирозгалуженим ланцюгом (наприклад, метальної фторметильну групу, a R6 являє собою дифтормегрупи, етильної групи, н-пропільної групи, ізопропітильну групу. льної групи, н-бутильної групи, втор-бутильної Дані винаходи з [1] по [21] нижче описані догрупи, трет-бутильної групи, н-пeнтильної групи і нкладно. гeксильної групи), гідроксильної групи, С1-С6 алкоДаний винахід стосується способу одержання ксигруп із нерозгалуженим ланцюгом або з розгасполуки 5-алкокси-4-гідроксиметилпіразолу, предлуженим ланцюгом (наприклад, метоксигрупи, ставленої загальною формулою (3), що включає етоксигрупи, н-пропоксигрупи і ізопропоксигрупи), реакцію сполуки піразолу, представленої загальС1-С6 гідроксіалкільних груп з нерозгалуженим ною формулою (1), зі сполукою, представленою ланцюгом або з розгалуженим ланцюгом (напризагальною формулою (2), у присутності основи і клад, гідроксиметильної групи і 1-гідроксіетильної формальдегіду, а також нового 5-алкокси-4групи), (з нерозгалуженим ланцюгом або з розгагідроксиметилпиразолу, що одержують за допомолуженим ланцюгом С1-С6 алкокси) - (з нерозгалугою зазначеного способу. женим ланцюгом або з розгалуженим ланцюгом У першу чергу, описана сполука піразолу, С1-С6 алкільних) груп (наприклад, метоксиметильпредставлена загальною формулою (1), застосоної групи, 1-метоксіетильної групи і 1вувана в даному винаході як вихідний матеріал. етоксіетильної групи), С1-С6 галогеналкільних груп Сполуку піразолу, представлена загальною з нерозгалуженим ланцюгом або з розгалуженим формулою (1), можна одержати за допомогою різланцюгом (наприклад, фторметильної групи, дифних способів, описаних, наприклад, у "Chemistry of торметильної групи і трифторметильної групи), Heterocyclic Compounds (written by Hiroshi карбоксильної групи, солей металів карбоксильної Yamanaka and others)", Chapter 5, 1988 (Kodansha групи, типовими представниками яких є солі лужScientific); і "Handbook of Heterocyclic Chemistry, них металів (наприклад, сіль натрію, сіль калію і 2nd edition (written by J.A. Joule and K. Mills)", сіль літію) або солі лужноземельних металів (наChapter 4.3.2.3, 2000 (Pergamon). приклад, сіль кальцію, сіль барію і сіль магнію), (з Відомий, наприклад, спосіб, що включає реакнерозгалуженим ланцюгом або з розгалуженим ланцюгом С1-С6алкокси)карбонільних груп (наприцію відповідної сполуки -кетоефіру зі сполукою клад, метоксикарбонільної групи і етоксикарбонігідразину. Конкретно говорячи, у Journal of льної групи), нітрогрупи, аміногрупи, моно- або Heterocyclic Chemistry, Vol. 27, p. 243 (1990) повіді(С1-С6 алкіл)аміногруп із нерозгалуженим ланцюдомлялося, що за допомогою нагрівання зі зворогом або з розгалуженим ланцюгом (наприклад, тним холодильником етил-4,4,4метиламіногрупи, диметиламіногрупи, етиламіногтрифторацетоацетату і метилгідразину у водному рупи і діетиламіногрупи), (з нерозгалуженим ланрозчиннику протягом 2 годин можна синтезувати цюгом або з розгалуженим ланцюгом С1-С6 ал1-метил-5-гідрокси-3-трифторметилпіразол з викіл)карбоніламіногруп (наприклад, ходом 49%. ацетиламіногрупи, пропіоніламіногрупи і бутириТакож описаний, у JP-A-1998-287654, спосіб, ламіногрупи), гідроксикарбоніл(С1-С6 алкільних) що включає реакцію сполуки діефіру щавелевооцгруп з нерозгалуженим ланцюгом або з розгалужетової кислоти зі сполукою гідразину для одержанним ланцюгом (наприклад, гідроксикарбонілметиня сполуки 3-(алкоксикарбоніл)-5-гідроксипіразолу льної групи і 1-гідроксикарбонілетильної групи), (з і спосіб перетворення алкоксикарбонільної групи нерозгалуженим ланцюгом або з розгалуженим сполуки 3-(алкоксикарбоніл)-5-гідроксипіразолу, ланцюгом С1-С6 алкокси)карбоніл-( С1-С6 алкільотриманого за допомогою вищевказаного способу, них) груп (наприклад, метоксикарбонілметильної у ціаногрупу. групи, 1-метоксикарбонілетильної групи і 1Також описаний, у JP-B-1976-33556, спосіб, що етоксикарбонілетильної групи), амінокарбоніл-(С1включає реакцію сполуки -ціанобурштинової кисС6 алкільних) груп з нерозгалуженим ланцюгом лоти зі сполукою солі дізонію для одержання споабо з розгалуженим ланцюгом (наприклад, амінолуки 3-ціано-5-гідроксипіразолу. карбонілметильної групи і 1-амінокарбонілетильної Як приклад замісника R1 загальної формули групи), (з нерозгалуженим ланцюгом або з розга(1), що представляє сполуку піразолу, застосовулуженим ланцюгом С1-С6 алкіл)амінокарбоніл- (з ваного як вихідний матеріал у даному винаході, нерозгалуженим ланцюгом або з розгалуженим можуть служити: ланцюгом С1-С6 алкільних) груп (наприклад, метиалкільні групи, які складаються з 1-6 атомів вуламінокарбонілметильної групи, 1глецю, з нерозгалуженим ланцюгом або з розгаметиламінокарбонілетильної групи і 1луженим ланцюгом (нижче атоми вуглецю, у випаетиламінокарбонілетильної групи), ціаногрупи, і дку, наприклад, 1-6 атомів вуглецю, скорочено т.д.]; і позначають як С1-С6), такі як метильна група, ети 9 90940 10 моноциклічні або конденсовані гетероарильні група (атомна група), що забирає електрон в іншогрупи, які мають щонайменше один гетероатом, го атома або атомної групи реагенту за допомогою вибраний з атома азоту, атома кисню й атома сіріндуктивного ефекту, або арильна група, заміщена ки, такі як піридильна група, тієнільна група, оксаатомною групою, що забирає електрон в іншого золільна група, тіазолільна група, ізоксазолільна атома або атомної групи реагенту за допомогою група і тому подібні [гетероарильні групи можуть індуктивного ефекту. Як конкретні приклади електмати, кожна, щонайменше один замісник, вибрароноакцепторної групи можуть бути згадані С1-С6 ний з С1-С6 алкільних груп з нерозгалуженим лангалогеналкільні групи з нерозгалуженим ланцюгом цюгом або з розгалуженим ланцюгом (наприклад, або з розгалуженим ланцюгом, такі як дифтормеметальної групи, етильної групи, н-пропільної грутильна група, трифторметильна група і тому подіпи, ізопропільної групи, н-бутильної групи, вторбні; карбоксильна група; солі металів карбоксильбутильної групи, трет-бутильної групи, нної групи, типовими представниками яких є солі пентильної групи і н-гексильної групи), гідроксильлужних металів, такі як сіль натрію, сіль калію, сіль ної групи, С1-С6 алкоксигруп із нерозгалуженим літію і тому подібні, і солі лужноземельних металів, ланцюгом або з розгалуженим ланцюгом (напритакі як сіль кальцію, сіль барію, сіль магнію і тому клад, метоксигрупи, етоксигрупи, н-пропоксигрупи і подібні; (з нерозгалуженим ланцюгом або з розгаізопропоксигрупи), С1-С6 гідроксіалкільних груп з луженим ланцюгом С1-С6 алкокси)карбонільні грунерозгалуженим ланцюгом або з розгалуженим пи, такі як метоксикарбонільна група, етоксикарланцюгом (наприклад, гідроксиметильної групи і бонільна група і тому подібні; атоми галогенів, такі гідроксіетильної групи), (з нерозгалуженим ланцюяк бром, хлор, фтор, йод і тому подібні; нітрогрупа; гом або з розгалуженим ланцюгом С1-С6 алкокси)формільна група; (з нерозгалуженим ланцюгом (з нерозгалуженим ланцюгом або з розгалуженим або з розгалуженим ланцюгом С1-С6 алланцюгом С1-С6 алкільних) груп (наприклад, метокіл)карбонільні групи, такі як метилкарбонільна ксиметильної групи, метоксіетильної групи і етокгрупа, етилкарбонільна група і тому подібні; арилсіетильної групи), С1-С6 галогеналкільних груп з карбонільні групи, такі як бензоїльна група, нафтонерозгалуженим ланцюгом або з розгалуженим їльна група і тому подібні; моноциклічні або конланцюгом (наприклад, фторметильної групи, дифденсовані гетероарилкарбонільні групи, що мають торметильної групи і трифторметильної групи), від одного до чотирьох гетероатомів, вибраних з карбоксильної групи, солей металів карбоксильної атома азоту, атома кисню й атома сірки, такі як групи, типовими представниками яких є солі лужпіридилкарбонільна група, тієнілкарбонільна група, них металів (наприклад, сіль натрію, сіль калію і фурилкарбонільна група і тому подібні; амінокарсіль літію) або солі лужноземельних металів (набонільна група; моно- або ді(з нерозгалуженим приклад, сіль кальцію, сіль барію і сіль магнію), (з ланцюгом або з розгалуженим ланцюгом С1-С6 нерозгалуженим ланцюгом або з розгалуженим алкіл)амінокарбонільні групи, такі як метиламіноланцюгом С1-С6 алкокси)карбонільних груп (наприкарбонільна група і диметиламінокарбонільна груклад, метоксикарбонільної групи і етоксикарбоніпа і тому подібні; і ціаногрупа. льної групи), атомів галогенів (наприклад, брому, Тому як конкретні приклади сполуки піразолу, хлору, фтору і йоду), нітрогрупи, аміногрупи, монопредставленої загальною формулою (1), можуть або ді(С1-С6 алкіл)аміногруп із нерозгалуженим бути згадані 5-гідрокси-1-метил-3ланцюгом або з розгалуженим ланцюгом (напритрифторметилпіразол, 3-етоксикарбоніл-5клад, метиламіногрупи, диметиламіногрупи, етигідрокси-1-метилпіразол, 3-хлор-5-гідрокси-1ламіногрупи і діетиламіногрупи), (з нерозгалужеметилпіразол, 5-гідрокси-1-метил-3-нітропіразол, ним ланцюгом або з розгалуженим ланцюгом С15-гідрокси-1-метил-3-(2-тіофенкарбоніл)піразол, 5С6 алкіл) карбоніламіногруп (наприклад, ацетилагідрокси-1-метил-3-(3-піридилкарбоніл)піразол, 3міногрупи, пропіоніламіногрупи і бутириламіногрудиметиламінокарбоніл-5-гідрокси-1-метилпіразол, пи), ціаногрупи, формільної групи, (з нерозгалуже3-(4-диметиламінокарбоніл)-5-гідрокси-1ним ланцюгом або з розгалуженим ланцюгом С1метилфенілпіразол, 5-гідрокси-1-н-пропіл-3С6 алкіл) карбонільних груп (наприклад, метилкартрифторметилпіразол, 3-ціано-1-н-гексил-5бонільної групи і етилкарбонільної групи), арилкагідроксипіразол, 1-трет-бутил-5-гідрокси-3рбонільних груп (наприклад, бензоїльної групи і трифторметилпіразол, 5-гідрокси-1-феніл-3нафтоїльної групи), і т.д.]. Як приклад замісника R1 трифторметилпіразол, 3-ціано-5-гідрокси-1можуть, крім того, служити: фенілпіразол, 1-(4-хлорфеніл)-3-етоксикарбоніл-5арильні групи, що мають щонайменше один гідроксипіразол, 3-етоксикарбоніл-5-гідрокси-1-(2замісник, вибраний з (арил у вищевказаному знаметилфеніл)піразол, 3-етоксикарбоніл-5-гідроксиченні) - карбонільних груп (наприклад, бензоїльної 1-(2-метоксиметилфеніл)піразол, 1-(4групи і нафтоїльної групи), (гетероарил у вищевкаацетилфеніл)-3-етоксикарбоніл-5-гідроксипіразол, заному значенні) - карбонільних груп (наприклад, 3-етоксикарбоніл-5-гідрокси-1-(3піридилкарбонільної групи, тієнілкарбонільної грунітрофеніл)піразол, 5-гідрокси-1-(2-метоксифеніл)пи і фурилкарбонільної групи), і т.д.; і 3-трифторметилпіразол, 5-гідрокси-3гетероарильні групи, що мають щонайменше трифторметил-1-(4-трифторметилфеніл)піразол, один замісник, вибраний з (гетероарил у вищевка1-(4-етоксикарбонілфеніл)-5-гідрокси-3заному значенні) - карбонільних груп (наприклад, трифторметилпіразол, 1-(4-диметиламінофеніл)-5піридилкарбонільної групи, тієнілкарбонільної гругідрокси-3-трифторметилпіразол, 1-(4пи і фурилкарбонільної групи), і т.д. ацетиламінофеніл)-5-гідрокси-3Під електроноакцепторною групою, представтрифторметилпіразол, 1-(4леною R2, загальної формули (1) мається на увазі метоксикарбонілметилфеніл)-5-гідрокси-3 11 90940 12 трифторметилпіразол, 1-(4па, 1-етил-1-метил-2-пропенільна група, 1-етил-2диметиламінокарбонілметилфеніл)-5-гідрокси-3метил-2-пропенільна група, 1-ізопропіл-2трифторметилпіразол, 1-(4-ціанофеніл)-5-гідроксипропенільна група, 2-метил-2-пентенільна група, 3-трифторметилпіразол, 1-(2-нафтил)-5-гідрокси-33-метил-3-пентенільна група, 4-метил-3трифторметилпіразол, 1-(2-бензотиазоліл)-5пентенільна група, 1,3-диметил-2-бутенільна гругідрокси-3-трифторметилпіразол, 5-гідрокси-1-(2па, 1,1-диметил-2-бутенільна група, 3-метил-4піридил)-3-трифторметилпіразол, і 5-гідрокси-1-(2пентенільна група, 4-метил-4-пентенільна група, пиримидил)-3-трифторметилпіразол. 1,2-диметил-3-бутенільна група, 1,3-диметил-3Потім описана сполука, представлена загальбутенільна група, 1,1,2-триметил-2-пропенільна ною формулою (2). група, 1,5-гексадієнільна група, 1-вініл-3Як приклад замісника R3 загальної формули бутенільна група, 2,4-гексадієнільна група і тому (2) можуть служити подібні; і С1-С6 алкільні групи з нерозгалуженим ланцюС2-С6 алкінільні групи з нерозгалуженим лангом або з розгалуженим ланцюгом, такі як метильцюгом або з розгалуженим ланцюгом, такі як етина група, етильна група, н-пропільна група, ізопронільна група, 1-пропінільна група, 2-пропінільна пільна група, н-бутильна група, втор-бутильна група, 1-бутинільна група, 1-метил-2-пропінільна група, ізобутил, трет-бутильна група, н-пентильна група, 2-бутинільна група, 3-бутинільна група, 1група, 1-метилбутильна група, 2-метилбутильна пентинільна група, 1-етил-2-пропінільна група, 2група, 3-метилбутильна група, 1-етилпропільна пентинільна група, 3-пентинільна група, 1-метил-2група, 1,1-диметилпропільна група, 1,2бутинільна група, 4-пентинільна група, 1-метил-3диметилпропільна група, неопентильна група, нбутинільна група, 2-метил-3-бутинільна група, 1гексильна група, 1-метилпентильна група, 2гексинільна група, 1-(н-пропіл)-2-пропінільна група, метилпентильна група, 1-етилбутильна група, 22-гексинільна група, 1-етил-2-бутинільна група, 3етилбутильна група, 1,1-диметилбутильна група, гексинільна група, 1-метил-2-пентинільна група, 11,2-диметилбутильна група, 1,3-диметилбутильна метил-3-пентинільна група, 4-метил-1-пентинільна група, 2,2-диметилбутильна група, 2,3група, 3-метил-1-пентинільна група, 5-гексинільна диметилбутильна група, 3,3-диметилбутильна гругрупа, 1-етил-3-бутинільна група, 1-етил-1-метилпа, 1,1,2-триметилпропільна група, 1,2,22-пропінільна група, 1,1-диметил-2-бутинільна грутриметилпропільна група, 1-етил-1па, 2,2-диметил-3-бутинільна група і тому подібні. метилпропільна група, 1-етил-2-метилпропільна Кожна з вищезгаданих С1-С6 алкільних груп з група і тому подібні; нерозгалуженим ланцюгом або з розгалуженим С3-С8 циклоалкільні групи, такі як циклопропіланцюгом, С3-С6 циклоалкільних груп, С4-С8 цикльна група, циклобутильна група, циклопентильна лоалкілалкільних груп, С2-С6 алкенільних груп з група, циклогексильна група, циклогептильна грунерозгалуженим ланцюгом або з розгалуженим па, циклооктильна група і тому подібні; ланцюгом і С2-С6 алкінільних груп з нерозгалужеC4-C8 циклоалкілалкільні групи, такі як циклопним ланцюгом або з розгалуженим ланцюгом може ропілметильна група, 1-циклопропілетильна група, мати щонайменше один замісник, вибраний з 2-циклопропілетильна група, 1атомів галогенів, таких як бром, хлор, фтор, циклопропілпропільна група, 2йод і тому подібних; циклопропілпропільна група, 3С1-С6 алкоксигруп із нерозгалуженим ланцюциклопропілпропільна група, циклобутилметильна гом або з розгалуженим ланцюгом, таких як метокгрупа, циклопентилметильна група, циклогексилсигрупа, етоксигрупа, н-пропоксигрупа, ізопропокметильна група і тому подібні; сигрупа, бутоксигрупа, пентилоксигрупа, С2-С6 алкенільні групи з нерозгалуженим лангексилоксигрупа і тому подібні; цюгом або з розгалуженим ланцюгом, такі як вініС1-С6 гідроксіалкільних груп з нерозгалуженим льна група, 1-пропенільна група, ізопропенільна ланцюгом або з розгалуженим ланцюгом, таких як група, 2-пропенільна група, 1-бутенільна група, 1гідроксиметильна група, 1-гідроксіетильна група і метил-1-пропенільна група, 2-бутенільна група, 1тому подібні; метил-2-пропенільна група, 3-бутенільна група, 2(з нерозгалуженим ланцюгом або з розгалужеметил-1-пропенільна група, 1,3-бутадієнільна груним ланцюгом С1-С6 алкокси)-(з нерозгалуженим па, 1-пентенільна група, 1-етил-2-пропенільна груланцюгом або з розгалуженим ланцюгом С1-С6 па, 2-пентенільна група, 1-метил-1-бутенільна груалкільних) груп, таких як метоксиметильна група, па, 3-пентенільна група, 1-метил-2-бутенільна етоксіетильна група, 1-метоксіетильна група, 1група, 4-пентенільна група, 1-метил-3-бутенільна метоксипропільна група, 1-метоксибутильна група, група, 3-метил-1-бутенільна група, 1,2-диметил-21-етоксіетильна група, 1-етоксипропільна група, 1пропенільна група, 1,1-диметил-2-пропенільна етоксибутильна група, 1-метокси-2група, 2-метил-2-бутенільна група, 3-метил-2метилпропільна група і тому подібні; бутенільна група, 1,2-диметил-1-пропенільна груС1-С6 галогеналкільних груп з нерозгалуженим па, 2-метил-3-бутенільна група, 3-метил-3ланцюгом або з розгалуженим ланцюгом, таких як бутенільна група, 1,3-пентадієнільна група, 1-вінілфторметильна група, хлорметильна група, бром2-пропенільна група, 1-гексенільна група, 1-пропілметильна група, дифторметильна група, дихлор2-пропенільна група, 2-гексенільна група, 1-метилметильна група, дибромметильна група, трифтор1-пентенільна група, 1-етил-2-бутенільна група, 3метильна група, трихлорметильна група, хлор гексенільна група, 4-гексенільна група, 5дифторметильна група, бромди фторметильна гексенільна група, 1-метил-4-пентенільна група, 1група, 2-фторетильна група, 1-хлоретильна група, етил-3-бутенільна група, 1-(ізобутил)вінільна гру2-хлоретильна група, 1-брометильна група, 2 13 90940 14 брометильна група, 2,2-дифторетильна група, 1,2ких як метилкарбонільна група, етилкарбонільна дихлоретильна група, 2,2-дихлоретильна група, група, н-пропілкарбонільна група, ізопропілкарбо2,2,2-трифторетильна група, 2,2,2-трихлоретильна нільна група, трет-бутилкарбонільна група і тому група, 1,1,2,2-тетрафторетильна група, пентафтоподібні; ретильна група, 2-бром-2-хлоретильна група, 2моноциклічних або конденсованих арильних хлор-1,1,2,2-тетрафторетильна група, 1-хлоргруп, що можуть мати замісник, таких як фенільна 1,2,2,2-тетрафторетильна група, 1-хлорпропільнагрупа, нафтильна група і тому подібні; група, 2-хлорпропільна група, 3-хлорпропільна моноциклічних або конденсованих гетероаригрупа, 1-бромпропільна група, 2-бромпропільна льних груп, що можуть мати замісник, що мають група, 3-бромпропільна група, 2-бром-1від одного до чотирьох гетероатомів, вибраних з метилетильна група, 3-йодпропільна група, 2,3атома азоту, атома кисню й атома сірки, типовими дихлорпропільна група, 2,3-дибромпропільна групредставниками яких є піридильна група, тієнільна па, 3,3,3-трифторпропільна група, 3,3,3група, оксазолільна група, тиазолільна група, ізоктрихлорпропільна група, 3-бром-3,3сазолільна група, і т.д.; дифторпропільна група, 3,3-дихлор-3арилкарбонільних груп, таких як бензоїльна фторпропільна група, 2,2,3,3-тетрафторпропільна група, нафтоїльна група і тому подібні; група, 1-бром-3,3,3-трифторпропільна група, моноциклічних або конденсованих гетероари2,2,3,3,3-пентафторпропільна група, 2,2,2лкарбонільних груп, що мають від одного до чотитрифтор-1-трифторметилетильна група, гептафрьох гетероатомів, вибраних з атома азоту, атома торпропільна група, 1,2,2,2-тетрафтор-1кисню й атома сірки, таких як піридилкарбонільна трифторметилетильна група, 2,3-дихлор-1,1,2,3,3група, тієнілкарбонільна група, фурилкарбонільна пентафторпропільна група, 2-хлорбутильна група, група і тому подібні; 3-хлорбутильна група, 4-хлорбутильна група, 2і так далі. хлор-1,1-диметилетильна група, 4-бромбутильна L загальної формули (2) являє собою відхідну група, 3-бром-2-метилпропільна група, 2-бром-1,1групу, і може являти собою будь-який атом або диметилетильна група, 2,2-дихлор-1,1атомну групу, якщо тільки він виконує роль відхіддиметилетильна група, 2-хлор-1-хлорметил-2ної групи у даній реакції. Якості її конкретні прикметилетильна група, 4,4,4-трифторбутильна група, лади можуть бути згадані 3,3,3-трифтор-1-метилпропільна група, 3,3,3атоми галогенів, таких як хлор, бром, йод і тотрифтор-2-метилпропільна група, 2,3,4му подібні; трихлорбутильна група, 2,2,2-трихлор-1,1алкілсульфонілоксигрупи, такі як метансульдиметилетильна група, 4-хлор-4,4фонілоксигрупа, дифторбутильна група, 4,4-дихлор-4етансульфонілоксигрупа і тому подібні; фторбутильна група, 4-бром-4,4-дифторбутильна галогеналкілсульфонілоксигрупи, такі як дифгрупа, 2,4-дибром-4,4-дифторбутильна група, 3,4торметансульфонілоксигрупа, трифторметансудихлор-3,4,4-трифторбутильна група, 3,3-дихлорльфонілоксигрупа і тому подібні; і 4,4,4-трифторбутильна група, 4-бром-3,3,4,4бензолсульфонілоксигрупи, що можуть мати тетрафторбутильна група, 4-бром-3-хлор-3,4,4як замісник атом галогену або алкільну групу, такі трифторбутильна група, 2,2,3,3,4,4як бензолсульфонілоксигрупа, 4гексафторбутильна група, 2,2,3,4,4,4хлорбензолсульфонілоксигрупа, 4гексафторбутильна група, 2,2,2-трифтор-1-метилметилбензолсульфонілоксигрупа і тому подібні. 1-трифторметилетильна група, 3,3,3-трифтор-2Тому як конкретні приклади сполуки, предстатрифторметилпропільна група, 2,2,3,3,4,4,4вленої загальною формулою (2), можуть бути згагептафторбутильна група, 2,3,3,3-тетрафтор-2дані метилхлорид, метилбромід, метилйодид, дитрифторметилпропільна група, 1,1,2,2,3,3,4,4метилсульфат, етилбромід, етилйодид, октафторбутильна група, нонафторбутильна грудіетилсульфат, н-пропілйодид, ізопропілбромід, нпа, 4-хлор-1,1,2,2,3,3,4,4-октафторбутильна група, бутилбромід, втор-бутилйодид, ізобутилйодид, 5-фторпентильна група, 5-хлорпентильна група, трет-бутилйодид, 1-метилбутилбромід, 25,5-дифторпентильна група, 5,5-дихлорпентильна метилбутилйодид, 1-етилпропілбромід, 1,1група, 5,5,5-трифторпентильна група, 6,6,6диметилпропілбромід, н-гексилйодид, 1трифторгексильна група, 5,5,5,6,6,6метилпентилйодид, 2-етилбутилйодид, 1,1гексафторгексильна група і тому подібні; диметилбутилйодид, 1,2-диметилбутилйодид, 1,3карбоксильної групи; диметилбутилйодид, 3,3-диметилбутилйодид, солей металів карбоксильної групи, типовими 1,1,2-триметилпропілйодид, циклопропілметилйопредставниками яких є солі лужних металів, такі як дид, 2-циклопропілпропілйодид, циклопентилмесіль натрію, сіль калію, сіль літію і тому подібні, тилбромід, циклопропілбромід, циклопентилброабо солі лужноземельних металів, такі як сіль камід, циклогексилбромід, вінілбромід, льцію, сіль барію, сіль магнію і тому подібні; ізопропенілбромід, 1-метил-1-пропенілбромід, 1(з нерозгалуженим ланцюгом або з розгалужеметил-3-бутенілбромід, 1-гексенілйодид, 1-етил-3ним ланцюгом С1-С6 алкокси)карбонільних груп, бутенілбромід, 1,1,2-триметил-2-пропенілбромід, таких як метоксикарбонільна група, етоксикарбоніетинілбромід, пропаргилбромід, 4-пентинілйодид, льна група, н-пропоксикарбонільна група, ізопро2-гексинілйодид, 1-етил-2-бутенілбромід, 2поксикарбонільна група, трет-бутоксикарбонільна брометанол, 4-бром-н-бутанол, 1-бром-2-бутанол, група і тому подібні; хлорфторметан, хлордифторметан, 2,2,2(з нерозгалуженим ланцюгом або з розгалужетрифторброметан, 1,1,2,2-тетрафторброметан, ним ланцюгом С1-С6 алкіл)карбонільних груп, та3,3,3-трифторпропілйодид, 3,3,3 15 90940 16 трифторпропілбромід, 1,1,2,2,3,3,4,4,4задовільне протікання даної реакції. Однак кільнонафторбутилбромід, 5,5,6,6,6кість складає, наприклад, від 1,0 до 20молів, перепентафторгексилбромід, метоксиметилбромід, важно від 3,0 до 10молів на 1моль сполуки піразоетоксиметилбромід, ізопропоксиметилйодид, хлолу (вихідна сполука), представленої загальною роцтова кислота, бромоцтова кислота, етилброформулою (1). мацетат, н-пропілбромацетат, ізобутилбромацеРозчинник, який використовується у даній реакції, може являти собою будь-який розчинник, яктат, бромацетон, йодацетон, -хлорацетофенон, що тільки він не заважає реакції. Можуть бути згабензилбромід, 2-бромметилнафталін, 2дані, наприклад, вода; спирти, такі як метанол, хлорметилпіридин, 2-бромметилфуран, петанол і тому подібні; ароматичні вуглеводні, такі толуолсульфонілметилпіран і 2-бромметилтіофен. як толуол, ксилол, хлорбензол і тому подібні; галоПотім описаний спосіб виробництва сполуки 5геновані аліфатичні вуглеводні, такі як дихлормеалкокси-4-гідроксиметилпіразолу, представленої тан, хлороформ і тому подібні; апротонні полярні загальною формулою (3), що включає реакцію розчинники, такі як диметилформамід (ДМФА), сполуки піразолу, представленої загальною фордиметилацетамід, N-метилпіролідон, тетраметилмулою (1), зі сполукою, представленою загальною сечовина, гексаметилфосфортриамід (ГМФА), формулою (2). пропіленкарбонат і тому подібні; ефірні розчинниФормальдегід, використовуваний у реакції, ки, такі як діетиловий ефір, тетрагідрофуран, діокможе бути в будь-якій формі. Однак для простого сан і тому подібні; і аліфатичні вуглеводні, такі як процесу переважно використовувати 35-50%-ний пентан, н-гексан і тому подібні. Вода, спирт або водний розчин формальдегіду, типовим представапротонний полярний розчинник переважні з погником якого є 35%-ний формалін (який вільно досляду розчинності основи і реактивності, і вода або тупний як комерційний продукт), або використовудиметилформамід (ДМФА) особливо переважні. вати параформальдегід (що являє собою полімер Розчинники можна застосовувати окремо або у формальдегіду, при гідролізі утворюючий формавигляді змішаного розчинника з будь-яким співвідльдегід у реакційній системі; тому його можна виношенням компонентів. користовувати як еквівалент формальдегіду). Використовувана кількість розчинника може Використовувана кількість формальдегіду мобути будь-якою кількістю, якщо тільки вона уможже являти собою кількість, яка щонайменше доріливлює задовільне перемішування реакційної сисвнює еквіваленту сполуки піразолу, представленої теми. Однак вона звичайно складає від 0,05 до 10 загальною формулою (1). Однак звичайно вона літрів, переважно від 0,5 до 2 літрів на 1моль споможе складати від 1,0 до 5,0 еквівалентів, перевалуки піразолу (вихідна сполука), представленої жно від 1,0 до 3,0 еквівалентів стосовно 1моля загальною формулою (1). сполуки піразолу, представленої загальною форТемпература реакції може складати, напримулою (1). клад, від 0°С до температури кипіння використовуВикористовувана кількість сполуки, представваного розчинника. Однак переважно реакцію проленої загальною формулою (2), може являти соводять при 20-50°С, а перемішування при бою кількість, яка щонайменше дорівнює еквівакімнатній температурі особливо переважно, оскіленту сполуки піразолу, представленої загальною льки воно є простим і дає гарний вихід. формулою (1). Однак звичайно вона може складаЩо стосується часу реакції, конкретні обмети від 1,0 до 10,0 еквівалентів, переважно від 1,0 ження відсутні. Однак звичайна реакція завершудо 3,0 еквівалентів стосовно 1моля сполуки пірається за 1-24 години. золу, представленої загальною формулою (1). У даній реакції сполуку 5-алкокси-4Як основа, застосовувана в даному винаході, гідроксиметилпіразолу, представлену загальною можуть бути згадані неорганічні основи, типовими формулою (3), можна одержувати з гарним вихопредставниками яких є гідриди лужних металів дом при простому процесі і м'яких умовах. Отри(наприклад, гідрид натрію, гідрид калію і гідрид мана сполука 5-алкокси-4-гідроксиметилпіразолу, літію), лужні метали (наприклад, металевий натрій, представлена загальною формулою (3), застосовметалевий калій і металевий літій), гідроксиди луна як проміжний продукт для виробництва медичжних металів (наприклад, гідроксид натрію, гідрокного, сільськогосподарського хімічного продукту, і сид калію і гідроксид літію), гідроксиди лужноземет.д. льних металів (наприклад, гідроксид барію, Потім описана дана сполука з [14] до [21]. гідроксид магнію і гідроксид кальцію), карбонати Сполука даного винаходу представлена загалужних металів (наприклад, карбонат натрію, карльною формулою (4) бонат калію, гідрокарбонат натрію і гідрокарбонат калію), оксиди лужноземельних металів (наприклад, оксид барію, оксид магнію й оксид кальцію) і т.д.; і органічні основи, типовими представниками яких є алкоксиди металів (наприклад, метоксид натрію, етоксид натрію, метоксид калію, етоксид калію і трет-бутоксид калію), і алкілметал, такий як н-бутиллітій і т.д. Однак переважним є гідроксид [де R4 являє собою С1-С6 алкільну групу, арилужного металу або карбонат лужного металу, і льну групу, яка може мати замісник, або гетероаособливо переважним є гідроксид натрію, гідрокрильну групу, яка може мати замісник, R5 являє сид калію або карбонат калію. собою С1-С6 галогеналкільну групу, ціаногрупу або Використовувана кількість основи може бути (С1-С6 алкокси)карбонільну групу, a R6 являє собудь-якою кількістю, якщо тільки вона уможливлює 17 90940 18 бою С1-С6 алкільну групу, що є незаміщеною або метилпропільна група, 1-етил-2-метилпропільна заміщеною галогеном, фенільною групою, ціаноггрупа і тому подібні; рупою або (С1-С6 алкокси)карбонільною групою, С3-С8 циклоалкільні групи, такі як циклопропіС3-С8 циклоалкільну групу, що є незаміщеною або льна група, циклобутильна група, циклопентильна заміщеною галогеном, фенільною групою, ціаноггрупа, циклогексильна група, циклогептильна грурупою або (С1-С6 алкокси)карбонільною групою, па, циклооктильна група і тому подібні; С1-С6 алкенільну групу, що є незаміщеною або С2-С6 алкенільні групи з нерозгалуженим ланзаміщеною галогеном, фенільною групою, ціаногцюгом або з розгалуженим ланцюгом, такі як вінірупою або (С1-С6 алкокси)карбонільною групою, льна група, 1-пропенільна група, ізопропенільна або С2-С6 алкінільну групу, що є незаміщеною або група, 2-пропенільна група, 1-бутенільна група, 1заміщеною галогеном, фенільною групою, ціаногметил-1-пропенільна група, 2-бутенільна група, 1рупою або (С1-С6 алкокси)карбонільною групою]. метил-2-пропенільна група, 3-бутенільна група, 2Як приклад замісника R4 загальні формули (4) метил-1-пропенільна група, 1,3-бутадієнільна груможуть служити: па, 1-пентенільна група, 1-етил-2-пропенільна груС1-С6 алкільні групи з нерозгалуженим ланцюпа, 2-пентенільна група, 1-метил-1-бутенільна гругом або з розгалуженим ланцюгом, такі як метильпа, 3-пентенільна група, 1-метил-2-бутенільна на група, етильна група, н-пропільна група, ізопрогрупа, 4-пентенільна група, 1-метил-3-бутенільна пільна група і тому подібні; група, 3-метил-1-бутенільна група, 1,2-диметил-2арильні групи, які можуть мати замісник, що пропенільна група, 1,1-диметил-2-пропенільна має те ж значення, що і замісник R1; і група, 2-метил-2-бутенільна група, 3-метил-2гетероарильні групи, які можуть мати замісник, бутенільна група, 1,2-диметил-1-пропенільна грущо має те ж значення, що і замісник R1. па, 2-метил-3-бутенільна група, 3-метил-3R5 загальної формули (4), зокрема, включає: бутенільна група, 1,3-пентадієнільна група, 1-вінілС1-С6 галогеналкільні групи з нерозгалуженим 2-пропенільна група, 1-гексенільна група, 1-пропілланцюгом або з розгалуженим ланцюгом, типови2-пропенільна група, 2-гексенільна група, 1-метилми представниками яких є С1-С6 фторалкільні гру1-пентенільна група, 1-етил-2-бутенільна група, 3пи з нерозгалуженим ланцюгом або з розгалужегексенільна група, 4-гексенільна група, 5ним ланцюгом, такі як дифторметильна група, гексенільна група, 1-метил-4-пентенільна група, 1трифторметильна група, 1,2-дифторетильна група, етил-3-бутенільна група, 1-(ізобутил)вінільна гру2,2-дифторетильна група, 2,2,2-трифторетильна па, 1-етил-1-метил-2-пропенільна група, 1-етил-2група, 1,1,2,2-тетрафторетильна група, пентафтометил-2-пропенільна група, 1-ізопропіл-2ретильна група, 3,3,3-трифторпропільна група, пропенільна група, 2-метил-2-пентенільна група, 2,2,3,3-тетрафторпропільна група, 1,1,3,3,33-метил-3-пентенільна група, 4-метил-3пентафторпропільна група, 2,2,2-трифтор-1пентенільна група, 1,3-диметил-2-бутенільна грутрифторметилетильна група, гептафторпропільна па, 1,1-диметил-2-бутенільна група, 3-метил-4група і тому подібні; пентенільна група, 4-метил-4-пентенільна група, ціаногрупу; і 1,2-диметил-3-бутенільна група, 1,3-диметил-3(з нерозгалуженим ланцюгом або з розгалужебутенільна група, 1,1,2-триметил-2-пропенільна ним ланцюгом С1-С6 алкокси)карбонільні групи, група, 1,5-гексадієнільна група, 1-вініл-3такі як метоксикарбонільна група, етоксикарбонібутенільна група, 2,4-гексадієнільна група і тому льна група, н-пропоксикарбонільна група, ізопроподібні; і поксикарбонільна група, н-бутоксикарбонільна С2-С6 алкінільні групи з нерозгалуженим лангрупа, 2-бутоксикарбонільна група, ізобутоксикарцюгом або з розгалуженим ланцюгом, такі як етибонільна група, н-пентилоксикарбонільна група, нільна група, 1-пропінільна група, 2-пропінільна неопентилоксикарбонільна група, нгрупа, 1-бутинільна група, 1-метил-2-пропінільна гексилоксикарбонільна група, 2група, 2-бутинільна група, 3-бутинільна група, 1метилпентилоксикарбонільна група, 2пентинільна група, 1-етил-2-пропінільна група, 2етилбутоксикарбонільна група і тому подібні. пентинільна група, 3-пентинільна група, 1-метил-2Як приклад замісника R6 можуть служити: бутинільна група, 4-пентинільна група, 1-метил-3С1-С6 алкільні групи з нерозгалуженим ланцюбутинільна група, 2-метил-3-бутинільна група, 1гом або з розгалуженим ланцюгом, такі як метильгексинільна група, 1-(н-пропіл)-2-пропінільна група, на група, етильна група, н-пропільна група, ізопро2-гексинільна група, 1-етил-2-бутинільна група, 3пільна група, н-бутильна група, втор-бутильна гексинільна група, 1-метил-2-пентинільна група, 1група, ізобутильна група, трет-бутильна група, нметил-3-пентинільна група, 4-метил-1-пентинільна пентильна група, 1-метилбутильна група, 2група, 3-метил-1-пентинільна група, 5-гексинільна метилбутильна група, 3-метилбутильна група, 1група, 1-етил-3-бутинільна група, 1-етил-1-метилетилпропільна група, 1,1-диметилпропільна група, 2-пропінільна група, 1,1-диметил-2-бутинільна гру1,2-диметилпропільна група, неопентильна група, па, 2,2-диметил-3-бутинільна група і тому подібні. н-гексильна група, 1-метилпентильна група, 2Кожна з С1-С6 алкільних груп з нерозгалужеметилпентильна група, 1-етилбутильна група, 2ним ланцюгом або з розгалуженим ланцюгом, С3етилбутильна група, 1,1-диметилбутильна група, С8 циклоалкільних груп, С2-С6 алкенільних груп з 1,2-диметилбутильна група, 1,3-диметилбутильна нерозгалуженим ланцюгом або з розгалуженим група, 2,2-диметилбутильна група, 2,3ланцюгом і С2-С6 алкінільних груп з нерозгалужедиметилбутильна група, 3,3-диметилбутильна груним ланцюгом або з розгалуженим ланцюгом, па, 1,1,2-триметилпропільна група, 1,2,2представлених R6, може мати щонайменше один триметилпропільна група, 1-етил-1замісник, вибраний з атомів галогенів (наприклад, 19 90940 20 брому, хлору, фтору і йоду), фенільної групи, ціагідроксиметилпіразолу, представлена загальною ногрупи і (з нерозгалуженим ланцюгом або з розформулою (4), даного винаходу не обмежена дагалуженим ланцюгом С1-С6 алкокси)карбонільних ними прикладами. На номер кожної сполуки дагруп (наприклад, метоксикарбонільної групи, етокються посилання в наступному описі. сикарбонільної групи, н-пропоксикарбонільної груУ даному випадку, скорочення, використані в пи, ізопропоксикарбонільної групи, нтаблиці 1 і таблиці 2, мають наступні значення. бутоксикарбонільної групи, 2-бутоксикарбонільної Me: метильна група групи, ізобутоксикарбонільної групи, нEt: етильна група пентилоксикарбонільної групи, неопентилоксикарn-Рr: н-пропільна група бонільної групи, н-гексилоксикарбонільної групи, 2iРr: ізопропільна група метилпентилоксикарбонільної групи і 2s-Bu: втор-бутильна група етилбутоксикарбонільної групи). n-Pen: н-пентильна група Типові приклади сполуки 5-алкокси-4с-Pen: циклопентильна група гідроксиметилтразолу, представленої загальною n-Hex: н-гексильна група формулою (4), даного винаходу показані в таблиці Ph: фенільна група 1 і таблиці 2. Однак сполука 5-алкокси-4 21 Приклади Далі спосіб виробництва даної сполуки конкретно описаний за допомогою прикладів. Однак даний винахід не обмежений даними прикладами. (Довідковий приклад 1) Синтез 5-гідрокси-1-метил-3трифторметилпіразолу 92,1г (0,5моль) етил-4,4,4трифторацетоацетату розчинили в 60,1г (1,0моль) оцтової кислоти. Розчин охолодили до 10°С або нижче при перемішуванні. До нього по краплях додали, за 1 годину, 65,8г (0,5моль) 35%-ного водного розчину метил гідразину. Після краплинного додавання суміш перемішували при кімнатній температурі протягом 1 години і потім при 80°С протягом 5 годин, щоб викликати реакцію. Після реакції суміш охолодили до кімнатної температури. До неї додали 150мл толуолу, 600мл води і 48г (1,2моль) гідроксиду натрію. Після розділення фаз до водної фази додали 154г (1,5моль) 35%-ний соляної кислоти. Отримані кристали зібрали за допомогою фільтрації, промили 50мл води двічі і висушили в 90940 22 сушарці з обігрівом гарячим повітрям, отримавши 71,8г (вихід 86,5%) названої сполуки у вигляді світло-жовтих кристалів. РХ-МС (ЕУ): m/z=166 (М+) Температура плавлення: 179-180°С (Довідковий приклад 2) Синтез 5-гідрокси-1-феніл-3трифторметилпіразолу 18,4г (0,1моль) етил-4,4,4трифторацетоацетату розчинили в 12,0г (0,2моль) оцтової кислоти. Розчин охолодили до 10°С або нижче при перемішуванні. До нього по краплях додали, за 0,5 години, 11,8г (0,11моль) фенілгідразину. Після краплинного додавання суміш перемішували при кімнатній температурі протягом 1 години і потім при 80°С протягом 5 годин, щоб викликати реакцію. Після реакції суміш охолодили до кімнатної температури. До неї додали 100мл води. Отримані кристали зібрали за допомогою фільтрації, промили 50мл води двічі і висушили в сушарці з обігрівом гарячим повітрям, отримавши 22,3г 23 90940 24 (вихід 98,0%) названої сполуки у вигляді світлоСинтез 5-дифторметокси-4-гідроксиметил-1жовтих кристалів. метил-3-трифторметилпіразолу РХ-МС (ЕУ): m/z=228 (М+) 16,6г (0,10моль) 5-гідрокси-1-метил-3Температура плавлення: 190-192°С трифторметилпіразолу, синтезованого, у довідко(Довідковий приклад 3) вому прикладі 1, розчинили в 35,0г (0,15моль) Синтез 3-етоксикарбоніл-5-гідрокси-124%-ного водного розчину гідроксиду калію. До метилпіразолу розчину, що перемішується при кімнатній темпе50,0г (0,24моль) солі діетилоксалоацетату наратурі, по краплях додали 9,7г (0,12моль) 37%трію суспендували в 500мл етанолу. Туди ж доданого розчину формаліну, потім йшло перемішули 25мл оцтової кислоти. Туди по краплях додали вання при тій же температурі протягом 1 години. при кімнатній температурі за 0,5 години при переПісля цього додали 70,0г (0,3моль) 24%-ного водмішуванні 15г (0,33моль) 97%-ного метилгідразиного розчину гідроксиду калію і 100мл ацетонітрину. Після краплинного додавання суміш перемішулу. Туди ж вдули 17,3г (0,20моль) хлордифтормевали при кімнатній температурі протягом 2 годин і тану при кімнатній температурі за 2 години, після потім при температурі кипіння протягом 5 годин. чого йшло перемішування при кімнатній темпераПісля охолодження етанол відганяли при знижетурі протягом 2 годин, щоб викликати реакцію. ному тиску. До залишку додали 200мл етилацетаПісля реакції органічний шар, що з'явився в рету і 100мл води. Після розділення фаз водний шар зультаті розділення фаз, концентрували при знипіддали реекстракції за допомогою 50мл етилацеженому тиску, одержуючи 26,5г (чистота 82,0%, тату. Два етилацетатних шари об'єднали і промивихід 88,2%) неочищеного розчину названої споли 50мл води і 50мл насиченого водного розчину луки. Неочищений розчин піддали вакуумній перехлориду натрію в зазначеному порядку. Отримагонці, отримавши названу сполуку у вигляді безний шар етилацетату висушили над безводним барвного прозорого розчину. 1 сульфатом натрію і піддали вакуумній перегонці, Н-ЯМР (300МГц, ДМСО-d6): 7,23 (т, J=72Гц, щоб видалити розчинник. До отриманих кристалів 1Н), 5,29 (т, J=5,1Гц, 1Н), 4,36 (д, J=5,1Гц, 2Н), додали 100мл води. Кристали зібрали за допомо3,77 (с, 3H) м. ч. гою фільтрації, промили 10мл води і висушили в ГХ-МС (ЕУ): m/z=246 (М+), 177 (основний) сушарці з обігрівом гарячим повітрям, отримавши Температура кипіння: 103-105°С/0,53кПа 29,2г (вихід 71,8%) названої сполуки у вигляді свіПриклад 2 тло-жовтих кристалів. Синтез 4-гідроксиметил-5-метокси-1-метил-3РХ-МС (ЕУ): m/z=170 (М+), 125 (основний) трифторметилпіразолу Температура плавлення: 151°С У 100мл ДМФА суспендували 16,6г (0,10моль) (Довідковий приклад 4) 5-гідрокси-1-метил-3-трифторметилпіразолу, синСинтез 3-ціано-5-гідрокси-1-фенілпіразолу тезованого в довідковому прикладі 1, і 20,9г 120мл води і 15мл 35%-ний соляної кислоти (0,15моль) карбонату калію. У цю суспензію, що додали до 5,6г (0,06моль) аніліну, щоб одержати перемішується при кімнатній температурі, помісрозчин. Розчин охолодили льодом до 0-5°С. До тили 4,5г (0,15моль) параформальдегіду, після нього по краплях додали, при перемішуванні, 24мл чого йшло перемішування при тій же температурі води, у якій розчинили 4,2г (0,06моль) нітриту напротягом 1 години. Потім додали 41,8г (0,30моль) трію, після чого проводили перемішування протякарбонату калію. Туди ж по краплях додали 42,6г гом 1 години. Потім цей водний розчин солі діазо(0,30моль) метилйодиду, після чого йшло перемінію по краплях додавали до 120мл розчину шування при кімнатній температурі протягом 2 піридину, що містить 10,2г (0,06моль) діетил- годин, щоб викликати реакцію. Після реакції додаціаносукцинату, при перемішуванні при охололи 200мл етилацетату і 200мл води. Відділили дженні льодом. Після краплинного додавання суорганічний шар, що з'явився в результаті роздіміш перемішували протягом 1 години при охололення фаз. Водний шар піддали реекстракції за дженні льодом і потім протягом 1 години при допомогою 50мл етилацетату. Два органічних шакімнатній температурі, щоб викликати реакцію. ри об'єднали і промили 50мл води, 30мл насичеПісля реакції додали 240мл 2%-ного водного розного водного розчину хлориду амонію і 30мл насичину гідроксиду натрію, потім йшло перемішування ченого водного розчину хлориду натрію в протягом 2 годин. Після цього реакційну суміш по зазначеному порядку. Отриманий органічний шар краплях додали до 240мл 35%-ний соляної кисловисушували над безводним сульфатом натрію і ти при охолодженні льодом. Отримані кристали потім концентрували при зниженому тиску, одерзібрали за допомогою фільтрації, промили 10мл жуючи 24,9г (чистота 67,5%, вихід 79,0%) неочиводи, і висушили в сушарці з обігрівом гарячим щеного розчину названої сполуки. Неочищений повітрям, отримавши 8,4г неочищених червонуварозчин піддали вакуумній перегонці, отримавши то-коричневих кристалів названої сполуки. Неочиназвану сполуку у вигляді світло-жовтого прозорощені кристали перекристалізували з діетилового го розчину. 1 ефір-петролейного ефіру і висушили в сушарці з Н-ЯМР (300МГц, CDCl3): 4,60 (с, 2Н), 4,13 (с, обігрівом гарячим повітрям, отримавши 5,7г (вихід 3H), 3,69 (с, 3H), 2,02 (ушир., 1Н) м. ч. 51,3%) названої сполуки у вигляді світло-жовтих ГХ-МС (ЕУ) m/z=210 (М+), 193 (основний) кристалів. Температура кипіння: 80-82°С/26,7Па РХ-МС (ЕУ): m/z=185 (М+), 125 (основний) Приклад 3 Температура плавлення: 190°С Синтез 4-гідроксиметил-5-метокси-1-метил-3Приклад 1 трифторметилпіразолу 25 90940 26 У 100мл ДМФА суспендували 16,6г (0,10моль) тезованого в довідковому прикладі 1, і 20,9г 5-гідрокси-1-метил-3-трифторметилпіразолу, син(0,15моль) карбонату калію. У цю суспензію, що тезованого в довідковому прикладі 1, і 20,9г перемішується при кімнатній температурі, поміс(0,15моль) карбонату калію. У цю суспензію, що тили 4,5г (0,15моль) параформальдегіду, після перемішується при кімнатній температурі, помісчого йшло перемішування при тій же температурі тили 4,5г (0,15моль) параформальдегіду, після протягом 1 години. Потім додали 41,8г (0,30моль) чого йшло перемішування при тій же температурі карбонату калію. Туди ж по краплях додали 36,9г протягом 1 години. Потім додали 41,8г (0,30моль) (0,30моль) ізопропілброміду. Реакційну суміш накарбонату калію. Туди ж по краплях додали 25,2г гріли до 60°С і перемішували протягом 12 годин, (0,20моль) диметилсульфату, потім йшло переміщоб викликати реакцію. Після реакції додали шування при кімнатній температурі протягом 2 200мл етилацетату і 200мл води. Відділили оргагодин, щоб викликати реакцію. Після реакції доданічний шар, що з'явився в результаті розділення ли 200мл етилацетату і 200мл води. Відділили фаз. Водний шар піддали реекстракції за допомоорганічний шар, що з'явився в результаті роздігою 50мл етилацетату. Два органічних шари об'єлення фаз. Водний шар піддали реекстракції за днали і промили 50мл води, 30мл насиченого воддопомогою 50мл етилацетату. Два органічних шаного розчину хлориду амонію і 30мл насиченого ри об'єднали і промили 50мл води, 30мл насичеводного розчину хлориду натрію в зазначеному ного водного розчину хлориду амонію і 30мл насипорядку. Отриманий органічний шар висушували ченого водного розчину хлориду натрію в над безводним сульфатом натрію і потім концентзазначеному порядку. Отриманий органічний шар рували при зниженому тиску, одержуючи 21,7г висушували над безводним сульфатом натрію і (чистота 59,4%, вихід 53,5%) неочищеного розчину потім концентрували при зниженому тиску, одерназваної сполуки. Неочищений розчин піддали жуючи 23,5г (чистота 75,4%, вихід 84,3%) неочивакуумній перегонці, отримавши названу сполуку у щеного розчину названої сполуки. Неочищений вигляді світло-жовтого прозорого розчину. 1 розчин піддали вакуумній перегонці, отримавши Н-ЯМР (300МГц, CDCl3): 4,7-4,6 (м, 1Н), 4,53 названу сполуку. Спектри даної сполуки виявилися (с, 2Н), 3,71 (с, 3H), 1,85 (ушир., 1Н), 1,38 (д, ідентичні приведеним у прикладі 2. J=6,3Гц, 6Н) м. ч. Приклад 4 ГХ-МС (ЕУ) m/z=231 (М+), 178 (основний) Синтез 5-етокси-4-гідроксиметил-1-метил-3Температура кипіння: 106-107°С/106,7Па трифторметилпіразолу Приклад 6 У 100мл ДМФА суспендували 16,6г (0,10моль) Синтез 5-циклопентилокси-4-гідроксиметил-15-гідрокси-1-метил-3-трифторметилпіразолу, синметил-3-трифторметилпіразолу тезованого, у довідковому прикладі 1, і 20,9г У 100мл ДМФА суспендували 16,6г (0,10моль) (0,15моль) карбонату калію. У цю суспензію, що 5-гідрокси-1-метил-3-трифторметилпіразолу, синперемішується при кімнатній температурі, помістезованого в довідковому прикладі 1, і 20,9г тили 4,5г (0,15моль) параформальдегіду, після (0,15моль) карбонату калію. У цю суспензію, що чого йшло перемішування при тій же температурі перемішується при кімнатній температурі, поміспротягом 1 години. Потім додали 41,8г (0,30моль) тили 4,5г (0,15моль) параформальдегіду, після карбонату калію. Туди ж по краплях додали 21,8г чого йшло перемішування при тій же температурі (0,20моль) брометану. Реакційну суміш нагріли до протягом 1 години. Потім додали 41,8г (0,30моль) 60°С і перемішували протягом 8 годин, щоб викликарбонату калію. Туди ж по краплях додали 44,7г кати реакцію. Після реакції додали 200мл етила(0,30моль) циклопентилброміду. Реакційну суміш цетату і 200мл води. Відділили органічний шар, що нагріли до 60°С, після чого йшло перемішування з'явився в результаті розділення фаз. Водний шар протягом 12 годин, щоб викликати реакцію. Після піддали реекстракції за допомогою 50мл етилацереакції додали 200мл етилацетату і 200мл води. тату. Два органічних шари об'єднали і промили Відділили органічний шар, що з'явився в результа50мл води, 30мл насиченого водного розчину хлоті розділення фаз. Водний шар піддали реекстракриду амонію і 30мл насиченого водного розчину ції за допомогою 50мл етилацетату. Два органічхлориду натрію в зазначеному порядку. Отриманих шари об'єднали і промили 50мл води, 30мл ний органічний шар висушували над безводним насиченого водного розчину хлориду амонію і сульфатом натрію і потім концентрували при зни30мл насиченого водного розчину хлориду натрію женому тиску, одержуючи 22,5г (чистота 82,7%, в зазначеному порядку. Отриманий органічний вихід 83,0%) неочищеного розчину названої спошар висушували над безводним сульфатом налуки. Неочищений розчин піддали вакуумній перетрію і потім концентрували при зниженому тиску, гонці, отримавши названу сполуку у вигляді безодержуючи 41,9г (чистота 42,2%, вихід 67,0%) небарвного прозорого розчину. очищеного розчину названої сполуки. Неочищений 1 Н-ЯМР (300МГц, CDCl3): 4,57 (с, 2Н), 4,36 розчин піддали вакуумній перегонці, отримавши (кв, J=7,2Гц, 2Н), 3,71 (с, 3H), 1,73 (ушир., 1Н), 1,43 названу сполуку у вигляді світло-жовтого прозоро(т, J=7,2Гц, 3H) м. ч. го розчину. + 1 ГХ-МС (ЕУ) m/z=224 (М ), 177 (основний) Н-ЯМР (300МГц, CDCl3): 5,0-5,1 (м, 1Н), 4,56 Температура кипіння: 95-97°С/26,7Па (с, 2Н), 3,68 (с, 3H), 2,19 (с, 1Н), 1,9-1,6 (м, 8Н) м.ч. Приклад 5 ГХ-МС (ЕУ): m/z=264 (М+), 178 (основний) Синтез 4-гідроксиметил-5-ізопропілокси-1Температура кипіння: 105-107°С/26,7Па метил-3-трифторметилпіразолу Приклад 7 У 100мл ДМФА суспендували 16,6г (0,10моль) Синтез 5-бензилокси-4-гідроксиметил-15-гідрокси-1-метил-3-трифторметилпіразолу, синметил-3-трифторметилпіразолу 27 90940 28 16,6г (0,10моль) 5-гідрокси-1-метил-3У 100мл ДМФА суспендували 16,6г (0,10моль) трифторметилпіразолу, синтезованого в довідко5-гідрокси-1-метил-3-трифторметилпіразолу, синвому прикладі 1, розчинили в 35,0г (0,15моль) тезованого в довідковому прикладі 1, і 20,9г 24%-ного водного розчину гідроксиду калію. До (0,15моль) карбонату калію. У цю суспензію, що розчину, що перемішується при кімнатній темпеперемішується при кімнатній температурі, помісратурі, по краплях додали 9,7г (0,12моль) 37%тили 4,5г (0,15моль) параформальдегіду, після ного розчину формаліну, після чого йшло перемічого йшло перемішування при тій же температурі шування при тій же температурі протягом 1 годипротягом 1 години. Потім додали 41,8г (0,30моль) ни. Потім додали 70,0г (0,3моль) 24%-ного водного карбонату калію. Туди ж по краплях додали 23,8г розчину гідроксиду калію і 100мл ацетонітрилу. (0,20моль) пропаргілброміду. Реакційну суміш наТуди ж по краплях додали 20,5г (0,12моль) бензигріли до 60°С і перемішували протягом 2 годин, лброміда при кімнатній температурі за 1 годину, щоб викликати реакцію. Після реакції додали після чого йшло перемішування при кімнатній тем200мл етилацетату і 200мл води. Відділили оргапературі протягом 12 годин, щоб викликати реакнічний шар, що з'явився в результаті розділення цію. Після реакції органічний шар, що з'явився в фаз. Водний шар піддали реекстракції за допоморезультаті розділення фаз, концентрували при гою 50мл етилацетату. Два органічних шари об'єзниженому тиску, одержуючи 26,1г (чистота 80,0%, днали і промили 50мл води, 30мл насиченого водвихід 73,1%) неочищеного розчину названої споного розчину хлориду амонію і 30мл насиченого луки. Неочищений розчин очистили за допомогою водного розчину хлориду натрію в зазначеному колонкової хроматографії із силікагелем (нпорядку. Отриманий органічний шар висушували гексан:етилацетат=5:1), отримавши названу спонад безводним сульфатом натрію і потім концентлуку у вигляді світло-жовтого прозорого розчину. рували при зниженому тиску, одержуючи 31,2г 1 (чистота 36,9%, вихід 49,2%) неочищеного розчину Н-ЯМР (300МГц, CDCl3): 7,4-7,3 (м, 5Н), 5,28 названої сполуки. Неочищений розчин піддали (с, 2Н), 4,56 (д, J=5,7Гц, 2Н), 3,51 (с, 3H), 1,74 (т, вакуумній перегонці, отримавши названу сполуку у J=5,7Гц, 1Н) м. ч. вигляді світло-жовтого прозорого розчину. ГХ-МС (ЕУ) m/z=286 (М+), 91 (основний) 1 Приклад 8 Н-ЯМР (300МГц, CDCl3): 4,95 (д, J=2,4Гц, Синтез 5-етоксикарбонілметилокси-42Н), 4,61 (с, 2Н), 3,77 (с, 3H), 2,63 (т, J=2,4Гц, 1Н), гідроксиметил-1-метил-3-трифторметилпіразолу 1,78 (с, 1Н) м. ч. У 100мл ДМФА суспендували 16,6г (0,10моль) ГХ-МС (ЕУ) m/z=234 (Μ+), 203 (основний) 5-гідрокси-1-метил-3-трифторметилпіразолу, синТемпература кипіння: 99-101°С/133,3Па тезованого в довідковому прикладі 1, і 20,9г Приклад 10 (0,15моль) карбонату калію. У цю суспензію, що Синтез 5-дифторметокси-4-гідроксиметил-1перемішується при кімнатній температурі, помісфеніл-3-трифторметилпіразолу тили 4,5г (0,15моль) параформальдегіду, після 22,8г (0,10моль) 5-гідрокси-1-феніл-3чого йшло перемішування при тій же температурі трифторметилпіразолу, синтезованого в довідкопротягом 1 години. Потім додали 41,8г (0,30моль) вому прикладі 2, розчинили в 35,0г (0,15моль) карбонату калію. Туди ж по краплях додали 93,4г 24%-ного водного розчину гідроксиду калію. До (0,20моль) етилбромацетату, після чого йшло перозчину, що перемішується при кімнатній темперемішування при кімнатній температурі протягом 2 ратурі, по краплях додали 9,7г (0,12моль) 37%годин, щоб викликати реакцію. Після реакції доданого розчину формаліну, після чого йшло переміли 200мл етилацетату і 200мл води. Відділили шування при тій же температурі протягом 1 годиорганічний шар, що з'явився в результаті роздіни. Потім додали 70,0г (0,3моль) 24%-ного водного лення фаз. Водний шар піддали реекстракції за розчину гідроксиду калію і 100мл ацетонітрилу. допомогою 50мл етилацетату. Два органічних шаТуди ж вдули 17,3г (0,20моль) хлордифторметану ри об'єднали і промили 50мл води, 30мл насичепри кімнатній температурі за 2 години, після чого ного водного розчину хлориду амонію і 30мл насийшло перемішування при кімнатній температурі ченого водного розчину хлориду натрію в протягом 2 годин, щоб викликати реакцію. Після зазначеному порядку. Отриманий органічний шар реакції органічний шар, що з'явився в результаті висушували над безводним сульфатом натрію і розділення фаз, концентрували при зниженому потім концентрували при зниженому тиску, одертиску, одержуючи 28,0г (чистота 93,6%, вихід жуючи 44,7г (чистота 63,0%, вихід 81,9%) неочи84,9%) неочищеного розчину названої сполуки. щеного розчину названої сполуки. Неочищений Неочищений розчин очистили за допомогою колорозчин піддали вакуумній перегонці, отримавши нкової хроматографії із силікагелем (нсвітло-жовтий прозорий розчин. До розчину додагексан:етилацетат=5:1), отримавши названу споли н-гексан. Отримані білі кристали зібрали за долуку у вигляді білих кристалів. 1 помогою фільтрування з відсмоктуванням, отриН-ЯМР (300МГц, CDCl3): 7,6-7,4 (м, 5Н), 6,67 мавши названу сполуку у вигляді білих кристалів. (т, J=72Гц, 1Н), 4,68 (д, J=5,7Гц, 2Н), 1,91 (т, 1 Н-ЯМР (300МГц, CDCl3): 5,18 (т, J=4,5Гц, J=5,7Гц, 1Н) м. ч. + 1Н), 5,06 (с, 2Н), 4,19 (кв, J=7,2Гц, 2Н), 3,75 (с, 3H), ГХ-МС (ЕУ) m/z=308 (М ), 77 (основний) 1,22 (т, J=7,2Гц, 3H) м. ч. Температура плавлення: 57-59°С Температура кипіння: 142°С/33,3Па Приклад 11 Температура плавлення: 57-59°С Синтез 3-етоксикарбоніл-5-дифторметокси-4Приклад 9 гідроксиметил-1-метилпіразолу Синтез 5-пропаргілокси-4-гідроксиметил-1У 50мл ДМФА суспендували 8,5г (0,05моль) 3метил-3-трифторметилпіразолу етоксикарбоніл-5-гідрокси-1-метилпіразолу, синте 29 90940 30 зованого в довідковому прикладі 3, і 10,5г ладі 4, розчинили в 35,0г (0,15моль) 24%-ного во(0,08моль) карбонату калію. У цю суспензію, що дного розчину гідроксиду калію. До розчину, що перемішується при кімнатній температурі, помісперемішується при кімнатній температурі, по кратили 2,3г (0,08моль) параформальдегіду, після плях додали 9,7г (0,12моль) 37%-ного розчину чого йшло перемішування при тій же температурі формаліну, після чого йшло перемішування при тій протягом 1 години. Потім додали 20,9г (0,15моль) же температурі протягом 1 години. Потім додали карбонату калію. Туди ж вдули 8,6г (0,10моль) 70,0г (0,3моль) 24%-ного водного розчину гідрокхлордифторметану. Реакційну суміш перемішувасиду калію і 100мл ацетонітрилу. Туди ж удули ли при кімнатній температурі протягом 2 годин, 17,3г (0,20моль) хлордифторметану при кімнатній щоб викликати реакцію. Після реакції додали температурі за 2 години, після чого йшло перемі200мл етилацетату і 200мл води. Відділили оргашування при кімнатній температурі протягом 2 нічний шар, що з'явився в результаті розділення годин, щоб викликати реакцію. Після реакції оргафаз. Водний шар піддали реекстракції 50мл етинічний шар, що з'явився в результаті розділення лацетату тричі. Органічні шари об'єднали і промифаз, концентрували при зниженому тиску, одерли 50мл води, 30мл насиченого водного розчину жуючи 24,6г (чистота 70,6%, вихід 65,5%) неочихлориду амонію і 30мл насиченого водного розчищеного розчину названої сполуки. Неочищений ну хлориду натрію в зазначеному порядку. Отрирозчин очистили за допомогою колонкової хромаманий органічний шар висушували над безводним тографії із силікагелем (н-гексан:етилацетат=3:1), сульфатом натрію і потім концентрували при зниотримавши названу сполуку у вигляді білих крисженому тиску, одержуючи 24,3г (чистота 42,2%, талів. 1 вихід 82,0%) неочищеного розчину названої споН-ЯМР (300МГц, CDCl3): 7,6-7,4 (м, 5Н), 4,72 луки. Неочищений розчин очистили за допомогою (д, J=5,1Гц, 2Н), 2,10 (т, J=5,1Гц, 1Н) м. ч. колонкової хроматографії із силікагелем (нГХ-МС (ЕУ) m/z=265 (М+), 77 (основний) гексан:етилацетат=1:1), отримавши названу споТемпература плавлення: 71-72°С луку у вигляді білих кристалів. Даний винахід пропонує новий спосіб промис1 Н-ЯМР (300МГц, CDCl3): 6,61 (кв, J=71,7Гц, лового одержання сполуки 5-алкокси-41Н), 4,62 (д, J=6,9Гц, 2Н), 4,46 (т, J=7,2Гц, 2Н), гідроксиметилпіразолу. Відповідно до даного спо3,84 (с, 3H), 3,62 (т, J=6,9Гц, 1Н), 1,43 (т, J=7,2Гц, собу сполука 5-алкокси-4-гідроксиметилпіразолу 3H) м. ч. утворюється зі сполуки піразолу, представленої ГХ-МС (ЕУ) m/z=250 (М+), 153 (основний) загальною формулою (1), без застосування спеціТемпература плавлення: 90-91°С ального реактора, або дорогого каталізатора, або Приклад 12 перехідного металу, за одну стадію при простому Синтез 3-ціано-5-дифторметокси-4виробничому процесі в м'яких умовах з гарним гідроксиметил-1-фенілпіразолу виходом. Більш того, даний спосіб не утворює шкі18,5г (0,10моль) 3-ціано-5-гідрокси-1дливих відходів від каталізатора або перехідного фенілпіразолу, синтезованого в довідковому прикметалу і має значне промислове значення. Комп’ютерна верстка О. Гапоненко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the production of 5-alkoxy-4-hydroxymethylpyrazole compound
Автори англійськоюUchida Yukio, Atsumi Naoya
Назва патенту російськоюСпособ получения соединений 5-алкокси-4-гидроксиметилпиразола и соединения 5-алкокси-4-гидроксиметилпиразола
Автори російськоюУтида Юкио, Ацуми Наойа
МПК / Мітки
МПК: C07D 231/20
Мітки: спосіб, сполук, одержання, сполуки, 5-алкокси-4-гідроксиметилпіразолу
Код посилання
<a href="https://ua.patents.su/15-90940-sposib-oderzhannya-spoluk-5-alkoksi-4-gidroksimetilpirazolu-ta-spoluki-5-alkoksi-4-gidroksimetilpirazolu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання сполук 5-алкокси-4-гідроксиметилпіразолу та сполуки 5-алкокси-4-гідроксиметилпіразолу</a>
Попередній патент: Ключ для згвинчування-розгвинчування замкових з’єднань
Наступний патент: Пристрій для змащування гребенів коліс
Випадковий патент: Імпульсне джерело пружних коливань












