Фумарат 4-[[4-[[4-(2-ціаноетеніл)-2,6-диметилфеніл]аміно]-2-піримідиніл]аміно]бензонітрилу
Номер патенту: 92469
Опубліковано: 10.11.2010
Автори: Копманс Алекс Герман, Вандекрюйс Роже Петрус Гереберн, Стапперс Альфред Елізабет, Пеетерс Йозеф, Стевенс Поль Теодоор Агнес
Формула / Реферат
1. Сполука формули (І)
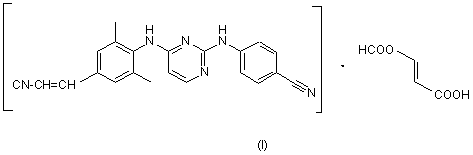
або її N-оксид, або стереохімічно ізомерна форма.
2. Сполука за п. 1, де зазначена сполука являє собою
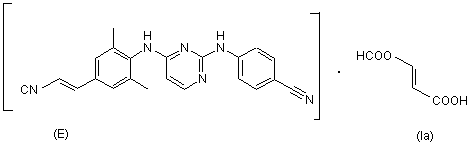 .
.
3. Сполука за п. 1 або 2 для використання як лікарського засобу.
4. Фармацевтична композиція, що містить фармацевтично прийнятний носій і як активний інгредієнт терапевтично ефективну кількість сполуки за п. 1 або 2.
5. Фармацевтична композиція за п. 4, де зазначена композиція придатна для перорального введення.
6. Фармацевтична композиція за п. 4 або 5, де зазначена композиція являє собою тверду композицію.
7. Фармацевтична композиція за будь-яким з пп. 4-6, яка додатково містить зволожуючий агент.
8. Фармацевтична композиція за п. 7, в якій зволожуючий агент являє собою Tween.
9. Фармацевтична композиція за будь-яким з пп. 4-8, де зазначена композиція має форму таблетки.
10. Фармацевтична композиція за п. 9, що має плівкове покриття.
11. Фармацевтична композиція за будь-яким з пп. 4-10, що має наступний склад:
(а) від 5 до 50 % активного інгредієнта;
(b) від 0,01 до 5 % зволожуючого агента;
(c) від 40 до 92 % розріджувача;
(d) від 0 до 10 % полімеру;
(e) від 2 до 10 % розпушувача;
(f) від 0,1 до 5 % гліданту;
(g) від 0,1 до 1,5 % лубриканту.
12. Спосіб одержання фармацевтичної композиції за будь-яким з пп. 4-11, в якому здійснюють наступні стадії:
(і) сухе перемішування активного інгредієнта і частини розріджувача;
(іі) одержання сполучного розчину за допомогою розчинення зв'язуючого і зволожуючого агента в розчиннику для сполучного розчину;
(ііі) розпилення сполучного розчину, отриманого на стадії (іі), на суміш, отриману на стадії (і);
(iv) сушіння вологого порошку, отриманого на стадії (ііі), з наступним просіванням і необов'язковим перемішуванням;
(v) змішування частини розріджувача, що залишилася, розпушувача і необов'язкового гліданту із сумішшю, отриманою на стадії (iv);
(vi) необов'язкове додавання лубриканту до суміші, отриманої на стадії (v);
(vii) пресування таблеток із суміші, отриманої на стадії (vi);
(viii) необов'язкове нанесення плівкового покриття на таблетку, отриману на стадії (vii).
13. Застосування сполуки за п. 1 або 2 для виробництва лікарського засобу для лікування або профілактики ВІЛ-інфекції.
14. Спосіб одержання сполуки формули (І) або (1а) за п. 1 або 2, який відрізняється тим, що здійснюють взаємодію відповідної вільної основи з фумаровою кислотою в присутності придатної кислоти.
15. Спосіб за п. 14, в якому придатною кислотою є оцтова кислота.
Текст
1. Сполука формули (І) H N H N N . N CN-CH=CH HCOO N C2 (21) a200702178 (22) 02.09.2005 (24) 10.11.2010 (86) PCT/EP2005/054341, 02.09.2005 (31) 05101447.0 (32) 25.02.2005 (33) EP (31) PCT/EP2004/052028 (32) 03.09.2004 (33) EP (31) PI20043578 (32) 02.09.2004 (13) COOH .. N CN N (E) 3. Сполука за п. 1 або 2 для використання як лікарського засобу. 4. Фармацевтична композиція, що містить фармацевтично прийнятний носій і як активний інгредієнт терапевтично ефективну кількість сполуки за п. 1 або 2. 5. Фармацевтична композиція за п. 4, де зазначена композиція придатна для перорального введення. (11) H N N HCOO COOH (Ia) . 6. Фармацевтична композиція за п. 4 або 5, де зазначена композиція являє собою тверду композицію. 7. Фармацевтична композиція за будь-яким з пп. 46, яка додатково містить зволожуючий агент. 8. Фармацевтична композиція за п. 7, в якій зволожуючий агент являє собою Tween. 9. Фармацевтична композиція за будь-яким з пп. 48, де зазначена композиція має форму таблетки. UA H N 2. Сполука за п. 1, де зазначена сполука являє собою (19) або її N-оксид, або стереохімічно ізомерна форма. 92469 (I) 3 92469 4 10. Фармацевтична композиція за п. 9, що має (iv) сушіння вологого порошку, отриманого на стаплівкове покриття. дії (ііі), з наступним просіванням і необов'язковим 11. Фармацевтична композиція за будь-яким з пп. перемішуванням; 4-10, що має наступний склад: (v) змішування частини розріджувача, що залиши(а) від 5 до 50 % активного інгредієнта; лася, розпушувача і необов'язкового гліданту із (b) від 0,01 до 5 % зволожуючого агента; сумішшю, отриманою на стадії (iv); (c) від 40 до 92 % розріджувача; (vi) необов'язкове додавання лубриканту до сумі(d) від 0 до 10 % полімеру; ші, отриманої на стадії (v); (e) від 2 до 10 % розпушувача; (vii) пресування таблеток із суміші, отриманої на (f) від 0,1 до 5 % гліданту; стадії (vi); (g) від 0,1 до 1,5 % лубриканту. (viii) необов'язкове нанесення плівкового покриття 12. Спосіб одержання фармацевтичної композиції на таблетку, отриману на стадії (vii). за будь-яким з пп. 4-11, в якому здійснюють насту13. Застосування сполуки за п. 1 або 2 для виробпні стадії: ництва лікарського засобу для лікування або про(і) сухе перемішування активного інгредієнта і часфілактики ВІЛ-інфекції. тини розріджувача; 14. Спосіб одержання сполуки формули (І) або (1а) за п. 1 або 2, який відрізняється тим, що здійс(іі) одержання сполучного розчину за допомогою розчинення зв'язуючого і зволожуючого агента в нюють взаємодію відповідної вільної основи з фурозчиннику для сполучного розчину; маровою кислотою в присутності придатної кисло(ііі) розпилення сполучного розчину, отриманого на ти. стадії (іі), на суміш, отриману на стадії (і); 15. Спосіб за п. 14, в якому придатною кислотою є оцтова кислота. Даний винахід відноситься до солі фумарату 4-[[4-[[4-(2-ціаноетеніл)-2,6-диметилфеніл]аміно]-2піримідиніл]аміно]бензонітрилу, фармацевтичних композицій, що містять зазначену сіль фумарат, до одержання даної солі і фармацевтичних композицій. WO 03/16306 розкриває похідні піримідину, що інгібують ВІЛ-реплікацію, серед яких 4-[[4-[[4-(2ціаноетеніл)-2,6-диметилфеніл]аміно]-2піримідиніл]аміно]бензонітрил і його фармацевтично прийнятні солі. WO 04/0162581 розкриває спосіб одержання 4-[[4-[[4-(2-ціаноетеніл)-2,6диметилфеніл]аміно]-2піримідиніл]аміно]бензонітрилу. 4-[[4-[[4-(2-ціаноетеніл)-2,6диметилфеніл]аміно]-2піримідиніл]аміно]бензонітрил, зокрема, Ε-ізомер, має добру активність інгібування ВІЛ реплікації щодо дикого типу ВІЛ, а також штамів ВІЛ з лікарською і мультилікарською стійкістю (тобто штамів, що стали стійкими щодо відомих в даній галузі ліків). Таким чином, дана сполука потенційно може бути добрим кандидатом для розробки лікарського засобу для лікування ВІЛ-інфекції. Однак висока фармакологічна активність, добрий фармакологічний профіль це не єдиний фактор, що визначає лікарську здатність сполуки. Добрий кандидат у ліки переважно повинен бути стабільним хімічно, а також фізично; повинен мати прийнятний профіль токсичності; повинен мати прийнятну біодоступність. Біодоступність сполуки впливає на дозу сполуки, яку необхідно ввести пацієнту для досягнення терапевтично ефективної концентрації сполуки. Сполуки, що мають низьку біодоступність, необхідно вводити при більш високих дозах у порівнянні зі сполуками, що мають більш високу біодоступність. Можливі наслідки необхідності більш високих доз можуть включати підвищений ризик несприятливих ефектів; збільшення розміру дозо ваної форми; збільшення частоти введення. Дані фактори можуть впливати на дотримання курсу антиретровірусної терапії. Суворе дотримання курсу лікування є одним з найбільш важливих факторів, що впливають на ефективність лікування ВІЛ. Збільшення частоти прийому дози і збільшення розміру таблетки може вести до зниження суворості дотримання курсу лікування і, отже, знижувати ефективність терапії. Таким чином, при розробці лікарського засобу для лікування ВІЛ, це, переважно, повинна бути активна сполука з прийнятною біодоступністю. Біодоступність сполуки, призначеної для перорального прийому, залежить від розчинності сполуки у воді, а також проникності сполуки (її здатності абсорбуватися через кишкову мембрану). Науковою основою для класифікації лікарських речовин на основі їх розчинності у воді і кишковій проникності є Біофармацевтична Система Класифікації або BCS. Згідно BCS, лікарські речовини класифікують таким чином: клас 1: висока розчинність - висока проникність; клас 2: низька розчинність - висока проникність; клас 3: висока розчинність - низька проникність; клас 4: низька розчинність - низька проникність. Сполуки з низькою розчинністю або низькою проникністю (клас 2-4) можуть страждати від низької біодоступності при пероральному введенні. Вільна основа 4-[[4-[[4-(2-ціаноетеніл)-2,6диметилфеніл]аміно]-2піримідиніл]аміно]бензонітрил може бути класифікована як сполука BCS-класу 2 і, таким чином, мати низьку розчинність у воді. 4-[[4-[[4-(2ціаноетеніл)-2.6-диметилфеніл]аміно]-2піримідиніл]аміно]бензонітрил демонструє низьку розчинність не тільки у воді, але також у кислому 5 92469 6 середовищі. Отже, при пероральному введенні у vivo у порівнянні з вільною основою. Фактично давигляді звичайної твердої дозованої форми можна на сіль, що вводиться у вигляді твердої дозованої очікувати на низьку біодоступність. форми, має in vivo біодоступність, що порівняна з Маючи справу зі сполукою BCS-класу 2, призбіодоступністю вільної основи, що вводиться пеначеною для перорального введення, фахівець в рорально у вигляді PEG 400-розчину. Завдяки підгалузі фармацевтичної технології зосереджує увавищеній біодоступності in vivo, сіль фумарат можгу на з'ясуванні можливостей підвищення розчинна одержати без необхідності застосування ності сполук, наприклад, одержуючи підходящу методик комплексоутворення. сіль. Даним шляхом діють у випадку 4-[[4-[[4-(2Виявлено також, що сіль фумарат за даним ціаноетеніл)-2,6-димeтилфеніл]аміно]-2винаходом є негігроскопічною та хімічно і фізично піримідиніл]аміно]бензонітрилу. Отримані солі, стабільною в різних умовах вологості і температуочевидно, мають тільки незначно поліпшену розри. чинність у воді та у HCl. Отримані солі ще налеТаким чином, даний винахід відноситься до жать до BCS-класу 2. Таким чином, для отриманих сполуки формули (I), тобто фумарату (транссолей також можна очікувати низьку біодоступСН(СООН)=СН(СООН)) 4-[[4-[[4-(2-ціаноетеніл)ність. 2,6-диметилфеніл]аміно]-2Несподівано, у даний час було виявлено, що піримідиніл]аміно]бензонітрилу, його N-оксиду або сіль фумарат (транс-СН(СООН)=СН(СООН)) 4-[[4стереохімічно ізомерних форм. [[4-(2-ціаноетеніл)-2,6-диметилфеніл]аміно]-2Таким чином, даний винахід відноситься, зокпіримідиніл]аміно]бензонітрилу, зокрема, його Εрема, до сполуки формули (І) ізомер, має значно поліпшену біодоступність in , її N-оксиду або стереохімічно ізомерної форми. Передбачається, що N-оксидні форми даної сполуки формули (І) включають сполуки формули (І), в яких один або декілька третинних атомів азоту окиснені до, так названого, N-оксиду. Як використовується в даній заявці вище, вираз "стереохімічно ізомерні форми" визначає всі можливі стереоізомер ні форми, що може мати сполука формули (І) і N-оксиди або четвертинні аміни. Якщо не вказано або не зазначено інше, хімічна назва сполуки позначає суміш усіх можливих стереохімічно ізомерних форм, а також будьяку з індивідуальних ізомерних форм сполуки фо рмули (І) і N-оксидів, сольватів або четвертинних амінів, що, власне кажучи, не містить інших ізомерів. Очевидно, мається на увазі, що стереохімічно ізомерні форми сполуки формули (І) включені в межі даного винаходу. Сполука формули (І) може існувати в 2 стереохімічних конфігураціях відносно подвійного зв'язку ціаноетенільного ланцюга, а саме, Еконфігурації (Entgegen=навпроти) (Ε-ізомер) і Zконфігурації (Zusammen=разом) (Z-ізомер). Позначення Ε і Ζ добре відомі фахівцю в даній галузі. Конкретний варіант сполуки формули (І) представляє Ε-ізомер, тобто сполуку формули (I-а) Інший конкретний варіант сполуки формули (І) представляє Z-ізомер, тобто сполуку формули (I-b). Коли б в даній заявці не згадувався б Εізомер, мається на увазі чистий Е-ізомер або будьяка ізомерна суміш Е- і Z-ізомерів, в якій Ε-ізомер переважає, тобто ізомерна суміш, що містить більше 50% або, зокрема, більше 80% Ε-ізомеру, або. більш конкретно, 90% Ε-ізомеру. Особливий 7 92469 8 інтерес представляє Ε-ізомер, який, власне кажудефіциту людини) являє собою етіологічний агент чи, не містить Z-ізомер. Вираз «власне кажучи не синдрому придбаного імунодефіциту (СНIД) у люмістить» у даному контексті позначає E-Z-суміші дей. Вірус ВІЛ переважно інфікує клітини Т-4 любез або майже без Z-ізомеру, наприклад, ізомерні дини і руйнує їх або змінює їх звичайну функцію, суміші, що містять більше 90%, зокрема, 95% або особливо координацію імунної системи. У резульнавіть 98% або 99% Е-ізомеру. таті, інфікований пацієнт постійно має знижену Коли б в даній заявці не згадувався б Z-ізомер, кількість клітин Т-4, що, крім того, поводяться аномається на увазі чистий Z-ізомер або будь-яка мально. Отже, імунологічна захисна система не ізомерна суміш Z- і Ε-ізомерів, в якій Z-ізомер пездатна боротися з інфекціями і новоутвореннями, і реважає, тобто ізомерна суміш, що містить більше ВІЛ-інфікований суб'єкт звичайно умирає від умов50% або, зокрема, більше 80% Z-ізомеру або. но-патогенних інфекцій, таких як пневмонія, або більш конкретно, більше 90% Z-ізомеру. Особливід ракових захворювань. Інші стани, асоційовані з вий інтерес представляє Z-ізомер, який, власне ВІЛ-інфекціями, включають тромбоцитопенію, саркажучи, не містить Ε-ізомер. Вираз «власне кажучи кому Капоши та інфекцію центральної нервової не містить» у даному контексті позначає E-Zсистеми, що характеризуються прогресуючою десуміші без або майже без Ε-ізомеру, наприклад, мієлінізацією, результатом якої є слабоумство і ізомерні суміші, що містять більше 90%, зокрема, такі симптоми, як прогресуюча дизартрія, атаксія і 95% або навіть 98% або 99% Z-ізомеру. дезорієнтація. Крім того, ВІЛ-інфікування також Поліморфні форми даних солей також вклюасоціюється з периферичною невропатією, прочені в межі даного винаходу. гресуючою генералізованою лімфаденопатією Поліморфні форми фармацевтичних сполук (PGL) і СНІД-пов'язаним комплексом (ARC). можуть становити інтерес для тих, хто займається Дані сполуки також демонструють активність розробкою підходящої дозованої форми, тому що проти ВІЛ-штамів з лікарською стійкістю і множинякщо поліморфна форма не зберігається незмінною лікарською стійкістю, зокрема, штамів ВІЛ-1 з ною протягом клінічних досліджень і дослідження лікарською стійкістю і множинною лікарською стійстабільності, то не можна зіставляти точну викокістю, більш конкретно, дані сполуки демонструристану або відміряну дозу при переході від однієї ють активність проти ВІЛ-штамів, особливо ВІЛ-1 серії до іншої. При одержанні фармацевтичної штамів, що мають придбану стійкість до одного сполуки для застосування важливо розпізнати або декількох відомих у даній галузі ненуклеозидполіморфну форму, доставлену в кожну дозовану пих інгібіторів зворотної транскриптази. Відомі в форму, щоб переконатися, що в процесі одержанданій галузі ненуклеозидні інгібітори зворотної ня використовується однакова форма і що в кожну транскриптази являють собою ненуклеозидні інгідозу включається однакова кількість ліків. Таким бітори зворотної транскриптази, відмінні від даних чином, треба обов'язково переконатися, що присусполук і, зокрема, комерційні ненуклеозидні інгібітня одна поліморфна форма або деяка відома тори зворотної транскриптази. комбінація поліморфних форм. Крім того, деякі Активність 4-[[4-[[4-(2-ціаноетеніл)-2,6поліморфні форми можуть демонструвати підвидиметилфепіл]аміно]-2щену термодинамічну стабільність і можуть більпіримідиніл]аміно]бензонітрилу інгібування ВІЛше, ніж інші поліморфні форми, підходити для реплікації описана в заявці WO 03/16306, що включення у фармацевтичні препарати. Як прийнвключена в дану заявку у вигляді посилання. ято в даній заявці, поліморфні форми сполук за Завдяки своїм антиретровірусним властивосданим винаходом являють собою однакову хімічну тям, зокрема, своїм анти-ВІЛ властивостям, особсутність, але в різній кристалічній структурі. ливо своїй інгібуючій реплікацію ВІЛ-1 активність, Форми з приєднаним розчинником (сольвати), дані сполуки придатні для лікування ВІЛякі здатні утворювати солі за даним винаходом, інфікованих індивідуумів і для профілактики даних також включені в межі даного винаходу. Приклаінфекцій. Взагалі, сполуки за даним винаходом дами таких форм є, наприклад, гідрати, алкоголяможуть бути корисні при лікуванні теплокровних ти і подібні. Сольвати також позначаються в даній ссавців, інфікованих вірусами, існування яких опозаявці як псевдополіморфні форми. Переважною є середковано або залежить відферменту зворотної безводна сіль. транскриптази. Стани, які можуть бути попереджеКоли б в даній заявці далі не використовувавні або які можна лікувати за допомогою сполук за ся б вираз "сполука формули (І), (I-а) або (І-b)", даним винаходом, особливо стани, асоційовані з мається на увазі, що він включає також N-оксидні ВІЛ і іншими патогенними ретровірусами, включаформи, стереохімічно ізомерні форми і поліморфні ють СНІД, СНІД-пов'язаний комплекс (ARC), проабо псевдополіморфні форми. Особливий інтерес гресуючу генералізовану лімфаденопатію (PGL), а представляє стереохімічно чиста форма сполуки також хронічні захворювання центральної нервоформули (І). Переважною сполукою формули (І) є вої системи, викликані ретровірусами, такі як, насполука формули (I-а). приклад, ВІЛ-опосередковане слабоумство і розсіСполуки формули (I), (I-а) або (І-b) можна одеяний склероз. Отже, сполуки формули (І), (I-а) або ржати за допомогою взаємодії відповідної вільної (І-b) можна застосовувати як лікарський засіб. основи з фумаровою кислотою в присутності підТаким чином, сполуки за даним винаходом ходящого розчинника, такого як, наприклад, підхоможна використовувати як лікарські засоби проти дяща кислота, наприклад, оцтова кислота. зазначених вище станів. Зазначене застосування Сполуки формули (I), (I-а) або (I-b) мають аняк лікарського засобу або спосіб лікування вклютиретровірусну активність. Вони здатні інгібувати чає введення ВІЛ-інфікованим суб'єктам кількості, реплікацію ВІЛ, зокрема, ВІЛ-1. ВІЛ (вірус імуноефективної для лікування станів, асоційованих з 9 92469 10 ВІЛ і іншими патогенними ретровірусами, особлиінгредієнти, наприклад, для сприяння розчинності. во з ВІЛ-1. Зокрема, дані сполуки можна викорисНаприклад, можна приготувати розчини для ін'єктовувати у виробництві лікарського засобу для цій, в яких носій включає фізіологічний розчин, лікування або профілактики ВІЛ-інфекції, переварозчин глюкози або суміш фізіологічного розчину і жно для лікування ВІЛ-інфекції. розчину глюкози. Можна також приготувати суЗ урахуванням корисності даних сполук, заспензії для ін'єкцій, в яких можна використовувати безпечений також спосіб лікування ссавців, вклюпідходящі рідкі носії, суспендуючі агенти і подібні. чаючи людей, або спосіб профілактики теплокровВключені також препарати у вигляді твердих них ссавців, включаючи людей, що страждають від форм, що призначені для перетворення в рідкі вірусних інфекцій, особливо, від ВІЛ-інфекцій. Заформи незадовго до використання. У композиціях, значений спосіб включає введення, переважно що підходять для крізьшкірного введення, носій пероральне введення, ссавцю, включаючи людей, необов'язково включає агент, що збільшує прониефективної кількості солі за даним винаходом. кання, і/або підходящий зволожуючий агент, неЗавдяки більш високій біодоступності даних обов'язково об'єднані з підходящими добавками сполук у порівнянні з відповідною вільною оснобудь-якої природи при незначному змісті, причому вою, можна одержати терапевтично ефективні зазначені добавки не здійснюють істотного шкідрівні в плазмі при введенні фармацевтичної комливого ефекту на шкіру. Зазначені добавки можуть позиції, що містить меншу кількість солі в порівсприяти введенню в шкіру і/або можуть бути коринянні з необхідною кількістю відповідної вільної сні для одержання необхідних композицій. Дані основи. Отже, можна зменшити розмір фармацевкомпозиції можна вводити різними способами, тичної композиції або знизити частоту дозування. наприклад, за допомогою трансдермального пласТаким чином, даний винахід також відноситься тиру, крапкового нанесення, у вигляді мазі. Солі за до фармацевтичної композиції, що містить фарданим винаходом також можна вводити за допомацевтично прийнятний носій і як активний інгремогою інгаляції або інсуфляції. застосовуючи медієнт терапевтично ефективну кількість сполуки тоди і препарати, що використовуються в даній формули (І) (I-а) або (I-b). галузі для введення даним способом. Таким чиЗокрема, даний винахід також відноситься до ном, взагалі, солі за даним винаходом можна ввофармацевтичної композиції, що містить фармацедити в легені у вигляді розчину, суспензії або суховтично прийнятний носій і як активний інгредієнт го порошку. Будь-яка система, розроблена для терапевтично ефективну кількість сполуки формудоставки розчинів, суспензій або сухих порошків за ли (І), (I-а) або (І-b), за умови, що композиція не допомогою пероральної або носової інгаляції або містить один або декілька нуклеозидних інгібіторів інсуфляції, підходить для введення даних сполук. зворотної транскриптази і/або один або декілька Сполуки за даним винаходом також можуть нуклеотидних інгібіторів зворотної транскриптази. бути введені місцево у вигляді крапель, зокрема, Для цілей введення дані сполуки формули (І), очних крапель. Зазначені очні краплі можуть зна(I-а) або (І-b) можна приготувати у вигляді різноходитися у вигляді розчину або суспензії. Будь-яка манітних фармацевтичних композицій. Як підхосистема, розроблена для доставки розчинів або дящі композиції можна привести всі композиції, які суспензій, така як очні краплі, підходить для ввезвичайно використовуються для системного придення даних сполук. йому ліків. Для одержання фармацевтичних комУ WO 2004/069812, що включена в дану заявку позицій за даним винаходом ефективну кількість у вигляді посилання, описується здатність похідсполуки формули (І), (I-а) або (I-b) як активний інгних піримідину, серед яких 4-[[4-[[4-(2-ціаноетеніл)редієнт поєднують у гомогенну суміш з фармацев2,6-диметилфеніл]аміно]-2тично прийнятним носієм, причому зазначений піримідиніл]аміно]бензонітрил і його фармацевтиносій може мати різноманітні форми в залежності чно прийнятні солі, запобігати ВІЛ-інфекції при від форми препарату, бажаної для введення. Дані статевих зносинах або інтимному контакті між парфармацевтичні композиції бажано виготовляти в тнерами. Таким чином, даний винахід також відностандартному дозованому вигляді, що підходить, ситься до фармацевтичної композиції у вигляді, зокрема, для перорального прийому. Наприклад, адаптованому для застосування в тому місці, де при одержанні композицій у вигляді дозованої фоможуть мати місце полові зносини або інтимний рми для перорального прийому можна використоконтакт, такому як геніталії, пряма кишка, рот, рувувати будь-яке зі звичайних фармацевтичних ки, низ живота, верх стегон, особливо піхва і рот, середовищ, наприклад, воду, гліколі, олії, спирти і що містин, фармацевтично прийнятний носій і як подібні, у випадку рідких препаратів для перораактивний інгредієнт ефективну кількість сполуки льного прийому, таких як суспензії, сиропи, еліксиформули (І), (I-а) або (I-b). Зокрема, даний винахід ри, емульсії і розчини; або тверді носії, такі як кротакож відноситься до фармацевтичної композиції у хмалі, цукри, каолін, розріджувачі, змазуючі вигляді, адаптованому для застосування в місці, речовини, зв'язуючі речовини, розпушувачі і подібде можуть мати місце полові зносини або інтимний ні у випадку порошків, пігулок, капсул і таблеток. контакт, такому як геніталії, пряма кишка, рот, руЧерез простоту введення таблетки і капсули явки, низ живота, верх стегон, особливо, піхва і рот, ляють собою найбільш переважні стандартні дощо містить фармацевтично прийнятний носій і як зовані форми для перорального прийому, в яких, активний інгредієнт ефективну кількість сполуки мабуть, використовують тверді фармацевтичні формули (І), (I-а) або (І-b), за умови, що композиносії. Носій для парентеральних композицій звиція не містить один або декілька нуклеозидних чайно включає стерильну воду, щонайменше, веінгібіторів зворотної транскриптази і/або один або лику частину, хоча можуть бути включені й інші декілька нуклеотидних інгібіторів зворотної транс 11 92469 12 криптази. Як підходящі спеціально адаптовані сті від оцінки лікаря, що прописує сполуки за дакомпозиції можна вказати всі композиції, що звиним винаходом. чайно використовуються в піхві, прямій кишці, у Пацієнти можуть приймати фармацевтичні роті і на шкірі, такі як, наприклад, гелі, желе, крекомпозиції за даним винаходом в будь-яку годину ми, мазі, плівки, губки, піни, внутрішньопіхвові кідня, незалежно від прийому їжі. Переважно прийльця, цервікальні ковпачки, супозиторії для ректамати дані композиції після прийому їжі. льного або вагінального застосування, вагінальні, Переважний варіант даного винаходу відноректальні або букальні таблетки, полоскання для ситься до пероральної фармацевтичної композирота. Для одержання таких фармацевтичних комції, тобто фармацевтичної композиції, що підхопозицій ефективну кількість активного інгредієнта дить для перорального введення, що містить поєднують у гомогенну суміш з фармацевтично фармацевтично прийнятний носій і як активний прийнятним носієм, причому зазначений носій моінгредієнт терапевтично ефективну кількість споже мати різні форми в залежності від форми ввелуки формули (І), (I-а) або (І-b); зокрема, фармадення. Для збільшення часу утримання такої фарцевтичній композиції, що підходить для пероральмацевтичної композиції на місці застосування ного введення, що містить фармацевтично може бути корисним включити в композицію біоадприйнятний носій і як активний інгредієнт терапевгезійний агент, зокрема, біоадгезійний полімер. тично ефективну кількість сполуки формули (І), (IБіоадгезійний агент можна визначити як матеріал, а) або (І-b), за умови, що композиція не містить що прилипає до живої біологічної поверхні, такої один або декілька нуклеозидних інгібіторів зворотяк, наприклад, слизувата мембрана або тканина ної транскриптази і/або один або декілька нуклеошкіри. тидних інгібіторів зворотної транскриптази. Таким чином, даний винахід також відноситься Зокрема, пероральна фармацевтична комподо фармацевтичної композиції, що містить фарзиція являє собою тверду фармацевтичну компомацевтично прийнятний носій і як активний інгрезицію для перорального прийому, більш конкретдієнт ефективну кількість сполуки формули (I), (I-а) но, таблетку або капсулу, більш конкретно, або (І-b), що характеризується тим, що дана фартаблетку Згідно з даним винаходом таблетку можмацевтична композиція є біоадгезійною щодо місна приготувати у формі таблетки для прийому ця застосування. Зокрема, даний винахід також один раз на день. відноситься до фармацевтичної композиції, що Переважно, щоб фармацевтичні композиції за містить фармацевтично прийнятний носій і як акданим винаходом містили такі кількості сполуки тивний інгредієнт ефективну кількість сполуки фоформули (I), (I-а) або (І-b), що еквівалентні прибрмули (I), (I-а) або (І-b), що характеризується тим, лизно 5-500 мг відповідної вільної основи 4-[[4-[[4що дана фармацевтична композиція є біоадгезій(2-ціаноетеніл)-2,6-диметилфеніл]аміно]-2ною щодо місця застосування, за умови, що компіримідиніл]аміно]бензонітрилу, його Е- або Zпозиція не містить один або декілька нуклеозидних ізомеру, більш переважно приблизно 10-250 мг інгібіторів зворотної транскриптази і/або один або відповідної вільної основи, більш переважно прибдекілька нуклеотидних інгібіторів зворотної транслизно 20-200 мі відповідної вільної основи. Перекриптази. Переважним місцем застосування є піхважно, щоб дані фармацевтичні композиції містива, пряма кишка, рот або шкіра, найбільш перевали такі кількості сполуки формули (І), (I-а) або (І-b), жним є піхва. що еквівалентні 25 мг, 50 мг, 75 мг, 100 мг або 150 Особливо корисно виготовляти зазначені вимг відповідної вільної основи (осн. екв.). ще фармацевтичні композиції у вигляді стандартЯк використовується в даній заявці вище або ної дозованої форми для простоти введення та далі, вираз "приблизно" відносно чисельних знаоднорідності дозування. Як використовується в чень x означає, наприклад, x±10%. даній заявці, стандартна дозована форма являє Розмір часток сполуки формули (I), (I-а) або (Ісобою фізично дискретні одиниці, що підходять як b) переважно складає менше 50 мкл, більш переєдині дози, причому кожна одиниця містить попеважно менше 25 мкм, ще більш переважно менше редньо визначену кількість активного інгредієнта, 20 мкм. Також переважним є розмір часток приброзраховану таким чином, щоб здійснювати бажализно 15 мкм або менше, або приблизно 12 мкм ний терапевтичний ефект, в поєднанні з необхідабо менше, або приблизно 10 мкм або менше, або ним фармацевтичним носієм. Прикладами таких приблизно 5 мкм або менше. Найбільш переважстандартних дозованих форм є таблетки (включаний розмір часток знаходиться в діапазоні від приючи таблетки з насічкою або таблетки з оболонблизно 0,2 до приблизно 15 мкм або від приблизно кою), капсули, пігулки, пакетики з порошками, пла0,2 до приблизно 10 мкм. стинки, супозиторії, розчини або суспензії для Фармацевтичні композиції за даним винахоін'єкцій і подібні, і їх різновиди. дом переважно включають зволожуючий агент. Точне дозування і частота введення залежать Щодо зволожуючого агента, в композиціях за давід конкретного стану, що підлягає лікуванню, важним винаходом можна використовувати будь-який кості стану, що підлягає лікуванню, віку, ваги, стаз фізіологічно припустимих зволожуючих агентів, ті, ступеня захворювання і загального фізичного що підходять для використання у фармацевтичній стану конкретного пацієнта, а також від іншого композиції. лікування, що може мати індивідуум, що добре У даній галузі добре відомо, що зволожуючий відоме фахівцям у даній галузі. Крім того, очевидагент є амфіфільною сполукою; він містить полярні но, що зазначена ефективна щоденна кількість гідрофільні фрагменти, а також неполярні гідроможе бути зменшена або збільшена в залежності фобні фрагменти. від реакції суб'єкта, якого лікують, і/або в залежно 13 92469 14 Терміни "гідрофільний" або "гідрофобний" є ринової кислоти, пальмітинової кислоти, олеїнової відносними. кислоти і подібних з PEG-8, 10, 12, 20, 32, 400 і Відносну гідрофільність або гідрофобність подібними, наприклад, PEG-8 дилаурат або дисзволожуючого агента можна виразити значенням теарат, PEG-10 дипальмітат, PEG-12 дилаурат, його гідрофільно-ліпофильного балансу (значенабо дистеарат, або діолеат, PEG-20 дилаурат, або ням HLB). Зволожуючі агенти з низьким значенням дистеарат, або діолеат, PEG-32 дилаурат, або HLB категоризовані як "гідрофобні" зволожуючі дистеарат, або діолеат, PEG-400 діолеат або дисагенти, тоді як зволожуючі агенти з високим знатеарат (зволожуючі агенти, що належать до даної ченням HLB категоризовані як "гідрофільні" звологрупи, відомі, наприклад, як Mapeg, Polyalso. жуючі агенти. Емпіричним правилом є: зволожуючі Kessco, Cithrol); агенти, що мають значення HLB більше приблизно c) суміші моно- і діефірів поліетиленгліколю і 10, звичайно вважаються гідрофільними зволожужирних кислот, такі як, наприклад, PEG 4-150 моючими агентами; зволожуючі агенти, що мають но- і дилаурат. PEG 4-150 моно- і діолеат, PEG 4значення HLB нижче приблизно 10, звичайно вва150 моно- і дистеарат та подібні (зволожуючі агенжаються гідрофобними зволожуючими агентами. ти, що належать до даної групи, відомі, наприклад, Дані композиції переважно містять гідрофільяк Kessco); ний зволожуючий агент. Варто брати до уваги, що d) поліетиленглікольгліцеринові ефіри жирних значення HLB зволожуючого агента є тільки грукислот, такі як. наприклад, PEG-20 гліцериллаубим показником гідрофільності/гідрофобності зворат, або гліцерилстеарат, або гліцерилолеат, ложуючого агента. Значення HLB конкретного звоPEG-30 гліцериллаурат або гліцерилолеат, PEGложуючого агента може змінюватися в залежності 15 гліцериллаурат, PEG-40 гліцериллаурат і подівід способу визначення HLB; може змінюватися в бні (зволожуючі агенти, що належать до даної грузалежності від його комерційного джерела; змінюпи, відомі, наприклад, як Tagat, Glycerox L, ватися від партії до партії. Фахівець в даній галузі Capmul); може легко ідентифікувати гідрофільні зволожуючі e) продукти трансетерифікації спирт-масло, агенти, що підходять для використання у фармащо включають складні ефіри спиртів або поліспирцевтичних композиціях за даним винаходом. тів, таких як гліцерин, пропіленгліколь. етиленгліЗволожуючий агент за даним винаходом може коль, поліетиленгліколь, сорбіт, пентаеритрит і бути аніонним, катіонним, цвітеріонним або неіонподібні, із природними і/або гідрогенізованими маним зволожуючим агентом, останній є переважслами або розчинними в маслах вітамінами, такиним. Зволожуючий агент за даним винаходом тами як касторова олія, гідрогенізована касторова кож може являти собою суміш двох або більш олія, вітамін А, вітамін D, вітамін E, вітамін K, харзволожуючих агентів. чова рослинна олія, наприклад, кукурудзяна олія, Підходящі зволожуючі агенти для використанмаслинова олія, арахісове масло, кісточкова паня в композиціях за даним винаходом перерахольмова олія, кісточкова абрикосова олія, мигдальвані нижче. Варто підкреслити, що зазначений не масло і подібні, наприклад, PEG-20 - касторова список зволожуючих агентів є тільки ілюстративолія, або гідрогенізована касторова олія, або гліним, характерним і невичерпаним. Таким чином, цериди кукурудзяної олії, або гліцериди мигдальвинахід не обмежений зволожуючими агентами, ної олії, PEG-23 - касторова олія, PEG-25 - гідроперерахованими нижче. У даних композиціях можгенізована касторова олія або триолеат, PEG-35 на також використовувати суміші зволожуючих касторова олія, PEG-30 - касторова олія або гідроагентів. генізована касторова олія, PEG-38 - касторова Підходящі зволожуючі агенти, які можна викоолія, PEG-40 - касторова олія, або гідрогенізована ристовувати в даному винаході, включають касторова олія, або кісточкова пальмова олія, a) моноефіри поліетиленгліколю і жирних кисPEG-45 - гідрогенізована касторова олія, PEG-50 лот, включаючи ефіри лауринової кислоти, олеїкасторова олія або гідрогенізована касторова олія, нової кислоти, стеаринової кислоти, рицинолевої PEG-56 - касторова олія, PEG-60 - касторова олія, кислоти і подібних з PEG 6, 7, 8, 9, 10, 12, 15, 20, або гідрогенізована касторова олія, або гліцериди 25, 30, 32, 40, 45, 50, 55, 100, 200, 300, 400, 600 і кукурудзяної олії, або гліцериди мигдальної олії, подібними, наприклад, PEG-6 лаурат або стеарат, PEG-80 - гідрогенізована касторова олія, PEG-100 PEG-7 олеат або лаурат, PEG-8 лаурат, або оле- касторова олія або гідрогенізована касторова ат, або стеарат, PEG-9 олеат або стеарат, PEG-10 олія, PEG-200 - касторова олія. PEG-8 - каприлолаурат, або олеат, або стеарат, PEG-12 лаурат, ві/капринові гліцериди, PEG-6 каприлоабо олеат, або стеарат, або рицинолеат, PEG-15 ві/капринові гліцериди, лауроїлмакрогол-32 гліцестеарат або олеат. PEG-20 лаурат, або олеат, або рид, стеароїлмакрогол гліцерид, токоферил PEGстеарат, PEG-25 стеарат, PEG-32 лаурат, або 1000 сукцинат (TPGS) (зволожуючі агенти, що наолеат, або стеарат, PEG-30 стеарат, PEG-40 лаулежать до даної групи, відомі, наприклад, як рат, або олеат, або стеарат, PEG-45 стеарат, Emalex, Cremophor, Emulgante, Eumulgin, Nikkol, PEG-50 стеарат, PEG-55 стеарат, PEG-100 олеат Thornley, Simulsol, Cerex, Crovol, Labrasol, Softigen, або стеарат, PEG-200 олеат, PEG-400 олеат, PEGGelucire, вітамін Ε TPGS); 600 олеат (зволожуючі агенти, що належать до f) полігліцеридні похідні жирних кислот, вклюданої групи, відомі, наприклад, як Cithrol, Algon, чаючи ефіри полігліцерину і жирних кислот, такі як, Kessco, Lauridac, Mapeg, Cremophor, Emulgante, наприклад, полігліцерил-10 лаурат, або олеат, або Nikkol, Myrj, Crodet, Albunol, Lactomul); стеарат, полі гліцерил-10 моно- і діолеат, полігліb) діефіри поліетиленгліколю і жирних кислот, церил полірицинолеат і подібні (зволожуючі агенщо включають діефіри лауринової кислоти, стеа 15 92469 16 ти, що належать до даної групи, відомі, наприклад, рним ангідридом; такі як карбоксилати, наприклад, як Nikkol Decaglyn, Caprol або Polymuls); сукцинільовані моногліцериди, стеарилфумарат g) похідні стерину, що включають поліетиленгнатрію, стеароїлпропіленгліколь гідросукцинат, лікольні похідні стерину, такі як PEG-24 холестемоно/діацетильовані складні ефіри винної кислоти риновий ефір, PEG-30 холестанол, PEG-25 фітосі моно- та дигліцеридів, складні ефіри лимонної терин, PEG-30 соєвий стерин і подібні (зволожуючі кислоти і моно- та дигліцеридів, гліцерилагенти, що належать до даної групи, відомі, наприлактоефіри жирних кислот, лактильні ефіри жирних кислот, стеароїл-2-лактилат кальцію/натрію, клад, як Solulan або Nikkol BPSH); стеароїллактилат кальцію/натрію, солі альгінати, h) ефіри поліетиленглікольсорбітану і жирних пропіленглікольальгінат, (простий кислот, такі як, наприклад, PEG-10 сорбітанлаурат, ефір)карбоксилати і подібні; такі як сульфати і суPEG-20 сорбітанмонолаурат, або сорбітантристельфонати, наприклад, етоксильовані алкілсульфаарат, або сорбітанмоноолеат, або сорбітантриоти, алкілбензолсульфати, альфалеат, або сорбітанмоноизостеарат, або сорбітанолефінсульфонати, ацилізетіонати, ацилтаурати, монопальмоат, або сорбітанмоностеарат, PEG-4 алкілгліцериловий ефір сульфонали, динатрійоксорбітанмонолаурат, PEG-5 сорбітанмоноолеат, тилсульфосукцинат, динатрійундециленамідоPEG-6 сорбітанмоноолеат, або сорбітанмонолауМЕА-сульфосукцинат і подібні; такі як катіонні зворат, або сорбітанмоностеарат, PEG-8 сорбітанмоложуючі агенти, наприклад, гексадецилтриамонійностеарат, PEG-30 сорбітантетраолеат, PEG-40 бромід. децилтриметиламонійбромід, цетшпримесорбітанолеат або сорбітантетраолеат, PEG-60 тиламонійбромід, додециламонійхлорид, солі сорбітантетрастеарат, PEG-80 сорбітанмонолауалкілбензилдиметиламонію, солі діізобутилфенократ, PEG сорбітгексаолеат (Atlas G-1086) і подібні сіетоксидиметилбензиламонію, солі алкілпіриди(зволожуючі агенти, що належать до даної групи, нію, бетаїни (лаурилбетаїн), етоксильовані аміни відомі, наприклад, як Liposorb, Tween, Dacol MSS, (поліоксіетилен-15 кокосовий амін) і подібні. Nikkol, Emalex, Atlas); Якщо в приведеному вище списку підходящих і) поліетиленглікольалкілові ефіри, такі як. назволожуючих агентів перераховані різні варіанти, приклад, PEG-10 олеїловий ефір, або цетиловий наприклад, PEG-20 олеїловий ефір або цетиловий ефір, або стеариловий ефір, PEG-20 олеїловий ефір, або стеариловий ефір, це означає, що маефір, або цетиловий ефір, або стеариловий ефір, ється на увазі PEG-20 олеїловий ефір і PEG-20 PEG-9 лауриловий ефір, PEG-23 лауриловий ефір цетиловий ефір, і PEG-20 стеариловий ефір. Та(laureth-23), PEG-100 стеариловий ефір і подібні ким чином, наприклад, вираз «PEG-20 касторова (зволожуючі агенти, що належать до даної групи, олія, або гідрогенізована касторова олія, або глівідомі, наприклад, як Volpo, Brij); цериди кукурудзяної олії, або гліцериди мигдальj) складні ефіри цукрів, такі як, наприклад, дисної олії» варто тлумачити як «PEG-20 касторова теарат/моностеарат сахарози, моностеарат, або олія і PEG-20 гідрована касторова олія, і PEG-20 монопальмітат, або монолаурат сахарози і подібні гліцериди кукурудзяної олії, і PEG-20 гліцериди (зволожуючі агенти, що належать до даної групи, мигдальної олії». відомі, наприклад, як ефір Sucro, Crodesta, моноПереважними зволожуючими агентами в далаурат сахарози); них композиціях є лаурилсульфат натрію, діоктилk) поліетиленглікольалкілфеноли, такі як, насульфосукцинат натрію або такі зволожуючі агенприклад, PEG-10-100 нонілфенол (серії Triton X), тів, що належать до групи ефірів PEG-15-100 октилфеноловий ефір (серії Triton N) і поліетиленглікольсорбігану і жирних кислот, наподібні; приклад, зволожуючі агенти, відомі як Tween, наl) блоккополімери поліоксіетиленприклад, Tween 20, 60, 80. Найбільш переважним поліоксипропілен (полоксамери), такі як, напризволожуючим агентом є Tween 20. клад, полоксамер 108, полоксамер 188, полоксаУ композиціях за даним винаходом зволожуюмер 237, полоксамер 288 і подібні (зволожуючі чий агент переважно присутній при концентрації агенти, що належать до даної групи, відомі, напривід приблизно 0,01 до приблизно 5% мас. щодо клад, як Synperonic ΡΕ, Pluronic, Emkalyx, Lutrol , загальної маси композиції, переважно від приблиSupronic, Monolan, Pluracare, Plurodac); зно 0,1 до приблизно 3% мас., більш переважно m) іонні зволожуючі агенти, включаючи катіонвід приблизно 0,1 до приблизно 1% мас. Кількість ні, аніонні і цвітеріонні поверхнево-активні речовизволожуючого агента, що використовується в дани, такі як солі жирних кислот, наприклад, олеат них композиціях, може залежати від кількості принатрію, лаурилсульфат натрію, лаурилсаркозинат сутньої в композиції сполуки формули (I), (I-а) або натрію, діоктилсульфосукцинат натрію, міристат (І-b) або від розміру часток сполуки формули (I), (Iнатрію, пальмітат натрію, стеарат натрію, рициноа) або (I-b). Більша кількість або менший розмір леат натрію і подібні; такі як жовчні солі, напричасток можуть потребувати більше зволожуючого клад, холат натрію, таурохолат натрію, глікохолат агента. натрію і подібні; такі як фосфоліпіди. наприклад, Згідно з даним винаходом, у випадку твердої яєчний/соєвий лецитин, гідроксильований лецифармацевтичної композиції для перорального тин, лізофосфатидилхолін. фосфати дилхолін, прийому, такої як таблетка або капсула, композифосфати дил етанол амін, фосфатидилгліцерин, ція може також додатково містити органічний пофосфатидилсерин і подібні; такі як складні ефіри лімер. фосфорної кислоти, наприклад, фосфат діетаноОрганічний полімер можна використовувати у ламонійполіоксіетилен-10 олеїлового ефіру, провиробництві композиції як зв'язуючу речовину. дукти етерифікації жирних спиртів або етоксилатів жирних спиртів фосфорною кислотою або фосфо 17 92469 18 Органічний полімер, що використовується у лизно 2,5 і молярного гідроксипропілзаміщення від композиціях за даним винаходом, може бути будьприблизно 0,05 до приблизно 3,0, звичайно є вояким з фізіологічно прийнятних водорозчинних дорозчинними. Ступінь метоксизаміщення вказує синтетичних, напівсинтетичних або несинтетичних середнє число метилефірних груп, що є присутніорганічних полімерів. ми на ангідроглюкозних ланках молекули целюлоТаким чином, полімер може бути, наприклад, зи. Молярне гідроксипропілзаміщення вказує сеприродним полімером, таким як полісахарид або реднє число молів пропіленоксиду, що поліпептид або їх похідні, або синтетичним поліпрореагували з кожною ангідроглюкозною ланкою мером, таким як поліалкіленоксид (наприклад, молекули целюлози. Переважною НРМС є гіпроPEG), поліакрилат, полівінілпіролідон і ін. Звичаймелоза 2910 15 мПа.с або гіпромелоза 2910 5 но, можна також використовувати змішані полімемПа.с, особливо, гіпромелоза 2910 15 мПа.с. Гідри, наприклад, блоккополімери і глікопептиди. роксипропілметилцелюлоза - це прийнята в США Зручно, якщо полімер має молекулярну масу в назва для гіпромелози (див. Martindale. The Extra діапазоні від 500 Да до 2 МДа та структурну в'язPharmacopoeia, 29th edition, page 1435). У чотирикість від 1 до 15000 мПа.с у 2% водному розчині значному номері "2910" перші дві цифри означапри 20 °С Наприклад, водорозчинний полімер моють приблизний процентний вміст метоксигруп, а же бути вибраний з групи, що включає третя і четверта цифри означають приблизний - алкілцелюлози, наприклад, метилцеліюлозу, процентний вміст гідроксипропоксигруп; 15 мПа.с - гідроксіалкілцелюлози, наприклад, гідроксиабо 5 мПа.с є показниками структурної в'язкості метилцелюлозу, гідроксіетилцелюлозу, гідроксип2% водного розчину при 20°С. ролілцелюлозу і гідроксибутилцелюлозу, В підходящих композиціях за даним винахо- гідроксіалкілалкілцелюлози. наприклад, гіддом органічний полімер може бути присутній у роксіетил метил целюлозу і гідроксипропілметил кількості приблизно до 10% мас., переважно від целюлозу, приблизно 0,1 до приблизно 5%, більш переважно - карбоксіалкілцелюлози, наприклад, карбоквід приблизно 0,5 до приблизно 3% мас. (щодо симетилцелюлозу, загальної маси композиції). - солі лужних металів і карбоксіалкілцелюлози, Згідно з даним винаходом, у випадку твердої наприклад, натрій-карбоксиметилцелюлозу, фармацевтичної композиції для перорального - карбоксіалкілалкілцелюлози, наприклад, карприйому, такої як таблетка або капсула, композибоксиметилетилцелюлозу, ція може також додатково містити розріджувач - складні ефіри карбоксіалкілцелюлози, і/або глідант. - крохмалі, Фармацевтично прийнятні розріджувачі вклюпектини, наприклад, натрійчають карбонат кальцію, двоосновний фосфат карбоксиметиламілопектин, кальцію, дигідрат двоосновного фосфату кальцію, - похідні хітину, наприклад, хітозан, триосновний фосфат кальцію, сульфат кальцію, - гепарин і гепариноїди, мікрокристалічну целюлозу, у тому числі силіцифі- полісахариди, наприклад, альгінову кислоту, ковану мікрокристалічну целюлозу, порошкоподібїї солі з лужними металами й амонієм, ну целюлозу, декстрати, декстрин, декстрозний - карагенани, галактоманани, тратакант, агарнаповнювач, фруктозу, каолін, лактитол, безводну агар, аравійську камедь, гуарову смолу і ксантанолактозу, моногідрат лактози, маніт. сорбіти крохву смолу, маль, попередньо желатинізований крохмаль, - поліакрилові кислоти і їх солі, хлорид натрію, сахарозу, пресований цукор, цук- поліметакрилові кислоти і їх солі, метакриларову глазур, висушену розпиленням суміш моногітні кополімери, драту лактози і мікрокристалічної целюлози - полівініловий спирт, (75:25), доступну комерційно як Місrосеlас , спі- полівінілпіролідон, кополімери полівінілпірольно оброблену висушену розпиленням суміш лідону з вінілацетатом, мікрокристалічної целюлози і колоїдного діоксиду - поліалкіленоксиди, наприклад, поліетиленоккремнію (98:2), доступну комерційно як Prosolv . сид і поліпропіленоксид, і кополімери етиленоксиПереважними ε моногідрат лактози, мікрокристаліду і пропіленоксиду, наприклад, полоксамери і чна целюлоза або силіцифікована мікрокристалічполоксаміни. на целюлоза. Для приготування композицій за даним винаФармацевтично прийнятні гліданти включають ходом також підходять полімери, що не були петальк, колоїдний діоксид кремнію, крохмаль, стеарераховані, які є фармацевтично прийнятними і рат магнію. Переважним є колоїдний діоксид кремають підходящі фізико-хімічні властивості, що мнію. визначені вданій заявці вище. У випадку таблеток, композиція може також Переважними органічними полімерами є крододатково містити розпушувач і лубрикант. хмаль, полівінілпіролідон або прості ефіри целюФармацевтично прийнятні розпушувачі вклюлози, наприклад, PVP K29-32, PVP K90, метилцечають крохмаль, іонообмінні смоли, наприклад, люлоза, гідроксипропілцелюлоза, Ambeilite. зшитий полівінілпіролідон, модифіковану гідроксіетилметилцелюлоза або гідроксипропілмецелюлозну смолу, наприклад, натрійтил целюлоза (НРМС). кроскармелозу (наприклад, Ac-di-Sol ), натрійЗазначена НРМС містить достатню кількість крохмальгліколят, натрій-карбоксиметилцелюлозу, гідроксипропільних груп і метоксигруп для забездодецилсульфат нагрію, модифікований кукурупечення розчинності у воді. НРМС, що мають студзяний крохмаль, мікрокристалічну целюлозу, мапінь метоксизаміщення від приблизно 0,8 до приб 19 92469 20 гнійалюмінійсилікат, альгінову кислоту, альгінат, (ііі) пресування таблеток із суміші, отриманої порошкоподібну целюлозу. на стадії (і) або на стадії (іі), у сухому стані; і Фармацевтично прийнятні лубриканти вклю(iv) необов'язкове нанесення плівкового покчають стеарат магнію, стеарат кальцію, стеаринориття на таблетку, отриману на стадії (ііі). ву кислоту, тальк, поліетиленгліколь, лаурилсульДаний винахід також відноситься до способу фат натрію, лаурилсульфат магнію. одержання таблетки, що містить сполуку формули Крім того, таблетки за даним винаходом мо(І), (I-а) або (І-b), що включає наступні стадії: жуть включати інші необов'язкові наповнювачі, такі (і) сухе перемішування активного інгредієнта і як, наприклад, ароматизатори, підсолоджувачі і частини розріджувача; барвники. (іі) одержання сполучного розчину за допомоТверді фармацевтичні композиції відповідно гою розчинення зв'язуючого і зволожуючого агента до даного винаходу можуть включати на масу, в розчиннику для сполучного розчину; базуючись на загальній масі композиції: (ііі) розпилення сполучного розчину, отримано(a) від 5 до 50% сполуки формули (І), (I-а) або го на стадії (іі), на суміш, отриману на стадії (і); (І-b); (iv) сушіння вологого порошку, отриманого на (b) від 0,01 до 5% зволожуючого агента; стадії (ііі), з наступним просіванням і необов'язково (c) від 40 до 92% розріджувача; перемішуванням; (d) від 0,1 до 5% гліданта. (ν) змішування частини розріджувача, що заТаблетки відповідно до даного винаходу молишилася, розпушувача і необов'язкового гліданта жуть включати на масу, базуючись на загальній із сумішшю, отриманою на стадії (iv); масі композиції: (vi) необов'язкове додавання лубриканта до (a) від 5 до 50% сполуки формули (І), (I-а) або суміші, отриманої на стадії (ν); (І-b); (vii) пресування таблеток із суміші, отриманої (b) від 0,01 до 5% зволожуючою агента; на стадії (vi); (c) від 40 до 92% розріджувача; (viii) необов'язкове нанесення плівкового пок(d) від 0 до 10% полімеру; риття на таблетку, отриману на стадії (vii). (e) від 2 до 10% розпушувача; Фахівець у даній галузі розпізнає найбільш пі(f) від 0,1 до 5% гліданта; дходяще устаткування, яке варто використовувати (g) від 0,1 до 1,5% лубриканта. для описаних вище способів. Фахівець у даній гаНа таблетки за даним винаходом необов'язколузі може модифікувати описаний вище загальний во можна нанести плівкове покриття, слідуючи спосіб одержання таблеток за даним винаходом, відомим у даній галузі методикам нанесення покнаприклад, додаючи деякі інгредієнти на інших риття. Таблетки з плівковим покриттям легше ковстадіях, ніж вказані вище. тати, ніж непокриті ядра таблеток, звичайно їх леДану сполуку формули (І), (I-а) або (І-b) можна гше відрізнити від інших таблеток (зокрема, якщо використовувати саму по собі або в комбінації з плівкові покриття містять барвник або пігмент), іншими терапевтичними агентами, такими як антивони можуть мати знижену липкість і, крім того, вірусні агенти, антибіотики, імуномодулятори або мати підвищену стабільність (збільшений термін вакцини для лікування вірусних інфекцій. Їх можна зберігання), наприклад, завдяки тому, що покриття також використовувати самі по собі або в комбінаможе захищати активний інгредієнт від впливу ції з іншими профілактичними агентами для просвітла. Переважно, щоб плівкове покриття являло філактики вірусних інфекцій. Дані сполуки можна собою покриття для швидкого вивільнення. Пліввикористовувати у вакцинах і способах для захискові покриття можуть включати плівкоутворюючий ту індивідуумів від вірусних інфекцій протягом триполімер і необов'язково пластифікатор або пігвалого періоду часу. Сполуки можна використовумент. Прикладом підходящого плівкоутворюючого вати в таких вакцинах самі по собі або разом з полімеру є гідроксипропілметилцелюлоза, і прикіншими антивірусними агентами способом, що ладом підходящого пластифікатора є поліетиленгузгоджується зі звичайним застосуванням інгібітоліколь, наприклад, макрогол 3000 або 6000 або рів зворотної транскриптази у вакцинах. Таким триацетин. Комерційно доступні підходящі покритчином, дані сполуки можна поєднувати з фарматя для фармацевтичних таблеток добре відомі цевтично прийнятними ад'ювантами, що звичайно фахівцю в даній галузі. Переважно, щоб плівкове використовуються у вакцинах, і вводити в профіпокриття було непрозорим плівковим покриттям. лактично ефективних кількостях для захисту індивідуумів протягом тривалого періоду часу від ВІЛПрикладом підходящого покриття є Opadry , зокінфекції. рема, порошкове покриття Opadry II White. Також можна використовувати як лікарський Таблетки за даним винаходом можна одержазасіб комбінацію антиретровірусної сполуки і споти прямим пресуванням або вологим гранулюванлуки формули (І), (I-а) або (І-b). Таким чином, даням. ний винахід відноситься також до продукту, що Таким чином, даний винахід відноситься також містить (а) сполуку формули (І), (I-а) або (I-b) i (b) до способу одержання таблетки, що містить споодну або декілька інших антиретровірусних сполук, луку формули (I), (I-а) або (І-b), який включає наяк комбінований препарат для одночасного, роздіступні стадії: льного або послідовного застосування при анти(і) сухе перемішування активного інгредієнта, ВІЛ-лікування. Зокрема, даний винахід відноситься розпушувача і необов'язковою гліданта з розрітакож до продукту, що містить (а) сполуку формуджувачем; ли (I), (I-а) або (I-b), і (b) одну або декілька інших (іі) необов'язкове змішування лубриканта із антиретровірусних сполук, як комбінований препасумішшю, отриманою на стадії (і); 21 92469 22 рат для одночасного, роздільного або послідовноваючи на антивірусну активність агентів. Дані комго застосування при анти-ВІЛ-лікуванні, за умови, бінації знижують можливості резистентності до що зазначені одна або декілька інших антиретротерапій із застосуванням одного агента, при цьому вірусних сполук відмінні від нуклеозидних інгібітознижуючи до мінімуму будь-яку асоційовану токсирів зворотної транскриптази і/або нуклеотидних чність. Дані комбінації можуть також збільшити інгібіторів зворотної транскриптази. Різні ліки можефективність звичайного агента без підвищення на поєднувати в єдиному препараті разом з фарасоційованої токсичності. мацевтично прийнятними носіями. Таким чином, Сполуки за даним винаходом можна також даний винахід також відноситься до фармацевтиприймати в комбінації з імуномодулючими агентачної композиції, що містить фармацевтично прими, наприклад, левамізолом, бропіриміном, антийнятний носій, (а) терапевтично ефективну кільтілом проти людського альфа-інтерферону, інтеркість сполуки формули (І), (I-а) або (I-b) і (b) один ферон-альфа, інтерлейкіном 2, метіонін або декілька антиретровірусних агентів. енкефаліном, діетилдитіокарбаматом, фактором Зазначені інші антиретровірусні сполуки монекрозу пухлини, налгрексоном і подібними; антижуть являти собою відомі антиретровірусні сполубіотиками, наприклад, пентамідин ізетіоратом і ки, такі як сурамін, пентамідин, тимопентин, кастаподібними; холінергічними агентами, наприклад, носпермін. декстран (декстрансульфат), такрином, ривастигміном, донепезилом, галантафоскарнет-натрій (тринатрійфосфоноформіат); міном і подібними; NMDA-блокаторами каналів, нуклеозидні інгібітори зворотної транскриптази, наприклад, мемантином, для профілактики або наприклад, зидовудин (3'-азидо-3'-деокситимідин, боротьби з інфекціями, захворюваннями або симAZT), диданозин (2',3'-дидеоксіінозин; dd), зальциптомами захворювань, пов'язаними з ВІЛтабін (дидеоксицитидин, dd) або ламівудин (2'-3'інфекціями, такими як СНІД і ARC. наприклад, дідеокси-3'-тіацитидин, ЗТС), ставудин (2',3'слабоумством. дидегідро-3'-деокситимідин, d4T), абакавір, абакаХоча даний винахід фокусується на застосувірсульфат, емтрицигабін ((-)FTC), рацемічний ванні даних сполук з метою профілактики або ліFTC і подібні; ненуклеозидні інгібітори зворотної кування ВІЛ-інфекцій, дані сполуки можна також транскриптази, такі як невірапін (11-циклопропілвикористовувати як інгібуючі агенти для інших ві5,11-дигідро-4-метил-6Н-дииіридо-[3,2-b:2',3'русів, що залежать від тих же зворотних транскрие][1,4]діазепін-6-он), ефавіренц, делавірдин, ТМСптаз для обов'язкових подій у їх життєвому циклі. 120, ТМС-125 і подібні; сполуки ТІВО (тетрагідроіЕкспериментальна частина мідазо[4,5,1-jk][1,4]-бензодіазепіин-2(1Н)-он і A. Синтез сполуки формули (I-а) тіон)тип, наприклад, (S)-8-хлор-4,5,6.7-тетрагідроОдин моль вільної основи (Е) 4-[[4-[[4-(25-метил-6-(3-метил-2-бутеніл)імідазо-[4,5,1ціаноетеніл)-2,6-диметилфеніл]аміно]-2jk][1,4]бензодіазепін-2(1Н)-тіон; сполуки типу (-АРА піримідиніл]аміно]бензонітрилу розчиняють в оц((-анілінофенілацетаміду), наприклад, (-[(2товій кислоті (2 л/моль при 80-100°С). Додають 1,2 нітрофеніл)аміно]-2,6-дихлорбензолацетамід і помоль фумарової кислоти. Додають порціями воду дібні; інгібітори білків, що транс-активують, такі як (2 л/моль) при 60-70°С. Суміш перемішують протяТАТ-інгібітори, наприклад, RO-5-3335, або REVгом ночі при кімнатній температурі. Осад відфільтінгібітори і подібні; інгібітори протеази, наприклад, ровують, двічі промивають водою і сушать у вакуіндинавір, ритонавір, саквінавір, лопінавір (АВТумі при 50°С, одержуючи 90% сполуки формули (I378), нелфінавір, ампренавір, ТМС-114, BMSа). 232632, VX-175 і подібні; інгібітори злиття, наприB. Дані з розчинності клад, Т-20, Т-1249 і подібні; антагоністи рецепторів В таблиці 1 представлені дані з розчинності CXCR4, наприклад, AMD-3100 і подібні; інгібітори вільної основи (Е) 4-[[4-[[4-(2-ціаноетеніл)-2,6вірусної інтегрази; інгібітори зворотної транскрипдиметилфеніл]аміно]-2тази нуклеотидного типу, наприклад, тенофовір, піримідиніл]аміно]бензонітрилу і сполуки формули тенофовір дифосфат, тенофовір дизопроксил фу(I-а). марат і подібні; інгібітори рибонуклеотидної редуктази, наприклад, гідроксикарбамід і подібні; CCR5 Таблиця 1 антагоністи, наприклад, анкривірок, аплавірок гідрохлорид, вікривірок. Концентрація в мг/мл При введенні сполуки за даним винаходом з Сполука 0,01 N PEG Вода іншими антивірусними агентами, метою яких є HCl 400 різні події у вірусному життєвому циклі, можна підВільна основа (Е-ізомер) 0,00002 0,019 40 силити терапевтичний ефект даних сполук КомбіСполука формули (I-а) 0,0009 0,013 наційні терапії, що описані вище, здійснюють синергічний ефект при інгібуванні ВІЛ-реплікації, Вільна основа, а також сіль фумарат мають завдяки тому, що кожен компонент комбінації діє слабку розчинність у воді, а також у 0,01 IN HCl. на різні сайти ВІЛ реплікації. Використовуючи такі Вільну основу і сіль фумарат можна класифікувати комбінації, можна зменшити дозування прийнятого як сполуки BCS-класу 2. Розчинність вільної оснозвичайного антиретровірусного агента, що потрібви істотно підвищується в PEG 400. но для досягнення бажаного терапевтичного або С. Дані зі стабтьності профілактичною ефекту, у порівнянні з введенням а) Хімічна стабільність даного агента при монотерапії. Дані комбінації Сполуку (I-а) зберігали в різних умовах воломожуть знизити або виключити побічні ефекти гості і температури. Після збереження сіль аналізвичайної антиретровірусної монотерапії, не впли 23 92469 зували методом високоефективної рідинної хроматографії (ВЕРХ) на вміст домішок. Результати наведені в таблиці 2 нижче. Можна зробити висновок, що сполука формули (I-а) є хімічно стабільною. Таблиця 2 Умови збере- Сума домішок, % (%, мас./мас.) ження 1 тиждень 4 тижні 8 тижнів Контроль 0,58 40°С/75% ВВ 0,62 0,61 50°С/повітря 0,62 0.61 КТ/
ДивитисяДодаткова інформація
Назва патенту англійськоюFumarate of 4-[[4-[[4-(2-cyanoethenyl)-2,6-dimethylphenyl]amino]-2-pyrimidinyl amino benzonitrile
Автори англійськоюStevens Paul Theodoor Agnes, Peeters Jozef, Vandecruys Roger Petrus Gerebe, Stappers Alfred Elisabeth, Copmans Alex Herman
Назва патенту російськоюФумарат 4-[[4-[[4-(2-цианоэтенил)-2,6-диметилфенил]амино]-2-пиримидинил]амино]бензонитрила
Автори російськоюСтевенс Поль Теодоор Агнес, Пеетерс Йозеф, Вандекрюйс Роже Петрус Гереберн, Стапперс Альфред Элизабет, Копманс Алекс Герман
МПК / Мітки
МПК: A61K 31/505, A61P 31/18
Мітки: 4-[[4-[[4-(2-ціаноетеніл)-2,6-диметилфеніл]аміно]-2-піримідиніл]аміно]бензонітрилу, фумарат
Код посилання
<a href="https://ua.patents.su/15-92469-fumarat-4-4-4-2-cianoetenil-26-dimetilfenilamino-2-pirimidinilaminobenzonitrilu.html" target="_blank" rel="follow" title="База патентів України">Фумарат 4-[[4-[[4-(2-ціаноетеніл)-2,6-диметилфеніл]аміно]-2-піримідиніл]аміно]бензонітрилу</a>
Попередній патент: Спосіб виробництва квасу
Наступний патент: Стабільний при зберіганні інфузійний розчин дигідроптеридинонів
Випадковий патент: Спосіб оцінки гігієнічного стану порожнини рота












