Донепезилу фумарат, придатний для отримання фармацевтичних композицій
Номер патенту: 88481
Опубліковано: 26.10.2009
Автори: Хофманне Фекете Валерія, Порч-Маккай Марта, Волк Балаж, Сіміг Дюла, Молнар Еніко, Месей Тібор, Лукаш Дьюла
Формула / Реферат
1. Сіль приєднання кислоти донепезилу [(±)-2-[(1-бензил-4-піперидиніл)метил]-5,6-
диметокси-1-інданону] загальної формули (II)
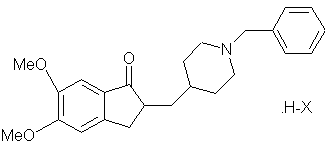 ,
,
де X позначає радикал фумарової кислоти, що одержується шляхом реакції основи донепезилу в етанолі або 2-пропанолі, як розчинника фумарової кислоти, відокремлення одержаної при цьому солі донепезилу і, можливо, промивання її органічним розчинником.
2. Сіль приєднання кислоти донепезилу за п. 1, яка відрізняється тим, що вона являє собою донепезилу фумарат (1 : 1).
3. Сіль приєднання кислоти донепезилу за будь-яким з пп. 1, 2, яка по суті не містить (±)-2-[(1-бензил-4-піперидиніл)метил]-5-гідрокси-6-метокси-1-інданону формули (III)
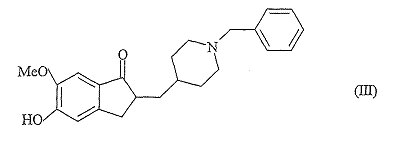 .
.
4. Сіль приєднання кислоти донепезилу за п. 1, яка відрізняється тим, що фумарова кислота використовується в кількості 1,0-1,3 молярних еквіваленти, переважно 1,0 молярний еквівалент.
5. Фармацевтична композиція, що включає як активний інгредієнт сіль донепезилу за будь-яким з пп. 1-4 разом з одним або більше носієм(ями) або допоміжною речовиною(ми), звичайно застосовуваними у фармацевтичній промисловості.
6. Спосіб отримання фармацевтичної композиції за п. 5, який включає змішування сполуки загальної формули (II) за будь-яким з пп. 1-4 з фармацевтично прийнятним носієм і, можливо, з іншою допоміжною речовиною, і виготовлення з одержаної суміші галенової форми.
7. Застосування солі приєднання кислоти донепезилу за будь-яким з пп. 1-4 для отримання фармацевтичної композиції, придатної для профілактики або лікування захворювань, пов'язаних з дефіцитом в головному мозку ацетилхоліну, хвороби Альцгеймера або старечого недоумства.
Текст
1. Сіль приєднання кислоти донепезилу [(±)-2[(1-бензил-4-піперидиніл)метил]-5,6диметокси-1-інданону] загальної формули (II) UA 1 Даний винахід відноситься до солей донепезилу, придатних для отримання фармацевтичних композицій. Крім того, даний винахід також відноситься до способу отримання вказаних солей, фармацевтичних композицій, що містять їх, і до застосування вказаних сполук для лікування хвороб. Конкретніше, даний винахід відноситься до солей 1-бензил-4-[(5,6-диметокси-1-інданон-2-іл)метил]-піперидину (міжнародна непатентована назва: донепезил) формули (І): 3 88481 4 сі Угорського патенту №211165. Були винайдені ще чотири поліморфні кристалічні форми хлористоводневої солі цього активного інгредієнта, і згідно них була подана заявка на патент. Вказані кристалічні форми, відмінні від визначених основним патентом, запропоновані в Міжнародній заявці на патент № WO97/46526. Ліки, що поступають в продаж, повинні відпоутворений з органічними кислотами загальної відати численним вимогам різних організацій. Відформули Н-Х, де X означає радикал органічної повідність вказаним вимогам, все більш і більш кислоти. жорсткою, повинна бути підтверджена відповідниДонепезил є компонентом фармацевтичних ми документами. Частина цих вимог відноситься композицій для лікування старечого недоумства, до активного інгредієнта, інша частина - до фарякий використовують у формі гідрохлориду для мацевтичної композиції, і всі ці вимоги строго взаприготування ліків. ємопов'язані при розробці композиції і складання Швидке зростання частки людей похилого віку ринкової документації. серед населення вимагає розробки дієвих спосоОдні з найжорсткіших вимог щодо фармацевбів лікування і профілактики розвитку старечого тично активних інгредієнтів відносяться до чистоти недоумства, що виникає, наприклад, унаслідок препарату. В більшості випадків активні інгредієнхвороби Альцгеймера. ти є органічними основами, що мають велику моПроводилося випробування різних інгредієнтів лекулярну масу, які нерозчинні у воді і не змочудля лікування недоумства, але при їх застосуванні ються водою. Гідрофобні властивості активного вдалося досягти лише часткового успіху. Проте інгредієнта викликають утруднення, особливо при було відмічено, що в організмі пацієнтів з хворостворенні лікарських форм. Представляється добою Альцгеймера концентрація ацетилхоліну знацільним перевести основний активний інгредієнт у чно нижча, ніж у здорових людей. На цій підставі форму солі з фармацевтично прийнятною органічможна зробити висновок про те, що спосіб лікуною сіллю і далі використовувати одержану таким вання вказаного захворювання може полягати у чином сіль для отримання фармацевтичної комповведенні ліків, що підвищують рівень ацетилхолізиції. Додаткова перевага застосування солей пону, особливо, в мозку. На практиці були запрополягає в тому, що вони краще розчинні у воді і нановані два шляхи, що ведуть до цієї мети. багато краще змочуються водою, ніж відповідні Згідно одного з цих двох рішень, в організм основи. Крім того, через їхню високу температуру вводять попередників ацетилхоліну, з яких в реплавлення порівняно з основами, їх можливо прозультаті складних біохімічних перетворень вихосто і ефективно очистити. дить ацетилхолін. Таким чином, такі речовини моНайважливіша вимога до фармацевтичних жуть бути віднесені до проліків. При їх введенні композицій, що потрапляють на ринок, полягає в може бути досягнута підвищена концентрація ацетому, що вони повинні залишатися стабільними тилхоліну в організмі. при випробуванні відповідно до фармакопейних Згідно іншого рішення, в організм доставляють вимог. Стабільність має на увазі, що зниження речовину, що інгібує фермент, який відповідає за активності активного інгредієнта у фармацевтичній розпад ацетилхоліну, тобто так званий інгібітор композиції в ході виробництва або зберігання не ацетилхолінестерази. При цьому пригнічується перевищує допустимого рівня. розпад ацетилхоліну. Такими інгібіторами ацетилУнаслідок різного роду механічних дій і нагріхолінестерази є фазостигмін і тетрагідроакридин. вання, що має місце в ході виробництва фармацеЦі речовини, проте, володіють небажаною побічвтичних композицій є складним завданням. При ною дією, оскільки вони пригнічують розпад ацеотриманні фармацевтичних композицій часто витилхоліну не тільки в мозку, але і у всьому органікористовують речовини, що служать для утворензмі. ня великої специфічної поверхні і, можливо, що Донепезил представляє собою перший могутнабрякають при дії вологості. На великій поверхні ній і високовідбірний фармацевтичний інгредієнт деякі хімічні процеси, такі як, наприклад, небажані тривалої дії, що інгібує ацетилхолінестеразу, який реакції розпаду, окислення або гідролізу, можуть підвищує рівень ацетилхоліну в мозку в значно прискорюватися, оскільки в таких випадках активбільшому ступені, ніж в інших частинах організму. ний інгредієнт входить в контакт з повітрям і волоЕфективність цієї речовини у разі втрати пам'яті, а гою на великій поверхні. Це, зокрема, має місце, також його переваги перед фазостигміном при якщо застосовуються фармацевтичні інгредієнти з клінічному застосуванні були доведені експеримемалим розміром частинок, наприклад, активний нтально. інгредієнт в тонкоподрібненому вигляді. Донепезил придатний для лікування і профілаДля того, щоб довести стабільність фармацектики захворювань головного мозку, які можуть втичних композицій, їх піддають строгим випробубути пов'язані з недоліком ацетилхоліну. Такі заванням згідно вимог організацій, що видають ліцехворювання включають, наприклад, хворобу Альцнзії, беручи до уваги, що реакції розкладання геймера, синдром Гентінгтона, атаксію або хворомайже ніколи не можуть бути передбачені напебу Піка. ред. Важливою частиною випробувань на стабільДонепезил запропонований в описі Угорського ність є витримка фармацевтичної композиції при патенту №214592. Застосування в медицині його постійній високій температурі (між 50°С і 70°С) в солі, утвореної з хлоридом водню, розкрито в опиумовах високої вологості, визначення вмісту акти 5 88481 6 вного інгредієнта через певні проміжки часу (звинепезилу з неорганічними кислотами, також має чайно через декілька місяців) і проведення кількісмісце і в специфічних умовах, характерних для ного і якісного аналізу домішок, що утворилися в пігулок. З метою порівняння, відповідно до порівкомпозиції внаслідок процесів розкладання. Для няльних Прикладів 1 і 2 (див. нижче) також були цього визначають структуру найважливіших доміодержані солі донепезилу, утворені з бромоводнешок, присутність яких очікується в кількості, що вою і сірчаною кислотами. Виявилось, що стабільперевищує певний рівень, і з них синтезують зраність пігулок, приготовлених з цих солей, практичзок, придатний як еталонна речовина. но така ж, як у разі пігулок, приготовлених з При випробуваннях стабільності пігулок, що хлористоводневої солі. містять донепезилу гідрохлорид, виявляються деМетою даного винаходу було отримання солей які домішки, присутні в різних концентраціях, які донепезилу, придатних для отримання стабільних можуть бути визначені за допомогою масфармацевтичних композицій, що по суті не містять спектрометрії (МС), ідентифіковані, та їхня концен(±)-2-[(1-бензил-4-піперидил)метил]-5-гідрокси-6трація може бути визначена високоефективною метокси-1-інданону формули (III). рідинною хроматографією (ВЕРХ). Даний винахід заснований на несподіваному Щоб довести, що домішка з ідентифікованою відкритті того, що якщо для отримання пігулок виструктурою і синтезована порівняльна речовина користовують сіль донепезилу, утворену з органічідентичні, необхідно провести окремі дослідження, ною кислотою, сполука формули (III) не виявляє в такі як МС або зв'язана МС-ВЕРХ. ході випробувань стабільності. В ході випробувань на стабільність пігулок, що Згідно одного з аспектів даного винаходу, замають різний склад, і що містять при цьому як акпропоновані солі донепезилу загальної формули тивний інгредієнт донепезилу гідрохлорид, у ви(II) пробовуваних зразках можуть бути виявлені різні Де X позначає радикал органічної кислоти, тадомішки. Автори даного винаходу визначили мокий як мурашина, оцтова, лярну масу таких домішок за допомогою масспектрометрії (МС). На підставі масспектрометричного дослідження було висловлено припущення, що однією з таких домішок є сполука формули (III) що утворюється з донепезилу в результаті часткового деметилування. Автори даного винаходу синтезували (±)-2-[(1-бензил-4-піперидил)метил]-5гідрокси-6-метокси-1-індан формули (III), і продемонстрували методом ВЕРХ, що та ж сама речовина утворюється в ході випробувань на стабільність пігулок, що містять донепезилу гідрохлорид. При вивченні технічної літератури було виявлено, що ароматичні метоксигрупи в ортоположенні, що є і в молекулі донепезилу, схильні до часткового гідролізу у присутності сильної неорганічної кислоти. Деметилування ароматичних метоксипохідних здійснюють у присутності соляної кислоти [Pyman J. - J. chem. Soc. 97, 275 (1910)] або у присутності бромистого водню в оцтовій кислоті [Tomit et al. - Yakugaku Zasshi 76, 1122 (1956)] при підвищеній температурі. У жорстких умовах звичайно відщеплюються обидві метоксигрупи, але, несподіваним чином, одна з метоксигруп в орто-положенні деметилується з утворенням гідроксигрупи навіть в дуже м'яких умовах, залежно від заступників при ароматичному кільці. Відносно літератури, часткове деметилування ароматичних метоксигруп в орто-положенні у присутності неорганічних кислот може відбуватися навіть при кімнатній температурі [Blasky G et al. - Tetrahedron Lett. 22, 3135-3138 (1981)]. Процес ортодеметилування, який відбувається при реакції до пропіонова, малеїнова, фумарова, янтарна, молочна, яблучна, винна, лимонна, аскорбінова, малонова, щавелева, мигдалева, гліколева, фталева, бензолсульфонова, толуолсульфонова, нафталінсульфонова або метансульфонова кислота, переважно фумарова, малеїнова, метансульфонова, бензолсульфонова або толуолсульфонова кислота, що приводить до вищих показників стабільності в порівнянні з солями донепезилу, утворених з неорганічними кислотами, відомими з літератури. З числа солей донепезилу, утворених, відносно до даного винаходу, з органічними кислотами, найкращими характеристиками володіє сіль фумарової кислоти. Фізичні властивості, стабільність і розчинність цієї солі особливо переважні для отримання фармацевтичних композицій. Розчинність цієї солі у воді практично ідентична розчинності хлористоводневої солі, відомої з літератури. Температура її плавлення складає близько 150°С, що особливо переважно при виготовленні лікарських форм, таких як пігулки. Фумарат донепезилу за винаходом по суті не містить домішки формули (III). Згідно іншого аспекту даного винаходу, запропонований спосіб отримання солей донепезилу загальної формули (II), утворених з органічними кислотами, який включає реакцію основи донепезилу у придатному органічному розчиннику з бажаною органічною кислотою, виділення солі донепезилу, що кристалізується, і, можливо, промивання її яким-небудь органічним розчинником. Як розчинник можуть використовувати С1-4спирт, простий або складний ефір, переважно діе 7 88481 8 тиловий ефір, етилацетат, метанол, етанол, 2цитратний, фосфатний буфери) і консерванти (напропанол або їхню суміші. приклад, метил-4-гідроксибензоат і т.п.) Органічну кислоту, що використовується для Рідкі фармацевтичні композиції для парентеутворення солі, беруть в кількості 1,0-1,3 молярних рального введення звичайно є стерильні ізотонічні еквівалента, переважно в еквімолярній кількості, розчини, буферні агенти, що іноді містять крім по відношенню до кількості основи донепезилу. розчинника, і консерванти. Згідно ще з одного аспекту даного винаходу, М'які фармацевтичні композиції, що містять як запропоновані фармацевтичні композиції, що місактивний інгредієнт сполуку загальної формули (І) тять як активний інгредієнт сполуку загальної фоабо його фармацевтично прийнятні солі приєдрмули (II) в суміші з одним або декількома носіями нання кислоти, такі як супозиторії, містять активабо допоміжними речовинами, вживаними у фарний інгредієнт, рівномірно розподілений в основмацевтичній промисловості. Фармацевтичні комному матеріалі супозиторія (наприклад, в поліетиленгліколі або маслі какао). позиції за даним винаходом по суті не містять (±)Фармацевтичні композиції за даним винахо2-[(1-бензил-4-піперидил)метил]-5-гідрокси-6дом, що містять сполуку загальної формули (II) метокси-1-інданону формули (III). можуть бути виготовлені відомими у фармацевтиЗгідно ще одного аспекту даного винаходу, зачній промисловості способами. Активний інгредіпропонований спосіб отримання фармацевтичних єнт змішують з фармацевтично прийнятними рідкомпозицій, які містять як активний інгредієнт сіль кими або твердими носіями і/або допоміжними донепезилу загальної формули (II), що включає речовинами, і з одержаної суміші виготовляють змішування вказаного активного інгредієнта з одгаленову форму. Носії і допоміжні речовини, а таним або декількома носіями або допоміжними рекож методи, які можуть застосовуватися у фармачовинами, прийнятими у фармацевтичній промисцевтичній промисловості, описані в літературі ловості, і виготовлення з одержаної суміші [Remington. Pharmaceutical Scienses, - Edition 18, галенової форми. Mack Publishing Co., Easton, USA, 1990]. Фармацевтичні композиції за даним винахоФармацевтичні композиції за даним винаходом звичайно містять 0,1-95мас.%, переважно 1дом звичайно містять одиницю дози активного 50мас.%, особливо переважно 5-30мас.% активноінгредієнта загальної формули (II). го інгредієнта. Згідно ще одного аспекту даного винаходу, заФармацевтичні композиції за даним винахопропоновано застосування сполук загальної фордом можуть бути призначені для перорального мули (II) як фармацевтичні інгредієнти. (наприклад, порошки, пігулки, пігулки, покриті обоДалі винахід докладніше проілюстровано нижлонкою; капсули, мікрокапсули, пілюлі, розчини, ченаведеними Прикладами, що не обмежують суспензії або емульсії), парентерального (наприйого об'єм охорони. клад, розчини для внутрішньовенного, внутріПриклад 1. шньом'язового, підшкірного або внутрішньочереОтримання донепезилу фумарату. винного введення), ректального (наприклад, В устаткуванні, що забезпечує інтенсивне песвічки), крізьшкірного (наприклад, пластири) або ремішування, відмірювали 550мл безводого етизовнішнього (наприклад, мазі або пластири) ввелового спирту, в якому при перемішуванні розчидення або для застосування у вигляді імплантата. няли 38,0г (0,10моль) основи донепезилу. До Тверді, м'які або рідкі фармацевтичні композиції за одержаного розчину додавали 11,6г (0,10моль) даним винаходом можуть бути виготовлені спософумарової кислоти при 60°С, розчин нагрівали до бами, прийнятими у фармацевтичній промисловості. кипіння, освітлювали 2,5г активованого вугілля і Тверді фармацевтичні композиції для перораостуджували при кімнатній температурі протягом льного введення, що містять сполуки загальної 2-х годин. Кристалізація починалася при 60°С. формули (І) або його фармацевтично прийнятні Одержану суспензію перемішували при 0°С протясолі приєднання кислоти, можуть містити наповгом 2-х годин, осад відокремлювали фільтруваннювачі або носії (такі як лактоза, глюкоза, крохням і промивали на фільтрі етиловим спиртом, що маль, фосфорнокислий кальцій, мікрокристалічна має температуру 0°С, до звільнення від маткового целюлоза), зв'язуючі речовини (такі як желатин, розчину. сорбіт, полівінілпіролідон) розпушувачі (такі як Вихід : 47,2г (95,4%) білих кристалів кроскармелоза, Na-карбоксиметилцелюлоза, кроТемпература плавлення: 170-171°С сповідон), допоміжні речовини для таблетування Аналітично обчислено для формули (такі як стеарат магнію, тальк, поліетиленгліколь, C24H29NO3×C4H4O4 (4955): кремнієва кислота, діоксид кремнію) і поверхневоРозрахунок: 67,86% С; 6,71% Н; 2,83% N активні речовини (наприклад, лаурилсульфат наДосвід: 67,74% С; 6,65% Н; 2,83% N трію). За даними ВЕРХ чистота продукту складала Рідкі композиції для перорального введення, 99,8%. що містять сполуки загальної формули (II), можуть Приклад 2. бути розчини, суспензії або емульсії. Такі композиОтримання донепезилу малеінату. ції можуть містити суспендуючі агенти (наприклад, В устаткуванні, що забезпечує інтенсивне пежелатин, карбоксиметилцелюлоза), емульгатори ремішування, відмірювали 100мл 2-пропанолу, в (наприклад, сорбітан моноолеат), розчинники (наякому при перемішуванні розчиняли 7,6г приклад, вода, масла, гліцерин, пропіленгліколь, (20ммоль) основи донепезилу. До одержаного етанол), буферні агенти (наприклад, ацетатний, розчину додавали 2,32г (20ммоль) малеїнової кислоти при 60°С, розчин нагрівали до кипіння, осві 9 88481 10 тлювали активованим вугіллям і остуджували при фільтрі етилацетатом, що має температуру 0°С, кімнатній температурі протягом 1 години. Одержадо звільнення від маткового розчину. ну суспензію перемішували при 0°С протягом 2-х Вихід : 9,29г (84,2%) білих кристалів годин, осад відокремлювали фільтруванням і проТемпература плавлення: 171-173°С мивали на фільтрі етилацетатом, що має темпеАналітично обчислено для формули ратуру 0°С, до звільнення від маткового розчину. C31H37NO6S (551,7): Вихід : 9,04г (91,2%) білих кристалів Розрахунок: 67,49% С; 6,76% Н; 2,54% N; 5,81% S Температура плавлення: 116-118°С Досвід: 67,54% С; 6,83% Н; 2,54% N; 5,76% S Аналітично обчислено для формули Приклад 6. C24H29NO3×C4H4O4 (495,5): Отримання (±)-2-[(1-бензил-4Розрахунок: 67,86% С; 6,71% Н; 2,83% N піперидиніл)метил]-5-гідрокси-6-метокси-1Досвід: 67,24% С; 6,85% Н; 2,79% N інданона гідрохлориду [сполуки формули (III)]. За даними ВЕРХ чистота продукту складала 7,6г (20ммоль) основи донепезилу перемішу99,8%. вали в суміші 50мл 48%-ного водного розчину Приклад 3. бромистого водню і 10мл оцтової кислоти на водяОтримання донепезилу метансульфоната. ній лазні протягом 20-ти годин. Потім розчин вилиВ устаткуванні, що забезпечує інтенсивне певали на 500г льоду, нейтралізували вуглекислим ремішування, відмірювали 100мл 2-пропанолу, в калієм, продукт екстрагували етилацетатом, і виякому при перемішуванні розчиняли 7,6г паровували розчин при зниженому тиску. Із зали(20ммоль) основи донепезилу. До одержаного шкової маслянистої рідини одержували гідрохлорозчину додавали 1,92г (20ммоль) метансульфорид в суміші діетилового ефіру і 2-пропанолу 5 :1 нової кислоти, розчин нагрівали до кипіння, освіт(об/об). лювали 2,5г активованого вугілля і остуджували до Вихід: 2,85г (35,4%) білих кристалів кімнатної температури. Одержаний осад відокреТемпература плавлення: 159-160°С млювали фільтруванням при 0°С і промивали на Аналітично обчислено для формули фільтрі етилацетатом, що має температуру 0°С, С23Н28СlNО3 (401,9): до звільнення від маткового розчину. Розрахунок: 68,73% С; 7,02% Н; 3,48% N; Вихід: 9,34г (89,2%) білих кристалів 8,82% СІ Температура плавлення: 180-182°С Досвід: 68,63% С; 7,12% Н; 3,45% N; 8,95% СІ Аналітично обчислено для формули Приклад 7. C25H33NO6S (475,6): Отримання (±)-2-[(1-бензил-4Розрахунок: 63,14% С; 6,99% Н; 2,95% N; піперидиніл)метил]-5-гідрокси-6-метокси-16,74% S інданона гідрохлориду [сполуки загальної формуДосвід: 62,98% С; 7,02% Н; 2,94% N; 6,70% S ли (III)]. Приклад 4. 7,6г (20ммоль) основи донепезилу перемішуОтримання донепезилу бензолсульфоната. вали в суміші 50мл 36,5%-ного водного розчину В устаткуванні, що забезпечує інтенсивне пебромистого водню і 10мл оцтової кислоти на водяремішування, відмірювали 100мл 2-пропанолу, в ній лазні при 80°С протягом 24-х годин. Потім розякому при перемішуванні розчиняли 7,6г чин виливали на 500г льоду, нейтралізували вуг(20ммоль) основи донепезилу. До одержаного лекислим калієм, продукт екстрагували розчину додавали 3,16г (20ммоль) бензолсульфоетилацетатом, і випаровували розчин при зниженової кислоти, розчин нагрівали до кипіння, освітному тиску. Із залишкової маслянистої рідини оделювали 2,5г активованого вугілля і остуджували до ржували гідрохлорид в етилацетаті. кімнатної температури. Одержаний осад відокреВихід: 2,10г (26,1%) білих кристалів млювали фільтруванням при 0°С і промивали на Температура плавлення: 158- 160°С фільтрі етилацетатом, що має температуру 0°С, Аналітично обчислено для формули до звільнення від маткового розчину. C23H28CINO3 (401,9): Вихід: 9,41г (87,5%) білих кристалів Розрахунок: 68,73% С; 7,02% Н; 3,48% N; Температура плавлення: 175-176°С 8,82% СІ Аналітично обчислено для формули Досвід: 68,55% С; 6,94% Н; 3,54% N; 8,71% СІ C30H35N06S (537,7): Приклад 8. Розрахунок: 67,02% С; 6,56% Н; 2,61% N; Отримання фармацевтичної композиції. 5,96% S Для отримання пігулок, що мають загальну ваДосвід: 66,94% С; 6,53% Н; 2,58% N; 5,91% S гу 100 міліграм і що містять 5 міліграм активного Приклад 5. інгредієнта, відмірювали наступні речовини (з розОтримання донепезилу п-толуолсульфоната. рахунку на одну пігулку): В устаткуванні, що забезпечує інтенсивне педонепезилу фумарат 5 міліграм ремішування, відмірювали 100мл 2-пропанолу, в лактоза 47 міліграм якому при перемішуванні розчиняли 7,6г кукурудзяний крохмаль 47 міліграм (20ммоль) основи донепезилу. До одержаного магнію стеарат 1 міліграм розчину додавали 3,45г (20ммоль) метансульфоСуміш порошків перемішували до гомогенності нової кислоти, розчин нагрівали до кипіння, освіті пресували в пігулки. лювали активованим вугіллям і остуджували до Приклад 9. кімнатної температури. Одержаний осад відокреОтримання фармацевтичної композиції. млювали фільтруванням при 0°С і промивали на 11 88481 12 Для отримання пігулок, що мають загальну васпензію фільтрували при 0°С, і промивали на фігу 100 міліграм і що містять 10 міліграм активного льтрі етилацетатом до звільнення від маткової інгредієнта, відмірювали наступні речовини (з розрідини. рахунку на одну пігулку): Вихід: 8,28г (89,9%) білих кристалів донепезилу фумарат 10 міліграм Температура плавлення: 246-247°С лактоза 30 міліграм Аналітично обчислено для формули кукурудзяний крохмаль 59 міліграм С24Н30ВrNО3 (460,7): магнію стеарат 1 міліграм Розрахунок: 62,61% С; 6,57% Н; 3,04% N; Суміш порошків перемішували до гомогенності 17,35% Вr і пресували в пігулки. Досвід: 62,33% С; 6,55% Н; 3,00% N; 17,57% Вr Приклад 10. Приклад 12. (Порівняльний експеримент) Отримання фармацевтичної композиції. Отримання донепезилу сульфату (1:1) Для отримання пігулок, що мають загальну ваВ устаткуванні, що забезпечує інтенсивне пегу 100 міліграм і що містять 25 міліграм активного ремішування, відміряли 100мл 2-пропанолу, і розінгредієнта, відмірювали наступні речовини (з розчиняли в ньому 7,6г (20ммоль) основи донепезилу. рахунку на одну пігулку): До цього розчину додавали 2-пропанол, що місдонепезилу фумарат 25 міліграм тить 2,45г (25ммоль) сірчаної кислоти. Суспензію лактоза 50 міліграм перемішували при 0°С протягом 2-х годин і промикукурудзяний крохмаль 24 міліграм вали на фільтрі етилацетатом до звільнення від магнію стеарат 1 міліграм маткової рідини. Суміш порошків перемішували до гомогенності Вихід: 8,83г (92,4%) білих кристалів і пресували в пігулки. Температура плавлення: 190-195°С Приклад 11. (Порівняльний експеримент) Аналітично обчислено для формули Отримання донепезилу гідроброміду C24H31NO7S (477,6): В устаткуванні, що забезпечує інтенсивне пеРозрахунок: 60,36% С; 6,54% Н; 2,93% N; ремішування, відмірювали 100мл 2-пропанолу і 6,71% S розчиняли в ньому 7,6г (20ммоль) основи донепеДосвід: 59,95% С; 6,52% Н; 2,87% N; 6,64% S зилу. До цього розчину додавали 2-пропанол, що містить 1,62г (20ммоль) бромистого водню. Су Комп’ютерна верстка А. Крижанівський Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюDonepezil fumarate suitable for the preparation of pharmaceutical compositions
Автори англійськоюMezei Tibor, Simig Gyula, Lukacs Gyula, Porcs-Makkay Marta, Volk Balazs, Molnar Enikoe, Hofmanne Fekete Valeria
Назва патенту російськоюДонепезила фумарат, пригодный для получения фармацевтических композиций
Автори російськоюМесей Тибор, Симиг Дьюла, Лукаш Дьюла, Порч-Маккай Марта, Волк Балаж, Молнар Энико, Хофманне Фекете Валерия
МПК / Мітки
МПК: C07D 211/32, A61K 31/445, A61P 25/28
Мітки: донепезилу, фумарат, отримання, придатній, фармацевтичних, композицій
Код посилання
<a href="https://ua.patents.su/6-88481-donepezilu-fumarat-pridatnijj-dlya-otrimannya-farmacevtichnikh-kompozicijj.html" target="_blank" rel="follow" title="База патентів України">Донепезилу фумарат, придатний для отримання фармацевтичних композицій</a>
Попередній патент: Спосіб оцінки нафтозаводської сировини
Наступний патент: Пробіотичний лікарський засіб для корекції дисбіотичних розладів
Випадковий патент: Препарат у формі змочуваного порошку для захисту посівів цукрових буряків від бур`янів










