Стабільний при зберіганні інфузійний розчин дигідроптеридинонів
Формула / Реферат
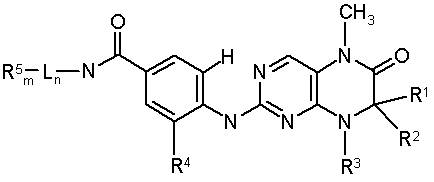
1. Стабільний при зберіганні водний інфузійний розчин, відповідно розчин для ін'єкцій, який містить діючу речовину загальної формули (І)
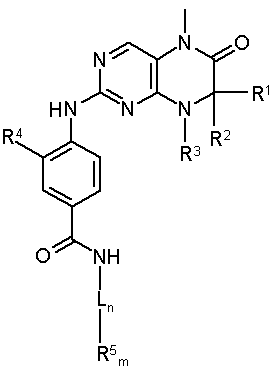 , (I)
, (I)
у якій
R1, R2 мають ідентичні або різні значення та означають водень або необов'язково заміщений С1-С6алкіл, або
R1 та R2 спільно означають 2-5-членний алкільний місток, який може містити 1 або 2 гетероатоми,
R3 означає водень або залишок, вибраний із групи, яка включає необов'язково заміщений С1-С12алкіл, С2-С12алкеніл, С2-С12алкініл і С6-С14арил, або залишок, вибраний із групи, яка включає необов'язково заміщений і/або з'єднаний містком С3-С12циклоалкіл, С3-С12циклоалкеніл, С7-С12поліциклоалкіл, С7-С12поліциклоалкеніл, С5-С12спіроциклоалкіл, С3-С12гетероциклоалкіл, який містить 1 або 2 гетероатоми, і С3-С12гетероциклоалкеніл, який містить 1 або 2 гетероатоми, або
R1 та R3 або R2 та R3 спільно утворюють насичений або ненасичений С3-С4алкільний місток, який може містити 1 гетероатом,
R4 означає залишок, вибраний із групи, яка включає водень, -CN, гідроксигрупу, -NR6R7 і галоген, або залишок, вибраний із групи, яка включає необов'язково заміщений С1-С6алкіл, С2-С6алкеніл, С2-С6алкініл, С1-С5алкілоксигрупу, С2-С5алкенілоксигрупу, С2-С5алкінілоксигрупу, С1-С6алкілтіогрупу, С1-С6алкілсульфоксогрупу і С1-С6алкілсульфоніл,
L означає лінкер, вибраний із групи, яка включає необов'язково заміщений С2-С10алкіл, С2-С10алкеніл, С6-С14арил, -С2-С4алкіл-С6-С14арил, -С6-С14арил-С1-С4алкіл, необов'язково з'єднаний містком С3-С12циклоалкіл і гетероарил, який містить 1 або 2 атоми азоту,
n означає 0 або 1,
m означає 1 або 2,
R5 означає залишок, вибраний із групи, яка включає необов'язково заміщений морфолініл, піперидиніл, піперазиніл, піперазинілкарбоніл, піролідиніл, тропеніл, R8-дикетометилпіперазиніл, сульфоксоморфолініл, сульфонілморфолініл, тіоморфолініл, -NR8R9 та азациклогептил,
R6, R7 мають ідентичні або різні значення та означають водень або С1-С4алкіл і
R8, R9 являють собою ідентичні або різні незаміщені замісники азоту при R5 і означають або водень, або залишок, вибраний із групи, яка включає С1-С6алкіл, -С1-С4алкіл-С3-С10циклоалкіл, С3-С10циклоалкіл, С6-С14арил, -С1-С4алкіл-С6-С14арил, піраніл, піридиніл, піримідиніл, С1-С4алкілоксикарбоніл, С6-С14арилкарбоніл, С1-С4алкілкарбоніл, С6-С14арилметилоксикарбоніл, С6-С14арилсульфоніл, С1-С4алкілсульфоніл і С6-С14арил-С1-С4алкілсульфоніл,
або її таутомери, рацемати, енантіомери, діастереомери або необов'язково їх фізіологічно ефективні похідні або метаболіти та фізіологічно сумісну кислоту або суміш фізіологічно сумісних кислот у достатній для розчинення діючої речовини та для стабілізації кількості, а також необов'язково містить інші придатні для парентерального введення в організм допоміжні речовини, використовувані в технології приготування лікарських засобів.
2. Стабільний при зберіганні водний інфузійний розчин, відповідно розчин для ін'єкцій за п. 1, який відрізняється тим, що дигідроптеридинони вибрані із групи, яка включає наступні сполуки загальної формули (І)
Приклад
R1
R2
Конфігурація R1 або R2
R3
R4
Ln-R5m
27
Н
![]()
R
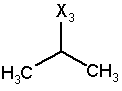
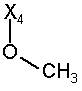
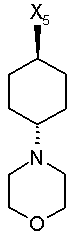
44
Н
![]()
R
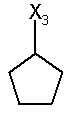
H
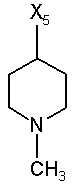
55
H
![]()
R

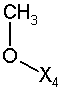
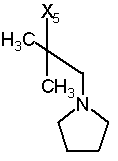
58
H
![]()
R


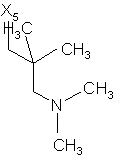
102
H
![]()
R


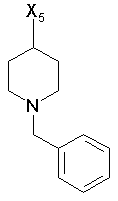
103
H
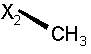
R



105
H

R

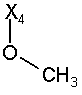
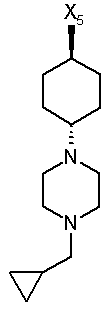
110
H
![]()
R



115
H

R
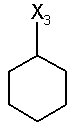

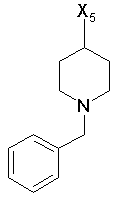
133
H
![]()
R



134
H
![]()
R


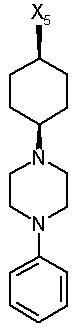
234
H
![]()
R


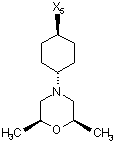
240
H
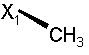
R


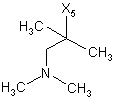
при цьому в наведеній вище таблиці кожне зі скорочень Х1, Х2, Х3, Х4 та Х5 використовується замість відповідного залишку R1, R2, R3, R4 та L-R5 для позначення положення, у якому він приєднаний до іншої частини молекули, представленої наведеною перед таблицею загальною формулою.
3. Стабільний при зберіганні водний інфузійний розчин, відповідно розчин для ін'єкцій за п. 1, який відрізняється тим, що дигідроптеридинон являє собою наступну сполуку загальної формули (І)

Приклад
R1
R2
Конфігурація R1 або R2
R3
R4
Ln-R5m
46
Н
![]()
R

![]()

при цьому в наведеній вище таблиці кожне зі скорочень Х1, Х2, Х3, Х4 та Х5 використовується замість відповідного залишку R1, R2, R3, R4 та L-R5 для позначення положення, у якому він приєднаний до іншої частини молекули, представленої наведеною перед таблицею загальною формулою.
4. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-3, який відрізняється тим, що вміст розчиненої діючої речовини в 1 мл інфузійного розчину, відповідно розчину для ін'єкцій, становить від 0,1 до 10,0 мг.
5. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-4, який відрізняється тим, що одна або декілька використовуваних для забезпечення стабільності при зберіганні та стабільності в розведеному стані кислот вибрані із групи, яка включає соляну кислоту, оцтову кислоту, гідроксіоцтову кислоту, метансульфонову кислоту, етансульфонову кислоту, фосфорну кислоту, азотну кислоту, сірчану кислоту, лимонну кислоту, винну кислоту, фумарову кислоту, бурштинову кислоту, глутарову кислоту, адипінову кислоту, пропіонову кислоту, аскорбінову кислоту, малеїнову кислоту, яблучну кислоту, глутамінову кислоту, глюконову кислоту, глюкуронову кислоту, галактуронову кислоту та молочну кислоту.
6. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-5, який відрізняється тим, що молярне співвідношення між фізіологічно сумісною кислотою або сумішшю фізіологічно сумісних кислот і діючою речовиною становить максимум 3:1
7. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-6, який відрізняється тим, що він містить одну або декілька додаткових допоміжних речовин, використовуваних у технології приготування лікарських засобів і вибраних із групи, яка включає комплексоутворювачі, світлостабалізатори, інгібітори кристалізації, загусники, агенти, що надають ізотонічності, антиокисники та засоби для підтримання нормального водного балансу організму.
8. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-7, який відрізняється тим, що його осмомолярність становить від 200 до 600 мОсмомоль/кг.
9. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-8, який відрізняється тим, що його значення рН становить від 2,4 до 5,3.
10. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-9, який відрізняється тим, що він містить у перерахунку на 100 мл свого об'єму від 1,25 до 3,0 моль соляної кислоти на моль діючої речовини та від 0,75 до 1,2 г NaCl і має осмомолярність від 260 до 350 мОсмомоль/кг, а також значення рН від 3,5 до 5,0.
11. Ліофілізати, концентрати та суспензії, які відрізняються тим, що з них додаванням до них води можливе одержання водного інфузійного розчину, відповідно розчину для ін'єкцій за будь-яким з пп. 1-10.
12. Інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-10, для застосування як лікарських засобів з антипроліферативною дією.
13. Емність, придатна для зберігання парентеральних лікарських форм, що являє собою скляну ємність або м'який пластиковий пакет або мішок, що містить інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-10.
Текст
1. Стабільний при зберіганні водний інфузійний розчин, відповідно розчин для ін'єкцій, який містить діючу речовину загальної формули (І) C2 2 (19) 1 3 92470 4 для стабілізації кількості, а також необов'язково рані із групи, яка включає наступні містить інші придатні для парентерального ввеної формули (І) дення в організм допоміжні речовини, використоO вувані в технології приготування лікарських засоH бів. R5m Ln N N 2. Стабільний при зберіганні водний інфузійний розчин, відповідно розчин для ін'єкцій за п. 1, який N N відрізняється тим, що дигідроптеридинони виб R4 Приклад R1 R2 27 Н X2 CH3 Конфігурація R1 R3 або R2 R сполуки загаль CH3 O N R1 N R2 R3 R4 X4 X3 Ln-R5m X5 O H3C CH3 CH3 N 44 Н X2 CH3 R X3 O X5 H N CH3 55 H X2 CH3 R X3 CH3 X5 H 3C O X4 CH3 58 H X2 CH3 R X3 N X5 H3C CH3 O X4 CH3 N CH3 CH3 5 102 H X2 92470 CH3 6 R CH3 X3 X5 O X4 CH3 H3C N 103 H X2 R CH3 X5 CH3 X3 O X4 N 105 H X2 R CH3 X4 X3 X5 O CH3 N N 110 H X2 CH3 R X3 X4 X5 O H3C CH3 CH3 N N 7 115 H X2 92470 R CH3 8 CH3 X3 X5 O X4 N 133 H X2 CH3 R X4 X3 X5 O CH3 N 134 H X2 CH3 R O X5 X4 X3 O CH3 N N 234 H X1 CH3 R X3 X5 X4 O H3C CH3 CH3 N O H3C 240 H R X1 CH3 X3 X5 CH3 H3C O CH3 X4 N H3C при цьому в наведеній вище таблиці кожне зі скорочень Х1, Х2, Х3, Х4 та Х5 використовується замість відповідного залишку R1, R2, R3, R4 та LR5 для позначення положення, у якому він приєд CH3 CH3 наний до іншої частини молекули, представленої наведеною перед таблицею загальною формулою. 9 92470 3. Стабільний при зберіганні водний інфузійний розчин, відповідно розчин для ін'єкцій за п. 1, який відрізняється тим, що дигідроптеридинон R5m Ln являє собою наступну сполуку загальної формули (І) 10 CH3 O H N N N R1 N N R4 Приклад R1 R2 46 Н X2 CH3 Конфігурація або R2 R R1 R3 R2 Ln-R5m O H3C N R3 R4 X3 O X4 X5 N CH3 при цьому в наведеній вище таблиці кожне зі скорочень Х1, Х2, Х3, Х4 та Х5 використовується замість відповідного залишку R1, R2, R3, R4 та LR5 для позначення положення, у якому він приєднаний до іншої частини молекули, представленої наведеною перед таблицею загальною формулою. 4. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-3, який відрізняється тим, що вміст розчиненої діючої речовини в 1 мл інфузійного розчину, відповідно розчину для ін'єкцій, становить від 0,1 до 10,0 мг. 5. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-4, який відрізняється тим, що одна або декілька використовуваних для забезпечення стабільності при зберіганні та стабільності в розведеному стані кислот вибрані із групи, яка включає соляну кислоту, оцтову кислоту, гідроксіоцтову кислоту, метансульфонову кислоту, етансульфонову кислоту, фосфорну кислоту, азотну кислоту, сірчану кислоту, лимонну кислоту, винну кислоту, фумарову кислоту, бурштинову кислоту, глутарову кислоту, адипінову кислоту, пропіонову кислоту, аскорбінову кислоту, малеїнову кислоту, яблучну кислоту, глутамінову кислоту, глюконову кислоту, глюкуронову кислоту, галактуронову кислоту та молочну кислоту. 6. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-5, який відрізняється тим, що молярне співвідношення між фізіологічно сумісною кислотою або сумішшю фізіологічно сумісних кислот і діючою речовиною становить максимум 3:1 7. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-6, який відрізняється тим, що він містить одну або декілька до даткових допоміжних речовин, використовуваних у технології приготування лікарських засобів і вибраних із групи, яка включає комплексоутворювачі, світлостабалізатори, інгібітори кристалізації, загусники, агенти, що надають ізотонічності, антиокисники та засоби для підтримання нормального водного балансу організму. 8. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-7, який відрізняється тим, що його осмомолярність становить від 200 до 600 мОсмомоль/кг. 9. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-8, який відрізняється тим, що його значення рН становить від 2,4 до 5,3. 10. Водний інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-9, який відрізняється тим, що він містить у перерахунку на 100 мл свого об'єму від 1,25 до 3,0 моль соляної кислоти на моль діючої речовини та від 0,75 до 1,2 г NaCl і має осмомолярність від 260 до 350 мОсмомоль/кг, а також значення рН від 3,5 до 5,0. 11. Ліофілізати, концентрати та суспензії, які відрізняються тим, що з них додаванням до них води можливе одержання водного інфузійного розчину, відповідно розчину для ін'єкцій за будьяким з пп. 1-10. 12. Інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-10, для застосування як лікарських засобів з антипроліферативною дією. 13. Емність, придатна для зберігання парентеральних лікарських форм, що являє собою скляну ємність або м'який пластиковий пакет або мішок, що містить інфузійний розчин, відповідно розчин для ін'єкцій за будь-яким з пп. 1-10. Даний винахід стосується стабільних при зберіганні водних інфузійних розчинів, відповідно роз чинів для ін'єкцій, які містять діючу речовину формули (І) 11 92470 12 тинок забруднюючих домішок можна у вирішальному ступені поліпшити за рахунок зберігання таких розчинів у скляних ємностях із силіконізованими поверхнями. В основу даного винаходу була покладена задача запропонувати стабільний інфузійний розчин, відповідно розчин для ін'єкцій з дигідроптеридинонами формули (І) для необхідного терапевтично оптимізованого інтервалу доз. Відповідно ще до однієї задачі винаходу такий стабільний інфузійний розчин, відповідно розчин для ін'єкцій для можливості гнучкого регулювання дози, що вводиться в організм, діючої речовини, яка міститься в ньому, повинен бути придатний і у вигляді готового до застосування розчину, і у вигляді концентрату для додаткового розбавлення або розведення звичайно використовуваними для парентерально1 2 3 4 5 у якій залишки L, R , R , R , R та R мають заго введення в організм розчинами, такими, напризначені у формулі винаходу та наступному описі клад, як ізотонічний розчин NaCl, ізотонічний роззначення, і фізіологічно сумісну кислоту або суміш чин декстрози або розчин Рингера, що містить фізіологічно сумісних кислот у достатній для розлактат. чинення діючої речовини та для стабілізації кільДокладний опис винаходу кості, а також необов'язково містять інші придатні При створенні винаходу несподівано було для парентерального введення в організм допомівстановлено, що одержання таких, які залишаютьжні речовини, використовувані в технології пригося стабільними при тривалому зберіганні та не тування лікарських засобів, а також стосується проявляють схильності до виділення частинок воспособу приготування пропонованих у винаході дних інфузійних розчинів, відповідно розчинів для інфузійних розчинів, відповідно розчинів для ін'єкін'єкцій, що містять діючу речовину загальної фоцій. рмули (І), фізіологічно сумісну кислоту або суміш Передумови створення винаходу фізіологічно сумісних кислот у достатній для розПропоновані у винаході дигідроптеридинони чинення діючої речовини та для стабілізації кільформули (І) являють собою сполуки, які мають кості, а також необов'язково містять інші придатні інноваційний, новий цитостатичний механізм дії та для парентерального введення в організм допомізавдяки цьому ефективно використовуються в жні речовини, використовувані в технології пригоонкології для лікування ракових пухлин різних титування лікарських засобів, можливо поза залежпів, що швидко ростуть. Звичайно цитостатичні ністю від конкретної якості діючої речовини та засоби застосовуються в складі парентеральних насамперед поза залежністю від характеру та лікарських форм, хоч можуть мати цілком достатособливостей домішок, що містяться у ній. ню біодоступність і при пероральному застосуванВідповідно до цього у винаході пропонуються ні. Причина, з якої цитостатичні засоби доводиться стабільні при зберіганні водні інфузійні розчини, вводити в організм парентерально, полягає у товідповідно розчини для ін'єкцій, які містять діючу му, що лікування цитостатичними засобами звиречовину загальної формули (І) чайно супроводжується побічними діями на шлунково-кишковий тракт, які часто проявляються у вигляді нудоти, блювоти і/або діареї і які тому при пероральному застосуванні цитостатичних засобів могли б знизити ефективність лікування. Сказане повною мірою відноситься й до дигідроптеридинонів формули (І), чим обумовлена необхідність їх парентерального застосування у складі інфузійного розчину, відповідно розчину для ін'єкцій. В ЕР 0219784 та WO 01/78732 описані способи приготування та заходи щодо стабілізації інфузійних розчинів, що містять ципрофлоксаксин, за рахунок застосування однієї або декількох фізіологічно сумісних органічних або неорганічних кислот. В ЕР 0287926 йдеться, що уникнути небезпеки утворення дисперсної твердої фази (частинок) у розчині ципрофлоксаксину дозволяє його застосуу якій вання у високочистому вигляді. В ЕР 0143478 А1 R1, R2 мають ідентичні або різні значення та описаний спосіб приготування стабільного соляноозначають водень або необов'язково заміщений кислого розчину цисплатину, який придатний для С1-С6алкіл або ін'єкцій і насамперед не містить ніяких додаткових R1 та R2 спільно означають 2-5-членний алкідобавок. В DE 19703023 йдеться, що стабільність льний місток, який може містити 1 або 2 гетероаінфузійних розчинів відносно виділення в них частоми, 13 92470 14 R3 означає водень або залишок, вибраний із містком С3-С12циклоалкіл і гетероарил, який місгрупи, яка включає необов'язково заміщений С1тить 1 або 2 атоми азоту, С12алкіл, С2-С12алкеніл, С2-С12алкініл і С6-С14арил, n означає 1, або залишок, вибраний із групи, яка включає неm означає 1 або 2, обов'язково заміщений і/або з'єднаний містком С3R5 означає залишок, приєднаний до L через С12циклоалкіл, С3-С12циклоалкеніл, С 7атом азоту та вибраний із групи, яка включає неС12поліциклоалкіл, С7-С12поліциклоалкеніл, С5обов'язково заміщений морфолініл, піперидиніл, С12спіроциклоалкіл, С3-С12гетероциклоалкіл, який R8-піперазиніл, піролідиніл, тропеніл, R 8містить 1 або 2 гетероатоми, і С 3дикетометилпіперазиніл, сульфоксоморфолініл, С12гетероциклоалкеніл, який містить 1 або 2 гетесульфонілморфолініл, тіоморфолініл, -NR8R9 і роатоми, або азациклогептил, і R1 та R3 або R2 та R3 спільно утворюють насиR8, R9 являють собою ідентичні або різні незачений або ненасичений С3-С4алкільний місток, міщені замісники азоту при R5 і означають водень який може містити 1 гетероатом, або залишок, вибраний із групи, яка включає С1R4 означає залишок, вибраний із групи, яка С6алкіл, -С1-С4алкіл-С3-С10циклоалкіл, С3включає водень, -CN, гідроксигрупу, -NR6R7 і галоС10циклоалкіл, С6-С14арил, -С1-С4алкіл-С6-С14арил, ген, або залишок, вибраний із групи, яка включає піраніл, піридиніл, піримідиніл, С 1необов'язково заміщений С1-С6алкіл, С2-С6алкеніл, С4алкілоксикарбоніл, Сб С6-С14арилкарбоніл, С1С2-С6алкініл, С2-С5алкілоксигрупу, С 2С4алкілкарбоніл, С6-С14арилметилоксикарбоніл, С5алкенілоксигрупу, С2-С5алкінілоксигрупу, С1С6-С14арилсульфоніл, С1-С4алкілсульфоніл і С6С6алкілтіогрупу, С1-С6алкілсульфоксогрупу і С1С14арил-С1-С4алкілсульфоніл, С6алкілсульфоніл, необов'язково у вигляді їх таутомерів, їх рацеL означає лінкер, вибраний із групи, яка вклюматів, їх енантіомерів, їх діастереомерів і їх сумічає необов'язково заміщений С2-С10алкіл, С2шей, а також необов'язково їх фармакологічно С10алкеніл, С6-С14арил, -С2-С4алкіл-С6-С14арил, прийнятних кислотно-адитивних солей. С6-С14арил-С1-С4алкіл, необов'язково з'єднаний Кращі далі стабільні при зберіганні розчини, містком С3-С12циклоалкіл і гетероарил, який місякі містять сполуки формули (І), у якій тить 1 або 2 атоми азоту, R1-R4, R6 та R7 мають зазначені вище значенn означає 0 або 1, ня, а m означає 1 або 2, L означає лінкер, вибраний із групи, яка вклюR5 означає залишок, вибраний із групи, яка чає необов'язково заміщений С2-С10алкіл, С2включає необов'язково заміщений морфолініл, С10алкеніл, С6-С14арил, -С2-С4алкіл-С6-С14арил, піперидиніл, піперазиніл, піперазинілкарбоніл, піС6-С14арил-С1-С4алкіл, необов'язково з'єднаний ролідиніл, тропеніл, R8-дикетометилпіперазиніл, містком С3-С12циклоалкіл і гетероарил, який міссульфоксоморфолініл, сульфонілморфолініл, тіотить 1 або 2 атоми азоту, морфолініл, -NR8R9 і азациклогептил, n означає 0 або 1, R6, R7 мають ідентичні або різні значення та m означає 1 або 2, означають водень або С1-С4алкіл і R5 означає залишок, приєднаний до L через 8 9 R , R являють собою ідентичні або різні незаатом вуглецю та вибраний із групи, яка включає міщені замісники азоту при R5 і означають або воR8-піперидиніл-, R8R9-піперазиніл, R8-піролідиніл, день, або залишок, вибраний із групи, яка включає R8-піперазинілкарбоніл, R8-тропеніл, R8С1-С6алкіл, -С1-С4алкіл-С3-С10циклоалкіл, С3морфолініл та R8-азациклогептил, і С10циклоалкіл, С6-С14арил, -С1-С4алкіл-С6-С14арил, R8, R9 являють собою ідентичні або різні незапіраніл, піридиніл, піримідиніл, С 1міщені замісники азоту при R5 і означають водень С4алкілоксикарбоніл, С6-С14арилкарбоніл, С1 або залишок, вибраний із групи, яка включає С1С4алкілкарбоніл, С6-С14арилметилоксикарбоніл, С6алкіл, -С1-С4алкіл-С3-С10циклоалкіл, С3С6-С14арилсульфоніл, С1-С4алкілсульфоніл і С6С10циклоалкіл, С6-С14арил, -С1-С4алкіл-С6-С14арил, С14арил-С1-С4алкілсульфоніл, піраніл, піридиніл, піримідиніл, С 1або її таутомери, рацемати, енантіомери, діасС4алкілоксикарбоніл, С6-С14арилкарбоніл, С1тереомери або необов'язково їх фізіологічно ефеС4алкілкарбоніл, С6-С14арилметилоксикарбоніл, ктивні похідні або метаболіти та фізіологічно суміС6-С14арилсульфоніл, С1-С4алкілсульфоніл і С6сну кислоту або суміш фізіологічно сумісних С14арил-С1-С4алкілсульфоніл, кислот у достатній для розчинення діючої речовинеобов'язково у вигляді їх таутомерів, їх рацени та для стабілізації кількості, а також необов'язматів, їх енантіомерів, їх діастереомерів і їх суміково містять інші придатні для парентерального шей, а також необов'язково їх фармакологічно введення в організм допоміжні речовини, викорисприйнятних кислотно-адитивних солей. товувані в технології приготування лікарських заОсобливо кращі стабільні при зберіганні розсобів. чини, які містять сполуки формули (І), у якій Кращі стабільні при зберіганні розчини, які місL, m, n та R3-R9 мають зазначені вище значентять сполуки формули (І), у якій ня, а R1-R4, R6 та R7 мають зазначені вище значенR1, R2 мають ідентичні або різні значення та ня, а означають залишок, вибраний із групи, яка вклюL означає лінкер, вибраний із групи, яка включає водень, Me, Et та Рr, або чає необов'язково заміщений С2-С10алкіл, С2R1 та R2 спільно утворюють С2-С4алкільний міС10алкеніл, С6-С14арил, -С2-С4алкіл-С6-С14арил, сток, С6-С14арил-С1-С4алкіл, необов'язково з'єднаний 15 92470 16 необов'язково у вигляді їх таутомерів, їх рацеR4 означає залишок, вибраний із групи, яка матів, їх енантіомерів, їх діастереомерів і їх сумівключає водень, ОМе, ОН, Me, Et, Pr, OEt, NHMe, шей, а також необов'язково їх фармакологічно NH2, F, СІ, Br, О-пропаргіл, О-бутиніл, CN, SMe, прийнятних кислотно-адитивних солей. NMe2, CONH2, етиніл, пропініл, бутиніл і аліл, і Найбільш кращі стабільні при зберіганні розL означає лінкер, вибраний із групи, яка включини, які містять сполуки формули І, у якій чає необов'язково заміщений феніл, фенілметил, R1, R2, m, n та R5-R8 мають зазначені вище циклогексил і розгалужений С1-С6алкіл, значення, а необов'язково у вигляді їх таутомерів, їх рацеR3 означає залишок, вибраний із групи, яка матів, їх енантіомерів, їх діастереомерів і їх сумівключає необов'язково заміщений С1-С10алкіл, С3шей, а також необов'язково їх фармакологічно С7циклоалкіл, С3-С6гетероциклоалкіл і С6-С14арил, прийнятних кислотно-адитивних солей. або Ще одним об'єктом винаходу є стабільний при R1 та R3 або R2 та R3 спільно утворюють насизберіганні розчин, який містить один з дигідроптечений або ненасичений С3-С4алкільний місток, ридинонів загальної формули (І), вибраний із груякий може містити 1 або 2 гетероатоми, пи, яка включає наступні сполуки загальної формули (І) 17 при цьому в наведеній вище таблиці кожне зі скорочень Х1, Х2, Х3, X4 та Х5 використовується замість відповідного залишку R1, R2, R3, R4 та L-R5 для позначення положення, у якому він приєднаний до іншої частини молекули, представленої наведеною перед таблицею загальною формулою. Під довгостроковою стабільністю відповідно до винаходу мається на увазі стабільність розчину при зберіганні протягом принаймні 12 місяців при 25°С/60%-вій відносній вологості та 30°С/70%-вій відносній вологості, краще протягом принаймні 36 92470 18 місяців при 25°С/60%-вій відносній вологості та 30°С/70%-вій відносній вологості. Пропоновані у винаході інфузійні розчини, відповідно розчини для ін'єкцій крім фізіологічно сумісної кислоти або суміші фізіологічно сумісних кислот можуть не містити ніяких інших гідротропних солюбілізаторів або органічних співрозчинників, насамперед органічних співрозчинників. Кращі водні інфузійні розчини, відповідно розчини для ін'єкцій, в 1 мл яких вміст розчиненої ді 19 92470 20 ючої речовини формули (І) становить від 0,1 до засобів і вибраних із групи, яка включає комплек10,0 мг, насамперед від 0,5 до 5 мг. соутворювачі, інгібітори кристалізації, загусники, Кращі далі водні інфузійні розчини, відповідно агенти, що надають ізотонічності, консерванти, розчини для ін'єкцій, у яких одна або декілька висвітлостабалізатори й антиокисники. користовуваних для забезпечення стабільності Як приклад придатних для застосування в при зберіганні та стабільності розведення кислот пропонованих у винаході розчинах комплексовибрані із групи, яка включає соляну кислоту, оцутворювачів можна назвати істинні (незаміщені) і тову кислоту, гідроксіоцтову кислоту, метансульзаміщені циклодекстрини, ЕДТК, альбуміни, а тафонову кислоту, етансульфонову кислоту, фосфокож лимонну кислоту, її солі та похідні. рну кислоту, азотну кислоту, сірчану кислоту, Як приклад придатних для застосування у лимонну кислоту, винну кислоту, фумарову кислопропонованих у винаході розчинах інгібіторів кристу, бурштинову кислоту, глутарову кислоту, адипіталізації можна назвати полівінілпіролідон, похідні нову кислоту, пропіонову кислоту, аскорбінову кицелюлози, альгінати, полоксамери та полісорбати. слоту, малеїнову кислоту, яблучну кислоту, Як приклад придатних для застосування у глутамінову кислоту, глюконову кислоту, глюкуропропонованих у винаході розчинах загусників можнову кислоту, галактуронову кислоту та молочну на назвати декстрани, гліцерин і розчинні похідні кислоту, краще із групи, яка включає оцтову кислоцелюлози, насамперед карбоксиметилцелюлозу і ту, соляну кислоту, фосфорну кислоту, винну кисїї солі, а також гідроксіалкілцелюлози. лоту, лимонну кислоту й фумарову кислоту, найЯк приклад придатних для застосування у краще із групи, яка включає соляну кислоту, пропонованих у винаході розчинах агентів, що лимонну кислоту й оцтову кислоту. надають ізотонічності, можна назвати NaCl, маніт, З урахуванням забезпечення рН-сумісності сорбіт, ксиліт, сахарозу, лактозу, глюкозу та гліцекращі, як випливає із прикладеного до опису кресрин, кращі серед яких NaCl, маніт, глюкоза, сахалення, водні інфузійні розчини, відповідно розчини роза та гліцерин, а особливо кращі NaCl, маніт та для ін'єкцій, у яких для встановлення їх рН на знаглюкоза. чення вище 2,4 молярне співвідношення між фізіЯк приклад придатних для застосування у ологічно сумісною кислотою або сумішшю фізіолопропонованих у винаході розчинах консервантів гічно сумісних кислот і діючою речовиною повинне можна назвати ефіри n-гідроксибензойної кислоти, становити максимум 3:1, краще від 1,25:1 до 3:1, бензиловий спирт, сорбінову кислоту та бензойну найкраще від 1,5:1 до 3:1. кислоту. У кращому варіанті винахід стосується також Як приклад придатних для застосування у інфузійних розчинів, відповідно розчинів для ін'єкпропонованих у винаході розчинах світлостабілізацій, які містять від 0,1 до 10,0 мг діючої речовини торів можна назвати похідні n-гідроксибензойної на мілілітр водного розчину та до 3,0 моль соляної кислоти, а також коричну кислоту та її похідні. кислоти в перерахунку на моль діючої речовини. Як приклад придатних для застосування у Кращий вміст соляної кислоти при цьому станопропонованих у винаході розчинах антиокисників вить від 1,25 до 3,0 моль, насамперед від 1,5 до можна назвати аскорбінову кислоту і її солі. 2,4 моль. Особливо кращі також водні інфузійні розчини, Ще одним об'єктом винаходу є інфузійні розвідповідно розчини для ін'єкцій, осмомолярність чини, відповідно розчини для ін'єкцій, які містять 4яких становить від 200 до 600 мосмомоль/кг, кра[[(7R)-8-циклопентил-7-етил-5,6,7,8-тетрагідро-5ще від 260 до 350 мосмомоль/кг. Осмомолярність метил-6-оксо-2-птеридиніл]аміно]-3-метокси-N-(1пропонованих у винаході розчинів можна встановметил-4-піперидиніл)бензамід та від 1,6 до 2,0 лювати на зазначені значення додаванням агентів, моль соляної кислоти на моль діючої речовини. що надають ізотонічності, таких як NaCl, маніт, Відповідно до модифікованого варіанта просорбіт, глюкоза, сахароза, ксиліт, фруктоза та гліпоновані у винаході інфузійні розчини, відповідно церин або суміші зазначених речовин. Кращі інфурозчини для ін'єкцій можуть також містити діючу зійні розчини, відповідно розчини для ін'єкцій, які речовину у кількості до 10 мг/мл і соляну кислоту в крім діючої речовини, води, кислоти(кислот) і інших кількості до 1 моль на моль діючої речовини, а допоміжних речовин, використовуваних у технолотакож одну або декілька інших фізіологічно сумісгії приготування лікарських засобів, містять NaCl них кислот, за умови, що сумарна кількість кислот або інший агент, що надає ізотонічності, у кількосповинна бути не менш ніж 1,25 моль та не більш ті, при якому розчин є ізотонічним або злегка гіпоніж 3,0 моль на моль діючої речовини. або гіпертонічним щодо рідини тканин організму Мінімально необхідна в перерахунку на моль людини або тварини. діючої речовини кількість кислоти залежить від Кращі, крім того, водні інфузійні розчини, відконцентрації діючої речовини та конкретно застоповідно розчини для ін'єкцій, значення рН яких совуваної(-их) кислоти(кислот) і тому не є постійзнаходиться в інтервалі від 2,4 до 5,3, краще від ною величиною. Однак вміст конкретної кислоти 3,5 до 5,0, найкраще від 3,9 до 4,5. або кислот, обмежений пропонованими у винаході Пропоновані у винаході інфузійні розчини, відмежами, можна визначити проведенням простих повідно розчини для ін'єкцій можна, крім того, з дослідів, як це описано, наприклад, в ЕР 0219784 і метою збагачення їх електролітами без додавання WO 01/78732. вуглеводів розбавляти або розводити наявними у Особливо кращі водні інфузійні розчини, відпродажу інфузійними фізіологічними розчинами, повідно розчини для ін'єкцій, які містять одну або відповідно фізіологічними розчинами для ін'єкцій, декілька додаткових допоміжних речовин, викоритакими як ізотонічний розчин NaCl, ізотонічний стовуваних у технології приготування лікарських розчин глюкози, розчин Рингера, що містить лак 21 92470 22 тат, та аналогічні розчини (Rote Liste 2004, вим захистом, наприклад, у вигляді алюмінієвої Verzeichnis der Fertigarzneimittel der Mitglieder des упаковки. Bundesverbandes der Pharmazeutischen Industrie Пропоновані у винаході інфузійні розчини, відe.V., Editio Cantor, Aulendorf/Wurtt., основні групи повідно розчини для ін'єкцій придатні для їх за52.1 та 52.2.1), з доведенням таким шляхом конключної стерилізації, наприклад, гострою водяною центрації, відповідно дози діючої речовини, яка парою, що тим самим дозволяє приготовляти їх з міститься в них, до необхідного рівня без небезпеособливо високою економічністю та з високою ки виникнення фізичної або хімічної несумісності. безпекою (з малим ризиком бактеріального забруТак само кращі водні інфузійні розчини, відподнення) у стерильному вигляді без пірогенних відно розчини для ін'єкцій, які в перерахунку на продуктів. 100 мл свого об'єму містять соляну кислоту в кільПропоновані у винаході інфузійні розчини, відкості від 1,25 до 3,0 моль, краще від 1,5 до 2,4 повідно розчини для ін'єкцій можна приготовляти моль, на моль діючої речовини та NaCl у кількості відомими з літератури методами приготування від 0,75 до 1,2 г, краще від 0,85 до 0,95 г, і які маводних рідких лікарських форм. ють осмомолярність від 260 до 350 мосмомоль/кг і Відповідно до цього даний винахід стосується значення рН від 3,5 до 5,0. також способу приготування пропонованих у ньоЩе одним об'єктом винаходу є ліофілізати, му інфузійних розчинів, відповідно розчинів для концентрати та суспензії, з яких додаванням до ін'єкцій, які містять на мілілітр їх об'єму від 0,1 до них води одержують один із пропонованих у вина10 мг діючої речовини формули (І). Такий спосіб ході водних інфузійних розчинів, відповідно розчивідрізняється тим, що взяту у відповідній кількості нів для ін'єкцій. діючу речовину, необов'язково у вигляді її солі з Ще одним об'єктом винаходу є пропоновані в аніонним протиіоном, гідрату або гідрату солі, або ньому інфузійні розчини, відповідно розчини для ж узяті у відповідній кількості суміші цих соін'єкцій для застосування як лікарських засобів з лей/гідратів змішують із фізіологічно сумісною кисантипроліферативною дією. лотою або сумішшю фізіологічно сумісних кислот, Ще одним об'єктом винаходу є застосування узятої в кількості, надлишковому відносно кількоспропонованих у ньому інфузійних розчинів, відпоті, яка потрібна безпосередньо для розчинення відно розчинів для ін'єкцій для приготування лікардіючої речовини, відповідно її солей або гідратів, а ського засобу, призначеного для лікування пухтакож для попередження фізичної нестабільності, линних, інфекційних, запальних і аутоімунних необов'язково додають інші допоміжні речовини, захворювань. використовувані в технології приготування лікарЩе одним об'єктом винаходу є спосіб лікуванських засобів, і додаванням води (для ін'єкцій) ня і/або профілактики пухлинних, інфекційних, заоб'єм інфузійного розчину, відповідно розчину для пальних і аутоімунних захворювань, краще пухін'єкцій доводять до величини, при якій концентралинних захворювань, який полягає у введенні в ція в ньому діючої речовини знаходиться в інтерорганізм пацієнта пропонованого у винаході інфувалі від 0,1 до 10 мг на мілілітр розчину. зійного розчину, відповідно розчину для ін'єкцій в При приготуванні інфузійних розчинів, відповіефективній кількості. дно розчинів для ін'єкцій необхідно також враховуЩе одним об'єктом винаходу є застосування вати, що за своїми властивостями відносно знапропонованих у ньому інфузійних розчинів, відпочення рН, вмісту кислоти(кислот) і осмомолярності відно розчинів для ін'єкцій у кількості, що відповівони повинні задовольняти вже розглянутим вище дає інтервалу доз від 0,1 до 50 мг діючої речовини вимогам. При використанні солі діючої речовини на кг ваги тіла, краще від 0,5 до 25 мг діючої речоможе виявитися доцільним використовувати кисвини на кг ваги тіла. лоту, аніон якої відповідає аніону солі діючої речоПропоновані у винаході інфузійні розчини, відвини, відповідно аніону гідрату такої солі. повідно розчини для ін'єкцій можна розфасовувати За потреби діючу речовину або її сіль або гідв придатні для цієї мети скляні ємності для паренрат суспендують у воді та додають фізіологічно теральних лікарських форм або в м'які пластикові сумісну кислоту або суміш фізіологічно сумісних пакети або мішки, краще з матеріалів, відмінних кислот, краще соляну кислоту, у кількості до 3,0 від полівінілхлориду, наприклад, з матеріалів на моль на моль діючої речовини. поліолефіновій основі, з місткістю від 20 до 1000 На завершення додають інші допоміжні речомл, краще від 50 до 500 мл. Такі ємності можуть вини, використовувані в технології приготування мати виконання, при якому вони забезпечують лікарських засобів, насамперед агенти, що надаспеціальний захист пропонованих у винаході інфують ізотонічності, краще NaCl, який у деяких випазійних розчинів, відповідно розчинів для ін'єкцій, дках може також утворюватися в результаті реакякі знаходяться у них, наприклад, від впливу світції нейтралізації в перероблюваній в інфузійний ла або контакту з киснем. Особлива обробка порозчин, відповідно розчин для ін'єкцій суміші, після верхонь первинних упаковок (наприклад, силіконічого об'єм розчину додаванням води доводять до зація поверхонь скляних ємностей (шляхом величини, при якій концентрація в ньому діючої випалу)) для підвищення стабільності пропоноваречовини відповідає необхідній. них у винаході інфузійних розчинів, відповідно роЗначення рН пропонованих у винаході інфузчинів для ін'єкцій, які зберігаються в них, у принзійних розчинів, відповідно розчинів для ін'єкцій ципі не потрібна, але й у той же час не ніяк можна встановлювати на зазначені вище значення негативно не впливає. М'які (гнучкі) пластикові за допомогою (фізіологічно) сумісних кислот і/або пакети або мішки можуть бути обладнані додаткооснов, насамперед NaOH. 23 92470 24 Для прискорення процесу приготування розПропоновані у винаході розчини мають високу чинів, насамперед для прискорення процесу розстабільність при зберіганні, що обумовлена присучинення твердих компонентів, розчини можна частністю в них видимих і не видимих неозброєним тинами або цілком злегка нагрівати, краще до оком частинок лише в кількості, яка не перевищує температури у межах від 20 до 80°С. припустимі межі, і відсутністю реакцій, що привоОсобливо економічний спосіб приготування дять до істотного розкладання діючої речовини. пропонованих у винаході розчинів полягає у попеПропоновані у винаході розчини мають із погредньому або проміжному приготуванні концентляду фармакодинамічних властивостей діючої рованих розчинів. Для цього діючу речовину в неречовини достатню локальну переносимість та не обхідній для приготування однієї порції суміші є гемолітичними. кількості змішують із фізіологічно сумісною кислоНижче на прикладах розглянуті деякі можливі тою або сумішшю фізіологічно сумісних кислот, склади пропонованих у винаході інфузійних розчиузятій в основній кількості (>90%), і розчиняють у нів, відповідно розчинів для ін'єкцій. Ці приклади ній, за потреби при слабкому нагріванні і/або при носять винятково ілюстративний характер і не обдодаванні невеликої кількості води. Одержаний межують обсяг винаходу. таким шляхом концентрат потім розбавляють воНа прикладеному до опису кресленні показадою, після чого додають інші допоміжні речовини, ний графік залежності значення рН готового до використовувані в технології приготування лікарзастосування розчину від молярного співвідноських засобів, і на завершення решту кількості шення в ньому між кислотою/сумішшю кислот і кислоти(кислот), відповідно води, доводячи об'єм діючою речовиною. У цьому випадку діючою речорозчину до номінального. виною є 4-[[(7R)-8-циклопентил-7-етил-5,6,7,8Після приготування розчину його незважаючи тетрагідро-5-метил-6-оксо-2-птеридиніл]аміно]-3на заключну стерилізацію гострою парою звичайно метокси-N-(1-метил-4-піперидиніл)бензамід (прикфільтрують через мембранний фільтр або фільтр лад 46 у таблиці 1). для глибокого очищення з розміром пор 0,2 мкм Для покращення локальної переносимості при для відділення можливо присутніх частинок і/або внутрішньовенній інфузії або ін'єкції максимальне пірогенних продуктів. Відповідні методи фільтрації молярне співвідношення між кислотою/сумішшю відомі з рівня техніки (M.J.Groves, Parenteral кислот і діючою речовиною в пропонованому у Technology Manual, в-во Interpharm Press Inc., 2-е винаході інфузійному розчині, відповідно розчині вид., 1988). Кількість частинок обмежують при для ін'єкцій обмежено величиною 3:1 з метою цьому регламентовано необхідною й економічно встановлення рН розчину на значення вище 2,4. доцільною величиною, наприклад, 6000 частинкаПриклади парентеральних інфузійних розчими розміром 10 мкм і 600 частинками розміром 25 нів, відповідно розчинів для ін'єкцій мкм в одній порції (одна порція відповідає 100 мл), У наведених нижче прикладах скорочення відповідно 25 частинками розміром 10 мкм і 3 час"ВДІ" означає "вода для ін'єкцій". тинками розміром 25 мкм на мілілітр (при об'ємі У представленому нижче загальному прикладі однієї порції більше 100 мл), USP 27 . 1 діючою речовиною є один з дигідроптеридинонів наведеної вище загальної формули (І). Загальний приклад 1 Діюча речовина Органічна або мінеральна кислота або суміш кислот Агент, що надає ізотонічності (наприклад, NaCl/маніт) ВДІ рН У наступних прикладах діючою речовиною є 4[[(7R)-8-циклопентил-7-етил-5,6,7,8-тетрагідро-5метил-6-оксо-2-птеридиніл]аміно]-3-метокси-N-(1метил-4-піперидиніл)бензамід (приклад 46 у таблиці 1). Приклад 2 Діюча речовина Соляна кислота, 1н. NaCl ВДІ рН мосмомоль/кг 2 мг/мл 6,8 мкл 0,009 г/мл до 1 мл 4,5 295 1-10 мг/мл 1,0-3,0 моль (у перерахунку на діючу речовину) наприклад, 9 мг/мл або 50 мг/мл до кінцевого об'єму, наприклад, 1,0 мл 3,0-4,5 Приклад 3 Діюча речовина Соляна кислота, 1н. NaCl ВДІ рН мосмомоль/кг 10,0000 г 36,6735 г 45,0000 г 4934,8265 г 4,3 300 Приклад 4 Діюча речовина Соляна кислота, 1н. NaCl ВДІ рН мосмомоль/кг 500 мг 1,6 мл 450,0 мг до 50 мл 4,0 290 25 92470 26 рН мосмомоль/кг Приклад 5 Діюча речовина Соляна кислота, 1н. NaCl ВДІ рН мосмомоль/кг Приклад 6 0,5 мг 1,705 мкл 9 мг до 1 мл 4,8 285 Діюча речовина Соляна кислота, 1н. NaCl ВДІ рН мосмомоль/кг 1 мг 3,6125 мкл 0,009 г до 1 мл 4,8 295 У наступних прикладах діючою речовиною є N[транс-4-[4-(циклопропілметил)-1піперазиніл]циклогексил]-4-[[(7R)-7-етил-5,6,7,8тетрагідро-5-метил-8-(1-метилетил)-6-оксо-2птеридиніл]аміно]-3-метокси-бензамід (приклад 110 у таблиці 1). Приклад 12 Діюча речовина 3НBr NaCl ВДІ рН 2мг 0,440 мкл 9мг до 1 мл 4,0 298 Приклад 8 Діюча речовина Оцтова кислота Декстроза ВДІ рН мосмомоль/кг 100 мг 16,4 мкл 2,5 г до 50 мл 4,4 305 Приклад 9 Діюча речовина Винна кислота Маніт ВДІ рН мосмомоль/кг 10 мг 4,32 мг 0,25 г до 5 мл 4,0 298 Приклад 10 Діюча речовина Лимонна кислота NaCl ВДІ рН мосмомоль/кг 2мг 1,104 мг 9мг до 1 мл 4,5 295 Приклад 11 Діюча речовина Соляна кислота, 1н. Оцтова кислота Na-ацетат NaCl ВДІ 2 мг/мл* (у перерахунку на основу) 9 мг/мл до 1,0 мл 3,5 Приклад 13 Приклад 7 Діюча речовина Фосфорна кислота (85%-ва) NaCl ВДІ рН мосмомоль/кг 4,0 305 2мг 6,8 мкл 0,501 мг 0,2260 мг 9мг до 1 мл Діюча речовина 3НСІ NaCl ВДІ рН 2 мг/мл* (у перерахунку на основу) 9 мг/мл до 1,0 мл 3,4 Приклад 14 Діюча речовина Фосфорна кислота, 85%-ва NaCl ВДІ рН 500 мг 157,5 мг 2,250 г до 250,0 мл 3,2 Приклад 15 Діюча речовина Винна кислота NaCl ВДІ рН 10 мг 4,85 мг 45 мг до 5 мл 3,5 Приклад 16 Діюча речовина Оцтова кислота NaCl ВДІ рН 2 мг/мл 0,39 мг 0,009 г до 1 мл 3,4 Приклад 17 Діюча речовина Лимонна кислота Маніт ВДІ рН 2мг 1,24 мг 50 мг до 1 мл 3,5 Пропоновані у винаході сполуки можна одержувати описаним нижче методом синтезу А, при цьому замісники в загальних формулах (А1)-(А9) мають зазначені вище значення. Цей метод лише ілюструє даний винахід і не обмежує його обсяг. 27 92470 28 Метод А (А2) можна одержувати відомими з літератури Стадія 1А методами, описаними, наприклад, у наступних Сполуку формули (А1) вводять у взаємодію зі публікаціях (a) F. Effenberger, U. Burkhart, J. сполукою формули (А2) з одержанням сполуки Willfahrt, Liebigs Ann. Chem. 1986, cc. 314-333, (б) формули (A3) (схема 1А). Цю реакцію можна проТ. Fukuyama, C.-K. Jow, M. Cheung, Tetrahedron водити відповідно до методу, що описаний у WO Lett. 36, 1995, cc. 6373-6374, (в) R.K. Olsen, J. Org. 00/43369 або WO 00/43372. Сполука (А1) являє Chem. 35, 1970, cc. 1912-1915, (г) F.E. Dutton, B.H. собою комерційно доступний продукт, що випускаByung, Tetrahedron Lett. 30, 1998, cc. 5313-5316, ється, наприклад, фірмою City Chemical LLC, розабо (д) J.M. Ranajuhi, M.M. Joullie, Synth. Commun. ташованою за адресою: 139 Allings Crossing Road, 26, 1996, cc. 1379-1384. West Haven, CT, 06516, USA. Сполуку формули На стадії 1Α 1 еквівалент сполуки (A1) та 11,5 еквівалента, краще 1,1 еквівалента, основи, краще карбонату калію, гідрокарбонату калію, карбонату натрію, гідрокарбонату натрію або карбонату кальцію, найкраще карбонату калію, перемішують у розріджувачі, змішаному в деяких випадках з водою, наприклад, в ацетоні, тетрагідрофурані, діетиловому ефірі, циклогексані, петролейному ефірі або діоксані, краще циклогексані або діетиловому ефірі. Далі при температурі 0-15°С, краще 5-10°С, по краплях додають 1 еквівалент амінокислоти формули (А2), розчиненої в органічному розчиннику, наприклад, ацетоні, тетрагідрофурані, діетиловому ефірі, циклогексані або діоксані. Після цього реакційну суміш при перемішуванні нагрівають до температури 18-30°С, краще приблизно 22°С, і потім перемішують ще протягом 10-24 год, краще приблизно 12 год. Після цього відганяють розріджувач, залишок змішують із водою й суміш два-три рази екстрагують органічним розчинником, наприклад, діетиловим ефіром або етилацетатом, краще етилацетатом. Об'єднані органічні екстракти сушать і відганяють розчинник. Залишок (сполука формули (A3)) можна без попереднього очищення використовувати на стадії 2. Стадія 2А Одержану на стадії 1А сполуку (A3) відновлюють за нітрогрупою та циклізують до сполуки формули (А4) (схема 2А). На стадії 2А 1 еквівалент нітросполуки формули (A3) розчиняють у кислоті, краще льодяній оцтовій кислоті, мурашиній кислоті або водній соляній кислоті, краще льодяній оцтовій кислоті, і нагрівають до 50-70°С, краще до приблизно 60°С. Потім до завершення екзотермічної реакції додають відновник, наприклад, цинк, олово або залізо, краще залізний порошок, і перемішують протягом 0,2-2 год, краще 0,5 год, при 100-125°С, краще при приблизно 117°С. Після охолодження до кімнатної температури залізну сіль відфільтровують і відганяють розчинник. Залишок розчиняють у розчиннику або суміші розчинників, на приклад, в етилацетаті або суміші дихлорметан/метанол у співвідношенні 9:1, і напівнасиченому розчині NaCl і фільтрують, наприклад, через кізельгур. Органічну фазу сушать та концентрують. Залишок (сполука формули (А4)) можна очищати шляхом хроматографії або кристалізації або використовувати для синтезу на стадії 3A у вигляді сирого продукту. Стадія 3A Одержану на стадії 2А сполуку формули (А4) можна шляхом електрофільного заміщення відповідно до схеми 3A перетворювати на сполуку формули (А5). 29 На стадії 3A 1 еквівалент аміду формули (А4) розчиняють в органічному розчиннику, наприклад, диметилформаміді або диметилацетаміді, краще диметилацетаміді, і охолоджують до температури в інтервалі приблизно від -5 до 5°С, краще до температури 0°С. Потім додають 0,9-1,3 еквіваленти гідриду натрію та 0,9-1,3 еквіваленти агенту метилування, наприклад, метилйодиду. Далі реакційну суміш перемішують протягом 0,1-3 год, краще протягом приблизно 1 год, при приблизно 0-10°С, краще при приблизно 5°С, і потім її за потреби можна залишати стояти ще на 12 год при температурі в зазначеному інтервалі. Після цього реакційну суміш зливають у суміш води з льодом і відокремлюють осад. Залишок (сполука формули (А5)) можна очищати шляхом хроматографії, Відповідно до варіанта 4.1 А, наприклад, 1 еквівалент сполуки формули (А5) і 1-3 еквівален 92470 30 краще на силікагелі, або шляхом кристалізації або використовувати для синтезу на стадії 4А у вигляді сирого продукту. Стадія 4А Одержану на стадії 3A сполуку формули (А5) можна амінувати до сполуки формули (А9) (схема 4А) відомими з літератури методами, які для варіанта 4.1 А, описані, наприклад, у наступних публікаціях: (a) M.P.V. Boarland, J.F.W. McOmie, J. Chem. Soc. 1951, cc, 1218-1221, або (б) F.H. S. Curd, F.C. Rose, J. Chem. Soc, 1946, cc. 343-348, а для варіанта 4.2А описані, наприклад, у наступних публікаціях: (а) Banks, J. Am. Chem. Soc. 66, 1944, с. 1131, (б) Ghosh та Dolly, J. Indian Chem. Soc. 58, 1981, cc. 512-513, або (в) N.P. Reddy та Μ. Tanaka, Tetrahedron Lett. 38, 1997, cc. 48074810. ти, краще приблизно 2 еквіваленти, сполуки формули (А6) без розчинника або в органічному 31 92470 32 розчиннику, такому, наприклад, як сульфолан, Відповідно до варіанта 4.3А, наприклад, 1 екдиметилформамід, диметилацетамід, толуол, Nвівалент сполуки формули (А5) і 1-3 еквіваленти метилпіролідон, диметилсульфоксид або діоксан, сполуки формули (А7) розчиняють у розчиннику, краще сульфолан, нагрівають до 100-220°С, наприклад, толуолі або діоксані, змішують із фокраще до приблизно 160°С, з витримуванням при сфіновими лігандами, наприклад, 2,2'-бісцій температурі протягом 0,1-4 год, краще 1 год. (дифенілфосфіно)-1,1'-бінафтилом, паладієвим Після охолодження продукт формули (А9) крискаталізатором, наприклад, тристалізують додаванням органічних розчинників (дибензиліденацетон)дипаладієм(0), і основою, або суміші розчинників, наприклад, суміші діетинаприклад, карбонатом цезію, і кип'ятять зі зволовий ефір/метанол, етилацетату, метиленхлоротним холодильником протягом 1-24 год, краще риду або діетилового ефіру, краще суміші діетипротягом 17 год. Потім реакційну суміш очищаловий ефір/метанол у співвідношенні 9:1, або ють, наприклад, на силікагелі та продукт формуочищають шляхом хроматографії. ли (А8) виділяють із розчину або одержують шляВідповідно до варіанта 4.2А, наприклад, 1 екхом відповідної кристалізації. вівалент сполуки формули (А5) і 1-3 еквіваленти Продукт формули (А8) розчиняють у прийнясполуки формули (А6) при нагріванні зі звороттному розчиннику, наприклад, діоксані, і змішуним холодильником перемішують протягом 1-48 ють із кислотою, наприклад, напівконцентровагод, краще протягом приблизно 5 год, з кислотою, ною соляною кислотою, наприклад, при наприклад, 1-10 еквівалентами 10-38%-вої соляспіввідношенні між розчинником і кислотою 3:1. ної кислоти, і/або спиртом, наприклад, етанолом, Після цього нагрівають зі зворотним холодильнипропанолом або бутанолом, краще етанолом. ком протягом 1-48 год, наприклад, протягом 12 Продукт, що випав в осад, формули (А9) відгод, і відокремлюють осад, який випав. За потрефільтровують, за потреби промивають водою, би продукт формули (А9) очищають шляхом крисушать і кристалізують із прийнятного органічного сталізації. розчинника. Стадія 5А На цій стадії, наприклад, 1 еквівалент сполуки формули (А9) розчиняють із 1 еквівалентом активатора, наприклад, тетрафторборату Обензотриазоліл-Ν,Ν,Ν',Ν'-тетраметилуронію (ТБТУ), і основою, взятою, наприклад, у кількості приблизно 1,5 еквіваленти, зокрема діізопропілетиламіном (ДІПЕА), в органічному розріджувачі, наприклад, дихлорметані, тетрагідрофурані, диметилформаміді, N-метилпіролідоні, диметилацетаміді, краще дихлорметані або диметилформаміді. Після додавання 1 еквівалента аміну формули (А10) реакційну суміш перемішують протягом 0,124 год, краще протягом приблизно 2 год, при температурі в інтервалі від 20 до 100°С. Продукт формули (A11) одержують, наприклад, кристалізацією або шляхом хроматографічного очищення. Сполуки загальної формули (І) можна синтезувати аналогічно до описаних нижче прикладів. Ці приклади, однак, призначені для більш детального пояснення даного винаходу та не обмежують його обсяг. Нижче розглянуте також одержання деяких проміжних сполук, використовуваних для синтезу сполук з відповідних прикладів. Одержання кислот Для синтезу сполук із прикладу 94 і прикладу 95 спочатку описаним нижче методом одержують проміжну сполуку Z1 50,0 г (0,48 моль) гідрохлориду метилового ефіру D-аланіну та 49,1 г (0,50 моль) циклогексанону додають в 300 мл дихлорметану та потім 33 92470 34 змішують із 41,0 г (0,50 моль) ацетату натрію та 159,0 г (0,75 моль) триацетоксиборгідриду натрію. Далі суміш залишають перемішуватися на ніч і потім додають 300 мл 10%-вого розчину гідрокарбонату натрію. Водну фазу екстрагують дихлорметаном. Об'єднані органічні фази промивають 10%вим розчином гідрокарбонату натрію, сушать над Na2SO4 та концентрують. Вихід: 72,5 г сполуки Z1a (прозора рідина). 72,5 г сполуки Z1a додають в 500 мл води та додають 76,6 г (0,39 моль) 2,4-дихлор-5нітропіримідину в 500 мл діетилового ефіру. Далі при температурі -5°С по краплях додають 100 мл Розчин 128,2 г (0,83 моль) гідрохлориду ети10%-вого розчину гідрокарбонату калію. Після цьолового ефіру D-аланіну та 71,5 г (0,85 моль) цикго спочатку перемішують протягом 3 год при -5°С, лопентанону в 1500 мл дихлорметану змішують із а потім ще протягом 12 год при кімнатній темпера70,1 (0,85 моль) ацетату натрію та 265,6 г (1,25 турі. Органічну фазу відокремлюють і сушать над моль) триацетоксиборгідриду натрію. Далі реакNa2SO4. При концентруванні викристалізовується ційну суміш перемішують протягом 12 год і потім продукт. зливають в 1,5 л 10%-вого розчину гідрокарбонату Вихід: 48,0 г сполуки Z1b (жовті кристали). натрію. Водну фазу екстрагують дихлорметаном. 48,0 г сполуки Z1b розчиняють в 350 мл льоОб'єднані органічні фази сушать над Na2SO4 та дяної оцтової кислоти та нагрівають до 60°С. Далі концентрують. порціями додають 47,5 г залізного порошку, що Вихід: 143,4 г сполуки Z2a (безбарвне масло). супроводжується підвищенням температури до 66,0 г сполуки Z2a додають в 500 мл води та 105°С. Потім реакційну суміш перемішують протязмішують із 85,0 г (0,44 моль) 2,4-дихлор-5гом трьох годин при 80°С, після чого в гарячому нітропіримідину в 500 мл діетилового ефіру. Далі стані фільтрують через целюлозу та концентрупри -5°С по краплях додають 100 мл 10%-вого ють. Залишок розмішують у воді й етилацетаті, розчину гідрокарбонату калію та реакційну суміш одержуючи світло-сірий осад, який відокремлюють перемішують протягом 48 год при кімнатній темвакуум-фільтрацією та промивають етилацетатом. пературі. Водну фазу екстрагують діетиловим ефіФільтрат промивають розведеним аміаком і вором, об'єднані органічні фази сушать над Na2SO4 дою, органічні фази сушать над Na2SO4, фільтрута концентрують. Розмішуванням з петролейним ють через активоване вугілля та концентрують. ефіром осаджують темно-червону тверду речовиТаким шляхом одержують додаткову кількість свіну, яку потім відокремлюють вакуум-фільтрацією. тло-сірої твердої речовини. Вихід: 88,0 г сполуки Z2b (жовті кристали). Вихід: 29,5 г сполуки Z1c (світло-сірі кристали). 88,0 г сполуки Z2b розчиняють в 1000 мл льо32,1 г сполуки Z1c додають в 300 мл диметидяної оцтової кислоти та при 60°С порціями змілацетаміду та змішують із 13 мл (0,2 моль) метилшують із 85 г залізного порошку, що супроводжуйодиду. Далі при -5°С порціями додають 6,4 г (0,16 ється підвищенням температури до 110°С. Далі моль) гідриду натрію у вигляді 60%-вої дисперсії в перемішують протягом 1 год при 60°С, після чого в мінеральному маслі. Через 2 год реакційну суміш гарячому стані піддають вакуум-фільтрації через зливають в 800 мл суміші води з льодом. Осад, що целюлозу та концентрують. Розмішуванням з 700 випав, відокремлюють вакуум-фільтрацією та мл води осаджують коричневу тверду речовину, промивають петролейним ефіром. яку відокремлюють вакуум-фільтрацією. Вихід: 33,0 г сполуки Z1d (бежеві кристали). Вихід: 53,3 г сполуки Z2c (коричнюваті криста4,0 г сполуки Z1d та 2,3 г (15 ммоль) 4-аміно-3ли). метилбензойної кислоти суспендують в 50 мл ета53,3 г сполуки Z2c розчиняють в 300 мл дименолу та 120 мл води, змішують із 2 мл конц. солятилацетаміду та змішують із 13 мл (0,21 моль) ної кислоти і протягом 48 год кип'ятять зі зворотметилйодиду. Далі при -5°С порціями додають 5,0 ним холодильником. Осад, що випав, при г (0,21 моль) гідриду натрію у вигляді 60%-вої дисохолодженні, відокремлюють вакуум-фільтрацією персії в мінеральному маслі. Через 12 год реакційта промивають водою, етанолом і діетиловим ефіну суміш зливають в 1000 мл суміші води з льодом ром. і осад, який утворився, відокремлюють вакуумВихід: 2,9 г сполуки Z1 (безбарвні кристали). фільтрацією. Для синтезу сполук із прикладу 188 і прикладу Вихід: 40,0 г сполуки Z2d (безбарвні кристали). 203 спочатку описаним нижче методом одержують 4,0 г сполуки Z2d та 2,8 г (16 ммоль) 4-аміно-3проміжну сполуку Z2 хлорбензойної кислоти суспендують в 25 мл етанолу і 60 мл води, змішують із 3 мл конц. соляної кислоти та кип'ятять зі зворотним холодильником протягом 43 год. Осад, що випав при охолодженні, відокремлюють вакуум-фільтрацією та промивають його водою, етанолом і діетиловим ефіром. Вихід: 0,9 г сполуки Z2 (безбарвні кристали). Для синтезу сполук із прикладів 19, 21, 22, 23, 45, 55, 58, 116, 128, 131, 133, 134, 136, 138, 177, 217, 231, 239, 46, 184, 166 та 187 спочатку описа 35 92470 36 ним нижче методом одержують проміжну сполуку при 0°С, а потім протягом 30 хв при кімнатній темZ3 пературі та на завершення додають лід. Після цього реакційну суміш концентрують і змішують із 300 мл води. Осад, що утворився, відокремлюють вакуум-фільтрацією та промивають петролейним ефіром. Вихід: 23,0 г сполуки Z3e (безбарвна тверда речовина). 6,0 г сполуки Z3e та 5,1 г (31 ммоль) 4-аміно-3метоксибензойної кислоти суспендують в 90 мл етанолу та 350 мл води, змішують із 3,5 мл конц. соляної кислоти та кип'ятять зі зворотним холодильником протягом 48 год. Далі реакційну суміш концентрують, залишок розмішують із сумішшю метанол/діетиловий ефір і осад, який утворився, відокремлюють вакуум-фільтрацією. 54,0 г (0,52 моль) D-2-аміномасляної кислоти Вихід: 6,3 г сполуки Z3 (світло-бежеві кристасуспендують в 540 мл метанолу та при охололи). дженні льодом повільно змішують з 132 г (1,1 Для синтезу сполук із прикладів 81, 82, 93, 137 моль) тіонілхлориду. Далі протягом 1,5 год кип'яспочатку описаним нижче методом одержують тять зі зворотним холодильником і потім концентпроміжну сполуку Z4 рують. Масло, що залишилося, змішують із 540 мл трет-бутилметилового ефіру та безбарвні кристали, що утворилися, відокремлюють вакуумфільтрацією. Вихід: 78,8 г сполуки Z3a (безбарвні кристали). 74,2 г сполуки Z3a та 43,5 мл (0,49 моль) циклопентанону розчиняють в 800 мл дихлорметану. Після додавання 40,0 г (0,49 моль) ацетату натрію та 150,0 г (0,71 моль) триацетоксиборгідриду натрію при 0°С перемішують протягом 12 год при кімнатній температурі та потім додають 500 мл 20%-вого розчину гідрокарбонату натрію. Водну фазу екстрагують дихлорметаном. Об'єднані органічні фази промивають водою, сушать над MgSO4 25,0 г (0,19 моль) гідрохлориду етилового ефіта концентрують. ру 1-аміноциклопропан-1-карбонової кислоти та Вихід: 85,8 г сполуки Z3b (жовтувате масло). 16,8 г (0,20 моль) циклопентанону розчиняють в 40,0 г сполуки Z3b і 30,0 г (0,22 моль) карбона300 мл дихлорметану й змішують із 16,4 г (0,20 ту калію суспендують в 600 мл ацетону та при моль) ацетату натрію та 61,7 г (0,29 моль) триацеохолодженні льодом змішують із 45,0 г (0,23 моль) токсиборгідриду натрію. Після цього реакційну 2,4-дихлор-5-нітропіримідину в 200 мл ацетону. суміш залишають перемішуватися на ніч і потім Через 12 год додають ще 5,0 г 2,4-дихлор-5зливають в 400 мл 10%-вого розчину гідрокарбонітропіримідину та перемішують протягом 3 год. нату натрію. Водну фазу екстрагують дихлорметаДалі реакційну суміш концентрують, розчиняють в ном. Об'єднані органічні фази сушать над Na2SO4 800 мл етилацетату й 600 мл води та водну фазу та концентрують. екстрагують етилацетатом. Об'єднані органічні Вихід: 34,5 г сполуки Z4a (безбарвне масло). фази промивають водою, сушать над MgSO4 та До суміші 34,5 г сполуки Z4a в 350 мл води концентрують. додають 42,5 г (0,22 моль) 2,4-дихлор-5Вихід: 75,0 г сполуки Z3c (коричневе масло). нітропіримідину в 350 мл діетилового ефіру. Далі 100 г сполуки Z3c розчиняють в 650 мл льодяпри -5°С змішують із 80 мл 10%-вого розчину гідної оцтової кислоти та при 70°С порціями змішурокарбонату калію та залишають перемішуватися ють із 20 г залізного порошку. Далі спочатку перена ніч при кімнатній температурі. Водну фазу екстмішують протягом 1 год при 70°С, а потім рагують діетиловим ефіром. Об'єднані органічні протягом 1,5 год при 100°С, після чого в гарячому фази сушать над Na2SO4 та концентрують. стані фільтрують через кізельгур. Потім реакційну Вихід: 53,8 г сполуки Z4b (коричневе масло). суміш концентрують, розчиняють у суміші мета20,1 г сполуки Z4b розчиняють в 200 мл льонол/дихлорметан, подають на силікагель і очищадяної оцтової кислоти та при 60°С порціями зміють шляхом екстракції етилацетатом у приладі шують із 19,1 г залізного порошку, що супроводжуСокслета. Розчинник видаляють і залишок осається підвищенням температури до 100°С. Потім джують розмішуванням з метанолом. суміш перемішують протягом 3 год при 60°С, після Вихід: 30,0 г сполуки Z3d (світло-коричневі чого піддають вакуум-фільтрації через целюлозу кристали). та концентрують. Залишок розмішують у воді й 25,0 г сполуки Z3d та 6,5 мл (0,1 моль) метилетилацетаті, одержуючи жовтий осад, який відойодиду додають в 250 мл диметилацетаміду та кремлюють вакуум-фільтрацією. Фільтрат промипри -10°С змішують із 3,8 г (0,95 моль) гідриду навають розведеним аміаком і водою, органічні фази трію у вигляді 60%-вої дисперсії в мінеральному маслі. Далі спочатку перемішують протягом 20 хв 37 92470 38 сушать над Na2SO4 та концентрують. Продукт крикремлюють вакуум-фільтрацією через кізельгур, сталізують після додавання діетилового ефіру. сушать над MgSO4, концентрують і очищають коВихід: 4,0 г сполуки Z4c (жовті кристали). лонковою хроматографією (елюент: етилаце7,8 г сполуки Z4c та 2,6 мл (0,04 моль) метилтат/циклогексан у співвідношенні 1:1). йодиду розчиняють в 100 мл диметилацетаміду та Вихід: 1,9 г сполуки Z5c (безбарвні кристали). при -5°С порціями змішують із 1,5 г (0,04 моль) 1,9 г сполуки Z5c розчиняють в 32 мл диметигідриду натрію у вигляді 60%-вої дисперсії в мінелацетаміду та при охолодженні льодом змішують ральному маслі. Через 2 год реакційну суміш злиіз 0,3 г (7 ммоль) гідриду натрію у вигляді 60%-вої вають у суміш води з льодом і осад, який утворивдисперсії в мінеральному маслі. Через 10 хв дося, відокремлюють вакуум-фільтрацією. дають 0,5 мл (7 ммоль) метилйодиду і протягом 3 Вихід: 7,5 г сполуки Z4d (коричнюваті кристагод перемішують при кімнатній температурі. Далі ли). реакційну суміш концентрують і змішують із водою. 3,0 г сполуки Z4d та 1,9 г (11 ммоль) 4-аміно-3Осад, що утворився, відокремлюють вакуумметоксибензойної кислоти суспендують в 40 мл фільтрацією та промивають петролейним ефіром. етанолу та 80 мл води, змішують із 2 мл конц. соВихід: 1,6 г сполуки Z5d (безбарвні кристали). ляної кислоти і протягом 20 год кип'ятять зі зворо14,0 г сполуки Z5d та 10,0 г (0,06 моль) 4тним холодильником. Після цього додають ще 0,5г аміно-3-метоксибензойної кислоти суспендують в 4-аміно-3-метоксибензойної кислоти та кип'ятять зі 200 мл діоксану та 80 мл води, змішують із 10 мл зворотним холодильником протягом 48 год. Осад, конц. соляної кислоти та кип'ятять зі зворотним який випав при охолодженні, відокремлюють вакухолодильником протягом 40 год. Осад, який випав ум-фільтрацією та промивають водою, етанолом і при охолодженні, відокремлюють вакуумдіетиловим ефіром. фільтрацією та промивають водою, діоксаном і Вихід: 2,1 г сполуки Z4 (безбарвні кристали). діетиловим ефіром. Для синтезу сполук із прикладів 162, 43, 53, Вихід: 13,9 г сполуки Z5 (безбарвні кристали). 161, 202, 211, 215 та 212 спочатку описаним нижче Для синтезу сполук із прикладів 88, 194, 229 та методом одержують проміжну сполуку Z5 89 спочатку описаним нижче методом одержують проміжну сполуку Z6 Суміш із 73,4 мл (0,5 моль) етилового ефіру 2бромізомасляної кислоти, 87,1 мл (0,75 моль) 3метил-1-бутиламіну, 82,5 г (0,6 моль) йодиду натрію та 76,0 г (0,6 моль) карбонату калію протягом 3 днів кип'ятять зі зворотним холодильником в 1000 мл етилацетату. Наявні солі відфільтровують і фільтрат концентрують. Вихід: 97,0 г сполуки Z5a (червоне масло). 49,0 г (0,25 моль) 2,4-дихлор-5-нітропіримідину та 38,3 г (0,28 моль) карбонату калію суспендують в 500 мл ацетону та при 0°С змішують із 93,0 г сполуки Z5a в 375 мл ацетону. Реакційну суміш залишають перемішуватися на ніч при кімнатній температурі, фільтрують та концентрують. Розчинений в етилацетаті залишок промивають водою й органічні фази сушать над MgSO4 та концентрують. Вихід: 102,7 г сполуки Z5b (коричневе масло). 22,7 г сполуки Z5b розчиняють в 350 мл льодяної оцтової кислоти та при 60°С порціями змішують із 17,4 г залізного порошку. Після завершенні цієї операції додавання протягом 0,5 год кип'ятять зі зворотним холодильником, після чого фільтрують у гарячому стані та концентрують. Залишок розчиняють в 200 мл суміші дихлорметан/метанол (у співвідношенні 9:1) і промивають розчином хлориду натрію. Органічну фазу відо 6,0 г (0,06 моль) L-2-аміномасляної кислоти додають в 80 мл 0,5-молярної сірчаної кислоти та при 0°С змішують із 5,5 г (0,08 моль) нітриту натрію в 15 мл води. Далі реакційну суміш протягом 22 год перемішують при 0°С, змішують із сульфатом амонію та фільтрують. Фільтрат екстрагують діетиловим ефіром і об'єднані органічні фази сушать над MgSO4 та концентрують. Вихід: 6,0 г сполуки Z6a (жовте масло). 200 мл метанолу при охолодженні льодом послідовно змішують із 65,0 мл (0,89 моль) тіонілхлориду та 76,0 г сполуки Z6a в 50 мл метанолу. Далі суміш спочатку перемішують протягом 1 год при 0°С, а потім протягом 2 год при кімнатній температурі та після цього метанол і залишковий тіонілхлорид видаляють у вакуумі при 0°С. Вихід: 40,0 г сполуки Z6b (жовте масло). 30,0 мл (0,17 моль) трифторметансульфонового ангідриду додають в 150 мл дихлорметану та при охолодженні льодом змішують протягом години з розчином 20,0 г сполуки Z6b та 14,0 мл (0,17 моль) піридину в 50 мл дихлорметану. Після цього суміш протягом 2 год перемішують при кімнатній температурі, солі, що утворилися, відокремлюють вакуум-фільтрацією та потім промивають 100 мл води. Органічну фазу сушать над MgSO4 та концентрують. 39 92470 40 Вихід: 42,0 г сполуки Z6c (світло-жовте масло). Для синтезу сполук із прикладів 26, 20, 32, 56, До розчину 15,5 мл (0,17 моль) аніліну та 101, 112, 209 спочатку описаним нижче методом 24,0мл (0,17 моль) триетиламіну в 400 мл дихлородержують проміжну сполуку Z7 метану при охолодженні льодом протягом години по краплях додають 42,0 г сполуки Z6c в 200 мл дихлорметану. Після цього суміш перемішують спочатку протягом 1 год при кімнатній температурі, а потім протягом 2 год при 35°С. Далі реакційну суміш промивають водою, сушать над MgSO4 та концентрують. Одержаний залишок очищають перегонкою (95-100°С, 1 10-3 мбар). Вихід: 14,0 г сполуки Z6d (безбарвне масло). 14,0 г сполуки Z6d та 16,0 г (0,1 моль) карбонату калію суспендують в 100 мл ацетону та при 10°С змішують із 16,0 г (0,08 моль) 2,4-дихлор-5нітропіримідину. Потім суміш перемішують протя50,0 г (0,36 моль) гідрохлориду метилового гом 4 год при 40°С, солі, що утворилися, відокремефіру D-аланіну суспендують в 500 мл дихлормелюють вакуум-фільтрацією і фільтрат концентрутану та 35 мл ацетону й змішують із 30,0 г (0,37 ють. Залишок розчиняють в 300 мл етилацетату та моль) ацетату натрію та 80,0 г (0,38 моль) триацепромивають водою. Органічну фазу сушать над токсиборгідриду натрію. Потім суміш перемішують MgSO4 та концентрують. протягом 12 год, після чого зливають в 400 мл Вихід: 31,0 г сполуки Z6e (коричневе масло). 10%-вого розчину гідрокарбонату натрію. Органіч31,0 г сполуки Z6e розчиняють в 200 мл льону фазу сушать над Na2SO4 та концентрують. дяної оцтової кислоти та при 60°С порціями зміВихід: 51,0 г сполуки Z7a (жовте масло). шують із 10 г залізного порошку, що супроводжуСуспензію 51,0 г сполуки Z7a в 450 мл води ється підвищенням температури до 85°С. Потім змішують із 80,0 г (0,41 моль) 2,4-дихлор-5суміш перемішують протягом наступної години при нітропіридину в 450 мл діетилового ефіру. Далі 60°С, фільтрують через кізельгур та концентрують. при -5°С по краплях додають 100 мл 10%-вого Залишок розмішують із метанолом, осаджуючи розчину гідрокарбонату калію. Після цього реакпродукт. ційну суміш перемішують протягом 3 год, органічні Вихід: 4,5 г сполуки Z6f (коричневі кристали). фази сушать над Na2SO4 та концентрують. До суміші 4,5 г сполуки Z6f та 1,0 мл (16 Вихід: 74 г сполуки Z7b (жовте масло). ммоль) метилйодиду в 100 мл диметилацетаміду 18,6 г сполуки Z7b розчиняють в 200 мл льопри -20°С порціями додають 0,6 г (16 ммоль) гіддяної оцтової кислоти та при 60°С порціями зміриду натрію у вигляді 60%-вої дисперсії у мінерашують із 20,0 г залізного порошку. Далі суміш прольному маслі. Через 1 год реакційну суміш змішутягом 2 год перемішують при 60°С, а потім ють із 50 мл води та концентрують. Залишок піддають вакуум-фільтрації через целюлозу. Зарозмішують із 200 мл води, осад відокремлюють лишок розчиняють в етилацетаті та промивають вакуум-фільтрацією та промивають петролейним водою та конц. аміаком. Органічну фазу сушать ефіром. над Na2SO4 та концентрують. Залишок кристаліВихід: 4,5 г сполуки Z6g (безбарвні кристали). зують із діетилового ефіру. Суспензію 1,5 г сполуки Z6g та 1,4 г (8 ммоль) Вихід: 9,8 г сполуки Z7c (безбарвні кристали). метилового ефіру 4-аміно-3-метоксибензойної 17,0 г сполуки Z7c та 7 мл (0,1 моль) метилйокислоти в 30 мл толуолу змішують із 0,4 г (0,6 диду розчиняють в 200 мл диметилацетаміду та ммоль) 2,2'-біс-(дифенілфосфіно)-1,1'-бінафтилу, при -5°С змішують із 4,0 г (0,1 моль) гідриду натрію 0,23 г (0,3 ммоль) трису вигляді 60%-вої дисперсії в мінеральному маслі. (дибензиліденацетон)дипаладію(0) і 7,0 г (21 Далі реакційну суміш перемішують протягом 30 хв ммоль) карбонату цезію та кип'ятять зі зворотним і потім зливають в 300 мл суміші води з льодом. холодильником протягом 17 год. Далі реакційну Осад, що утворився, відокремлюють вакуумсуміш подають на силікагель і очищають колонкофільтрацією та виділяють, розмішуючи з петровою хроматографією (елюент: суміш дихлормелейним ефіром. тан/метанол у співвідношенні 9:1). Вихід: 14,8 г сполуки Z7d (бежеві кристали). Вихід: 1,7 г сполуки Z6h (жовті кристали). 0,9 г сполуки Z7d та 1,5 г (9 ммоль) 4-аміно-31,7 г сполуки Z6h розчиняють в 50 мл діоксану, метоксибензойної кислоти нагрівають до 210°С з змішують із 15 мл напівконцентрованої соляної витримуванням при цій температурі протягом кислоти і протягом 12 год кип'ятять зі зворотним 30хв. Після охолодження залишок розмішують із холодильником. Осад, що утворився після охолоетилацетатом, одержуючи осад, який відокремдження, відокремлюють вакуум-фільтрацією. люють вакуум-фільтрацією. Вихід: 1,1 г сполуки Z6 (безбарвна тверда реВихід: 1,2 г сполуки Z7 (сірі кристали). човина). Аналогічно розглянутим вище методам синтезу одержують, наприклад, наступні кислоти: 41 Синтез амінових фрагментів L-R5 Представлені нижче аміни одержують наступними методами. 1,1-диметил-2-диметиламіно-1-ілетиламін та 1,1-диметил-2-піперидин-1-ілетиламін Зазначені сполуки одержують методами, описаними в наступних літературних джерелах: (a) S. Schuetz та ін., Arzneimittel-Forschung 21, 1971, сс. 739-763, (б) V.M. Belikov та ін., Tetrahedron 26, 1970, сс. 1199-1216, та (в) Е.В. Butler та McMillan, J. Amer. Chem. Soc. 72, 1950, с. 2978. Інші аміни одержують модифікаціями описаних у вищевказаних публікаціях методів наступним шляхом. 1,1-диметил-2-морфолін-1-ілетиламін 92470 42 утворився, відокремлюють вакуум-фільтрацією. Вихід: 21,7 г білого порошку. 5 г цього білого порошку розчиняють в 80 мл метанолу та при додаванні 2 г нікелю Ренея протягом 40 хв обробляють воднем при температурі 35°С і тиску 50 фунтів/кв. дюйм. Таким шляхом одержують 3,6 г 1,1диметил-2-морфолін-1-ілетиламіну. Аналогічно цьому методу одержують наступні аміни. 1,1-диметил-N-метилпіперазин-1-ілетиламін 1,1--диметил-2-піролідин-1-ілетиламін Синтез 1,3-диморфолін-2-амінопропану До 8,7 мл морфоліну та 9,3 мл 2-нітропропану при охолодженні льодом повільно по краплях додають (
ДивитисяДодаткова інформація
Назва патенту англійськоюDihydropteridinone infusion solution having a long shelf life
Автори англійськоюMohr Detlef, Veit Claus, Traulsen Fridtjof
Назва патенту російськоюСтабильный при хранении инфузионный раствор дигидроптеридинонов
Автори російськоюМор Детлеф, Вейт Клаус, Траульсен Фридтйоф
МПК / Мітки
МПК: A61P 35/00, A61K 31/4985, A61K 31/519
Мітки: дигідроптеридинонів, стабільний, інфузійний, розчин, зберіганні
Код посилання
<a href="https://ua.patents.su/54-92470-stabilnijj-pri-zberiganni-infuzijjnijj-rozchin-digidropteridinoniv.html" target="_blank" rel="follow" title="База патентів України">Стабільний при зберіганні інфузійний розчин дигідроптеридинонів</a>
Попередній патент: Фумарат 4-[[4-[[4-(2-ціаноетеніл)-2,6-диметилфеніл]аміно]-2-піримідиніл]аміно]бензонітрилу
Наступний патент: Спосіб плазмоелектричної генерації енергії та плазмоелектрична система для його здійснення (варіанти)
Випадковий патент: Комплексна домішка