Застосування синбіотика для покращення кишкової мікробіоти у дітей, народжених шляхом кесаревого розтину
Номер патенту: 97662
Опубліковано: 12.03.2012
Автори: Спренгер Норберт, Рошат Флоренс, Фішот Марі-Клер, Хубер-Хааг Карл-Йозеф
Формула / Реферат
1. Застосування пробіотичного штаму Lactobacillus rhamnosus і суміші олігосахаридів, яка містить від 5 % до 70 мас. % принаймні одного N-ацетильованого олігосахариду, вибраного з групи, що включає GalNAcα1,3Galβ1,4Glc і Galβ1,6GalNAcα1,3Galβ1,4Glc, 20-90 мас. % принаймні одного нейтрального олігосахариду, вибраного з групи, що включає Galβ1,6Gal, Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc і Galβ1,3Galβ1,3Galβ1,4Glc, і 5-50 мас. % принаймні одного сіалійованого олігосахариду, вибраного з групи, що включає NeuAcα2,3Galβ1,4Glc і NeuAcα2,6Galβ1,4Glc як стимулятора розвитку ранньої біфідогенної кишкової мікробіоти у дітей, народжених шляхом кесарева розтину, у виробництві лікарського засобу або лікувальної харчової композиції.
2. Застосування пробіотичного штаму Lactobacillus rhamnosus і суміші олігосахаридів, яка містить від 5 % до 70 мас. % принаймні одного N-ацетильованого олігосахариду, вибраного з групи, що включає GalNAcα1,3Galβ1,4Glc і Galβ1,6GalNAcα1,3Galβ1,4Glc, 20-90 мас.% принаймні одного нейтрального олігосахариду, вибраного з групи, що включає Galβ1,6Gal, Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc і Galβ1,3Galβ1,3Galβ1,4Glc, і 5 - 50 мас. % принаймні одного сіалійованого олігосахариду, вибраного з групи, що включає NeuAcα2,3Galβ1,4Glc і NeuAcα2,6Galβ1,4Glc як препарату для зменшення ризику розвитку алергії у дітей, народжених шляхом кесарева розтину, у виробництві лікарського засобу або лікувальної харчової композиції.
3. Застосування пробіотичного штаму Lactobacillus rhamnosus і суміші олігосахаридів, яка містить від 5 % до 70 мас. % принаймні одного N-ацетильованого олігосахариду, вибраного з групи, що включає GalNAcα1,3Galβ1,4Glc і Galβ1,6GalNAcα1,3Galβ1,4Glc, 20-90 мас. % принаймні одного нейтрального олігосахариду, вибраного з групи, що включає Galβ1,6Gal, Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc і Galβ1,3Galβ1,3Galβ1,4Glc, і 5-50 мас.% принаймні одного сіалійованого олігосахариду, вибраного з групи, що включає NeuAcα2,3Galβ1,4Glc і NeuAcα2,6Galβ1,4Glc як препарату для запобігання або лікування діареї у дітей, народжених шляхом кесарева розтину, у виробництві лікарського засобу або лікувальної харчової композиції.
4. Застосування за будь-яким з пунктів 1-3, яке відрізняється тим, що пробіотик є Lactobacillus rhamnosus ATCC 53103 або Lactobacillus rhamnosus CGMCC 1.3724.
5. Застосування за будь-яким з пунктів 1-3, яке відрізняється тим, що суміш олігосахаридів містить від 10 % до 70 мас. % N-ацетильованих олігосахаридів, від 20 % до 80 мас. % нейтральних олігосахаридів і від 10 % до 50 мас. % сіалійованих олігосахаридів.
6. Застосування за будь-яким з пунктів 1-3, яке відрізняється тим, що суміш олігосахаридів містить від 15 % до 40 мас. % N-ацетильованих олігосахаридів, від 40 % до 60 мас. % нейтральних олігосахаридів і від 15 % до 30 мас. % сіалійованих олігосахаридів.
7. Застосування за будь-яким з пунктів 1-3, яке відрізняється тим, що суміш олігосахаридів містить від 5 % до 20 мас. % N-ацетильованих олігосахаридів, від 60 % до 90 мас. % нейтральних олігосахаридів і від 5 % до 30 мас. % сіалійованих олігосахаридів.
8. Застосування за будь-яким з пунктів 1-7, яке відрізняється тим, що лікарський засіб або лікувальна харчова композиція вводиться дитині відразу після пологів і протягом наступних принаймні 2 місяців.
9. Застосування за будь-яким з пунктів 1-8, яке відрізняється тим, що лікарський засіб або лікувальна харчова композиція вводиться дитині протягом принаймні 6 місяців після пологів.
10. Застосування за будь-яким з п. 1-9, яке відрізняється тим, що лікувальна харчова композиція є сумішшю для дитячого харчування.
11. Застосування за п. 10, яке відрізняється тим, що суміш для дитячого харчування містить в одному грамі композиції між 103 і 1012 КУО (в сухій масі) пробіотика Lactobacillus rhamnosus і від 0,2 до 5 грамів суміші олігосахаридів на один літр розведеної суміші.
Текст
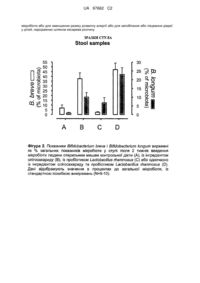
Реферат: Застосування пробіотичного штаму Lactobacillus rhamnosus і суміші олігосахаридів, що містить 5-70 мас. % принаймні одного N-ацетильованого олігосахариду, вибраного з групи, що включає GalNAcα1,3Galβ1,4Glc і Galβ1,6GalNAcα1,3Galβ1,4Glc, 20-90 мас. % принаймні одного нейтрального олігосахариду, вибраного з групи, що включає Galβ1,6Gal, Galβ1,6Galβ1,4Glc Galβ1,6Galβ1,6Glc, Galβ1,3Galβ1,3Glc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4Glc, Galβ1,6Galβ1,3Galβ1,4Glc Galβ1,3Galβ1,6Galβ1,4Glc і Galβ1,3Galβ1,3Galβ1,4Glc, і 5-50 мас. % принаймні одного сіалійованого олігосахариду, вибраного з групи, що включає NeuAcα2,3Galβ1,4Glc і NeuAcα2,6Galβ1,4Glc, у виробництві лікарського засобу або лікувальної харчової композиції, призначених для стимулювання розвитку ранньої біфідогенної кишкової UA 97662 C2 (12) UA 97662 C2 мікробіоти або для зменшення ризику розвитку алергії або для запобігання або лікування діареї у дітей, народжених шляхом кесарева розтину. UA 97662 C2 5 10 15 20 25 30 35 40 45 50 55 Даний винахід відноситься до введення грудним дітям, народженим шляхом кесарева розтину, спеціальної синбіотичної суміші, тобто, пробіотика і олігосахариду, яка сприяють розвитку ранньої біфідогенної кишкової мікробіоти. Вважається, що безпосередньо перед пологами шлунково-кишковий тракт дитини є стерильним. В процесі природних пологів він контактує з бактеріями травного тракту, шкіри матері і навколишнього її середовища і починає колонізуватися. У фекальній мікробіоті здорової вагинально-народженої, вигодовуваної грудьми дитини у віці від 2 до 4 тижнів, яку можна прийняти за оптимальну мікробіоту для вказаної вікової групи, домінують види біфідобактерій з деякими видами лактобацил і незначними кількостями бактероїдів, таких як Bacteriodes fragilis, за винятком потенційних патогенів, таких як клостридії. Після закінчення періоду відняття від грудей у віці приблизно 2 років встановлюється склад кишкової мікробіоти, схожий з складом кишкової мікробіоти дорослої людини. Слід відмітити, що у здорової, вагинально-народженої, вигодовуваної грудьми дитини біфідобактерії формують основу мікробіоти, налічуючи від 60% до 90% загальної кількості бактерій в кишечнику немовляти. Грудне вигодовування сприяє також розвитку захисного кишкового бар'єру, що в умовах домінування біфідобактерій приводить до поліпшення всмоктування і, отже, утилізації споживаних харчових речовин. Grönlund et аl. вивчали фекальну мікробіоту здорових дітей, народжених шляхом кесарева розтину, і порівнювали її з фекальною мікробіотою відповідної за віком групи вагінальнонароджених дітей. Вони прийшли до висновку, що кишкова флора дітей, народжених шляхом кесарева розтину, може змінюватися в період до шести місяців після народження. Вони особливо відзначили, що швидкість колонізації кишківника біфідобактеріями і лактобацилами в групі дітей, народжених шляхом кесарева розтину, досягала швидкості колонізації кишківника в групі вагінально-народжених дітей лише через один місяць і 10 днів, відповідно (Grönlund et al., "Fecal Microflora in Heathy Infants Born by Different Methods of Delivery: Permanent Changes in Intestinal Flora After Cesarean Delivery", Journal of Pediatric Gastroenterology and Nutrition, 28:1925). Інші дослідники висловили припущення, що ця сповільнена/аберрантна колонізація може мати специфічні наслідки в рамках подальшого розвитку немовляти, і що існує можливий зв'язок між цими наслідками і відмінностями в кишковій мікробіоті. Наприклад, Laubereau еt аl., встановили, що діти, народжені шляхом кесарева розтину, відносяться до групи підвищеного ризику розвитку діареї в порівнянні з вагінально-народженими дітьми. Negele et аl., встановили, що пологи з допомогою кесарева розтину можуть бути додатковим чинником ризику проявів укладненого дихання і підвищеної чутливості до харчових алергенів у віці до двох років (Negele et аl. "Mode of delivery and development of atopic disease during the first 2 years of life", Pediatr. Allergy Immunol. 2004, 15: 48-54). Висловлювалося також припущення, що систематичні незначні запалення і субоптимальна кишкова мікробіота також можуть призводити до розвитку ожиріння (Fantuzzi G. "Adipose tissue, adipokines, and inflammation", J. Allergy Clin. Immunol. 2005, 115: 911919; Bäckhed F., Ding H., Wang T., et al. "The gut microbiota as an environmental factor that regulates fat storage", Proc. Natl. Acad. Sci. USA. 2004, 101:15718-15723). Вигодовування материнським молоком рекомендується для всіх грудних дітей. Проте в деяких випадках грудне вигодовування є недостатнім або безуспішним за медичними показниками або сама мати відмовляється годувати грудьми. Для таких ситуацій розроблені суміші для дитячого харчування. Останнім часом певні штами бактерій викликали підвищений інтерес, що пояснюється тим, що при попаданні в організм людини вони проявляють, як було встановлено, цінні для його здоров'я властивості. Зокрема, було встановлено, що специфічні штами роду Lactobacilli і роду Bifidobacteria здатні колонізувати кишечник, знижувати здібність патогенних бактерій до прилипання до кишкового епітелію, викликати імуномодулюючий ефект і полегшувати підтримку хорошого самопочуття. Такі бактерії іноді називають пробіотиками, і вже запропоновано додавати відповідні пробіотичні бактерії в суміші для дитячого харчування. Проведені екстенсивні дослідження по ідентифікації нових пробіотичних штамів, наприклад, в EP 0 199 535, EP 0 768 375, WO 97/00078, EP 0 577 903 і WO 00/53200 розкриваються специфічні штами лактобацил і біфідобактерій і їх корисна для здоров'я дія. Зовсім нещодавно почало виявлятися деяке турбування у зв'язку із додаванням пробіотичних бактерій до суміші для харчування немовлят, що є єдиним джерелом харчування для немовлят у перші шість місяців життя. Ці побоювання були узагальнені в медицинському меморандумі Комітета по харчуванню ESPGHAN (Європейське товариство педіатричної гастроентерології, гепатології і харчування), що зветься "Пробіотичні бактерії в дієтичних 1 UA 97662 C2 5 10 15 20 25 30 35 40 45 50 55 60 продуктах для немовлят" ("Probiotic Bacteria in Dietetic Products for Infants", Journal of Paediatric Gastroenterology and Nutrition, 38: 365-374). Іншим підходом до стимулювання кількості та/або активності корисних бактерій в товстій кишці є додавання в їжу пребіотиків. Пребіотик - це неперетравлюваний компонент харчового продукта, який сприятливо діє на організм реципієнта, вибірково стимулюючі зростання та/або активність однієї бактерії або певної кількості видів бактерій у товстій кишці, тим самим поліпшуючи стан здоров'я організму. Такі інгредієнти є неперетравлюваними в тому смислі, що вони не розпадаються і не поглинаються шлунком або тонкою кишкою і таким чином проходять неушкодженими в товсту кишку, де вибірково ферментуються корисними бактеріями. Приклади пребіотиків включають деякі олігосахариди, такі як фруктоолігосахариди (FOS) і галактоолігосахариди (GOS). Жіноче молоко, як відомо, містить велику кількість неперетравлюваних олігосахаридів, ніж будь-які інші види тваринного молока. Фактично неперетравлювані олігосахариди являють собою третій і найзначніший з представлених твердих компонентів грудного молока (після лактози і ліпідів), що зустрічається в концентрації 12 - 15 г/л в молозиві і 5 - 8 г/л в зрілому молоці. Олігосахариди жіночого молока є дуже стійкими до ферментативного гідролізу, що говорить про те, що ці олігосахариди можуть виявляти життєво важливі функцій, не пов'язані безпосередньо із їх калорійністю. По мірі того, як композиція жіночого молока стає більш зрозумілою, пропонується також додавати пребіотики до сумішей для харчування немовлят. В продажу наявні різноманітні суміші для харчування немовлят, доповнені пребіотиками, такими як, наприклад, суміші фруктоолігосахаридів і галактоолігосахаридів. Однак, такі суміші тільки в цілому наближені до суміші олігосахаридів жіночого молока. В жіночому молоці знайдено більше 100 різних олігосахариди их компонентів, деякі з яки поки що взагалі не знайдені в молоці тварин, наприклад, коров'ячому молоці, або були знайдені лише в малих кількостях. Прикладами класів олігосахаридів жіночого молока, які наявні в коров'ячому молоці і молозиві лише в дуже малих кількостях, або зовсім відстутні, є сіалійовані і фукозиловані олігосахариди. В ході безупинних пошуків, метою яких є отримання сумішей для харчування немовлят, що відтворюють композицію і ефективність жіночого молока настільки близько, наскільки це можливо, були також запропоновані суміші для харчування немовлят, які містять одночасно і пробіотики, і пребіотики. Наприклад, в WO 2005/000748 пропонується доповнити суміш для харчування немовлят сумішшю штама Bifidobacterium breve, галактоолігосахаридів і фруктоолігосахаридів (інулін). Заявляється, що ця суміш, яка характеризується як синбіотик, регулює популяцію Bifidobacterium в товстій кишці немовлят, які споживають дану доповнену рецептуру, що стану популяції більш «близької до немовлят», тобто, що має знижений вміст видів Bifidobacterium catenulatum, Bifidobacterium pseudocatenulatum і Bifidobacterium adolescentis і збільшений - видів Bifidobacterium infantis, Bifidobacterium breve і Bifidobacterium Іоngum. Також заявляється, що суміш є корисною для профілактики або терапії стану імунної системи. Кишкова мікробіота має важливу роль в гідролізі неперетравлюваних олігосахаридів і полісахаридів, який перетворює їх на моносахариди, що поглинаються, а також активації ліпопротеїнліпази при безпосередній дії на ворсинчастий епітелій. Крім того, нещодавно було доведено, що жіноче молоко містить не лише олігосахариди, але також і біфідобактерії. Одночасно, геномні дослідження переконливо продемонстрували, що наявні у кишківнику виготовуваних грудьми дітей біфідобактерії, такі як Bifidobacterium Іоngum, забезпечуються спеціально для утилізації в якості нутрієнтів олігосахаридів грудного молока. Bifidobacterium longum також адаптовані до умов товстого кишківника, де проходить виділення енергії із вуглеводів, що повільно поглинаються. Дуже скоро буде отримано все більше доказів того, що розвиток відповідної кишкової мікробіоти протягом ранніх періодів життя є дуже вагомим для подальшого здоров'я особи. Кількість випадків пологів за допомогою кесарева розтини продовжує рости, досягаючи в деяких країнах 70% загального числа пологів. Звідси ясно, що існує необхідність забезпечення засобів для зниження ризику того, щоб діти, народжені шляхом кесарева розтину, не страждали від негативних для їх здоров'я наслідків вказаного виду пологів. Така необхідність встала особливо гостро останнім часом у зв'язку з тим, що згідно сталій практиці вагітним жінкам, яких чекають пологи із кесаревим розтином, призначаються профілактичні дози антибіотиків. Як зазначалося вище, у здорової, вагінально народженої, вигодовуваної грудьми дитини бактерії рода Bifidobacteria утворюють основу мікробіоти, що становить 60 - 90% загальної кількості бактерій у кишківнику дитини. Види біфідобактерій, що переважно встановлюють у таких немовлят, відносяться до Bifidobacterium breve, Bifidobacterium infantis і Bifidobacterium 2 UA 97662 C2 5 10 15 20 25 30 35 40 45 50 55 60 longum. Автори даного винаходу із подивом встановили, що спільне введення особливих підвидів молочнокислих бактерій, а саме, пробіотичного штама Lactobacillus rhamnosus і суміші олігосахаридів, що містить 5-70 мас.% принаймні одного N-ацетильованого олігосахарида, обраного з групи, що містить GalNAcα1,3GaIβ1,4GIc і GaIβ1,6GalNAcα1,3GaIβ1,4GIc, 20 - 90 мас.% принаймні одного нейтрального олігосахарида, обраного з групи, що містить GaIβ1,6GaI, GaIβ1,6GaIβ1,4GIc Galβ1,6Galβ1,6Glc, GaIβ1,3GaIβ1,3GIc, GaIβ1,3GaIβ1,4GIc, GaIβ1,6GaIβ1,6GaIβ1,4GIc, GaIβ1,6GaIβ1,3GaIβ1,4GIc GaIβ1,3GaIβ1,6GaIβ1,4GIc и Galβ1,3Galβ1,3GaIβ1,4GIc, і 5 - 50 мас.% принаймні одного сіалійованого олігосахарида, обраного з групи, що включає NeuAcα2,3GaIβ1,4GIc і NeuAcα2,6GaIβ1,4GIc, синергічно стимулює розвиток ранньої біфідогенної кишкової мікробіоти у немовлят, народжених шляхом кесарева розтину. Відповідно, даний винахід забезпечує застосування пробіотичного штама Lactobacillus rhamnosus і суміші олігосахаридів, яка містить 5-70 мас.% принаймні одного N-ацетильованого олігосахариду, обраного з групи, що включає GalNAcα1,3Galβ1,4GIc і GaIβ1,6GalNAcα1,3GaIβ1,4GIc, 20 - 90 мас.% принаймні одного нейтрального олігосахариду, обраного з групи, що включає GaIβ1,6GaI, GaIβ1,6GaIβ1,4GIc GaIβ1,6GaIβ1,6GIc, GaIβ1,3GaIβ1,3GIc, GaIβ1,3GaIβ1,4GIc, GaIβ1,6GaIβ1,6GaIβ1,4GIc, GaIβ1,6GaIβ1,3GaIβ1,4GIc Galβ1,3GaIβ1,6GaIβ1,4GIc і GaIβ1,3GaIβ1,3GaIβ1,4GIc, і 5 - 50 мас.% принаймні одного сіалійованого олігосахариду, обраного з групи, що включає NeuAcα2,3GaIβ1,4GIc і NeuAcα2,6Galβ1,4GIc, у виробництві лікарського засобу або лікувальної харчової композиції, призначених для стимулювання розвитку ранньої біфідогенної кишкової мікробіоти у немовлят, народжених за допомогою кесарева розтину. Винахід, крім цього, забезпечує застосування пробіотичного штама Lactobacillus rhamnosus і суміші олігосахаридів, яка містить 5-70 мас.% принаймні одного N-ацетильованого олігосахариду, обраного з групи, що включає GalNAcα1,3GaIβ1,4GIc і GaIβ1,6GalNAcα1,3GaIβ1,4GIc, 20-90 мас.% принаймні одного нейтрального олігосахариду, обраного з групи, що включає GaIβ1,6GaI, GaIβ1,6GaIβ1,4GIc GaIβ1,6GaIβ1,6GIc, GaIβ1,3GaIβ1,3GIc, GaIβ1,3GaIβ1,4GIc, GaIβ1,6GaIβ1,6GaIβ1,4GIc, GaIβ1,6GaIβ1,3GaIβ1,4GIc Galβ1,3Galβ1,6GaIβ1,4GIc і Galβ1,3Galβ1,3GaIβ1,4GIc, і 5 - 50 мас.% принаймні одного сіалійованого олігосахариду, обраного з групи, що включає NeuAcα2,3Galβ1,4GIc і NeuAcα2,6Galβ1,4GIc, у виробництві лікарського засобу або лікувальної харчової композиції, призначених для зниження ризику наступного розвитку алергії у немовлят, народжених шляхом кесарева розтину. В наступному об'єкті винаходу винахід забезпечує застосування пробіотичного штама Lactobacillus rhamnosus і суміші олігосахаридів, яка містить 5 - 70 мас.% принаймні одного Nацетильованого олігосахариду, обраного з групи, що включає GalNAcα1,3GaIβ1,4GIc і GaIβ1,6GalNAca1,3GaIβ1,4GIc, 20 - 90 мас.% принаймні одного нейтрального олігосахариду, обраного з групи, що включає GaIβ1,6GaI, GaIβ1,6GaIβ1,4GIc Galβ1,6GaIβ1,6GIc, GaIβ1,3GaIβ1,3GIc, GaIβ1,3GaIβ1,4GIc, GaIβ1,6GaIβ1,6GaIβ1,4GIc, GaIβ1,6GaIβ1,3Galβ1,4GIc GaIβ1,3Galβ1,6Galβ1,4GIc і GaIβ1,3GaIβ1,3GaIβ1,4GIc, і 5 - 50 мас.% принаймні одного сіалійованого олігосахариду, обраного з групи, що включає NeuAcα2,3GaIβ1,4GIc і NeuAcα2,6GaIβ1,4GIc, у виробництві лікарського засобу або лікувальної харчової композиції, призначених для профілактики або терапії діареї у немовлят, народжених шляхом кесарева розтину. Винахід поширюється на спосіб стимулювання розвитку ранньої біфідогенної кишкової мікробіоти у немовлят, народжених шляхом кесарева розтину, який передбачає введення терапевтичної кількості пробіотичного штама Lactobacillus rhamnosus і суміші олігосахаридів, яка містить 5 - 70 мас.% принаймні одного N-ацетильованого олігосахариду, обраного з групи, що включає GalNAcα1,3GaIβ1,4GIc і GaIβ1,6GalNAcα1,3GaIβ1,4GIc, 20 - 90 мас.% принаймні одного нейтрального олігосахариду, обраного з групи, що включає GaIβ1,6GaI, GaIβ1,6GaIβ1,4GIc GaIβ1,6GaIβ1,6GIc, GaIβ1,3GaIβ1,3GIc, GaIβ1,3GaIβ1,4GIc, GaIβ1,6Galβ1,6GaIβ1,4GIc, GaIβ1,6GaIβ1,3GaIβ1,4GIc Galβ1,3GaIβ1,6GaIβ1,4GIc і GaIβ1,3GaIβ1,3GaIβ1,4GIc, і 5 - 50 мас.% принаймні одного сіалійованого олігосахариду, обраного з групи, що включає NeuAcα2,3GaIβ1,4GIc і NeuAcα2,6Galβ1,4GIc, немовляті, народженому шляхом кесарева розтину, що потребує вищенаведеного. Винахід, крім того, поширюється на спосіб зниження ризику того, що у немовляти, народженого шляхом кесарева розтину, згодом розвиватиметься алергія, який передбачає введення терапевтичної кількості пробіотичного штама Lactobacillus rhamnosus і суміші олігосахаридів, яка містить 5-70 мас.% принаймні одного N-ацетильованого олігосахариду, обраного з групи, що включає GalNAcα1,3Galβ1,4GIc і GaIβ1,6GalNAcα1,3GaIβ1,4GIc, 20 - 90 3 UA 97662 C2 5 10 15 20 25 30 35 40 45 50 55 60 мас.% принаймні одного нейтрального олігосахариду, обраного з групи, що включає GaIβ1,6GaI, GaIβ1,6GaIβ1,4GIc GaIβ1,6Galβ1,6Glc, GaIβ1,3GaIβ1,3GIc, GaIβ1,3GaIβ1,4GIc, GaIβ1,6GaIβ1,6GaIβ1,4GIc, GaIβ1,6GaIβ1,3GaIβ1,4GIc GaIβ1,3GaIβ1,6GaIβ1,4GIc и GaIβ1,3GaIβ1,3GaIβ1,4GIc, і 5 - 50 мас.% принаймні одного сіалійованого олігосахариду, обраного з групи, що включає NeuAcα2,3GaIβ1,4GIc і NeuAcα2,6Galβ1,4GIc, немовляті, народженому шляхом кесарева розтину, що потребує вищенаведеного. Винахід, крім того, поширюється на спосіб профілактики або терапії діареї у немовляти, народженого шляхом кесарева розтину, який передбачає введення терапевтичної кількості пробіотичного штама Lactobacillus rhamnosus і суміші олігосахаридів, яка містить 5-70 мас.% принаймні одного N-ацетильованого олігосахариду, обраного з групи, що включає GalNAcα1,3GaIβ1,4GIc і GaIβ1,6GalNAcα1,3GaIβ1,4GIc, 20 - 90 мас.% принаймні одного нейтрального олігосахариду, обраного з групи, що включає GaIβ1,6GaI, GaIβ1,6GaIβ1,4GIc GaIβ1,6Galβ1,6Glc, GaIβ1,3Galβ1,3Glc, GaIβ1,3GaIβ1,4GIc, GaIβ1,6GaIβ1,6GaIβ1,4GIc, GaIβ1,6GaIβ1,3GaIβ1,4GIc GaIβ1,3GaIβ1,6GaIβ1,4GIc и GaIβ1,3GaIβ1,3GaIβ1,4GIc, і 5 - 50 мас.% принаймні одного сіалійованого олігосахариду, обраного з групи, що включає NeuAcα2,3GaIβ1,4GIc і NeuAcα2,6GaIβ1,4GIc, немовляті, народженому шляхом кесарева розтину, що потребує вищенаведеного. Не обмежуючись теорією, автори даного винаходу вважають, що введення пробіотичного штама Lactobacillus rhamnosus і суміші олігосахаридів, яка містить 5 - 70 мас.% принаймні одного N-ацетильованого олігосахариду, обраного з групи, що включає GalNAcα1,3GaIβ1,4GIc і GaIβ1,6GalNAcα1,3GaIβ1,4GIc, 20 - 90 мас.% принаймні одного нейтрального олігосахариду, обраного з групи, що включає GaIβ1,6GaI, GaIβ1,6GaIβ1,4GIc GaIβ1,6GaIβ1,6GIc, GaIβ1,3GaIβ1,3GIc, GaIβ1,3GaIβ1,4GIc, GaIβ1,6GaIβ1,6GaIβ1,4GIc, GaIβ1,6GaIβ1,3GaIβ1,4GIc GaIβ1,3GaIβ1,6GaIβ1,4GIc и GaIβ1,3GaIβ1,3GaIβ1,4GIc, і 5 - 50 мас.% принаймні одного сіалійованого олігосахариду, обраного з групи, що включає NeuAcα2,3GaIβ1,4GIc і NeuAcα2,6GaIβ1,4GIc, немовляті, народженому шляхом кесарева розтину, певним, ще не зовсім зрозумілим чином, готує шлунково-кишковий тракт немовляти для сприяння подальшій колонізації тими видами біфідобактерій, які звичайно встановлюються у тракті здорових немовлят, народжених вагінально. Вважається, що ця сприятлива колонізація знижує ризик епізодів діареї, яка, як було показано, охоплює немовлят, народжених шляхом кесарева розтину. Крім того, передбачається, що сприятлива колонизація знижує ризик наступного розвитку алергії, що виявляється, наприклад, в диханні зі свистом і/або в збільшенні чутливості до алергенів їжі. Слід відзначити, що ані метою, ані очікуваним ефектом такої терапії не є стимулювання колонізації самим пробіотиком Lactobacillus rhamnosus, а насправді вони полягають у стимулюванні колонізації іншими видами так, щоб забезпечити ранню біфідогенну кишкову мікробіоту, яку можливо спів ставити із наявною у здорових, вигодовуваних грудьми, народжених вагінально немовлят. Фігура 1 показує вміст через 14 днів Staphylococcus aureus і Clostridium perfringens у зразках фекалій гнотобіологічних мишей з введенною через зонд мікробіотою дитини людини; і Фігура 2 показує вміст через 14 днів Bifidobacterium breve и Bifidobacterium longum в зразках фекалій гнотобіологічних мишей з введенною через зонд мікробіотою дитини людини;. У даному описі нижченаведені терміни мають наступні значення: "початкова біфідогенна кишкова мікробіота" означає кишкову мікробіоту немовляти у віці до 12 місяців, в якій домінують біфідобактерії, такі як Bifidobacterium breve, Bifidobacterium infantis и Bifidobacterium longum, за винятком популяцій таких видів, як клостридії і стрептококи, і яка в більшості випадків порівнянна з кишковою мікробіотою вагинально-народженої, вигодовуваної грудьми дитини такого ж віку; "немовля" відноситься до дитини у віці до 12 місяців; "пребіотик" означає неперетравлюваний харчовий інгредієнт, який позитивно впливає на особу, вибірково стимулюючи зростання і/або активність одного або певної кількості видів бактерій в товстій кишці і покращуючи, тим самим, здоров'я особи (Gibson and Roberfroid "Dietary Modulation of the Human Colonic Microbiota: Introducing the Concept of Prebiotics", J. Nutr. 125:1401-1412); "пробіотик" означає препарати мікробних клітин або компоненти мікробних клітин, що мають сприятливий ефект для здоров'я або самопочуття особи (Salminen S., Ouwehand A., Benno Y. et al. "Probiotics: how should they be defined", Trends Food Sci. Technol. 1999,10:107-110). Всі посилання на величину процентів означають зміст в мас. %, якщо не зазначено інше. Прийнятні пробіотичні молочнокислі бактерії включають штам Lactobacillus rhamnosus ATCC 53103, що реалізується на ринку, зокрема, фірмою Valio Oy (Фінляндія) під торговою маркою 4 UA 97662 C2 5 10 15 20 25 30 35 40 45 50 55 60 LGG; штами Lactobacillus rhamnosus CGMCC 1.3724. Прийнятна добова доза пробіотичних 5 11 7 бактерій складає від 10 до 10 утворюючих колонії одиниць (КУО), переважніше - від 10 до 10 10 КУО. Переважно пробіотичні бактерії вводять разом із сумішшю олігосахаридів, яка містить від 5% до 70 мас.% принаймні одного N-ацетильованого олігосахариду, обраного з групи, що включає GalNAcα1,3GaIβ1,4GIc і GaIβ1,6GalNAcα1,3GaIβ1,4GIc; від 20% до 90 мас.% принаймні одного нейтрального олігосахариду, обраного з групи, що включає GaIβI,6GaI, GaIβ1,6GaIβ1,4GIc GaIβ1,6GaIβ1,6GIc, GaIβ1,3GaIβ1,3GIc, GaIβ1,3GaIβ1,4GIc, GaIβ1,6GaIβ1,6GaIβ1,4GIc, GaIβ1,6GaIβ1,3GaIβ1,4GIc GaIβ1,3GaIβ1,6GaIβ1,4GIc і GaIβ1,3GaIβ1,3GaIβ1,4GIc, і від 5% до 50 мас.% принаймні одного сіалійованого олігосахариду, обраного з групи, що включає NeuAcα2,3GaIβ1,4GIc і NeuAcα2,6GaIβ1,4GIc Така суміш олігосахаридів детальніше описана в WO 2007/090894, посилання на яку наведено для інформації, далі по тексту ця суміш олігосахаридів зветься "вищеописаною сумішшю олігосахаридів". Термін «спільне введення» означає як одночасне введення пробіотика Lactobacillus rhamnosus і суміші олігосахаридів, так і послідовне введення пробіотика і суміші олігосахаридів. Переважно вищеописана суміш олігосахаридів містить від 10% до 70 мас.% вищезгаданого N-ацетильованого олігосахариду(дів), від 20% до 80 мас.% вищезгаданого нейтрального олігосахариду(дів) і від 10% до 50 мас.% вищезгаданого сіалійованого олігосахариду(дів). Переважніше, суміш містить від 15% до 40 мас.% N-ацетильованого олігосахариду(дів), від 40% до 60 мас.% іншого нейтрального олігосахариду(дів) і від 15% до 30 мас.% сіалійованого олігосахариду(дів). Особливо переважною сумішшю є суміш з 30 мас.% N-ацетильованого олігосахариду(дів), 50 мас.% нейтрального олігосахариду(дів) і 20 мас.% сіалійованого олігосахариду(дів). Альтернативно, вищеописана суміш олігосахаридів може відповідно містити від 5% до 20 мас.% вищезгаданого N-ацетильованого олігосахариду(дів), від 60% до 90 мас.% вищезгаданого нейтрального олігосахариду(дів) і від 5% до 30 мас.% вищезгаданого сіалійованого олігосахариду(дів). Вищеописана суміш олігосахаридів може бути приготована з молока одного або декількох видів тварин. Молоко може бути отримане від будь-якого ссавця, зокрема, від корів, кіз, буйволів, коней, слонів, верблюдів або овець. Альтернативно вищеописана суміш олігосахаридів може бути приготована змішуванням окремих придбаних в торговій мережі компонентів. Наприклад, синтезовані галактоолігосахариди, такі як Galβ1,6Galβ1,4GIc Galβ1,6Galβ1,6GIc, Galβ1,3Galβ1,4Glc, Galβ1,6Galβ1,6Galβ1,4GIc, Galβ1,6Galβ1,3Galβ1,4Glc і Galβ1,3Galβ1,6Galβ1,4GIc, та їх суміші реалізуються на ринку під товарними знаками Vivinal® і ЕІіх'оr®. Іншими постачальниками олігосахаридів є Dextra Laboratories, Sigma-Aldrich Chemie GMBH і Kyowa Hakko Kogyo Co., Ltd. Альтернативно для отримання нейтральних олігосахаридів можуть використовуватися специфічні глікозилтрансферази, такі як галактозилтрансферази. N-ацетильовані олігосахариди можуть бути отримані в процесі дії глюкозамінідази і/або галактозамінідази на N-ацетил-глюкозу і/або N-ацетил-галактозу. Аналогічним чином для цієї мети можуть використовуватися N-ацетил-галактозилтрансферази і/або N-ацетилглікозилтрансферази. N-ацетильовані олігосахариди можуть бути отримані також за технологією ферментації із застосуванням відповідних ферментів (рекомбінантних або природних) і/або мікробної ферментації. У останньому випадку мікроорганізми можуть виділяти свої природні ферменти і субстрати, або можуть рекомбінуватися з метою подальшого отримання відповідних субстратів і ферментів. Можуть використовуватися культури одного виду мікроорганізмів або змішані культури. Утворення N-ацетильованого олігосахариду може ініціюватися акцепторними субстратами, починаючи з будь-якого ступеня полімеризації (DP) від DP=1 і вище. Іншим методом є хімічна конверсія кетогексоз (наприклад, фруктози), як вільних, так і пов'язаних з олігосахаридом (наприклад, з лактулозою), в N-ацетилгексозамін або в N-ацетилгексозамін, що містить олігосахарид, як описано в Wrodnigg, Т.M.; Stutz, А.Е. (1999) Angew. Chem. Int. Ed. 38: 827-828. Сіалійовані олігосахариди - 3'-сіалил-лактоза і 6'-сіалил-лактоза - можуть бути виділені технікою хроматографії або фільтрації з природного джерела, такого як молоко тварин. Альтернативно, вони можуть бути також отримані за допомогою біотехнологій, в яких застосовуються специфічні сіалилтрансферази або за допомогою технології ферментації (ферменти можуть бута рекомбінантними або природними), або за допомогою технології мікробної ферментації. У останньому випадку мікроорганізми-можуть виділяти свої природні ферменти і субстрати або можуть рекомбінуватися з метою подальшого продукування ними 5 UA 97662 C2 5 10 15 20 25 30 35 40 45 50 55 60 відповідних субстратів і ферментів. Можуть використовуватися культури одного виду мікроорганізмів або змішані культури. Утворення сіалійованого олігосахариду може ініціюватися акцепторними субстратами, починаючи з будь-якого ступеня полімеризації (DP) - від DP=1 і вище. Інші пробіотичні бактерії можуть вводитися з пробіотиком Lactobacillus rhamnosus. Можуть застосовуватись будь-які молочнокислі бактерії або біфідобактерії із визначеними пробіотичними властивостями. Прийнятні пробіотичні молочнокислі бактерії включають Lactobacillus reuteri ATCC 55730, що пропонуються компанією Biogaia, або Lactobacillus paracasei CNCM I-2116. Прийнятні пробіотичні штами біфідобактерій включають Bifidobacterium lactis CNCM І-3446, які, inter alia (серед іншого) пропонуються до продажу датською компаниєю Christian Hansen під торговою маркою Вb12, Bifidobacterium longum ATCC ВАА-999, які реалізуються Morinaga Milk Industry Co. Ltd. (Япония) під торговою маркою ВВ536, штам Bifidobacterium breve, що пропонується Danisco під торговою маркою Вb-03, штам Bifidobacterium breve, що пропонується Morinaga торговою маркою M-16V, і штам Bifidobacterium breve, що пропонується lnstitut Rosell (Lallemand) торговою маркою R0070. Може використовуватись суміш молочнокислих бактерій і біфідобактерій. Пробіотик Lactobacillus rhamnosus і суміш олігосахаридів переважно вводяться дитині відразу після пологів і протягом принаймні перших двох місяців життя дитини. Переважніше, введення пробіотичних бактерій триває до досягнення дитиною 6-місячного віку. Пробіотик Lactobacillus rhamnosus і суміш олігосахаридів легко вводяться у дитяче харчування. Суміш для дитячого харчування в рамках застосування згідно даного винаходу може містити джерело білка в кількості не більше 2,0 г/100 ккал, переважно - від 1,8 до 2,0 г/100 ккал. Вид білка не є критичним в даному винаході за умови, що він відповідає мінімальним вимогам до вмісту основних амінокислот і забезпечує задовільне зростання, хоча краще, щоб понад 50 мас.% джерела білка складала молочна сироватка. Так, можуть застосовуватися джерела білка на основі сироватки, казеїну і їх сумішей, а також джерела білка на основі сої. Що стосується сироваткових білків, то джерело білка може бути на основі кислої сироватки або солодкої сироватки, або їх сумішей, і може включати альфа-лактальбумин і бета-лактоглобулін в будьяких необхідних співвідношеннях. Білки можуть бути інтактними або гідролізованими або сумішшю інтактних і гідролізованих білків. Бажаним є використання частково гідролізованих білків (ступінь гідролізу між 2% і 20%), наприклад, для грудних дітей з передбачуваним ризиком розвитку алергії на коров'яче молоко. Якщо потрібні гідролізовані білки, то процес гідролізу може здійснюватися будь-яким прийнятним методом, відомим з рівня техніки. Наприклад, сироватково-білковий гідролізат може бути отриманий ферментативним гідролізом сироваткової фракції, із однією або декількома стадіями. Встановлено, що, якщо як початковий матеріал використовується сироваткова фракція, що практично не містить лактози, то білок в процесі гідролізу набагато менше зазнає лізинової блокади. Це дозволяє понизити ступінь лізинової блокади приблизно з 15 мас.% загального лізину до менше 10 мас.% лізину, наприклад, приблизно до 7 мас.% лізину, що значно покращує поживні властивості джерела білка. Суміш для дитячого харчування може містити джерело вуглеводів. Може використовуватися будь-яке джерело вуглеводів, що традиційно вживається в сумішах для дитячого харчування, наприклад, лактоза, сахароза, мальтодекстрин, крохмаль і їх суміші, хоча переважним джерелом вуглеводів є лактоза. Переважно джерела вуглеводів забезпечують від 35% до 65% загальної енергії суміші. Суміш для дитячого харчування може містити джерело ліпідів. Джерело ліпідів може бути будь-яким ліпідом або жиром, які підходять для використання в сумішах для дитячого харчування. До кращих джерел жиру відносяться пальмовий олеїн, високоолеїнова соняшникова олія і високоолеїнова сафлорова олія. Можуть додаватися також основні жирні кислоти - лінолієва і а-ліноленова, так само як і невеликі кількості олій з високим вмістом заздалегідь сформованих арахидонової і докозагексаєнової кислот, таких як риб'ячий жир або мікробні олії. В цілому вміст жиру переважно повинен бути таким, щоб за рахунок його забезпечувалося від 30% до 55% загальної енергії суміші. Джерело жиру переважно має співвідношення n-6 жирних кислот до n-3 жирних кислот, приблизно від5:1 до 15:1, наприклад, приблизно від 8:1 до 10:1. Суміш для дитячого харчування може також містити всі вітаміни і мінерали, які вважаються незамінними в щоденному раціоні, в значащих на харчові потреби кількостях. Існують мінімальні потреби в деяких вітамінах і мінералах. Приклади мінералів, вітамінів і інших нутрієнтів, необов'язково присутніх в суміші для дитячого харчування, включають вітамін А, 6 UA 97662 C2 5 10 15 20 25 30 35 40 45 вітамін В1, вітамін В2, вітамін В6, вітамін В12, вітамін Е, вітамін K1 вітамін С, вітамін D, фолієву кислоту, інозит, ніацин, біотин, пантотенову кислоту, холін, кальцій, фосфор, йод, залізо, магній, мідь, цинк, марганець, хлорид, калій, натрій, селен, хром, молібден, таурин і L-карнітин. Мінерали зазвичай додаються у формі солей. Присутність і кількість специфічних мінералів і інших вітамінів вар'юватимуться залежно від грудних дітей, для якої вони призначені. При необхідності, суміш для дитячого харчування може містити емульгатори і стабілізатори, такі як соєвий лецитин, лимоннокислі ефіри моно- і дігліцеридів тощо. Переважно суміш для дитячого харчування міститиме вищеописану суміш олігосахаридів в кількості від 0,2 до 5 г/л відновленої суміші, переважніше - від 1 до 2 г/л. Суміш для дитячого харчування може необов'язково містити і інші речовини, здатні мати корисний ефект, такі як лактоферрин, нуклеотиди, нуклеозиди тощо. Як суміш для дитячого харчування, так і харчова композиція, описана вище, можуть готуватися будь-яким відповідним способом. Наприклад, вони можуть готуватися змішуванням білка, джерела вуглеводів і джерела жиру у відповідних пропорціях. На цій же стадії можуть вводитися емульгатори, якщо такі використовуються. Вітаміни і мінерали також можуть додаватися на цій стадії, але зазвичай вони додаються пізніше, щоб уникнути їх розпаду при нагріві. Будь-які ліпофильні вітаміни, емульгатори тощо можливо заздалегідь розчиняти в джерелі жиру перед змішуванням. Потім можливо додавати воду, переважно, воду, оброблену зворотним осмосом, для отримання рідкої суміші. Зручна температура води для полегшення диспергування інгредієнтів складає приблизно від 50C до 80°С. Для отримання рідкої суміші можуть використовуватися наявні на ринку розріджувачі. Потім рідка суміш гомогенізується, наприклад, в дві стадії. Далі рідка суміш з метою зниження її бактерійного навантаження може піддаватися тепловій обробці шляхом швидкого нагріву рідкої суміші, наприклад, до температури приблизно від 80C до 150C протягом приблизно від 5 секунд до 5 хвилин. Це можна здійснювати за допомогою інжекції пари, в автоклаві або теплообміннику, наприклад, в пластинчастому теплообміннику. Після цього рідка суміш може охолоджуватися до температури приблизно від 60C до 85°С, наприклад, шляхом миттєвого охолоджування. Потім рідка суміш може повторно гомогенізуватися, наприклад, в дві стадії, під тиским приблизно від 10 Мпа до 30 Мпа на першій стадії і приблизно від 2 Мпа до 10 Мпа на другій стадії. Суміш, що гомогенізується, може далі охолоджуватися до температури додавання чутливих до нагріву компонентів, таких як вітаміни і мінерали. На цій стадії зручно регулювати величину рН і вміст сухих речовин в суміші, що гомогенізується. Суміш, що гомогенізується, переносять у відповідний сушильний апарат, наприклад, в сушарку-розпилювач або сушарку із сублімацією, і перетворюється на порошок. Вміст вологи в порошку повинен бути до приблизно 5 мас.%. Пробіотик Lactobacillus rhamnosus може культивуватися будь-яким відповідним методом і піддаватися обробці перед додаванням в харчову композицію або в суміш для дитячого харчування, наприклад, в сушарці-розпилювачі або сушарці із сублімацією. Альтернативно можна придбати бактерійні препарати у постачальників, що спеціалізуються на їх виробництві, таких як Christian Hansen і Valio, вже у готовому вигляді, придатному для додавання в харчові продукти, такі як харчова композиція і суміші для дитячого харчування. Пробіотичні бактерії 3 12 7 можуть додаватися в суміш в кількості від 10 до 10 КУО/г порошку, переважніше - від 10 до 12 10 КУО/г порошку. Винахід надалі ілюструють наступним прикладами. Приклад 1 Приклад складу суміші для дитячого харчування, придатної для застосування згідно даного винаходу, наводиться нижче. 7 UA 97662 C2 Нутрієнт Енергія (ккал) Білок (г) Жир (г) Лінолієва кислота (г) α-ліноленова кислота (мг) Лактоза (г) Мінерали (г) Na (мг) К(мг) Cl (мг) Ca (мг) Р(мг) Mg (мг) Mn (мкг) Se (мкг) Вітамін А (мкг RE (ретинолу)) Вітамін D (мкг) Вітамін E (міліграм ТЕ (токоферола)) Вітамін К1 (мкг) Вітамін C (міліграм) Вітамін В1 (міліграм) Вітамін В2 (міліграм) Ніацин (міліграм) Вітамін В6 (міліграм) Фолієва кислота (мкг) Пантотенова кислота (мг) Вітамін В12 (мкг) Біотин (мкг) Холін (міліграм) Fe (мг) І (мкг) Cu (мг) Zn (мг) L rhamnosus ATCC 53103 5 10 15 20 На 100 ккал На літр 100 670 1,83 12,3 5,3 35,7 0,79 5,3 101 675 11,2 74,7 0,37 2,5 23 150 89 590 64 430 62 410 31 210 7 50 8 50 2 13 105 700 1,5 10 0,8 5,4 8 54 10 67 0,07 0,47 0,15 1 1 6,7 0,075 0,5 9 60 0,45 3 0,3 2 2,2 15 10 67 1,2 8 15 100 0,06 0,4 0,75 5 7 2x10 КУЕ/г порошку, живі бактерії Приклад 2 В цьому прикладі порівнюється дія Lactobacillus rhamnosus CGMCC 1.3724 спільно із олігосахаридним інгредієнтом, що включає N-ацетильовані олігосахариди, нейтральні олігосахариди і сіалійовані олігосахариди (що надалі звуться CMOS-GOS), на процес встановлення ранньої біфідогенної кишкової мікробіоти в гнотобіологічній моделі з народженими в результаті кесарева розтину мишами, з дією окремо взятих пробіотика і суміші олігосахаридів, а також з контролем. Ця модель є прийнятною експериментальною моделлю на тварині для немовлят, народжених шляхом кесарева розтину і таких, що мають недостатню кишкову мікробіоту по відношенню до популяції біфідобактерій. В доповнення до спостереженням за розміром популяції біфідобактерій ця модель є також прийнятною для відстежування сприятливої дії біфідобактерій в якості бар'єра по відношенню до потенційно патогенних бактерій, таких як Clostridium perfringens. Методи і матеріали Стерильні самки і самці мишей лінії С3Н були закуплені в Charles River Laboratories (Франція) и доставлені до Дослідницького центру Nestle в транспортних ізоляторах. Після перевірки їх стерильного статуса тварини були перенесені в ізолятори для розведення. В даному дослідженні використовувалась жіноча частина потомства цієї популяції розведення. Тварини потім були випадковим чином розподілені по чотирьох групах спостереження: А контрольна дієта і контрольне пиття; В - контрольна дієта із 3% суміші олігосахаридів і контрольне пиття; C - контрольна дієта і пробіотик L rhamnosus CGMCC 1.3724 в питті; D контрольна дієта з 3% суміші олігосахаридів і пробіотик L rhamnosus CGMCC 1.3724 в питті. 8 UA 97662 C2 5 10 15 20 25 30 35 40 45 50 55 Тварини містилися у двох різних ізоляторах в клітках по 5 тварин в кожній. Групи А і В утримувалися в одному ізоляторі, а групи C і D утримувалися в іншому ізоляторі для уникнення перехресного забруднення L rhamnosus в кінці дослідження. Стерильний статус відстежувався щотижнево по свіжодібраних фекаліях, взятих від однієї тварини з кожної клітки. Протягом цього періода тварини отримували дієту AIN-93, що не містить досліджуваних композицій. У віці 7 - 8 тижнів по дві тварини з кожної клітки повторно перевірялись на стерильний статус, і кожна тварина після цього отримувала через шлунковий зонд одноразову дозу в 200 мкл, що містить суміш мікробіоти дитини людини (HBF), як представлено в Таблиці 1. В той же день дієта замінювалася на суміш AIN (для груп А і C) або AIN-CMOS-GOS (для груп В і D), а питна вода замінялася на мінералізовану питну воду, що містить 0,5% (по oб’ємy) MRS (для груп А і В) або на мінералізовану питну воду, що містить 0,5% (по об'єму) MRS і кінцеву концентрацію L. 7 rhamnosus 2х10 КУО/мл. Цей день розглядався як день «-1». На наступний день (що розглядається як день 0) у кожної тварини відбиралися свіжі фекалії і негайно після цього здійснювався аналіз на мікробіоту шляхом чашкового підрахунку. Зразок збагаченого олігосахаридом коров'ячого молока (CMOS) готувався, виходячи з промислового депротеїнізованого і демінералізованого сироваткового пермеату (Lactoserum France, Франція). Коротко, підданий ультрафільтрації сироватковий пермеат коров'ячого молока був демінералізований на промисловій ліній для демінералізації, обладнаній модулями електродіалізу і аніонними і катіонними іонообмінювачами (Lactoserum France). Демінералізований сироватковий пермеат був потім підданий двом послідовним промисловим циклам кристалізації лактози, а потім висушений розпиленням (Lactoserum France). Отриманий порошок модифікованого маткового розчину розчинявся у воді в концентрації 30% (співвідношення маси до об'єму) і освітлювався пропусканням через фільтр-поглинач із активованого вугілля, супроводжуваним фільтрацією на 0,22 мкм фильтрі (МіІІіроге). Кінцевий фільтрат завантажувався в препаративну колонку (50х850 мм) з біогелем Р2 (BioRad), через яку пропускався 20 ммоль розчин бікарбоната аммонія (NH4HC03) при швидкості потока 2 мл/хв. Фракції, що містять олігосахариди, і елюйовані до лактози фракції відбиралися, об'єдувалися і піддавалися ліофілізації. Ліофілізовані олігосахариди змішувалися із промислово виробленими галактозилолігосахаридами (Vivinal GOS, DOMO Friesland Foods) для отримання кінцевої суміші, яка містить біля 9 мас.% N-ацетильованих олігосахаридів, близько 85 мас.% нейтральних олігосахаридів і близько 6 мас.% сіалійованих олігосахаридів. Цей CMOS-GOS інгредієнт був включений в напівсинтетичну дієту для гризунів AIN-93 з отриманням кінцевого вмісту олігосахариду в 3 мас.%. Контрольна дієта AIN-93 була доповнена глюкозою і лактозою для регулювання вмісту глюкози і лактози, що вносяться в дієту CMOS-GOS із застосуваними вихідними матеріалами. L. rhamnosus готувалися із використанням Колекцій культур компанії Nestle. Коротко, була виконана реактивація NCC4007 і вирощування культури на поживному середовищі MRS (Man, 8 Rogosa, Sharpe) до отримання близько 4-5x10 КУО/мл. Після цього L. rhamnosus концентрувалися центрифугуванням із використовуваного поживного середовища MRS і 9 розводилися до 4 х 10 КУО/мл свіжого поживного середовища MRS. Після цього L. rhamnosus були розподілені на аліквоти по 1 мл, які заморожувалися при -80C до моменту застосування. Кожен день в ізолятори вносилася одна свіжорозморожена 1 мл аліквота L rhamnosus в MRS (або 1 мл MRS для груп без L. rhamnosus), розчинялася в 200 мл фізіологічного розчину і рівномірно розподілялася по чотирьох пляшечках для пиття. При середньому споживанні 8 однією мишою 5 мл/день кожна тварина в групах з пробіотиком отримувала близько 10 КУО L. rhamnosus на добу. На 14 день відбиралися зразки фекалій і аналізувалися чашечним підрахунком. Коротко, по одній фекальній грудочці від кожної миші гомогенізувалося в 0,5 мл розчину Рінгера (Oxoid, Великобританія), доповненому 0,05% (співвідношення маси до об'єму) L-цистеїну (HCI), і різноманітні розведення бактеріального розчину висівалися на селективне і напівселективне середовище для виконання підрахунку конкретних видів мікроорганізмів: біфідобактерії на томатне поживне середовище Eugom, молочнокислі бактерії на поживне середовище MRS з додаванням антибіотиків (фосфоміцин, сульфаметоксазол і триметоприм), С. perfringens на середовище з NN-агара, Enterobacteriaceae на поживне середовище Drigalski і Bacteroides на поживне середовище Shaedler Нео Vanco. Чашки інкубувалися при 37C протягом 24 годин в аеробних умовах для підрахунку Enterobacteriaceae і протягом 48 годин в анаеробних умовах у випадку біфідобактерій, молочнокислих бактерій, Bacteroides і C. perfringens. 9 UA 97662 C2 Таблиця 1 Композиція мікробіоти Фенотип колонії на чашці Штам біла, крупна сіра, невелика біла, велика сіра, невелика Bifidobacterium breve NCC452 (viv4) Bifidobacterium longum NCC572 (viv5) Staphylococcus aureus FSM124 (viv3) Staphylococcus epidermidis FSM115 (viv2) Escherichia coli FSM325 (viv1) Bacteroides distesonis ESM24 (viv20) 5,0 Clostridium perfringens FSMC14 (viv19) 5 10 Концентрація введення Іоg(КОЕ/мл)
ДивитисяДодаткова інформація
Назва патенту англійськоюSynbiotic to improve gut microbiota in infants delivered by caesarean section
Автори англійськоюHuber-Haag, Karl-Josef, Fichot, Marie-Claire, Rochat, Florence, Sprenger, Norbert
Назва патенту російськоюПрименение синбиотика для улучшения кишечной микробиоты у детей, родившихся путем кесаревого сечения
Автори російськоюХубер-Хааг Карл-Йозеф, Фишот Мари-Клер, Рошат Флоренс, Спренгер Норберт
МПК / Мітки
МПК: A61P 1/00, A61P 37/04, A61K 35/74, A61K 31/702, A23L 1/30
Мітки: покращення, синбіотика, дітей, мікробіоти, розтину, шляхом, кесаревого, кишкової, народжених, застосування
Код посилання
<a href="https://ua.patents.su/15-97662-zastosuvannya-sinbiotika-dlya-pokrashhennya-kishkovo-mikrobioti-u-ditejj-narodzhenikh-shlyakhom-kesarevogo-roztinu.html" target="_blank" rel="follow" title="База патентів України">Застосування синбіотика для покращення кишкової мікробіоти у дітей, народжених шляхом кесаревого розтину</a>
Попередній патент: Планування динамічного широкомовного каналу
Наступний патент: Застосування bifidobacterium lactis cncm i-3446 для покращення кишкової мікробіоти у дітей, народжених шляхом кесарева розтину
Випадковий патент: Покрівля з внутрішнім стоком