Похідні бензолу, заміщені гетероциклами, та гербіциди
Номер патенту: 57738
Опубліковано: 15.07.2003
Автори: Кавана Такасі, Когуті Масамі, Такахасі Акіхіро, Міяхара Осаму, Адаті Хіроюкі, Ямагуті Масао, Танака Кацунорі
Формула / Реферат
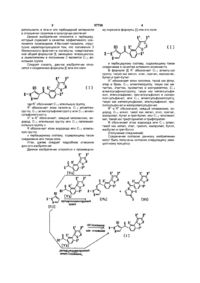
1. Соединение формулы (I):
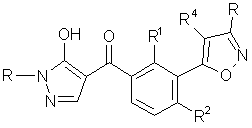 (I)
(I)
или его соль, где R1 обозначает C1-6алкильную группу,
R2 обозначает С1-6алкилсульфонилгруппу,
R3 и R4 обозначают, каждый независимо, водород, C1-6алкильную группу и
R обозначает С1-6алкильную группу.
2. Соединение по п. 1, где R1 и R3 обозначают метил, R2 обозначает метилсульфонил, R4 обозначает водород и R обозначает метил или этил.
3. Гербицидная композиция, отличающаяся тем, что содержит в качестве активного агента одно или несколько соединений формулы (1):
 (I)
(I)
или их соли, где R1, R2, R3, R4 и R определены выше.
Текст
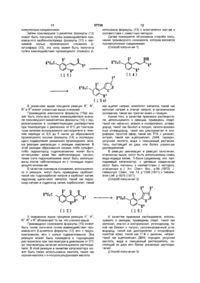
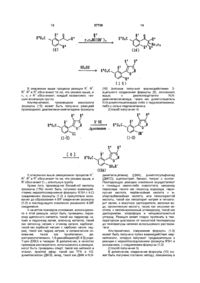
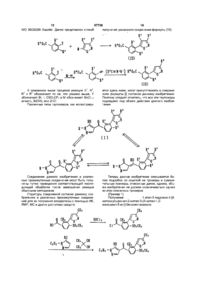
1 Соединение формулы (І) ГЕРБІЦИДИ или его соль, где к обозначает Сі єалкильную группу, R обозначает Сі єалкилсульфонилгруппу, R3 и R4 обозначают, каждый независимо, водород, Сі балкильную группу и R обозначает Сі єалкильную группу 2 Соединение по п 1, где R1 и R3 обозначают метил, R2 обозначает метилсульфонил, R4 обозначает водород и R обозначает метил или этил 3 Гербицидная композиция, отличающаяся тем, что содержит в качестве активного агента одно или несколько соединений формулы (1) R ОН или их соли выше к R определены о 00 го 1 ю Данное изобретение относится к новому производному пиразола, замещенному бензоильной группой в положении 4 кольца пиразола, и гербициду Предпосылки создания изобретения - В WO 93/18031 Gazette соединение формулы [II] CI П описано в качестве активного компонента гербицида, имеющего скелет пиразола, замещенного бензоильной группой в положении 4 кольца пира зола С другой стороны, в WO 96/26206 Gazette описано соединение формулы С ) Ш Цель данного изобретения - создать гербицид, который можно выгодно синтезировать в промышленных масштабах, который является устойчиво эффективным при более низких дозах и высоко безопасным, а также имеет более высокую изби 57738 рательность в плане его гербицидной активности в отношении сорняков и культурных растений Данное изобретение относится к гербициду, который содержит в качестве эффективного компонента производное 4-бензоил-пиразола, структурно характеризующееся тем, что положение 3 бензоильного фрагмента молекулы, представленной общей формулой [I], замещено гетероциклом, и заместителем в положении 2 является Сі є алкильная группа Следует сказать, данное изобретение относится к соединению формулы [I] или его соли СП где R1 обозначает Сі є алкильную группу, R обозначает атом галогена, Сі є алкилтиогруппу, Сі є алкилсульфинилгруппу или Сі є алкилсульфонил группу, R3 и R4 обозначают, каждый независимо, водород, Сі є алкильную группу или Сі є галогеналкильную группу и R обозначает атом водорода или Сі є алкильную группу, и гербицидному составу, содержащему такое соединение или такую соль Итак, далее следует подробное описание данного изобретения Данное изобретение относится к производно му пиразола формулы [I] или его соли СП и гербицидному составу, содержащему такое соединение в качестве активного компонента В формуле [I] R1 обозначает Сі є алкильную группу, такую как метил, этил, пропил, изопропил, бутил и трет-бутил R2 обозначает атом галогена, такой как фтор, хлор и бром, Сі є алкилтиогруппу, такую как метилтио, этилтио, пропилтио и изопропилтио, Сі 6 алкилсульфинилгруппу, такую как метилсульфинил, этилсульфинил, пропилсульфинил и изопропил-сульфинил, или Сі 6 алкилсульфонилгруппу, такую как метилсульфонил, этилсульфонил, пропилсульфонил и изопропилсульфонил R3 и R4 обозначают, каждый независимо, водород, Сі є алкил, такой как метил, этил, пропил, изопропил, бутил и трет-бутил, или Сі б галогеналкил, такой кактрифторметил и трифторэтил R обозначает атом водорода или Сі є алкил, такой как метил, этил, пропил, изопропил, бутил, изобутил и трет-бутил (Получение соединений) Соединения согласно данному изобретению могут быть получены согласно следующему реакционному процессу 57738 где R1, R2, R3, R4 и R определены выше, и Q обозначает атом галогена, алкилкарбонилоксигруппу, алкоксикарбонилокси-группу или бензоилоксигруппу В процессе, проиллюстрированном выше, соединения формулы [IVa] и [IVb] могут быть, соответственно, получены путем взаимодействия соединения формулы [VII] в количестве 1 моль с соединением формулы [Va] в количестве 1 моль, где Q обозначает то же, что указано выше, причем в указанной реакции может быть использовано избыточное количество либо соединения формулы [VII], либо соединения формулы [Va], в присутствии основания в количестве 1 моль или в избыточном количестве В качестве примера основания, которое может быть использовано в реакции, описанной выше, могут быть приведены гидроксид щелочного металла, такой как КОН и NaOH, карбонат щелочного металла, такой как карбонат натрия и карбонат калия, гидроксид щелочноземельного металла, такой как гидроксид кальция и гидроксид магния, карбонат щелочноземельного металла, такой как карбонат кальция, три(Сі є алкил)амин, такой как триэтиламин и диизопропилэтиламин, органическое основание, такое как пиридин, и фосфат натрия и т п Кроме того, в качестве примера растворителя, который может быть использован в реакции, описанной выше, могут быть приведены вода, метиленхлорид, хлороформ, толуол, этилацетат, диметилформамид (ДМФ), тетрагидрофуран ЛТФ), диметоксиэтан (ДМЭ), ацетонитрил и тому подобное Смесь, приготовленную для описанной выше реакции, перемешивают при температуре в диапазоне от 0°С до температуры кипения используемого растворителя в течение всего периода до завершения указанной реакции В дополнение, реакция может быть проведена в двухфазной системе с использованием межфазного катализатора, такого как соль четвертичного аммониевого основания Кроме того, соединения формул [IVa] и [IVb] могут быть также получены путем взаимодействия соединения формулы [VII] и соединения формулы [Vb] в присутствии агента дегидроконденсации, такого как дициклогексилкарбодиимид (ДЦК) Примеры растворителя, который может быть использован в реакции с ДЦК или тому подобным, включают метиленхлорид, хлороформ, толуол, этилацетат, ДМФ, ТГФ, диметоксиэтан, ацетонитрил и трет-амиловый спирт Реакционную смесь перемешивают при температуре в диапазоне от 10°С до температуры кипения используемого растворителя до завершения реакции Реакционная смесь может быть обработана обычным методом Соединения формул [IVa] и [IVb] используют в виде смеси в следующей реакции превращения Реакция превращения может быть проведена в присутствии цианосоединения и мягкого основания Следует сказать, что соединение формулы [I] может быть получено путем взаимодействия смеси соединений формул [IVa] и [IVb] в количестве 1 моль с основанием в количестве от 1 до 4 моль, предпочтительно 1 - 2 моль, и цианосоединением в количестве от 0,01 до 1,0 моль, предпочтительно 0,05 - 0,2 моль В качестве основания, которое может быть использовано здесь, может быть использовано любое из указанных выше оснований Кроме того, в качестве примеров цианосоединения приведены цианид калия, цианид натрия, циангидрин ацетона, цианистоводородная кислота и полимер, содержащий цианид калия Если добавить небольшое количество межфазного катализатора, такого как краун-эфир, реакция может быть завершена в более короткий период времени Температура реакции менее, чем 80°С, предпочтительно в диапазоне от комнатной температуры до 40°С В качестве примеров растворителя, описанного выше, приведены 1,2-дихлорэтан, толуол, ацетонитрил, метиленхлорид, хлороформ, этилацетат, ДМФ, метилизобутилкетон, ТГФ и диметокси-этан Кроме того, эта реакция превращения может быть также проведена в растворителе в присутствии основания, такого как карбонат калия, карбонат натрия, триэтиламин и пиридин Количество основания, которое должно быть использовано в реакции, находится в диапазоне от 0,5 до 2,0 моль в расчете на соединения формул [IVa] и [IVb], и в качестве растворителя в реакции могут быть использованы ТГФ, диоксан, трет-амиловый спирт и трет-бутиловый спирт Температура реакции находится в диапазоне от комнатной температуры до температуры кипения используемого растворителя Кроме того, подобная реакция превращения может быть также проведена путем добавления цианосоединения и основания, как описано выше, к реакционной смеси без выделения соединений формул [IVa] и [IVb] Более того, соединение формулы [I] может быть также получено использованием основания вместе с агентом дегидроконденсации, таким как ДЦК, без выделения соединений формул [IVa] и [IVb] В качестве примеров указанных выше оснований даны карбонат калия, карбонат натрия, триэтиламин и пиридин Количество используемого здесь основания находится в диапазоне от 0,5 до 2,0 моль в расчете на соединение формулы [VII] В дополнение, в качестве примеров растворителя, пригодного для использования в этой реакции, приведены ТГФ, диоксан, трет-амиловый спирт, трет-бутиловый спирт и т п , и температура реакции находится в диапазоне от комнатной температуры до температуры кипения используемого растворителя Производные 5-гидроксипиразола формулы [VII] могут быть получены согласно следующим процессам, которые описаны в патентной публикации Японии Laid-open No Sho 62-234069 Gazette и в патентной публикации Японии Laid-open No Неї 3-44375 Gazette 57738 (a) ГГЛ RCH*HKClUCH*COHCB! (H*CO)JCHCH*COMH«HJ (НзС0)гЄНСН2СОШ=С-СНгСН(СН3) «aC0)tCHCHtC0M-N«C-CH»CH(CH3)e R Clh H+ IT 0 R Производное альдегида формулы (3) и производное карбоновой кислоты формулы (4), которые являются важными синтетическими промежуточ ными соединениями в получении соединения согласно данному изобретению, могут быть получены согласно следующей формуле реакции где R1 и R2 обозначают то же, что указано выше, R6 обозначает водород или низшую алкильную группу и W обозначает атом галогена Альдегидное соединение формулы (3) может быть получено из производного толуола формулы (1) согласно известному методу, например, методом воздействия либо одним галогеном, таким как хлор и бром, либо агентом галогенирования, таким как N-бромсукцинимид (NBS) и Nхлорсукцинимид (NCS), в присутствии света (фотоинициатора) или радикального инициатора реакции, такого как пероксид бензоила, до получения производного бензилгалогенида формулы (2), затем превращением его в соответствии с методом, описанным в J Am Chem Soc , Vol 71, p 1767 (1949), в альдегидное соединение формулы (3) Более конкретно, альдегидное соединение формулы (3) может быть получено взаимодействием производного бензилгалогенида формулы (2) с солью щелочного металла нитроалкана, такого как 2-нитропропан, в спиртовом растворителе, таком как метанол и этанол, при температуре от 0°С до температуры кипения используемого растворителя Далее, производное карбоновой кислоты формулы (4) может быть получено из производного толуола формулы (1) путем реакции окисления с перманганатом калия или тому подобным, или, альтернативно, оно может быть получено из альдегидного соединения формулы (3) согласно известному методу с использованием реакции окисления с любым из реагентов Джонса, хромовой кислоты, перманганата калия или тому подобного Кроме того, при использовании как альдегидного соединения формулы (3), так и производного карбоновой кислоты формулы (4) промежуточные соединения могут быть получены так, как показано ниже 57738 10 e B'CHiMgV ^ R O 2 C 9 R 02C (1 1 2 6 где R , R и R обозначают то же, что указано выше, R7 обозначает низшую алкильную группу и 4 R обозначает водород или низшую алкильную группу Соответствующее ацильное соединение формулы (6) может быть получено путем получения вначале спиртового производного формулы (5), которое может быть получено в реакции альдегидного соединения формулы (3) с реагентом Гриньяра, и последующего окисления спиртового производного формулы (5) чем-либо из активированного диоксида марганца, хромовой кислоты и тому подобного Производное винилкетона формулы (10) может быть получено взаимодействием альдегидного соединения формулы (3) с производным метилкетона формулы (7) в присутствии катализатора при температуре от 0 до 100°С в течение от 1 до 50 часов в растворителе, таком как вода, толуол и хлороформ или смешанный растворитель, состоящий из воды и толуола, хлороформа и т п , до образования альдольного соединения формулы (8) и затем дегидратации альдольного соединения в присутствии катализатора в подходящем растворителе В качестве примеров катализатора, исполь 0) зуемого в реакции получения указанного альдольного соединения формулы (8), приведены гидроксид металла, такой как гидроксид натрия и гидроксид бария, и органическое основание, такое как пиперидин и пиридин Кроме того, в качестве примеров катализатора, который может быть использован в реакции дегидратации, описанной выше, приведены кислоты, такие как концентрированная серная кислота и п-толуолсульфоновая кислота В дополнение, в качестве примеров растворителя, используемого в указанной реакции дегидратации, даны углеводород, такой как бензол и толуол, и галогенированный углеводород, такой как дихлорметан и хлороформ Производное винилкетона формулы (10) может быть также получено путем взаимодействия альдегидного соединения формулы (3) с фосфолановым соединением формулы (9) в подходящем растворителе при температуре в диапазоне от комнатной температуры до температуры кипения используемого растворителя в течение периода от 10 минут до 30 часов Производное р-дикетона формулы (12) может быть получено согласно следующему процессу э Е ОаС a R G2C (13) 2) R80iC АА, H где R1, R2, R3 и R6 обозначают то же, что указано выше, и R" и R9 обозначают, каждый независимо, низшую алкильную группу В процессе реакции, как показано выше, производное карбоновой кислоты формулы (4) подвергают реакции с агентом хлорирования, таким как фосген, тионилхлорид и оксалилхлорид, в инертном растворителе, таком как углеводород, подобный бензолу или толуолу, и галогенированный углеводород, подобный метиленхлориду или хлороформу, чтобы получить производное карбонилхлорида формулы (11), которое является про 57738 12 11 межуточным соединением кетоэфира формулы (13) с алкоголятом магния в соответствии с известным методом Затем производное р-дикетона формулы (12) Далее приводится объяснение способа полуможет быть получено путем взаимодействия прочения производного изоксазола, которое является изводного карбонилхлорида формулы (11) с магпромежуточным соединением ниевой солью производного сложного р(Способ получения 1) кетоэфира (13), эта соль может быть получена путем взаимодействия производного сложного р R'OzC R°0 2 C (1 (1 0) 4) R s ChC В указанном выше процессе реакции R1, R2, R и R имеют указанные выше значения Производное изоксазола формулы (15а) может быть получено путем взаимодействия вначале производного винилкетона формулы (10) с гидроксиламином в соответствующем растворителе при температуре в диапазоне от 0°С до температуры кипения используемого растворителя в течение периода от 0,5 до 5 часов до образования производного оксима формулы (14) и последующего подвергания указанного производного оксима реакции циклизации и реакции окисления В этой реакции образования оксима либо сульфат, либо гидрохлорид гидроксиламина может быть использован даже без нейтрализации, однако, такие соли гидроксиламина могут быть использованы после нейтрализации их с помощью подходящего основания 3 В качестве примеров основания, используемого в реакции, могут быть приведены карбонат, такой как гидрокарбонат натрия и карбонат калия, гидроксид щелочного металла, такой как гидроксид натрия и гидроксид калия, карбоксилат, такой как ацетат натрия, алкоголят металла, такой как метилат натрия и этилат натрия, и органическое основание, такое кактриэтил-амин и пиридин Кроме того, в качестве примеров растворителя, используемого в реакции, приведены спирт, такой как метанол, этанол и изопропанол, углеводород, такой как бензол и толуол, галогенированный углеводород, такой как дихлорметан и хлороформ, простой эфир, такой как ТГФ и диоксан, нитрил, такой как ацетонитрил, ДМФ, пиридин, уксусная кислота, вода и смешанный растворитель, состоящий из двух или более указанных растворителей В реакции циклизации и реакции окисления, описанных выше, могут быть использованы смесь иода-иодида калия, N-бром-сукцинимид или паллад иевый катализатор, и целевые соединения могут быть полнены в соответствии с методом, описанным в J Am Chem Soc, р 94 (1972), J Heterocycl Chem , Vol 14, p 1289 (1977) и Tetrahedron Lett p 5075 (1977) (Способ получения 2) RaO3C - ( і 2) (1 1 2 В описанном выше процессе реакции R , R , R3, R4 и R6 обозначают то же, что указано выше Производное изоксазола формулы (15) может быть также получено путем взаимодействия производного р-дикетона формулы (12) или с гидроксиламином, или с солью гидроксиламина Эта реакция может быть проведена в подходящем растворителе при температуре в диапазоне от 0°С до температуры кипения используемого растворителя В этой реакции в качестве катализатора может быть также использована кислота, такая как серная кислота и п -толуол сул ьфо новая кислота 5) В качестве примеров растворителя, используемого в реакции, приведены спирт, такой как метанол, этанол и изопропанол, углеводород, такой как бензол и толуол, галогенированный углеводород, такой как дихлорметан и хлороформ, простой эфир, такой как ТГФ и диоксан, нитрил, такой как ацетонитрил, ДМФ, пиридин, уксусная кислота, вода и смешанный растворитель, состоящий из двух или более указанных растворителей (Способ получения 3) 57738 13 ** 14 ПГіНС(ОЕ'): НІШ В описанном выше процессе реакции R1, R2, R , R4 и R6 обозначают то же, что указано выше, и r-і, Г и R1 обозначают, каждый независимо, низ2 шую алкильную группу Альтернативно, производное изоксазола формулы (15) может быть получено реакцией производного диалкиламинометилидена формулы (16) (которое получают взаимодействием 3ацильного соединения формулы (6), описанного выше, с диалкилацеталем N,Nдиалкилалкиламида, таким как диметилацеталь N.N-диметилацетамида) либо с гидроксиламином, либо с солью гидроксиламина (Способ получения 4) 3 * В3 R'SH „основание (I-3) [0] ReO2C В описанном выше реакционном процессе R1, R , R и R обозначают то же, что указано выше, и R' обозначает Сі є алкильную группу Кроме того, производное бензойной кислоты формулы (15Ь) может быть получено взаимодействием меркаптосоединения формулы R'SH с 4-CI соединением формулы (1-2) в присутствии основания до образования 4-SR' соединения формулы (1-3) и последующего окисления указанного 4-SR' соединения В качестве примеров основания, используемого в этой реакции, могут быть приведены гидроксид щелочного металла, такой как гидроксид натрия и гидроксид калия, алкоксид металла, такой как метоксид натрия и этоксид натрия, карбонат, такой как карбонат натрия и карбонат калия, гидрид, такой как гидрид натрия, и органическое основание, такое как триэтиламин, диизопропилэтиламин, 1,8-диазабицикло[5 4 0]-унде7-цен (DBU) и пиридин В дополнение, в качестве примеров растворителя, используемого в реакции, могут быть приведены спирт, такой как метанол и этанол, простой эфир, такой как ТГФ и 1/2диметоксиэтан (ДМЭ), амид, такой как ДМФ и N,N диметилацетамид (ДМ А), диметилсульфоксид (ДМСО), ацетонитрил, бензол, толуол и ксилол Последующую реакцию окисления осуществляют с помощью какого-либо окислителя, например пероксида, такого как пероксид водорода, перуксусная кислота, пербензойная кислота и мхлорпербензойная кислота, или гипохлористой кислоты, такой как гипохлорит натрия и гипохлорит калия, в инертном растворителе, включая воду, органическую кислоту, такую как уксусная кислота, и галогенированный углеводород, такой как дихлорметан, хлороформ и четыреххлористый углерод Реакция может гладко протекать в температурном диапазоне от комнатной температуры до температуры кипения используемого растворителя Альтернативно, соединение формулы (1-3) может быть получено путем взаимодействия меркаптосоли, которую получают предварительно в реакции с меркаптосоединением формулы R'SH и основанием, с соединением формулы (1-2) (Способ получения 5) В дополнение, соединение формулы (15) может быть получено согласно методу, описанному в 15 57738 WO 96/26206 Gazette Далее представлен способ 16 получения указанного соединения формулы (15) V-/ О (15) fl R Q2C^ В описанном выше процессе реакции R1, R2, R и R6 обозначают то же, что указано выше, Y обозначает Br, I, OSO2CF3 и М обозначает Sn(Ci є алкил)з, В(ОН)2 или ZnCI Различные типы таутомеров, как иллюстриру ется здесь ниже, могут присутствовать в соединениях формулы [I] согласно данному изобретению Поэтому следует отметить, что все эти таутомеры подпадают под объем действия данного изобретения Соединения данного изобретения и различные промежуточные соединения могут быть получены путем проведения соответствующей последующей обработки после завершения реакции обычными методиками Структуры соединений согласно данному изобретению и различных промежуточных соединений для их получения определены с помощью ИК, ЯМР, МС и других доступных средств Теперь данное изобретение описывается более подробно со ссылкой на примеры и сравнительные примеры, описанные далее, однако, объем изобретения не должен ограничиваться одним из этих описанных примеров (Пример 1) Получение 1 -этил-5-гидрокси-4-[4метансульфонил-2-метил-3-(3-метил-1,2изоксазол-5-ил)] бензоилпиразола 3 SOCI HQ Ч СНз. , Н О 57738 17 4-метансульфонил-2-метил-3-(3-метил-1,2изоксазол-5-ил)бензойную кислоту в количестве 1,35г (4,61 ммоль) растворяют в 15мл бензола и добавляют 0,71г (5,97 ммоль) тионил-хлорида и одну каплю пиридина с последующим перемешиванием в течение 2 часов при кипячении с обратным холодильником После этого раствору позволяют остыть, растворитель отгоняют при пониженном давлении, чтобы получить 1,43г 4метансульфонил-2-метил-3-(3-метил-1,2изоксазол-5-ил) бензоилхлорида 0,38г (2,6 ммоль) гидрохлорида 1-этил-5гидроксипиразола и 0,51 г (5,1 ммоль) триэтиламина растворяют в 10мл метиленхлорида и добавляют по каплям при комнатной температуре 2мл раствора метиленхлорида, содержащего 0,71 г (2,3 ммоль) 4-метансульфонил-2-метил-3- (3-метил1,2-изоксазол-5-ил) бензоилхлорида с последующим перемешиванием при комнатной температуре в течение 1 часа Полученную реакционную смесь промывают 1н хлористоводородной кисло 18 той и затем насыщенным раствором хлорида натрия, а потом сушат над безводным сульфатом магния и растворитель отгоняют при пониженном давлении Полученный осадок, растворяют в 10мл ацетонитрила и добавляют 0,47г (4,7 ммоль) триэтиламина и 0,06г (0,7 ммоль) циангидрина ацетона с последующим перемешиванием при комнатной температуре в течение ночи Растворитель отгоняют при пониженном давлении и остаток растворяют в этилацетате После этого раствор промывают 1 н хлористоводородной кислотой и затем насыщенным раствором хлорида натрия, а потом сушат над безводным сульфатом магния и растворитель отгоняют при пониженном давлении Оставшиеся кристаллы промывают метанолом, чтобы получить 0,50г целевого соединения Тпл = 186-189°С Типичные примеры соединений, полученных согласно данному изобретению, как описано выше, даны в Таблице 1 ТаОлица 1 R3 Сседада. № 1 сі Сі 2 СН3 SGiCHs 3 рц s til SujCaHs 4 ен3 Cl 6 СЭ Н СН3 7 Сз Н 8 СЯ, 9 ся, сна '5 10 11 12 L3 14 15 16 га was са, са, сн 3 SOaCHs SQsCsHs V 1 В H H H H H н в 8 н н н н к н н н н к н н я а сн, в $оген3 в SOiC2H, н Сі н • SOzCH, н SOaCjHs н Cl .н СІ SQjCHs й' Сз Н SOsCiH CH, ' SQaCiHs H H H H H H CH, CH, CH3 CH, CHS CH, 48 . CHs РЕ" C l SdCHa SthCsHs C l SO 2 CK 3 SOtCafi» Cl ' Lfl, on rti CHa SOjCH, CHS CH3 CK3 CH, CHa CR, SQ S CH 3 Cl Ca H SQjCHa CRi SO a C s R s C l SOjCH, CH, 47 48 49 50 51 52 53 54 55 > 56 57 58 CHS CH, H H H к H H H H H Темп.пл. {°С} CHs Ca H C s Hs C:HS CHi CH, CH, CH, CH3 ИЗО-Сэй7 1 • Ca H трвт.-СЙ CiHj В Mi н н к н к н І-СаНт t-C 4 B B CH, C» H CH, CH, CH, CH, СНЇ Ca H CH, СН3 24 57738 23 Соєдин R R1 V V R 59 • сн8 Ca H SDICJHI CH 3 CH3 C, H CiHs CjHj 60 1 зол 61 62 СНЇ 63 CHa 64 CHj *' 65 ен3 ся, ся, 66 67 68 . СВі 69 сн* CHj 70 Сі CHi CHj CH3 Ctb CfU CHs CH3 SJH OC J CHj CH3 ИЗО-СЗН, ЗО г С г Нї CHs CHs изо-СэНт Cl СНЇ CH, тре*.-С,Н, Qfl ГН CHj CB3 т р е т . -:С^І* sosc3m CHa CHa т р е т . -С«Н, Cl CtHs* CHj Н SOjCH* СгНя н н н н н . н SJJ » OCH C l 71 СЭ Н SO*CH S і-С.Нт CHs ru voj .72 Сз Н SOjCHs t-C.Hg CHj 73 СЇН5 Ci C« H H 74 с«нб с,н. S Q A Ca H H S0sCafl3 CH, К H • H H H 75 76 СіН» Cl 77 СЇНЇ SQ 2 CH, 78 C3HS schema 79 с,в. Cl Cfi, fa vita CH3 ли Са Н Са Н сн3 • СгНа Темп.пя. (°С) 25 57738 26 V Ссетн. № V V R н н н к н н н н в н н, н н н н н н н СгН* 80 CtHs SGJCHJ Сй3 81 СгНь 30г€3Н4 СНз 82 СЇН6 Сі сн, 83 CjHs SOJCHI СН3 84 Сгйз ЗОгСгНї КіпЗ Сі 85 сна сгна SQaCH3 CHJ 87 SOzCzH, 88 І-СаЯт Сі 89 і-СНт S sH OC a 90 ; л и ї-Ьзйі СІ ск, н н єн* 91 і-СаИт S0:CH3 Са Н 86 92 СНа SCH3 СРз 93 єн* S0CH3 CFj 94 СН3 SCiHs С?, 95 Са Н SGCaHs СРЭ 96 Са Н Сі 97 СН3 SOICH1 с?3 Ca F (Ссылочный пример 1) Получение метил-4-метансульфонил-2-метил Теш. an. (°С) CtHs изо-СэН? ИЗО-СэН7 Т р е т . -С4Н5 К к н н CHS сн, Сйа сн* С:Н* CiHs 3-(3-метил-1/ 2-изоксазол-5-ил)бензоата NBS РГНО; 1)РЬ3Р=СНС0СНз 2>ННаОН НС1 3) U 10,8г (0,045 моль) метил-2,3-диметил-4метансульфонил-бензоата растворяют в 80мл тетрахлорида углерода и затем добавляют 8,3г (0,047 моль) N-бромсукцинимида и 0,1 г пероксида бензоила с последующим перемешиванием в течение 3 часов при нагревании с обратным холодильником После этого раствору позволяют остыть, нерастворенное вещество удаляют фильтрованием, а полученный фильтрат промывают водным раствором кислого бисульфита натрия и затем сушат над безводным сульфатом магния Затем растворитель отгоняют при пониженном давлении, остаток очищают колоночной хроматографией на силикагеле, чтобы получить 6,2г метил-3-бромметил-4-метансульфонил-2метилбензоата в кристаллическом состоянии Выход = 43,4% 2,6г (0,014 моль) раствора метанола, содержащего 28% метилата натрия, добавляют к 20мл метанола и добавляют по каплям при комнатной температуре 1,3г (0,015 моль) 2-нитропропана Затем добавляют 4,4г (0,014 моль) метил-3бромметил-4-метансульфонил-2-метилбензоата с последующим перемешиванием в течение 1 часа при кипячении с обратным холодильником После этого раствору позволяют остыть, добавляют 50мл 1н хлористоводородной кислоты к реакционному раствору, проводят экстракцию этилаце 27 28 57738 татом Слой этилацетата промывают насыщенным раствором хлорида натрия и затем сушат над безводным сульфатом магния Затем раствор упаривают (концентрируют) при пониженном давлении, чтобы получить 3,1 г метил-З-формил-4метансульфонил-2-метилбензоата в кристаллическом состоянии Выход = 88% 30мл бензола и затем 3,85г (0,012 моль) 2оксо-пропилидентрифенилфосфолана добавляют к 3,1 г (0,012 моль) метил-З-формил-4метансульфонил-2-метилбензоата с последующим перемешиванием в течение 1 часа при кипячении с обратным холодильником Затем раствору позволяют остыть Нерастворенное вещество удаляют фильтрованием, а раствор концентрируют при пониженном давлении, чтобы получить метил-4-метансульфонил-3-(3-оксо-1-бутенил)-2метилбензоат Полученный таким образом метил4-метансульфонил-3-(3-оксо-1-бутенил)-2метилбензоат растворяют в растворителе из 10мл этанола и 10мл пиридина и добавляют 1,1г (0,016 моль) гидрохлорида гидроксиламина с последующим перемешиванием в течение 1 часа при кипячении с обратным холодильником Полученную реакционную смесь выливают в ледяную воду и проводят экстракцию этилацетатом После этого полученный слой этилацетата промывают 1н хлористоводородной кислотой и затем насыщенным раствором хлорида натрия и потом сушат над безводным сульфатом магния После этого рас творитель отгоняют при пониженном давлении Полученный таким образом метил-4метансульфонил-3-(3-гидроксиимино-1-бутенил)2-метилбензоат растворяют в 15мл ТГФ и к раствору добавляют 15мл воды, содержащей 1,4г (0,017 моль) гидрокарбоната натрия Вслед за этим добавляют водный раствор, полученный растворением 2,5г (0,015 моль) иодида калия и 1,1г (0,05 моль) иода в 12мл воды, и раствор нагревают с обратным холодильником в течение 3 часов в условиях без доступа света Реакционную смесь выливают в ледяную воду и добавляют кислый сульфит натрия с последующей экстракциейэтилацетатом Полученный органический слой промывают насыщенным раствором хлорида натрия и затем сушат над безводным сульфатом магния После этого растворитель отгоняют при пониженном давлении Полученный остаток очищают колоночной хроматографией на силикагеле, чтобы получить 0,84г метил-4-метансульфонил-2метил-3-(3-метил-1,2-изоксазол-5-ил)бензоата Выход = 23% 1 Н-ЯМР (CDCI3l 5 м д ) 2,36 (ЗН, с), 2,45 (ЗН, с), 2,92 (ЗН, с), 3,98 (ЗН, с), 6,41 (1Н, с), 8,07 (1Н, Д), 8,16 (1Н, д) (Ссылочный пример 2) Получение метил-4-метансульфонил-2-метил3-(3-метил-1,2-изоксазол-5-ил)бензоата ВВг 3 TfiO SQ 2 CH : foCH// NN -* С э Н LIC1 Юг (0,044 моль) метил-3-метокси-2-метил-4метилтиобензоата растворяют в 90мл метиленхлорида и раствор добавляют по каплям к 90мл метиленхлорида, содержащего 8,4мл (0,088 моль) трибромида бора, при 5 - 10°С После перемешивания при комнатной температуре в течение 4 часов добавляют по каплям 50мл метанола при охлаждении льдом и затем промывают раствор водой, а потом насыщенным раствором хлорида натрия После сушки над безводным сульфатом магния растворитель отгоняют при пониженном давлении, чтобы получить 9,2г метил-3-гидрокси2-метил-4-метилтиобензоата Выход = 98% 9,2г (0,043 моль) метил-3-гидрокси-2-метил-4метилтиобензоата растворяют в 50мл уксусной кислоты и затем добавляют 14,8г (0,130 моль) 30%-ного пероксида водорода с последующим перемешиванием при 80°С в течение 3 часов Затем реакционную смесь выливают в ледяную воду и осажденные кристаллы собирают фильтрованием, промывают водой и затем сушат, чтобы получить 8,8г метил-3-гидрокси-4-метансульфонил-2метилбензоата Выход = 83% 8,8г (0,036 моль) метил-З-гидрокси-4метансульфонил-2-метилбензоата растворяют в 100мл метиленхлорида и добавляют 8,3г (0,11 моль) пиридина Потом раствор охлаждают до 0°С, добавляют 12,2г (0,043 моль) ангидрида трифторметансульфоновой кислоты После перемешивания при комнатной температуре в течение 1 часа реакционную смесь промывают 1н хлористоводородной кислотой и затем насыщенным 57738 30 29 раствором хлорида натрия и после этого сушат метилфенола с последующим перемешиванием над безводным сульфатом магния Растворитель при 140°С в течение 3 часов в автоклаве Затем отгоняют при пониженном давлении, чтобы полураствору позволяют остыть, нерастворенное вечить 13,5г метил-4-метансульфонил-2-метил-3щество удаляют фильтрованием и растворитель (трифторметансульфонил)окси-бензоата Выход = отгоняют при пониженном давлении Остаток 99% очищают с помощью колоночной хроматографии на силикагеле, чтобы получить 0,74г метил-41,65г (4,4 ммоль) метил-4-метансульфонил-2метансульфонил-2-метил-3-(3-метил-1,2метил-3-(трифторметансульфонил)оксибензоата и изоксазол-5-ил)бензоата Выход = 55% 1,97г (5,3 ммоль) З-метил-5(трибутилстаннил)изоксазола растворяют в 20мл (Сравнительный пример 3) диоксана и добавляют 0,58г (14 ммоль) хлорида Получение 4-метансульфонил-2-метил-3-(3лития, 0,1 г тетракис (трифенилфосфин)метил-1,2-изоксазол-5-ил)бензойной кислоты палладия-(О) и 0,01 г 2,6-ди-трет-бутил-4 НаОН 3,11г (10,1 ммоль) метил-4-метансульфонил2-метил-3-(3-метил-1,2-изоксазол-5-ил)бензоата растворяют в 30мл метилового спирта и затем добавляют 30мл 1н водного раствора едкого натра с последующим перемешиванием при комнатной температуре в течение ночи Полученную реакционную смесь выливают в ледяную воду и затем подкисляют концентрированной хлористоводородной кислотой После этого осажденные кристаллы собирают фильтрованием, промывают водой и затем сушат, чтобы получить 2,85г 4метансульфонил-2-метил-3-(3-метил-1,2изоксазол-5-ил) бензойной кислоты Выход = 96% и т пл = 242°С (Получение соединений, используемых для сравнения) Соединение А для цели сравнения описано в WO 93/17083 Gazette и соединения В и С являются соединениями, описанными в WO 96/26206 Gazette А также соединение D дано в качестве примера в WO 96/26206 Gazette Соединение D получают согласно тому же способу, как описано в Примере 1, используя 4-метансульфонил-2-метил3-(3-метил-1,2-изоксазол-5-ил) бензойную кислоту, которую получают в Ссылочном примере 3, и 1,3диметил-5-гидроксипиразол в качестве исходного материала Т пл =137-139°С САЗ СО (Полезный эффект изобретения) Соединения данного изобретения могут обеспечивать высокую гербицидную активность даже в условиях двух способов нанесения, включая обработку почвы и нанесение на листву, в условиях полеводства, и они эффективны против различных видов вредных сорняков, таких как лисохвост, дурнишник, лебеда белая и овсюг Соединения данного изобретения включают соединения, которые избирательно нетоксичны по отношению к культурным растениям, таким как кукуруза, пшеница, ячмень, соя и хлопок Более того, соединения данного изобретения включаютсоединения, которые могут проявлять способность регулировать рост растений, такую как ингибирование роста, в отношении полезных растений, таких как сельскохозяйственные культуры, декоративные цветочные растения, фруктовые деревья и т д Кроме того, соединения данного изобретения оказывают особенно хорошее гербицидное воздействие на сорняки, такие как куриное просо, Cyperus difformis, Sagittana tnfoha и Scirpus juncoides, и имеют селективность по отношению к 31 57738 растениям риса Более того, соединения данного изобретения могут быть применены для борьбы с сорняками в плодовых питомниках, на газонах, железнодорожных путях, пустующих землях и тому подобное [Гербицид] Гербицид ный препарат согласно данному изобретению содержит одно или несколько соединений данного изобретения в качестве активных компонентов При фактическом применении соединение данного изобретения может быть использовано в чистом виде без добавления какихлибо других компонентов и для цели использования соединений изобретения в качестве химиката для защиты растений, соединения по изобретению могут быть использованы в виде препарата, обычно используемого в химикатах для защиты растений Например, в виде смачиваемых порошков, гранул, дустов, эмульгируемых концентратов, растворимых в воде порошков, суспензии или текучих препаратов В качестве добавки или носителя, который может быть использован в составе твердого препарата, могут быть использованы порошки растительного происхождения, такие как соевая мука и пшеничная мука, тонкие минеральные порошки, такие как диатомовая земля, апатит, гипс, тальк, бентонит, пирофилит и глина, и органические и неорганические соединения, такие как бензоат натрия, мочевина и глауберова соль В случае, когда предполагается использование жидкого препарата, может быть использован растворитель, например фракции нефти, такие как керосин, ксилол и сольвент-нафта, циклогексан, циклогексанон, диметилформамид, диметилсульфоксид, спирты, ацетон, трихлорэтилен, метилизобутилкетон, минеральные масла, растительные масла и вода Чтобы сохранить препарат в однородном и стабильном состоянии, может быть добавлено поверхностно-активное вещество, если необходимо Концентрация активного компонента в гербицидном препарате данного изобретения зависит от формы указанного выше агента, но, например, в случае смачиваемого порошка она находится в диапазоне от 5 до 90%, предпочтительно от 10 до 85%, в случае эмульсии она находится в диапазоне от 3 до 70%, предпочтительно от 5 до 60%, и в случае гранул она находится в диапазоне от 0,01 до 50%, предпочтительно от 0,05 до 40% Полученный таким образом смачиваемый порошок или эмульсию, соответственно, разбавляют до заданной концентрации водой, чтобы получить суспензию или эмульсию, а гранулы могут быть просто разбросаны на почву или смешаны с ней до или после прорастания сорняков Фактически, когда применяют гербицид данного изобретения, подходящим для нанесения количеством активного компонента является 0,1 г или более на гектар Кроме того, гербицид данного изобретения может быть использован в смеси с каким-либо из известных фунгицидов, инсектицидов, акарицидов, других гербицидов, регуляторов роста растений и удобрений В частности, когда гербицид данного изобретения смешивают с другими гербицидами, количество гербицида по данному изобретению может быть уменьшено Кроме того, 32 использование гербицида данного изобретения ведет к снижению трудозатрат, и можно также ожидать более высоких эффектов данного изобретения за счет синергетического эффекта смешанных агентов В этом случае возможно также смешивать гербицид данного изобретения со множеством известных гербицидов Примеры агентов, которые подходят для смешивания с гербицидом данного изобретения, включают анилидсодержащие гербициды, такие как дифлуфеникан и пропанил, хлорацетанилидсодержащие гербициды, такие как алахлор и претилахлор, гербициды, содержащие арилоксиалкановую кислоту, такие как 2,4-D и 2,4-DB, гербициды, содержащие арилоксифеноксиалкановую кислоту, такие как диклофоп-метил и феноксапропэтил, гербициды, содержащие арилкарбоновую кислоту, такие как дикамба и пиритиобакнатрий, гербициды, содержащие имидазолинон, такие как имазаквин и имазетапир, гербициды, содержащие мочевину, такие как диурон и изопротурон, гербициды, содержащие карбамат, такие как хлорпрофам и фенмедифам, гербициды, содержащие тиокарбамат, такие как тиобенкарб и ЕРТС, гербициды, содержащие динитроанилин, такие как трифлуралин и пендиметалин, гербициды, содержащие простой дифениловый эфир, такие как ацифлуорфен-натрий и фомезафен, гербициды, содержащие сульфонил-мочевину, такие как бенсульфурон-метил и никосульфурон, гербициды, содержащие триазинон, такие как метрибузин и метамитрон, гербициды, содержащие триазин, такие как атразин и цианазин, гербициды, содержащие триазопиримидин, такие как флуметсулам, гербициды содержащие нитрил, такие как бромоксинил и дихлобенил, гербициды, содержащие пиридазинон, такие как хлоридазон и норфлуразон, гербициды, содержащие фосфорную кислоту, такие как глифосат и глюфозинат, гербициды, содержащие соль четвертичного аммониевого основания, такие как паракват и дифензокват, гербициды, содержащие циклический амид, такие как флумиклорак-пентил и флутиацетметил, другие гербициды, такие как изоксабен, этофумезат, оксадиазон, квинклорак, кломазон, сулкотрион, цинметилин, дитиопир, пиразолат, пиридат, флупоксам, бентазон и бенфурезат, и гербициды, содержащие циклогександион, такие как сетоксидим и тралкоксидим Кроме того, к смеси этих активных компонентов может быть добавлено растительное масло или маслянистый конденсат [Примеры] (Гербицид) Далее описаны некоторые примеры рецептур гербицидного препарата согласно данному изобретению, однако, соединения активного компонента, добавки и их соотношение не лимитируются тем, что описано в этих примерах, и они могут изменяться или расширяться в широком диапазоне В примерах рецептур "часть(части)" обозначает "часть(части) по массе" (Пример 2) Рецептура смачиваемого порошка Соединение данного изобретения 20 частей Белая сажа 20 частей Диатомовая земля 52 части 57738 33 Алкилсульфат натрия 8 частей Эти материалы однородно смешивают и затем тонко измельчают для получения смачиваемого порошка, содержащего 20% эффективного компонента (Пример 3) Состав эмульгируемого концентрата Соединение данного изобретения 20 частей Ксилол 55 частей Диметилформамид 15 частей Фениловый эфир полиоксиэтилена 10 частей Эти материалы однородно смешивают и растворяют, чтобы получить эмульсию, содержащую 20% эффективного компонента (Пример 4) Гранулированный состав Соединение данного изобретения 5 частей Тальк 40 частей Глина 38 частей Бентонит 10 частей Алкилсульфат натрия 7 частей Эти материалы однородно смешивают, тонко измельчают и затем гранулируют, чтобы получить 34 гранулы, имеющие диаметр от 0,5 до 1,0мм, и содержащие 5% эффективного компонента [Примеры испытания] Далее описаны примеры испытания в отношении гербицидного эффекта гербицидов согласно данному изобретению Гербицидный эффект оценивают в соответствии со следующим критерием оценки и выражают в виде показателей, отражающих силу гербицидного препарата Критерий оценки Уничтоженные сорняки в % Гербицидный показатель 0% 0 20 - 29% 2 40 - 49% 4 60 - 69% 6 80 - 89% 8 100% 10 Кроме того, величины 1, 3, 5, 7 и 9 обозначают величины между 0 и2, 2 и 4, 4 и 6, 6 и 8 и 8 и 10, соответственное (Свежая масса побегов на необработа нном участке Свежая масса побегов на обработанном участке) % уничтоженн ых сорняков = :100 Свежая масса побегов на необработа нном участке (Пример испытания 1) Нанесение на листву наземной части сорняков на суходольных полях культурных посевов Горшки размером 200см2 заполняют почвой и семена канатника, лебеды, дурнишника, лисохвоста и кукурузы высаживают в горшки, соответственно После этого семена покрывают почвой, оставляют для выращивания в теплице Когда растения вырастут до высоты 5 - 25см, на стебли и листья сорняков распыляют небольшим распылителем разбавленные водные растворы эмульсии, указанной в Примере 3, содержащей образцы соединения, так чтобы активный компонент в количестве 250г/га был внесен в каждый из горшков Через 3 недели оценивают гербицидные эффекты соответствующих соединений в отношении сорняков (результаты приведены в Таблице 2) Показано, что соединения согласно данному изобретению обеспечивают превосходную гербицидную активность против различных типов сорняков и, в частности, имеют высокую селективность по отношению к растениям кукурузы, не оказывая на них вредного воздействия Таблица 2 Соединение № 20 23 А В С D Канатник 10 10 6 7 10 10 Лебеда 10 10 8 2 7 10 Как описано выше, соединение формулы [1] имеет превосходную селективность гербицидной активности по отношению к культурным растениям и сорнякам и, конкретно, оно селективно безопасно для растений кукурузы Поэтому гербицидный Комп'ютерна верстка А Крулевський Дурнишник 10 10 10 10 10 9 Лисохвост 10 10 9 6 10 10 Кукуруза 0 0 2 0 4 7 препарат, содержащий соединение согласно данному изобретению, может быть полезен в качестве селективного гербицида для борьбы с сорняками на полях кукурузы Підписано до друку 05 08 2003 Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ТОВ "Міжнародний науковий комітет", вул Артема, 77, м Київ, 04050, Україна
ДивитисяДодаткова інформація
Назва патенту англійськоюDerivatives of benzene substituted by heterocycles and herbicides
Назва патенту російськоюПроизводные бензола, замещенные гетероциклами, и гербициды
МПК / Мітки
МПК: A01N 43/56, A01P 13/00, C07D 413/10, A01N 43/80
Мітки: похідні, бензолу, гетероциклами, гербіциди, заміщені
Код посилання
<a href="https://ua.patents.su/17-57738-pokhidni-benzolu-zamishheni-geterociklami-ta-gerbicidi.html" target="_blank" rel="follow" title="База патентів України">Похідні бензолу, заміщені гетероциклами, та гербіциди</a>
Попередній патент: Спосіб одержання карведилолу та проміжні сполуки
Наступний патент: Антифрикційне пластичне мастило
Випадковий патент: Рекламна огорожа