Орто-похідні бензойної кислоти для лікування резистентності до інсуліну
Формула / Реферат
1. Сполука формули І
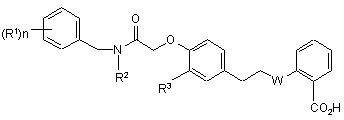 , (I)
, (I)
де n дорівнює 0, 1 або 2;
R1 представляє галоген, С1-4алкіл, який, як варіант, заміщено одним або більше атомами флуору, С1-4алкоксил, який, як варіант, заміщено одним або більше атомами флуору, а коли n дорівнює 2, замісники R1 можуть бути однаковими або різними;
R2 представляє нерозгалужений С2-7алкіл;
R3 представляє Н або ОСН3;
a W представляє О або S;
та її фармацевтичнo прийнятні солі та проліки.
2. Сполука за п. 1, де W представляє О.
3. Сполука за п. 1, де W представляє S.
4. Сполука за п. 1, вибрана з групи:
2[2-(4-{2-[етил(2-флуорбензил)аміно]-2-оксоетокси}феніл)етокси]бензойна кислота;
2-[2-(4-{2-[(2,4-дифлуорбензил)(гептил)аміно]-2-оксоетокси}-3-метоксифеніл)етокси]бензойна кислота;
2-[2-(4-{2-[(4-хлорбензил)(етил)аміно]-2-оксоетокси}феніл)етилтіо]бензойна кислота;
2-[2-(4-{2-[(4-хлорбензил)(етил)аміно]-2-оксоетокси}феніл)етокси]бензойна кислота;
2-[2-(4-{2-[етил(4-трифлуорметилбензил)аміно]-2-оксоетокси}феніл)етокси]бензойна кислота;
2-[2-(4-{2-[етил(4-трифлуорметилбензил)аміно]-2-оксоетокси}феніл)етилтіо]бензойна кислота;
2-{2-[4-(2-{бутил[2-флуор-4-(трифлуорметил)бензил]аміно}-2-оксоетокси)феніл]етокси}бензойна кислота;
2-[2-(4-{2-[(2,4-дифлуорбензил)(пропіл)аміно]-2-оксоетокси}феніл)етокси]бензойна кислота;
2-[2-(4-{2-[бензил(етил)аміно]-2-оксоетокси}феніл)етокси]бензойна кислота;
2-{[2-(4-{2-[бензил(етил)аміно]-2-оксоетокси}феніл)етил]тіо}бензойна кислота;
2-[2-(4-{2-[(4-трет-бутилбензил)(етил)аміно]-2-оксоетокси}феніл)етокси]бензойна кислота;
2-[2-(4-{2-[етил(4-флуорбензил)аміно]-2-оксоетокси}феніл)етокси]бензойна кислота;
2-{[2-(4-{2-[етил(2-флуорбензил)аміно]-2-оксоетокси}феніл)етил]тіо}бензойна кислота або 2-{[2-(4-{2-[(2-хлорбензил)(етил)аміно]-2-оксоетокси}феніл)етил]тіо}бензойна кислота; та її фармацевтичнo прийнятні солі.
5. Фармацевтична композиція, що містить сполуку за будь-яким з попередніх пунктів у суміші з фармацевтичнo прийнятними ад'ювантами, розріджувачами та/або носіями.
6. Спосіб лікування або попередження резистентності до інсуліну, при якому вводять сполуку за будь-яким одним з пп. 1-4 ссавцю, що цього потребує.
7. Застосування сполуки за будь-яким одним з пп. 1-4 у виробництві медикаменту для лікування резистентності до інсуліну.
8. Спосіб отримання сполуки формули І, при якому здійснюють реакцію сполуки формули II
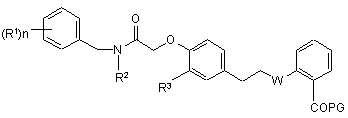 , (ІI)
, (ІI)
в якій R1, R2, R3, W та n визначено раніше, a PG представляє захисну групу для карбоксильного гідроксилу, із засобом зняття захисту.
9. Сполука загальної формули II, у якій R1, R2, R3, W та n визначено раніше, а PG представляє захисну групу для карбоксильного гідроксилу.
10. Комбінаційне лікування, при якому ссавцю, що цього потребують, вводять сполуку за будь-яким одним з пп. 1-4 у комбінації з іншим терапевтичним засобом, який є корисним у лікуванні розладів, асоційованих з розвитком та прогресом атеросклерозу, як-то гіпертензія, гіперліпідемії, дисліпідемії, діабети та ожиріння.
Текст
1. Сполука формули І 3 76627 4 9. Сполука загальної формули II, у якій R1, R2, R3, одним з пп. 1-4 у комбінації з іншим терапевтичW та n визначено раніше, а PG представляє захиним засобом, який є корисним у лікуванні розладів, сну групу для карбоксильного гідроксилу. асоційованих з розвитком та прогресом атеро10. Комбінаційне лікування, при якому ссавцю, що склерозу, як-то гіпертензія, гіперліпідемії, дисліпіцього потребують, вводять сполуку за будь-яким демії, діабети та ожиріння. Представлений винахід стосується деяких нових похідних бензойної кислоти, способів отримання таких сполук, їх корисності у лікуванні клінічних станів, асоційованих з резистентністю до інсуліну, способів їх терапевтичного застосування та фармацевтичних композицій, що їх містять. Синдром резистентності до інсуліну (СРІ), залучаючи цукровий діабет типу 2, який стосується сукупності виявів, залучаючи резистентність до інсуліну з супроводжуючою гіперінсулінемією, можливий цукровий діабет типу 2, артеріальну гіпертензію, центральне (вісцеральне) ожиріння, дисліпідемію, виявлювану як ненормальні рівні ліпопротеїнів, звичайно охарактеризовані підвищеними концентраціями ЛДНГ (ліпопротеїни дуже низької густини), частинок ЛНГ низької густини та зменшеними концентраціями ЛВГ (ліпопротеїн високої густини) та зменшеним фібринолізом. Нещодавнє епідеміологічне дослідження доказало, що особи з резистентністю до інсуліну мають значно збільшений ризик серцево-судинно захворюваності та смертності, особливо потерпаючи від інфаркту міокарду та нападу. При цукровому діабеті типу 2 пов'язані з атеросклерозом стани викликають до 80% усіх смертей. У клінічній медицині відома необхідність у збільшенні чутливості до інсуліну у потерпаючих від СРІ пацієнтів, а тим корекції дисліпідемії, яка, як вважають, викликає прискорений прогрес атеросклерозу. Однак, зараз це не є всесвітньо добре визначеною хворобою. S-енантіомер сполуки формули С нижче 2-етокси-3-[4-(2-{4метансульфонілоксифеніл}етокси)феніл]пропанова кислота, розкрито у міжнародній патентній публікації WO99/62872. Цю сполуку показано, як модулятор активованих пероксизомним проліфератором рецепторів [АППР, для огляду АППР дивись Т. M.Willson et al, J Med Chem 2000, Vol 43,527] та має комбіновану ΑΠΠΡ /ΑΠΠΡ -агоністичну активність [Structure, 2001, Vol 9, 699, P. Cronet et al]. Ця сполука є ефективною у лікуванні станів, асоційованих з резистентністю до інсуліну. Несподівано виявлено серію сполук, які є селективними модуляторами АППР Представлений винахід стосується сполуки формули І де n дорівнює 0, 1 або 2; R1 представляє галоген, С1-4алкіл, який, як варіант, заміщено одним або більше флуором, С14алкоксил, який, як варіант, заміщено одним або більше флуором, а коли n дорівнює 2, замісники R1 можуть бути однаковими або різними; R2 представляє нерозгалужений С2-7алкіл; R3 представляє Η або ОСН3; a W представляє О або S та її фармацевтично прийнятних солей та проліків. Подальші значення R1, R2, R3 та W у сполуках формули І нижченаведено. Зрозуміло, що такі значення можна використовувати з будь-яких визначень, пунктів патентної формули або втілень, визначених вище або далі. Згідно з першим аспектом R1 представляє галоген, С1-4алкіл або С1-4алкоксил, а n дорівнює 0, 1 або 2. Особливо, R1 представляє флуор, хлор або трифлуорметил, коли n дорівнює 1. Особливо R1 представляє флуор, коли n дорівнює 2. Згідно з другим аспектом R2 представляє етил або гексил. Згідно з третім аспектом R3 представляє Н. Згідно з четвертим аспектом R3 представляє ОМе. Згідно з п'ятим аспектом W представляє О. Згідно з шостим аспектом W представляє S. Термін нерозгалужений С2-7алкіл означає насичений аліфатичний вуглеводень з лінійним ланцюгом, що має від 2 до 7 атомів карбону. Приклади вказаного алкілу залучають етил, н-пропіл, нбутил, н-пентил, н-гексил та н-гептил. Фахівцям зрозуміло, що термін перерваний, який використано вище, означає, що атом оксигену розташовано всередині алкільного ланцюга, а не є кінцевим атомом. Термін "проліки", який використано у цьому описі залучає похідні карбоксильної групи, які перетворюються у ссавці, особливо людині, у карбоксильну групу або її сіль чи кон'югат. Зрозуміло, що без звернення до теорії, вважають, що більша частина активності, асоційована з проліками, обумовлена активністю сполуки формули І, у яку перетворюються проліки. Проліки можна отримати звичайними способами, доступними фахівцям. Різноманітні проліки на основі карбоксигрупи відомі у рівні техніки. Наприклад, дивись про такі похідні проліків: a) Design Prodrugs, edited by Η. Bundgaard, (Elsevier, 1985) та Methods in Enzymology. 42: 309 5 766276 396, edited by K. Widder, et d. (Academic Press, 2-оксоетокси}феніл)етокси]бензойна кислота; 1985); 2-[2-(4-{2-[бензил(етил)аміно]-2b) A Textbook of Drug Design and Development, оксоетокси}феніл)етокси]бензойна кислота; або edited by Krogsgaard-Larsen та Н. Bundgaard, 2-[2-(4-{2-[етил(4-флуорбензил)аміно]-2Chapter 5 "Design and Application of Prodrugs", by оксоетокси}феніл)етокси]бензойна кислота; H. Bundgaard p.113-191 (1991); Також зрозуміло, що деякі сполуки представc) Н. Bundgaard, Advanced Drug Delivery леного винаходу можуть бути сольватованими, а Reviews, 8; 1-38 (1992); також несольватованими. Зрозуміло, що предстаd) H. Bundgaard, et al, Journal of Pharmaceutical влений винахід стосується усіх таких сольватів. Sciences, 77:285 (1988); та Деяк сполуки представленого винаходу можуть e) N. Kakeya, et al., Chem Pharm Bull, 32:692 бути таутомерами. Зрозуміло, що представлений (1984). винахід стосується усіх таких таутомерів. Вищенаведені документи а-e уведені як посиВ описі та доданій формулі винаходу, хімічна лання. формула або назва залучає усі стерео та оптичні Розщепювані in vivo естери є як раз одним тиізомери та їх рацемати, а також суміші окремих пом проліків вихідної молекули. енантіомерів у різних пропорціях, коли такі ізомери Сполуки формули І мають активність, як медита енантіомери існують, а також їх фармацевтично каменти, зокрема, сполуки формули І є селективприйнятні солі. Ізомери можна розділяти, застосовуючи звичайні способи, наприклад, хроматограними агоністами АППР , їх ЕК50 для АППР є прифією або фракційною кристалізацією. Енантіомери наймні у чотири рази нижче, а переважно можна виділяти розділенням рацемату, наприпринаймні у 10 або 50 разів нижче їх відповідних клад, фракційною кристалізацією, розділенням або ЕК50 для ΑΠΠΡ , де ЕК50 виміряно та розраховано, ВЕРХ. Діастереомери можна виділяти розділеняк описано у дослідженнях подалі у цьому докуменям ізомерних сумішей, наприклад, фракційною нті. Сполуки формули І є потужними та селективкристалізацією, ВЕРХ або флеш-хроматографією. ними. Альтернативно стереоізомери можна отримувати Представлений винахід стосується сполук, вихіральним синтезом з хіральних вихідних матеріабраних з групи: лів в умовах, які не викликатимуть рацемізації або 2[2-(4-{2-[етил(2-флуорбензил)аміно]-2епімеризації, або дериватизацією хіральним реаоксоетокси}феніл)етокси]бензойна кислота; гентом. Усі стереоізомери залучено в рамки вина2-[2-(4-{2-[(2,4-дифлуорбензил)(гептил)аміно]ходу. 2-оксоетокси}-3-метоксифеніл)-етокси]бензойна Способи отримання кислота; Сполуки винаходу можна отримати, як нижче2-[2-(4-{2-[(4-хлорбензил)(етил)аміно]-2наведено. Однак, винахід не обмежено цими спооксоетокси}феніл)етилтіо]бензойна кислота; собами, сполуки можна також отримати, як описа2-[2-(4-{2-[(4-хлорбензил)(етил)аміно]-2но для структурно споріднених сполук у сучасному оксоетокси}феніл)етокси]бензойна кислота; рівні техніки Реакції можна проводити стандарт2-[2-(4-{2-[етил(4ними способами, або як описано в експериментатрифлуорметилбензил)аміно]-2льному розділі. оксоетокси}феніл)етокси]бензойна кислота; Сполуки формули І можна отримати реакцією 2-[2-(4-{2-[етил(4сполуки формули II трифлуорметилбензил)аміно]-2оксоетокси}феніл)етилтіо]бензойна кислота; 2-{2-[4-(2-{бутил[2-флуор-4(трифлуорметил)бензил]аміно}-2оксоетокси)феніл]-етокси}бензойна кислота; 2-[2-(4-{2-[(2,4-дифлуорбензил)(пропіл)аміно]2-оксоетокси}феніл)етокси]бензойна кислота; 2-[2-(4-{2-[бензил(етил)аміно]-2оксоетокси}феніл)етокси]бензойна кислота; в якій R1, R2, R3, W та n визначено раніше, a 2-{[2-(4-{2-[бензил(етил)аміно]-2PG представляє захисну групу для карбоксильного оксоетокси}феніл)етил]тіо}бензойна кислота; гідроксилу, яку описано у довіднику ["Protective 2-[2-(4-{2-[(4-трет-бутилбензил)(етил)аміно]-2Group in Organic Synthesis", 2 Edition (1991) by оксоетокси}феніл)етокси]бензойна кислота; Greene та Wuts], із засобом зняття захисту. Захис2-[2-(4-{2-[етил(4-флуорбензил)аміно]-2ною групою може також бути смола, як-то смола оксоетокси}феніл)етокси]бензойна кислота; Ванга або 2-хлортритилхлоридна смола. Захисні 2-{[2-(4-{2-[етил(2-флуорбензил)аміно]-2групи можна видаляти способами, які добре відомі оксоетокси}феніл)етил]тіо}бензойна кислота; або фахівцям. Одною такою є захисна група, де PG 2-{[2-(4-{2-[(2-хлорбензил)(етил)аміно]-2представляє С1-6алкоксил або арилалкоксил, наоксоетокси}феніл)етил]тіо}бензойна кислота та приклад, бензил, так що COPG представляє естер. їх фармацевтично прийнятні солі. Такі естери можуть реагувати з гідролізувальним Особливо сполуку вибрано з групи: засобом, наприклад, літій гідроксидом у присутно2-[2-(4-{2-[етил(2-флуорбензил)аміно]-2сті розчиннику, наприклад, суміші ТГФ та води або оксоетокси}феніл)етокси]бензойна кислота; калій гідроксидом у С1-3спирті, наприклад, метано2-[2-(4-{2-[(4-хлорбензил)(етил)аміно]-2лі, при температурі у межах 0-200°С або мікрохвиоксоетокси}феніл)етилтіо]бензойна кислота; льовим опроміненням, з утворенням сполуки фор2-[2-(4-{2-[(2,4-дифлуорбензил)(пропіл)аміно] 7 76627 8 мули І. етапи способу можна здійснювати у різній посліСполуки формули II можна отримати реакцією довності, та/або конкретні реакції можна здійснюсполуки формули III вати на різних етапах загального шляху (тобто хімічні трансформації можна здійснювати з інтермедіатами, відмінними від асоційованих з вищенаведеними конкретними реакціями). У будь-якому з попередніх способів отримання, де необхідно, гідрокси, аміно або інші реакційні групи можна захистити, застосовуючи захисну групу RP, яку описано у довіднику ["Protective Group in 1 або її солі, наприклад, гідрохлориду, в якій R , Organic Synthesis", 2 Edition (1991) by Greene та R2 та n визначено раніше, зі сполукою формули IV Wuts]. Захисною групою може також бути смола, як-то смола Ванга або 2-хлортритилхлоридна смола. Захист та зняття захисту з функціональних груп можна здійснювати до або після будь-якого з реакційних етапів, описаних вище. Захисні групи можна видаляти способами, які добре відомі фахівцям. Вираз "інертний розчинник" стосується розчиннику, як не реагує з вихідними матеріалами, 3 або її хлорангідридом, в яких R , W та PG виреактивами, інтермедіатами або продуктами спозначено раніше в інертному розчиннику, наприсобом, який шкідливо впливає на вихід потрібного клад, дихлорметані, як варіант, у присутності запродукту. собу сполучення, наприклад, 4Фармацевтичні препарати диметиламінопіридину або 1-етил-3-(3Сполуки винаходу звичайно застосовуватидиметиламінопропіл)карбодіімід гідрохлориду, при муть перорально, парентерально, внутрішньовентемпературі у межах -25°С до 150°С. но, внутрішньом'язово, підшкірно або іншими приСполуки формули n можна також отримати датними для ін'єкції шляхами, букально, реакцією сполуки формули V ректально, вагінапьно, трансдермально та/або назально, та/або інгаляціями, у формі фармацевтичних препаратів, що містять активний інгредієнт як вільну кислоту або фармацевтично прийнятну сіль у фармацевтично прийнятній дозованій формі. Залежно від розладу та пацієнта, якого лікують, та шляху застосування, композиції можна застосовувати у різних дозах. Придатні добові дози сполук винаходу у терав якій PG визначено раніше, зі сполукою форпевтичному лікуванні людей є приблизно 0,0001мули VI 100мг/кг маси тіла, переважно 0,001-10мг/кг маси тіла. Пероральні композиції є кращими, особливо таблетки або капсули, які можна формувати способами, відомими фахівцям для забезпечення дози активної сполуки у межах 0,5мг до 500мг, наприклад, 1мг, 3мг, 5мг, 10мг, 25мг, 50мг, 100мг та 250мг. в якій R, R2, R3, W та n визначено раніше, a L Згідно з наступним аспектом винаходу запропредставляє відщеплювану групу, наприклад, мепоновано фармацевтичну композицію, що містить тилсульфонілокси або галоген, наприклад, бром, будь-яку сполуку винаходу, або її фармацевтично як варіант, у присутності розчиннику, наприклад, прийнятну сіль, у суміші з фармацевтично прийняацетонітрилу, та, як варіант, у присутності основи, тними ад'ювантами, розріджувачами та/або носінаприклад, калій карбонату, при температурі у ями. межах 0-150°С. Фармакологічні властивості Сполуки формул III, IV, V та VI можна отримаПредставлені сполуки формули (І) є кориснити способами, описаними у прикладах або аналоми для профілактики та/або лікування клінічних гічними способами, відомими фахівцям. станів, асоційованих з притаманною чи індуковаСполуки формули II, III, IV та V є корисними інною зменшеною чутливістю до інсуліну (резистентермедіатами при отриманні сполук формули І. тністю до інсуліну) та асоційованими розладами Деякі з цих сполук, можна вважати, є новими. Нові метаболізму (також відомими, як метаболічний сполуки формули II, або формули III, або формули синдром). Ці клінічні стани залучають, але без обIV або формули V заявлені, як наступний аспект меження, загальне ожиріння, абдомінальне ожипредставленого винаходу. ріння, артеріальну гіпертензію, гіперінсулінемію, Сполуки винаходу можна виділяти з їх реакгіперглікемію, діабет типу 2 та дисліпідемію, що ційної суміші, застосовуючи звичайні способи. характеристично проявляються резистентністю до Фахівцям зрозуміло, що для отримання сполуінсуліну. Ця дисліпідемія, також відома, як атероки винаходу альтернативним, а у деяких випадках, генічний профіль ліпопротеїну, охарактеризована більш зручним способом, вищезазначені конкретні 9 76627 10 помірно підвищеними неестерифікованими жиртерапевтичним засобом, що є корисним у лікуванні ними кислотами, підвищеними збагаченими трирозладів, асоційованих з розвитком та прогресом гліцеридами частинками ліпопротеїну дуже низької атеросклерозу, як-то гіпертензії, гіперліпідемії, густини (ЛДНГ), високими рівнями Аро В, низькими дисліпідемії, діабету та ожиріння. Сполуки винахорівнями ліпопротеїну високої густини (ЛВГ), асоціду можна комбінувати з іншим терапевтичним зайованими з низькими рівнями частинок ароАІ та собом, що зменшує співвідношення ЛНГ:ЛВГ або високими рівнями Аро В у присутності невеликих, засобом, що викликає зменшення циркуляційних щільних частинок ліпопротеїнів низької густини рівнів ЛНГ-холестерину. У пацієнтів з цукровим (ЛНГ), фенотипу В. діабетом сполуки винаходу можна також комбінуСполуки представленого винаходу, як очікувати з терапевтичними засобами, використовувають, є корисними у лікуванні пацієнтів з комбіноними для лікування ускладнень, споріднених з ваними або змішаними гіперліпідеміями або різмікро-ангіопатіями. номанітними ступенями гіпертригліцеридемій та Сполуки винаходу можна використовувати попісляобідньої дисліпідемії з іншими виявами метаруч з іншими терапіями для лікування метаболічболічного синдрому або без них. ного синдрому або діабету типу 2 та асоційованих Лікування представленими сполуками, як очіз ними ускладнень, що залучають бігуанідні ліки, кують, знижуватиме серцево-судинну захворюванаприклад, метформін, фенформін та буформін, ність та смертність, асоційовані з атеросклерозом інсулін (синтетичні аналоги інсуліну, амілін) та певнаслідок їх антидисліпідеічних, а також антизапароральні антигіпергліцемічні засоби (які поділяють льних властивості. Стани серцево-судинних хвона регулятори глюкози з їжі та інгібітори альфароб залучають макро-ангіопатії різноманітних внуглюкозтдази). Прикладом інгібітору альфатрішніх органів, що спричиняють інфаркт міокарду, глюкозтдази є акарбоз або воглібоз або міглітол. застійну серцеву недостатність, цереброваскулярПрикладом регулятору глюкози з їжі є репаглінід ну хворобу та периферійну артеріальну недостатабо натеглінід. ність нижніх кінцівок. Внаслідок їх ефекту сенсибіЗгідно з іншим аспектом винаходу, сполуку лізування стосовно інсуліну сполуки формули І, як формули І або її фармацевтично прийнятну сіль, очікують, також попереджуватимуть та затримувасольват, сольват такої солі або її проліки, можна тимуть розвиток діабету типу 2 від метаболічного застосовувати в асоціації з іншим АППРсиндрому та діабету вагітних. Відтак розвиток довмодулювальним засобом. АППР-модулювальні готермінових ускладнень, асоційованих з хронічзасоби залучають, але без обмеження агоніст ною гіперглікемією при цукровому діабеті, як-то АППР-альфа та/або гама та /або дельта, або його мікро-ангіопатії, що спричиняють хворобу нирок, фармацевтично прийнятні солі, сольвати, сольвапошкодження сітчатки та, як очікують, затримувати таких солей або проліки. Придатні агоністи тимуть хворобу периферійних судин нижніх кінціАППР альфа та/або гама, їх фармацевтично привок. Крім того сполуки можуть бути корисними у йнятні солі, сольвати, сольвати таких солей або лікуванні різноманітних станів поза серцевопролі-ків, відомі у рівні техніки. Вони залучають судинною системою, асоційованих або ні з резиссполуки, описані у [WO 01/12187, WO 01/12612, тентністю до інсуліну, типу синдрому полікістозноWO 99/62870, WO 99/62872, WO 99/62871, WO го яєчнику, ожиріння, раку та станів запальної хво98/57941, WO 01/40170, J Med Chem, 1996,39, 665, роби, залучаючи нейродегенеративні розлади, якExpert Opinion on Therapeutic Patents, 10 (5), 623то помірні когнитивні порушення, хвороба Альц634 (зокрема, сполуки, описані у патентній заявці геймера, хвороба Паркінсона та розсіяний склена стор.634) та J Med Chem, 2000, 43, 527, що роз. уведені як посилання]. Особливо агоніст АППР Сполуки представленого винаходу, як очікуальфа та/або гама стосується BMS 298585, клофіють, є корисними у регулюванні рівнів глюкози у брату, фенофібрату, безафібрату, гемфіброзилу потерпаючих від діабету типу 2 пацієнтів. та ципрофібрату; GW9578, піоглітазону, розигПредставлений винахід стосується способу лілітазону, ривоглітазону, балаглітазону, KRP-297, кування або попередження дисліпідемій, синдрому JTT-501, SB 213068, GW1929, GW 7845, GW 0207, резистентності до інсуліну та/або розладів метаL-796449, L-165041 та GW 2433. Особливо агоніст болізму (які визначено вище), що залучає застосуАППР альфа та/або гама стосується (S)-2-етоксивання сполуки формули І до ссавця (особливо 3-[4-(2-{4-метансульфонілоксилюдини), що цього потребує. феніл}етокси)феніл]пропанової кислоти та її фарПредставлений винахід стосується способу лімацевтично прийнятних солей. кування або попередження діабету типу 2, що заНа додаток комбінацію винаходу можна виколучає застосування ефективної кількості сполуки ристовувати у сполученні з сульфоніл-сечовиною, формули І до ссавця (особливо людини), що цього як-то глімепірид, глібенкламід (глімідин), гліклазид, потребує. гліпізид, гліхідон, хлорпропамід, толбутамід, ацеЗгідно з наступним аспектом представлений тогексамід, глісопірамід, карбутамід, глібонурид, винахід стосується застосування сполуки формули глізоксепід, глібутіазол, глібузол, глігексамід, гліміІ, як медикаменту. дин, гліпінамід, фенбутамід, толциламід та толаЗгідно з наступним аспектом представлений замід. Переважно сульфонілсечовиною є глімепівинахід стосується застосування сполуки формули рид або глібенкпамід (глімідин). Більше переважно І у виробництві медикаменту для лікування резиссульфонілсечовиною є глімепірид. Відтак предстатентності до інсуліну та/або розладів метаболізму. влений винахід стосується застосування сполуки Комбінаційна терапія представленого винаходу у сполученні з одним, Сполуки винаходу можна комбінувати з іншим двома або більше існуючими терапіями, описани 11 76627 12 ми у цьому розділі. Дози інших існуючих терапій 01/68637, WO 01/68096, WO 02/08211, WO для лікування діабету типу 2 та асоційованих з 00/38725, WO 00/38726, WO 00/38727, WO ними ускладнень відомі фахівцям та затверджені 00/38728, WO 00/38729, DB 19825804, JP для застосування регуляторними органами, на10072371, US 5070103, EP 251315, EP 417725, EP приклад, FDA та можуть бути знайденими у 489423, EP 549967, EP 573848, EP 624593, EP Orange Book, опублікованою FDA Альтернативно 624594, EP 624595, EP 869121, EP 864582, та ЕР менші дози можна використовувати, як результат 1070703, зміст цих патентних заявок, особливо корисності завдяки комбінації. Представлений висполук, описаних у п.1 та названих прикладах, нахід також стосується сполук представленого уведено як посилання. винаходу у комбінації із засобом зниження холесОсобливими класами інгібіторів ТККЖК, притерину. Засоби зниження холестерину стосовно датних для застосування згідно з представленим цієї заявки залучають, але без обмеження, інгібівинаходом, є бензотієпіни та сполуки, описані у тори редуктази HMG-CoA (3-гідрокси-3формулах винаходів, особливо п.1 WO 00/01687, метилглутарил-кофермент редуктази А). ВідповідWO 96/08484 та WO 97/33882, що уведені як посино інгібітором редуктази HMG-CoA є статин, виблання. Іншими придатними класами інгібіторів раний з групи, що складається з аторвастатину, ТККЖК є 1,2-бензотіазепіни, 1,4-бензотіазепіни та бервастатину, церивастатину, далвастатину, флу1,5-бензотіазепіни. Наступним придатним класом вастатину, ітавастатину, ловастатину, мевастатиінгібіторів ТККЖК є 1,2,5-бензотіадіазепіни. ну, нікостатину, нівастатину, правастатину та симОдною особливо придатною сполукою, що вивастатину, або їх фармацевтично прийнятної солі, являє інгібіторну активність стосовно ТККЖК є особливо натрію або кальцію, або сольвату, або (3R,5R)-3-бутил-3-етил-1,1-діоксидо-5-фенілсольвату такої солі. Особливим статином є атор2,3,4,5-тетрагідро-1,4-бензотіазепін-8-іл (3-Dвастатин, або його фармацевтично прийнятні сіль, глюкопіранозидуронова кислота (ЕР 864582). Інші сольват, сольват такої солі або проліки. Ще більпридатні інгібітори ТККЖК залучають один з групи: ше особливим статином є сіль аторвастатину і 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8кальцію. Особливо кращим статинм є, однак, спо(N-{(R)-1'-феніл-1'-[N'лука з хімічною назвою (Е)-7-[4-(4-флуорфеніл)-6(карбоксимеізопропіл-2-[метил(метилсульфоніл)-аміно]тил)карбамоїл]метил}карбамоїлметокси)-2,3,4,5пірімідин-5-іл](3R,5S)-3,5-дигідроксигепт-6-енова тетрагідро-1,5-бензотіазепін; кислота, [також відома як (Е)-7-[4-(4-флуорфеніл)1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-86-ізопропіл-2-[N-метил-N-(метилсульфоніл)-аміно](N-{(R)- -[N'-(карбоксиметил)карбамоїл]-4пірімідин-5-іл](3R,5S)-3,5-дигідроксигепт-6-енова гідроксибензил}карбамоїлметокси)-2,3,4,5кислота] або її фармацевтично прийнятна сіль або тетрагідро-1,5-бензотіазепін; сольват, або сольват такої солі. Сполуку (Е)-7-[41,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(4-флуорфеніл)-6-ізопропіл-2-[метил(N-{(R)-1'-феніл-1'-(N'-(2(метилсульфоніл)-аміно]-пірімідин-5-іл](3R,5S)-3,5сульфоетил)карбамоїл]метил]карбамоїлметокси)дигідроксигепт-6-енова кислота та її солі кальцію 2,3,4,5-тетрагідро-1,5-бензотіазепін; та натрію розкрито у Європейській патентній заяв1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіоці, публікація №ЕР-А-0521471, та у Bioorganic та 8-(N-{(R)-1'-феніл-1'-[N'-(2Medicinal Chemistry, (1997), 5(2), 437-444. Цей сульфоетил)карбамоїл]метил}карбамоїлметокси)останній статин є зараз відомим під загальною 2,3,4,5-тетрагідро-1,5-бензотіазепін; назвою розувастатин. 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8У представленій заявці термін "засіб зниження (N-{(R)- -[N-(2-сульфоетил)карбамоїл]-4холестерину" також залучає хімічні модифікації гідроксибензил}карбамоїлметокси)-2,3,4,5інгібіторів HMG-CoA-редуктази, як-то естери, протетрагідро-1,5-бензотіазепін; ліки та метаболіти, активні або неактивні. 1,1-дюксо-3-бутил-3-етил-5-феніл-7-метилтіоПредставлений винахід також стосується спо8-(N-{(R)- -[N'-(2-сульфоетил)карбамоїл]-4лук представленого винаходу у комбінації з комгідроксибензил}карбамоїлметокси)-2,3,4,5плексотвірною сполукою жовчної кислоти, напритетрагідро-1,5-бензотіазепін; клад, холестипол або холестирамін або 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіохолестагель. 8-(N-{(R)- -[N'-(2Представлений винахід також стосується спокарбоксіелуки представленого винаходу у комбінації з інгібітил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5тором транспортної системи клубово-кишкових тетрагідро-1,5-бензотіазепін; жовчних кислот (інгібітор ТККЖК). 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8Придатні сполуки, що виявляють інгібіторну (N-{(R)- -[N'-(2-карбоксиетил)карбамоїл]-4активність стосовно ТККЖК, описано, дивись, нагідроксибензил}карбамотметокси)-2,3,4,5приклад, сполуки, описані у WO 93/16055, WO тетрагідро-1,5-бензотіазепін; 94/18183, WO 94/18184, WO 94/24087, WO 1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо96/05188, WO 96/08484, WO 96/16051, WO 8-(N-{(R)- -[N'-(597/33882, WO 98/07749, WO 98/38182, WO карбоксипен98/40375, WO 98/56757, WO 99/32478, WO тил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,599/35135, WO 99/64409, WO 99/64410, WO тетрагідро-1,5-бензотіазепін; 00/01687, WO 00/20392, WO 00/20393, WO 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-800/20410, WO 00/20437, WO 01/34570, WO (N-{(R)- -[N'-(200/35889, WO 00/47568, WO 00/61568, WO карбоксіе 13 76627 14 тил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8тетрагідро-1,5-бензотіазепін; (N-{(R)- -[N-((S)-1-карбокси-2-(R)1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8гідроксипропіл)карбамоїл]-4(N-( -[N'-(2-сульфоетил)карбамоїл]-2гідроксибензил}карбамоїлметокси)-2,3,4,5флуорбензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-81,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо(N-{(R)- -[N-((S)-1-карбокси-28-(N-{(R)- -[N'-(R)-(2-гідрокси-1метилпропіл)карбамоїл]-4карбоксіегідроксибензил}карбамоїлметокси)-2,3,4,5тил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,2,5-бензотіадіазепін; тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-81,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8(N-{(R)- -[N-((S)-1-карбоксибутил)карбамоїл]-4(N-{(R)- -[N'-(R)-(2-гідрокси-1гідроксибензил}карбамоїлметокси)-2,3,4,5карбоксіететрагідро-1,2,5-бензотіадіазепін; тил)карбамоїл]бензил}карбамоїл]метокси)-2,3,4,51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8тетрагідро-1,5-бензотіазепін; (N-{(R)- -[N-((S)-11,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8карбоксипро(N-{(R)- -[N'-(R)-1-[N"-(R)-(2-гідрокси-1піл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5карбоксіетил)карбамоїл]-2тетрагідро-1,2,5-бензотіадіазепін; гідроксіетил}карбамоїл)бензил]карбамоїлметокси}1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-82,3,4,5-тетрагідро-1,5-бензотіазепін; (N-{(R)- -[N-((3)-11,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіокарбоксіе8-(N-{(R)- -[N'-(R)тил)карбамоїл]бензил)карбамоїлметокси)-2,3,4,5(карбоксимететрагідро-1,2,5-бензотіадіазепін; тил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8тетрагідро-1,5-бензотіазепін; (N-{(R)- -[N-((S)-1-карбокси-2-(R)1,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіогідроксипро8-(N-{(R)- -[N'-(R)-((етокси)(метил)фосфорилпіл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5метил)карбамоїл]бензил}карбамоїлметокси)тетрагідро-1,2,5-бензотіадіазепін; 2,3,4,5-тетрагідро-1,5-бензотіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-81,1-діоксо-3-бутил-3-етил-5-феніл-7-метилтіо(N-{(R)- -[N-(2-сульфоетил)карбамоїл]-48-{N-[(R)- -[N'-(R)-{2гідроксибензил}карбамоїлметокси)-2,3,4,5[(гідроктетрагідро-1,2,5-бензотіадіазепін; си)(метил)фосфорил]етил}карбамоїл)бензил]карб 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8амоїлметокси}-2,3,4,5-тетрагідро-1,5(N-{(R)- -[N-((S)-1-карбоксіетил)карбамоїл]-4бензотіазепін; гідроксибензил}карбамоїлметокси)-2,3,4,51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8тетрагідро-1,2,5-бензотіадіазепін; (N-{(R)- -[N'-(2-метилтіо-11,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8карбоксіе(N-{(R)- -[N-((R)-1-карбокси-2тил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5метилтіоететрагідро-1,5-бензотіазепін; тил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8тетрагідро-1,2,5-бензотіадіазепін; (N-{(R)- -[N'-{21,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8[(метил)(етил)фосфорил]етил}карбамоїл)-4(N-{(R)- -[N-((S)-1-[N-((S)-2-гідрокси-1гідроксибензил]карбамоїлметокси}-2,3,4,5карбоксіететрагідро-1,5-бензотіазепін; тил)карбамоїл]пропіл}карбамоїл]бензил}карбамоїл 1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8метокси)-2,3,4,5-тетрагідро-1,2,5-бензотіадіазепін; (N-{(R)- -[N'-{21,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8[(метил)(гідрокси)фосфорил]етил}карбамоїл)-4(N-{(R)- -[N-((S)-1-карбокси-2гідроксибензил]карбамоїлметокси}-2,3,4,5метилпротетрагідро-1,5-бензотіазепін; піл)карбамоїл]бензил}карбамоїлметокси)-2,3,4,51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8тетрагідро-1,2,5-бензотіадіазепін; (N-{(R)- -[N'-(2-метилсульфініл-11,1-Діоксо-3,3-дибутил-5-феніл-7-метилтіо-8карбоксіе(N-{(R)- -[N-((S)-1-карбоксипропіл)карбамоїл]-4тил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5гідроксибензил}карбамоїлметокси)-2,3,4,5тетрагідро-1,5-бензотіазепін; тетрагідро-1,2,5-бензотіадіазепін; 1,1-діоксо-3,3-дибутил-5-феніл-7-метокси-8-(N1,1-Діоксо-3,3-дибутил-5-феніл-7-метилтіо-8{(R)- -[N'-(2-сульфоетил)карбамоїл]-4[N-((R,S)- -{N-[1-(R)-2-(S)-1-гідрокси-1-(3,4гідроксибензил}карбамоїлметокси)-2,3,4,5дигідроксифеніл)проп-2-іл]карбамоїл}-4тетрагідро-1,5-бензотіазепін; гідроксибензил)карбамоїлметокси]-2,3,4,51,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8тетрагідро-1,2,5-бензотіадіазепін; (N-{(R)- -[N'-1-карбокси-21,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8метилтіоетил)карбамоїл]-4(N-{(R)- -[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6гідроксибензил}карбамоїлметокси)-2,3,4,5пентагідроксигексил)карбамоїл]-4тетрагідро-1,2,5-бензотіадіазепін; гідроксибензил}карбамоїлметокси)-2,3,4,5 15 76627 16 тетрагідро-1,2,5-бензотіадіазепін; та лорид, беназеприлат, бензоїлкаптоприл, каптоп1,1-діоксо-3,3-дибутил-5-феніл-7-метилтіо-8рил, каптоприл-цистеїн, каптоприл-глутатіон, церанаприл, цераноприл, церонаприл, цилазаприл, (N-{(R)- -[N-(2-(S)-3-(R)-4-(R)-5-(R)-2,3,4,5,6цилазаприлат, делаприл, делаприл-діацид, енапентагідроксигеклаприл, еналаприлат, енаприл, епікаптоприл, фосил)карбамоїл]бензил}карбамоїлметокси)-2,3,4,5роксимітин, фосфеноприл, фосеноприл, фосеноптетрагідро-1,2,5-бензотіадіазепін; рил натрій, фосиноприл, фосиноприл натрій, або його фармацевтично прийнятну сіль, софосиноприлат, фосиноприлова кислота, глікопльват, сольват такої солі або проліки. рил, геморфін-4, ідраприл, імідаприл, індолаприл, Згідно з додатковим аспектом представленого індолаприлат, лібензаприл, лізиноприл, ліціумін А, винаходу запропоновано комбінаційне лікування, ліціумін В, міксанприл, моексиприл, моексиприлат, що залучає застосування ефективної кількості мовелітиприл, мурацеїн А, мурацеїн В, мурацеїн сполуки формули І або її фармацевтично прийнятС, пентоприл, периндоприл, періадоприлат, піваної солі, сольвату, сольвату такої солі або проліків, лоприл, півоприл, хінаприл, хінаприл гідрохлорид, як варіант, разом з фармацевтично прийнятним хінаприлат, раміприл, раміприлат, спіраприл, спірозріджувачем або носієм, з одночасним, послідораприл гідрохлорид, спіраприлат, спіроприл, співним або окремим застосуванням одного або біроприл гідрохлорид, темокаприл, темокаприл гідльше з наступних засобів, вибраних з групи рохлорид, тепротид, трандолаприл, інгібітор БПХЕ (білок переносу холестериловотрандолаприлат, утибаприл, забіциприл, забіципго естеру), наприклад, описаний у WO 00/38725 рилат, зофеноприл та зофеноприлат. Кращими стор.7 стр.22-стор.10, стр.17, що уведено як посиінгібіторами АКФ для застосування згідно з предлання; ставленим винаходом є раміприл, раміприлат, антагоніст поглинання холестерину, наприлізиноприл, еналаприл та еналаприлат. Ще краклад, азетидинони, як-то SCH 58235 та описані у щими АКФ інгібіторами для застосування згідно з US 5767115, які уведені як посилання; представленим винаходом є раміприл та раміприінгібітор БМП (білок мікросомального перенолат. су), наприклад, описаний у Science, 282, 751-54, Кращі антагоністи ангіотензину II, їх фармаце1998, що уведено як посилання; втично прийнятні солі, сольвати, сольвати таких похідне нікотинової кислоти, залучаючи продусолей або проліки для застосування у комбінації зі кти з уповільненим вивільненням та комбінації, сполукою формули І залучають, але без обмеженнаприклад, нікотинову кислоту (ніацин), аципімокс ня, сполуки: кандесартан, кандесартан цилексета ніцеритрол; фітостеринову сполуку, наприклад, тил, лосартан, валсартан, ірбесартан, тасосартан, етаноли; пробукол; селмісартан та епроартан. Особливо кращими сполука проти ожиріння, наприклад, орлістат антагоністами ангіотензину II або їх фармацевтич(ЕР 129,748) та сибутрамін (GB 2184122 та US но прийнятними похідними для застосування згід4929629); омега-3 жирна кислота, наприклад, но з представленим винаходом є кандесартан та Omacor ; кандесартан цилексетил. антигіпертензивна сполука, наприклад, інгібіВідтак згідно з додатковою особливістю винатор ангіотензин-конвертувального ферменту ходу, запропоновано спосіб лікування діабету типу (АКФ), антагоніст рецептору ангіотензину II, адре2 та асоційованих з ним ускладнень у теплокровнергічний блокатор, альфа адренергічний блоканих тварин, як-то людини, що потребують такого тор, бета адренергічний блокатор, наприклад, метерапевтичного лікування, який залучає застосутопролол, змішаний альфа/бета адренергічний вання до вказаної тварини ефективної кількості блокатор, адренергічний стимулятор, блокатор сполуки формули І, або її фармацевтично прийняканалу кальцію, блокатор АТ-1, салуретик, діуретної солі, сольвату, сольвату такої солі або пролітик або судинорозширювач; ків при одночасному, послідовному або окремому антагоніст або інверсивний агоніст СВ1, назастосуванні з ефективною кількістю одної іншої приклад, який описано у WO 01/70700 та ЕР сполуки, описаної тут, або фармацевтично прийн65635; ятної солі, сольвату, сольвату такої солі або проліаспірин; ків. антагоніст меланін-концентруючого гормону Відтак згідно з додатковою особливістю вина(МКГ); інгібітор PDK, або ходу, запропоновано спосіб лікування гіперліпідемодулятори ядерних рецепторів, наприклад, мічних станів у теплокровних тварин, як-то людиLXR, FXR, RXR, та ROR-альфа; або ни, що потребує такого терапевтичного лікування, їх фармацевтично прийнятні солей, сольватів, як залучає застосування до вказаної тварини ефесольватів таких солей або проліків, як варіант, ктивної кількості сполуки формули І, або її фармаразом з фармацевтично прийнятним розріджувацевтично прийнятної солі, сольвату, сольвату тачем або носієм, до теплокровної тварини, як-то кої солі або проліків при одночасному, людини, що потребує такого терапевтичного лікупослідовному або окремому застосуванні з ефеквання. тивною кількістю одної іншої сполуки, описаної тут, Особливі інгібітори АКФ або їх фармацевтично або її фармацевтично прийнятної солі, сольвату, прийнятні солі, сольвати, сольвати таких солей сольвату такої солі або проліків. або проліки, залучаючи активні метаболіти, які Згідно з наступним аспектом винаходу запроможна використовувати у комбінації зі сполукою поновано фармацевтичну композицію, як містить формули І, залучають, але без обмеження, такі сполуку формули І або її фармацевтично прийнятсполуки: алацеприл, алатриоприл, алтіоприл кану сіль, сольват, сольват такої солі або проліки, та льцію, анковенін, беназеприл, беназеприл гідрох 17 76627 18 одну іншу сполуку, описану тут, або її фармацевносієм до теплокровної тварини, як-то людини, що тично прийнятну сіль, сольват, сольват такої солі потребує такого терапевтичного лікування або проліки, в асоціації з фармацевтично прийнятРобочі приклади 1 ним розріджувачем або носієм. Н ЯМР та 13С ЯМР Виміри здійснюють на спеЗгідно з наступним аспектом представленого ктрометрах Varian Mercury 300 або Varian UNITY 1 винаходу запропоновано комплект, що містить plus 400, 500 або 600, працюючи при частотах Н сполуку формули І або її фармацевтично прийнят300, 400, 500 та 600МГц, відповідно, та при частону сіль, сольват, сольват такої солі або проліки, та тах 13С 75, 100, 125 та 150МГц, відповідно. Виміри одну іншу сполуку, описану тут, або її фармацевроблять на дельта-шкалі ( ). тично прийнятну сіль, сольват, сольват такої солі Якщо не вказано інше, хімічні зсуви представабо проліки. лено у млн.-1 з розчинником як внутрішнім стандаЗгідно з наступним аспектом представленого ртом. винаходу запропоновано комплект, що містить: Скорочення a) сполуку формули І або її фармацевтично СРІ синдром резистентності до інсуліну прийнятну сіль, сольват, сольват такої солі або ТШХ тонко-шарова хроматографія проліки, у першій одиничній дозованій формі; НОВТ 1 -гідроксибензотриазол-гідрат b) одну іншу сполуку, описану тут, або її фарDIB АН діізобутилалюміній гідрид мацевтично прийнятну сіль, сольват, сольват такої ДМСО диметилсульфоксид солі або проліки; у другій одиничній дозованій фоEtOAc етилацетат рмі; та DMF Ν,Ν-диметилформамід c) контейнер, що містить вказані першу та друТГФ тетрагідрофуран гу дозовані форми. ВЕРХ високоефективна рідинна хроматограЗгідно з наступним аспектом представленого фія винаходу запропоновано комплект, що містить: MeCN ацетонітрил a) сполуку формули І або її фармацевтично ТФОК трифлуороцтова кислота прийнятну сіль, сольват, сольват такої солі або Pd/C паладій на вугіллі проліки, разом з фармацевтично прийнятним розHATU O-(7-аzабензотриазоліл-1-іл)-N,N,N\N'ріджувачем або носієм, у першій одиничній дозотетраметилуроній гексафлуорфосфат ваній формі; ДХМ дихлорметан b) одної іншої сполуки, описаної тут, або її фаTBTU О-(бензотриазол-1-іл)-N,N,N',N'рмацевтично прийнятної солі, сольвату, сольвату тетраметилуронійтетрафлуорборат такої солі або проліків, у другій одиничній дозоваDIPEA Ν,Ν-діізопропілетиламін ній формі; та DMAP 4-диметиламінопіридин c) контейнер, що містить вказані першу та друТрисамін Трис(гідроксиметил)амінометан гу дозовані форми. ISOLUTE FLASH Si - колонка з оксидом сиЗгідно з іншою особливістю винаходу запроліцію, придатним для хроматографії поновано застосування сполуки формули І, або її Борогідрид на полімерній підкладці - борогідфармацевтично прийнятної солі, сольвату, сольрид на Amberlite IRA-400 від Aldrich вату такої солі або проліків, та одної з інших споРХ-МС рідинна хроматографія - маслук, описаних тут, або її фармацевтично прийнятспектроскопія ної солі, сольвату, сольвату такої солі або проліків, t триплет у виробництві медикаменту для застосування у s синглет лікуванні метаболічного синдрому або діабету тиd дублет пу 2 та асоційованих з ними ускладнень у теплокq квартет ровних тварин, як-то людини. qvint квінтет Згідно з іншою особливістю винаходу запроm мультиплет поновано застосування сполуки формули І, або її br широкий фармацевтично прийнятної солі, сольвату, сольbs широкий синглет вату такої солі або проліків, та одної з інших споdm дублет мультиплету лук, описаних тут, або її фармацевтично прийнятbt широкий триплет ної солі, сольвату, сольвату такої солі або проліків, dd дублет дублетів у виробництві медикаменту для застосування у Приклад 1 лікуванні гіперліпідемічних станів у теплокровних a) трет-бутил [4-(2тварин, як-то людини. гідроксіетил)фенокси]ацетат Згідно з наступним аспектом представленого Суміш 4-(2-гідроксіетил)фенол (3,8мл, винаходу запропоновано комбінаційне лікування, 25,834ммоль) розчиняють у ацетонітрил (25мл), що залучає застосування ефективної кількості калій карбонат 7,085г, 51,267ммоль) та третсполуки формули І, або її фармацевтично прийнябутилбромацетат (5,000г, 25,834ммоль) кип'ятять тної солі, сольвату, сольвату такої солі або проліпід зворотним холодильником протягом 16 годин. ків, як варіант, разом з фармацевтично прийнятРозчинник випарюють під зменшеним тиском. Заним розріджувачем або носієм, з одночасним, лишок розчиняють у EtOAc та промивають розсопослідовним або окремим застосуванням ефектилом та водою, сушать сульфатом магнію та випавної кількості одної з інших сполук, описаних тут, рюють під зменшеним тиском з утворенням або її фармацевтично прийнятної солі, сольвату, потрібного продукту (6,00г, вихід 92,8%) 1 сольвату такої солі або проліків, як варіант, разом Н-ЯМР (400МГц, CDCI3): 1,52 (s, 9H), 2,98 (t, з фармацевтично прийнятним розріджувачем або 2H), 3,46 (t, 2H), 4,92 (s, 2H), 6,89-6,97 (m, 4H) 19 76627 20 b) Трет-бутил (4-(2очищають препаративною ВЕРХ (починаючи з [(метилсульфоніл)окси]етил]фенокси)ацетат суміші ацетонітрил/буфер 60/40 та тоді збільшуТрет-бутил [4-(2-гідроксіетил)фенокси]ацетат ють концентрацію ацетонітрилу до 100% ацетоніт(6,000г, 23,781ммоль) та триетиламін (9,9мл, рилу протягом 25 хвилин, буфером є суміш ацето71,341ммоль) розчиняють у ДХМ. Суміш охолонітрил/вода 10/90 та амоній ацетат (0,1М), колонка джують до -10°С та додають краплями до суміші KR-100-7-C8, 50*500, потік 80мл/хвилин). 145мг метансульфонілхлорид (2,8мл, 35,671ммоль). Репотрібного продукту отримують після сушки субліакційній суміші дають досягти кімнатної темперамацією (вихід 71,1%) 1 тури та перемішують протягом 16 годин. Суміш Н-ЯМР (400МГц, CD3CO) (ротамери); розводять ДХМ. Органічний шар промивають во1,08,1,17 (t, t, 3Н), 2,96 (s, 3Н), 3,07 (m, 2H), 3,31, дою, розсолом та 0,3Μ KHSO4, сушать сульфатом 3,36 (m, 2Н), 4,21 (m, 2Н), 4,85 (s, 2Н), 4,56-4,82 магнію, та випарюють під зменшеним тиском. (m, 2Н), 6,18 (d, 1Н), 6,88-7,06 (m, 3Н), 7,18 -7,35 Отримано 7,5г світло-жовтих кристалів (вихід (m, 6H), 7,42 (m, 1H), 7,70 (d, 1H) 95,5%). f) 2-[2-(4-(2-(етил(2-флуорбензил)аміно]-21 Н-ЯМР (490МГц, CDCI3): 1,52 (s, 9Н), 2,98 (t, оксоетокси]феніл)етокси]бензойна кислота 2Н), 3,10 (s, 3Н), 3,46 (t, 2H), 4,92 (s, 2H), 6,89-6,97 Метил 2-[2-(4-{2-[етил(2-флуорбензил)аміно](m, 4H) 2-оксоетокси}феніл)етокси]бензоат c) Метил 2-{2-[4-(2-трет-бутокси-2(0,200г, 0,115ммоль) розчиняють у 3мл ТГФ в оксоетокси)феніл]етокси)бензоат ампулі синтезатора Сміта, а тоді додають до амМетилсаліцилат (2,7мл, 21,187ммоль) розчипули 1,5мл води та літій гідроксид (0,032г, няють в ацетонітрилі, та додають калій карбонат 1,335ммоль). Ампулу закривають та переносять у (5,856г, 42,373ммоль). Суміш охолоджують до мікрохвильову шафу (синтезатор Сміта). Реакцій10°С, тоді додають трет-бутил (4-{2ну суміш тоді гріють до 150°С протягом 6 хвилин. [(метилсульфоніл)окси]етил}фенокси)ацетат. СуЗгідно з РХ-МС реакція завершується. Розчинник міш кип'ятять під зворотним холодильником протявипарюють. Залишок розчиняють у діетиловому гом 16 годин, та тоді розчинник випарюють під етері (30мл) та промивають натрій гідрокарбоназменшеним тиском. Залишок розчиняють у EtOAc, том (насичен.) (2 20мл). Основний водний шар промивають водою та розсолом, тоді органічний підкислюють до рН 1 з 2М HCL. Водний шар екстшар сушать магній сульфатом та розчинник видарагують трьома порціями по 20мл ДХМ, які поєдляють випарюванням. Сирий матеріал очищають нують, сушать та випарюють, з утворенням 160мг флеш-хроматографією (силікагель 60 0,004чистого потрібного продукту 1 0,063мм), застосовуючи EtOAc:толуол 50:50, як Н-ЯМР (400МГц, CD3CO) (ротамери)-, елюент. Фракції, як містять потрібний продукт по1,07,1,15 (t, t, 3Н), 3,10 (m, 2H), 3,30,3,36 (m, m, єднують, та розчинник випарюють. Це дає 5,0г 2H), 4,21 (m, 2H), 4,55-4,67 (m, 2H), 4,90 (s, 2H), чистого продукту (вихід 61,1%). 1Н-ЯМР (400МГц, 6,20 (d, 1H), 6,87-7,06 (m, 3Н), 7,18-7,35 (m, 6H), CDCI3); 1,48 (s, 9Н), 3,08 (s, 3Н), 3,87 (t, 2H), 4,18 7,40(m, 1H), 7,70 (d, 1H) (t, 2H), 4,49 (s, 2H), 6,84 (d, 2H), 6,90-6,98 (m, 2H), Приклад 2 7,26-7,26 (m, 2H), 7,38-7,43 (m, 1H), 7,7 (dd, 1H) а) 2-Бром-N-(2,4-дифлуорбензил)-Nd) (4-{2-[2гептилацетамід (метоксикарбоніл]фенокси]етил}фенокси)оцтова N-(2,4-дифлуорбензил)-N-гептилацетамід кислота (2,004г, 8,304ммоль) розчиняють у ДХМ (30мл), а Метил 2-{2-[4-(2-трет-бутокси-2тоді охолоджують у льодяній бані. Триетиламін оксоетокси)феніл]етокси}бензоат (0,400г, (1,092г, 10,796ммоль) додають, а тоді уводять 1,0351ммоль) розчиняють у ДХМ та додають трикраплями бромацетилхлорид (1,438г, 9,135ммоль). флуороцтову кислоту (0,8мл, 8,281ммоль). Суміш Суміш перемішують протягом 2 годин (льодяна перемішують при кімнатній температурі протягом 3 баня), а тоді промивають водою (з додатковою 1% годин. Розчинник випарюють з утворенням 325мг гідрохлоридною кислотою, рН~3), водою та розсобілого порошку. лом, та сушать магній сульфатом та випарюють. 1 Н-ЯМР (600МГц, CDCI3); 3,08 (t, 2H), 3,86 (s, Сирий маслянистий продукт розчиняють у ДХМ, 3Н), 4,18 (t, 2H), 4,64 (s, 2H), 6,84-6,96 (m, 4H), 7,23 тоді завантажують у колонку (ISOLUTE SI (d, 2H), 7,37-7,42 (m, 1H), 7,75 (dd, 1H) 5г/25мл) та елюють ще ДХМ. Маслянистий продукт e) Метил 2-[2-{4-[2-[етил(22,412г отримують, вихід 80% 1 флуорбензил)аміно]-2Н ЯМР (ротамер, 500МГц, CDCI3): 0,88-0,93 оксоетокси]феніл)етокси]бензоат (m, 3Н), 1,27-1,34 (m, 8H), 1,52-1,68 (m, 2Н), 3,28(4-{2-[23,35 (m, 2Н), 3,90-4,15 (m, 2Н), 4,61, 4,63 (s, s, 2H), (Метоксикарбоніл)фенокси]етил}фенокси)оцтову 6,81-6,94 (m, 2H) та 7,15-7,20, 7,34-7,39 (m, 1H). кислоту (0,200мг, 0,605ммоль) розчиняють.у ДМФ b) N-[2,4-дифлуорбензил)-N-гептил-2-[4-(2та охолоджують на льодяній бані. N-(4гідроксіетил)-2-метоксифенокси]ацетамід Флуорбензил)-N-етанамін (0,102г, 0,666ммоль), 2-Бром-N-2,4-дифлуорбензил)-NTBTU (0,214г, 0,666ммоль) та DPEA (0,22мл, гептилацетамід (135мг, 0,373ммоль), гомованілі1,271ммоль) додають. Реакційну суміш перемішуловий спирт (63мг, 0,373ммоль) та безводний кають протягом 16 годин при кімнатній температурі, лій карбонат (77мг, 0,559ммоль) змішують в ацедодають EtOAc та органічну фазу промивають тонітрилі (10мл). Суміш гріють до кипіння під двома порціями по 20мл NaCO3 (насичен.). Оргазворотним холодильником протягом 4 годин та нічний шар сушать сульфатом магнію та розчинтоді випарюють досуха. Залишок (з додатковим ник видаляють випарюванням. Сирий матеріал ДХМ, 1мл 2) завантажують у колонку (ISOLUTE 21 76627 22 SI, 1г/6мл), елюють ДХМ, а тоді МеОН/ДХМ тримають у шафі ще 10 хвилин, РХ-МС показує (0,5:99,5, тоді 1:99). Фракції продукту поєднують та майже відсутність змін. Ще 3мг літій гідроксиду випарюють. Маслянистий продукт 132мг отримудодають та потім тримають у шафі при 150°С проють, вихід 79%. тягом 8 хвилин. РХ-МС показує те ж саме, що до 1 того. Ще 3мг літій гідроксиду та 1мл води додають. Н ЯМР (ротамер, 400МГц, CDCI3): 0,82-0,87 Утворену суміш тримають у шафі при 150°С протя(m, 3Н), 1,17-1,28 (m, 8H), 1,43-1,68 (m, 2H), 2,75гом 10 хвилин та РХ-МС показує завершення реа2,80 (m, 2H),3,24-3,32 (m, 2H), 3,73-3,84 (m, 5H), кції, суміш випарюють для видалення ТГФ. Зали4,58,4,66 (s, s, 2H), 4,74, 4,76 (s, s, 2H), 6,67-6,86 шок підкислюють 1% гідрохлоридною кислотою, (m, 5H) та 7,08-7,14, 7,23-7,29 (m, 1H). рН~5, та екстрагують етилацетатом (10мл). Екстc) 2-(4-(2-(2,4-Дифлуорбензил)(гептил)аміно]ракти сушать магній сульфатом та випарюють 2-оксоетокси)-3-метоксифеніл)етил метансульфонат Хроматографія залишку на колонці (ISOLUTE SI, N-(2,4-дифлуорбензил)-N-гептил-2-[4-(21г/6мл), застосовуючи ДХМ та тоді МеОН/ДХМ гідроксіетил)-2-метоксифенокси]ацетамід (А) (1:99), як елюент, дає 60мг потрібного продукту, (132мг, 0,294ммоль) розчиняють у ДХМ (10мл), вихід 83%. 1Н ЯМР (ротамер, 400МГц, CDCI3): охолоджують у льодяній бані. Триетиламін 0,82-0,87 (m, 3Н), 1,18-1,28 (m, 8H), 1,43-1,61 (m, (0,05мл, 0,352ммоль) додають та тоді уводять 2Н), 3,10-3,15(m, 2Н), 3,24-3,31 (m, 2Н), 3,77-3,85 краплями метансульфонілхлорид (37мг, (s, s, 3Н), 4,39-4,44 (m, 2H), 4,59,4,66 (s, s, 2H), 0,323ммоль). Охолоджувальну баню видаляють 4,77,4,78 (s, s, 2H), 6,72-6,91 (m, 5H), 7,01 (d, 1H), після 30 хвилин. Суміш перемішують при кімнатній 7,09 (t, 1H), 7,10-7,17,7,26-7,32 (m, m, 1H), 7,51 (t, температурі протягом ночі. МСНР показує, що 1H) та 8,13 (d, 1H). 13 приблизно 50% of А не реагують. Суміш охолоC ЯМР (ротамери, 75МГц, CDCI3): 14,07, джують у льодяній бані та додають 0,05мл триети22,55, 26,79,27,02, 28,57, 28,93, 31,70, 35,18, ламіну, а потім 0,025мл метансульфонілхлориду. 41,30, 41,34, 44,02, 45,89, 46,99, 55,71, 55,82, Після додавання охолоджувальну баню видаля68,19, 68,94, 70,66, 103,38(t), 103,88(t), 111,35(d), ють та суміш перемішують протягом більше 5 го111,39(d), 112,32, 112,41, 112,46, 114,76, 117,64, дин, а тоді промивають водою ( 2) та розсолом, 119,60(dd), 120,07(dd), 120,53, 122,06, 129,50(dd), сушать магній сульфатом та випарюють. Масля130,54, 130,59, 131,55(dd), 133,60, 134,78, 146,26, нистий продукт 138мг залишають та використову146,39,149,67, 157,10, 161,60(dd), 160,68(dd), ють на наступному етапі без очистки. 161,97(dd), 162,24(dd), 165,12, 167,75 та 167,93. d) Метил 2-[2-(4-{2-[(2,4Приклад 3 дифлуорбензил)(гептил]аміно]-2-оксоетокси)-3а) N-(4-хлорбензил)ацетамід етоксифеніл]-етокси]бензоат Оцтову кислоту (1,321g, 22,000ммоль) розчи2-(4-{2-[(2,4-дифлуорбензил)(гептил)аміно]-2няють у ДМФ(10мл), додають 1-(4оксоетокси}-3-метоксифеніл)етил метансульфонат хлорфеніл)метанамін (2,804г, 19,800ммоль) та (138мг, 0,262ммоль) розчиняють в ацетонітрилі суміш охолоджують до 0°С. N-[(1H-1,2,3(10мл). 2-Гідроксибензойної кислоти метиловий бензотриазол-1-ілокси)(диметиламіно)метилен]-Nестер (40мг, 0,262ммоль) додають, а тоді додають метилметанамоній тетрафлуорборат (7,770г, безводний калій карбонат (54мг, 0,392ммоль). Су24,200ммоль) та N-етил-N,N-діізопропіламін міш гріють до кипіння під зворотним холодильни(5,971г, 46,200ммоль) додають. Розчин перемішуком протягом ночі та тоді випарюють досуха. Воду ють протягом двох годин при кімнатній температу(10мл) та етилацетат (10мл) додають та дві фази рі. EtOAc (20мл) додають та органічну фазу провідокремлюють. Органічну фазу промивають вомивають Na2CO3 (3 X 20мл, водн.) та НСІ (0,5М, 2 дою та розсолом, сушать магній сульфатом та X, 10мл). Органічний шар сушать магній сульфавипарюють. Хроматографія залишку на колонці том та розчинник видаляють випарюванням. За(ISOLUTE SI, 2г/6мл), застосовуючи ДХМ, Мелишок очищають препаративною ВЕРХ (початкова ОН/ДХМ (1:99) як елюент, дає 78мг потрібного рухома фаза є ізократичною сумішшю ацетонітпродукту, вихід 45% (два етапи). рил/буфер 60/40, а тоді концентрацію ацетонітри1 лу збільшують до 100%, буфером є суміш ацетоніН ЯМР (ротамер, 500МГц, CDCI3): 0,87-0,91 трил/вода 10/90 та амоній ацетат (0,1М, колонка (m, 3Н), 1,22-1,32 (m, 8H), 1,48-1,63 (m, 2H), 3,09KR-100-7-C8,50мм X 250мм, потік 40мл/хвилин). 3,14 (m, 2H), 3,28-3,35 (m, 2H), 3,80, 3,89 (s, s, 3Н), Фракції з вмістом продукту поєднують та ацетоніт3,89 (s, 3Н), 4,21-4,25 (m, 2H), 4,62, 4,71 (s, s, 2H), рил видаляють випарюванням. EtOAc (10мл) до4,79, 4,81 (s, s, 2H), 6,77-7,01 (m, 7H), 7,28-7,33 (m, дають та органічну фазу промивають двома порці1H), 7,13-7,18,7,28-7,33 (m, m, 1H), 7,45 (t, 1H) та ями розсолу та сушать магній сульфатом і 7,81 (d, 1H). розчинник видаляють випарюванням та отримують е) 2-[2-(4-(2-{[2,42,337г N-(4-хлорбензил)ацетаміду (вихід 57,8%). дифлуорбензил)(гептил)аміно]-2-оксоетокси)-31 метоксифеніл]-етокси]бензойна кислота Н ЯМР (500МГц, CDCI3): 1,96 (s, 3Н), 4,31 (d, Метил 2-[2-(4-{2-[(2,42H), 6,46 (bs, 1H), 7,16 (d, 2H), 7,25 (d, 2H). дифлуорбензил)(гептил)аміно]-2-оксоетокси)-3b) N-(4-хлорбензил)-N-етиламін етоксифеніл]-етокси]бензоат (74мг, 0,127ммоль) N-(4-хлорбензил)ацетамід (2,337г, розчиняють у ТГФ (2мл), змішують з літій гідрокси12,726ммоль) розчиняють у ТГФ (100мл) та оходом (6,1мг, 0,254ммоль), що розчиняють у воді лоджують до 0°С в атмосфері аргону. (Метил(1мл). Суміш опромінюють у мікрохвильовій шафі тіо)метановий комплекс з бораном (1:1) (2,417г, (синтезатор Сміта) при 150°С протягом 8 хвилин. 31,815ммоль) додають та суміш кип'ятять під звоРХ-МС показує, що реакція не завершується, Це ротним холодильником протягом ночі при кімнат 23 76627 24 ній температурі. НСІ (15мл, 10%) обережно дода0,035ммоль) та N-етил-N,N-діізопропіламін (0,157г, ють та перемішують протягом ночі і розчинник ви1,212ммоль). Розчин перемішують протягом ночі даляють випарюванням. Діетиловий етер (20мл) при кімнатній температурі. Воду (100мл) додають додають та продукт екстрагують у водну фазу ката водну фазу екстрагують діетиловим етером (3 X лій карбонатом (3 X 15мл). Водну фазу підкислю20мл). Органічну фазу промивають натрій карбоють НСІ (10мл, 10%) та продукт екстрагують в орнатом (3 X 20мл, водн.) та НСІ (0,5М, 2 X, 10мл). ганічну фазу EtOAc (3 X 15мл). Органічну фазу Органічний шар сушать магній сульфатом та розсушать магній сульфатом та розчинник видаляють чинник видаляють випарюванням. Залишок очивипарюванням з утворенням 0,938г N-(4щають флеш-хроматографією (починаючи з ізокхлорбензил)-N-етиламіну (вихід 43,4%). ратичної суміші гептан/EtOAc 30/70 та тоді 1 концентрацію EtOAc збільшують до 100%, (силікаН ЯМР (500МГц, CDCI3): 1,11 (t, 3Н), 2,65 (q, гель 60 0,004-0,063мм). Продукт, що містить фра2H), 3,74 (s, 2H), 7,23-7,28 (m, 4H). кції, поєднують та розчинник видаляють випарюc) Метил 2-((2-[4-(2-трет-бутокси-2ванням з утворенням 0,085г метил 2-{[2-(4-{2-[(4оксоетокси)феніл]етил]тіо)бензоат хлорбензил)(етил)аміно]-2Трет-бутил (4-{2оксоетокси}феніл)етил]тіо}бензоату (вихід 29,6%). [(метилсульфоніл)окси]етил}фенокси)ацетат 1 Н ЯМР (ротамери, 300МГц, CDCI3): 1,09(5,454г, 17,347ммоль) розчиняють в ацетонітрилі (100мл), додають метил 2-меркаптобензоат 1,21 (m, 3Н), 2,91-2,99 (m, 2H), 3,11-3,18 (m, 2H), (3,502г, 20,816ммоль) та калій карбонат (4,795г, 3,32-3,43 (m, 2H), 3,92 (s, 3Н), 4,57-4,75 (m, 4H), 34,694ммоль). Розчин перемішують протягом 10 6,78, 6,92 (d, d, 2H), 7,12-7,46 (m, 9H), 7,96 (d, 1H). годин при 60°С. EtOAc (40мл) додають та органічf) 2-{[2-(4-(2-[(4-хлорбензил)(етил)аміно]-2ну фазу промивають двома порціями розеолу (2 Χ оксоетокси)феніл)етил]тіо]бензойна кислота 40мл, водн.). Органічний шар сушать магній сульМетил 2-{[2-(4-{2-[(4-хлорбензил)(етил)аміно]фатом та розчинник видаляють випарюванням з 2-оксоетокси}феніл)етил]тіо}бензоат (0,085г, утворенням 6,931г метил 2-({2-[4-(2-трет-бутокси0,170ммоль) розчиняють у суміші ацетоніт2-оксоетокси)феніл]етил}тіо)бензоату. Цей матерірил/вода (1/1, 4мл) та додають літій гідроксид ал використовують на наступному етапі без очис(0,008г, 0,341ммоль). Реакційну суміш перетворютки. ють в одиничному вузлі мікрохвильової шафи d) [4-(2-{[2-(Метоксикарбоніл)феніл]-тіо)етил)(5мм, 150град.). Розчинник видаляють випарюванфенокси]оцтова кислота ням та тоді додають НСІ (2мл, 1М). Водну фазу Метил 2-({2-[4-(2-трет-бутокси-2екстрагують двома порціями EtOAc (20мл). Комбіоксоетокси)феніл]етил}тіо)бензоат (4,630г, новану органічну фазу сушать магній сульфатом 11,502ммоль) уводять у ДХМ (50мл) та оброблята розчинник видаляють випарюванням та отриють трифлуороцтовою кислотою (44,40г, мують 0,073г 2-{[2-(4-{2-[(4389,405ммоль) при кімнатній температурі протягом хлорбензил)(етил)аміно]-24 годин. Суміш випарюють та переганяють з толуоксоетокси}феніл)етил]тіо}бензойної кислоти (виолом. Сирий матеріал очищають препаративною хід 88,4%), як масло, яке стверджується при охоВЕРХ (початкова рухома фаза є ізократичною сулодженні та стоянні. 1 мішшю ацетонітрил/буфер 60/40 та тоді концентН ЯМР (ротамери, 400МГц, CDCI3): 1,09рацію ацетонітрилу збільшують до 100%, буфером 1,20 (m, 3Н), 2,91-2,98 (m, 2H), 3,11-3,17(m, 2H), є суміш ацетонітрил/вода 10/90 та амоній ацетат 3,33-3,42 (m, 2H), 4,58-4,77 (m, 4H), 6,79, 6,92 (d, d, (0,1М, колонка KR-100-7-C8, 50мм X 250мм, потік 2H), 7,11-7,49 (m, 9H), 8,10(d, 1H). 13 40мл/хвилин). Продукт, що містить фракції, поєдС ЯМР (ротамери, 100МГц, CDCI3): 12,23, нують та ацетонітрил видаляють випарюванням. 13,77, 33,70, 33,82, 41,09, 41,30, 47,42, 49,64, EtOAc (10мл) додають та органічну фазу проми67,37, 67,91, 114,69, 114,81, 123,97-135,58 (складвають двома порціями розсолу та сушать магній ний мультиплет), 142,22, 156,45, 156,57, 168,20, сульфатом. Розчинник видаляють випарюванням з 170,63. утворенням 3,825г [4-(2-{[2Наступні два приклади отримують подібним (метоксикарбоніл)феніл]-тіо}етил)способом: фенокси]оцтової кислоти (вихід після двох етапів Приклад 4 63,9% від загального). 2-[2-(4-{2-[(4-Хлорбензил)(етил)аміно]-21 Н ЯМР (500МГц, CDCI3): 2,93-2,98 (m, 2H), оксоетокси}феніл)етокси]бензойна кислота. 3,12-3,17 (m, 2H), 3,92 (s, 3Н), 4,67 (s, 2H), 6,88 (d, Приклад 5 2H), 7,13-7,21 (m, 3Н), 7,33 (d, 1H), 7,41-7,46 (m, 2-[2-(4-{2-[Етил(41H), 7,96 (dd, 1H). трифлуорметилбензил)аміно]-2e) Метил 2-{[2-(4-{2-[(4оксоетокси}феніл)етокси]бензойна кислота. хлорбензил)(етил)аміно]-2Приклад 6 оксоетокси)феніл}етил]тіо]бензоат a) Оцтову кислоту (1,321г, 22,000ммоль) роз[4-(2-{[2чиняють у ДМФ (10мл), додають 1-[4(Метоксикарбоніл)феніл]тіо}етил)фенокси]оцтову (трифлуорметил)феніл]метанамін (3,468г, кислоту (0,200г, 0,577ммоль) розчиняють у ДМФ 19,800ммоль) та суміш охолоджують до 0°С. N(10мл), додають N-(4-хлорбензил)-N-етиламін [(1Н-1,2,3-бензотриазол-1(0,108г, 0,635ммоль) та суміш охолоджують до ілокси)(диметиламіно)метилен]-N0°С. Додають N-[(1Н-1,2,3-бензотриазол-1метилметанамоній тетрафлуорборат (7,770г, ілокси)(диметиламіно)метилен]-N24,200ммоль) та N-етил-N,N-діізопропіламін метилметанамоній тетрафлуорборат (0,204г, (5,971г, 46,200ммоль) додають. Розчин перемішу 25 76627 26 ють протягом двох годин при кімнатній температунітрил видаляють випарюванням. EtOAc (10мл) рі. EtOAc (20мл) додають та органічну фазу прододають та органічну фазу промивають двома мивають натрій карбонатом (3 X 20мл, водн.) та порціями розсолу та сушать магній сульфатом. НСІ (0,5М, 2 X, 10мл). Органічний шар сушать магРозчинник видаляють випарюванням, отримуючи ній сульфатом та розчинник видаляють випарю3,825г [4-(2-{[2ванням. Сирий матеріал очищають препаратив(метоксикарбоніл)феніл]тіо}етил)фенокси]оцтової ною ВЕРХ (починаючи з ізократичної суміші кислоти (вихід після двох етапів 63,9% від загальацетонітрил/буфер 60/40 та тоді концентрацію ного). 1 ацетонітрилу збільшують до 100%, буфером є суН ЯМР (500МГц, CDCI3): 2,82 (t, 2H), 3,15 (t, міш ацетонітрил/вода 10/90 та амоній ацетат 2H), 3,82 (s, 3Н), 4,35 (s, 2H), 6,78 (d, 2H), 7,18 (d, (0,1М, колонка KR-100-7-C8, 50мм X 250мм, потік 2H), 7,23 (t, 1H), 7,51 (d, 1H), 7,55 (t, 1H), 7,85 (d, 40мл/хвилин). Продукт, що містить фракції, поєд1H). нують та ацетонітрил видаляють випарюванням, e) [4-(2-{[2додають EtOAc (10мл) та органічну фазу проми(метоксикарбоніл)феніл]тіо}етил)фенокси]оцтову вають двома порціями розсолу і сушать магній кислоту (0,200г, 0,577ммоль) розчиняють у ДМФ сульфатом та розчинник видаляють випарюван(10мл), додають N-[4ням і отримують 3,085г N-[4(трифлуорметил)бензил]етанамін (0,129г, (трифлуорметил)бензил]ацетаміду (вихід 64,6%). 0,635ммоль) та суміш охолоджують до 0°С. N-[(1Н1 Н ЯМР (500МГц, CDCI3): 2,0 (s, 3Н), 4,42 (d, 1,2,3-бензотриазол-12H), 6,58 (bs, 1H), 7,35 (d, 2H), 7,55 (d, 2H) ілокси)(диметиламіно)метилен]-Nb) N-[4-(трифлуорметил)бензил]ацетамід метилметанамоній тетрафлуорборат (0,204г, (3,085г, 14,204ммоль) розчиняють у ТГФ (100мл) 0,635ммоль) та додають N-етил-N,N-ізопропіламін та охолоджують до нуля градусів в атмосфері ар(0,157г, 1,212ммоль). Розчин перемішують протягону, (комплекс (метилтіо)метану з бораном (1:1) гом ночі при кімнатній температурі. Воду (100мл) (2,698г, 35,511ммоль) додають та суміш кип'ятять додають та водну фазу екстрагують діетиловим під зворотним холодильником протягом ночі при етером (3 X 20мл). Органічну фазу промивають кімнатній температурі. НСІ (15мл, 10%) обережно натрій карбонатом (3 X 20мл, водн.) та НСІ (0,5М, додають та перемішують протягом ночі. Розчинник 2 X, 10мл). Органічний шар сушать магній сульфавидаляють випарюванням. Діетиловий етер (20мл) том та розчинник видаляють випарюванням. Сидодають та продукт екстрагують у водну фазу карий матеріал очищають флеш-хроматографією лій карбонатом (3 X 15мл), водну фазу підкислю(починаючи з ізократичної суміші гептан/EtOAc ють НСІ (10мл, 10%) та продукт екстрагують в ор30/70 та тоді концентрацію EtOAc збільшують до ганічну фазу EtOAc (3 X 15мл). Органічну фазу 100%, (силікагель 60 0,004-0,063мм). Продукт, що сушать магній сульфатом та розчинник видаляють містить фракції, поєднують та розчинник видалявипарюванням з утворенням 0,809г N-[4ють випарюванням з утворенням 0,085г метил 2(трифлуорметил)бензил]етанаміну (вихід 28%). ({2-[4-(2-{етил[4-(трифлуорметил)бензил]аміно}-21 оксоетокси)феніл]етил}тіо)бензоату (вихід 27,7%). Н ЯМР (500МГц, CDCI3): 1,05 (t, 3Н), 1,3 (s, 1 1H), 2,62 (q, 2H), 3,78 (s, 2H), 7,38 (d, 2H), 7,3 (d, Н ЯМР (ротамери, 500МГц, CDCI3): 1,1-1,23 2H) (bm, 3Н), 2,95 (q, 2H), 3,15 (q, 2H), 3,42 (m, 2H), 3,9 с) Трет-бутил (4-{2(s, 3Н), 4,7-4,82 (bm, 4H), 6,75-6,95 (m, 2H), 7,1-7,5 [(метилсульфоніл)окси]етил}фенокси)ацетат (m, 9H), 7,97 (d, 1H). (5,454г, 17,347ммоль) розчиняють в ацетонітрилі f) Метил 2-({2-[4-(2-{етил[4(100мл), додають метил 2-меркаптобензоат (трифлуорметил)бензил]аміно}-2(3,502г, 20,816ммоль) та дикалій карбонат (4,795г, оксоетокси)феніл]-етил}тіо)бензоат (0,085г, 34,694ммоль). Розчин перемішують протягом 10 0,160ммоль) розчиняють у суміші ацетонітгодин при 60°С. EtOAc (40мл) додають та органічрил/вода (1/1,4мл), тоді додають літій гідроксид ну фазу промивають двома порціями розеолу (2 Χ (0,008г, 0,320ммоль). Реакційну суміш перетворю40мл, водн.). Органічний шар сушать магній сульють в одиничному вузлі мікрохвильової шафи (5 фатом та розчинник видаляють випарюванням з хвилин, 150град). Обробляють видаленням розутворенням 6,931г сирого метил 2-({2-[4-(2-третчинник випарюванням та додавання НСІ (2мл, бутокси-2-оксоетокси)феніл]етил}тіо)бензоату. 1М). Водну фазу екстрагують двома порціями Сирий матеріал використовують на наступному EtOAc (20мл), органічну фазу сушать магній сульетапі без очистки. фатом та розчинник видаляють випарюванням та d) Метил 2-({2-[4-(2-трет-бутокси-2отримують 0,07773г 2-({2-[4-(2-{етил[4оксоетокси)феніл]етил}тіо)бензоат (4,630г, (трифлуорметил)бензил]аміно}-211,502ммоль) уводять у ДХМ (50мл) та обробляоксоетокси)феніл]етил}тіо)бензойної кислоти (виють трифлуороцтовою кислотою (44,40г, хід 93,0%). 1 389,405ммоль) при кімнатній температурі протягом Н ЯМР (ротамери, 400МГц, CDCI3): 1,024 годин. Суміш випарюють та переганяють з толу1,25 (bm, 3Н), 2,95 (q, 2H), 3,15 (q, 2H), 3,38 (m, олом. Сирий матеріал очищають препаративною 2H), 4,60-4,82 (bm, 4H), 6,75-6,95 (m, 2H), 7,1-7,5 ВЕРХ (починаючи з ізократичної суміші ацетоніт(m, 9H), 7,97 (d, 1H). рил/буфер 60/40 та тоді концентрацію ацетонітриПриклад 7 лу збільшують до 100%, буфером є суміш ацетоніМетил 2-{2-[4-(2-{бутил[2-флуор-4трил/вода 10/90 та амоній ацетат (0,1М, колонка (трифлуорметил)бензил]аміно}-2KR-1QO-7-C8,50мм X 250мм, потік 40мл/хвилин). оксоетокси)феніл]-етокси}бензоат (0,230г, Продукт, що містить фракції, поєднують та ацето0,410ммоль) розчиняють у суміші ТГФ/вода (1/1, 27 76627 28 4мл). Літій гідроксид (0,015г, 0,617ммоль) додаметилметанамоній тетрафлуорборат (0,160г, ють. Реакційну суміш перетворюють в одиничному 0,499ммоль), N-етил-]-N,N-діізопропіламін (0,123г, вузлі мікрохвильової шафи (14 хвилин, 150град). 0,954ммоль) додають. Розчин перемішують протяОбробляють видаленням розчиннику випарювангом двох годин при кімнатній температурі. EtOAc ням та додаванням НСІ (2мл, 1М). Водну фазу (20мл) додають та органічну фазу промивають екстрагують двома порціями EtOAc (20мл). Органатрій карбонатом (2 X 20мл, водн.) та НСІ (0,5М, нічну фазу сушать магній сульфатом та розчинник 2 X, 10мл). Органічний шар сушать магній сульфавидаляють випарюванням з утворенням 0,212г 2том та розчинник видаляють випарюванням з {2-[4-(2-{бутил[2-флуор-4утворенням 0,138г метил 2-[2-(4-{2(трифлуорметил)бензил]аміно}-2[бензил(етил)аміно]-2оксоетокси)феніл]етокси}бензойної кислоти (вихід оксоетокси}феніл)етокси]бензоату (вихід 67,9%). 1 94,5%). Н ЯМР (ротамери, 500МГц, CDCI3): 1,071 Н ЯМР (ротамери, 500МГц, CDCI3): 0,82-1,0 1,22 (bm, 3Н), 3,1 (m, 2H), 3,20 (bm, 2H), 3,9 (s, 3Н), (bm, 3Н), 1,2-1,4 (bm, 2H), 1,65-1,7 (bm, 2H), 3,13 4,2 (q, 2H), 4,6-4,8 (Μ, 4Η), 6,8-7,02 (bm, 4H), 6,18(m, 2H), 3,32 (m, 2H), 4,4 (m, 2H), 4,63-4,8 (Μ, 4Η), 7,5 (bm, 8H), 7,78 (d, 1H). 6,7-7,6 (bm, 10H), 8,1(d, 1H). b) Метил 2-[2-(4-{2-[бензил(етил)аміно]-2Приклад 8 оксоетокси}феніл)етокси]бензоат (0,138г, a) (4-{2-[20,308ммоль) розчиняють у суміші ТГФ/вода (Метоксикарбоніл)фенокси]етил}фенокси)оцтову (1/1,4мл). Літій гідроксид (0,015г, 0,617ммоль) докислоту (0,150г, 0,454ммоль) розчиняють у ДМФ дають. Реакційну суміш перетворюють в одинич(10мл), додають N-(2,4-дифлуорбензил)-Nному вузлі мікрохвильової шафи (14 хвилин, пропіламін (0,084г, 0,454ммоль) та суміш охоло150град). Обробляють видаленням розчиннику джують до 0°С. N-[(1Н-1,2,3-бензотриазол-1випарюванням та додаванням НСІ (2мл, 1М). Водтокси)(диметиламiно)метилен]-Nну фазу екстрагують двома порціями EtOAc метилметанамоній тетрафлуорборат (0,160г, (20мл), органічну фазу сушать магній сульфатом 0,499ммоль) та додають N-етил-N,Nта розчинник видаляють випарюванням з утворендіізопропіламін (0,123г, 0,954ммоль). Розчин пеням 0,146г 2-[2-(4-{2-[бензил(етил)аміно]-2ремішують протягом двох годин при кімнатній темоксоетокси}феніл)етокси]бензойної кислоти. 1 пературі. EtOAc (20мл) додають та органічну фазу Н ЯМР (ротамери, 500МГц, CDCI3): 1,02промивають натрій карбонатом (3 X 20мл, водн.) 1,22 (bm, 3Н), 3,1 (m, 2H), 3,25-3,5 (bm, 2H), 4,2 (q, та НСІ (0,5М, 2 X, 10мл). Органічний шар сушать 2H), 4,55-4,8 (Μ, 4Η), 6,8-7,4 (bm, 11Н), 7,5 (m, 1H), магній сульфатом та розчинник видаляють випа8,1 (d, 1H). рюванням з утворенням 0,220г метил 2-[2-(4-{2Приклад 10 [(2,4-дифлуорбензил)(пропіл)аміно]-2a) Трет-бутил (4-{2оксоетокси}феніл)-етокси]бензоату (вихід 97,4%). [(метилсульфоніл)окси]етил}фенокси)ацетат 1 Н ЯМР (ротамери, 500МГц, CDCI3): 0,8-1,0 (5,454г, 17,347ммоль) розчиняють в ацетонітрилі (bm, 3Н), 1,45-1,7 (bm, 2H) 3,1 (m, 2H), 3,28 (bm, (100мл), додають метил 2-меркаптобензоат 2К), 3,9 (s, 3Н), 4,2 (q, 2H), 4,6-4,75 (Μ, 4Η), 6,7-7,0 (3,502г, 20,816ммоль) та дикалій карбонат (4,795г, (bm, 6H), 7,1-7,3 (bm, 3Н), 7,4 (m, 1H), 7,78 (d, 1H). 34,694ммоль). Розчин перемішують протягом 10 b) Метил 2-[2-(4-{2-[(2,4годин при 60°С. EtOAc (40мл) додають та органічдифлуорбензил)(пропіл)аміно]-2ну фазу промивають двома порціями розсолу (2 X оксоетокси}феніл)-етокси]-бензоат (0,22г, 40мл, водн.). Органічний шар сушать магній суль0,442ммоль) розчиняють у суміші ТГФ/вода (1/1, фатом та розчинник видаляють випарюванням з 4мл). Літій гідроксид (0,021г, 0,884ммоль) додаутворенням 6,931г сирого метил 2-({2-[4-(2-третють. Реакційну суміш перетворюють в одиничному бутокси-2-оксоетокси)феніл]етил}тіо)-бензоату. вузлі мікрохвильової шафи (14мм, 150град). ОбСирий матеріал використовують на наступному робляють видаленням розчиннику випарюванням етапі без очистки. та додаванням НСІ (2мл, 1Μ). Водну фазу екстраb) Метил 2-({2-[4-(2-трет-бутокси-2гують двома порціями EtOAc (20мл), органічну оксоетокси)феніл]етил}тіо)бензоат (4,630г, фазу сушать магній сульфатом та розчинник ви11,502ммоль) уводять у ДХМ (50мл) та оброблядаляють випарюванням з утворенням 0,180г 2-[2ють трифлуороцтовою кислотою (44,40г, (4-{2-[(2,4-дифлуорбензил)(пропіл)-аміно]-2389,405ммоль) при кімнатній температурі протягом оксоетокси}феніл)етокси]-бензойної кислоти (вихід 4 годин. Суміш випарюють та переганяють з толу84,2%). олом. Сирий матеріал очищають препаративною 1 ВЕРХ (починаючи з ізократичної суміші ацетонітН ЯМР (ротамери, 500МГц, CDCI3): 0,8-1,0 рил/буфер 60/40 та тоді концентрацію ацетонітри(bm, 3Н), 1,45-1,7 (bm, 2H), 3,14 (m, 2H), 3,28 (bm, лу збільшують до 100%, буфером є суміш ацетоні2H), 4,4 (q, 2H), 4,62 (s, 2H), 4,75 (s, 2H), 6,7-7,35 трил/вода 10/90 та амоній ацетат (0,1М, колонка (bm, 9H), 7,52 (t, 1H), 8,12 (d, 1H). KR-100-7-C8,50мм Х 250мм, потік 40мл/хвилин). Приклад 9 Продукт, що містить фракції, поєднують та ацетоa) (4-{2-[2нітрил видаляють випарюванням. EtOAc (10мл) (метоксикарбоніл)фенокси]етил}фенокси)оцтову додають та органічну фазу промивають двома кислоту (0,150г, 0,454ммоль) розчиняють у ДМФ порціями розсолу та сушать магній сульфатом. (10мл), N-бензил-N-етиламін (0,061г, 0,454ммоль) Розчинник видаляють випарюванням з утворенням додають та суміш охолоджують до 0°С. N-[(1Н3,825г [4-(2-{[2-(метоксикарбоніл)феніл]тіо}етил)1,2,3-бензотриазол-1фенокси]оцтової кислоти (вихід після двох етапів ілокси)(диметиламіно)метилен]-N 29 76627 30 63,9% від загального). 4,63-4,8 (m, 2H) 6,77-7,43 (m, HH), 7,78 (d, 1H). 1 b) Метил 2-[2-(4-{2-[(4-третН ЯМР (500МГц, CDCI3): 2,82 (t, 2H), 3,15 (t, бутилбензил)(етил)аміно]-2-оксоетокси}феніл)2H), 3,82 (s, 3Н), 4,35 (s, 2H), 6,78 (d, 2H), 7,18 (d, етокси]бензоат (0,2290г, 0,455ммоль) розчиняють 2H), 7,23 (t, 1H), 7,51(d, 1H), 7,55 (t, 1H), 7,85 (d, у суміші ТГФ (свіжо-перегнаний)/вода (2/1,3мл), 1H). додають літій гідроксид (0,218г, 0,909ммоль). Реаc) [4-(2-{[2-(метоксикарбоніл)феніл]тіо}етил) кційну суміш перетворюють в одиничному вузлі фенокси]оцтову кислоту (0,200г, 0,577ммоль) розмікрохвильової шафи (5 хвилин, 150град). ТГФ чиняють у ДМФ (10мл), N-бензил-N-етиламін видаляють випарюванням. Додають воду (10мл) (0,086г, 0,635ммоль) додають та суміш охолоджута основну водну фазу промивають діетиловим ють до 0°С. N-[(1Н-1,2,3-бензотриазол-1етером (2 X 10мл). Додають НСІ (2мл, 1М, рН 1). ілокси)(диметиламіно)метилен]-NВодну фазу екстрагують двома порціями ДХМ метилметанамоній тетрафлуорборат (0,204г, (20мл), органічну фазу сушать магній сульфатом 0,635ммоль) та N-етил-Ν,Ν-діізопропіламін (0,157г, та розчинник видаляють випарюванням з утворен1,212ммоль) додають. Розчин перемішують протяням 0,163г 2-[2-(4-{2-[(4-третгом ночі при кімнатній температурі. Воду (100мл) бутилбензил)(етил)аміно]-2додають та водну фазу екстрагують діетиловим оксоетокси}феніл)етокси]бензойної кислоти (вихід ете-ром (3 X 20мл). Органічну фазу промивають 73,2%). натрій карбонатом (3 X 20мл, водн.) та НСІ (0,5М, 1 2 X, 10мл). Органічний шар сушать магній сульфаН ЯМР (ротамери, 500МГц, CDCI3): 1,07том та розчинник видаляють випарюванням. Си1,21 (bm, 3Н), 2,28 (m, 9H), 3,12 (m, 2H), 3,28-3,5 рий матеріал очищають флеш-хроматографією (bm, 2H), 4,4 (m, 2H), 4,58 (d, 2H), 4,63-4,78 (m, 2H) (починаючи з ізократичної суміші гептан/EtOAc 6,80-7,55 (m, 11Н), 8,1 (d, 1H). 30/70 та тоді концентрацію EtOAc збільшують до Приклад 12 100%, (силікагель 60 0,004-0,063мм). Продукт, що а) Оцтову кислоту (1,321г, 22,000ммоль) розмістить фракції, поєднують та розчинник видалячиняють у ДМФ (10мл), 1-(4ють випарюванням з утворенням 0,137г метил 2(флуорфеніл)метанамін (2,478г, 19,800ммоль) {[2-(4-{2-бензил(етил)аміно]-2-оксоетокси}феніл)додають та суміш охолоджують до 0°С. N-[(1Нетил]тіо}бензоату (вихід 51,2%). 1,2,3-бензотриазол-1d) Метил 2-{[2-(4-{2-[бензил(етил)аміно]-2ілокси)(диметиламіно)метилен]-Nоксоетокси}феніл)етил]тіо}бензоат (0,137г, метилметанамоній тетрафлуорборат (7,770г, 0,296ммоль) розчиняють у суміші ацетоніт24,200ммоль) та N-етил-N,N-дізопропіламін рил/вода (1/1, 4мл), додають літій гідроксид (5,971г, 46,200ммоль) додають. Розчин перемішу(0,014г, 0,591ммоль). Реакційну суміш перетворюють протягом двох годин при кімнатній температують в одиничному вузлі мікрохвильової шафи (5 рі. EtOAc (20мл) додають та органічну фазу прохвилин, 150град). Обробляють видаленням розмивають натрій карбонатом (3 X 20мл, водн.) та чиннику випарюванням та додаванням НСІ (2мл, НСІ (0,5М, 2 X, 10мл). Органічний шар сушать маг1М). Водну фазу екстрагують двома порціями ній сульфатом та розчинник видаляють випарюEtOAc (20мл), органічну фазу сушать магній сульванням. Сирий матеріал очищають препаративфатом та розчинник видаляють випарюванням та ною ВЕРХ (починаючи з ізократичної суміші отримують 0,111г 2-{[2-(4-{2-[бензил(етил)аміно]-2ацетонітрил/буфер 60/40 та тоді концентрацію оксоетокси}феніл)етил]-тіо}бензойної кислоти (виацетонітрилу збільшують до 100%, буфером є сухід 83,5%). міш ацетонітрил/вода 10/90 та амоній ацетат 1 (0,1М, колонка KR-100-7-С8, 50мм X 250мм, потік Н ЯМР (ротамери, 400МГц, CDCI3): 1,0240мл/хвилин). Продукт, що містить фракції, поєд1,30 (bm, 3Н), 2,95 (q, 2H), 3,15 (q, 2H), 3,40 (m, нують та ацетонітрил видаляють випарюванням. 2H), 4,58 (s, 2H), 4,63-4,92 (bm, 4H), 6,85-7,0 (bm, EtOAc (10мл) додають та органічну фазу проми2H), 7,0-7,53 (m, 10Н), 7,97 (d, 1H). вають двома порціями розсолу та сушать магній Приклад 11 сульфатом і розчинник видаляють випарюванням а) N-(4-трет-бутилбензил)-N-етиламін (0,143г, та отримують 1,344г N-(4-флуорбензил)ацетаміду 0,746ммоль) розчиняють у сухому ацетонітрилі під (вихід 36,5%). азотом та додають N-етил-N,N-діізопропіламін 1 (0,371г, 2,867ммоль). Суміш перемішують протяН ЯМР (500МГц, CDCI3): 1,98 (s, 3Н), 4,35 (d, гом 30 хвилин та додають метил 2-{2-[4-(2-хлор-22H), 6,25 (bs, 1H), 6,95-7,25 (bm, 4H) оксоетокси)феніл]етокси}бензоат (0,200г, b) N-(4-Флуорбензил)ацетамід (1,344г, 0,573ммоль). Розчин перемішують протягом ночі 8,039ммоль) розчиняють у ТГФ (100мл) та охолопри кімнатній температурі. Сирий матеріал очиджують до нуля градусів в атмосфері аргону, (комщають флеш-хроматографією (починаючи з ізокплекс (метилтіо)метану з бораном (1:1) (1,527г, ратичної суміші гептан/EtOAc 50/50 та тоді концен20,098ммоль) додають та суміш кип'ятять під звотрацію EtOAc збільшують до 100%, (силікагель 60 ротним холодильником протягом ночі при кімнат0,004-0,063мм). Продукт, що містить фракції, поній температурі. НСІ (15мл, 10%) обережно додаєднують та EtOAc видаляють випарюванням з ють та перемішують протягом ночі. Розчинник утворенням 0,229г метил 2-[2-(4-{2-[(4-третвидаляють випарюванням. Діетиловий етер (20мл) бутилбензил)(етил)аміно]-2додають та продукт екстрагують у водну фазу каоксоетокси}феніл)етокси]бензоату (вихід 79,3%). лій карбонатом (3 Х 15мл). Водну фазу підкислю1 ють НСІ (10мл, 10%) та продукт екстрагують в орН ЯМР (ротамери, 500МГц, CDCI3): 1,07ганічну фазу EtOAc (3 X 15мл). Органічну фазу 1,23 (bm, 3H), 2,23 (m, 9H), 3,08 (m, 2H), 3,30-3,5 сушать магній сульфатом та розчинник видаляють (bm, 2H), 3,87 (s, 3H), 4,18 (m, 2H), 4,58 (d, 2H), 31 76627 32 випарюванням з утворенням 0,309г N-(4ВЕРХ (починаючи з ізократичної суміші ацетонітфлуорбензил)етанаміну (вихід 25,1%). рил/буфер 60/40 та тоді концентрацію ацетонітри1 лу збільшують до 100%, буфером є суміш ацетоніН ЯМР (400МГц, CDCI3): 1,05 (t, 3Н), 1,1 (s, трил/вода 10/90 та амоній ацетат (0,1М, колонка 1H), 2,58 (q, 2H), 3,64 (s, 2H), 6,9 (t, 2H), 7,2 (t, 2H). KR-100-7-С8,50мм X 250мм, потік 40мл/хвилин). c) N-(4-флуорбензил)етанам1н (0,114г, Продукт, що містить фракції, поєднують та ацето0,745ммоль) розчиняють у сухому ацетонітрилі під нітрил видаляють випарюванням. EtOAc (10мл) азотом та додають N-етил-N-дизопропіламін додають та органічну фазу промивають двома (0,371г, 2,867ммоль). Суміш перемішують протяпорціями розсолу та сушать магній сульфатом. гом 30 хвилин та додають метил 2-{2-[4-(2-хлор-2Розчинник видаляють випарюванням з утворенням оксоетокси)феніл]-етокси}бензоат (0,200г, 3,825г [4-(2-{[20,573ммоль). Розчин перемішують протягом ночі (метоксикарбоніл)феніл]тіо}етил)фенокси]-оцтової при кімнатній температурі. Сирий матеріал очикислоти (вихід після двох етапів 63,9% від загальщають флеш-хроматографією (починаючи з ізокного). ратичної суміші гептан/EtOAc 50/50 та тоді концен1 Н ЯМР (500 МГц, CDCI3): 2,82 (t, 2H), 3,15 (t, трацію EtOAc збільшують до 100%, (силікагель 60 0,004-0,063мм). Продукт, що містить фракції, по2H), 3,82 (s, 3Н), 4,35 (s, 2H), 6,78 (d, 2H), 7,18 (d, єднують та EtOAc видаляють випарюванням з 2H), 7,23 (t, 1H), 7,51 (d, 1H), 7,55 (t, 1H), 7,85 (d, утворенням 0,223г метил 2-[2-(4-{2-[етил(41H). флуорбензил)аміно]-2c) [4-(2-{[2-(Метоксикарбоніл)феніл]тіо}етил) оксоетокси}феніл)етокси]бензоат (вихід 83,5%). фенокси]оцтову кислоту (0,250г, 0,722ммоль) роз1 чиняють у ДХМ (10мл), додають N-(2Н ЯМР (400МГц, CDCI3): 1,07-1,23 (bm, 3Н), флуорбензил)етанамін (0,105г, 0,686ммоль). N3,08 (m, 2H), 3,30-3,45 (bm, 2H), 3,87 (s, 3Н), 4,18 [(1Н-1,2,3-бензотриазол-1(m, 2H), 4,58 (s, 2H), 4,63-4,8 (m, 2H) 6,77-7,45 (m, ілокси)(диметиламіно)метилен]-N11Н), 7,78 (d, 1H). метилметанамоній тетрафлуорборат (0,255г, d) Метил 2-[2-(4-{2-[етил(40,0,794ммоль) та N-етил-N,N-дізопропіламін флуорбензил)аміно]-2-оксоетокси}феніл)етокси](0,187г, 1,443ммоль) додають. Розчин перемішубензоат (0,223г, 0,479ммоль) розчиняють у суміші ють протягом 2 годин при кімнатній температурі. ТГФ (свіжо-перегнаний)/вода (2/1,3мл), додають Сирий матеріал очищають флеш-хроматографією літій гідроксид (0,229г, 0,958ммоль). Реакційну (починаючи з ізократичної суміші ДХМ 100% та суміш перетворюють в одиничному вузлі мікрохтоді МеОН концентрацію збільшують від 0,5% до вильової шафи (5 хвилин, 150град). ТГФ видаля20%, (силікагель 60 0,004-0,063мм). Продукт, що ють випарюванням. Додають воду (10мл) та осномістить фракції, поєднують та EtOAc видаляють вну водну фазу промивають діетиловим етером (2 випарюванням. Речовина потребує кращої очистки X 10мл). Додавання НСІ (2мл, 1М, рН 1). Водну та її очищають препаративною ВЕРХ (починаючи з фазу екстрагують двома порціями ДХМ (20мл), ізократичної суміші ацетонітрил/буфер 60/40 та органічну фазу сушать магній сульфатом та розтоді концентрацію ацетонітрилу збільшують до чинник видаляють випарюванням з утворенням 100%, буфером є суміш ацетонітрил/вода 10/90 та 0,196г 2-[2-(4-{2-[етил(4-флуорбензил)аміно]-2амоній ацетат (0,1М, колонка KR-100-7-С8,50мм X оксоетокси}феніл)етокси]бензойної кислоти (вихід 250мм, потік 40мл/хвилин). Продукт, що містить 90,6%). 1 фракції, поєднують та ацетонітрил видаляють виН ЯМР (ротамери, 500МГц, CDCI3): 1,03парюванням. Амоній ацетат видаляють сушкою 1,21 (bm, 3Н), 3,1 (m, 2H), 3,23-3,4 (bm, 2H), 4,38 сублімацією продукту протягом ночі, з утворенням (m, 2H), 4,55 (s, 2H), 4,63-4,78 (m, 2H), 6,75-7,22 0,1г метил 2-{[2-(4-{2-[етил(2-флуорбензил)аміно](m, ЮН), 7,47 (t, 1H), 8,07 (d, 1H). 2-оксоетокси}феніл)етил]тіо}бензоату (вихід Приклад 13 29,1%). а) Трет-бутил (4-{21 Н ЯМР (ротамери, 500МГц, CDCI3): 1,03[(метилсульфоніл)окси]етил}фенокси)ацетат 1,23 (bm, 3Н), 2,95 (q, 2H), 3,15 (m, 2H), 3,40 (m, (5,454г, 17,347ммоль) розчиняють в ацетонітрилі 2H), 3,9 (s, 3Н), 4,6-4,8 (bm, 4H), 6,75-6,95 (m, 2H), (100мл), додають метил 2-меркаптобензоат 6,97-7,5 (m, 9H), 7,97 (d, 1H). (3,502г, 20,816ммоль) та дикалій карбонат (4,795г, d) Метил 2-{[2-(4-{2-[етил(234,694ммоль). Розчин перемішують протягом 10 флуорбензил)аміно]-2-оксоетокси}феніл)етил]тіо}годин при 60°С. EtOAc (40мл) додають та органічбензоат розчиняють у суміші ТГФ (свіжону фазу промивають двома порціями розеолу (2 Χ перегнаний)/вода (2/1,3мл), додають літій гідрок40мл, водн.). Органічний шар сушать магній сульсид (0,015г, 0,629ммоль). Реакційну суміш перетфатом та розчинник видаляють випарюванням з ворюють в одиничному вузлі мікрохвильової шафи утворенням 6,931г сирого метил 2-({2-[4-(2-трет(5 хвилин, 150град). ТГФ видаляють випарюванбутокси-2-оксоетокси)феніл]етил}тіо)-бензоату. ням. Додають воду (10мл) та основну водну фазу Сирий матеріал використовують на наступному промивають діетиловим етером (2 X 10мл). Додаетапі без очистки. ють НСІ (2мл, 1М, рН 1). Водну фазу екстрагують b) Метил 2-({2-[4-(2-трет-бутокси-2двома порціями ДХМ (20мл), органічну фазу суоксоетокси)феніл]етил}тіо)бензоат (4,630г, шать магній сульфатом та розчинник видаляють 11,502ммоль) уводять у ДХМ (50мл) та оброблявипарюванням з утворенням 0,095г 2-{[2-(4-{2ють трифлуороцтовою кислотою (44,40г, [етил(2-флуорбензил)аміно]-2389,405ммоль) при кімнатній температурі протягом оксоетокси}феніл)етил]тіо}бензойної кислоти (ви4 годин. Суміш випарюють та переганяють з толухід 96,9%) олом. Сирий матеріал очищають препаративною 33 76627 34 парюванням. Амоній ацетат видаляють сушкою Н ЯМР (ротамери, 400МГц, CDCI3): 1,02сублімацією продукту протягом ночі, з утворенням 1,25 (bm, 3Н), 2,95 (q, 2H), 3,15 (q, 2H), 3,42 (m, 0,111г метил 2-{[2-(4-{2-[(22H), 4,60-4,80 (bm, 4H), 6,75-6,95 (m, 2H), 6,95-7,5 хлорбензил)(етил)аміно]-2(m, 9H), 8,1 (d, 1H). оксоетокси}феніл)етил]тіо}бензоату (вихід 30,9%). Приклад 14 1 a) Трет-бутил (4-{2Н ЯМР (ротамери, 500МГц, CDCI3): 1,10[(метилсульфоніл)окси]етил}фенокси)ацетат 1,25 (bm, 3Н), 2,95 (m, 2H), 3,15 (m, 2H), 3,40 (m, (5,454г, 17,347ммоль) розчиняють в ацетонітрилі 2H), 3,9 (s, 3Н), 4,6-4,8 (bm, 4H), 6,75-6,95 (m, 2H), (100мл), додають метил 2-меркаптобензоат 7,02-7,5 (m, 9H), 7,95 (d, 1H). (3,502г, 20,816ммоль) та дикалій карбонат (4,795г, d) Метил 2-{[2-(4-{2-[(234,694ммоль). Розчин перемішують протягом 10 хлорбензил)(етил)аміно]-2годин при 60°С. EtOAc (40мл) додають та органічоксоетокси}феніл)етил]тіо}-бензоат розчиняють у ну фазу промивають двома порціями розеолу (2 Χ суміші ТГФ (свіжо-перегнаний)/вода (2/1,3мл), літій 40мл, водн.). Органічний шар сушать магній сульгідроксид (0,015г, 0,629ммоль) додають. Реакційну фатом та розчинник видаляють випарюванням з суміш перетворюють в одиничному вузлі мікрохутворенням 6,931г сирого метил 2-({2-[4-(2-третвильової шафи, (5 хвилин, 150град). ТГФ видалябутокси-2-оксоетокси)феніл]етил}тіо)бензоату. ють випарюванням. Додають воду (10мл) та осноСирий матеріал використовують на наступному вну водну фазу промивають діетиловим етером (2 етапі без очистки. X 10мл). Додають НСІ (2мл, 1М, рН 1). Водну фазу b) Метил 2-({2-[4-(2-трет-бутокси-2екстрагують двома порціями ДХМ (20мл). Органічоксоетокси)феніл]етил}тіо)бензоат (4,630г, ну фазу сушать магній сульфатом та розчинник 11,502ммоль) уводять у ДХМ (50мл) та оброблявидаляють випарюванням з утворенням 0,103г 2ють трифлуороцтовою кислотою (44,40г, {[2-(4-{2-[(2-хлорбензил)(етил)аміно]-2389,405ммоль) при кімнатній температурі протягом оксоетокси}феніл)етил]тіо}бензойної кислоти (ви4 годин Суміш випарюють та переганяють з толухід 95,5%) 1 олом. Сирий матеріал очищають препаративною Н ЯМР (ротамери, 400МГц, CDCI3): 1,07ВЕРХ (починаючи з ізократичної суміші ацетоніт1,25 (bm, 3Н), 2,95 (m, 2H), 3,15 (m, 2H), 3,42 (m, рил/буфер 60/40 та тоді концентрацію ацетонітри2H), 4,62-4,85 (bm, 4H), 6,75-6,95 (m, 2H), 7,02-7,5 лу збільшують до 100%, буфером є суміш ацетоні(m, 9H), 8,1 (d, 1H). трил/вода 10/90 та амоній ацетат (0,1М, колонка Біологічна активність KR-100-7-C8,50мм X 250мм, потік 40мл/хвилин). Композиції Продукт, що містить фракції, поєднують та ацетоСполуки розчиняють у ДМСО для отримання нітрил видаляють випарюванням. EtOAc (10мл) 16мМ вихідних розчинів. Для дослідження вихіддодають та органічну фазу промивають двома ний розчини подалі розводять ДМСО та культивапорціями розсолу та сушать магній сульфатом. ційними середовищами. Розчинник видаляють випарюванням з утворенням Загальні хімікати та реактиви 3,825г [4-(2-{[2-(метоксикарбоніл)феніл]тіо}етил)Реагент дослідження люциферази отримано фенокси]оцтової кислоти (вихід після двох етапів від Packard, USA. Рестрикційні ферменти отрима63,9% від загального). но від Boehringer та Vent-полімераза від New 1 Н ЯМР (500МГц, CDCI3): 2,82 (t, 2H), 3,15 (t, England Biolabs. 2H), 3,82 (s, 3Н), 4,35 (s, 2H), 6,78 (d, 2H), 7,18 (d, Лінії клітин та умови культивації клітин 2H), 7,23 (t, 1H), 7,51 (d, 1H), 7,55 (t, 1H), 7,85 (d, U2-OS, (Остеогенна саркома людини) отрима1H). но з АТСС, USA. Клітини нарощують та знов замоc) [4-(2-{[2-(метоксикарбоніл)феніл]тіо}етил) рожують партіями від числа переносу 6. Клітини фенокси]оцтову кислоту (0,250г, 0,722ммоль) розкультивують у середовищі Дульбекко, модифікочиняють у ДХМ (10мл) та додають N-(2ваному Іглом (DMEM) з 25мМ глюкози, 2мМ глутахлорбензил)-N-етиламiн (0,116г, 0,686ммоль). Nміну або 4мМ L-аланіл-L-глутаміну, 10% сироватки [(1Н-1,2,3-бензотриазол-1зародка теляти, при 5% СО2. Використовують буілокси)(диметиламіно)метилен]-Nферований фосфатом фізіологічний розчин етилметанамоній тетрафлуорборат (0,255г, (БФФР) без додавання кальцію або магнію. Усі 0,0,794ммоль) та N-етил-N,N-діізопропіламін реактиви культур клітин отримано від Gibco (USA) (0,187г, 1,443ммоль) додають. Розчин перемішута 96-коміркові планшети культур клітин отримано ють протягом 2 годин при кімнатній температурі. від Wallach. Сирий матеріал очищають флеш-хроматографією Констракти плазмід для гетерологічної експре(починаючи з ізократичної суміші ДХМ 100% та сії тоді концентрацію МеОН збільшують від 0,5% до Стандартні рекомбінантні способи ДНК прово20%, (силікагель 60 0,004-0,063мм). Продукт, що дять, як описано Ausubel (7). Репортерний люцимістить фракції, поєднують та EtOAc видаляють феразний вектор, pGLSUAS (клон складається з 5 випарюванням. Речовина потребує кращої очистки копій зв'язувальної послідовності ДНК GAL4, 5'та її очищають препаративною ВЕРХ (починаючи з CGACGGAGTACTGTCCTCCGAGCT-3', клоновано ізократичної суміші ацетонітрил/буфер 60/40 та у сайти Sacl/Xhol промотеру pGL3 (Promega). Фратоді концентрацію ацетонітрилу збільшують до гмент Sacl/Xhol, що несе сайти UAS, створюють, 100%, буфером є суміш ацетонітрил/вода 10/90 та застосовуючи гібридизовані перекривувані олігоамоній ацетат (0,1М, колонка KR-100-7-C8,50мм X нуклеотиди. 250мм, потік 40мл/хвилин). Продукт, що містить Використані вектори експресії базуються на фракції, поєднують та ацетонітрил видаляють виpSG5 (Stratagene). Усі вектори містять фрагмент 1 35 76627 36 EcoRI/Nhel, що кодує зв'язувальний домен ДНК ΑΠΠΡ , клітинне середовищ доповнюють десорGAL4 (що кодує амінокислотні позиції 1-145, вхідбованою смолою-вугіллям сироваткою зародка ний номер бази даних Р04386), а потім конденсотеляти (СЗТ) для запобігання зворотного активуваний у рамці з фрагментом, що кодує послідоввання жирно-кислотними компонентами СЗТ. Деність нуклеарної локалізації від Т-антигену вірусу сорбовану смолою-вугіллям СЗТ продукують, як поліоми. Послідовність нуклеарної локалізації нижченаведено; до 500мл активованої теплом створюють, застосовуючи гібридизовані перекриСЗТ додають 10г вугілля та 25г аніонообмінної вувані олігонуклеотиди, створені Nhel/Kpnl клейсмоли для аналізу Bio-Rad 200-400меш, та розчин кими кінцями (5'перемішують на магнітній мішалці при кімнатній CTAGCGCTCCTAGAAGAAACGCAAGGTTGGTACтемпературі протягом ночі. Наступної доби СЗТ 3'). Ліганд-зв'язувальні домени від АППР людини центрифугують та десорбування повторюють протягом 4-6 годин. Після другої обробки, СЗТ та миші та АППР людини та миші ПЛРцентрифугують та фільтр стерилізують для видаампліфікують, як фрагменти Kpnl/BamHI та клонулення залишків вугілля та смоли. ють у рамці до зв'язувального домену ДНК GAL4 Спосіб дослідження та послідовності нуклеарної локалізації. ПослідовВихідний розчини сполук у ДМСО розводять ності усіх використаних констрактів плазмід підтдо прийнятної концентрації в еталонних планшеверджені секвенсуванням. Наступні вектори екстах. З еталонних планшетів сполуки розводять у пресії використовують для тимчасових культиваційних середовищах для отримання розтрансфекцій: чинів тест-сполук для кінцевих доз. Після доведення кількості середовища клітин підтип кодованого довідкові послівектор до 75мкл у кожній комірці, додають 50мкл розчину АППР довності тест-сполуки. Тимчасово трансфектовані клітини S74349, nt 625pSGGALhPPa ΑΠΠΡ людини піддають дії сполуки протягом приблизно 24 годин 1530 до здійснення дослідження люциферази. Для досХ57 638, nt 668pSGGALmPPa ΑΠΠΡ миші лідження люциферази, 100мкл реагенту для дос1573 лідження додають вручну до кожної комірки та U63415, nt 613pSGGALhPPg ΑΠΠΡ людини планшети залишають протягом приблизно 20 хви1518 лин для лізису клітин. Після лізису люциферазну U09138, nt 652pSGGALmPPg АППР миші активність виміряно у мультикомірковому лічиль1577 нику 1420, Victor, від Waflach. Контрольні сполуки 1 стосується позиції нуклеотиду з входу бази TZD-піоглітазон використовують, як контрольданих, що використано для вираження лігандну речовину для активування АППР людини та зв'язувального домену. миші. 5,8,11,14-Ейкозатетрайонову кислоту (ЕТЙК) використовують, як контрольну речовину для Перехідні трансфекції АППР людини. Заморожені вихідні розчини клітин від числа Розрахунки та аналіз переносу 6 розморожують та нарощують до числа Для розрахунку величин ЕК50 будують криву переносу 8 для трансфекції. Конфлюєнтні клітини концентрація-ефект. Використані величини є похітрипсинізують, промивають та гранулюють дними від середнього двох або трьох незалежних центрифугуванням при 270 g протягом 2 хвилин. вимірів (після віднімання фонової середньої велиГранулу клітин ресуспендують у холодному БФФР чини) та виражені, як процент від максимального 6 до концентрації клітин приблизно 18 10 клітин/мл. активування, отриманого від контрольної сполуки. Після додавання ДНК, суспензію клітин інкубують Величини відкладають проти логарифмів концентна льоду протягом приблизно 5 хвилин до електрацій тест-сполук. Величини ЕК50 встановлюють ропорації при 230V, 960мкФ у Biorad's Gene лінійною інтерполяцією між даними точками та Pulser партіями по 0,5мл. Усього 50мкг ДНК дорозрахованими концентраціями, потрібними для дають до кожної партії по 0,5мл клітини, залучаюдосягнення 50% максимального активування, чи 2,5мкг вектору експресії, 25мкг репортерного отриманого від контрольної сполуки. вектору та 22,5мкг неспецифічної ДНК (pBluescript, Сполуки формули І мають ЕК50 менше Stratagene). 50мкмоль/л для АППР , а кращі сполуки мають Після електропорації, клітини розводять до ЕК50 менше 5мкмоль/л, наприклад, ЕК50 з деяких концентрації приблизно 320000клітин/мл у DMEM прикладів для АППР-альфа людини такі: без фенол-червоного, та приблизно Приклад 3 0,499мкмоль/л; та приклад 5 25000клітин/комірку засівають у 96-коміркові 0,048мкмоль/л. планшети. Для зворотного отримання клітин засіяні планшети інкубують при 37°С протягом 3-4 годин до додавання тест-сполук. У дослідженнях Комп’ютерна верстка О. Гапоненко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюBenzoic acid derivatives with ortho-substituents for treating insulin resistance
Автори англійськоюLi Lanna
Назва патенту російськоюОрто-производные бензойной кислоты для лечения резистентности к инсулину
Автори російськоюЛи Ланна
МПК / Мітки
МПК: A61P 3/06, C07C 323/62, A61K 31/19, C07C 235/20, A61P 3/10
Мітки: лікування, бензойної, кислоти, орто-похідні, резистентності, інсуліну
Код посилання
<a href="https://ua.patents.su/18-76627-orto-pokhidni-benzojjno-kisloti-dlya-likuvannya-rezistentnosti-do-insulinu.html" target="_blank" rel="follow" title="База патентів України">Орто-похідні бензойної кислоти для лікування резистентності до інсуліну</a>
Попередній патент: Конвекторне кільце
Наступний патент: Пристрій для виявлення дефектів на працюючому обладнанні
Випадковий патент: Трансформаторна підстанція












