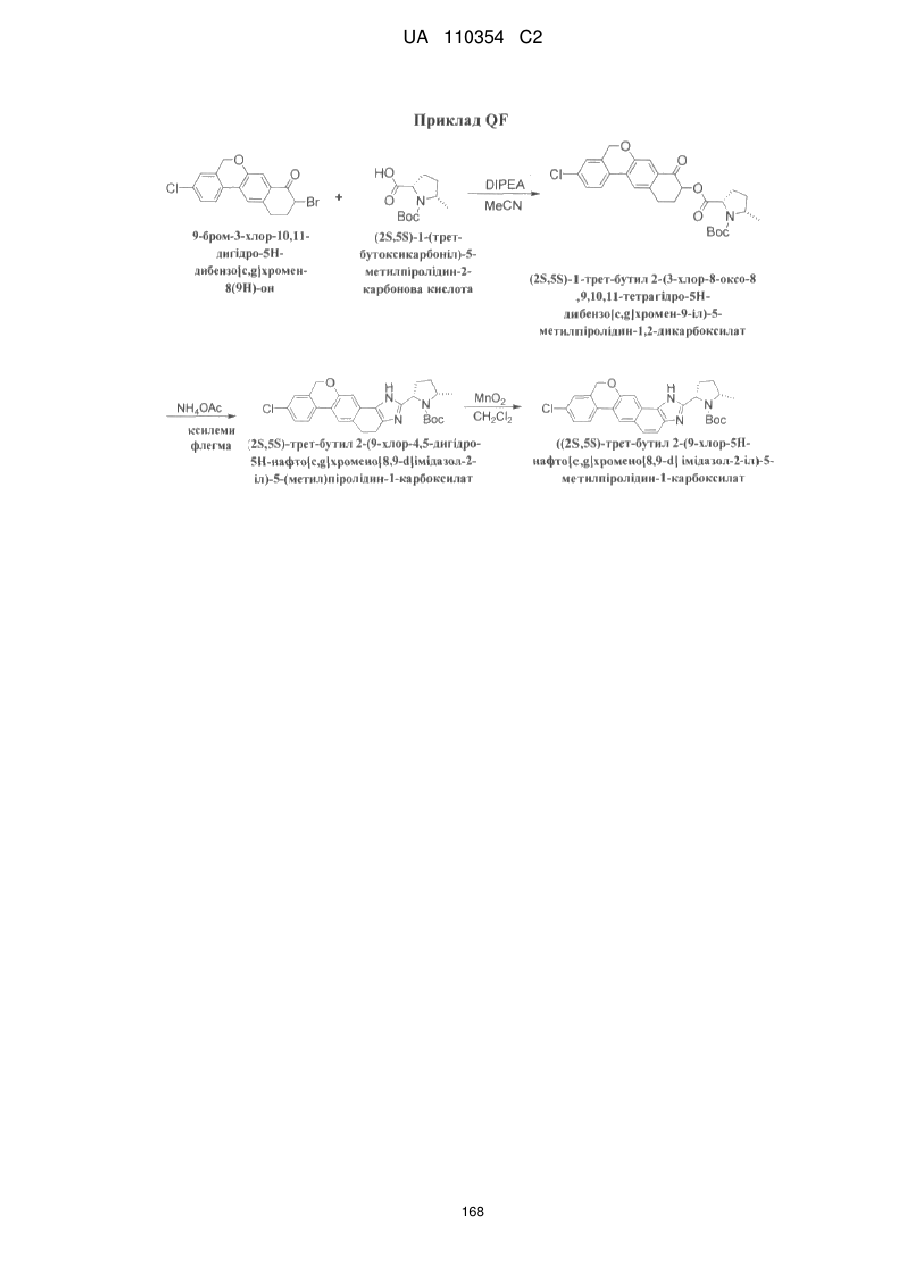
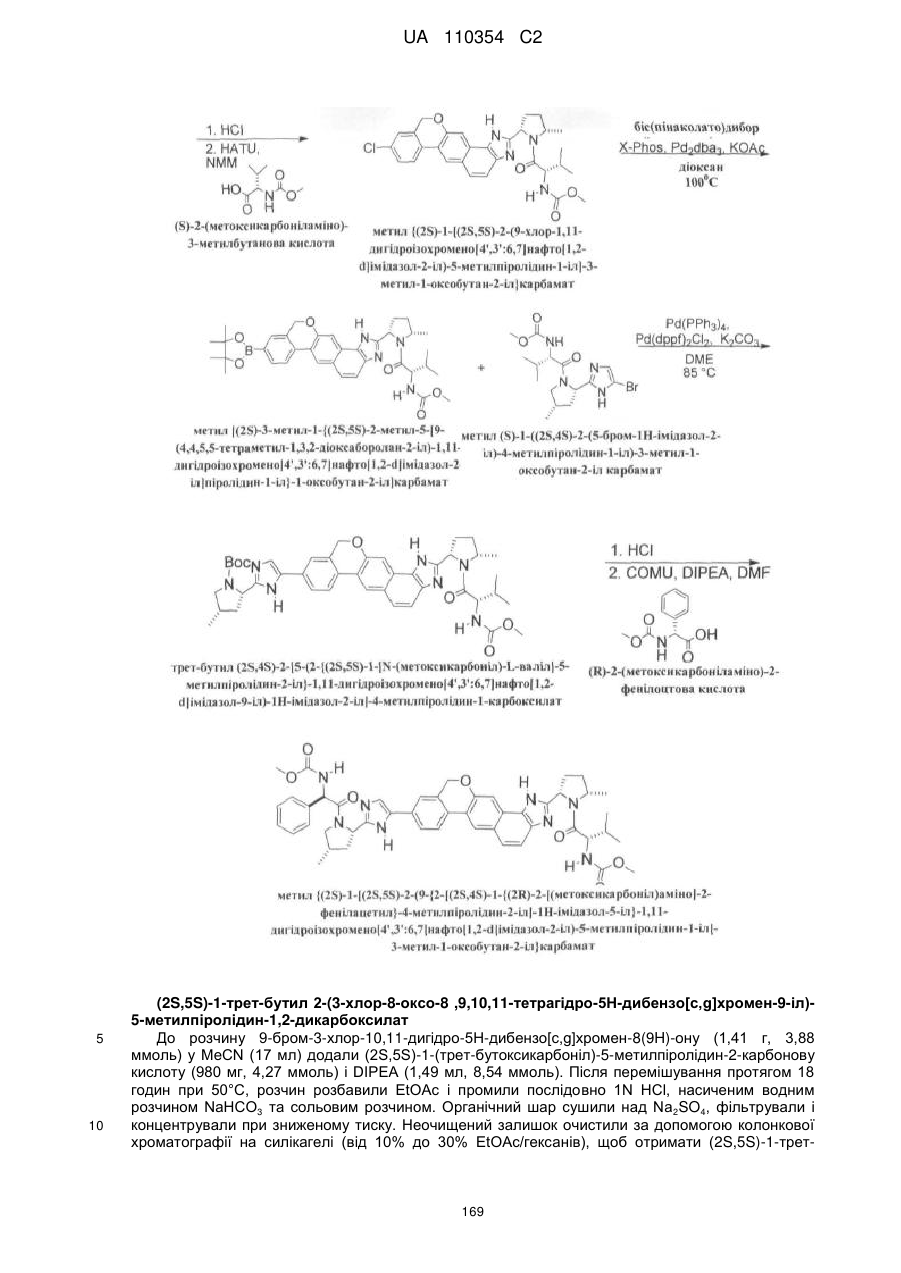
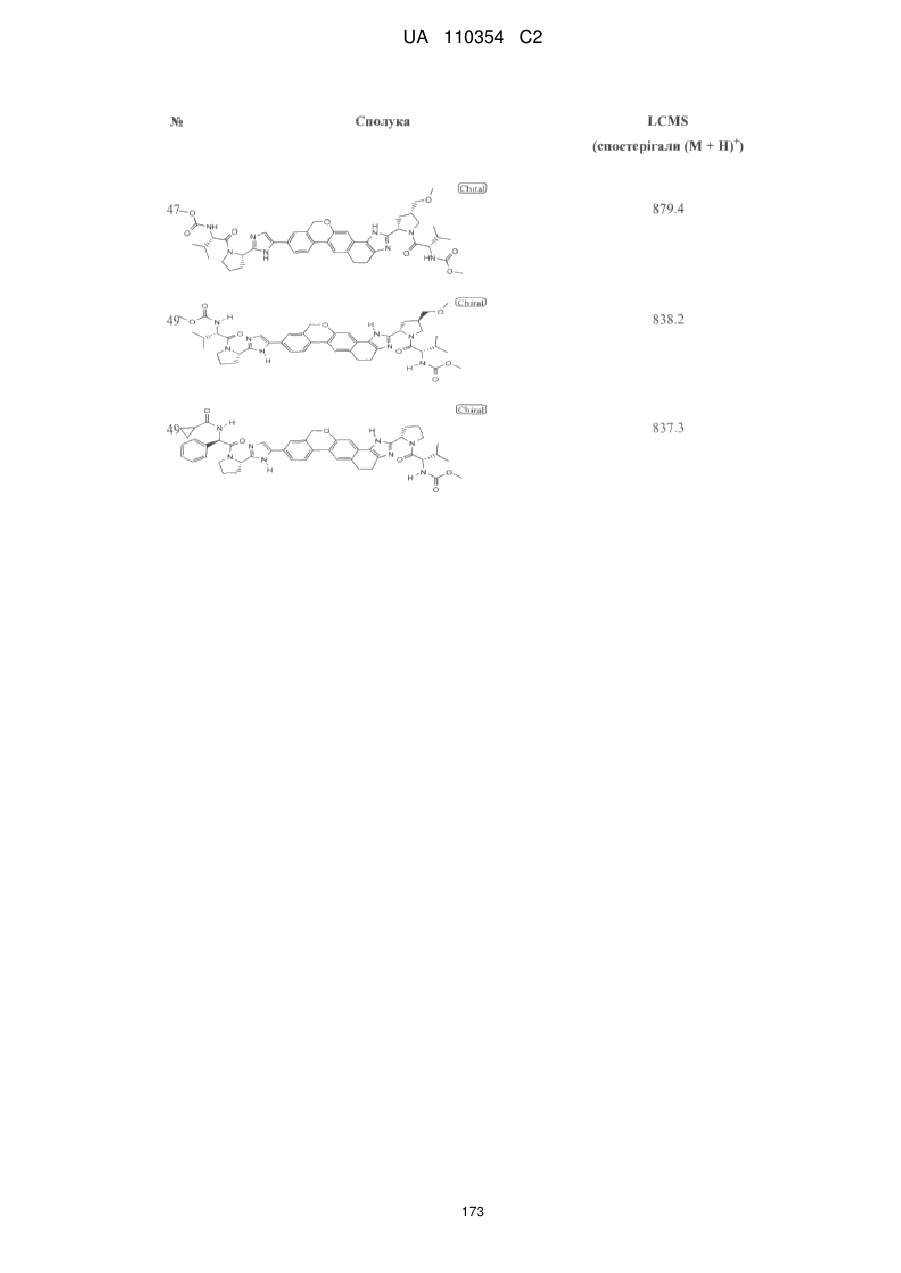
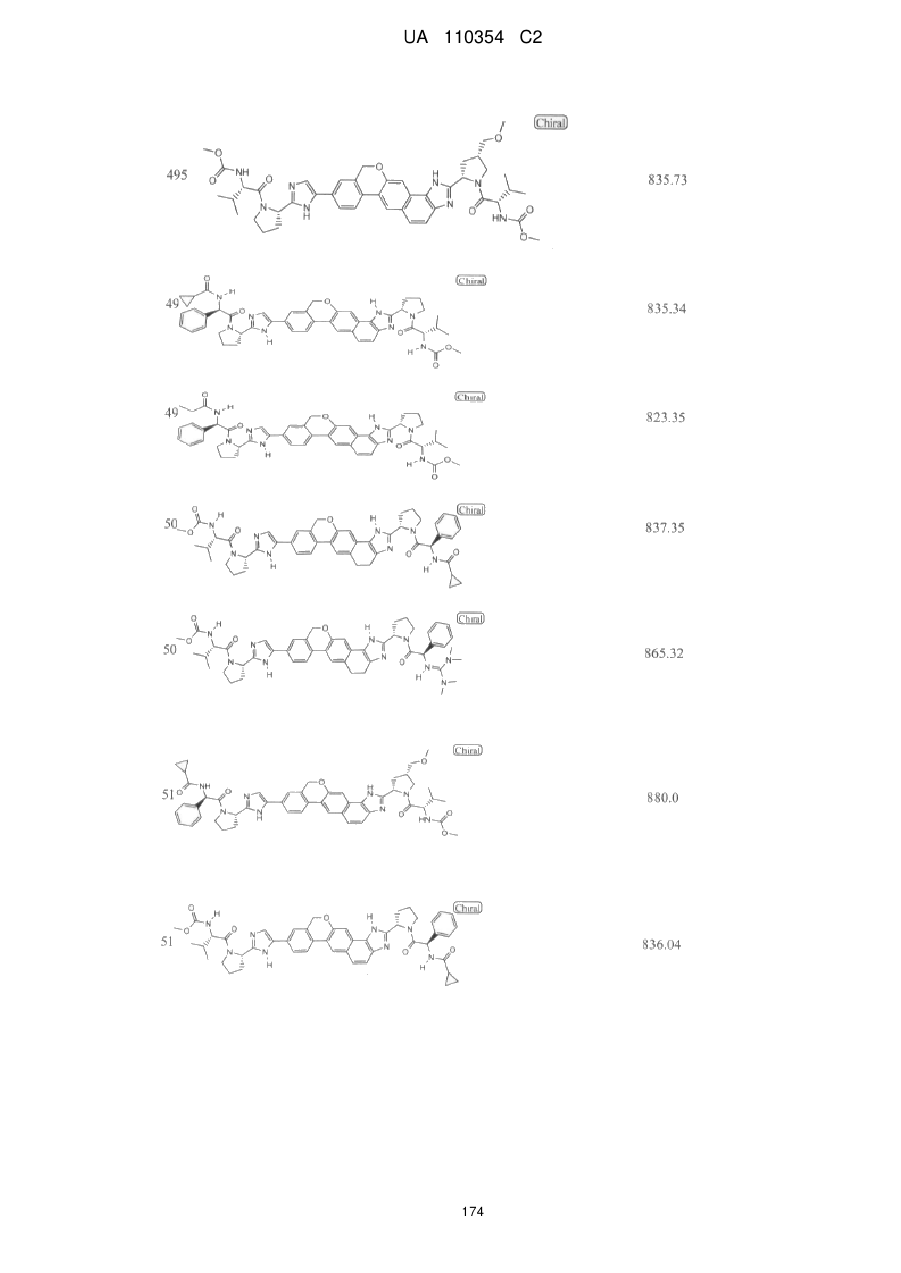
Противірусні сполуки
Номер патенту: 110354
Опубліковано: 25.12.2015
Автори: Тран Чінх В'єт, Лінк Джон О., Коттелл Джеромі Дж., Катана Ешлі Енн, Кейто Дерріл, Криговські Еван С., Тейлор Джеймс, Ян Чжен-Ю, Бейкон Елізабет М., Ципфель Шейла, Трехо Мартін Тереса Алехандра
Формула / Реферат
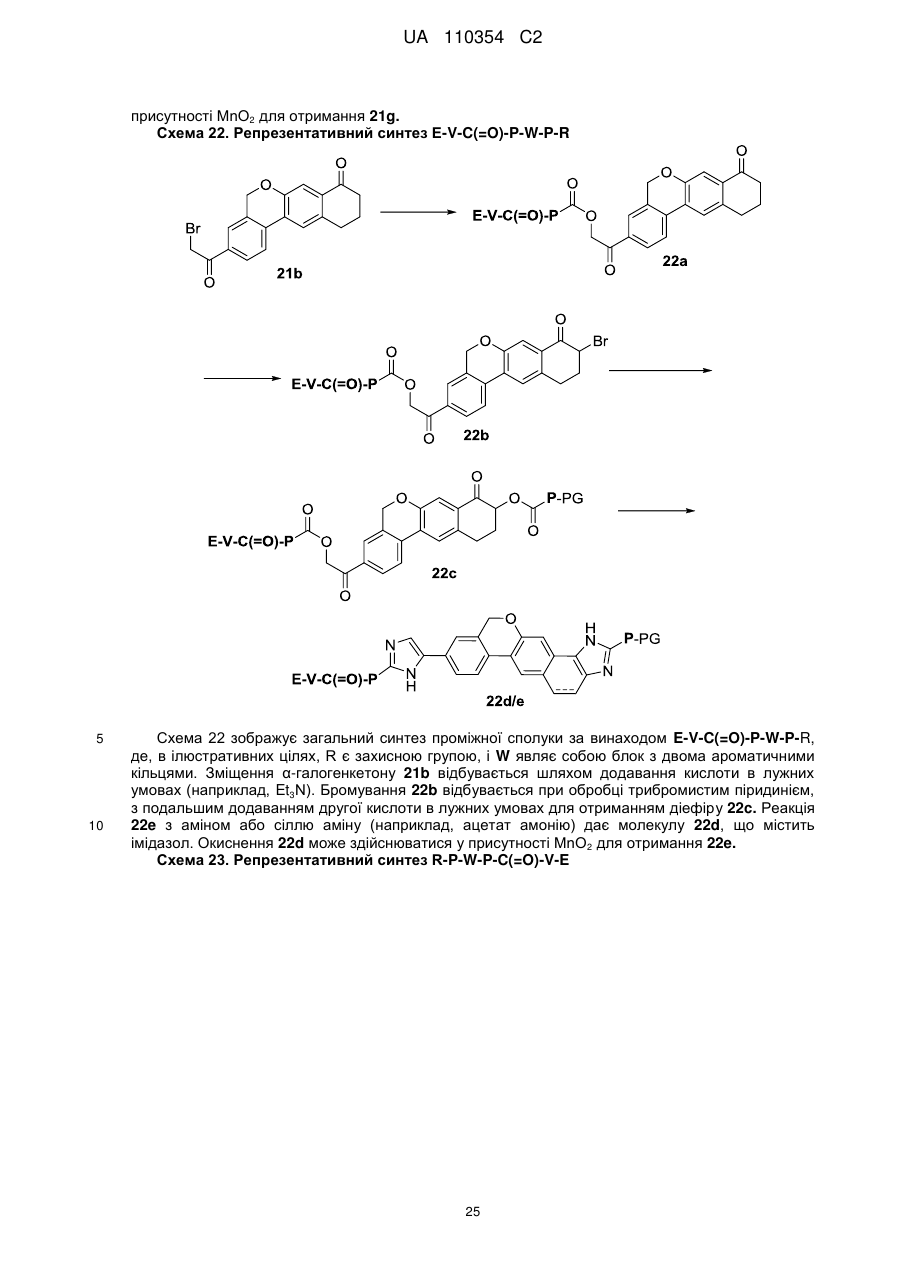
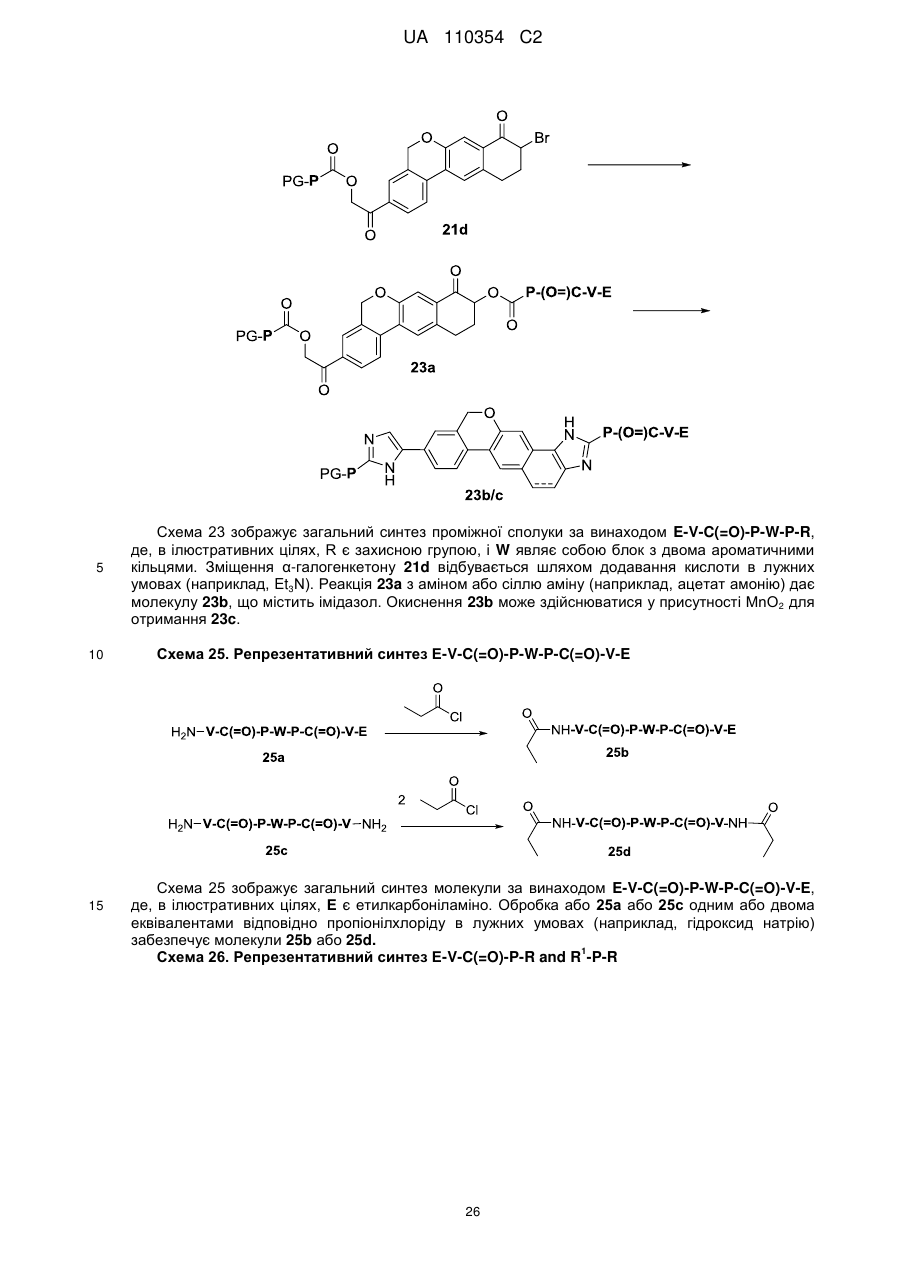
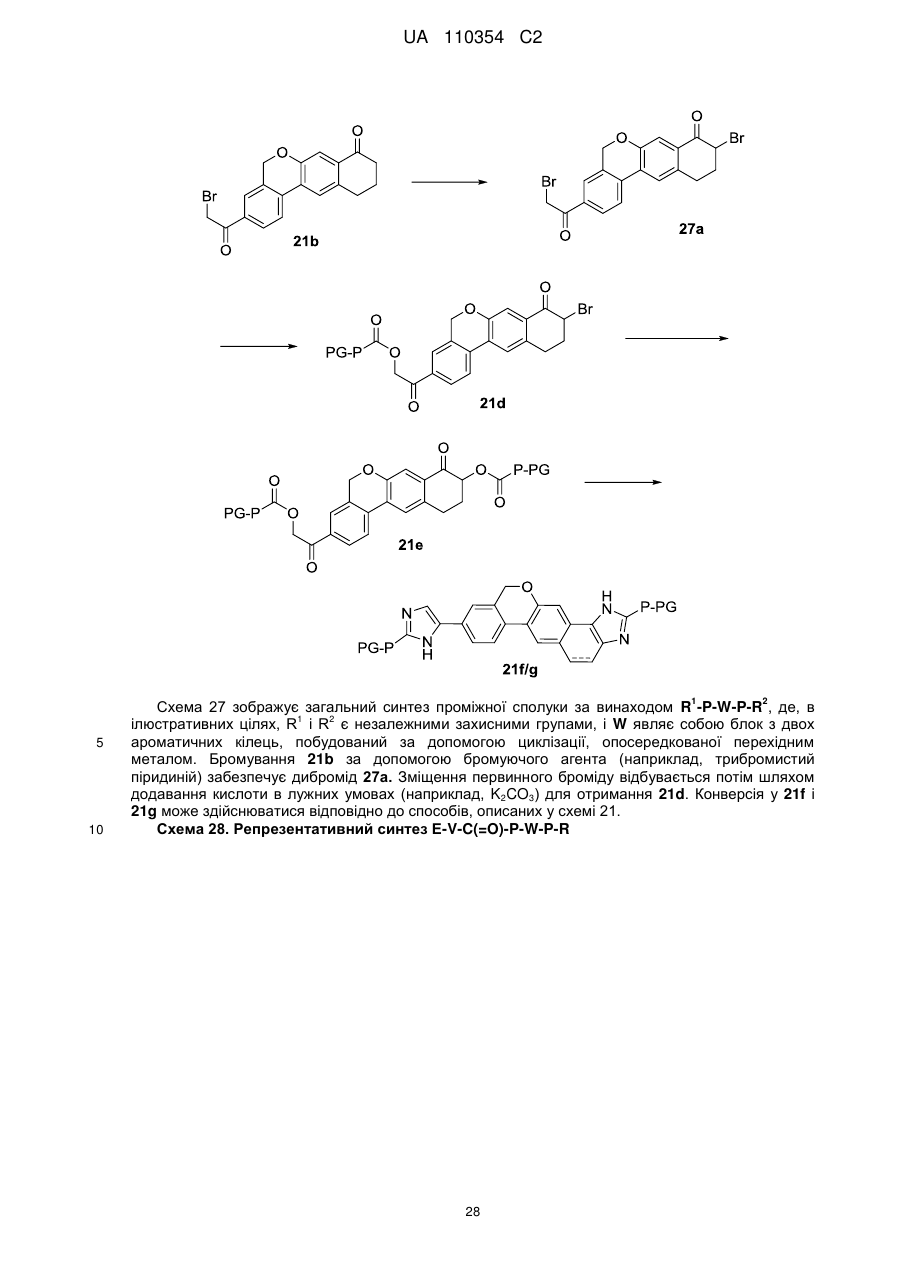
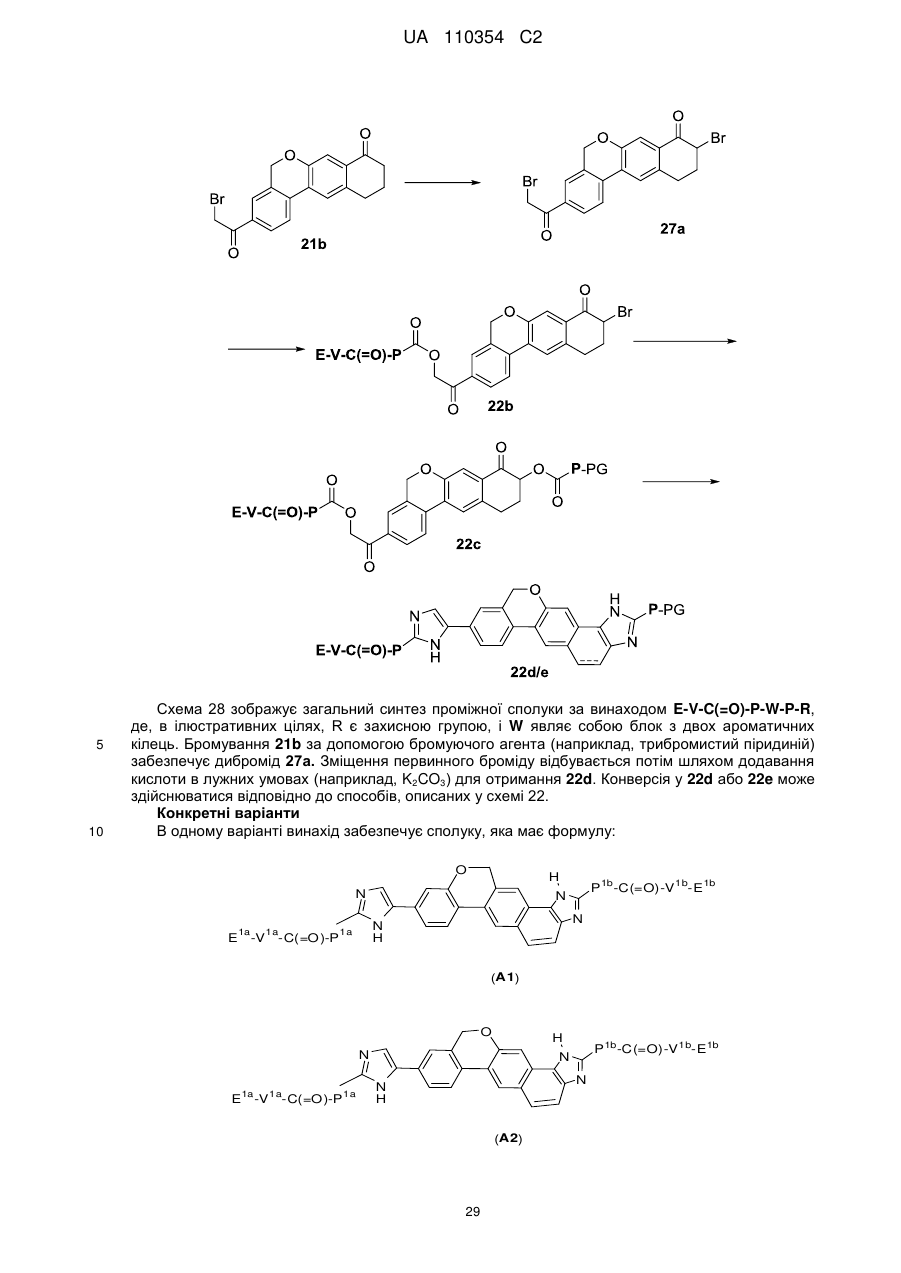
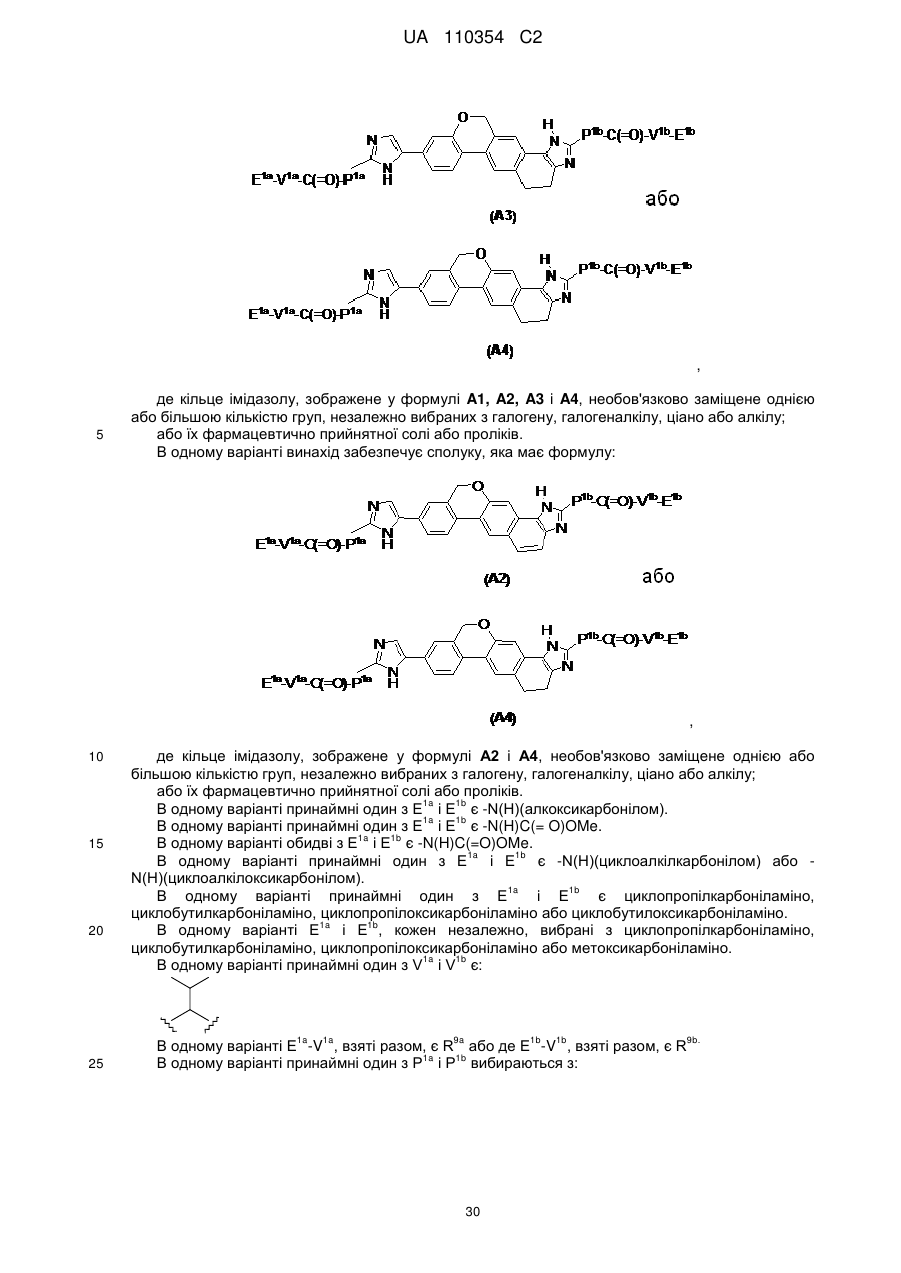
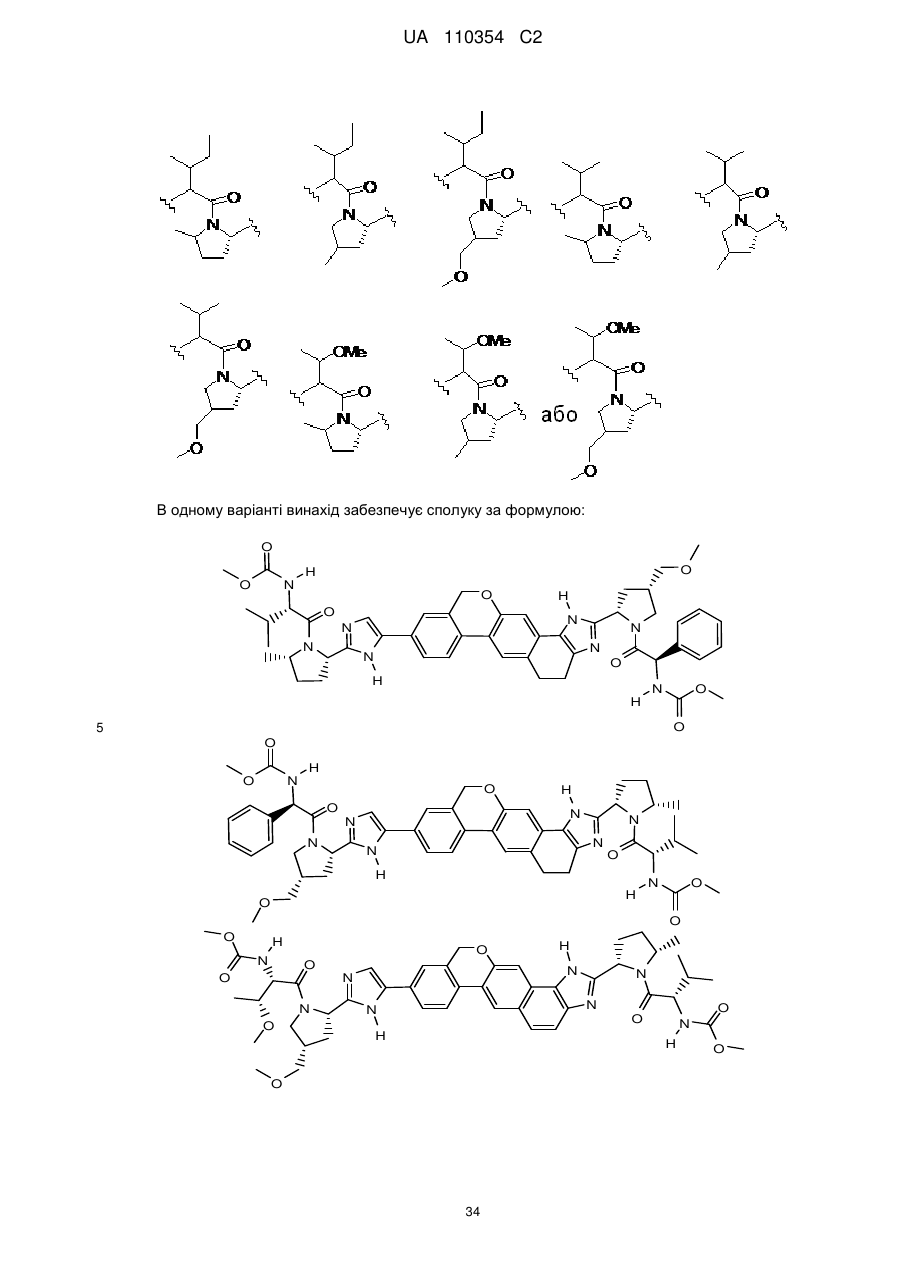
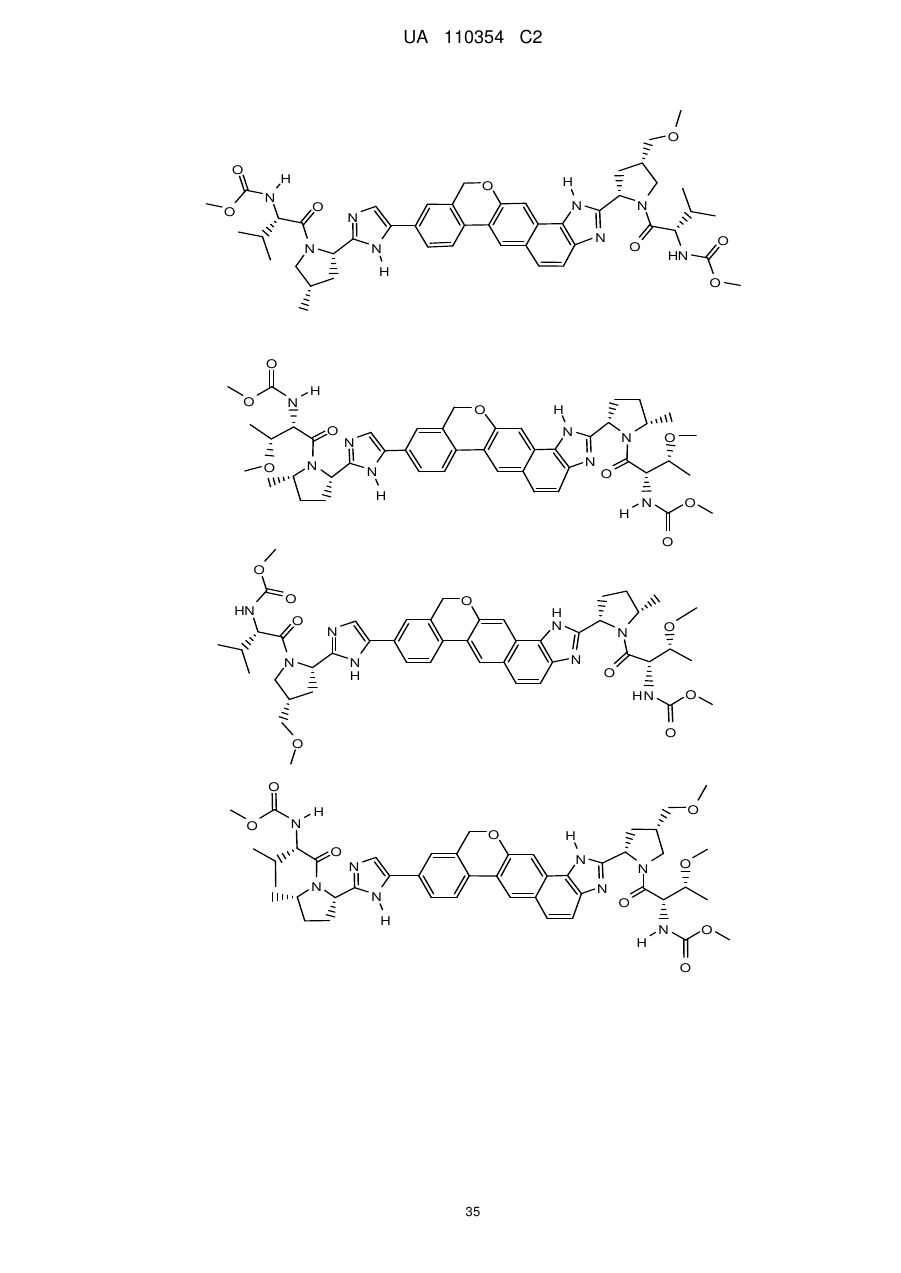
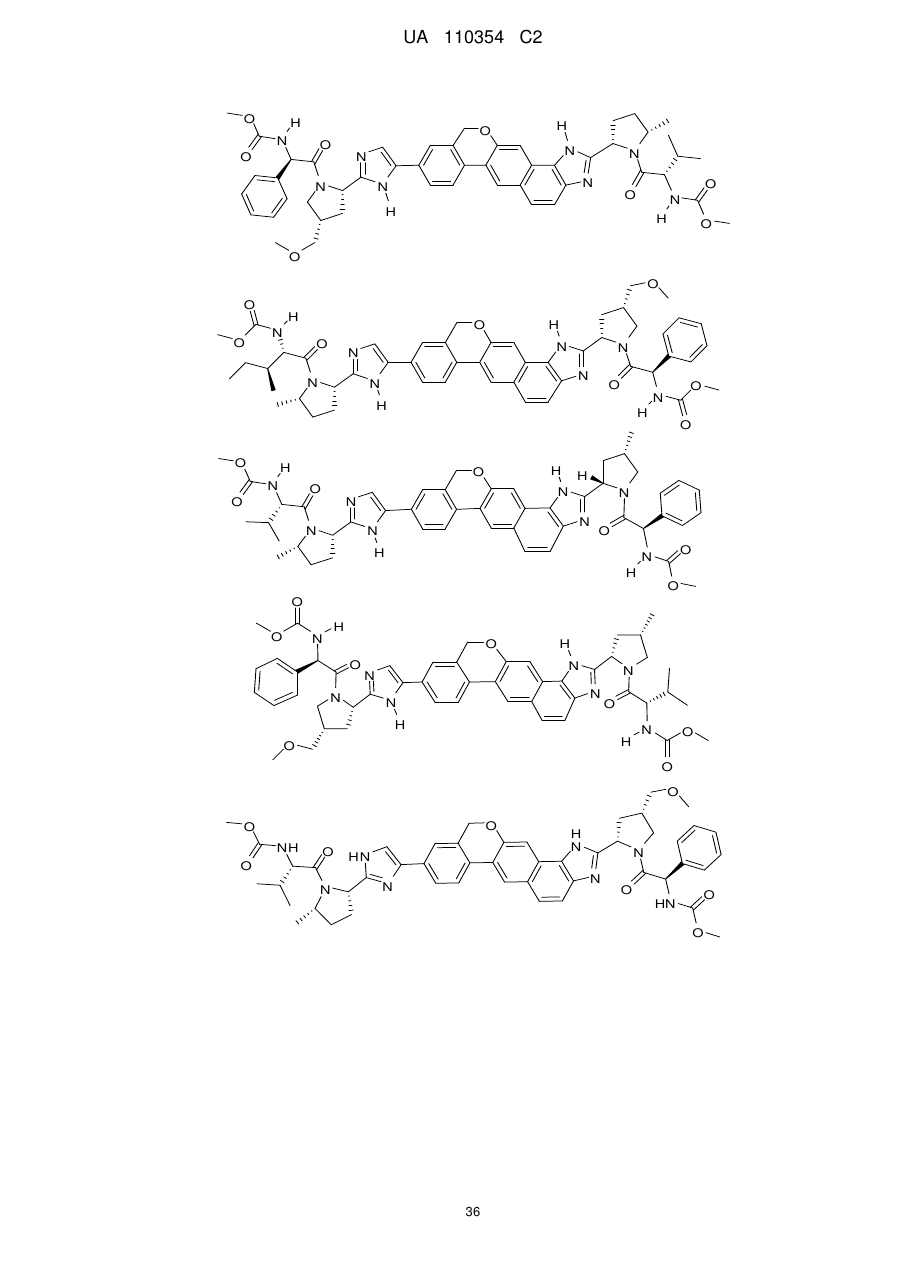
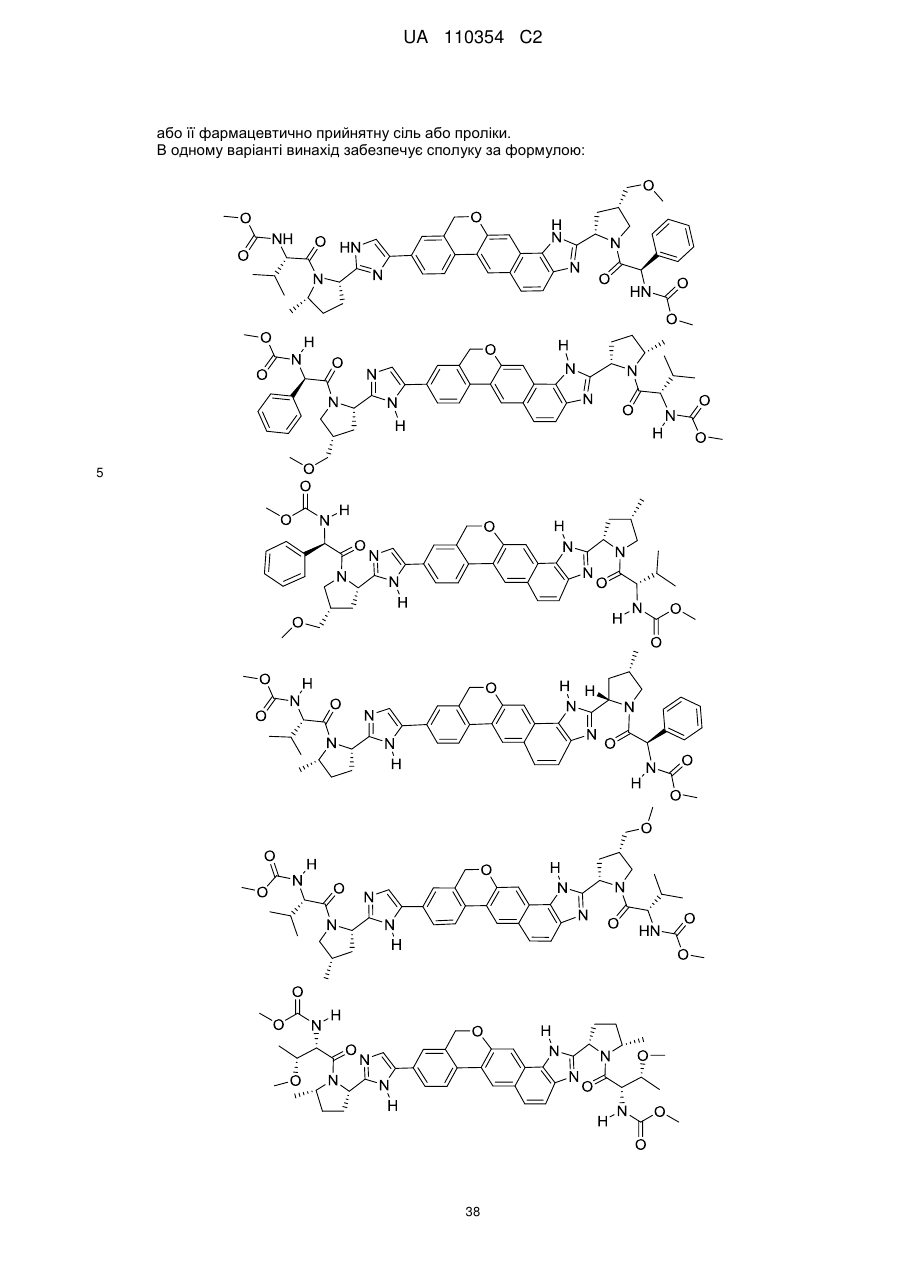
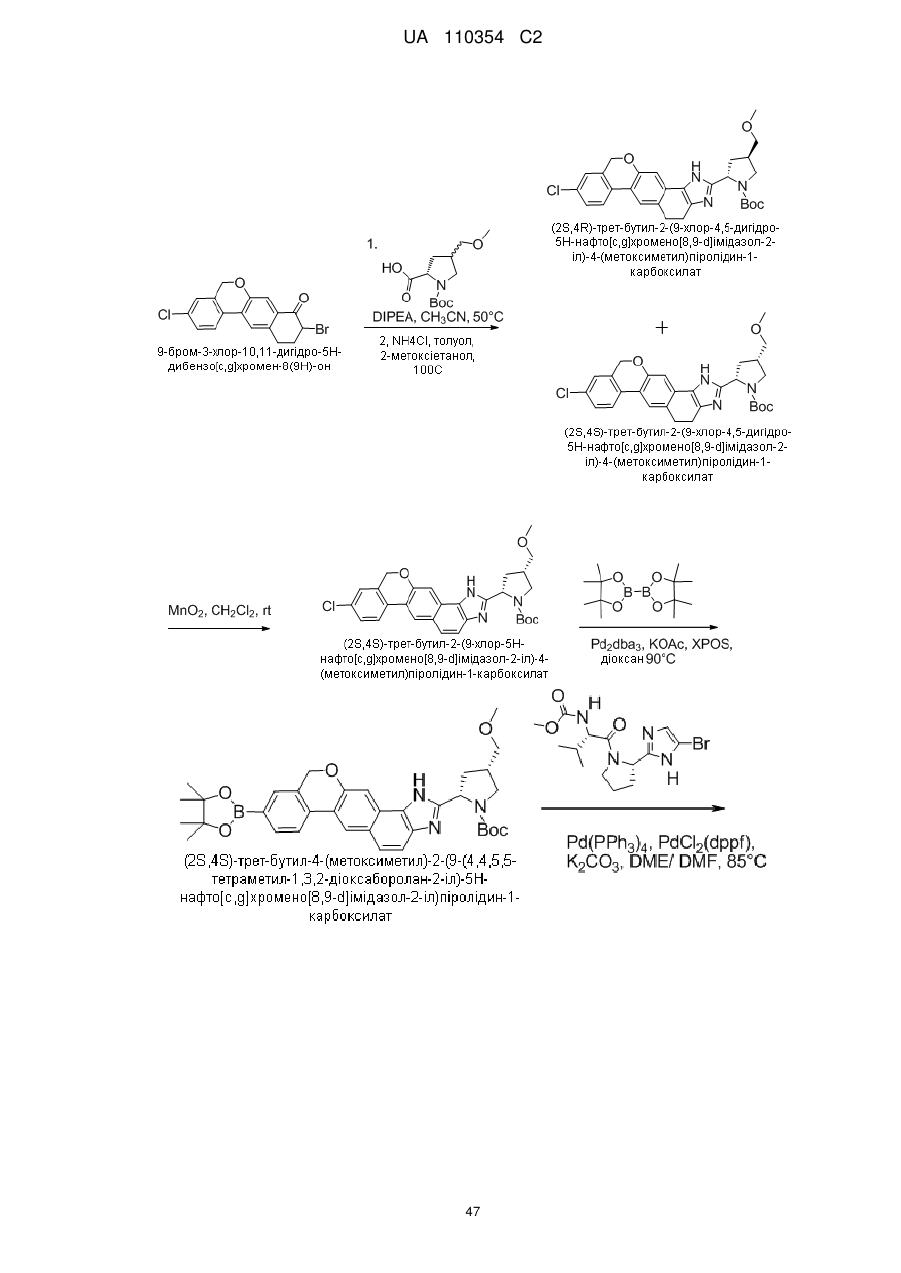
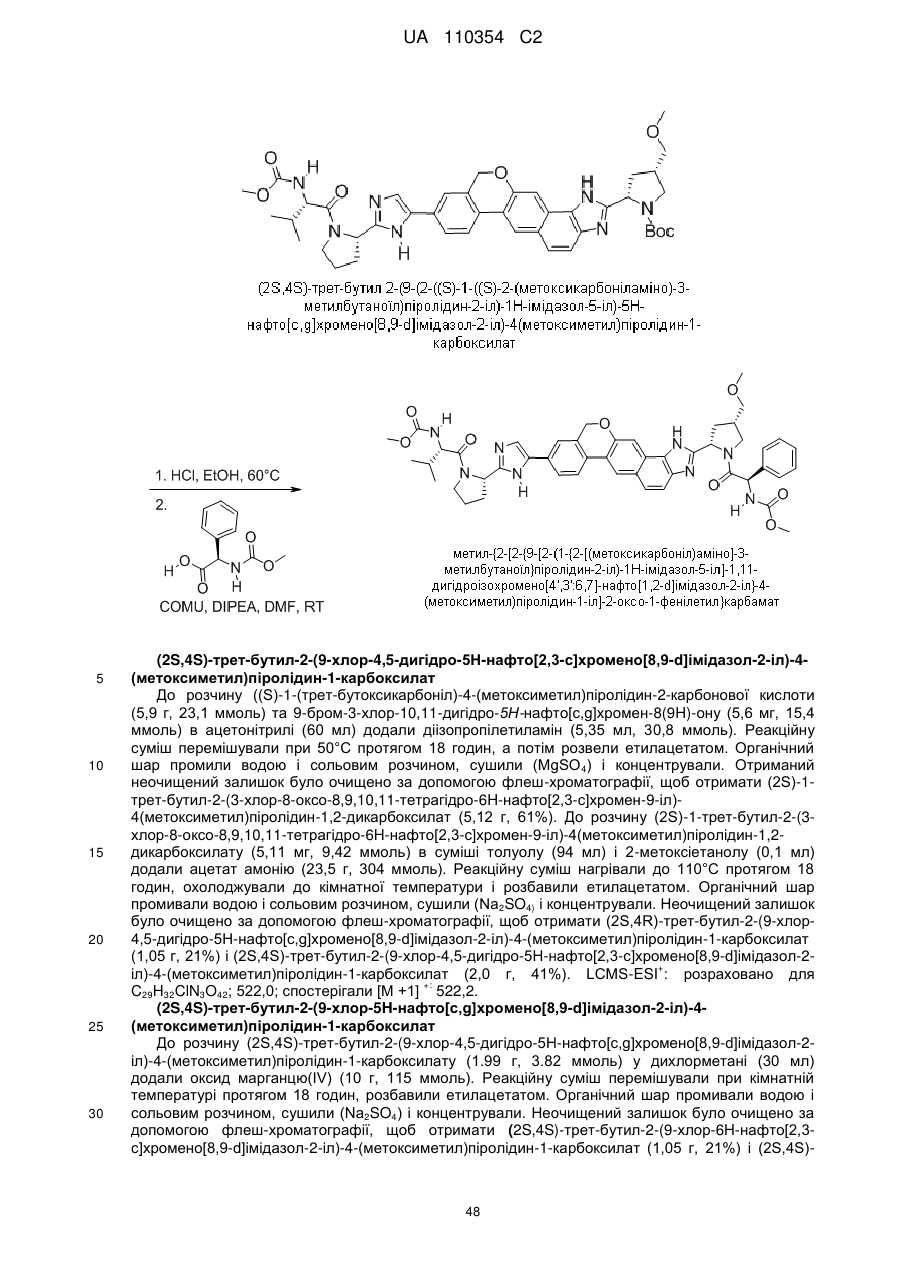
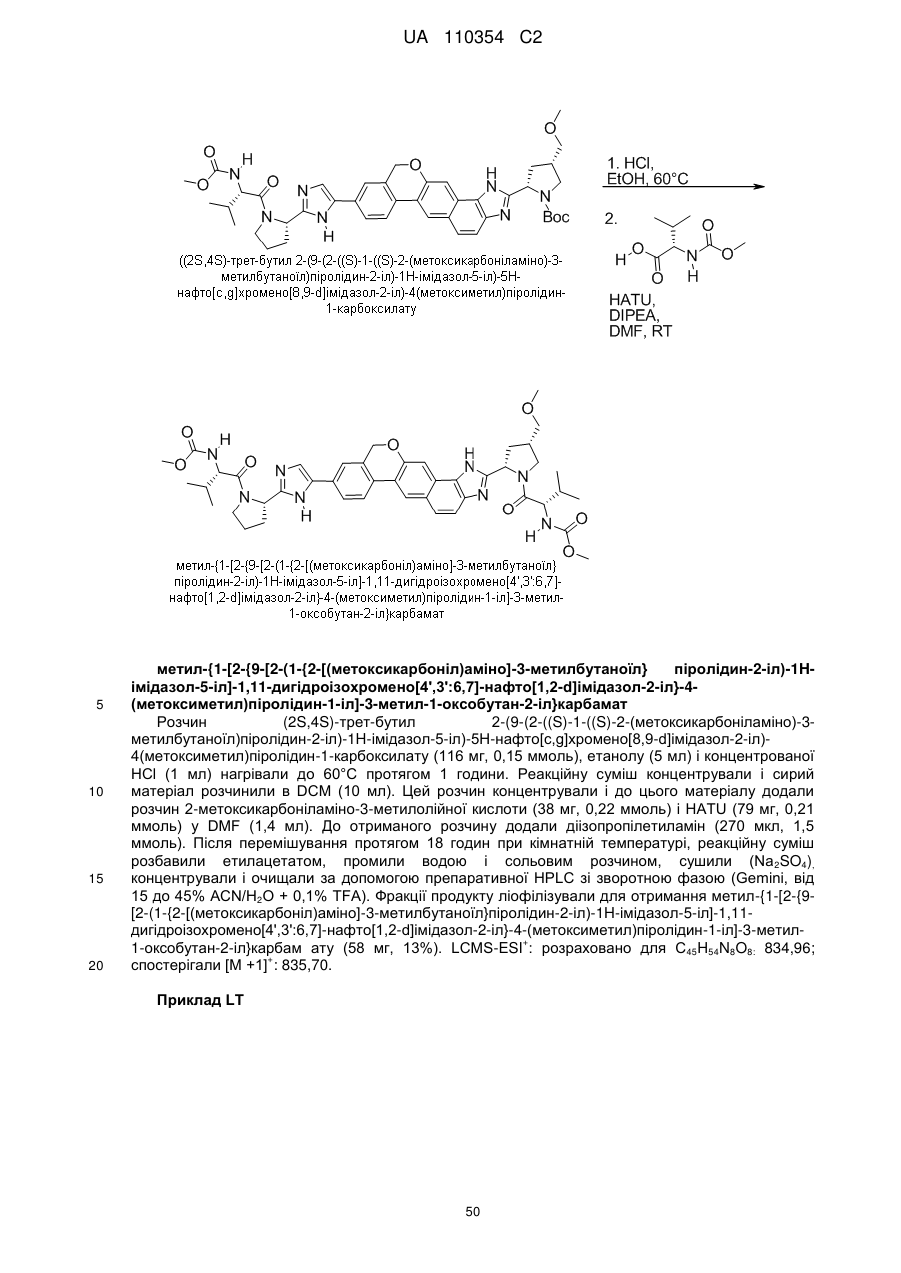
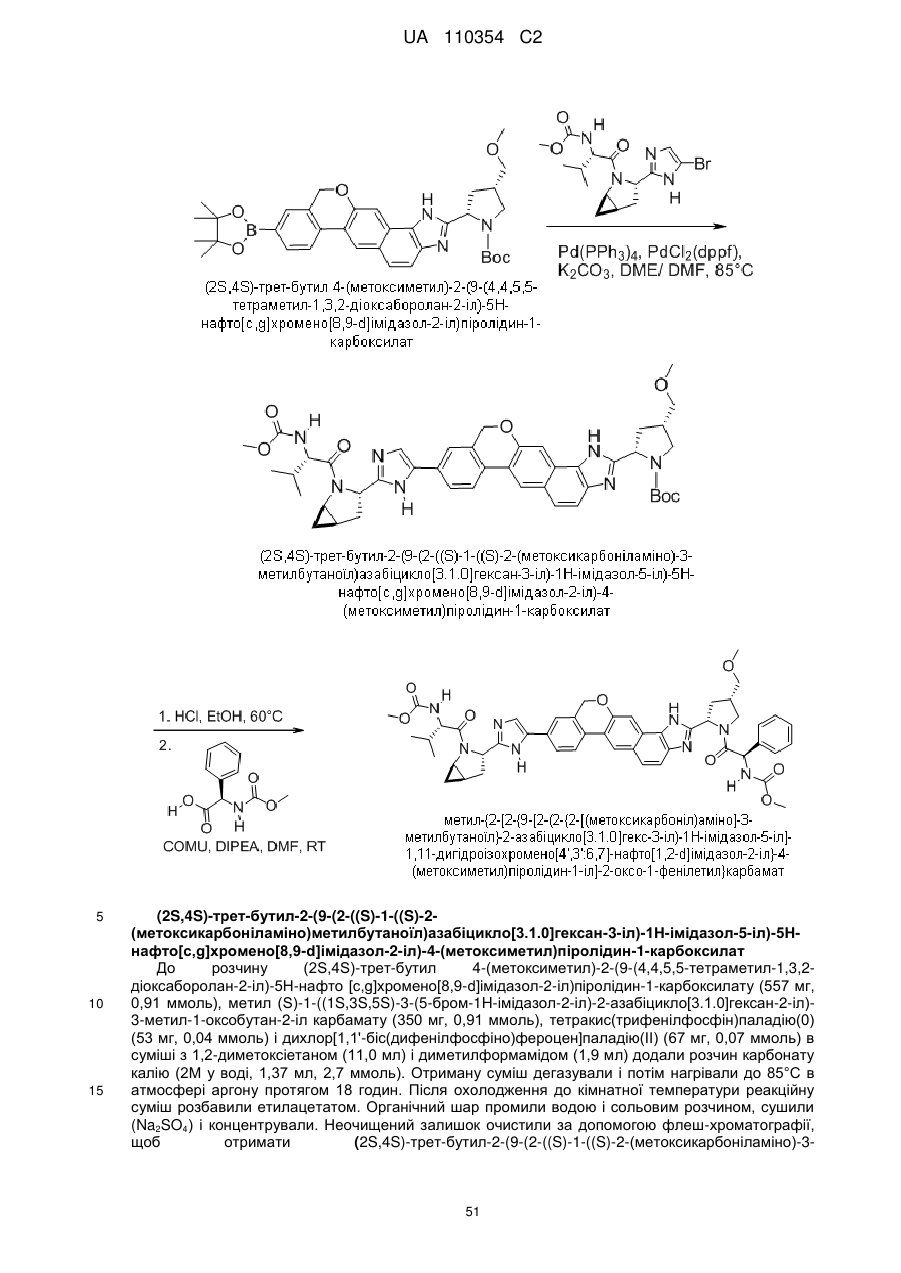
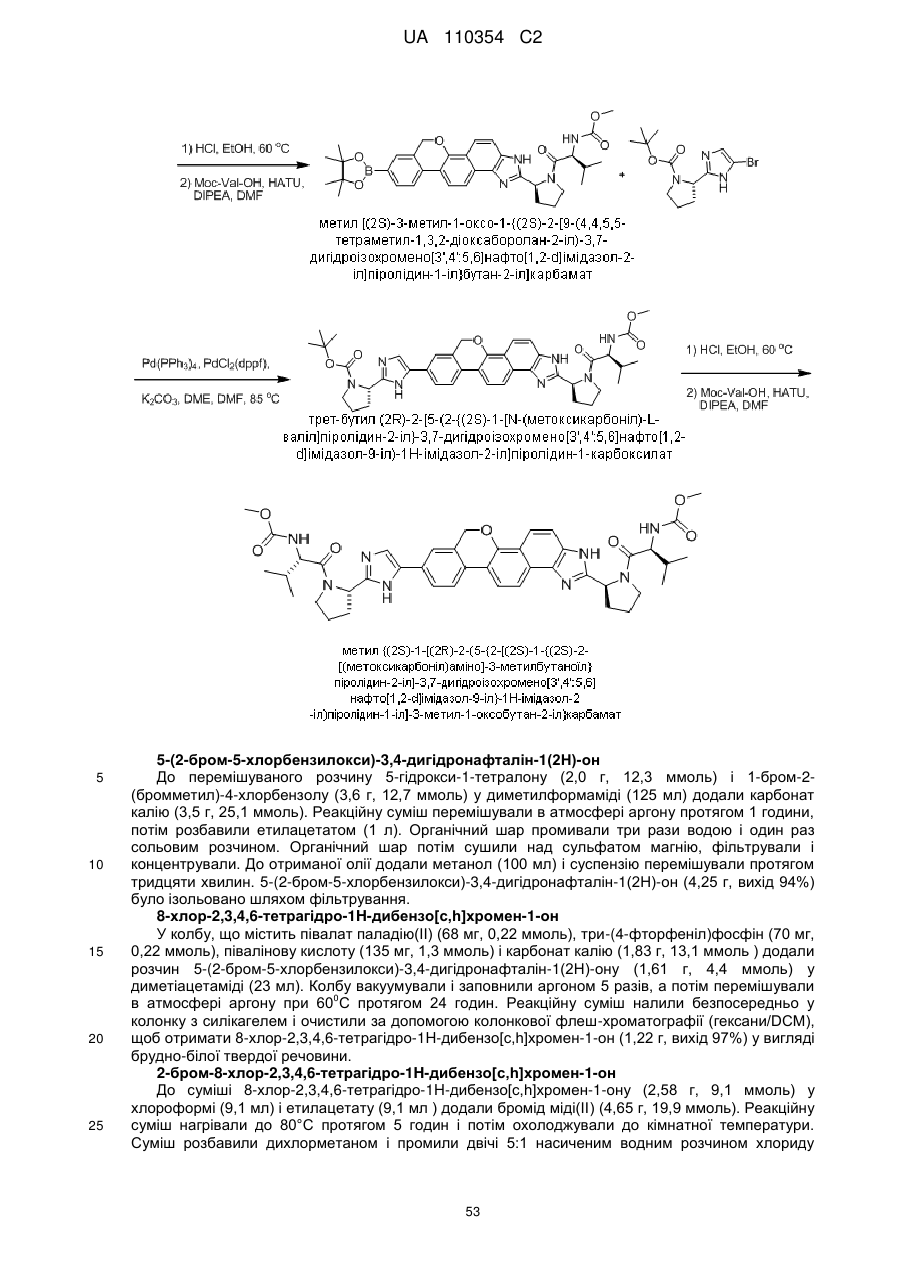
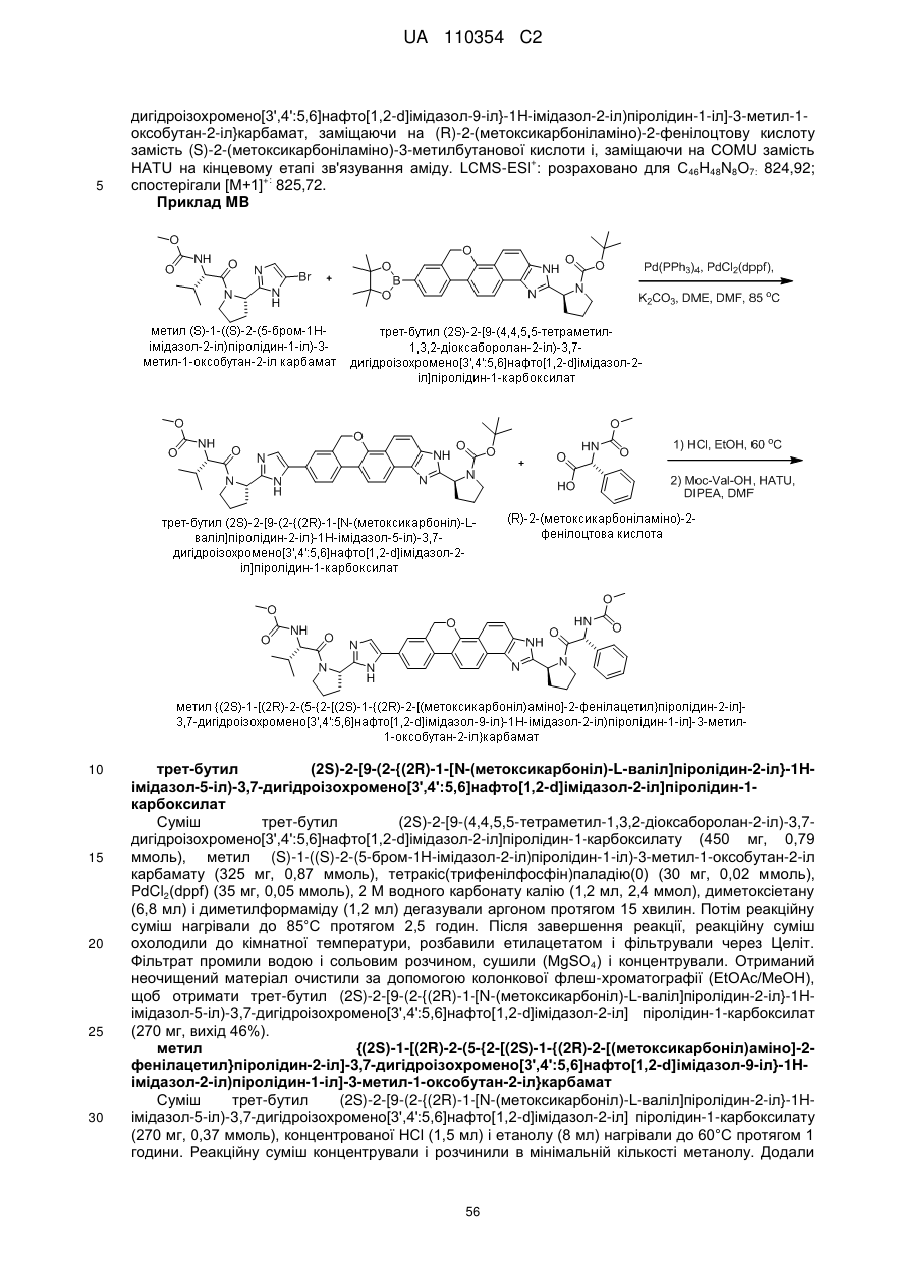
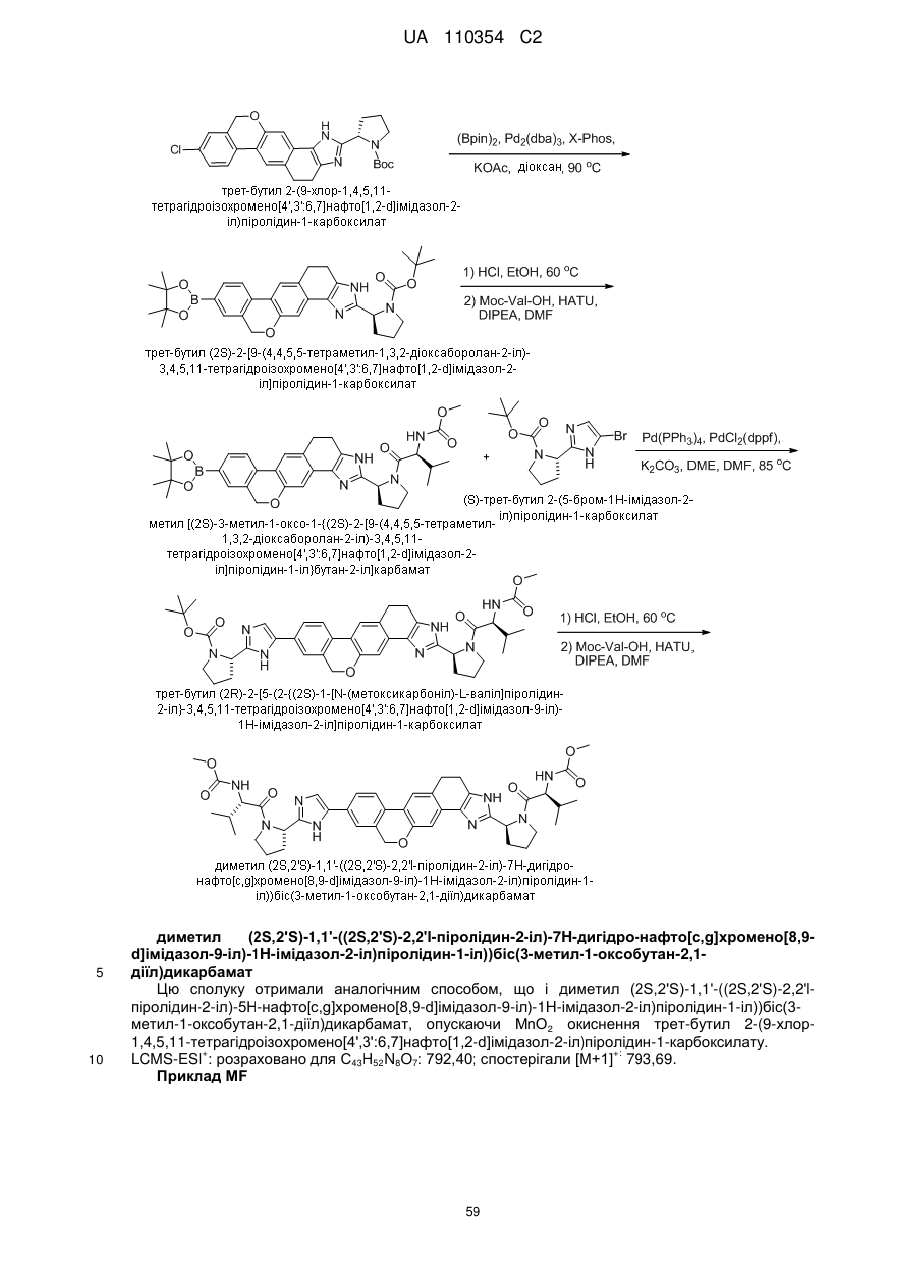
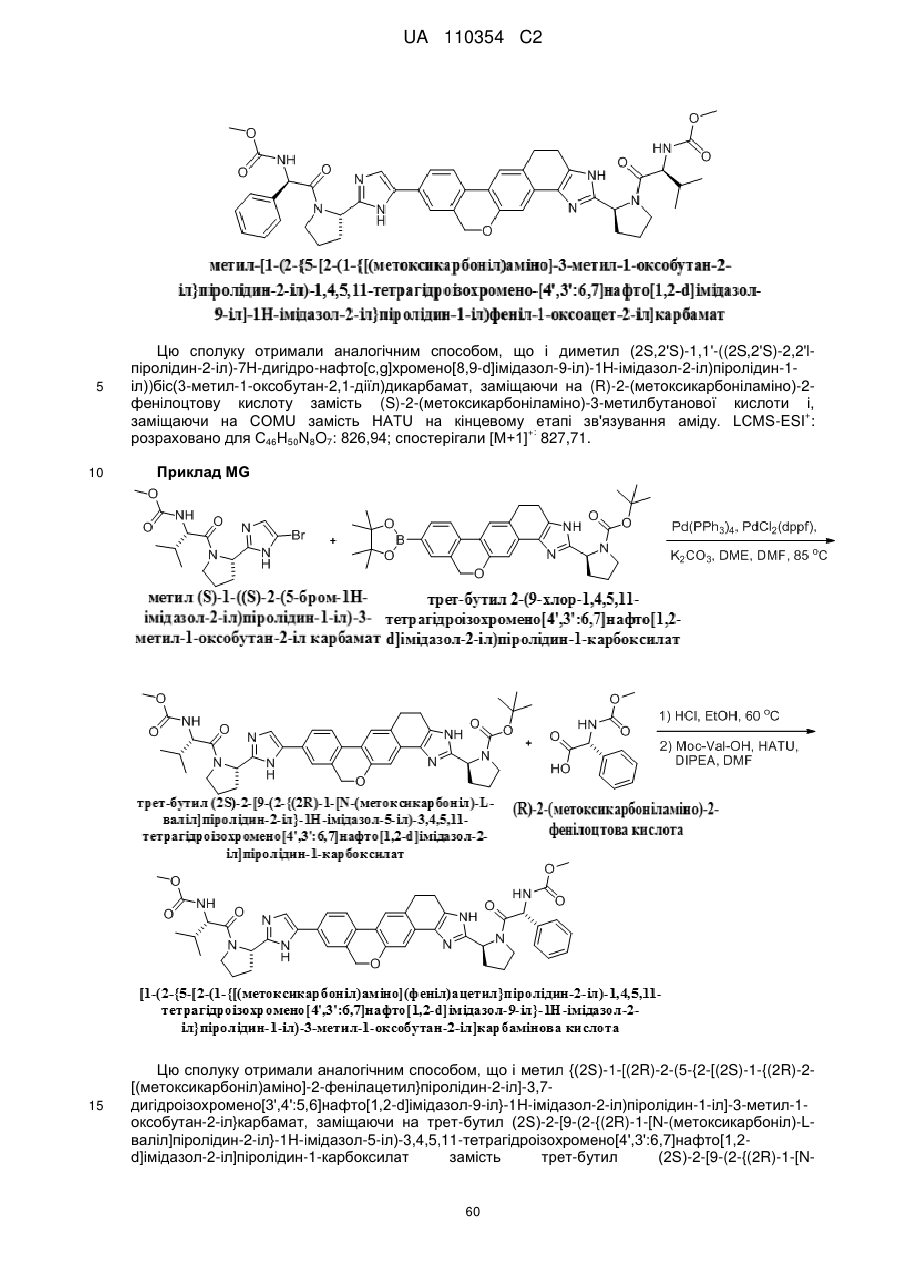
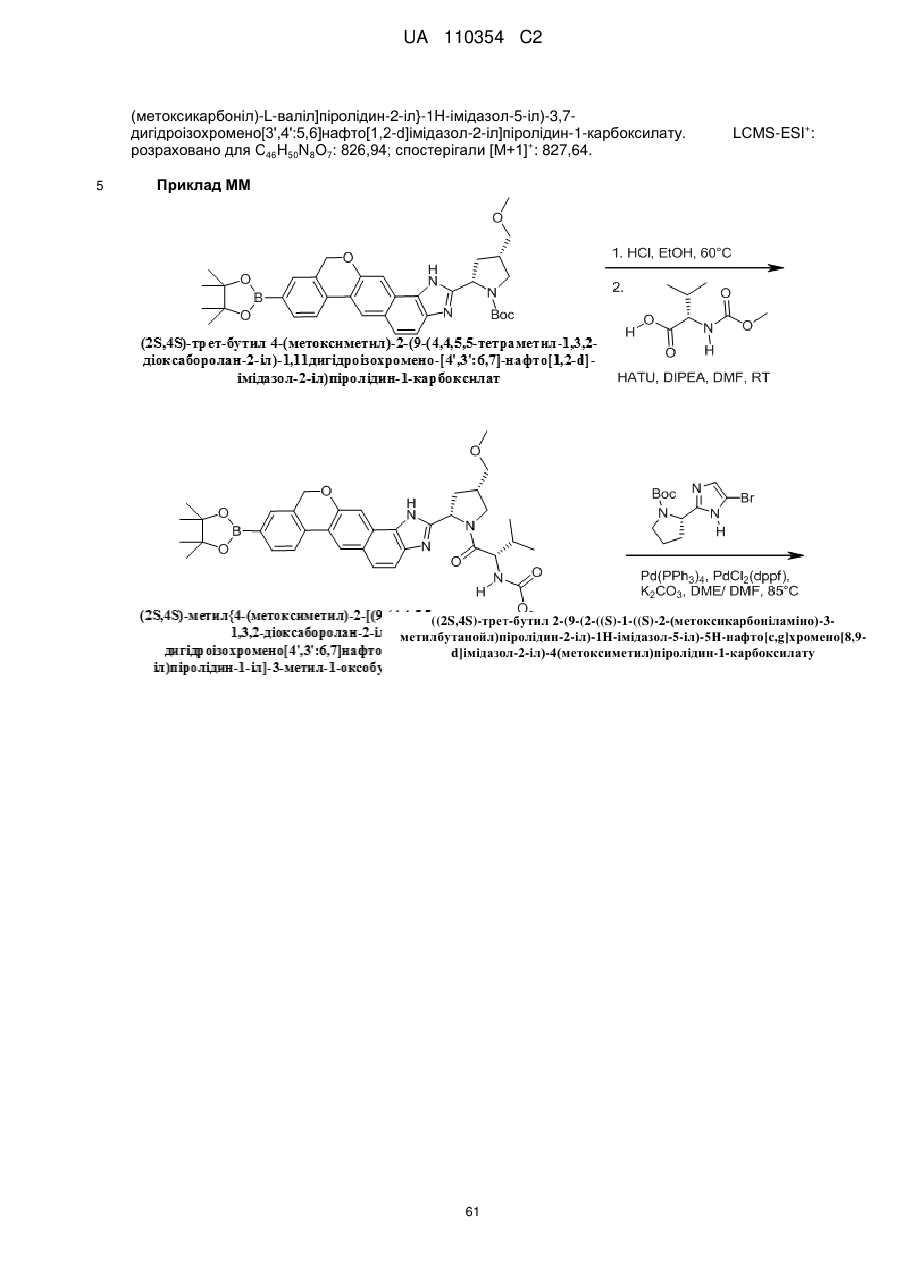
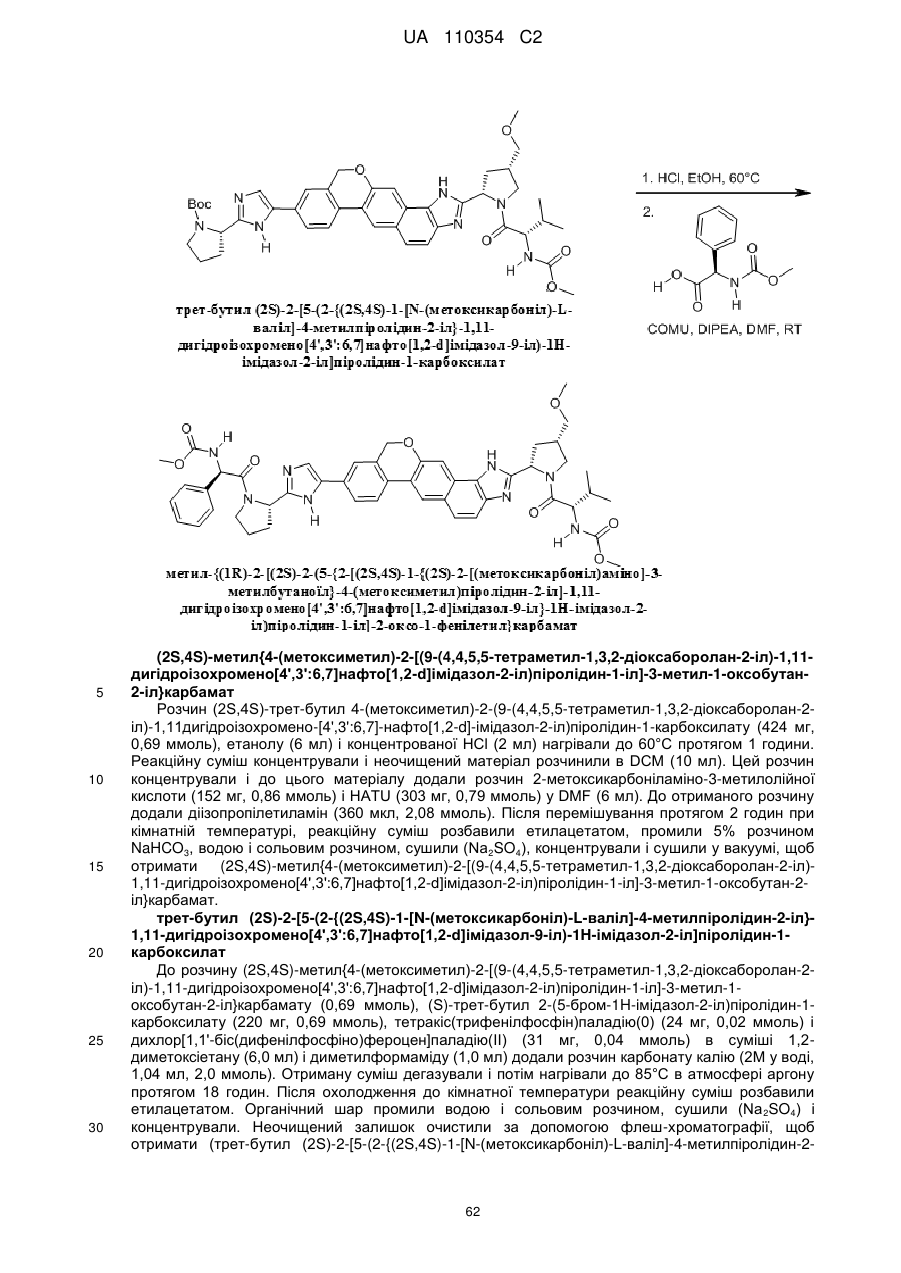
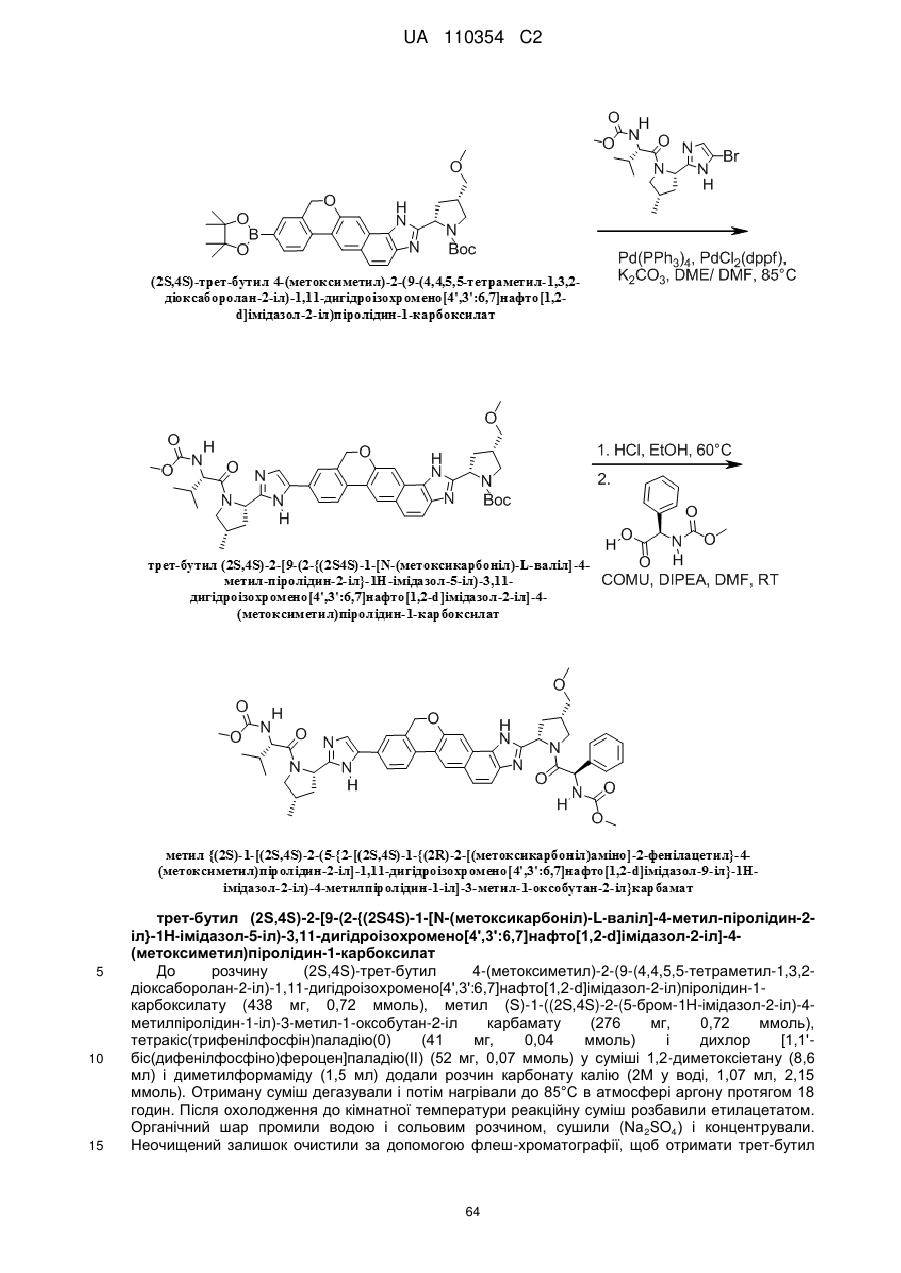
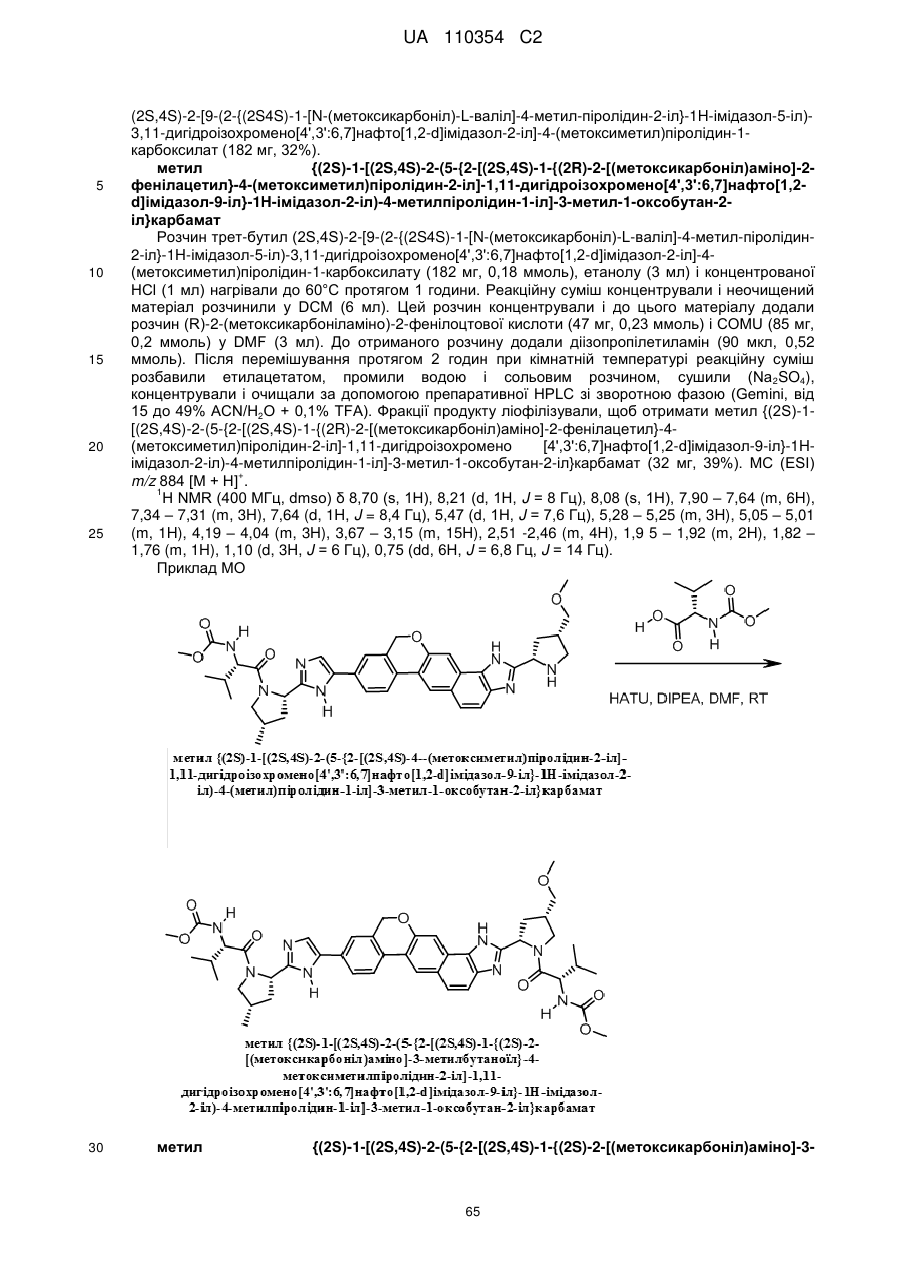
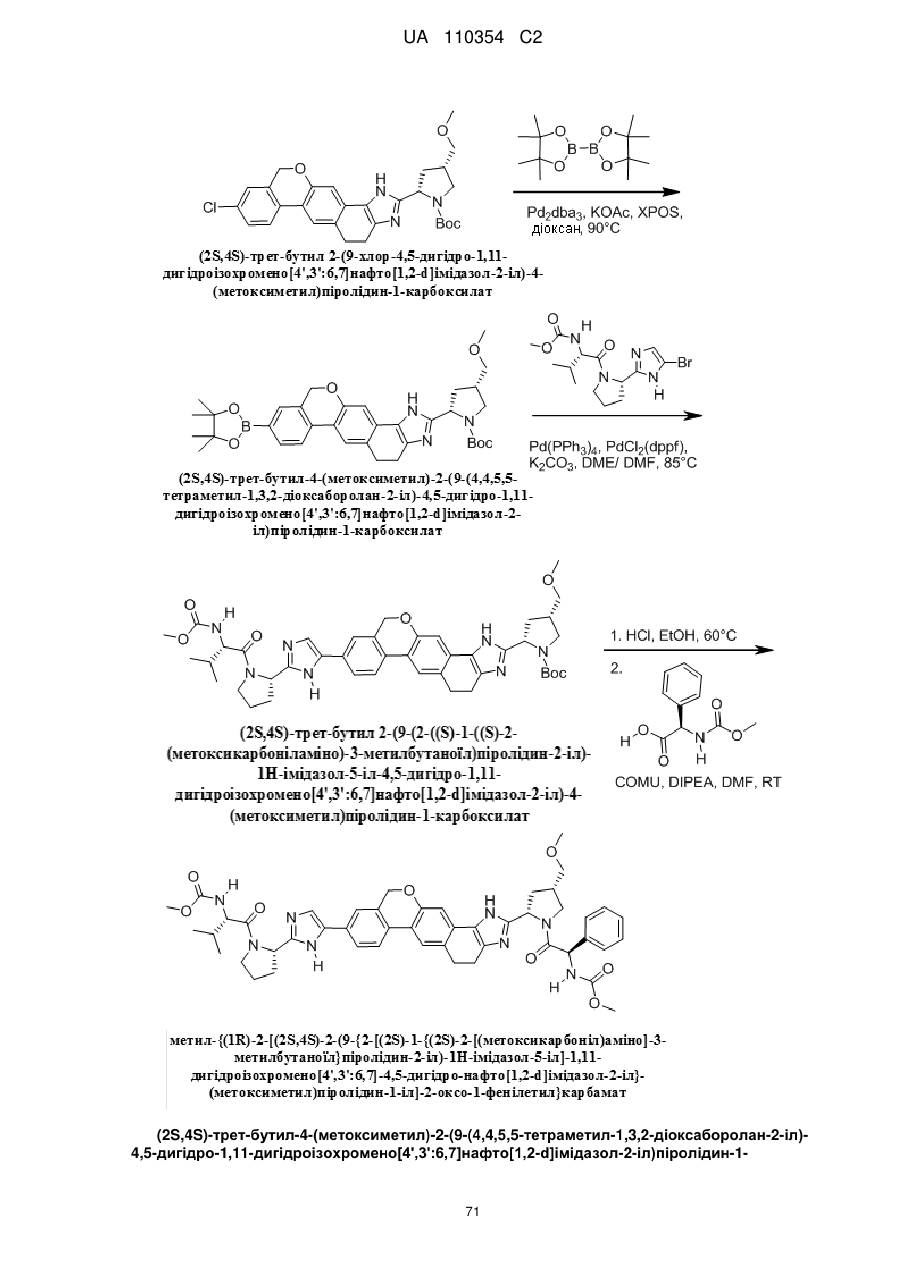
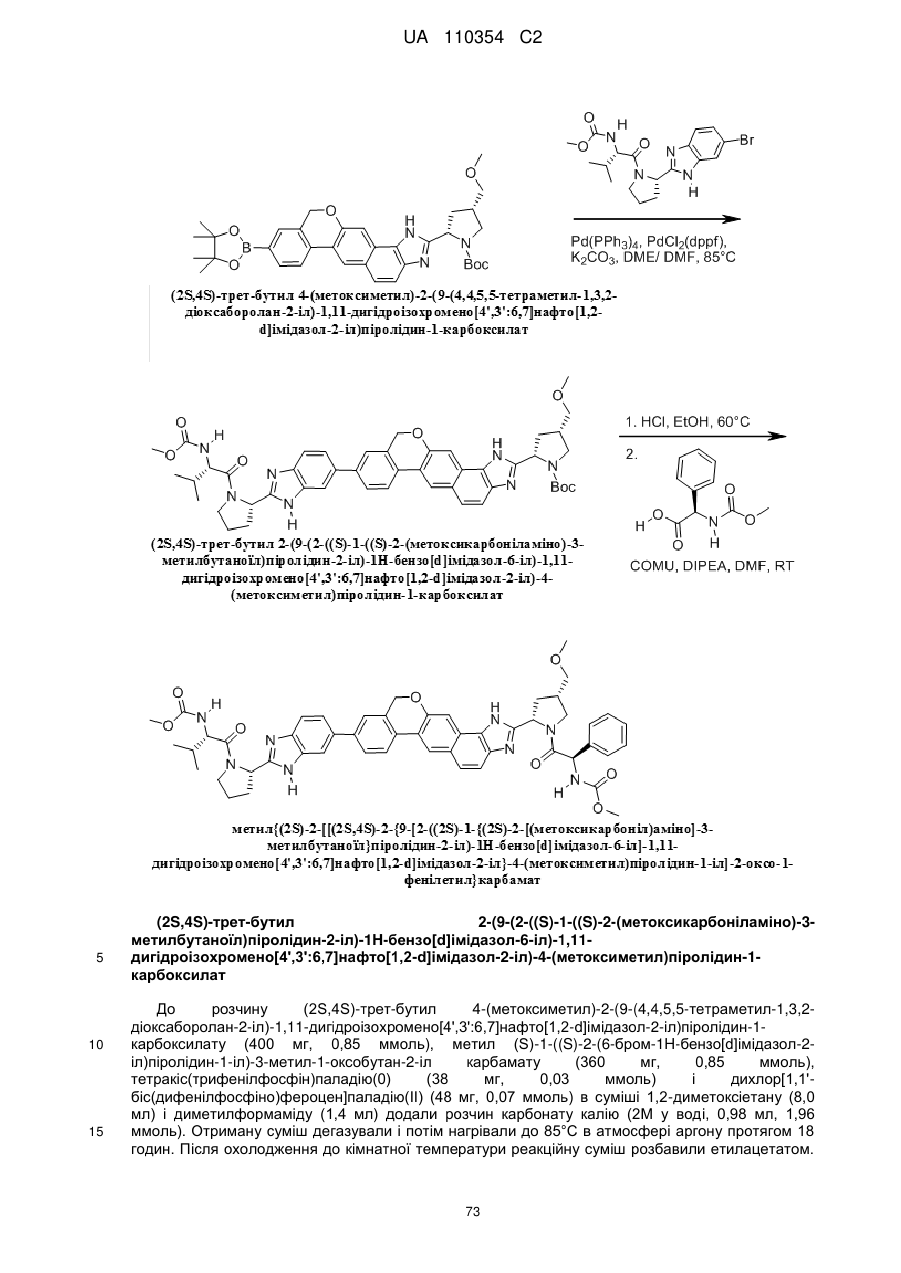
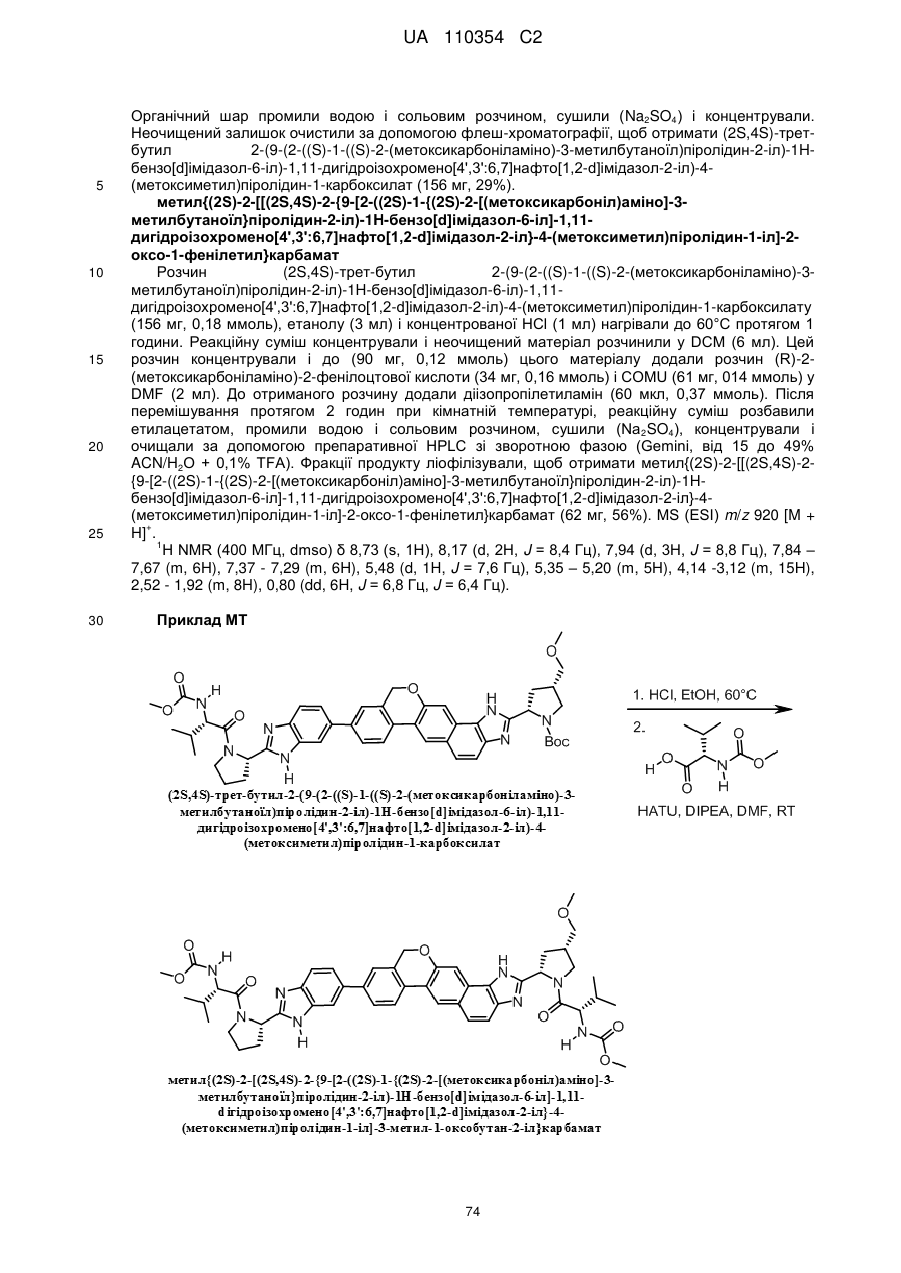
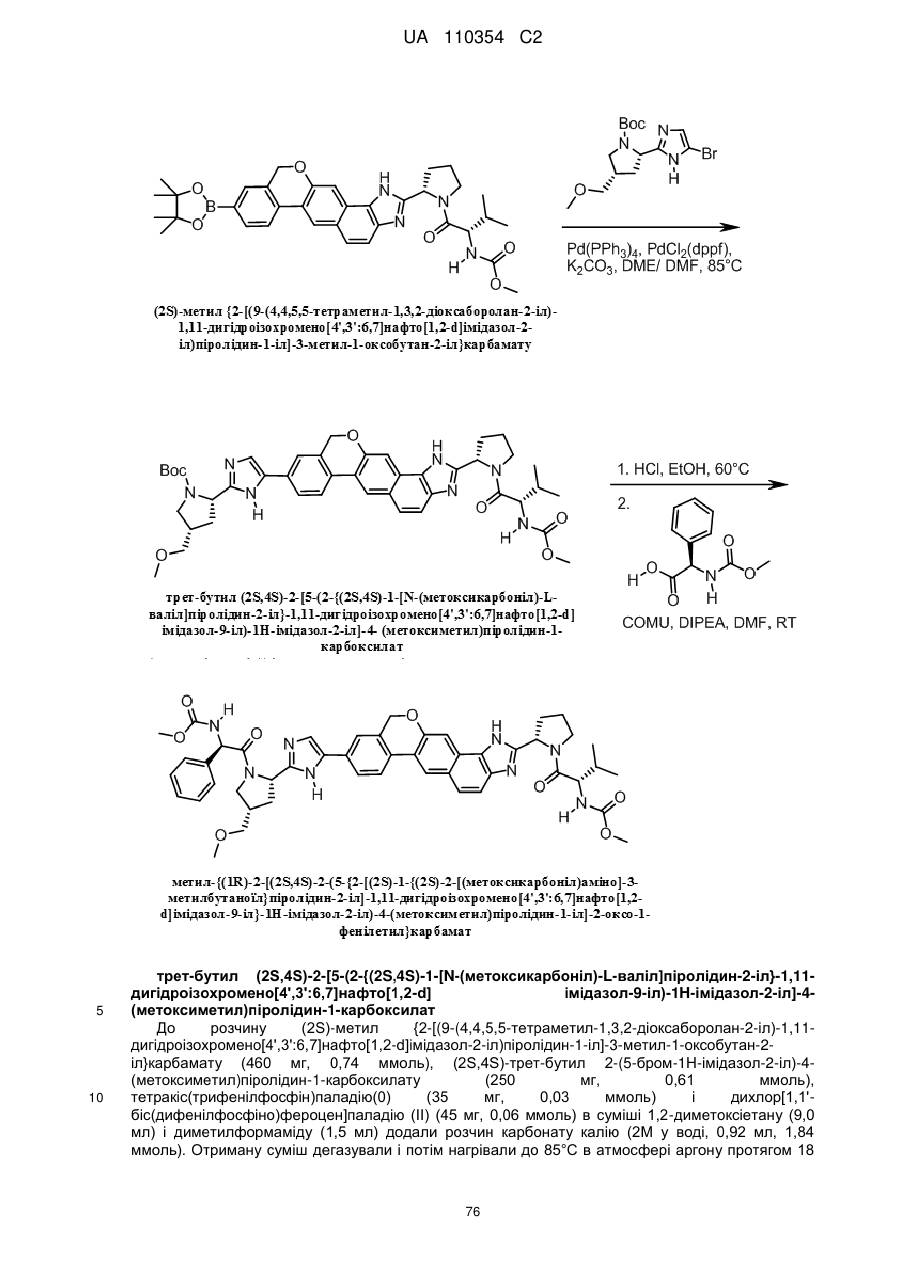
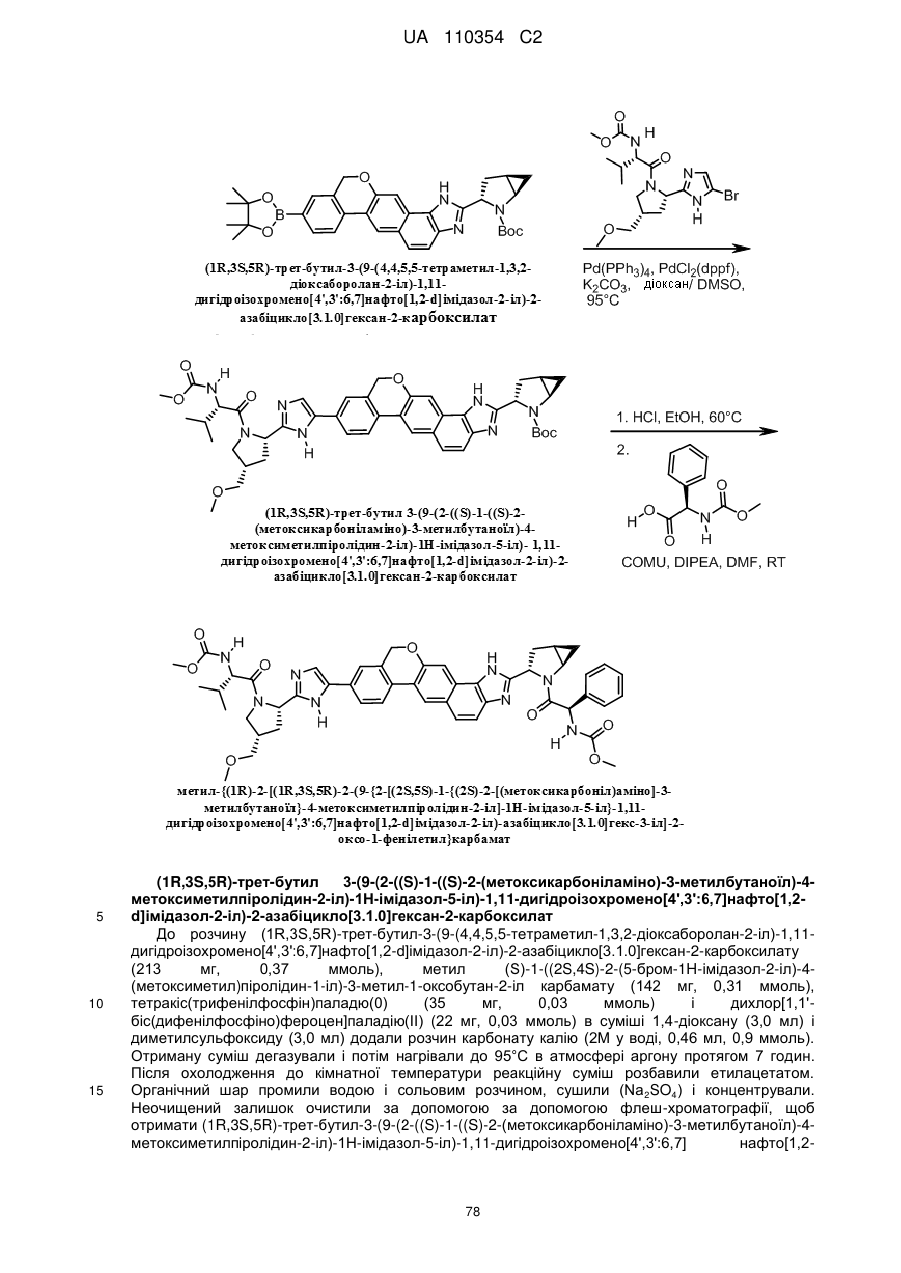
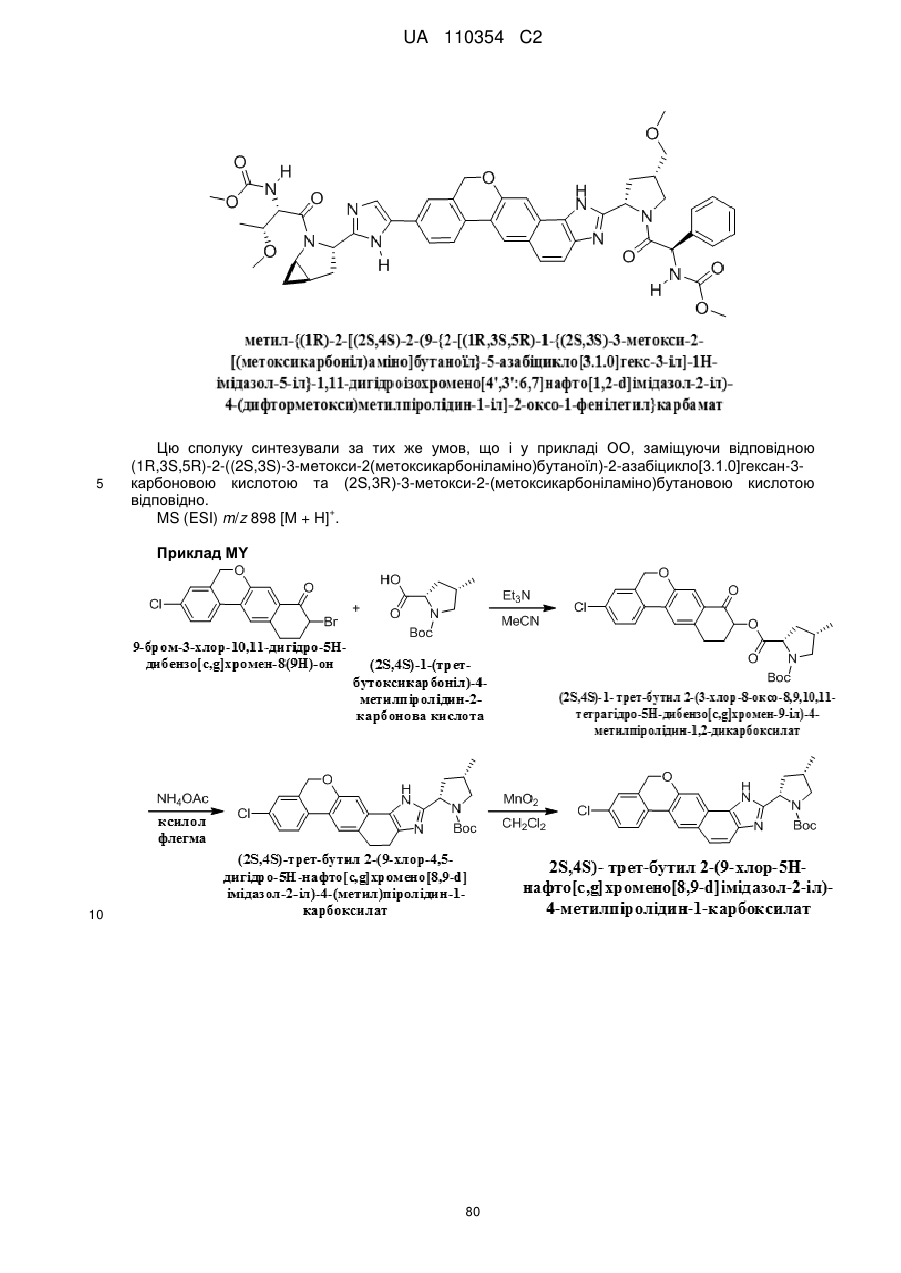
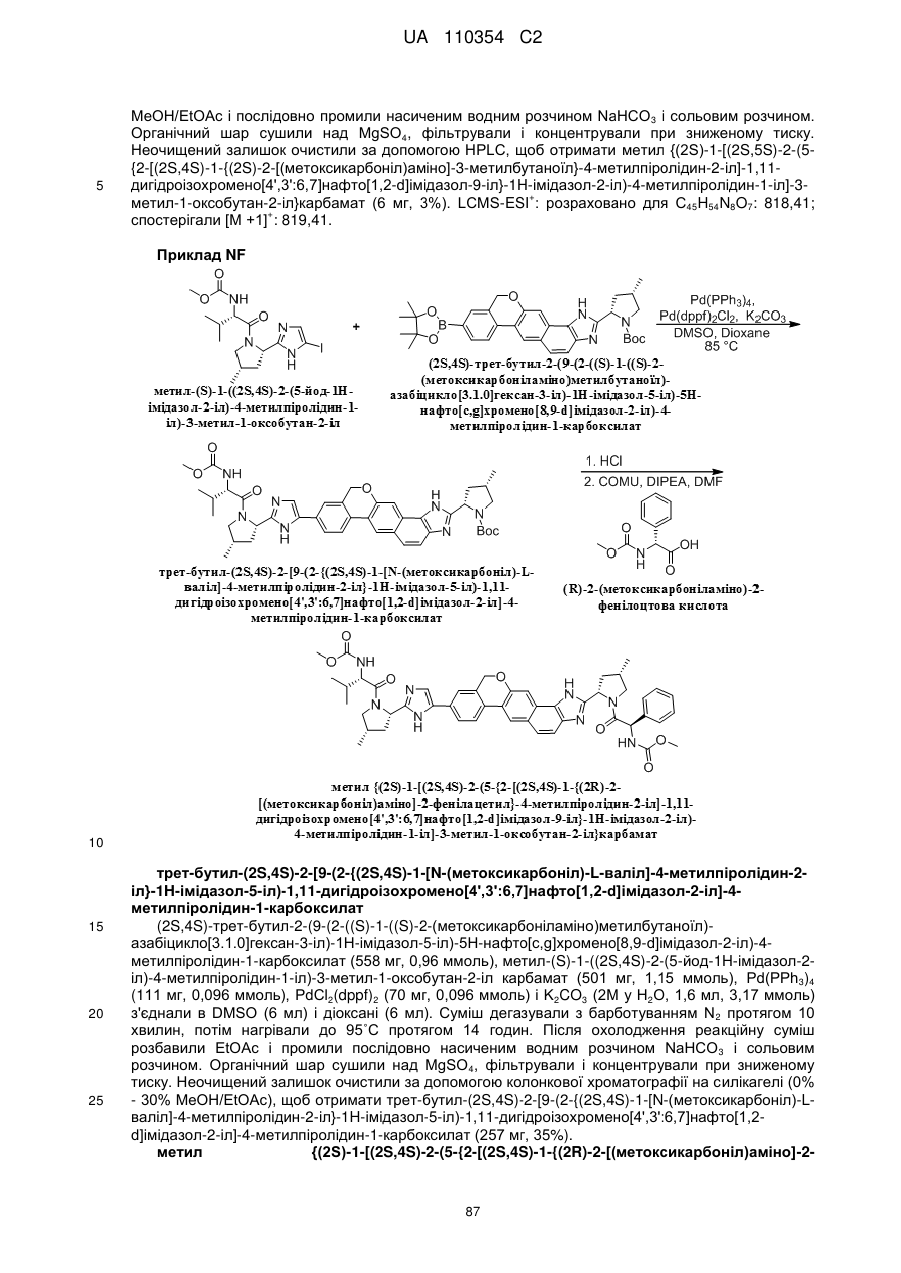
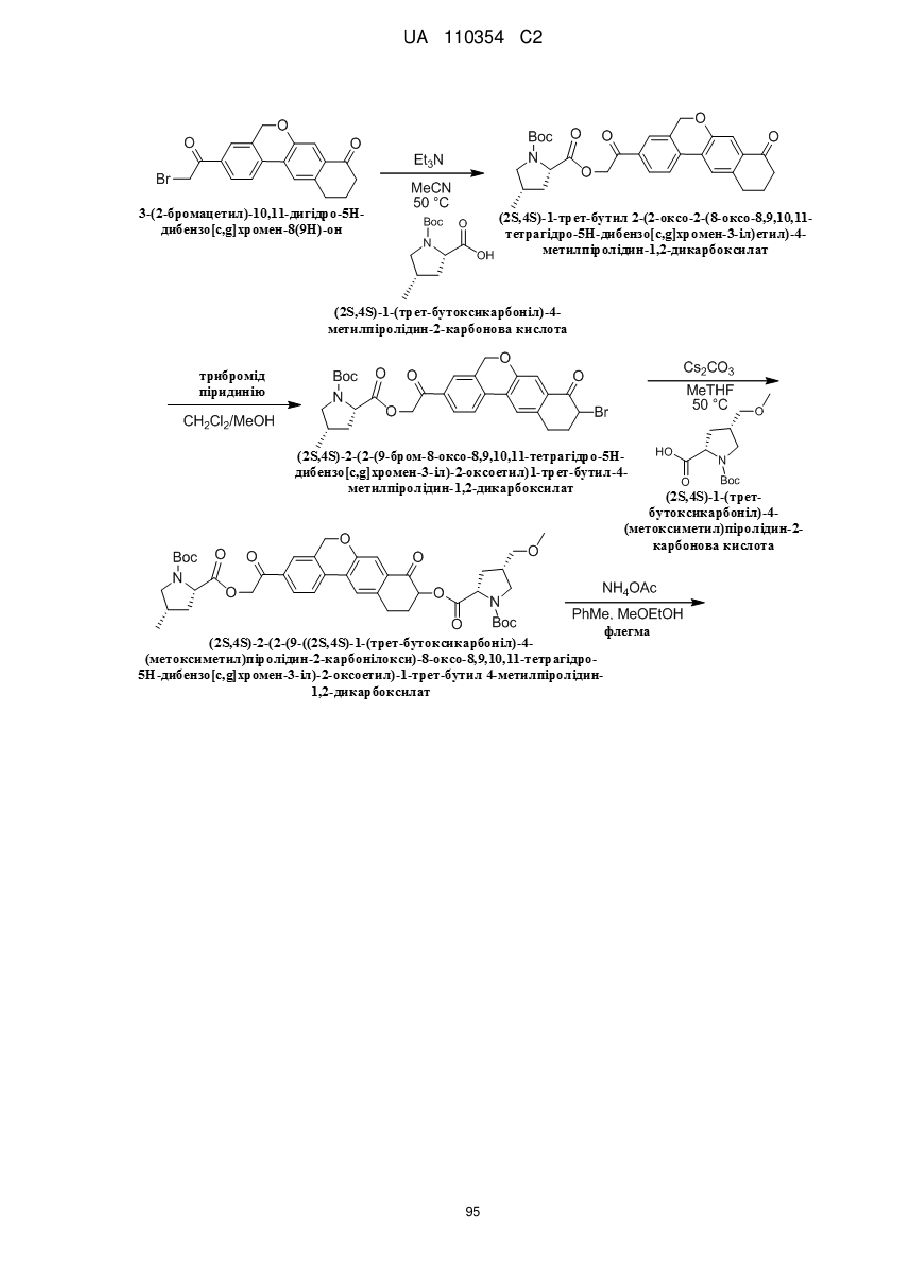
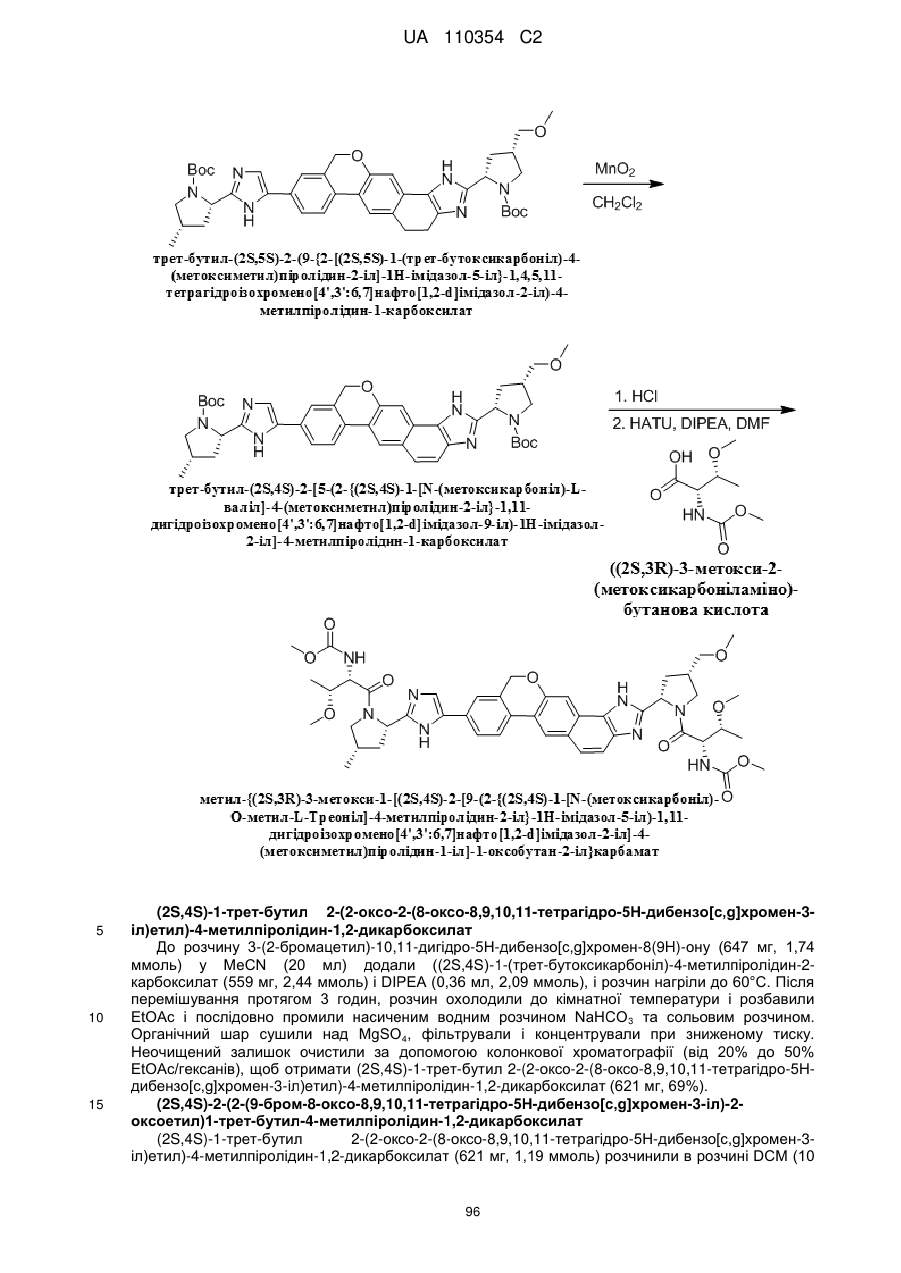
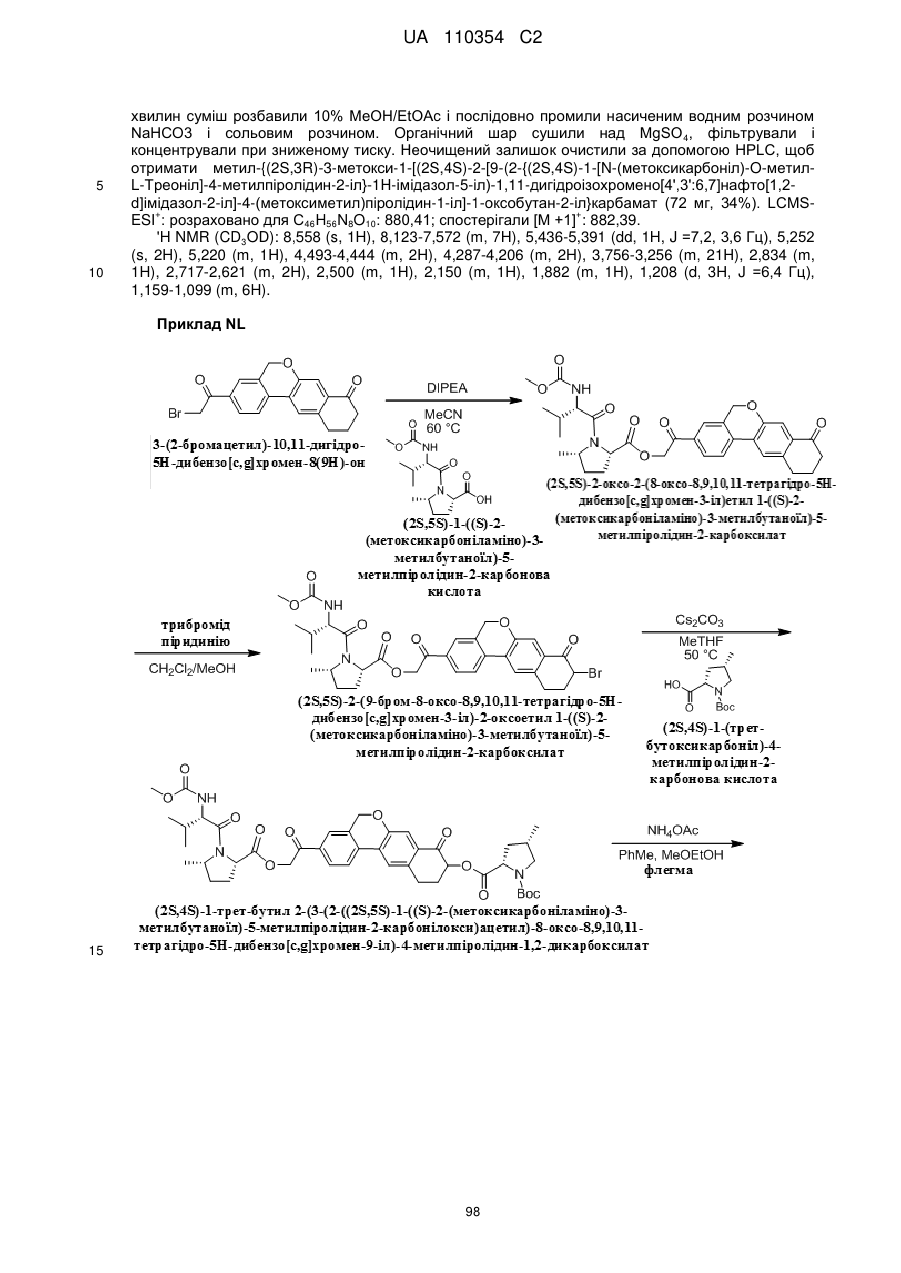
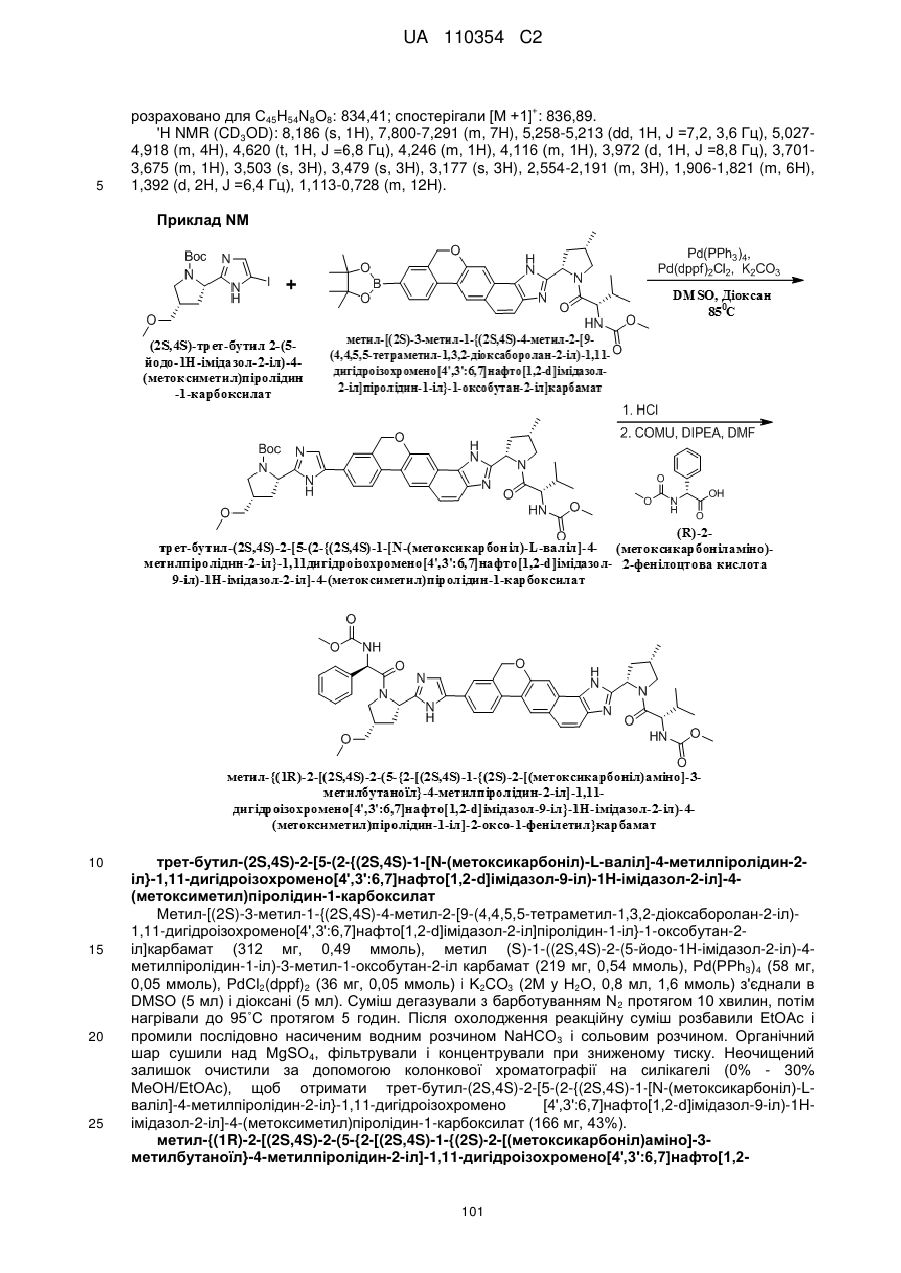
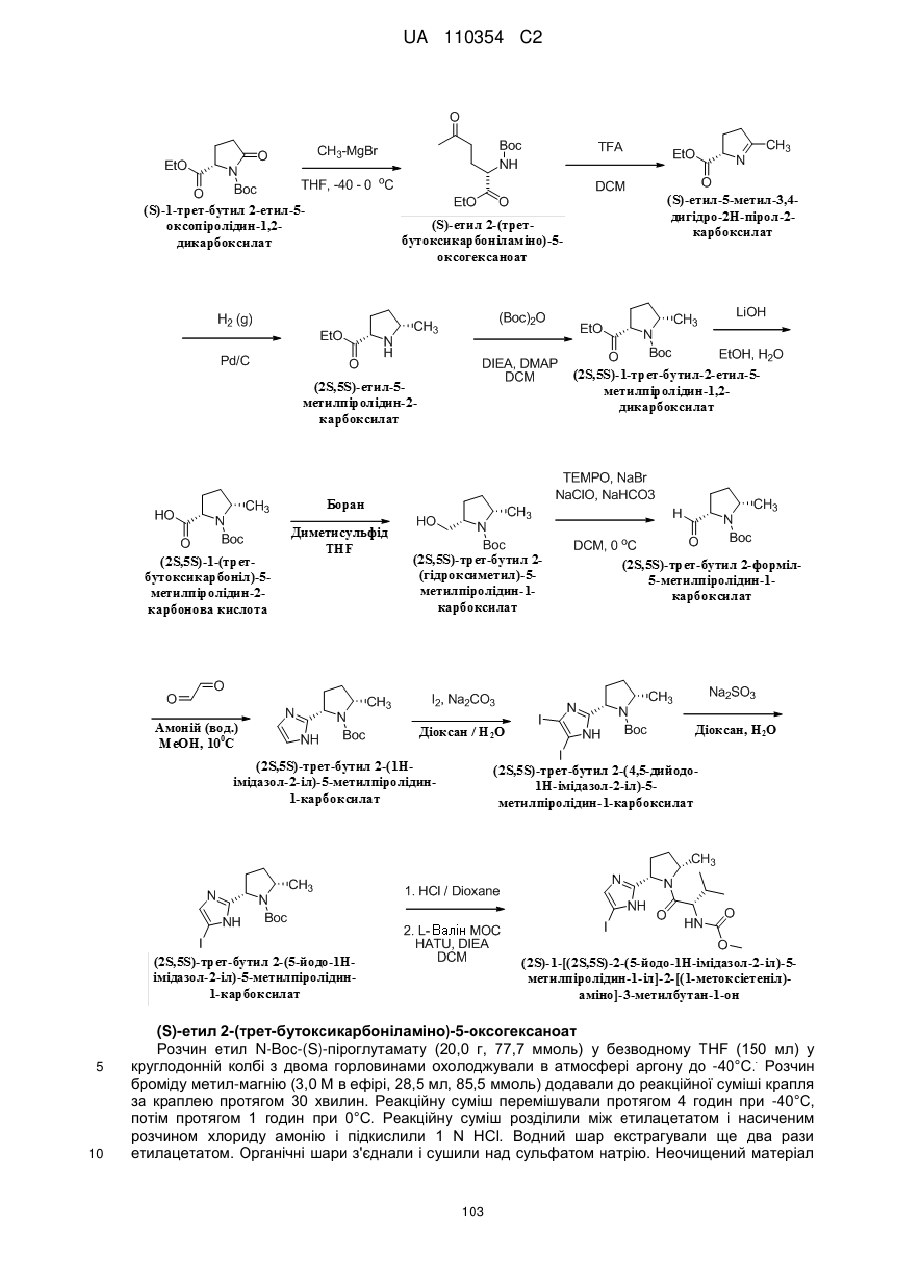
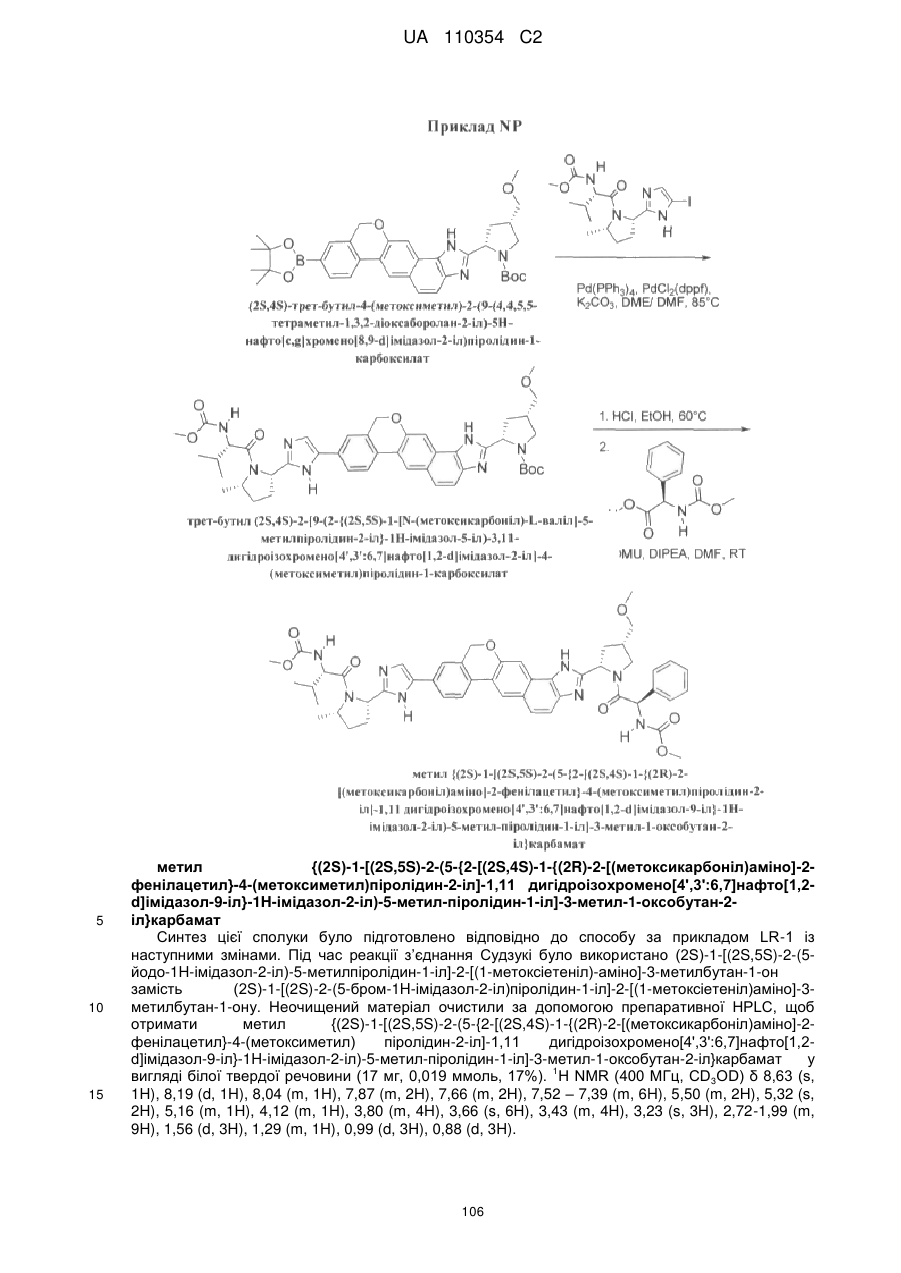
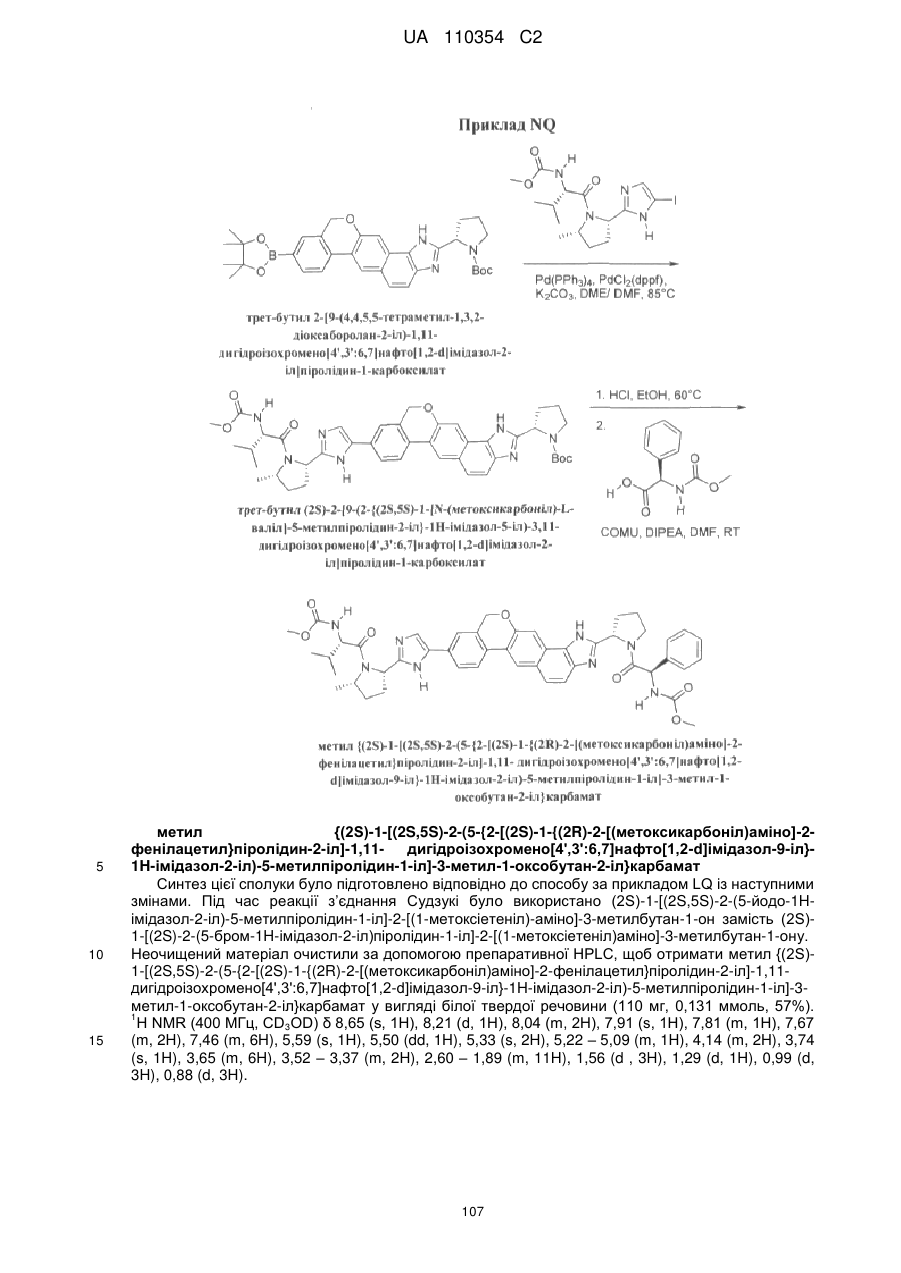
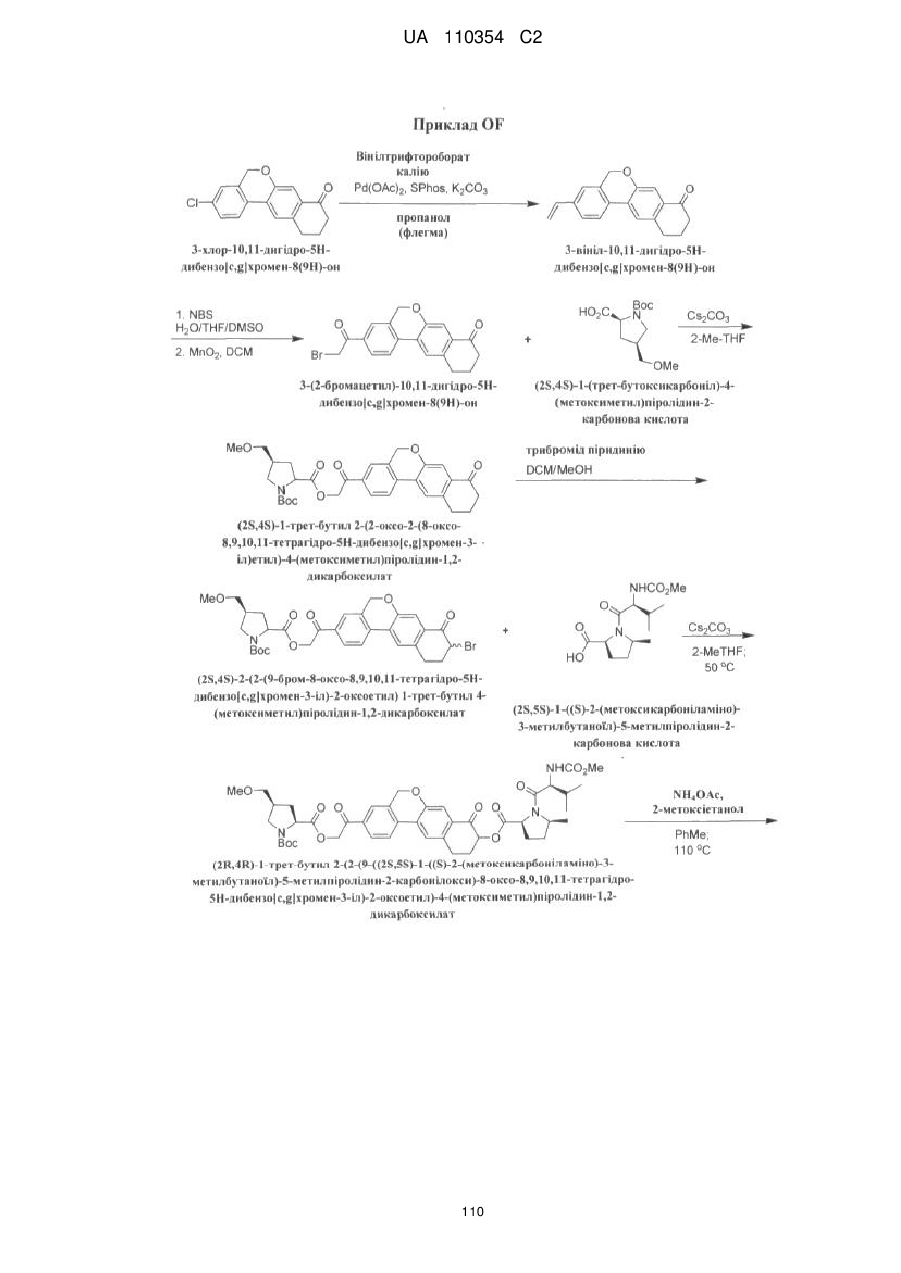
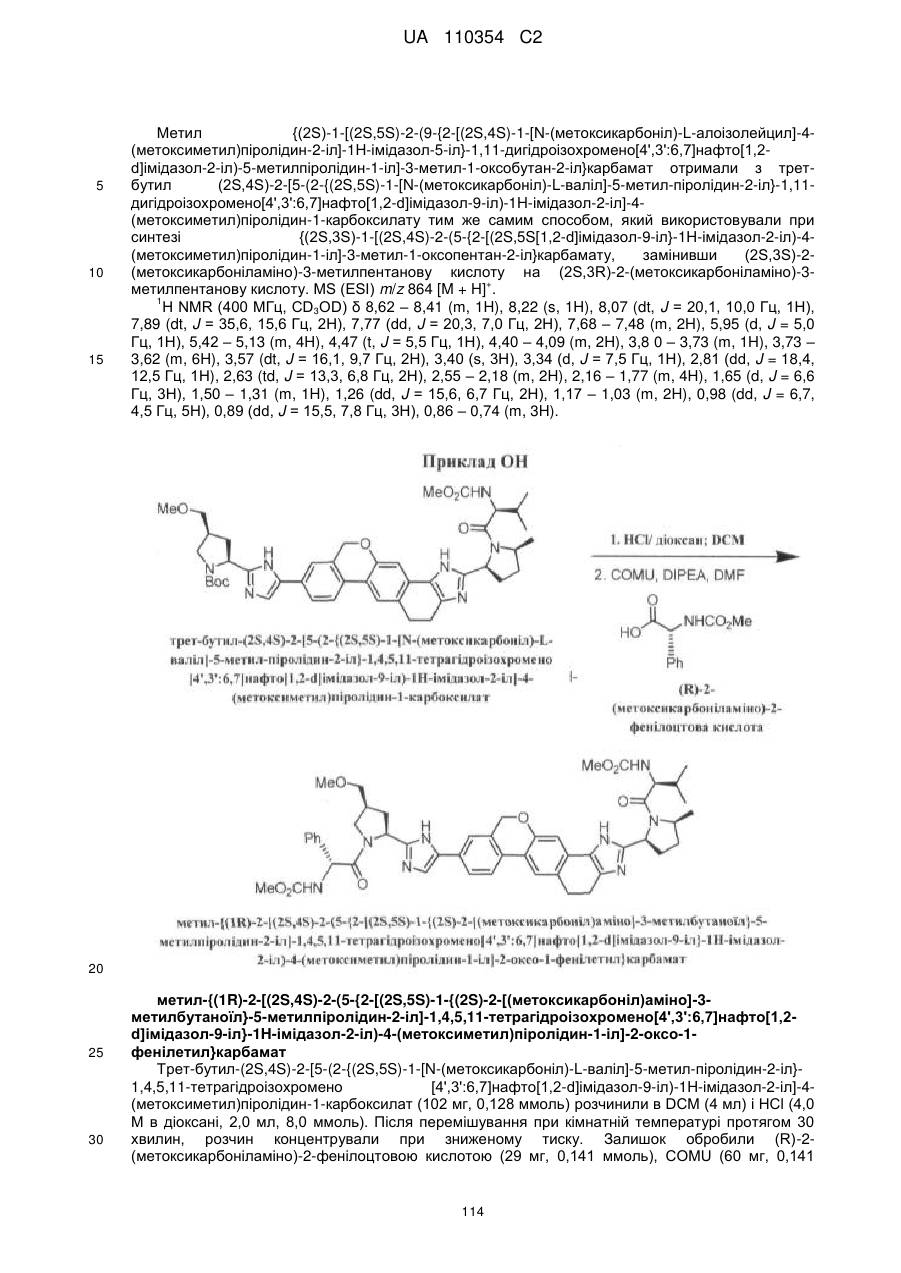
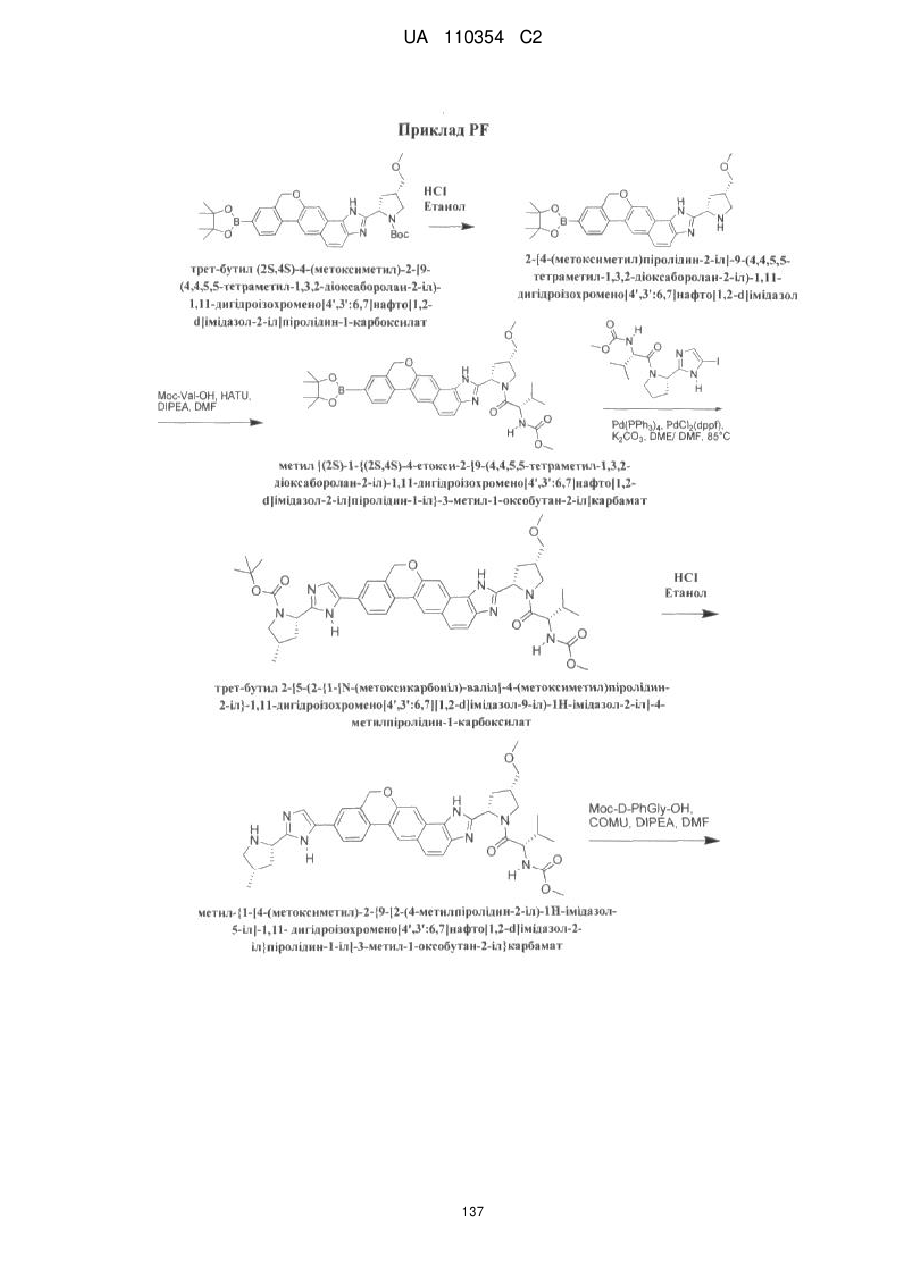
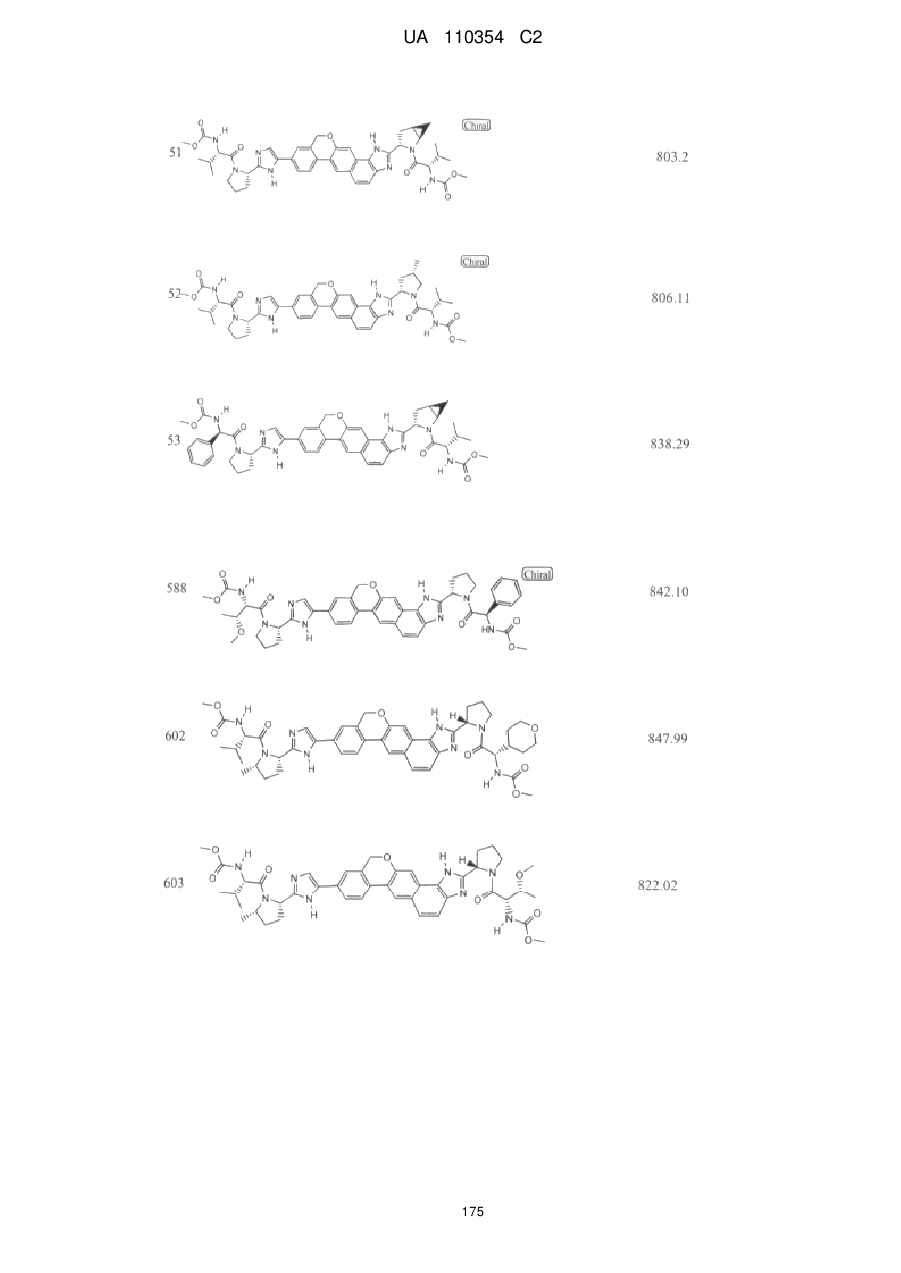
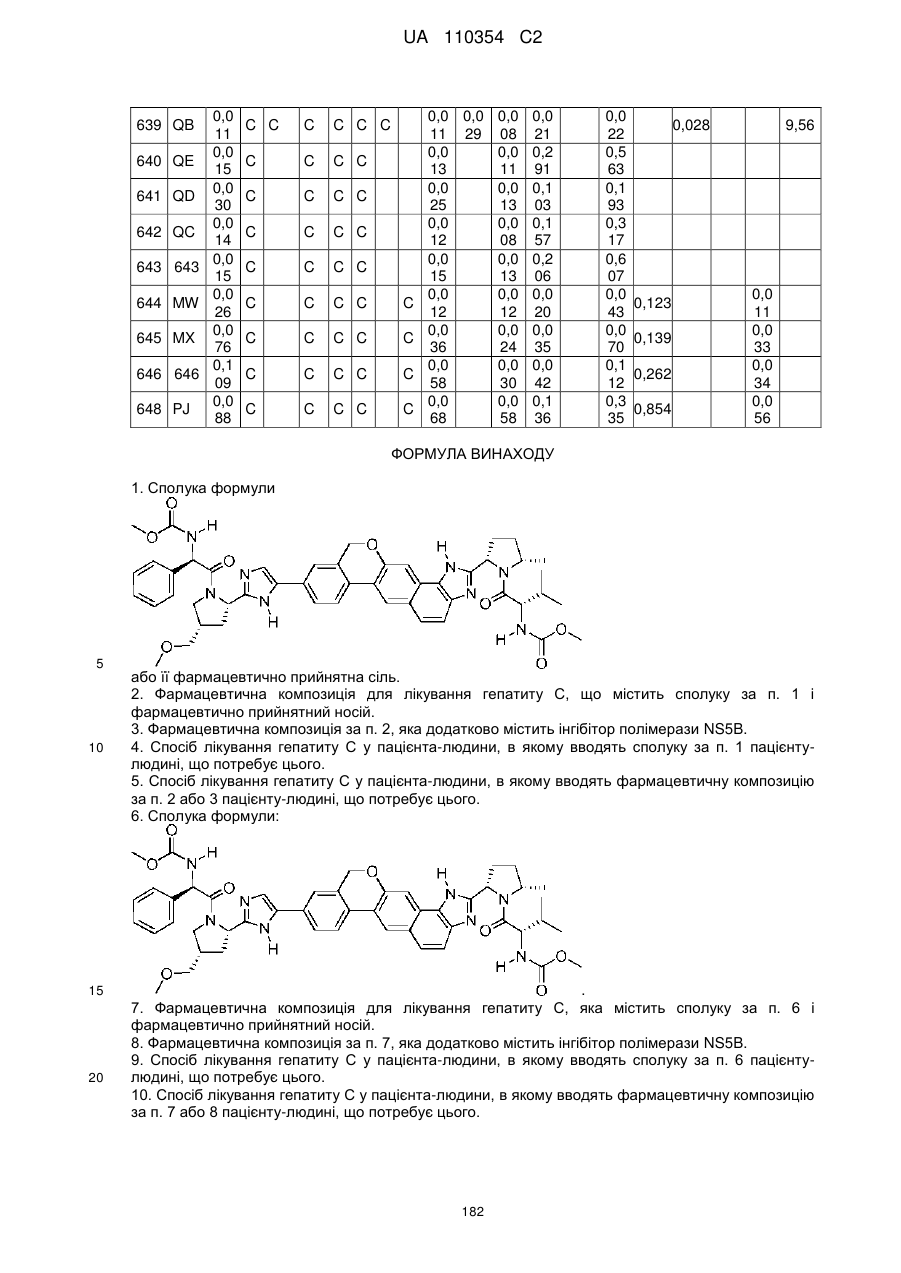
1. Сполука формули
або її фармацевтично прийнятна сіль.
2. Фармацевтична композиція для лікування гепатиту С, що містить сполуку за п. 1 і фармацевтично прийнятний носій.
3. Фармацевтична композиція за п. 2, яка додатково містить інгібітор полімерази NS5B.
4. Спосіб лікування гепатиту С у пацієнта-людини, в якому вводять сполуку за п. 1 пацієнту-людині, що потребує цього.
5. Спосіб лікування гепатиту С у пацієнта-людини, в якому вводять фармацевтичну композицію за п. 2 або 3 пацієнту-людині, що потребує цього.
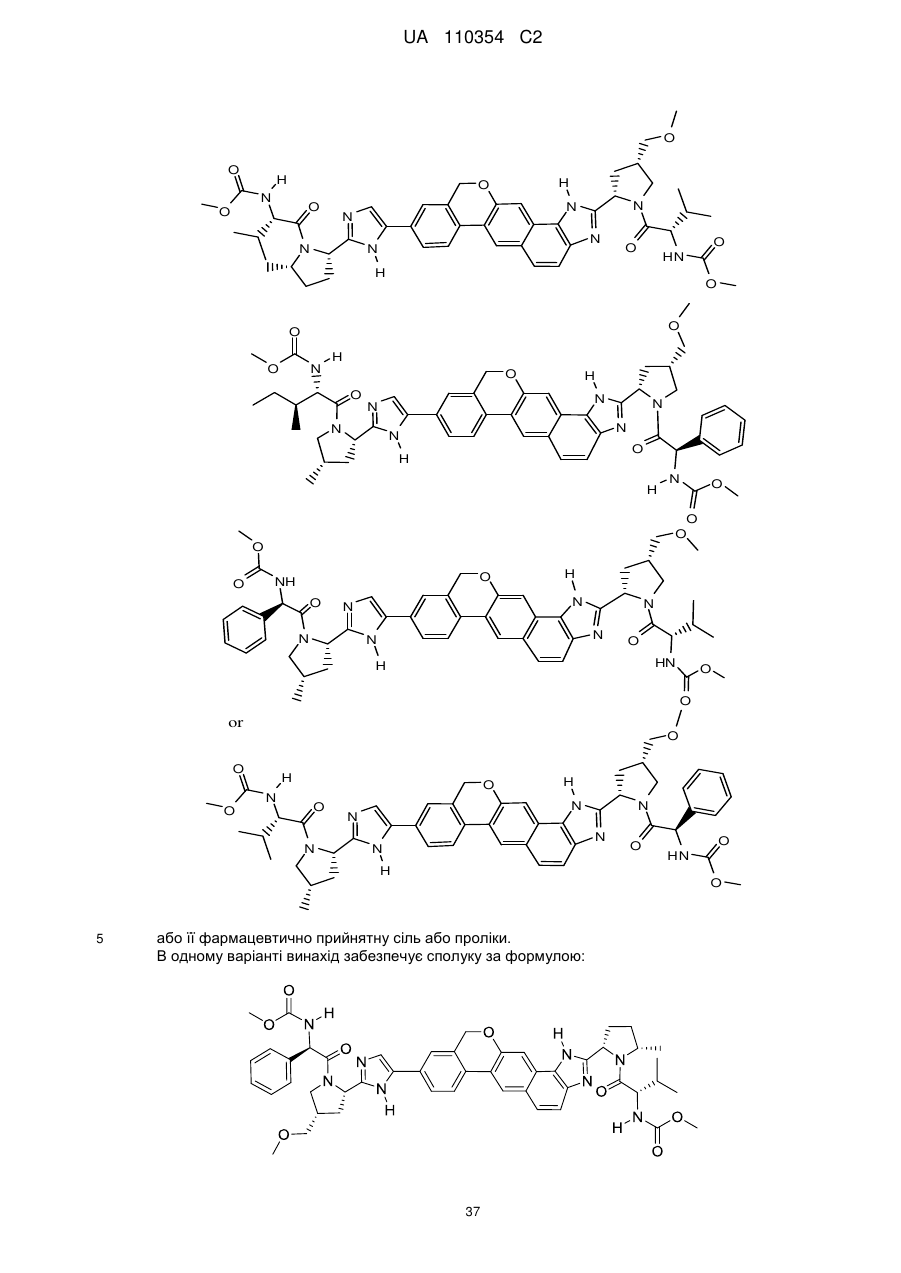
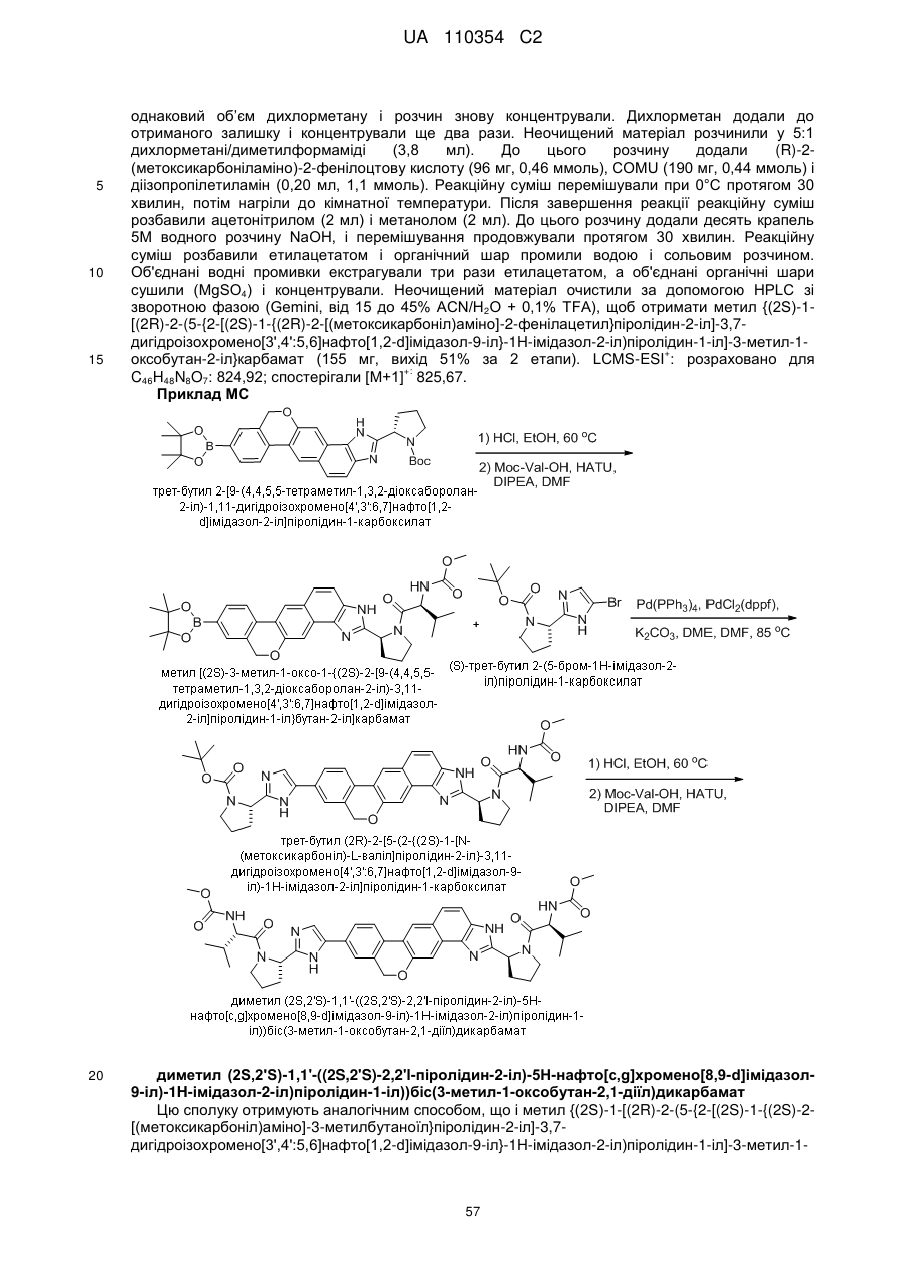
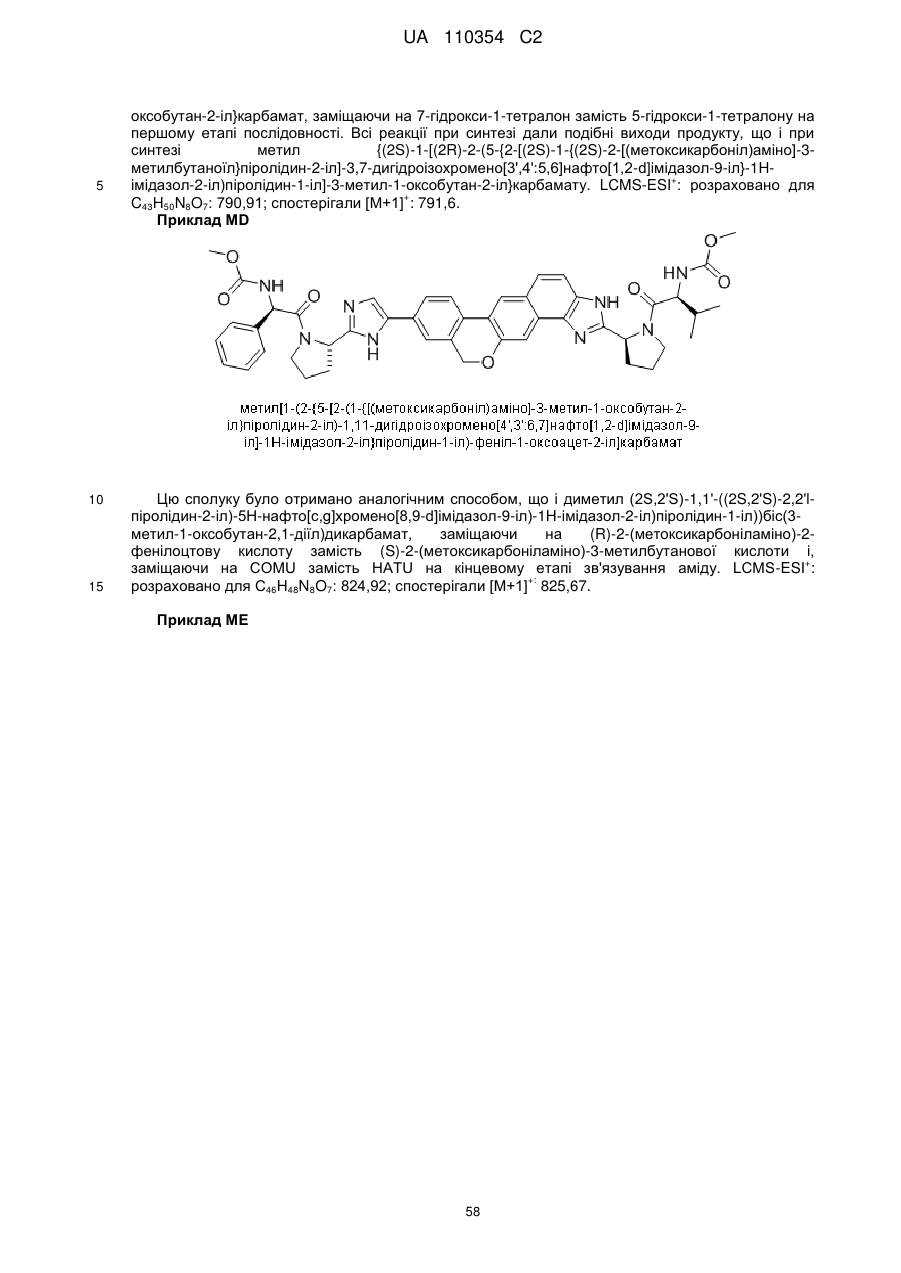
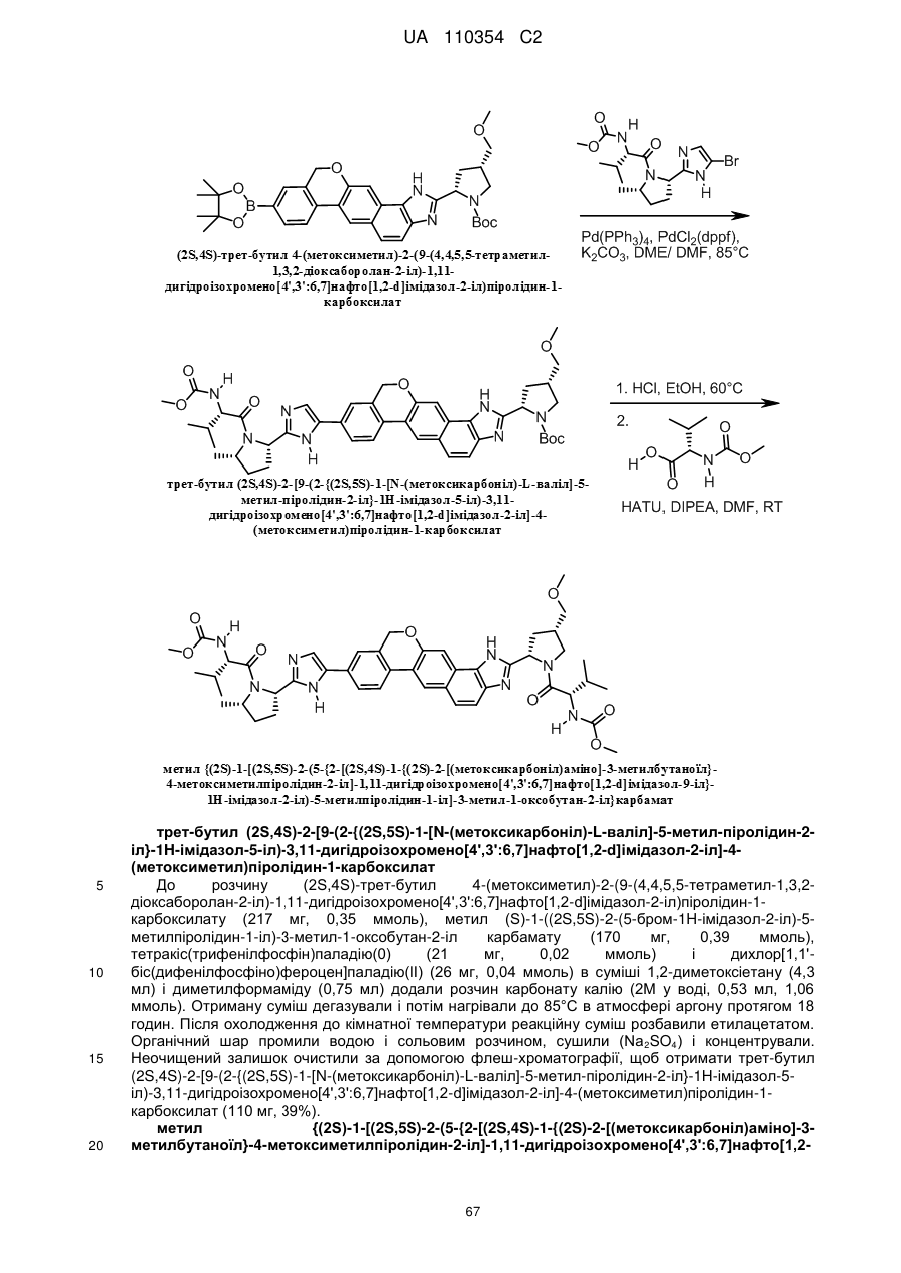
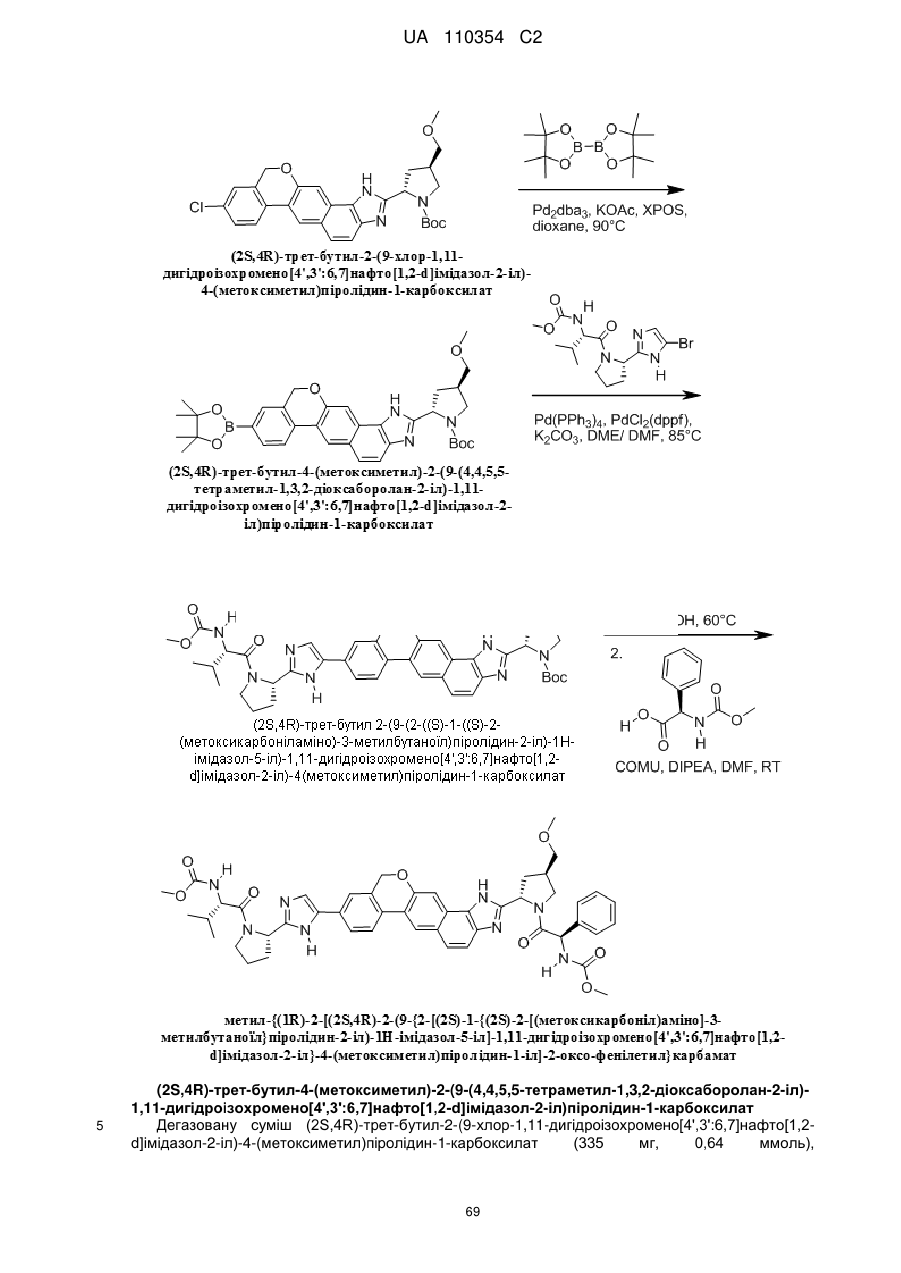
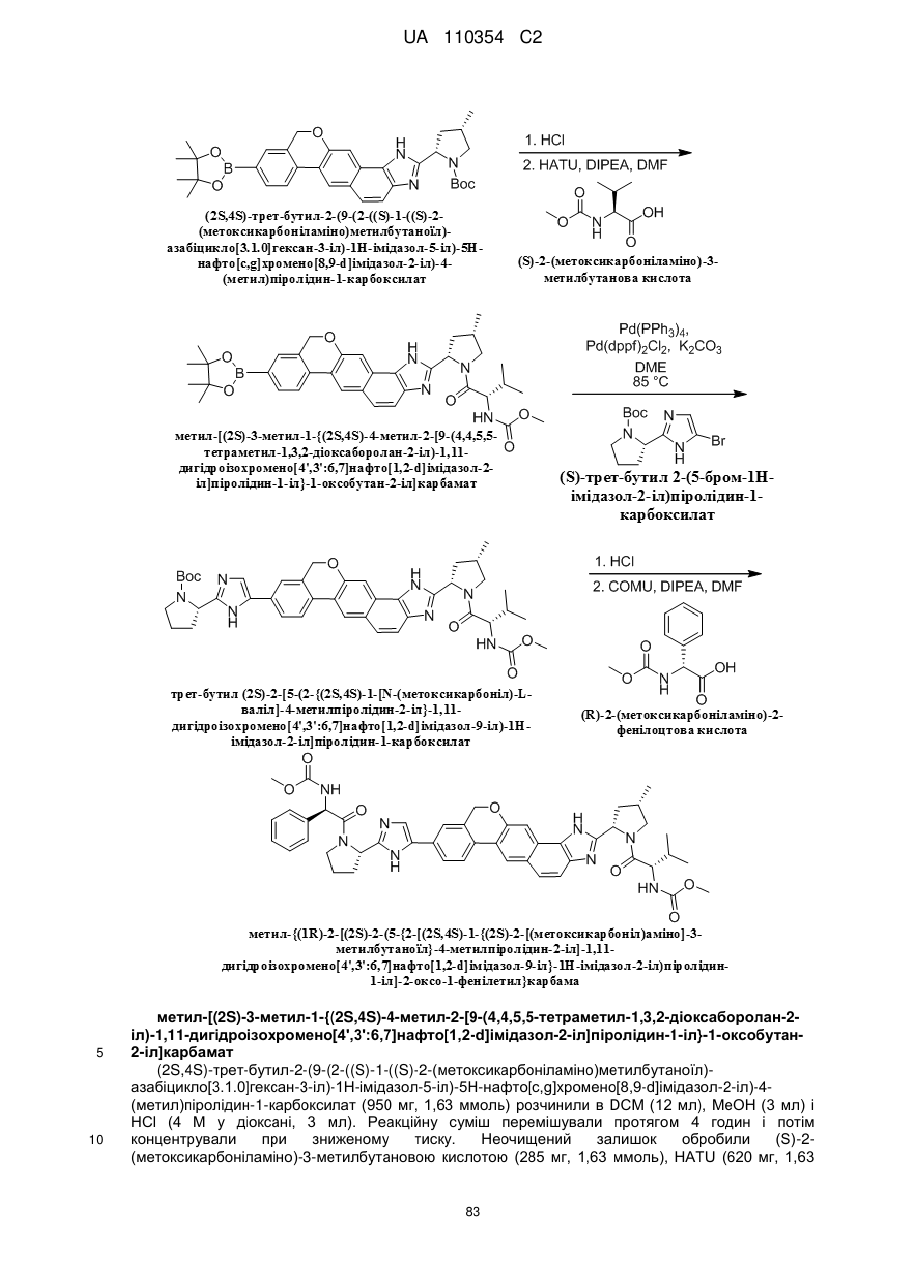
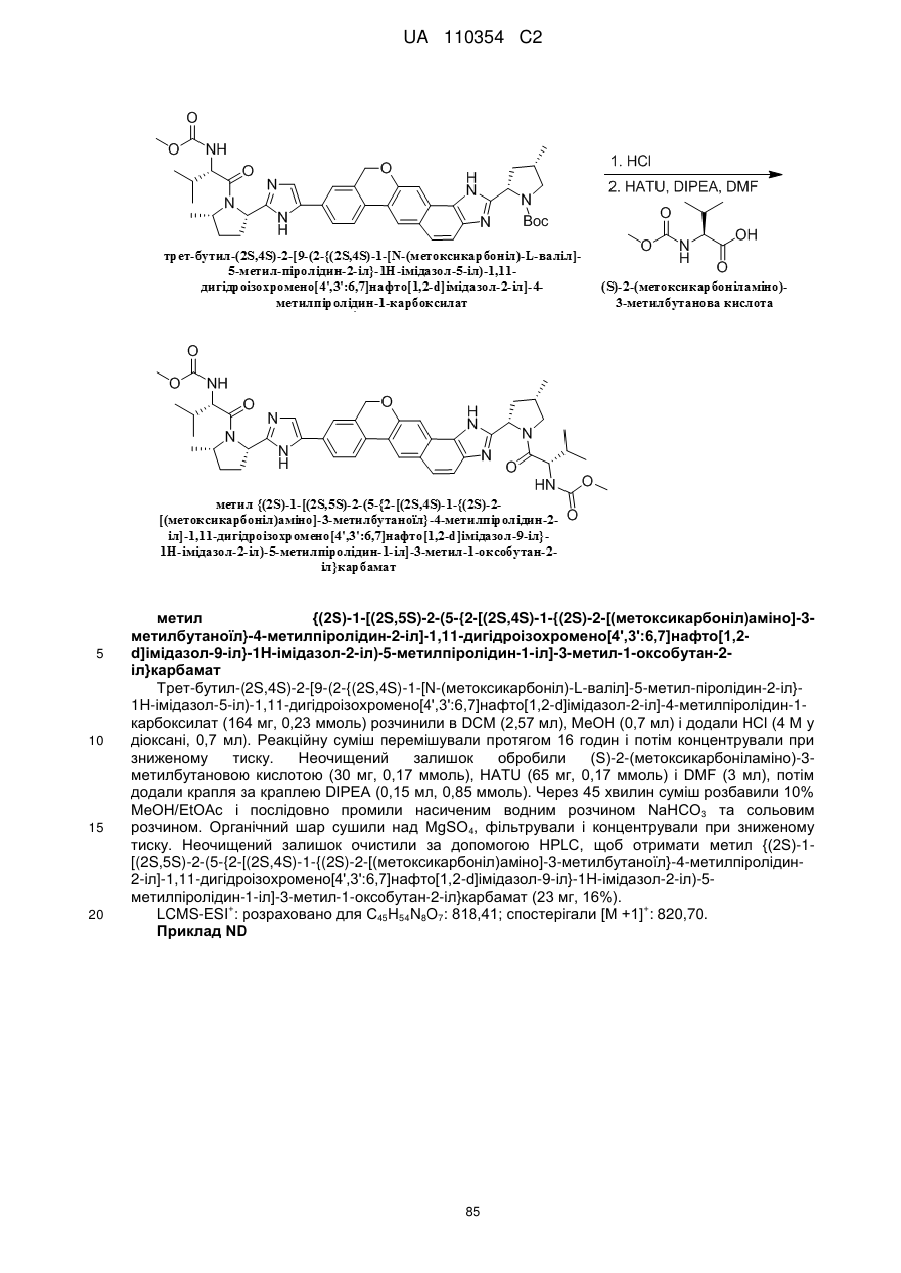
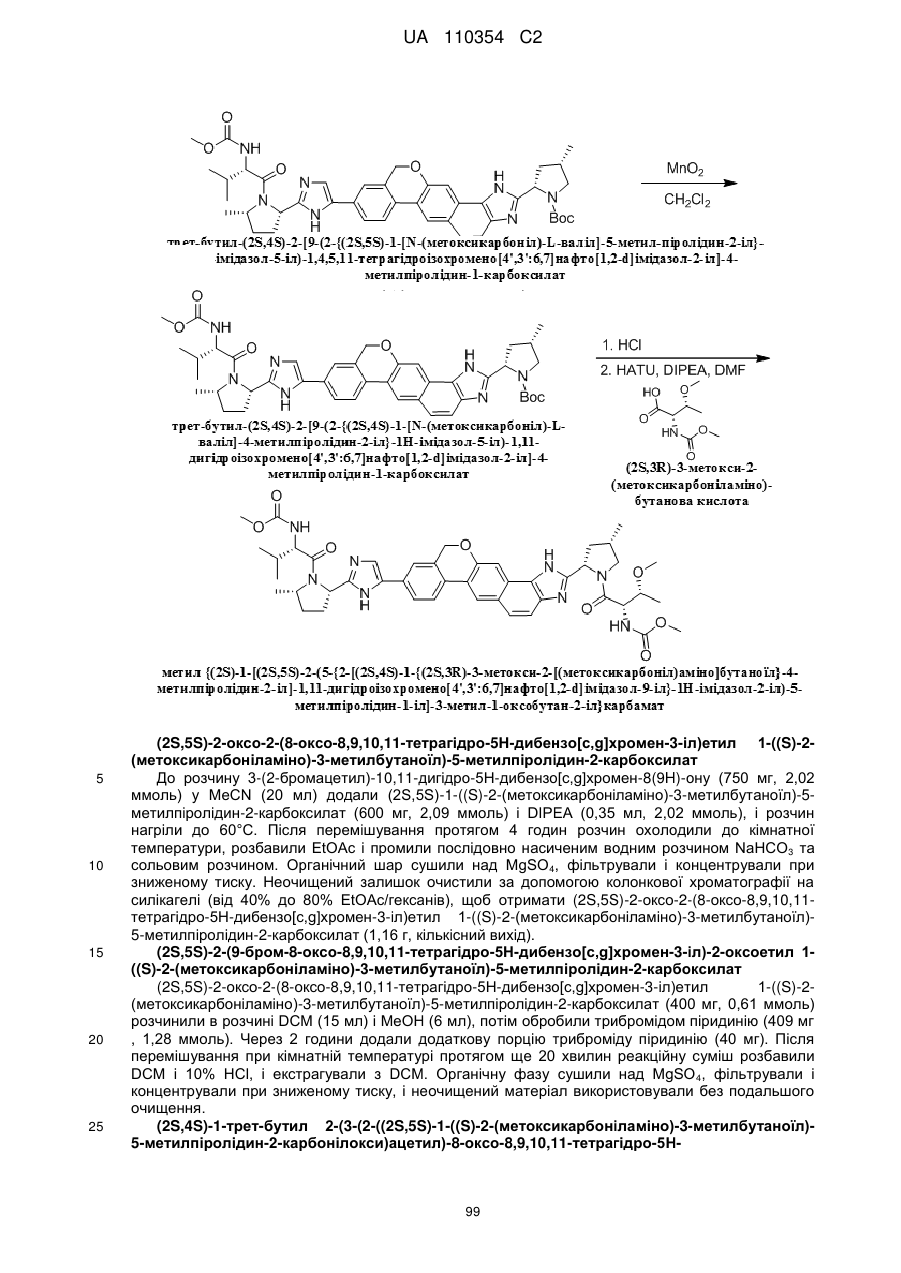
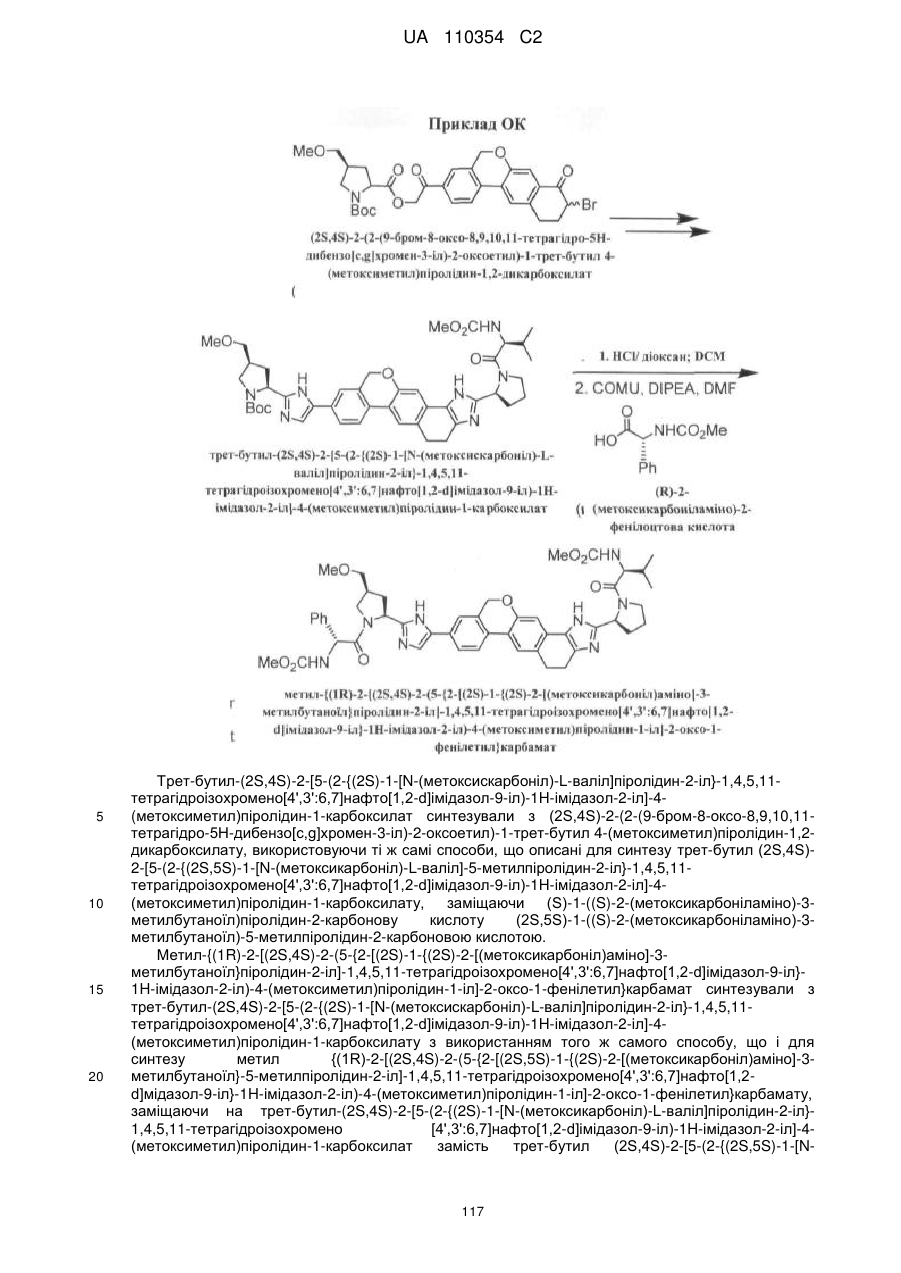
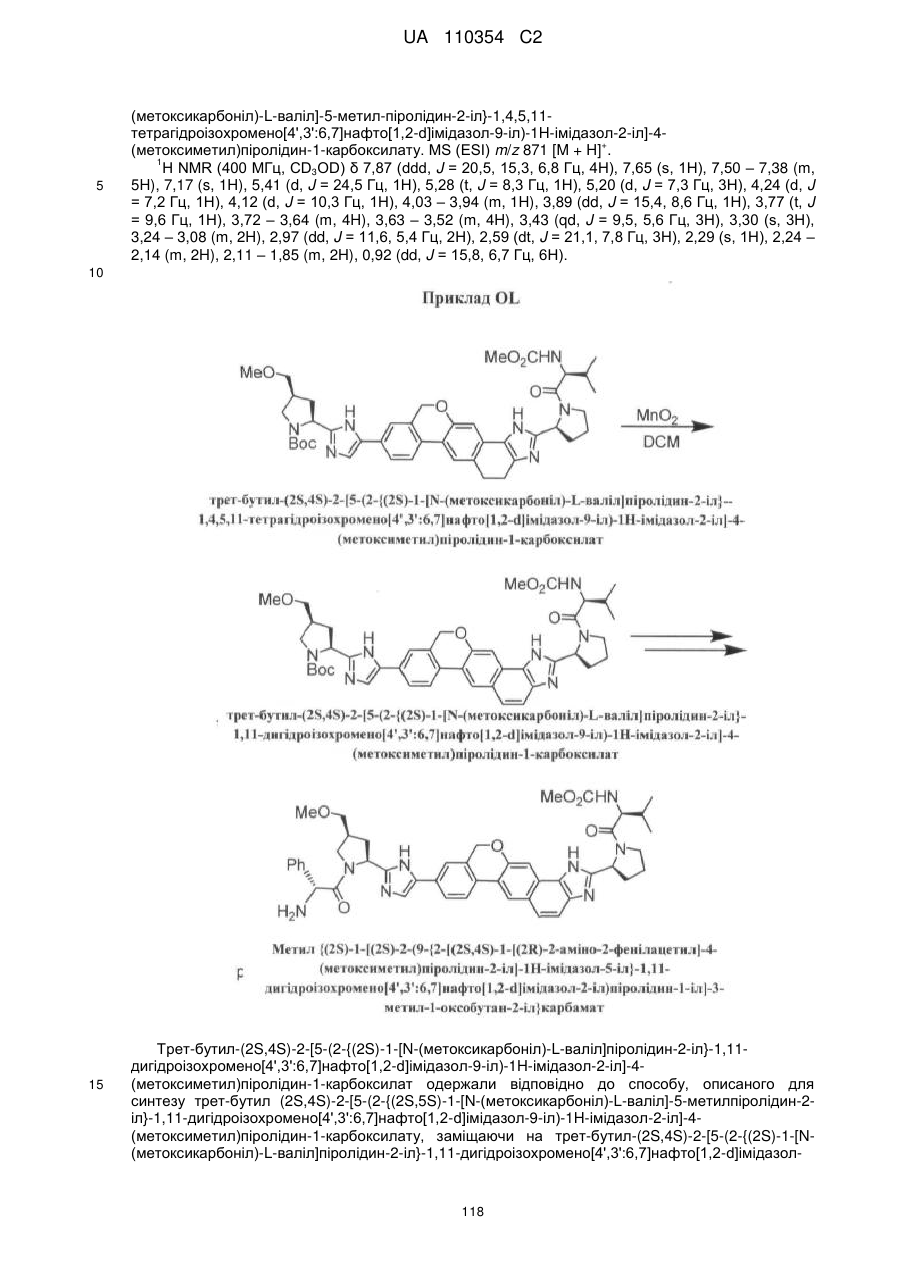
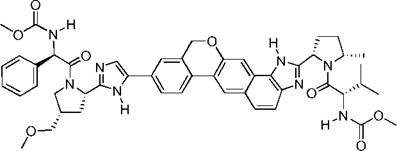
6. Сполука формули:
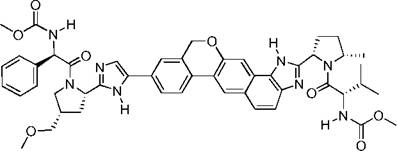 .
.
7. Фармацевтична композиція для лікування гепатиту С, яка містить сполуку за п. 6 і фармацевтично прийнятний носій.
8. Фармацевтична композиція за п. 7, яка додатково містить інгібітор полімерази NS5B.
9. Спосіб лікування гепатиту С у пацієнта-людини, в якому вводять сполуку за п. 6 пацієнту-людині, що потребує цього.
10. Спосіб лікування гепатиту С у пацієнта-людини, в якому вводять фармацевтичну композицію за п. 7 або 8 пацієнту-людині, що потребує цього.
Текст
Реферат: Винахід стосується противірусних сполук, композицій, що містять такі сполуки, і терапевтичних способів лікування, які включають введення таких сполук, а також способів і проміжних продуктів, які використовуються для отримання таких сполук. UA 110354 C2 (12) UA 110354 C2 UA 110354 C2 5 10 15 20 ПРОТИВІРУСНІ СПОЛУКИ ПЕРЕХРЕСНЕ ПОСИЛАННЯ НА СПОРІДНЕНІ ЗАЯВКИ Ця заявка пред’являє свої вимоги згідно з § 119 (е) тому 35 Зведення законів США щодо пріоритету по заявці на патент США з тимчасовим номером заявки 61/560,654, зареєстрованої 16 листопада 2011 року, яка в повному обсязі включена до цієї заявки шляхом даного посилання. ПЕРЕДУМОВИ ВИНАХОДУ Гепатит С вважається хронічною вірусною хворобою печінки, що характеризується захворюванням печінки. Попри те, що ліки для лікування печінки мають широке застосування і засвідчили свою ефективність, токсичність та інші побічні ефекти обмежують їх корисність. Інгібітори вірусу гепатиту С (HCV) є корисними для обмеження розвитку та прогресування інфекції HCV, а також у діагностичних тестах на HCV. Існує потреба в нових терапевтичних агентах HCV. Зокрема, існує потреба у терапевтичних агентах HCV, які відзначаються широкою активністю проти генотипів HCV (наприклад, генотипів 1a, 1b, 2а, 3а, 4а). Існує також особлива потреба в агентах, які є менш сприйнятливими до вірусного опору. Мутації резистентності до інгібіторів були описані стосовно HCV NS5A для генотипів 1a і 1b у "Антимікробних агентах і хіміотерапії", (Antimicrobial Agents and Chemotherapy), вересень 2010 року, том 54, стор. 3641 - 3650. КОРОТКИЙ ОПИС СУТІ ВИНАХОДУ В одному з варіантів винахід забезпечує сполуку за винаходом, яка є сполукою формули (I): 1a 1a E -V де: 1a W є 1a –C(=O)-P -W 1a 1b 1b -P -C(=O)-V -E 1b (I) Y5 H N N N X5 H 25 N 1a 30 і W є необов'язково заміщеним однією або кількома групами, незалежно вибраними з галогену, алкілу, галогеналкілу, або ціано; 5 5 Y є -O-CH2-, або - СН2-О-, X є -CH2-CH2 - або -CH=CH-; 1а E є -N(H)(алкоксикарбонілом), -N(H)(циклоалкілкарбонілом) або 1a 1a 9а -N(H)(циклоалкілоксикарбонілом), або E -V взяті разом є R ; 1b E є -N(H)(алкоксикарбонілом), -N(H)(циклоалкілкарбонілом) або 1b 1b 9b; -N(H)(циклоалкілоксикарбонілом), або E -V взяті разом є R 1a 1b V і V , кожен незалежно, вибрані з: ; 35 1a P вибраний з: ; 40 1b P вибраний з: ; і 9a 9b R і R є незалежно одне від одного: 1 UA 110354 C2 5 10 15 20 25 30 35 40 45 50 55 ; або їх фармацевтично прийнятна сіль або проліки. Винахід також забезпечує збагачені ізотопами сполуки, які є сполуками за винаходом, що містять збагачений ізотоп в одному або декількох положеннях у сполуці. Даний винахід також забезпечує фармацевтичну композицію, що містить сполуку за винаходом або її фармацевтично прийнятну сіль або проліки, і принаймні один фармацевтично прийнятний носій. Даний винахід також забезпечує фармацевтичну композицію для застосування при лікуванні гепатиту С (HCV). В одному з варіантів композиція включає принаймні один додатковий терапевтичний агент для лікування HCV. В одному з варіантів цей терапевтичний агент вибрано з рибавірину, інгібітору протеази NS3, нуклеозидного або нуклеотидного інгібітору полімерази NS5B HCV, інгібітору альфа-глюкозидази 1, гепатопротектору, ненуклеозидного інгібітору полімерази HCV, або їх комбінацій. В одному з варіантів композиція також містить нуклеозидний або нуклеотидний інгібітор полімерази NS5B HCV. В одному з варіантів нуклеозидний або нуклеотидний інгібітор полімерази NS5B HCV вибрано з рибавірину, вірамідину, левовірину, Lнуклеозиду або ізаторибіну. В одному з варіантів забезпечується фармацевтична композиція, що містить сполуку, як описано у цій заявці, і принаймні один нуклеозидний або нуклеотидний інгібітор полімерази NS5B HCV, і принаймні один фармацевтично прийнятний носій. В одному варіанті композиція додатково містить інтерферон, пегільований інтерферон, рибавірин або їх комбінації. В одному варіанті сполука є сполукою, проілюстрованою у прикладі PY. В одному з варіантів нуклеозидний або нуклеотидний інгібітор полімерази NS5B HCV є софосбувіром. Даний винахід також забезпечує фармацевтичну композицію, яка додатково містить інтерферон або пегільований інтерферон. Даний винахід також забезпечує фармацевтичну композицію, яка додатково містить аналог нуклеозиду. Даний винахід також забезпечує фармацевтичну композицію, у якій зазначений аналог нуклеозиду вибраний з рибавірину, вірамідин, левовірин, L-нуклеозиду та ізаторибіну, і зазначений інтерферон є α-інтерфероном або пегільованим α-інтерфероном. Даний винахід також забезпечує спосіб лікування гепатиту С, причому зазначений спосіб включає введення пацієнту-людині фармацевтичної композиції, яка містить терапевтично ефективну кількість сполуки за винаходом. Даний винахід також забезпечує спосіб інгібування HCV, що включає введення ссавцю, який страждає на стан, пов’язаний з активністю HCV, кількості сполуки за винаходом, ефективної для інгібування HCV. Даний винахід також забезпечує сполуку за винаходом для застосування в медичній терапії (наприклад, для застосування при інгібуванні активності HCV або для лікування стану, пов'язаного з активністю HCV), а також застосування сполуки за винаходом для виготовлення лікарського засобу, придатного для інгібування HCV або лікування стану, пов'язаного з активністю HCV у ссавця. Даний винахід також забезпечує способи синтезу і нові проміжні сполуки, описані тут, які є придатними для отримання сполук даного винаходу. Деякі зі сполук за винаходом є придатними для отримання інших сполук даного винаходу. В іншому аспекті даний винахід забезпечує сполуку за винаходом, або її фармацевтично прийнятну сіль або проліки, для використання при профілактичному або терапевтичному лікуванні гепатиту С та розладу, пов'язаного з гепатитом С. В іншому аспекті даний винахід забезпечує спосіб інгібування активності HCV у зразку, що включає обробку зразка сполукою за винаходом. Було встановлено, що сполуки за формулою (I) мають корисну активність проти генотипів 1 HCV. Крім того, деякі сполуки за формулою (I) мають значну активність проти резистентних штамів в GT1. Відповідно, деякі сполуки за формулою (I) мають корисні фармакологічні властивості, які роблять їх придатними для забезпечення поточної потреби у HCV-агентах з такими корисними властивостями. В одному варіанті винахід забезпечує сполуку, яка має поліпшені інгібуючі або фармакокінетичні властивості, в тому числі підвищену активність проти розвитку вірусної 2 UA 110354 C2 5 10 15 20 25 резистентності, поліпшену біодоступність при пероральному введенні, вищу активність (наприклад, для інгібування активності HCV) або подовжений ефективний період напіврозпаду in vivo. Деякі сполуки за винаходом можуть мати менше побічних ефектів, менш складні режими дозування, або бути перорально активними. ДЕТАЛЬНИЙ ОПИС ВИНАХОДУ Далі буде зроблене детальне посилання на певні варіанти втілення винаходу, приклади яких проілюстровані на супроводжувальних структурах і формулах. Хоча винахід буде описаний в поєднанні з перерахованими варіантами втілення, слід розуміти, що вони не призначені для обмеження винаходу цими варіантами. Навпаки, винахід охоплює всі альтернативи, модифікації та еквіваленти, які можуть бути включені в обсяг даного винаходу, як визначено у варіантах втілення. Сполуки Сполуки за винаходом виключають досі відомі сполуки. Тим не менш, у межах винаходу використовуються сполуки, які раніше не були відомі, як такі, що мають противірусні властивості, для противірусних цілей (наприклад, для отримання противірусного ефекту у тварини). Що стосується Сполучених Штатів, сполуки або композиції тут виключають сполуки, які передбачені згідно § 102 тому 35 Зведення законів США, або які є очевидними відповідно до § 103 тому 35 Зведення законів США. Кожного разу, коли сполука, описана у цьому документі, є заміщеною більш ніж одним з тієї 1 " 3" ж самої зазначеної групи, наприклад, "R " або А , то слід розуміти, що групи можуть бути однаковими або різними, тобто кожна група є незалежно вибраною. "Відсутня" - Деякі групи визначені таким чином, що вони можуть бути відсутні. Коли група відсутня, вона стає стиковим зв'язком. Дві групи, які могли б бути з'єднані з цією відсутньою групою, з'єднуються одне з одним через зв'язок. 1a 1b Групи "P" (наприклад, P і Р ) визначені для формули (I) тут, мають один зв'язок з -С(=O)1a за формулою (I) і один зв'язок з групою W . Слід розуміти, що азот групи Р приєднаний до 1a C(=O)- групи за формулою (I), а вуглець групи Р приєднаний до групи W . Y5 H N N N X5 H 30 1a 5 N 5 У групі W присутня група Y . Коли така група Y є визначеною як група -O-CH2-, або -CH2-O5 5 1a , такі групи Y мають спрямованість. Група Y приєднана до групи W в такій ж спрямованості 5 зліва направо, що і кожна зображена. Так, наприклад, коли Y є -О-СН2-, мається на увазі безпосередньо наступна структура: 35 5 Наприклад, коли Y є -CH2-O-, мається на увазі безпосередньо наступна структура: 40 1а 45 1a У структурі I, група W має спрямованість зліва направо, як зображено на I та W , як вони накреслені. 1a 1a 1a 1a 1b 1b 1b E -V –C(=O)-P -W -P -C(=O)-V -E (I), де: 1a W є 3 UA 110354 C2 Y5 H N N N X5 H 1a 5 10 15 1a 25 30 35 40 45 50 1b Наприклад, група P приєднана до групи імідазолу W , а група Р приєднана до 1a пентациклічної кільцевої системи W . "Алкіл" є нормальними, вторинними, третинними або циклічними атомами вуглецю С 1-С18, що містять вуглеводень. Прикладами є метил (Me, -СН3), етил (Et, -СН2СН3), 1-пропіл (н-Pr, нпропіл, -CH2CH2CH3), 2-пропіл (і-Pr , і-пропіл, -СН(СН3)2), 1-бутил-(н-Bu, н-бутил, CH2CH2CH2CH3), 2-метил-1-пропіл (і-Bu, і-бутил, -CH2CH(CH3)2), 2-бутил-(s-Bu, s-бутил, СН(СН3)СН2СН3), 2-метил-2-пропіл (t-Bu, t-бутил, -С(СН3)3), 1-пентил (н-пентил, CH2CH2CH2CH2CH3), 2-пентил (-СН(СН3)СН2СН2СН3), 3-пентил (-СН(СН2СН3)2), 2-метил-2-бутил (-С(СН3)2СН2СН3), 3-метил-2-бутил (-СН(СН3)CH(CH3)2), 3-метил-1-бутил (-CH2CH2CH(CH3)2), 2метил-1-бутил-(-CH2CH(CH3)CH2CH3), 1-гексил (-CH2CH2CH2CH2CH2CH3), 2-гексил (CH(CH3)CH2CH2CH2CH3), 3-гексил (-СН(СН2CH3)(CH2CH2CH3)), 2-метил-2-пентил (C(CH3)2CH2CH2CH3), 3-метил-2-пентил (-СН(СН3)СН(СН3)СН2СН3), 4-метил-2-пентил (CH(CH3)CH2CH(CH3)2), 3-метил-3-пентил (-С(СН3)(СН2СН3)2), 2-метил-3-пентил (CH(CH2CH3)CH(CH3)2), 2,3-диметил-2-бутил (-С(СН3)2CH(CH3)2), 3,3-диметил-2-бутил-( * 20 N CH2 СН(СН3)С(СН3)3, і циклопропілметил . "Алкеніл" є нормальними, вторинними, третинними або циклічними атомами вуглецю С 2-С18, що містять вуглеводень, з принаймні однією ділянкою ненасиченості, тобто вуглець2 вуглецевим, sp подвійним зв'язком. Приклади включають, але не обмежуються, етилен або вініл (-CH=CH2), аліл (-CH2CH=CH2), циклопентеніл (-C5H7), і 5-гексеніл (CH2CH2CH2CH2CH=CH2). "Алкініл" є нормальними, вторинними, третинними або циклічними атомами вуглецю С2-С18, що містять вуглеводень, з принаймні однією ділянкою ненасиченості, тобто вуглецьвуглецевим, sp потрійним зв'язком. Приклади включають, але не обмежуються, ацетиленові (C=CH) і пропаргіл (-CH2C=CН). "Алкілен" стосується насиченого, з розгалуженим або прямим ланцюгом, або циклічного вуглеводневого радикалу, що містить 1-18 атомів вуглецю, і має два одновалентні радикальні центри, отриманих шляхом видалення двох атомів водню з одного й того ж або двох різних атомів вуглецю від вихідного алкану. Типові алкіленові радикали включають, але не обмежуються, метилен (-CH2-) 1,2-етил-(-CH2CH2-), 1,3-пропіл (-CH2CH2CH2-), 1, 4-бутил-(-CH2CH2CH2CH2-), та їм подібні. "Алкенілен" стосується насиченого, з розгалуженим або прямим ланцюгом, або циклічного вуглеводневого радикалу, що містить 2-18 атомів вуглецю, і має два одновалентні радикальні центри, отриманих шляхом видалення двох атомів водню з одного й того ж або двох різних атомів вуглецю від вихідного алкену. Типові радикали алкенілену включають, але не обмежуються, 1,2етилен (-CH=CH-). "Алкінілен" стосується насиченого, з розгалуженим або прямим ланцюгом, або циклічного вуглеводневого радикалу, що містить 2-18 атомів вуглецю, і має два одновалентні радикальні центри, отриманих шляхом видалення двох атомів водню з одного й того ж або двох різних атомів вуглецю від вихідного алкіну. Типові радикали алкінілену включають, але не обмежуються, ацетилен (-C=C-), пропаргіл (-СН2С=C-) і 4-пентиніл (-CH2CH2CH2C=CН). Термін "алкокси" або "алкілокси", як використовується тут, стосується алкільної групі, приєднаної до основної частини молекули через атом кисню. Термін "алкоксикарбоніл", як використовується тут, стосується алкокси групи, приєднаної до основної частини молекули через карбонільну групу. Термін "циклоалкіл", як використовується тут, означає насичену моноциклічну вуглеводневу кільцеву систему, яка має від трьох до семи атомів вуглецю, і нуль гетероатомів. Репрезентативні приклади циклоалкільних груп включають, але не обмежуються, циклопропіл, циклопентил і циклогексил. Циклоалкільні групи за даним винаходом необов'язково заміщені одним, двома, трьома, чотирма або п'ятьма замісниками, незалежно вибраними з алкокси, алкілу, арилу, ціано, галогену, галогеналкокси, галогеналкілу, гетероциклілу, гідрокси, х у гідроксіалкілу, нітро та -NR R , де арил і гетероцикліл необов'язково додатково заміщені одним, 4 UA 110354 C2 5 10 15 20 25 30 двома або трьома замісниками, незалежно вибраними з алкокси, алкілу, ціано, галогену, галогеналкокси, галогеналкілу, гідрокси та нітро. Термін "циклоалкілкарбоніл", як використовується тут, стосується циклоалкільної групи, приєднаної до основної частини молекули через карбонільну групу. Термін "циклоалкілокси", як використовується тут, стосується циклоалкільної групи, приєднаної до основної частини молекули через атом кисню. Термін "циклоалкілоксикарбоніл", як використовується тут, стосується циклоалкілокси групи, приєднаної до основної частини молекули через карбонільну групу. "Арил" означає одновалентний ароматичний вуглеводневий радикал з 6-20 атомами вуглецю, отриманий шляхом видалення одного атома водню від одного атома вуглецю вихідної ароматичної кільцевої системи. Типові арильні групи включають, але не обмежуються, радикали, утворені з бензолу, заміщеного бензолу, нафталіну, антрацену, біфенілу, тощо. "Арилалкіл" стосується ациклічного алкільного радикалу, в якому один з атомів водню, 3 зв'язаних з атомом вуглецю, типово з кінцевим або sp атомом вуглецю, є заміщеним арильним радикалом. Типові арилалкільні групи включають, але не обмежуються, бензил, 2-фенілетан-1іл, нафтилметил, 2-нафтилетан-1-іл, нафтобензил, 2-нафтофенілетан-1-іл, тощо. Арилалкільна група включає від 6 до 20 атомів вуглецю, наприклад, алкільний фрагмент, що включає алканільну, алкенільну або алкінільну групи, арилалкільної групи, містить від 1 до 6 атомів вуглецю, і арильний фрагмент містить від 5 до 14 атомів вуглецю. "Заміщений алкіл", "заміщений арил" і "заміщений арилалкіл" означає алкіл, арил і арилалкіл, відповідно, в яких один або більше атомів водню, кожен незалежно, замінені неводневим замісником. Типові замісники включають, але не обмежуються, галоген (наприклад, F, Cl, Br, I), -R, -OR, -SR, -NR2, - CF3, -CCl3, -OCF3, -CN, -NO2 - N(R)C(=O)R, -C(=O)R, -OC(=O)R, C(O)OR, -C(=O)NRR,-S(=O)R, -S(=O)2OR, -(=O) 2R, -OS(=O)2OR, -S(=O)2NRR, а кожен R є незалежно - Н, алкілом, арилом, арилалкілом або гетероциклом. Алкіленові, алкеніленові і алкініленові групи також можуть бути зміщені аналогічним чином. Термін "необов'язково заміщений" стосовно певної частини сполуки за формулою I (наприклад, необов'язково заміщена арильна група) стосується частини, що містить 0, 1, 2 або більше замісників. Символ "-----" в кільцевій структурі означає, що зв'язок є одинарним або подвійним зв'язком. L L E E У прикладі, що не має обмежувального характеру D L E D 35 40 45 50 L L може бути D L або . "Галогеналкіл", як використовується тут, включає алкільну групу, заміщену одним або кількома атомами галогену (наприклад, F, Cl, Br або I). Репрезентативні приклади галогеналкілу включають трифторметил, 2,2,2-трифторетил і 2,2,2-трифтор-1-(трифторметил)етил. "Гетероцикл" або "гетероцикліл", як використовується тут, включає як приклад, а не обмеження, ці гетероцикли, описані у "Принципах сучасної гетероциклічної хімії" (Paquette, Leo A.; Principles of Modern Heterocyclic Chemistry, WA Benjamin, Нью-Йорк, 1968), зокрема, глави 1, 3, 4 , 6, 7 і 9; "Хімія гетероциклічних сполук, Серія монографій" (The Chemistry of Heterocyclic Compounds, A Series of Monographs, John Wiley & Sons, Нью-Йорк, 1950 по теперішній час), зокрема Томи 13, 14, 16, 19, і 28, і J. Am. Chem. Soc. (1960) 82:5566. В одному конкретному варіанті "гетероцикл" включає в себе "карбоцикл", як визначено тут, в якому один або більше (наприклад, 1, 2, 3 або 4) атомів вуглецю були замінені на гетероатом (наприклад, О, N або S). Термін гетероцикл також включає "гетероарил", який є гетероциклом, де принаймні одне з гетероциклічних кілець є ароматичним. Приклади гетероциклів включають, як приклад, а не обмеження, піридил, дигідропіридил, тетрагідропіридил (піперидил), тіазоліл, тетрагідротіофеніл, окиснений сіркою тетрагідротіофеніл, піримідиніл, фураніл, тієніл, піроліл, піразоліл, імідазоліл, тетразоліл, бензофураніл, тіанафталеніл, індоліл, індоленіл, хінолініл, ізохінолініл, бензімідазол, піперидиніл, 4-піперидоніл, піролідиніл, 2-піролідоніл, піролініл, тетрагідрофураніл, тетрагідрохінолініл, тетрагідроізохінолініл, декагідрохінолініл, октагідроізохінолініл, азоциніл, триазиніл, 6H-1,2,5-тіадіазиніл, 2H,6H-1,5,2-дитіазиніл, тієніл, тіантреніл, піраніл, ізобензофураніл, хроменіл, ксантеніл, феноксантеніл, 2Н-піроліл, ізотіазоліл, ізоксазоліл, піразиніл, піридазиніл, індолізиніл, ізоіндоліл, 3Н-індоліл, 1Н-індазоліл, пуриніл, 4H-хінолізініл, 5 UA 110354 C2 5 фталазиніл, нафтиридиніл, хіноксалін, хіназолініл, цінолініл, птеридиніл, 4Н-карбазоліл, карбазоліл, β-карболініл, фенантридиніл, акридиніл, піримідиніл, фенантролініл, феназиніл, фенотіазиніл, фуразаніл, феноксазиніл, ізохроманіл, хроманіл, імідазолідиніл, імідазолініл, піразолідиніл, піразолініл, піперазиніл, індолініл, ізоіндолініл, хіноклідиніл, морфолініл, оксазолідиніл, бензотриазоліл, бензизоксазоліл, оксиндоліл, бензоксазолініл, ізатіаноїл і бістетрагідрофураніл: O . O 10 15 20 25 30 35 40 45 50 55 Як приклад, а не обмеження, гетероцикли, зв'язані вуглецем, є пов’язаними в положенні 2, 3, 4, 5 або 6 піридину, положенні 3, 4, 5 або 6 піридазину, положенні 2, 4, 5 або 6 піримідину, положенні 2, 3, 5 або 6 піразину, положенні 2, 3, 4 або 5 фурану, тетрагідрофурану, тіофурану, тіофену, піролу або тетрагідропіролу, в положенні 2, 4, або 5 оксазолу, імідазолу або тіазолу, положенні 3, 4 або 5 ізоксазолу, піразолу або ізотіазолу, положенні 2 або 3 азиридину, положенні 2, 3 або 4 ацетидину, в положенні 2, 3, 4, 5, 6, 7 або 8 хіноліну або положенні 1, 3, 4, 5, 6, 7 або 8 ізохіноліну. Ще більш типово гетероцикли, зв'язані вуглецем, включають 2-піридил, 3-піридил, 4-піридил, 5-піридил, 6-піридил, 3-піридазиніл, 4-піридазиніл, 5-піридазиніл, 6піридазиніл, 2-піримідиніл, 4-піримідиніл, 5-піримідиніл, 6-піримідиніл, 2-піразиніл, 3-піразиніл, 5піразиніл, 6-піразиніл, 2-тіазоліл, 4-тіазоліл або 5-тіазоліл. Як приклад, а не обмеження, гетероцикли, зв’язані азотом, є пов'язаними в положенні 1 азиридину, ацетидину, піролу, піролідіну, 2-піроліну, 3-піроліну, імідазолу, імідазолідинілу, 2імідазоліну, 3-імідазоліну, піразолу, піразоліну, 2-піразоліну, 3-піразоліну, піперідину, піперазину, індолу, індоліну, 1Н-індазолу, у положенні 2 ізоіндолу або ізоіндоліну, положенні 4 морфоліну і положенні 9 карбазолу або β-карболіну. Ще більш типово, гетероцикли, зв’язані азотом, включають 1-азиридил, 1-ацетедил, 1-піроліл, 1-імідазоліл, 1-піразоліл і 1-піперидиніл. "Карбоцикл" стосується насиченого, ненасиченого або ароматичного кільця, що має близько 25 атомів вуглецю. Типово, карбоцикл має від 3 до 7 атомів вуглецю у якості моноциклу, близько від 7 до 12 атомів вуглецю як біцикл, і близько до 25 атомів вуглецю як поліцикл. Моноциклічні карбоцикли типово мають від 3 до 6 кільцевих атомів, ще більш типово від 5 або 6 кільцевих атомів. Біциклічні карбоцикли типово мають від 7 до 12 кільцевих атомів, наприклад, розташованих у вигляді біцикло [4,5], [5,5], [5,6] або [6,6], системи або 9 або 10 кільцевих атомів, розташованих у вигляді біцикло [5,6] або [6,6] системи. Термін "карбоцикл" включає в себе "циклоалкіл", який є насиченим або ненасиченим карбоциклом. Приклади моноциклічних карбоциклів включають циклопропіл, циклобутил, циклопентил, 1-циклопентил-1-еніл, 1циклопентил-2-еніл, 1-циклопентил-3-еніл, циклогексил, 1-циклогексен-1-еніл, 1-циклогекс-2еніл, 1-циклогекс-3-еніл, феніл, спірил і нафтил. Термін "аміно", як використовується тут, стосується -NH2. Термін "хіральний" стосується молекул, які мають властивість ненакладання дзеркального партнера, тоді як термін "ахіральний" стосується молекул, що накладаються на їх дзеркального партнера. Термін "стереоізомери" стосується сполук, які мають ідентичний хімічний склад, але відрізняються за розташуванням атомів або груп у просторі. "Діастереомер" стосується стереоізомеру з двома або більше центрами хіральності, і чиї молекули не є дзеркальними відображеннями одне одного. Діастереомери мають різні фізичні властивості, наприклад, температуру плавлення, температуру кипіння, спектральні властивості та реакційну здатність. Суміші діастереомерів може розділятися шляхом аналітичних процедур з високою роздільною здатністю, таких як електрофорез і хроматографія. "Енантіомери" стосуються двох стереоізомерів сполуки, які є дзеркальними відображеннями одне одного, що не накладаються. Термін "лікування" або "лікувати" в тій мірі, в якій він стосується хвороби або стану, включає запобігання виникненню захворювання або стану, інгібування захворювання або стану, усунення захворювання або стану, і/або полегшення одного або більше симптомів захворювання або стану. Стереохімічні визначення та умовні позначення, які використовуються тут, як правило, відповідають "Словнику хімічних термінів" (1984 р.) С.П Паркера, видавництва "McGraw-Hill" (S.P. Parker, Ed., McGraw-Hill Dictionary of Chemical Terms) компанії "McGraw-Hill Book Company", 6 UA 110354 C2 5 10 15 20 25 30 35 40 45 50 55 60 Нью-Йорк, та "Стереохімії органічних сполук" (1994 р.) Еліїл. Е., і Вілен, С., (Eliel, E. and Wilen, S., Stereochemistry of Organic Compounds) видавництва "John Wiley & Sons, Inc", Нью-Йорк. Багато органічних сполук існують в оптично активних формах, тобто вони мають здатність обертати площину лінійно поляризованого світла. При описі оптично активної сполуки префікси (D і L) або (R і S) використовуються для позначення абсолютної конфігурації молекули щодо її хірального центру (-ів). Префікси d і l або (+) і (-) використовуються для позначення знака обертання лінійно поляризованого світла сполукою, причому (-) або 1 означає, що сполука є лівообертальною. Сполука з префіксом (+) або d є правообертальною. Для даної хімічної структури ці стереоізомери є ідентичними, за винятком того, що вони є дзеркальними відображеннями одне одного. Конкретний стереоізомер може також називатися енантіомером, а суміш таких ізомерів часто називають енантіомерною сумішшю. Суміш енантіомерів у співвідношенні 50:50 називають рацемічною сумішшю або рацематом, яка може виникнути за відсутності стереоселекції або стереоспеціфічності в хімічній реакції або процесі. Терміни "рацемічна суміш" і "рацемат" стосуються еквімолярної суміші двох енантіомерних видів, позбавленої оптичної активності. Винахід включає всі стереоізомери сполук, описаних тут. Проліки Термін "проліки", як використовується тут, стосується будь-якої сполуки, яка при введенні в біологічну систему генерує сполуку за винаходом, що інгібує активність HCV ("активна інгібуюча сполука"). Сполука може бути утворена з проліків в результаті: (I) спонтанної хімічної реакції (ій), (II), каталізованої ферментом хімічної реакції (-ій), (III), фотолізу і/або (IV), метаболічної хімічної реакції (-ій). "Фрагмент проліків" стосується лабільної функціональної групи, яка відділяється від активної інгібуючої сполуки в процесі обміну речовин, системно, всередині клітини, шляхом гідролізу, ферментативного розщеплення, або будь-яким іншим процесом (Бунгаард, Ганс, "Розробка та застосування проліків" в "Підручнику з розробки та створення лікарських засобів" (1991)) (Bundgaard, Hans, "Design and Application of Prodrugs" in A Textbook of Drug Design and Development (1991), P. Krogsgaard-Larsen and H. Bundgaard, Eds. Harwood Academic Publishers, стоp. 113-191). Ферменти, які наділені механізмом ферментативної активації сполук проліків за винаходом, включають, але не обмежуються, амідази, естерази, мікробні ферменти, фосфоліпази, холінестерази та фосфази. Фрагменти проліків можуть сприяти підвищенню розчинності, поглинання і ліпофільності для оптимізації доставки лікарських засобів, біодоступності та ефективності. Фрагмент проліків може включати активний метаболіт або сам препарат. Приклади фрагментів проліків включають гідролітично чутливі або лабільні складні ефіри 99 99 99 ацилоксиметилу CH2OC(=O)R і карбонати ацилоксиметилу CH2OC(=O)OR , де R є С1-С6 алкіл, С1-С6 заміщений алкіл, C6-C20 арил або С6-С20 заміщений арил. Складний ефір ацилоксіалкілу вперше був використаний як стратегія проліків для карбонових кислот, а потім застосовувався до фосфатів та фосфонатів Фаркухаром та співавт. (Farquhar et al.) (1983) J. Pharm. Sci. 72: 324; також патенти США № № 4816570, 4968788, 5663159 і 5792756. Згодом, складний ефір ацилоксіалкілу використовувався для перенесення фосфонових кислот через клітинні мембрани і для підвищення біодоступності. Близький варіант складного ефіру ацилоксіалкілу, складний ефір алкоксикарбонілоксіалкілу (карбонат) може також підвищити біодоступність при пероральному введенні як фрагменту проліків у сполуках комбінацій за винаходом. Прикладом складного ефіру ацилоксиметилу є півалоїлоксиметокси, (POM)CH2OC(=O)C(CH3)3. Прикладом фрагменту проліків карбонату ацилоксиметилу є півалоїлоксиметилкарбонат (POC)- CH2OC(=O)OC(CH3)3. Арилові ефіри фосфорних груп, зокрема, складні фенілові ефіри, як повідомляється, підвищують біодоступність при пероральному введенні (De Lombaert et al. (1994) J. Med Chem 37: 498). Складні фенілові ефіри, що містять ортофосфат складного ефіру карбонової кислоти також були описані (Khamnei and Torrence, (1996) J. Med. Chem. 39:4109-4115). Складні бензилові ефіри, як повідомляється, генерують вихідні фосфонові кислоти. У деяких випадках замісники в орто- або пара- положенні можуть прискорити гідроліз. Бензилові аналоги з ацильованим фенолом або алкільованим фенолом можуть генерувати фенольну сполуку під дією ферментів, наприклад, естераз, оксидаз і т. д., яка, у свою чергу піддається розщепленню у бензильному C-О зв'язку для отримання фосфорної кислоти і проміжного продукту хінонметиду. Приклади цього класу проліків описані Мітчелом та співавт. (Mitchell et al.) (1992) J. Chem. Soc. Perkin Trans. II 2345; Glazier WO 91/19721. Крім того, були описані інші бензильні проліки, які містять групу, що містить складний ефір карбонової кислоти, приєднану до бензильного метилену (Glazier WO 91/19721). Проліки, що містять тіо-, як повідомляють, використовуються для внутрішньоклітинної доставки фосфонатних препаратів. Ці проефіри містять етілтіо групу, в 7 UA 110354 C2 5 10 15 20 25 30 35 40 45 50 55 60 якій тіольна група є або етерифікованою ацильною групою або комбінована з іншою тіольною групою для формування дисульфіду. Деетерифікація або зменшення дисульфіду генерує вільний тіо проміжний продукт, який згодом розпадається на фосфорну кислоту і епісульфід (Puech et al. (1993) Antiviral Res ., 22: 155-174; Benzaria et al. (1996) J. Med. Chem. 39: 4958). Захисні групи У контексті даного опису захисні групи включають фрагменти проліків і хімічні захисні групи. "Захисна група" стосується фрагменту сполуки, який маскує або змінює властивості функціональної групи або властивості сполуки в цілому. Хімічні захисні групи і стратегії захисту / зняття захисту є добре відомими в даній галузі техніки. Див, наприклад, "Захисні групи в органічній хімії", (Protective Groups in Organic Chemistry, Theodora W. Greene, John Wiley & Sons, Inc., New York, 1991). Захисні групи часто використовуються для маскування реакційної здатності певних функціональних груп, для сприяння ефективності бажаних хімічних реакцій, наприклад, створення і розриву хімічних зв'язків упорядкованим і планомірним чином. Захист функціональних груп сполуки змінює інші фізичні властивості, крім реакційної здатності захищеної функціональної групи, такі як полярність, ліпофільність (гідрофобність) та інші властивості, які можливо виміряти за допомогою загальних аналітичних інструментів. Хімічно захищені проміжні продукти самі можуть бути біологічно активними або неактивними. Захищені сполуки можуть також проявляти змінені, а в деяких випадках, оптимізовані властивості in vitro та in vivo, наприклад, проходження через клітинні мембрани і стійкість до ферментативного розкладання або секвестрації. У цій ролі, захищені сполуки із передбачуваним терапевтичним ефектом можуть називатися проліками. Інша функція захисної групи полягає в перетворенні вихідного препарату в проліки, причому вихідний лікарський засіб вивільнюється під час перетворення проліків in vivo. Оскільки активні проліки можуть бути поглинені більш ефективно, ніж вихідний препарат, проліки можуть мати більш високу активність in vivo, ніж вихідний препарат. Захисні групи видаляють або in vitro, у випадку хімічних проміжних продуктів, або in vivo, у випадку проліків. У випадку проміжних хімічних речовин, не так важливо, щоб отримані в результаті продукти після видалення захисної групи, наприклад, спирти, були фізіологічно прийнятними, хоча в цілому більш бажано, якщо продукти є фармакологічно нешкідливими. Захисні групи є доступними, загально відомими і використовуваними, і, необов'язково, використовуються для запобігання побічним реакціям із захищеною групою в процесі синтезу, тобто маршрути або способи отримання сполук за винаходом. Здебільшого рішення про те, які групи захистити, коли це зробити, і природа хімічної захисної групи "PG" залежатиме від хімічного середовища реакції, що повинне бути захищене (наприклад, кислі, лужні, окиснювальні, відновлювальні або інші умови), і передбачуваного напрямку синтезу. PG не повинні бути, і зазвичай не є, такими ж, якщо сполуку заміщено кількома PG. Загалом, PG буде використовуватися для захисту функціональних груп, таких як карбоксил, гідроксил, тіо- або аміногрупи, і тим самим, для запобігання побічним реакціям або іншим чином для сприяння синтетичній ефективності. Порядок видалення захисної групи для отриманням вільних незахищених груп залежить від передбачуваного напряму синтезу та умов реакції, які можуть виникнути, і може відбуватися в будь-якому порядку, як визначено фахівцем у даній галузі. Різні функціональні групи сполук за винаходом можуть бути захищені. Наприклад, захисні групи для груп -ОН (як то гідроксил, карбонова кислота, фосфонова кислота або інші функції) включають в себе "складноефірні або ефір-формуючі групи". Складноефірні або ефір-формуючі групи здатні функціонувати в якості хімічних захисних груп у схемах синтезу, викладених в даному документі. Проте, деякі гідроксильні і тіо-захисні групи не є ні складноефірними, ні ефірформуючими групами, як буде зрозуміло фахівцям в даній галузі, і включені до амідів, що обговорюються нижче. Дуже велика кількість гідроксильних захисних груп та амідоформуючих груп і відповідних хімічних реакцій розщеплення описані в "Захисних групах в органічному синтезі" (Protective Groups in Organic Synthesis, Theodora W. Greene (John Wiley & Sons, Inc., New York, 1991, ISBN 0-471-62301-6) ("Greene")). Дивіться також працю "Захисні групи" (Kocienski, Philip J.; Protecting Groups (Georg Thieme Verlag Stuttgart, New York, 1994)), що включена як посилання у повному обсязі. Зокрема Глава 1, Захисні групи: Огляд, стор 1-20, Глава 2, Гідроксильні захисні групи, стор. 21-94, Глава 3, Діольні захисні групи, стор. 95-117, Глава 4, Карбоксильні захисні групи, стор. 118 - 154, Глава 5, Карбонільні захисні групи, стор. 155-184. Щодо захисних груп для карбонової кислоти, фосфонової кислоти, фосфонату, сульфокислоти та інших захисних груп для кислот дивіться "Greene", як викладено нижче. Як приклад, а не обмеження, змінні, описані тут можуть бути рекурсивними замісниками у деяких варіантах. Типово, кожна з них може незалежно зустрічатися 20, 19, 18, 17, 16, 15, 14, 8 UA 110354 C2 5 10 15 20 25 30 35 40 45 50 55 60 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1 або 0 разів у даному варіанті. Більш типово, кожна з них може незалежно зустрічатися 12 разів або меншу кількість разів, в даному варіанті. Кожен раз, коли сполука, описана у цьому документі, заміщується більш ніж однією з тієї ж самої 1" 3" зазначеної групи, наприклад, "R або "R , то слід розуміти, що групи можуть бути однаковими або різними, тобто кожна група є незалежно вибраною. Хвилясті лінії вказують на ділянку приєднань ковалентного зв'язку до прилягаючих груп, фрагментів або атомів. В одному варіанті винаходу, сполука знаходиться в ізольованій і очищеній формі. Загалом, термін "ізольований і очищений" означає, що сполука по суті є вільною від біологічних матеріалів (наприклад, крові, тканини, клітин і т. д.). В одному конкретному варіанті втілення винаходу, цей термін означає, що сполука або кон'югат за винаходом принаймні приблизно на 50 мас% вільні від біологічних матеріалів; в іншому конкретному варіанті термін означає, що сполука або кон'югат за винаходом принаймні приблизно на 75 мас% вільні від біологічних матеріалів; в іншому конкретному варіанті термін означає, що сполука або кон'югат за винаходом принаймні приблизно на 90 мас% вільні від біологічних матеріалів; в іншому конкретному варіанті термін означає, що сполука або кон'югат за винаходом принаймні приблизно на 98 мас% вільні від біологічних матеріалів; та в іншому варіанті термін означає, що сполука або кон'югат за винаходом принаймні приблизно на 99 мас% вільні від біологічних матеріалів. В іншому конкретному варіанті винахід забезпечує сполуку або кон'югат за винаходом, які були отримані синтетичним шляхом (наприклад, ex vivo). Стереоізомери Сполуки за даним винаходом можуть мати хіральні центри, наприклад, хіральні атоми вуглецю або фосфору. Сполуки за винаходом, таким чином, включають рацемічні суміші всіх стереоізомерів, включаючи енантіомери, діастереомери, атропізомери. Крім того, сполуки за винаходом, включають збагачені або результуючі оптичні ізомери в будь-яких або всіх асиметричних, хіральних атомах. Іншими словами, хіральні центри, що є очевидними на зображеннях, передбачені як хіральні ізомери або рацемічні суміші. Як рацемічні, так і діастереомерні суміші, а також окремі оптичні ізомери, ізольовані або синтезовані, по суті вільні від їх енантіомерних або діастереомерних партнерів, знаходяться в межах обсягу винаходу. Рацемічні суміші розділяються на їх індивідуальні, по суті оптично чисті ізомери, за допомогою добре відомих методів, таких як, наприклад, поділ діастереомерних солей, утворених з оптично активними добавками, наприклад, кислотами або лугами, з подальшим зворотним перетворенням в оптично активні речовини. У більшості випадків, бажаний оптичний ізомер синтезується за допомогою стереоспецифічних реакцій, починаючи з відповідного стереоізомера цільового вихідного матеріалу. Сполуки за винаходом можуть також існувати у вигляді таутомерних ізомерів в деяких випадках. Попри те, що тільки один таутомер може бути описаний, всі такі форми розглядаються в межах обсягу даного винаходу. Наприклад, ене-амін таутомери можуть існувати для пурину, піримідину, імідазолу, гуанідину, амідину, а тетразольні системи і всі їх можливі таутомерні форми включені в обсяг даного винаходу. Солі та гідрати Приклади фізіологічно або фармацевтично прийнятних солей сполук за винаходом включають солі, отримані з відповідної основи, такої як лужний метал (наприклад, натрій), + лужноземельний метал (наприклад, магній), амоній і NX4 (де Х є С1-С4 алкілом). Фізіологічно прийнятні солі атому водню або аміногрупи включають солі органічних карбонових кислот, наприклад, оцтової, бензойної, молочної, фумарової, винної, малеїнової, малонової, яблучної, ізетіонової, лактобіонової та бурштинової кислот, органічні сульфокислоти, такі як метансульфонова, етансульфонова, бензолсульфонова і п-толуолсульфонова кислоти; і неорганічні кислоти, такі як хлористоводнева, сірчана, фосфорна і сульфамінова кислоти. Фізіологічно прийнятні солі сполуки гідроксильної групи включають аніон зазначеної сполуки в + + поєднанні з прийнятним катіоном, таким як Na і NX4 (де X незалежно вибраний з Н або С1-С4 алкільної групи). Для терапевтичного застосування солі активних інгредієнтів сполук даного винаходу будуть типово фізіологічно прийнятними, тобто вони будуть солями, утвореними з фізіологічно прийнятної кислоти або основи. Проте, солі кислот або основ, які не є фізіологічно прийнятними, можуть також знайти своє застосування, наприклад, при приготуванні або очищенні фізіологічно прийнятної сполуки. Усі солі, незалежно від того, чи були отримані від фізіологічно прийнятної кислоти або основи, знаходяться в межах об'єму даного винаходу. Солі металів зазвичай отримують шляхом реакції гідроксиду металу зі сполукою за винаходом. Приклади солей металів, які отримують таким чином, включають солі, що містять + + + Li , Na і K . Менш розчинна сіль металу може бути осаджена з розчину більш розчинної солі 9 UA 110354 C2 5 10 15 20 25 30 35 40 45 50 55 60 шляхом додавання відповідної сполуки металу. Крім того, солі можуть бути утворені шляхом додавання деяких органічних і неорганічних кислот, наприклад,HCl, HBr, H2SO4, H3PO4 або органічних сульфонових кислот, до основних центрів, зазвичай амінів або кислотних груп. Зрештою, слід розуміти, що композиції за даним винаходом включають сполуки за винаходом у їх неіонізованій, а також цвітеріонній формі, та їх комбінації зі стехіометричними кількостями води, як у гідратах. Також включеними в об'єм даного винаходу є солі вихідних сполук з однією або більшою кількістю амінокислот. Будь-яка з природних або неприродних амінокислот є придатною, зокрема, амінокислоти природного походження, такі як білкові компоненти, хоча амінокислота типово є такою, що несе бічний ланцюг з лужною або кислотною групою, наприклад, лізин, аргінін або глутамінова кислота, або нейтральну групу, таку як гліцин, серин, треонін, аланін, ізолейцин або лейцин. Способи інгібування HCV Інший аспект винаходу стосується способів інгібування активності HCV, що включає етап обробки зразка, який імовірно містить HCV, сполукою або композицією за винаходом. Сполуки за даним винаходом можуть діяти як інгібітори HCV, як проміжні сполуки для таких інгібіторів або мати інші корисні властивості, як описано нижче. Інгібітори зазвичай приєднуються до місць на поверхні або в порожнині печінки. Сполуки, що зв’язуються в печінці, можуть бути зв'язані з різним ступенем оборотності. Сполуки, які зв'язуються по суті необоротно, є ідеальними кандидатами для використання в даному способі винаходу. Мічені сполуки, які по суті зв’язуються необоротно, можуть бути використані як зонди для виявлення HCV. Відповідно, винахід стосується способів виявлення NS3 у зразку, який імовірно містить HCV, що включає етапи: обробки зразка, який імовірно містить HCV, композицією, що містить сполуку за винаходом, зв'язану з міткою, і спостереження за дією зразка на активність мітки. Відповідні мітки є добре відомими в галузі діагностики і включають стабільні вільні радикали, флуорофори, радіоізотопи, ферменти, хемілюмінесцентні групи і хромогени. Сполуки за винаходом позначені традиційним способом з використанням функціональних груп, таких як гідроксильні або аміногрупи. В одному варіанті винахід забезпечує сполуку за будь-якою з формул (I) і (А1) - (А4), яка містить або яка зв'язана, або пов'язана з однією або більшою кількістю виявлюваних міток. У контексті опису винаходу зразки, які імовірно містять HCV, включають природні або штучні матеріали, такі як живі організми, тканину або клітинні культури; біологічні зразки, такі як зразки біологічного матеріалу (кров, сироватка, сеча, спинномозкова рідина, сльози, мокрота, слина, зразки тканин, тощо); лабораторні зразки; зразки їжі, води або повітря; зразки біопродукту, такі як екстракти клітин, зокрема, рекомбінантні клітини, що синтезують бажаний глікопротеїн, тощо. Зазвичай зразок буде імовірно з підозрою на вміст HCV. Зразки можуть зберігатися в будь-якому середовищі, включаючи воду та суміші органічного розчинника/води. Зразки включають живі організми, такі як людина, і штучні матеріали, такі як клітинні культури. Етап обробки за винаходом включає додавання сполуки за винаходом до зразка або він включає додавання попередника композиції до зразка. Етап додавання включає будь-який спосіб введення, як описано вище. Якщо бажано, активність HCV після застосування сполуки може спостерігати будь-яким способом, включаючи прямі та опосередковані способи виявлення активності HCV. Розглядаються усі кількісні, якісні та напівкількісні способи визначення активності HCV. Типово один зі способів скринінгу, описаних вище, застосовується, проте будь-який інший спосіб, такий як спостереження за фізіологічними властивостями живого організму, є також застосовними. Багато організмів містять HCV. Сполуки за даним винаходом використовуються для лікування або профілактики станів, пов'язаних з активацією HCV у тварин або людини. Тим не менш, в процесі скринінгу сполук, здатних інгібувати активність HCV, слід мати на увазі, що результати ферментних аналізів не завжди можуть корелюватися з аналізами клітинної культури. Таким чином, аналіз на основі клітин має бути, як правило, первинним інструментом скринінгу. Фармацевтичні композиції Сполуки за винаходом утворюють форми зі звичайними носіями і наповнювачами, які будуть вибрані відповідно до звичайної практики. Таблетки будуть містити ексципієнти, речовини, що сприяють ковзанню, наповнювачі, зв’язувальні речовини тощо. Водні композиції готують у стерильній формі, а якщо вони призначені для доставки іншим ніж пероральним способом введення, зазвичай вони будуть ізотонічними. Усі композиції будуть необов’язково містити наповнювачі, такі як визначені у Довіднику фармацевтичних наповнювачів (Handbook of Pharmaceutical Excipients) (1986). Наповнювачі включають аскорбінову кислоту та інші 10 UA 110354 C2 5 10 15 20 25 30 35 40 45 50 55 60 антиоксиданти, хелатоутворюючі агенти, такі як етилендіамінтетраоцтова кислота (EDTA), вуглеводи, такі як декстрин, гідроксіалкілцелюлоза, гідрооксіалкілметилцелюлоза, стеаринова кислота тощо. Значення рН композицій знаходиться в діапазоні від приблизно 3 до приблизно 11, але зазвичай приблизно від 7 до 10. Типово, сполуку вводять в дозі від 0,01 мг до 2 грам. В одному варіанті доза буде складати від приблизно 10 мг до 450 мг. В іншому варіанті доза буде складати від приблизно 25 мг до приблизно 250 мг. В іншому варіанті доза становитиме близько 50 мг або 100 мг. В одному варіанті доза становитиме близько 100 мг. Передбачається, що сполука може бути введена один, два або три рази на добу. Попри можливе введення активних інгредієнтів окремо, краще представити їх у фармацевтичних композиціях. Композиції за винаходом, як у ветеринарії, так і для використання людиною, включають принаймні один активний інгредієнт, як визначено вище, разом з одним або декількома прийнятними носіями для нього і, необов'язково інші терапевтичні інгредієнти. Носій (-ї) має бути "прийнятним" в сенсі сумісності з іншими інгредієнтами композиції і має бути фізіологічно нешкідливим для його реципієнта. Композиції включають такі композиції, що є прийнятними для вищезазначених способів введення. Композиції можуть бути зручно представлені у формі одиничної дози і можуть бути приготовані будь-яким із способів, добре відомих в галузі фармації. Способи і склади зазвичай можна знайти в "Remington Pharmaceutical Sciences" (Mack Publishing Co., Easton, PA). Такі способи включають етап поєднання активного інгредієнта з носієм, який складається з одного або декількох допоміжних інгредієнтів. Загалом, композиції отримують шляхом рівномірного і ретельного змішування активного інгредієнта з рідкими носіями або тонко подрібненими твердими носіями або обома, а потім, якщо необхідно, шляхом формування продукту. Композиції даного винаходу, придатні для перорального введення, можуть бути представлені у вигляді дискретних одиниць, таких як капсули, облатки або таблетки, кожна з яких містить певну визначену кількість активного інгредієнта у вигляді порошку або гранул, у вигляді розчину або суспензії у водній або неводній рідині, або у вигляді рідкої емульсії "олія в воді" або рідкої емульсії "вода в олії". Активний інгредієнт може бути також введений у вигляді болюсу, лікарської кашки або пасти. Таблетка виготовляється шляхом пресування або формуванням, необов'язково з одним або більшою кількістю допоміжних інгредієнтів. Пресовані таблетки можуть бути отримані шляхом пресування у відповідній машині активного інгредієнта у вільно-плинній формі, такій як порошок або гранули, необов'язково змішаного зі зв’язувальною речовиною, змащувальною речовиною, інертним розчинником, консервантом, поверхнево-активним або диспергуючим агентом. Формовані таблетки можуть бути виготовлені шляхом формування у відповідній машині суміші порошкоподібного активного інгредієнта, зволоженого інертним рідким розріджувачем. Таблетки необов'язково можуть мати покриття або нанесені насічки і, необов’язково сформовані таким чином, щоб забезпечити повільне або контрольоване вивільнення активного інгредієнта з неї. Для введення в око або інші зовнішні тканини, наприклад, рот і шкіру, композиції переважно наносять у вигляді місцевої мазі або крему, які містять активний інгредієнт (-и) в кількості, наприклад, від 0,075 до 20% ваг./ваг. (включаючи активний інгредієнт (-и) в діапазоні від 0,1% до 20% з кроком в 0,1 % ваг./ваг., наприклад, 0,6% ваг./ваг., 0,7% ваг./ваг. і т. д.), переважно від 0,2 до 15% ваг./ваг., і більш переважно від 0,5 до 10% ваг./ваг. При приготуванні у вигляді мазі активні інгредієнти можуть бути використані або з парафіновою, або з водорозчинною мазевою основою. Альтернативно, активні інгредієнти можуть бути приготовані у вигляді крему з кремовою основою "олія в воді". Якщо бажано, водна фаза кремової основи може включати, наприклад, принаймні, 30% ваг./ваг. багатоатомного спирту, тобто спирту, що має дві або більше гідроксильних груп, таких як пропіленгліколь, бутан 1,3-діол, манітол, сорбіт, гліцерин і поліетиленгліколь (включаючи PEG 400), а також їх суміші. Склади для місцевого застосування можуть при бажанні включати сполуку, яка збільшує поглинання або проникнення активного інгредієнта через шкіру або інші уражені ділянки. Приклади таких підсилювачів проникнення через шкіру включають диметилсульфоксид та споріднені аналоги. Олійна фаза емульсій за даним винаходом може бути сформована з відомих інгредієнтів відомим способом. Хоча фаза може містити тільки емульгатор (інакше відомий як емульгент), бажано, щоб вона містила суміш принаймні одного емульгатора з жиром або олією, або як і з жиром, так і олією. Переважно, гідрофільний емульгатор включають разом з ліпофільним емульгатором, який діє в якості стабілізатора. Також переважно слід включати як олію, так і жир. Разом, емульгатор (-и) із стабілізатором (-ами) або без нього утворює так званий емульгуючий віск, а віск разом з олією і жиром утворюють так звану емульгуючу мазеву основу, яка утворює олійну дисперсну фазу кремових форм. 11 UA 110354 C2 5 10 15 20 25 30 35 40 45 50 55 60 Емульгатори та стабілізатори емульсії, придатні для використання у композиції за ® ® винаходом, включають Tween 60, Span 80, цетостеариловий спирт, бензиловий спирт, міристиловий спирт, гліцерилмоностеарат і лаурилсульфат натрію. Вибір відповідних масел або жирів для композиції ґрунтується на досягненні бажаних косметичних властивостей. Крем повинен бути переважно нежирним, не залишати плям і змиватися з прийнятною консистенцією, щоб уникнути витоку з тюбиків та інших контейнерів. Моно- або двоосновні складні алкілові ефіри з прямим або розгалуженим ланцюгом, такі як діізоадипат, ізоцетіловий стеарат, пропіленгліколь діефір жирних кислот кокосової олії, ізопропілміристат, децілолеат, ізопропілпальмітат, бутилстеарат, 2-етілгексілпальмітат або суміш складних ефірів з розгалуженим ланцюгом, відомих як Crodamol CAP, можуть бути використані, при чому останні три є складними ефірами, яким надається перевага. Вони можуть бути використані окремо або в поєднанні, залежно від необхідних властивостей. Альтернативно, використовуються ліпіди з високою температурою плавлення, такі як білий м'який парафін і/або рідкий парафін, або інші мінеральні оливи. Фармацевтичні композиції за даним винаходом включають одну або більше сполук за винаходом разом з одним або декількома фармацевтично прийнятними носіями або наповнювачами і необов'язково іншими терапевтичними агентами. Фармацевтичні композиції, що містять активний інгредієнт, можуть знаходитися в будь-якій формі, придатній для передбачуваного способу введення. При використанні для перорального застосування можуть бути приготовлені, наприклад, таблетки, пастилки, льодяники, водні або олійні суспензії, диспергуючі порошки або гранули, емульсії, тверді або м'які капсули, сиропи або еліксири. Композиції, призначені для перорального застосування, можуть бути отримані відповідно до будь-якого способу, відомого в даній галузі для виробництва фармацевтичних композицій, і такі композиції можуть містити один або більше агентів, включаючи підсолоджувачі, ароматизатори, барвники і консерванти, з тим щоб забезпечити препарат з приємним смаком. Таблетки, що містять активний інгредієнт в суміші з нетоксичним фармацевтично прийнятним наповнювачем, які придатні для виготовлення таблеток, є прийнятними. Ці ексципієнти можуть бути, наприклад, інертними розріджувачами, такими як карбонат кальцію або карбонат натрію, лактоза, моногідрат лактози, кроскармелоза натрію, повідон, фосфат кальцію або фосфат натрію; гранулюючими і дезінтегруючими агентами, такими як кукурудзяний крохмаль або альгінова кислота; зв’язувальними агентами, такими як целюлоза, мікрокристалічна целюлоза, крохмаль, желатин або аравійська камедь, і змащувальними агентами, такими як стеарат магнію, стеаринова кислота або тальк. Таблетки можуть бути непокритими або можуть бути покриті відомими способами, включаючи мікрокапсулювання з метою затримати дезінтеграцію і адсорбцію в шлунково-кишковому тракті, і тим самим забезпечити пролонговану дію протягом більш тривалого періоду. Наприклад, може бути використаний матеріал тимчасової затримки, такий як гліцерилмоностеарат або гліцерилдістеарат, один або разом з воском. Композиції для перорального застосування можуть бути також представлені у вигляді твердих желатинових капсул, де активний інгредієнт змішаний з інертним твердим розріджувачем, наприклад, фосфатом кальцію або каоліном, або у вигляді м'яких желатинових капсул, де активний інгредієнт змішаний з водою або олійним середовищем, таким як арахісова олія, рідкий парафін або оливкова олія. Водні суспензії винаходу містять активні матеріали в суміші з наповнювачами, придатними для отримання водних суспензій. Такі наповнювачі включають суспендуючий агент, такий як натрій карбоксиметилцелюлоза, метилцелюлоза, гідроксипропілметилцелюлоза, альгінат натрію, полівінілпіролідон, трагакантова камедь та аравійська камедь, і диспергуючі або зволожуючі агенти, такі як природні фосфатиди (наприклад, лецитин), продукт конденсації алкіленоксиду з жирною кислотою (наприклад, поліоксіетіленстеарат), продукт конденсації етиленоксиду з довголанцюжковим аліфатичним спиртом (наприклад, гептадекаетиленоксицетанол), продукт конденсації етиленоксиду з неповним ефіром, отриманим з жирної кислоти, і гексит ангідрид (наприклад, поліоксіетиленсорбітанмоноолеат). Водна суспензія може також містити один або більше консервантів, таких як етил або н-пропілп-гідроксибензоат, один або більше барвників, один або кілька ароматизуючих агентів, і один або більше підсолоджувачів, таких як сахароза або сахарин. Олійні суспензії можуть бути приготовані шляхом суспендування активного інгредієнта в рослинній олії, наприклад, арахісовій олії, оливковій олії, кунжутній олії або кокосовій олії, або в мінеральному маслі, такому як рідкий парафін. Суспензії для перорального введення можуть містити загущувач, наприклад, бджолиний віск, твердий парафін або цетиловий спирт. Підсолоджувачі, такі як зазначені вище, і ароматизатори можуть бути додані, щоб забезпечити приємний смак перорального препарату. Ці композиції можуть бути збережені шляхом 12 UA 110354 C2 5 10 15 20 25 30 35 40 45 50 55 60 додавання антиоксиданту, такого як аскорбінова кислота. Дисперсні порошки та гранули за винаходом, придатні для отримання водної суспензії шляхом додавання води, забезпечують активний інгредієнт в суміші з диспергуючим або зволожувальним агентом, суспендуючим агентом і одним або декількома консервантами. Придатні диспергуючі або зволожуючі агенти і суспендуючі агенти представлені тими, що описані вище. Додаткові ексципієнти, наприклад, підсолоджувачі, смакові добавки та барвники, також можуть бути присутніми. Фармацевтичні композиції за винаходом можуть бути також у формі емульсій "олія в воді". Олійна фаза може бути рослинною олією, наприклад, оливковою олією або арахісовою олією, мінеральним маслом, наприклад, рідким парафіном, або їх сумішшю. Відповідні емульгатори включають природні камеді, такі як аравійська камедь і трагакантова камедь, природні фосфатиди, наприклад, соєвий лецитин, складні ефіри або неповні ефіри, отримані з жирних кислот і гексит ангідриди, наприклад, моноолеат сорбітану, і продукти конденсації цих неповних ефірів з етиленоксидом, наприклад, моноолеат поліоксіетиленсорбітану. Емульсія може також містити підсолоджувачі та ароматизатори. Сиропи та еліксири можуть бути приготовані з підсолоджувачами, наприклад, гліцерином, сорбітом або сахарозою. Такі композиції можуть також містити засіб, що зменшує подразнення, консервант, ароматизатор або барвник. Фармацевтичні композиції за винаходом можуть бути у формі стерильного ін'єкційного препарату, наприклад, стерильні ін'єкційні водні або маслянисті суспензії. Ці суспензії можуть бути отримані відповідно до відомих способів з використанням відповідних диспергуючих або зволожуючих агентів і суспендуючих агентів, які були згадані вище. Стерильний ін'єкційний препарат може також бути стерильним ін'єкційним розчином або суспензією в нетоксичному парентерально прийнятному розріджувачі або розчиннику, наприклад, розчин у 1,3-бутандіолі або приготований у вигляді ліофілізованого порошку. Серед прийнятних носіїв і розчинників, які можна використовувати, слід вказати воду, розчин Рінгера та ізотонічний розчин хлориду натрію. Крім того, стерильні нелеткі олії можуть традиційно використовуватися у якості розчинника або суспендуючого середовища. Для цієї цілі може використовуватися будь-яка м'яка нелетка олія, включаючи синтетичні моно- або дигліцериди. Крім того, жирні кислоти, такі як олеїнова кислота, також можуть використовуватися для приготування препаратів для ін'єкцій. Кількість активного інгредієнта, який може комбінуватися з матеріалом носія для отримання одиничної дозованої форми, буде змінюватись залежно від суб'єкта, який піддається лікуванню, і конкретного способу введення. Наприклад, композиція з повільним вивільненням, призначена для перорального введення людині, може містити приблизно від 1 до 1000 мг активної речовини, змішаної з відповідною і прийнятною кількістю матеріалу носія, який може варіюватися приблизно від 5 до приблизно 95% від загальної композиції (вага: вага). Фармацевтична композиція може бути отримана для забезпечення легко вимірної кількості для введення. Наприклад, водний розчин, призначений для внутрішньовенної інфузії може містити від близько 3 до 500 мкг активного інгредієнта на мілілітр розчину для здійснення інфузії відповідного обсягу зі швидкістю приблизно 30 мл/годину. Композиції, придатні для введення в око, включають очні краплі, в яких активний інгредієнт розчинений або суспендований у відповідному носії, зокрема, у водному розчиннику для активного інгредієнта. Активний компонент переважно присутній в таких композиціях в концентрації від 0,5 до 20%, більш переважно від 0,5 до 10%, зокрема близько 1,5% ваг./ваг. Композиції, придатні для місцевого застосування у порожнині рота, включають льодяники, що містять активний інгредієнт на ароматизованій основі, зазвичай цукрозу та аравійську камедь або трагакант, пастилки, що містять активний інгредієнт в інертній основі, такий як желатин і гліцерин, або цукрозу і аравійську камедь; і полоскання, що містить активний інгредієнт у прийнятному рідкому носії. Композиції для ректального введення можуть бути представлені у вигляді супозиторію з відповідною основою, яка містить, наприклад, какао масло або саліцилат. Композиції, придатні для внутрішньолегеневого або назального введення мають розмір частинок, наприклад, в діапазоні від 0,1 до 500 мкм (включаючи розміри частинок в діапазоні між 0,1 і 500 мкм з кроком мікронів, наприклад, 0,5, 1, 30 мкм, 35 мкм, і т. д.), які вводяться шляхом швидкої інгаляції через носовий хід або шляхом інгаляції через рот так, щоб досягати альвеолярних мішків. Відповідні композиції включають водні або олійні розчини активного інгредієнта. Композиції, придатні для введення аерозолю або сухого порошку, можуть бути отримані у відповідності зі звичайними способами і можуть бути доставлені з іншими терапевтичними агентами, такими як сполуки, які до цих пір використовуються для лікування або профілактики станів, пов'язаних з активністю HCV. Композиції, придатні для вагінального введення, можуть бути представлені у вигляді 13 UA 110354 C2 5 10 15 20 25 30 35 40 45 50 55 60 вагінальних супозиторіїв, тампонів, кремів, гелів, паст, пін або спреїв, які містять на додаток до активного інгредієнта такі носії, які є відомими в даній галузі техніки як доречні. Композиції, придатні для парентерального введення включають водні та неводні стерильні ін'єкційні розчини, які можуть містити антиоксиданти, буфери, бактеріостати і розчинені речовини, які надають композиції ізотонічності з кров'ю передбачуваного реципієнта, а також водні та неводні стерильні суспензії, які можуть включати суспендуючі агенти та загусники. Композиції представлені в контейнерах з одиничною дозою або в багатодозових контейнерах, наприклад, ампулах та флаконах, і можуть зберігатися у висушеному заморожуванням (ліофілізованому) стані, що вимагає тільки додавання стерильного рідкого носія, наприклад, води для ін'єкцій безпосередньо перед використанням. Розчини та суспензії для ін'єкцій, приготовані для негайного прийому, одержують із стерильних порошків, гранул і таблеток раніше описаного типу. Переважні рецептури з одиничним дозуванням є ті, які містять денну дозу або одиничну денну субдозу, як описано вище, або відповідну її частину, активного інгредієнта. Слід розуміти, що на додаток до інгредієнтів, які конкретно згадувалися вище, композиції за винаходом можуть включати інші агенти, традиційні в даній області, з урахуванням типу розглянутої композиції, наприклад, придатні для перорального введення можуть включати смакові агенти. Винахід також забезпечує ветеринарні композиції, що містять принаймні один активний інгредієнт, як визначено вище, разом з його ветеринарним носієм. Ветеринарними носіями є матеріали, використовувані для цілей введення композиції, які можуть бути твердими, рідкими або газоподібними речовинами, які інакше є інертними або прийнятними у ветеринарії і сумісні з активним інгредієнтом. Ці ветеринарні композиції можуть вводитися перорально, парентерально або будь-яким іншим бажаним шляхом. Сполуки за даним винаходом можуть бути також приготовлені для забезпечення контрольованого вивільнення активного інгредієнта, щоб дозволити менш часте дозування або поліпшити фармакокінетичний профіль або профіль токсичності активного інгредієнта. Відповідно, винахід також забезпечує композиції, що містять одну або кілька сполук за винаходом, приготовлені для уповільненого або контрольованого вивільнення. Ефективна доза активного інгредієнта залежить принаймні від природи стану, що підлягає лікуванню, токсичності, чи сполука використовується профілактично (менші дози), способу доставки, а також фармацевтичної композиції, і буде визначена лікуючим лікарем з використанням традиційних досліджень з ескалацією дози. Шляхи введення Одна або більше сполук за винаходом (названих тут активними інгредієнтами) вводяться будь-яким шляхом, відповідним стану, що підлягає лікуванню. Відповідні шляхи включають пероральний, ректальний, назальний, місцевий (включаючи букальний і сублінгвальний), вагінальний або парентеральний (включаючи підшкірний, внутрішньом'язовий, внутрішньовенний, внутрішньошкірний, інтратекальний і епідуральний) тощо. Слід розуміти, що шлях, якому надається перевага, може змінюватися в залежності, наприклад, від стану реципієнта. Перевага сполук за даним винаходом полягає в тому, що вони є біодоступними при пероральному введенні і можуть дозуватися перорально. Комбінована терапія HCV В іншому варіанті, приклади, що не мають обмежувального характеру, придатних комбінацій включають комбінації однієї або більшої кількості сполук за формулами (I) і (А1-А4) з одним або декількома інтерферонами, рибавірином або його аналогами, інгібіторами протеази NS3 HCV, інгібіторами альфа-глюкозидази 1, гепатопротекторами, нуклеозидними або нуклеотидними інгібіторами полімерази NS5B HCV, ненуклеозидними інгібіторами полімерази NS5B HCV, інгібіторами NS5A HCV, агоністами TLR-7, інгібіторами циклофіліну, інгібіторами ділянки внутрішньої посадки рибосоми (IRES) HCV, фармакокінетичними підсилювачами та іншими препаратами або терапевтичними агентами для лікування HCV. Більш конкретно, одна або більше сполук, описаних тут, може комбінуватися з однією або більшою кількістю сполук, вибраних з групи, що складається з: 1) пегільованого rIFN альфа-2b (PEG-Інтрон), пегільованого rIFN-альфа-2а (Пегасис), rIFN альфа-2b (Інтрон А), rIFN-альфа-2а (Роферон-А), інтерферону альфа (MOR-22, OPC-18, Альфаферон, Альфанатів, Мультиферон, субалін), інтерферону альфакон-1 (Інферген), інтерферону альфа-н1 (Велферон), інтерферону альфа-н3 (Алферон), бета-інтерферону (Авонекс, DL-8234), омега-інтерферону (омега Duros, Biomed 510), альбінтерферону альфа-2b (Альбуферон), IFN альфа-2b XL, BLX-883 (Локтерон), DA-3021, глікозильованого інтерферону альфа-2b (AVI-005), PEG-Інферген, ПЕГільованого інтерферону лямбда-1 (ПЕГільований IL-29), 14 UA 110354 C2 5 10 15 20 25 30 35 40 45 50 55 60 та белерофону; 2) рибавірину та його аналогів, наприклад, рибавірин (Ребетол, Копегус) і тарибавірин (Вірамідин); 3) інгібіторів протеази NS3 HCV, наприклад, боцепревір (SCH-503034, SCH-7), телепревір (VX-950), TMC435350, BI-1335, BI-1230, МК-7009, VBY-376, VX-500, GS-9256, GS-9451, BMS605339, PHX-1766, AS-101, YH-5258, YH5530, YH5531, ABT-450, ACH-1625, ITMN-191, MK5172, MK6325, і MK2748; 4) інгібіторів альфа-глюкозидази 1, наприклад, селгозивір (MX-3253), Міглітол і UT-231B; 5) гепатопротекторів, наприклад, емеріказан (IDN-6556), ME-3738, GS-9450 (LB-84451), силибілін і MitoQ; 6) нуклеозидних або нуклеотидних інгібіторів полімерази NS5B HCV, наприклад, R1626, R7128 (R4048), IDX184, IDX-102, ВСX-4678, валопіцитабін (NM-283), МК-0608, софосбувір (GS7977 (раніше PSI- 7977)), та INX-189 (зараз BMS986094); 7) ненуклеозидних інгібіторів полімерази NS5B HCV, наприклад, PF-868554, VCH-759, VCH916, JTK-652, MK-3281, GS-9190, VBY-708, VCH-222, A848837, ANA-598, GL60667, GL59728, A63890, A-48773, A-48547, BC-2329, VCH-796 (несбувір), GSK625433, BILN-1941, XTL-2125, ABT072, ABT-333, GS-9669, PSI-7792, і GS-9190; 8) інгібіторів NS5A HCV, наприклад, AZD-2836 (A-831), BMS-790052, ACH-3102, ACH-2928, MK8325, MK4882, MK8742, PSI-461, IDX719, і А-689; 9) агоністів TLR-7, наприклад, іміквімод, 852A, GS-9524, ANA-773, ANA-975, AZD-8848 (DSP3025) і SM-360320; 10) інгібіторів циклофіліну, наприклад, DEBIO-025, SCY-635, і NIM811; 11) інгібіторів IRES HCV, наприклад, MCI-067; 12) фармакокінетичних підсилювачів, наприклад, BAS-100, SPI-452, PF-4194477, TMC41629, GS-9350, GS-9585 та рокситроміцин; і 13) інших препаратів для лікування гепатиту С (HCV), наприклад, тимозин альфа-1 (Задаксин), нітазоксанід (Alinea, NTZ), BIVN-401 (віростат), PYN-17 (алтирекс), KPE02003002, актилон (CPG-10101), GS-9525, KRN-7000, сивацир, GI-5005, XTL-6865, BIT225, PTX-111, ITX2865, TT-033i, 971 ANA, NOV-205, тарвацин, EHC-18, VGX-410C, EMZ-702, AVI 4065, BMS650032, BMS-791325, Бавітуксимаб, MDX-1106 (ONO-4538), Оглуфанід і VX-497 (меримеподіб). Більш конкретно, одна або більше сполук, описаних тут, можуть комбінуватися з однією або більшою кількістю сполук, вибраних з групи, що складається з ненуклеозидних інгібіторів полімерази NS5B HCV (ABT-072 і ABT-333), інгібіторів NS5A HCV (ACH-3102 і ACH-2928) та інгібіторів протеази NS3 HCV (ABT-450 і ACH-1625). У ще одному варіанті дана заявка описує фармацевтичні композиції, що містять сполуку, як описано тут, або її фармацевтично прийнятну сіль, сольват, і/або її складний ефір у комбінації принаймні з одним додатковим терапевтичним агентом, і фармацевтично прийнятний носій або наповнювач. Відповідно до одного варіанту, терапевтичним агентом, використовуваним в комбінації зі сполукою, як описано тут, може бути будь-який агент, що має терапевтичний ефект при використанні в комбінації зі сполукою, як описано тут. Наприклад, терапевтичним агентом, використовуваним в комбінації зі сполукою, як описано тут, можуть бути інтерферони, аналоги рибавірину, інгібітори протеази NS3, інгібітори полімерази NS5B, інгібітори альфа-глюкозидази 1, гепатопротектори, ненуклеозидні інгібітори HCV, а також інші лікарські засоби для лікування HCV. В іншому варіанті ця заявка забезпечує фармацевтичні композиції, які включають сполуку за формулою (I), або її фармацевтично прийнятну сіль, сольват, і/або складний ефір у комбінації принаймні з одним додатковим терапевтичним агентом, вибраним з групи, що складається з пегільованого rIFN альфа-2b, пегільованого rIFN-альфа-2а, rIFN альфа-2b, IFN альфа-2b XL, rIFN-альфа-2а, IFN-альфа консенсусу, Інфергену, ребіфу, локтерону, AVI-005, PEG-Інфергену, пегільованого IFN-бета, перорального альфа-інтерферону, ферону, реaферону, Інтермакс альфа, r-IFN-бета, інфергену + актимуну, IFN-омега з DUROS, альбуферону, ребетолу, копегусу, левовірину, VX-497, вірамідину (тарибавірину), A-831, A-689, NM-283, валопіцитабіну, R1626, PSI-6130 (R1656), HCV-796, BILB 1941, МК-0608, NM-107, R7128, VCH-759, PF-868554, GSK625433, XTL-2125, SCH-503034 (SCH-7), VX-950 (Телепревіру), ITMN-191, і BILN-2065, MX3253 (селгозивіру), UT-231B, IDN-6556, ME 3738, MitoQ і LB-84451, похідних бензімідазолу, похідних бензо-1,2,4-тіадіазину та похідних фенілаланіну, задаксину, нітазоксаніду (Alinea), BIVN-401 (віростату), DEBIO-025, VGX-410С EMZ-702, AVI 4065, Бавітуксимабу, оглуфаніду, PYN-17, KPE02003002, актилону (CPG-10101), KRN-7000, сівациру, GI-5005, ANA-975 (ізаторибіну), XTL-6865, ANA 971, NOV-205, тарвацину, EHC-18 і NIM811, та фармацевтично 15 UA 110354 C2 5 10 15 прийнятний носій або наповнювач. У ще одному варіанті ця заявка забезпечує комбінацію фармацевтичного агента, що включає: а) першу фармацевтичну композицію, яка містить сполуку за формулою (I), або її фармацевтично прийнятну сіль, сольват або складний ефір; і б) другу фармацевтичну композицію, яка містить принаймні один додатковий терапевтичний агент, вибраний з групи, що складається зі сполук, які інгібують протеазу ВІЛ, ненуклеозидних інгібіторів зворотної транскриптази ВІЛ, нуклеозидних інгібіторів зворотної транскриптази ВІЛ, нуклеотидних інгібіторів зворотної транскриптази ВІЛ, інгібіторів інтегрази ВІЛ, інгібіторів gp41, інгібіторів CXCR4, інгібіторів gp120, інгібіторів CCR5, інтерферонів, аналогів рибавірину, інгібіторів протеази NS3, інгібіторів альфа-глюкозидази 1, гепатопротекторів, ненуклеозидних інгібіторів HCV, а також інших лікарських засобів для лікування HCV, та їх комбінацій. В іншому варіанті забезпечується фармацевтична композиція, яка містить сполуку за формулою (I), як описано тут, та нуклеозидні або нуклеотидні інгібітори полімерази NS5B HCV і, необов’язково, інтерферон або рибавірин. В одному варіанті сполукою є метил{(2S)-1-[(2S,5S)2-(9-{2-[(2S,4S)-1-{(2R)-2-[(метоксикарбоніл)аміно]-2-фенілацетил}-4-(метоксиметил) піролідин2-іл]-1H-імідазол-5-іл}-1,11-дигідроізохромено[4',3':6,7]нафто[1,2-d] імідазол-2-іл)-5метилпіролідин-1-іл]-3-метил-1-оксобутан-2-іл}карбамат, що має формулу: , 20 25 30 35 40 45 50 а інгібітором є софосбувір. Комбінації сполук за формулою I та додаткові активні терапевтичні агенти можуть бути вибрані для лікування пацієнтів, інфікованих вірусом гепатиту С та інших захворювань, таких як ВІЛ-інфекцій. Відповідно, сполуки за формулою I можуть комбінуватися з однією або більшою кількістю сполук, що використовуються у лікуванні ВІЛ, наприклад, сполуки, що інгібують протеазу ВІЛ, ненуклеозидні інгібітори зворотної транскриптази ВІЛ, нуклеозидні інгібітори зворотної транскриптази ВІЛ, нуклеотидні інгібітори зворотної транскриптази ВІЛ, інгібітори інтегрази ВІЛ, інгібітори gp41, інгібітори CXCR4, інгібітори gp120, інгібітори CCR5, інтерферони, аналоги рибавірину, інгібітори протеази NS3, інгібітори полімерази NS5B, інгібітори альфаглюкозидази 1, гепатопротектори, ненуклеозидні інгібітори HCV, а також інші лікарські засоби для лікування HCV. Більш конкретно, одна або більше сполук за формулами (I) або (А1) - (А4) можуть комбінуватися з однією або більшою кількістю сполук, вибраних з групи, що складається з 1) інгібіторів протеази ВІЛ, наприклад, ампренавір, атазанавір, фосампренавір, індинавір, лопінавір, ритонавір, лопінавір + ритонавір, нелфінавір, саквінавір типранавір, бреканавір, дарунавір, TMC-126, TMC-114, мозенавір (DMP-450), JE-2147 (AG1776), AG1859, DG35, L756423, RO0334649, KNI-272, DPC-681, DPC-684, і GW640385X, DG17, PPL-100, 2) ненуклеозидного інгібітору зворотної транскриптази ВІЛ, наприклад, каправірин, емівірин, делавіридин, ефавіренц, невірапін, (+) каланолід А, етравірин, GW5634, DPC-083, DPC-961, DPC-963, MIV-150 і TMC-120, TMC-278 (рилпівірин), ефавіренц, BILR 355 BS, VRX 840773, UK453,061, RDEA806, 3) нуклеозидного інгібітору зворотної транскриптази ВІЛ, наприклад, зидовудин, емтрицитабін, диданозин, ставудин, залцитабін, ламівудин, абакавір, амдоксовір, елвуцитабін, аловудін, MIV-210, рацивір (-FTC), D-d4FC, емтрицитабін фосфазід, фоцивудін тидохіл, фозалвудин тидоксил, априцитибін (AVX754), амдоксовір, KP-1461, абакавір + ламівудин, абакавір + ламівудин + зидовудин, зидовудин + ламівудин, 4) нуклеотидного інгібітору зворотної транскриптази ВІЛ, наприклад, тенофовір, тенофовір дизопроксил фумарат + емтрицитабін, тенофовір дизопроксил фумарат + емтрицитабін + ефавіренц, і адефовір, 5) інгібітору інтеграли ВІЛ, наприклад., куркумін, похідні куркуміну, хіорова кислота, похідні хіорової кислоти, 3,5-дикафеойлхінна кислота, похідні 3,5-дикафеойлхінної кислоти, ауринтрикарбонова кислота, похідні ауринтрикарбонової кислоти, фенетил ефір кавової кислоти, похідні фенетил 16 UA 110354 C2 5 10 15 20 25 30 35 40 45 50 55 60 ефіру кавової кислоти, тірфостин, похідні тірфостину, кверцетин, похідні кверцетину, S-1360, цинтевір (AR-177), L-870812 і L-870810, МК-0518 (ралтегравір), BMS-707035, МК-2048, BA-011, BMS-538158, GSK364735C, 6) інгібітору gp41, наприклад, енфувіртид, сульфувіртид, FB006M, TRI-1144, SPC3, DES6, Locus gp41, CovX і REP 9, 7) інгібітору CXCR4, наприклад, AMD -070, 8) інгібітору входу, наприклад, SP01A, TNX-355, 9) інгібітору gp120, наприклад, BMS-488043 і BlockAide/CR, 10) інгібітору G6PD і NADH-оксидази, наприклад, імунітин, 10) інгібітору CCR5, наприклад, аплавірок, вікривірок, INCB9471, PRO-140, INCB15050, PF-232798, CCR5mAb004 і маравірок, 11) інтерферону, наприклад, пегільований rIFN альфа-2b, пегільований rIFN-альфа2а, rIFN альфа-2b, IFN альфа-2b XL, rIFN-альфа-2а, консенсус IFN альфа, інферген, ребіф, локтерон, AVI-005, PEG-Інферген, пегільованих IFN-бета, пероральний інтерферон альфа, ферон, реаферон, інтермакс альфа, r-IFN-бета, інферген + актимун, IFN-омега з DUROS, і альбуферон, 12) аналогів рибавірину, наприклад, ребетол, копегус, левовірин, VX-497, і вірамідин (тарибавірин) 13) інгібіторів NS5a, наприклад, A-831, A-689 і BMS-790052, 14) інгібіторів полімерази NS5b, наприклад, NM-283, Валопіцитабін, R1626, PSI-6130 (R1656), HCV796, BILB 1941, МК-0608, NM-107, R7128, VCH-759, PF-868554, GSK625433 і XTL-2125, 15) інгібіторів протеази NS3, наприклад, SCH-503034 (SCH-7), VX-950 (Телепревір), ITMN-191, і BILN-2065, 16) інгібіторів альфа-глюкозидази 1, наприклад, MX-3253 (селгозівір) і UT-231B, 17) гепатопротекторів, наприклад, IDN-6556, ME 3738, MitoQ і LB-84451, 18) ненуклеозидних інгібіторів HCV, наприклад, похідні бензімідазолу, бензо-1,2,4-тіадіазін і похідні фенілаланіну, 19) інших препаратів для лікування гепатиту С, наприклад, задаксин, нітазоксанід (Alinea), BIVN401 (віростат), DEBIO-025, VGX-410C, ЕМЗ-702, AVI 4065, Бавітуксимаб, оглуфанід, PYN-17, KPE02003002, актилон (CPG-10101), KRN-7000, сивацир, GI-5005, ANA-975 (ізаторибін), XTL6865, ANA 971, NOV-205, тарвацин, EHC-18, і NIM811, 19) фармакокінетичних підсилювачів, наприклад, BAS-100 і SPI452, 20) інгібіторів Н рибонуклеази, наприклад, ODN-93 і ODN-112, 21) інших анти-ВІЛ агентів, наприклад, VGV-1, PA-457 (бевіримат), ампліген, HRG214, цитолін, полімун, VGX-410, KD247, АМЗ 0026, CYT 99007, A-221 HIV, BAY 50-4798, MDX010 (іплімумаб), PBS119, ALG889 і PA-1050040. Передбачається, що другий терапевтичний агент буде вводитися у такий спосіб, що є відомим в даній галузі, а доза може бути вибрана фахівцем в даній галузі техніки. Наприклад, другий агент може вводитися в дозі від приблизно 0,01 мг до приблизно 2 г на добу. Метаболіти сполук Також підпадають під обсяг даного винаходу метаболічні продукти in vivo сполук, описаних в даному документі. Такі продукти можуть утворюватися, наприклад, внаслідок окиснення, відновлення, гідролізу, амідування, етерифікації, тощо сполуки, що вводиться, насамперед через ферментативні процеси. Відповідно, винахід включає сполуки, отримані за способом, який включає контактування сполуки за винаходом з ссавцем протягом часу, достатнього для отримання його метаболічного продукту. Такі продукти типово визначаються шляхом 14 3) приготування міченої радіоактивним ізотопом (наприклад, C або H сполуки за винаходом, її введення парентерально у виявлюваній дозі (наприклад, більше ніж приблизно 0,5 мг/кг) тваринам, таким як щур, миша, морська свинка, мавпа, або людині, забезпечуючи достатній час для того, щоб відбувся обмін речовин (зазвичай від близько 30 секунд до 30 годин), і виділення його продуктів переробки з сечі, крові або інших біологічних зразків. Ці продукти легко виділити, оскільки вони помічені (інші ізольовані за допомогою антитіл, здатних зв'язувати епітопи, що вижили в метаболіті). Структури метаболіту визначаються традиційним способом, наприклад, шляхом аналізу MS (мас-спектрометрії) або NMR (ядерної магнітно-резонансної спектрометрії). Загалом, аналіз метаболітів здійснюється таким же чином, як і традиційні дослідження метаболізму ліків, добре відомі фахівцям в даній галузі. Продукти переробки, доти, доки вони інакше не знайдені in vivo, є корисними в діагностичних аналізах для терапевтичного дозування сполук за винаходом, навіть якщо вони не володіють HCV-інгібуючою активністю самі по собі. Способи визначення стабільності сполук у сурогатних шлунково-кишкових секреціях є відомими. Ілюстративні способи отримання сполук Даний винахід також стосується способів отримання композицій за винаходом. Ці композиції отримують за допомогою будь-якого із застосовних способів органічного синтезу. Багато таких способів добре відомі в даній галузі. Проте багато з відомих способів детально опрацьовані у "Збірці органічних синтетичних методів" (Compendium of Organic Synthetic Methods) (John Wiley & Sons, New York), Том 1, Ian T. Harrison and Shuyen Harrison, 1971; Том 2, Ian T. Harrison and Shuyen Harrison, 1974; Том 3, Louis S. Hegedus and Leroy Wade, 1977; Том 4, Leroy G. Wade, Jr., 1980; Том 5, Leroy G. Wade, Jr., 1984; і Том 6, Michael B. Smith; а також у Марч, Дж., "Поглиблена органічна хімія", третє видання (March, J., Advanced Organic Chemistry, Third 17 UA 110354 C2 5 10 15 20 25 30 35 40 45 50 55 60 Edition, John Wiley & Sons, New York, 1985), "Комплексний органічний синтез. Вибірковість, стратегія і ефективність у сучасній органічній хімії" У 9 томах, Баррі M. Трост, головний редактор (Comprehensive Organic Synthesis. Selectivity, Strategy & Efficiency in Modern Organic Chemistry. In 9 Volumes, Barry M. Trost, Editor-in-Chief (Pergamon Press, New York, друк 1993 р.). Інші способи, придатні для отримання сполук за винаходом, описані в міжнародній патентній заявці за номером публікації WO 2006/020276. Ряд ілюстративних способів отримання композицій за винаходом наведено у схемах і прикладах нижче. Ці способи призначені для ілюстрації природи таких препаратів і не призначені для обмеження обсягу застосовних способів. Загалом, умови реакції, такі як температура, час реакції, розчинники, процедури обробки, тощо, будуть загальноприйнятими в цій галузі для конкретної реакції, що має бути виконана. Наведений довідковий матеріал, разом із матеріалом, наведеним у ньому, містить докладні описи таких умов. Типово температура буде становити від -100°C до 200°C, розчинники будуть апротонними або протонними, а час реакції буде складати від 10 секунд до 10 днів. Обробка типово складається з гасіння будь-яких реагентів, що не прореагували, з наступним розділенням між системою води/органічного шару (екстракція) та розділення шару, що містить продукт. Реакції окиснення та відновлення зазвичай виконуються при температурі, близькій до кімнатної температури (близько 20°С), хоча для металогідридного відновлення часто температура знижується від 0°С до -100°С, розчинники є зазвичай апротонними для відновлення, і можуть бути як протонними, так і апротонними для окиснення. Час реакції регулюють для досягнення бажаних перетворень. Реакції конденсації зазвичай виконуються при температурах, близьких до кімнатної температури, хоча для незрівноважувальних, кінетично контрольованих конденсацій знижені температури (від 0°C до -100°C) є також поширеними. Розчинники можуть бути або протонними (поширені у зрівноважувальних реакціях) або апротонними (поширені в кінетично контрольованих реакціях). Стандартні синтетичні способи, такі як азеотропне видалення побічних продуктів реакції і використання безводних умов реакції (наприклад, середовища інертного газу) є загальнопоширеними в даній галузі і будуть застосовуватися, коли це доречно. Терміни "оброблений", "оброблення", "обробка", тощо, якщо використовуються у зв'язку з хімічною синтетичною операцією, означають контактування, змішування, реагування, введення в реакцію, приведення до контакту та інші терміни, поширені в цій галузі техніки для зазначення того, що одна або більше хімічних сполук обробляються таким чином, щоб перетворити їх в одну або більше інших хімічних сполук. Це означає, що "обробка сполуки один сполукою два" є синонімом "введення сполуки один в реакцію зі сполукою два", "контактування сполуки один зі сполукою два", "реагування сполуки один зі сполукою два" та інших виразів, загальноприйнятих в галузі органічного синтезу, для належного позначення того, що сполука один була "оброблена", "вступила в реакцію", "її ввели в реакцію" і т. д., зі сполукою два. Наприклад, оброблення визначає належний і звичайний спосіб, у який органічні хімічні речовини вводять в реакцію. Якщо не зазначене інше, передбачені нормальні концентрації (від 0,01 М до 10 М, типово від 0,1 М до 1М), температури (від -100°С до 250°С, типово від -78°С до 150°С, більш типово від -78°С до 100°С, ще більш типово від 0°C до 100°C), реакційні посудини (типово, скло, пластик, метал), розчинники, тиск і середовища (типово повітря для реакцій, нечутливих до кисню і води, або азот чи аргон для реакцій, чутливих до кисню або води) і т. д. Знання подібних реакцій, відомих в галузі органічного синтезу, використовується при виборі умов і пристрою для "обробки" в даному процесі. Зокрема, фахівець в галузі органічного синтезу обирає умови і пристрій, від яких обґрунтовано слід очікувати успішного виконання хімічних реакцій описаних процесів на основі знань у даній галузі. Модифікації кожної з ілюстративних схем і в Прикладах (далі "ілюстративні схеми") призводять до отримання різних аналогів конкретних ілюстративних матеріалів. Наведені вище посилання, що описують придатні способи органічного синтезу, є застосовними до таких модифікацій. У кожній з ілюстративних схем може бути корисно відокремлювати продукти реакції одне від одного і/або від вихідних матеріалів. Цільові продукти кожного етапу або ряду етапів відокремлюються і/або очищуються (далі відокремлені) до бажаного ступеню однорідності за допомогою способів, загальноприйнятих в даній галузі. Типово такі розділення передбачають багатофазну екстракцію, кристалізацію з розчинника або суміші розчинників, дистиляцію, сублімацію або хроматографію. Хроматографія може включати в себе будь-яку кількість способів, включаючи, наприклад, способи і пристрій рідинної хроматографії з зворотною фазою 18 UA 110354 C2 5 10 15 20 25 30 35 40 45 50 55 60 і нормальною фазою; ексклюзійної хроматографії; іонообмінної хроматографії; рідинної хроматографії високого, середнього і низького тиску; маломасштабної аналітичної; з псевдорухомим шаром (SMB) і препаративної тонкошарової або товстошарової хроматографії, а також способи маломасштабної тонкошарової і флеш-хроматографії. Інший клас способів розділення передбачає обробку суміші реагентом, вибраним для того, щоб зв'язувати або інакшим чином зробити відокремлюваним бажаний продукт, вихідний матеріал, який не прореагував, побічний продукт реакції або тому подібне. Такі реагенти включають адсорбенти або абсорбенти, такі як активоване вугілля, молекулярні сита, іонообмінні середовища або їм подібні. Альтернативно, реагенти можуть бути кислотами в разі лужного матеріалу, лугами у випадку кислотного матеріалу, зв'язувальними реагентами, такими як антитіла, зв’язувальними білками, селективними хелатуючими агентами, такими як краунефіри, рідинно-рідинними іоноекстракційними реагентами (LIX), або їм подібними. Вибір відповідних способів розділення залежить від природи використовуваних матеріалів. Наприклад, точка кипіння і молекулярна вага у дистиляції і сублімації, наявність або відсутність полярних функціональних груп у хроматографії, стабільність матеріалів в кислому і лужному середовищі у багатофазній екстракції, тощо. Фахівець у даній галузі буде застосувати ті способи, що є найбільш прийнятними для досягнення бажаного розділення. Окремий стереоізомер, наприклад, енантіомер, практично вільний від його стереоізомеру, може бути отриманий шляхом розділення рацемічної суміші з використанням такого способу, як утворення діастереомерів з використанням оптично активних розділяючих агентів ("Стереохімія вуглецевих сполук") (Stereochemistry of Carbon Compounds, (1962) by E. L. Eliel, McGraw Hill; Lochmuller, C. H., (1975) J. Chromatogr., 113, 3) 283-302). Рацемічні суміші хіральних сполук за винаходом можуть бути розділені і ізольовані будь-яким придатним способом, включаючи: (1) утворення іонних діастереомерних солей з хіральними сполуками і розділення шляхом фракційної кристалізації або іншими способами, (2) утворення діастереомерних сполук з хіральними дериватизуючими реагентами, розділення діастереомерів і перетворення у чисті стереоізомери, і (3) розділення, по суті, чистих або збагачених стереоізомерів безпосередньо у хіральних умовах. За способом (1), діастереомерні солі можуть бути отримані шляхом реакції енантіомерно чистих хіральних основ, таких як бруцин, хінін, ефедрин, -метил--фенілетиламін (амфетамін), тощо з асиметричними сполуками, що мають кислі функціональні можливості, такі як карбонові кислоти і сульфонові кислоти. Діастереомерні солі можуть піддаватися розділенню шляхом фракційної кристалізації або іонної хроматографії. Для розділення оптичних ізомерів аміносполук, додавання хіральних карбонових або сульфонових кислот, таких як камфорсульфонова кислота, винна кислота, мигдальна кислота або молочна кислота, може привести до утворення діастереомерних солей. Альтернативно, за способом (2), субстрат, який необхідно розділити, вступає у реакцію з одним енантіомером хіральної сполуки для утворення діастереомерної пари ("Стереохімія органічних сполук") (Eliel, E. and Wilen, S. (1994) Stereochemistry of Organic Compounds, John Wiley & Sons, Inc., p. 322). Діастереомерні сполуки можуть бути отримані шляхом реакції асиметричних сполук з енантіомерно чистими хіральними дериватизуючими реагентами, такими як похідні ментилу, з наступним розділенням діастереомерів і гідролізом для отримання вільного, енантіомерно збагаченого субстрату. Спосіб визначення оптичної чистоти включає отримання хіральних складних ефірів, таких як ментиловий ефір, наприклад, (-) ментиловий ефір хлормурашиної кислоти в присутності основи, або складного ефіру Мошера, -метокси-(трифторметил)феніл ацетату (Jacob III. (1982) J. Org. Chem. 47:4165) рацемічної суміші, і аналіз NMR-спектра на наявність двох атропізомерних діастереомерів. Стабільні діастереомери атропізомерних сполук можуть бути розділені і ізольовані за допомогою хроматографії з нормальною і оберненою фазою відповідно до способів розділення атропізомерних нафтилізохінолінів (Hoye, T., WO 96/15111). За способом (3), рацемічна суміш двох енантіомерів може бути розділена за допомогою хроматографії з використанням хіральної стаціонарної фази ("Хіральна рідинна хроматографія") (Chiral Liquid Chromatography (1989) W. J. Lough, Ed. Chapman and Hall, New York; Okamoto, (1990) J. of Chromatogr. 513:375-378). Збагачені або очищені енантіомери можливо виділити способами, які використовуються для виділення інших хіральних молекул з асиметричними атомами вуглецю, таких як оптичне обертання і циркулярний дихроїзм. Схеми і приклади Загальні аспекти цих ілюстративних способів описані нижче і в Прикладах. Кожен з продуктів наступних процесів необов'язково розділяється, ізолюється і/або очищується перед його використанням в подальших процесах. 19 UA 110354 C2 5 10 Ряд ілюстративних способів отримання сполук за винаходом представлені в описі, наприклад, у наведених нижче Прикладах. Ці способи призначені для ілюстрації природи таких препаратів і не призначені для обмеження обсягу застосовних способів. Деякі сполуки за винаходом можуть бути використані в якості проміжних сполук для отримання інших сполук даного винаходу. В ілюстративних способах, описаних тут, фрагмент E-V- також може бути записаний у вигляді R9-. PG являє собою захисну групу, спільну для даної функціональної групи, до якої вона прикріплена. Введення і видалення захисної групи може здійснюватися з використанням стандартних способів, таких як описані у "Захисних групах в органічному синтезі" (Wuts, P.G.M., Greene, T. Protective Groups in Organic Synthesis, 4th ed.; John Wiley & Sons, Inc.: Hoboken, New Jersey, 2007). Схема 1. Репрезентативний синтез E-V-C(= O)-P-W-P-C(=O)-V-E O O O Cl NH-V-C(=O)-P-W-P-C(=O)-V-E H2N V-C(=O)-P-W-P-C(=O)-V-E O 1a 1b O 2 O O Cl O 1c 15 O NH-V-C(=O)-P-W-P-C(=O)-V-NH H2N V-C(=O)-P-W-P-C(=O)-V NH2 O 1d Схема 1 зображує загальний синтез E-V-C(=O)-P-W-P-C(=O)-V-E молекули за винаходом, де, в ілюстративних цілях, Е є метоксикарбоніламіно. Обробка або 1а або 1с одним або двома еквівалентами відповідно метилхлорформіату в лужних умовах (наприклад, гідроксид натрію) забезпечує молекулу 1b або 1d. Схема 2. Репрезентативний синтез E-V-C(=O)-P-W-P-C(=O)-V-E HO E-V-C(=O)-P-W V-E N H 2a O E-V-C(=O)-P-W N 2c 2b E-V H N HO W N H 2d V-E 2 V-E O N W O N 2b 2e 20 25 O O V-E Схема 2 зображує загальний синтез E-V-C(=O)-P-W-P-C(=O)-V-E молекули за винаходом, де, в ілюстративних цілях, P є піролідином. З'єднання аміну 2a з кислотою 2b здійснюється за допомогою пептидного зв'язувального реагенту (наприклад, HATU) для отримання 2с. Альтернативно, амін 2d з'єднується з двома еквівалентами 2b в аналогічних умовах для отримання 2e. 1 2 Схема 6. Репрезентативний синтез R -V-C(=O)-P-R 20 UA 110354 C2 HO E-V-C(=O)-P-W E-V-C(=O)-P-W V-NH-PG N H 6a N O 6c 6b O V-NH-PG HO PG-HN-V-C(=O)-P-W V-E N H 6d PG-HN-V-C(=O)-P-W N O 6f 6e O V-E HO PG-HN-V-C(=O)-P-W V-NH-PG N H 6d PG-HN-V-C(=O)-P-W N O 6g 6b O V-NH-PG HO PG-HN-P-W 6h PG-HN-P-W V-E N H N O 6i 6e O V-E HO PG-HN-P-W 6h PG-HN-P-W V-NH-PG N H O N 6j 6b O V-NH-PG HO PG-HN-W 6k PG-HN-W V-E N H O N 6l 6e O V-E HO PG-HN-W 6k PG-HN-W V-NH-PG N H O N 6m 6b 1 5 O 2 V-NH-PG Схема 6 зображує загальний синтез проміжної сполуки R -V-C(=O)-P-R , де, в ілюстративних 1 цілях, P є піролідином, R є спорідненою групою, яка зображена або як –E, або як амінозахисна 2 група, і R є спорідненою групою, яка зображена як W-P-C(=O)-V-E, -W-P-C(=O)-V-NH-PG, -W-PNH-PG або -W-NH-PG. З'єднання аміну 6а (або 6d, 6h, 6k) з кислотою 6b або 6e здійснюється з використанням пептидного зв’язувального реагенту (наприклад, HATU) для отримання 6c (або 6f, 6g, 6i, 6j, 6l, 6m), відповідно. 1 Схема 7. Репрезентативний синтез E-V-C(=O)-R 10 21 UA 110354 C2 O O O Cl NH-V-C(=O)-P-W-P-C(=O)-V-NH-PG H2N V-C(=O)-P-W-P-C(=O)-V-NH-PG O 7a 7b O O H2N V-C(=O)-P-W-P-PG O Cl NH-V-C(=O)-P-W-P-PG O 7c 7d O O H2N V-C(=O)-P-W-PG O Cl NH-V-C(=O)-P-W-PG O 7e 7f O O H2N V-C(=O)-P-PG O Cl NH-V-C(=O)-P-PG O 7g 7h O O H2N V-C(=O)-O-PG O Cl NH-V-C(=O)-O-PG O 7i 7j 1 5 Схема 7 зображує загальний синтез проміжної сполуки E-V-C(=O)-R , де, в ілюстративних 1 цілях, Е є метоксикарбоніламіно, і R є спорідненою групою, яка зображена або як -P-W-PC(=O)-V-NH-PG, -P-W-P-PG, -P-W-PG, -P-PG, або як -O-PG. Обробка 7а (або 7c, 7e, 7g, 7i) метиловим ефіром хлормурашиної кислоти в лужних умовах (наприклад, гідроксид натрію) забезпечує молекулу 7b (або 7d, 7f, 7h, 7j). 1 Схема 9. Репрезентативний синтез R -P-R 2 10 NH2 Br NH2 HO NH2 P-C(=O)-V-E O Br 9b NH P-C(=O)-V-E 9a O 9c H N P-C(=O)-V-E N Br 9d NH2 Br NH2 HO NH2 P-PG O Br 9e NH P-PG 9a O 9f H N P-PG N Br 9g 1 15 2 Схема 9 зображує загальний синтез проміжної сполуки R -P-R , де, в ілюстративних цілях, 2 R є -C(=O)-V-E або захисною групою, і R є заміщеним бензімідазолом. Утворення бензімідазолу досягається шляхом з'єднання кислоти 9b або 9e з ариламіно 9а, з 1 22 UA 110354 C2 5 10 15 20 використанням пептидного зв’язувального реагенту, такого як HATU, для отримання 9с або 9d. Циклізація аміду в присутності кислоти (наприклад, оцтової кислоти) дає бензімідазол, який містить молекулу 9d або 9g. Утворення численних бензімідазолів здійснюється таким же чином, починаючи з біс-діаміну, для отриманням відповідного біс-бензімідазолу. 1 2 Схема 20. Репрезентативний синтез R -P-W-P-R 1 2 Схема 20 зображує загальний синтез проміжної сполуки за винаходом R -P-W-P-R , де, в 1 2 ілюстративних цілях, R і R є незалежними захисними групами, і W являє собою блок з двох ароматичних кілець, побудований за допомогою циклізації, опосередкованої перехідним металом. Алкілування фенолу 20b з алкілбромідом, наприклад, 20а, забезпечує ефір 20c. Циклізація ароматичних кілець в присутності паладієвого каталізатора дає сполуку 20d. Обробка 20d CuBr2 дає α-галогенкетон 20e, який дає 20f при додаванні кислоти в лужних умовах (наприклад, Et3N). Реакція 20f з аміном або сіллю аміну (наприклад, ацетат амонію) дає молекулу 20g, що містить імідазол. Окиснення 20g, 20i, або 20l може здійснюватися шляхом нагрівання в присутності MnO2 для отримання 20h, 20j або 20m відповідно. Конвертування 20g або 20h з паладієвим каталізатором, таким як Pd2dba3 та X-Phos, і джерелом бору, таким як біс(пінаколато)дибор забезпечує борний ефір 20i і 20j. Борний ефір з'єднується з відповідним зв'язувальним партнером (наприклад, 20k) з використанням паладієвого каталізатора, такого як 23 UA 110354 C2 5 Pd(PPh3)4 або PdCl2(dppf) для отриманням 20l або 20m. Для кожної реакції крос-поєднання, опосередкованої перехідним металом, ролі нуклеофілу і електрофілу можуть обертатися для забезпечення однакового зв’язувального продукту. Інші крос-поєднання, опосередковані перехідним металом, які забезпечують формування W, але використовують альтернативні зв'язувальні партнери і реагенти, включають, але не обмежуються, з'єднання Негіші (Negishi), Кумада (Kumada), Стіле (Stille) і Ульмана (Ullman). Для підготовки альтернативних груп W, що містять два ароматичні кільця, ця загальна схема може бути застосована шляхом відповідного вибору вихідних реагентів. 1 2 Схема 21. Репрезентативний синтез R -P-W-P-R 10 O O O O 21a 20d Cl O O O O O PG-P O Br 21c O 21b O O O O PG-P Br O 21d O O O O PG-P P-PG O O O 21e O O N PG-P H N P-PG N N H 21f/g 15 20 25 1 2 Схема 21 зображує загальний синтез проміжної сполуки за винаходом R -P-W-P-R , де, в 1 2 ілюстративних цілях, R і R є незалежними захисними групами, і W являє собою блок з двох ароматичних кілець, побудований за допомогою циклізації, опосередкованої перехідним металом. Обробка 20d активованим вініловим реагентом (наприклад, вінілтрифторборат калію) у присутності паладієвого каталізатора (наприклад, ацетат паладію і S-Phos), забезпечує вінілову сполуку 21а. Перетворення у відповідний α-галогенкетон може здійснюватися шляхом бромування з N-бромсукцинімідом, з подальшим окисненням з MnO 2. Зміщення α-галогенкетону відбувається шляхом додавання кислоти в лужних умовах (наприклад, Et3N). Бромування 21d відбувається при обробці трибромистим піридинієм, з подальшим додаванням другої кислоти в лужних умовах для отримання діефіру 21e. Реакція 21e з аміном або сіллю аміну (наприклад, ацетат амонію) дає молекулу 21f, що містить імідазол. Окиснення 21f може здійснюватися у 24 UA 110354 C2 присутності MnO2 для отримання 21g. Схема 22. Репрезентативний синтез E-V-C(=O)-P-W-P-R 5 10 Схема 22 зображує загальний синтез проміжної сполуки за винаходом E-V-C(=O)-P-W-P-R, де, в ілюстративних цілях, R є захисною групою, і W являє собою блок з двома ароматичними кільцями. Зміщення α-галогенкетону 21b відбувається шляхом додавання кислоти в лужних умовах (наприклад, Et3N). Бромування 22b відбувається при обробці трибромистим піридинієм, з подальшим додаванням другої кислоти в лужних умовах для отриманням діефіру 22c. Реакція 22e з аміном або сіллю аміну (наприклад, ацетат амонію) дає молекулу 22d, що містить імідазол. Окиснення 22d може здійснюватися у присутності MnO2 для отримання 22e. Схема 23. Репрезентативний синтез R-P-W-P-C(=O)-V-E 25 UA 110354 C2 5 10 15 Схема 23 зображує загальний синтез проміжної сполуки за винаходом E-V-C(=O)-P-W-P-R, де, в ілюстративних цілях, R є захисною групою, і W являє собою блок з двома ароматичними кільцями. Зміщення α-галогенкетону 21d відбувається шляхом додавання кислоти в лужних умовах (наприклад, Et3N). Реакція 23a з аміном або сіллю аміну (наприклад, ацетат амонію) дає молекулу 23b, що містить імідазол. Окиснення 23b може здійснюватися у присутності MnO2 для отримання 23c. Схема 25. Репрезентативний синтез E-V-C(=O)-P-W-P-C(=O)-V-E Схема 25 зображує загальний синтез молекули за винаходом E-V-C(=O)-P-W-P-C(=O)-V-E, де, в ілюстративних цілях, Е є етилкарбоніламіно. Обробка або 25а або 25с одним або двома еквівалентами відповідно пропіонілхлоріду в лужних умовах (наприклад, гідроксид натрію) забезпечує молекули 25b або 25d. 1 Схема 26. Репрезентативний синтез E-V-C(=O)-P-R and R -P-R 26 UA 110354 C2 1 5 10 Схема 26 зображує загальний синтез молекули за винаходом E-V-C(=O)-P-R і R -P-R, де, в ілюстративних цілях, R є галогенімідазолом. Обробка альдегіду 26a гліоксалем у присутності гідроксиду амонію забезпечує імідазол 26b. Обробка або N-бромсукцинамідом, або йодом, дає відповідний галогенімідазол 26c і 26d відповідно. Відокремлення від відповідної бісгалогенованої сполуки може здійснюватися за допомогою препаративної високоефективної рідинної хроматографії (HPLC). Конвертування біс-галогенімідазолу у моно-галогенімідазол також може здійснюватися при нагріванні в присутності сульфіту натрію. Подальша функціоналізація групи P може бути досягнута шляхом видалення захисної групи і з'єднання з відповідною кислотою (E-V-C(=O)-ОН). 1 Схема 27. Репрезентативний синтез R -P-W-P-R 27 2 UA 110354 C2 1 5 10 2 Схема 27 зображує загальний синтез проміжної сполуки за винаходом R -P-W-P-R , де, в 1 2 ілюстративних цілях, R і R є незалежними захисними групами, і W являє собою блок з двох ароматичних кілець, побудований за допомогою циклізації, опосередкованої перехідним металом. Бромування 21b за допомогою бромуючого агента (наприклад, трибромистий піридиній) забезпечує дибромід 27а. Зміщення первинного броміду відбувається потім шляхом додавання кислоти в лужних умовах (наприклад, K2CO3) для отримання 21d. Конверсія у 21f і 21g може здійснюватися відповідно до способів, описаних у схемі 21. Схема 28. Репрезентативний синтез E-V-C(=O)-P-W-P-R 28
ДивитисяДодаткова інформація
Назва патенту англійськоюCondensed imidazolylimidazoles as antiviral compounds
Автори англійськоюBacon, Elizabeth, M., Cottell, Jeromy, J., Katana, Ashley, Anne, Kato, Darryl, Krygowski, Evan, S., Link, John, O., Taylor, James, Tran, Chinh Viet, Trejo Martin, Teresa, Alejandra, Yang, Zheng-Yu, Zipfel, Sheila
Автори російськоюБейкон Элизабет М., Коттелл Джероми Дж., Катана Эшли Энн, Кэйто Деррил, Криговски Эван С., Линк Джон О., Тэйлор Джэймс, Тран Чинх Вьет, Трехо Мартин Тереса Алехандра, Ян Чжен-Ю, Ципфель Шейла
МПК / Мітки
МПК: A61K 31/4188, C07D 491/052
Мітки: сполуки, противірусні
Код посилання
<a href="https://ua.patents.su/185-110354-protivirusni-spoluki.html" target="_blank" rel="follow" title="База патентів України">Противірусні сполуки</a>
Попередній патент: Спосіб одержання фільтруючого матеріалу, пристрій для його реалізації і спосіб очищення підземної води
Наступний патент: Сцинтиляційний детектор реєстрації теплових нейтронів
Випадковий патент: Фотометр