Спосіб одержання заміщених 3-піридилметиламонію бромідів
Номер патенту: 103502
Опубліковано: 25.10.2013
Автори: Ляйхт Роберт, Цех Гельмут, Єгерленер Тоні, Шрьодер Йохен, Рак Міхаель, Гебхардт Йоахім, Менгес Фредерік, Орстен Штефан, Кайл Міхаель, Кліма Родні Ф., Кортес Девід
Формула / Реферат
1. Спосіб одержання 5,6-дизаміщених-3-піридилметиламонію бромідів (І)
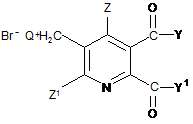 , (І)
, (І)
де
Q являє собою третинний аліфатичний або циклічний, насичений, частково ненасичений або ароматичний амін;
Z являє собою водень або галоген;
Z1 являє собою водень, галоген, ціано або нітро;
Y і Y1, кожний незалежно, являють собою OR1, NR1R2, або разом YY1 являють собою -О-, -S- або NR3-;
R1 і R2, кожний незалежно, являють собою водень, С1-С4алкіл, необов'язково заміщений С1-С4алкокси або фенілом, необов'язково заміщеним однією-трьома С1-С4алкільними групами, С1-С4алкоксигрупами або атомами галогену, або феніл, необов'язково заміщений однією-трьома С1-С4алкільними групами, С1-С4алкоксигрупами або атомами галогену;
R3 являє собою водень або С1-С4алкіл;
який включає стадії, за якими проводять:
(і) взаємодію сполуки формули (II)
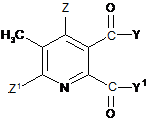 (II)
(II)
де символи мають значення, вказані для формули (І), із бромом у присутності радикального ініціатора в суміші розчинників, що містить водну фазу й органічну фазу, де органічна фаза містить розчинник, вибраний з 1,2-дихлоретану, хлорбензолу, 1,2-дихлорбензолу, 1,3-дихлорбензолу, 1,4-дихлорбензолу й тетрахлорметану, і де значення рН водної фази становить від 3 до <8, одержуючи 3-бромметил-5,6-дизаміщену піридинову сполуку (III)
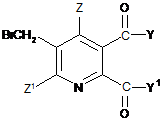 , (III)
, (III)
де Y, Y1, Z і Z1 мають значення, вказані для формули (І), і
(іі) взаємодію бромованої сполуки формули (III) із третинною аміновою основою Q у розчиннику при температурі в інтервалі від 0 °C до 100 °C.
2. Спосіб, як заявлено в пункті 1, де як органічний розчинник на стадії (і) використовують 1,2-дихлоретан.
3. Спосіб, як заявлено в пункті 1 або 2, де Q+ у формулі (І) являє собою
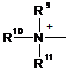 ;
; 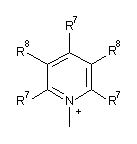 ;
;
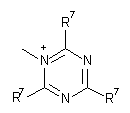 ;
; 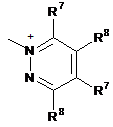 ;
; 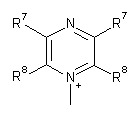 ;
;
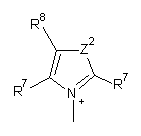 ;
;
Z2 являє собою О, S або NR12;
R12 являє собою С1-С4алкіл;
R7 і R8, кожний незалежно, являють собою водень, галоген, С1-С4алкіл або С1-С4алкокси, або R7 і R8 разом утворюють 5- або 6-членне насичене або ненасичене кільце, яке необов'язково містить О, S або NR12 і необов'язково заміщене одним-трьома атомами галогену, С1-С4алкільними групами або С1-С4алкоксигрупами, де
R9, R10 і R11, кожний незалежно, являють собою С1-С4алкіл, або R9 і R10 разом утворюють 5- або 6-членне кільце, у якому R9R10 представлений структурою: -(СН2)n-, яка необов'язково містить О, S або NR9, де n представляє собою ціле число 3, 4 або 5, за умови, що R11 являє собою С1-С4алкіл.
4. Спосіб, як заявлено в будь-якому з пунктів 1-3, де сполука формули (І) являє собою сполуку формули (Іа):
 (Ia).
(Ia).
5. Спосіб, як заявлено в будь-якому з пунктів 1-4, де реакцію на стадії (і) здійснюють аж до перетворення сполуки (II) до 20-60 %.
6. Спосіб, як заявлено в будь-якому з пунктів 1-5, де органічну фазу на стадії (іі) застосовують повторно на стадії (і) з необов'язковим додаванням сполуки (II).
7. Спосіб, як заявлено в будь-якому з пунктів 1-6, де значення рН водної фази на стадії (і) становить від 3 до 7.
8. Спосіб, як заявлено в будь-якому з пунктів 1-7, де ініціатор на стадії (і) вибирають із азобісізобутиронітрилу, 2,2'-азобіс(2-метилбутаннітрилу), 2,2'-азобіс(2,4-диметилпентаннітрилу або 1,1'-азобіс(циклогексанкарбонітрилу).
9. Спосіб, як заявлено в будь-якому з пунктів 1-8, де молярне відношення піридинової сполуки (II) до брому на стадії (і) підтримують 1:0,5-1,2.
10. Спосіб, як заявлено в будь-якому з пунктів 1-9, де стадію (і) здійснюють при температурі від 50 °C до 120 °C.
11. Спосіб, як заявлено в будь-якому з пунктів 1-10, де третинний амін Q на стадії (іі) являє собою триметиламін.
12. Спосіб, як заявлено в будь-якому з пунктів 1-11, який додатково включає стадію, за якою проводять:
(ііі) взаємодію сполуки формули (І) у метанолі, толуолі або суміші метанол/толуол з основою, вибраною з МОСН3 і МОН (якщо розчинник містить метанол), де М являє собою лужний метал або лужноземельний метал, з утворенням 5,6-дизаміщеного-3-метоксиметилпіридину формули (IV)
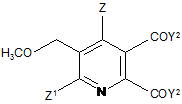 , (IV)
, (IV)
де
Z являє собою водень або галоген;
Z1 являє собою водень, галоген, ціано або нітро;
Y2 являє собою ОСН3 або ОМ.
13. Спосіб, як заявлено в пункті 12, який додатково включає стадію, за якою проводять:
(iv) перетворення сполуки формули (IV) у гербіцидну імідазолінонову сполуку формули (V)
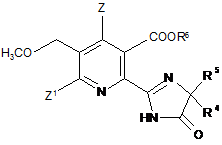 , (V)
, (V)
де
Z являє собою водень або галоген;
Z1 являє собою водень, галоген, ціано або нітро;
R4 являє собою С1-С4алкіл;
R5 являє собою С1-С4алкіл, С3-С6циклоалкіл; або
R4 і R5 разом з атомом, до якого вони приєднані, являють собою С3-С6циклоалкільну групу, необов'язково заміщену метилом,
R6 являє собою водень; групу формули -N=C(нижчий алкіл)2; С1-С12алкіл, необов'язково заміщений однією з наступних груп: С1-С3алкокси, галоген, гідроксил, С3-С6циклоалкіл, бензилокси, фурил, феніл, галогенфеніл, нижчий алкілфеніл, нижчий алкоксифеніл, нітрофеніл, карбоксил, нижчий алкоксикарбоніл, ціано або три(нижчий алкіл)амоній; С3-С12алкеніл, необов'язково заміщений однією з наступних груп: С1-С3алкокси, феніл, галоген або нижчий алкоксикарбоніл, або двома С1-С3алкоксигрупами, або двома галогеновими групами; С3-С6циклоалкіл, необов'язково заміщений однією або двома С1-С3алкільними групами; або катіон.
14. Спосіб, як заявлено в пункті 13, який додатково включає стадії, за якими проводять:
(iv-1) необов'язкове приготування ангідриду (VII) сполуки (IV);
(iv-2) взаємодію сполуки (IV) або її ангідриду (VII) у присутності основи з 2-аміноалканкарбоксамідом формули (VI)
H2N‑CR4R5‑CONH2, (VI)
де R4 і R5 мають значення, як вказано у формулі (V).
15. Спосіб, як заявлено в пункті 13, який додатково включає стадії, за якими проводять:
(iv-1) перетворення сполуки (IV) в ангідрид (VII)
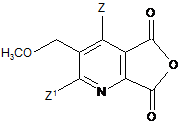 , (VII)
, (VII)
(iv-2) взаємодію ангідриду (VII) з амінокарбонітрилом (IX)
H2N‑CR4R5‑CN, (IX)
де R4 і R5 мають значення, як вказано у формулі (V), з одержанням амідонітрильної сполуки (X)
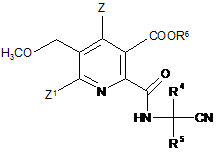 , (Х)
, (Х)
де символи мають значення, як вказано у формулі (V) у пункті 13,
R6 являє собою Н;
(iv-3) гідроліз нітрильної групи в сполуці (X), з одержанням аміду (VIII)
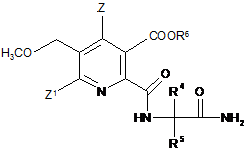 , (VIII)
, (VIII)
де символи мають значення, як вказано у формулі (V) у пункті 13,
R6 являє собою Н,
(iv-4) конденсацію аміду (VIII), з одержанням гербіцидного імідазолінону (V).
Текст
Реферат: Спосіб одержання 5,6-дизаміщених-3-піридилметиламонійю бромідів (І) z Z Br - Q+H2C Z1 O C N Y C Y O 1 , (І) де Q являє собою третинний аліфатичний або циклічний, насичений, частково ненасичений або ароматичний амін; Z являє собою водень або галоген; 1 Z являє собою водень, галоген, ціано або нітро; 1 1 1 2 1 Y і Y , кожний незалежно, являють собою OR , NR R , або разом YY являють собою -О-, -S3 або NR -; UA 103502 C2 (12) UA 103502 C2 1 2 R і R , кожний незалежно, являють собою водень, С1-С4алкіл, необов'язково заміщений С1С4алкокси або фенілом, необов'язково заміщеним однією-трьома С1-С4алкільними групами, С1С4алкоксигрупами або атомами галогену, або феніл, необов'язково заміщений однією-трьома С1-С4алкільними групами, С1-С4алкоксигрупами або атомами галогену; 3 R являє собою водень або С1-С4алкіл; в якому здійснюють (і) взаємодію сполуки формули (II) z Z O C N Z1 Y C H3C Y 1 O , (II) де символи мають значення, вказані для формули (І), із бромом у присутності радикального ініціатора в суміші розчинників, що містить водну фазу й органічну фазу, де органічна фаза містить розчинник, вибраний з 1,2-дихлоретану, хлорбензолу, 1,2-дихлорбензолу, 1,3-дихлорбензолу, 1,4-дихлорбензолу й тетрахлорметану, і де значення рН водної фази становить від 3 до 95 % (як визначено за допомогою ВЕРХ). Приклад 2 Синтез [(5,6-дикарбокси-3-піридил)метил] триметиламоній броміду, простий диметиловий ефір (Ia) Синтез здійснювали, як описано в прикладі 1, за винятком того, що на стадії (a) усю кількість 13,65 г (0,071 моль) 2,2’-азобіс(2-метилбутиронітрилу) (Vazo 67) в 160,0 г EDC додавали при 72 °C, і через 5 хвилин додавали 135,8 г (0,85 моль) брому протягом 2 годин під контролем pН (pН 5) шляхом дозування приблизно 375,0 г водного NaОН (15 %). Загальний ступінь перетворення сполуки (IІa) становив 96,6 %. Вихід сполуки (Ia) (за 7 циклів) становив 78,2 % із чистотою > 95 % (як визначено за допомогою ВЕРХ). Приклад 3 Синтез [(5,6-дикарбокси-3-піридил)метил] піридиній броміду, простий диметиловий ефір Стадію (a) здійснювали відповідно до процедури із прикладу 1. 11 UA 103502 C2 Синтез сполуки (Ib) Br COOCH3 Br + N N N N COOCH3 10 15 COOCH3 (Ib) (IIIa) 5 COOCH3 82,4 г (0,286 моль) сполуки (ІІІa) у суміші з ди- і трибромованими побічними продуктами) в EDC (1183,8 г органічна фаза зі стадії a, включаючи непрореаговану сполуку (IІa) і інтенсивно бромовані побічні продукти) завантажували. Суміш нагрівали до 40 °C. По краплях додавали 27,88 г (0,292 моль) піридину протягом 60 хвилин при 40 °C. Суміш перемішували при 55 °C додатково протягом однією години. Надлишок піридину відганяли разом з EDC при 55-60 °C у вакуумі (~ 90 тор) доти, поки загальна вага суміші не становила 382,7 г. Додавали 134,8 г води. Суміш перемішували протягом 15 хвилин і потім дозволяли осісти й розділитися протягом 15 хвилин. Фази розділяли й аналізували. Вихід сполуки (Ib) для одного перетворення становив 73,4 % (виходячи з молів перетвореної монобром сполуки (ІІІa)). Приклад 4 Одержання диметил 5-(метоксиметил)-2,3-піридиндикарбоксилату (відповідно до прикладу 7 з EP-A 0 548 532) + Br (CH3)3N -CH2 CH3OCH2 CO2CH3 CO2CH3 CH3ONa N 20 25 N CH3OH CO2CH3 CO2CH3 Суміш 25 % метилату натрію в метанолі (320,0 г, 1,5 моль) і [(5,6-дикарбокси-3-піридил)метил]триметиламонійбромиду, складний диметиловий ефір (160,0 г, 0,5 моль) у метанолі (630 мл) нагрівали в колбі зі зворотним холодильником протягом 6 годин в атмосфері азоту. Реакційну суміш охолоджували до 5 °C і додавали оцтову кислоту (90 г) і воду (200 мл). Метанол видаляли у вакуумі, додавали воду й суміш екстрагували метиленхлоридом. Приклад 5 Одержання 5-(метоксиметил)-2,3-піридиндикарбонової кислоти (відповідно до прикладу 8 з EP-A 0 548 532) 30 CH3OCH2 CO2CH3 N 35 40 CO2CH3 1. NaOH, H2O 2. H2SO4 CH3OCH2 CO2H N CO2H Суміш диметил 5-(метоксиметил)-2,3-піридиндикарбоксилату (60,0 г, 0,25 моль) і 50 % розчину гідроксиду натрію (50,0 г, 0,63 моль) у воді нагрівали при 90-110 °C протягом 2 годин в атмосфері азоту, у той час як відганяли метанол і воду. Реакційну суміш охолоджували до 10 °C, обробляли сірчаною кислотою для доведення pН до 2,0 і фільтрували, одержуючи тверду речовину. Тверду речовину промивали водою й висушували у вакуумі, одержуючи вказаний у заголовку продукт у вигляді білої твердої речовини (44,3 г, t пл. 161-162 °C). Приклад 6 Одержання 5-(метоксиметил)-2,3-піридиндикарбонової кислоти (відповідно до прикладу 3 з EP-A 0 548 532) 12 UA 103502 C2 + Br (CH3)3N -CH2 CO2CH3 1. CH3ONa, CH3OCH2 COOH CH3OH N 5 10 15 CO2CH3 + N Br NaOOC 25 COOH Суміш 25 % метилату натрію в метанолі (270 г, 1,25 моль) і [(5,6-дикарбокси-3-піридил)метил]триметиламоній броміду, складний диметиловий ефір (Ia) (347 г, 1,00 моль) у метанолі (650 мл) нагрівали в колбі зі зворотним холодильником протягом 1 години на атмосфері азоту. Додавали воду (1 л) і гідроксид натрію (80,0 г, 2,0 моль) і реакційну суміш дистилювали, доти, поки посудина не становила 100-105 °C. Реакційну суміш охолоджували до кімнатної температури, обробляли сірчаною кислотою для доведення pН до значення від 1,5 до 2 і фільтрували, одержуючи тверду речовину. Тверду речовину промивали водою й висушували у вакуумній сушильній шафі, одержуючи вказаний у заголовку продукт у вигляді білої твердої речовини (tпл. 161-162 °C), який характеризувався чистотою більше 99 % згідно із ВЕРХ аналізом. Приклад 7 Одержання динатрій 5-(метоксиметил)піридин-2,3-дикарбоксилату з динатрій [5,6(дикарбоксилат-3-піридил)метил]триметиламоній броміду (відповідно до прикладу 3 з EP-A 0 747 360) NaOOC 20 N 2. NaOH, H2O 3. H2SO4 N NaOCH3 CH3OH 120°C, P OCH3 NaOOC NaOOC N Суміш динатрій [(5,6-дикарбоксилат-3-піридил)метил]триметиламоній броміду (5,0 г, 13,8 ммоль) і 25 мас. % розчину метилату натрію в метанолі (4,46 г, 20,7 ммоль NaOCH 3) в 75 г метанолу нагрівали при 120 °C протягом 21 години на реакторі під тиском. Реакцію охолоджували до кімнатної температури, обробляли водою й концентрували до кінцевої ваги 55,03 г. Зразок 5,0 г аналізували шляхом РХ аналізу (30 % CH3CN, 0,77 M H3PO4). Реакційний розчин, що залишився, упарювали насухо, одержуючи твердий залишок, який ідентифікували шляхом ЯМР аналізу. ФОРМУЛА ВИНАХОДУ 30 1. Спосіб одержання 5,6-дизаміщених-3-піридилметиламонію бромідів (І) z O Z Br - Q+H2C Z1 C N Y C Y 1 O 35 40 , (І) де Q являє собою третинний аліфатичний або циклічний, насичений, частково ненасичений або ароматичний амін; Z являє собою водень або галоген; 1 Z являє собою водень, галоген, ціано або нітро; 1 1 1 2 1 Y і Y , кожний незалежно, являють собою OR , NR R , або разом YY являють собою -О-, -S3 або NR -; 1 2 R і R , кожний незалежно, являють собою водень, С1-С4алкіл, необов'язково заміщений С1С4алкокси або фенілом, необов'язково заміщеним однією-трьома С1-С4алкільними групами, С1С4алкоксигрупами або атомами галогену, або феніл, необов'язково заміщений однією-трьома С1-С4алкільними групами, С1-С4алкоксигрупами або атомами галогену; 13 UA 103502 C2 3 R являє собою водень або С1-С4алкіл; який включає стадії, за якими проводять: (і) взаємодію сполуки формули (II) z Z O C N Z1 Y C H3C Y 1 O 5 (II) де символи мають значення, вказані для формули (І), із бромом у присутності радикального ініціатора в суміші розчинників, що містить водну фазу й органічну фазу, де органічна фаза містить розчинник, вибраний з 1,2-дихлоретану, хлорбензолу, 1,2-дихлорбензолу, 1,3дихлорбензолу, 1,4-дихлорбензолу й тетрахлорметану, і де значення рН водної фази становить від 3 до
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for manufacturing substituted 3-pyridylmethyl ammonium bromides
Автори англійськоюGebhardt, Joachim, Menges Frederik, Rack, Michael, Keil, Michael, Schroder, Jochen, Orsten, Stefan, Zech, Helmut, Klima, Rodney, F., Cortes, David, Leicht, Robert, Yegerlehner, Tony
Автори російськоюГебхардт Йоахим, Менгес Фредерик, Рак, Михаэль, Кайль Михаэль
МПК / Мітки
МПК: C07D 401/04, A61K 31/4439, C07D 213/80, A61K 31/44
Мітки: заміщених, 3-піридилметиламонію, спосіб, одержання, бромідів
Код посилання
<a href="https://ua.patents.su/19-103502-sposib-oderzhannya-zamishhenikh-3-piridilmetilamoniyu-bromidiv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання заміщених 3-піридилметиламонію бромідів</a>
Попередній патент: Вірус бичачої вірусної діареї з модифікованим erns білком
Наступний патент: Дискове гальмо
Випадковий патент: Спосіб оцінки реалізованого генетичного прогресу за показниками молочної продуктивності в родинах корів молочних порід












