Гідроксибензоатні солі метанікотинових сполук
Формула / Реферат
1. Сіль, одержана як продукт реакції (4Е)-N-метил-5-(5-iзопропокси-3-піридиніл)-4-пентен-2-аміну і гідроксибензойної кислоти, де гідроксибензойна кислота має формулу:
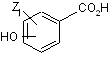 ,
,
де гідроксигрупа може бути присутньою в орто-, мета- або пара-положенні відносно групи карбонової кислоти, Z являє собою неводневий замісник, вибраний з групи, яка складається з алкілу, заміщеного алкілу, алкенілу, заміщеного алкенілу, гетероциклілу, заміщеного гетероциклілу, циклоалкілу, заміщеного циклоалкiлу, арилу, заміщеного арилу, алкіларилу, заміщеного алкіларилу, арилалкілу, заміщеного арилалкілу, F, Сl, Br, I, NR'R", CF3, CN, NO2, C2R', SH, SCH3, N3, SO2CH3, OR', (CR'R")qOR', O-(CR'R")qC2R', SR', C(=O)NR'R", NR'C(=O)R", C(=O)R', C(=O)OR', OC(=O)R', (CR'R")qOCH2C2R', (CR'R")qC(=O)R', (CR'R")qC2(CHCH3)OR', O(CR'R")qC(=O)OR', (CR'R")qC(=O)NR'R", (CR'R")qNR'R", CH=CHR', OC(=O)NR'R" і NR'C(=O)OR",
де q являє собою ціле число, що має значення від 1 до 6, і R' і R", кожний незалежно являє собою водень, С1-10 алкіл, циклоалкіл, неароматичне гетероциклічне кільце, де гетероатом гетероциклічного фрагмента відділений від якого-небудь іншого атома азоту, кисню або сірки щонайменше двома атомами вуглецю, або групу, що містить ароматичну групу, вибрану з групи, яка складається з піридинілу, хінолінілу, піримідинілу, фуранілу, фенілу і бензилу, де будь-який з вищезгаданих може бути відповідним чином заміщений щонайменше однією групою замісника, такою, як замісники алкіл, гідроксил, алкоксил, галоген або аміно,
і j являє собою число, що має значення від нуля до трьох, яке являє собою кількість замісників Z, яка може бути присутньою в кільці,
де молярне відношення (4Е)-N-метил-5-(5-ізопропокси-3-піридиніл)-4-пентен-2-аміну до гідроксибензойної кислоти знаходиться в інтервалі від 1:2 до 2:1.
2. Сіль за п. 1, де гідроксибензойна кислота являє собою о-, м- або п-гідроксибензойну кислоту.
3. Сіль за п. 1, де гідроксибензойна кислота являє собою гентизинову кислоту (2,5-дигідроксибензойну кислоту).
4. Сполука, позначена як п-гідроксибензоат (2S)-(4E)-N-мeтил-5-(5-ізопропокси-3-піридиніл)-4-пентен-2-аміну.
5. Сіль за п. 1, де (4Е)-N-метил-5-(5-ізопропокси-3-піридиніл)-4-пентен-2-амін являє собою (2S)-(4Е)-N-метил-5-(5-ізопропокси-3-піридиніл)-4-пентен-2-амін.
6. Фармацевтична композиція, яка містить сіль за будь-яким з пп. 1-5 разом з фармацевтично прийнятним носієм.
7. Спосіб лікування розладу ЦНС, який включає введення суб'єкту, потребуючому цього, ефективної кількості композиції, яка містить сіль за будь-яким з пп. 1-5, де вказану сіль необов'язково можна вводити разом з фармацевтично прийнятним носієм.
8. Спосіб одержання (2S)-(4Е)-N-метил-5-(5-ізопропокси-3-піридиніл)-4-пентен-2-аміну або його відповідної гідроксибензоатної солі,
в якому здійснюють стадії:
a) реакції поєднання Гека між 3-галоген-5-ізопропоксипіридином і сполукою формули (S)-CH2=CH-CH2-CH(CH3)-N(CH3)(pg), де pg являє собою захисну групу для аміну, і
b) зняття захисту з аміногрупи, або
c) реакції поєднання Гека між 3-галоген-5-ізопропоксипіридином і сполукою формули (R)-CH2=CH-CH2-CH(CH3)-OH і
d) перетворення групи ОН в групу NHCH3,
з одержанням суміші сполук, яка містить (2S)-(4Е)-N-метил-5-(5-ізопропокси-3-піридиніл)-4-пентен-2-амін, відповідну Z-метанікотинову сполуку та інші ізомери,
e) утворення гідроксибензоатної солі шляхом взаємодії вказаної суміші з гідроксибензойною кислотою формули:
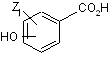 ,
,
де гідроксигрупа може бути присутньою в орто-, мета- або пара-положенні відносно групи карбонової кислоти, Z являє собою неводневий замісник, вибраний з групи, яка складається з алкілу, заміщеного алкілу, алкенілу, заміщеного алкенілу, гетероциклілу, заміщеного гетероциклілу, циклоалкілу, заміщеного циклоалкілу, арилу, заміщеного арилу, алкіларилу, заміщеного алкіларилу, арилалкілу, заміщеного арилалкілу, F, Сl, Br, I, NR'R", CF3, CN, NO2, C2R', SH, SCH3, N3, SO2CH3, OR', (CR'R")qOR', O-(CR'R")qC2R', SR', C(=O)NR'R", NR'C(=O)R", C(=O)R', C(=O)OR', OC(=O)R', (CR'R")qOCH2C2R', (CR'R")qC(=O)R', (CR'R")qC2(CHCH3)OR', O(CR'R")qC(=O)OR', (CR'R")qC(=O)NR'R", (CR'R")qNR'R", CH=CHR', OC(=O)NR'R" і NR'C(=O)OR",
де q являє собою ціле число, що має значення від 1 до 6, і R' і R", кожний незалежно являє собою водень, С1-10 алкіл, циклоалкіл, неароматичне гетероциклічне кільце, де гетероатом гетероциклічного фрагмента відділений від якого-небудь іншого атома азоту, кисню або сірки щонайменше двома атомами вуглецю, або групу, що містить ароматичну групу, вибрану з групи, яка складається з піридинілу, хінолінілу, піримідинілу, фуранілу, фенілу і бензилу, де будь-який з вищезгаданих може бути відповідним чином заміщений щонайменше однією групою замісника, такою як замісники алкіл, гідроксил, алкоксил, галоген або аміно,
і j являє собою число, що має значення від нуля до трьох, яке являє собою кількість замісників Z, яка може бути присутньою в кільці,
де молярне відношення Е-метанікотину до гідроксибензойної кислоти знаходиться в інтервалі від 1:2 до 2:1,
f) виділення гідроксибензоатної солі (2S)-(4Е)-N-метил-5-(5-ізопропокси-3-піридиніл)-4-пентен-2-аміну і
g) необов'язково, перетворення гідроксибензоатної солі (2S)-(4E)-N-мeтил-5-(5-ізопропокси-3-піридиніл)-4-пентен-2-аміну в (2S)-(4Е)-N-метил-5-(5-ізопропокси-3-піридиніл)-4-пентен-2-амін.
9. Спосіб за п. 8, де гідроксибензойна кислота являє собою о-, м- або п-гідроксибензойну кислоту.
10. Спосіб за п. 8 або 9, де гідроксибензоатну сіль перетворюють в іншу фармацевтично прийнятну сольову форму.
11. Застосування композиції, яка містить сіль за будь-яким з пп. 1-5, для одержання лікарського засобу, корисного для лікування розладу ЦНС.
Текст
1. Сіль, одержана як продукт реакції (4Е)-Nметил-5-(5-iзопропокси-3-піридиніл)-4-пентен-2аміну і гідроксибензойної кислоти, де гідроксибензойна кислота має формулу: 2 (19) 1 3 амін, відповідну Z-метанікотинову сполуку та інші ізомери, e) утворення гідроксибензоатної солі шляхом взаємодії вказаної суміші з гідроксибензойною кислотою формули: Zj CO2H HO , де гідроксигрупа може бути присутньою в орто-, мета- або пара-положенні відносно групи карбонової кислоти, Z являє собою неводневий замісник, вибраний з групи, яка складається з алкілу, заміщеного алкілу, алкенілу, заміщеного алкенілу, гетероциклілу, заміщеного гетероциклілу, циклоалкілу, заміщеного циклоалкілу, арилу, заміщеного арилу, алкіларилу, заміщеного алкіларилу, арилалкілу, заміщеного арилалкілу, F, Сl, Br, I, NR'R", CF3, CN, NO2, C2R', SH, SCH3, N3, SO2CH3, OR', (CR'R")qOR', O-(CR'R")qC2R', SR', C(=O)NR'R", NR'C(=O)R", C(=O)R', C(=O)OR', OC(=O)R', (CR'R")qOCH2C2R', (CR'R")qC(=O)R', (CR'R")qC2(CHCH3)OR', O(CR'R")qC(=O)OR', (CR'R")qC(=O)NR'R", (CR'R")qNR'R", CH=CHR', OC(=O)NR'R" і NR'C(=O)OR", де q являє собою ціле число, що має значення від 1 до 6, і R' і R", кожний незалежно являє собою водень, С1-10 алкіл, циклоалкіл, неароматичне гетероциклічне кільце, де гетероатом гетероциклічного фрагмента відділений від якого-небудь іншо Даний винахід стосується способів одержання нікотинових сполук і їх фармацевтично прийнятних солей, а також фармацевтичних композицій і способів лікування різних станів і розладів, пов'язаних з порушенням функції центральної і вегетативної нервової системи. Нікотин був запропонований як такий, що володіє різними фармакологічними ефектами. Див., наприклад, Pullan et al., N. Engl. J. Med. 330: 811815 (1994). Деякі з таких ефектів можна віднести до ефектів, що впливають на вивільнення нейротрансмітерів. Були повідомлення про вивільнення ацетилхоліну, допаміну, норепінефрину, серотоніну і глутамату при введенні нікотину (Rowell et al., J. Neurochem. 43: 1593 (1984); Rapier et al., J. Neurochem. 50: 1123 (1988); Sandor et al., Brain Res. 567: 313 (1991); Vizi, Br. J. Pharmacol. 47: 765 (1973); Hall et al., Biochem. Pharmacol. 21: 1829 (1972); Hery et al., Arch. Int. Pharmacodyn. Ther. 296: 91 (1977); Toth et al., Neurochem Res. 17: 265 (1992)). Підтверджуючі повідомлення і останні додаткові дослідження містили модуляцію в центральній нервовій системі (ЦНС) глутамату, оксиду азоту, ГАМК, тахікінінів, цитокінів і пептидів (описано в Brioni et al., Adv. Pharmacol. 37: 153 (1997)). Крім того, нікотин, як це повідомлялось, підсилює фармакологічну дію деяких фармацевтичних композицій, які застосовуються для лікування деяких розладів. Див., наприклад, Sanberg et al., Pharmacol. Biochem. & Behavior 46: 303 (1993); 88792 4 го атома азоту, кисню або сірки щонайменше двома атомами вуглецю, або групу, що містить ароматичну групу, вибрану з групи, яка складається з піридинілу, хінолінілу, піримідинілу, фуранілу, фенілу і бензилу, де будь-який з вищезгаданих може бути відповідним чином заміщений щонайменше однією групою замісника, такою як замісники алкіл, гідроксил, алкоксил, галоген або аміно, і j являє собою число, що має значення від нуля до трьох, яке являє собою кількість замісників Z, яка може бути присутньою в кільці, де молярне відношення Е-метанікотину до гідроксибензойної кислоти знаходиться в інтервалі від 1:2 до 2:1, f) виділення гідроксибензоатної солі (2S)-(4Е)-Nметил-5-(5-ізопропокси-3-піридиніл)-4-пентен-2аміну і g) необов'язково, перетворення гідроксибензоатної солі (2S)-(4E)-N-мeтил-5-(5-ізопропокси-3піридиніл)-4-пентен-2-аміну в (2S)-(4Е)-N-метил-5(5-ізопропокси-3-піридиніл)-4-пентен-2-амін. 9. Спосіб за п.8, де гідроксибензойна кислота являє собою о-, м- або п-гідроксибензойну кислоту. 10. Спосіб за п.8 або 9, де гідроксибензоатну сіль перетворюють в іншу фармацевтично прийнятну сольову форму. 11. Застосування композиції, яка містить сіль за будь-яким з пп.1-5, для одержання лікарського засобу, корисного для лікування розладу ЦНС. Harsing et al., J. Neurochem. 59: 48 (1993); Hughes, Proceedings from Intl. Symp. Nic. S40 (1994). Крім того, були припущення про нейрозахисну дію нікотину, див., наприклад, Sjak-shie et al., Brain Res. 624: 295 (1993). Також були запропоновані інші сприятливі фармакологічні ефекти. Див., наприклад, Decina et al., Biol. Psychiatry 28: 502 (1990); Wagner et al., Pharmacopsychiatry 21: 301 (1988); Pomerleau et al., Addictive Behaviors 9: 265 (1984); Onaivi et al., Life Sci. 54(3): 193 (1994); Tripathi et al., J. Pharmacol. Exp. Ther. 221: 91 (1982); Hamon, Trends in Pharmacol. Res. 15: 36 (1994). Повідомлялось про різні сполуки, мішенню для яких є nAChR (нікотинові ацетилхолінергічні рецептори), як корисні для лікування широкого ряду станів і розладів. Див., наприклад, Williams et al, DN&P 7(4): 205 (1994); Americ et al., CNS Drug Rev. 1(1): 1 (1995); Americ et al., Exp. Opin. Invest. Drug 5(1): 79 (1996); Bencherif et al., J. Pharmacol. Exp. Ther. 279: 1413 (1996); Lippiello et al., J. Pharmacol. Exp. Ther. 279: 1422 (1996); Damaj et al., J. Pharmacol. Exp. Ther. 291: 390 (1999); Chiari et al., Anesthesiology 91: 1447 (1999); Lavand'homme and Eisenbach, Anesthesiology 91: 1455 (1999); Holladay et al., J. Med. Chem. 40(28): 4169 (1997); Bannon et al., Science 279: 77 (1998); PCT WO 94/08992; PCT WO 96/31475; PCT WO 96/40682; і патенти США №№5583140, виданий на ім'я Bencherif et al.; 5597919, виданий на ім'я Dull et al.; 5604231, виданий на ім'я Smith et al.; і 5852041, виданий на ім'я 5 Cosford et al. Повідомлялось, що нікотинові сполуки є особливо корисними для лікування широкого ряду розладів ЦНС. Дійсно, різні нікотинові сполуки, як повідомлялось, володіють терапевтичними властивостями. Див, наприклад, Bencherif and Schmitt, Current Drag Targets: CNS and Neurological Disorders 1(4): 349-357 (2002), Levin and Rezvani, Current Drug Targets: CNS and Neurological Disorders 1(4): 423-431 (2002), O'Neill, et al. Current Drug Targets: CNS and Neurological Disorders 1(4): 399-411 (2002), патенти США №№5187166, виданий на ім'я Kikuchi et al., 5672601, виданий на ім'я Cignarella, PCT WO 99/21834 і PCT WO 97/40049, патентна заявка Великобританії GB 2295387 і європейська патентна заявка 297858. Розлади ЦНС є розладом неврологічного типу. Розлади ЦНС можуть бути індуковані лікарськими засобами; їх причиною може бути генетична схильність, інфекція або травма; або їх етіологія може бути невідомою. Розлади ЦНС включають нейропсихіатричні розлади, неврологічні захворювання і психічні захворювання, і включають нейродегенеративні захворювання, поведінкові розлади, когнітивні розлади і когнітивно-афективні розлади. Існують деякі розлади ЦНС, клінічний прояв яких віднесений до порушення функції ЦНС (тобто розлади, які є результатом невідповідних рівнів вивільнення нейротрансмітерів, невідповідних властивостей нейротрансмітерних рецепторів і/або невідповідної взаємодії між нейротрансмітерами і нейротрансмітерними рецепторами). Деякі розлади ЦНС можуть виникати за рахунок дефіциту ацетилхоліну, допаміну, норепінефрину і/або серотоніну. Відносно поширені розлади ЦНС включають пресенільну деменцію (ранній початок хвороби Альцгеймера), старечу деменцію (деменцію Альцгеймерового типу), мікроінфарктну деменцію, деменцію, пов'язану зі СНІДом, судинну деменцію, хворобу Creutzfeld-Jakob, хворобу Pick, Паркінсонізм, включаючи хворобу Паркінсона, деменцію за типом тільця Lewy, прогресивний супрануклеарний параліч, хорею Гентінгтона, пізню дискінезію, гіперкінезію, епілепсію, маніакальний синдром, розлад, пов'язаний з дефіцитом уваги, неспокій, легастенію, шизофренію, депресію, обсесивнокомпульсивний розлад і синдром Tourette. Підтипи nAChR присутні як в центральній, так і в периферичній нервовій системі, але розподіл цих підтипів гетерогенний. Наприклад, підтипи, які переважно присутні в головному мозку хребетних, являють собою α4β2, α7 і α3β2, тоді як підтипи, які переважно присутні у вегетативних гангліях, являють собою α3β4, а підтипи, присутні в невром'язовому синапсі являють собою α1β1dg і α1β1dε (див., наприклад Dwoskin et al., Exp. Opin. Ther. Patents 10: 1561 (2000); Schmitt and Bencherif, Annual Reports in Med. Chem. 35: 41 (2000)). Обмеження деяких нікотинових сполук пов'язане з тим, що вони викликають різні небажані фармакологічні ефекти внаслідок взаємодії з nAChR в периферичних тканинах (наприклад, шляхом стимуляції підтипів nAChR, присутніх в м'язах і гангліях). Тому існує потреба у сполуках, композиціях І способах профілактики і/або ліку 88792 6 вання різних станів або розладів (наприклад, розладів ЦНС), в тому числі для полегшення симптомів таких розладів, де сполуки виявляють нікотинову фармакологію зі сприятливим ефектом на nAChR ЦНС (наприклад, на функціонування ЦНС), але без яких-небудь суттєвих супутніх ефектів на периферичні nAChR (сполуки, специфічні у відношенні nAChR ЦНС). Також надзвичайно бажано одержати сполуки, композиції і способи, які впливають на функцію ЦНС, що не впливають при цьому істотним чином на ті підтипи рецепторів, які можуть викликати небажані побічні ефекти (наприклад, помітна дія у серцево-судинній і скелетном'язовій ділянках). Способи лікування і/або профілактики описаних вище станів і розладів шляхом введення Еметанікотинових1 сполук, особливо тих, які підсилюють вплив на функцію ЦНС, не впливаючи при цьому істотним чином на ті підтипи рецепторів, які можуть викликати небажані побічні дії, описані у відомому рівні техніки. Репрезентативні Еметанікотинові сполуки для застосування в лікуванні і/або профілактиці описаних вище розладів, розкриті, наприклад, у патенті US №5212188, виданому на ім'я Caldwell et al., патенті US №5604231, виданому на ім'я Smith et al., патенті US №5616707, виданому на ім'я Crooks et al.; патенті US №5616716, виданому на ім'я Dull et al., патенті US №5663356, виданому на ім'я Ruecroft et al., патенті US №5726316, виданому на ім'я Crooks et al., патенті US №5811442, виданому на ім'я Bencherif et al., патенті US №5861423, виданому на ім'я Caldwell et al., PCT WO 97/40011; РСТ WO 99/65876 РСТ WO 00/007600; і патентній заявці США серійний №09/391747, поданій 8 вересня 1999 року, при цьому зміст кожного з вказаних документів включений в дану заявку за допомогою посилання. Способи синтезу для одержання Еметанікотинових сполук, описані у відомому рівні техніки, звичайно включають здійснення реакції Гека (Heck) між галогензаміщеним гетероарильним кільцем, таким як галоген-піридин або галоген-піримідин, і сполукою, яка містить подвійний зв'язок. Сполука, яка містить подвійний зв'язок, типово включає або гідроксигрупу, яку перетворюють в аміногрупу з утворенням Е-метанікотину, або містить захищену аміногрупу, з якої знімають захист після реакції Гека з одержанням Еметанікотину. Обмеженням хімічної реакції поєднання Гека є той факт, що, хоча основним продуктом реакції є необхідний Е-метанікотин, утворюються другорядні продукти реакції, в тому числі Zметанікотин, метанікотинова сполука, де подвійний зв'язок перемістився з положення, суміжного з гетероарильним (таким як піридинове або піримідинове) кільцем (тобто незв'язаний подвійний зв'язок), і сполука, в якій гетероарильна група приєднана по вторинному (у протиставлення первинному) вуглецю алкену (тобто метиленова сполука або "екзо" подвійний зв'язок). Видалення таких другорядних продуктів реакції може бути ускладненим, особливо при великомасштабному синтезі. 7 Було б вигідним забезпечення нових способів одержання очищених Е-метанікотинових сполук, які, по суті, не містять описаних вище другорядних продуктів реакції. Також було б вигідним забезпечення нових форм солей цих лікарських засобів для поліпшення їх біодоступності, і/або сприяючих одержанню великих кількостей таких сполук розумним з комерційної точки зору способом. Даний винахід забезпечує такі нові способи синтезу і нові форми солей. В даній заявці описані нові способи синтезу Еметанікотинових сполук, а також нові фармацевтично прийнятні форми солей Е-метанікотинових сполук. Також розкриті фармацевтичні композиції, які містять нові форми солей, і способи лікування і/або профілактики із застосуванням нових форм солей. Способи синтезу Е-метанікотинових сполук типово включають стадію здійснення реакції Гека між галогензаміщеним гетероарильним кільцем, таким як галоген-піридин або галоген-піримідин, і сполукою, яка містить подвійний зв'язок. Сполука, яка містить подвійний зв'язок, типово містить або гідроксигрупу, яку потім перетворюють в аміногрупу з утворенням Е-метанікотинової сполуки, або містить захищену аміногрупу, з якої знімають захист після реакції Гека з утворенням Еметанікотинової сполуки. Після реакції Гека і утворення Е-метанікотину з вільною аміногрупою (або шляхом перетворення гідроксигрупи, або зняття захисту із захищеної аміногрупи) наступна стадія включає утворення гідроксибензоатної солі Е-метанікотинової сполуки. При певних умовах можна здійснити осадження гідроксибензоатної солі Е-метанікотинової сполуки з розчину, залишаючи при цьому в розчині другорядні продукти реакції у вигляді домішок (Zметанікотин і/або ізомери Е-метанікотинової сполуки, в яких подвійний зв'язок мігрував в положення, яке відрізняється від безпосередньо суміжного з гетероарильним кільцем, або в яких приєднання арильної групи до алкенового ланцюга має місце по вторинному вуглецю подвійного зв'язку). Таке поліпшення забезпечує відносно легке видалення таких другорядних продуктів реакції, особливо при великомасштабному виробництві. В одному варіанті здійснення винаходу синтез Е-метанікотинів включає утворення проміжної сполуки амінзахищеного 4-пентен-2-аміну і поєднання цієї проміжної сполуки через реакцію Гека з галогензаміщеним гетероарильним кільцем. Вибір гетероарильного кільця не є суттєвим для успішного здійснення реакції поєднання Гека, хоча піридинове і піримідинове кільця можуть бути переважними. (2S)-(4Е)-N-метил-5-[3-(5ізопропоксипіридин)іл)]-4-пентен-2-амін є типовим Е-метанікотином, п-гідроксибензоат є типовою гідроксибензоатною сіллю, і п-гідроксибензоат (2S)-(4Е)-N-метил-5-[3-(5-ізопропоксипіридин)іл)]4-пентен-2-аміну є типовою гідроксибензоатною сіллю Е-метанікотину. Приклад реакції представлений нижче: Су-галоген+CH2=CH-CH2CH(CH3)N(CH3)(Boc)® (E) Cy-CH=CH-CH2CH(CH3)N(CH3)(Boc) +(Ζ) Cy-CH=CH-CH2CH(CH3)N(CH3)(Boc) 88792 8 +(Ε і/або Ζ) Cy-CH2CH=CHCH(CH3)N(CH3)(Boc) +Cy-C(=CH2)-CH2CH(CH3)N(CH3)(Boc) де Су являє собою п'яти- або шести-членне гетероарильне кільце. В іншому варіанті здійснення винаходу реакцію поєднання Гека здійснюють із застосуванням гідроксіалкену, такого як 4-пентен-2-ол, і гідроксигрупу перетворюють в аміногрупу після здійснення реакції поєднання Гека. Перетворення можна здійснити, наприклад, шляхом перетворення гідроксигрупи в тозилат і заміщення тозилату придатним аміном, таким як метиламін. У цьому варіанті здійснення винаходу реакція поєднання Гека все ще утворює основні і другорядні продукти, за винятком випадків, коли вони включають гідроксигрупу, а не захищену аміногрупу. Після утворення амінвмісної сполуки (тобто (Е)-метанікотину), якщо домішки (тобто другорядні продукти реакції поєднання Гека) на цей момент ще не видалені, хімічні способи, що застосовуються для утворення гідроксибензоатних солей, по суті, ті ж самі. Після зняття захисту з аміногрупи (в першому варіанті здійснення винаходу) або утворення аміногрупи (у другому варіанті здійснення винаходу) може бути утворена гідроксибензоатна сіль Еметанікотину шляхом взаємодії з гідроксибензойною кислотою, як описано в даній заявці. Утворюються гідроксибензоатні солі основного продукту ((Е)-метанікотину) і другорядних продуктів. Однак в певних умовах гідроксибензоатна сіль основного продукту реакції, гідроксибензоатна сіль (Е)метанікотину, осаджується з розчину у відносно чистій формі, залишаючи вихідний розчин, збагачений другорядними продуктами реакції, присутніми у вигляді домішок. Такий результат є суттєвим просуванням в синтезі і очищенні (Е)метанікотинів. В одному варіанті здійснення винаходу гідроксибензоатні солі виділяють і потім застосовують у вигляді проміжних сполук з утворенням різних форм солей шляхом взаємодії з різними фармацевтично прийнятними кислотами або їх солями. Однак в іншому варіанті здійснення винаходу гідроксибензоатні солі Е-метанікотину застосовують як активні фармацевтичні інгредієнти (АРІ). Гідроксибензоатні солі можна застосовувати безпосередньо, або вони можуть бути включені у фармацевтичні композиції шляхом об'єднання їх з фармацевтично прийнятним ексципієнтом. Гідроксибензоатні солі і/або фармацевтичні композиції можна застосовувати для лікування і/або профілактики широкого ряду станів або розладів. Розлади, зокрема, являють собою ті розлади, які характеризуються порушенням функції нікотинової холінергічної нейротрансмісії, включаючи розлади, при яких відбувається нейромодуляція вивільнення нейротрансмітерів, наприклад, вивільнення допаміну. Сполуки можна застосовувати у способах лікування і/або профілактики розладів, таких як розлади центральної нервової системи (ЦНС), які характеризуються зміною нормального вивільнення нейротрансмітерів. Сполуки також можна застосовувати для лікування певних станів (наприклад, спосіб полегшення болю). Способи включають введення суб'єкту ефективної кількості 9 гідроксибензоатної солі Е-метанікотину або фармацевтичної композиції, яка містить гідроксибензоатну сіль Е-метанікотину, як описано в даній заявці. Фармацевтичні композиції, при їх застосуванні в ефективних кількостях, можуть взаємодіяти з відповідними ділянками нікотинових рецепторів в організмі пацієнта і діяти як терапевтичні і/або профілактичні засоби відносно широкого ряду станів і розладів, зокрема, розладів ЦНС, які характеризуються зміною нормального вивільнення нейротрансмітерів. Фармацевтичні композиції можуть забезпечувати терапевтичну користь суб'єктам, страждаючим від таких розладів, і у яких спостерігаються клінічні прояви таких розладів, що полягає в тому, що сполуки в таких композиціях, коли їх застосовують в ефективних кількостях, можуть (і) проявляти нікотинову фармакологію і впливати на відповідні ділянки нікотинових рецепторів (наприклад, активувати нікотинові рецептори), і (іі) модулювати виділення нейротрансмітерів і, отже, запобігати і придушувати симптоми, пов'язані з такими розладами. Крім того, сполуки можуть (і) збільшувати кількість нікотинових холінергічних рецепторів в головному мозку пацієнта, (іі) проявляти нейрозахисну дію і (ііі) при застосуванні в ефективних кількостях можуть демонструвати відносно низькі рівні несприятливих побічних дій (наприклад, значне підвищення кров'яного тиску і частоти серцевих скорочень, суттєва негативна дія на шлунковокишковий тракт і суттєва негативна дія на скелетні м'язи). Описані вище й інші аспекти даного винаходу детально пояснюються у представлених нижче докладному описі винаходу і прикладах. Гідроксибензоатні солі, описані в даній заявці, одержані з Е-метанікотинів і гідроксибензойних кислот, володіють багатьма перевагами у порівнянні з іншими солями, одержаними з Еметанікотинів та інших кислот. В основному, солі Е-метанікотинів з гідроксибензойними кислотами являють собою водорозчинні речовини, які в природі звичайно є високо кристалічними і менш гігроскопічними у порівнянні з іншими солями. Наприклад, п-гідроксибензоатна сіль (2S)-(4E)-Nметил-5-[3-(5-ізопропоксипіридин)іл)]-4-пентен-2аміну являє собою фізично і хімічно стабільний, вільнотекучий кристалічний порошок. Такі властивості представляють певні переваги для розробки фармацевтичних композицій і виробництва фармацевтичних засобів. Якщо необхідно, цю сіль можна подрібнити до прийнятних розмірів частинок для одержання фармацевтичних засобів. Ця сіль сумісна з широким рядом ексципієнтів, які можуть бути вибрані для виготовлення твердих пероральних лікарських форм. Це особливо стосується тих ексципієнтів, наприклад, похідних полісахаридів, які являють собою фармацевтично визначені гідрати, і тих, які містять лише слабо пов'язану на поверхні воду. Як ілюстрація, солі, одержані з деяких Е-метанікотинів, таких як Еметанікотин, і фумарової кислоти, схильні до утворення домішок всередині солі. Наприклад, домішки виникають внаслідок реакції приєднання по Міхаелю вторинного аміну в Е-метанікотині до 88792 10 олефіну у фумаровій кислоті. Такі домішки знижують хімічну чистоту солі і несприятливо впливають на хімічну цілісність солі при тривалому зберіганні. Способи синтезу, описані в даній заявці, будуть краще зрозумілі з представлених нижче переважних варіантів здійснення винаходу. Для визначення об'єму даного винаходу будуть застосовані наступні визначення: Як визначено в даній заявці, термін "ароматичний" стосується 3-10-, переважно, 5- і 6-членних ароматичних і гетероароматичних кілець. Як визначено в даній заявці, "групи, що містять ароматичну групу" стосуються фрагментів, які є або містять ароматичну групу. Відповідно, фенільна і бензильна групи включені в це визначення, оскільки обидві ці групи являють собою або містять ароматичну групу. Як визначено в даній заявці, термін "арил" стосується ароматичних радикалів, що містять від шести до десяти атомів вуглецю, таких як феніл, нафтил і т.п.; "заміщений арил" стосується арильних радикалів, що додатково містять одну або декілька груп замісників, визначених в даній заявці. Як визначено в даній заявці, термін "алкіларил" стосується алкілзаміщених арильних радикалів; "заміщений алкіларил" стосується алкіларильних радикалів, що додатково містять одну або декілька груп замісників, визначених в даній заявці; "арилалкіл" стосується арилзаміщених алкільних радикалів; і "заміщений арилалкіл" стосується арилалкільних радикалів, що додатково містять одну або декілька груп замісників, визначених в даній заявці. Як визначено в даній заявці, С1-6алкільні радикали (нижчі алкільні радикали) містять від 1 до 6 атомів вуглецю в лінійному або розгалуженому ланцюгу, і також містять С3-6циклоалкільні групи і алкільні радикали, які містять С3-6циклоалкільні групи. Як визначено в даній заявці, термін "алкеніл" стосується вуглеводневих радикалів з лінійним або розгалуженим ланцюгом, включаючи С1-8, переважно, С1-5, і що містить щонайменше один вуглець-вуглецевий подвійний зв'язок; "заміщений алкеніл" стосується алкенільних радикалів, що додатково містять одну або декілька груп замісників, визначених в даній заявці. Як визначено в даній заявці, С16алкоксирадикали містять від 1 до 6 атомів вуглецю в лінійному або розгалуженому ланцюгу, а також містять С3-6циклоалкільні і алкоксирадикали, які містять С3-6циклоалкільні групи. Як визначено в даній заявці, арильні радикали вибрані з фенілу, нафтилу та інденілу. Як визначено в даній заявці, циклоалкільні радикали являють собою насичені або ненасичені радикали, які містять циклічне кільце, що містять від трьох до восьми атомів вуглецю, переважно, від трьох до шести атомів вуглецю; "заміщений циклоалкіл" стосується циклоалкільних радикалів, що додатково містять одну або декілька груп замісників, визначених в даній заявці. Як визначено в даній заявці, галоген являє собою хлор, йод, фтор або броми. 11 Як визначено в даній заявці, гетероарильні радикали містять від 3 до 10 членів, переважно, 5 або 6 членів, включаючи один або декілька гетероатомів, вибраних з кисню, сірки і азоту. Приклади придатних 5-членних кільцевих гетероарильних груп являють собою фурил, піроліл, імідазоліл, оксазоліл, тіазоліл, тієніл, тетразоліл і піразоліл. Приклади придатних 6-членних кільцевих гетероарильних груп являють собою піридиніл, піримідиніл і піразиніл, з яких піридиніл і піримідиніл є переважними. Як визначено в даній заявці, "гетероцикліл" стосується насичених або ненасичених циклічних радикалів, які містять один або декілька гетероатомів (наприклад, О, N, S) як частину кільцевої структури, і які містять від двох до семи атомів вуглецю в кільці; "заміщений гетероцикліл" стосується гетероциклільних радикалів, які додатково містять одну або декілька груп замісників, визначених в даній заявці. Приклади придатних гетероциклільних груп являють собою, але не обмежені цим, піперидиніл, морфолініл, піролідиніл, імідазолідиніл, піразолідиніл, ізотіазолідиніл, тіазолідиніл, ізоксазолідиніл, оксазолідиніл, піперазиніл, тетрагідропіраніл і тетрагідрофураніл. Як визначено в даній заявці, поліциклоалкільні радикали являють собою сконденсовані циклічні кільцеві структури. Типові поліциклоалкільні радикали являють собою, але не обмежені цим, адамантил, борнаніл, норборнаніл, борненіл і норборненіл. Поліциклоалкільні радикали можуть також містити один або декілька гетероатомів, таких як Ν, Ο або S. Як визначено в даній заявці, циклоалкільні радикали містять від 3 до 8 атомів вуглецю. Приклади відповідних циклоалкільних радикалів являють собою, але не обмежені цим, циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил, і циклооктил. Як визначено в даній заявці, ітермін "заміщений", як він використаний з будь-яким з вказаних вище термінів, означає присутність одного, двох або трьох замісників, таких як алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, гетероцикліл, заміщений гетероцикліл, циклоалкіл, заміщений циклоалкіл, арил, заміщений арил, алкіларил, заміщений алкіларил, арилалкіл, заміщений арилалкіл, F, СІ, Br, I, NR'R", CF3, CN, NO2, C2R', SH, SCH3, N3, SO2CH3, OR', (CR'R")qOR', O(CR'R")qC2R', SR', C(=O)NR'R'', NR'C(=O)R", C(=O)R', C(=O)OR, OC(=O)R', (CR'R")qOCH2C2R', (CR'R")qC(=O)R', (CR'R")qC2(CHCH3)OR', O(CR'R")qC(=O)OR', (CR'R")qC(=O)NR'R", (CR'R")qNR'R", CH=CHR', OC(=O)NR'R" і NR'C(=O)OR", де q являє собою ціле число, що має значення від 1 до 6, і R' і R", кожний незалежно являє собою водень або алкіл (наприклад, С110алкіл, переважно, С1-5алкіл і, більш переважно, метил, етил, ізопропіл, третинний бутил або ізобутил), циклоалкіл (наприклад, циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил і адамантил), неароматичне гетероциклічне кільце, де гетероатом гетероциклічного фрагмента відділений від якого-небудь іншого атома азоту, кисню або сірки щонайменше двома атомами вуглецю 88792 12 (наприклад, хінуклідиніл, піролідиніл і піперидиніл), групи, що містять ароматичну групу (наприклад, піридиніл, хінолініл, піримідиніл, фураніл, феніл і бензил, де будь-який з вищезгаданих може бути відповідним чином заміщений щонайменше однією групою замісників, таких як замісники алкіл, гідроксил, алкоксил, галоген або аміно). Як визначено в даній заявці, термін "агоніст" означає речовину, яка стимулює партнера, з яким зв'язується, типово - рецептор. Стимуляція визначається в контексті конкретного аналізу або може бути очевидною з того, що обговорюється в даному описі при порівнянні з фактором або речовиною, яка прийнята як "агоніст" або "антагоніст" конкретного партнера, що зв'язується з ним, у, по суті, однакових умовах, як повинно бути зрозуміло фахівцям в даній галузі. Стимуляцію можна визначити за посиленням конкретної дії або функції, що індукується шляхом взаємодії агоніста або часткового агоніста з партнером, з яким він зв'язується, і може містити алостеричні дії. Як визначено в даній заявці, термін "антагоніст" означає речовину, яка інгібує партнера, з яким зв'язується, типово - рецептор. Інгібування визначається в контексті конкретного аналізу або може бути очевидним з того, що обговорюється в даному описі при порівнянні з фактором або речовиною, яка прийнята як "агоніст" або "антагоніст" конкретного партнера, що зв'язується з ним, у, по суті, однакових умовах, як повинно бути зрозуміло фахівцям в даній галузі. Інгібування можна визначити за ослабленням конкретної дії або функції, що індукується шляхом взаємодії антагоніста з партнером, з яким він зв'язується, і може містити алостеричні дії. Як визначено в даній заявці, термін "частковий агоніст" означає речовину, яка забезпечує певний рівень стимуляції свого партнера зі зв'язування, який є проміжним між тим, який забезпечується повним або довершеним антагоністом і агоністом, що визначається за допомогою будь-якого прийнятого стандарту визначення агоністичної активності. Повинно бути зрозуміло, що стимуляцію, а отже, й інгібування визначають як, по суті, характерні для якої-небудь речовини або класу речовин, що підлягає визначенню, чи є вони агоністами, антагоністами або частковими агоністами. Як визначено в даній заявці, "характеристична активність", або "ефективність", стосується деякої міри біологічної ефективності комплексу партнерів, що зв'язуються. Відносно фармакології рецепторів контекст, в якому потрібно визначати характеристичну активність або ефективність, буде залежати від контексту комплексу партнерів (наприклад, рецептор/ліганд), що зв'язуються, і розгляду активності відносно конкретного біологічного результату. Наприклад, у деяких обставинах, характеристична активність може варіювати, в залежності від другої посередницької системи, що бере участь. Див. Hoyer, D. і Boddeke, Η., Trends Pharmacol Sci. 14(7): 270-5 (1993). Коли є доречними такі специфічні для певного контексту оцінки, і яким чином вони можуть відповідати в контексті даного винаходу, це повинне бути очевидним для фахівців в даній галузі. 13 Як визначено в даній заявці, нейротрансмітери, вивільнення яких опосередковане сполуками, описаними в даній заявці, являють собою, але не обмежені цим, ацетилхолін, допамін, норепінефрин, серотонін і глутамат, і сполуки, описані в даній заявці, функціонують як агоністи або часткові агоністи на одному або декількох nAChR центральної нервової системи (ЦНС). І. Сполуки Сполуки, описані в даній заявці, являють собою гідроксибензоатні солі сполук (Е)метанікотинового типу. А. Гідроксибензойні кислоти Гідроксибензойні кислоти, які можна застосовувати для одержання гідроксибензоатних солей сполук (Е)-метанікотинового типу, мають наступну загальну формулу: де гідроксигрупа може бути присутньою в орто-, мета- або пара-положенні відносно карбоновокислотної групи, Ζ являє собою неводневий замісник, і j означає число від нуля до трьох, яке являє собою кількість замісників Z, які можуть бути присутніми в кільці. Приклади придатних замісників Ζ являють собою алкіл, заміщений алкіл, алкеніл, заміщений алкеніл, гетероцикліл, заміщений гетероцикліл, циклоалкіл, заміщений циклоалкіл, арил, заміщений арил, алкіларил, заміщений алкіларил, арилалкіл, заміщений арилалкіл, F, СІ, Br, I, NR'R", CF3, CN, NO2, C2R', SH, SCH3, N3, SO2CH3, OR', (CR'R")qOR', O-(CR'R")qC2R', SR', C(=O)NR'R", NR'C(=O)R", C(=O)R', C(=O)OR', OC(=O)R, (CR'R")qOCH2C2R', (CR'R")qC(=O)R', (CR'R")qC2(CHCH3)OR', O(CR'R")qC(=O)OR', (CR'R")qC(=O)NR'R", (CR'R")qNR'R", CH=CHR', OC(=O)NR'R" і NR'C(=O)OR", де q являє собою ціле число, що має значення від 1 до 6, і R' і R", кожний незалежно являє собою водень або алкіл (наприклад, С1-10алкіл, переважно, С1-5алкіл і, більш переважно, метил, етил, ізопропіл, третинний бутил або ізобутил), циклоалкіл (наприклад, циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил і адамантил), неароматичне гетероциклічне кільце, де гетероатом гетероциклічного фрагмента відділений від якого-небудь іншого атома азоту, кисню або сірки щонайменше двома атомами вуглецю (наприклад, хінуклідиніл, піролідиніл і піперидиніл), групи, які містять ароматичну групу (наприклад, піридиніл, хінолініл, піримідиніл, фураніл, феніл і бензил, де будь-яка з вищеперелічених груп може бути відповідним чином заміщена щонайменше однією групою замісників, таких як замісники алкіл, гідроксил, алкоксил, галоген або аміно). Інші типові ароматичні кільцеві системи описані в Gibson et al., J. Med. Chem. 39:4065 (1996). R' і R" можуть являти собою лінійний або розгалужений алкіл, або R' і R" і проміжні атоми можуть об'єднуватись з утворенням кільцевої структури (наприклад, циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил, адамантил або хінуклідиніл). Гідроксибензойні кислоти можуть бути необов'язково заміщені хіра 88792 14 льною функціональною групою, що може сприяти очищенню Е-метанікотинів, які містять хіральний вуглець, шляхом утворення діастереомерів. Типові бензойні кислоти, які можна застосовувати, включають саліцилову кислоту, метагідроксибензойну кислоту, пара-гідроксибензойну кислоту, ванілінову кислоту, ізованілінову кислоту, гентизинову кислоту, галову кислоту, 5аміносаліцилову кислоту, бузкову кислоту, 4метилсаліцилову кислоту, З-хлор-4-оксибензойну кислоту і 5-гідроксіізофталеву кислоту. В. Е-метанікотини Е-метанікотинові сполуки являють собою сполуки формули: де: Су являє собою 5- або 6-членне гетероарильне кільце, Ε і Е', кожний незалежно являє собою водень, алкіл, заміщений алкіл, галогензаміщений алкіл, циклоалкіл, заміщений циклоалкіл, гетероцикліл, заміщений гетероцикліл, арил, заміщений арил, алкіларил, заміщений алкіларил, арилалкіл або заміщений арилалкіл; Ζ' і Ζ", кожний незалежно являє собою водень або алкіл (включаючи циклоалкіл), і переважний щонайменше один з Ζ' і Ζ" являє собою водень і, найбільш переважно, Ζ' являє собою водень, a Z" являє собою метил; альтернативно, Ζ', Ζ" і пов'язаний з ними атом азоту можуть утворювати кільцеву структуру, таку як азиридиніл, азетидиніл, піролідиніл, піперидиніл, піперазиніл, морфолініл, і обидві групи Ε подвійного зв'язку, переважно, являють собою водень, і m має значення 1, 2, 3, 4, 5 або 6. В одному варіанті здійснення винаходу всі групи Ε і Е' являють собою водень, а в іншому варіанті здійснення винаходу щонайменше одна з груп Ε або Е1 являє собою алкіл, а інші групи Ε і Е' являють собою водень. У переважному варіанті здійснення винаходу Е' являє собою алкільну групу, переважно, метильну групу. Ізомери, суміші, включаючи рацемічні суміші, енантіомери, діастереомери і таутомери цих сполук, а також їх фармацевтично прийнятні солі також входять в об'єм даного винаходу. В одному варіанті здійснення винаходу Су являє собою шестичленний кільцевий гетероарил, який має формулу: де кожний з X, X', X", X'" і X''" незалежно являє собою азот, азот, пов'язаний з киснем (наприклад, N-оксид або функціональна група N-O), або вуглець, пов'язаний з Η або групою неводневого замісника. Не більше трьох з X, X', X", X"' і X"" можуть являти собою азот або азот, пов'язаний з киснем, і переважно, щоб тільки один або два з X, X', X", X'" і X"" являли собою азот або азот, пов'язаний з ки 15 снем. Крім того, особливо переважно, щоб не більше одного з X, X', X", X'" і X"" являв собою азот, пов'язаний з киснем; і переважно, щоб у випадку, коли один з вказаних замісників являє собою азот, пов'язаний з киснем, цей замісник являв собою X'". Найбільш переважно, коли X'" являє собою азот. У певних переважних обставинах X' і X'", обидва являють собою азот. Типово, X, X" і X"" являють собою вуглець, пов'язаний з групою замісника, і типово, коли замісники у X, X" і X''" являють собою водень. Для деяких інших переважних сполук, де X"' являє собою вуглець, пов'язаний з групою замісника, такою як водень, X і X', обидва являють собою азот. У деяких інших переважних сполуках, де X' являє собою вуглець, пов'язаний з групою замісника, такою як водень, X і X'", обидва являють собою азот. Придатні неводневі замісники визначені вище при описі Ζ. В іншому варіанті здійснення винаходу Су являє собою 5-членний кільцевий гетероарил, що має формулу: де Υ і Υ", кожний незалежно являє собою азот, азот, пов'язаний з групою замісника, кисень, сірку або вуглець, пов'язаний з групою замісника, і Υ' і Υ'" являють собою азот або вуглець, пов'язаний з групою замісника. Пунктирні лінії означають, що зв'язки (між Υ і Y' і між Υ' і Υ") можуть бути або простими, або подвійними зв'язками. Однак, коли зв'язок між Υ і Υ' являє собою простий зв'язок, зв'язок між Υ і Υ" повинен являти собою подвійний зв'язок, і навпаки. У випадках, коли Υ або Υ" являє собою кисень або сірку, тільки один з Υ і Υ" може являти собою або кисень, або сірку. Щонайменше один з Υ, Υ', Υ" і Υ"' повинен являти собою кисень, сірку, азот або азот, пов'язаний з групою замісника. Переважно, щоб не більше трьох з Υ, Υ', Υ" і Υ'" являли собою кисень, сірку, азот або азот, пов'язаний з групою замісника. Крім того, переважно, щоб щонайменше один, але не більше трьох, з Υ, Υ', Υ" і Υ'" являли собою азот. Групи замісників у X, X', Χ", Χ"', Χ"", Υ, Υ', Υ" і Υ'", коли вони знаходяться у суміжному положенні, можуть об'єднуватись з утворенням одного або декількох насичених або ненасичених, заміщених або незаміщених карбоциклічних або гетероциклічних кілець, що містять, іале не обмеженими цим, такі функціональні групи, як простий ефір, ацеталь, кеталь, амін, кетон, лактон, лактам, карбамат або сечовина. В залежності від природи і положення кожного окремого Ε і E', деякі сполуки можуть бути оптично активними (наприклад, сполуки можуть мати один або декілька хіральних центрів з R- або Sконфігурацією). Даний винахід стосується рацемічних сумішей таких сполук, а також окремих енантіомерних сполук. Особливий інтерес представляють арилзаміщені амінові сполуки формули: 88792 16 де Χ', Ε, Ε', Ζ', Ζ" і m визначені вище, і А, А' і А" являють собою водень або групу замісників Z, визначену вище при описі гідроксибензойних кислот. Переважно, всі Ε являють собою водень, і Е' являє собою алкіл, переважно, метил. Переважно, Ζ' являє собою водень, і Ζ" являє собою водень або метил. Переважно, m має значення 1 або 2. Прикладами арилзаміщених амінових сполук є сполуки, описані в патенті US №5212188, виданому на ім'я Caldwell et al.; патенті US №5604231, виданому на ім'я Smith et al.; патенті US №5616707, виданому на ім'я Crooks et al.; патенті US №5616716, виданому на ім'я Dull et al.; патенті US №5663356, виданому на ім'я Ruecroft et al.; патенті US №5726316, виданому на ім'я Crooks et al.; патенті US №5811442, виданому на ім'я Bencherif et al.; патенті US №5861423, виданому на ім'я Caldwell et al.; патенті US №6337351, виданому на ім'я Dull et al.; WO 97/40011; WO 99/65876; і WO 00/007600. Перераховані вище посилальні документи включені в дану заявку за допомогою посилання у всій їх повноті з метою розкриття типових сполук, прийнятних для здійснення даного винаходу. Приклади сполук, прийнятних відповідно до даного винаходу, являють собою сполуки метанікотинового типу. Типові переважні сполуки являють собою (Е)-метанікотин, (3Е)-N-метил-4-(5етокси-3-піридиніл)-3-бутен-1-амін, (2S)-(4E)-Nметил-5-(3-піридиніл)-4-пентен-2-амін, (2R)-(4Е)-Nметил-5-(3-тридиніл)-4-пентен-2-амін, (2S)-(4Е)-Nметил-5-(5-метокси-3-піридиніл)-4-пентен-2-амін, (2R)-(4Е)-N-метил-5-(5-метокси-3-піридинІл)-4пентен-2-амін, (2S)-(4E)-N-метил-5-(5-ізопропокси3-піридиніл)-4-пентен-2-амін, (2R)-(4Е)-N-метил-5(5-ізопропокси-3-піридиніл)-4-пентен-2-амін, (3Е)N-метил-4-(5-нітро-6-аміно-3-піридиніл)-3-бутен-1амін, (3Е)-N-метил-4-(5-(N-бензилкарбоксамідо)-3піридиніл)-3-бутен-1-амін, (2S)-(4Е)-N-метил-5-(5піримідиніл)-4-пентен-2-амін, (2R)-(4Е)-N-метил-5(5-піримідиніл)-4-пентен-2-амін, (4Е)-N-метил-5-(2аміно-5-піримідиніл)-4-пентен-2-амін, (4Е)-Nметил-5-(5-аміно-3-піридиніл)-4-пентен-2-амін, (2S)-(4E)-N-метил-5-(5-ізопропокси-1-оксо-3піридиніл)-4-пентен-2-амін, (3Е)-N-метил-4-(5ізобутокси-3-піридиніл)-3-бутен-1-амін, (3Е)-Nметил-4-(1-оксо-3-піридиніл)-3-бутен-1-амін, (4Е)N-метил-5-(1-оксо-3-піридиніл)-4-пентен-2-амін, (3Е)-N-метил-4-(5-етилтіо-3-піридиніл)-3-бутен-1амін, (4Е)-N-метил-5-(5-трифторметил-3піридиніл)-4-пентен-2-амін, (4Е)-N-метил-5-(5((карбоксиметил)окси)-3-піридиніл)-4-пентен-2амін, (4Е)-5-(5-ізопропокси-3-піридиніл)-4-пентен2-амін і (4Е)-N-метил-5-(5-пдрокси-3-піридиніл)-4пентен-2-амін. Додаткові типові приклади являють собою (2S)-(4E)-N-метил-5-(5-циклогексилокси-3піридиніл)-4-пентен-2-амін, (2R)-(4Е)-N-метил-5-(5циклогексилокси-3-піридиніл)-4-пентен-2-амін, (2S)-(4Е)-N-метил-5-(5-фенокси-3-піридиніл)-4 17 пентен-2-амін, (2R)-(4Е)-N-метил-5-(5-фенокси-3піридиніл)-4-пентен-2-амін, (2S)-(4Е)-N-метил-5-(5(4-фторфенокси)-3-піридиніл)-4-пентен-2-амін, (2R)-(4Е)-N-метил-5-(5-(4-фторфенокси)-3піридиніл)-4-пентен-2-амін, (2S)-(4Е)-N-метил-5-(5(4-хлорфенокси)-3-піридиніл)-4-пентен-2-амін, (2R)-(4E)-N-метил-5-(5-(4-хлорфенокси)-3піридиніл)-4-пентен-2-амін, (2S)-(4Е)-N-метил-5-(5(3-ціанофенокси)-3-піридиніл)-4-пентен-2-амін, (2R)-(4E)-N-метил-5-(5-(3-ціанофенокси)-3піридиніл)-4-пентен-2-амін, (2S)-(4Е)-N-метил-5-(5(5-индолилокси)-3-піридиніл)-4-пентен-2-амін і (2R)-(4E)-N-метил-5-(5-(5-индолилокси)-3піридиніл)-4-пентен-2-амін. II. Одержання сполук Спосіб, за допомогою якого синтезують сполуки (Е)-метанікотинового типу, описані в даній заявці, може варіювати. Наприклад, сполуки можна одержати шляхом каталізованої паладієм реакції поєднання ароматичного галогеніду і кінцевого олефіну, що містить захищений аміновий замісник, зняття захисної групи з одержанням первинного або вторинного аміну і необов'язкового алкілування з одержанням вторинного або третинного аміну. Зокрема, деякі сполуки метанікотинового типу можна одержати, піддаючи 3-галогензаміщену, необов'язково 5-заміщену, піридинову сполуку або 5галогензаміщену піримідинову сполуку каталізованій паладієм реакції поєднання із застосуванням олефіну, що містить захищену функціональну групу аміну (наприклад, такого олефіну, як одержаний взаємодією фталімідної солі з 3-галоген-1пропеном, 4-галоген-1-бутеном, 5-галоген-1пентеном або 6-галоген-1-гексеном). Див., Frank et al., J. Org. Chem., 43(15): 2947-2949 (1978); і Malek et al., J. Org. Chem., 47: 5395-5397 (1982). В іншому варіанті здійснення винаходу сполуки синтезують шляхом конденсації спирту олефінового ряду, такого як 4-пентен-2-ол, з ароматичною галогензаміщеною сполукою, такою як 3бромпіридин або 3-йодпіридин. Типово, застосовують способи, описані в Frank et al., J. Org. Chem., 43: 2947-2949 (1978), і Malek et al., J. Org. Chem., 47: 5395-5397 (1982), які включають каталізоване паладієм поєднання олефіну і ароматичної галогензаміщеної сполуки. Спирт олефінового ряду необов'язково може бути захищений у вигляді простого трет-бутилдиметилсилілового ефіру до реакції поєднання. Потім десилілування дає спирт олефінового ряду. Потім продукт конденсації спирту перетворюють в амін із застосуванням способів, аналогічних і описаним в deCosta et al., J. Org. Chem., 35: 4334-4343 (1992). Типово, продукт конденсації спирту перетворюють в арилзаміщений олефіновий амін шляхом активації спирту із застосуванням метансульфонілхлориду або птолуолсульфонілхлориду, з подальшим заміщенням мезилату або тозилату, застосовуючи аміак або первинний або вторинний амін. Таким чином, коли амін являє собою аміак, одержують сполуки арилзаміщеного олефінового первинного аміну; коли амін являє собою первинний амін, такий як метиламін або циклобутиламін, одержують сполуки арилзаміщеного олефінового вторинного аміну; і коли амін являє собою вторинний амін, такий як 88792 18 диметиламін або піролідин, одержують сполуки арилзаміщеного олефінового третинного аміну. Інші типові спирти олефінового ряду являють собою 4-пентен-1-ол, 5-гексен-2-ол, 5-гексен-3-ол, Зметил-3-бутен-1-ол, 2-метил-3-бутен-1-ол, 4метил-4-пентен-1-ол, 4-метил-4-пентен-2-ол, 1октен-4-ол, 5-метил-1-гептен-4-ол, 4-метил-5гексен-2-ол, 5-метил-5-гексен-2-ол, 5-гексен-2-ол і 5-метил-5-гексен-3-ол. Трифторметилзаміщені спирти олефінового ряду, такі як 1,1,1-трифтор-4-пентен-2-ол, можна одержати з 1-етокси-2,2,2-трифторетанолу і алілтриметилсилану із застосуванням способів, описаних Kubota et al., Tetrahedron Letters, 33(10): 13511354 (1992), або зі складного етилового ефіру трифтороцтової кислоти і алілтрибутилстанану із застосуванням способів, описаних в Ishihara et al., Tetrahedron Letters, 34(56): 5777-5780 (1993). Деякі спирти олефінового ряду є оптично активними, і їх можна застосовувати у вигляді енантіомерних сумішей або у вигляді чистих енантіомерів, щоб одержати відповідні оптично активні форми сполук арилзаміщених олефінових амінів. Коли аліліловий спирт олефінового ряду, такий як металіловий спирт, піддають взаємодії з ароматичною галогензаміщеною сполукою, одержують арилзаміщений олефіновий альдегід; і одержаний альдегід може бути перетворений у сполуку арилзаміщеного олефінового аміну шляхом відновного амінування (наприклад, шляхом обробки з використанням алкіламіну і ціаноборгідриду натрію). Переважними ароматичними галогензаміщеними сполуками є сполуки 3-бромпіридинового типу і сполуки 3йодпіридинового типу. Типово, групи замісників таких сполук 3-галогенпіридинового типу являють собою групи, які можуть витримати контакт з такими хімічними продуктами (наприклад, тозилхлоридом і метиламіном) і реакційні умови, що використовуються для одержання сполуки арилзаміщеного олефінового аміну. Альтернативно, замісники, такі як -ОН, -NH2 і SH, можуть бути захищені як відповідні ацильні сполуки, або замісники, такі як -NH2, можуть бути захищені як фталімідна функціональна група. У випадку дигалогенароматичної сполуки, можливі послідовні каталізовані паладієм (по типу Гека) поєднання з двома різними олефіновими бічними ланцюгами. В одному варіанті здійснення винаходу сполуки (Е)-метанікотинового типу містять розгалужений бічний ланцюг, наприклад, (4Е)-N-метил-5-(5ізопропокси-3-піридиніл)-4-пентен-2-амін. Застосовуючи один синтетичний підхід, згадана останньою сполука може бути синтезована конвергентним способом, в якому бічний ланцюг, N-метил-N(трет-бутоксикарбоніл)-4-пентен-2-амін, з'єднують із 3-заміщеним 5-галогензаміщеним піридином, 5бром-3-ізопропоксипіридином, в умовах реакції Гека, з подальшим видаленням третбутоксикарбонільної захисної групи. Типово, застосовують способи, аналогічні описаним в W. С Frank et al., J. Org. Chem. 43: 2947 (1978) and N. J. Malek et al., J. Org. Chem. 47:5395 (1982), що включають каталізоване паладієм поєднання олефіну і ароматичної галогензаміщеної сполуки. Необхідний N-метил-N-(трет-бутоксикарбоніл)-4 19 пентен-2-амін може бути синтезований таким чином: (і) комерційно доступний 4-пентен-2-ол (Aldrich Chemical Company, Lancaster Synthesis Inc.) може бути оброблений птолуолсульфонілхлоридом в піридині з одержанням п-толуолсульфонату 4-пентен-2-олу, раніше описаного Т. Michel, et al., Liebigs Ann. 11: 1811 (1996); (ii) одержаний тозилат можна піддати нагріванню з надмірною кількістю метиламіну з одержанням N-метил-4-пентен-2-аміну; (ііі) можна здійснити взаємодію одержаного аміну, такого як описаний раніше A. Viola et al., J. Chem. Soc, Chem. Commun. 21: 1429 (1984), з 1,2 молярного еквівалента ди-трет-бутилдикарбонату в безводному тетрагідрофурані з одержанням бічного ланцюга, N-метил-N-(трет-бутоксикарбоніл)-4-пентен2-аміну. Галогензаміщений піридин (наприклад, 5бром-3-ізопропоксипіридин), може бути синтезований щонайменше двома різними шляхами. В одному способі одержання 3,5-дибромпіридин нагрівають при 140°С протягом 14 годин з 2 молярними еквівалентами ізопропоксиду калію в безводному ізопропанолі у присутності мідного порошку (5% мас/мас. 3,5-дибромпіридину) в герметично закритій скляній пробірці з одержанням 5-бром-3ізопропоксипіридину. Другий спосіб одержання 5бром-3-ізопропоксипіридину з 5-бромнікотинової кислоти можна здійснити таким чином: (і) 5бромнікотинову кислоту перетворюють в 5бромнікотинамід шляхом обробки тіонілхлоридом з подальшою взаємодією проміжної сполуки хлорангідриду кислоти з водним розчином аміаку; (іі) одержаний 5-бромнікотинамід, раніше описаний С. V. Greco et al., J. Heterocyclic Chem. 7(4): 761 (1970), піддають розщепленню по Гофману шляхом обробки гідроксидом натрію і 70% розчином гіпохлориту кальцію; (ііі) одержаний З-аміно-5бромпіридин, раніше описаний С V. Greco et al., J. Heterocyclic Chem. 7(4): 761 (1970), може бути перетворений в 5-бром-3-ізопропоксипіридин шляхом діазотування з використанням ізоамілнітриту в кислотних умовах, з подальшою обробкою проміжної сполуки - діазонієвої солі -ізопропанолом з одержанням 5-бром-3-ізопропоксипіридину. Каталізоване паладієм поєднання 5-бром-3ізопропоксипіридину і N-метил-N-(третбутоксикарбоніл)-4-пентен-2-аміну здійснюють в ацетонітрилі-триетиламіні (2:1, об./об.) з використанням каталізатора, що складається з 1моль.% ацетату паладію(II) і 4моль.% три-о-толілфосфіну. Реакцію можна здійснити шляхом нагрівання компонентів при 80°С протягом 20 годин з одержанням (4Е)-N-метил-N-(трет-бутоксикарбоніл)-5-(5ізопропокси-3-піридиніл)-4-пентен-2-аміну. Видалення трет-бутоксикарбонільної захисної групи можна здійснити шляхом обробки 30 молярними еквівалентами трифтороцтової кислоти в анізолі при 0°С з одержанням (4Е)-N-метил-5-(5ізопропокси-3-піридиніл)-4-пентен-2-аміну. Різні Nметил-5-(5-алкокси або 5-арилокси-3-піридиніл)-4пентен-2-аміни можна одержати з 3,5дибромпіридину із застосуванням такого типу технології (тобто обробки алкоксидами або арилоксидами натрію або калію з подальшим поєднанням по Геку і зняттям захисту). 88792 20 В іншому варіанті здійснення винаходу сполука, така як (4Е)-N-метил-5-(5-метокси-3-піридиніл)4-пентен-2-амін, може бути синтезована шляхом поєднання галогензаміщеного піридину, 5-бром-3метоксипіридину, з олефіном, що містить функціональну групу вторинного спирту, 4-пентен-2-олу, в умовах реакції Гека; і одержана проміжна сполука піридинілового спирту може бути перетворена в її п-толуолсульфонатний ефір з подальшою обробкою метиламіном. Типово, застосовують способи, аналогічні описаним в W. С. Frank et al., J. Org. Chem. 43: 2947 (1978) and N. J. Malek et al., J. Org. Chem. 47: 5395 (1982), що включають каталізоване паладієм поєднання олефіну і ароматичної галогензаміщеної сполуки. Галогензаміщений піридин, 5-бром-3-метоксипіридин, синтезують способом, аналогічним описаному в Н. J. den Hertog et al., Reel. Trav. Chim. Pays-Bas 67: 377 (1948), а саме, шляхом нагрівання 3,5-дибромпіридину з 2,5 молярного еквівалента метоксиду натрію в безводному метанолі у присутності мідного порошку (5% мас/мас. 3,5-дибромпіридину) в герметично закритій скляній пробірці при 150°С протягом 14 годин з одержанням 5-бром-3-метоксипіридину. Одержаний 5-бром-3-метоксипіридин, раніше описаний D. L. Comins, et al., J. Org. Chem. 55: 69 (1990), можна піддати поєднанню з 4-пентен-2-олом в ацетонітрилі-триетиламіні (1:1, об./об.) з використанням каталізатора, що складається з 1моль.% ацетату паладію(II) і 4моль.% три-о-толілфосфіну. Реакцію здійснюють шляхом нагрівання компонентів в герметично закритій скляній пробірці при 140°С протягом 14 годин з одержанням (4Е)-N-метил-5-(5метокси-3-тридиніл)-4-пентен-2-олу. Одержаний спирт обробляють 2 молярними еквівалентами птолуолсульфонілхлориду в безводному піридині при 0°С з одержанням п-толуолсульфонату (4Е)-Nметил-5-(5-метокси-3-піридиніл)-4-пентен-2-олу. Проміжний тозилат обробляють 120 молярними еквівалентами метиламіну у вигляді 40% водного розчину, що містить невелику кількість етанолу як співрозчинника, з одержанням (4Е)-N-метил-5-(5метокси-3-піридиніл)-4-пентен-2-аміну. Коли 3,5дибромпіридин піддають поєднанню по Геку з Nметил-N-(трет-бутоксикарбоніл)-4-пентен-2-аміном в умовах, описаних вище, одержують N-метил-N(трет-бутоксикарбоніл)-5-(5-бром-3-піридиніл)-4пентен-2-амін. Цю сполуку можна піддати поєднанню в подальшій реакції Гека зі стиролом зі зняттям захисту (видалення третбутоксикарбонільної групи), як описано вище, з одержанням (4Е)-N-метил-5-[3-(5-транс-бетастирилпіридин)іл]-4-пентен-2-аміну. Аналогічне друге поєднання з етинілбензолом і подальше зняття захисту дає (4Е)-N-метил-5-[3-(5фенілетинилпіридин)іл]-4-пентен-2-амін. Можна одержати оптично активні форми деяких арилзаміщених олефінових амінових сполук, таких як (2S)-(4Е)-N-метил-5-(3-піридиніл)-4пентен-2-амін. В одному синтетичному підході вказаний останнім тип сполук синтезують шляхом поєднання галогензаміщеного піридину, 3бромпіридину, з олефіном, що містить хіральну функціональну групу вторинного спирту, (2R)-4пентен-2-олу, в умовах реакції Гека. Одержану 21 хіральну проміжну сполуку піридинілового спирту, (2R)-(4Е)-5-(3-піридиніл)-4-пентен-2-ол, перетворюють в її відповідний складний птолуолсульфонатний ефір, який потім обробляють метиламіном, що дає заміщення тозилату з інверсією конфігурації. Типово, застосовують способи, аналогічні описаним в W. С. Frank et al., J. Org. Chem. 43: 2947 (1978), і N. J. Malek et al, J. Org. Chem. 47: 5395 (1982), що включають каталізоване паладієм поєднання ароматичної галогензаміщеної сполуки і олефіну. Хіральний бічний ланцюг, (2R)-4-пентен-2-ол, можна одержати шляхом обробки хірального епоксиду, (R)-(+)-пропіленоксиду (комерційно доступний від Fluka Chemical Company), вінілмагнійбромідом і йодидом міді(І) в тетрагідрофурані при низьких температурах (від 25 до -10°С) із застосуванням загальних способів синтезу, описаних в A. Kalivretenos, J. K. Stille, L. S. Hegedus, J. Org. Chem. 56: 2883 (1991), з одержанням (2R)-4-пентен-2-олу. Одержаний хіральний спирт піддають реакції Гека з 3-бромпіридином в ацетонітрилі-триетиламіні (1:1, об./об.) із застосуванням каталізатора, що складається з 1моль.% ацетату паладію(II) і 4моль.% три-о-толілфосфіну. Реакцію здійснюють шляхом нагрівання компонентів при 140°С протягом 14 годин в герметично закритій скляній пробірці з одержанням продукту реакції Гека, (2R)-(4Е)-5-(3-піридиніл)-4-пентен-2олу. Одержаний хіральний піридиніловий спирт обробляють 3 молярними еквівалентами птолуолсульфонілхлориду в безводному піридині при 0°С з одержанням проміжної тозилатної сполуки. Складний п-олуолсульфонатний ефір нагрівають з 82 молярними еквівалентами метиламіну у вигляді 40% водного розчину, що містить невелику кількість етанолу як співрозчинника, з одержанням (2S)-(4E)-N-метил-5-(3-піридиніл)-4пентен-2-аміну. Аналогічним способом можна синтезувати відповідний енантіомер арилзаміщеного олефінового аміну, такий як (2R)-(4Е)-N-метил-5-(3-піридиніл)4-пентен-2-амін, застосовуючи поєднання по Геку 3-бромпіридину і (2S)-4-пентен-2-олу. Одержану проміжну сполуку, (2S)-(4Е)-5-(3-піридиніл)-4пентен-2-ол, перетворюють в її птолуолсульфонат, який піддають заміщенню метиламіну. Хіральний спирт, (2S)-4-пентен-2-ол, одержують з (S)-(-)-пропіленоксиду (комерційно доступний від Aldrich Chemical Company) із застосуванням способу, аналогічного описаному для одержання (2R)-4-пентен-2-олу з (R)-(+)пропіленоксиду, як повідомлялось в A. Kalivretenos, J. К. Stille, L. S. Hegedus, J. Org. Chem. 56: 2883 (1991). В іншому варіанті можна одержати такі сполуки, як (3Е)-N-метил-4-(3-(6-амшопіридин)іл)-3бутен-1-амін, піддаючи 3-галогензаміщений піридин, такий як 2-аміно-5-бромпіридин (Aldrich Chemical Company), каталізованій паладієм реакції поєднання з олефіном, що містить захищену амінову функціональну групу, таким як N-метил-N-(3бутен-1-іл)бензамід. Бензоїл-захисну групу з одержаного продукту реакції Гека можна видалити шляхом нагрівання з водним розчином кислоти з одержанням (3Е)-N-метил-4-(3-(6-амінопіридин)іл) 88792 22 3-бутен-1-аміну. Олефінову вихідну сполуку, Nметил-N-(3-бутен-1-іл)бензамід, можна одержати шляхом взаємодії 4-бром-1-бутену з надмірною кількістю сконденсованого метиламіну в N,Nдиметилформаміді у присутності карбонату калію з одержанням N-метил-3-бутен-1-аміну. Обробка вказаної останньої сполуки бензоїлхлоридом в дихлорметані, що містить триетиламін, дає олефіновий бічний ланцюг, N-метил-N-(3-бутен-1іл)бензамід. Сполуки, описані в даній заявці, можуть містити піразинове або піридазинове кільце. Застосовуючи способи, описані М. Hasegawa, et al. (Європейський патент №0516409 В1), 2-метилпіразин або 3-метилпіридазин (обидва доступні від Aldrich Chemical Company) можна сконденсувати з Nметил-N-(трет-бутоксикарбоніл)-3-амінобутаналєм з одержанням (4Е)-N-метил-N-(третбутоксикарбоніл)-5-(2-піразиніл)-4-пентен-2-аміну і (4Е)-N-метил-N-(трет-бутоксикарбоніл)-5-(3піридазиніл)-4-пентен-2-аміну, відповідно. Видалення трет-бутоксикарбонільної групи за допомогою трифтороцтової кислоти дає (4E)-N-метил-5(2-піразиніл)-4-пентен-2-амін і (4Е)-N-метил-5-(3піридазиніл)-4-пентен-2-амін, відповідно. Необхідний N-метил-N-(трет-бутоксикарбоніл)-3амінобутаналь може бути одержаний з відповідного спирту із застосуванням способів, описаних М. Adamczyk, Υ. Υ. Chen в Міжнародній заявці РСТ WO 9212122. Спирт, N-метил-N-(третбутоксикарбоніл)-3-аміно-1-бутанол, може бути одержаний з комерційно доступного 4-гідрокси-2бутанону (Lancaster Synthesis, Inc.) шляхом послідовного відновного амінування (з використанням метиламіну і ціаноборгідриду натрію і хімічних способів, описаних R. F. Borch, Org. Syn., 52: 124 (1974)) і захисту із застосуванням ди-третбутилдикарбонату. Реакція поєднання Гека, описана вище, також є прийнятною для одержання сполук, які містять деякі сконденсовані гетероцикли. Такі сполуки можуть бути синтезовані шляхом каталізованого паладієм поєднання бромвмісної гетероциклічної сполуки, такої як 6-бром-2-метил-1H-імідазо[4,5b]піридин, з вказаним вище бічним ланцюгом олефінового аміну, N-метил-N-(трет-бутоксикарбоніл)4-пентен-2-аміном. Типово, для реакції поєднання застосовують способи, аналогічні описаним у W. С. Frank et al., J. Org. Chem. 43: 2947 (1978) і N. J. Malek et al., J. Org. Chem. 47: 5395 (1982), що включають каталізоване паладієм поєднання олефіну і ароматичної галогензаміщеної сполуки. Одержану трет-бутоксикарбонілзахищену (Восзахищену) проміжну сполуку можна піддати обробці сильною кислотою, такою як трифтороцтова кислота, з одержанням (4Е)-N-метил-5-(6-(2метил-1H-імідазо[4,5-b]піридин)іл)-4-пентен-2аміну. Необхідний бромімідазопіридин, 6-бром-2метил-1Н-імідазо[4,5-b]піридин, можна одержати з 82% виходом шляхом нагрівання 2,3-діаміно-5бромпіридину з оцтовою кислотою в поліфосфорній кислоті, згідно зі способами, описаними P. K. Dubey et al., Indian J. Chem. 16B(6): 531-533 (1978). 2,3-діаміно-5-бромпіридин можна одержати з 97% виходом шляхом нагрівання 2-аміно-5-бром-3 23 нітропіридину (комерційно доступний від Aldrich Chemical Company і Lancaster Synthesis, Inc.) з дигідратом хлориду олова(II) в киплячому етанолі, згідно зі способом, описаним S. X. Cai et al., J. Med. Chem. 40(22): 3679-3686 (1997). В іншому прикладі бромвмісний сконденсований гетероцикл, такий як 6-бром-1,3-діоксоло[4,5b]піридин, можна піддати поєднанню з описаним вище бічним ланцюгом олефінового аміну, Nметил-N-(трет-бутоксикарбоніл)-4-пентен-2аміном, із застосуванням реакції Гека. З одержаної Вос-захищеної проміжної сполуки можна зняти захист за допомогою сильної кислоти, такої як трифтороцтова кислота, з одержанням (4Е)-Nметил-5-(6-(1,3-діоксоло[4,5-b]піридин)іл)-4пентен-2-аміну. Необхідна бромвмісна сполука, 6бром-1,3-діоксоло[4,5-b]піридин, може бути синтезована з 5-бром-2,3-дигідроксипіридину, також відомого, як 5-бром-3-гідрокси-2(1Н)-піридинон, за допомогою способу метиленування з використанням бромхлорметану, у присутності карбонату калію і Ν,Ν-диметилформаміду, згідно зі способом F. Dallacker et al., Z. Naturforsch. 34 b: 1729-1736 (1979). 5-бром-2,3-дигідроксипіридин можна одержати з фурфуралю (2-фуральдегід, комерційно доступний від Aldrich Chemical Company і Lancaster Synthesis, Inc.) із застосуванням способів, описаних в F. Dallacker et al., Z. Naturforsch. 34 b: 17291736 (1979). Альтернативно, 5-бром-2,3дигідроксипіридин можна одержати згідно зі способом, описаним в ЕР 0081745, виданому на ім'я D. Rose і N. Маак. В іншому прикладі сполука, що містить сконденсований гетероцикл, бромвмісна сполука, 7бром-2,3-дигідро-1,4-діоксино[2,3-b]піридин (також відомий, як 7-бром-5-аза-4-оксахроман), може бути сконденсована з описаним вище бічним ланцюгом олефінового аміну, N-метил-N-(третбутоксикарбоніл)-4-пентен-2-аміном, із застосуванням реакції Гека. З одержаної Вос-захищеної сполуки може бути знятий захист за допомогою сильної кислоти, такої як трифтороцтова кислота, з одержанням (4Е)-N-метил-5-(7-(2,3-дигідро-1,4діоксино[2,3-b]піридин)іл-4-пентен-2-аміну. Бромвмісну сполуку, 7-бром-2,3-дигідро-1,4-діоксино[2,3b]піридин, можна одержати шляхом обробки 5бром-2,3-дигідроксипіридину 1,2-диброметаном і карбонатом калію в Ν,Ν-диметилформаміді, згідно зі способом F. Dallacker et al., Z. Naturforsch. 34 b: 1729-1736 (1979). 5-бром-2,3-дигідроксипіридин можна одержати з фурфуралю, як описано вище. Інші поліциклічні ароматичні сполуки можна одержати за допомогою реакції Гека. Таким чином, деякі сполуки можна синтезувати за допомогою каталізованого паладієм поєднання бромвмісного сконденсованого гетероциклу, такого як 6-бром1H-імідазо[4,5-b]піридин-2-тіол, з описаним вище бічним ланцюгом олефінового аміну, N-метил-N(трет-бутоксикарбоніл)-4-пентен-2-аміном. Восзахищену проміжну сполуку, продукт реакції Гека, можна піддати обробці сильною кислотою, такою як трифтороцтова кислота, з одержанням (4Е)-Nметил-5-(6-(2-тіо-1Н-імідазо[4,5-b]піридин)іл)-4пентен-2-аміну. Необхідну бромвмісну сполуку, 6бром-1H-імідазо[4,5-b]піридин-2-тіол, можна одер 88792 24 жати шляхом обробки 6-бром-1H-імідазо[4,5b]піридин сіркою при 230-260°С, згідно зі способами, описаними в Y. М. Yutilov, Khim. Geterotsikl Doedin. 6: 799-804 (1988). 6-бром-1H-імідазо[4,5b]піридин може бути одержаний від Sigma-Aldrich Chemical Company. Альтернативно, 6-бром-1Hімідазо[4,5-b]піридин можна одержати шляхом обробки 2,3-діаміно-5-бромпіридину мурашиною кислотою в поліфосфорній кислоті, із застосуванням способу, аналогічного описаному Р. К. Dubey et al., Indian J. Chem. 16B(6): 531-533 (1978). 2,3діаміно-5-бромпіридин можна одержати з 97% виходом шляхом нагрівання 2-аміно-5-бром-3нітропіридину (комерційно доступний від Aldrich Chemical Company і Lancaster Synthesis, Inc.) з дигідратом хлориду олова(ІІ) в киплячому етанолі, згідно зі способом, описаним в S. X. Cai et al., J. Med. Chem., 40(22): 3679-3686 (1997). Альтернативно, 6-бром-1Н-імідазо[4,5-b]піридин-2-тіол можна одержати шляхом нагрівання 2,3-діаміно-5бромпіридину з K+- SCSOEt у водному етанолі із застосуванням способу, аналогічного описаному Т. С Kuhler et al., J. Med Chem. 38(25): 4906-4916 (1995). 2,3-діаміно-5-бромпіридин можна одержати з 2-аміно-5-бром-3-нітропіридину, як описано вище. У відповідному прикладі 6-бром-2фенілметилтіо-1Н-імідазо[4,5-b]піридин можна піддати поєднанню через реакцію Гека з описаним вище бічним ланцюгом олефінового аміну, Nметил-N-(трет-бутоксикарбоніл)-4-пентен-2аміном. Одержану Вос-захищену проміжну сполуку можна піддати обробці з сильною кислотою, такою як трифтороцтова кислота, з одержанням (4E)-Nметил-5-(6-(2-фенілметилтіо-1Н-імідазо[4,5b]піридин)іл)-4-пентен-2-аміну. Бромвмісну сполуку, 6-бром-2-фенілметилтіо-1Н-імідазо[4,5b]піридин, можна одержати шляхом алкілування описаного 6-бром-1Н-імідазо[4,5-b]піридин-2-тіолу за допомогою бензилброміду, у присутності карбонату калію і Ν,Ν-диметилформаміду. В іншому прикладі 6-бромоксазоло[4,5b]піридин, коли його послідовно піддають каталізованому паладієм поєднанню з N-метил-N-(третбутоксикарбоніл)-4-пентен-2-аміном і зняттю захисту за допомогою трифтороцтової кислоти, дає (4Е)-N-метил-5-(6-оксазоло[4,5-b]піридиніл)-4пентен-2-амін. Необхідний 6-бромоксазоло[4,5b]піридин може бути одержаний з 2-аміно-5-бром3-піридинолу шляхом конденсації з мурашиною кислотою або триалкілортоформіатом за допомогою способу, аналогічного описаному М-С. Viaud et al., Heterocycles 41: 2799-2809 (1995). Застосування інших карбонових кислот дає 2-заміщені-6бромоксазоло[4,5-b]піридини, які також є субстратами для реакції Гека. Синтез 2-аміно-5-бром-3піридинолу здійснюють з фурфуриламіну (Aldrich Chemical Company). Таким чином, 5-бром-3піридинол (одержаний з фурфуриламіну відповідно до патенту США №4192946) може бути хлорований за допомогою способів, описаних в V. Koch et al., Synthesis, 499 (1990), з одержанням 2-хлор5-бром-3-піридинолу, який, в свою чергу, може бути перетворений в 2-аміно-5-бром-3-піридинол шляхом обробки аміаком. 25 5-бромоксазоло[5,4-b]піридин, ізомерний внаслідок орієнтації конденсації циклів в напрямі раніше описаного 6-бромоксазоло[4,5-b]піридину, також можна застосовувати в реакції поєднання Гека з N-метил-N-(трет-бутоксикарбоніл)-4-пентен2-аміном. Подальше видалення третбутоксикарбонільної захисної групи забезпечує (4Е)-N-метил-5-(5-оксазоло[5,4-b]піридиніл)-4пентен-2-амін. 5-бромоксазоло[5,4-b]піридин може бути синтезований з 3-аміно-5-бром-2-піридинолу (3-аміно-5-бром-2-піридон) шляхом конденсації з мурашиною кислотою (або її похідним), як описано вище. 3-аміно-5-бром-2-піридинол може бути одержаний шляхом бромування (із застосуванням способу, описаного Т. Batkowski, Rocz. Chem. 41: 729-741 (1967)) і подальшого відновлення за допомогою хлориду олова(II) (згідно зі способом, описаним S. X. Cai et al., J. Med. Chem. 40(22): 3679-3686 (1997)) комерційно доступного 3-нітро2-піридинолу (Aldrich Chemical Company). Інші поліциклічні ароматичні сполуки за даним винаходом можна одержати за допомогою реакції Гека. Таким чином, 5-бромфуро[2,3-b]піридин і 5бром-1Н-піроло[2,3-b]піридин, обидва можна піддати каталізованому паладієм поєднанню з описаним вище бічним ланцюгом олефінового аміну, Nметил-N-трет-бутоксикарбоніл)-4-пентен-2-аміном, з одержанням (4E)-N-метил-N-третбутоксикарбоніл)-5-(5-фуро[2,3-b]піридиніл)-4пентен-2-аміну і (4Е)-N-метил-N-(третбутоксикарбоніл)-5-(5-1H-піроло[2,3-b]піридиніл)-4пентен-2-аміну, відповідно. Подальше видалення трет-бутоксикарбонільної групи за допомогою трифтороцтової кислоти дає (4Е)-N-метил-5-(5фуро[2,3-b]піридиніл)-4-пентен-2-амін і (4Е)-Nметил-5-(5-1H-піроло[2,3-b]піридиніл)-4-пентен-2амін. Необхідні 5-бромфуро[2,3-b]піридин і 5-бром1H-піроло[2,3-b]піридин можуть бути одержані з 2,3-дигідрофуро[2,3-b]піридин і 2,3дигідропіроло[2,3-b]піридин, відповідно, шляхом бромування (бром і бікарбонат натрію в метанолі) і дегідрування (2,3-дихлор-5,6-диціано-1,4бензохінон), із застосуванням хімічних способів, описаних в Е. С Taylor et al., Tetrahedron 43: 51455158 (1987). 2,3-дигідрофуро[2,3-b]піридин і 2,3дигідропіроло[2,3-b]піридин, в свою чергу, одержують з 2-хлорпіримідину (Aldrich Chemical Company), як описано А. Е. Frissen et al., Tetrahedron 45: 803-812 (1989), шляхом нуклеофільного заміщення хлориду (з використанням натрієвої солі 3-бутин-1-олу або 4-аміно-1-бутану) і подальшою внутрішньомолекулярною реакцією Дільса-Альдера. Із застосуванням аналогічних хімічних способів 2,3-дигідрофуро[2,3-b]піридин і 2,3-дигідропіроло[2,3-b]піридин також можуть бути одержані з 3-метилтіо-1,2,4-триазену (Е. С Taylor et al., Tetrahedron 43: 5145-5158 (1987)), який, в свою чергу, одержують з гліоксалю і Sметилтіосемікарбазиду (W. Paudler et al., J. Heterocyclic Chem. 7: 767-771 (1970)). Бромовані дигідрофуропіридини, дигідропіролопіридини і дигідропіранопіридини також є субстратами для каталізованого паладієм поєднання. Наприклад, 5-бром-2,3-дигідрофуро[2,3-b]піридин і 5-бром-2,3-дигідрошроло[2,3-b]піридин (одержані 88792 26 бромуванням 2,3-дигідрофуро[2,3-b]піридину і 2,3дигідропіроло[2,3-b]піридину, як описано вище), обидва можна піддати поєднанню з описаним вище бічним ланцюгом олефінового аміну, застосовуючи спосіб Гека. Подальше зняття захисту дає відповідні (4Е)-N-метил-5-(5-(2,3-дигідрофуро[2,3b]піридин)іл)-4-пентен-2-амін і (4Е)-N-метил-5-(5(2,3-дигідропіроло[2,3-b]піридин)іл)-4-пентен-2амін. Аналогічна обробка 6-бром-2,3дигідрофуро[3,2-b]піридину (ізомерний по конденсації циклів з [2,3-b] системою) дає (4Е)-N-метил-5(6-(2,3-дигідрофуро[3,2-b]піридин)іл)-4-пентен-2амін. Необхідний 6-бром-2,3-дигідрофуро[3,2b]піридин може бути одержаний з 5-бром-2-метил3-піридинолу шляхом послідовної обробки двома еквівалентами діізопропіламіду літію (для утворення 2-метиленіл, 3-оксидіаніону) і одним еквівалентом дибромметану. Альтернативно, із застосуванням хімічних способів, аналогічних описаним М. U. Koller. et al., Synth. Commun. 25: 2963-74 (1995), силілзахищений піридинол (5-бром-2метил-3-триметилсилілоксипіридин) можна послідовно обробити одним еквівалентом діізопропіламіду літію і алкіл- або арилальдегідом з одержанням 2-(2-(1-алкіл- або 1-арил-1-гідрокси)етил)-5бром-3-(триметилсилілокси)піридину. Такі речовини можуть бути перетворені за допомогою способів (таких як каталізована кислотою циклізація або синтез Вільямсона), відомих фахівцям в даній галузі, у відповідні циклічні прості ефіри (2-алкіл- або 2-арил-6-бром-2,3-дигідрофуро[3,2-b]піридини). Аналогічний хімічний спосіб, в якому епоксиди (замість альдегідів) застосовують у взаємодії з піридинілметильним карбаніоном, приводить до 2алкілі 2-арил-7-бром-2,3-дигідропірано[3,2b]піридинів. Ці 2-заміщені бромовані дигідрофуроі дигідропіранопіридини також є субстратами для реакції Гека. Наприклад, 6-бром-2,3-дигідро-2фенілфуро[3,2-b]піридин можна піддати поєднанню, в каталізованому паладієм способі, з N-метилN-(трет-бутоксикарбоніл)-4-пентен-2-аміном, обробити продукт поєднання трифтороцтовою кислотою (для видалення трет-бутоксикарбонільної групи) з одержанням (4Е)-N-метил-5-(6-(2,3дигідро-2-фенілфуро[3,2-b]піридин)іл)-4-пентен-2аміну. 5-бром-2-метил-3-піридинол, що використовується для синтезу бромованих дигідрофуро- і дигідропіранопіридинів, одержують шляхом стандартних перетворень комерційно доступних речовин. Таким чином, 2-метилнікотинову кислоту (Aldrich Chemical Company) можна перетворити, шляхом послідовної обробки тіонілхлоридом, бромом і аміаком (спосіб, описаний С V. Greco et al., J. Heterocyclic Chem. 7: 761-766 (1970)), в 5-бром-2метилнікотинамід. Перегрупування Гофмана 5бром-2-метилнікотинаміду з гіпохлоритом дає 3аміно-5-бром-2-метилпіридин, який може бути перетворений в 5-бром-2-метил-3-піридинол шляхом діазотування з використанням нітриту натрію у водному розчині сірчаної кислоти. Альтернативно, складний аланінетиловий ефір (Aldrich Chemical Company) перетворюють (з використанням етилформіату) в його N-формільне похідне, яке потім перетворюють в 5-етокси-4-метилоксазол за до 27 помогою пентоксиду фосфору (N. Takeo et al., патент Японії №45012732). Реакція Дільса-Альдера 5-етокси-4-метилоксазолу з акрилонітрилом дає 5гідрокси-6-метилнікотинонітрил (Т. Yoshikawa et al., Chem. Pharm. Bull. 13: 873 (1965)), який перетворюють в 5-аміно-2-метил-3-піридинол шляхом гідратування і перегрупування Гофмана (Υ. Morisawa et al., Agr. Biol. Chem. 39: 1275-1281 (1975)). 5-аміно-2-метил-3-піридинол можна потім перетворити, шляхом діазотування у присутності броміду міді, в необхідний 5-бром-2-метил-3піридинол. Кожний з цих способів забезпечує сполуки (Е)метанікотинового типу як основний продукт, але також приводить до утворення невеликих кількостей відповідних сполук (Z)-метанікотинового типу та інших ізомерів, як описано вище. Ці другорядні продукти реакції можна видалити за допомогою традиційних способів, якщо це потрібно. Альтернативно, як описано більш детально нижче, сполуки (Е)-метанікотинового типу можна виділити у вигляді гідроксибензоатних солей, які можуть осідати у, по суті, чистій формі з реакційної суміші, включаючи гідроксибензоатні солі сполук (Z)метанікотинового типу та інших другорядних продуктів реакції. Для одержання сполук можна застосовувати інші способи, крім реакції поєднання Гека. Наприклад, сполуки (Е)-метанікотинового типу можна одержати за допомогою способів, описаних Loffler et al., Chem. Ber., 42:3431-3438 (1909) і Laforge, J.A.C.S., 50:2477 (1928), зі сполук типу заміщених нікотинів. Деякі сполуки типу 6-заміщених метанікотинів можна одержати з відповідних сполук 6заміщених нікотинів, застосовуючи загальні способи, описані Acheson et al., J. Chem. Soc, Perkin Trans. 1(2): 579-585 (1980). Необхідні попередники для таких сполук, сполуки типу 6-заміщених нікотинів, можуть бути синтезовані зі складних ефірів 6-заміщених нікотинових кислот із застосуванням загальних способів, описаних Rondahl, Acta Pharm. Suec, 14: 113-118 (1977). Одержання деяких сполук типу 5-заміщених метанікотинів можна здійснити з відповідних сполук типу 5-заміщених нікотинів із застосуванням загального способу, розкритого Acheson et al., J. Chem. Soc, Perkin Trans. 1(2): 579-585 (1980). Сполуки 5галогензаміщених нікотинів (наприклад, типу фтор- і бромзаміщених нікотинових сполук) і сполуки типу 5-амінонікотинових можна одержати із застосуванням загальних способів, розкритих Rondahl, Act. Pharm. Suec, 14: 113-118 (1977). Сполуки 5-трифторметилнікотинового типу можна одержати із застосуванням технології і речовин, описаних в Ashimori et al., Chem. Pharm. Bull., 38(9): 2446-2458 (1990), і Rondahl, Acta Pharm. Suec, 14: 113-118 (1977). Одержання Е-метанікотингідроксибензоатів (Е)-метанікотингідроксибензоати одержують шляхом взаємодії сполук Е-метанікотинового типу, описаних вище, з гідроксибензойними кислотами. Стехіометрія окремих компонентів (Е-метанікотин і гідроксибензойна кислота), які використовуються для одержання солей, може варіювати. Молярне відношення оксибензойної кислоти до основи (Е 88792 28 метанікотин) звичайно складає від 2:1 до 1:2, більш переважно, 2:1 або 1:1, але можливі інші відношення (такі як 3:2). Переважно, коли молярне відношення кислоти до основи становить 1:1. В залежності від того, яким способом одержують солі за даним винаходом, ці солі можуть мати кристалічні структури, які можуть поглинати розчинники, присутні в процесі утворення солі. Таким чином, солі за даним винаходом можуть бути у формі гідратів та інших сольватів з різною стехіометрією розчинника відносно арилзаміщеного аміну. Спосіб одержання сполук за даним винаходом може варіювати. Наприклад, одержання (2S)-(4Е)N-метил-5-(5-ізопропокси-3-піридиніл)-4-пентен-2аміну у формі п-гідроксибензоату може включати: (і) додавання розчину прийнятно чистої сполуки, розчиненої в етанолі, до розчину пгідроксибензойної кислоти (1,1 еквівалента) в етанолі, нагрівання при температурі кипіння зі зворотним холодильником, з утворенням осаду; (іі) застосування нагрівання і/або води і етанолу (кількість води не перевищує 10%) для розчинення осаду, (ііі) охолоджування одержаного розчину, якщо необхідно, щоб викликати осадження солі, і (iv) фільтрацію і збирання солі. Стехіометрія, суміш розчинників, концентрація розчиненої речовини і температура, що використовується, можуть варіювати, але одержання солей відоме фахівцям, кваліфікованим в даній галузі. Одержання інших форм солей За необхідності, після виділення гідроксибензоатних солей можуть бути утворені інші форми солей, наприклад, шляхом безпосередньої взаємодії з іншими фармацевтично прийнятними кислотами або шляхом виділення спочатку вільної основи (шляхом взаємодії з сильною основою і екстракції у відповідний розчинник), а потім взаємодії з іншою фармацевтично прийнятною кислотою. Такі способи відомі фахівцям в даній галузі. III. Фармацевтичні композиції Фармацевтичні композиції за даним винаходом містять гідроксибензоати, описані в даній заявці, в чистому вигляді або у формі композиції, в якій сполуки об'єднані з яким-небудь іншим фармацевтично сумісним продуктом, який може бути інертним або фізіологічно активним. Такі композиції можна вводити, наприклад, перорально, парентерально, ректально або місцевим шляхом. Приклади твердих композицій для перорального введення являють собою, але не обмежені цим, таблетки, пілюлі, порошки (желатинові капсули, саше) і гранули. У таких композиціях активну сполуку змішують з одним або декількома інертними розріджувачами, такими як крохмаль, целюлоза, сахароза, лактоза або діоксид кремнію; ідеально, під потоком інертного газу, такого як аргон. Композиції також можуть містити речовини, які відрізняються від розріджувачів, наприклад, одну або: декілька змащувальних речовин, таких як стеарат магнію або тальк, барвник, покриття (таблетки з покриттям) або лак. Приклади рідких композицій для перорального введення являють собою, але не обмежені цим, розчини, суспензії, емульсії, сиропи і еліксири, які 29 є фармацевтично прийнятними і типово містять інертні розріджувачі, такі як вода, етанол, гліцерин, рослинні олії або рідкий парафін. Такі композиції можуть містити речовини, які відрізняються від розріджувачів, наприклад, змочувальні речовини, підсолоджувачі, загусники, віддушки і стабілізатори. Стерильні композиції для парентерального введення можуть являти собою, наприклад, водні або неводні розчини, суспензії і емульсії. Приклади придатних розчинників і носіїв являють собою, але не обмежені цим, водні розчини, переважно, забуферені водні розчини, пропіленгліколь, поліетиленгліколь, рослинні олії, особливо оливкову олію, придатні для ін'єкцій складні органічні ефіри, наприклад, етилолеат, та інші придатні органічні розчинники. Такі композиції також можуть містити ад'юванти, зокрема, змочувальні речовини, речовини для придання ізотонічності, емульгатори, розпушувачі і стабілізатори. Такі стерильні композиції можна стерилізувати різними способами, наприклад, шляхом асептичного фільтрування, шляхом введення стерилізуючих речовин в композицію, шляхом опромінення; і шляхом нагрівання. їх також можна одержувати у формі стерильних твердих композицій, які можна розчинити під час використання у стерильній воді або будьякому іншому стерильному середовищі для ін'єкцій. Приклади композицій для ректального введення являють собою, але не обмежені цим, супозиторії і ректальні капсули, які крім активної речовини можуть включати ексципієнти, такі як масло какао, напівсинтетичні гліцериди і поліетиленгліколі. Композиції для місцевого введення можуть бути, наприклад, у формі кремів, лосьйонів, очних примочок, розчинів· для полоскання рота, назальних крапель або аерозолів. Фармацевтичні композиції такoж можуть містити різні інші компоненти у вигляді домішок або допоміжних речовин. Приклади фармацевтично прийнятних компонентів або допоміжних речовин, які застосовують у відповідних обставинах, являють собою антиоксиданти, акцептори вільних радикалів, пептиди, фактори росту, антибіотики, бактеріостатичні речовини, імуносупресори, антикоагулянти, буферні речовини, протизапальні засоби, жарознижуючі засоби, зв'язувальні для контрольованого вивільнення, анестезуючі засоби, стероїди і кортикостероїди. Такі компоненти можуть забезпечувати додаткову терапевтичну користь, впливати на терапевтичну дію фармацевтичної композиції, або їх дія може бути спрямована на запобігання яким-небудь потенційним побічним діям, які можуть виникати внаслідок введення фармацевтичної композиції. У деяких обставинах сполуки за даним винаходом можна застосовувати як частину фармацевтичної композиції з іншими сполуками, призначеними для профілактики або лікування певного захворювання. IV. Способи лікування Гідроксибензоатні солі, описані в даній заявці, є корисними для лікування тих станів і розладів, для яких були запропоновані інші типи нікотинових 88792 30 сполук як терапевтичні засоби. Див., наприклад, Williams et al., DN&P 7(4): 205-227 (1994); Arneric et al., CNS Drug Rev. 1(1): 1-26 (1995); Arneric et al., Exp. Opin. Invest. Drags 5(1):79-100 (1996); Bencherif et al., J. Pharmacol. Exp. Ther. 279: 1413 (1996); Lippiello et al., J. Pharmacol. Exp. Ther. 279: 1422 (1996); Damaj et al., Neuroscience (1997); Holladay et al., J. Med. Chem. 40(28): 4169-4194 (1997); Bannon et al., Science 279: 77-80 (1998); PCT WO 94/08992; PCT WO 96/31475; і Патенти США №№5583140, виданий на ім'я Bencherif et al.; 5597919, виданий на ім'я Dull et al.; і 5604231, виданий на ім'я Smith et al. Солі також можна застосовувати як допоміжну терапію в поєднанні з існуючими терапевтичними засобами для лікування вказаних вище типів захворювань і розладів. У таких ситуаціях переважно вводити активні інгредієнти таким чином, щоб звести до мінімуму впливи на підтипи nAChR, такі як впливи, пов'язані з м'язами і гангліями. Це можна здійснювати шляхом спрямованої доставки лікарського засобу і/або шляхом коректування дози таким чином, щоб необхідний вплив досягався без наближення до тієї порогової дози, яка викликає значні побічні дії. Фармацевтичні композиції можна застосовувати для полегшення яких-небудь симптомів, пов'язаних з вказаними станами, захворюваннями і розладами. Приклади станів і розладів, які можна лікувати, являють собою неврологічні розлади, нейродегенеративні розлади, зокрема, розлади ЦНС, і запальні розлади. Розлади ЦНС можуть бути індуковані лікарськими засобами; їх причиною може бути генетична схильність, інфекція або травма; або їх етіологія може бути невідомою. Розлади ЦНС являють собою нейропсихіатричні розлади, неврологічні захворювання і психічні захворювання, і являють собою нейродегенеративні захворювання, поведінкові розлади, когнітивні розлади і когнітивно-афективні розлади. Існують деякі розлади ЦНС, клінічний прояв яких віднесений до порушення функції ЦНС (тобто розлади, які є результатом неприйнятних рівнів вивільнення нейротрансмітерів, неприйнятних властивостей нейротрансмітерних рецепторів і/або неприйнятної взаємодії між нейротрансмітерами і нейротрансмітерними рецепторами). Деякі розлади ЦНС можуть виникати за рахунок дефіциту ацетилхоліну, допаміну, норепінефрину і/або серотоніну. Приклади розладів ЦНС, які можна лікувати за допомогою Е-метанікотинових сполук і гідроксибензоатних солей, описаній в даній заявці, і фармацевтичних композицій, які містять такі сполуки і солі, являють собою пресенільну деменцію (ранній початок хвороби Альцгеймера), старечу деменцію (деменцію Альцгеймерового типу), деменцію по типу тілець Lewy, мікроінфарктну деменцію, деменцію, пов'язану зі СНІДом, ВІЛ-індуковану деменцію, множинні церебральні інфаркти, Паркінсонізм, включаючи хворобу Паркінсона, хворобу Pick, прогресивний супрануклеарний параліч, хорею Гентінгтона, пізню дискінезію, гіперкінезію, епілепсію, маніакальний синдром, розлад, пов'язаний з дефіцитом уваги, неспокій, депресію, дислексію, депресію, пов'язану з шизофренією, обсесивно 31 компульсивний розлад, синдром Tourette, легке порушення пізнавальної здатності (МСІ), вікове погіршення пам'яті (ААМІ), ранні амнезійні і когнітивні розлади, пов'язані з віком або виникаючі внаслідок алкоголізму, або синдромом імунодефіциту, або пов'язані з судинними розладами, з генетичними змінами (такими як, наприклад, трисомія 21) або з дефіцитом уваги або дефіцитом пізнавальної здатності, гострі або хронічні нейродегенеративні стани, такі як бічний аміотрофічний склероз, розсіяний склероз, периферичні нейротрофії і травми головного або спинного мозку. Крім того, сполуки можна застосовувати для лікування нікотинової залежності і/або інших поведінкових розладів, пов'язаних з речовинами, які викликають залежність (наприклад, алкоголь, кокаїн, героїн і опіати, психостимулюючі засоби, бензодіазепіни і барбітурати), і для лікування ожиріння. Сполуки також можна застосовувати для лікування патологій запального характеру шлунково-кишкової системи, таких як хвороба Крона, синдром подразненої товстої кишки і виразковий коліт, і діареї. Способи введення гідроксибензоатних солей можуть бути різними. Солі можна вводити шляхом інгаляції (наприклад, у формі аерозолю, або назальним шляхом, або із застосуванням пристроїв для доставки, наприклад, таких, які описані в патенті US №4922901, виданому на ім'я Brooks et al.); місцевим шляхом (наприклад, у формі лосьйону); перорально (наприклад, в рідкій формі в розчиннику, такому як водна або неводна рідина, або в твердому носії); внутрішньовенно (наприклад, в розчині декстрози або фізіологічному розчині); у вигляді інфузії або ін'єкції (наприклад, у вигляді суспензії або у вигляді емульсії у фармацевтично прийнятній рідині або суміші рідин); інтраректально; інтрацеребровентрикулярно; або черезшкірним шляхом (наприклад, із застосуванням черезшкірного пластиру). Хоча можна вводити солі у формі нерозфасованої активної хімічної речовини, переважно представляти кожну сіль у формі фармацевтичної композиції або препарату ефективного і дійового введення. Приклади способів введення таких солей повинні бути очевидні для фахівців. Наприклад, солі можна вводити у формі таблетки, твердої желатинової капсули або у формі капсули з контрольованим вивільненням. Як інший приклад, солі можна доставляти черезшкірно способами із застосуванням пластирів, які доступні від Novartis and Alza Corporation. Фармацевтичні композиції за даним винаходом можна вводити з перервами, або поступово, безперервно, з постійною або контрольованою швидкістю, теплокровній тварині (наприклад, ссавцеві, такому як миша, щур, кішка, кролик, собака, свиня, корова або мавпа); але, переважно, сполуки є переважними для введення людині. Крім того, час введення і кількість введень на день фармацевтичного препарату, що вводиться, можуть варіювати. Введення, переважно, повинне бути таким, щоб активні інгредієнти фармацевтичної композиції взаємодіяли з ділянками рецепторів в організмі суб'єкта, які впливають на функціонування ЦНС або шлунково-кишкового (GI) тракту. Більш конкретно, при лікуванні розладів ЦНС введення, пе 88792 32 реважно, повинне бути таким, щоб оптимізувати ефект на ті відповідні підтипи рецепторів, які впливають на ЦНС, в той же час зводячи до мінімуму дію на м'язові рецептори. Інші придатні способи введення солей описані в патенті US №5604231, виданому на ім'я Smith et al., розкриття якого включене в дану заявку за допомогою посилання у всій його повноті. Прийнятна доза солей являє собою таку кількість, яка є ефективною для запобігання виникненню симптомів розладу або для лікування деяких симптомів розладу, від якого страждає пацієнт. Під "ефективною кількістю", "терапевтичною кількістю" або "ефективною дозою" мається на увазі кількість, достатня, щоб викликати необхідну фармакологічну або терапевтичну дії, таким чином, приводячи до ефективної профілактики або лікування розладу. Таким чином, при лікуванні розладу ЦНС ефективна кількість гідроксибензоатних солей являє собою таку кількість, яка необхідна для доставки через гематоенцефалічний бар'єр суб'єкта достатньої кількості вільної основи лікарського засобу для зв'язування з відповідними ділянками рецепторів в головному мозку суб'єкта і для модулювання відповідних підтипів нікотинових рецепторів (наприклад, забезпечення секреції нейротрансмітерів, забезпечуючи, таким чином, ефективну профілактику або лікування розладу). Профілактика розладу очевидна щонайменше з відстрочки виникнення симптомів розладу або зниження тяжкості симптомів. Лікування розладу очевидне щонайменше зі зменшення симптомів, пов'язаних з розладом, або зменшення випадків повторного виникнення симптомів розладу. Ефективна доза може варіювати, в залежності від таких факторів, як стан пацієнта, тяжкість симптомів розладу і способу, що застосовується для введення фармацевтичної композиції. Коли пацієнтом є людина, ефективна доза типових солей, як правило, вимагає введення таких солей в кількості, достатній для модуляції відповідних рецепторів для впливу на вивільнення нейротрансмітерів (наприклад, допаміну), але цієї кількості повинно бути недостатньо для індукції впливів на скелетні м'язи і ганглії значною якою-небудь мірою. Ефективна доза гідроксибензоатної солі, звичайно, буде розрізнюватись для різних пацієнтів, але, як правило, містить кількості, починаючи з яких виявляються впливи на ЦНС або інші необхідні терапевтичні дії, але нижче кількості, при якій спостерігаються м'язові дії. Дози залежать від необхідної дії, тривалості лікування і шляху введення, що застосовується; як правило, вони знаходяться в межах від 0,05мг до 100мг активної речовини на день при пероральному введенні дорослому пацієнту. Звичайно лікуючий лікар визначає прийнятну дозу з урахуванням віку, ваги і всіх інших факторів, специфічних для конкретного пацієнта. Солі за даним винаходом, при застосуванні в ефективних кількостях згідно зі способом за даним винаходом, часто не здатні викликати активацію nAChR ганглію людини значною якою-небудь мірою. Така селективність солей за даним винаходом проти тих nAChR, які відповідальні за серце 33 во-судинні побічні ефекти, демонструється відсутністю здатності таких солей активувати нікотинову функцію хромафінної тканини надниркової залози. Як такі, такі солі володіють низькою здатністю викликати приток ізотопних рубідієвих іонів через nAChR в клітинних препаратах, одержаних з надниркової залози. В основному, типові переважні солі, прийнятні для здійснення даного винаходу, максимально активують приток ізотопних рубідієвих іонів менше 10 процентів, переважно, менше 5 процентів від максимально забезпечуваного S(-) нікотином. Солі є ефективними в тому, що в деякій мірі забезпечують запобігання розвитку розладів ЦНС, полегшуючи симптоми розладів ЦНС, і в деякій мірі зменшуючи повтори розладів ЦНС. Однак такі ефективні кількості таких солей не є достатніми, щоб викликати які-небудь помітні небажані нікотинові дії, як продемонстровано шляхом зниження ефектів на препаратах, які, як вважають, відображають впливи на серцево-судинну систему або впливи на м'язово-скелетну систему. Таким чином, введення солей за даним винаходом забезпечує терапевтичне вікно, в рамках якого забезпечується лікування деяких розладів ЦНС за відсутності небажаних периферичних нікотинових впливів/побічних дій. Тобто ефективна доза сполуки за даним винаходом є достатньою для забезпечення необхідних впливів на ЦНС, але вона є недостатньою (тобто не є досить високою), щоб викликати небажані побічні дії. Переважно, ефективне введення сполуки за даним винаходом, яке забезпечує лікування розладів ЦНС, являє собою введення менше 1/3, переважно, менше 1/5 і, більш переважно, менше 1/10 від кількості, достатньої, щоб викликати які-небудь значні побічні дії. Наступні синтетичні і аналітичні приклади представлені для ілюстрації даного винаходу і не повинні розглядатись як такі, що обмежують винахід. У цих прикладах всі частини і проценти є масовими, якщо не вказане інше. Виходи реакцій вказані в мольних процентах. Приклад 1: синтез п-гідроксибензоату (2S)(4Е)-N-метил-5-(5-ізопропокси-3-піридиніл)-4пентен-2-аміну п-гідроксибензоат(2S)-(4Е)-N-метил-5-(5ізопропокси-3-піридиніл)-4-пентен-2-аміну п-гідроксибензойну кислоту (2,62г, 19,0ммоль) додавали порціями до перемішуваного розчину (2S)-(4Е)-N-метил-5-(5-ізопропокси-3-піридиніл)-4пентен-2-аміну (4,79г, чистота 93%, 19,0ммоль) в ізопропілацетаті (50мл). В процесі додавання спостерігали кристалізацію солі. По завершенні додавання п-гідроксибензойної кислоти суспензію нагрівали при температурі близько її точки кипіння, при цьому повільно додавали ізопропанол. Після додавання 15мл ізопропанолу досягали повне розчинення. Охолоджування розчину до температури навколишнього середовища (протягом ночі) давало осадження кристалічної маси, яку збирали шляхом фільтрування з відсмоктуванням і сушили на повітрі (4,03г). Другу партію (0,82г) виділяли з концентрованого фільтрату шляхом додавання ацетону. Дві партії кристалів об'єднували і перекристалізовували з ацетону (50мл). Тверду речо 88792 34 вину збирали шляхом фільтрування з відсмоктуванням і сушили у вакуумній печі (50°С) протягом 18 годин. Одержували 4,24г (60,0%) білих кристалів (чистота 98+%, визначена методами ГХМС і РХМС; т. пл. 99-101°С). Приклад 2: синтез (2S)-(4Е)-N-метил-5-(5ізопропокси-3-піридиніл)-4-пентен-2-аміну (через реакцію Гека з (S)-N-метил-N-(третбутоксикарбоніл)-4-пентен-2-аміном) і використання п-гідроксибензоатної солі для полегшення виділення і очищення (2S)-(4Е)-N-метил-5-(5ізопропокси-3-піридиніл)-4-пентен-2-аміну 3-бром-5-ізопропоксипіридин ' У 72-л реактор завантажували послідовно трет-пентоксид натрію (2,2кг, 20моль) і 1-метил-2піролідинон (17,6л). Одержану суміш перемішували протягом 1 години, а потім додавали 2пропанол (12л) протягом 2 годин. Потім в реактор додавали 3,5-дибромпіридин (3,0кг, 13моль) і суміш нагрівали при 75°С протягом 12 годин в атмосфері азоту. Суміш потім охолоджували, розбавляли толуолом (15л) і промивали водою (30л). Водну фазу екстрагували толуолом (15л) і об'єднані толуольні фази промивали водою (15л) і концентрували при зниженому тиску з одержанням 2,5кг темної олії. Одержану олію об'єднували з рівного розміру партією речовини другої фракції і піддавали вакуумній перегонці (т.кип.65°С при 0,3мм) з одержанням 3,1кг (57%) 3-бром-5ізопропоксипіридину у вигляді блідо-жовтої олії. (2R)-4-пентен-2-ол (2R)-4-пентен-2-ол одержували з виходом 82,5% з (R)-(+)-пропіленоксиду згідно зі способами, описаними в A. Kalivretenos, J. K. Stille, L. S. Hegedus, J. Org. Chem. 56: 2883 (1991). (S)-N-метил-N-(трет-бутоксикарбоніл)-4пентен-2-амін Суміш (R)-4-пентен-2-олу (7,62г, 88,5ммоль), піридину (15мл) і безводного (одержаного перегонкою з гідридом кальцію) дихлорметану (30мл) перемішували на крижаній бані, додаючи при цьому п-толуолсульфонілхлорид (18,6г, 97,4ммоль) протягом 3 хвилин. Суміш перемішували 20 хвилин при 0°С і 16 годин при температурі навколишнього середовища, при цьому відбувалось утворення важкого осаду. Додавали насичений водний розчин бікарбонату натрію (75мл) і двофазну суміш інтенсивно перемішували протягом 3 годин. Дихлорметанову фазу і два дихлорметанових екстракти (по 50мл кожний) водної фази об'єднували, сушили (Na2SO4) і концентрували за допомогою роторного випарника. Обробка у високому вакуумі давала 18,7г світло-жовтої олії, які об'єднували з диметилформамідом (ДМФА) (35мл) і 40% водним розчином метиламіну (35мл). Одержаний розчин перемішували при температурі навколишнього середовища протягом 48 годин і потім виливали в суміш насиченого водного розчину хлориду натрію (300мл) і 2,5Μ гідроксиду натрію (50мл). Одержану суміш екстрагували простим ефіром (5´250мл) і ефірні екстракти сушили (Na2SO4) і концентрували за допомогою роторного випарника (з охолоджуючої крижаної бані) до об'єму близько 250мл. Розчин, що залишився, об'єднували з ди-третбутилдикарбонатом (16,9г, 77,4ммоль) і ТГФ 35 (100мл) і суміш перемішували при температурі навколишнього середовища протягом 16 годин. Леткі речовини випаровували за допомогою роторного випарника і залишок переганяли у вакуумі при тиску 5мм (т.кип.79-86°С) з одержанням 7,74г (вихід 43,9%) прозорої безбарвної рідини. п-гідроксибензоат(2S)-(4Е)-N-метил-5-(5ізопропокси-3-піридиніл)-4-пентен-2-аміну Суміш 3-бром-5-ізопропоксипіридину (21,0г, 97,2ммоль), (S)-N-метил-N-(трет-бутоксикарбоніл)4-пентен-2-аміну (24,0г, 120ммоль), ДМФА (53мл), K2СО3 (22г, 159ммоль), ацетату паладію(II) (0,22г, 0,98ммоль) і три-о-толілфосфіну (0,57г, 1,9ммоль) дегазували і вміщували в атмосферу азоту. Перемішувану суміш потім нагрівали при 130°С протягом 2,5 години. Для видалення паладієвої солі додавали Smopex™ (20г) і етилацетат (100мл). Перемішувану суміш нагрівали при 50°С протягом 5 годин і при температурі навколишнього середовища протягом 16 годин і потім фільтрували. Фільтрат концентрували при зниженому тиску і залишок (83г) розчиняли в метанолі (25мл), охолоджували на холодній водяній бані (
ДивитисяДодаткова інформація
Назва патенту англійськоюHydroxybenzoate salts of metanicotine compounds
Автори англійськоюMunoz Julio A., Genus John, Moore James R.
Назва патенту російськоюГидроксибензоатные соли метаникотиновых соединений
Автори російськоюМуньос Хулио А., Дженус Джон, Мур Джеймс Р.
МПК / Мітки
МПК: A61K 31/4406, C07D 213/46
Мітки: метанікотинових, сполук, солі, гідроксибензоатні
Код посилання
<a href="https://ua.patents.su/19-88792-gidroksibenzoatni-soli-metanikotinovikh-spoluk.html" target="_blank" rel="follow" title="База патентів України">Гідроксибензоатні солі метанікотинових сполук</a>
Попередній патент: Ізольований твердим електроізоляційним матеріалом полюс вимикача із з’єднанням рухомої контакт-деталі на стороні торця
Наступний патент: Антитромботичні подвійні інгібітори, що містять залишок біотину
Випадковий патент: Блок датчиків вологості та температури












