Застосування інгібіторів мієлопероксидази для лікування множинної системної атрофії
Формула / Реферат
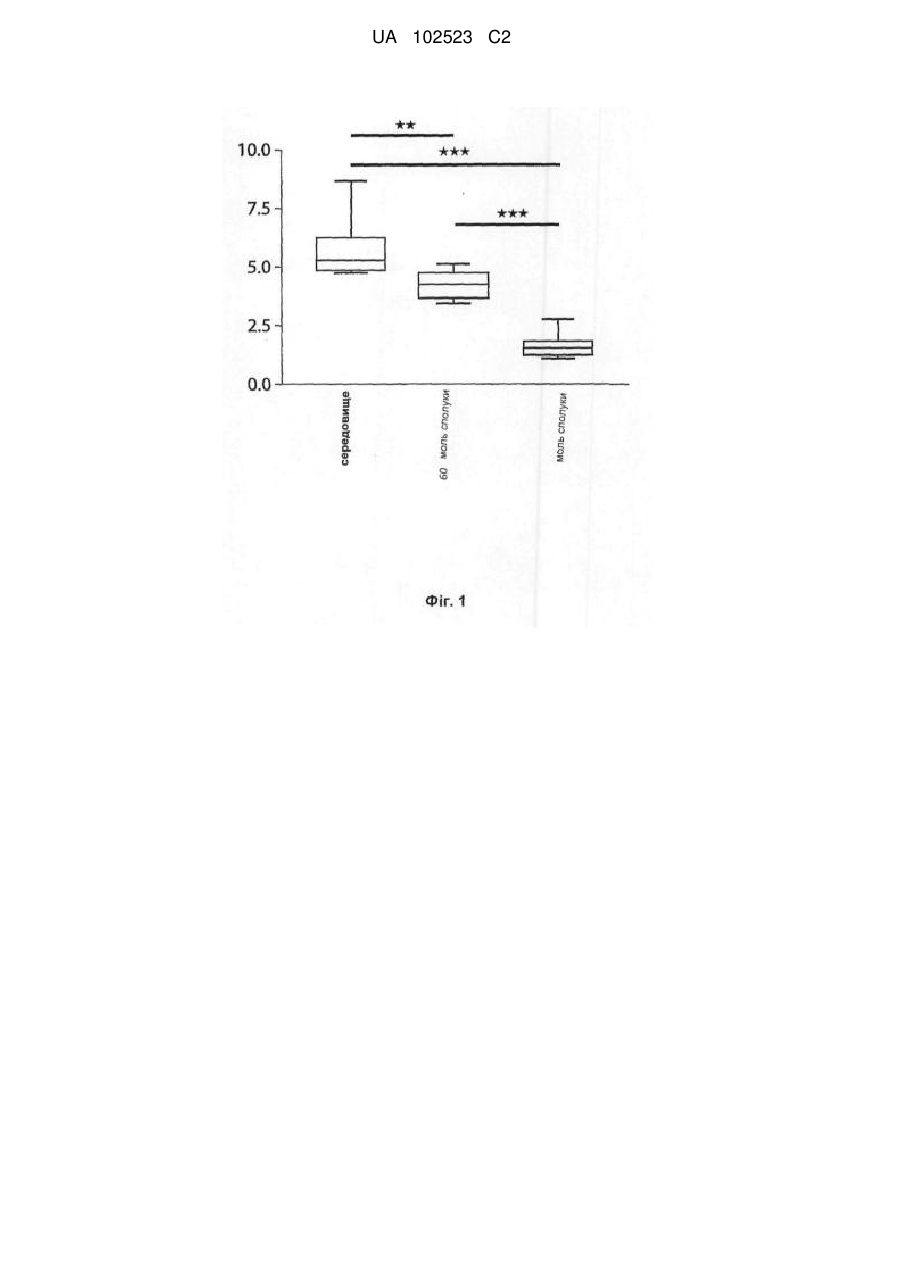
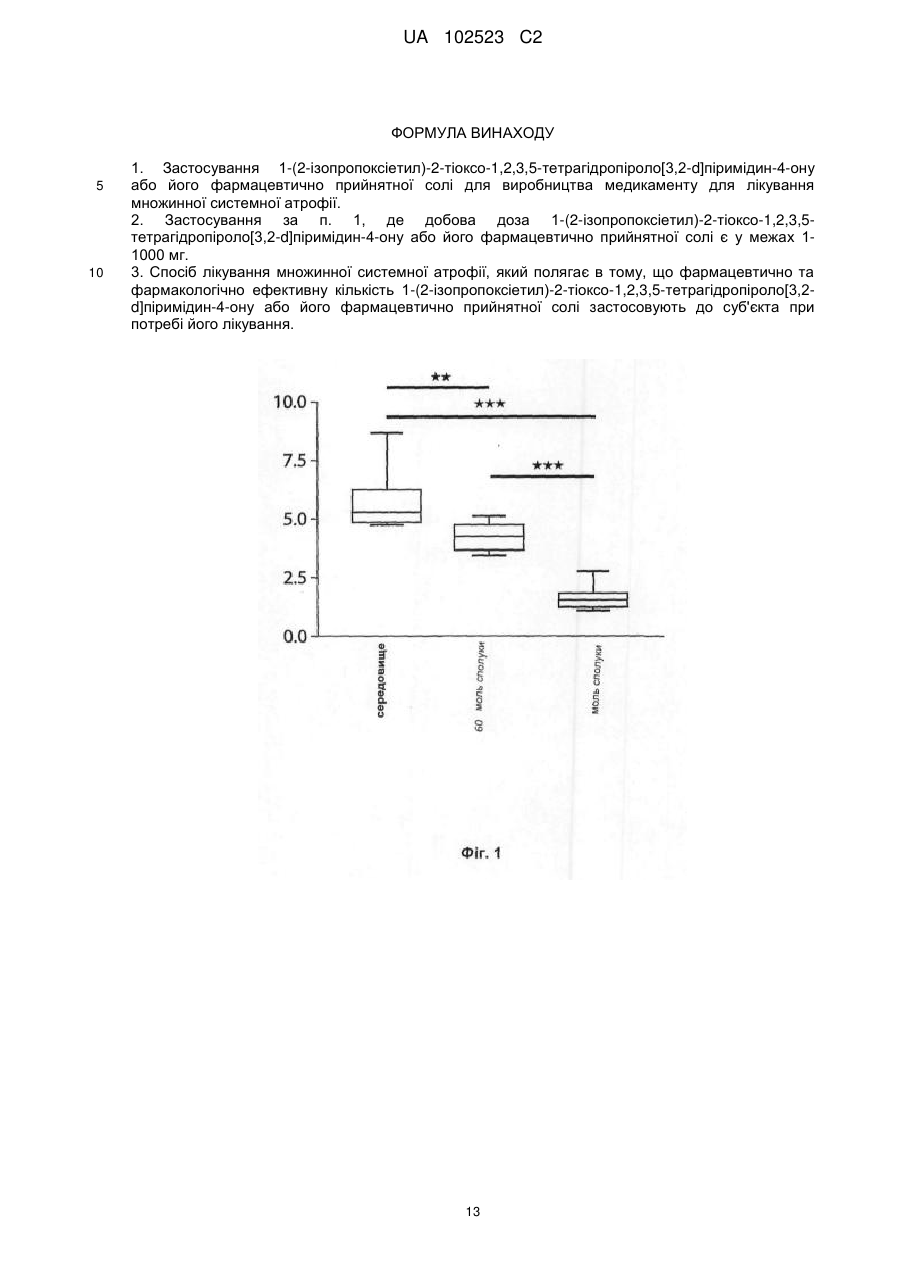
1. Застосування 1-(2-ізопропоксіетил)-2-тіоксо-1,2,3,5-тетрагідропіроло[3,2-d]піримідин-4-ону або його фармацевтично прийнятної солі для виробництва медикаменту для лікування множинної системної атрофії.
2. Застосування за п. 1, де добова доза 1-(2-ізопропоксіетил)-2-тіоксо-1,2,3,5-тетрагідропіроло[3,2-d]піримідин-4-ону або його фармацевтично прийнятної солі є у межах 1-1000 мг.
3. Спосіб лікування множинної системної атрофії, який полягає в тому, що фармацевтично та фармакологічно ефективну кількість 1-(2-ізопропоксіетил)-2-тіоксо-1,2,3,5-тетрагідропіроло[3,2-d]піримідин-4-ону або його фармацевтично прийнятної солі застосовують до суб'єкта при потребі його лікування.
Текст
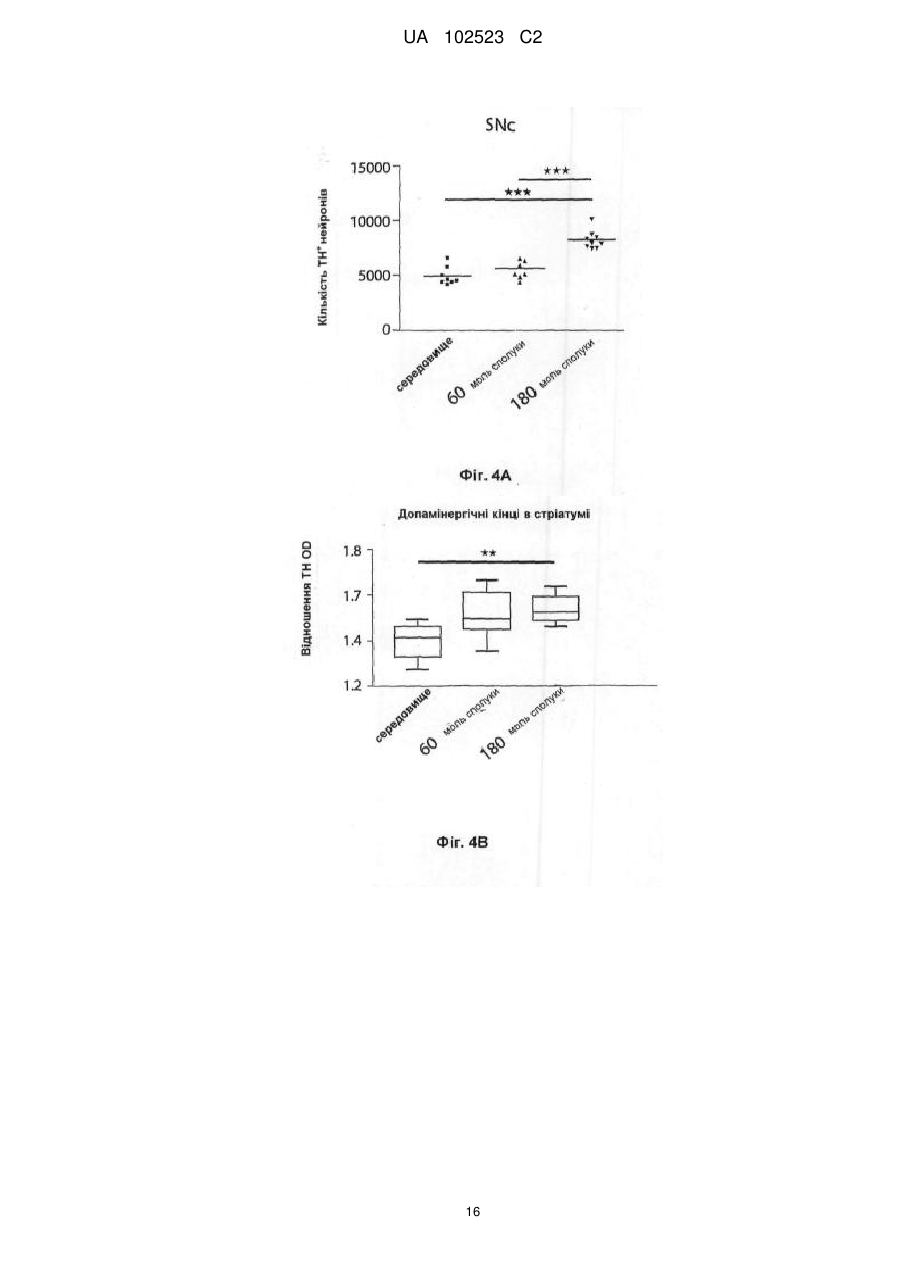
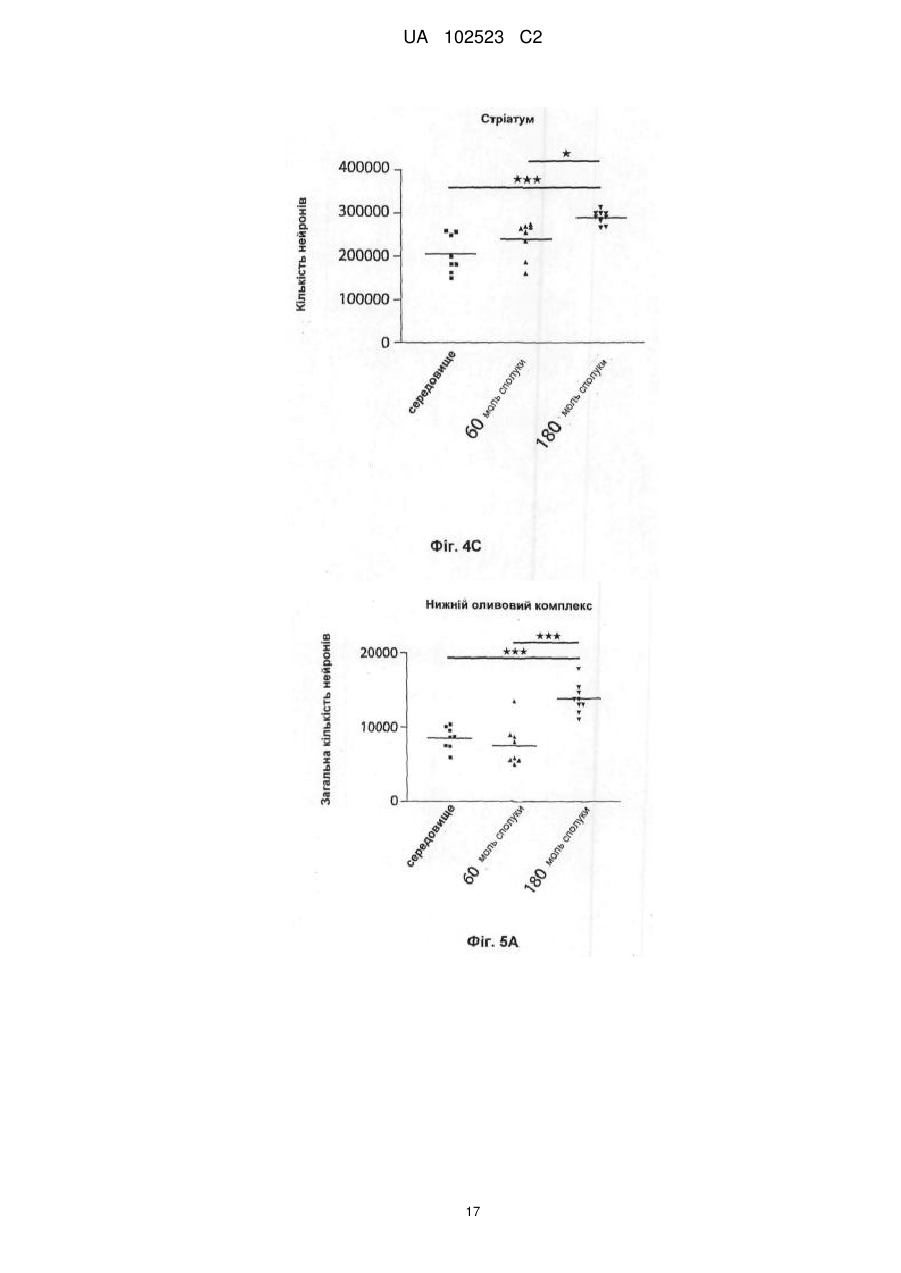
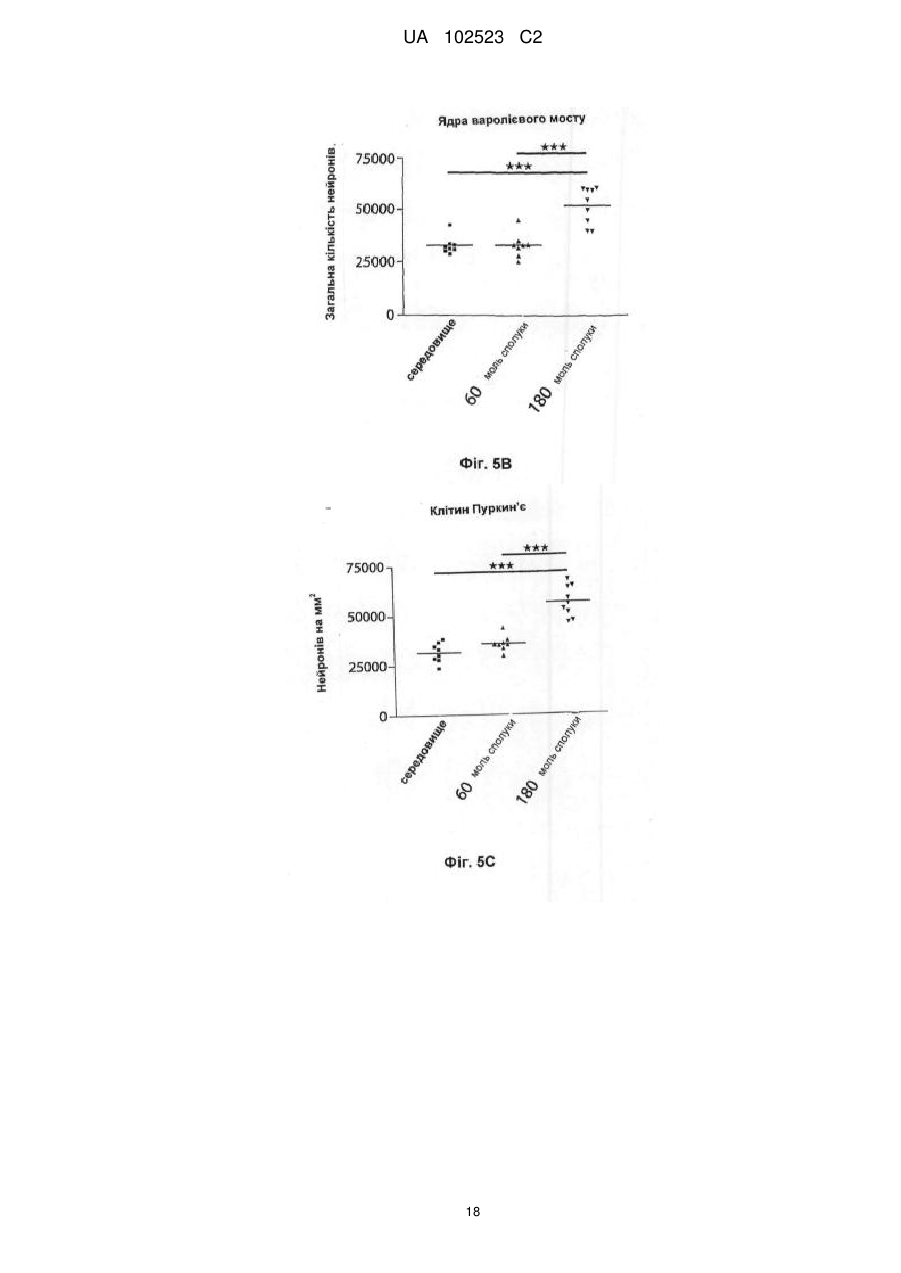
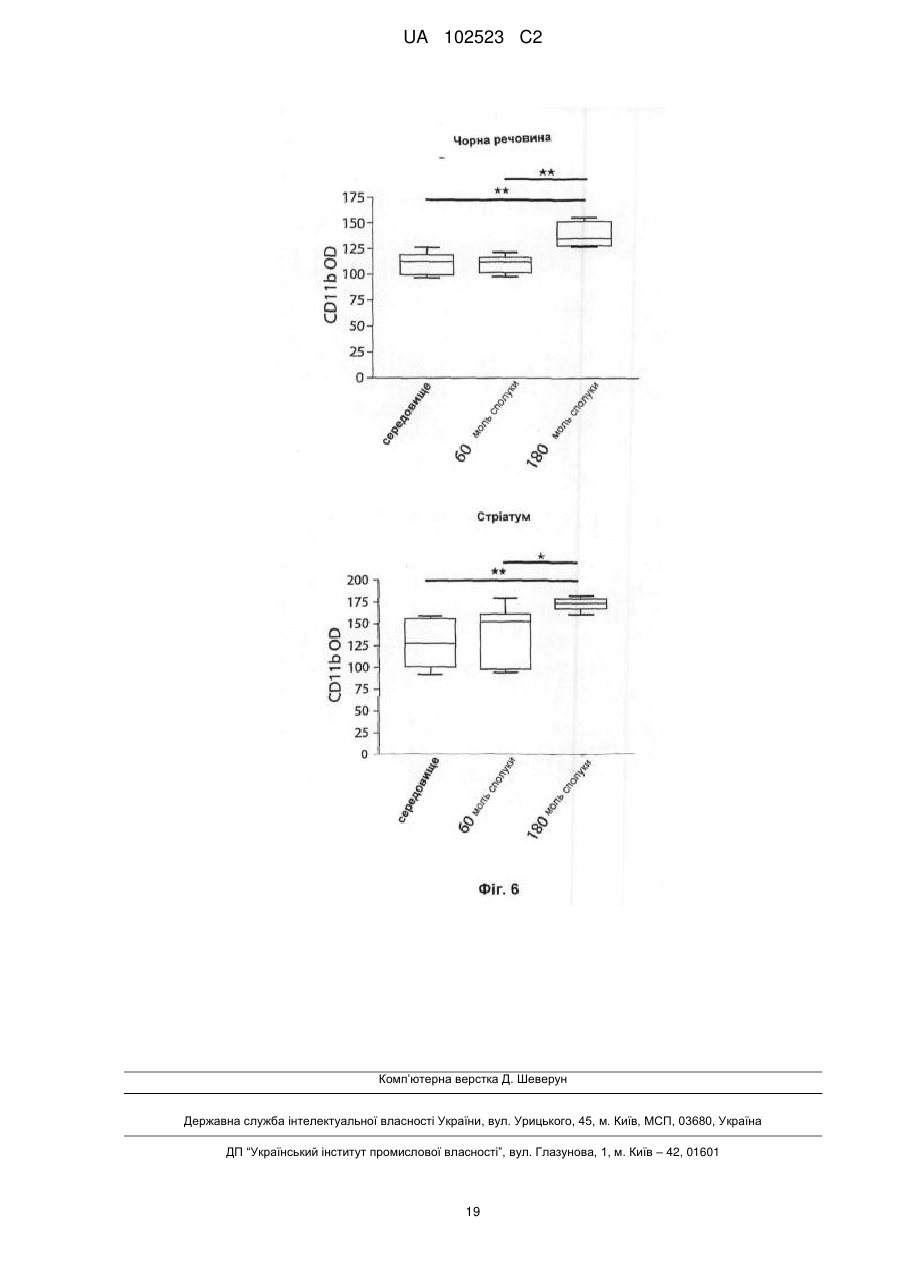
Реферат: Винахід належить до галузі медицини і стосується застосування інгібіторів мієлопероксидази (МРО), зокрема 1-(2-ізопропоксіетил)-2-тіоксо-1,2,3,5-тетрагідропіроло[3,2-d]піримідин-4-ону або його фармацевтично прийнятної солі, при лікуванні множинної системної атрофії. UA 102523 C2 (12) UA 102523 C2 UA 102523 C2 5 10 15 20 25 30 35 40 45 50 55 60 Заявлений винахід стосується застосування інгібіторів мієлопероксидази (MPO) або їх фармацевтично прийнятних солей для лікування множинної системної атрофії (MSA). Заявлений винахід також стосується застосування інгібіторів мієлопероксидази (MPO) або їх фармацевтично прийнятних солей для лікування хвороби Хантингтона (HD). Заявлений винахід також стосується застосування інгібіторів мієлопероксидази (MPO) або їх фармацевтично прийнятних солей для нейрозахисту. Мієлопероксидаза (MPO) − фермент з умістом гему переважно виявлено y поліморфонуклеарних лейкоцитах (PMN). MPO є одним зі членів сімейства різноманітних білків пероксидаз ссавців, що також охоплює пероксидазу еозинофілу, тироїдну пероксидазу, слинну пероксидазу, лактопероксидазу, простгландин-H-синтазу та інші. Зрілий фермент є димером ідентичних половин. Кожна половина молекули містить ковалентно зв’язаний гем, що виявляє незвичайні спектральні властивості, що відповідають характерному зеленому кольору MPO. Розщеплення дисульфідного містка, що зв’язує дві половини MPO, утворює гемі-фермент, що виявляє спектральні та каталітичні властивості, які не відрізняється від таких у цілого ферменту. Фермент застосовує гідрогенпероксид для окиснення хлориду до гіпохлоритної кислоти. Інші галогеніди та псевдогалогеніди (типу тіоціанату) також є фізіологічними субстратами щодо MPO. PMN є особливо важливими для агресивних інфекцій. Ці клітини містять MPO із добре документально підтвердженою мікробіцидною дією. PMN діють неспецифічно фагоцитозом щодо поглинання мікроорганізмів, інкорпоруванням їх у вакуолі, названі фагoсомами, котрі поєднуються із гранулами, що містять мієлопероксидазу, для утворення фагoлізосом. У фагoлізосомах ферментативна активність мієлопероксидази призводить до утворення гіпохлоритної кислоти, сильної бактерицидної сполуки. Гіпохлоритна кислота як така є окисником та реагує найбільш активно з тіолами та тіоетерами, але також перетворює аміни в хлораміни та хлорує ароматичні амінокислоти. Макрофаги є великими фагоцитарними клітинами типу PMN, котрі здатні до фагoцитозування мікроорганізмів. Макрофаги можуть генерувати гідрогенпероксид та після активації також утворювати мієлопероксидазу. MPO та гідрогенпероксид також може вивільнюватися із клітин, де реакція із хлоридом може індукувати ураження суміжної тканини. Взаємозв’язок між активністю мієлопероксидази та хворобою може залучатися y неврологічні хвороби з нейрозапальною реакцією, охоплюючи розсіяний склероз, хворобу Альцгеймера та хворобу Паркінсона. Реальні клітини MPO є досить наявними y кровообігу в тканині, що піддається запаленню. Більш конкретно MPO, що містить макрофаги, мікроглії, астрогліоцити та/або нейрони, засвідчувались протягом хвороби y ЦНС; при розсіяному склерозі (Nagra RM, et al. Journal of Neuroimmunology 1997; 78(1-2):97-107; Marik C, et al. Brain. 2007; 130: 2800-15; Gray E, et al. Brain Pathology. 2008; 18: 86-95), хворобі Паркінсона (Choi D-K. et al. J. Neurosci. 2005; 25(28):6594-600) та хворобі Альцгеймера (Reynolds WF, et al. Experimental Neurology. 1999; 155:31-41; Green PS. et al. Journal of Neurochemistry. 2004; 90(3):724-33). Це припускає, що деякі аспекти хронічних запалення призводять до величезної деструкції, де фактори від реакції MPO мають важливе значення. Фермент вивільняється зовнішньоклітинно, а також у фагoлізосоми в нейтрофіли (Hampton MB, Kettle AJ, Winterbourn CC. Кров 1998; 92(9):3007-17). Передумовою для активності MPO є присутність гідрогенпероксиду, генерованого оксидазою NADPH, та наступна дисмутація супероксиду. Окиснений фермент є здатним до застосування багатьох різних субстратів, із котрих найбільш визнаним є хлорид. Як результат цієї реакції утворюється сильний нерадикальний окисник - гіпохлоритна кислота (HOCl). HOCl дуже ефективно окиснює сульфур, який містять амінокислоти типу цистеїну та метіоніну (Peskin AV, Winterbourn CC. Free Radical Biology and Medicine 2001; 30(5):572-9). Це також утворює хлораміни з аміногрупою y білках та інших біомолекулах (Peskin AV. et al. Free Radical Biology and Medicine 2004; 37(10):1622-30). Це хлорує феноли (типу тирозину) (Hазеn SL. et al. Мас Free Radical Biology and Medicine 1997; 23(6):909-16) та ненасичені зв’язки y ліпідах (Albert CJ. et al. J. Biol. Chem. 2001; 276(26):2373341), окиснює центри феруму (Rosen H, Klebanoff SJ. Journal of Biological Chemistry 1982; 257(22):13731-354) та поперечно зшиті білки (Fu X, Mueller DM, Heinecke JW. Biochemistry 2002; 41(4):1293-301). Різні сполуки, що є інгібіторами MPO, розкрито в WO 01/85146, J. Heterocyclic Chemistry, 1992, 29, 343-354, J. Chem. Soc., 1962, 1863, WO03/089430 та WO2006/062465. Множинна системна атрофія (MSA) Множинна системна атрофія (MSA) є нейродегенеративним розладом, обумовленим автономною недостатністю та погіршенням моторності від L-допа-несприйнятливого паркінсонізму, мозочкової атаксії та пірамідальних симптомів. Гістологічно існує втрата нейронів 1 UA 102523 C2 5 10 15 20 25 30 35 40 45 50 55 y стріатумі, чорної субстанції pars compacta, мозочку, варолієвому мосту, нижніх оливах та міжмедіалатеральній колонці спинного хребта. Гліальна патологія охоплює астрогліоз, мікрогліальну активацію та α-синуклеїн, що містить олігодендрогліальні цитоплазматичні включення. Явне нейрозапалення із внеском активованої мікроглії, а також цитоплазматичних тілець включення, що містять агреговані та оксидативно модифіковані білки, робить це цікавим для розгляду важливого внеску активності MPO y прогресуючу нейродегенерацію, що характеризує патологію MSA. Підтримку для інгібування MPO y патології MSA-типу можна генерувати через застосування моделі доклінічної хвороби для MSA, подібної до трансгенних мишей з олігодендрогліальною надекспресією α-синуклеїну людини з або без додавання токсину типу 3-нітропропіонової кислоти. Хвороба Хантингтона (HD) Хвороба Хантингтона (HD) є спадкоємним прогресуючим нейродегенеративним розладом, що клінічно характеризується моторними та психіатричними розладами, та патологічно втратою нейронів та гліозом (реакційний астрoцитоз), зокрема, y стріатумі та корі головного мозку. HD є нейродегенеративним розладом, спричиненим розповсюдженням повторного CAG y ген HD, що кодує поліглутамін y білку хантингтину. Пояснення патологічних механізмів охоплюють оксидативний стрес, послаблений енергетичний метаболізм та аномальні взаємодії білок–білок. Такі механізми є можливими для зв’язування активності MPO, котрі можуть виявлятися через спостережену надекспресію y патологічну тканину HD (Choi D-K. et al. J. Neurosci. 2005; 25(28):6594-600). Підтримку для інгібування MPO y патології HD-типу можна генерувати через застосування моделі доклінічної хвороби для HD. Такими моделями можуть бути миші або щури, оброблені мітохондріальними токсинами типу 3-нітропропіонової кислоти або малонату (Matthews RT. et al J. Neurosci. 1998; 18:156-63). Корисними моделями також можуть бути трансгенні миші, які експресують мутанти білку хантінгтіну з або без додавання токсину типу 3-нітропропіонової кислоти (Bogdanov MB. et al. J. Neurochem. 1998; 71:2642-44). Існує велика незадоволена потреба в медикаментах, які можна застосовувати для лікування хвороби Хантингтона, для лікування множинної системної атрофії та/або для нейрозахисту. Виявлено, що інгібітори MPO можна застосовувати для лікування множинної системної атрофії (MSA). Отже, заявлений винахід стосується застосування інгібітору MPO для виробництва медикаменту для лікування множинної системної атрофії (MSA). Формулювання "множинна системна атрофія", як тут застосовано, означає згубний прогресуючий нейродегенеративний розлад. Це означає спорадичну альфа-синуклеїнoпатію з вегетативною дистонією та паркинсонічною та/або мозочковою моторною недостатністю. Також виявлено, що інгібітори MPO або їх фармацевтично прийнятні солі можна застосовувати для лікування хвороби Хантингтона (HD). Отже, заявлений винахід також стосується застосування інгібітору MPO або його фармацевтично прийнятної солі для виробництва медикаменту для лікування хвороби Хантингтона. Формулювання "хвороба Хантингтона", як тут застосовано, означає спадкоємний прогресуючий нейродегенеративний розлад, що клінічно характеризується моторними та психіатричними розладами та патологічно характеризується втратою нейронів та гліозу (реакційний астрoцитоз), зокрема, y стріатумі та корі головного мозку. Далі заявлений винахід також стосується застосування інгібіторів MPO або їх фармацевтично прийнятної солі для нейрозахисту. Отже, заявлений винахід стосується застосування інгібітору MPO для виробництва медикаменту для нейрозахисту. Термін “нейрозахист”, як тут застосовано, визначено як запобігання втрати нервових клітин та/або резерву волокон нервових клітин. Термін "лікування", як тут застосовано, стосується реверсування, пом’якшення, затримання або інгібування розвитку або запобігання розладу або стану, до котрого такий термін стосується, або одного або більше симптомів такого розладу або стану. Приклади сполук, що можна застосовувати як MPO-інгібітори, є наступними: 1) Сполука формули (I) 2 UA 102523 C2 Y H H N N (I) X N R L R 5 10 15 20 25 30 35 40 45 50 12 1 де: Принаймні, один X та Y – S, та інший – O або S; L – безпосередній зв’язок або C1-7алкілен, де вказаний C1-7алкілен, як варіант, містить 6 гетероатом, вибраний із групи: O, S (O) n та NR , та вказаний C1-7алкілен, як варіант, містить один або два подвійні зв’язки карбон-карбон, та вказаний C1-7алкілен, як варіант, заміщено 4 5 одним або більше замісниками, незалежно вибраними із групи: OH, галоген, CN та NR R , C16алкіл та C1-6алкоксил, вказаний C1-6алкоксил, як варіант, містить карбоніл, суміжний з оксигеном; n – ціле число 0, 1 або 2; 1 R – гідроген або 1 R – насичене або частково ненасичене 3 – 7-членне кільце, що, як варіант, містить один або два гетероатоми, незалежно вибрані із групи: O, N та S, та, як варіант, містить карбоніл, де вказане кільце, як варіант, заміщено одним або більше замісниками, незалежно вибраними із 9 9 10 2 3 2 3 3 групи: галоген, SO2R , SO2NR R , OH, C1-7алкіл, C1-7алкоксил, CN, CONR R , NR COR та COR , де вказаний C1-7алкоксил, як варіант, далі заміщено C1-6алкоксилом, та, як варіант, містить карбоніл суміжний з оксигеном, та вказаний C1-7алкіл, як варіант, далі заміщено гідроксилом або C1-6алкоксилом, та вказаний C1-7алкіл або C1-6алкоксил, як варіант, містить карбоніл, суміжний з оксигеном або на будь-якій позиції в C1-7алкілі; або 1 R – ароматична кільцева система, вибрана із групи: феніл, біфеніл, нафтил або моноциклічна або біциклічна гетероароматична кільцева структура, що містить 1 – 3 гетероатоми, незалежно вибрані із групи: O, N та S, указана ароматична кільцева система, як варіант, є заміщеною одним або більше замісниками, незалежно вибраними із групи: галоген, 9 9 10 2 3 2 3 3 SO2R , SO2NR R , OH, C1-7алкіл, C1-7алкоксил, CN, CONR R , NR COR та COR ; вказаний C17алкоксил, як варіант, далі заміщено C1-6алкоксилом, та вказаний C1-6алкоксил, як варіант, містить карбоніл, суміжний з оксигеном, та вказаний C1-7алкіл, як варіант, далі заміщено гідроксилом або C1-6алкоксилом та вказаний C1-7алкіл або C1-6алкоксил, як варіант, містить карбоніл, суміжний з оксигеном або на будь-якій позиції в алкілі; 12 R – гідроген, галоген або карбон, як варіант, заміщений одним – трьома атомами галогену; 2 3 4 5 6 9 10 у кожному випадку, R , R , R , R , R , R та R незалежно – гідроген, C1-6алкіл або C16алкоксил, указаний алкоксил, як варіант, містить карбоніл, суміжний з оксигеном, указаний C 16алкіл, як варіант, далі заміщено наступним: галоген, C 1-6алкоксил, CHO, C2-6алканоїл, OH, 7 8 7 8 CONR R та NR COR ; 2 3 4 5 9 10 або групи NR R , NR R та NR R кожна незалежно – 5 – 7-членне насичене азациклічне 11 кільце, яке, як варіант, містить один додатковий гетероатом, вибраний із групи: O, S та NR , указане азациклічне кільце, як варіант, далі заміщено наступним: галоген, C1-6алкоксил, CHO, 7 8 7 8 C2-6алканоїл, OH, CONR R та NR COR ; 7 8 11 7 8 у кожному випадку R , R та R незалежно – гідроген або C1-6алкіл, або група NR R – 5 – 7членне насичене азациклічне кільце, яке, як варіант, містить один додатковий гетероатом, 11 вибраний із групи: O, S та NR ; або її фармацевтично прийнятні солі, сольвати, сольвати їх солей. Ці сполуки описано в WO 2006/062465. 2) Сполука, вибрана із групи: 1-бутил-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-iзoбутил-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-(піридин-2-ілметил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-(2-флуор-бензил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-[2-(2-метоксіетокси)-3-пропоксибензил]-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин4-он; 1-(6-етокси-піридин-2-ілметил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-піперидин-3-ілметил-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-бутил-4-тіоксо-1,3,4,5-тетрагідро-2H-піроло[3,2-d]піримідин-2-он; 1-(2-iзoпропоксіетил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 3 UA 102523 C2 1-(2-метокси-2-метилпропіл)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-(2-етокси-2-метилпропіл)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-(піперидин-4-ілметил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-[(1-метилпіперидин-3-іл)метил]-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-[2-гідрокси-2-(4-метоксифеніл)етил]-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-(2-метоксибензил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-(3-метоксибензил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-(2,4-диметоксибензил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-[(3-хлорпіридин-2-іл)метил]-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-{[3-(2-етоксіетокси)піридин-2-іл]метил}-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4 5 10 он; 1-[(6-оксо-1,6-дигідропіридин-2-іл)метил]-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4он; 1-(1H-індол-3-ілметил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-(1H-бензімідазол-2-ілметил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-[(5-хлоро-1H-індол-2-іл)метил]-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-[(5-флуоро-1H-індол-2-іл)метил]-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-(1H-індол-6-ілметил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-(1H-індол-5-ілметил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-[(5-флуоро-1H-індол-3-іл)метил]-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-(1H-імідазол-5-ілметил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-(1H-імідазол-2-ілметил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; 1-[(5-хлоро-1H-бензімідазол-2-іл)метил]-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4 15 20 он; 25 30 1-[(4,5-диметил-1H-бензімідазол-2-іл)метил]-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2d]піримідин-4-он; 7-бромо-1-iзoбутил-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; та 1-(3-хлорфеніл)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он; або її фармацевтично прийнятні солі, сольват або сольват її солі. Ці сполуки описано в WO 2006/062465. 3) Сполука формули (IIa) або (IIb) 15 Y R Y R 13 X R N N R N N R 14 16 13 X 40 45 R N R 16 N 15 R 14 (IIb) (IIa) 35 N N or де: один X та Y – S, та інший – O або S; 13 R – гідроген або C1-6алкіл; 14 R – гідроген або C1-6алкіл; указаний C1-6алкіл, як варіант, заміщено наступним: i) насичене або частково ненасичене 3 – 7-членне кільце, як варіант, містить один або два гетероатоми, незалежно вибрані із групи: O, N та S, та, як варіант, містить карбоніл; указане кільце, як варіант, заміщено одним або більше замісниками, незалежно вибраними із групи: галоген, гідроксил, C1-6алкоксил та C1-6алкіл; указаний C1-6алкіл, як варіант, далі заміщено гідроксилом або C1-6алкоксилом; або ii) C1-6алкоксил; або iii) ароматичне кільце, вибране із групи: феніл, фурил або тiєніл; указане ароматичне кільце, як варіант, далі заміщено наступним: галоген, C1-6алкіл або C1-6алкоксил; 15 16 R та R незалежно – гідроген або C1-6алкіл; або її фармацевтично прийнятна сіль, сольват або сольват її солі. Ці сполуки описано в WO 2003/089430. Згідно з одним аспектом заявленого винаходу вказаний інгібітор MPO вибрано зі сполуки формули (IIa) або (IIb) 4 UA 102523 C2 15 Y Y R 13 R R N N 16 R N N X 13 14 X 15 20 25 30 35 40 N N 15 R R (IIb) (IIa) 10 16 R 14 R 5 N N or де: X – S, та Y – O; 13 R – гідроген або C1-6алкіл; 14 R – C1-6алкіл, заміщений насиченим або частково ненасиченим 3 – 7-членним кільцем, як варіант, містить один або два гетероатоми, незалежно вибрані із групи: O, N та S, та, як варіант, містить карбоніл; указане кільце, як варіант, заміщено одним або більше замісниками, незалежно вибраними із групи: галоген, гідроксил, C 1-6алкоксил та C1-6алкіл; указаний алкіл, як варіант, далі заміщено гідроксилом або C1-6алкоксилом; 15 16 R та R незалежно – гідроген або C1-6алкіл; або фармацевтично прийнятні солі, сольвати або сольвати їх солі. Ці сполуки описано в WO 2003/089430. 4) Сполука, вибрана із групи:: 1,3-діізoбутил-8-метил-6-тіоксантин; 1,3-дибутил-8-метил-6-тіоксантин; 3-iзoбутил-1,8-диметил-6-тіоксантин; 3-(2-метилбутил)-6-тіоксантин; 3-iзoбутил-8-метил-6-тіоксантин; 3-iзoбутил-2-тіоксантин; 3-iзoбутил-2,6-дитіоксантин; 3-iзoбутил-8-метил-2-тіоксантин; 3-iзoбутил-7-метил-2-тіоксантин; 3-циклогексилметил-2-тіоксантин; 3-(3-метоксипропіл)-2-тіоксантин; 3-циклопропілметил-2-тіоксантин; 3-iзoбутил-1-метил-2-тіоксантин; 3-(2-тетрагідрофурил-метил)-2-тіоксантин; 3-(2-метокси-етил)-2-тіоксантин; 3-(3-(1-морфолініл)-пропіл)-2-тіоксантин; 3-(2-фурил-метил)-2-тіоксантин; 3-(4-метоксибензил)-2-тіоксантин; 3-(4-флуорбензил)-2-тіоксантин; 3-фенетил-2-тіоксантин; (+)-3-(2-тетрагідрофурил-метил)-2-тіоксантин; (-)-3-(2-тетрагідрофурил-метил)-2-тіоксантин; та 3-н-бутил-2-тіоксантин; або її фармацевтично прийнятна сіль, сольват або сольват її солі. Ці сполуки описано в WO 2003/089430. (-)-Енантіомер 3-(2-тетрагідрофурил-метил)-2-тіоксантин – 3-(2R-тетрагідрофурил-метил)-2тіоксантин та (+)-енантіомер 3-(2-тетрагідрофурил-метил)-2-тіоксантин – 3-(2Sтетрагідрофурил-метил)-2-тіоксантин. 5) Сполука формули (III) Y H H N N X N N L R 17 III 5 UA 102523 C2 5 10 15 20 25 30 35 40 45 50 55 60 де Принаймні, один X та Y – S, та інший – O або S; 18 19 20 18 19 20 L – (R )p-Q-(CR R )r; де (R )p та (CR R )r кожний, як варіант, містить один або два подвійні або потрійні зв’язки; 21 21 21 де Q – O, S(O)n, NR , NR C(O), C(O)NR або зв’язок; 18 де R вибрано із групи: C1-6алкіл або C1-6алкоксил, указаний C1-6алкіл або вказаний C122 23 6алкоксил, як варіант, заміщено наступним: OH, галоген, CF 3, CHF2, CFH2, CN, NR R , феноксил або арил; та, де вказаний феноксил, як варіант, заміщено наступним: C 1-6алкіл, галоген або C1-6алкоксил; та, де вказаний феноксил, як варіант, містить карбоніл, суміжний з оксигеном та, де вказаний C1-6алкоксил, як варіант, містить карбоніл, суміжний з оксигеном; 19 20 де R та R незалежно вибрані із групи: гідроген, OH, галоген, CF 3, CHF2, CFH2, CN, 22 23 NR R , C1-6алкіл, феноксил та C1-6алкоксил; де вказаний феноксил або C1-6алкоксил, як варіант, містить карбоніл, суміжний з оксигеном; та, де вказаний феноксил, як варіант, заміщено наступним: C1-6алкіл, галоген або C1-6алкоксил; де p – ціле число 0, 1, 2, 3 або 4 та r – ціле число 0, 1, 2, 3 або 4; та, де 1 < p+ r < 7; 17 R – моно- або біциклічна гетероароматична кільцева система, що містить один або більше гетероатомів, вибраних із групи: N, O та S; де вказана моно- або біциклічна гетероароматична кільцева система, як варіант, є конденсованою з одним або двома 5- або 6-членними насиченими або частково насиченими кільцями, що містять один або більше атомів, вибраних із групи: C, N, O та S, де вказана моно- або біциклічна гетероароматична кільцева система як така або конденсована з одним або двома 5- або 6- членними насиченими або частково насиченими кільцями, як варіант, є заміщеною одним або більше замісниками, незалежно вибраними із 24 24 25 26 22 23 групи: галоген, CHF2, CH2F, CF3, SO(n)R , SO(n)NR R , (CH2)nR , NR R , OH, C1-7алкіл, C127 26 2 26 26 7алкоксил, феноксил, арил, CN, C(O)NR R , NR C(O)R , C(O)R , 5- або 6-членне насичене або частково насичене кільце, що містить один або більше атомів, вибраних із групи: C, N, O або S, та моно- або біциклічна гетероароматична кільцева система, що містить один або більше гетероатомів, вибраних із групи: N, S або O; та, де вказаний C1-7алкоксил, як варіант, заміщено наступним: C1-7алкоксил або арил; та, де вказаний C 1-7алкоксил або указаний феноксил, як варіант, містить карбоніл, суміжний з оксигеном; та, де вказаний C 1-7алкіл, як варіант, заміщено гідроксилом або C1-6алкоксилом; та, де вказаний C1-7алкіл, як варіант, містить карбоніл на будьякій позиції в C1-7алкілі; та, де вказаний феноксил, як варіант, заміщено наступним: C 1-6алкіл, галоген або C1-6алкоксил; 27 26 22 23 21 24 25 у кожному випадку, R , R , R , R , R , R та R незалежно вибрано із групи: гідроген, C16алкіл, C1-6алкоксил, арил та феноксил; указаний C 1-6алкоксил або феноксил, як варіант, містить карбоніл, суміжний з оксигеном; та вказаний C1-6алкіл, як варіант, заміщено наступним: галоген, 28 29 28 29 C1-6алкоксил, CHO, C2-6алканоїл, OH, C(O)NR R або NR C(O)R ; та вказаний арил або указаний феноксил, як варіант, заміщено наступним: C1-6алкіл, галоген або C1-6алкоксил; 27 26 22 23 24 25 або групи NR R , NR R та NR R кожна незалежно – 5 – 7-членне насичене азациклічне кільце, яке, як варіант, містить один додатковий гетероатом, вибраний із групи: O, S 30 та NR , указане кільце, як варіант, далі заміщено наступним: галоген, C 1-6алкоксил, CHO, C228 29 28 29 або NR C(O)R ; 6алканоїл, OH, C(O)NR R 28 29 30 28 29 у кожному випадку R , R та R незалежно – гідроген або C1-6алкіл, або група NR R – 5 – 7-членне насичене азациклічне кільце, яке, як варіант, містить один додатковий гетероатом, 30 вибраний із групи: O, S та NR ; n – ціле число 0, 1 або 2; 17 за умови, що для R тiєніл або фурил є виключеними; 21 21 21 та за умови, що коли Q – O, S(O)n, NR , NR C(O) або C(O)NR , тоді є p більшим або дорівнює 1; або її фармацевтично прийнятна сіль, сольват або сольват її солі. Ці сполуки описано в PCT/SE2007/000349. 6) Сполука, вибрана із групи:: 3-(піридин-2-ілметил)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-(піридин-3-ілметил)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-(піридин-4-ілметил)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-{[3-етокси-4-(2-етоксіетокси)піридин-2-іл]метил}-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[(5-флуоро-1H-індол-2-іл)метил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[(5-флуоро-1H-індол-2-іл)метил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[(2-бутил-4-хлоро-1H-імідазол-5-іл)метил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-(1H-бензімідазол-2-ілметил)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[1-(1H-бензімідазол-2-іл)етил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 6 UA 102523 C2 5 10 15 20 25 30 35 40 45 50 55 60 3-[(5-хлоро-1H-індол-3-іл)метил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он та 3-[(4-флуоро-1H-індол-3-іл)метил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[2-(1H-бензімідазол-2-іл)етил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-(1H-піразол-3-ілметил)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[(5-метилпіразин-2-іл)метил)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[(3-ізoпропілізоксазол-5-іл)метил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[(4-метил-1,2,5-оксадіазол-3-іл)метил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[(6-бутоксипіридин-2-іл)метил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[(4-бутоксипіридин-2-іл)метил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[(3-бутоксипіридин-2-іл)метил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[2-(піридин-2-ілметокси)пропіл]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[(3,5-диметилізоксазол-4-іл)метил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[(1-детил-1H-індол-2-іл)метил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-(2-феніл-2-піридин-2-ілетил)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-(хінолін-4-ілметил)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[(6-феноксипіридин-3-іл)метил]-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-{2-[(хінолін-4-ілметил)аміно]етил}-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-(2-{[(1-метил-1H-індол-3-іл)метил]аміно}етил)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-{2-[метил(хінолін-4-ілметил)аміно]етил}-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-(2-амінопропіл)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он трифлуорацетат; 3-{2-[(піридин-2-ілметил)аміно]пропіл}-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он трифлуорацетат; 3-{2-[(піридин-3-ілметил)аміно]пропіл}-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-{2-[(піридин-4-ілметил)аміно]пропіл}-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-(2-{[(6-хлорпіридин-3-іл)метил]аміно}пропіл)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он трифлуорацетат; 3-[2-({[6-(трифлуорметил)піридин-3-іл]метил}аміно)пропіл]-2-тіоксо-1,2,3,7-тетрагідро-6Hпурин-6-он трифлуорацетат; 3-(2-{[(4,6-дихлорпіримідин-5-іл)метил]аміно}пропіл)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6он; 3-[2-({[2-(диметиламіно)піримідин-5-іл]метил}аміно)пропіл]-2-тіоксо-1,2,3,7-тетрагідро-6Hпурин-6-он; 3-{2-[(хінолін-2-ілметил)аміно]пропіл}-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он трифлуорацетат; 3-{2-[(хінолін-3-ілметил)аміно]пропіл}-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-(2-{[(1-трет-бутил-3,5-диметил-1H-піразол-4-іл)метил]аміно}пропіл)-2-тіоксо-1,2,3,7тетрагідро-6H-пурин-6-он; 3-[2-({[1-(1,1-діоксидотетрагідро-3-тiєніл)-3,5-диметил-1H-піразол-4-іл]метил} аміно)пропіл]2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-{2-[(1H-бензоімідазол-2-ілметил)аміно]пропіл}-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[2-({[1-(фенілсульфоніл)-1H-пірол-2-іл]метил}аміно]пропіл]-2-тіоксо-1,2,3,7-тетрагідро-6Hпурин-6-он трифлуорацетат; 3-{2-[({1-[(4-метилфеніл)сульфоніл]-1H-пірол-2-іл}метил)аміно]пропіл}-2-тіоксо-1,2,3,7тетрагідро-6H-пурин-6-он трифлуорацетат; 3-(2-{[(1-метил-1H-пірол-2-іл)метил]аміно}пропіл)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-[2-({[1-(4-втор-бутилфеніл)-1H-пірол-2-іл]метил}аміно)пропіл)-2-тіоксо-1,2,3,7-тетрагідро6H-пурин-6-он; 3-[2-({[1-(3-метоксифеніл)-1H-пірол-2-іл]метил}аміно)пропіл]-2-тіоксо-1,2,3,7-тетрагідро-6Hпурин-6-он; 3-[2-({[2,5-диметил-1-(1,3-тіазол-2-іл)-1H-пірол-3-іл]метил}аміно)пропіл]-2-тіоксо-1,2,3,7тетрагідро-6H-пурин-6-он; 3-[2-({[4-(3-хлорбензоїл)-1-метил-1H-пірол-2-іл]метил}аміно)пропіл]-2-тіоксо-1,2,3,7тетрагідро-6H-пурин-6-он; 3-{2-[(1H-імідазол-2-ілметил)аміно]пропіл}-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 3-(2-{[(1-метил-1H-імідазол-2-іл)метил]аміно}пропіл)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6он; 3-(2-{[(4-бромо-1-метил-1H-імідазол-5-іл)метил]аміно}пропіл)-2-тіоксо-1,2,3,7-тетрагідро-6Hпурин-6-он; 3-(2-{[(1-метил-1H-індол-3-іл)метил]аміно}пропіл)-2-тіоксо-1,2,3,7-тетрагідро-6H-пурин-6-он; 2-тіоксо-3-{2-[(1H-1,2,3-триазол-5-ілметил)аміно]пропіл}-1,2,3,7-тетрагідро-6H-пурин-6-он; 7 UA 102523 C2 5 10 15 20 25 30 35 40 45 50 55 60 3-[2-({[1-(бензилокси)-1H-імідазол-2-іл]метил}аміно)пропіл]-2-тіоксо-1,2,3,7-тетрагідро-6Hпурин-6-он; 3-(2-{[(6-бромо-2-метилімідазо[1,2-a]піридин-3-іл)метил]аміно}пропіл}-2-тіоксо-1,2,3,7тетрагідро-6H-пурин-6-он; 3-{2-[({1-[2-(2-метоксифенокси)етил]-1H-пірол-2-іл}метил)аміно]пропіл]-2-тіоксо-1,2,3,7тетрагідро-6H-пурин-6-он; N-[1-метил-2-(6-оксо-2-тіоксо-1,2,6,7-тетрагідро-3H-пурин-3-іл)етил]піридин-2-карбоксамід; N-[1-метил-2-(6-оксо-2-тіоксо-1,2,6,7-тетрагідро-3H-пурин-3-іл)етил]нікотинамід; N-[1-метил-2-(6-оксо-2-тіоксо-1,2,6,7-тетрагідро-3H-пурин-3-іл)-етил] iзoнікотинамід; N-[1-метил-2-(6-оксо-2-тіоксо-1,2,6,7-тетрагідро-3H-пурин-3-іл)етил]-1,8-нафтиридин-2карбоксамід; N-[1-метил-2-(6-оксо-2-тіоксо-1,2,6,7-тетрагідро-3H-пурин-3-іл)етил]хінолін-2-карбоксамід; N-[1-метил-2-(6-оксо-2-тіоксо-1,2,6,7-тетрагідро-3H-пурин-3-іл)етил]піримідин-2-карбоксамід; та N-[1-метил-2-(6-оксо-2-тіоксо-1,2,6,7-тетрагідро-3H-пурин-3-іл)етил]-1H-імідазол-2карбоксамід трифлуорацетат; або її фармацевтично прийнятна сіль, сольват або сольват її солі. Ці сполуки описано в PCT/SE2007/000349. Для застосування в медицині фармацевтично прийнятні солі можуть бути корисними для отримання сполук згідно із заявленим винаходом. Описані тут придатні фармацевтично прийнятні солі сполук охоплюють кислотно-адитивні солі, котрі, наприклад, можна отримувати змішуванням розчину сполуки, згідно із заявленим винаходом, з розчином фармацевтично прийнятної кислоти, як-то хлоридна кислота, сульфатна кислота, метансульфонова кислота та фумарова кислота. Крім того, де сполуки мають кислотну частину, їх придатні фармацевтично прийнятні солі можуть охоплювати солі лужних металів, наприклад, солі натрію або калію; солі лужноземельних металів, наприклад, солі кальцію або магнію; та солі, утворені із придатними органічними лігандами, наприклад, четвертинні солі амонію. Вираз "фармацевтично прийнятні солі" охоплює фармацевтично прийнятні кислотноадитивні солі та фармацевтично прийнятні катіонні солі. Вираз "фармацевтично прийнятні катіонні солі" означає, але без обмеження, такі солі, як солі лужних металів, (наприклад, натрію та калію), солі лужноземельних металів (наприклад, кальцію та магнію), солі алюмінію, солі амонію, та солі з органічними амінами, як-то бензaтин (N,N'-дибензилетилендіамін) та холін. Вираз "фармацевтично прийнятні кислотно-адитивні солі" означає, але без обмеження, так солі, як гідрохлорид, гідробромід та сульфат. Фармацевтично прийнятні катіонні солі, що містять вільні карбонові кислоти, можна легко отримувати реакцією вільної кислотної форми із прийнятною основою. Типовими основами є натрій гідроксид, натрій метоксид та натрій етоксид. Фармацевтично прийнятні кислотноадитивні солі, що містять вільні групи аміну, можна легко отримувати реакцією вільної основної форми із прийнятною кислотою. Застосування оптичних ізомерів інгібіторів MPO є також у рамках заявленого винаходу. Інгібітори MPO, що мають асиметричний атом карбону, є хіральними сполуками, і залежно від присутності асиметричних атомів інгібітори MPO можуть існувати у формі сумішей ізомерів, зокрема, рацематів, або у формі чистих ізомерів, як-то конкретні енантіомери. Фармацевтичні композиції Описані тут інгібітори MPO або їх фармацевтично прийнятні солі можна застосовувати стандартними способами, як-то перорально, парентерально, через слизову оболонку (наприклад, сублінгвально або букально), місцево, трансдермально, ректально, інгаляцією (наприклад, назально або глибокою інгаляцією в легені). Парентеральне застосування охоплює, але без обмеження, внутрішньовенне, інтраартеріальне, інтраперитонеальне, підшкірне, внутрішньом’язове, інтратекальне або способом високого тиску. Для букального застосування інгібітори MPO або їх фармацевтично прийнятні солі можуть бути у формі таблеток або пастилок, утворених звичайним способом. Наприклад, таблетки та капсули для перорального застосування можуть містити звичайні наповнювачі, як-то зв’язуючі (наприклад, сироп, гуміарабік, желатина, сорбіт, трагакант, рослинний клей із крохмалю або полівінілпіролідон), наповнювачі (наприклад, лактоза, мікрокристалічна целюлоза, крохмаль із маїсу, кальцій фосфат або сорбіт), змащувачі (наприклад, магній стеарат, стеаринова кислота, тальк, поліетиленгліколь або діоксид силіцію), дезінтегратори (наприклад, картопляний крохмаль або натрій крохмаль-гліколят), або зволожувальні агенти (наприклад, натрій лаурилсульфат). Таблетки можна покривати способами, які добре відомі в рівні техніки. Такі препарати також можна формувати як супозиторії для ректального застосування, які, 8 UA 102523 C2 5 10 15 20 25 30 35 40 45 50 55 60 наприклад, містять звичайні основи супозиторію, як-то масло какао або інші гліцериди. Композиції для інгаляції, що містять інгібітори MPO або їх фармацевтично прийнятні солі типово постачають у формі розчину, суспензії або емульсії, та їх можна застосовувати у вигляді сухого порошку, або у формі аерозолю, застосовуючи звичайний пропелент, як-то дихлордифлуорметан або трихлорфлуорметан. Типові місцеві та трансдермальні композиції містять звичайні водні або неводні наповнювачі, як-то краплі для очей, креми, мазі, лосьйони та пасти, або є у формі лікувального пластиру, бляшки або плівки. Додатково описані тут інгібітори MPO або їх фармацевтично прийнятні солі можна компонувати для парентерального застосування ін’єкцією або подовженою інфузією. Композиції для ін’єкції можуть бути у формі суспензій, розчинів або емульсій y оливному або водному наповнювачі, та можуть містити складові композиції, як-то суспендувальні агенти, стабілізатори та/або диспергатори. Альтернативно, активні складові можуть бути y формі порошку для компонування перед застосуванням із придатним наповнювачем (наприклад, стерильною водою без пірогену). Інгібітори MPO або їх фармацевтично прийнятні солі згідно із заявленим винаходом також можна компонувати, як депо-препарат. Так довгодіючі композиції можна застосовувати імплантацією (наприклад, підшкірно або внутрішньом’язово) або внутрішньом’язовою ін’єкцією. Відповідно, сполуки заявленого винаходу можна компонувати із придатними полімерними або гідрофобними матеріалами (наприклад, як емульсія y прийнятній олії), іонообмінними смолами, або, як важкорозчинні похідні (наприклад, як важкорозчинна сіль). Для перорального застосування фармацевтична композиція, що містить інгібітори MPO або їх фармацевтично прийнятні солі згідно із заявленим винаходом може мати наступні форми: розчини, суспензії, таблетки, пігулки, капсули, порошки, тощо. Таблетки, що містить різні наповнювачі, як-то натрій цитрат, кальцій карбонат та кальцій фосфат застосовують із різними дезінтеграторами, як-то крохмаль, переважно − картопляний, або тапіоковий крохмаль, та певним комплексом силікатів разом із зв’язуючими, як-то полівінілпіролідон, сахароза, желатина та гуміарабік. Додатково для утворення таблетки можна застосовувати змащувачі, як-то магній стеарат, натрій лаурилсульфат та тальк. Тверді композиції подібного типу також застосовують як наповнювачі y м’яких та твердих желатинових капсулах; кращі матеріали при цьому також охоплюють лактозу або молочний цукор, а також поліетиленгліколі високої молекулярної маси. Альтернативно, інгібітори MPO або описані тут їх фармацевтично прийнятні солі можна вводити в рідкі пероральні препарати, як-то водні або оливні суспензії, розчини, емульсії, сиропи або, наприклад, еліксири. Більш того, композиції, що містить ці сполуки можна надавати як сухий продукт для поєднання перед застосування з водою або іншим придатним наповнювачем. Такі рідкі препарати можуть містити звичайні добавки, як-то суспендувальні агенти, як-то сорбіт сироп, синтетичні та природні смоли, як-то трагакант, гуміарабік, альгінат, декстран, натрій карбоксиметилцелюлоза, метилцелюлоза, полівінілпіролідон або желатина, сироп глюкоза/цукор, желатина, гідроксіетилцелюлоза, гідроксипропілметилцелюлоза, гель алюміній стеарату, емульгатори, як-то лецитин, сорбітмоноолєат, або гуміарабік; неводні наповнювачі (котрі охоплюють їстівні олії), як-то мигдалева олія, фракціонована кокосова олія, жирні естери, пропілeнгліколь та етиловий спирт; і консерванти, як-то метил- або пропіл-пгідроксибензоат та сорбінова кислота. Рідкі форми, у які описані тут композиції можна вводити для застосування перорально або ін’єкцією, охоплюють водні розчини, придатні ароматизовані сиропи, водні або олійні суспензії та ароматизовані емульсії з їстівними оліями, як-то бавовняна олія, кунжутна олія, кокосова олія або арахісова олія, а також еліксири та адекватні фармацевтичні наповнювачі. Коли водні суспензії та/або еліксири є бажаними для перорального застосування, описані тут сполуки можна комбінувати з різними підсолоджувачами, ароматизаторами, барвниками, емульгаторами та/або суспендувальними агентами, а також такими розріджувачами, як вода, етанол, пропілeнгліколь, гліцерин та їх комбінаціями різного типу. Придатні диспергатори або суспендувальні агенти для водних суспензії охоплюють наступне: синтетичні та природні смоли, як-то трагакант, гуміарабік, альгінат, декстран, натрій карбоксиметилцелюлоза, метилцелюлоза, полівінілпіролідон або желатина. Інгібітори MPO або описані тут їх фармацевтично прийнятні солі також можна застосовувати y композиції контрольованого (визначеного) вивільнення, як-то композиція повільного вивільнення або швидкого вивільнення. Такі описані тут композиції контрольованого вивільнення можна отримувати, застосовуючи способи, добре відомі спеціалістам. Спосіб застосування повинен визначати лікар або інший спеціаліст у рівні техніки після оцінки стану та потреб пацієнта. Таким чином, ефективна доза інгібітору MPO або їх фармацевтично прийнятних солей 9 UA 102523 C2 5 10 15 20 25 30 35 40 45 50 55 60 згідно із заявленим винаходом можна змінювати залежно від факторів, як-то стан пацієнта, суворість симптомів розладу, а також ефективності вибраної конкретної сполуки, способу застосування, віку та маси пацієнта, тощо. Визначення дози є в межах кваліфікації звичайного спеціаліста. Точність композиції, шлях застосування та дозування може вибирати окремий спеціаліст залежно від стану пацієнта. Кількість дозування та інтервал можна регулювати індивідуально для забезпечення в плазмі рівнів активної частини, котрі достатніми для підтримування терапевтичної дії. Типово, ефективна доза інгібіторів MPO або їх фармацевтично прийнятних солей загалом потребує застосування сполук у межах 1 – 1 000 мг. Згідно з одним втіленням заявленого винаходу вказана межа дорівнює 2 − 800 мг або 2 − 400 мг. В альтернативному втіленні заявленого винаходу кількість інгібітору MPO вибрано, приблизно, із групи: 5, 10, 50, 100, 150, 200, 250, 300, 350, 400, 500, 550, 600, 700 та 800 мг. Опис способів Лікування трансгенних (tg) або дикого типу мишей 3NP також складає найбільш прийнятні моделі HD (Brouillet E. et al. Prog. Neurobiol. 1999; 59:427-68). Це стосується підгострої системної ін’єкції цього мітохондріального комплексу токсину II. Цей токсин створює в мишей стріарні враження HD-типу та створює метаболічне порушення, що виникає в HD. Протягом його широкого застосування (Fernagut PO. et al. Neuroscience. 2002; 114:1005-17) продемонстровано кореляцію між часом курсу та інтенсивністю моторного розладу, застосовуючи напівкількісну шкалу (оцінку брадикінезії, тулубовудистонію, дистонію задньої кінцівки та затиск та послаблення поступального контролю) та суворість стріарного ураження (втрата нейронів та астрoцитна реакція). Також продемонстровано погіршення сенсомоторної інтеграції, застосовуючи кількісні тести, відомі як чутливі до стріатонігральної дисфункції, як-то загальна активність, полюс-тест та тест напряму переміщення. Отже, деякі важливі поведінкові та патофзіологічні кінцеві положення, важливі для HD, є такими, як y застосовуваній моделі MSA. Таким чином, стратіарна патологія, охоплюючи втрату нейронів та складові моторного режиму в моделі MSA, згаданої нижче, також відображають патологію HD. Нову модель мишей MSA розроблено індукуванням оксидативного стресу в трансгенних мишей олігодендрогліальною α-синуклеїновою експресією (описаною тут). Ця модель репродукує головні невропатологічні особливості хвороби, охоплюючи наступне: стріатонігральна дегенерація (SND), оливомостомозочкова атрофія (OPCA), астрогліоз та мікрогліоз, комбіновані з олігодендрогліальними нерозчинними α-синуклеїновими включеннями. Мітохондріальне інгібування за допомогою 3NP у присутності гліальних цитоплазматичних включень y трансгенних мишей індукує картину селективної нейронної смерті клітин, типової для MSA y цих тварини (Stefanova N. et al. Am. J. Pathol. 2005; 166:869-76). Таким чином, у заявленому винаході, інгібітори MPO застосовували для послаблення активності MPO y моделі мишей з MSA, що складається з олігодендрогліальної α-SYN надекспресії y трансгенних мишей, яких піддавали мітохондріальному інгібуванню 3нітропропіоновою кислотою (3NP). Дії супроводжувались застосуванням установлених імуногістoлогічних та поведінкових способів для оцінки участі MPO y патогенезі MSA та можливої нейрозахисної дії моделі MSA. Трансгенна чорна субстанція pars compacta (SNc) піддівали ранній втраті нейронів, асоційованій з олігодендрогліальною α-синуклеїнoпатією протягом часу між двома та чотирма місяцями віку. Ця рання втрата нейронів корелювала з мікрогліальною активацією y SNc. Пригнічення мікрогліозу протягом періоду віку між 2 та 4 місяцями виявило нейрозахисну дію для нігральних нейронів. Отримані дані дозволять припустити, що комбінована трансгенна та нейротоксична модель MSA у мишей являє собою доклінічний тест для нових терапевтичних кандидатур щодо MSA, для ранньої “мінімальної зміни ” або пізно розвинутої “різко вираженої ” MSA-парадигми. Мікрогліальна активація є видатною знахідкою y MSA мозку. У надекспресії трансгенних дикого типу мишей α-синуклеїном людини під контролем промотору протеоліпідного білку (PLP) було показано, що такі миші мали інтенсивну мікрогліальну активацію, головним чином, y білій речовині, що не є випадком y дикого типу мишей C57Bl/6 (Stefanova N. et al. Am. J. Pathol. 2005; 166:869-76). Крім того, мікрогліальна активація є високо інтенсифікованим наслідком після впливу 3NP, супроводжуваним нейронною дегенерацією MSA-типу. Кореляція мікрогліальної активації із втратою нейронних клітин означає, що мікрогліальні фактори здатні, принаймні, частково опосередковувати нейродегенерацію вивільненням різновиду реакційних часточок оксигену, нітроген оксиду (NO), цитокінів або хемокінезу. Тварини Застосовували всього 30 (PLP)-α-синуклеїнованих трансгенних мишей. Тварин тримали при 10 UA 102523 C2 5 10 15 20 25 30 35 40 45 50 55 60 12/12 годинному циклі темноти/світла з вільним доступом до їжі та води y приміщенні для тварин Медичного університету Інсбруку. Усі експерименти проводили згідно із законом Австрії та після дозволу федерального міністра освіти, науки та культури Австрії для експериментів з тваринами. Групи Контрольна група (n=10) мишей з MSA (tg+3NP), оброблена наповнювачем (циклодекстрином, отриманим від AstraZeneca) п.o. (пероральним застосуванням) Низькодозова група (n=10) мишей з MSA (tg+3NP), оброблена 1-(2-ізoпропоксіетил)-2-тіоксо1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-оном (сполука I; отримана від AstraZeneca), 2x60 мкмоль/кг, п.o. Високодозова група (n=10) мишей з MSA (tg+3NP), оброблена сполукою I (отримана від AstraZeneca), 2x180 мкмоль/кг, п.o. 1-(2-Iзoпропоксіетил)-2-тіоксо-1,2,3,5-тетрагідро-піроло[3,2-d]піримідин-4-он (сполука I, лікування) починали протягом одного тижня до першої інтоксикації 3NP та зупиняли через три тижні після першої інтоксикації 3NP (дивись протокол інтоксикації 3NP, нижче). Тварини піддавали поведінковим тестам протягом 3-4 тижнів після початку експерименту. На 28 добу тварини піддавали перфузії під глибокою анестезією тіопенталом та мозок збирали для гістологічного аналізу втрати нейронів та гліозу. Інтоксикація 3NP Мишей хронічно інтоксикували 3NP повільним збільшенням дози токсину згідно з раніше застосовуваною схемою (тобто інтраперитонеальні ін’єкції 4x10 мг/кг, 4x20 мг/кг, 4x40 мг/кг, 4x50 мг/кг кожну 12-ту годину протягом 8 діб) для моделювання MSA (Stefanova N. et al. Am. J. Pathol. 2005; 166:869-76) Сполука I, лікування Ліки та наповнювач (0,1 моль/л меглуміну із 20мас./об.% гідроксипропіл-β-циклодекстрином, pH 10,8) зберігали при 4°C. Миші отримували потрібну дозу ліків/наповнювачу (10 мл/кг) двічі щоденно перорально через зонд протягом указаного періоду. Поведінка Поведінкові тести проводили не зважаючи на лікувальний статус згідно з обґрунтованою процедурою: оцінка клінічної шкали, полюсний тест та тест довжини кроку спонтанної локомоторної активності (Stefanova N. et al. Am. J. Pathol. 2005; 166:869-76) Клінічної оцінка масштабу моторності. Раніше описано шкалу рейтингу для оцінки затиску задньої кінцівки, загальної локомоторної активності, дистонії задньої кінцівки, дистонії тулубу та реакції на постуральну стимуляцію (0, нормально; 1 слабко порушено, та 2 явно ушкоджено). (Fernagut PO. et al. Neuroscience. 2002; 114:1005-17) Активність відкритого поля Для тесту локомоторної активності мишей застосовували Flex Field Activity System (San Diego Instruments, CA, USA), котра дозволяє моніторинг та підрахунок реального часу горизонтальної та вертикальної локомоторної активності 544 каналами фотовипромінювання. Мишей розташовували в центрі відкритого поля (40,5 x 40,5 x 36,5 см) та тестували фотовипромінюванням протягом 15 хвилин завжди в то же самий час доби (17,00 год.). Тести проводили y темній кімнаті, що була повністю ізольованою від зовнішніх перешкод та світла протягом період тесту. Довжина кроку Довжина кроку передніх кінцівок та задніх кінцівок мишей вимірювали після звикання до тесту протягом 3 діб перед його виконанням згідно з Fernagut et al. (Fernagut PO. et al. Neuroscience. 2002; 114:1005-17) зі слабкою модифікацією. Кінцівки кожної тварини зволожували нетоксичним харчовим барвником, та кожній миші дозволяли пробігти по смузі паперу (42 см довжини, 4,5 см ширини) донизу по яскравому коридору в напрямку до темного боксу. Після трьох пробіжок вимірювали довжину кроку задніх кінцівок з кожного боку, вилучаючи початок (7 см) та кінець пробіжки (7 см). Визначали величину довжини кроку для кожної кінцівки. Препарат тканини Тварин під наддозою тіопенталу піддавали перфузії 4% параформальдегіду (PFA) pH=7,4. Мозок швидко видаляли та зберігали протягом 24 годин y 4% PFA при 4°C. Після кріозахисту в 20% сахарозі/0,1M розчин PBS, pH 7,4, мозок заморожували та зберігали при -80°C. Серійні зрізи (всього 7 комплектів) робили на кріостаті (Leica) та збирали для гістологічних забарвлень (одна серія на предметні стекла) та імуногістохімії (6 серій вільного блукання). Забарвлення Нісла: коронарні зрізи через увесь мозок наносили на предметні стекла та 11 UA 102523 C2 5 10 15 20 25 30 35 40 45 50 55 обробляли для стандартного забарвлення крезиловим фіолетовим. Імуноцитохімію робили згідно зі стандартними протоколами (Stefanova N. et al. Am. J. Pathol. 2005; 166:869-76) на зрізках вільного блукання (40 мкм) для аналізу нейронної та гліальної патології в моделі MSA у мишей. Застосовували наступні первинні антитіла: анти-TH тирозингідроксилaза (Sigma); анти-DARPP-32 (допамін та фосфопротеїн 32, регульований циклічним аденозин 3',5'-монофосфатом); анти-GFAP (гліальний волоконцевий кислотний білок, Roche Diagnostics GmbH); анти-CD11b: (Serotec). Вторинними антитілами, як прийнятними, біотинілували анти-мишині або анти-пацюкові IgG,. Коротко, після промивання y буферованому фосфатом фізіологічному розчині (PBS) зрізи інкубували y 0,3% H 2O2, промивали знов та блокували протягом 1 години в 10% нормальній козиній сироватці y PBS з 0,3% Triton-X100 (PBS-T), а потім протягом ночі інкубували в первинному антитілі пси 4°C. Після промивання y PBS-T, зрізи інкубували протягом 1 годин y вторинному антитілі, знов промивали та інкубували ще одну годину в комплексу авідину-біотину (Elite Kit, Vector). Кінець кінцем, реакцію візуалізували 3,3’-діамінобензидином. Стереологію робили, застосовуючи автоматизовану систему аналізу зображення (мікроскоп Nikon E-800, відеокамера CCD, Optronics MicroFire, Goleta, USA; Stereo Investigator Software, MicroBrightField Europe e.K., Magdeburg, Germany). Для підрахунку нейронів y стріатумі, чорної субстанції pars compacta, ядра варолієвого мосту та нижніх олив застосовували оптичний фракціонатор. Клітини Пуркин’є рахували тальки в області, що охоплює шар клітин Пуркин’є, як раніше повідомлено (German DC. et al. Neuroscience. 2001; 105:999-1005). Усі дані були виражені як середнє значення ± SEM. Гліальну активацію y чорній субстанції та стріатумі вимірювали визначенням оптичної щільності y цільовій області трансдиференціюванням цієї області в серійні зрізи. Для всіх отриманих статистичних критеріїв уважався достовірним рівень вірогідності 5% (p
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of myeloperoxidase inhibitors for the treatment of multiple system atrophy
Автори англійськоюEriksson, Hakan, Poewe, Werner
Назва патенту російськоюПрименение ингибиторов миелопероксидазы для лечения множественной системной атрофии
Автори російськоюЭрикссон Гакан, Поэв Вернер
МПК / Мітки
МПК: A61K 31/519, A61P 25/28
Мітки: атрофії, застосування, множинної, системної, лікування, інгібіторів, мієлопероксидази
Код посилання
<a href="https://ua.patents.su/21-102523-zastosuvannya-ingibitoriv-miehloperoksidazi-dlya-likuvannya-mnozhinno-sistemno-atrofi.html" target="_blank" rel="follow" title="База патентів України">Застосування інгібіторів мієлопероксидази для лікування множинної системної атрофії</a>
Попередній патент: Стійка до грибків трансгенна рослина solanaceae
Наступний патент: Гідродинамічна муфта
Випадковий патент: Зубна шина