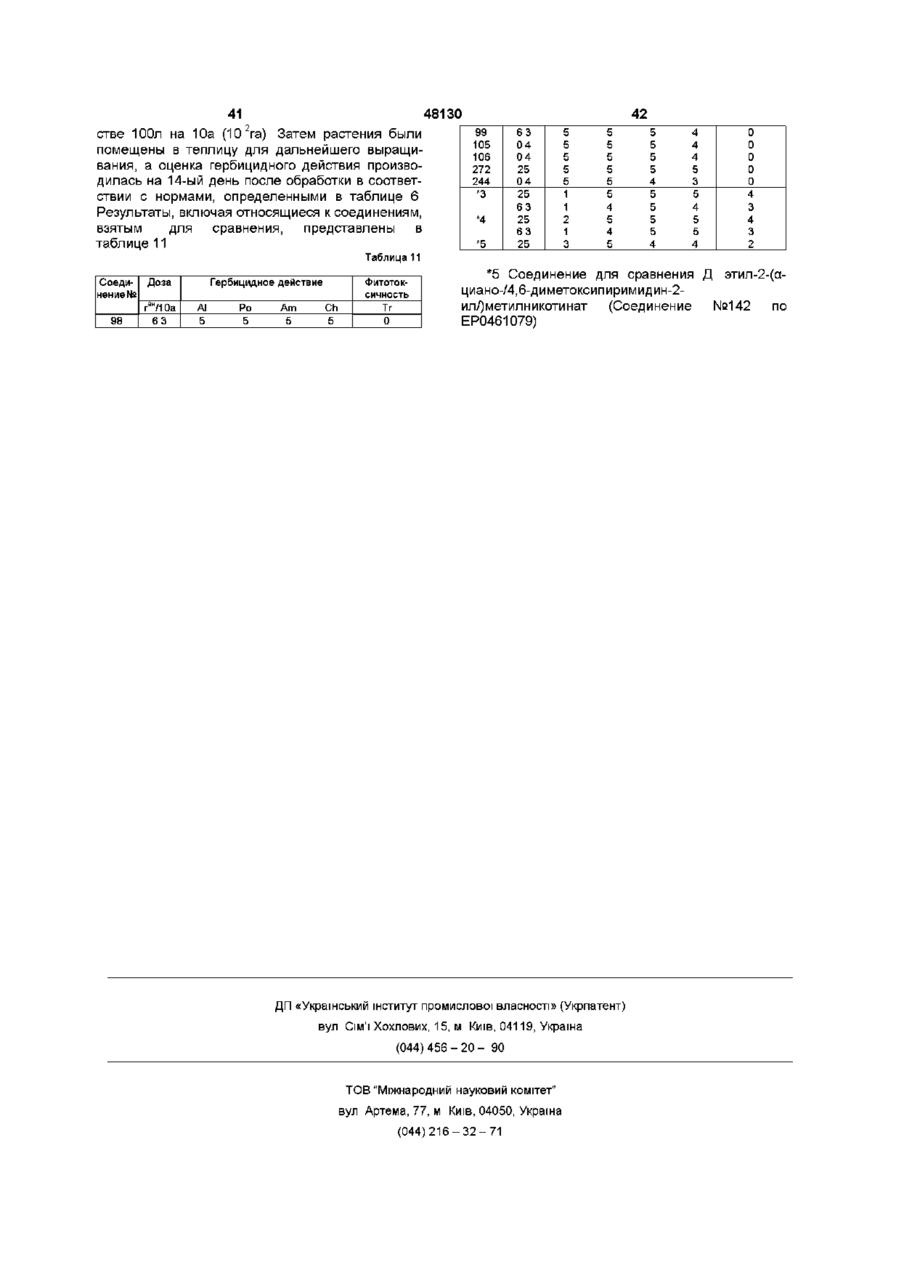
Похідні нікотинової кислоти, спосіб їх отримання і гербіцидна композиція на їх основі
Номер патенту: 48130
Опубліковано: 15.08.2002
Автори: Міязакі Масахіро, ІТО Йошіхіро, МІЯЗАВА Такешіге, ТАШІКАВА Шігехіко, ОХБА Нобуюкі, ЙОКОТА Суміо, ВАДА Нобухіде
Формула / Реферат
1. Производное никотиновой кислоты, представленное общей формулой (I)
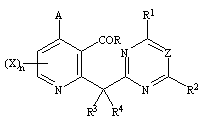 ,
,
(I)
где А представляет одну из групп формул А-1, А-2, А-3 и А-4
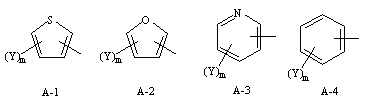 ,
,
где Y представляет атом галоида, С1-С7-алкоксигруппу, С1-С7-алкильную группу или нитрогруппу;
m = 0 или представляет целое число от 1 до 2, при условии, что когда m = 2, Y может быть комбинацией из различных групп;
R представляет собой С1-С7-алкоксигруппу, С1-С7-алкокси-С1-С7-алкоксигруппу, С1-С7-галогеналкоксигруппу, бензилоксигруппу, галогензамещенную бензилоксигруппу, С2-С7-алкенилоксигруппу, С1-С7-алкилтиогруппу, 1-имидазолильную группу, изопропилиденаминооксигруппу, ди-С1-С7-алкиламиногруппу, ди-С1-С7-алкиламинооксигруппу;
Х – С1- С7-алкильная группа;
n – 0 или 1;
Z – СН-группа;
группа формулы =CR3R4 представляет собой фрагмент формулы
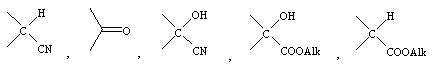 ,
,
где Alk – С1- C7 -алкильная группа,
или COR-группа вместе с R4 -группой образует группу-С(= O)-O-
с образованием структуры (II)
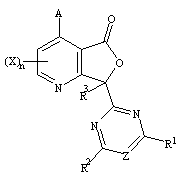 ,
,
(II)
где R3 представляет группу, выбранную из СN, ОН, Н и COOAlk и группы А, X, Alk и Z имеют указанные значения;
R1 и R2 каждый- С1- С7-алкоксигруппа, или его соль.
2. Производное никотиновой кислоты по п. 1, отличающееся тем, что А в общей формуле (I) или (II) представляет формулу А -1 или формулу А - 2.
3. Производное никотиновой кислоты по п. 1, отличающееся тем, что А в общей формуле (I) или (II) представляет формулу А -3.
4. Производное никотиновой кислоты по п. 1, отличающееся тем, что А в общей формуле (I) или (II) представляет формулу А -4.
5. Производное никотиновой кислоты по п. 1, где А представляет группу формулы А - 4, где m = 0 или 1; Y представляет собой атом галогена, С1-С7-алкоксигруппу или С1- С7-алкильную группу;
R представляет С1- С7-алкоксигруппу, С1-С7-алкокси-С1-С7-алкоксигруппу или С1-С7-галогеналкоксигруппу, С1-С7-алкилтиогруппу, бензилоксигруппу, галогензамещенную бензилоксигруппу, ди-С1-С7- алкиламиногруппу или ди-С1-С7-алкиламинооксигруппу;
R1 и R2 каждый представляет метоксигруппу, группа формулы = CR3R4 представляет собой фрагмент формулы
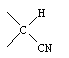 или
или 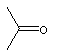
n = 0, Z - СН, или COR-группа вместе с R4 -группой образует группу -С(=O)-O- с образованием соединения II, где R3 представляет группу, выбранную из -ОН или -СN.
6. Способ получения производных никотиновой кислоты по п. 1, где группа формулы = CRЗR4 представляет собой фрагмент формулы =СНCN
или =СО, либо COR-группа вместе с R4 -группой образует группу -С(=O)-O- = СО с образованием соединения формулы (II), где R3 представляет группу ОН или CN, отличающийся тем, что включает взаимодействие соединения общей формулы а
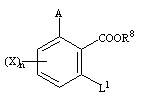 ,
,
где А представляет одну из групп формулы
 ,
,
где Y представляет атом галогена, С1-С7-алкоксигруппу, С1-С7-алкильную группу или нитрогруппу;
m = 0 или представляет целое число от 1 до 2 при условии, что если m = 2, Y может быть комбинацией различных групп;
R8 представляет С1-С7-алкильную группу;
Х представляет С1-С7-алкильную группу;
n = 0 или представляет целое число 1;
L1 представляет атом галогена, с соединением общей формулы b
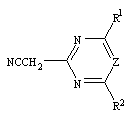 ,
,
где каждый R1 и R2 представляют С1-С7-алкоксигруппу;
Z представляет группу метина,
в присутствии по крайней мере двух эквивалентов основания в растворителе с последующим подкислением с получением соединения (Iс) общей формулы
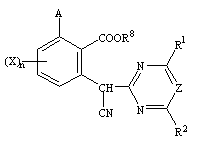 ,
,
которое при необходимости для получения соединения общей формулы (IId)
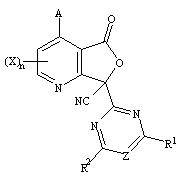 ,
,
где А, Хn, R1, R2 или Z имеют указанные ранее значения,
обрабатывают органической перекисью в растворителе и далее полученное соединение (IId) при необходимости для получения соединения общей формулы (IIе)
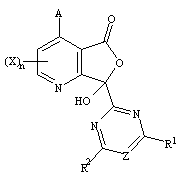 ,
,
где А, Хn , R1, R2 или Z имеют указанные ранее значения, обрабатывают в присутствии основания водой или водным растворителем с последующим подкислением и далее при необходимости для получения соединения (I) общей формулы g
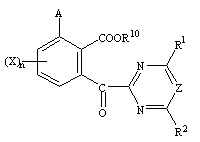 ,
,
где А, Хn, R1, R2, R10 или Z имеют указанные
ранее значения,
соединение общей формулы IIе подвергают взаимодействию с соединением, представленным общей формулой f
R10L1,
где R10 представляет С1-С7-алкокси-С1-С7-алкильную группу, С1-С7-галогеналкильную группу, С1-С7-алкильную группу, необязательно замещенную галогеном бензильную группу, С2-С7-алкенильную группу;
L1 представляет атом галогена, либо для получения соединения I, представленного общей формулой і
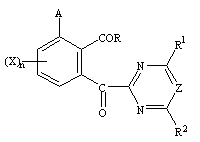 ,
,
где А, Xn, R, R1, R2 или Z имеют указанные ранее значения,
соединение общей формулы (IIe) подвергают взаимодействию с соединением общей формулы h
RH,
где R имеет указанное в п. 1 значение, в присутствии конденсирующего агента в растворителе.
7. Гербицидная композиция, содержащая производное никотиновой кислоты в качестве активного ингредиента и целевые добавки, отличающаяся тем, что в качестве указанного активного ингредиента содержит соединение по п. 1 или его соль в эффективном количестве.
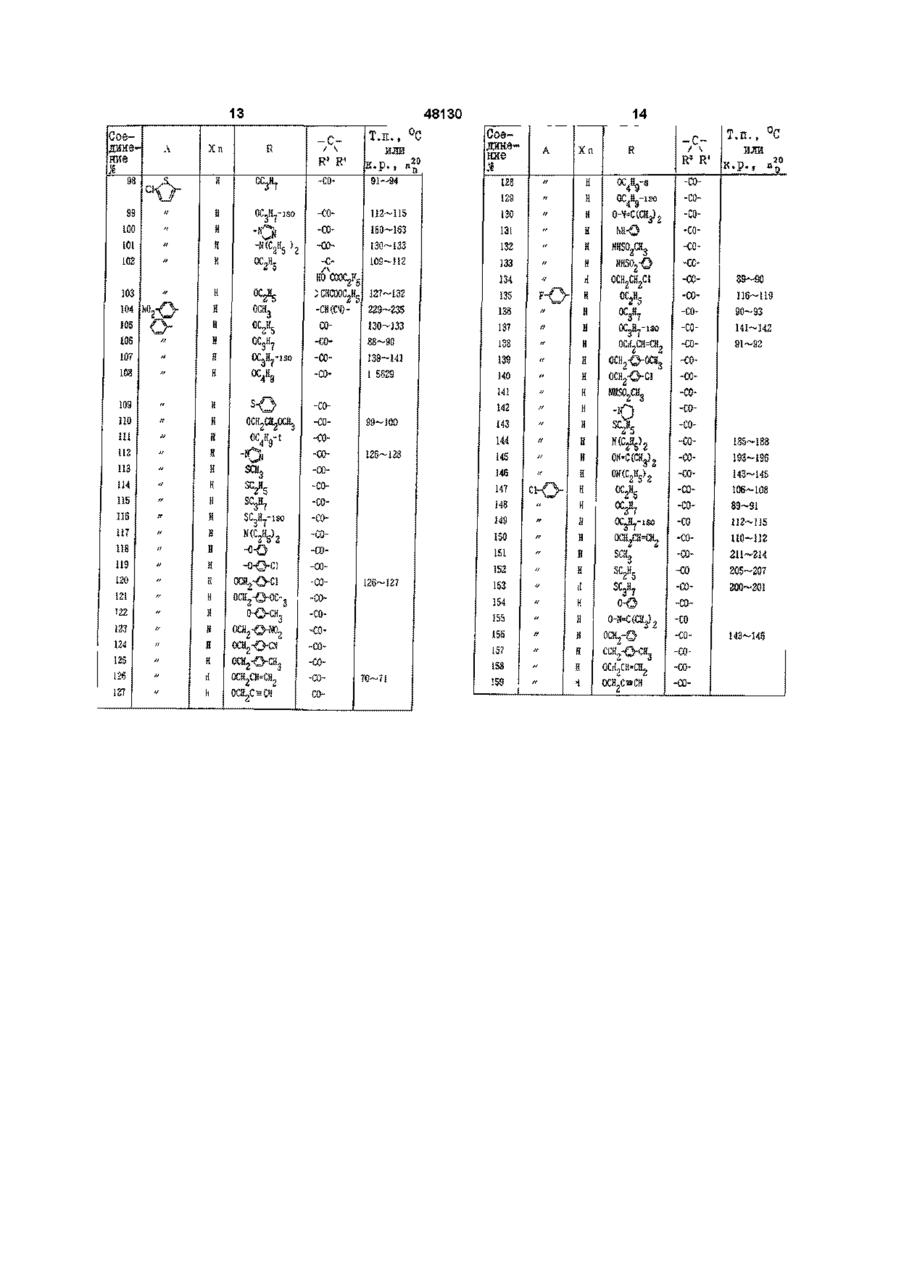
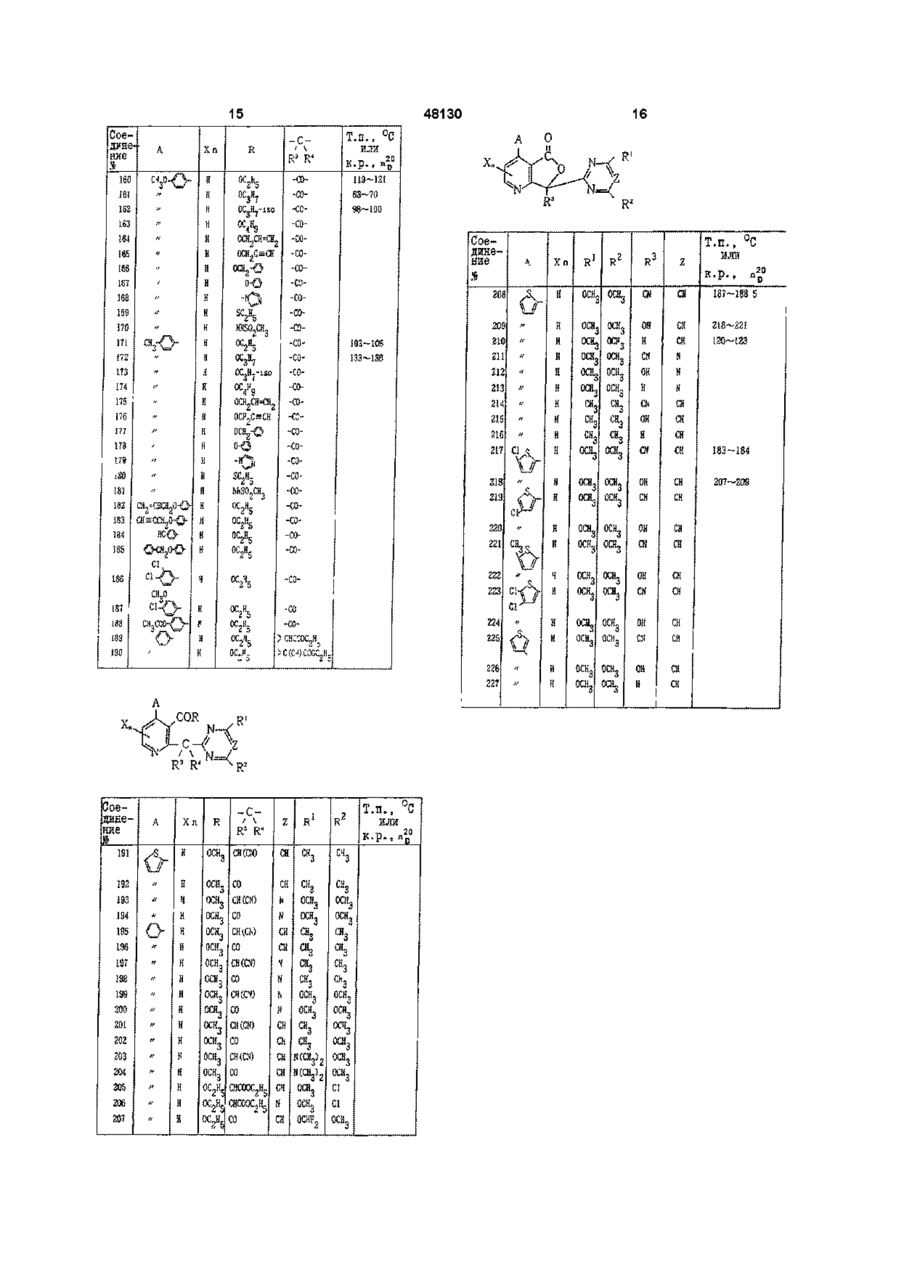
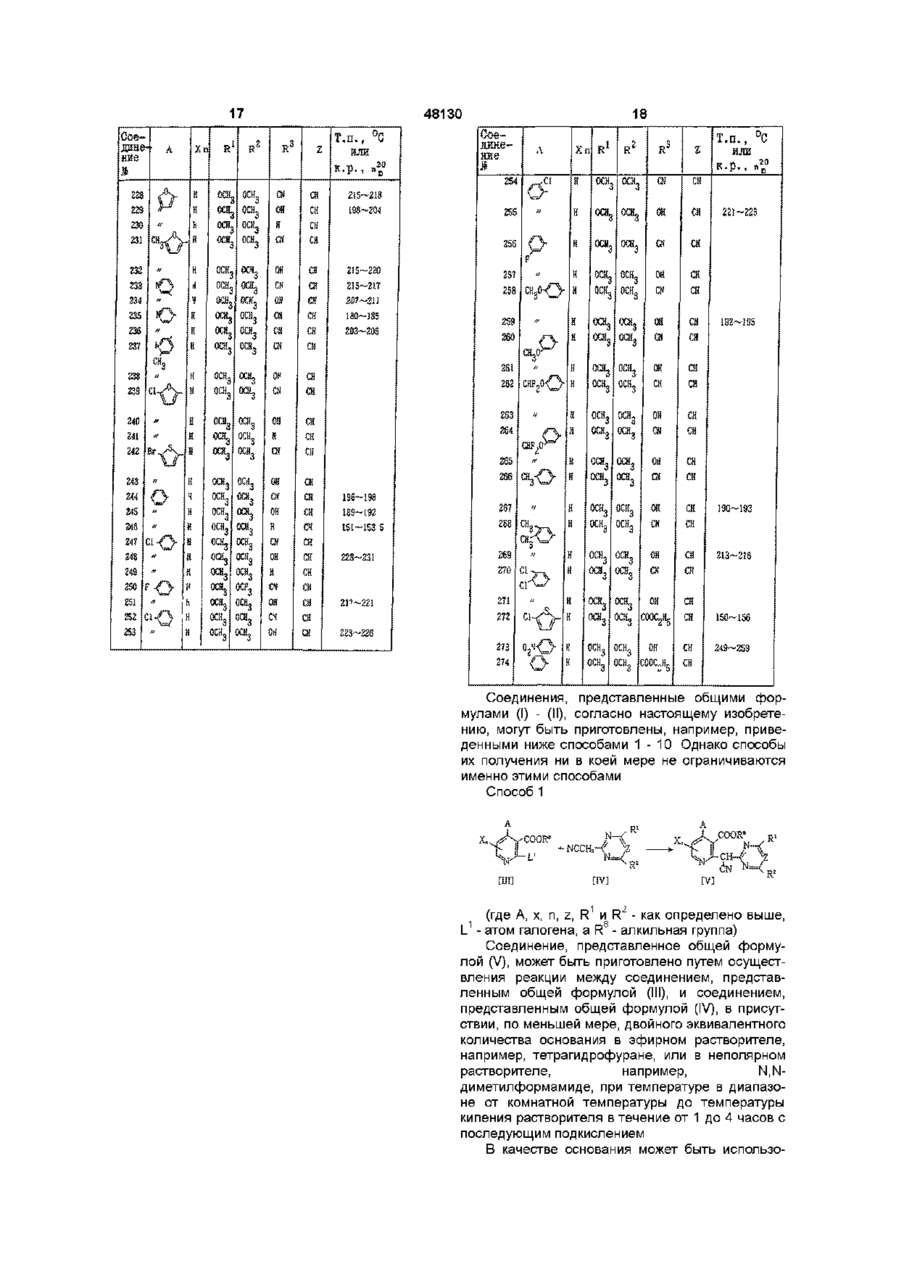
Текст
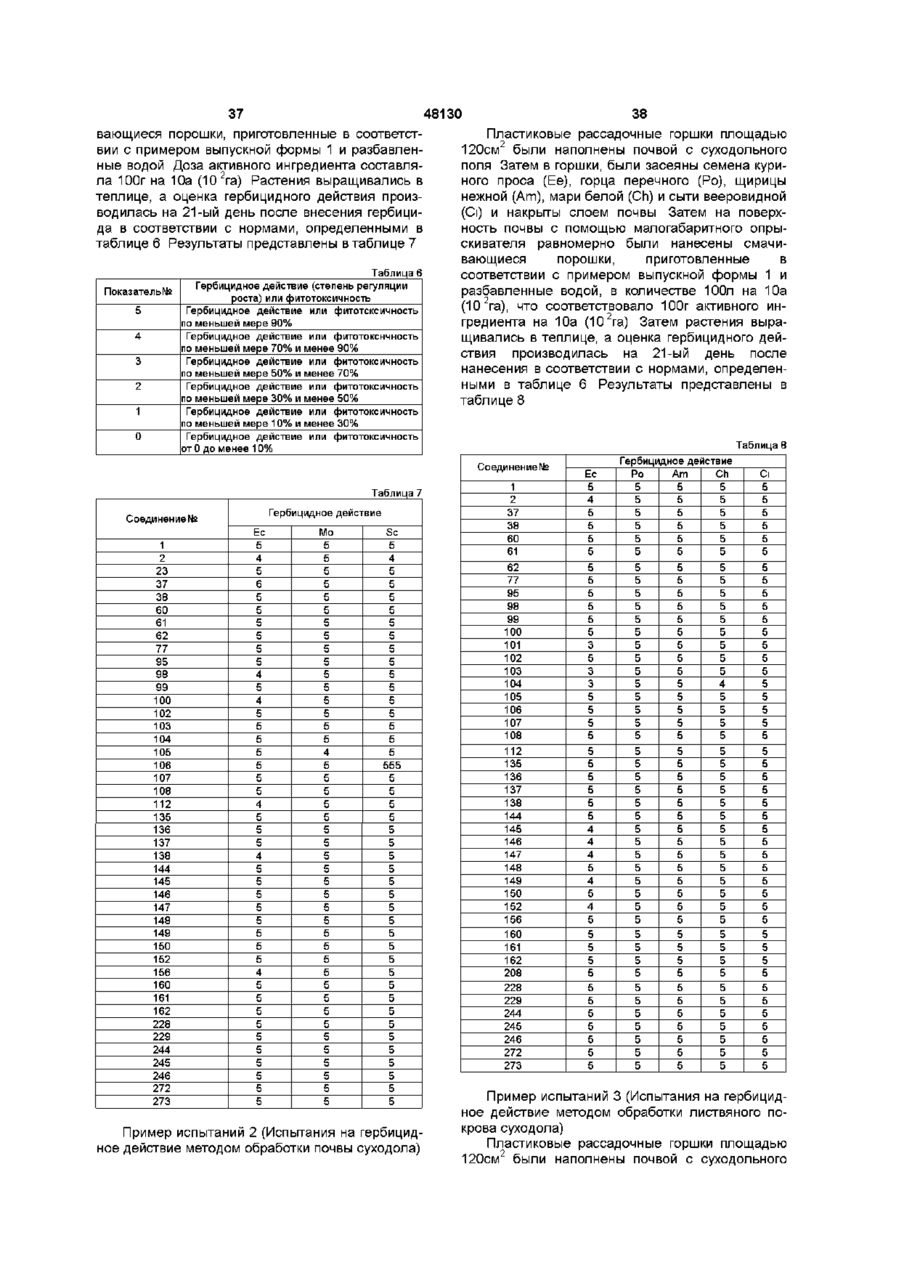
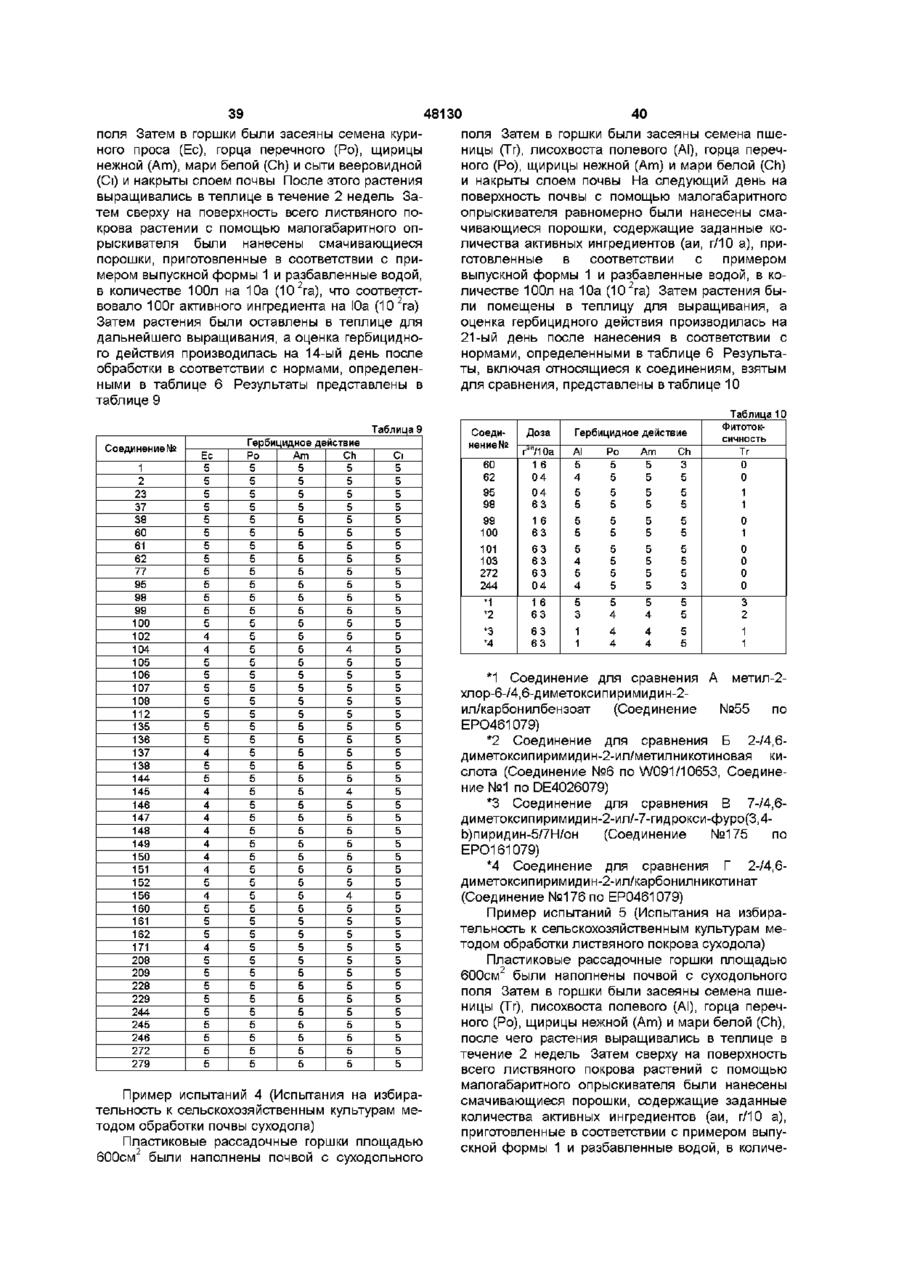
1 Производное никотиновой кислоты, представленное общей формулой (I) Z - СН-группа, Z. — V^n-I (jyillld, группа формулы =CR3R4 фрагмент формулы представляет собой где Alk - С г С7 -алкильная группа, или COR-группа вместе с R4 -группой образует группу-С(= О)-Ос образованием структуры (II) А А О (I) где А представляет одну из групп формул А-1, А-2, А-3 и А-4 (И) ООь где Y представляет атом галоида, С1-С7алкоксигруппу, СгСуалкильную группу или нитрогруппу, m = 0 или представляет целое число от 1 до 2, при условии, что когда m = 2, Y может быть комбинацией из различных групп, R представляет собой СгСуалкоксигруппу, С1-С7алкокси-Сі-С7-алкоксигруппу, С1-С7галогеналкоксигруппу, бензилоксигруппу, галогензамещенную бензилоксигруппу, С2-С7алкенилоксигруппу, СгС7-алкилтиогруппу, 1имидазолильную группу, изопропилиденаминооксигруппу, ди-Сі-С7-алкиламиногруппу, ДИ-С1-С7алкиламинооксигруппу, X - d - С7-алкильная группа, п - 0 или 1, з где R представляет группу, выбранную из CN, ОН, Н и COOAlk и группы А, X, Alk и Z имеют указанные значения, R1 и R 2 каждый- С г С7-алкоксигруппа, или его соль 2 Производное никотиновой кислоты по п 1, отличающееся тем, что А в общей формуле (I) или (II) представляет формулу А -1 или формулу А - 2 3 Производное никотиновой кислоты по п 1, отличающееся тем, что А в общей формуле (I) или (II) представляет формулу А -3 4 Производное никотиновой кислоты по п 1, отличающееся тем, что А в общей формуле (I) или (II) представляет формулу А -4 5 Производное никотиновой кислоты по п 1 , г д е А представляет группу формулы А - 4, где m = 0 или 1, Y представляет собой атом галогена, С1-С7алкоксигруппу или С г С?-алкильную группу, R представляет С г С?-алкокси группу, С1-С7алкокси-Сі-С7-алкоксигруппу или С1-С7галогеналкоксигруппу, СгС7-алкилтиогруппу, бензилоксигруппу, галогензамещенную бензилокси О ГО 00 48130 группу, ДИ-С1-С7- алкиламиногруппу или ДИ-С1-С7алкиламинооксигруппу, 1 2 R и R каждый представляет метоксигруппу, груп4 па формулы = CR R представляет собой фрагмент формулы \ ' с н C N CN ИЛИ 4 п = 0, Z - СН, или COR-группа вместе с R -группой образует группу -С(=О)-О- с образованием соединения II, где R представляет группу, выбранную из -ОН или -CN 6 Способ получения производных никотиновой кислоты по п 1, где группа формулы = CR3R4 представляет собой фрагмент формулы =CHCN 4 или =СО, либо COR-группа вместе с R -группой образует группу -С(=О)-О- = СО с образованием 3 соединения формулы (II), где R представляет группу ОН или CN, отличающийся тем, что включает взаимодействие соединения общей формулы а COOR где А представляет одну из групп формулы которое при необходимости для получения соединения общей формулы (lid) где А, Хп, R1, R2 или Z имеют указанные ранее значения, обрабатывают органической перекисью в растворителе и далее полученное соединение (lid) при необходимости для получения соединения общей формулы (Не) А Оь О где Y представляет атом галогена, С1-С7алкоксигруппу, Сі-С?-алкильную группу или нитрогруппу, m = 0 или представляет целое число от 1 до 2 при условии, что если m = 2, Y может быть комбинацией различных групп, R представляет Сі-С?-алкильную группу, X представляет Сі-С?-алкильную группу, п = 0 или представляет целое число 1, L1 представляет атом галогена, с соединением общей формулы b где А, Хп , R1, R2 или Z имеют указанные ранее значения, обрабатывают в присутствии основания водой или водным растворителем с последующим подкислением и далее при необходимости для получения соединения (I) общей формулы g А NCCH2 1 ? где каждый R и R представляют С1-С7алкоксигруппу, Z представляет группу метина, в присутствии по крайней мере двух эквивалентов основания в растворителе с последующим подкислением с получением соединения (Ic) общей формулы 1 ? 1П ' где А, Хп, R , R , R или Z имеют указанные ранее значения, соединение общей формулы Не подвергают взаимодействию с соединением, представленным общей формулой f 48130 R10L1. где R представляет Сі-Суалкокси-Сі-Су алкильную группу, Сі-Сугалогеналкильную группу Сі-Суалкильную группу, необязательно замещен ную галогеном бензил ьную группу, Сг-Су алкенильную группу, 1 L представляет атом галогена, либо для получения соединения I, представленного общей формулой і Настоящее изобретение относится к новым производным никотиновой кислоты или их солям и гербицидам, содержащим, их в качестве активных ингредиентов Известно, что производные никотиновой кислоты обладают гербицидной активностью Гербицидной активностью обладают, например, производные никотиновой кислоти, представленные формулой •і(0), x (опубликованное описание WO91 (10653), гетероциклические представленные формулой с—f ( x y f изобретения производные, Wrв wE W-V 4. 3 Wr Y (опубликованное описание изобретения EPO461079) и производное никотиновой кислоты, представленное формулой 6 1 2 где А, Хп, R, R , R или Z имеют указанные ранее значения, соединение общей формулы (Не) подвергают взаимодействию с соединением общей формулы h RH, где R имеет указанное в п 1 значение, в присутствии конденсирующего агента в растворителе 7 Гербицидная композиция, содержащая производное никотиновой кислоты в качестве активного ингредиента и целевые добавки, отличающаяся тем, что в качестве указанного активного ингредиента содержит соединение по п 1 или его соль в эффективном количестве (опубликованное описание изобретения DE4026177) С точки зрения гербицидного действия, соединения, раскрытые в упомянутых выше опубликованных описаниях изобретений, не обязательно являются эффективными Был разработан ряд других гербицидов, обеспечивающих экономию труда в сельскохозяйственных работах и повышающих производительность Однако при практическом использовании таких гербицидов также возникают различные проблемы, связанные с гербицидным действием и сохранностью сельскохозяйственных культур В частности, при выращивании ячменя и пшеницы лишь некоторые гербициды могут уничтожать травянистые сорняки, принадлежащие к тому же роду, что и ячмень и пшеница, например, лисохвост водяной, лисохвост полевой и мятлик однолетний, в течение длительного промежутка времени от пред всход о во го периода до периода вегетации Кроме того, лишь некоторые гербициды обладают широкою избирательностью в отношении ячменя или пшеницы Авторами настоящего изобретения были проведены обширные исследования производных никотиновой кислоты с целью разработки соединений, не обладающих фитотоксичностью по отношению к ценным сельскохозяйственным культурам и имеющих высокую гербицидную активность В результате было обнаружено, что соединения, предложенные в соответствии с настоящим изобретением, которые представляют собой пиримидиновые и триазиновые производные, связанные с никотиновой кислотой, замещенной фенильной группой или гетероциклическим кольцом, облада 7 48130 8 ют высокой гербициднои активностью не только по группа или алкоксикарбони-льная группа или же 4 отношению к однолетним сорнякам, но также и по R и R могут совместно представлять атом киотношению к многолетним сорнякам и полностью слорода, х - атом галогена, алкильная группа, албезопасны в отношении сельскохозяйственных коксильная группа, аминогруппа, алкиламиногрупкультур Именно на этом открытии и основано напа, диалкиламиногруппа или ациламиногруппа, п стоящее изобретение 0 или целое число от 1 до 2, при условии, что, когда п - 2, х может представлять собой комбинацию Раскрытие изобретения различных групп, а z-метиновая группа или атом Более конкретно, настоящее изобретение отазота/, или их соли и гербицидам, содержащим их носится к производным никотиновой кислоты, в качестве активных ингредиентов Когда представленным общей формулой А COR V v 4 > по (где А - одна из групп формул (А - Ц (А - 2) - 3) (А - 4) (где Y - атом галогена, гидроксильная группа, факультативно замещенная алкоксильная группа, алкенилоксильная группа, алкинилоксильная группа, факультативно галоген-замещенная алкильная группа, ацилоксильная группа, бензилоксильная группа или нитрогруппа, а т - 0 или целое число от 1 до 3, при условии, что, когда т - 2 или 3, у может представлять собой комбинацию различных групп), R - гидроксильная группа, факультативно замещенная алкоксильная группа, Факультативно замещенная бензилоксильная группа, алкенилоксильная группа, алкинилоксильная группа, факультативно замещенная феноксильная группа, факультативно замещенная фенилтиогруппа, алкилтиогруппа, 1-имидазолнльная группа, изопропилиденаминоксильная группа или группа, представленная формулой -NR5R6 (где каждый из R5 и R6 , которые могут быть одинаковыми или различными, - атом водорода, алкильная группа, факультативно замещенная фенильная группа, алкилсульфонильная группа или факультативно замещенная фенилсульфонильная группа, пли же R5 и R6 могут образовывать совместно с атомом азота кольцо) или формулой -ONR5R6 (где R5 и R6 - как определено выше), каждый из R1 и R2, которые могут быть одинаковыми или различными, - атом водорода, алкоксильная группа, атом галогена, алкиламиногруппа, диалкиламиногруппа, галоген-замещенная алкоксильная группа или алкильная группа, каждый из R3 и R4, которые могут быть одинаковыми или различными, - атом водорода, гидроксильная группа, циано представляет собой цианометиленовую группу, настоящее изобретение охватывает их таутомеры Соединение общей формулы (I), 3 4 где R - гидроксильная группа, a R и R совместно представляют атом кислорода, соответствует соединению общей формулы (II), где R3 - гидроксильная группа В общих формулах (I), (II), (А-1), (А-2), (А-3) и (А-4) факультативно замещенная алкоксильная группа в качестве R представляет собой линейную или разветвленную алко-ксильную группу Сі 7, которая может быть замещена алкоксильной группой или атомом галогена, например, метоксильной группой, этоксильной группой, изопропоксильной группой, t-бутоксильной группой, метоксиэтоксильной группой или хлорэтоксильной группой Факультативно замещенная бензилоксильная группа, факультативно замещенная феноксильная группа и факультативно замещенная фенилтиогруппа являются соответствующими группами, которые могут быть замещены атомом галогена, алкильной группой, алкоксильной группой, нитрогруппой или цианогруппой Алкоксильная группа в качестве R1 или R2 представляет собой линейную или разветвленную алкоксильную группу Сі 7, например, метоксильную группу, этоксильную группу или изопропоксильную группу Атомом галогена является один из атомов хлора, брома, фтора или йода Алкиламиногруппа представляет собой линейную или разветвленную алкилапиногруппу Сі 3, например, метиламиногруппу или этиламино-группу Диалкнламиногруппа представляет собой линейную или разветвленную диалкпламиногруппу Сі 3, например, диметиламиногруппу, диэтиламиногруппу или метилэтиламиногруппу Галоген-замещенная алкоксильная группа представляет собой линейную или разветвленную алкоксильную группу Сі 7, частично или полностью замещенную упомянутыми выше атомами галогенов, например, дифторметоксильную группу или трифторметоксильную группу Алкильная группа представляет собой линейную или разветвленную алкильную группу Сі 7, например, метильную группу, этильную группу или изопропильную группу Алкоксикарбонильная группа в качестве R3 или R4 представляет собой линейную пли разветвленную алкоксикарбонильнуо группу Сі 7, например, метоксикарбонильную группу, этоксикарбонильную группу или изопропоксикарбонильную группу Алкильная группа в качестве R5 или R6 аналогична группам, описанным выше для алкильной группы в качестве заместителей R1 или R2 Фа 48130 10 культативно замещенная фенильная группа предпильную группу, тифторметильную группу или ставляет собой, например, фенильнуп группу, кохлорэтильную группу торая может быть замещена атомом галогена, Атом галогена, алкильная группа, алкоксильалкильной группой, алкоксильной группой или ная группа, алкиламиногруппа и диалкиламино5 6 нитрогруппой R и R могут образовывать совмегруппа в качестве х аналогичны соответствующим стно с атомом азота кольцо, например, пирролигруппам, описанным выше для атома галогена, динильнуо группу или пиперазиновую группу алкильной группы, алкоксильной группы, алкиламиногруппы и диалкиламиногруппы в качестве Атом галогена в качестве у аналогичен опи2 заместителей R или R Ациламиногруппа предсанным выше для атома галогена в качестве за1 2 ставляет собой ациламиногруппу Сі 7, например, местителя R или R Факультативно замещенная формиламиногруппу, ацетиламиногруппу или проалкоксильная группа представляет собой линейпиониламиногруппу ную или разветвленную алкоксильную группу Сі 7, которая может быть замещена атомом галогена В представленных ниже таблицах 1 - 3 привеили алкоксильной группой, например, метоксильдены конкретные примеры соединения, предлоной группой, этоксильной группой пли дифтормеженного в соответствии с настоящим изобретенитоксильной группой Факультативно галогенем В следующем ниже описании делаются замещенная алкильная группа представляет соссылки на порядковые номера соединений бой линейную или разветвленную алкильную В заголовке последней графы указанных табгруппу Сі 7, которая может быть частично или поллиц сокращения "т п " и "к р " обозначают соответностью заменена атомами галогенов, например, ственно температуру плавления и коэффициент метил ьнуо группу, этильную группу, изопрорефракции Соединение Таблица 1 Т.п., Xn К.р., n R' 24 оси, осн, -СЯСО) 25 26 Соелзше і А п Хд > Т . п . , °С — С— / \ О! £\ Г>4 К /К г 3 І s Я « б-св3 ОСЯд -СИ(Ю к S к Й;И3 -а> ос 2 я 5 -снI С0ОС.Н, 5-СК, ОСНд или К.p., nf 2 22 4 0-0 -СК(Ш > ' '' осн 3 -CHCCN) -сн(Ш-Ш(Ш) 2f 2 8 ссн 3 29 -со ЗО осн 3 -HC J C C N Ееизмєрж/. -G C 17 20 9—0 18 12 2~3 З! оск 3 -00 32 ссл -снсш с, Э 6 7 S-C! 3 6-hH, осн3 СНССН) S-SHCH3 ОСЯд -СН ССЧ) ~ ЙСНд -GKC0 есн 3 -сжао-тоо 9 to и 1 2 п и 1 5 1 6 1 7 1 8 1 9 2 S 2 1 2 2 2 3 « » '' °\}~ ''' '' ~ "ЧУ 6-ОСК, 5.5-(СН 3 ) 2 б-йасос300°С Пример 2 Приготовление 7-циано-7-/4,6диметоксипиримидин-2-ил/-4-/2-тиенил/фуро(3,4Ь)пиридин-5/7Н/она (Соединение №208) Было отвешено 1,01 г метил-2-(а-циано-/4,6 28 диметокси-пиримидин-2-ил/метил)-4-/2тиенил/никотината, после чего к нему было добавлено 50мл хлороформа Затем смесь была подвергнута перемешиванию при -ЮС Затем к ней было добавлено 0,75г 70%-ной тхлорпербензойной кислоты, после чего смесь была подвергнута перемешиванию при комнатной температуре в течение ЗОмин Затем смесь была промыта насыщенным тиосульфатом натрия и водой и просушена над безводным сульфатом магния Растворитель был отогнан, а полученный остаток был подвергнут очистке методом колоночной хроматографии на силикагеле /проявляющий растворитель этилапетат/гексан = 1/2/, в результате чего было получено 0,40г требуемого соединения (выход 41,0%) в виде желтых кристаллов Температура плавления 187 188,5°С Пример 3 Приготовление 7-/4,6-диметоксипиримидин-2ил/-4-/2-фурил/-7-гидроксифуро(3,4-Ь)пиридин5/7Н/она (Соединение №229) Было отвешено 0,42г 7-циано-7-/4,6диметоксипиримидин-2-ил/-4-/2-фурил/фуро(3,4Ь)пиридин-5/7Н/она, после чего к нему было добавлено 14мл тетрагидрофурана Полученная смесь была подвергнута перемешиванию в условиях охлаждения льдом Затем к ней по каплям было добавлено 14мл 0,25г водного раствора гидроксида натрия, после чего смесь была подвергнута перемешиванию при комнатной температуре в течение ЗОмин Затем смесь была залита в воду, водный слой был дважды промыт этилацетатом, подкислен 10%-ной хлористоводородной кислотой и подвергнут экстрагированию 100мл этилацетата Экстракт был промыт насыщенным водным раствором хлорида натрия и просушен над безводным сульфатом магния Растворитель был отогнан, а полученные кристаллы были промыты метиловым спиртом, в результате чего было получено 0,40г (выход 94,6%) требуемого соединения в виде желтых кристаллов Температура плавления 198-204°С Пример 4 Приготовление метил-2-/4,6диметоксипиримидин-2-ил-карбонил/-4-/2фурил/никотината (Соединение №38) Было отвешено 2,1 г 7-/4,6диметоксипиримидин-2-ил/-4-/2-фурил/-7гидроксифуро (3,4-Ь) пиридин-5/7Н/она, после чего к нему было добавлено 50мл N,Nдиметилформамида и 0,82г карбоната калия Смесь была подвергнута перемешиванию при комнатной температуре Затем к ней по каплям было добавлено 0,Зг метилиодида, после чего смесь была оставлена на ночь при комнатной температуре в условиях постоянного перевешивания, а затем залита в воду и подвергнута экстрагированию 200мл этилацетата Экстракт был промыт насыщенным водным раствором хлорида натрия и просушен над безводным сульфатом магния Растворитель был отогнан, а остаток был подвергнут очистке методом колоночной хроматографии на силикагеле (проявляющий растворитель этил ацетат/гексан = 1/3), в результате чего было получено 1,1 г (выход 50,7%) требуемого 29 48130 соединения Температура плавления 135-140°С Пример 5 Приготовление 7-/4,6-диметоксипиримидин-2ил/-4-/2-тиенил/фуро(3,4-Ь)пиридин-5/7Н/она (Соединение №210) В 30мл этилового спирта было растворено 0,7г 7-/4,6-диметокспипримидин-2-ил/-7-гидрокси4-/2-тиенил/фуро(3,4-Ь)пиридин-5/7Н/она, после чего к нему в условиях постоянного перемешивания и охлаждения льдом было добавлено 0,07г борогидрида натрия Затем смесь была подвергнута перемешивание при комнатной температуре в течение ЗОмин, после чего вакуумной перегонкой был удален этиловый спирт Остаток был подкислен 10%-ной хлористоводородной кислотой и подвергнут экстрагированию 200мл этилацетата Экстракт был промыт насыщенным водным раствором хлорида натрия и просушен над безводным сульфатом магния Растворитель был отогнан, а полученный остаток был подвергнут очистке методом колоночной хроматографии на силигагеле (проявляющий растворитель этилацетат/гексан = 1/2), в результате чего было получено 0,35г (выход 52,0%) требуемого соединения Температура плавления 120-123°С Пример 6 Приготовление 2-/4,6-диметоксипиримидин-2ил-карбонил/-4-/2-тленил/никотината натрия (Соединение ,№96) В 100мл бензола было растворено 0,4г 7-/4,6димето-ксипиримидин-2-ил/-4-/2-тиенил/-7гидроксифуро (3,4-Ь) пиридин-5/7Н/она, после чего к нему в условиях охлаждения льдом было добавлено 0,05г 60%-ного гидрида натрия Затем полученная смесь была подвергнута перемешиванию при комнатной температуре в течение суток, а полученные кристаллы были промыты достаточным количеством бензола, в результате чего было получено 0,4г (выход 97%) требуемого соединения Температура плавления >300°С Пример 7 Приготовление метил-2-(а-циано-/4,6диметоксипиримидин-2-ил/метил)-4фенилникотината (Соединение ,№60) 3,2г 60%-ного гидрида натрия было промыто n-гексаном, после чего к нему было добавлено 100мл N.N-диметилформамида Затем к нему в условиях охлаждения льдом было добавлено 6г 4,6-диметоксипиримидин-2-ил-ацетонитрила, после чего полученная смесь была подвергнута перемешиванию в течение ЗОмин Затем к ней было добавлено Юг метил-2-бром-4-фенилникотината, после чего реакционный-раствор был подвергнут перемешиванию при 80°С в течение 2 часов Затем реакционный раствор был залит в ледяную воду и отрегулирован разбавленной хлористоводородной кислотой до рН2 - 3 Осажденные кристаллы были отфильтрованы и промыты достаточным количеством толуола и этилацетата Полученные таким образом кристаллы были просушены, в результате чего было получено 5г (выход 38%) требуемого соединения Температура плавления 198-199°С Пример 8 Приготовление метил-2-(а-цнано- а-гидрокси1-/4,6-диметоксипиримидин-2-ил/метил)-4 30 фенилникотината (Соединение №95) В 50мл хлороформа было суспендировано 3,9г метил-2-(а-циано/4,6-диметоксипиримидин-2ил/метил)-4-фенилникотината, после чего к нему было добавлено Зг 70%-ной т-хлорпербензойной кислоты Затем суспензия была подвергнута перемешиванию при комнатной температуре в течение ЗОмин, после чего она была промыта достаточным количеством водного раствора сульфита натрия, насыщенного водного раствора гидрокарбоната натрия и насыщенного водного раствора хлорида натрия и просушен над безводным сульфатом магния Растворитель был отогнан, а остаток был подвергнут кристаллизации с использованием смеси растворителей, состоящей из изопропилового эфира и этилацетата, в результате чего было получено 2,9г (выход 73%) требуемого соединения Температура плавления 126 129°С Пример 9 Приготовление 7-циано-7/4,6диметоксипиримидин-2-ил/-4-фенилфуро(3,4Ь)пиридин-5/7Н/она (Соединение №244) В 20мл дихлорметана было суспендировано 1г метил-2-(а-циано-/4,6-диметоксипиримидин-2ил/метил)-4-фенилникотината, после чего к нему было добавлено 0,8г 70%-ной тхлорпербензойной кислоты Затем реакционная суспензия была подвергнута перемешиванию при комнатной температуре в течение 2 часов и промыта достаточным количеством водного раствора бисульфита натрия, насыщенного водного раствора гидрокарбоната натрия и насыщенного водного раствора хлорида натрия с последующим просушиванием Затем был отогнан растворитель Полученный сырой продукт был растворен в 20мл этанола, после чего к нему было добавлено 0,5мл концентрированной хлористоводородной кислоты Затем смесь была подвергнута перемешиванию при 40°С в течениеЗО мин Этанол был отогнан, а к остатку была добавлена ледяная вода Затем осажденные кристаллы были подвергнуты перекристаллизации этанолом, в результате чего было получено 0,31г (выход 31%) требуемого соединения Температура плавления 196-198 С Пример 10 Приготовление 7-/4,6-диметоксипиримидин-2ил/-7-гидрокси-4-/4-хлорфенил/фуро(3,4Ь)пиридин-5/7Н/она (Соединение №248) В 50мл хлороформа было растворено 2,2г метил-2-(а-циано-/4,6-диметоксипиримидин-2ил/метил)-4-/4-хлорфенил/-никотината, после чего к нему было добавлено 1,07г 70%-ной т хлорпербензойной кислоты Полученный реакционный раствор был подвергнут перемешиванию при комнатной температуре в течение 1 часа, хорошо промыт насыщенным водным раствором бисульфита натрия, насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и просушен над безводным сульфатом магния Растворитель был отогнан, а полученный сырой продукт быт растворен в 50мл тетрагидрофурана Затем к нему было добавлено 30мл водного раствора 0,7г гидроксида натрия, после чего полученный реакционный раствор был подвергнут перемешиванию при комнат 31 48130 ной температуре в течение 2 часов Затем реакционный раствор был залит в ледяную воду, отрегулирован разбавленной хлористоводородной кислотой до рН2 - 3 и подвергнут экстрагированию этилацетатом Экстракт быт промыт достаточным количеством воды и просушен над безводным сульфатом магния Растворитель был отогнан, а полученные сырые кристаллы были промыты достаточным количеством этанола, в результате чего было получено 1,5г (выход 75%) требуемого соединения Температура плавления 228-231 °С Пример 11 Приготовление 7-/4,6-диметоксипиримидин-2ил/-4-фенилфуро(3,4-Ь)пиридин-5/7Н/она (Соединение №246) В 30мл этанола было растворено 1г 7-/4,6диметоксипиримидин-2-ил/-7-гидрокси-4фенилфуро(3,4-Ь) пиридин-5-/7Н/она, после чего к нему при комнатной температуре было добавлен 2,1 г борогидрида натрия Полученная смесь была подвергнута перемешиванию при комнатной температуре в течение 6 часов, после чего этанол был отогнан К остатку была добавлена ледяная вода, после чего полученная смесь была отрегулирована разбавленной хлористоводородной кислотой до рН2 - 3 и подвергнута экстрагированию етилацетатом Экстракт был промыт достаточным количеством воды и просушен над безводным сульфатом магния, после чего растворитель был отогнан Полученный сырой продукт был подвергнут очистке методом колоночной хроматографии на силикагеле, в результате чего было получено 0,7г (выход 73%) требуемого соединения Температура плавления 151 - 153°С 32 комнатной температуре Осажденные кристаллы были отфильтрованы и промыты достаточным количеством ацетона, в результате чего было получено 0,25г (выход 60%) требуемого соединения Температура плавления 263 - 267°С Пример 14 Приготовление 2-/4,6-диметоксипиримидин-2ил-карбонил/-3-/имидазол-1-ил-карбонил/-4фенилпиридина (Соединение №112) В 20мл тетрагидрофурана было растворено 1,5г 7-/4,6-диметоксипиримидин-2-ил/-7-гидрокси4-фенилфуро-(3,4-Ь)пиридин-5/7Н/она, после чего к нему было добавлено 0,6г N,Nкарбонилдиимидазола После перемешивания при комнатной температуре в течение 2 суток реакционный раствор был залит в воду и подвергнут экстрагированию этилацетатом Экстракт был промыт достаточным количеством воды и просушен над безводным сульфатом магния Растворитель был отогнан, а полученный остаток был подвергнут кристаллизации изопропиловым эфиром, в результате чего было получено 1,3г (выход 78,5%) требуемого соединения Температура плавления 126- 128°С Пример 12 Приготовление бензил-2-/4,6диметоксипиримидин-2-ил-карбонил/-4фенилникотината (Соединение №62) В 10мл N.N-диметилформамида было растворено 0,5г 7-/4,6-диметоксипиримидин-2-ил/-7гидрокси-4-фенилфуро-(3,4-Ь)пирндин-5/7Н/она, после чего к нему было добавлено 0,2г карбоната калия Затем реакционный раствор был подвергнут перемешиванию в достаточной степени После этого к реакционному раствору по каплям при комнатной температуре было добавлено 0,23г бензилбромида, после чего он был подвергнут перемешивание в течение суток Затем реакционный раствор был залит в ледяную воду, после чего подвергнут экстрагирование этилацетатом Экстракт был промыт достаточным количеством воды и просушен над безводным сульфатом магния Растворитель был отогнан, а полученные сырые кристаллы были промыты изопропиловым эфиром, в результате чего было получено 0,5г (виход 80%) требуемого соединения Температура плавления 124-126°С Пример 15 Приготовление этил-4-/5-хлортиофен-2-ил/-2(/4,6-диметоксипиримидин-2-ил/-аэтоксикарбонилметил)-никотината (Соединение №103) В 80мл этанола было растворено 2,9г натрия, после чего к нему при комнатной температуре было добавлено 9,7г ацетоуксусного эфира Полученная смесь была подвергнута перемешивание в течение 15мин Затем к ней была добавлена смесь, содержащая 0,4г ацетата меди и 14г 2бром-4-/5-хлортиофен-2-ил/никотиновой кислоты, после чего полученный реакционный раствор был подвергнут дефлегмации в течение 3 часов По завершении реакции к нему было добавлено 40мл уксусной кислоты, после чего растворитель был отогнан Остаток был подвергнут экстрагированию этилацетатом, а экстракт был промыт водой и просушен над безводным сульфатом магния Этилацетат был отогнан, а остаток был растворен в 50мл N.N-диметилформамида Затем к раствору было добавлено 9,8г этилиодида и Юг карбоната калия Полученный раствор был оставлен для протекания реакции на 3 часа при комнатной температуре По завершении реакции реакционный раствор был залит в воду и подвергнут экстрагированию етилацетатом Экстракт был промыт водой и просушен над безводным сульфатом магния Этилацетат был отогнан, а остаток был подвергнут очистке методом колоночной хроматографии на силикагеле /гексан етилацетат=5 1/, в результате чего было получено 8,9г этил-4-/5хлортиофен-2-ил/-2-/а Пример 13 Приготовление 2-/4,6-диметоксипиримидин-2ил-карбонил/-4-/4-хлорфенил/никотината натрия (Соединение №97) В 100мл толуола было растворено 0,4г 7-/4,6-диметоксипиримидин-2-ил/-4-/4хлорфенил/-7-гидроксифуро-(3,4-Ь)пиридин5/7Н/она, после чего к нему было добавлено 0,05г 60%-ного гидрида натрия Полученная смесь была подвергнута перемешиванию в течение суток при этоксикарбонилметил/никотината при выходе = 50% Затем к 50мл N.N-диметилформамида было добавлено 2,9г t-бутоксида калия К полученной смеси по каплям при -10°С было добавлено 8,9г этил-4-/5-хлортиофен-2-ил/2-/аэтоксикарбонилметил/никотината, растворенного в N.N-диметилформамиде, после чего полученный реакционный раствор был подвергнут перемеши 33 48130 ванию при комнатной температуре в течение 1 часа Затем к нему было добавлено 5,6г 4,6-диметокси-2-метилсульфонилпиримидина, после чего реакционный раствор был подвергнут перемешиванию при 60 - 80°С в течение 8 часов По завершении реакции реакционный раствор был залит в воду, отрегулирован до рН 4 - 5 и подвергнут экстрагированию этилацетатом Экстракт был промыт водой и просушен над безводным сульфатом магния Затем етилацетат был отогнан, а остаток был подвергнут очистке методом колоночной хроматографии на силикагеле /гексан этилацетат=5 1/, в результате чего было получено 2,7г (выход 23%) требуемого соединения Температура плавления 127-132°С Пример 16 Приготовление 5-этил-2-/4,6диметоксипиримидин-2-ил-карбонил/-4-/4хлорфенил/пиридин-3-карботиоата (Соединение №152) В 20мл дихлорметана было растворено 0,5г 7/4,6-диметоксипиримидин-2-ил/-7-гидрокси-4-/4хлорфенил/фуро-(3,4-Ь)пиридин-5/7Н/она, после чего к раствору было добавлено 0,29г 3-/3диметиламинопропил/-1-этилкарбодиимид гидрохлорида и 0,09г N,Nдиметиламинопиридина Полученная смесь была подвергнута перемешиванию при комнатной температуре в течение ЗОмин Затем к ней было добавлено 0,08г этилмеркаптана, после чего реакционный раствор был подвергнут перемешиванию в течение 2 часов Затем реакционный раствор был промыт достаточным количеством воды и просушен над безводным сульфатом магния Растворитель был отогнан, а полученный остаток был подвергнут кристаллизации диизопропиловым эфиром, в результате чего было получено 0,45г (выход 81%) требуемого соединения Температура плавления 205 - 207°С Пример 17 Приготовление 4-/5-хлортиофен-2-ил/-2-(/4,6диметоксипиримидин-2-ил/-а-этоксикарбонил-агидроксиметил)никотината (Соединение №102) В 10мл хлороформа было растворено 1,0г этил-4-/5-хлортиофен-2-ил/-2-(/4,6диметоксипиридин-2-ил/-аэтэксикарбонилметил)никотината, после чего к нему было добавлено 0,6г 80%-ной тхлорпербензойной кислоты После перемешивания при комнатной температуре в течение 2 часов реакционный раствор был промыт насыщенным водным раствором гидрокарбоната натрия и насыщенным водным раствором хлорида натрия и просушен над безводным сульфатом магния Растворитель был отогнан, а полученный остаток был подвергнут кристаллизации диизопропиловым эфиром, в результате чего было получено 0,9г (выход 97%) требуемого соединения Температура плавления 109-112°С Пример 18 Приготовление 4-/5-хлортиофен-2-ил/-7-/4,6диметокси-пиримидин-2-ил/-7-этоксикарбонилфуро (3,4-Ь)пиридин-5/7Н/-она (Соединение №272) В 10мл тетрагидрофурана было растворено 0,9г этил-4-/5-хлортиофен-2-ил/-2-(/4,6 34 диметоксипиримидин-2-ил/-а-(-этоксикарбонил-агидроксиметил)никотината, после чего к нему в условиях охлаждения льдом было добавлено 0,08г 60%-ного гидрида натрия После перемешивания при комнатной температуре в течение 1 часа реакционный раствор был залит в ледяную воду и подвергнут экстрагированию этилацетатом Экстракт был промыт достаточным количеством насыщенного водного раствора хлорида натрия и просушен над безводным сульфатом магния Растворитель был отогнан, а полученный остаток был подвергнут кристаллизации диизопропиловым эфиром, в результате чего было получено 0,4г (выход 79%) требуемого соединения Температура плавления 150-156 С Гербициды, предложенные в соответствии с настоящим изобретением, содержат производные никотиновой кислоты общей формулы (I) или (II) в качестве активных ингредиентов В качестве гербицидов соединения, предложенные в соответствии с настоящим изобретением, могут быть использованы сами по себе Однако они могут быть использованы также и в виде выпускных форм, например, дуста, смачивающегося порошка, концентрата эмульсии, микрогранул или гранул, путем их смешивания с разбавителями, поверхностно-активными веществами, диспергирующими агентами или адьювантами, которые широко используются для приготовления выпускных форм В качестве добавок, применяемых для таких выпускных форм, могут быть использованы твердые добавки, например, циклит, тальк, бентонит, глина, каолин, диатомовая земля, белая сажа, вермикулит, карбонат кальция, гашеная известь, кремнистый песок, сульфат аммония или мочевина, или жидкие добавки, например, изопропиловый спирт, ксилол, циклогексанон или метилнафталин В качестве поверхностно-активных веществ и диспергирующих агентов могут быть упомянуты, например, металлическая соль алкилбензолсульфоновой кислоты, металлическая соль динафтилметандисульфоновой кислоты, соль сложного эфира серной кислоты, алкиларилсульфонат, лигнинсульфонат, эфир полиоксиэтиленгликоля, полиоксиэтиленалкилариловый эфир или полиоксиэтиленсорбитмоноалкилат Адьювантами могут быть, например, карбоксиметилцеллюлоза, полиэтиленгликоль или гуммиарабик При практическом применении гербициды могут перед нанесением разбавляться до подходящей концентрадии или наноситься непосредственно Гербициды, предложенные в соответствии с настоящим изобретением, могут использоваться для нанесения на поверхность листвы, почвы или воды Дозировка активного ингредиента при смешивании выбирается с учетом конкретных обстоятельств Однако в случае применения дуста или гранулированного материала доза активного ингредиента выбирается в пределах от 0,01 до 10% по массовой доле, предпочтительно от 0,05 до 5% В случае применения концентрата эмульсии или смачивающегося порошка доза активного ингредиента выбирается в пределах от 1 до 50% по массовой доле, предпочтительно от 5 до 30% 35 36 налкилариловый полимер и алкиларилсульфонат, после чего смесь была подвергнута тщательному перемешиванию с целью получения концентрата эмульсии Пример выпускной формы 5 гранулированный материал 10 частей соединения №246, 80 частей наполнителя, содержащего смесь талька и бентонита при соотношении компонентов 1 3, 5 частей бедой сажи, 5 частей поверхностно-активной смеси, содержащей полиоксиэтиленсорбиталкилат, полиоксиэтиленалкилариловый полимер и алкиларилсульфонат, и 10 частей воды были смешаны и тщательно перемешаны с целью получения пасты, которая была подвергнута экструдированию сквозь сито с отверстиями диаметром 0,7мм Экстру-дированный продукт был просушен и разрезан на отрезки длиной от 0,5 до 1мм с целью получения гранул Соединения, предложенные в соответствии с настоящим изобретением, обладают превосходным гербицидным действием по отношению к различным сорным растениям, которые являются помехой на суходольных участках, в частности, широколистным сорнякам, например, веронике персидской, пупавке венгерской, пастушьей сумке, горцу перечному, щирице нежной, мари белой, канатнику Теофраста, грудинке колючей, конопле, вьюнку пурпурному и дурнишнику обыкновенному, многолетним и однолетним осоковым сорнякам, например, осоке пурпуровой, чуфе, сыти коротколистной, сыти вееровидной, и злаковым сорнякам, например, куриному просу, щетиннику зеленому, мятлику однолетнему, джонсоновой траве, лисохвосту полевому и овсюгу пустому, в широком временном диапазоне от пред всход о во го периода до вегитационного периода Соединения, предложенные в соответствии с настоящим изобретением, могут быть использованы для борьбы с однолетними сорняками рисовых полей, например, куриным просом, сытью длиной мелкоцветной и монохорией, и многолетними сорняками рисовых полей, например, стрелолистом широколистным японским, стрелолистом заостренным, сытью вееровидной, водокрасом, камышом болотным и частухой обыкновенной узколистной 48130 Доза гербицида согласно настоящему изобретению варьируется в зависимости от типа соединения, вида сорных растений, подлежащих уничтожению, характера их роста и развития, условий окружающей среды и вида применяемой выпускной формы Однако в случае применения дуста или гранулированного материала, который используется сам по себе, доза активного ингредиента выбирается в пределах от 0,1 г до 5кг, предпочтительно от 1 г до 1кг, на 10а (102га) В случае применения концентрата эмульсии или смачивающегося порошка, который используется в жидком состоянии, доза активного ингредиента выбирается в пределах от 0,1 до 50000 частей на миллион, предпочтительно от 10 до 10000 частей на миллион Кроме того, соединения, предложенные в соответствии с настоящим изобретением, могут быть использованы в комбинации с инсектицидами, фунгицидами, другими гербицидами, регуляторами роста растений, удобрениями и т п в зависимости от обстоятельств Ниже следует описание способов составления выпускных форм, ведущееся со ссылками на примеры типичных выпускных форм Соединения, типы добавок и соотношения компонентов смесей не ограничиваются такими конкретными примерами и могут быть изменены в широких диапазонах В следующем ниже описании термин "части" относится к массовой доле Пример выпускной формы 1 смачивающийся порошок К 10 частям соединения №244 было подмешано 0,5 части полиоксиэтиленоктилфенилового эфира, 0,5 части натриевой соли конденсата рнафталинсульфоновая кислота-формалин, 20 частей диатомовой земли и 69 частей глины, после чего смесь была подвергнута измельчению с целью получения смачивающегося порока Пример выпускной формы 2 смачивающийся порошок К 10 частям соединения №105 было добавлено 0,5 части полиоксиэтиленоктилфенилового эфира, 0,5 части натриевой соли конденсата рнафталинсульфоновая кислота-формалин, 20 частей диатомовой земли, 5 частей белой сажи и 64 части глины, после чего смесь была подвергнута измельчение с целью получения смачивающегося порошка Пример выпускной формы 3 смачивающийся порошок К 10 частям соединения №3 было подмешано 0,5 части полиоксиэтиленоктилфенилового эфира, 0,5 части натриевой соли конденсата рнафталинсульфоновая кислота-формалин, 20 частей диатомовой земли, 5 частей белой сани и 64 части карбоната кальция, после чего смесь была подвергнута измельчению с целью получения смачивающегося порошка Пример выпускной формы 4 концентрат эмульсии К 30 частям соединения №245 было добавлено 60 частей смеси, состоящей из равных количеств ксилола и изофорона, и 10 частей поверхностно-активной смеси, содержащей полиоксиэтиленсорбиталкилат, полиоксиэтиле Кроме того, соединения, предложенные в соответствии с настоящим изобретением, являются в высшей степени безопасными по отношению к культурам сельскохозяйственного назначения, в частности, к пшенице и ячменю Ниже следует описание гербицидного действия соединений, предложенных в соответствии с настоящим изобретением, ведущееся со ссылками на примеры испытаний Пример испытаний 1 (Испытания на гербицидное действие методом обработки почвы рисового поля) Пластиковые рассадочные горшки площадью 100см2 были наполнены почвой с рисового поля После уплотнения и выравнивания в горшки были засеяны семена куриного проса (Ее), монохории (Мо) и камыша болотного (Sc), после чего горшки были залиты водой с толщиной поверхностного водяного слоя Зсм На следующий день на водную поверхность по каплям были нанесены смачи 37 48130 вающиеся порошки, приготовленные в соответствии с примером выпускной формы 1 и разбавленные водой Доза активного ингредиента составляла ЮОг на 10а (10 2га) Растения выращивались в теплице, а оценка гербицидного действия производилась на 21-ый день после внесения гербицида в соответствии с нормами, определенными в таблице 6 Результаты представлены в таблице 7 Показатель№ 5 4 3 2 1 0 Таблица 6 Гербицидное действие (степень регуляции роста) или фитотоксичность Гербицидное действие или фитотсксичность по меньшей мере 90% Гербицидное действие или фитотокснчность по меньшей мере 70% и менее 90% Гербицидное действие или фитотоксичность по меньшей мере 50% и менее 70% Гербицидное действие или фитотоксичность по меньшей мере 30% и менее 50% Гербицидное действие или фитотоксичность по меньшей мере 10% и менее 30% Гербицидное действие или фитотоксичность отО до менее 10% 38 Пластиковые рассадочные горшки площадью 120см2 были наполнены почвой с суходольного поля Затем в горшки, были засеяны семена куриного проса (Ее), горца перечного (Ро), щирицы нежной (Am), мари белой (Сп) и сыти вееровидной (Сі) И накрыты слоем почвы Затем на поверхность почвы с помощью малогабаритного опрыскивателя равномерно были нанесены смачивающиеся порошки, приготовленные в соответствии с примером выпускной формы 1 и разбавленные водой, в количестве 100л на 10а (102га), что соответствовало ЮОг активного ингредиента на 10а (102га) Затем растения выращивались в теплице, а оценка гербицидного действия производилась на 21 -ый день после нанесения в соответствии с нормами, определенными в таблице 6 Результаты представлены в таблице 8 Таблица 8 Соединение№ Таблица 7 Гербицидное действие Соединение№ 1 2 23 37 38 60 61 62 77 95 98 99 100 102 103 104 105 106 107 108 112 135 136 137 138 144 145 146 147 148 149 150 152 156 160 161 162 228 229 244 245 246 272 273 Ее 5 4 5 6 5 5 5 5 5 5 4 5 4 5 5 5 5 5 5 5 4 5 5 5 4 5 5 5 5 5 5 5 5 4 5 5 5 5 5 5 5 5 5 5 Мо 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 4 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 Sc 5 4 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 555 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 Пример испытаний 2 (Испытания на гербицидное действие методом обработки почвы суходола) 1 2 37 38 60 61 Ее 5 4 5 5 5 5 62 77 95 98 99 100 101 102 103 104 105 106 107 108 112 135 136 137 138 144 145 146 147 148 149 150 152 156 160 161 162 208 228 229 244 245 246 272 273 5 5 5 5 5 5 3 5 3 3 5 5 5 5 5 5 5 5 5 5 4 4 4 5 4 5 4 5 5 5 5 5 5 5 5 5 5 5 5 Гербицидное действие Ро Am Ch 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 4 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 Сі 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 Пример испытаний 3 (Испытания на гербицидное действие методом обработки листвяного покрова суходола) Пластиковые рассадочные горшки площадью 120см2 были наполнены почвой с суходольного 39 48130 поля Затем в горшки были засеяны семена куриного проса (Ее), горца перечного (Ро), щирицы нежной (Am), мари белой (Ch) и сыти вееровидной (Сі) И накрыты слоем почвы После этого растения выращивались в теплице в течение 2 недель Затем сверху на поверхность всего листвяного покрова растении с помощью малогабаритного опрыскивателя были нанесены смачивающиеся порошки, приготовленные в соответствии с примером выпускной формы 1 и разбавленные водой, в количестве 100л на 10а (10 2 га), что соответствовало ЮОг активного ингредиента на Юа (102га) Затем растения были оставлены в теплице для дальнейшего выращивания, а оценка гербицидного действия производилась на 14-ый день после обработки в соответствии с нормами, определенными в таблице 6 Результаты представлены в таблице 9 Таблица 9 Соединение№ 1 2 23 37 38 60 61 62 77 95 98 99 100 102 104 105 106 107 108 112 135 136 137 138 144 145 146 147 148 149 150 151 152 156 160 161 162 171 208 209 228 229 244 245 246 272 279 Ее 5 5 5 5 5 5 5 5 5 5 5 5 5 4 4 5 5 5 5 5 5 5 4 5 5 4 4 4 4 4 4 4 5 4 5 5 5 4 5 5 5 5 5 5 5 5 5 Гербицидное действие Ро Am Ch 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 4 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 4 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 4 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 Сі 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 Пример испытаний 4 (Испытания на избирательность к сельскохозяйственным культурам методом обработки почвы суходола) Пластиковые рассадочные горшки площадью 600см2 были наполнены почвой с суходольного 40 поля Затем в горшки были засеяны семена пшеницы (Тг), лисохвоста полевого (АІ), горца перечного (Ро), щирицы нежной (Am) и мари белой (Ch) и накрыты слоем почвы На следующий день на поверхность почвы с помощью малогабаритного опрыскивателя равномерно были нанесены смачивающиеся порошки, содержащие заданные количества активных ингредиентов (аи, г/10 а), приготовленные в соответствии с примером выпускной формы 1 и разбавленные водой, в ко2 личестве 100л на 10а (10 га) Затем растения были помещены в теплицу для выращивания, а оценка гербицидного действия производилась на 21-ый день после нанесения в соответствии с нормами, определенными в таблице 6 Результаты, включая относящиеся к соединениям, взятым для сравнения, представлены в таблице 10 Соединение № Доза Гербицидное действие Таблица 10 Фитотоксичность Тг 0 0 1 1 60 62 95 98 ган/10а 16 04 04 63 Al 5 4 5 5 Po 5 5 5 5 Am 5 5 5 5 Ch 3 5 5 5 99 100 16 63 5 5 5 5 5 5 5 5 0 1 101 103 272 244 63 63 63 04 5 4 5 4 5 5 5 5 5 5 5 5 5 5 5 3 0 0 0 0 "1 "2 16 63 5 3 5 4 5 4 5 5 3 2 "3 "4 63 63 1 1 4 4 5 5 1 1 4 4 *1 Соединение для сравнения А метил-2хлор-6-/4,6-диметоксипиримидин-2ил/карбонилбензоат (Соединение №55 по ЕРО461079) *2 Соединение для сравнения Б 2-/4,6диметоксипиримидин-2-ил/метил никотиновая кислота (Соединение №6 по W091 /10653, Соединение №1 по DE4026079) *3 Соединение для сравнения В 7-/4,6диметоксипиримидин-2-ил/-7-гидрокси-фуро(3,4Ь)пиридин-5/7Н/он (Соединение №175 по ЕРО161079) *4 Соединение для сравнения Г 2-/4,6диметоксипиримидин-2-ил/карбонилникотинат (Соединение №176 по ЕР0461079) Пример испытаний 5 (Испытания на избирательность к сельскохозяйственным культурам методом обработки листвяного покрова суходола) Пластиковые рассадочные горшки площадью 600см2 были наполнены почвой с суходольного поля Затем в горшки были засеяны семена пшеницы (Тг), лисохвоста полевого (AI), горца перечного (Ро), щирицы нежной (Am) и мари белой (Ch), после чего растения выращивались в теплице в течение 2 недель Затем сверху на поверхность всего листвяного покрова растений с помощью малогабаритного опрыскивателя были нанесены смачивающиеся порошки, содержащие заданные количества активных ингредиентов (аи, г/10 а), приготовленные в соответствии с примером выпускной формы 1 и разбавленные водой, в количе 41 48130 2 стве 100л на 10а (10 га) Затем растения были помещены в теплицу для дальнейшего выращивания, а оценка гербицидного действия производилась на 14-ый день после обработки в соответствии с нормами, определенными в таблице 6 Результаты, включая относящиеся к соединениям, взятым для сравнения, представлены в таблице 11 Таблица 11 Соеди- Доза нение № ан г /10а 98 63 Гербицидное действие Al 5 Po 5 Am 5 Ch 5 Фитотоксичность Тг 0 42 99 105 106 272 244 "3 "4 "5 63 04 04 25 04 25 63 25 63 25 5 5 5 5 5 1 1 2 1 3 5 5 5 5 5 5 4 5 4 5 5 5 5 5 4 5 5 5 5 4 4 4 4 5 3 5 4 5 5 4 0 0 0 0 0 4 3 4 3 2 *5 Соединение для сравнения Д этил-2-(ациано-/4,6-диметоксипиримидин-2ил/)метилникотинат (Соединение №142 по ЕР0461079) ДП «Український інститут промислової власності» (Укрпатент) вул Сім'ї Хохлових, 15, м Київ, 04119, Україна ( 0 4 4 ) 4 5 6 - 2 0 - 90 ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)216-32-71
ДивитисяДодаткова інформація
Назва патенту англійськоюNicotinic acid derivatives, a process for their producing and a herbicidal composition on their basis
Автори англійськоюMiyazawa Takeshige
Назва патенту російськоюПроизводные никотиновой кислоты, способ их получения и гербицидная композиция на их основе
Автори російськоюМиязава Такешиге
МПК / Мітки
МПК: C07D 401/06, C07D 405/14, C07D 401/14, A01N 43/08, A01P 13/00, A01N 43/10, C07D 409/14, A01N 43/40, A01N 43/54
Мітки: похідні, отримання, спосіб, композиція, гербіцидна, нікотинової, основі, кислоти
Код посилання
<a href="https://ua.patents.su/21-48130-pokhidni-nikotinovo-kisloti-sposib-kh-otrimannya-i-gerbicidna-kompoziciya-na-kh-osnovi.html" target="_blank" rel="follow" title="База патентів України">Похідні нікотинової кислоти, спосіб їх отримання і гербіцидна композиція на їх основі</a>
Попередній патент: Ванна та спосіб хімічного полірування поверхонь з нержавіючої сталі
Наступний патент: Cпосіб одержання ацетилену і синтез-газу
Випадковий патент: Автоматична побутова пральна машина з умивальником