Комбіноване застосування інгібітора pde4 та інгібітора нmg-cоa-редуктази для профілактики або зцілювального лікування запального захворювання легенів
Номер патенту: 106422
Опубліковано: 26.08.2014
Автори: Браун Клеменс, Воллін Штефан-Лутц, Маркс Дегенхард, Вользен Андреа
Формула / Реферат
1. Фармацевтична композиція, що являє собою фармацевтичну лікарську форму, що містить у певній кількості інгібітор PDE4, у певній кількості інгібітор HMG-CoA-редуктази і щонайменше одну фармацевтично прийнятну допоміжну речовину, де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою симвастатин або його фармацевтично прийнятну сіль, і де перша кількість і друга кількість разом становлять ефективну кількість для профілактики або зцілювального лікування запального захворювання легенів.
2. Фармацевтична композиція за п. 1, в якій інгібітор PDE4 являє собою рофлуміласт.
3. Фармацевтична композиція за п. 1, в якій інгібітор PDE4 являє собою рофлуміласт-N-оксид.
4. Фармацевтична композиція за будь-яким з пп. 1-3, в якій інгібітор НМО-СоА-редуктази являє собою симвастатин.
5. Фармацевтична композиція за будь-яким з пп. 1-4, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію.
6. Фармацевтична композиція за будь-яким з пп. 1-4, де запальне захворювання легенів являє собою ХОЗЛ.
7. Комбінація, що містить наступні компоненти: (А) у певній кількості інгібітор PDE4; (Б) у певній кількості інгібітор HMG-CoA-редуктази; де перша кількість і друга кількість разом становлять ефективну кількість для профілактики або зцілювального лікування запального захворювання легенів, і де кожний з компонентів (А) і (Б) включений до складу препаративної форми разом із щонайменше однією фармацевтично прийнятною допоміжною речовиною, і де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою симвастатин або його фармацевтично прийнятну сіль.
8. Комбінація за п. 7, в якій інгібітор PDE4 являє собою рофлуміласт.
9. Комбінація за п. 7, в якій інгібітор PDE4 являє собою рофлуміласт-N-оксид.
10. Комбінація за будь-яким з пп. 7-9, в якій інгібітор HMG-CoA-редуктази являє собою симвастатин.
11. Комбінація за будь-яким з пп. 7-10, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію.
12. Комбінація за будь-яким з пп. 7-10, де запальне захворювання легенів являє собою ХОЗЛ.
13. Набір, що містить наступні компоненти: (А) фармацевтичну лікарську форму, що містить у певній кількості інгібітор PDE4 в суміші з щонайменше однією фармацевтично прийнятною допоміжною речовиною; (Б) фармацевтичну лікарську форму, що містить у певній кількості інгібітор PIMG-CoA-редуктази в суміші з щонайменше однією фармацевтично прийнятною допоміжною речовиною; де перша кількість і друга кількість разом становлять ефективну кількість для профілактики або зцілювального лікування запального захворювання легенів, і де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою симвастатин або його фармацевтично прийнятну сіль.
14. Набір за п. 13, в якому інгібітор PDE4 являє собою рофлуміласт.
15. Набір за п. 13, в якому інгібітор PDE4 являє собою рофлуміласт-N-оксид.
16. Набір за будь-яким з пп. 13-15, в якому інгібітор HMG-CoA-редуктази являє собою симвастатин.
17. Набір за будь-яким з пп. 13-16, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію.
18. Набір за будь-яким з пп. 13-16, де запальне захворювання легенів являє собою ХОЗЛ.
19. Застосування інгібітора PDE4 або його фармацевтично прийнятної солі і інгібітора HMG-CoA-редуктази або його фармацевтично прийнятної солі для приготування лікарського засобу, що являє собою фармацевтичну композицію згідно з винаходом, призначеного для профілактики або зцілювального лікування запального захворювання легенів, де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор НМО-СоА-редуктази являє собою симвастатин або його фармацевтично прийнятну сіль.
20. Застосування інгібітора PDE4 або його фармацевтично прийнятної солі і інгібітора HMG-CoA-редуктази або його фармацевтично прийнятної солі для приготування призначеного для профілактики або зцілювального лікування запального захворювання легенів лікарського засобу, що являє собою комбінацію або набір згідно з винаходом, який можна вводити послідовно або роздільно, де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою симвастатин або його фармацевтично прийнятну сіль.
21. Застосування за будь-яким з пп. 19 або 20, де інгібітор PDE4 являє собою рофлуміласт.
22. Застосування за будь-яким з пп. 19 або 20, де інгібітор PDE4 являє собою рофлуміласт-N-оксид.
23. Застосування за будь-яким з пп. 19, 20, 21 або 22 де інгібітор HMG-CoA-редуктази являє собою симвастатин.
24. Застосування за будь-яким з пп. 19-23, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію.
25. Застосування за будь-яким з пп. 19-23, де запальне захворювання легенів являє собою ХОЗЛ.
26. Спосіб приготування фармацевтичної композиції за будь-яким з пп. 1-6, який полягає в тому, що змішують інгібітор PDE4 або його фармацевтично прийнятну сіль із інгібітором HMG-CoA-редуктази або його фармацевтично прийнятною сіллю.
27. Фармацевтична композиція, що являє собою фармацевтичну лікарську форму, що містить у певній кількості інгібітор PDE4, у певній кількості інгібітор HMG-CoA-редуктази і щонайменше одну фармацевтично прийнятну допоміжну речовину, де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-oкcид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою аторвастатин або його фармацевтично прийнятну сіль, і де перша кількість і друга кількість разом становлять ефективну кількість для профілактики або зцілювального лікування запального захворювання легенів.
28. Фармацевтична композиція за п. 27, в якій інгібітор PDE4 являє собою рофлуміласт.
29. Фармацевтична композиція за п. 27, в якій інгібітор PDE4 являє собою рофлуміласт-N-оксид.
30. Фармацевтична композиція за будь-яким з пп. 27-29, в якій інгібітор HMG-CoA-редуктази являє собою аторвастатин.
31. Фармацевтична композиція за будь-яким з пп. 27-29, в якій інгібітор HMG-CoA-редуктази являє собою сесквігідрат аторвастатин гемікальцію.
32. Фармацевтична композиція за будь-яким з пп. 27-31, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію.
33. Фармацевтична композиція за будь-яким з пп. 27-31, де запальне захворювання легенів являє собою ХОЗЛ.
34. Комбінація, що містить наступні компоненти: (А) у певній кількості інгібітор PDE4; (Б) у певній кількості інгібітор HMG-CoA-редуктази; де перша кількість і друга кількість разом становлять ефективну кількість для профілактики або зцілювального лікування запального захворювання легенів, і де кожний з компонентів (А) і (Б) включений до складу препаративної форми разом із щонайменше однією фармацевтично прийнятною допоміжною речовиною, і де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою аторвастатин або його фармацевтично прийнятну сіль.
35. Комбінація за п. 34, в якій інгібітор PDE4 являє собою рофлуміласт.
36. Комбінація за п. 34, в якій інгібітор PDE4 являє собою рофлуміласт-N-оксид.
37. Комбінація за будь-яким з пп. 34-36, в якій інгібітор HMG-CoA-редуктази являє собою аторвастатин.
38. Комбінація за будь-яким з пп. 34-36, в якій інгібітор HMG-CoA-редуктази являє собою сесквігідрат аторвастатин гемікальцію.
39. Комбінація за будь-яким з пп. 34-38, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію.
40. Комбінація за будь-яким з пп. 34-38, де запальне захворювання легенів являє собою ХОЗЛ.
41. Набір, що містить наступні компоненти: (А) фармацевтичну лікарську форму, що містить у певній кількості інгібітор PDE4 в суміші з щонайменше однією фармацевтично прийнятною допоміжною речовиною; (Б) фармацевтичну лікарську форму, що містить у певній кількості інгібітор HMG-CoA-редуктази в суміші з щонайменше однією фармацевтично прийнятною допоміжною речовиною; де перша кількість і друга кількість разом становлять ефективну кількість для профілактики або зцілювального лікування запального захворювання легенів, і де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою аторвастатин або його фармацевгично прийнятну сіль.
42. Набір за п. 41, в якому інгібітор PDE4 являє собою рофлуміласт.
43. Набір за п. 41, в якому інгібітор PDE4 являє собою рофлуміласт-N-оксид.
44. Набір за будь-яким з пп. 41-43, в якому інгібітор HMG-CoA-редуктази являє собою аторвастатин.
45. Набір за будь-яким з пп. 41-43, в якому інгібітор HMG-CoA-редуктази являє собою сесквігідрат аторвастатин гемікальцію.
46. Набір за будь-яким з пп. 41-45, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію.
47. Набір за будь-яким з пп. 41-45, де запальне захворювання легенів являє собою ХОЗЛ.
48. Застосування інгібітора PDE4 або його фармацевтично прийнятної солі і інгібітора HMG-CoA-редуктази або його фармацевтично прийнятної солі для приготування лікарського засобу, що являє собою фармацевтичну композицію згідно з винаходом, призначеного для профілактики або зцілювального лікування запального захворювання легенів, де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою аторвастатин або його фармацевтично прийнятну сіль.
49. Застосування інгібітора PDE4 або його фармацевтично прийнятної солі і інгібітора НMG-CoA-редуктази або його фармацевтично прийнятної солі для приготування призначеного для профілактики або зцілювального лікування запального захворювання легенів лікарського засобу, що являє собою комбінацію або набір згідно з винаходом, який можна вводити послідовно або роздільно, де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийняту сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою аторвастатин або його фармацевтично прийнятну сіль.
50. Застосування за будь-яким з пп. 48 або 49, в якому інгібітор PDE4 являє собою рофлуміласт.
51. Застосування за будь-яким з пп. 48 або 49 в якому інгібітор PDE4 являє собою рофлуміласт-N-оксид.
52. Застосування за будь-яким з пп. 48, 49, 50 або 51, в якому інгібітор HMG-CoA-редуктази являє собою аторвастатин.
53. Застосування за будь-яким з пп. 48, 49, 50 або 51, в якому інгібітор HMG-CoA-редуктази являє собою сесквігідрат аторвастатин гемікальцію.
54. Застосування за будь-яким з пп. 48-53, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію.
55. Застосування за будь-яким з пп. 48-53, де запальне захворювання легенів являє собою ХОЗЛ.
56. Спосіб приготування фармацевтичної композиції за будь-яким з пп. 27-33, який полягає в тому, що змішують інгібітор PDE4 або його фармацевтично прийнятну сіль із інгібітором HMG-CoA-редуктази або його фармацевтично прийнятною сіллю.
Текст
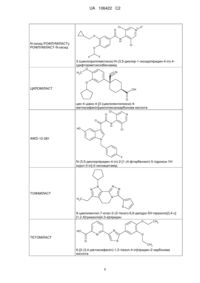
Реферат: Винахід стосується комбінованого застосування інгібітора PDE 4 (рофлуміласту) і інгібітора HMG-СоА-редуктази (симвастатину, аторвастатину) для профілактики або зцілювального лікування запального захворювання легень. UA 106422 C2 (12) UA 106422 C2 UA 106422 C2 5 10 15 20 25 30 35 40 45 50 55 Даний винахід належить до комбінації певних відомих терапевтичних сполук, призначеної для терапевтичних цілей. Сполуки, які застосовують у комбінаціях, пропонованих у винаході, являють собою відомі діючі речовини із класу інгібіторів фосфодіестерази 4 (PDE4) і діючі речовини із класу інгібіторів HMG-CoA-редуктази. Статини широко застосовують як терапевтичні засоби, що знижують рівень холестерину. Вони знижують рівні холестерину шляхом конкурентного інгібування 3-гідрокси-3метилглутарил-кофермент А-(HMG-Co)-редуктази, що має вирішальне значення ферменту, що регулює синтез холестерину. Знижуюча рівень холестерину дія статинів обумовлена також збільшенням поглинання холестерину клітинами в результаті внутрішньоклітинного виснаження холестерину й посилення експресії рецепторів ліпопротеїну низкої щільності (ЛПНП). Однак статини мають певні властивості крім їхньої понижувальної рівень ліпідів дії. Зазначені не пов'язані зі зниженням рівня ліпідів властивості включають інгібування ізопреноїдного шляху, у тому числі шляху попередника холестерину мевалонату, що є необхідним попередником для пренилювання численних білків, що приводять до зміни функції [Drugs of Today, 40, 2004, сс. 975-990]. Наприклад, симвастатин модулює експресію хемокіну й хемокінового рецептора за допомогою геранілізопреноїдного шляху в людських ендотеліальних клітинах і макрофагах [Veillard N.R. і ін., Simvastatin modulates chemokine and chemokine receptor expression by geranylgeranyl isoprenoid pathway in human endothelial cells and macrophages. Atherosclerosis, 28 листопада 2005 p.; електронна публікація вищевказаної статті (Epub ahead of print)]. Статини грають також важливу роль як антиоксиданти, викликаючи понижувальну регуляцію запалення [Drugs of Today, 40, 2004, сс. 975-990]. Результати сучасних досліджень свідчать про те, що статини інгібують індукцію експресію головного комплексу гістосумісності (ГКГ) класу II, викликувану інтерферон-гамма (IFN-гамма), приводячи до пригнічення опосередковуваної ГКГ II Т-клітинної активації. Крім того, статини інгібують експресію специфічних рецепторів клітинної поверхні на моноцитах, молекулах адгезії, а також залежну від інтегрину адгезію лейкоцитів [Timely Top Med Cardiovasc Dis, 9, 2005, с. Е3]. Статини роблять додаткові впливи на запалення шляхом зниження синтезу IL-6, IL-8 і МСР-1 у людських гладком'язових судинних клітинах (VSMC) in vitro [Cardiovas Res, 59, 2003, сс. 755-766]. Симвастатин інгібує експресію фактора росту й модулює профіброгенні маркери в легеневих фібробластах [Am J Respir Cell Моl Biol., 32, 2005, сс. 290-300]. Крім того, статини підвищують біологічну доступність оксиду азоту. Церивастатин підвищує експресію eNOS і вивільнення NO у людських епітеліальних клітинах [J Physiol Pharmacol., 53, 2002, сс. 585-595]. In vivo статини чинять протизапальні дії на багатьох моделях запальних захворювань дихальних шляхів типу астми й хронічного обструктивного захворювання легень (ХОЗЛ). Було встановлено, що симвастатин інгібує акумулювання запальних клітин у легень і вивільнення IL-4 і IL-5 в альвеолярну порожнину після контрольного зараження алергеном у мишей J Immunol., 172, 2004, сс. 2903-2908]. Симвастатин інгібує індуковану палінням сигарет емфізему й легеневу гіпертензію в легких щурів [Am J Respir Crit Care Med., 172, 2005, cc. 987-993]. У цілому, статини мають інгібуючі властивості відносно запалення й мають здатність модулювати імунну систему. У міжнародній заявці на патент WO 00/48626 (на ім'я University of Washington) описані аерозольні композиції інгібіторів HMG-СоА-редуктази, призначені для інгібування запалення, асоційованого із захворюваннями легень, такими як астма, інтерстиціальний пневмоніт, емфізема, хронічний бронхіт, респіраторний дистрес -синдром дорослих (ARDS) і муковісцидоз. В ЕР 1275388 (на ім'я фірми Takeda) описані деякі статини як засоби, придатні для лікування асоційованих з TNF (захворювань, таких як запальні, включаючи астму й ХОЗЛ). В US 2005 0119330 описане застосування HMG-СоА-редуктази для лікування проліферативних судинних захворювань легень, таких, наприклад, як легенева гіпертензія й фіброз легень. Існує виражена потреба в удосконалюванні лікування запальних захворювань легень, таких як астма й ХОЗЛ. Зазначені запальні захворювання характеризуються багатофакторними патологіями. У них беруть участь кілька запальних медіаторів, а також різні типи клітин. Тому в медичній практиці лікування, наприклад, астми й ХОЗЛ шляхом спрямованого впливу на один медіатор або тип клітин не дає задовільних результатів. У цей час як для астми, так і для ХОЗЛ, використають комбіновану терапію, однак у багатьох випадках вона має обмежений успіх, насамперед у відношенні ХОЗЛ. Інгібітори циклічної нуклеотидфосфодіестерази (PDE), насамперед типу 4 (PDE4), можна застосовувати для лікування різноманітних алергійних і запальних захворювань, наприклад, захворювань дихальних шляхів, таких як астма й хронічне обструктивне захворювання легень. Інгібітори HMG-СоА-редуктази, механізм дії яких відмінний від механізму дії інгібіторів PDE4, також можна застосовувати при лікуванні запальних захворювань. 1 UA 106422 C2 5 10 15 20 25 30 35 40 45 50 55 60 Існує потреба в розробці комбінацій і способів лікування, які завдяки перевазі використання різних терапевтичних механізмів дії інгібітора PDE4 і інгібітори HMG-СоА-редуктази дозволяють більш ефективно лікувати запальні порушення, насамперед астму й ХОЗЛ. При створенні винаходу несподівано було встановлено, що спільне застосування інгібітора PDE4 і інгібітори HMG-СоА-редуктази підсилює протизапальну дію кожного з індивідуальних компонентів. Таким чином, першим об'єктом даного винаходу є фармацевтична композиція, що являє собою фармацевтичну препаративну форму, що містить у певній кількості інгібітор PDE4 або його фармацевтично прийнятну сіль, у певній кількості інгібітор HMG-СоА-редуктази або його фармацевтично прийнятну сіль, де перша кількість і друга кількість разом становлять кількість, ефективну для профілактики або зцілювального лікування запального захворювання легень, і щонайменше одне фармацевтично прийнятна допоміжна речовина. Зазначена вище фармацевтична композиція містить призначені для введення інгібітор PDE4 або його фармацевтично прийнятну сіль у сполученні з інгібітором HMG-СоА-редуктази або його фармацевтично прийнятною сіллю й, таким чином, являє собою єдину препаративну форму. В альтернативному варіанті інгібітор PDE4 або його фармацевтично прийнятна сіль і інгібітор HMG-СоА-редуктази або його фармацевтично прийнятна сіль можуть бути присутнім у різних препаративних формах, де щонайменше одна з таких препаративних форм містить інгібітор PDE4 або його фармацевтично прийнятну сіль і щонайменше одна містить інгібітор HMG-СоА-редуктази або його фармацевтично прийнятну сіль. Таким чином, об'єктами винаходу, що випливають, є: Комбінований продукт, що включає наступні компоненти: (А) інгібітор PDE4 або його фармацевтично прийнятну сіль у певній кількості; (Б) інгібітор HMG-СоА-редуктази або його фармацевтично прийнятну сіль у певній кількості; де перша й друга кількості разом становлять кількість, ефективну для профілактики або зцілювального лікування запального захворювання легень, і де кожний з компонентів (А) і (Б) входить до складу препаративної форми в суміші щонайменше з одною фармацевтично прийнятною допоміжною речовиною. Набір, що включає наступні компоненти: (А) фармацевтичну композицію, що містить у певній кількості інгібітор PDE4 або його фармацевтично прийнятну сіль у суміші щонайменше з одним фармацевтично прийнятною допоміжною речовиною; (Б) фармацевтичну композицію, що містить у певній кількості інгібітор HMG-СоА-редуктази або його фармацевтично прийнятну сіль у суміші щонайменше з одним фармацевтично прийнятною допоміжною речовиною; де перша й друга кількості разом становлять кількість, ефективну для профілактики або зцілювального лікування запального захворювання легень. Комбінації, пропоновані у винаході, можна застосовувати для профілактики або зцілювального лікування запального захворювання легень, такого, наприклад, як астма, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легень і легенева гіпертензія. Таким чином, об'єктами винаходу, що випливають, є: Комбінація інгібітора PDE4 або його фармацевтично прийнятні солі й інгібітора HMG-СоАредуктази або його фармацевтично прийнятної солі, призначена для застосування як лікарський засіб. Комбінація інгібітора PDE4 або його фармацевтично прийнятної солі й інгібітора HMG-СоАредуктази або його фармацевтично прийнятної солі, призначена для профілактики або зцілювального лікування запального захворювання легень. Фармацевтична композиція, комбінований продукт або набір, зазначені в попередніх параграфах, призначені для застосування як лікарський засіб. Фармацевтична композиція, комбінований продукт або набір, зазначені в попередніх параграфах, призначені для профілактики або зцілювального лікування запального захворювання легень. Застосування інгібітора PDE4 або його фармацевтично прийнятні солі й інгібітора HMG-СоАредуктази або його фармацевтично прийнятної солі для готування лікарського засобу, насамперед фармацевтичної композиції, пропонованої у винаході, для профілактики або зцілювального лікування запального захворювання легень. Ще одним об'єктом даного винаходу є застосування інгібітора PDE4 або його фармацевтично прийнятні солі й інгібітора HMG-СоА-редуктази або його фармацевтично прийнятної солі для готування лікарського засобу, насамперед комбінованого продукту або набору, пропонованого у винаході, яке можна застосовувати шляхом послідовного або роздільного спільного введення, для профілактики або зцілювального лікування запального захворювання легень. 2 UA 106422 C2 5 10 15 20 25 30 35 40 45 50 55 60 Наступним об'єктом даного винаходу є спосіб профілактичного або зцілювального лікування запального захворювання легень, що полягає в тім, що пацієнтові, що потребує цього, уводять фармацевтичну композицію, що являє собою фармацевтичну препаративну форму, що містить у певній кількості інгібітор PDE4 або його фармацевтично прийнятну сіль, у певній кількості інгібітор HMG-СоА-редуктази або його фармацевтично прийнятну сіль; де перша й друга кількості разом становлять кількість, ефективну для профілактики або зцілювального лікування запального захворювання легень, і щонайменше одну фармацевтично прийнятну допоміжну речовину. Іншим об'єктом даного винаходу є спосіб профілактичного або зцілювального лікування запального захворювання легень, що полягає в тім, що пацієнтові, що потребує цього, уводять комбінований продукт, що включає наступні компоненти: (А) інгібітор PDE4 або його фармацевтично прийнятну сіль у певній кількості; (Б) інгібітор HMG-СоА-редуктази або його фармацевтично прийнятну сіль у певній кількості, де перша й друга кількості разом становлять кількість, ефективну для профілактики або зцілювального лікування запального захворювання легень; де кожний з компонентів (А) і (Б) включений до складу препаративної форми в суміші щонайменше з одним фармацевтично прийнятною допоміжною речовиною; і де компоненти (А) і (Б) уводять одночасно, послідовно або окремо. Фармацевтичні композиції, пропоновані у винаході, можна наготовлювати шляхом змішування першого діючої речовини із другою діючою речовиною. При здійсненні зазначеного вище процесу змішування першу діючу речовину й другу діючу речовину можна а) змішувати на першій стадії самі по собі, після чого піддавати обробці із застосуванням щонайменше одної фармацевтично прийнятної допоміжної речовини й, у завершення, наприклад, спресовувати в таблетки або каплетки, або б) на першій стадії окремо піддавати обробці із застосуванням щонайменше одної фармацевтично прийнятної допоміжної речовини з одержанням гранул або пелетів, кожна(ий) з яких містить тільки одну із двох діючих речовин; потім пелети або гранули у свою чергу можна змішувати у відповідному співвідношенні й або спресовувати (необов'язково разом з додатковими фармацевтично прийнятними допоміжними речовинами) з одержанням, наприклад, таблеток або каплеток, або ними можна без обробки заповнювати капсули. Таким чином, ще одним об'єктом даного винаходу є спосіб готування фармацевтичної композиції, що полягає в тім, що змішують першу діючу речовину, що являє собою інгібітор PDE4 або його фармацевтично прийнятну сіль, із другою діючою речовиною, що являє собою інгібітор HMG-СоА-редуктази або його фармацевтично прийнятну сіль. Одночасне введення інгібітора PDE4 або його фармацевтично прийнятної солі й інгібітора HMG-СоА-редуктази або його фармацевтично прийнятної солі можна здійснювати переважно шляхом введення пацієнтові, що має потребу в терапії запального захворювання легень, фармацевтичної композиції, пропонованої у винаході, у вигляді однієї лікарської форми, такої, наприклад, як одна капсула, таблетка, або за допомогою однократної ін'єкції. Компоненти (А) і (Б) комбінованого продукту, а також набору, можна вводити послідовно або роздільно в процесі профілактики або зцілювального лікування запального захворювання легень. Послідовне або роздільне введення інгібітора PDE4 або його фармацевтично прийнятної солі й інгібітора HMG-СоА-редуктази або його фармацевтично прийнятної солі можна переважно здійснювати шляхом введення пацієнтові, що потребує терапії запального захворювання легень, компонентів (А) і (Б), що входять до складу комбінованого продукту або набору, пропонованого у винаході, у вигляді (декількох) індивідуальних форм, таких, наприклад, як індивідуальні капсули, таблетки, або вводити шляхом індивідуальних ін'єкцій. Компоненти (А) і (Б), що входять до складу комбінованого продукту або набору, пропонованого у винаході, можна вводити також одночасно, наприклад, шляхом проковтування двох таблеток, що містять обидві діючих речовини, у той самий час або з використанням інгаляційної системи, що містить обидві діючих речовини у різних контейнерах, але дозволяє здійснювати їхнє спільне введення. В альтернативному варіанті один з компонентів (А) і (Б) може перебувати у вигляді такої препаративної форми, як таблетка або капсула, а другий компонент може перебувати у вигляді препаративної форми, призначеної для введення, наприклад, шляхом ін'єкції або інгаляції. Послідовне введення має на увазі короткий проміжок часу між введенням компонентів (А) і (Б), що входять до складу комбінованого продукту або набору, пропонованого у винаході (наприклад, проміжок часу, необхідний для проковтування однієї таблетки після іншої). 3 UA 106422 C2 5 10 15 20 25 30 35 40 45 50 55 Роздільне введення відноситься як до відносно коротких, так і відносно довгих проміжків часу між введенням компонентів (А) і (Б), що входять до складу комбінованого продукту або набору, пропонованого у винаході. Однак, для цілей даного винаходу щонайменше один з компонентів уводять у той період часу, коли інший компонент усе ще впливає на пацієнта, що піддається лікуванню. У кращому варіанті здійснення винаходу вплив на пацієнта, що піддається лікуванню, є синергетичним. Комбіноване введення інгібітора PDE4 або його фармацевтично прийнятні солі й інгібітора HMG-СоА-редуктази або його фармацевтично прийнятної солі у формі фармацевтичної композиції, комбінованого продукту або набору, пропонованого у винаході, дозволяє здійснювати ефективне профілактичне або зцілювальне лікування запального захворювання легень і в кращому варіанті здійснення винаходу є більш ефективним у порівнянні із застосуванням кожної діючої речовини індивідуально. Більше того, у найбільш кращому варіанті здійснення винаходу комбіноване введення інгібітора PDE4 або його фармацевтично прийнятної солі й інгібітора HMG-СоА-редуктази або його фармацевтично прийнятної солі робить синергетичний вплив при лікуванні запального захворювання легень. У контексті даного опису поняття "синергетичний" відноситься до комбінації інгібітора PDE4 або його фармацевтично прийнятної солі й інгібітора HMG-СоА-редуктази або його фармацевтично прийнятної солі у формі фармацевтичної композиції, комбінованого продукту або набору, пропонованого у винаході, ефективність якого відносно профілактики або зцілювального лікування запального захворювання легень перевищує очікувану суму впливів компонентів при їхньому індивідуальному введенні. Синергетичні дії для різних варіантів здійснення даного винаходу включають додаткові несподівані переваги відносно профілактики або зцілювального лікування запального захворювання легень. Такі додаткові переваги можуть включати (але не обмежуючись тільки ними) зниження необхідної дози одної або декількох діючих речовин, що входять у комбінацію, зниження побічних дій одної або декількох діючих речовин, що входять у комбінацію, або досягнення більшої переносимості одної або декількох діючих речовин пацієнтом, що потребує терапії запального захворювання легень. Комбіноване введення інгібітора PDE4 або його фармацевтично прийнятні солі й інгібітора HMG-СоАредуктази або його фармацевтично прийнятної солі можна застосовувати також для зниження необхідної кількості окремих доз, що потенційно поліпшує дотримання режиму й схеми лікування пацієнтом, що потребує в терапії запального захворювання легень. Терапевтичний вплив комбінацій, пропонованих у винаході, може проявлятися також відносно швидкого зниження функції легень, що є ознакою ХОЗЛ, впливи можуть проявлятися відносно системного запалення, що також є характерною ознакою ХОЗЛ. Тривалий вплив комбінацій, пропонованих у винаході, повинний полягати в збереженні функції легень і можливо в меншій супутній захворюваності (оцінюваної по впливі на системне запалення). Поняття "діюча речовина" у контексті даного опису відноситься до сполуки, яку можна застосовувати для профілактики або зцілювального лікування захворювання. Поняття "ефективна кількість" у контексті даного опису відноситься до терапевтично ефективної кількості для лікування запального захворювання легень. Стосовно до комбінованої терапії поняття "ефективна кількість" відноситься до сумарної кількості компонентів, що входять у комбінацію, що є терапевтично ефективним для профілактики або зцілювального лікування запального захворювання легень. Поняття "пацієнт" включає як людину, так і інших ссавців. У кращому варіанті здійснення винаходу поняття "пацієнт" означає людину. Поняття "інгібітор PDE4" у контексті даного опису відноситься до діючої речовини, що володіє здатністю знижувати фізіологічну дія ізоферменту фосфодіестерази PDE4 більшою мірою, чим інших ізоферментів фосфодіестерази. Приклади інгібіторів PDE4 (не обмежуючий обсяг винаходу), які можна застосовувати у фармацевтичних композиціях, комбінованих продуктах і наборах, пропонованих у винаході, перераховані в таблиці 1. В одному з варіантів здійснення даного винаходу інгібітор PDE4 вибирають із групи, що включає РОФЛУМІЛАСТ (CAS-No. 162401-32-3), Рофлуміласт-N-оксид (CAS-No. 292135-78-5), ЦИЛОМІЛАСТ (CAS-No. 153259-65-5), AWD-12-281 (CAS-No. 257892-33-4), ТОФІМІЛАСТ (CASNo. 185954-27-2), ТЕТОМІЛАСТ (CAS-No. 145739-56-6), ЛІРИМІЛАСТ (CAS-No. 329306-27-6), L869298 (CAS-No. 362718-73-8), ОГЛЕМІЛАСТ (CAS-No. 778576-62-8), 2-{4-[(4a, 8a)-4-(3,4диметоксифеніл)-1-оксо-4a, 5,8,8a-тетрагідро-1H-фталазин-2-іл]піперидин-1-іл}ацетамід (нижче в даному описі позначено як СПОЛУКИ А; СAS-No. 449760-58-1) і фармацевтично прийнятні солі цих сполук. 4 UA 106422 C2 5 10 15 20 25 30 В іншому варіанті здійснення даного винаходу інгібітор PDE4 вибирають із групи, що включає РОФЛУМіЛАСТ, фармацевтично прийнятну сіль РОФЛУМІЛАСТу, Рофлуміласт-Nоксид, і фармацевтично прийнятну сіль Рофлуміласт-N-оксиду. У наступному варіанті здійснення даного винаходу інгібітор PDE4 являє собою РОФЛУМІЛАСТ. У наступному варіанті здійснення даного винаходу інгібітор PDE4 являє собою РофлуміластN-оксид. У наступному варіанті здійснення даного винаходу інгібітор PDE4 являє собою ЦИЛОМІЛАСТ або його фармацевтично прийнятну сіль. В іншому варіанті здійснення даного винаходу переважними фармацевтично прийнятними солями ЦИЛОМІЛАСТу є літієва, натрієва, етилендіамінова й трометамінова сіль ЦИЛОМІЛАСТу. Найбільш кращою фармацевтично прийнятною сіллю ЦИЛОМІЛАСТУ є натрієва сіль ЦИЛОМІЛАСТУ. Іншою найбільш кращою фармацевтично прийнятною сіллю ЦИЛОМІЛАСТу є літієва сіль ЦИЛОМІЛАСТу. Як приклад гідрату ЦИЛОМІЛАСТу слід зазначити моногідрат літієвої солі ЦИЛОМІЛАСТу. У наступному варіанті здійснення даного винаходу інгібітор PDE4 являє собою AWD-12-281 або його фармацевтично прийнятну сіль. У наступному варіанті здійснення даного винаходу краща фармацевтично прийнятна сіль AWD-12-281 являє собою натрієву сіль AWD-12-281. У наступному варіанті здійснення даного винаходу інгібітор PDE4 являє собою ТОФІМІЛАСТ або його фармацевтично прийнятну сіль. У наступному варіанті здійснення даного винаходу інгібітор PDE4 являє собою ТЕТОМІЛАСТ або його фармацевтично прийнятну сіль. У наступному варіанті здійснення даного винаходу інгібітор PDE4 являє собою ЛІРИМІЛАСТ або його фармацевтично прийнятну сіль. У наступному варіанті здійснення даного винаходу інгібітор PDE4 являє собою L-869298 або його фармацевтично прийнятну сіль. У наступному варіанті здійснення даного винаходу інгібітор PDE4 являє собою ОГЛЕМІЛАСТ або його фармацевтично прийнятну сіль. У наступному варіанті здійснення даного винаходу кращими фармацевтично прийнятними солями ОГЛЕМІЛАСТу є однонатрієва й двонатрієва солі ОГЛЕМІЛАСТу. У наступному варіанті здійснення даного винаходу інгібітор PDE4 являє собою СПОЛУКИ А або його фармацевтично прийнятну сіль. Таблиця 1 Міжнародна назва (INN) або використовуваний у дослідженнях код Структура/хімічна назва O O РОФЛУМІЛАСТ Cl N N H Cl O F F 3-(циклопропілметокси)-N-(3,5-дихлорпіридин-4-іл)-4(дифторметокси)бензамід 35 5 UA 106422 C2 O O N-оксид РОФЛУМІЛАСТу РОФЛУМІЛАСТ-N-оксид + O N Cl N H Cl O F F 3-(циклопропілметокси)-N-(3,5-дихлор-1-оксидопіридин-4-іл)-4(дифторметокси)бензамід H3C O N O ЦИЛОМІЛАСТ OH O цис-4-ціано-4-[3-(циклопентилокси)-4метоксифеніл]циклогексанкарбонова кислота O O Cl N N H HO Cl AWD-12-281 N F N-(3,5-дихлорпіридин-4-іл)-2-[1-(4-фторбензил)-5-гідрокси-1Ніндол-3-іл]-2-оксоацетамід N N N N ТОФІМІЛАСТ N H3C S 9-циклопентил-7-етил-3-(2-тієніл)-6,9-дигідро-5H-піразоло[3,4-с] [1,2,4]триазоло[4,3-а]піридин O CH3 N HO N ТЕТОМІЛАСТ O S O CH3 6-[2-(3,4-діетоксифеніл)-1,3-тіазол-4-іл]піридин-2-карбонова кислота 6 UA 106422 C2 O HN ЛІРИМІЛАСТ O Cl O S H3C NH2 O O Cl O 3-[(амінокарбоніл)аміно]-2-(2,4-дихлорбензоіл)-1-бензофуран-6ілметансульфонат F F F OH F F N F S O L-869298 O + N F F O 2-{5-[(1S)-1-[3-(циклопропілокси)-4-(дифторметокси)феніл]-2-(1оксидопіридин-3-іл)етил]-1,3-тіазол-2-іл}-1,1,1,3,3,3гексафторпропан-2-ол Cl H O H H3C ОГЛЕМІЛАСТ S O N N N Cl O O O F F N-(3,5-дихлорпіридин-4-іл)-4-(дифторметокси)-8[(метилсульфоніл)аміно]дибензо[b,d]фуран-1-карбоксамід O NH2 N O СПОЛУКИ А N O N H H O 2-{4-[(4а,8а)-4-(3,4-диметоксифеніл)-1-оксо-4а,5,8,8а-тетрагідро1Н-фталазин-2-іл]піперидин-1-іл}ацетамід 7 UA 106422 C2 5 10 15 20 25 30 35 40 45 50 55 Додаткову інформацію відносно одержання, придатних форм лікарських засобів і діапазонів доз таких інгібіторів PDE4, як РОФЛУМІЛАСТ, Рофлуміласт-N-оксид і їх фармацевтично прийнятні солі, можна знайти в наступних патентах / заявках на патент: WO 9501338, WO 03070279 і WO 2006032676. Додаткову інформацію відносно одержання, придатних форм лікарських засобів і діапазонів доз таких інгібіторів PDE4, як ЦИЛОМІЛАСТ, AWD-12-281, ТОФІМІЛАСТ, ТЕТОМІЛАСТ, ЛІРИМІЛАСТ, L-869298, ОГЛЕМІЛАСТ, СПОЛУКИ А і їх фармацевтично прийнятні солі, можна знайти в наступних патентах / заявках на патент: WO 9319749, WO 9809946, WO 9955696, WO 9639408, WO 9209586, ЕР 0731099, WO 0170738, WO 04089940 і WO 02064584. Поняття "інгібітор HMG-CoА-редуктази" у контексті даного опису відноситься до конкурентних інгібіторів 3-гідрокси-3-метилглутарил - кофермент А (HMG-Co)-редуктази, що каталізує ранню обмежуючу швидкість стадію біосинтезу холестерину, знижуючи тим самим рівні холестерину й тригліцеридів у пацієнтів з гіперліпідемією. Прикладами інгібіторів HMG-CoA-редуктази (але не обмежуючись тільки ними), які можна застосовувати у фармацевтичних композиціях, комбінованих продуктах і наборах, пропонованих у винаході, є сполуки, перераховані в таблиці 2. В одному з варіантів здійснення даного винаходу інгібітор HMG-CoA-редуктази вибирають із групи, що включає ЛОВАСТАТИН (CAS-No. 75330-75-5), ПРАВАСТАТИН (CAS-No. 081093-37-0), СИМВАСТАТИН (CAS-No. 079902-63-9), АТОРВАСТАТИН (CAS-No. 134523-00-5), ФЛУВАСТАТИН (093957-54-1), РОСУВАСТАТИН (CAS-No. 287714-41-4), ПІТАВАСТАТИН (CASNo. 147511-69-1), БЕРВАСТАТИН (CAS-No. 132017-01-7), ДАЛВАСТАТИН (CAS-No. 132100-551), ГЛЕНВАСТАТИН (CAS-No. 122254-45-9) і фармацевтично прийнятні солі цих сполук. В іншому варіанті здійснення даного винаходу інгібітор HMG-CoA-редуктази являє собою ЛОВАСТАТИН або його фармацевтично прийнятну сіль. У наступному варіанті здійснення даного винаходу інгібітор HMG-CoA-редуктази являє собою ПРАВАСТАТИН або його фармацевтично прийнятну сіль. У наступному варіанті здійснення даного винаходу кращими фармацевтично прийнятними солями ПРАВАСТАТИНу є калієва, літієва, натрієва й напівкальцієва сіль ПРАВАСТАТИНУ. Найбільш кращою фармацевтично прийнятною сіллю ПРАВАСТАТИНУ є натрієва сіль ПРАВАСТАТИНУ. В іншому варіанті здійснення даного винаходу інгібітор HMG-CoA-редуктази являє собою СИМВАСТАТИН або його фармацевтично прийнятну сіль. У наступному варіанті здійснення даного винаходу фармацевтично прийнятна сіль СИМВАСТАТИНУ являє собою натрієву сіль СИМВАСТАТИНУ. В іншому варіанті здійснення даного винаходу інгібітор HMG-CoA-редуктази являє собою АТОРВАСТАТИН або його фармацевтично прийнятну сіль. У наступному варіанті здійснення даного винаходу кращими фармацевтично прийнятними солями АТОРВАСТАТИНу є калієва, натрієва й напівкальцієва солі АТОРВАСТАТИНУ. Найбільш кращою фармацевтично прийнятною сіллю АТОРВАСТАТИНу є напівкальцієва сіль АТОРВАСТАТИНу. Як приклад гідрату АТОРВАСТАТИНу слід зазначити тригідрат і полуторний гідрат напівкальцієвої солі АТОРВАСТАТИНу. В іншому варіанті здійснення даного винаходу інгібітор HMG-СоА-редуктази являє собою ФЛУВАСТАТИН або його фармацевтично прийнятну сіль. У наступному варіанті здійснення даного винаходу фармацевтично прийнятна сіль ФЛУВАСТАТИНу являє собою натрієву сіль ФЛУВАСТАТИНу. В іншому варіанті здійснення даного винаходу інгібітор HMG-СоА-редуктази являє собою РОСУВАСТАТИН або його фармацевтично прийнятну сіль. У наступному варіанті здійснення даного винаходу кращими фармацевтично прийнятними солями РОСУВАСТАТИНу є калієва, літієва, натрієва, напівмагнієва й напівкальцієва солі РОСУВАСТАТИНу. Найбільш кращою фармацевтично прийнятною сіллю РОСУВАСТАТИНу є напівкальцієва сіль РОСУВАСТАТИНу. Іншою найбільш кращою фармацевтично прийнятною сіллю РОСУВАСТАТИНу є натрієва сіль РОСУВАСТАТИНу. В іншому варіанті здійснення даного винаходу інгібітор HMG-СоА-редуктази являє собою ПІТАВАСТАТИН або його фармацевтично прийнятну сіль. У наступному варіанті здійснення даного винаходу кращими фармацевтично прийнятними солями ПіТАВАСТАТИНу є калієва, натрієва й напівкальцієва солі ПІТАВАСТАТИНу. Найбільш кращої фармацевтично прийнятною сіллю ПІТАВАСТАТИНАу є напівкальцієва сіль ПІТАВАСТАТИНу. 8 UA 106422 C2 5 В іншому варіанті здійснення даного винаходу інгібітор HMG-СоА-редуктази являє собою БЕРВАСТАТИН або його фармацевтично прийнятну сіль. В іншому варіанті здійснення даного винаходу інгібітор HMG-СоА-редуктази являє собою ДАЛВАСТАТИН або його фармацевтично прийнятну сіль. В іншому варіанті здійснення даного винаходу інгібітор HMG-СоА-редуктази являє собою ГЛЕНВАСТАТИН або його фармацевтично прийнятну сіль. Таблиця 2 Міжнародна назва (1NN) або використовуваний у дослідженнях код Структура/хімічна назва HO O H O O H O H3C H3C ЛОВАСТАТИН H H H H H CH3 H CH3 (1S,3R,7S,8S,8а)-8-{2-[(2R,4R)-4-гідроксі-6-оксотетрагідро-2H-піран-2іл]етил}-3,7-диметил-1,2,3,7,8,8а-гексагідронафталін-1-іл-(2S)-2метилбутаноат O HO O OH HO O H3C H3C ПРАВАСТАТИН H H H H H H H CH3 HO CH3 (3S,5R)-3,5-дигідрокси-7-[(1S,2S,6S,8S,8a)-6-гідрокси-2-метил-8-{[(2S)-2меетилбутаноїл]окси}-1,2,6,7,8,8а-гексагідронафталін-1-іл]гептанова кислота HO O H O O H СИМВАСТАТИН O H3C H3C CH3 H H H H CH3 H3C H (1R,3S,7R,8R,8а)-8-{2-[(2R,4R)-4-гідроксі-6-оксотетрагідро-2H-піран-2іл]етил}-3,7-диметил-1,2,3,7,8,8а-гексагідронафталін-1-іл 2,2-диметил 9 UA 106422 C2 OH HO OH F O CH3 N CH3 АТОРВАСТАТИН N H O (3S,5R)-7-[3-(анілінокарбоніл)-5-(4-фторфеніл)-2-ізопропіл-4-феніл-1Нпірол-1-іл]-3,5-дигідроксигептанова кислота CH3 H3C H OH H OH N ФЛУВАСТАТИН OH O F (3R,5S,6E)-7-[3-(4-фторфеніл)-1-ізопропіл-1Н-індол-2-іл]-3,5дигідроксигепт-6-енова кислота F H РОСУВАСТАТИН O CH3 S O OH H O OH N N OH CH3 N CH3 CH3 (3R,5R)-7-{4-(4-фторфеніл)-6-ізопропіл-2-[мітив (метилсульфоніл)аміно]піримідин-5-іл}-3,5-дигідроксигептанова кислота F OH O OH ПІТАВАСТАТИН OH N (3R,5S,6E)-7-[2-циклопропіл-4-(4-фторфеніл)хинолін-3-іл]-3,5дигідроксигепт-6-енова кислота 10 UA 106422 C2 H O O HO O CH3 OH H БЕРВАСТАТИН F етил (3S,5S,6E)-7-[4-(4-фторфеніл)спиро[хромен-2,1'-циклопентан]-3іл]-3,5-дигідроксигепт-6-еноат O H O H OH CH3 H3C ДАЛВАСТАТИН H3C CH3 H3C F (4R,6S)-6-{(E)-2-[2-(4-фтор-3-метилфеніл)-4,4,6,6-тетраметилциклогекс1-ен-1-іл]вініл}-4-гідрокситетрагідро-2H-піран-2-он O O HO CH3 CH3 ГЛЕНВАСТАТИН F N (4R,6S)-6-{(E)-2-[4-(4-фторфеніл)-2-ізопропіл -6-фенілпіридин-3-іл]вініл}4-гідрокситетрагідро-2H-піран-2-он 5 10 Інгібітори HMG-СоА-редуктази ЛОВАСТАТИН, ПРАВАСТАТИН, СИМВАСТАТИН, АТОРВАСТАТИН, ФЛУВАСТАТИН, РОСУВАСТАТИН і ПІТАВАСТАТИН, перераховані в таблиці 2, є в продажі. Фахівцеві в даній галузі відомі придатні препаративні форми й діапазони доз цих сполук. Додаткову інформацію відносно одержання, придатних лікарських форм і діапазонів доз цих інгібіторів HMG-СоА-редуктази і їх фармацевтично прийнятних солей можна знайти в наступних патентах/заявках на патент: ЕР 022478, DE 3122499, ЕР 033538, ЕР 0247633, ЕР 0114027, ЕР 0521471 і ЕР 0304063. Додаткову інформацію відносно одержання, придатних лікарських форм і діапазонів доз таких інгібіторів HMG-СоА-редуктази, як БЕРВАСТАТИН, ДАЛВАСТАТИН, ГЛЕНВАСТАТИН і їх фармацевтично прийнятних солей можна знайти в наступних патентах/заявках на патент: ЕР 0380392, WO 8905639 і ЕР 0307342. 11 UA 106422 C2 5 10 15 20 25 30 35 40 45 50 55 60 Солі, що підпадають під поняття "фармацевтично прийнятні солі" не обмежені наведеними вище прикладами. Поняття відноситься до нетоксичних солей інгібітора PDE4 або інгібітори HMG-СоА-редуктази, які, як правило, одержують шляхом взаємодії вільної основи із придатною органічною або неорганічною кислотою (кислотно-адитивна сіль) або шляхом взаємодії вільної кислоти із придатною органічною або неорганічною основою. Кислотно-адитивні солі включають (але не обмежуючись тільки ними), гідрохлориди, гідроброміди, фосфати, нітрати, сульфати, ацетати, цитрати, D-глюконати, бензоати, 2-(4-гідроксибензоіл) бензоати, бутирати, сульфосаліцилати, малеати, лаурати, малати, фумарати, сукцинати, оксалати, тартрати, стеарати, толуолсульфонати, метансульфонати, 3-гідрокси-2-нафтоати й трифторацетати. Приклади солей приєднання основ включають (але не обмежуючись тільки ними) солі літію, натрію, калію, кальцію, алюмінію, магнію, титану, амонію, меглуміну й гуанідинію. Варто розуміти, що інгібітори PDE4, інгібітори HMG-СоА-редуктази, а також їх фармацевтично прийнятні солі можуть бути присутнім також у формі їх фармацевтично прийнятних сольватів і, зокрема, у формі їх фармацевтично прийнятних гідратів. Комбінації, пропоновані у винаході, можна вводити будь-яким придатним шляхом, наприклад, оральним, під'язичним, трансбукальним, внутрішньовенним, внутрішньоартеріальним, внутрішньом'язовим, підшкірним, внутрішньошкірним, місцевим, трансдермальним, інтраназальним, внутрішньочеревним, ректальним або вагінальним шляхом, за допомогою інгаляції або інсуфляції. Для орального введення придатні, наприклад, таблетки, таблетки з покриттям (драже), пігулки, крохмальні капсули, капсули (каплетки), гранули, розчини, емульсії й суспензії. Зокрема, зазначені лікарські форми можна адаптувати таким чином, щоб вони являли собою, наприклад, ентеральну форму, форму зі швидким вивільненням, форму з уповільненим вивільненням, форму з повторним вивільненням дози, форму із пролонгованим вивільненням або форму із тривалим вивільненням. Такі форми можна наготовлювати, наприклад, шляхом нанесення покриття на таблетки, шляхом поділу таблеток на декілька компартментів, відділених один від одного шарами, які руйнуються в різних умовах (наприклад, при різних значеннях р), або шляхом сполучення діючої речовини з біорозкладальним полімером. Введення шляхом інгаляції переважно здійснюють із використанням аерозолю. Аерозоль являє собою дисперсію рідини в газі, дисперсію твердої речовини в газі або змішаній дисперсії рідини /твердої речовини в газі. Аерозоль можна створювати за допомогою пристроїв для створення аерозолю, таких як інгалятори для сухого порошку (DPI), дозованих інгаляторів під тиском (PMDI) і розпилювачів (небулайзерів). Залежно від типу діючої речовини, що підлягає введенню, пристрій для створення аерозолю може містити діючу речовину формі порошку, розчину або дисперсії. Порошок може містити, наприклад, одне або декілька з наступних допоміжних речовин: носії, стабілізатори й наповнювачі. Розчин може містити крім розчинника, наприклад, одне або декілька з наступних допоміжних речовин: пропеленти, солюбілізатори (співрозчинники), поверхнево-активні речовини, стабілізатори, буфери, агенти для регулювання тонічності, консерванти й коригенти. Дисперсія може містити крім диспергатора, наприклад, одне або декілька з наступних допоміжних речовин: пропеленти, поверхнево-активні речовини, стабілізатори, буфери, консерванти й коригенти. Прикладами носіїв є (але не обмежуючись тільки ними) сахариди, наприклад, лактоза й глюкоза. Прикладами пропелентів є (але не обмежуючись тільки ними) фторовані вуглеводні, наприклад, 1,1,1,2-тетрафторетан і 1,1,1,2,3,3,3-гептафторпропан. Розмір аерозольних часток (твердих, рідких або твердих/рідких часток) переважно становить менше 100 мкм, більш переважно перебувають у діапазоні від 0,5 до 10 мкм, насамперед у діапазоні від 2 до 6 мкм (значення D50, вимірюване методом лазерної дифракції). Для введення парентеральним шляхом, таким, наприклад, як внутрішньовенне, внутрішньоартеріальне, внутрішньом'язове, підшкірне, внутрішньошкірне й внутрішньочеревне введення, переважно використають розчини (наприклад, стерильні розчини, ізотонічні розчини). Їх переважно вводять шляхом ін'єкції або інфузії. Фармацевтичні композиції (препаративні форми), що містять інгібітор PDE4 або його фармацевтично прийнятну сіль і/або інгібітор HMG-СоА-редуктази або його фармацевтично прийнятну сіль і щонайменше одну фармацевтично прийнятну допоміжну речовину, можна наготовлювати відомим фахівцеві в даній галузі методом, наприклад, з використанням процесів розчинення, змішання, гранулювання, виготовлення драже, розтирання в порошок, емульгування, капсулювання, уловлювання або ліофілізації. Як фармацевтично прийнятні допоміжні речовини можна застосовувати будь-які допоміжні речовини, у відношенні яких відомо, що їх можна використати для готування фармацевтичних композицій (препаративних 12 UA 106422 C2 5 10 15 20 25 30 35 40 45 50 55 60 форм). Їхніми прикладами є (але не обмежуючись тільки ними) розчинники, ексципієнти, диспергатори, мульгатори, солюбілізатори, желюючі агенти, масляні основи, антиоксиданти, консерванти, стабілізатори, носії, наповнювачі, зв'язувальні речовини, загущувачі, комплексоутворюючі агенти, розпушувачі, буфери, речовини, що підсилюють проникнення, полімери, змащувачі, агенти для нанесення покриття, пропеленти, агенти для регулювання тонічності, поверхнево-активні речовини, барвники, коригенти, речовини, що підсолоджують, й пігменти. Застосовують насамперед допоміжні речовини, що відповідають необхідній препаративній формі й необхідному шляху введення. Найбільш кращим шляхом введення РОФЛУМІЛАСТу, Рофлуміласт-N-оксиду або фармацевтично прийнятної солі кожного з них є оральний. В іншому кращому варіанті здійснення винаходу РОФЛУМІЛАСТ, Рофлуміласт-N-оксид або фармацевтично прийнятну сіль кожного з них уводять шляхом внутрішньовенної інфузії або ін'єкції. У наступному варіанті здійснення винаходу РОФЛУМІЛАСТ, Рофлуміласт-N-оксид або фармацевтично прийнятну сіль кожного з них уводять шляхом внутрішньом'язової або підшкірної ін'єкції. Можна використати також інші шляхи введення, включаючи, наприклад, інтраназальний і трансдермальний шляхи, а також введення шляхом інгаляції. Кращим шляхом введення таких інгібіторів PDE4, як ЦИЛОМІЛАСТ, ТЕТОМІЛАСТ, ЛІРИМІЛАСТ, L-869298, ОГЛЕМІЛАСТ і СПОЛУКИ А, є оральний шлях введення, у той час як кращим шляхом введення інгібіторів PDE4 AWD-12-281 і ТОФІМІЛАСТу є введення шляхом інгаляції. Кращим шляхом введення таких інгібіторів HMG-СоА-редуктази, як ЛОВАСТАТИН, ПРАВАСТАТИН; СИМВАСТАТИН; АТОРВАСТАТИН, ФЛУВАСТАТИН, РОСУВАСТАТИН, ПІТАВАСТАТИН, БЕРВАСТАТИН, ДАЛВАСТАТИН і ГЛЕНВАСТАТИН, є оральний шлях введення. Точна доза й схема введення інгібітора PDE4 або його фармацевтично прийнятної солі в комбінації з інгібітором HMG-СоА-редуктази або його фармацевтично прийнятною сіллю повинні залежати від активності й тривалості дії застосовуваних діючих речовин, природи й серйозності запального захворювання легень, що підлягає лікуванню, а також від статі, віку, ваги, загального стану здоров'я й індивідуальної реактивності пацієнта, що підлягає лікуванню, а також від інших відповідних обставин. При використанні як складена частина комбінованої терапії, пропонованої у винаході, інгібітор PDE4 або його фармацевтично прийнятну сіль і інгібітор HMG-СоА-редуктази або його фармацевтично прийнятну сіль застосовують у дозах, які один по одному величини відповідають дозам, використовуваним для монотерапії, більш імовірно, з огляду на те, що індивідуальні дії впливають і підсилюються, може виявитися можливим знижувати відповідні дози при комбінованому введенні інгібітора PDE4 або його фармацевтично прийнятної солі й інгібітор HMG-СоА-редуктази або його фармацевтично прийнятної солі в порівнянні зі звичайною дозою. Добова доза, що вводиться оральним шляхом (для дорослого пацієнта) інгібіторів PDE4 або їх фармацевтично прийнятних солей, як правило (але не обмежуючись тільки зазначеними дозами) становить від приблизно 0,05 до приблизно 200 мг; добова доза (для дорослого пацієнта) інгібітора PDE4 або його фармацевтично прийнятної солі при введенні шляхом інгаляції, як правило (але не обмежуючись тільки зазначеними дозами) становить від приблизно 0,05 до приблизно 100 мг. У випадку орального введення 3-циклопропілметокси-4-дифторметокси-N-(3,5-дихлорпірид4-ил)бензаміду (РОФЛУМІЛАСТ) добова доза (для дорослого пацієнта) при монотерапії становить від 50 до 1000 мкг у день, переважно від 50 до 500 мкг у день, і її переважно вводять один раз у день. У випадку внутрішньовенного введення 3-циклпропілметокси-4дифторметокси-N-(3,5-дихлорпірид-4-ил)бензаміду (РОФЛУМІЛАСТ) добова доза (для дорослого пацієнта) при монотерапії становить від 50 до 500 мкг у день, переважно від 150 до 300 мкг у день. У випадку орального введення ЦИЛОМІЛАСТА добова доза (для дорослого пацієнта) при монотерапії, як правило, становить від 10 до 40 мг у день, переважно від 20 до 30 мг у день, і її переважно вводять двічі в день. У випадку введення шляхом інгаляції AWD-12-281 добова доза (для дорослого пацієнта) при монотерапії, як правило, становить від 500 до 2000 мкг у день. У випадку орального введення ЛІРИМІЛАСТУ добова доза (для дорослого пацієнта) при монотерапії, як правило, становить від 1 до 10 мг у день. У випадку орального введення ОГЛЕМІЛАСТу добова доза (для дорослого пацієнта) при монотерапії, як правило, становить від 1 до 10 мг у день. 13 UA 106422 C2 5 У випадку орального введення СПОЛУКИ А добова доза (для дорослого пацієнта) при монотерапії, як правило, становить від 0,1 до 10 мг один раз у день, переважно від 0,1 до 2 мг один раз у день. Добова доза, що вводиться оральним шляхом (для дорослого пацієнта) інгібіторів HMGСоА-редуктази або їх фармацевтично прийнятних солей, як правило, повинна становити від приблизно 0,01 до приблизно 200 мг, переважно від 10 до 80 мг, більш переважно від 5 до 40 мг; при введенні шляхом інгаляції кращими є дози від 0,001 до приблизно 25 мг, ще більш краща доза становить від 0,1 до 25 мг. Таблиця 3 Кращі комбінації Номер приклада 1 2 3 4 5 6 7 8 9 10 РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид 11 РОФЛУМІЛАСТ 12 РОФЛУМІЛАСТ-N-оксид 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид РОФЛУМІЛАСТ РОФЛУМІЛАСТ-N-оксид ЦИЛОМІЛАСТ ЦИЛОМІЛАСТ ЦИЛОМІЛАСТ ЦИЛОМІЛАСТ ЦИЛОМІЛАСТ 38 ЦИЛОМІЛАСТ 39 40 41 ЦИЛОМІЛАСТ ЦИЛОМІЛАСТ ЦИЛОМІЛАСТ Комбінація ЛОВАСТАТИН ЛОВАСТАТИН ПРАВАСТАТИН ПРАВАСТАТИН ПРАВАСТАТИН, натрієва сіль ПРАВАСТАТИН, натрієва сіль СИМВАСТАТИН СИМВАСТАТИН АТОРВАСТАТИН АТОРВАСТАТИН АТОРВАСТАТИН, полуторний гідрат напівкальцієвої солі АТОРВАСТАТИН, полуторний гідрат напівкальцієвої солі ФЛУВАСТАТИН ФЛУВАСТАТИН ФЛУВАСТАТИН, натрієва сіль ФЛУВАСТАТИН, натрієва сіль РОСУВАСТАТИН РОСУВАСТАТИН РОСУВАСТАТИН, напівкальцієва сіль РОСУВАСТАТИН, напівкальцієва сіль РОСУВАСТАТИН, натрієва сіль РОСУВАСТАТИН, натрієва сіль ПІТАВАСТАТИН ПІТАВАСТАТИН ПІТАВАСТАТИН, напівкальцієва сіль ПІТАВАСТАТИН, напівкальцієва сіль БЕРВАСТАТИН БЕРВАСТАТИН ДАЛВАСТАТИН ДАЛВАСТАТИН ГЛЕНВАСТАТИН ГЛЕНВАСТАТИН ЛОВАСТАТИН ПРАВАСТАТИН ПРАВАСТАТИН, натрієва сіль СИМВАСТАТИН АТОРВАСТАТИН АТОРВАСТАТИН, полуторний гідрат напівкальцієвої солі ФЛУВАСТАТИН ФЛУВАСТАТИН, натрієва сіль РОСУВАСТАТИН 14 UA 106422 C2 42 43 44 45 46 47 48 49 50 51 52 53 ЦИЛОМІЛАСТ ЦИЛОМІЛАСТ ЦИЛОМІЛАСТ ЦИЛОМІЛАСТ ЦИЛОМІЛАСТ ЦИЛОМІЛАСТ ЦИЛОМІЛАСТ AWD-12-281 AWD-12-281 AWD-12-281 AWD-12-281 AWD-12-281 54 AWD-12-281 55 56 57 58 59 60 61 62 63 61 65 66 67 68 69 AWD-12-281 AWD-12-281 AWD-12-281 AWD-12-281 AWD-12-281 AWD-12-281 AWD-12-281 AWD-12-281 AWD-12-281 AWD-12-281 ТОФІМІЛАСТ ТОФІМІЛАСТ ТОФІМІЛАСТ Т ТОФІМІЛАСТ ТОФІМІЛАСТ 70 ТОФІМІЛАСТ 71 72 74 75 76 77 78 79 80 81 82 83 84 85 86 ТОФІМІЛАСТ ТОФІМІЛАСТ ТОФІМІЛАСТ ТОФІМІЛАСТ ТОФІМІЛАСТ ТОФІМІЛАСТ ТОФІМІЛАСТ ТОФІМІЛАСТ ТОФІМІЛАСТ ТОФІМІЛАСТ ТЕТОМІЛАСТ ТЕТОМІЛАСТ ТЕТОМІЛАСТ ТЕТОМІЛАСТ ТЕТОМІЛАСТ 87 ТЕТОМІЛАСТ 88 89 90 91 92 93 94 95 96 97 ТЕТОМІЛАСТ ТЕТОМІЛАСТ ТЕТОМІЛАСТ ТЕТОМІЛАСТ ТЕТОМІЛАСТ ТЕТОМІЛАСТ ТЕТОМІЛАСТ ТЕТОМІЛАСТ ТЕТОМІЛАСТ ТЕТОМІЛАСТ РОСУВАСТАТИН, напівкальцієва сіль РОСУВАСТАТИН, натрієва сіль ПІТАВАСТАТИН ПІТАВАСТАТИН, напівкальцієва сіль БЕРВАСТАТИН ДАЛВАСТАТИН ГЛЕНВАСТАТИН ЛОВАСТАТИН ПРАВАСТАТИН ПРАВАСТАТИН, натрієва сіль СИМВАСТАТИН АТОРВАСТАТИН АТОРВАСТАТИН, полуторний гідрат напівкальцієвої солі ФЛУВАСТАТИН ФЛУВАСТАТИН, натрієва сіль РОСУВАСТАТИН РОСУВАСТАТИН, напівкальцієва сіль РОСУВАСТАТИН, натрієва сіль ПІТАВАСТАТИН ПІТАВАСТАТИН, напівкальцієва сіль БЕРВАСТАТИН ДАЛВАСТАТИН ГЛЕНВАСТАТИН ЛОВАСТАТИН ПРАВАСТАТИН ПРАВАСТАТИН, натрієва сіль СИМВАСТАТИН АТОРВАСТАТИН АТОРВАСТАТИН, полуторний гідрат напівкальцієвої солі ФЛУВАСТАТИН ФЛУВАСТАТИН, натрієва сіль РОСУВАСТАТИН РОСУВАСТАТИН, напівкальцієва сіль РОСУВАСТАТИН, натрієва сіль ПІТАВАСТАТИН ПІТАВАСТАТИН, напівкальцієва сіль БЕРВАСТАТИН ДАЛВАСТАТИН ГЛЕНВАСТАТИН ЛОВАСТАТИН ПРАВАСТАТИН ПРАВАСТАТИН, натрієва сіль СИМВАСТАТИН АТОРВАСТАТИН АТОРВАСТАТИН, полуторний гідрат напівкальцієвої солі ФЛУВАСТАТИН ФЛУВАСТАТИН, натрієва сіль РОСУВАСТАТИН РОСУВАСТАТИН, напівкальцієва сіль РОСУВАСТАТИН, натрієва сіль ПІТАВАСТАТИН ПІТАВАСТАТИН, напівкальцієва сіль БЕРВАСТАТИН ДАЛВАСТАТИН ГЛЕНВАСТАТИН 15 UA 106422 C2 98 99 100 101 102 103 20 COMPOUND A 120 121 122 123 124 125 126 127 128 129 15 ОГЛЕМіЛАСТ ОГЛЕМіЛАСТ ОГЛЕМіЛАСТ ОГЛЕМіЛАСТ ОГЛЕМіЛАСТ ОГЛЕМіЛАСТ ОГЛЕМіЛАСТ ОГЛЕМіЛАСТ ОГЛЕМіЛАСТ ОГЛЕМіЛАСТ COMPOUND A COMPOUND A COMPOUND A COMPOUND A COMPOUND A 119 10 ОГЛЕМіЛАСТ 104 105 106 107 108 109 110 111 112 113 114 115 116 117 118 5 ОГЛЕМіЛАСТ ОГЛЕМіЛАСТ ОГЛЕМіЛАСТ ОГЛЕМіЛАСТ ОГЛЕМіЛАСТ COMPOUND A COMPOUND A COMPOUND A COMPOUND A COMPOUND A COMPOUND A COMPOUND A COMPOUND A COMPOUND A COMPOUND A ЛОВАСТАТИН ПРАВАСТАТИН ПРАВАСТАТИН, натрієва сіль СИМВАСТАТИН АТОРВАСТАТИН АТОРВАСТАТИН, полуторний гідрат напівкальцієвої солі ФЛУВАСТАТИН ФЛУВАСТАТИН, натрієва сіль РОСУВАСТАТИН РОСУВАСТАТИН, напівкальцієва сіль РОСУВАСТАТИН, натрієва сіль ПІТАВАСТАТИН ПІТАВАСТАТИН, напівкальцієва сіль БЕРВАСТАТИН ДАЛВАСТАТИН ГЛЕНВАСТАТИН ЛОВАСТАТИН ПРАВАСТАТИН ПРАВАСТАТИН, натрієва сіль СИМВАСТАТИН АТОРВАСТАТИН АТОРВАСТАТИН, полуторний гідрат напівкальцієвої солі ФЛУВАСТАТИН ФЛУВАСТАТИН, натрієва сіль РОСУВАСТАТИН РОСУВАСТАТИН, напівкальцієва сіль РОСУВАСТАТИН, натрієва сіль ПІТАВАСТАТИН ПІТАВАСТАТИН, напівкальцієва сіль БЕРВАСТАТИН ДАЛВАСТАТИН ГЛЕНВАСТАТИН Фармакологія: Синергетичне інгібування індукованого ЛПС системного вивільнення TNF (у щурів за допомогою комбінації полуторного гідрату напівкальцієвої солі АТОРВАСТАТИНУ й 2-(4[(4а,8а)-4-(3,4-диметоксифеніл)-1-окс-4а, 5,8,8а-тетрагідро-1Н-фталазин-2-іл]піперидин-1іл}ацетаміду (СПОЛУКИ А) Тварини: самці щурів лінії Spraque Dawley вагою 200-280 г. Лікарські засоби: полуторний гідрат напівкальцієвої солі АТОРВАСТАТИНА (фірма Alexis Pharmaceuticals, Сан-Дієго, шт. Каліфорнія, США) і СПОЛУКИ А (фірма ALT ANA Pharma, Констанц, Німеччина). Методи: Лікарські засоби вводили за допомогою шлункового зонда у вигляді суспензії в метоцелі/поліетиленгліколі 400 за 1 год. перед внутрішньовенним введенням ЛПС (0,1 мг/кг). Через 90 хв. тварин забивали шляхом ін'єкції пентобарбиталу (48 мг/кг) і гепарину (1000 од./кг). Гепаринізовану кров брали шляхом серцевої пункції. Кров центрифугували (21000 × g, 4 °C, 15 хв.), і зразки плазми зберігали в замороженому стані при - 80 °C до здійснення визначення рівнів TNFα за допомогою поступаючого в продаж набору для ELISA (Quantakine®M, набір для імуноаналіза щурячого TNFα, фірма R&D, шт. Міннесота, США). Статистичний аналіз: Всі дані представляли у вигляді середнього значення ± С.К.О. Статистичну значимість розраховували для вихідних (основних) концентрацій TNFα при порівнянні з даними, отриманими для контрольної групи, підданої LPS-стимулюванню, за допомогою дисперсійного аналізу (ANOVA) з наступним застосуванням критерію Дуннета з використанням пакета програм Graph Pad Prism. Розходження, для яких р 50 % (Р < 0,01). Висновки: несподівано встановлено, що комбінація субефективних доз інгібітора PDE4, що являє собою СПОЛУКИ А, і інгібітора HMG-СоА-редуктази, що являє собою полуторний гідрат напівкальцієвої солі АТОРВАСТАТИНУ, робить виражену (синергетичну) і ефективну інгібуючу дію на запальні процеси. На кресленнях полуторний гідрат напівкальцієвої солі АТОРВАСТАТИНУ позначений просто як "АТОРВАСТАТИН Са". На кресленнях показано: на фіг. 1 - інгібування СПОЛУКИ А індукованого ЛПС (системного) вивільнення TNFα в організмі щурів; на фіг. 2 - інгібування полуторним гідратом напівкальцієвої солі АТОРВАСТАТИНУ індукованого ЛПС (системного) вивільнення TNFα в організмі щурів; на фіг. 3: інгібування індукованого ЛПС (системного) вивільнення TNFα в організмі щурів комбінацією СПОЛУКИ А і полуторного гідрату напівкальцієвої солі АТОРВАСТАТИНУ. ФОРМУЛА ВИНАХОДУ 1. Фармацевтична композиція, що являє собою фармацевтичну лікарську форму, що містить у певній кількості інгібітор PDE4, у певній кількості інгібітор HMG-CoA-редуктази і щонайменше одну фармацевтично прийнятну допоміжну речовину, де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою симвастатин або його фармацевтично прийнятну сіль, і де перша кількість і друга кількість разом становлять ефективну кількість для профілактики або зцілювального лікування запального захворювання легенів. 2. Фармацевтична композиція за п. 1, в якій інгібітор PDE4 являє собою рофлуміласт. 3. Фармацевтична композиція за п. 1, в якій інгібітор PDE4 являє собою рофлуміласт-N-оксид. 4. Фармацевтична композиція за будь-яким з пп. 1-3, в якій інгібітор НМО-СоА-редуктази являє собою симвастатин. 5. Фармацевтична композиція за будь-яким з пп. 1-4, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію. 6. Фармацевтична композиція за будь-яким з пп. 1-4, де запальне захворювання легенів являє собою ХОЗЛ. 7. Комбінація, що містить наступні компоненти: (А) у певній кількості інгібітор PDE4; (Б) у певній кількості інгібітор HMG-CoA-редуктази; де перша кількість і друга кількість разом становлять ефективну кількість для профілактики або зцілювального лікування запального захворювання легенів, і де кожний з компонентів (А) і (Б) включений до складу препаративної форми разом із щонайменше однією фармацевтично прийнятною допоміжною речовиною, і де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMGCoA-редуктази являє собою симвастатин або його фармацевтично прийнятну сіль. 8. Комбінація за п. 7, в якій інгібітор PDE4 являє собою рофлуміласт. 9. Комбінація за п. 7, в якій інгібітор PDE4 являє собою рофлуміласт-N-оксид. 10. Комбінація за будь-яким з пп. 7-9, в якій інгібітор HMG-CoA-редуктази являє собою симвастатин. 11. Комбінація за будь-яким з пп. 7-10, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію. 12. Комбінація за будь-яким з пп. 7-10, де запальне захворювання легенів являє собою ХОЗЛ. 17 UA 106422 C2 5 10 15 20 25 30 35 40 45 50 55 60 13. Набір, що містить наступні компоненти: (А) фармацевтичну лікарську форму, що містить у певній кількості інгібітор PDE4 в суміші з щонайменше однією фармацевтично прийнятною допоміжною речовиною; (Б) фармацевтичну лікарську форму, що містить у певній кількості інгібітор PIMG-CoA-редуктази в суміші з щонайменше однією фармацевтично прийнятною допоміжною речовиною; де перша кількість і друга кількість разом становлять ефективну кількість для профілактики або зцілювального лікування запального захворювання легенів, і де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою симвастатин або його фармацевтично прийнятну сіль. 14. Набір за п. 13, в якому інгібітор PDE4 являє собою рофлуміласт. 15. Набір за п. 13, в якому інгібітор PDE4 являє собою рофлуміласт-N-оксид. 16. Набір за будь-яким з пп. 13-15, в якому інгібітор HMG-CoA-редуктази являє собою симвастатин. 17. Набір за будь-яким з пп. 13-16, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію. 18. Набір за будь-яким з пп. 13-16, де запальне захворювання легенів являє собою ХОЗЛ. 19. Застосування інгібітора PDE4 або його фармацевтично прийнятної солі і інгібітора HMGCoA-редуктази або його фармацевтично прийнятної солі для приготування лікарського засобу, що являє собою фармацевтичну композицію згідно з винаходом, призначеного для профілактики або зцілювального лікування запального захворювання легенів, де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор НМОСоА-редуктази являє собою симвастатин або його фармацевтично прийнятну сіль. 20. Застосування інгібітора PDE4 або його фармацевтично прийнятної солі і інгібітора HMGCoA-редуктази або його фармацевтично прийнятної солі для приготування призначеного для профілактики або зцілювального лікування запального захворювання легенів лікарського засобу, що являє собою комбінацію або набір згідно з винаходом, який можна вводити послідовно або роздільно, де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою симвастатин або його фармацевтично прийнятну сіль. 21. Застосування за будь-яким з пп. 19 або 20, де інгібітор PDE4 являє собою рофлуміласт. 22. Застосування за будь-яким з пп. 19 або 20, де інгібітор PDE4 являє собою рофлуміласт-Nоксид. 23. Застосування за будь-яким з пп. 19, 20, 21 або 22 де інгібітор HMG-CoA-редуктази являє собою симвастатин. 24. Застосування за будь-яким з пп. 19-23, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію. 25. Застосування за будь-яким з пп. 19-23, де запальне захворювання легенів являє собою ХОЗЛ. 26. Спосіб приготування фармацевтичної композиції за будь-яким з пп. 1-6, який полягає в тому, що змішують інгібітор PDE4 або його фармацевтично прийнятну сіль із інгібітором HMG-CoAредуктази або його фармацевтично прийнятною сіллю. 27. Фармацевтична композиція, що являє собою фармацевтичну лікарську форму, що містить у певній кількості інгібітор PDE4, у певній кількості інгібітор HMG-CoA-редуктази і щонайменше одну фармацевтично прийнятну допоміжну речовину, де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-oкcид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою аторвастатин або його фармацевтично прийнятну сіль, і де перша кількість і друга кількість разом становлять ефективну кількість для профілактики або зцілювального лікування запального захворювання легенів. 28. Фармацевтична композиція за п. 27, в якій інгібітор PDE4 являє собою рофлуміласт. 29. Фармацевтична композиція за п. 27, в якій інгібітор PDE4 являє собою рофлуміласт-N-оксид. 30. Фармацевтична композиція за будь-яким з пп. 27-29, в якій інгібітор HMG-CoA-редуктази являє собою аторвастатин. 31. Фармацевтична композиція за будь-яким з пп. 27-29, в якій інгібітор HMG-CoA-редуктази являє собою сесквігідрат аторвастатин гемікальцію. 18 UA 106422 C2 5 10 15 20 25 30 35 40 45 50 55 60 32. Фармацевтична композиція за будь-яким з пп. 27-31, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію. 33. Фармацевтична композиція за будь-яким з пп. 27-31, де запальне захворювання легенів являє собою ХОЗЛ. 34. Комбінація, що містить наступні компоненти: (А) у певній кількості інгібітор PDE4; (Б) у певній кількості інгібітор HMG-CoA-редуктази; де перша кількість і друга кількість разом становлять ефективну кількість для профілактики або зцілювального лікування запального захворювання легенів, і де кожний з компонентів (А) і (Б) включений до складу препаративної форми разом із щонайменше однією фармацевтично прийнятною допоміжною речовиною, і де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMGCoA-редуктази являє собою аторвастатин або його фармацевтично прийнятну сіль. 35. Комбінація за п. 34, в якій інгібітор PDE4 являє собою рофлуміласт. 36. Комбінація за п. 34, в якій інгібітор PDE4 являє собою рофлуміласт-N-оксид. 37. Комбінація за будь-яким з пп. 34-36, в якій інгібітор HMG-CoA-редуктази являє собою аторвастатин. 38. Комбінація за будь-яким з пп. 34-36, в якій інгібітор HMG-CoA-редуктази являє собою сесквігідрат аторвастатин гемікальцію. 39. Комбінація за будь-яким з пп. 34-38, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію. 40. Комбінація за будь-яким з пп. 34-38, де запальне захворювання легенів являє собою ХОЗЛ. 41. Набір, що містить наступні компоненти: (А) фармацевтичну лікарську форму, що містить у певній кількості інгібітор PDE4 в суміші з щонайменше однією фармацевтично прийнятною допоміжною речовиною; (Б) фармацевтичну лікарську форму, що містить у певній кількості інгібітор HMG-CoA-редуктази в суміші з щонайменше однією фармацевтично прийнятною допоміжною речовиною; де перша кількість і друга кількість разом становлять ефективну кількість для профілактики або зцілювального лікування запального захворювання легенів, і де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою аторвастатин або його фармацевгично прийнятну сіль. 42. Набір за п. 41, в якому інгібітор PDE4 являє собою рофлуміласт. 43. Набір за п. 41, в якому інгібітор PDE4 являє собою рофлуміласт-N-оксид. 44. Набір за будь-яким з пп. 41-43, в якому інгібітор HMG-CoA-редуктази являє собою аторвастатин. 45. Набір за будь-яким з пп. 41-43, в якому інгібітор HMG-CoA-редуктази являє собою сесквігідрат аторвастатин гемікальцію. 46. Набір за будь-яким з пп. 41-45, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію. 47. Набір за будь-яким з пп. 41-45, де запальне захворювання легенів являє собою ХОЗЛ. 48. Застосування інгібітора PDE4 або його фармацевтично прийнятної солі і інгібітора HMGCoA-редуктази або його фармацевтично прийнятної солі для приготування лікарського засобу, що являє собою фармацевтичну композицію згідно з винаходом, призначеного для профілактики або зцілювального лікування запального захворювання легенів, де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийнятну сіль рофлуміласт-N-оксиду, а інгібітор HMGCoA-редуктази являє собою аторвастатин або його фармацевтично прийнятну сіль. 49. Застосування інгібітора PDE4 або його фармацевтично прийнятної солі і інгібітора НMGCoA-редуктази або його фармацевтично прийнятної солі для приготування призначеного для профілактики або зцілювального лікування запального захворювання легенів лікарського засобу, що являє собою комбінацію або набір згідно з винаходом, який можна вводити послідовно або роздільно, де інгібітор PDE4 вибраний з групи, яка включає рофлуміласт, фармацевтично прийнятну сіль рофлуміласту, рофлуміласт-N-оксид і фармацевтично прийняту сіль рофлуміласт-N-оксиду, а інгібітор HMG-CoA-редуктази являє собою аторвастатин або його фармацевтично прийнятну сіль. 50. Застосування за будь-яким з пп. 48 або 49, в якому інгібітор PDE4 являє собою рофлуміласт. 19 UA 106422 C2 5 10 51. Застосування за будь-яким з пп. 48 або 49 в якому інгібітор PDE4 являє собою рофлуміластN-оксид. 52. Застосування за будь-яким з пп. 48, 49, 50 або 51, в якому інгібітор HMG-CoA-редуктази являє собою аторвастатин. 53. Застосування за будь-яким з пп. 48, 49, 50 або 51, в якому інгібітор HMG-CoA-редуктази являє собою сесквігідрат аторвастатин гемікальцію. 54. Застосування за будь-яким з пп. 48-53, де запальне захворювання легенів вибрано з групи, яка включає астму, ХОЗЛ, склероз, альвеоліт, саркоїдоз, ідіопатичний фіброз легенів і легеневу гіпертензію. 55. Застосування за будь-яким з пп. 48-53, де запальне захворювання легенів являє собою ХОЗЛ. 56. Спосіб приготування фармацевтичної композиції за будь-яким з пп. 27-33, який полягає в тому, що змішують інгібітор PDE4 або його фармацевтично прийнятну сіль із інгібітором HMGCoA-редуктази або його фармацевтично прийнятною сіллю. 20 UA 106422 C2 21 UA 106422 C2 Комп’ютерна верстка Л. Литвиненко Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 22
ДивитисяДодаткова інформація
Автори англійськоюWollin Stefan-Lutz, Wohlsen Andrea, Braun, Clemens, Marx, Degenhard
Автори російськоюВоллин Штефан-Лутц, Маркс Дегенхард
МПК / Мітки
МПК: A61P 11/00, A61K 45/06, A61K 31/502, A61K 31/40
Мітки: захворювання, інгібітора, легенів, запального, профілактики, лікування, зцілювального, нmg-coa-редуктази, комбіноване, застосування
Код посилання
<a href="https://ua.patents.su/24-106422-kombinovane-zastosuvannya-ingibitora-pde4-ta-ingibitora-nmg-coa-reduktazi-dlya-profilaktiki-abo-zcilyuvalnogo-likuvannya-zapalnogo-zakhvoryuvannya-legeniv.html" target="_blank" rel="follow" title="База патентів України">Комбіноване застосування інгібітора pde4 та інгібітора нmg-cоa-редуктази для профілактики або зцілювального лікування запального захворювання легенів</a>
Попередній патент: Лопатевий гвинт брозінського
Наступний патент: Поліуретанове вібраційне сито
Випадковий патент: Авіаційна бомба "адрос" калібру 500/1000/1500/3000 кг