Поліморфні форми сульфатів зипразидону
Номер патенту: 100843
Опубліковано: 11.02.2013
Автори: Ярсіц Юрска, Смрколь Матей, Стергар Матей, Хвалец Міран, Пецавар Аніца, Макуц Сімон, Зайц Наталія, Рузіц Мілош, Заднік Юрней
Формула / Реферат
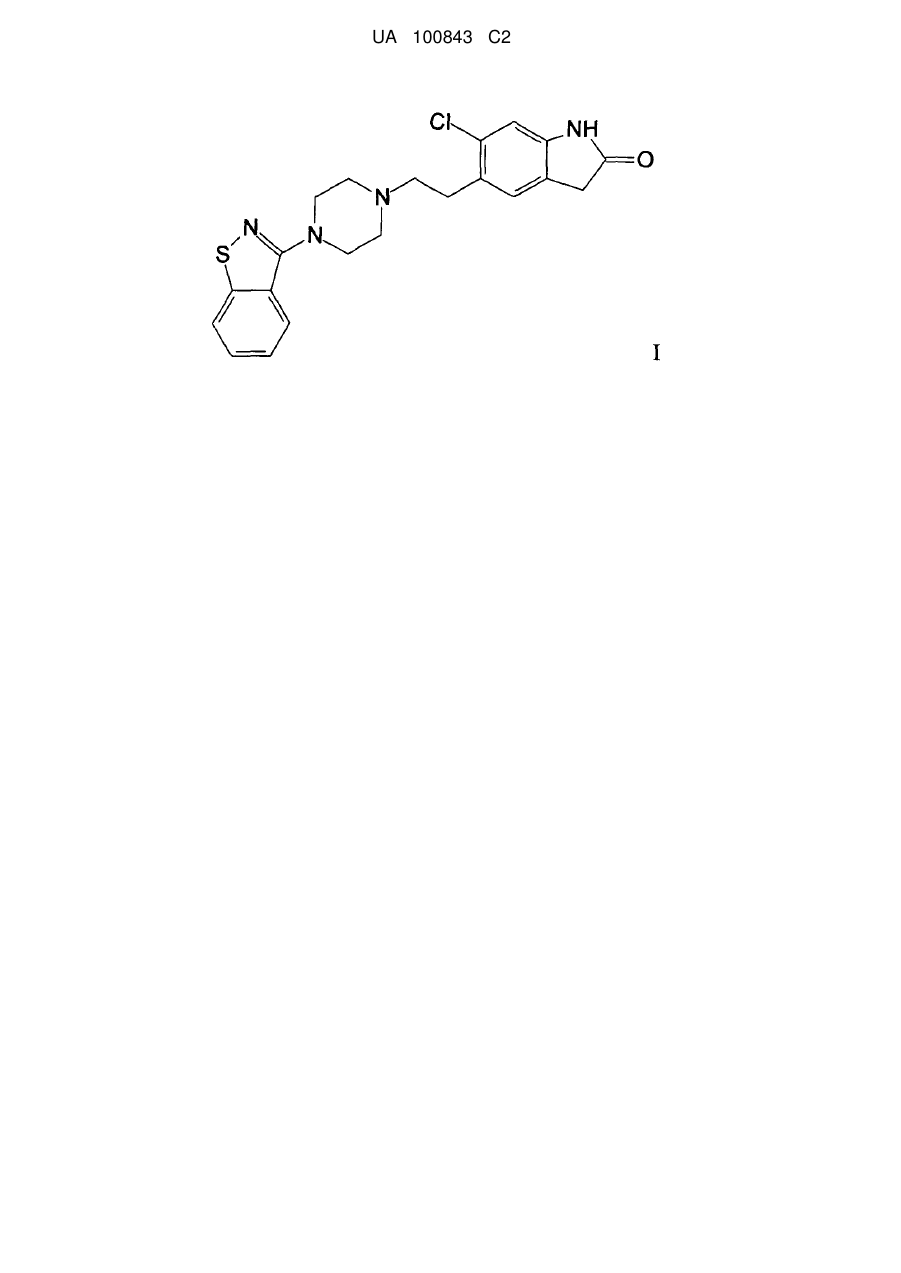
1. Сполука формули І:
[зипразидон*Н]n+[X]*ZН2О, де
зипразидон є сполукою формули
 ,
,
Н є воднем;
n=1 або 2;
X є HSO4- або SO42-; і
Z>0,28 до 30,
вказана сполука розчинна в діапазоні від приблизно 50 мл/л до приблизно 800 мл/л.
2. Сполука за п. 1, де Z>0,28 до 2.
3. Сполука за будь-яким з пп. 1, 2, яка відрізняється тим, що вказана сполука має розмір частинок, що знаходиться в діапазоні від приблизно 5 мкм до приблизно 300 мкм.
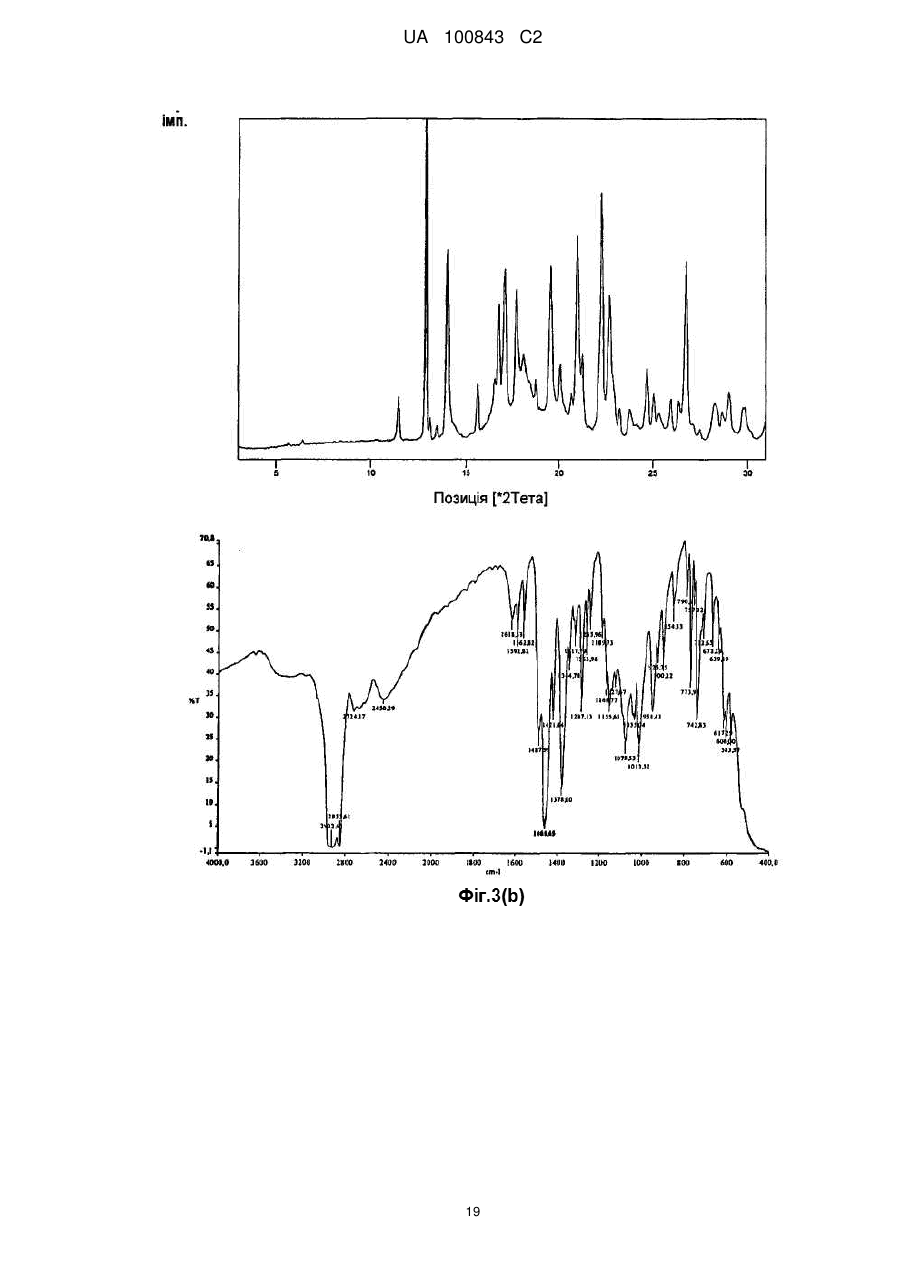
4. Сполука за п. 1, яка відрізняється тим, що характеризується картиною дифракції рентгенівських променів на порошку, що демонструє характеристичні кути дифракції при 8,6; 12,1; 13,6; 17,6; 19,8; 23,4 і 24,3°±0,2°-тета.
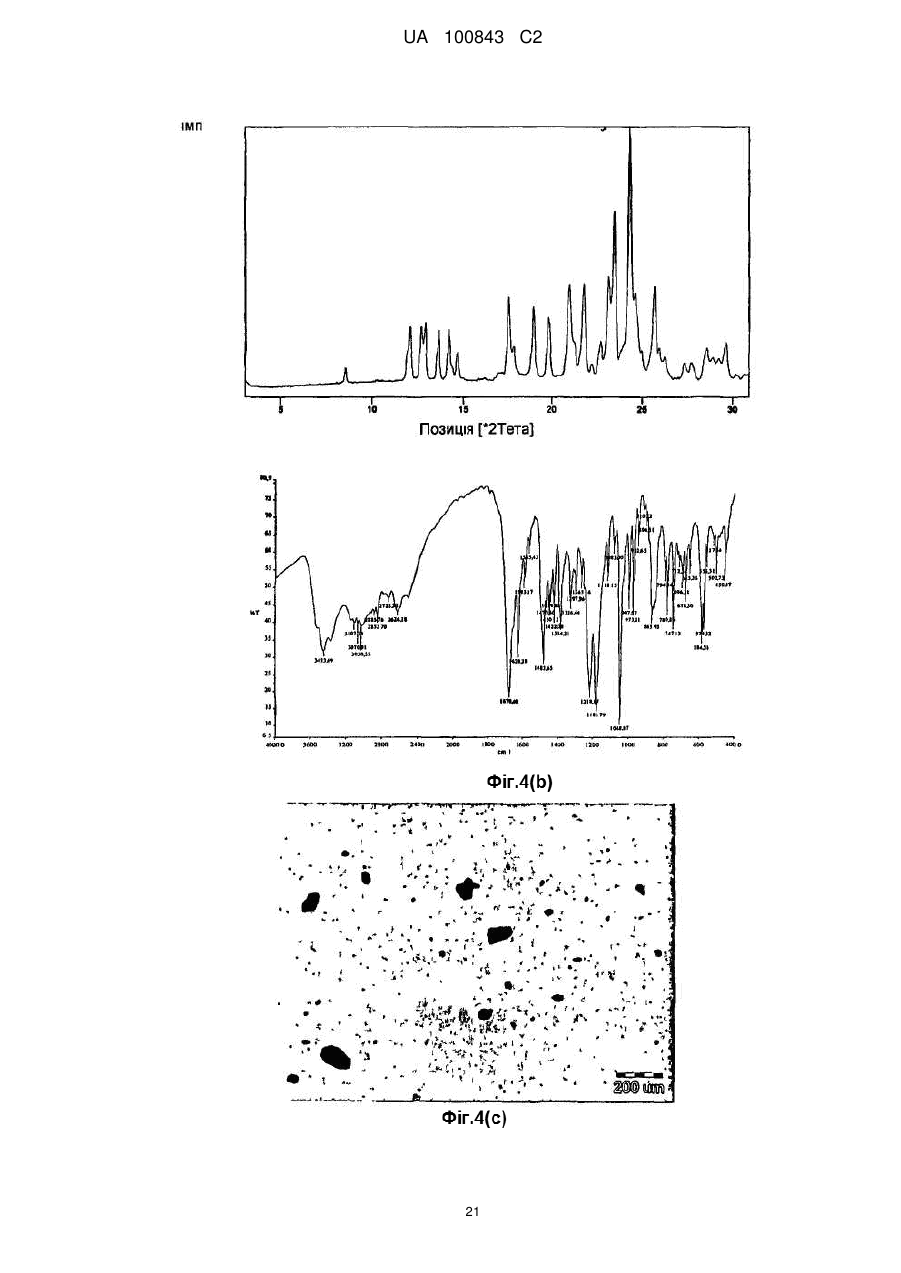
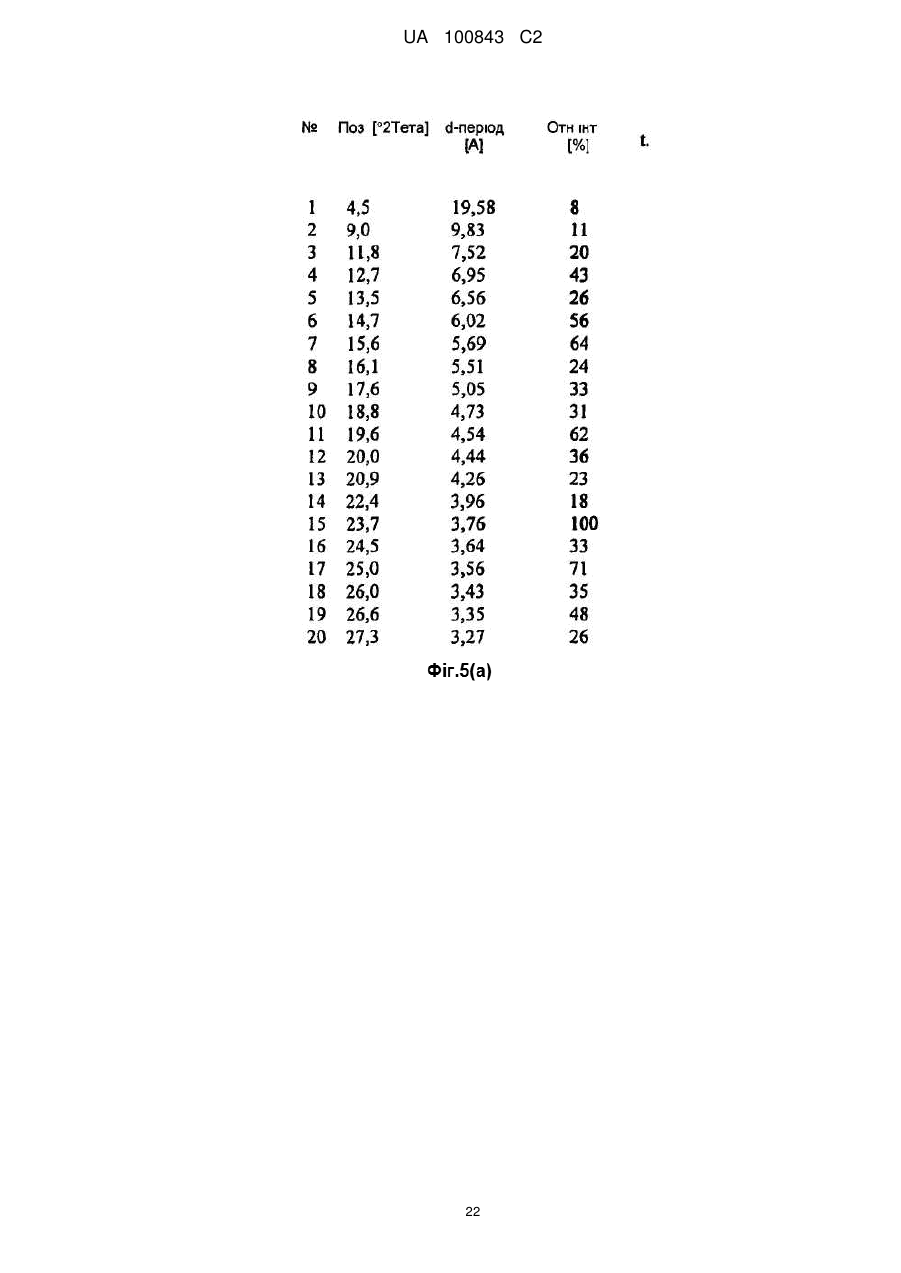
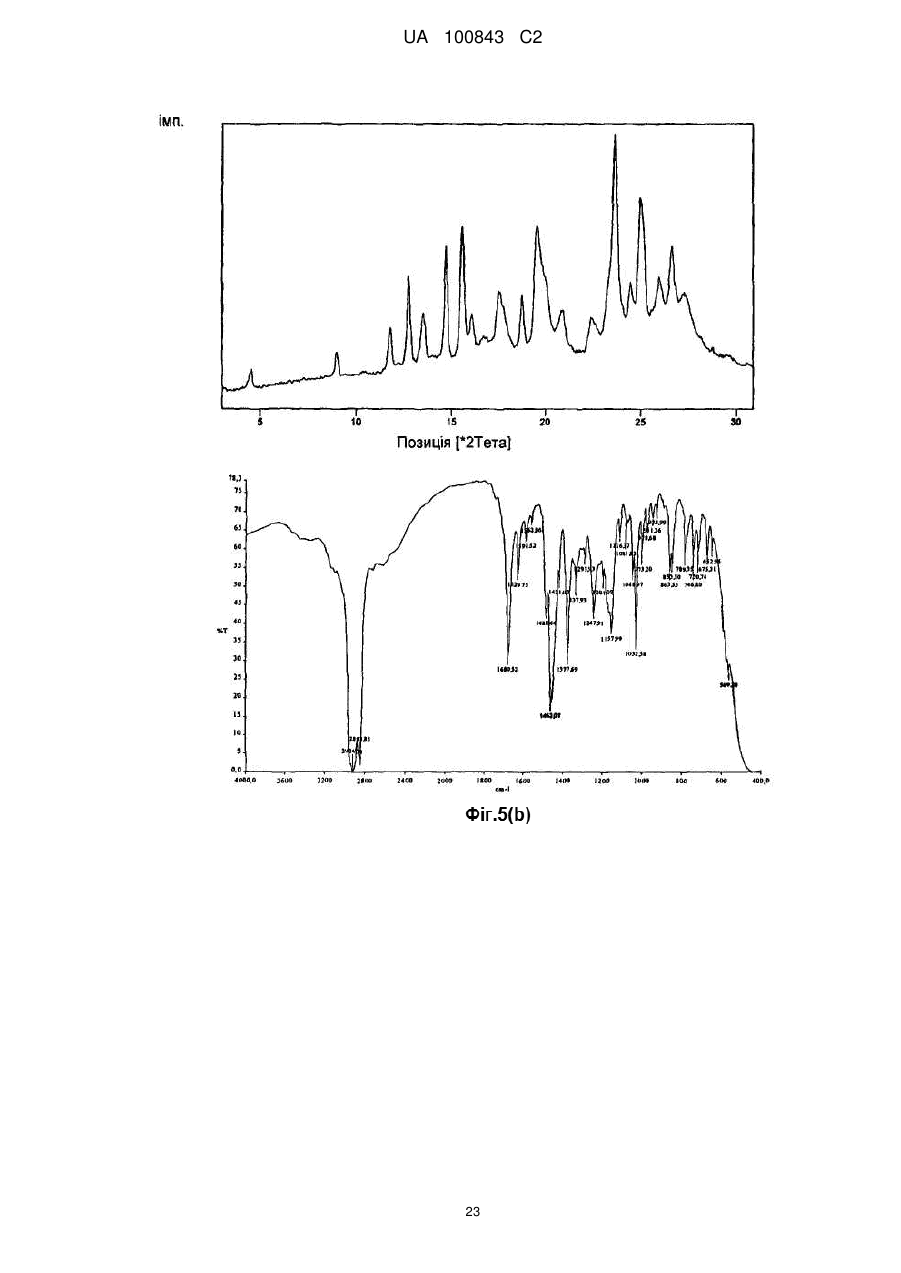
5. Сполука за п. 1, яка відрізняється тим, що характеризується картиною дифракції рентгенівських променів на порошку, що демонструє характеристичні кути дифракції при 4,5; 9,0; 15,6; 23,7; 25,0 і 26,6°±0,2°2-тета.
6. Спосіб одержання сполуки формули І, що включає стадії:
одержання основи зипразидону;
взаємодії з водою і сірчаною кислотою;
можливо, охолодження і/або сушіння;
одержання сполуки формули І.
7. Спосіб за п. 6, який відрізняється тим, що безводну основу зипразидону одержують шляхом реакції 6-хлор-5-(2-хлоретил)-1,3-дигідро-2Н-індол-2-ону і 3-(1-піперазиніл)-1,2-бензізотіазолу у присутності лужної сполуки і органічного розчинника, можливо, змішаного з водою.
8. Спосіб за п. 7, який відрізняється тим, що лужна сполука є Na2CO3.
9. Спосіб за п. 7, який відрізняється тим, що органічний розчинник є іонною рідиною.
10. Спосіб за п. 9, який відрізняється тим, що іонна рідина вибрана з групи 1-R-3-R1-імідазолу Н(+) х А(-), де R і R1 є нижчим алкілом, а А(-) є моно- або поліпротонний аніон кислоти.
11. Застосування сполуки за будь-яким з пп. 1-5 для одержання фармацевтичної композиції для профілактики і/або лікування психотичних станів.
12. Застосування за п. 11, яке відрізняється тим, що психотичні стани включають шизофренію і тривожні розлади.
Текст
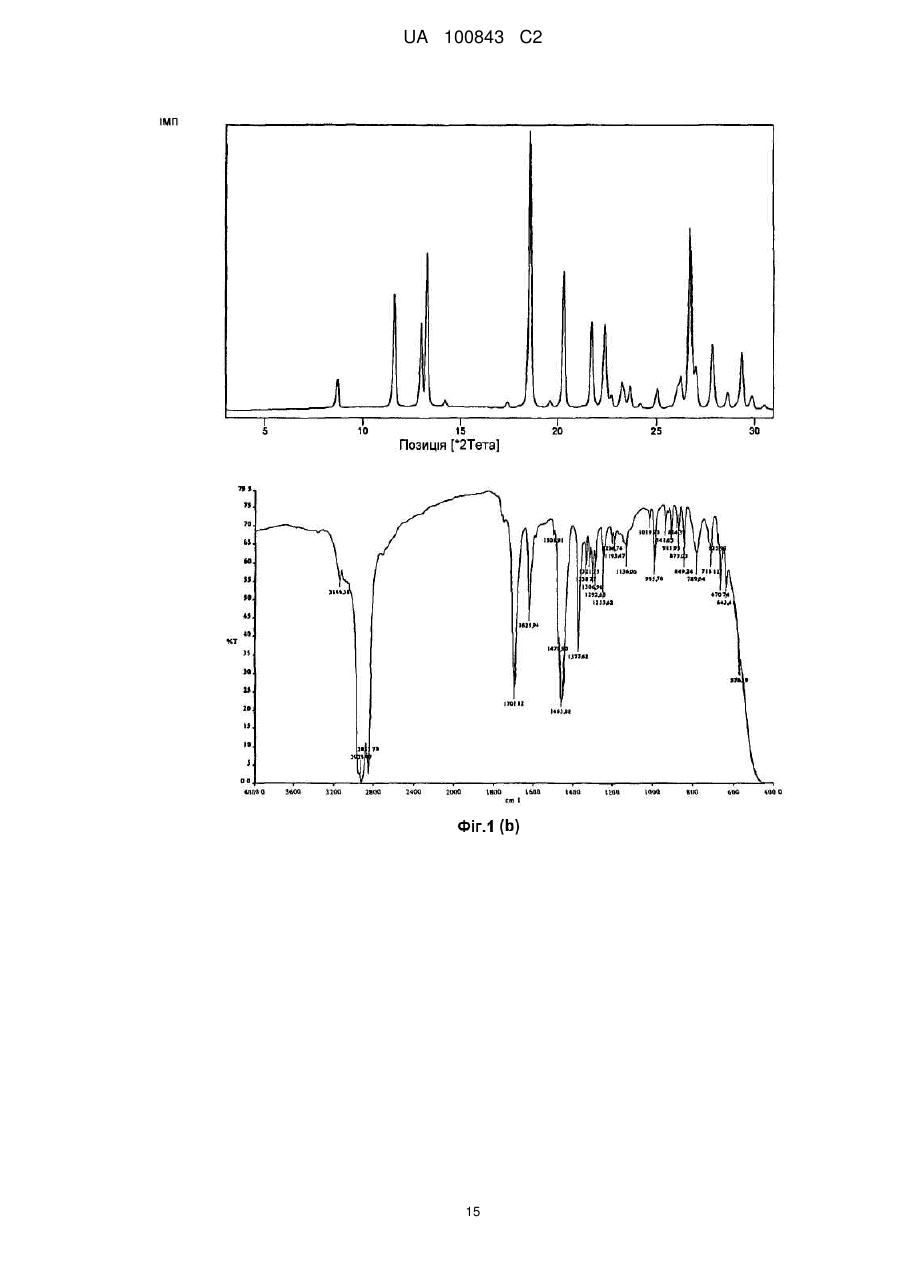
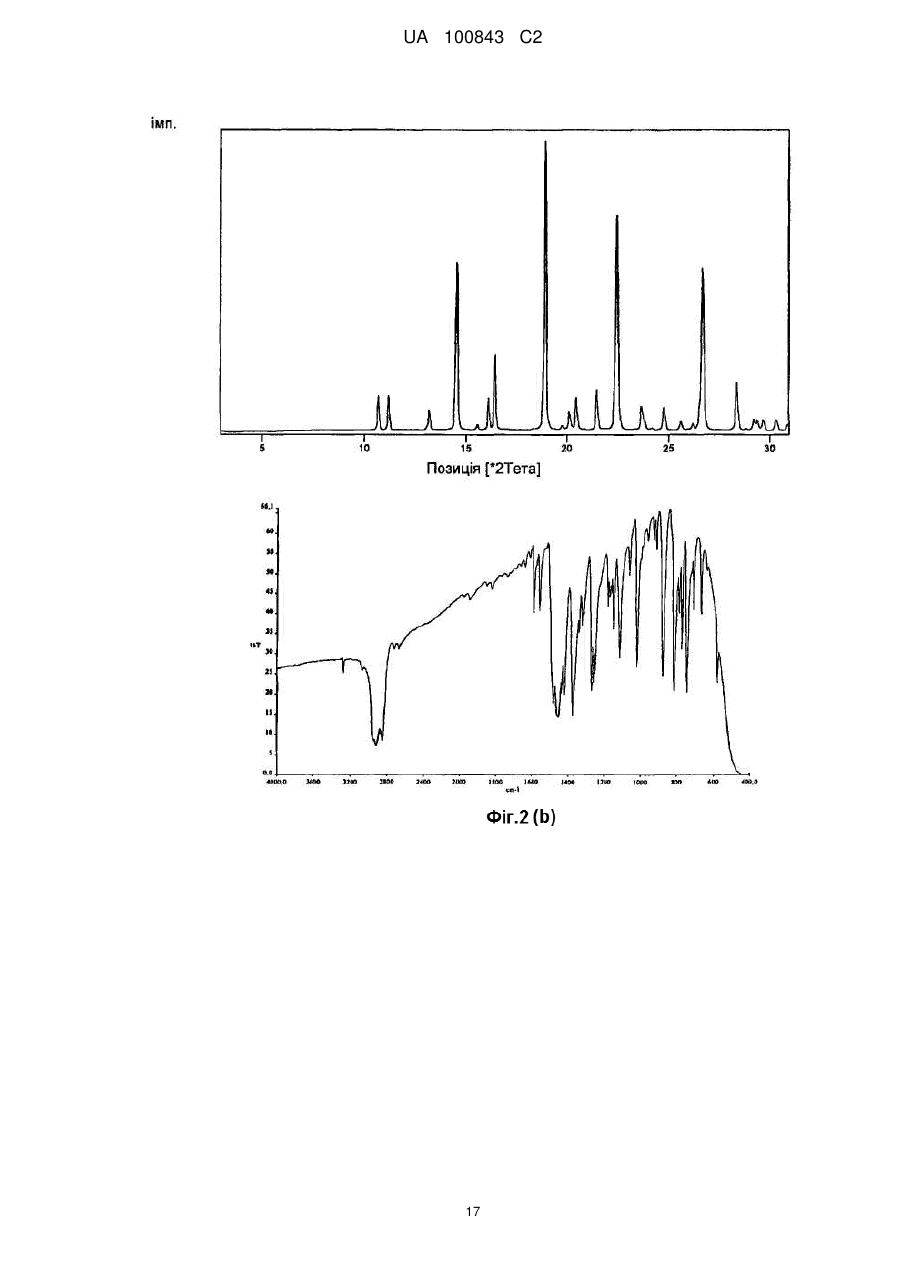
Реферат: Даний винахід стосується нових поліморфних форм сульфатів зипразидону, а також способу їх одержання і фармацевтичних препаратів, що їх містять. Поліморфні форми сульфатів зипразидону за даним винаходом характеризуються малим середнім розміром частинок і високою розчинністю, що додає сполукам покращувану біодоступність. UA 100843 C2 (12) UA 100843 C2 UA 100843 C2 5 Даний винахід відноситься до нових поліморфних форм сульфатів зіпразідона, а також до способу їх одержання і фармацевтичних препаратів, що містять їх. Поліморфні форми сульфатів зіпразідона згідно даного винаходу характеризуються невеликими середніми розмірами частинок і високою розчинністю, що додає сполукам покращувану біодоступність в порівнянні з наявними в даний час солями зіпразідона. Попередній рівень техніки Зіпразідон є тривіальною назвою для 5-[2-[4-(1,2-бензитіазол-3-іл)-1-піперазиніл]Етилу]-6хлор-1,3-дигідро-2H-індол-2-она формули: 10 15 20 25 30 35 40 45 50 активного фармацевтичного інгредієнта, що володіє нейролептичною активністю. В EP 0281309 описаний спосіб одержання зіпразідона за допомогою реакції сполучення, що здійснюється в органічних полярних розчинниках, таких як етанол N, N-диметилформамiд (ДМФ) і метилізобутилкетон (МІБК). У Прикладі 16 EP 0 281 309-A1 розкритий спосіб одержання зіпразідона гідрохлориду в напівгідратованій формі. В EP 0584903 розкритий альтернативний підхід до одержання зіпразідона, солей зіпразідона, включаючи гідрохлорид і метансульфонат, де реакцію сполучення здійснюють у воді у присутності надлишку карбонату натрію в якості нейтралізуючого агенту. Відповідно до EP 0281309, EP 0584903 і EP 1029861 фармацевтично прийнятні солі сполуки кислоти зіпразідона можуть бути одержані звичайним способом шляхом обробки розчину або суспензії вільної основи зіпразідона приблизно одним хімічним еквівалентом фармацевтично прийнятної кислоти. Для виділення солей використовують звичайні способи концентрації і перекристалізації. EP 0918772 і EP 0904273 відносяться до солей дигідратів і тригідратів зіпразідона мезілата, які, як зазначено, мают підвищену гігроскопічну стабільність і покращувану розчинність у воді в порівнянні з солями соляної кислоти. В WO2006/034964 розкритий спосіб застосування органічних полярних розчинників, таких як ацетонітрил, для приготування фармацевтично прийнятної солі сполуки кислоти зіпразідона, такий як малеат або ацетат. Беручи до уваги попередній рівень техніки, дотепер існує необхідність в покращуваному способі одержання солей зіпразідона. Завдання винаходу Завдання даного винаходу полягає в тому, щоб створити солі зіпразідона, що мають певні властивості, що роблять їх більш відповідними для виготовлення фармацевтичних композицій. Інше завдання даного винаходу полягає в створенні солей зіпразідона, які можуть краще переноситися після поглинання. Даний винахід вирішує вищеописані проблеми шляхом того, що запропоновані сульфати зіпразідона, тобто зіпразідона сульфат і гідросульфат містять конкретні кількості кристалічної води. Сульфати зіпразідона за даним винаходом можуть бути одержані з високою чистотою, мають високу стабільність і сприятливі властивості препарату, зокрема, в порівнянні з гідрохлоридною формою зіпразідона. Автори даного винаходу несподівано виявили, що сполука за даним винаходом забезпечує покращувані властивості відносно розчинності і розміру частинок. На розчинність сполук з одного боку прямо впливає вміст кристалічної води і, з іншого боку, малий розмір частинок. Вказані ефекти, у свою чергу, впливають на переносимість і впровадження вказаних сполук після поглинання, оскільки у відповідних фармацевтичних композиціях може використовуватися менша кількість лікарських засобів, що демонструє, при цьому, таку ж або навіть покращувану біодоступність в порівнянні із сполуками попереднього рівня техніки. Графічні матеріали На кресленнях, де це актуально, (а) означає таблицю, (б) означає ГІК (інфрачервоний) спектр з перетворенням Фур'є (FT-IR спектр) і (c) означає мікроскопічний знімок. 1 UA 100843 C2 5 10 15 20 25 30 35 40 45 50 На Фіг. 1 показаний спектр дифракції рентгенівських променів на порошку для 6-хлор-5-(2хлоретил)-1,3-дигідро-2H-індол-2-она (INT 1). На Фіг. 2 показаний спектр дифракції рентгенівських променів на порошку для (3-(1піперазиніл)-1,2-бензизотіазола) (INT 2). На Фіг. 3 показаний спектр дифракції рентгенівських променів на порошку для (3-(1піперазиніл)-1,2-бензизотіазола) сульфату гідрату (INT 2 сульфату гідрат). На Фіг. 4 показаний спектр дифракції рентгенівських променів на порошку для 5-[2-[4-(1,2бензизотіазол-3-іл)-1-піперазиніл]Етилу]-6-хлор-1,3-дигідро-2H-індол-2-она гідросульфату дигідрату (зіпразідона гідросульфата дигідрату). На Фіг. 5 показаний спектр дифракції рентгенівських променів на порошку для безводого 5[2-[4-(1,2бензізотіазол-3-іл)-1-піперазиніл]Етилу]-6-хлор-1,3-дигідро-2H-індол-2-она гідросульфату. Докладний опис винаходу Відповідно до першого втілення даного винаходу запропоновано сполуку формули I, зіпразідона сульфат або зіпразідона гідросульват, загальної формули: [Зіпразідон * H]n+ [X] * Z H2O, де зіпразідон є сполукою формули; Н є воднем; n=1 або 2; 2 X є HSO4- або SO4 -; і Z=0-30. Z0,28 позначає безводну сполуку або ті, що не містять води I з приблизним вмістом води менше 1 мас. %. Переважно, сполука є зіпразідона сульфатом моногідратом або зіпразідона сульфатом дигідратом. Відповідно до одного з втілень, сполука за даним винаходом має розмір частинок, що знаходиться в діапазоні від приблизно 5 мкм до приблизно 300 мкм, переважно в діапазоні від приблизно 10 мкм до приблизно 150 мкм, і переважніше, в діапазоні від приблизно 20 мкм до приблизно 80 мкм. Середній розмір частинок або розмір частинок по відношенню до об'ємного середнього діаметру частинок сполук за даним винаходом можна визначити за допомогою будь-якого відповідного способу, відомого фахівцеві в даній області техніки. Приклади відповідних способів засновані, наприклад, на способах осадження, розсіяння лазерного випромінювання при лазерній дифракції або електричного диференціючого аналізу рухливості. Переважно застосовують розсіяння лазерного випромінювання. У ще одному втіленні сполука за даним винаходом має розчинність, що знаходиться в діапазоні від приблизно 50 мг/л до приблизно 800 мг/л, переважно в діапазоні від приблизно 100 мг/л до приблизно 500 мг/л, і переважніше, в діапазоні від приблизно 250 мг/л до приблизно 400 мг/л. Для визначення вмісту води можуть бути використані різні способи, відомі фахівцям в даній області техніки, такі як спосіб згідно Карлу Фішеру, який описаний, зокрема, в Європейській Фармакопеї, 5-е видання 2006; спосіб 2.5.12, на який у даному описі здійснюються посилання. Як невеликий середній розмір частинок, так і висока розчинність сприяють високій біологічній доступності сполуки за даним винаходом, являє собою міру швидкості і кількості терапевтично активного лікарського засобу, що досяг системи кровообігу і доступного місця дії. Відповідно до ще одного втілення, сполука за даним винаходом характеризуються картиною дифракції рентгенівських променів на порошку, що демонструє характерну дифракцію при 8,6; 12,1; 13,6; 17,6; 19,8; 23,4 в 24,3° ± 0,2°2 тета (Форма I) або 4,5; 9,0; 15,6; 23,7; 25,0 в 26,6° ± 2 UA 100843 C2 5 10 15 20 25 30 35 40 45 50 55 60 0,2°2 тета (Форма II). Переважно, форми I і II характеризуються картиною дифракції рентгенівських променів на порошку, представленій, відповідно, на Фіг. 4 і Фіг. 5. Картини дифракції рентгенівських променів на порошку особливо підходять для опису поліморфних форм. Відкриття нових поліморфних форм фармацевтично корисної сполуки забезпечує нову можливість поліпшення робочих характеристик фармацевтичного продукту. Це розширює спектр матеріалів, які доступні для ученого, що займається розробкою препаратів, наприклад фармацевтичної лікарської форми лікарського засобу, що володіє бажаним профілем вивільнення або іншою бажаною характеристикою. Відповідно до ще одного переважного втілення даного винаходу запропонований ще один спосіб одержання сполук за даним винаходом. Спосіб включає стадії (1) одержання основи зіпразідона, (2) реакції основи зіпразідона з певними кількостями води і сірчаної кислоти, (3) можливого охолоджування і/або сушки, і (4) одержання сполуки формули I, що має певний вміст води, що характеризується специфічними кристалічними структурами. Слід розуміти, що як альтернатива на першій стадії також можуть бути присутніми вода і/або сірчана кислота, які можуть послідовно реагувати з залишковим початковим продуктом(ами). Як альтернатива, замість основи зіпразідона можна використовувати суміш основи зіпразідона і солі зіпразідона. Як альтернатива, можна використовувати будь-яку іншу реакцію що дає, наприклад, неочищений зіпразідон гідрохлорид, які, наприклад, описані в EP 0281309, EP 0584903, EP 1029861 WO2006/034964, WO2006/034965, WO2006/011157, WO2006/047893, WO2005/085240, WO2005/04160, US2006/0089502. Такі сполуки, у свою чергу, можуть бути перетворені на сульфати зіпразідона за допомогою способів, відомих фахівцям в даній області техніки. Відповідна безводна сполука I, що характеризується Z0,28, може бути одержана за допомогою стандартних способів сушки для видалення розчинників. Приклади відповідних способів сушки включають застосування низького тиску або ексикатору, що містить одну або більше хімічну сполуку, відповідно для видалення розчинника, наприклад, шляхом сполучення з ним. Для одержання бажаного продукту, тобто сульфату зіпразідона, що має певний вміст води, безводну сполуку піддають реакції з певною кількістю сірчаної кислоти або води. Як альтернатива, можуть використовувати надлишок води з подальшою стадією сушки, наприклад, шляхом сушки на повітрі або за допомогою будь-якого іншого приведеного вище способу сушки, до бажаного ступеня (при визначенні, наприклад, за допомогою способу згідно Карлу Фішеру). Слід розуміти, що для описаного вище перетворення з одержанням бажаної сполуки можна використовувати сірчану кислоту з будь-яким вмістом води або безводну сірчану кислоту, або навіть олеум. У таких випадках вміст води в сірчаній кислоті може бути врахований і включений в розрахунок співвідношення використання сірчаної кислоти і води. У реакції може бути використано будь-яке відношення основи зіпразідона, сірчаної кислоти і води. Тривалість і температура реакції можуть бути вибрані відповідно до загальних знань. Переважно, реакцію здійснюють протягом 1-6 годин при температурі, що знаходиться в діапазоні 20-80 °C. Переважніше, реакцію здійснюють спочатку при температурі навколишнього середовища, тобто в діапазоні від 20 до 25 °C, протягом 10-120 хвилин, і потім нагрівають до 50-70 °C в продовж ще 2-5 годин. Після проведення реакції одержана суміш може бути додатково охолоджена, фільтрована і/або висушена. Відповідно до ще одного втілення може бути одержано основу зіпразідона або неочищений зіпразідон. Основу зіпразідон або неочищений зіпразідон одержують шляхом реакції 6-хлор-5(2-хлоретил)-1,3-дигідро-2H-індол-2-она (INT 1) і (3-(1-піперазиніл)-1,2-бензизотіазол) гідросульвату (INT 2) або його сульфату (INT 2 сульфату) у присутності лужної сполуки, і органічного розчинника, можливо змішаного з водою. Органічний розчинник переважно вибраний з групи іонних рідин. Іонні рідини можуть бути вибрані з групи 1-R-3-R1-імідазолу H(+) x A(-), де R і R1 є нижчим алкілом, а A(-) є моно- або поліпротонний аніон кислоти. Термін "нижчий алкіл" відноситься до C1-С10 вуглецю, які можуть містити лінійні і/або розгалужені ланцюги, насичені і/або ненасичені атоми, і гетероатоми. Приклади відповідних іонних рідин є 1,2,3-триметилімідазола метилсульфат, 1-бутил-2,3диметилімідазолу хлориду, 1-бутил-3-метилімідазолу ацетату, 1-бутил-3-метилімідазола броміду, 1-бутил-1,3-метилімідазола хлориду, 1-бутил-3-метилімідазолу гексафторфосфат, 1бутил-3-метилімідазолу гідросульват, 1-бутил-3-метилімідазолу метансульфонат, 1-бутил-3 3 UA 100843 C2 5 10 15 20 25 30 35 40 45 50 55 60 метилімідазолу метилсульфат, 1-бутил-3-метилімідазолу тетрахлоралюмінат, 1-бутил-3метилімідазолу тетрафторборат, 1-бутил-3-метилімідазолу тіоціанату, 1-етил-2,3диметилімідазолу етилсульфату, 1-етил-3-метилімідазолу ацетату, 1-етил-3-метилімідазолу хлориду, 1-етил-3-метилімідазолу метилсульфат, 1-етил-3-метилімімідазолу гідросульват, 1етил-3-метилімімідазолу метансульфонат, 1-етил-3-метилімімідазолу метилсульфат, 1-етил-3метилімімідазолу тетрахлоралюмінат, 1-етил-3-метилімімідазолу тетрафторборат, 1-етил-3метилімімідазолу тіоціанату, 1-гексил-3-метилімімідазолу тетрафторборат, 1-гексил-3метилімімідазолу тетрафторборат, 1-гексил-3-метилімімідазолу трифтор-метансульфонат, 1метил-3-октилімідазолу гексафторфосфат, 1-метил-3-октил-імідазолу трифторметансульфонат, метилімідазола хлорид, метилімідазола гідросульват, метил-трі-н-бутіламмонія метилсульфат. Переважно використовують 1-етил-3-метил-імідазолу етилсульфату або 1-етил-3метилімідазолу метилсульфат. Іонні рідини можуть бути одержані, наприклад з Merck, Німеччини. Також можуть бути використані в суміші однієї або більш ніж однієї іонної рідини з водою. Доведено, що із згаданих вище іонних рідин, особливо 1-етил-3-метилімідазолу, найбільш підходять для одержання сполук за даним винаходом метилсульфат і 1-етил-3метилімімідазолу етилсульфат зважаючи на добру розчинність початкових продуктів. Переважно використовують Na2CO3 і 1-етил-3-метилімідазолу метилсульфат. Фахівцям в даній області техніки відомі відповідні кількості сполук, температура і тривалість реакції. Переважно, реаккцію здійснюють при температурі в діапазоні від кімнатної температури до температури дефлегмації вживаного розчинника, переважніше, при температурі, вибраній в діапазоні від 80 °C до 120 °C. Переважно, реакцію здійснюють при вибраній температурі протягом від 3 до 80 год. переважніше, протягом 10-30 год. Використаний тут термін "кімнатна температура" відноситься до температури приблизно 22 °C. У ще одному втіленні основа зіпразідона може бути одержана шляхом відновлення 5-[2-[4(1,2-бензизотіазол-3-іл)-1-піперазиніл]-1-оксоетил]-6-хлор-1,3-дигідро-2H-індол-2-она ("оксоетил-зіпразідон") або його сполуки солей. Після завершення реакції реакційну суміш переважно охолоджують до кімнатної температури, і продукт осаджують шляхом додавання води або органічного розчинника або їх сумішей. У переважному втіленні органічні розчинники вибрані з С1-C5 спирту, ацетонітрилу або тетрагідрофурану, оцетової кислоти, ацетону і/або простих ефірів. Переважніше спирти вибрані з метанолу, етанолу і ізопропанолу, а прості ефіри вибрані з ізопропілового ефіру. Відношення доданої води або органічного розчинника, або їх сумішей до початкової кількості 3-(1-піперазиніл)-1,2-бензизотіазолу знаходиться в діапазоні від 1:1 до 100:1, переважно, від 3:1 до 50:1, і найпереважніше, від 5:1 до 20:1 (г/г). У переважному втіленні основу зіпразідона далі очищають шляхом гарячої мацерації або осадження у вищезазначених розчинниках. Обидва способи очищення добре відомі фахівцям в даній області техніки. До утворення солі основу зіпразідона, можливо, заздалегідь гранулюють. Відповідно до ще одного переважного втілення сульфати зіпразідона одержують змішуванням основи зіпразідона або суміші основи зіпразідона і солі зіпразідона з органічною або неорганічною кислотою у вищезазначених розчинниках або воді, або їх сумішах. Температура може знаходитися в діапазоні від кімнатної, тобто 22 °C, до температури дефлегмації використовуваного розчинника, переважно, температура знаходиться в діапазоні від 50 °C до 60 °C. Після цього зіпразідона (гідро) сульфату гідрат виділяют/одержують. Неорганічні кислоти є такими ж, як описано вище. Інші відповідні неорганічні кислоти і органічні кислоти відомі фахівцям в даній області техніки. Розчинники, основа зіпразідона, а також відповідна сіль зіпразідона можуть бути одержані і використані, як описано вище. Відношення змішаної основи зіпразідона або суміші основи зіпразідона і солі зіпразідона до розчинників або води, або їх сумішам знаходиться в діапазоні від 1:1 (г основи зіпразідона до мл розчинників або води) до 1:1000, переважно від 1:5 до 1:100, і найпереважніше, від 1:7 до 1:15. Відношення змішаної основи зіпразідона або суміші основи зіпразідона до солі зіпразідона і органічної або неорганічної кислоти знаходиться в діапазоні від 1:0,01 до 1:100 (г основи зіпразідона на г основи), переважно, від 1:0,1 до 1:10, і найпереважніше, від 1:0,2 до 1:0,5. Кількість зіпразідона змішують в одну стадію повністю або додають дробовими порціями. Зіпразідона сульфати можуть одержувати шляхом змішування з розчинником або основою, або їх сумішами в будь-якій послідовності. Переважно, основу зіпразідона і сіль зіпразідона змішують з розчинником і кислотою. У ще одному втіленні основа може бути додана до суміші зіпразідона і розчинника, як представлено в прикладах. Розчин можуть фільтрувати і потім охолоджувати до температури від -10 до 30 °C, переважно, до кімнатної температури. 4 UA 100843 C2 5 10 15 20 25 30 35 40 45 50 55 60 Осад фільтрують і продукт сушать переважно при температурі від 10 °C до 60 °C, переважніше від 40 °C до 50 °C. Висушування можуть здійснювати за допомогою нагрівання, переважно при тиску навколишнього середовища або зниженому тиску або шляхом контакту солі зіпразідона з вологим повітрям в сушарці з псевдозрідженим шаром, причому атмосфера в сушарці з псевдозріженим шаром має вологість щонайменше 15 %. Переважно здійснюють сушку на повітрі в наявній в продажі сушарці з вологим повітрям. Відповідно до переважного втілення, сполуку за даним винаходом застосовують для виготовлення фармацевтичної композиції для профілактики і/або лікування психотичних станів і, переважно, шизофренії, шизоафектного розладу, маревного розладу, біполярного розладу, психотичної депресії, короткочасного психічного розладу і тривожних розладів. Відповідні фармацевтичні композиції містять попередні фармацевтичні композиції для ентерального і парентерального введення, з використанням відповідних носіїв в різних кількостях. Фармацевтичні композиції можуть знаходитися в твердій лікарській формі. Типові лікарські форми включають пігулки, капсули, саше, коржика, порошки, пілюлі або гранули. Тверда лікарська форма може бути, наприклад, лікарська форма з негайним вивільненням, швидкорозчинна лікарська форма, лікарська форма з контрольованим вивільненням, ліофілізована лікарська форма, лікарська форма із сповільненим вивільненням, лікарська форма з тривалим вивільненням, лікарська форма з імпульсним вивільненням, змішана лікарська форма з негайним вивільненням і контрольованим вивільненням або їх комбінації. Переважний твердий препарат у вигляді пігулки. Тверда лікарська форма переважно є лікарською формою з негайним вивільненням, що забезпечує переваги відносно біологічної доступності активної сполуки. Лікарська форма може бути приготована відповідно до звичайних способів, при яких активний інгредієнт або речовину, одну і більше, ніж одну змішують і гранулюють, додаючи розчинник в мішалку з невеликими або великими зусиллями зсуву або за допомогою гранулятора з псевдозрідженим шаром. Гранулят сушать, наприклад, в сушарці з псевдозрідженим шаром. Висушений гранулят доводять до необхідного розміру частинок. Доведення частинок мікроматриксу до необхідного розміру може бути здійснено з використанням вібраційного гранулятора, подрібнючого млину або будь-якого іншого звичайного способу. Сито, використовуване для сортування за розміром, може мати отвори від 0,25 мм до 5 мм. Альтернативно, частинки ядра можна одержувати шляхом екструзії, сферонізації, гранулювання з розплаву або за допомогою вальцової компактизації. Частинки ядра можуть бути покриті розчином одного або більш, ніж одного агента, контролюючого вивільнення, за допомогою будь-якого відомого способу, що включає застосування спрею. Розпилювання можуть здійснювати за допомогою апарату для нанесення оболонки в псевдозрідженому шарі (переважно апарату для нанесення оболонки Вурстера), або в системі з дражіровочним казаном. Альтернативно, покриття частинок ядра одним або більш, ніж одним агентом, контролюючим швидкість вивільнення, можуть здійснювати за допомогою способу гарячого плавлення з використанням гранулятора або апарату для нанесення оболонки в псевдозрідженому шарі (переважно апарату для нанесення оболонки Вурстера), або в системі з дражіровочним казаном. Пресування мікропігулок здійснюють в звичайних таблетуючих апаратах (наприклад, апаратах Манесті, Кадмака або Киліана). Можуть одержувати мікропігулки різних розмірів і форм, наприклад, круглі, овальні, довгасті, у формі капсул, трикутні, квадратні і т.д. Переважна форма мікропігулок є круглою, двоопуклою, а переважний діаметр мікропігулки складає від 1,5 мм до 9,5 мм. Мікропігулки можуть бути покриті розчином одного або більше ніж одного агента, контролюючого вивільнення, за допомогою будь-якого відомого способу, що включає застосування спрею. Розпилювання можуть здійснювати з використанням апарату для нанесення оболонки в киплячому шарі (переважно апарату Вурстера для нанесення оболонки), або в системі нанесення оболонки з дражіровочним казаном. Композиція за даним винаходом також може бути представлена в конкретній лікарській формі для додаткового поліпшення біологічної доступності сполуки за даним винаходом. Біологічна доступність ліків, що вводяться перорально визначається чинниками, які включають природу молекули, її стабільність і препарат, що вводиться, і чинники, що відносяться до пацієнта, такі як зменшена площа поверхні кишечника, як результат колік або видалення кишечника, і те, чи приймалися ліки з їжею. Чинники, що впливають на біологічну доступність, можуть включати погану абсорбцію з шлунково-кишкового тракту, ефект першого проходження крізь печінку і деградацію ліків до досягнення системи кровообігу, але не обмежуватися ними. Для поліпшення біологічної доступності сполуки за даним винаходом, наприклад, розмір 5 UA 100843 C2 5 10 15 20 25 30 35 40 45 50 55 60 фракцій частинок може бути адаптований шляхом додаткового дроблення. Переважний розмір частинок після дроблення є d90, тобто середній діаметр частинок для 90 % частинок, що становить менше ніж 30 мкм, переважніше, менше ніж 20 мкм, найпереважніше менше ніж 10 мкм. Відповідно до ще одного втілення фармацевтична композиція за даним винаходом може містити додатково до сполук за даним винаходом один або більш ніж один розбавлювач, зв'язуючий агент, розпушувач, мастило, підсолоджувач, що змащує речовину, коррігент, фарбник і інші ексципієнти, залежно від бажаної лікарської форми. Відповідні розбавлювачі включають фармацевтично прийнятних наповнювачів, такі як лактозу, мікрокристалічну целюлозу, двоосновний фосфат кальцію, сахариди і/або суміші вищезазначених речовин. Приклади розбавлювачів включають мікрокристалічну целюлозу, таку ® ® як Avicel PH 101 и Avicel PH 102; лактозу, таку як моногідрат лактози, безводна лактоза і ® ® Pharmatose DCL 21; двоосновний фосфат кальцію, такий як Emcompress ; маніт, крохмаль, сорбіт, сахарозу і глюкозу. Найбільш переважними є мікрокристалічна целюлоза і лактоза. Зв'язуючі агенти переважно вибрані з полівінілпірролідону, сортів крохмалю (прежелатинізований або звичайний), похідних целюлози, таких як гідроксипропілметилцелюлоза (ГПМЦ), гідроксипропілцелюлоза (ГПЦ) і карбоксиметилцелюлоза (КМЦ), і їх солей і желатину, причому найбільш переважною є ГМПЦ. Відповідні розпушувачі включають кроськармелозу натрію, кросповідон, натрію крохмаль гліколят, кукурудзяний крохмаль, картопляний крохмаль, маїсовий крохмаль і модифіковані силікатами кальцію крохмалі, низькозаміщену гідроксипропілцелюлозу і т.п. Найбільш переважною є кроськармелоза натрію. Змащуючі речовини переважно вибрані з групи, що складається із стеарата магнію, лаурілсульфата магнію і стеарілфумарата натрію, складних ефірів сахарози або жирних кислот, поліетіленгліколя, стеаринової кислоти і т.п. Підсолоджувачі переважно вибрані з групи, що складається з аспртама, натрієвого сахарину, дікалія гліциррізіната, аспартама, паськонника кропиволистного, тауматіна і т.п. Змащуючі речовини переважно вибрані з групи, що складається з діоксиду кремнію, тальку і силікату алюмінію. Як корригенти, фарбники або замутняючі агенти і пігменти можуть бути використані будь-які відповідні сполуки, відомi фахівцевi в даній області. Композиції, відповідні для парентерального введення, містять стерильні водні і неводні розчини активної сполуки для ін'єкцій, де препарати переважно ізотонічні крові передбачуваного реципієнта. Ці препарати можуть містити антиоксиданти, буфери, бактеріостатичні препарати і розчини, які роблять композиції ізотонічними крові передбачуваного реципієнта. Водні і неводні стерильні суспензії можуть включати суспендуючі агенти і загусники. Композиції можуть бути представлені в однодозових або багатодозових контейнерах, наприклад, запаяних ампулах або віалах, і можуть зберігатися у висушеному заморожуванням або ліофілізованому стані, що вимагає тільки додавання стерильного рідкого носія, наприклад, фізіологічного розчину або води для ін'єкцій, безпосередньо перед застосуванням. Розчини, що готують безпосередньо перед застосуванням, для ін'єкцій і суспензії можуть бути приготовані із стерильних порошків, гранул і пігулок описаного вище типу. Концентрація активних сполук в композиції за даним винаходом залежатиме, наприклад від абсорбції, інактівації, швидкості екскреції, схеми введення лікарського засобу і кількості, що вводиться, а також інших чинників, відомих фахівцям в даній області техніки. Інші інгредієнти для приготування, наприклад, композиції для ентерального застосування, такі як пігулки або капсули, або інші відповідні форми, також добре відомі фахівцям в даній області техніки і можуть бути приготовані залежно від бажаної консистенції і інших передбачених властивостей. Наступні приклади ілюструють винахід, але не обмежують його об'єм. Приклади Сполуки за даним винаходом характеризували відносно температури їх плавлення за допомогою апарату Коффлера для вимірювання температури плавлення, інфрачервоних (ГІК) спектрів, одержаних на ІК-СПЕКТРОМЕТРІ з перетворенням Фур'є Paragon 100 Perkin-Elmer (на -1 -1 системі FT-IR SPECTRUM GX Perkin Elmer [4000-400] см з дозволом 4 см , з одержанням табл. KBr.) і картин дифракції рентгенівських променів на порошцi (одержаних за допомогою дифрактометра Phillips PW3040/60 X'Pert PRO з використанням випромінювання СиКa). Вміст води у відповідних сполуках тестували з використанням способу Карла Фішера. Картини частинок одержували на мікроскопі Olympus BX 50, обладнаному камерою Olympus DP70. Спосіб ВЕРХ (високоефективної рідинної хроматографії) високого дозволу використовували 6 UA 100843 C2 5 10 15 20 25 30 35 40 45 50 55 60 для визначення кількості і чистоти INT 1, INT 2, оксоетилзіпразідону і основи зіпразідона. Тести здійснювали на колонці Zorbax Eclipse XDB-C18, 1,8 мкм, 50×4,6 мм і колонці X-bridge С18, 2,5 мкм, 75×4,6 мм. Рухома фаза є градієнтом 0,01 M діаммонію гiдрофосфату, pH 3 і ацетонітрилу/метанолу (відношення 20/80). Хроматограф обладнаний детектором УФ, встановленим на 230 нм, швидкість потоку складає 1,0 мл за хвилину при 40 °C. Середній розмір частинок визначають шляхом розсіювання лазерного випромінювання з використанням апарату Malvern-Mastersizer MS 2000. Частинки, які піддають вимірюванню ® розміру, спочатку суспендують в ізопарафіновому маслі (Isopar ) і потім піддають визначенню розміру в приладі Malvern Mastersizer MS 2000. Звичайно 100-800 міліграмiв речовини диспергують в 5-8 мл рослинного масла. Відповідно до інформації виробників, Malvern Mastersizers дає можливість вимірювати розподіли розміру частинок в діапазоні від 20 нм до 2000 мкм, з точністю, більшою ніж 0,5 %. Розміри частинок визначають за допомогою вимірювання кутового розподілу лазерного світла, що розсіюється в гомогенній суспензії частинок. Розподіл розміру визначають відповідно до даних розсіювання світла з використанням теорії розсіювання світла, розробленої Густавом Мі. Приклад 1 Одержання (3-(1-піперазиніл)-1,2-бензизотіазол) сульфату гідрата (INT 2 сульфат) 1 г 3-(1-піперазиніл)-1,2-бензизотіазолу (INT2), 10 мл демінералізованої води і 1,9 г H 2SO4 (відношення INT2:H2SO4 1:5) змішували при кімнатній температурі протягом ночі. Після завершення процесу прозорий розчин ставав білим. Продукт фільтрували і сушили протягом 2 годин при 30 °C. Одержували білий осад 3-(1-піперазиніл)-1,2-бензизотіазолу сульфату гідрату (INT2 сульфат) в кількості 0,3. Вміст води, при визначенні способом згідно Карлу Фішеру, складав 2,5 %. Приклад 2 Одержання (3-(1-піперазиніл)-1,2-бензизотіазол) сульфату гідрата (INT 2 сульфат) 50 г 3-(1-піперазиніл)-1,2-бензизотіазолу (INT2), 500 мл демінералізованої води і 33,5 г H2SO4 (відношення INT 2:H2SO4 1:1,5) перемішували при кімнатній температурі протягом 47 годин. Після завершення процесу прозорий розчин ставав білим. Продукт фільтрували, промивали 125 мл демінералізованої води і сушили протягом 2 годин при 30 °C. Одержували білий осад 3-(1-піперазиніл)-1,2-бензизотіазолу сульфату гідрату (INT2 сульфат) в кількості 42,6 р. Приклад 3 Одержання 5-[2-[4-(1,2-бензизотіазол-3-iл)-1-піперазиніл]Етилу]-6-хлор-1,3-дигідро-2H-індол2-она (основа зіпразідона) У круглодонну колбу поміщали 1 г 6-хлор-5-(2-хлоретил)-1,3-дигідро-2H-індол-2-она (INT 1), 1,1 г 3-(1-піперазиніл)-1,2-бензизотіазолу (INT2), 1,46 г Na2CO3 і 8 мл 1-етил-3-метилімідазолу метилсульфату, нагрівали до 100 °C і перемішували протягом 24 годин. Після завершення реакції наявність 5-[2-[4-(1,2-бензизотіазола-3-іл)-1-піперазиніл]Етилу]-6-хлор-1,3-дигідро-2Hіндол-2-она підтверджували за допомогою ВЕРХ. Реакційну суміш охолоджували до кімнатної температури і додавали 30 мл метанолу для осадження продукту. Реакційну суміш перемішували протягом приблизно 1 годину і фільтрували. Одержували вологу неочищену основу зіпразідона в кількості 1,8 г (чистоту 88,0 % визначали за допомогою ВЕРХ). Зразок далі поміщали цілком в круглодонну колбу об'ємом 50 мл з 20 мл демінералізованої води і нагрівали при 79 °C протягом 30 хвилин, фільтрували і охолоджували до кімнатної температури. 2,65 г осадженої вологої основи зіпразідона сушили у вакуумній сушарці протягом 1 години при температурі 50 °C і протягом ночі при кімнатній температурі. Одержували основу зіпразідона в кількості 1,03 р. Приклад 4 Одержання 5-[2-[4-(1,2-бензизотіазол-3-iл)-1-піперазиніл]Етилу]-6-хлор-1.3-дигідро-2H-індол2-она (основа зіпразідона) Приклад 2 повторювали за винятком того, що застосовували 1-бутил-3-метилімімідазолу тетрафторборат замість 1-етил-3-метилімідазолу метилсульфату. Після завершення реакції наявність 5-[2-[4-(1,2-бензизотіазол-3-iл)-1-піперазиніл]Етилу]-6-хлор-1,3-дигідро-2H-індол-2-она підтверджували за допомогою ВЕРХ. Приклад 5 Одержання 5-[2-[4-(1,2-бензизотіазол-3-iл)-1-піперазиніл]Етилу]-6-хлор-1,3-дигідро-2H-індол2-она (основа зіпразідона) Приклад 2 повторювали за винятком того, що використовували 10 мл 1-бутил-3метилімімідазолу броміду замість 8 мл 1-етил-3-метилімімідазолу метилсульфату. Після завершення реакції наявність 5-[2-[4-(1,2-бензизотіазол-3-iл)-1-піперазиніл]Етилу]-6-хлор-1,3 7 UA 100843 C2 5 10 15 20 25 30 35 40 45 50 55 60 дигідро-2H-індол-2-она підтверджували за допомогою ВЕРХ. Приклад 6 Одержання 5-[2-[4-(1,2-бензизотіазол-3-iл)-1-піперазиніл]Етилу]-6-хлор-1,3-дигідро-2H-індол2-она гідросульвату дигідрату (зіпразідона гідросульвату дигідрат) У круглодонну колбу поміщали 2 г безводного (що містить менш ніж 1 % води при визначенні способом згідно Карлу Фішеру) 5-[2-[4-(1,2-бензизотіазол-3-іл)-1-піперазиніл]Етилу]-6-хлор-1,3дигідро-2H-індол-2-она (основи зіпразідона), 20 мл демінералізованої води і 0,95 г сірчаної кислоти, і змішували при кімнатній температурі протягом 15-60 хвилин. Гомогенну суміш нагрівали до 60 °C і інтенсивно перемішували протягом, приблизно, 3 годин. Потім суміш охолоджували до кімнатної температури, фільтрували і промивали демінералізованою водою. Одержаний продукт сушили в повітряній сушарці протягом, приблизно, 2 годин при 30 °C до одержання постійної маси. Одержували 2,46 г продукту. Вміст води склав 7,1 % при визначенні способом згідно Карлу Фішеру. Розчинність одержаного зіпразідона гідросульвату дигідрату складала 0,36 міліграмiв/мл у воді (pH 6,8) + 2 % додецилсульфата натрію (SDS-sodium dodecylsulphate) при кімнатній температурі. Двотижневі тести стабільності (40 °C, вологість 75 % і 50 °C) продемонстрували відсутність деградації початкового продукту, що дає у результаті чистоту 99,7 % і 99,7 % зіпразідона, відповідно, при визначені за допомогою ВЕРХ. Приклад 7 Одержання 5-[2-[4-(1,2-бензизотіазол-3-iл)-1-піперазиніл]Етилу]-6-хлор-1,3-дигідро-2H-індол2-она гідросульвату дигідрату (зіпразідона гідросульвату дигідрат) У круглодонну колбу поміщали 23 г безводного (що містить менш ніж 2 % води при визначенні способом згідно Карлу Фішеру) 5-[2-[4-(1,2-бензизотіазол-3-iл)-1-піперазиніл]Етилу]6-хлор-1,3-дигідро-2H-індол-2-она (основи зіпразідона), 230 мл демінералізованої води і 11 г сірчаної кислоти і змішували при кімнатній температурі протягом 15-60 хвилин. Гомогенну суміш нагрівали до 60 °C і інтенсивно перемішували протягом, приблизно, 3 годин. Потім суміш охолоджували до кімнатної температури, фільтрували і промивали демінералізованою водою. Одержаний продукт сушили в повітряній сушарці протягом, приблизно, 2 годин при 30 °C до досягнення постійної маси. Одержали 29,9 г продукту. Вміст води склав 6,8 % при визначенні способом згідно Карлу Фішеру. Приклад 8 Одержання 5-[2-[4-(1,2-бензизотіазол-3-iл)-1-піперазиніл]Етилу]-6-хлор-1,3-дигідро-2H-індол2-она гідросульвату дигідрату (зіпразідона гідросульвату дигідрат) У круглодонну колбу поміщали 7,5 г безводного (що містить менш, чим 1 % води при визначенні способом згідно Карлу Фішеру) 5-[2-[4-(1,2-бензизотіазол-3-iл)-1-піперазиніл]Етилу]6-хлор-1,3-дигідро-2H-індол-2-она (основи зіпразідона), 75 мл демінералізованої води і 1,95 г сірчаної кислоти і перемішували при кімнатній температурі 15-60 хвилин. Гомогенну суміш нагрівали до 60 °C і інтенсивно перемішували протягом, приблизно, 3 годин. Потім суміш охолоджували до кімнатної температури, фільтрували і промивали демінералізованою водою. Одержаний продукт сушили в повітряній сушарці протягом, приблизно, 2 годин при 30 °C до досягнення постійної маси. Одержували 10,1 г продукту. Вміст води склав 6,9 % при визначенні способом згідно Карлу Фішеру. Приклад 9 Одержання 5-[2-[4-(1,2-бензизотіазол-3-iл)-1-піперазиніл]Етилу]-6-хлор-1,3-дигідро-2H-індол2-она гідросульвату дигідрату (зіпразідона гідросульват безводний) 300 г зіпразідона гідросульвату дигідрату, одержаного згідно Прикладу 6, сушили протягом 12 ч при температурі 100 °C в повітряній сушарці. Вміст води в одержаному безводому гідросульватi зіпразідона склав менше 0,5 % при визначені способом згідно Карлу Фішеру. Приклад 10 Одержання 5-[2-[4-(1,2-мул)-1-піперазиніл]Етилу]-6-хлор-1,3-дигідро-2H-індол-2-она гідросульвату дигідрату (зіпразідона гідросульват безводний) 1 г зіпразідона гідросульвату дигідрату, одержаного в Прикладі 6, сушили протягом 12 ч при температурі у вакуумній сушарці. Вміст води в одержаному безводному гідросульватi зіпразідона склав менше 0,5 % при визначені способом згідно Карлу Фішеру. Приклад 11 20 міліграмів зіпразідона гідросульвату дигідрату піддавали аналізу сорбції води (Surface Measurement Systems Ltd., London, UK; два повні 11-стадійні цикли від 0 % відносної вологості (ОВ) до 95 % ОВ при температурі 25 °C і швидкості потоку азоту 200 мл/хв; мінімальний час затримки на стадії, коли dm/dt 99 % відповідно до ВЕРХ). Вміст води складав 2,3 % при визначенні способом згідно Карлу Фішеру. Приклад 18 Капсули, що містять зіпразідона гідросульвату дигідрат Капсули, що містять зіпразідона гідросульвату дигідрат, що мають склад, представлений в Таблиці, готували там самим способом, що і в Прикладі 12. Склад зіпразідона гідросульфата дигідрат лактози моногдрат (100) Крохмаль 1500 (прежелатинізований) маїсовий крохмаль ПВП K 25 етанол (96 відсотків) очищена вода стеарат магнію Разом A 26,50 60,45 10,00 / 2,55 д.к. / 0,50 100,0 B C D % в капсулі (мас./мас.) 26,50 26,50 26,50 60,95 51,20 52,00 10,00 9,00 9,00 / 12,50 12,50 2,55 / / д.к. / / / д.к. д.к. / 0,80 / 100,0 100,0 100,0 E 26,50 60,45 10,00 / 2,05 / / 1,00 100,0 Гранульованою/iнкапсульованою сумішшю потім заповнювали тверді желатинові капсули: 40 11 UA 100843 C2 доза (мг) 20 розмір 4 Ковпачок Корпус 17.090 LT GREEN OP.C090 ІндІго кармін-FD&C Синій2 0,0170 % Діоксид титану 2,0000 % Жовтий оксид заліза 0,2500 % L500 WHITE діоксид титану 2,0000 % Желатин д.к. 100 % Желатин достатня кількість (д.к.) 100 % 40 60 80 5 10 15 20 3 2 1 18.385 DARK GREEN OP.C385 Індіго кармін-FD&C Синій 2 0,0890 % Діоксид титану 0,7418 % Жовтий оксид заліза 0,6120 % Желатин д.к. 100 % 18.385 DARK GREEN OP.C385 Індіго кармін-FD&C Синій 2 0,0890 % Діоксид титану 0,7418 % Жовтий оксид заліза 0,6120 % Желатин д.к. 100 % 17.090 LT GREEN OP.C090 Індіго кармін-FD&C Синій 2 0,0170 % Діоксид титану 2,0000 % Жовтий оксид заліза 0,2500 % Желатин д.к. 100 % 17.090 LT GREEN OP.C090 Індіго кармін-FD&C Синій 2 0,0170 % Діоксид титану 2,0000 % Жовтий оксид заліза 0,2500 % Желатин д.к. 100 % L500 WHITE діоксид тітану Желатин д.к. 2,0000 % 100 % L500 WHITE діоксид титану 2,0000 % Желатинд.к. 100 % Приклад 19 Приготування зіпразідона сульфату форми II До 2 г основи зіпразідона додавали 20 мл демінералізованої води. Температуру підвищували до 75-80 °C при перемішуванні. Потім через 15 хвилин в тих же умовах поволі додавали 0,62 г сірчаної кислоти (перемішування і підтримка температури на рівні 75-80 °C). Після додавання сірчаної кислоти температуру реакції зменшували до 60 °C і перемішували протягом наступних 3 годин. Потім суміш охолоджували до кімнатної температури, перемішували протягом 15 хвилин, фільтрували і промивали демінералізованою водою. Вологий продукт сушили в повітряній сушарці при температурі не більше 50 °C до досягнення постійної маси. Одержаний продукт характеризували за допомогою дифракції рентгенівських променів на порошку, що демонструє характеристичні кути дифракції 7,7; 12,4; 14,4; 15,5; 19,4; 20,1 і 27,1±0,2°тета. Приклад 20 Капсули, що містять подрібнений зіпразідона гідросульват дигідрат Зіпразідона гідросульват дигідрат, що має розмір частинок 64 мкм, 115 мкм і 100 мкм, подрібнювали на струменевому млині Hosokawa PK 57.01 (3000 об./хв) і одержували частинки розміром 13 мкм, 15 мкм і 18 мкм, відповідно. Капсули, що містять зіпразідона гідросульвату дигідрат, що мають склад, приведений в Прикладі 18, готували таким же способом, причому використовували подрібнений зіпразідона гідросульвату дигідрат, що має розмір частинок 13 мкм, 15 мкм і 18 мкм. ФОРМУЛА ВИНАХОДУ 25 1. Сполука формули І: + [зипразидон*Н]n [X]*ZН2О, де зипразидон є сполукою формули 12 UA 100843 C2 Cl NH O N S 5 10 15 20 25 30 N N , Н є воднем; n=1 або 2; 2 X є HSO4- або SO4 -; і Z>0,28 до 30, вказана сполука розчинна в діапазоні від приблизно 50 мл/л до приблизно 800 мл/л. 2. Сполука за п. 1, де Z>0,28 до 2. 3. Сполука за будь-яким з пп. 1, 2, яка відрізняється тим, що вказана сполука має розмір частинок, що знаходиться в діапазоні від приблизно 5 мкм до приблизно 300 мкм. 4. Сполука за п. 1, яка відрізняється тим, що характеризується картиною дифракції рентгенівських променів на порошку, що демонструє характеристичні кути дифракції при 8,6; 12,1; 13,6; 17,6; 19,8; 23,4 і 24,3°±0,2°-тета. 5. Сполука за п. 1, яка відрізняється тим, що характеризується картиною дифракції рентгенівських променів на порошку, що демонструє характеристичні кути дифракції при 4,5; 9,0; 15,6; 23,7; 25,0 і 26,6°±0,2°2-тета. 6. Спосіб одержання сполуки формули І, що включає стадії: одержання основи зипразидону; взаємодії з водою і сірчаною кислотою; можливо, охолодження і/або сушіння; одержання сполуки формули І. 7. Спосіб за п. 6, який відрізняється тим, що безводну основу зипразидону одержують шляхом реакції 6-хлор-5-(2-хлоретил)-1,3-дигідро-2Н-індол-2-ону і 3-(1-піперазиніл)-1,2-бензізотіазолу у присутності лужної сполуки і органічного розчинника, можливо, змішаного з водою. 8. Спосіб за п. 7, який відрізняється тим, що лужна сполука є Na2CO3. 9. Спосіб за п. 7, який відрізняється тим, що органічний розчинник є іонною рідиною. 10. Спосіб за п. 9, який відрізняється тим, що іонна рідина вибрана з групи 1-R-3-R1-імідазолу Н(+) х А(-), де R і R1 є нижчим алкілом, а А(-) є моно- або поліпротонний аніон кислоти. 11. Застосування сполуки за будь-яким з пп. 1-5 для одержання фармацевтичної композиції для профілактики і/або лікування психотичних станів. 12. Застосування за п. 11, яке відрізняється тим, що психотичні стани включають шизофренію і тривожні розлади. 13 UA 100843 C2 14 UA 100843 C2 15 UA 100843 C2 16 UA 100843 C2 17 UA 100843 C2 18 UA 100843 C2 19 UA 100843 C2 20 UA 100843 C2 21 UA 100843 C2 22 UA 100843 C2 23 UA 100843 C2 Комп’ютерна верстка А. Крижанівський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 24
ДивитисяДодаткова інформація
Назва патенту англійськоюPolymorphic forms of ziprasidone sulfates
Автори англійськоюZadnik Jernej, Hvalec Miran, Makuc Simon, Jursic Urska, Zajc, Natalija, Ruzic, Milos, Smrkolj, Matej, Pecavar, Anica, Stergar Matej
Назва патенту російськоюПолиморфные формы сульфатов зипразидона
Автори російськоюЗадник Юрней, Хвалец Миран, Макуц Симон, Ярсиц Юрска, Зайц Наталия, Рузиц Милош, Смрколь Матей, Пецавар Аница, Смрколь Матей
МПК / Мітки
МПК: C07D 275/04, A61K 31/427, C07D 417/12
Мітки: форми, поліморфні, зипразидону, сульфатів
Код посилання
<a href="https://ua.patents.su/26-100843-polimorfni-formi-sulfativ-ziprazidonu.html" target="_blank" rel="follow" title="База патентів України">Поліморфні форми сульфатів зипразидону</a>
Попередній патент: Спосіб деполімеризації поліорганосилоксанів
Наступний патент: Вагранка і спосіб одержанння кремнеземних розплавів
Випадковий патент: Спосіб визначення вмісту чорних і важких металів у порошкових пробах руд