Застосування інгібіторів dpp iv
Формула / Реферат
1. Застосування інгібітора DPP IV формули (І)
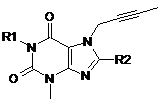 (I)
(I)
або формули (II)
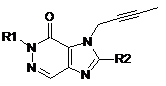 , (II)
, (II)
або однієї з його солей, де
R1 означає ([1,5]нафтиридин-2-іл)метил, (хіназолін-2-іл)метил, (хіноксалін-6-іл)метил, (4-метилхіназолін-2-іл)метил, 2-ціанобензил, (3-ціанохінолін-2-іл)метил, (3-ціанопіридин-2-іл)метил, (4-метилпіримідин-2-іл)метил або (4,6-диметилпіримідин-2-іл)метил,
R2 означає 3-(R)-амінопіперидин-1-іл, (2-аміно-2-метилпропіл)метиламіногрупу або (2-(S)-амінопропіл)метиламіногрупу,
для приготування лікарського засобу, призначеного для терапії пацієнта, у якого діагностовано фізіологічне функціональне порушення, вибране із групи, яка включає діабетичну стопу, діабетичну виразку, гестаційний діабет та адренергічний постпрандіальний синдром і серцеву недостатність, або для терапії пацієнта із трансплантованими панкреатичними острівцями або b-клітинами.
2. Застосування інгібітора DPP IV формули (І)
 (I)
(I)
або формули (II)
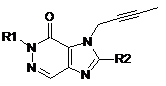 , (II)
, (II)
або однієї з його солей, де
R1 означає ([1,5]нафтиридин-2-іл)метил, (хіназолін-2-іл)метил, (хіноксалін-6-іл)метил, (4-метилхіназолін-2-іл)метил, 2-ціанобензил, (3-ціанохінолін-2-іл)метил, (3-ціанопіридин-2-іл)метил, (4-метилпіримідин-2-іл)метил або (4,6-диметилпіримідин-2-іл)метил, і
R2 означає 3-(R)-амінопіперидин-1-іл, (2-аміно-2-метилпропіл)метиламіногрупу або (2-(S)-амінопропіл)метиламіногрупу,
для приготування лікарського засобу, призначеного для терапії пацієнтів, у яких діагностовано явний діабет типу 2, де, застосовуючи вказаний лікарський засіб, зменшують існуючий незважаючи на лікування ризик погіршення глюкозного обміну, зменшують існуючий незважаючи на лікування ризик підвищення рівня гемоглобіну НbА1с, зменшують існуючий незважаючи на лікування ризик підвищення рівня глюкози натще, зменшують ризик виникнення необхідності в інсулінотерапії, зменшують ризик розвитку діабетичної стопи, зменшують ризик розвитку діабетичної виразки або зменшують ризик виникнення макроваскулярного ускладнення.
3. Застосування за п. 2, в якому макроваскулярне ускладнення вибране із групи, яка включає інфаркт міокарда, гострий коронарний синдром, нестабільну стенокардію, стабільну стенокардію, геморагічний або ішемічний інсульт, облітеруючий ендартеріїт, кардіоміопатію, лівошлуночкову недостатність, правошлуночкову недостатність, тотальну серцеву недостатність, порушення серцевого ритму і рестеноз судин.
4. Застосування за п. 1, в якому лікарський засіб призначений для терапії гестаційного діабету.
5. Застосування за п. 1, в якому лікарський засіб призначений для терапії адренергічного постпрандіального синдрому.
6. Застосування за п. 1, в якому лікарський засіб призначений для терапії серцевої недостатності.
7. Застосування за п. 2, в якому, застосовуючи вказаний лікарський засіб, зменшують ризик подальшого підвищення рівня гемоглобіну НbА1с, підвищення рівня глюкози натще й виникнення необхідності в інсулінотерапії.
8. Застосування за будь-яким з попередніх пунктів, де інгібітор DPP IV додатково комбінують з активною речовиною, вибраною з групи антидіабетичних засобів інших класів, з діючих речовин, які знижують рівень цукру в крові, з діючих речовин, які знижують рівень ліпідів у крові, з діючих речовин, які підвищують рівень ліпопротеїнів високої щільності (ЛВЩ) у крові, з діючих речовин, які знижують кров'яний тиск, і з діючих речовин, показаних при лікуванні атеросклерозу або ожиріння.
9. Застосування за п. 8, де інгібітор DPP IV додатково комбінують з антидіабетичним засобом іншого класу або діючою речовиною, яка знижує кров'яний тиск.
10. Застосування за п. 9, де інгібітор DPP IV додатково комбінують з метформіном, піоглітазоном, міглітолом, аторвастатином, метопрололом, амлодипіном, раміприлом, валсартаном або телмісартаном.
11. Застосування інгібітора DPP IV формули (І)
 (I)
(I)
або формули (II)
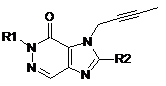 , (II)
, (II)
або однієї з його солей, де
R1 означає ([1,5]нафтиридин-2-іл)метил, (хіназолін-2-іл)метил, (хіноксалін-6-іл)метил, (4-метилхіназолін-2-іл)метил, 2-ціанобензил, (3-ціанохінолін-2-іл)метил, (3-ціанопіридин-2-іл)метил, (4-метилпіримідин-2-іл)метил або (4,6-диметилпіримідин-2-іл)метил, а
R2 означає 3-(R)-амінопіперидин-1-іл, (2-аміно-2-метилпропіл)метиламіногрупу або (2-(S)-амінопропіл)метиламіногрупу,
у дозі 0,5-50 мг для перорального введення,
для приготування лікарської комбінації з діючою речовиною, вибраною із групи антидіабетичних засобів інших класів, з діючими речовинами, які знижують рівень цукру в крові, з діючими речовинами, які знижують рівень ліпідів у крові, з діючими речовинами, які підвищують рівень ліпопротеїнів високої щільності (ЛВЩ) у крові, з діючими речовинами, які знижують кров'яний тиск, і з діючими речовинами, показаними при лікуванні атеросклерозу або ожиріння.
12. Застосування за п. 11, де доза інгібітора DPP IV при пероральному введенні становить від 2,5 до 50 мг, краще від 0,5 до 10 мг (як, наприклад, 0,5 мг, 1 мг, 2,5 мг, 5 мг або 10 мг).
13. Застосування за п. 11, де лікарську комбінацію готують з інгібітора DPP IV і антидіабетичного засобу іншого класу або діючої речовини, яка знижує кров'яний тиск.
14. Застосування за п. 11, де лікарську комбінацію готують з інгібітора DPP IV і метформіну, піоглітазону, міглітолу, аторвастатину, метопрололу, амлодипіну, раміприлу, валсартану або телмісартану.
15. Застосування за п. 11, де лікарську комбінацію готують з інгібітора DPP IV і метформіну, піоглітазону, міглітолу, аторвастатину, валсартану або телмісартану.
16. Застосування за п. 11, де лікарська комбінація призначена для терапії пацієнта, у якого діагностовано фізіологічне функціональне порушення, вибране із групи, яка включає діабетичну стопу, діабетичну виразку, гестаційний діабет, адренергічний постпрандіальний синдром і серцеву недостатність.
17. Застосування за п. 11, де лікарська комбінація призначена для терапії пацієнта, у якого діагностовано явний діабет типу 2, яке відрізняється тим, що, застосовуючи вказану лікарську комбінацію, зменшують існуючий незважаючи на лікування ризик погіршення глюкозного обміну, зменшують існуючий незважаючи на лікування ризик підвищення рівня гемоглобіну НbА1с, зменшують існуючий незважаючи на лікування ризик підвищення рівня глюкози натще, зменшують ризик виникнення необхідності в інсулінотерапії, зменшують ризик розвитку діабетичної стопи, зменшують ризик розвитку діабетичної виразки або зменшують ризик виникнення макроваскулярного ускладнення.
18. Застосування за п. 17, де макроваскулярне ускладнення вибране із групи, яка включає інфаркт міокарда, гострий коронарний синдром, нестабільну стенокардію, стабільну стенокардію, геморагічний або ішемічний інсульт, облітеруючий ендартеріїт, кардіоміопатію, лівошлуночкову недостатність, правошлуночкову недостатність, тотальну серцеву недостатність, порушення серцевого ритму й рестеноз судин.
19. Застосування інгібітора DPPIV за п. 11, для приготування лікарського засобу, призначеного для лікування переддіабету або діабету типу 2, де інгібітор DPP IV комбінують з метформіном або глітазоном, або тіазолідиндіоном (наприклад, піоглітазоном).
20. Застосування за будь-яким з попередніх пунктів, де інгібітор DPPIV вибирають з групи, що складається з
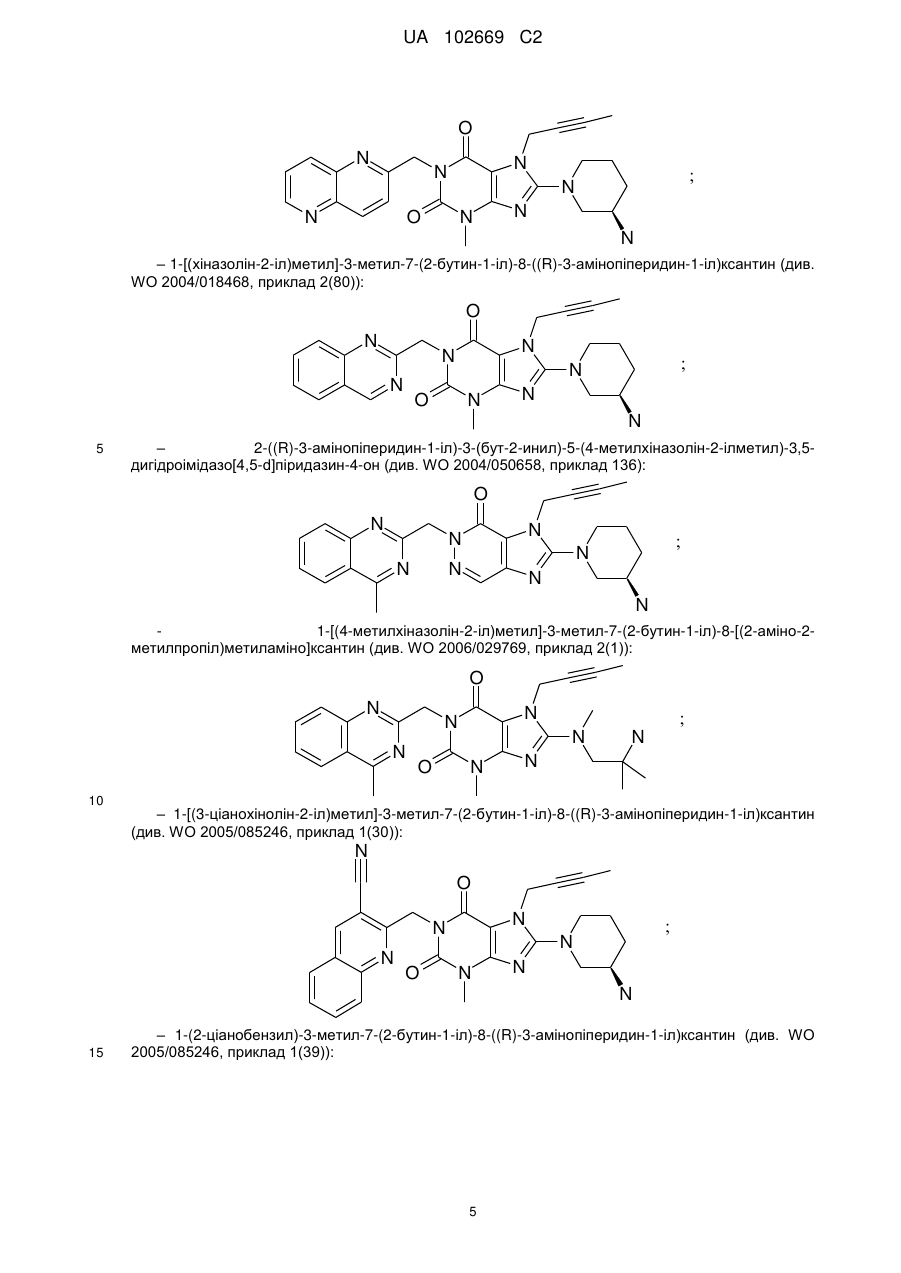
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину,
1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-иніл)-5-(4-метилхіназолін-2-ілметил)-3,5-дигідроімідазо[4,5-d]піридазин-4-ону,
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2-метилпропіл)метиламіно]ксантину,
1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-(2-ціанобензил)-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
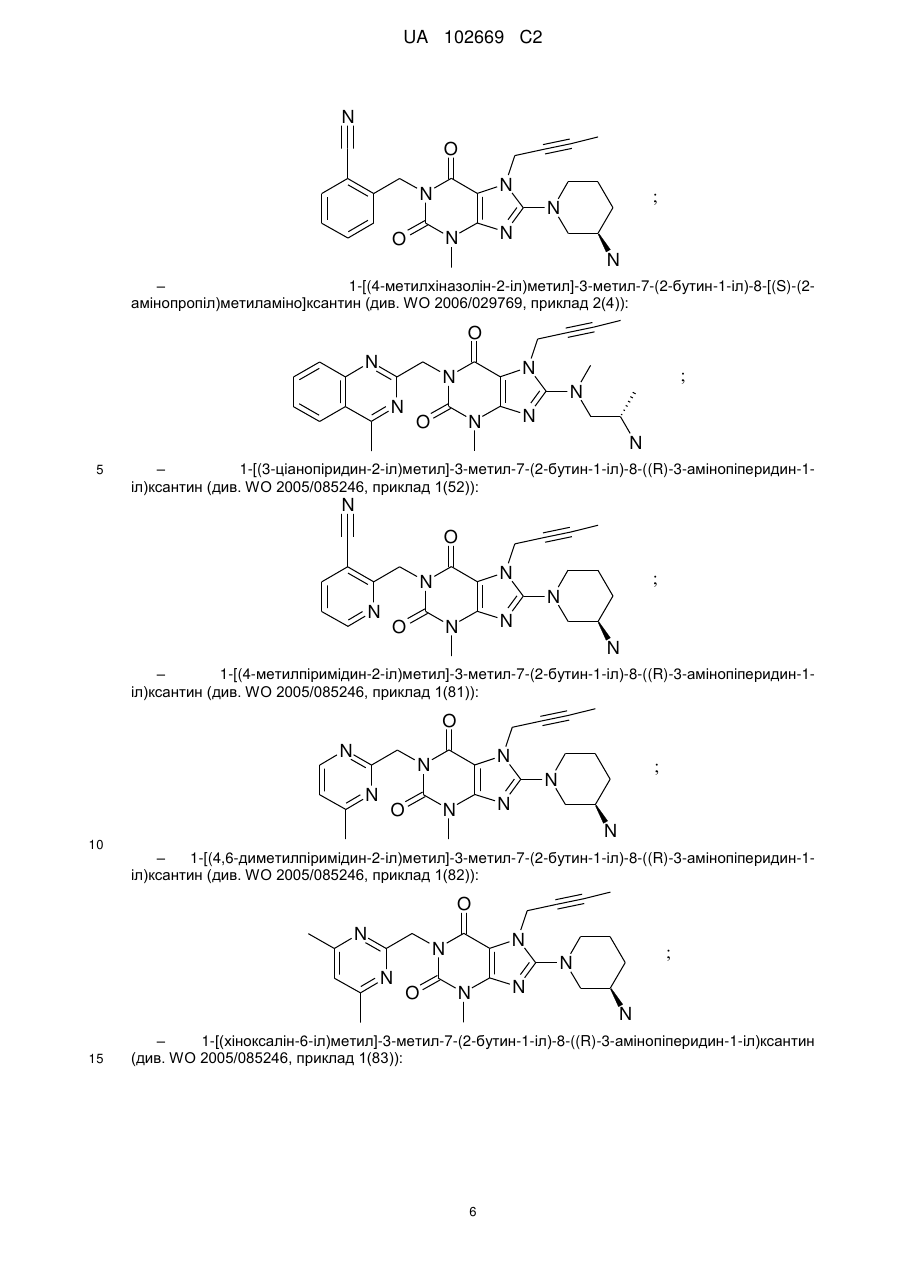
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S)-(2-амінопропіл)метиламіно]ксантину,
1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину та
1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
або його терапевтично активної солі.
21. Застосування інгібітора DPP IV для приготування лікарського засобу, призначеного для комбінованого лікування з метформіном, де інгібітор DPP IV має формулу І
 (I)
(I)
або являє собою одну із солей цієї сполуки, де
R1 означає (4-метилхіназолін-2-іл)метил, та
R2 означає 3-(R)-амінопіперидин-1-іл.
22. Застосування інгібітора DPP IV для приготування лікарського засобу, призначеного для комбінованого лікування з глітазоном або тіазолідиндіоном (наприклад, піоглітазоном), де інгібітор DPP IV має формулу І
 (I)
(I)
або являє собою одну із солей цієї сполуки, де
R1 означає (4-метилхіназолін-2-іл)метил, та
R2 означає 3-(R)-амінопіперидин-1-іл.
23. Застосування інгібітора DPP IV для приготування лікарського засобу, призначеного для комбінованого лікування з телмісартаном, де інгібітор DPP IV має формулу І
 (I)
(I)
або являє собою одну із солей цієї сполуки, де
R1 означає (4-метилхіназолін-2-іл)метил, та
R2 означає 3-(R)-амінопіперидин-1-іл.
24. Застосування інгібітора DPP IV, який вибирають з групи, що складається з
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину,
1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-иніл)-5-(4-метилхіназолін-2-ілметил)-3,5-дигідроімідазо[4,5-d]піридазин-4-ону,
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2-метилпропіл)метиламіно]ксантину,
1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-(2-ціанобензил)-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S)-(2-амінопропіл)метиламіно]ксантину,
1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
або його терапевтично активної солі,
в дозі від 0,5 до 50 мг при пероральному введенні, для приготування лікарського засобу, призначеного для лікування переддіабету або діабету типу 2, де інгібітор DPP IV комбінують з метформіном або глітазоном, або тіазолідиндіоном (наприклад, піоглітазоном), у вигляді вільної комбінації або у вигляді фіксованої комбінації, у складі таблетки.
25. Застосування за п. 24, де доза інгібітора DPP IV при пероральному введенні становить від 2,5 до 50 мг, краще від 0,5 до 10 мг (як, наприклад, 0,5 мг, 1 мг, 2,5 мг, 5 мг або 10 мг).
26. Застосування за будь-яким з пп. 21-25, де комбіноване лікування проводять у вигляді вільної комбінації.
27. Застосування за будь-яким з пп. 21-25, де комбіноване лікування проводять у вигляді фіксованої комбінації, наприклад, у складі таблетки або капсули.
28. Застосування інгібітора DPP IV, який вибирають з групи, що складається з
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину,
1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-иніл)-5-(4-метилхіназолін-2-ілметил)-3,5-дигідроімідазо[4,5-d]піридазин-4-ону,
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2-метилпропіл)метиламіно]ксантину,
1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-(2-ціанобензил)-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S)-(2-амінопропіл)метиламіно]ксантину,
1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
або його терапевтично активної солі,
для приготування лікарського засобу для попередження або зниження ризику виникнення макроваскулярного ускладнення у пацієнтів із діабетом типу 2 або з переддіабетом.
29. Застосування за п. 28, де макроваскулярне ускладнення вибране із групи, яка включає інфаркт міокарда, гострий коронарний синдром, нестабільну стенокардію, стабільну стенокардію, удар, облітеруючий ендартеріїт, кардіоміопатію, серцеву недостатність, порушення серцевого ритму й рестеноз судин.
30. Застосування за п. 28, де лікарський засіб з інгібітором DPP IV комбінують з діючою речовиною, вибраною із групи антидіабетичних засобів інших класів, з діючих речовин, які знижують рівень цукру в крові, з діючих речовин, які знижують рівень ліпідів у крові, з діючих речовин, які підвищують рівень ліпопротеїнів високої щільності (ЛВЩ) у крові, з діючих речовин, які знижують кров'яний тиск, і з діючих речовин, показаних при лікуванні атеросклерозу або ожиріння.
31. Застосування за п. 30, де лікарський засіб з інгібітором DPP IV комбінують з антидіабетичним засобом іншого класу або діючою речовиною, яка знижує кров'яний тиск.
32. Застосування за п. 30, де лікарський засіб з інгібітором DPP IV комбінують з метформіном, піоглітазоном, міглітолом, аторвастатином, метопрололом, амлодипіном, раміприлом, валсартаном або телмісартаном.
33. Застосування інгібітора DPP IV, який вибирають з групи, що складається з
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину,
1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-иніл)-5-(4-метилхіназолін-2-ілметил)-3,5-дигідроімідазо[4,5-d]піридазин-4-ону,
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2-метилпропіл)метиламіно]ксантину,
1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-(2-ціанобензил)-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S)-(2-амінопропіл)метиламіно]ксантину,
1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину та
1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
або його терапевтично активної солі,
в дозі від 0,5 до 50 мг при пероральному введенні, краще від 2,5 до 50 мг, особливо краще від 0,5 до 10 мг (як, наприклад, 0,5 мг, 1 мг, 2,5 мг, 5 мг або 10 мг), для приготування лікарського засобу, призначеного для лікування діабету типу 2.
34. Застосування інгібітора DPP IV, який вибирають з групи, що складається з
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину,
1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-иніл)-5-(4-метилхіназолін-2-ілметил)-3,5-дигідроімідазо[4,5-d]піридазин-4-ону,
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2-метилпропіл)метиламіно]ксантину,
1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-(2-ціанобензил)-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S)-(2-амінопропіл)метиламіно]ксантину,
1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину та
1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину,
або його терапевтично активної солі,
краще в дозі від 0,5 до 50 мг при пероральному введенні, краще від 2,5 до 50 мг, особливо краще від 0,5 до 10 мг (як, наприклад, 0,5 мг, 1 мг, 2,5 мг, 5 мг або 10 мг),
для приготування лікарського засобу, призначеного для лікування пацієнта з діабетом типу 2 або переддіабетом, або з метаболічним синдромом, де інгібітор DPP IV комбінують з інгібітором АСЕ (наприклад, з дозою раміприлу, що становить від 2,5 до 15 мг), антагоністом рецептора AT1 (наприклад, з дозою телмісартану, що становить від 20 до 160 мг), блокатором b-рецепторів (наприклад, з дозою метопрололу, що становить від 50 до 200 мг) або сечогінним засобом (наприклад, з дозою гідрохлортіазиду, що становить від 12,5 до 25 мг), у вигляді вільної комбінації або у вигляді фіксованої комбінації, у складі таблетки.
Текст
Реферат: Винахід стосується застосування інгібітора DPP IV формули (І) O R1 N N O R2 N N (I) або формули (II) O R1 N N N R2 N , (II) або однієї з його солей, для виробництва лікарського засобу, призначеного для лікування фізіологічних функціональних порушень, а також для зниження ризику виникнення таких UA 102669 C2 (12) UA 102669 C2 фізіологічних функціональних порушень у пацієнтів відповідних груп ризику, а також застосування вказаних інгібіторів DPP IV в комбінації з діючими речовинами інших класів, що дозволяє домогтися переважних результатів при лікуванні подібних фізіологічних функціональних порушень. UA 102669 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід стосується застосування вибраних інгібіторів DPP IV для лікування фізіологічних функціональних порушень, а також для зниження ризику виникнення таких фізіологічних функціональних порушень у пацієнтів відповідних груп ризику. Винахід також стосується застосування вказаних інгібіторів DPP IV у сполученні з діючими речовинами інших класів, що дозволяє домогтися переважних результатів при лікуванні подібних фізіологічних функціональних порушень. Для подібного застосування інгібіторів DPP IV на їх основі можна готувати відповідні лікарські засоби. Фермент DPP IV (дипептидилпептидаза IV), відомий також за назвою CD26, являє собою серинпротеазу, що сприяє відщепленню дипептидів у білків із проліновим або аланіновим залишком на N-кінці. Тим самим інгібітори DPP IV впливають на рівень біоактивних пептидів, включаючи пептид GLP-1, у плазмі крові й вважаються багатообіцяючими молекулами при лікуванні цукрового діабету. Віднесений до аутоімунних захворювань цукровий діабет типу 1 зустрічається переважно в молодих людей у віці до 30-ти років. При цьому при відповідній генетичній схильності під впливом різних факторів розвивається інсуліт з наступним руйнуванням B-клітин, у результаті чого підшлункова залоза стає здатна виробляти інсулін лише в істотно менших кількостях або навіть повністю перестає виробляти його. Цукровий же діабет типу 2 не розглядається як аутоімунне захворювання й проявляється в тому, що рівень цукру в крові натще перевищує 125 мг глюкози на дл плазми, при цьому визначення глюкози в крові є стандартним методом аналізу в повсякденній медичній практиці. Підстави підозрювати в пацієнта переддіабет (переддіабетичний стан) можна в тому випадку, коли рівень цукру в крові натще перевищує максимальне нормальне значення, що дорівнює 99 мг глюкози на дл плазми, але не перевищує релевантного для діабету граничного значення, рівного 125 мг глюкози на дл плазми. У цьому випадку говорять також про патологічно підвищений вміст глюкози натще ("порушений рівень глюкози натще" (англ. "impaired fasting glucose")). Іншою ознакою, що вказує на переддіабетичний стан, є порушена толерантність до глюкози, тобто стан, при якому при проведенні проби на толерантність до глюкози її рівень у крові через 2 години після прийому натще 75 г глюкози становить від 140 до 199 мг на дл плазми. У хворого на діабет через 2 години після прийому натще 75 г глюкози рівень цукру в крові, який визначає пробій на толерантність до глюкози, перевищує 199 мг глюкози на дл плазми. При проведенні проби на толерантність до глюкози досліджуваному після голодування протягом 10-12 год. дають прийняти перорально 75 г глюкози й відразу ж після прийому глюкози, а також через 1 год., відповідно через 2 год. після прийому глюкози визначають рівень цукру в крові. У здорової людини рівень цукру в крові перед прийомом глюкози повинен знаходитися в межах від 60 до 99 мг на дл плазми, через годину після прийому глюкози повинен бути нижче 200 мг на дл плазми, а після закінчення 2 годин після прийому глюкози повинен бути нижче 140 мг на дл плазми. Вміст же цукру в крові після закінчення 2 годин після прийому глюкози на рівні від 140 до 199 мг свідчить також про порушену толерантність до глюкози або іноді про непереносимість глюкози. При терапевтичному контролі за цукровим діабетом першорядне значення має рівень гемоглобіну HbА1c у крові, що представляє собою продукт неферментативного глікозилування (глікування) β-ланцюга гемоглобіну. Гемоглобін HbА1c, оскільки його утворення в основному залежить від рівня цукру в крові й часі життя еритроцитів, за типом "пам'яті", що зберігає інформацію про рівень цукру в крові, відбиває середнє його значення за минулі 4-12 тижнів. Пацієнти, що страждають від діабету, у яких вміст гемоглобіну HbА1c у крові за рахунок інтенсифікованої терапії діабету довгостроково підтримується на прийнятному рівні (тобто нижче 6,5 % від загального гемоглобіну в зразку крові), набагато переважне захищені від діабетичної мікроангіопатії. У хворого на діабет концентрацію гемоглобіну HbА1c можна існуючими методами лікування діабету знижувати в середньому на величину порядку 1,0-1,5 %. Однак подібного зниження концентрації гемоглобіну HbА1c виявляється достатнім не для всіх хворих діабетом для зменшення в них рівня гемоглобіну HbА1c до необхідних значень, що лежать нижче 6,5 %, переважно нижче 6 %. Найбільш показовою ознакою, що вказує на наявність комплексного порушення обміну речовин - переддіабету, є можливість виявлення в пацієнта інсулінорезистентності. Слід зазначити, що перевищення потребою однієї людини в інсуліні для підтримання її глюкозного гомеостазу в 2-3 рази потреби іншої людини в інсуліні може не бути прямою вказівкою на наявність патологічного стану. Найбільш інформативним методом виявлення інсулінорезистентності є гіперінсулінемічний еуглікемічний "клемп"-тест (гіперінсулінемічне еуглікемічне навантаження). Цим методом визначають відношення концентрації інсуліну в крові 1 UA 102669 C2 5 10 15 20 25 30 35 40 45 50 55 до концентрації глюкози в крові при комбінованої тривалої інфузії інсуліну одночасно із глюкозою. Про інсулінорезистентність можна говорити в тому випадку, коли ступінь поглинання (засвоєння) глюкози лежить нижче 25-го процентиля від фонової популяції, що досліджувалася (відповідно до визначення ВООЗ). Трохи менш складними в порівнянні з дослідженням "клемп"методом є так звані мінімальні моделі, при використанні яких у ході внутрішньовенної проби на толерантність до глюкози через задані часові інтервали вимірюють концентрації інсуліну й глюкози в крові й на основі отриманих даних оцінюють інсулінорезистентність. Іншим методом виявлення інсулінорезистентності є математична модель HOMA (від англ. "Homeostasis Model Assesment", модельна оцінка гомеостазу). У цьому випадку інсулінорезистентність оцінюють за концентрацією глюкози й інсуліну в плазмі натще. Однак цей метод не дозволяє відрізнити печінкову інсулінорезистентність від периферичної. У повсякденній практиці всі ці методи мало придатні для оцінки інсулінорезистентності. У повсякденній клінічній практиці для оцінки інсулінорезистентності звичайно використовують інші параметри. Переважно для цього використовувати, наприклад, метод, заснований на визначенні концентрації тригліцеридів у крові пацієнта, оскільки між підвищеним рівнем тригліцеридів і наявністю інсулінорезистентності існує значима кореляція. На практиці використовують трохи спрощений підхід, відповідно до якого виходять із того, що про інсулінорезистентність в людини можна говорити при наявності принаймні двох наступних ознак: 1) наявність надлишкової ваги або ожиріння, 2) наявність підвищеного кров'яного тиску, 3) наявність дисліпідемії (зміненого загального вмісту ліпідів у крові), 4) наявність принаймні одного родича першого ступеня з діагностованою порушеною толерантністю до глюкози або діабетом типу 2. Про надлишкову вагу говорять при цьому в тому випадку, коли індекс (або показник) маси тіла (ІМТ), що розраховується як відношення виміряної в кілограмах маси тіла до піднесеного у 2 квадрат росту в метрах, становить від 25 до 30 кг/м . При явному ожирінні ІМТ перевищує 2 30 кг/м . З наведеного вище визначення інсулінорезистентності з усією очевидністю безпосередньо можна зробити висновок, що для його лікування засоби, які знижують кров'яний тиск, (гіпотензивні) придатні й показані в тому випадку, коли в пацієнта виявлений, зокрема, така ознака, як підвищений кров'яний тиск. Аналогічним чином всі підстави підозрювати в людини переддіабетичний стан можна й при наявності умов, що вказують на наявність метаболічного синдрому, основною ознакою якого є інсулінорезистентність. Відповідно до директив ATP IHINCEP [Executive Summary of the Third Report of the National Cholesterol Education Program (NCEP) в Journal of the American Medical Association 285, 2001, стор. 2486-2497] про метаболічному синдром у пацієнта говорять при наявність принаймні трьох наступних ознак: 1) наявність ожиріння нижньої частини тулуба, коли в чоловіків об'єм (окружність) талії перевищує 40 дюймів або 102 см, а в жінок перевищує 35 дюймів або 94 см, 2) наявність підвищеного рівня тригліцеридів у крові, що становить більше 150 мг/дл, 3) наявність у чоловіків зниженого рівня вхідного до складу ліпопротеїнів високої щільності (ЛВЩ) холестерину, що становить менш 40 мг/дл, 4) наявність підвищеного кров'яного тиску, коли систолічний тиск перевищує 130, а діастолічний - 85 мм рт.ст., 5) наявність підвищеного рівня цукру в крові натще, що становитьбільше 110 мг/дл. З наведеного вище визначення метаболічного синдрому з усією очевидністю безпосередньо можна зробити висновок, що для його лікування гіпотензивні засоби придатні й показані в тому випадку, коли в пацієнта виявлено, зокрема, підвищений кров'яний тиск. Підстави припускати наявність переддіабетичного стану є й у тому випадку, коли концентрація тригліцеридів у крові перевищує 150 мг/дл. Подібна підозра підсилюється при низькому рівні вхідні до складу ЛВЩ холестерину в крові. У жінок за низький рівень вхідні до складу ЛВЩ холестерину (ЛВЩ-холестерину) вважається рівень нижче 55 мг на дл плазми, а в чоловіків - нижче 45 мг на дл плазми. Метод визначення рівня тригліцеридів і ЛВЩ-холестерину в крові також стосується стандартних методів аналізу в медицині й описаний, наприклад, в Thomas L. (ред.) в "Labor und Diagnose", вид-во TH-Books Verlagsgesellschaft mbН, Frankfurt/Main, 2000. Підозра на наявність переддіабетичного стану додатково підсилюється в тому випадку, коли рівень цукру в крові натще одночасно перевищує 99 мг глюкози на дл плазми. 2 UA 102669 C2 5 10 15 20 25 30 35 40 45 50 55 Гестаційним діабетом (діабетом вагітних) називають форму цукрової хвороби, що виникає під час вагітності й звичайно знову припиняється безпосередньо після пологів. Гестаційний діабет діагностують шляхом скринінг-дослідження, проведеного в період між 24-м і 28-м тижнями вагітності. Мова при цьому переважно йде про простий скринінг-тест, при якому через одну годину після введення 50 г розчину глюкози визначають рівень цукру в крові. Якщо цей вимірюваний через 1 год. після введення глюкози показник перевищує 140 мг/дл, то існує підозра на наявність гестаційного діабету. Для остаточної постановки діагнозу можна проводити стандартну пробу на толерантність до глюкози із прийомом 75 г глюкози. Гіперглікемія являє собою функціональне порушення, для якого характерний занадто високий рівень глюкози в крові, а саме: або в стані натще (вміст глюкози в крові підвищено до значень в інтервалі від 100 до 125 мг/дл, відповідно при діабетичній гіперглікемії перевищує 125 мг/дл при нормальному рівні, що становить менше 100 мг/дл), або в стані не натще (вміст глюкози в крові перевищує 180 мг/дл). Під адренергічним постпрандіальним синдромом (реактивною гіпоглікемією) у медицині мається на увазі функціональне порушення, при якому непропорційно високий рівень інсуліну в крові приводить до зниження рівня цукру в крові (гіпоглікемія) через диспропорцію між вуглеводами, які швидко розпадаються, і високим рівнем інсуліну в крові, який більш довгостроково зберігається після прийому їжі. Діабетичною стопою називають ураження стоп внаслідок цукрового діабету, першопричиною якого є поліневропатія, обумовлена недостатньою регуляцією обміну речовин. Діабетичну стопу діагностують за появою на стопі типових уражень (наприклад, виразок) при існуючому цукровому діабеті. Діабетичною виразкою називають виразковий запальний дефект шкіри у хворого на цукровий діабет. Діабетичну виразку діагностують на підставі типового анамнезу й обстеження тіла (наприклад, огляду стоп). Про діабетичну гіперліпідемію говорять у тому випадку, коли у хворого на цукровий діабет виявлений підвищений рівень загального холестерину або, що більш типово при діабетичній гіперліпідемії, підвищений рівень тригліцеридів у плазмі з одночасним зниженням рівня ЛВЩхолестерину або без такого зниження. Про діабетичну дисліпідемію говорять у тому випадку, коли рівень загального холестерину не підвищений, однак змінений розподіл холестерину, що входить до складу ліпопротеїнів високої щільності (ЛВЩ-холестерину) і холестерину, що входить до складу ліпопротеїнів низької щільності (ЛНП-холестерину), тобто коли в пацієнта виявлений занадто низький рівень ЛВЩхолестерину (наприклад, менше 55 мг/дл для жінок і менше 45 мг/дл для чоловіків). Про серцеву недостатність говорять у тому випадку, коли або суб'єктивні симптоми, або об'єктивного даного обстеження вказують на нездатність серця забезпечувати необхідний викид крові. Як приклад суб'єктивних симптомів можна назвати задишку при навантаженні або в спокої. До об'єктивних даних обстеження належать, наприклад, знижений серцевий викид при ультразвуковому дослідженні (знижена фракція вигнання), застій у легенях, що виявляється при рентгенологічному дослідженні, та/або скорочена дистанція при ходьбі. Деякі вибрані інгібітори DPP IV особливо придатні для приготування лікарського засобу, призначеного для терапії пацієнтів, у яких діагностовано медичне, відповідно фізіологічне функціональне порушення, вибране із групи, яка включає переддіабет, непереносимість глюкози (порушена толерантність до глюкози (англ. "impaired glucose tolerance")), патологічно підвищений вміст глюкози натще (порушений рівень глюкози натще), діабетичну стопу, діабетичну виразку, діабетичну гіперліпідемію, діабетичну дисліпідемію, знову діагностований діабет типу 1 (для збереження залишкової секреції інсуліну підшлунковою залозою), гестаційний діабет (діабет вагітних), гіперглікемію, адренергічний постпрандіальний синдром (реактивну гіпоглікемію) і серцеву недостатність. Такі лікарські засоби можна також використовувати для зменшення ризику погіршення глюкозного обміну, що існує незважаючи на лікування, ризику підвищення рівня гемоглобіну HbА1c, що існує незважаючи на лікування, ризику підвищення рівня глюкози натще, що існує незважаючи на лікування, ризику прояву діабету типу 2, що існує незважаючи на лікування, ризику розвитку діабетичної стопи, що існує незважаючи на лікування, ризику розвитку діабетичної виразки, що існує незважаючи на лікування, ризику розвитку діабетичної гіперліпідемії, що існує незважаючи на лікування або ризику розвитку діабетичної дисліпідемії, що існує незважаючи на лікування, для зменшення існуючого незважаючи на лікування ризику виникнення необхідності в інсулінотерапії або для зниження ризику виникнення макроваскулярних ускладнень. 3 UA 102669 C2 5 10 15 20 Як приклади подібних макроваскулярних ускладнень можна назвати інфаркт міокарда, гострий коронарний синдром, нестабільну стенокардію, стабільну стенокардію, геморагічний або ішемічний інсульт, облітеруючий ендартеріїт, кардіоміопатію, лівошлуночкову недостатність, правошлуночкову недостатність, тотальну серцеву недостатність, порушення серцевого ритму й рестеноз судин. Всі такі макроваскулярні ускладнення відомі фахівцям у даній галузі й докладно описані в широко розповсюджених підручниках. Крім цього після трансплантації панкреатичних острівців (острівців Лангенгранса) або βклітин (базофільних інсулоцитів) такі речовини можуть використовуватися для підвищення життєздатності й посилення секреторної здатності клітин і тим самим для забезпечення сприятливого перебігу посттрансплантаційних процесів. Поряд із цим подібні речовини можуть також використовуватися на стадії виділення й трансплантації панкреатичних острівців або βклітин, для чого такі речовини додають у звичайне середовище для виділення або зберігання панкреатичних острівців або β-клітин у прийнятній концентрації, що становить від 1 нмоля/л до 1 мкмоля/л, переважно в концентрації від 1 до 100 нмолів/л. Таким шляхом вдається підвищити якість трансплантованого матеріалу. Якість трансплантованого матеріалу підвищується насамперед при додаванні інгібіторів DPP IV у сполученні з пептидом GLP-1 (глюкагоноподібний пептид 1), переважно в концентрації від 1 до 100 нмолів/л. Відповідні середовища для виділення або зберігання панкреатичних острівців або β-клітин, а також відповідні методи підвищення їх життєздатності й посилення їх секреторної здатності шляхом додавання інгібіторів DPP IV до використовуваних середовищ є наступним об'єктом винаходу. Вказані інгібітори придатні далі для лікування різних форм артриту, але насамперед ревматоїдного артриту. Згідно із даним винаходом вибрані інгібітори DPP IV можна представити структурною формулою (I) O R1 (I) R2 N N O 25 N N або структурною формулою (II) O R1 R2 N 30 35 (II), N N N де R1 означає ([1,5]нафтиридин-2-іл)метил, (хіназолін-2-іл)метил, (хіноксалін-6-іл)метил, (4метилхіназолін-2-іл)метил, 2-ціанобензил, (3-ціанохінолін-2-іл)метил, (3-ціанопіридин-2іл)метил, (4-метил-піримідин-2-іл)метил або (4,6-диметилпіримідин-2-іл)метил, а R2 означає 3(R)-амінопіперидин-1-іл, (2-аміно-2-метилпропіл)метиламіногрупу або (2-(S)амінопропіл)метиламіногрупу. До особливо переважних інгібіторів DPP IV належать наступні сполуки і їх терапевтично ефективні солі: – 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1іл)ксантин (див. WO 2004/018468, приклад 2(142): O N N N N O ; N N N N – 1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1іл)ксантин (див. WO 2004/018468, приклад 2(252)): 4 UA 102669 C2 O N N N N ; N N N O N – 1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантин (див. WO 2004/018468, приклад 2(80)): O N N N N ; N N O N N 5 – 2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-инил)-5-(4-метилхіназолін-2-ілметил)-3,5дигідроімідазо[4,5-d]піридазин-4-он (див. WO 2004/050658, приклад 136): O N N N N ; N N N N 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2метилпропіл)метиламіно]ксантин (див. WO 2006/029769, приклад 2(1)): O N N 10 N N N O ; N N N – 1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантин (див. WO 2005/085246, приклад 1(30)): N O N N N O ; N N N N 15 – 1-(2-ціанобензил)-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантин (див. WO 2005/085246, приклад 1(39)): 5 UA 102669 C2 N O N N ; N N N O N – 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S)-(2амінопропіл)метиламіно]ксантин (див. WO 2006/029769, приклад 2(4)): O N N N N ; N N N O N 5 – 1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1іл)ксантин (див. WO 2005/085246, приклад 1(52)): N O N N N ; N N N O N – 1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1іл)ксантин (див. WO 2005/085246, приклад 1(81)): O N N 10 N N N N O ; N N – 1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1іл)ксантин (див. WO 2005/085246, приклад 1(82)): O N N N N O ; N N N N 15 – 1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантин (див. WO 2005/085246, приклад 1(83)): 6 UA 102669 C2 O N N N N O . N N N N 5 10 15 20 25 30 35 40 45 50 Ці інгібітори DPP IV перевершують структурно порівнянні з ними інгібітори DPP IV, оскільки вони мають винятково високу ефективність і тривалість дії в сполученні з оптимальними фармакологічними властивостями, здатністю селективно зв'язуватися з відповідними рецепторами й оптимальним профілем побічних дій або при застосуванні в комбінація з іншими фармацевтичними діючими речовинами, дозволяючи домогтися несподіваних переваг або поліпшень у терапії. Одержання таких інгібіторів DPP IV описано в вказаних публікаціях. Оскільки різні метаболічні функціональні порушення часто виникають одночасно, нерідко представляється доцільним комбінувати між собою декілька різних механізмів дії. Так, зокрема, залежно від діагностованих функціональних порушень домогтися переважних результатів у їх лікуванні можна, використовуючи інгібітор DPP IV у комбінації з діючою речовиною іншого типу, вибраним із групи антидіабетичних засобів інших класів, насамперед із групи діючих речовин, які знижують рівень цукру або ліпідів у крові, які підвищують рівень ЛВЩ у крові, які знижують кров'яний тиск або показаних при лікуванні атеросклерозу або ожиріння. Для досягнення необхідної дії інгібітори DPP IV доцільно вводити в організм від 1 до 4 разів на день у дозі, яка при внутрішньовенному введенні становить від 0,1 до 10 мг, переважно від 0,25 до 5 мг, а при пероральному введенні становить від 0,5 до 100 мг, переважно від 2,5 до 50 мг. Із цією метою інгібітори DPP IV, необов'язково в сполученні з діючою речовиною іншого типу, переробляють разом з одним або декількома звичайними інертними носіями та/або розріджувачами, наприклад, з кукурудзяним крохмалем, лактозою, тростинним цукром, мікрокристалічною целюлозою, стеаратом магнію, полівінілпіролідоном, лимонною кислотою, винною кислотою, водою, водою/етанолом, водою/гліцерином, водою/сорбітом, водою/поліетиленгліколем, пропіленгліколем, цетилстеариловим спиртом, карбоксиметилцелюлозою або жировмісними речовинами, такими як отверділий жир, або їх прийнятними сумішами, у звичайні галенові форми, такі як таблетки, драже, капсули, порошки, суспензії або супозиторії. Лікарські форми із застосовуваними відповідно до винаходу інгібіторами DPP IV виготовляють, таким чином, з використанням допущених до застосування в технології приготування лікарських засобів допоміжних речовин за методами, описаними у рівні техніці. Як приклад подібних допоміжних речовин можна назвати розріджувачі, сполучні, носії, наповнювачі, ковзаючі речовини, засоби, які сприяють розтіканню, інгібітори кристалізації, розпушувачі, гідротропні солюбілізатори, барвники, регулятори pН, поверхнево-активні речовини й емульгатори. Як приклад придатних для застосування в технології приготування лікарських засобів розріджувачів можна назвати порошкову целюлозу, гідрофосфат кальцію, еритрит, гідроксипропілцелюлозу (з низьким ступенем заміщення), маніт, попередньо желатинізований крохмаль або ксиліт. Як приклад придатних для застосування в технології приготування лікарських засобів сполучних можна назвати співполімери вінілпіролідону з іншими похідними вінілу (коповідон), гідроксипропілметилцелюлозу (ГПМЦ), гідроксипропілцелюлозу (ГПЦ) полівінілпіролідон (повідон), попередньо желатинізований крохмаль або гідроксипропілцелюлозу з низьким ступенем заміщення. Як приклад придатних для застосування в технології приготування лікарських засобів ковзаючі речовин можна назвати тальк, поліетиленгліколь, бегенат кальцію, стеарат кальцію, гідрогенізована рицинова олія або стеарат магнію. Як приклад придатних для застосування в технології приготування лікарських засобів розпушувачів можна назвати кукурудзяний крохмаль або кросповідон. Для приготування фармацевтичних композицій із застосовуваними відповідно до винаходу інгібіторами DPP IV можна використовувати наступні способи: - пряме таблетування порошкових сумішей з діючою речовиною разом із прийнятними таблетувальними допоміжними речовинами, 7 UA 102669 C2 5 10 15 20 25 30 35 40 45 50 55 60 - гранулювання разом із прийнятними допоміжними речовинами з наступним змішанням грануляту із прийнятними допоміжними речовинами й таблетуванням, а також нанесенням плівкового покриття або - розфасовування порошкових сумішей або гранулятів у капсули. Як приклад прийнятних методів гранулювання можна назвати наступні: - вологе гранулювання в змішувачі інтенсивної дії з наступним сушінням у псевдозрідженому шарі, - гранулювання в одному апарату, - гранулювання в псевдозрідженому шарі або - сухе гранулювання (наприклад, шляхом ущільнення на валках) разом із прийнятними допоміжними речовинами з наступним таблетуванням або розфасовуванням у капсули. Вказані інгібітори DPP IV можна також використовувати в комбінації з діючими речовинами інших типів, що дозволяє домогтися переважних результатів при лікуванні описаних вище фізіологічних функціональних порушень. При подібному комбінованому лікуванні діючі речовини можна застосовувати у вигляді вільної комбінації або у вигляді фіксованої комбінації, наприклад, у складі однієї таблетки або капсули. Необхідні для цього фармацевтичні композиції з використовуваними в комбінації між собою діючими речовинами або є в продажі у вигляді відповідних лікарських засобів, або їх можна готувати традиційними способами. Наявні в продажі у вигляді лікарських засобів діючі речовини багаторазово описані в рівні техніки, ® наприклад, у регістрі лікарських засобів "Rote Liste ", який щорічно видається Федеральним союзом фармацевтичної промисловості (Німеччина) (Bundesverband der pharmazeutischen Industrie), або в щорічно оновлюваному збірнику з інформацією про виробників лікарських засобів, що відпускають за рецептом, який називається "Physicians' Desk Reference". Як приклад антидіабетичних засобів, які можна використовувати в комбінації з інгібіторами DPP IV, можна назвати метформін, сульфонілсечовини, такі як глібенкламід, толбутамід, глімепірид, гліпізид, гліквідон (Gliquidon), гліборнурид і гліклазид, натеглінід, репаглінід, тіазолідиндіони, такі як росиглітазон і піоглітазон, модулятори рецептора PPARγ, такі як метаглідасен (Metaglidasen), агоністи рецептора PPARγ, такі як GI 262570, антагоністи рецептора PPARγ, модулятори рецептора PPARγ/α, такі як тезаглітазар, мураглітазар і KRP297, модулятори рецептора PPARγ/α/δ, активатори AMPK, такі як AICAR, інгібітори ацетил-КоА– карбоксилази (ACC1 і ACC2), інгібітори діацилгліцерол-ацетилтрансферази (DGAT), агоністи GCRP-протеїну на поверхні β-клітин панкреатичних острівців, такі як агоністи SMT3-рецептора й GPR119, інгібітори 11β-HSD, агоністи або аналоги FGF19, блокатори α-глюкозидази, такі як акарбоза, воглібоза й міглітол, α2-антагоністи, інсулін і його аналоги, такі як людський інсулін, інсулін лізпро, інсулін глузилін, отриманий методом рекомбінантних ДНК інсулін аспарт, НПХінсулін, інсулін детемір, інсулін-цинк суспензія й інсулін гларгин, пептид, який пригнічує секрецію шлунка (GIP), прамлінтид, амілін або GLP-1 і аналоги GLP-1, такі як ексендин-4, інгібітори SGLT2, такі як KGT-1251, інгібітори (білок-тирозин)-фосфатази, інгібітори глюкозо-6-фосфатази, модулятори фруктозо-1,6-бісфосфатази, модулятори глікогенфосфорилази, антагоністи глюкагонового рецептора, інгібітори фосфоєнолпіруваткарбоксикінази (PEPCK), інгібітори [піруватдегідрогеназа]–кінази (PDK), інгібітори тирозин-кіназ (у дозі від 50 до 600 мг), таких як кіназа PDGF-рецептора (див. EP-A-564409, WO 98/35958, US 5093330, WO 2004/005281 і WO 2006/041976), модулятори глюкокінази/регуляторного білка, включаючи активатори глюкокінази, інгібітори [глікогенсинтаза]–кінази, інгібітори інозитол-5-фосфатази типу 2, яка містить SH2-домен (SHIP2), інгібітори IKK, такі як високодозований саліцилат, інгібітори JNK1, інгібітори (протеїнкінази C)-тета, β3-агоністи, такі як ритобегрон, YM 178, солабегрон, талібегрон, N-5984, GRC-1087, рафабегрон і FMP825, інгібітори альдозоредуктази (альдегідредуктази), такі як AS 3201, зенарестат, фідарестат, епалрестат, ранірестат, NZ-314, CP-744809 і CT-112, SGLT-1, відповідно інгібітори SGLT-2, інгібітори каналу KV 1.3, модулятори GPR40, інгібітори SCD-1, антагоністи CCR-2 і інші інгібітори DPP IV. Приклади інгібіторів 11β-HSD1 описані в WO 2007/013929, WO 2007/007688, WO 2007/003521, WO 2006/138508, WO 2006/135795, WO 2006/135667, WO 2006/134481, WO 2006/134467, WO 2006/132436, WO 2006/132197, WO 2006/113261, WO 2006/106423, WO 2006/106052, WO 2006/105127, WO 2006/104280, WO 2006/100502, WO 2006/097337, WO 2006/095822, WO 2006/094633, WO 2006/080533, WO 2006/074330, WO 2006/074244, WO 2006/068992, WO 2006/068991, WO 2006/068199, WO 2006/066109, WO 2006/055752, WO 2006/053024, WO 2006/051662, WO 2006/050908, WO 2006/049952, WO 2006/048750, WO 2006/048331, WO 2006/048330, WO 2006/040329, WO 2006/037501, WO 2006/030805, WO 2006/030804, WO 2006/017542, WO 2006/024628, WO 2006/024627, WO 2006/020598, WO 2006/010546, WO 2006/002349, WO 2006/002350, WO 2006/012173, WO 2006/012227, 8 UA 102669 C2 5 10 WO 2006/012226, WO 2006/000371, WO 2005/118538, WO 2005/116002, WO 2005/110992, WO 2005/110980, WO 2005/108359, WO 2005/108361, WO 2005/108360, WO 2005/108368, WO 2005/103023, WO 2005/097764, WO 2005/097759, WO 2005/095350, WO 2005/075471, WO 2005/063247, WO 2005/060963, WO 2005/047250, WO 2005/046685, WO 2005/044192, WO 2005/042513, WO 2005/016877, WO 2004/113310, WO 2004/106294, WO 2004/103980, WO 2004/089896, WO 2004/089380, WO 2004/089471, WO 2004/089470, WO 2004/089367, WO 2005/073200, WO 2004/065351, WO 2004/058741, WO 2004/056745, WO 2004/056744, WO 2004/041264, WO 2004/037251, WO 2004/033427, WO 2004/011410, WO 2003/104208, WO 2003/104207, WO 2003/065983, WO 2003/059267, WO 2003/044009, WO 2003/044000, WO 2003/043999, WO 2002/076435, WO 2001/090094, WO 2001/090093, WO 2001/090092, WO 2001/090091, WO 2001/090090, US 2007/049632, US 2006/148871, US 2006/025445, US 2006/004049, US 2005/277647, US 2005/261302, US 2005/245534, US 2005/245532, US 2005/245533 і JP 2005-170939. Як приклад одного із представників інгібіторів 11β-HSD1 можна назвати сполуку формули Cl N N N F 15 20 25 30 35 40 45 , а також її солі. Приклади модуляторів глікогенфосфорилази описані в WO 2006/126695, WO 2006/082401, WO 2006/082400, WO 2006/059165, WO 2006/059164, WO 2006/059163, WO 2006/056815, WO 2006/055463, WO 2006/055462, WO 2006/055435, WO 2006/053274, WO 2006/052722, WO 2005/085245, WO 2005/085194, WO 2005/073231, WO 2005/073230, WO 2005/073229, WO 2005/067932, WO 2005/020987, WO 2005/020986, WO 2005/020985, WO 2005/019172, WO 2005/018637, WO 2005/013981, WO 2005/013975, WO 2005/012244, WO 2004/113345, WO 2004/104001, WO 2004/096768, WO 2004/092158, WO 2004/078743, WO 2004/072060, WO 2004/065356, WO 2004/041780, WO 2004/037233, WO 2004/033416, WO 2004/007455, WO 2004/007437, WO 2003/104188, WO 2003/091213, WO 2003/084923, WO 2003/084922, WO 2003/074532, WO 2003/074531, WO 2003/074517, WO 2003/074513, WO 2003/074485, WO 2003/074484, WO 2003/072570, WO 2003/059910, WO 2003/037864, WO 2002/096864, WO 2002/020530, WO 2001/094300, WO 2000/123347, WO 1996/39384, WO 1996/39385, EP 1391460, EP 1136071, EP 1125580, EP 1088824, EP 0978279, JP 2004-196702, US 2004/002495, US 2003/195243 і US 5998463. Приклади активаторів глюкокінази описані в WO 2007/017649, WO 2007/007910, WO 2007/007886, WO 2007/007042, WO 2007/007041, WO 2007/007040, WO 2007/006814, WO 2007/006761, WO 2007/006760, WO 2006/125972, WO 2006/125958, WO 2006/112549, WO 2006/059163, WO 2006/058923, WO 2006/049304, WO 2006/040529, WO 2006/040528, WO 2006/016194, WO 2006/016178, WO 2006/016174, WO 2005/121110, WO 2005/103021, WO 2005/095418, WO 2005/095417, WO 2005/090332, WO 2005/080360, WO 2005/080359, WO 2005/066145, WO 2005/063738, WO 2005/056530, WO 2005/054233, WO 2005/054200, WO 2005/049019, WO 2005/046139, WO 2005/045614, WO 2005/044801, WO 2004/081001, WO 2004/076420, WO 2004/072066, WO 2004/072031, WO 2004/063194, WO 2004/063179, WO 2004/052869, WO 2004/050645, WO 2004/031179, WO 2004/002481, WO 2003/095438, WO 2003/080585, WO 2003/055482, WO 2003/047626, WO 2003/015774, WO 2003/000267, WO 2003/000262, WO 2002/048106, WO 2002/046173, WO 2002/014312, WO 2002/008209, WO 2001/085707, WO 2001/085706, WO 2001/083478, WO 2001/083465, WO 2001/044216 і WO 2000/058293. Як приклад представників активаторів глюкокінази можна назвати сполуку формули 9 UA 102669 C2 O H N G1 O , G2 O S O у якій G1 означає циклопропіл або циклобутил, а G2 означає 5-фтортіазол-2-іл, 1-метил-1Hпіразол-3-іл або піразин-2-іл, і сполука формули G4 G3 O , O S O 5 10 15 20 у якій G3 означає метил або етил, а G4 означає тіазол-2-іл, 4-метилтіазол-2-іл, 5метилтіазол-2-іл або піразин-2-іл, а також їх солі. Приклади інгібіторів SGLT1, відповідно SGLT2 описані в WO 2006/108842, WO 2006/087997, WO 2006/080577, WO 2006/080421, WO 2006/073197, WO 2006/064033, WO 2006/062224, WO 2006/054629, WO 2006/037537, WO 2006/035796, WO 2006/018150, WO 2006/008038, WO 2006/002912, WO 2006/010557, WO 2006/011502, WO 2006/011469, WO 2005/121161, WO 2005/012326, WO 2005/095429, WO 2005/095372, WO 2005/095373, WO 2005/092877, WO 2005/085267, WO 2005/085265, WO 2005/085237, WO 2005/063785, WO 2005/021566, WO 2005/012243, WO 2005/012242, WO 2005/012326, WO 2005/012318, WO 2005/011592, WO 2004/113359, WO 2004/099230, WO 2004/089967, WO 2004/089966, WO 2004/087727, WO 2004/080990, WO 2004/058790, WO 2004/052903, WO 2004/052902, WO 2004/019958, WO 2004/018491, WO 2004/014932, WO 2004/014931, WO 2004/013118, WO 2003/099836, WO 2003/080635, WO 2003/020737, WO 2003/011880, WO 2003/000712, WO 2002/098893, WO 2002/088157, WO 2002/083066, WO 2002/068440, WO 2002/068439, WO 2002/064606, WO 2002/053573, WO 2002/044192, WO 2002/036602, WO 2002/028872, WO 2001/074835, WO 2001/074834, WO 2001/068660, WO 2001/027128, WO 2001/016147, JP 2005-247834, JP 2004-359630, JP 2004-196788, JP 2003-012686 і US 2006/063722. Як приклад представників інгібіторів SGLT1, відповідно SGLT2 можна назвати наступні сполуки і їх солі, відповідно їх комплекси із природними амінокислотами: 10 UA 102669 C2 HO , O HO HO OH OH O HO , HO OH OH а також G8 G5 G6 , O HO G7 HO OH OH 5 10 15 де G5 і G8 незалежно один від одного означають водень, фтор, хлор, бром, ціан, метил, етил, ізопропіл, дифторметил, трифторметил, етиніл, проп-1-ін-1-іл, бут-1-ин-1-іл, гідроксигрупу, метоксигрупу, етоксигрупу, дифторметоксигрупу, циклопропілоксигрупу, циклобутилоксигрупу, циклопентилоксигрупу або циклогексилоксигрупу, G6 означає фтор, хлор, метил, етил, метоксигрупу, етоксигрупу, дифторметоксигрупу, трифторметоксигрупу, триметилсилілетил, етиніл, 2-гідроксипроп-2-ілетиніл, 2-метоксипроп-2ілетиніл, 3-гідрокси-1-пропін-1-іл, 3-метокси-1-пропін-1-іл, циклопропіл, циклобутил, циклопентил, циклогексил, циклопропілоксигрупу, циклобутилоксигрупу, циклопентилоксигрупу, циклогексилоксигрупу, тетрагідрофуран-3-ілоксигрупу, тетрагідропіран-4-ілоксигрупу, піперидин4-ілоксигрупу, N-метилпіперидин-4-ілоксигрупу або N-ацетилпіперидин-4-ілоксигрупу, а G7 означає водень або фтор, G S HO O HO O OH OH де 11 , UA 102669 C2 G означає фтор, хлор, метил, етил, етиніл, метоксигрупу, етоксигрупу, дифторметоксигрупу, трифторметоксигрупу, циклобутилоксигрупу, циклопентилоксигрупу, 3тетрагідрофуранілоксигрупу або 4-тетрагідропіранілоксигрупу, G S HO , O HO OH OH 5 де G означає фтор, хлор, метил, етил, етиніл, метоксигрупу, етоксигрупу, дифторметоксигрупу, трифторметоксигрупу, циклобутилоксигрупу, циклопентилоксигрупу, 3тетрагідрофуранілоксигрупу або 4-тетрагідропіранілоксигрупу, G9 G8 O O , O HO OH OH 10 де G8 означає водень, метоксикарбоніл або етоксикарбоніл, а G9 означає фтор, хлор, метил, етил, етиніл, метоксигрупу, етоксигрупу, дифторметоксигрупу, трифторметоксигрупу, циклобутилоксигрупу, циклопентилоксигрупу, 3тетрагідрофуранілоксигрупу або 4-тетрагідропіранілоксигрупу, а також G13 G11 G10 G12 N G14 N G15 O O HO 15 20 25 O , OH OH де G10 означає C1-C3алкіл або перфтор-C1-C3алкіл, G11 означає водень, C1-C3алкіл або перфтор-C1-C3алкіл, G12 означає фтор, хлор, бром, C1-C6алкіл, C1-C6алкіл, заміщений 1-3 атомами фтору, C1C6алкоксигрупу, C1-C6алкоксигрупу, заміщену 1-3 атомами фтору, C1-C6алкілтіогрупу, C2C6алкеніл, C2-C6алкініл, перфтор-C1-C3алкіл, циклобутилоксигрупу, циклопентилоксигрупу, циклогексилоксигрупу, тетрагідрофуранілоксигрупу або 4-тетрагідропіранілоксигрупу, G13 і G14 незалежно один від одного означають водень, фтор, хлор, бром, C1-C6алкіл, C1C6алкіл, заміщений 1-3 атомами фтору, C1-C6алкоксигрупу, C1-C6алкоксигрупу, заміщену 1-3 атомами фтору, C1-C6алкілтіогрупу, C2-C6алкеніл, C2-C6алкініл або перфтор-C1-C3алкіл, а G15 означає водень, C2-C20алканоїл, C1-C6алкоксикарбоніл або бензоил. 12 UA 102669 C2 5 10 15 20 25 30 35 40 45 50 55 60 Особливо переважним прикладом антидіабетичного засобу, який можна використовувати в комбінації з інгібітором DPP IV, є метформін, який використовують у дозах від приблизно 100 до 500 мг або від 200 до 850 мг від 1 до 3 разів на день або від приблизно 300 до 1000 мг 1 або 2 рази в день, або метформін-ретард, який використовують у дозах від приблизно 100 до 1000 мг або переважно від 500 до 1000 мг 1 або 2 рази в день або від приблизно 500 до 2000 мг 1 раз у день. Іншим особливо переважним прикладом є піоглітазон, який використовують у дозах від приблизно 1 до 10 мг, 15 мг, 30 мг або 45 мг 1 раз у день. Ще одним особливо переважним прикладом є міглітол, який використовують у дозах від приблизно 10 до 50 мг або в дозах аж до 100 мг від 1 до 3 разів у день. Як приклад засобів, які понижують рівень ліпідів у крові і які можна використовувати в комбінації з інгібітором DPP IV, можна назвати інгібітори ГМГ-КоА–редуктази, такі як симвастатин, аторвастатин, ловастатин, флувастатин, правастатин і розувастатин, фібрати, такі як безафібрат, фенофібрат, клофібрат, гемфіброзил, етофібрат і етофулінклофібрат, нікотинову кислоту і її похідні, такі як аципімокс, агоністи рецептора PPARα, агоністи рецептора PPARδ, інгібітори ацил-кофермент A-холестерол-ацилтрансферази (ACAT, КФ 2.3. 1.26), такі як авасиміб, інгібітори усмоктування холестерину, такі як езетиміб, що зв'язуються з жовчними кислотами речовини, такі як колестирамін, колестипол і колесевелам, інгібітори транспорту жовчних кислот, що діють речовини-модулятори ЛВЩ, такі як D4F, Reverse-D4F, діючі речовинимодулятори LXR і діючі речовини-модулятори FXR, інгібітори CETP, такі як торцетрапіб, JTT-705 або сполука 12 з WO 2007/005572, модулятори рецепторів ЛНП і антисмислову РНК ApoВ100. Особливо переважним прикладом є аторвастатин, який використовують у дозах від приблизно 1 до 40 мг або 10 до 80 мг один раз у день. Як приклад засобів, які понижують кров'яний тиск і які можна використовувати в комбінації з інгібітором DPP IV, можна назвати блокатори β-рецепторів, такі як атенолол, бісопролол, целіпролол, метопролол і карведілол, сечогінні засоби, такі як гідрохлортіазид, хлорталідон, ксипамід, фуросемід, піретанід, торасемід, спіронолактон, еплеренон, амілорид і триамтерен, блокатори кальцієвих каналів, такі як амлодипін, ніфедипін, нітрендипін, нісолдипін, нікардипін, фелодипін, лацидипін, лерканідипін, манидипін, ізрадипін, нілвадипін, верапаміл, галопаміл і дилтіазем, інгібітори ACE, такі як раміприл, лізиноприл, цилазаприл, хінаприл, каптоприл, єналаприл, беназеприл, периндоприл, фозиноприл і трандолаприл, а також блокатори рецептора ангіотензину II (ARB), такі як телмісартан, кандесартан, валсартан, лосартан, ірбесартан, олмесартан і епросартан. Особливо переважними прикладами є метопролол, який використовують у дозах від 50 до 200 мг щодня, амлодипін, який використовують у дозах від 2,5 до 10 мг щодня, раміприл, який використовують у дозах від 2,5 до 15 мг щодня, валсартан, який використовують у дозах від 80 до 160 мг щодня, і телмісартан, який використовують у дозах від 20 до 320 мг або від 40 до 160 мг щодня. Як приклад засобів, які підвищують рівень ЛВЩ у крові і які можна використовувати в комбінації з інгібітором DPP IV, можна назвати інгібітори білка-переносника холестерилового ефіру (CETP), інгібітори ендотеліальної ліпази, регулятори ABC1, антагоністи LXRα, агоністи LXRβ, агоністи рецептора PPARδ, регулятори LXRα/β і речовини, які підсилюють експресію аполіпопротеїну A-I та/або які підвищують його концентрацію в плазмі. Як приклад засобів для лікування ожиріння, які можна використовувати в комбінації з інгібітором DPP IV, можна назвати сибутрамін, тетрагідроліпстатин (орлістат), алізим, дексфенфлурамін, аксокайн (Axokine), антагоністи канабіноїдного рецептора 1, такі як антагоніст CB1-рецептора римонобант, антагоністи рецептора MCH-1, агоністи рецептора MC4, антагоністи NPY5, а також NPY2, агоністи β3-AR, такі як SB-418790 і AD-9677, агоністи 5HT2cрецептора, такі як APD 356, інгібітори міостатину, Acrp30 і адіпонектин, інгібітори стеароїл-КоА– десатурази (SCD1), інгібітори (жирна кислота)-синтази (FAS), агоністи рецептора CCK, модулятори грелінового рецептора, Pyy 3-36, антагоністи орексинового рецептора й тезофензин (Tesofensine). Як приклад засобів для лікування атеросклерозу, які можна використовувати в комбінації з інгібітором DPP IV, можна назвати інгібітори фосфоліпази A2, інгібітори тирозин-кіназ (у дозі від 50 до 600 мг), таких як кіназа PDGF-рецептора (див. EP-A-564409, WO 98/35958, US 5093330, WO 2004/005281 і WO 2006/041976), антитіла до oxLDL (до окислених ліпопротеїнів низької щільності) і вакцини проти oxLDL, протеїн apoA-1 Milano, ацетилсаліцилову кислоту (АСК) і інгібітори VCAM-1. Як приклад засобів для лікування серцевої недостатності, які можна використовувати в комбінації з інгібітором DPP IV, можна назвати блокатори β-рецепторів, такі як атенолол, бісопролол, целіпролол і метопролол, сечогінні засоби, такі як гідрохлортіазид, хлорталідон, ксипамід, фуросемід, піретанід, торасемід, спіронолактон, еплеренон, амілорид і триамтерен, 13 UA 102669 C2 5 10 15 20 25 30 35 40 45 50 55 60 інгібітори ACE, такі як раміприл, лізиноприл, цилазаприл, хінаприл, каптоприл, єналаприл, беназеприл, периндоприл, фозиноприл і трандолаприл, а також блокатори рецептора ангіотензину II (ARB), такі як телмісартан, кандесартан, валсартан, лосартан, ірбесартан, олмесартан і епросартан, серцеві глікозиди, такі як дігоксин і дигітоксин, комбіновані блокатори α/β-рецепторів, такі як карведілол, натрійуретичний пептид B-типу (BNP) і пептиди-похідні BNP, а також продукти злиття BNP. Особливо переважними прикладами є метопролол, який використовують у дозах від 50 до 200 мг щодня, раміприл, який використовують у дозах від 2,5 до 15 мг щодня, валсартан, який використовують у дозах від 80 до 160 мг щодня, телмісартан, який використовують у дозах від 20 до 320 мг або 40 до 160 мг щодня, еплеренон, який використовують у дозах від 25 до 00 мг, дігоксин, який використовують у дозах від 0,25 до 0,6 мг щодня, карведілол, який використовують у дозах від 3,25 до 100 мг, BNP-пептид (наприклад, несіритид), який використовують у дозі 2 мкг/кг шляхом ін'єкції ударної дози з наступною інфузією у кількості 0,01 мкг/кг/хв. В лікарських комбінаціях з вибраними інгібіторами DPP IV можна використовувати, наприклад, глібенкламід у кількості від 1,75 до 10,5 мг, толбутамід у кількості від 500 до 3000 мг, глімепірид у кількості від 0,5 до 6 г, гліпізид у кількості від 2,5 до 40 мг, гліквідон у кількості 1430 мг, гліборнурид у кількості до 325 мг, гліклазид у кількості від 80 до 160 мг, метформін у кількості від 500 до 1000 мг, переважно 500 мг, 850 мг або 1000 мг, натеглінід у кількості від 60 до 180 мг, репаглінід у кількості від 0,25 до 4 мг, тіазолідиндіони в кількості від 2 до 45 мг, метаглідасен у кількості від 200 до 600 мг, модулятори рецептора PPARγ/α у кількості від 2,5 до 5 мг, блокатори α-глюкозидази в кількості від 0,1 до 100 мг, інсулін у кількості від 1 до 250 МЕ, прамлінтид у кількості від 15 до 120 мкг, статин у кількості від 5 до 80 мг, фібрат у кількості від 50 до 1000 мг, нікотинову кислоту або її похідне в кількості від 1000 до 3000 мг, аципімокс у кількості приблизно 250 мг, інгібітор усмоктування холестерину в кількості приблизно 10 мг, речовину, що зв'язує жовчні кислоти, в кількості від 0,5 до 30 г, інгібітор CETP у кількості від 10 до 600 мг, переважно від 10 до 120 мг, блокатор β-рецептора в кількості від 2,5 до 100 мг, сечогінний засіб у кількості від 3 до 200 мг, блокатор кальцієвих каналів у кількості від 2,5 до 500 мг, інгібітор ACE у кількості від 1 до 40 мг, блокатор рецептора ангіотензину II у кількості від 5 до 600 мг, сибутрамін у кількості від 10 до 15 мг, орлістат у кількості приблизно 120 мг, дексфенфлурамін у кількості від 15 до 30 мг або антагоніст канабіноїдного рецептора в кількості від 5 до 20 мг, а також еплеренон у дозі від 25 до100 мг, дігоксин у дозі від 0,25 до 0,6 мг щодня, карведілол у дозі від 3,25 до 100 мг, BNP-пептид (наприклад, несіритид) у дозі 2 мкг/кг шляхом ін'єкції ударної дози з наступною інфузією у кількості 0,01 мкг/кг/хв. Приклади Приклад 1: Лікування переддіабету Ефективність запропонованого у винаході застосування інгібітора DPP IV у терапії переддіабету, для якого характерний патологічно підвищений вміст глюкози натще та/або порушена толерантність до глюкози, можна перевіряти клінічними дослідженнями. У короткострокових дослідженнях (наприклад, тривалістю 2-4 тижні) ефективність лікування контролюють, визначаючи після закінчення курсу лікування рівні глюкози в крові натще та/або після прийому їжі або шляхом проби з навантаженням глюкозою (проба на толерантність до глюкози з її пероральним введенням або проба на толерантність до глюкози після прийому певної їжі) і порівнюючи отримані значення з показниками, отриманими перед початком дослідження, та/або з показниками, отриманими в групі досліджуваних, які одержували плацебо. Крім цього можна також визначати рівень фруктозаміну в крові до й після лікування й порівнювати отримані значення з вихідними показниками та/або з показниками, отриманими в групі досліджуваних, які одержували плацебо. Значне зниження рівня глюкози в крові натще або не натще свідчить про ефективність лікування. У довгострокових дослідженнях (тривалістю 12 тижнів і більше) ефективність лікування контролюють, визначаючи рівень гемоглобіну HbА1c у крові й порівнюючи отримані значення з вихідними показниками та/або з показниками, отриманими в групі досліджуваних, які одержували плацебо. Значна зміна рівня гемоглобіну HbА1c у порівнянні з вихідним показником та/або з показником, отриманим у групі досліджуваних, які одержували плацебо, свідчить про ефективність застосування інгібітора DPP IV у терапії переддіабету. Приклад 2: Запобігання розвитку діабету типу 2 Лікування пацієнтів з патологічно підвищеним вмістом глюкози натще та/або порушеною толерантністю до глюкози (переддіабет) також має мету перешкодити розвитку явного діабету типу 2. Ефективність лікування можна перевіряти в клінічному порівняльному дослідженні, при якому пацієнти із переддіабетом протягом тривалого періоду часу (наприклад, протягом 1-5 років) або приймають діючу речовину (інгібітор DPP IV), відповідно комбінацію діючих речовин, 14 UA 102669 C2 5 10 15 20 25 30 35 40 45 50 55 60 або приймають плацебо, або проходять курс немедикаментозної терапії, або приймають інші медикаменти. При проведенні й наприкінці лікування визначають рівень глюкози в крові натще та/або проводять пробу з навантаженням глюкозою (наприклад, пробу на толерантність до глюкози з її пероральним введенням, пПТГ) і таким шляхом контролюють, у скількох пацієнтів розвився явний діабет типу 2, тобто рівень глюкози в крові натще перевищує 125 мг/дл та/або рівень глюкози в крові через 2 години при проведенні пПТГ перевищує 199 мг/дл. Значне зменшення кількості пацієнтів, у яких незважаючи на лікування діючою речовиною, відповідно комбінацією діючих речовин розвився явний діабет типу 2, у порівнянні з кількістю пацієнтів, що проходили курс лікування одним з інших методів, свідчить про ефективність застосування діючої речовини, відповідно комбінації діючих речовин у запобіганні переходу від переддіабету до явного діабету. Пример 3: Лікування діабету типу 2 Лікування пацієнтів з діабетом типу 2 застосовуваними відповідно до винаходу діючими речовинами поряд з явним поліпшенням глюкозного обміну довгочасно запобігає також погіршення обміну речовин у цілому. Подібний ефект можна спостерігати при лікуванні пацієнтів протягом тривалого періоду часу, наприклад, протягом 1-6 років, застосовуваними відповідно до винаходу діючими речовинами, відповідно комбінацією діючі речовини й при порівнянні з пацієнтами, яких лікують іншими антидіабетичними медикаментами. Підтвердженням успішної терапії в порівнянні з пацієнтами, яких лікують іншими антидіабетичними медикаментами, служить повна відсутність або лише незначне підвищення рівня глюкози в крові натще та/або рівня гемоглобіну HbА1c у крові. Іншим підтвердженням успішної терапії служить істотне в порівнянні з кількістю пацієнтів, який лікують іншими медикаментами, зменшення відсотка пацієнтів, у яких незважаючи на лікування застосовуваною відповідно до винаходу діючою речовиною, відповідно застосовуваною відповідно до винаходу комбінацією діючих речовин глюкозний обмін погіршується настільки (наприклад, рівень гемоглобіну HbА1c у крові стає вище 6,5 % або 7 %), що їм доводиться призначати лікування додатковим антидіабетичним медикаментом, прийнятим усередину, або інсуліном або його аналогом або лікування, засноване на іншому антидіабетичному принципі (наприклад, на застосуванні аналога GLP-1). Приклад 4: Лікування інсулінорезистентності У клінічних дослідженнях різної тривалості (наприклад, від 2 тижнів до 12 місяців) ефективність лікування перевіряють за допомогою гіперінсулінемічного еуглікемічного "клемп"тесту з навантаженням глюкозою. Значне збільшення швидкості вливання глюкози наприкінці дослідження в порівнянні з вихідними показниками, відповідно в порівнянні з показниками в групі досліджуваних, які одержували плацебо, або з показниками в групі досліджуваних, які проходили курс лікування іншим методом, свідчить про ефективність застосування діючої речовини, відповідно комбінації діючих речовин у терапії інсулінорезистентності. Приклад 5: Лікування діабетичної гіпер- або дисліпідемії У клінічних дослідженнях різної тривалості (наприклад, від 2 тижнів до 60 місяців) на пацієнтах з діабетом типу 2 ефективність лікування перевіряють шляхом визначення загального холестерину, ЛНП-холестерину, ЛВЩ-холестерину й рівня тригліцеридів у плазмі. Значне зниження загального холестерину, ЛНП-холестерину або рівня тригліцеридів у плазмі та/або зростання рівня ЛВЩ-холестерину в ході або наприкінці дослідження в порівнянні з вихідними показниками, відповідно в порівнянні з показниками в групі досліджуваних, які одержували плацебо, або з показниками в групі досліджуваних, які проходили курс лікування іншим методом, свідчить про ефективність застосування діючої речовини, відповідно комбінації діючих речовин у терапії діабетичної дис- або гіперліпідемії. Приклад 6: Лікування гіперглікемії У клінічних дослідженнях різної тривалості (наприклад, від 1 дня до 24 місяців) ефективність лікування пацієнтів з гіперглікемією перевіряють, визначаючи рівень глюкози в крові натще або рівень глюкози в крові не натще (наприклад, після прийому їжі або шляхом проби з навантаженням глюкозою проведенням пПТГ або проби на толерантність до глюкози після прийому певної їжі). Значне зниження показників вмісту глюкози в крові в ході або наприкінці дослідження в порівнянні з вихідними показниками, відповідно в порівнянні з показниками в групі досліджуваних, які одержували плацебо, або з показниками в групі досліджуваних, які проходили курс лікування іншим методом, свідчить про ефективність застосування діючої речовини, відповідно комбінації діючих речовин у терапії гіперглікемії. Приклад 7: Лікування гестаційного діабету У короткострокових клінічних дослідженнях (наприклад, тривалістю 2-4 тижня) ефективність лікування перевіряють, визначаючи після закінчення курсу лікування рівні глюкози в крові натще та/або після прийому їжі або шляхом проби з навантаженням глюкозою (проба на толерантність 15 UA 102669 C2 5 10 15 20 25 30 35 40 45 50 55 60 до глюкози з її пероральним введенням або проба на толерантність до глюкози після прийому певної їжі) і порівнюючи отримані значення з показниками, отриманими перед початком дослідження, та/або з показниками, отриманими в групі досліджуваних, які одержували плацебо. Крім цього можна також визначати рівень фруктозаміну в крові до й після лікування й порівнювати отримані значення з вихідними показниками та/або з показниками, отриманими в групі досліджуваних, які одержували плацебо. Значне зниження рівня глюкози в крові натще або не натще свідчить про ефективність застосування діючої речовини, відповідно комбінації діючих речовин. У довгострокових дослідженнях (тривалістю 12 тижнів і більше) ефективність лікування контролюють, визначаючи рівень гемоглобіну HbА1c у крові (який порівнюють із вихідними показниками та/або з показниками, отриманими в групі досліджуваних, які одержували плацебо). Значна зміна рівня гемоглобіну HbА1c у порівнянні з вихідними показниками та/або з показниками, отриманими в групі досліджуваних, які одержували плацебо, свідчить про ефективність застосування діючої речовини, відповідно комбінації діючих речовин у терапії гестаційного діабету. Приклад 8: Лікування жінок, які перенесли гестаційний діабет У пацієнток з гестаційним діабетом після вагітності надалі існує значно підвищений ризик захворювання явним діабетом типу 2. У цьому випадку терапія має на меті перешкодити розвитку явного діабету типу 2. Для цього жінки з гестаційним діабетом в анамнезі протягом тривалого періоду часу (наприклад, протягом 1-4 років) або приймають застосовувану відповідно до винаходу діючу речовину (інгібітор DPP IV), відповідно застосовувану відповідно до винаходу комбінацію діючих речовин, або приймають плацебо, або проходять курс немедикаментозної терапії, або приймають інші медикаменти. У ході й наприкінці лікування визначають рівень глюкози в крові натще та/або проводять пробу з навантаженням глюкозою (наприклад, пПТГ) і таким шляхом контролюють, у скількох пацієнток розвився явний діабет типу 2 (рівень глюкози в крові натще перевищує 125 мг/дл та/або рівень глюкози в крові через 2 години при проведенні пПТГ перевищує 199 мг/дл). Значне зменшення кількості пацієнток, у яких незважаючи на лікування застосовуваною відповідно до винаходу діючою речовиною, відповідно застосовуваною відповідно до винаходу комбінацією діючих речовин розвився явний діабет типу 2, у порівнянні з кількістю пацієнток, що проходили курс лікування одним з інших методів, свідчить про ефективність застосування діючої речовини, відповідно комбінації діючих речовин у запобіганні розвитку явного діабету в жінок з гестаційним діабетом в анамнезі. Пример 9: Профілактика мікро- або макроваскулярних ускладнень Лікування пацієнтів з діабетом типу 2 або переддіабетом застосовуваною відповідно до винаходу діючою речовиною, відповідно застосовуваною відповідно до винаходу комбінацією діючих речовин дозволяє запобігти розвитку або знизити ризик розвитку мікроваскулярних ускладнень (наприклад, діабетичній невропатії, діабетичній ретинопатії, діабетичній нефропатії, діабетичної стопи, діабетичної виразки) або макроваскулярних ускладнень (наприклад, інфаркту міокарда, гострого коронарного синдрому, нестабільній стенокардії, стабільній стенокардії, інсульту, облітеруючого ендартеріїту, кардіоміопатії, серцевої недостатності, порушення серцевого ритму, рестенозу судин). Пацієнтам з діабетом типу 2 або із переддіабетом призначають тривалий, який здійснюють, наприклад, від 1 до 6 років курс лікування застосовуваною відповідно до винаходу діючою речовиною, відповідно застосовуваною відповідно до винаходу комбінацією діючих речовин і порівнюють стан їх здоров'я зі станом здоров'я пацієнтів, що приймають інші антидіабетичні медикаменти або плацебо. Підтвердженням ефективності лікування в порівнянні з пацієнтами, які приймають інші антидіабетичні медикаменти або плацебо, служить зменшення кількості ускладнень, які проявилися окремості або декількох ускладнень, які спільно виявилися. У випадку макроваскулярних ускладнень, діабетичної стопи та/або діабетичної виразки вказану кількість підраховують на підставі анамнезу й результатів різних методів обстеження. У випадку діабетичної ретинопатії ефективність лікування визначають шляхом комп'ютерної офтальмоскопії й оцінки стану очного дна або іншими офтальмологічними методами. У випадку діабетичної невропатії поряд з анамнезом і клінічним обстеженням, наприклад, за допомогою еталонованого камертону, можна також вимірювати швидкість проведення по нерву. У випадку діабетичної нефропатії можна перед початком, у ході й наприкінці дослідження контролювати наступні параметри: викид альбуміну, кліренс по креатиніну, вміст креатиніну в сироватці, час до подвоєння вмісту креатиніну в сироватці, час до виникнення необхідності в діалізі. Приклад 10: Лікування метаболічного синдрому Ефективність лікування запропонованими у винаході діючими речовинами, відповідно комбінаціями діючих речовин можна перевіряти в клінічних дослідженнях різної тривалості (наприклад, від 12 тижнів до 6 років), визначаючи рівень глюкози в крові натще або рівень 16 UA 102669 C2 5 10 15 20 25 30 глюкози в крові не натще (наприклад, після прийому їжі або шляхом проби з навантаженням глюкозою проведенням пПТГ або проби на толерантність до глюкози після прийому певної їжі), відповідно визначаючи рівень гемоглобіну HbА1c у крові. Значне зниження показників вмісту глюкози, відповідно гемоглобіну HbА1c у крові в ході або наприкінці дослідження в порівнянні з вихідними показниками, відповідно в порівнянні з показниками в групі досліджуваних, які одержували плацебо, або з показниками в групі досліджуваних, які проходили курс лікування іншим методом, свідчить про ефективність застосування діючої речовини, відповідно комбінації діючих речовин у терапії метаболічного синдрому. Про позитивний вплив на метаболічний синдром можна також судити за поліпшенням інших характерних ознак або симптомів метаболічного синдрому. Як приклад при цьому можна назвати зниження систолічного та/або діастолічного кров'яного тиску, зниження рівня тригліцеридів у плазмі, зниження загального холестерину або ЛНП-холестерину, підвищення рівня ЛВЩ-холестерину або зменшення маси тіла або в порівнянні з відповідними вихідними показниками на початку дослідження, або в порівнянні із групою досліджуваних, які одержували плацебо або проходили курс лікування іншим методом. Приклад 11: Таблетки із плівковим покриттям, які містять інгібітор DPP IV Для приготування розчину для гранулювання коповідон розчиняють при кімнатній температурі в очищеній воді. Крім цього в прийнятному змішувачі попередньо готують суміш (премікс) з інгібітора DPP IV, маніту, попередньо желатинізованого крохмалю й кукурудзяного крохмалю. Цю попередньо приготовлену суміш зволожують розчином для гранулювання й потім гранулюють у змішувачі, що працює з високим зсувним зусиллям. Вологий гранулят просіюють через сито з розміром комірок 1,6 мм. Після цього гранулят сушать у сушарці із псевдозріжденим (рухомим) шаром при температурі приблизно 60 °C до зменшення маси матеріалу, що висушують, на 2-4 %. З остаточно отриманої суміші потім пресують серцевини таблеток. В прийнятному змішувачі при кімнатній температурі гідроксипропілметилцелюлозу (ГПМЦ), поліетиленгліколь (ПЕГ), тальк, діоксид титану й оксид заліза суспендують в очищеній воді, готуючи таким шляхом суспензію для нанесення покриття на таблетки. Цією суспензією покривають серцевини таблеток до збільшення їх маси на 3 %. Таким способом можна виготовляти таблетки, наприклад, наступного складу: Компонент мг Інгібітор DPP IV 0,500 Маніт 67,450 Попередньо желатинізований крохмаль 9,000 Кукурудзяний крохмаль 9,000 Коповідон 2,700 Стеарат магнію 1,350 Загальна маса (серцевини таблетки) 90,000 ГПМЦ 1,500 ПЕГ 0,150 Діоксид титану 0,750 Тальк 0,525 Оксид заліза, жовтий 0,075 Загальна маса (таблетки із плівковим 93,000 покриттям) 35 40 мг 1,000 66,950 9,000 9,000 2,700 1,350 90,000 1,500 0,150 0,750 0,525 0,075 мг 2,500 65,450 9,000 9,000 2,700 1,350 90,000 1,500 0,150 0,750 0,525 0,075 мг 5,000 130,900 18,000 18,000 5,400 2,700 180,000 2,500 0,250 1,250 0,875 0,125 мг 10,000 125,900 18,000 18,000 5,400 2,700 180,000 2,500 0,250 1,250 0,875 0,125 93,000 93,000 185,000 185,000 Приклад 12: Підвищення життєздатності й посилення секреторної здатності панкреатичних острівців або β-клітин Для підвищення життєздатності й посилення секреторної здатності панкреатичних острівців або панкреатичних β-клітин їх після успішного виділення й до моменту трансплантації зберігають, транспортують або культивують у середовищі, що містить інгібітори DPP IV у концентрації від 1 нмоля/л до 1 мкмоля/л, переважно від 1 до 100 нмолів/л. Крім цього пацієнтам (якими можуть також бути тварини) після трансплантації панкреатичних острівців або панкреатичних β-клітин для підвищення життєздатності й посилення секреторної здатності трансплантата призначають інгібітор DPP IV у щоденній дозі від 1 до 200 мг, переважно в дозі від 5 до 100 мг. Ефективність застосування інгібітора DPP IV перевіряють шляхом аналізу секреції інсуліну після стимуляції глюкозою або іншу, підвищувальну секрецію інсуліну засобом. Додатково якісне поліпшення вказаних параметрів можна перевіряти in vitro або ж на тваринах 17 UA 102669 C2 5 10 15 20 25 30 35 40 45 50 55 60 моделях методом TUNEL, описаним в Diabetologia 42, 1999, с. 566, або в Diabetes 48, 1999, с. 738 (дослідження апоптозу та його інгібування). Приклад 13: Комбіноване лікування інгібітором DPP IV і метформіном При лікуванні діабету типу 2 або переддіабету застосовуваний відповідно до винаходу інгібітор DPP IV можна використовувати в сполученні з речовиною, яка має антидіабетичну дію, - метформіном, разом з якою інгібітор DPP IV можна використовувати або у вигляді вільної комбінації, або у вигляді фіксованої комбінації, наприклад, у складі однієї таблетки. Терапевтично ефективну дозу інгібітора DPP IV (наприклад, дозу від 0,1 до 100 мг) можна комбінувати з разовими дозами метформіну, наприклад, з разовими дозами метформіну, що дорівнюють 500 мг, 850 мг або 1000 мг при його загальній добовій дозі в межах від 500 до 2850 мг, відповідно з дозою метформіну, що дорівнює 500 мг, 1000 мг, 1500 мг або 2000 мг при його застосуванні у вигляді ретард-форми. Клінічну ефективність застосування подібної комбінації інгібітора DPP IV з метформіном перевіряють у клінічному дослідженні. Для цього пацієнтам з діабетом типу 2 або із переддіабетом дають приймати або тільки інгібітор DPP IV, або тільки метформін, або інгібітор DPP IV у сполученні з метформіном. Тривалість лікування становить від 2 тижнів до 6 років. Підтвердженням доцільності й ефективності застосування комбінації з інгібітора DPP IV і метформіну служить зниження рівня глюкози в крові натще та/або не натще та/або рівня гемоглобіну HbА1c до значно більш низьких значень у порівнянні з пацієнтами, які приймали тільки інгібітор DPP IV або тільки метформін. Пример 14: Комбіноване лікування інгібітором DPP IV і глітазонами При лікуванні діабету типу 2 або переддіабету застосовуваний відповідно до винаходу інгібітор DPP IV можна використовувати в сполученні з речовиною, яка має антидіабетичну дію, із групи глітазонів, відповідно тіазолідиндіонів (наприклад, у сполученні з піоглітазоном або росиглітазоном), разом з якою інгібітор DPP IV можна використовувати або у вигляді вільної комбінації, або у вигляді фіксованої комбінації, наприклад, у складі однієї таблетки. Терапевтично ефективну дозу інгібітора DPP IV (наприклад, дозу від 0,1 до 100 мг) можна комбінувати з разовими дозами піоглітазону (15 мг, 30 мг або 45 мг) або росиглітазону (2 мг, 4 мг або 8 мг або один раз, або два рази в день). Клінічну ефективність застосування подібної комбінації інгібітора DPP IV з росиглітазоном або піоглітазоном перевіряють у клінічному дослідженні. Для цього пацієнтам з діабетом типу 2 або із переддіабетом дають приймати або тільки інгібітор DPP IV, або тільки росиглітазон, відповідно піоглітазон, або інгібітор DPP IV у сполученні з росиглітазоном, відповідно піоглітазоном. Тривалість лікування становить від 2 тижнів до 6 років. Підтвердженням доцільності й ефективності застосування комбінації з інгібітора DPP IV і росиглітазону, відповідно піоглітазону служить зниження рівня глюкози в крові натще та/або не натще та/або рівня гемоглобіну HbА1c до значно більш низьких значень у порівнянні з пацієнтами, які приймали тільки інгібітор DPP IV або тільки росиглітазон, відповідно піоглітазон. Приклад 15: Комбіноване лікування інгібітором DPP IV і інгібітором SGLT2 При лікуванні діабету типу 2 або переддіабету застосовуваний відповідно до винаходу інгібітор DPP IV можна використовувати в сполученні з речовиною, яка має антидіабетичну дію, із групи інгібіторів SGLT2, разом з якою інгібітор DPP IV можна використовувати або у вигляді вільної комбінації, або у вигляді фіксованої комбінації, наприклад, у складі однієї таблетки. Терапевтично ефективну дозу інгібітора DPP IV (наприклад, дозу від 0,1 до 100 мг) можна комбінувати з разовими дозами інгібітора SGLT2 (від 0,5 до 1000 мг). Клінічну ефективність застосування подібної комбінації інгібітора DPP IV з інгібітором SGLT2 перевіряють у клінічному дослідженні. Для цього пацієнтам з діабетом типу 2 або із переддіабетом дають приймати або тільки інгібітор DPP IV, або тільки інгібітор SGLT2, або інгібітор DPP IV у сполученні з інгібітором SGLT2. Тривалість лікування становить від 2 тижнів до 6 років. Підтвердженням доцільності й ефективності застосування комбінації з інгібітора DPP IV і інгібітора SGLT2 служить зниження рівня глюкози в крові натще та/або не натще та/або рівня гемоглобіну HbА1c до значно більш низьких значень у порівнянні з пацієнтами, які приймали тільки інгібітор DPP IV або тільки інгібітор SGLT2. Пример 16: Комбіноване лікування інгібітором DPP IV і гіпотензивним засобом При лікуванні пацієнтів з діабетом типу 2 або переддіабетом або з метаболічним синдромом застосовуваний відповідно до винаходу інгібітор DPP IV можна використовувати в сполученні з речовиною, яка має гіпотензивну дію, разом з якою інгібітор DPP IV можна використовувати або у вигляді вільної комбінації, або у вигляді фіксованої комбінації, наприклад, у складі однієї таблетки. Терапевтично ефективну дозу інгібітора DPP IV (наприклад, дозу від 0,1 до 100 мг) можна комбінувати з разовими дозами інгібіторів ACE (наприклад, з дозою раміприлу, що становить від 2,5 до 15 мг), антагоністів рецептора AT1 (наприклад, з дозою телмісартану, що 18 UA 102669 C2 5 10 15 20 25 30 35 40 45 50 55 становить від 20 до 160 мг), блокаторів β-рецепторів (наприклад, з дозою метопрололу, що становить від 50 до 200 мг) або сечогінних засобів (наприклад, з дозою гідрохлортіазиду, що становить від 12,5 до 25 мг). Клінічну ефективність застосування подібної комбінації інгібітора DPP IV з гіпотензивними засобами перевіряють у клінічному дослідженні. Для цього пацієнтам з діабетом типу 2 або із переддіабетом або з метаболічним синдромом дають приймати або тільки інгібітор DPP IV, або тільки гіпотензивний засіб, або інгібітор DPP IV у сполученні з гіпотензивним засобом. Тривалість лікування становить від 2 тижнів до 6 років. Підтвердженням доцільності й ефективності застосування комбінації з інгібітора DPP IV і гіпотензивного засобу служить зниження рівня глюкози в крові натще та/або не натще та/або рівня гемоглобіну HbА1c принаймнідо таких же значень, що й при застосуванні тільки інгібітора DPP IV, і зниження систолічного та/або діастолічного артеріального тиску принаймні до таких же значень, що й при застосуванні тільки гіпотензивного засобу. Пример 17: Комбіноване лікування інгібітором DPP IV і засобом, який понижує рівень ліпідів При лікуванні пацієнтів з діабетом типу 2 або переддіабетом або з метаболічним синдромом або з діабетичної дис- або гіперліпідемією застосовуваний відповідно до винаходу інгібітор DPP IV можна використовувати в сполученні з засобом, який понижує рівень ліпідів, / засобом, який підвищує рівень ЛВЩ, разом з яким інгібітор DPP IV можна використовувати або у вигляді вільної комбінації, або у вигляді фіксованої комбінації, наприклад, у складі однієї таблетки. Терапевтично ефективну дозу інгібітора DPP IV (наприклад, дозу від 0,1 до 100 мг) можна комбінувати з разовими дозами статинів (наприклад, з дозою аторвастатину, що становить від 10 до 80 мг, або з дозою симвастатину, що становить від 10 до 80 мг), фібратів (наприклад, фенофібрату), інгібіторів абсорбції холестерину або речовин, які підвищують рівень ЛВЩ, таких як інгібітори CETP (наприклад, з дозою торцетрапібу, що становить від 10 до 120 мг один раз на день або 120 мг двічі в день). Клінічну ефективність застосування подібної комбінації інгібітора DPP IV з засобами, які понижують рівень ліпідів, / засобами, які підвищують рівень ЛВЩ, перевіряють у клінічному дослідженні. Для цього пацієнтам з діабетом типу 2 або переддіабетом або з метаболічним синдромом або з діабетичної дис- або гіперліпідемією дають приймати або тільки інгібітор DPP IV, або тільки засіб, який понижує рівень ліпідів, / засіб, який підвищує рівень ЛВЩ, або інгібітор DPP IV у сполученні з засобом, який понижує рівень ліпідів, / засобом, який підвищує рівень ЛВЩ. Тривалість лікування становить від 2 тижнів до 6 років. Підтвердженням доцільності й ефективності застосування комбінації з інгібітора DPP IV і засобу, який понижує рівень ліпідів, / засобу, який підвищує рівень ЛВЩ, служить зниження рівня глюкози в крові натще та/або не натще та/або рівня гемоглобіну HbА1c принаймні до таких же значень, що й при застосуванні тільки інгібітора DPP IV, і зниження загального холестерину або рівня ЛНП-холестерину в крові або рівня тригліцеридів у плазмі, відповідно підвищення рівня ЛВЩ-холестерину в крові принаймні до таких же значень, що й при застосуванні тільки засобу, який понижує рівень ліпідів, / засобу, який підвищує рівень ЛВЩ. Пример 18: Комбіноване лікування пацієнтів із серцевою недостатністю інгібітором DPP IV і BNP/пептидами-похідними BNP або продуктами злиття BNP При лікуванні пацієнтів з гострою серцевою недостатністю застосовуваний відповідно до винаходу інгібітор DPP IV можна використовувати в сполученні із речовиною, яка сприятливо впливає на серцеву недостатність, разом з якою інгібітор DPP IV можна використовувати або у вигляді вільної комбінації, або у вигляді фіксованої комбінації, наприклад, у складі однієї таблетки. Терапевтично ефективну дозу інгібітора DPP IV (наприклад, дозу від 0,1 до 100 мг) можна комбінувати з разовими дозами інгібіторів ACE (наприклад, з дозою раміприлу, що становить від 2,5 до 15 мг), антагоністів рецептора AT1 (наприклад, з дозою телмісартану, що становить від 20 до 160 мг), блокаторів β-рецепторів (наприклад, з дозою метопрололу, що становить від 50 до 200 мг), комбінованих блокаторів α/β-рецепторів (наприклад, з дозою карведілолу, що становить від 3,25 до 100 мг), сечогінних засобів (наприклад, з дозою гідрохлортіазиду, що становить від 12,5 до 25 мг), антагоністами мінералокортикоїдного рецептора (наприклад, з дозою еплеренону, що становить від 25 до 100 мг) та/або натрійуретичного пептиду B-типу (BNP) (наприклад, з дозою несіритиду, що становить 2 мкг/кг шляхом ін'єкції ударної дози з наступною інфузією у кількості 0,01 мкг/кг/хв), пептид-похідного BNP або продуктом злиття BNP. Комбіноване застосування BNP і інгібітора DPP IV приводить до збільшення концентрації BNP повної довжини (1-32) in vivo. Клінічну ефективність застосування вказаних комбінацій перевіряють у клінічних дослідженнях. Тривалість лікування становить від 1 дня до 6 років. Підтвердженням ефективності застосування такої комбінації в лікуванні гострої серцевої недостатності служить значне в порівнянні з лікуванням іншим методом поліпшення клінічної картини (підвищення серцевого викиду та/або скорочення застою 19 UA 102669 C2 5 10 в легенів та/або зменшення заклинювального тиску у легеневій артерії та/або зниження смертності, обумовленої гострою серцевою недостатністю). Приклад 19: Лікування пацієнтів із серцевою недостатністю інгібітором DPP IV При лікуванні пацієнтів із хронічною серцевою недостатністю можна використовувати застосовуваний відповідно до винаходу інгібітор DPP IV. Таке лікування приводить до збільшення концентрації ендогенного BNP повної довжини (1-32) in vivo. Клінічну ефективність подібної терапії перевіряють у клінічних дослідженнях. Тривалість лікування становить від 2 тижнів до 6 років. Підтвердженням ефективності запропонованого у винаході застосування інгібітора DPP IV при лікуванні хронічної серцевої недостатності служить значне в порівнянні з лікуванням іншим методом або в порівнянні із застосуванням плацебо поліпшення клінічної картини (рідше виникає необхідність у госпіталізації із приводу гострої серцевої недостатності, збільшення дистанції при ходьбі, здатність переносити підвищене фізичне навантаження при ергометрії, збільшення серцевого викиду та/або скорочення застою в легенів та/або зниження смертності, обумовленої серцевою недостатністю). 15 ФОРМУЛА ВИНАХОДУ 1. Застосування інгібітора DPP IV формули (І) O R1 N N O R2 N N (I) 20 або формули (II) O R1 N N R2 N 25 30 N , (II) або однієї з його солей, де R1 означає ([1,5]нафтиридин-2-іл)метил, (хіназолін-2-іл)метил, (хіноксалін-6-іл)метил, (4метилхіназолін-2-іл)метил, 2-ціанобензил, (3-ціанохінолін-2-іл)метил, (3-ціанопіридин-2іл)метил, (4-метилпіримідин-2-іл)метил або (4,6-диметилпіримідин-2-іл)метил, R2 означає 3-(R)-амінопіперидин-1-іл, (2-аміно-2-метилпропіл)метиламіногрупу або (2-(S)амінопропіл)метиламіногрупу, для приготування лікарського засобу, призначеного для терапії пацієнта, у якого діагностовано фізіологічне функціональне порушення, вибране із групи, яка включає діабетичну стопу, діабетичну виразку, гестаційний діабет та адренергічний постпрандіальний синдром і серцеву недостатність, або для терапії пацієнта із трансплантованими панкреатичними острівцями або -клітинами. 2. Застосування інгібітора DPP IV формули (І) O R1 N N O R2 N N (I) 35 або формули (II) O R1 N N N R2 N або однієї з його солей, де 20 , (II) UA 102669 C2 5 10 15 20 25 30 35 R1 означає ([1,5]нафтиридин-2-іл)метил, (хіназолін-2-іл)метил, (хіноксалін-6-іл)метил, (4метилхіназолін-2-іл)метил, 2-ціанобензил, (3-ціанохінолін-2-іл)метил, (3-ціанопіридин-2іл)метил, (4-метилпіримідин-2-іл)метил або (4,6-диметилпіримідин-2-іл)метил, і R2 означає 3-(R)-амінопіперидин-1-іл, (2-аміно-2-метилпропіл)метиламіногрупу або (2-(S)амінопропіл)метиламіногрупу, для приготування лікарського засобу, призначеного для терапії пацієнтів, у яких діагностовано явний діабет типу 2, де, застосовуючи вказаний лікарський засіб, зменшують існуючий незважаючи на лікування ризик погіршення глюкозного обміну, зменшують існуючий незважаючи на лікування ризик підвищення рівня гемоглобіну НbА1с, зменшують існуючий незважаючи на лікування ризик підвищення рівня глюкози натще, зменшують ризик виникнення необхідності в інсулінотерапії, зменшують ризик розвитку діабетичної стопи, зменшують ризик розвитку діабетичної виразки або зменшують ризик виникнення макроваскулярного ускладнення. 3. Застосування за п. 2, в якому макроваскулярне ускладнення вибране із групи, яка включає інфаркт міокарда, гострий коронарний синдром, нестабільну стенокардію, стабільну стенокардію, геморагічний або ішемічний інсульт, облітеруючий ендартеріїт, кардіоміопатію, лівошлуночкову недостатність, правошлуночкову недостатність, тотальну серцеву недостатність, порушення серцевого ритму і рестеноз судин. 4. Застосування за п. 1, в якому лікарський засіб призначений для терапії гестаційного діабету. 5. Застосування за п. 1, в якому лікарський засіб призначений для терапії адренергічного постпрандіального синдрому. 6. Застосування за п. 1, в якому лікарський засіб призначений для терапії серцевої недостатності. 7. Застосування за п. 2, в якому, застосовуючи вказаний лікарський засіб, зменшують ризик подальшого підвищення рівня гемоглобіну НbА1с, підвищення рівня глюкози натще й виникнення необхідності в інсулінотерапії. 8. Застосування за будь-яким з попередніх пунктів, де інгібітор DPP IV додатково комбінують з активною речовиною, вибраною з групи антидіабетичних засобів інших класів, з діючих речовин, які знижують рівень цукру в крові, з діючих речовин, які знижують рівень ліпідів у крові, з діючих речовин, які підвищують рівень ліпопротеїнів високої щільності (ЛВЩ) у крові, з діючих речовин, які знижують кров'яний тиск, і з діючих речовин, показаних при лікуванні атеросклерозу або ожиріння. 9. Застосування за п. 8, де інгібітор DPP IV додатково комбінують з антидіабетичним засобом іншого класу або діючою речовиною, яка знижує кров'яний тиск. 10. Застосування за п. 9, де інгібітор DPP IV додатково комбінують з метформіном, піоглітазоном, міглітолом, аторвастатином, метопрололом, амлодипіном, раміприлом, валсартаном або телмісартаном. 11. Застосування інгібітора DPP IV формули (І) O R1 N N O R2 N N (I) 40 або формули (II) O R1 N N 45 N R2 N , (II) або однієї з його солей, де R1 означає ([1,5]нафтиридин-2-іл)метил, (хіназолін-2-іл)метил, (хіноксалін-6-іл)метил, (4метилхіназолін-2-іл)метил, 2-ціанобензил, (3-ціанохінолін-2-іл)метил, (3-ціанопіридин-2іл)метил, (4-метилпіримідин-2-іл)метил або (4,6-диметилпіримідин-2-іл)метил, а R2 означає 3-(R)-амінопіперидин-1-іл, (2-аміно-2-метилпропіл)метиламіногрупу або (2-(S)амінопропіл)метиламіногрупу, у дозі 0,5-50 мг для перорального введення, 21 UA 102669 C2 5 10 15 20 25 30 35 40 45 50 55 для приготування лікарської комбінації з діючою речовиною, вибраною із групи антидіабетичних засобів інших класів, з діючими речовинами, які знижують рівень цукру в крові, з діючими речовинами, які знижують рівень ліпідів у крові, з діючими речовинами, які підвищують рівень ліпопротеїнів високої щільності (ЛВЩ) у крові, з діючими речовинами, які знижують кров'яний тиск, і з діючими речовинами, показаними при лікуванні атеросклерозу або ожиріння. 12. Застосування за п. 11, де доза інгібітора DPP IV при пероральному введенні становить від 2,5 до 50 мг, краще від 0,5 до 10 мг (як, наприклад, 0,5 мг, 1 мг, 2,5 мг, 5 мг або 10 мг). 13. Застосування за п. 11, де лікарську комбінацію готують з інгібітора DPP IV і антидіабетичного засобу іншого класу або діючої речовини, яка знижує кров'яний тиск. 14. Застосування за п. 11, де лікарську комбінацію готують з інгібітора DPP IV і метформіну, піоглітазону, міглітолу, аторвастатину, метопрололу, амлодипіну, раміприлу, валсартану або телмісартану. 15. Застосування за п. 11, де лікарську комбінацію готують з інгібітора DPP IV і метформіну, піоглітазону, міглітолу, аторвастатину, валсартану або телмісартану. 16. Застосування за п. 11, де лікарська комбінація призначена для терапії пацієнта, у якого діагностовано фізіологічне функціональне порушення, вибране із групи, яка включає діабетичну стопу, діабетичну виразку, гестаційний діабет, адренергічний постпрандіальний синдром і серцеву недостатність. 17. Застосування за п. 11, де лікарська комбінація призначена для терапії пацієнта, у якого діагностовано явний діабет типу 2, яке відрізняється тим, що, застосовуючи вказану лікарську комбінацію, зменшують існуючий незважаючи на лікування ризик погіршення глюкозного обміну, зменшують існуючий незважаючи на лікування ризик підвищення рівня гемоглобіну НbА1с, зменшують існуючий незважаючи на лікування ризик підвищення рівня глюкози натще, зменшують ризик виникнення необхідності в інсулінотерапії, зменшують ризик розвитку діабетичної стопи, зменшують ризик розвитку діабетичної виразки або зменшують ризик виникнення макроваскулярного ускладнення. 18. Застосування за п. 17, де макроваскулярне ускладнення вибране із групи, яка включає інфаркт міокарда, гострий коронарний синдром, нестабільну стенокардію, стабільну стенокардію, геморагічний або ішемічний інсульт, облітеруючий ендартеріїт, кардіоміопатію, лівошлуночкову недостатність, правошлуночкову недостатність, тотальну серцеву недостатність, порушення серцевого ритму й рестеноз судин. 19. Застосування інгібітора DPPIV за п. 11, для приготування лікарського засобу, призначеного для лікування переддіабету або діабету типу 2, де інгібітор DPP IV комбінують з метформіном або глітазоном, або тіазолідиндіоном (наприклад, піоглітазоном). 20. Застосування за будь-яким з попередніх пунктів, де інгібітор DPPIV вибирають з групи, що складається з 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину, 1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-иніл)-5-(4-метилхіназолін-2-ілметил)-3,5дигідроімідазо[4,5-d]піридазин-4-ону, 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2метилпропіл)метиламіно]ксантину, 1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-(2-ціанобензил)-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S)-(2амінопропіл)метиламіно]ксантину, 1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1іл)ксантину та 1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, або його терапевтично активної солі. 21. Застосування інгібітора DPP IV для приготування лікарського засобу, призначеного для комбінованого лікування з метформіном, де інгібітор DPP IV має формулу І 22 UA 102669 C2 O R1 O 5 N N R2 N N (I) або являє собою одну із солей цієї сполуки, де R1 означає (4-метилхіназолін-2-іл)метил, та R2 означає 3-(R)-амінопіперидин-1-іл. 22. Застосування інгібітора DPP IV для приготування лікарського засобу, призначеного для комбінованого лікування з глітазоном або тіазолідиндіоном (наприклад, піоглітазоном), де інгібітор DPP IV має формулу І O R1 O 10 N N R2 N N (I) або являє собою одну із солей цієї сполуки, де R1 означає (4-метилхіназолін-2-іл)метил, та R2 означає 3-(R)-амінопіперидин-1-іл. 23. Застосування інгібітора DPP IV для приготування лікарського засобу, призначеного для комбінованого лікування з телмісартаном, де інгібітор DPP IV має формулу І O R1 O 15 20 25 30 35 40 N N R2 N N (I) або являє собою одну із солей цієї сполуки, де R1 означає (4-метилхіназолін-2-іл)метил, та R2 означає 3-(R)-амінопіперидин-1-іл. 24. Застосування інгібітора DPP IV, який вибирають з групи, що складається з 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину, 1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-иніл)-5-(4-метилхіназолін-2-ілметил)-3,5дигідроімідазо[4,5-d]піридазин-4-ону, 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2метилпропіл)метиламіно]ксантину, 1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-(2-ціанобензил)-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S)-(2амінопропіл)метиламіно]ксантину, 1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1іл)ксантину, 1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, або його терапевтично активної солі, в дозі від 0,5 до 50 мг при пероральному введенні, для приготування лікарського засобу, призначеного для лікування переддіабету або діабету типу 2, де інгібітор DPP IV комбінують з метформіном або глітазоном, або тіазолідиндіоном (наприклад, піоглітазоном), у вигляді вільної комбінації або у вигляді фіксованої комбінації, у складі таблетки. 25. Застосування за п. 24, де доза інгібітора DPP IV при пероральному введенні становить від 2,5 до 50 мг, краще від 0,5 до 10 мг (як, наприклад, 0,5 мг, 1 мг, 2,5 мг, 5 мг або 10 мг). 23 UA 102669 C2 5 10 15 20 25 30 35 40 45 50 55 60 26. Застосування за будь-яким з пп. 21-25, де комбіноване лікування проводять у вигляді вільної комбінації. 27. Застосування за будь-яким з пп. 21-25, де комбіноване лікування проводять у вигляді фіксованої комбінації, наприклад, у складі таблетки або капсули. 28. Застосування інгібітора DPP IV, який вибирають з групи, що складається з 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину, 1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-иніл)-5-(4-метилхіназолін-2-ілметил)-3,5дигідроімідазо[4,5-d]піридазин-4-ону, 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2метилпропіл)метиламіно]ксантину, 1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-(2-ціанобензил)-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S)-(2амінопропіл)метиламіно]ксантину, 1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1іл)ксантину, 1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, або його терапевтично активної солі, для приготування лікарського засобу для попередження або зниження ризику виникнення макроваскулярного ускладнення у пацієнтів із діабетом типу 2 або з переддіабетом. 29. Застосування за п. 28, де макроваскулярне ускладнення вибране із групи, яка включає інфаркт міокарда, гострий коронарний синдром, нестабільну стенокардію, стабільну стенокардію, удар, облітеруючий ендартеріїт, кардіоміопатію, серцеву недостатність, порушення серцевого ритму й рестеноз судин. 30. Застосування за п. 28, де лікарський засіб з інгібітором DPP IV комбінують з діючою речовиною, вибраною із групи антидіабетичних засобів інших класів, з діючих речовин, які знижують рівень цукру в крові, з діючих речовин, які знижують рівень ліпідів у крові, з діючих речовин, які підвищують рівень ліпопротеїнів високої щільності (ЛВЩ) у крові, з діючих речовин, які знижують кров'яний тиск, і з діючих речовин, показаних при лікуванні атеросклерозу або ожиріння. 31. Застосування за п. 30, де лікарський засіб з інгібітором DPP IV комбінують з антидіабетичним засобом іншого класу або діючою речовиною, яка знижує кров'яний тиск. 32. Застосування за п. 30, де лікарський засіб з інгібітором DPP IV комбінують з метформіном, піоглітазоном, міглітолом, аторвастатином, метопрололом, амлодипіном, раміприлом, валсартаном або телмісартаном. 33. Застосування інгібітора DPP IV, який вибирають з групи, що складається з 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину, 1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-иніл)-5-(4-метилхіназолін-2-ілметил)-3,5дигідроімідазо[4,5-d]піридазин-4-ону, 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2метилпропіл)метиламіно]ксантину, 1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-(2-ціанобензил)-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S)-(2амінопропіл)метиламіно]ксантину, 1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1іл)ксантину та 1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, або його терапевтично активної солі, в дозі від 0,5 до 50 мг при пероральному введенні, краще від 2,5 до 50 мг, особливо краще від 0,5 до 10 мг (як, наприклад, 0,5 мг, 1 мг, 2,5 мг, 5 мг або 10 мг), для приготування лікарського засобу, призначеного для лікування діабету типу 2. 24 UA 102669 C2 5 10 15 20 25 34. Застосування інгібітора DPP IV, який вибирають з групи, що складається з 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину, 1-[([1,5]нафтиридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(хіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 2-((R)-3-амінопіперидин-1-іл)-3-(бут-2-иніл)-5-(4-метилхіназолін-2-ілметил)-3,5дигідроімідазо[4,5-d]піридазин-4-ону, 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(2-аміно-2метилпропіл)метиламіно]ксантину, 1-[(3-ціанохінолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-(2-ціанобензил)-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-[(S)-(2амінопропіл)метиламіно]ксантину, 1-[(3-ціанопіридин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4-метилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, 1-[(4,6-диметилпіримідин-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1іл)ксантину та 1-[(хіноксалін-6-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-((R)-3-амінопіперидин-1-іл)ксантину, або його терапевтично активної солі, краще в дозі від 0,5 до 50 мг при пероральному введенні, краще від 2,5 до 50 мг, особливо краще від 0,5 до 10 мг (як, наприклад, 0,5 мг, 1 мг, 2,5 мг, 5 мг або 10 мг), для приготування лікарського засобу, призначеного для лікування пацієнта з діабетом типу 2 або переддіабетом, або з метаболічним синдромом, де інгібітор DPP IV комбінують з інгібітором АСЕ (наприклад, з дозою раміприлу, що становить від 2,5 до 15 мг), антагоністом рецептора AT1 (наприклад, з дозою телмісартану, що становить від 20 до 160 мг), блокатором рецепторів (наприклад, з дозою метопрололу, що становить від 50 до 200 мг) або сечогінним засобом (наприклад, з дозою гідрохлортіазиду, що становить від 12,5 до 25 мг), у вигляді вільної комбінації або у вигляді фіксованої комбінації, у складі таблетки. Комп’ютерна верстка Г. Паяльніков Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 25
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of dpp-iv inhibitors
Автори англійськоюDugi, Klaus, Himmelsbach Frank, Mark Mikhaehl
Назва патенту російськоюПрименение ингибиторов dpp iv
Автори російськоюДуги Клаус, Химмельсбах Франк, Марк Михаель
МПК / Мітки
МПК: A61K 31/4985, A61K 31/522, A61P 3/10, A61P 9/04
Мітки: застосування, інгібіторів
Код посилання
<a href="https://ua.patents.su/27-102669-zastosuvannya-ingibitoriv-dpp-iv.html" target="_blank" rel="follow" title="База патентів України">Застосування інгібіторів dpp iv</a>
Попередній патент: Дельта-5-десатураза і її застосування в продукуванні поліненасичених жирних кислот
Наступний патент: Похідні піридопіримідиндіонів для лікування опосередкованого pde 4 хворобливого стану
Випадковий патент: Вітродвигун