Спосіб одержання ізоксазол-3-карбонової кислоти
Номер патенту: 55609
Опубліковано: 27.12.2010
Автори: Толмачов Андрій Олексійович, Вовк Михайло Володимирович, Лебедь Павло Соломонович
Формула / Реферат
Спосіб одержання ізоксазол-3-карбонової кислоти формули:
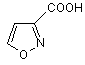 ,
,
який відрізняється тим, що як вихідну сполуку використовують метиловий естер 5-етокси-4,5-дигідро-3-ізоксазолкарбонової кислоти, який обробляють киплячою концентрованою соляною кислотою з наступним виділенням цільового продукту звичайними методами.
Текст
Спосіб одержання ізоксазол-3-карбонової кислоти формули: 2 3 55609 Задача досягається гідролізом з одночасною ароматизацієюметилового естеру 5-етокси-4,5дигідро-3-ізоксазолкарбонової кислоти з використанням дешевого реагента і водночас розчинника соляної кислоти. Спосіб отримання сполуки, яка заявляється полягає в тому, що метиловий естер 5-етокси-4,5дигідро-3-ізоксазолкарбонової кислоти обробляють киплячою концентрованою соляною кислотою впродовж 2 год. Вихід цільового продукту, який виділяють із реакційної суміші стандартними методами, становить 70 %. COOMe EtO O N COOH HCl -MeOH, -EtOH O N Запропонований спосіб є технологічним і економічно ефективним, оскільки не вимагає використання органічних розчинників і значних енергетичних затрат на процес нагріву реакційної суміші. З врахуванням відносної лабільності 4,5дигідроізоксазольного циклу до дії як нуклеофільних, так і електрофільних реагентів, не можна було заздалегідь передбачити перебіг селективного процесу елімінування етанолу із вказаної сполуки. З врахуванням наявності в ній декількох нуклеофільних центрів - атомів кисню екзоциклічної етоксильної групи та ендоциклічної оксіміногрупи, не виключалась можливість протонування останньої, що могло б приводити до деструкції 4,5дигідроізоксазольної системи. Насправді ж в процесі реакції відбувається кислотний гідроліз складноестерної групи з одночасним елімінуванням етанолу, що супроводжується ароматизацією частково гідрованого ізоксазольного циклу, найвірогідніше, за механізмом Е1. Цим самим знайдений спосіб принципово відрізняється від аналогів, в котрих карбоксильна функція формується на базі наявного ізоксазольного ядра. Вихідний реагент для отримання ізоксазол-3карбонової кислоти - метиловий естер 5-етокси4,5-дигідро-3-ізоксазолкарбонової кислоти є доступною сполукою, яка з виходом 61 % утворюється із комерційно доступних гідрохлориду гліцину та етилвінілового етеру через стадію проміжного метоксикарбонілгідроксамоїлхлориду [10-13]. Будова та склад цільової сполуки доведені даними елементного аналізу та спектру ЯМР 1Н, а також їх співставленням із заздалегідь відомими характеристиками. Вихід ілюструється способом отримання ізоксазол-3-карбонової кислоти. Спосіб одержання ізоксазол-3-карбонової кислоти. В реактор об'ємом 2 л поміщали 213.5 г (1.55 моль) метилового естеру 5-етокси-4,5-дигідро-3ізоксазолкарбонової кислоти, 700 мл 35 %-ної соляної кислоти і кип'ятили при перемішуванні впродовж 2 год. Реакційну суміш охолоджували, розчинник упарювали на роторному насосі, до твердого залишку додавали 500 мл етилацетату, нагрівали до кип'ятіння і фільтрували. Розчинник відганяли, залишок кристалізували із суміші бен 4 зол-метанол, 50:1. Вихід 70 %, т. топл. 147-148 °С. Спектр ЯМР 1Н, δ, м. ч.: 6.82 с (1Н, СН=), 9.02 с (1H, СН=), 13.56 ш. с. (1H, СООН). Знайдено, % : С 42. 65; Н 2.56; N 12.58. C4H3NO3. Вирахувано, % : С 42.49; Н 2.67; N 12.39. Таким чином, запропонований спосіб одержання ізоксазол-3-карбонової кислоти є препаративно простим та синтетично ефективним, що суттєво відрізняє його від відомих, які характеризуються важкодоступністю вихідних сполук, енергозатратністю та екологічною небезпечністю процесів, які лежать в їх основі. Джерела інформації: 1. Lepage F., Tombret F., Cuvier G., Marivain A., Gillardin J.M. New N-aryl isoxazolecarboxamides and N-isoxazolylbenzamides as anticonvulsant agents //Eur. J. Med. Chem. - 1992. - Vol. 27, №6. - P. 581593. 2. Takada S., Sasatani Т., Chomei N., Adachi M, Fujishita T. Synthesis and Structure-Activity Relationship of Fused Imidazopyridines : A New Series of Benzodiazepine Receptor Ligands //J. Med. Chem. - 1996. - Vol. 39, № 14. - P. 2844-2851. 3. Feng D.-M., DiPardo R.M., Wai J.M., Chang R.K., Di Marco C.N., Murphy K.L., Ranson R.M., Reiss D.R., Tang C, Prueksitanont Т., Pettibone D.J., Bock M.G., Kuduk S.D. A new class of braykin B! receptor antagonists with high oral bioactivity and minimal PRX activity //Bioorg. Med. Chem. Lett 2008. - Vol. 18. - P. 682-687. 4. Pat. USA 2855402. 07 Oct. 1958. - 3,3'Biisoxazole and its preparation from acetylene and nitric oxide /Cramer R.D., Pa L. Chem. Abstr. - 1959. - Vol. 53, P. 5286g. 5. Cramer R., McClellan W.R. Isoxazole Derivatives from Acetylene and nitrogen oxides //J. Org. Chem. - 1961. - Vol. 26. - P. 2976-2979. 6. Mina G.A., Rateb L., Soliman G. Reactions of hydroxymethylene ketones. Part.l. Synthesis of isoxazoles and pyrazoles from cinnamoylacetaldehyde and its derivatives //J. Chem. Soc - 1962. - P. 4234-4241. 7. Panizzi L. Heterocyclic synthesis. III. Gaz. Chim. Ital. - 1942. - Vol. 72. - P. 475-483. 8. Quilico A., Simonetta M. The flilminic synthesis of isoxazoles. VII. Nitrolic acids and acetylene compounds //Gaz. Chim. Ital. - 1947. - Vol. 77. - P. 586-595. 9. Quilico A., Freri M. The isoxazole group and the action of nitric acid on unsaturated compounds. XVII. Diisoxalolylketone //Gaz. Chim. Ital.-1946. - Vol. 76. - P. 3-29. 10. Kozikowski A.P., Adamcz M. Methods for the stereoselective cis-cyanohydroxylation andcarboxyhydroxylation of olefins //J. Org. Chem. 1983. - Vol. 48, № 3. - P. 366-372. 11. Burkhart D.J., Zhou P., Blumenfeld A., Twamley В., Natale N.R. An improved procedure for the lateral lithiation of ethyl 4-acethyl-5-methyl-3isoxazolyl carboxylate //Tetrahedron. - 2001. - Vol. 57. -№ 38. - P. 8039-8046. 12. Paul R., Tchelitcheff S. Oxydes de nitriles. I. Synthese de Quelques nouvelles isoxazoline mono et bicycliques a partir de l’acetate de vinile et de divers 5 55609 ethers viniliques //Bull. Soc. Chim. Fr. - 1962. - Vol. 11. - P. 2216-2221. 13. Moriya O., Urata Y., Endo T. Dehydrochlorination of hydroxymic acid chlorides by Комп’ютерна верстка Г. Паяльніков 6 the use of organotin compound : application for the synthesis of isoxazolines and isoxazoles //J. Chem. Soc. Chem. Comuun. - 1991. - P. 17-18. Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of isoxazol-3-carboxylic acid
Автори англійськоюVovk Mykhailo Volodymyrovych, Lebed Pavlo Solomonovych, Tolmachov Andrii Oleksiiovych
Назва патенту російськоюСпособ получения изоксазол-3-карбоновой кислоты
Автори російськоюВовк Михаил Владимирович, Лебедь Павел Соломонович, Толмачов Андрей Алексеевич
МПК / Мітки
МПК: C07D 261/00
Мітки: одержання, спосіб, кислоти, ізоксазол-3-карбонової
Код посилання
<a href="https://ua.patents.su/3-55609-sposib-oderzhannya-izoksazol-3-karbonovo-kisloti.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання ізоксазол-3-карбонової кислоти</a>
Попередній патент: Установка для фільтрації планктону із виростних ставків
Наступний патент: Матеріал декоративного облицювального покриття
Випадковий патент: Спосіб та пристрій для очищення стічних вод







