Спосіб одержання 1,3,4-триалкілпіразолів та їх карбоциклічних аналогів
Формула / Реферат
Спосіб одержання 1,2,3-триалкілпіразолів та їх карбоциклічних аналогів за реакцією Вільсмеєра-Хаака загальної формули:
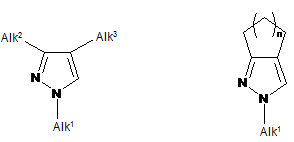 ,
,
де Alk1 = Me, iPr, ffiu Alk2= Me, Et, iPr, tBu Alk3= Me, Et n= 1, 2, 3,
який відрізняється тим, що алкілгідразони кетонів піддають послідовній взаємодії з комплексом диметилформаміду та хлороксиду фосфору при 80-90 °С та 30 %-ним гідроксидом натрію при кімнатній температурі в водному розчині з наступним виділенням цільових продуктів звичайними методами.
Текст
Спосіб одержання 1,2,3-триалкілпіразолів та їх карбоциклічних аналогів за реакцією Вільсмеєра-Хаака загальної формули: 2 3 n Alk3 Alk2 1 де Alk = Me, iPr, ffiu Alk = Me, Et, iPr, tBu Alk = Me, Et n= 1, 2, 3, який відрізняється тим, що алкілгідразони кетонів піддають послідовній взаємодії з комплексом диметилформаміду та хлороксиду фосфору при 8090 °С та 30 %-ним гідроксидом натрію при кімнатній температурі в водному розчині з наступним виділенням цільових продуктів звичайними методами. N N N N Alk1 Alk1 N N N N N Alk1 N Alk1 Alk1 n N N Alk , де Alk =Me, iPr, tBu Alk =Me, Et, iPr, tBu 3 Alk =Me, Et n=1, 2, 3. Сполуки даного типу та їх найпростіші похідні знаходять широке застосування як базові об'єкти для одержання низки фармакологічно важливих піразоловмісних систем [1-6]. Спосіб одержання 1,2,3-триалкілпіразолів та їх карбоциклічних аналогів, який заявляється, в нау1 2 1 (11) n Alk3 UA 3 Alk2 Alk Alk2 ковій літературі та патентних виданнях не описаний. 2-Метилтетрагідроіндазол утворюється в суміші з ізомерним 1-алкілтетрагідроіндазолами при циклізації відповідних похідних циклогексанону [7, 8] або алкілуванням тетрагідроіндазолу [9]. Задачею корисної моделі є пошук нового способу отримання 1,2,3-триалкілпіразолів та їх карбоциклічних аналогів. Задача вирішується формілюванням з подальшою циклізацією легкодоступних алкілгідразонів метилалкілкетонів за допомогою доступних та дешевих реактантів - диметилформаміду, хлороксиду фосфору та гідроксиду натрію. Спосіб отримання сполук, які заявляються, полягає в тому, що алкілгідразони кетонів піддають взаємодії з комплексом диметилформаміду та хлороксиду фосфору при 80 °C та 30 %-ним гідроксидом натрію при кімнатній температурі в водному розчині. Цільові продукти виділяють із реакційної суміші стандартними методами. їх виходи становлять 72-82 %. (19) Корисна модель належить до органічної хімії, а саме до нового способу одержання 1,2,3триалкілпіразолів та їх карбоциклічних аналогів загальної формули: 66523 (13) U , 3 66523 Alk1 N Alk3 Alk2 N 1,2 N N Alk2 Alk1 Alk3 Alk1 N N n 1,2 N N Alk1 . 1. ДМФА, Р(О)С13; 2. 30 % NaOH, 1 2 де Alk =Me, iPr, tBu Alk =Me, Et, iPr, tBu 3 Alk =Me, Et n=1, 2, 3 Запропонований спосіб дозволяє отримати один ізомер і не потребує хроматографічної очистки. Аналіз спеціальної літератури засвідчує, що очікуваний результат не можна було заздалегідь передбачити. Адже відомо, що формілювання кетонів приводить до утворення енамінокетонів. Вихідні реагенти є доступними сполуками, які з високими виходами утворюються із відповідних кетонів та алкілгідразинів. Будова та склад як вихідних, так і цільових продуктів доведені результатами елементного 1 аналізу та спектрів ЯМР Н. Корисна модель ілюструється загальним способом одержання 1,2,3-триалкілпіразолів та їх карбоциклічних аналогів. Загальний спосіб одержання 1,2,3триалкілпіразолів та їх карбоциклічних аналогів. До 100 мл охолодженого до 0 °C диметилформаміду додають при перемішуванні 38.0 г (25 ммоль) хлороксиду фосфору з такою швидкістю, щоб температура реакційної суміші не перевищувала 5 °C. Через 0.5 год. температуру реакційної суміші знижують до -20 °C та додають по краплям у продовж 1 год. розчин 25 ммоль відповідного Nалкілгідразону кетону в 10 мл диметилформаміду. Через 3 год. Температуру реакційної суміші підвищують до 80 °C та перемішують 2 год. при цій температурі, охолоджують, виливають в 300 мл льодяної води, нейтралізують при охолодженні 30 % NaOH до рН 9-10, екстрагують 3500 мл хлороформу і переганяють. Приклад 1. 1,2,3-Триметилпіразол. Вихід 75 %, 1 т. кип. 152-155 °C. Спектр ЯМР Н, , м.ч.: 1.94 (3Н, с, СН3), 2.14 (3Н, с, СН3), 3.73 (3Н, с, СН3), 7.00 (1H, с, Н-5). Знайдено, %: С 65.47; Н 9.11; N 25.39. C6H10N2. Вирахувано, %: С 65.42; Н 9.15; N25.43. Приклад 2. 1-ізопропіл-3.4-диметилпіразол. 1 Вихід 82 %, т. кип. 185-187 °C. Спектр ЯМР Н, , м.ч.: 1.52 (6Н, д, СН3), 1.92 (3Н, с, СН3), 2.15 (3Н, с, СН3), 4.48 (1H, м, СН), 7.04 (1H, с, Н-5). Знайдено, %: С 69.61; Н 10.27; N 19.95. C8H14N2. Вирахувано, %: С 69.52; Н 10.21; N 20.27. 4 Приклад 3. 1-третбутил-3.4-диметилпіразол. 1 Вихід 79 %, т. кип. 210-212 °C. Спектр ЯМР Н, , м.ч.: 1.55 (9Н, с, СН3), 1.96 (3Н, с, СН3), 2.16 (3Н, с, СН3), 7.01 (1H, с, Н-5). Знайдено, %: С 71.15; Н 10.64; N 18.36. C9H16N2. Вирахувано, %: С 71.01; Н 10.59; N 18.40. Приклад 4. 1,4-Диметил-3-етилпіразол. Вихід 1 75 %, т. кип. 165-167 °C. Спектр ЯМР Н, , м.ч.: 1.27 (3Н, т, СН3), 2.19 (3Н, с, СН3), 2.38 (2Н, к, СН2), 3.68 (3Н, с, СН3), 7.02 (1H, с, Н-5). Знайдено, %: С 67.74; Н 9.72; N 22.49. C7H12N2. Вирахувано, %: С 67.70; Н 9.74; N 22.56. Приклад 5. 1,4-Диметил-3-третбутилпіразол. 1 Вихід 82 %, т. кип. 203-205 °C. Спектр ЯМР Н, , м.ч.: 1.33 (9Н, с, СН3), 2.15 (3Н, с, СН3), 3.71 (3Н, с, СН3), 6.97 (1H, с, Н-5). Знайдено, %: С 70.95; Н 10.54; N 18.44. C9H16N2. Вирахувано, %: С 71.01; Н 10.59; N 18.40. Приклад 6. 1-Метил-3-пропіл-4-етилпіразол. 1 Вихід 73 %, т. кип. 214-216 °C. Спектр ЯМР Н, , м.ч.: 0.94 (3Н, м, СН3), 1.21 (3Н, т, СН3), 1.62 (2Н, м, СН2), 2.37 (2Н, к, СН2), 2.55 (2Н, м, СН2), 3.73 (3Н, с, СН3), 7.11 (1Н, с, Н-5). Знайдено, %: С 71.12; Н 10.61; N 18.37. C9H16N2. Вирахувано, %: С 71.01; Н 10.59; N18.40. Приклад 7. 2-Метил-2,4,5,6тетрагідроциклопента[с]піразол. Вихід 76 %, т. кип. 1 207-210 °C. Спектр ЯМР Н, , м.ч.: 2.30 (2Н, м, СН2), 3.03 (4Н, м, СН2), 3.87 (3Н, с, СН3), 7.05 (1H, с, Н-5). Знайдено, %: С 68.79; Н 8.27; N 22.87. C7H10N2. Вирахувано, %: С 68.82; Н 8.25; N 22.93. Приклад 8. 2-ізопропіл-2,4,5,6тетрагідроциклопента[с]піразол. Вихід 81 %, т. кип. 1 225-227 °C. Спектр ЯМР Н, , м.ч.: 1.53 (6Н, д, СН3), 2.28 (2Н, м, СН2), 3.00 (4Н, м, СН2), 4.37 (1H, м, СН), 7.01 (1H, с, Н-5). Знайдено, %: С 72.04; Н 9.41;N 18.62. C9H14N2. Вирахувано, %: С 71.96; Н 9.39; N 18.65. Приклад 9. 2-Метил-4,5,6,7-тетрагідро-2Ніндазол. Вихід 72 %, т. кип. 119-121 °С/20 мм.рт.ст. 1 Спектр ЯМР Н, , м.ч.: 1.72 (4Н, м, СН2), 2.49 (2Н, м, СН2), 2.63 (2Н, м, СН2), 3.79 (3Н, с, СН3), 7.00 (1H, с, Н-5). Знайдено, %: С 70.62; Н 8.91; N 20.52. C8H12N2. Вирахувано, %: С 70.55; Н 8.88; N 20.57. Приклад 10. 2-третбутил-4,5,6,7-тетрагідро2Н-індазол. Вихід 82 %, т. кип. 145-146 °C/20 1 мм.рт.ст. Спектр ЯМР Н, , м.ч.: 1.58 (3Н, с, СН3), 1.70 (4Н, м, СН2), 2.30 (2Н, м, СН2), 2.50 (2Н, м, СН2), 7.00 (1H, с, Н-5). Знайдено, %: С 74.17; Н 10.22; N 15.77. C11H18N2. Вирахувано, %: С 74.11; Н 10.18;N 15.71. Приклад 11. 2-Метил-2,4,5,6,7,8гексагідроциклогепта[с]піразол. Вихід 74 %, т. кип. 1 134-135 °C/20 мм.рт.ст. Спектр ЯМР Н, , м.ч.: 1.40 (6Н, м, СН2), 2.79 (4Н, м, СН2), 3.82 (3Н, с, СН3), 7.01 (1H, с, Н-5). Знайдено, %: С 72.04; Н 9.41; N 18.72. C9H14N2. Вирахувано, %: С 71.96; Н 9.39; N 18.65. Джерела інформації: 1. Condesed heterocyclic compounds as PDE-IV inhibitors for the treatment of inflammory and allergic disorders./ Glenmark Pharmaceuticals LTD// WO 2004016596 2004-02-26. 2. Fused heterocyclic compounds./ Bristol-Myers Squibb// US 20050250783 2005-11-10. 5 3. Oxime derivative hydroyethylamine aspartyl protease inhibitors./ Elan Pharmaceuticals inc.// WO 2006010094 2006-01-26. 4. Idazole compounds./ Chng-Min Sun, MinLiang// US 2008032501 2008-06-05. 5. Heterocyclic cyclopamine analogs and metods of use thereof/ Infiniti Pharmaceuticals inc.// WO 2008109184 2008-09-12. 6. Novel compounds./ Glaxo Group LTD// WO 2009109608 2009-09-11. Комп’ютерна верстка М. Ломалова 66523 6 7. Albright J.D., Goldman L. Proton magnetic resonance spectra of isomeric N-Methyl-3(5)pyrazoles // J.Org.Chem. - 1966. - Vol.31, - P.273276. 8. Гранберг И.И., Кост А.Н., Ягужинский Л.С. Новый метод синтеза тетрагидроиндазолов и индазолов. // ЖОХ. - 1959. - Т. 29. - С.2537-2541. 9. Chou T.S., Chen H.Ch., Yang W.Ch, Li W.S, Lee S.J. Type-two intramolecular Diels-Alder reactions of pyrazolo-o-quinodimethanes. // J.Org.Chem. - 2000. - Vol.65, - P.5760-5767. Підписне Тираж 23 прим. Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 1,2,3-trialkylpyrazoles and carbocyclic analogs thereof
Автори англійськоюIvonin Serhii Pavlovych
Назва патенту російськоюСпособ получения 1,3,4-триалкилпиразолов и их карбоциклических аналогов
Автори російськоюИвонин Сергей Павлович
МПК / Мітки
МПК: C07D 231/22
Мітки: спосіб, одержання, аналогів, карбоциклічних, 1,3,4-триалкілпіразолів
Код посилання
<a href="https://ua.patents.su/3-66523-sposib-oderzhannya-134-trialkilpirazoliv-ta-kh-karbociklichnikh-analogiv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 1,3,4-триалкілпіразолів та їх карбоциклічних аналогів</a>
Попередній патент: Змішувач сипучих матеріалів з малими кількостями рідини
Наступний патент: Установка для одержання вуглецевих наноструктур
Випадковий патент: Гелеподібна та порошкоподібна композиції, способи їх одержання та способи використання в галузі сільського господарства та гігієни







