Спосіб одержання 1,1′-дибромо-5-арил-1,2,4-триазоло[4,3-с]бензо[е]телуротіазинів
Номер патенту: 88251
Опубліковано: 25.09.2009
Автори: Лендєл Василь Георгійович, Сливка Михайло Васильович, Русин Іван Федорович
Формула / Реферат
1. Спосіб одержання 1,1'-дибромо-5-арил-1,2,4-триазоло[4,3-с]бензо[е]телуротіазинів формули 2 (а, б), який відрізняється тим, що сполуки формули 1 (а, б) піддають взаємодії з телур(IV) бромідом та наступній внутрішньомолекулярній циклізації з утворенням цільових продуктів:
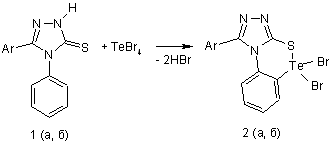 ,
,
де Аr = С6Н5 (1а, 2а), 4-СН3С6Н4 (1б, 2б).
2. Спосіб за п. 1, який відрізняється тим, що додатково використовують розчинник – льодяну оцтову кислоту, взаємодію проводять 1 годину, а цільові продукти кристалізують від 24 до 72 годин.
Текст
1. Спосіб одержання 1,1'-дибромо-5-арил1,2,4-триазоло[4,3-с]бензо[е]телуротіазинів формули 2 (а, б), який відрізняється тим, що сполуки формули 1 (а, б) піддають взаємодії з телур(IV) , де Аr = С6Н5 (1а, 2а), 4-СН3С6Н4 (1б, 2б). 2. Спосіб за п. 1, який відрізняється тим, що додатково використовують розчинник – льодяну оцтову кислоту, взаємодію проводять 1 годину, а цільові продукти кристалізують від 24 до 72 годин. Винахід відноситься до органічної хімії, а саме до способів одержання бензотелуровмісних конденсованих гетероциклічних систем. Відомі два підходи при синтезі телуровмісних конденсованих гетероциклічних систем. Найбільш поширеним є метод електрофільного заміщення в ароматичному ядрі при дії тетрагалогенідів телуру на ароматичні системи з наступним дегалогенуванням утворених проміжних адуктів [1]. Цей прийом успішно використовується при синтезі телурофенів та арілтелургалогенідів. Окрім цього, описаний метод характеризується, як правило, багатостадійністю, що призводить до ускладнення експерименту. Використовується також метод одержання телуровмісних гетероциклів шляхом введення елементарного телуру [2]. Цей спосіб характеризується використанням як правило жорстких умов і використовується для одержання телурофенів. Найбільш близьким за технічною сутністю до заявляємого є спосіб електрофільної гетероциклізації, який включає в себе електрофільну дію телур (IV) броміду на тіопохідні гетероциклів, яка передбачає електрофільне приєднання по кратному зв'язку з наступною внутрішньомолекуляр ною атакою нуклеофільного центру, як правило гетероатому [3]. Цей прийом характеризується універсальністю щодо природи гетероциклу, і є прийнятний лише для процесів, які включають стадію приєднання електрофільного реагенту до кратного зв'язку, тобто непридатний для утворення бензотелуровмісних гетероциклів. Недоліком цього способу є виключення можливості участі в процесі ароматичних фрагментів, для яких нехарактерні реакції приєднання при звичайних умовах. Завданням винаходу є розробка способу одержання бензотелуровмісних конденсованих гетероциклічних систем, який характеризується простотою експерименту, доступністю реагентів та високими виходами, так як відомі методи створення телуровмісних конденсованих гетероциклічних систем є неприйнятними для їх синтезу. Поставлене завдання досягається таким чином, що в способі одержання 1,1'-дибромо-5-арил1,2,4-триазоло[4,3-с]-бензо[е]телуротіазинів формули 2 (а,б), який відрізняється тим, що сполуки формули 1 (а,б) піддають взаємодії з телур (IV) бромідом та наступній внутрішньомолекулярній циклізації з утворенням цільових продуктів. бромідом та наступній внутрішньомолекулярній циклізації з утворенням цільових продуктів: H N Ar N N N N S + TeBr4 Ar - 2HBr N S Te Br Br UA (11) 88251 (13) C2 2 (а, б) (19) 1 (a, б) 3 88251 4 їдного фрагменту 1,2,4-триазол-3-тіонів 1 (а,б), що призводить до утворення аддукту А, який зазнає внутрішньомолекулярної циклізації за рахунок електрофільної атаки відносно позитивно зарядженим атомом Телуру екзоциклічного атому Сульфуру. Склад синтезованих бензотелуровмісних конденсованих гетероциклічних систем 2 (а,б) підтверджено даними елементного аналізу; індивідуальність методом тонкошарової хроматографії (ТШХ); будову доведено методом спектроскопії протонного магнітного резонансу (ПМР) високої Поставлене завдання досягається також тим, роздільної здатності (300МГц) та хімічними перещо додатково використовують розчинник - льодятвореннями (зокрема, обробка 1,2,4-триазоло[4,3ну оцтову кислоту, взаємодію проводять 1 годину, с]бензо-[е]телуротіазинів 2 (а,б) ацетоном чи 10%а цільові продукти кристалізують від 24 до 72 гоним водним розчином натрій сульфіду призводить дин. до дебромування (аддукт В) з наступною екструзіМодельні об'єкти - 4-феніл-5-арил-1,2,4єю телуру і утворенням бензотіазолотриазолів 3 триазол-3-тіони 1 (а,б) можна отримати майже з (а,б), фізико-хімічні характеристики яких ідентичні кількісними виходами методом, описаним в роботі описаним [4]). [4]. Суть розробленого способу одержання бензоПриклад. телуровмісних конденсованих гетероциклічних Схема одержання похідних 1,1-дибромо-1,2,4систем полягає в тому, що на першій стадії відбутриазоло[4,3-с]бензо[е]-телуротіазину 2 (а,б) вається електрофільна атака телур (IV) броміду орто-Карбону 4-фенільного замісника фенілтіоуре 1,1'-Дибромо-5-арил-1,2,4-триазоло[4,3с]бензо[е]телуротіазини 2 (а,б). До розчинів триазолів 1 (а,б) (0.003 моль) в 120мл льодяної кислоти оцтової при постійному перемішуванні додають по краплям розчин 0.003 моль телур (IV) оксиду в 0.012 моль кислоти гідрогенобромідної, доведений до об'єму 20мл льодяною оцтовою кислотою або розчин 0.003 моль телур (IV) броміду в 50мл льодяної кислоти оцтової. Суміш перемішують при кімнатній температурі протягом 1год. Сполуки 1 (а,б) кристалізуються з реакційного середовища протягом 24-72 годин; осад що випав, відфільтровують, промивають оцтовою кислотою. 1,1’-Дибромо-5-феніл-1,2,4-триазоло[4.3с]бензо[е]телуротіазин (2а). Кристали жовтого кольору. Вихід 63.3%, Ттопл 205°С (з розкл.). Спектр ПМР в ДМСО-D6 (d, м.д., J, Гц): 7.18-7.36, 7.46-7.59 2м (9 Н, С6Н5 , С6Н4). Знайдено,%: С 31.79; Н 1.77; Вr 29.11; N 7.89. C14H9Br2N3STe. Вирахувано, %: С 31.21; Н 1.68; Вr 29.66; N 7.80. Rf 0.75 (етанол : хлороформ = 2:1). 1,1'-Дибромо-5-(4-метилфеніл)-1,2.4триазоло[4,3-с]бензо[е]телуротіазин (2б). Вихід 60.0%, ттопл. 185°С (з розкл.). Спектр ПМР в ДМСОD6 (d, м.д., J, Гц): 2.32 с (3Н, СН3); 7.11-7.39, 7.487.62 2м (8Н, 4-СН3С6Н4, С6Н4). Знайдено, %: С 32.88; Н 2.07; Вr 28.67; N 7.66. C15H11Br2N3STe. Вирахувано, %: С 32.59; Н 2.01; Вr 28.91; N 7.60. Rf 0.67 (етанол : хлороформ =1:1). Схема хімічних перетворень на основі похідних 1,1’-дибромо-1,2,4-триазоло[4,3с]бензо[е]телуротіазину 2 (а,б) 5 88251 Сполуки 2 (а,б) (0.001 моль) в 30мл ацетону (чи в 30мл 10%-ного водного розчину натрій сульфіду) перемішують протягом однієї години; розчинник упарюють; із сухого залишку екстрагують трьома порціями по 10мл гарячого етанолу бензотіазолотриазоли 3 (а,б), які потім виділяють із об'єднаного екстракту шляхом видалення розчинника. Фізико-хмічні характеристики бензотіазолотриазолів 3 (а,б) ідентичні описаним [4]. Таким чином, було розроблено спосіб взаємодії телур (IV) броміду із гетероциклами, які містять фенілтіоуреїдний фрагмент, що забезпечило замикання бензотелуротіазинового циклу з утворенням трициклічної ангулярної бензотелуровмісної конденсованої гетероциклічної системи при звичайних умовах без використання важкодоступних реагентів та складного апаратурного оформлення. Використання запропонованого способу електрофільної дії телур (IV) броміду на похідні гетероциклів, що містять фенілтіоуреїдний фрагмент, забезпечує селективність утворення бензотелуровмісних конденсованих гетероциклічних систем, для синтезу яких відомі методи створення телуровмісних гетероциклів є неприйнятними. Спосіб Комп’ютерна верстка В. Мацело 6 може бути використаний для p-електронодонорних гетероциклічних систем. Спосіб може бути використаний у науководослідних хімічних та хіміко-фармацевтичних лабораторіях. Джерела інформації: 1. В.А.Потапов, С.В.Амосова. Новые способы получения селен- и теллурорганических соединений из элементных халькогенов. // Журнал органической химии. - 2003. - Т.39. Вып.10. - С.1449 1455. 2. Садеков И.Д., Максименко А.А., Минкин В.И. Химия теллурорганических соединений. - Издательство Ростовского университета. - 1983. - 328с. 3. Хрипак С.М., Русин І.Ф., Сливка М.В., Лендєл В.Г. Взаємодія телуровмісних тієно[3,2е][1,3]тіазоло[3,2-а]піримідин-11-Ій галогенідів з Онуклеофілами. // Укр.Хім.Журн. - 2007. - т.73, №3. С.39-43. Прототип. 4. С.М. Хрипак, В.И. Станинец, М.В. Сливка, Ю.Л. Зборовский. Окислительная гетероциклизация натриевых солей 3-меркапто-4-фенил-3//1,2,4-триазолов. // Укр. Хім. Журн. - 2001. - т.67, №4. - С.110-113. Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 1,1'-dibromo-5-aryl-1,2,4-triazolo[4,3-с]benzo[е]telluro-thiazines
Автори англійськоюSlyvka Mykhailo Vasyliovych, Rusyn Ivan Fedorovych, Lendiel Vasyl Heorhiiovych
Назва патенту російськоюСпособ получения 1,1'-дибромо-5-арил-1,2,4-триазоло[4,3-с]бензо[е]теллуротиазинов
Автори російськоюСливка Михаил Васильевич, Русин Иван Федорович, Лендел Василий Георгиевич
МПК / Мітки
МПК: C07D 517/00
Мітки: спосіб, одержання, 1,1'-дибромо-5-арил-1,2,4-триазоло[4,3-с]бензо[е]телуротіазинів
Код посилання
<a href="https://ua.patents.su/3-88251-sposib-oderzhannya-11-dibromo-5-aril-124-triazolo43-sbenzoetelurotiaziniv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 1,1′-дибромо-5-арил-1,2,4-триазоло[4,3-с]бензо[е]телуротіазинів</a>
Попередній патент: Акрилова композиція для кріплення анкерних болтів
Наступний патент: Спосіб корегування середовища знаходження біологічного об’єкта та пристрій для його здійснення
Випадковий патент: Склад для тістечка повітряного "грильяж"







