Карбаматні похідні хінуклідину і фармацевтична композиція, яка містить ці сполуки
Номер патенту: 85541
Опубліковано: 10.02.2009
Автори: Буіл Альберо Марія Антонія, Фернандес Форнер Марія Долорс, Прат Кіньонес Марія
Формула / Реферат
1. Сполука, яка являє собою четвертинні амонієві солі карбамату формули (II)
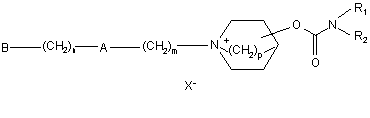 , (ІІ)
, (ІІ)
у якій
R1 означає групу, вибрану з фенілу, 2-фурилу, 3-фурилу, 2-тієнілу, 3-тієнілу, бензилу, фуран-2-ілметилу, фуран-3-ілметилу, тіофен-2-ілметилу, тіофен-3-ілметилу;
R2 означає групу, вибрану з необов'язково заміщеного нижчого алкілу, необов'язково заміщеного нижчого алкенілу, необов'язково заміщеного нижчого алкінілу, насиченого або ненасиченого циклоалкілу, насиченого або ненасиченого циклоалкілметилу, фенілу, бензилу, фенетилу, фуран-2-ілметилу, фуран-3-ілметилу, тіофен-2-ілметилу, тіофен-3-ілметилу, піридилу і піридилметилу; де карбоциклічні фрагменти в циклоалкільній, циклоалкілметильній, фенільній, бензильній або фенетильній групах можуть бути необов'язково місточковими або спряженими з іншим насиченим, ненасиченим або ароматичним карбоциклічним фрагментом або з циклічним фрагментом, який включає атоми вуглецю і 1 або 2 атоми кисню;
циклічні групи, які присутні у R1 і R2, необов'язково заміщені одним, двома або трьома замісниками, вибраними з галогену, лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкокси, -SH, лінійного або розгалуженого необов'язково заміщеного нижчого алкілтіо, нітро, ціано, -NR'R", -CO2R', -С(О)-NR'R", -N(R"')C(O)-R', -N(R'")-C(O)NR'R", де R', R" і R'" кожен незалежно являє собою атом водню або лінійну або розгалужену, необов'язково заміщену нижчу алкільну групу, або R' і R" разом з атомом, до якого вони приєднані, утворюють циклічну групу;
р означає 1 або 2, і карбаматна група приєднана в положеннях 2, 3 або 4 азоніабіциклічної кільцевої системи,
m означає ціле число від 0 до 8;
n означає ціле число від 0 до 4;
А являє собою групу, вибрану з -СН2-, -CH=CR'-, -CR'=CH-, -CR'R"-, -C(O)-, -О-, -S-, -S(O)-, -S(O)2- і -NR'-, де R' і R" є такими, як визначено вище;
В являє собою атом водню або групу, вибрану з лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкокси, ціано, нітро, -CH=CR'R", -C(O)OR', -OC(O)R' -SC(O)R' -C(O)NR'R", -NR'C(O)OR", -NR'C(O)NR", циклоалкілу, фенілу, нафталенілу, 5,6,7,8-тетрагідронафталенілу, бензо[1.3]діоксолілу, гетероарилу або гетероциклілу; R' і R" є такими, як визначено вище; і де циклічні групи, представлені як В, необов'язково заміщені одним, двома або трьома замісниками, вибраними з галогену, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, фенілу, -OR', -SR', -NR'R", -NHCOR', -CONR'R", -CN, -NO2 і -COOR'; R' і R" є такими, як визначено вище;
X- являє собою фармацевтично прийнятний аніон моно- або полівалентної кислоти;
включаючи всі індивідуальні стереоізомери формули (II) і їх суміші;
за умови, що в тому випадку, коли циклічна група, яка присутня у R1, є незаміщеною або має тільки один замісник, то R2 має принаймні один замісник; з додатковою умовою, що сполука формули (II) не є однією з наступних сполук:
l-aлiл-3-(R)-[бeнзил(4-фтopфeнiл)кapбoмoїлoкcи]-1-aзoнiaбiциклo[2,2,2]oктaн трифторацетат,
3-(R)-[бензил(4-фторфеніл)карбомоїлокси]-1-(3-фенілпропіл)-1-азоніабіцикло[2,2,2]октан трифторацетат,
1-аліл-3-(R)-[бензил-n-толілкарбомоїлокси]-1-азоніабіцикло[2,2,2]октан трифторацетат,
3-(R)-[бензил-n-толілкарбомоїлокси]-1-(3-фенілпропіл)-1-азоніабіцикло[2,2,2]октан трифторацетат.
2. Сполука формули (II) за п. 1, у якій в тому випадку, коли р означає 2;
карбаматна група приєднана в положенні 3 азоніабіциклічної кільцевої системи, яка має (3R)-конфігурацію;
R1 являє собою фенільну групу, яка необов'язково заміщена атомом фтору або метильною групою;
R2 являє собою незаміщену циклогексилметильну групу або бензильну групу, яка необов'язково заміщена одним або трьома атомами фтору;
і X- означає йод;
то тоді послідовність B-(CH2)n-A-(CH2)m- не може являти собою метильну групу.
3. Сполука формули (II) за будь-яким з пунктів 1-2, за умови, що вказана сполука не є однією з наступних сполук:
(3R)-3-[(4-фторбензил)фенілкарбамоїлокси]-1-метил-1-азоніабіцикло[2.2.2]октан йодид;
(3R)-3-(бензил-о-толілкарбамоїлокси)-1-метил-1-азоніабіцикло[2.2.2]октан йодид;
(3R)-1-метил-3-[о-толіл(2,4,5-трифторбензил)карбамоїлокси]-1-азоніабіцикло[2.2.2]октан йодид;
(3R)-3-[(4-фторбензил)-м-толілкарбамоїлокси]-1-метил-1-азоніабіцикло[2.2.2]октан йодид;
(3R)-3-[бензил(2-фторфеніл)карбамоїлокси]-1-метил-1-азоніабіцикло[2.2.2]октан йодид;
(3R)-3-[циклогексилметил(2-фторфеніл)карбамоїлокси]-1-метил-1-азоніабіцикло[2.2.2]октан йодид.
4. Сполука формули (II) за будь-яким з пп. 1-3, у якій R1 являє собою групу, вибрану з фенілу, 2-тієнілу, 3-тієнілу, тіофен-2-ілметилу, тіофен-3-ілметилу, фуран-2-ілметилу або фуран-3-ілметилу, причому циклічні групи, які є в R1, необов'язково заміщені замісниками в кількості від одного до трьох, вибраними з фтору, хлору, брому, метилу, метокси, трифторметилу, етилу, трет-бутилу, гідрокси і ціано.
5. Сполука формули (II) за п. 4, у якій R1 являє собою групу, вибрану з фенілу, 2-фторфенілу, 3-фторфенілу, 4-фторфенілу, 3-метилфенілу, 4-метилфенілу, 2,5-дифторфенілу, 2,6-дифторфенілу, 2,4,5-трифторфенілу, 5-метилфуран-2-ілметилу, 4-фтор-2-метилфенілу, 3-фтор-4-метоксифенілу, 3-метилтіофен-2-ілметилу, 4,5-диметилтіофен-2-ілметилу, тіофен-3-ілметилу, 5-метилфуран-2-ілметилу, 5-метил-2-трифторметилфуран-3-ілметилу і 2,5-диметилфуран-3-ілметилу.
6. Сполука формули (II) за будь-яким з пп. 1-5, у якій R2 являє собою групу пент-4-еніл, пентил, бутил, аліл, бензил, тіофен-2-ілметил, тіофен-3-ілметил, фуран-2-ілметил, фуран-3-ілметил, фенетил, циклопентил, циклогексил або циклогексилметил, причому циклічні групи, які присутні у R2, необов'язково заміщені замісниками в кількості від одного до трьох, вибраними з фтору, хлору, брому, метилу, метокси, трифторметилу, етилу, трет-бутилу, гідрокси і ціано.
7. Сполука за п. 6, у якій R2 являє собою групу, вибрану з 3-фторбензилу, 2,4,5-трифторбензилу, 3,4,5-трифторбензилу, 5-бромтіофен-2-ілметилу, 3,4-диметоксифенілетилу, 3-метилтіофен-2-ілметилу, тіофен-3-ілметилу, 4-бром-5-метилтіофен-2-ілметилу, 4,5-диметилфуран-2-ілметилу, фуран-3-ілметилу, 2-фтор-4-метоксибензилу, 2-(4-фторфеніл)етилу, бутилу, пент-4-енілу і циклопентилу.
8. Сполука формули (II) за будь-яким з пп. 1-7, у якій А являє собою -СН2-, значення як m, так і n дорівнює 0, і В являє собою групу, вибрану з лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкокси, ціано, нітро, -CH=CR'R", -C(O)OR', -OC(O)R', -SC(O)R', -C(O)NR'R", -NR'C(O)OR", -NR'C(O)NR", циклоалкілу, фенілу, нафталенілу, 5,6,7,8-тетрагідронафталенілу, бензо[1.3]діоксолілу, гетероарилу або гетероциклілу; причому R' і R" є такими, як вказано в п. 1; і де циклічні групи, позначені як В, необов'язково заміщені одним, двома або трьома замісниками, вибраними з галогену, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, фенілу, -OR', -SR', -NR'R", -NHCOR', -CONR'R", -CN, -NO2 і -COOR'; R' і R" є такими, як визначено вище.
9. Сполука формули (II) за будь-яким з пп. 1-7, у якій А являє собою -СН2-, В є таким, як визначено в п. 1, і значення принаймні однієї з величин m або n не дорівнює 0.
10. Сполука формули (II) за будь-яким з пп. 1-7, у якій В означає тіофен-2-ільну групу або фенільну групу, яка необов'язково заміщена замісниками в кількості від одного до трьох, вибраними з атомів галогену або гідрокси, метилу, або груп -СН2ОН, -ОМе, -NMe2, -NHCOMe, -CONH2, -CN, -NO2, -COOMe або -CF3.
11. Сполука за п. 10, у якій В являє собою фенільну, 4-фторфенільну, 3-гідроксифенільну або тіофен-2-ільну групу.
12. Сполука формули (II) за будь-яким з пп. 1-7, 10 або 11, у якій n=0 або 1; m означає ціле число від 1 до 6; і
А являє собою групу -СН2, -СН=СН-, -CO-, -NMe-, -О- або -S-.
13. Сполука формули (II) за п. 12, у якій m означає 1, 2 або 3, і А являє собою групу -СН2, -СН=СН-, або -О-.
14. Сполука формули (II) за будь-яким з пп. 1-7, у якій послідовність В-(СН2)n-А-(СН2)m- являє собою групу, вибрану з 3-феноксипропілу, 2-феноксіетилу, 3-фенілалілу, фенетилу, 3-фенілпропілу, 3-(3-гідроксифенокси)пропілу, 3-(4-фторфенокси)пропілу, 3-тіофен-2-ілпропілу, алілу, гептилу, 3-ціанопропілу і метилу.
15. Сполука формули (II) за будь-яким з пп. 1-14, у якій X- являє собою хлорид-аніон, бромід-аніон, трифторацетат-аніон або метансульфонат-аніон.
16. Сполука формули (II) за будь-яким з попередніх пунктів, у якій р означає 2.
17. Сполука формули (II) за будь-яким з попередніх пунктів, у якій азоніабіциклічна кільцева система заміщена в 3-положенні.
18. Сполука формули (II) за п. 17, у якій атом вуглецю в 3-положенні азоніабіциклічної кільцевої системи має R-конфігурацію.
19. Сполука формули (II) за п. 17, у якій атом вуглецю в 3-положенні азоніабіциклічної кільцевої системи має S-конфігурацію.
20. Сполука за будь-яким з попередніх пунктів, яка являє собою окремий ізомер.
21. Сполука формули (II) за п. 1, яка являє собою одну з наступних сполук:
(3R)-3-[(3-фторбензил)-(3-фторфеніл)карбамоїлокси]-1-(2-феноксіетил)-1-азоніабіцикло[2.2.2]октан бромід;
(3R)-3-[(3-фторбензил)-(3-фторфеніл)карбамоїлокси]-1-(3-фенілпропіл)-1-азоніабіцикло[2.2.2]октан бромід;
(3R)-1-(2-феноксіетил)-3-[м-толіл-(2,4,5-трифторбензил)карбамоїлокси]-1-азоніабіцикло[2.2.2]октан бромід;
(3R)-1-(3-фенілпропіл)-3-[м-толіл-(2,4,5-трифторбензил)карбамоїлокси]-1-азоніабіцикло[2.2.2]октан бромід;
(3R)-3-[(3-фторфеніл)-(3,4,5-трифторбензил)карбамоїлокси]-1-(2-феноксіетил)-1-азоніабіцикло[2.2.2]октан бромід;
(3R)-1-аліл-3-[[2-(3,4-диметоксифеніл)етил]-(5-метилфуран-2-ілметил)карбамоїлокси]-1-азоніабіцикло[2.2.2]октан бромід;
(3R)-3-[(5-бромтіофен-2-ілметил)-(2,4,5-трифторфеніл)карбамоїлокси]-1-(3-феноксипропіл)-1-азоніабіцикло[2.2.2]октантрифторацетат;
(3R)-3-[[2-(3,4-диметоксифеніл)етил]-(5-метилфуран-2-ілметил)карбамоїлокси]-1-(4-етоксикарбонілбутил)-1-азоніабіцикло[2.2.2]октан трифторацетат;
(3R)-3-[(4-фтор-2-метилфеніл)-(3-метилтіофен-2-ілметил)карбамоїлокси]-1-(2-феноксіетил)-1-азоніабіцикло[2.2.2]октан трифторацетат;
(3R)-3-[(3-фтор-4-метоксифеніл)тіофен-3-ілметилкарбамоїлокси]-1-(3-фенілаліл)-1-азоніабіцикло[2.2.2]октан трифторацетат;
(3R)-1-фенетил-3-[тіофен-3-ілметил(2,4,5-трифторбензил)карбамоїлокси]-1-азоніабіцикло[2.2.2]октантрифторацетат;
(3R)-3-[(4-бром-5-метилтіофен-2-ілметил)-(3-метилтіофен-2-ілметил)карбамоїлокси]-1-(3-фенілпропіл)-1-азоніабіцикло[2.2.2]октантрифторацетат;
(3R)-3-[(4,5-диметилфуран-2-ілметил)-(5-метилфуран-2-ілметил)карбамоїлокси]-1-[3-(3-гідроксифенокси)пропіл]-1-азоніабіцикло[2.2.2]октан трифторацетат;
(3R)-1-[3-(4-фторфенокси)пропіл]-3-[фуран-3-ілметил-(5-метил-2-трифторметилфуран-3-ілметил)карбамоїлокси]-1-азоніабіцикло[2.2.2]октан трифторацетат;
(3R)-3-[(2,5-диметилфуран-3-ілметил)-(2-фтор-4-метоксибензил)карбамоїлокси]-1-(3-тіофен-2-ілпропіл)-1-азоніабіцикло[2.2.2]октан трифторацетат;
(3R)-1-аліл-3-[2-(4-фторфеніл)етил]-(3-метилтіофен-2-ілметил)карбамоїлокси]-1-азоніабіцикло[2.2.2]октан трифторацетат;
(3R)-3-[бутил-(2,5-дифторфеніл)карбамоїлокси]-1-гептил-1-азоніабіцикло[2.2.2]октан трифторацетат;
(3R)-1-(3-ціанопропіл)-3-[(2,6-дифторфеніл)пент-4-енілкарбамоїлокси]-1-азоніабіцикло[2.2.2]октан трифторацетат;
(3R)-3-[(3-фторфеніл)-(3,4,5-трифторбензил)карбамоїлокси]-1-(3-фенілпропіл)-1-азоніабіцикло[2.2.2]октан бромід;
(3R)-3-[(5-етилтіофен-2-ілметил)-(3-метилтіофен-2-ілметил)карбамоїлокси]-1-(3-фенілпропіл)-1-азоніабіцикло[2.2.2]октан бромід;
(3R)-3-[[2-(3,4-диметоксифеніл)етил]-(5-метилфуран-2-ілметил)карбамоїлокси]-1-(4-етоксикарбонілбутил)-1-азоніабіцикло[2.2.2]октан форміат;
(3R)-3-[(4-фтор-2-метилфеніл)-(3-метилтіофен-2-ілметил)карбамоїлокси]-1-(2-феноксіетил)-1-азоніабіцикло[2.2.2]октан бромід;
(3R)-3-[(3-фтор-4-метоксифеніл)тіофен-3-ілметилкарбамоїлокси]-1-(3-фенілаліл)-1-азоніабіцикло[2.2.2]октан бромід;
(3R)-1-аліл-3-[2-(4-фторфеніл)етил]-(3-метилтіофен-2-ілметил)карбамоїлокси]-1-азоніабіцикло[2.2.2]октан бромід.
22. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-21 у суміші з фармацевтично прийнятним носієм або розріджувачем.
23. Сполука за будь-яким з пп. 1-21 для лікування хворобливого стану або захворювання, стан пацієнта при яких може поліпшуватися при антагоністичному впливі на М3 мускаринові рецептори.
24. Застосування сполуки за будь-яким з пп. 1-21 для одержання лікарського засобу, призначеного для лікування хворобливого стану або захворювання, стан пацієнта при яких може поліпшуватися при антагоністичному впливі на М3 мускаринові рецептори.
25. Застосування за п. 24, у якому хворобливий стан являє собою респіраторне, урологічне або шлунково-кишкове захворювання, порушення або розлад.
26. Спосіб лікування пацієнта, який має хворобливий стан або захворювання, стан пацієнта при яких може поліпшуватися при антагоністичному впливі на М3 мускаринові рецептори, при якому вводять вказаному пацієнту ефективну кількість сполуки за будь-яким з пп. 1-21.
27. Спосіб за п. 26, у якому хворобливий стан являє собою респіраторне, урологічне або шлунково-кишкове захворювання, порушення або розлад.
28. Комбінований продукт, який містить (і) сполуку за будь-яким з пп. 1-21; і
(іі) іншу сполуку, ефективну при лікуванні респіраторного, урологічного або шлунково-кишкового захворювання або розладу, для одночасного, окремого або послідовного використання.
29. Комбінований продукт за п. 28, який містить (і) сполуку за будь-яким з пп. 1-21; і
(іі) ![]() -агоніст, стероїд, протиалергічний лікарський засіб, інгібітор фосфодіестерази IV і/або антагоніст лейкотриєну D4 (LTD4) для одночасного, окремого або послідовного використання при лікуванні респіраторного захворювання.
-агоніст, стероїд, протиалергічний лікарський засіб, інгібітор фосфодіестерази IV і/або антагоніст лейкотриєну D4 (LTD4) для одночасного, окремого або послідовного використання при лікуванні респіраторного захворювання.
Текст
1. Сполука, яка являє собою четвертинні амонієві солі карбамату формули (II) UA 2 (19) 1 C2 (54) КАРБАМАТНІ ПОХІДНІ ХІНУКЛІДИНУ І ФАРМАЦ ЕВТИЧНА КОМПОЗИЦІЇ, ЯКА МІСТИТЬ ЦІ СПОЛУКИ 3 85541 заміщеного нижчого алкокси, -SH, лінійного або розгалуженого необов'язково заміщеного нижчого алкілтіо, нітро, ціано, -NR'R", -CO2R', -С(О)-NR'R", N(R"')C(O)-R', -N(R'")-C(O)NR'R", де R', R" і R'" кожен незалежно являє собою атом водню або лінійну або розгалужену, необов'язково заміщену нижчу алкільну групу, або R' і R" разом з атомом, до якого вони приєднані, утворюють циклічну групу; р означає 1 або 2, і карбаматна група приєднана в положеннях 2, 3 або 4 азоніабіциклічної кільцевої системи, m означає ціле число від 0 до 8; n означає ціле число від 0 до 4; А являє собою гр упу, вибрану з -СН2-, -CH=CR'-, CR'=CH-, -CR'R"-, -C(O)-, -О-, -S-, -S(O)-, -S(O)2- і NR'-, де R' і R" є такими, як визначено вище; В являє собою атом водню або групу, вибрану з лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкокси, ціано, нітро, -CH=CR'R", -C(O)OR', OC(O)R' -SC(O)R' -C(O)NR'R", -NR'C(O)OR", NR'C(O)NR", циклоалкілу, фенілу, нафталенілу, 5,6,7,8-тетрагідронафталенілу, бензо[1.3]діоксолілу, гетероарилу або гетероциклілу; R' і R" є такими, як визначено вище; і де циклічні групи, представлені як В, необов'язково заміщені одним, двома або трьома замісниками, вибраними з галогену, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, фенілу, -OR', -SR', -NR'R", -NHCOR', -CONR'R", -CN, -NO2 і -COOR'; R' і R" є такими, як визначено вище; X- являє собою фармацевтично прийнятний аніон моно- або полівалентної кислоти; включаючи всі індивідуальні стереоізомери формули (II) і їх суміші; за умови, що в тому випадку, коли циклічна група, яка присутня у R1, є незаміщеною або має тільки один замісник, то R2 має принаймні один замісник; з додатковою умовою, що сполука формули (II) не є однією з наступних сполук: l-aлiл-3-(R)-[бeнзил(4-фтopфeнiл)кapбoмoїлoкcи]1-aзoнiaбiциклo[2,2,2]oктaн трифторацетат, 3-(R)-[бензил(4-фторфеніл)карбомоїлокси]-1-(3фенілпропіл)-1-азоніабіцикло[2,2,2]октан трифторацетат, 1-аліл-3-(R)-[бензил-n-толілкарбомоїлокси]-1азоніабіцикло[2,2,2]октан трифторацетат, 3-(R)-[бензил-n-толілкарбомоїлокси]-1-(3фенілпропіл)-1-азоніабіцикло[2,2,2]октан трифторацетат. 2. Сполука формули (II) за п.1, у якій в тому випадку, коли р означає 2; карбаматна група приєднана в положенні 3 азоніабіциклічної кільцевої системи, яка має (3R)конфігурацію; R1 являє собою фенільну групу, яка необов'язково заміщена атомом фтору або метильною групою; R2 являє собою незаміщену циклогексилметильну груп у або бензильну груп у, яка необов'язково заміщена одним або трьома атомами фтору; і X- означає йод; то тоді послідовність B-(CH2)n-A-(CH2) m- не може являти собою метильну групу. 4 3. Сполука формули (II) за будь-яким з пунктів 1-2, за умови, що вказана сполука не є однією з наступних сполук: (3R)-3-[(4-фторбензил)фенілкарбамоїлокси]-1метил-1-азоніабіцикло[2.2.2]октан йодид; (3R)-3-(бензил-о-толілкарбамоїлокси)-1-метил-1азоніабіцикло[2.2.2]октан йодид; (3R)-1-метил-3-[о-толіл(2,4,5трифторбензил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан йодид; (3R)-3-[(4-фторбензил)-м-толілкарбамоїлокси]-1метил-1-азоніабіцикло[2.2.2]октан йодид; (3R)-3-[бензил(2-фторфеніл)карбамоїлокси]-1метил-1-азоніабіцикло[2.2.2]октан йодид; (3R)-3-[циклогексилметил(2фтор феніл)карбамоїлокси]-1-метил-1азоніабіцикло[2.2.2]октан йодид. 4. Сполука формули (II) за будь-яким з пп.1-3, у якій R1 являє собою групу, вибрану з фенілу, 2тієнілу, 3-тієнілу, тіофен-2-ілметилу, тіофен-3ілметилу, фуран-2-ілметилу або фуран-3ілметилу, причому циклічні групи, які є в R1, необов'язково заміщені замісниками в кількості від одного до трьох, вибраними з фтору, хлор у, брому, метилу, метокси, трифторметилу, етилу, третбутилу, гідрокси і ціано. 5. Сполука формули (II) за п.4, у якій R1 являє собою групу, вибрану з фенілу, 2-фтор фенілу, 3фтор фенілу, 4-фтор фенілу, 3-метилфенілу, 4метилфенілу, 2,5-дифторфенілу, 2,6дифторфенілу, 2,4,5-трифтор фенілу, 5метилфуран-2-ілметилу, 4-фтор-2-метилфенілу, 3фтор-4-метоксифенілу, 3-метилтіофен-2-ілметилу, 4,5-диметилтіофен-2-ілметилу, тіофен-3-ілметилу, 5-метилфуран-2-ілметилу, 5-метил-2трифторметилфуран-3-ілметилу і 2,5диметилфуран-3-ілметилу. 6. Сполука формули (II) за будь-яким з пп.1-5, у якій R2 являє собою групу пент-4-еніл, пентил, бутил, аліл, бензил, тіофен-2-ілметил, тіофен-3ілметил, фуран-2-ілметил, фуран-3-ілметил, фенетил, циклопентил, циклогексил або циклогексилметил, причому циклічні групи, які присутні у R2, необов'язково заміщені замісниками в кількості від одного до трьох, вибраними з фтору, хлор у, брому, метилу, метокси, трифторметилу, етилу, третбутилу, гідрокси і ціано. 7. Сполука за п.6, у якій R 2 являє собою групу, вибрану з 3-фторбензилу, 2,4,5-трифторбензилу, 3,4,5-трифторбензилу, 5-бромтіофен-2-ілметилу, 3,4-диметоксифенілетилу, 3-метилтіофен-2ілметилу, тіофен-3-ілметилу, 4-бром-5метилтіофен-2-ілметилу, 4,5-диметилфуран-2ілметилу, фуран-3-ілметилу, 2-фтор-4метоксибензилу, 2-(4-фторфеніл)етилу, бутилу, пент-4-енілу і циклопентилу. 8. Сполука формули (II) за будь-яким з пп.1-7, у якій А являє собою -СН2-, значення як m, так і n дорівнює 0, і В являє собою групу, вибрану з лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкокси, ціано, нітро, -CH=CR'R", -C(O)OR', -OC(O)R', SC(O)R', -C(O)NR'R", -NR'C(O)OR", -NR'C(O)NR", циклоалкілу, фенілу, нафталенілу, 5,6,7,8 5 85541 тетрагідронафталенілу, бензо[1.3]діоксолілу, ге тероарилу або гетероциклілу; причому R' і R" є такими, як вказано в п.1; і де циклічні групи, позначені як В, необов'язково заміщені одним, двома або трьома замісниками, вибраними з галогену, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, фенілу, -OR', -SR', NR'R", -NHCOR', -CONR'R", -CN, -NO2 і -COOR'; R' і R" є такими, як визначено вище. 9. Сполука формули (II) за будь-яким з пп.1-7, у якій А являє собою -СН2-, В є таким, як визначено в п.1, і значення принаймні однієї з величин m або n не дорівнює 0. 10. Сполука формули (II) за будь-яким з пп.1-7, у якій В означає тіофен-2-ільну гр упу або фенільну груп у, яка необов'язково заміщена замісниками в кількості від одного до трьох, вибраними з атомів галогену або гідрокси, метилу, або груп -СН2ОН, ОМе, -NMe 2 , -NHCOMe, -CONH2, -CN, -NO 2, COOMe або -CF3 . 11. Сполука за п.10, у якій В являє собою фенільну, 4-фторфенільну, 3-гідроксифенільну або тіофен-2-ільну гр упу. 12. Сполука формули (II) за будь-яким з пп.1-7, 10 або 11, у якій n=0 або 1; m означає ціле число від 1 до 6; і А являє собою групу -СН2, -СН=СН-, -CO-, -NMe-, О- або -S-. 13. Сполука формули (II) за п.12, у якій m означає 1, 2 або 3, і А являє собою групу -СН2, -СН=СН -, або -О-. 14. Сполука формули (II) за будь-яким з пп.1-7, у якій послідовність В-(СН2)n-А-(СН2) m- являє собою груп у, вибрану з 3-феноксипропілу, 2феноксіетилу, 3-фенілалілу, фенетилу, 3фенілпропілу, 3-(3-гідроксифенокси)пропілу, 3-(4фтор фенокси)пропілу, 3-тіофен-2-ілпропілу, алілу, гептилу, 3-ціанопропілу і метилу. 15. Сполука формули (II) за будь-яким з пп.1-14, у якій X- являє собою хлорид-аніон, бромід-аніон, трифторацетат-аніон або метансульфонат-аніон. 16. Сполука формули (II) за будь-яким з попередніх пунктів, у якій р означає 2. 17. Сполука формули (II) за будь-яким з попередніх пунктів, у якій азоніабіциклічна кільцева система заміщена в 3-положенні. 18. Сполука формули (II) за п.17, у якій атом вуглецю в 3-положенні азоніабіциклічної кільцевої системи має R-конфігурацію. 19. Сполука формули (II) за п.17, у якій атом вуглецю в 3-положенні азоніабіциклічної кільцевої системи має S-конфігурацію. 20. Сполука за будь-яким з попередніх пунктів, яка являє собою окремий ізомер. 21. Сполука формули (II) за п.1, яка являє собою одну з наступних сполук: (3R)-3-[(3-фторбензил)-(3фтор феніл)карбамоїлокси]-1-(2-феноксіетил)-1азоніабіцикло[2.2.2]октан бромід; (3R)-3-[(3-фторбензил)-(3фтор феніл)карбамоїлокси]-1-(3-фенілпропіл)-1азоніабіцикло[2.2.2]октан бромід; (3R)-1-(2-феноксіетил)-3-[м-толіл-(2,4,5трифторбензил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан бромід; 6 (3R)-1-(3-фенілпропіл)-3-[м-толіл-(2,4,5трифторбензил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан бромід; (3R)-3-[(3-фторфеніл)-(3,4,5трифторбензил)карбамоїлокси]-1-(2-феноксіетил)1-азоніабіцикло[2.2.2]октан бромід; (3R)-1-аліл-3-[[2-(3,4-диметоксифеніл)етил]-(5метилфуран-2-ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан бромід; (3R)-3-[(5-бромтіофен-2-ілметил)-(2,4,5трифторфеніл)карбамоїлокси]-1-(3феноксипропіл)-1азоніабіцикло[2.2.2]октантрифторацетат; (3R)-3-[[2-(3,4-диметоксифеніл)етил]-(5метилфуран-2-ілметил)карбамоїлокси]-1-(4етоксикарбонілбутил)-1-азоніабіцикло[2.2.2]октан трифторацетат; (3R)-3-[(4-фтор-2-метилфеніл)-(3-метилтіофен-2ілметил)карбамоїлокси]-1-(2-феноксіетил)-1азоніабіцикло[2.2.2]октан трифторацетат; (3R)-3-[(3-фтор-4-метоксифеніл)тіофен-3ілметилкарбамоїлокси]-1-(3-фенілаліл)-1азоніабіцикло[2.2.2]октан трифторацетат; (3R)-1-фенетил-3-[тіофен-3-ілметил(2,4,5трифторбензил)карбамоїлокси]-1азоніабіцикло[2.2.2]октантрифторацетат; (3R)-3-[(4-бром-5-метилтіофен-2-ілметил)-(3метилтіофен-2-ілметил)карбамоїлокси]-1-(3фенілпропіл)-1азоніабіцикло[2.2.2]октантрифторацетат; (3R)-3-[(4,5-диметилфуран-2-ілметил)-(5метилфуран-2-ілметил)карбамоїлокси]-1-[3-(3гідроксифенокси)пропіл]-1азоніабіцикло[2.2.2]октан трифторацетат; (3R)-1-[3-(4-фторфенокси)пропіл]-3-[фуран-3ілметил-(5-метил-2-трифторметилфуран-3ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан трифторацетат; (3R)-3-[(2,5-диметилфуран-3-ілметил)-(2-фтор-4метоксибензил)карбамоїлокси]-1-(3-тіофен-2ілпропіл)-1-азоніабіцикло[2.2.2]октан трифторацетат; (3R)-1-аліл-3-[2-(4-фторфеніл)етил]-(3метилтіофен-2-ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан трифторацетат; (3R)-3-[бутил-(2,5-дифторфеніл)карбамоїлокси]-1гептил-1-азоніабіцикло[2.2.2]октан трифторацетат; (3R)-1-(3-ціанопропіл)-3-[(2,6-дифторфеніл)пент-4енілкарбамоїлокси]-1-азоніабіцикло[2.2.2]октан трифторацетат; (3R)-3-[(3-фторфеніл)-(3,4,5трифторбензил)карбамоїлокси]-1-(3-фенілпропіл)1-азоніабіцикло[2.2.2]октан бромід; (3R)-3-[(5-етилтіофен-2-ілметил)-(3-метилтіофен2-ілметил)карбамоїлокси]-1-(3-фенілпропіл)-1азоніабіцикло[2.2.2]октан бромід; (3R)-3-[[2-(3,4-диметоксифеніл)етил]-(5метилфуран-2-ілметил)карбамоїлокси]-1-(4етоксикарбонілбутил)-1-азоніабіцикло[2.2.2]октан форміат; (3R)-3-[(4-фтор-2-метилфеніл)-(3-метилтіофен-2ілметил)карбамоїлокси]-1-(2-феноксіетил)-1азоніабіцикло[2.2.2]октан бромід; 7 85541 8 (3R)-3-[(3-фтор-4-метоксифеніл)тіофен-3ілметилкарбамоїлокси]-1-(3-фенілаліл)-1азоніабіцикло[2.2.2]октан бромід; (3R)-1-аліл-3-[2-(4-фторфеніл)етил]-(3метилтіофен-2-ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан бромід. 22. Фармацевтична композиція, яка містить сполуку за будь-яким з пп.1-21 у суміші з фармацевтично прийнятним носієм або розріджувачем. 23. Сполука за будь-яким з пп.1-21 для лікування хворобливого стану або захворювання, стан пацієнта при яких може поліпшуватися при антагоністичному впливі на М3 мускаринові рецептори. 24. Застосування сполуки за будь-яким з пп.1-21 для одержання лікарського засобу, призначеного для лікування хворобливого стану або захворювання, стан пацієнта при яких може поліпшуватися при антагоністичному впливі на М3 мускаринові рецептори. 25. Застосування за п.24, у якому хворобливий стан являє собою респіраторне, урологічне або шлунково-кишкове захворювання, порушення або розлад. 26. Спосіб лікування пацієнта, який має хворобливий стан або захворювання, стан пацієнта при яких може поліпшуватися при антагоністичному впливі на М3 мускаринові рецептори, при якому вводять вказаному пацієнту ефективну кількість сполуки за будь-яким з пп.1-21. 27. Спосіб за п.26, у якому хворобливий стан являє собою респіраторне, урологічне або шлунковокишкове захворювання, порушення або розлад. 28. Комбінований продукт, який містить (і) сполуку за будь-яким з пп.1-21; і (іі) іншу сполук у, ефективну при лікуванні респіраторного, урологічного або шлунково-кишкового захворювання або розладу, для одночасного, окремого або послідовного використання. 29. Комбінований продукт за п.28, який містить (і) сполуку за будь-яким з пп.1-21; і (іі) b 2 -агоніст, стероїд, протиалергічний лікарський засіб, інгібітор фосфодіестерази IV і/або антагоніст лейкотриєну D4 (LTD4) для одночасного, окремого або послідовного використання при лікуванні респіраторного захворювання. Даний винахід стосується нових карбаматних похідних хінуклідину, придатних для терапевтичного використання, а також деяких способів їх одержання і фармацевтичних композицій, які містять ці сполуки. Сполуки згідно із даним винаходом являють собою антимускаринові агенти, які мають ефективну і тривалу дію. Зокрема, ці сполуки мають високу спорідненість і селективність по відношенню до мускаринових М3 рецепторів у порівнянні з М2 рецепторами. Підвид М3 мускаринового рецептори присутній у залозах і гладенькій мускулатурі і є медіатором збуджувального впливу парасимпатичної системи на гландулярну секрецію і на скорочення внутрішньої гладенької мускулатури [Chapter 6, Cholinergic Transmission, in H.P. Rang et al., Pharmacology, Churchill Livingstone, New York, 1995]. Відомо, що М3 антагоністи можуть бути використані для лікування захворювань, які характеризуються підвищеним парасимпатичним тонусом, надлишковою гландулярною секрецією або надлишковим скороченням гладенької мускулатури [R.M. Eglen, S.S. Hegde, (1997), Drug News Perspect., 10(8): 462-469]. Прикладами такого типу захворювань є респіраторні порушення і розлади, такі як хронічне обструктивне захворювання легень (ХОЗЛ), бронхіт, бронхіальна гіперреактивність, астма, кашель і риніт; урологічні порушення і розлади, такі як мимовільне сечовипускання і нетримання сечі, полакіурія (прискорене сечовипускання), неврогена дисфункція сечового міхура або гіперреактивний сечовий міхур, цистоспазм і хронічний цистит; шлунково-кишкові захворювання, такі як синдром подразненого кишечнику, спастичний коліт, дивертикуліт і пептична виразка; а також захворювання серцево-судинної системи, такі як вагусно індукована синусова брадикардія [Chapter 7, Muscarinic Receptor Agonists and Antagonists, in Goodman and Gilman's The Pharmacological Basis of Therapeutics, 10th edition, McGraw Hill, Ney York, 2001]. Сполуки згідно із даним винаходом можуть бути використані окремо або в сполученні з іншими лікарськими засобами, ефективність яких для лікування таких захворювань загальновідома. Наприклад, їх можна вводити в сполученні з β2, агоністами, стероїдами, протиалергічними лікарськими засобами, інгібіторами фосфодіестерази IV і/або антагоністами лейкоториєну D4 (LTD4), здійснюючи одночасне, окреме або послідовне використання при лікуванні респіраторних захворювань. Даний винахід стосується нових карбаматних похідним хінуклідину, які мають значну антагоністичну активність по відношенню до мускаринових М3 рецепторів, хімічна структура цих похідних описується формулою (І), або їх фармацевтично прийнятних солей, включаючи четвертинні солі формули (II). Формула (І) стосується карбамату наступної структури: (I) у цій формулі R1 являє собою групу, вибрану з фенілу, 2фурилу, 3-фурилу, 2-тієнілу, 3-тієнілу, бензилу, фуран-2-ілметилу, фуран-3-ілметилу, тіофен-2ілметилу і тіофен-3-ілметилу; R2 являє собою групу, вибрану з необов'язково заміщеного нижчого алкілу, необов'язково заміщеного нижчого алкенілу, необов'язково заміщеного нижчого алкінілу, насиченого або 9 85541 ненасиченого циклоалкілу, насиченого або ненасиченого циклоалкілметилу, фенілу, бензилу, фенетилу, фуран-2-ілметилу, фуран-3-ілметилу, тіофен-2-ілметилу, тіо фен-3-ілметилу, піридилу і піридилметилу; де карбоциклічні фрагменти циклоалкільної, циклоалкілметильної, фенільної, бензильної або фенетильної груп можуть бути необов'язково місточковими або спряженими з іншим насиченим, ненасиченим або ароматичним карбоциклічним фрагментом або з циклічним фрагментом, який включає атоми вуглецю і 1 або 2 атоми кисню; циклічні групи, які є в R1 і R2, необов'язково заміщені одним, двома або трьома замісниками, вибраними з галогену, лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкокси, -SH, лінійного або розгалуженого необов'язково заміщеного нижчого алкілтіо, нітро, ціано, -NR'R", -CO2R', -C(O)-NR'R", N(R"')C(O)-R', -N(R"')-C(O)NR'R", де R', R" і R'" кожен незалежно являє собою атом водню або лінійну або розгалужену, необов'язково заміщену нижчу алкільну групу, або R' і R" разом з атомом, до якого вони приєднані, утворюють циклічну групу; p означає 1 або 2, і карбаматна група приєднана в положеннях 2, 3 або 4 азабіциклічної кільцевої системи, а також його фармацевтично прийнятні солі, включаючи четвертинні амонієві солі формули (II): (II) у якій R1, R2 і ρ є такими, як визначено вище; m означає ціле число від 0 до 8; n означає ціле число від 0 до 4; А являє собою групу, вибрану з -СН2., CH=CR'-, -CR'=CH-, -CR'R"-, -C(O), -О-, -S-, -S(O)-, -S(O)2- і -NR'-, де R' і R" є такими, як визначено вище; В являє собою атом вуглецю або груп у, вибрану з лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкокси, ціано, нітро, -CH=CR'R", -C(O)OR', OC(O)R', -SC(O)R', -C(O)NR'R", -NR'C(O)OR", NR'C(O)NR", циклоалкілу, фенілу, нафталенілу, 5,6,7,8-тетрагідронафталенілу, бензо[1.3]діоксолілу, гетероарилу або гетероциклілу; R' і R" є такими, як визначено вище; і де циклічні групи, представлені як В, необов'язково заміщені одним, двома або трьома замісниками, вибраними з галогену, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, фенілу, -OR', -SR', -NR'R", -NHCOR', -CONR'R", -CN, -NO2 і -COOR'; R' і R" є такими, як визначено вище; X- являє собою фармацевтично прийнятний одно- або багатовалентний аніон кислоти; включаючи всі індивідуальні стереоізомери формули (І) або (II) і їх суміші; за умови, що сполука формули (І) не являє собою наступну сполуку: 10 1-азабіцикло[2.2.2]окт-3-иловий складний ефір дифенілкарбамінової кислоти або 1-азабіцикло[2.2.2]окт-3-иловий складний ефір етилфенілкарбамінової кислоти. Іншою метою даного винаходу є створення способів одержання вказаних сполук, фармацевтичних композицій, які включають ефективну кількість вказаних сполук; застосування сполук для одержання лікарських засобів, призначених для лікування таких захворювань, стан пацієнта при яких може поліпшитися при антагоністичному впливі на М3 мускаринові рецептори; і способи лікування таких захворювань, стан пацієнта при яких може поліпшуватися при антагоністичному впливі на М3 мускаринові рецептори, ці способи включають введення сполук згідно із даним винаходом пацієнту, який потребує такого лікування. Переважно, щоб у сполуках згідно із даним винаходом принаймні один з R1 або R2 був заміщеним. Особливо переважні такі сполуки формули (І) або (II), у яких у тому випадку, коли циклічна група, яка присутня у R1, є незаміщеною або містить тільки один замісник, то R2 має принаймні один замісник. Також переважні такі сполуки, у яких у тому випадку, коли R2 є незаміщеним, то циклічна група, яка присутня у R1, має принаймні два замісники. У статті: [J. L. G. Nilsson et al. Acta Pharm. Suecica, 5: 71-76 (1968)] описана група карбаматних похідних хінуклідину, які мають протималярійну активність, серед цих сполук згадуються 1азабіцикло[2.2.2]окт-3-иловий складний ефір дифенілкарбамінової кислоти і 1азабіцикло[2.2.2]окт-3-иловий складний ефір етилфенілкарбамінової кислоти. В опублікованій [міжнародній заявці WO 02/00652] розкрита група сполук, які підпадають під загальну стр уктурну формулу (І) або (II). Ці конкретні сполуки, описані в вказаній заявці, виключені з обсягу даного винаходу. Таким чином, у ти х сполуках формули (І), що описані вище, де: p означає 2; карбаматна група приєднана в положенні 3 азабіциклічної кільцевої системи; і R1 являє собою незаміщену інданільну груп у або фенільну гр упу, яка необов'язково заміщена одним або двома замісниками, вибраними з хлору, фтор у, брому, метилу, гідрокси і ціано; то в такому випадку R2 не може являти собою одну з наступних груп: незаміщений циклопропілметил; незаміщений циклобутилметил; незаміщений циклопентилметил; циклогексилметил, необов'язково заміщений метальною або ізопропенільною групою; незаміщений циклогексеніл; незаміщений норборненіл; незаміщений біцикло[2.2.1]гептаніл; незаміщений бензо[1.3]діоксоліл; незаміщений 2,3дигідробензо[1.4]діоксиніл; незаміщений бензил; бензильну груп у, яка заміщена одним або двома замісниками, вибраними з фтору, хлору, брому, метокси, метилу, трифторметилу, етилу, третбутилу, гідрокси, гідроксиметилу, ціано, амінокарбонілу, трифторметокси, бензилокси, ізопропілок 11 85541 си; і бензильну груп у, яка заміщена трьома атомами фтору. Крім того, у тих сполуках формули (II), як описано вище, де: p означає 2; карбаматна група, приєднана в положенні 3 азоніабіциклічної кільцевої системи, має (3R)конфігурацію; R1 являє собою фенільну груп у, яка необов'язково заміщена атомом фтору або метальною групою; R2 являє собою незаміщену циклогексилметильну груп у або бензильну груп у, яка необов'язково заміщена одним або трьома атомами фтору; і X - йод; у такому випадку послідовність B-(CH2)n-A(CH2)m- не може являти собою метальну груп у. Більш конкретно, з обсягу даного винаходу явно виключаються наступні сполуки: (3R)-3-(бензилфенілкарбамоїлокси)-1-метил-1азоніабіцикло[2.2.2]октан йодид; (3R)-3-[(4-фторбензил)фенілкарбамоїлокси]-1метил-1-азоніабіцикло[2.2.2]октан йодид; (3R)-3-(бензил-о-толілкарбамоїлокси)-1-метил1-азоніабіцикло[2.2.2]октан йодид; (3R)-1-метил-3-[о-толіл-(2,4,5трифторбензил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан йодид; (3R)-3-[(4-фторбензил)-м-толілкарбамоїлокси]1-метил-1-азоніабіцикло[2.2.2]октан йодид; (3R)-3-[бензил-(2-фторфеніл)карбамоїлокси]1-метил-1-азоніабіцикло[2.2.2]октан йодид; (3R)-3-[циклогексилметил-(2фтор феніл)карбамоїлокси]-1-метил-1азоніабіцикло[2.2.2]октан йодид. При використанні в тексті даної заявки група або фрагмент алкіл, алкеніл або алкініл можуть бути лінійними або розгалуженими, і звичайно являють собою нижчу алкільну, алкенільну або алкінільну гр упу. Нижча алкільна група містить від 1 до 8, переважно, від 1 до 6 атомів вуглецю. Приклади включають метальну, етильну, пропільну, включаючи ізопропільну, бутильну, включаючи нбутильну, втор-бутильну і трет-бутильну, 1метилбутильну, 1-етилпропільну, 1,2диметилпропільну, н-гексильну або 1етилбутильну групи. Більш переважно, нижча алкільна група містить від 1 до 4 атомів вуглецю. Нижча алкенільна або алкінільна група містить від 2 до 8, переважно, від 2 до 6 атомів вуглецю. Приклади включають вінільну, алільну, 1-пропенільну, 4-пентенільну, 1-пропінільну, 2-пропінільну, 1бутинільну, 2-бутинільну або 3-бутинільну групи. Більш переважно, нижча алкенільна або алкінільна група містить від 2 до 4 атомів вуглецю. Необов'язково заміщена нижча алкільна, алкенільна або алкінільна групи, згадані в тексті даної заявки, включають лінійну або розгалужену нижчу алкільну, алкенільну або алкінільну гр упи, як визначено вище, які можуть бути незаміщеними або заміщеними в будь-якому положенні одним або більше замісниками, наприклад, 1, 2 або 3 замісниками. У тому випадку, коли є два або більше замісників, кожен замісник може бути однаковим або різної. Замісник (замісники) звичайно яв 12 ляють собою атоми галогену, переважно, атоми фтор у і гр упи гідрокси або алкокси. Групи алкокси й алкілтіо, вказані в тексті даної заявки, звичайно являють собою нижчі алкокси і нижчі алкілтіо групи, тобто групи, які містять від 1 до 8, переважно, від 1 до 6, і більш переважно, від 1 до 4 атомів вуглецю, вуглеводневий ланцюг є розгалуженим або лінійним, і ці групи необов'язково заміщені в будь-якому положенні одним або більше замісниками, наприклад, 1, 2 або 3 замісниками. У тому випадку, коли є два або більше замісників, кожний із замісників може бути однаковим або різним. Замісник (замісники) звичайно являють собою атоми галогену, найбільш переважно, атоми фтору і гідроксигрупи. Переважні необов'язково заміщені алкоксигрупи включають метокси, етокси, н-пропокси, ізопропокси, нбутокси, втор-бутокси, трет-бутокси, трифторметокси, дифторметокси, гідроксиметокси, 2гідроксіетокси або 2-гідроксипропокси. Переважні необов'язково заміщені алкілтіогрупи включають метилтіо, етилтіо, н-пропілтіо, ізопропілтіо, нбутилтіо, втop-бутилтіо, трет-бутилтіо, три фторметилтіо, дифторметилтіо, гідроксиметилтіо, 2гідроксіетилтіо або 2-гідроксипропілтіо. Циклічні групи, згадані в тексті даної заявки, включають, якщо не вказане інше, карбоциклічні і гетероциклічні групи. Циклічні групи можуть містити одне або більше кілець. Карбоциклічні групи можуть бути ароматичними або аліциклічними, наприклад, такими як циклоалкільні групи. Гетероциклічні групи також включають гетероарильні групи. Циклоалкільні групи й аліциклічні групи, вказані в тексті даної заявки, якщо не вказане інше, звичайно містять від 3 до 7 атомів вуглецю. Циклоалкільні групи й аліциклічні кільцеві системи, що складаються з від 3 до 7 атомів вуглецю, включають циклопропіл, циклобутил, циклопентил, циклогексил і циклогептил. При використанні в тексті даної заявки терміна «ароматична група» вказана група звичайно містить від 5 до 14, переважно, від 5 до 10 атомів вуглецю. Приклади ароматичних груп включають феніл і нафталеніл. Гетероциклічна або гетероароматична група, вказана в тексті даної заявки, звичайно являє собою 5-10-членну груп у, таку як 5-, 6- або 7-членна група, яка містить один або більше гетероатомів, вибраних з N, S і О. Звичайно присутні 1, 2, 3 або 4 гетероатоми, переважно, 1 або 2 гетероатоми. Гетероциклічна або гетероароматична група може являти собою одне кільце або два або більше спряжених кілець, де принаймні одне кільце містить гетероатом. Приклади гетероциклічних груп включають піперидил, піролідил, піперазиніл, морфолініл, тіоморфолініл, піроліл, імідазоліл, імідазолідиніл, піразолініл, індолініл, ізоіндолініл, піридил, піразиніл, піримідиніл, піридазиніл, індозиніл, ізоіндоліл, індоліл, індазоліл, пуриніл, хінолізиніл, ізохіноліл, хіноліл, фталазиніл, нафтиридиніл, хіноксалініл, хіназолініл, циннолініл, птеридиніл, хінуклідиніл, триазоліл, піразоліл, тетразоліл і тієніл. Приклади гетероароматичних груп включають піридил, тієніл, фурил, піроліл, імідазо 13 85541 ліл, бензотіазоліл, піридиніл, піразоліл, піразиніл, піримідиніл, піридазиніл, індоліл, індазоліл, пуриніл, хіноліл, ізохіноліл, фталазиніл, нафтиридиніл, хіноксалініл, хіназолініл, циннолініл, триазоліл і піразоліл. При використанні в тексті даної заявки термін «атом галогену» включає атом фтору, хлору, брому або йоду, звичайно атом фтору, хлору або брому. При використанні в тексті даної заявки термін «фармацевтично прийнятна сіль» включає солі з фармацевтично прийнятними кислотами або основами. Фармацевтично прийнятні кислоти включають як неорганічні кислоти, наприклад, хлороводневу, сірчану, фосфорну, дифосфорну, бромоводневу, йодоводневу й азотну кислоту, так і органічні кислоти, наприклад, лимонну, фумарову, малеїнову, яблучн у, мурашин у, мигдалеву, аскорбінову, ща влеву, янтарну, виннокам'яну, бензойну, оцтову, метансульфонову, етансульфонову, бензолсульфонову або n-толуолсульфонову кислоту. У четвертинних амонієвих сполуках згідно із даним винаходом, включаючи сполуки, представлені формулою (II), еквівалент аніона (X-) асоційований з позитивним зарядом атома N. X- може являти собою аніон різних мінеральних кислот, наприклад, такий як хлорид, бромід, йодид, сульфат, нітрат, фосфат, або аніон органічної кислоти, наприклад, такий як ацетат, трифторацетат, малеат, фумарат, цитрат, оксалат, сукцинат, тартрат, малеїнат, аніон мигдалевої кислоти, форміат, метансульфонат і n-толуолсуль фонат. Х- являє собою, переважно, аніон, вибраний з таких аніонів як хлорид, бромід, йодид, сульфат, нітрат, ацетат, трифторацетат, форміат, метансульфонат, малеїнат, оксалат або сукцинат. Більш переважно, Xявляє собою хлорид, бромід, форміат, трифторацетат або метансульфонат. Переважні сполуки формули (І) згідно із даним винаходом, як визначено вище, являють собою такі сполуки, у яких R1 являє собою груп у, вибрану з 2-фурилу, 3-фурилу, 2-тієнілу, 3-тієнілу, бензилу, фуран-2-ілметилу, фуран-3-ілметилу, тіофен-2ілметилу, тіофен-3-ілметилу; циклічні групи, які присутні у R1, необов'язково заміщені одним, двома або трьома замісниками, вибраними з галогену, лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкокси, -SH, лінійного або розгалуженого, необов'язково заміщеного нижчого алкілтіо, нітро, ціано, -NR'R", -CO2R', -C(O)-NR'R", -N(R"')C(O)-R', -N(R'")C(O)NR'R", де R', R" і R'" кожен незалежно являє собою атом водню або лінійну або розгалужену, необов'язково заміщену нижчу алкільну групу, або R' і R" разом з атомом, до якого вони приєднані, утворюють циклічну груп у. Також переважні сполуки формули (І), як визначено вище, у яких R2 являє собою необов'язково заміщену груп у, вибрану з нижчого алкілу, нижчого алкенілу, нижчого алкінілу, насиченого або ненасиченого циклоалкілу, фенілу, фенетилу, фуран-2-ілметилу, фуран-3-ілметилу, тіофен-2ілметилу, тіофен-3-ілметилу, піридилу і піридил 14 метилу, або насичену або ненасичену циклоалкілметильну груп у, яка містить принаймні один замісник і яку вибирають із заміщеного циклопропілметилу, заміщеного циклобутилметилу і заміщеного циклопентилметилу; причому замісники циклічних груп, які присутні у R2, являють собою один, два або три замісники, вибрані з галогену, лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкокси, -SH, лінійного або розгалуженого необов'язково заміщеного нижчого алкілтіо, нітро, ціано, -NR'R", -CO2R', -C(O)-NR'R", -N(R'")C(O)-R', -N(R"')C(O)NR'R", де R', R" і R'" кожен незалежно являє собою атом водню або лінійну або розгалужену, необов'язково заміщену нижчу алкільну групу, або R' і R" разом з атомом, до якого вони приєднані, утворюють циклічну груп у. Переважні сполуки формули (II) згідно із даним винаходом, як визначено вище, є такими сполуками, у яких R1 являє собою групу, вибрану з фенілу, 2-тієнілу, 3-тієнілу, тіо фен-2-ілметилу, тіофен-3-ілметилу, фуран-2-ілметилу або фуран-3ілметилу, циклічні групи, які присутні у R1, необов'язково заміщені замісниками в кількості від одного до трьох, вибраними з фтору, хлору, брому, метилу, метокси, трифторметилу, етилу, третбутлу, гідрокси і ціано. Відповідно до особливо переважних варіантів здійснення винаходу R1 являє собою групу, вибраний з фенілу, 2-фторфенілу, 3-фторфенілу, 4фтор фенілу, 3-метилфенілу, 4-метилфенілу, 2,5дифторфенілу, 2,6-дифторфенілу, 2,4,5трифторфенілу, 5-метилфуран-2-ілметилу, 4фтор-2-метилфенілу, 3-фтор-4-метоксифенілу, 3метилтіофен-2-ілметилу, 4,5-диметилтіофен-2ілметилу, тіофен-3-ілметилу, 5-метил-фуран-2ілметилу, 5-метил-2-трифторметил-фуран-3ілметилу і 2,5-диметил-фуран-3-ілметилу. Також переважні сполуки формули (II), як вказано вище, у яких R2 являє собою групу пент-4еніл, пентил, бутил, аліл, бензил, тіофен-2ілметил, тіофен-3-ілметил, фуран-2-ілметил, фуран-3-ілметил, фенетил, циклопентил, циклогексил або циклогексилметил, циклічні групи, які присутні у R2, необов'язково заміщені замісниками в кількості від одного до трьох, вибраними з фтору, хлору, брому, метилу, метокси, трифторметилу, етилу, трет-бутилу, гідрокси і ціано. Відповідно до особливо переважних варіантів здійснення даного винаходу R2 являє собою гр упу, вибрану з 3-фторбензилу, 2,4,5-трифторбензилу, 3,4,5-трифторбензилу, 5-бромтіофен-2-ілметилу, 3,4-диметоксифенілетилу, 3-метилтіофен-2ілметилу, тіофен-3-ілметилу, 4-бром-5метилтіофен-2-ілметилу, 4,5-диметилфуран-2ілметилу, фуран-3-ілметил, 2-фтор-4метоксибензилу, 2-(4-фторфеніл)етилу, бутилу, пент-4-енілу і циклопентану. Інші переважні сполуки формули (II) - це такі сполуки, у яких А являє собою -СН2-, значення як m так і n дорівнює 0, і В являє собою групу, вибрану з лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого 15 85541 алкокси, ціано, нітро, -CH=CR'R", -C(O)OR', OC(O)R', -SC(O)R', -C(O)NR'R", -NR'C(O)OR", NR'C(O)NR", циклоалкілу, фенілу, нафталенілу, 5,6,7,8-тетрагідронафталенілу, бензо[1.3]діоксолілу, гетероарилу або гетероциклілу; R' і R" є такими, як визначено вище; і в яких циклічні групи, позначені як В, необов'язково заміщені одним, двома або трьома замісниками, вибраними з галогену, гідрокси, лінійного або розгалуженого, необов'язково заміщеного нижчого алкілу, фенілу, -OR', -SR', -NR'R", -NHCOR', -CONR'R", -CN, -NO2 і -COOR'; R' і R" є такими, як визначено вище. Відповідно до інших варіантів сполук формули (II) А являє собою -СН2-, В є таким, як визначено вище, і принаймні один з показників m або n не дорівнює 0. Також переважні сполуки формули (II), у яких фрагмент В являє собою тіофен-2-ільну груп у або фенільну групу, яка необов'язково заміщена замісниками в кількості від одного до трьох, вибраними з атомів галогену або гідрокси, метилу, гр уп СН2ОН, -ОМе, -N Me 2, -NHCOMe, -CONH 2, -CN, NO2, -COOMe або -CF3. Найбільш переважні сполуки, у яких фрагмент В являє собою фенільну, 4фтор фенільну, 3-гідроксифенільну або тіофен-2ільну групу. Зокрема, переважні сполуки формули (II), у якій n=0 або n=1; m означає ціле число від 1 до 6; і фрагмент А являє собою гр упу -СН2-, -СН=СН -, CO-, -NMe-, -O-або -S-. Найбільш переважними є сполуки, у яких ш означає 1, 2 або 3, і фрагмент А являє собою групу -СН2-, -СН=СН- або -О-. Переважно, у сполуках формули (II) послідовність B-(CH2)n-A-(CH2) m- являє собою групу, вибрану з 3-феноксипропілу, 2-феноксіетилу, 3фенілалілу, фенетилу, 3-фенілпропілу, 3-(3гідроксифенокси)пропілу, 3-(4фтор фенокси)пропілу, 3-тіофен-2-ілпропілу, алілу, гептилу, 3-ціанопропілу і метилу. Відповідно до переважних варіантів сполук формули (II) згідно із даним винаходом X- являє собою такий аніон як хлорид, бромід, трифторацетат або метансульфонат. Також переважні сполуки формули (І) або (II), у яких p означає 2 і/або в яких азабіциклічна кільцева система заміщена в 3-положенні. Сполуки згідно із даним винаходом, представлені формулою (І) і їх солі, такі як представлені формулою (II), можуть містити один або більше асиметричних атомів вуглецю. В обсяг винаходу входять усі можливі стереоізомери, такі як сполуки формули (І) або (II), у яких атом вуглецю в 3положенні азабіциклічної кільцевої системи має або R-, або S-конфігурацію. Всі окремі ізомери і суміші ізомерів входять в обсяг даного винаходу. Наступні сполуки загальної формули (І), як передбачається, вказані для ілюстрації обсягу даного винаходу: (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (3-фторбензил)-(3-фторфеніл)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір м-толіл-(2,4,5-трифторбензил)карбамінової кислоти; 16 (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (3-фтор феніл)-(3,4,5трифторбензил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір циклогексилметил-(2фтор феніл)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір [2-(3,4-диметоксифеніл)етил]-(5-метилфуран2-ілметил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (5-бромтіофен-2-ілметил)-(2,4,5трифторфеніл)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (4-фтор-2-метилфеніл)-(3-метилтіофен-2ілметил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (3-фтор-4-метоксифеніл)тіофен-3ілметилкарбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір тіофен-3-ілметил-(2,4,5трифторбензил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (4-бром-5-метилтіофен-2-ілметил)-(3метилтіофен-2-ілметил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (4,5-диметилфуран-2-ілметил)-(5метилфуран-2-ілметил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір фуран-3-ілметил-(5-метил-2трифторметилфуран-З -ілметил)карбамінової кислоти; (3R)-1-аза-біцикло[2.2.2]окт-3-иловий складний ефір (2,6-дифторфеніл)пент-4-енілкарбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (2,5-диметилфуран-3-ілметил)-(2-фтор-4метоксибензил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір [2-(4-фторфеніл)етил]-(3-метилгіофен-2ілметил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір бутил-(2,5-дифторфеніл)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір циклопентил-(4,5-диметилтіофен-2ілметил)карбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)иловий складний ефір бензилфенілкарбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)иловий складний ефір бензил(4-фторфеніл)карбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)иловий складний ефір бензил-n-толілкарбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)иловий складний ефір бутилфенілкарбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)иловий складний ефір фенілтіофен-2-ілметилкарбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)иловий складний ефір фенетилфенілкарбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)иловий складний ефір пентилфенілкарбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)иловий складний ефір пент-4-енілфенілкарбамінової кислоти; фенілтіофен-3-ілметилкарбамінової кислоти 1азабіцикло[2.2.2]окт-3-(R)иловий складний ефір; 17 85541 1-азабіцікло[2.2.2]окт-3-(R)иловий складний ефір бутилтіофен-2-ілметилкарбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)иловий складний ефір біс-тіофен-2-ілметилкарбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)иловий складний ефір фуран-2-ілметил-2-тіофен-2ілметилкарбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)иловий складний ефір алілтіофен-2-ілметилкарбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)иловий складний ефір циклопентилтіофен-2-ілметилкарбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)иловий складний ефір фуран-2-ілметилфенілкарбамінової кислоти; 1-азабіцикло[2.2.2]окт-3-(R)-иловий складний ефір біс-фуран-2-ілметилкарбамінової кислоти; 1-азабіцикло[2.2.1]гепт-4-иловий складний ефір бензилфенілкарбамінової кислоти; 1-азабіцикло[2.2.2]окт-4-иловий складний ефір бензилфенілкарбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (5-етилтіофен-2-ілметил)-(3-метилтіофен-2ілметил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір циклопентил-(5-етилтіофен-2ілметил)карбамінової кислоти; і їх фармацевтично прийнятні солі. Наступні солі загальної формули (II) наводяться для ілюстрації обсягу даного винаходу: (3R)-3-[(3-фторбензил)-(3фтор феніл)карбамоїлокси]-1-(2-феноксіетил)-1азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[(3-фторбензил)-(3фтор феніл)карбамоїлокси]-1-(3-фенілпропіл)-1азоніабіцикло[2.2.2]октан, бромід; (3R)-1-(2-феноксіетил)-3-[м-толіл-(2,4,5трифторбензил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, бромід; (3R)-1-(3-фенілпропіл)-3-[м-толіл-(2,4,5трифторбензил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[(3-фторфеніл)-(3,4,5трифторбензил)карбамоїлокси]-1-(2-феноксіетил)1-азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[циклогексилметил-(2фтор феніл)карбамоїлокси]-1-(2-феноксіетил)-1азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[циклогексилметил-(2фтор феніл)карбамоїлокси]-1-(3-фенілпропіл)-1азоніабіцикло[2.2.2]октан, бромід; (3R)-1-аліл-3-[[2-(3,4-диметоксифеніл)етил]-(5метилфуран-2-ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[(5-бромтіофен-2-ілметил)-(2,4,5трифторфеніл)карбамоїлокси]-1-(3феноксипропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[[2-(3,4-диметоксифеніл)етил]-(5метилфуран-2-ілметил)карбамоїлокси]-1-(4етоксикарбонілбутил)-1-азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[[2-(3,4-диметоксифеніл)етил]-(5метилфуран-2-ілметил)карбамоїлокси]-1-(4етоксикарбонілбутил)-1-азоніабіцикло[2.2.2]октан, форміат; 18 (3R)-3-[(4-фтор-2-метилфеніл)-(3метилтіофен-2-ілметил)карбамоїлокси]-1-(2феноксіетил)-1-азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[(4-фтор-2-метилфеніл)-(3метилтіофен-2-ілметил)карбамоїлокси]-1-(2феноксіетил)-1-азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[(3-фтор-4-метоксифеніл)тіофен-3ілметилкарбамоїлокси]-1-(3-фенілаліл)-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[(3-фтор-4-метоксифеніл)тіофен-3ілметилкарбамоїлокси]-1-(3-фенілаліл)-1азоніабіцикло[2.2.2]октан, бромід; (3R)-1-фенетил-3-[тіофен-3-ілметил-(2,4,5трифторбензил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[(4-бром-5-метилтіофен-2-ілметил)-(3метилтіофен-2-ілметил)карбамоїлокси]-1-(3фенілпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[(4,5-диметилфуран-2-ілметил)-(5метилфуран-2-ілметил)карбамоїлокси]-1-[3-(3гідроксифенокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-1-[3-(4-фторфенокси)пропіл]-3-[фуран-3ілметил-(5-метил-2-трифторметилфуран-3ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[(2,5-диметилфуран-3-ілметил)-(2-фтор4-метоксибензил)карбамоїлокси]-1-(3-тіофен-2ілпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-1-аліл-3-[2-(4-фторфеніл)етил]-(3метилтіофен-2-ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-1-аліл-3-[2-(4-фторфеніл)етил]-(3металтіофен-2-ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[бутил-(2,5дифторфеніл)карбамоїлокси]-1-гептил-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-1-(3-ціанопропіл)-3-[(2,6дифторфеніл)пент-4-енілкарбамоїлокси]-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[циклопентил-(4,5-диметилтіофен-2ілметил)карбамоїлокси]-1-метил-1азоніабіцикло[2.2.2]октан, трифторацетат; 3-(R)(бензилфенілкарбамоїлокси)-1-(3фенілаліл)-1-азоніабіцикло[2.2.2]октан, бромід; 1-аліл-3-(R)(бензилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, бромід; 3-(R)(бензилфенілкарбамоїлокси)-1-фенетил1-азоніабіцикло[2.2.2]октан, бромід; 3-(R)(бензилфенілкарбамоїлокси)-1-(3-тіофен2-іл-пропіл)-1-азоніабіцикло[2.2.2]октан, бромід; 3-(R)(бензилфенілкарбамоїлокси)-1-(3фенілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід; 3-(R)(бензилфенілкарбамоїлокси)-1-(2феноксіетил)-1-азоніабіцикло[2.2.2]октан, бромід; 3-(R)(бутилфенілкарбамоїлокси)-1-(3фенілаліл)-1-азоніабіцикло[2.2.2]октан, бромід; 1-аліл-3-(R)(бутилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан; бромід; 3-(R)(бутилфенілкарбамоїлокси)-1-(2феноксіетил)-1-азоніабіцикло[2.2.2]октан, бромід; 19 85541 3-(R)(бутилфенілкарбамоїлокси)-1-[3-(3гідроксифенокси)пропіл]-1-азоніабіцикло [2.2.2]октан, бромід; 3-(R)(бутилфенілкарбамоїлокси)-1-[3-(4фтор фенокси)пропіл]-1-азоніабіцикло[2.2.2] октан, бромід; 3-(R)(бутилфенілкарбамоїлокси)-1-(3-тіофен-2ілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід; 3-(R)(бутилфенілкарбамоїлокси)-1-(3фенілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід; 3-(R)(фенілтіофен-2-ілметилкарбамоїлокси)-1(3-тіофен-2-ілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід; 1-(2-фенокси-етил)-3-(R)-(фенілтіофен-2ілметил-карбамоїлокси)-1-азоніабіцикло [2.2.2]октан, бромід; 1-аліл-3-(R)(фенілтіофен-2ілметилкарбамоїлокси)-1азоніабіциюіо[2.2.2]октан, бромід; 3-(R)(фенетилфенілкарбамоїлокси)-1-(2феноксіетил)-1-азоніабіцикло[2.2.2]октан, трифторацетат; 1-гептил-3-(R)(пент-4енілфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат; 1-аліл-3-(R)-(фенілтіофен-3-ілметилкарбамоїлокси)-1-азоніабіцикло[2.2.2]октан, трифторацетат; 3-(R)(фенілтіофен-3-ілметилкарбамоїлокси)-1(3-тіофен-2-ілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід; 1-(2-феноксіетил)-3-(R)(фенілтіофен-3ілметилкарбамоїлокси)-1-азоніабіцикло [2.2.2]октан, бромід; 3-(R)(біс-тіофен-2-ілметилкарбамоїлокси)-1-(3фенілпропіл)-1-азоніабіцикло [2.2.2]октан, бромід; 3-(R)(біс-тіофен-2-ілметилкарбамоїлокси)-1-(3тіофен-2-ілпропіл)-1-азоніабіцикло [2.2.2]октан, бромід; 1-аліл-3-(R)(алілтіофен-2ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат; 3-(R)(циклопентилтіофен-2ілметилкарбамоїлокси)-1-(3-фенілпропіл)-1азоніабіцикло[2.2.2]октан, трифторацетат; 3-(R)(фуран-2-ілметилфенілкарбамоїлокси)-1(3-фенілпропіл)-1-азоніабіцикло [2.2.2]октан, трифторацетат; 1-аліл-3-(R)(біс-фуран-2ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[(3-фторфеніл)-(3,4,5трифторбензил)карбамоїлокси]-1-(3-фенілпропіл)1-азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[(5-етилтіофен-2-ілметил)-(3метилтіофен-2-ілметил)карбамоїлокси]-1-(3фенілпропіл)- 1-азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[циклопентил-(5-етилтіофен-2ілметил)карбамоїлокси]-1-метил-1азоніабіцикло[2.2.2]октан, бромід. Особливо переважні індивідуальні сполуки формули (І) включають наступні сполуки: (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір [2-(3,4-диметоксифеніл)етил]-(5-метилфуран2-ілметил)карбамінової кислоти; 20 (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (5-бромтіофен-2-ілметил)-(2,4,5трифторфеніл)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (4-фтор-2-метилфеніл)-(3-метилтіофен-2ілметил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (3-фтор-4-метоксифеніл)тіофен-3ілметилкарбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір тіофен-3-ілметил-(2,4,5трифторбензил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (4-бром-5-метилтіофен-2-ілметил)-(3метилтіофен-2-ілметил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (4,5-диметилфуран-2-ілметил)-(5метилфуран-2-ілметил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір фуран-3-ілметил-(5-метил-2трифторметилфуран-3-ілметил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (2,5-диметилфуран-3-ілметил)-(2-фтор-4метоксибензил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір [2-(4-фтор феніл)етил]-(3-метилтіофен-2ілметил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір бутил-(2,5-дифторфеніл)карбамінової кислоти; (3R)-1-аза-біцикло[2.2.2]окт-3-иловий складний ефір (2,6-дифторфеніл)пент-4-енілкарбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір циклопентил-(4,5-диметилтіофен-2ілметил)карбамінової кислоти; (3R)-1-азабіцикло[2.2.2]окт-3-иловий складний ефір (5-етилтіофен-2-ілметил)-(3 -метилтіофен-2ілметил)карбамінової кислоти. Особливо переважні індивідуальні сполуки формули (II) включають наступні сполуки: (3R)-3-[(3-фторбензил)-(3фтор феніл)карбамоїлокси]-1-(2-феноксіетил)-1азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[(3-фторбеюил)-(3фтор феніл)карбамоїлокси]-1-(3-фенілпропіл)-1азоніабіцикло[2.2.2]октан, бромід; (3R)-1-(2-феноксіетил)-3-[м-толіл-(2,4,5трифторбензил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, бромід; (3R)-1-(3-фенілпропіл)-3-[м-толіл-(2,4,5трифторбензил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[(3-фторфеніл)-(3,4,5трифторбензил)карбамоїлокси]-1-(2-феноксіетил)1-азоніабіцикло[2.2.2]октан, бромід; (3R)-1-аліл-3-[[2-(3,4-диметоксифеніл)етил]-(5метилфуран-2-ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[(5-бромтіофен-2-ілметил)-(2,4,5трифторфеніл)карбамоїлокси]-1-(3феноксипропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат; 21 85541 (3R)-3-[[2-(3,4-диметоксифеніл)етил]-(5метилфуран-2-ілметил)карбамоїлокси]-1-(4етоксикарбонілбутил)-1-азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[(4-фтор-2-метилфеніл)-(3метилтіофен-2-ілметил)карбамоїлокси]-1-(2феноксіетил)-1-азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[(3-фтор-4-метоксифеніл)тіофен-3ілметилкарбамоїлокси]-1-(3-фенілаліл)-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-1-фенетил-3-[тіофен-3-ілметил-(2,4,5трифторбензил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[(4-бром-5-метилтіофен-2-ілметил)-(3метилтіофен-2-ілметил)карбамоїлокси]-1-(3фенілпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[(4,5-диметилфуран-2-ілметил)-(5метилфуран-2-ілметил)карбамоїлокси]-1-[3-(3гідроксифенокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-1-[3-(4-фторфенокси)пропіл]-3-[фуран-3ілметил-(5-метил-2-трифторметилфуран-3ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[(2,5-диметилфуран-3-ілметил)-(2-фтор4-метоксибензил)карбамоїлокси]-1-(3-тіофен-2ілпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-1-аліл-3-[2-(4-фторфеніл)етил]-(3метилтіофен-2-ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[бутил-(2,5дифторфеніл)карбамоїлокси]-1-гептил-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-1-(3-ціанопропіл)-3-[(2,6дифторфеніл)пент-4-енілкарбамоїлокси]-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[циклопентил-(4,5-диметилтіофен-2ілметил)карбамоїлокси]-1-метил-1азоніабіцикло[2.2.2]октан, трифторацетат; (3R)-3-[(3-фторфеніл)-(3,4,5трифторбензил)карбамоїлокси]-1-(3-фенілпропіл)1-азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[(5-eтилтioфeн-2-iлмeтил)-(3мeтилтioфeн-2-iлмeтил)кapбaмoїлoкcи]-1-(3фенілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[[2-(3,4-диметоксифеніл)етил]-(5метилфуран-2-ілметил)карбамоїлокси]-1-(4етоксикарбонілбутил)-1-азоніабіцикло[2.2.2]октан, форміат; (3R)-3-[(4-фтор-2-метилфеніл)-(3метилтіофен-2-ілметил)карбамоїлокси]-1-(2феноксіетил)-1-азоніабіцикло[2.2.2]октан, бромід; (3R)-3-[(3-фтор-4-метоксифеніл)тіофен-3ілметилкарбамоїлокси]-1-(3-фенілаліл)-1азоніабіцикло[2.2.2]октан, бромід; (3R)-1-аліл-3-[2-(4-фторфеніл)етил]-(3метилтіофен-2-ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, бромід. Даний винахід також стосується способів одержання сполук формул (І) і (II). Сполуки загальної формули (І) можуть бути отримані способом (а), який показаний на наступ 22 ній схемі і докладно описаний в розділі, присвяченому експериментальним прикладам. У формулах (I), (III) і (IV) R1, R2 і р є такими, як визначено вище. Сполуки загальної формули (III) можуть бути отримані з відповідних вторинних амінів відповідно до загального способу (б), описаного у літературі. Аміни загальної формули (V), які не є комерційно доступними, можуть бути отримані за допомогою синтезу відповідно до загальноприйнятих методик, такими як алкілування анілінів або відновне алкілування. Наприклад, аміни, у яких R1 являє собою заміщений тіофен-2-ілметил або заміщений фуран-2-ілметил, і R2 є таким, як визначено вище, можуть бути отримані відновними алкілуванням. Відповідний альдегід обробляють відповідним первинним аміном з одержанням при цьому іміну, який відновлюють боргідридом натрію в МеОН, одержуючи при цьому вторинний амін. Карбамати формули (І) можуть бути перетворені у фармацевтично прийнятні солі з використанням методик, відомих з попереднього рівня техніки. Звичайно карбамат формули (І) обробляють неорганічною або органічною кислотою, такою як фумарова, виннокам'яна, мурашина, янтарна або хлороводнева. Четвертинні амонієві похідні загальної формули (II) можуть бути отримані взаємодією алкілувального агента загальної формули (VI) із сполуками загальної формули (І), як показано на наведеній нижче схемі. У формулах (І), (II) і (VI) значення R1, R2, А, В, X, n, m і р є такими, як визначено вище. У формулі (VI) W являє собою будь-яку придатну гр уп у, яку відщеплюють, наприклад, таку як група X, як це визначено вище. Переважно, W являє собою групу X. Ця реакція алкілування може бути проведена з використанням двох різних експериментальних 23 85541 методик, (в) і (г), які описані нижче в розділі, присвяченому експериментальним прикладам. Спосіб (г), зокрема, являє собою новий спосіб проведення експерименту, з використанням методики твердофазної екстракції, яка дозволяє паралельно здійснити одержання декількох сполук. Якщо W являє собою групу іншу, ніж X, четвертинну амонієву сіль формули (II) одержують із продукту, одержуваного способом (в) або (г) за допомогою проведення обмінної реакції відповідно до загальноприйнятої методики, використовуваної для заміни аніона W на необхідний аніон X-. Способи (в) і (г) описані в розділі, присвяченому експериментальним прикладам. Сполуки загальної формули (VI), які не є комерційно доступними, одержують синтезом з використанням загальноприйнятих методик. Наприклад, сполуки, у яких n=0 і А=-О-, -S- або -NR4, де R4 є таким, як визначено вище, одержують взаємодією відповідного похідного спирту, тіолу або аміну або його натрієвої або калієвої солі з алкілувальним агентом загальної формули Y-(CH2)m-W, у якій W може являти собою галоген, і Υ може являти собою галоген або залишок складного ефіру - суль фонату. Відповідно до інших прикладів сполуки загальної формули (VI), у якій n>=1, синтезують з відповідного похідного спирту загальної формули (VII) відповідно до відомих способів. (VII) Сполуки формули (IV) можуть являти собою наступні сполуки: 4-гідрокси-1-азабіцикло[2.2.1]гептан, ця сполука описана в [WO93/15080]; 4-гідрокси-1-азабіцикло[2.2.2]октан, ця сполука описана в статті: [Grob, C.A. et.al. Helv.Chim.Acta (1958), ν.41, p.1184-1190]; (3R)-3-гідрокси-1-азабіцикло[2.2.2]октан або (3S)-3-гідрокси-1-азабіцикло[2.2.2]октан, ця сполука описана в статті: [Ringdahl, R. Acta Pharm Suec. (1979), 16, 281-283] і комерційно доступна від фірми «CU Chemie Uetikon GmbH». Структуру отриманих сполук підтверджують методами гH-ЯМР (ядерного магнітного резонансу) і мас-спектроскопії. Спектри ЯМР реєструють з використанням спектрометра «Varian», 300МГц, хімічні зсуви виражають у мільйонних частках (м.ч.) (δ) у порівнянні з внутрішнім стандартом тетраметилсиланом. Чистоту сполук визначають методом РХВР (рідинної хроматографії високого розділення) з використанням обернено-фазової хроматографії на приладі «Waters». Молекулярні іони одержують за допомогою мас-спектроскопії з іонізацією електроспреєм з використанням апаратури фірми «Hewlett Packard». PXBP-MC (рідинна хроматографія високого розділення в сполученні з мас-спектроскопією) здійснюють на приладі фірми «Gilson», обладнаному бінарним насосом («Gilson piston pump 321»); вакуумним дегазатором («Gilson 864»); колектором введення фракцій («Gilson liquid handler 215»); двома модулями інжекції, аналітичним і препаративним (Gilson 819); вентилем («Gilson Valvemate 7000); спліттером 1/1000 («Acurate, LC Packings»); підкачувальним насосом («Gilson 307»); детектором з діодною матрицею («Gilson 170») і мас-спектрометричним 24 детектором («Thermoquest Finnigan aQa», квадрупольним мас-спектрометром з використанням ES АРСІ іонізації). При роботі устаткування для РХВРМС керування здійснюють з використанням IBM PC-сумісного комп'ютера. Спосіб (а) Приклад 1 Одержання (3R)-1-азабіцикло[2.2.2]окт-3илового складного ефіру бутилфенілкарбамінової кислоти До 70мл сухого толуолу додають 0,65г (28,50ммоль) натрію. Суспензію кип'ятять зі зворотним холодильником при інтенсивному перемішуванні. Після того, як весь натрій розчиниться, додають 3,60г (28,30ммоль) (3R)-3-гідрокси-1азабіцикло[2.2.2]октану і продовжують перемішування протягом 2 годин, за цей час весь натрій вступить у реакцію з утворенням при цьому алкоголяту. Потім повільно додають 6,00г (28,30ммоль) фенілбутил-карбамоїлхлориду (проміжна сполука 1-1), розчиненого в 30мл толуолу. Отриману суміш кип'ятять зі зворотним холодильником протягом однієї години, і потім реакційну суміш перемішують протягом ночі при кімнатній температурі. С успензію фільтрують і отриманий фільтрат упарюють. До залишку додають ефір і перемішують протягом 10хв. С успензію фільтрують і концентрують фільтрат у вакуумі, одержуючи при цьому 7,18г коричневої маслянистої речовини. Цей продукт очищають колонковою хроматографією (силікагель, суміш хлороформ/етанол/аміак у співвідношенні 140:8:1) з одержанням при цьому 1,78г (5,89ммоль) (вихід 22%) чистої сполуки, структура якої підтверджується даними 1Н-ЯМР. 1 Н-ЯМР (300МГц, СОСI3): δ 0,9 (m, 3Н), 1,3 (m, 4Н), 1,5 (m, 4Н), 1,9 (s, 1Н), 2,7 (m, 5H), 3,2 (m, 1H), 3,7 (m, 2H), 4,7 (m, 1H), 7,2-7,4 (m, 5H); мас-спектроскопія, [М+1]+: 303. Приклад 2 Одержання (3R)-1-азабіцикло[2.2.2]окт-3илового складного ефіру циклопентилтіофен-2ілметилкарбамінової кислоти До 70мл сухого толуолу додають 0,57г (24,59ммоль) натрію. Суспензію кип'ятять зі зворотним холодильником при інтенсивному перемішуванні. Після того, як весь натрій розчиниться, додають, 3,11г (24,42ммоль) (3R)-3-гідрокси-1азабіцикло[2.2.2]октану і перемішують протягом 2 годин, за цей час весь натрій вступає в реакцію з утворенням при цьому алкоголяту. Потім повільно додають 4,96г (20,35ммоль) циклопентилтіофен-2ілметилкарбамоїлхлориду (проміжна сполука 1-2), розчиненого в 30мл толуолу. Отриману суміш кип'ятять зі зворотним холодильником протягом п'я ти годин, і потім реакційну суміш перемішують протягом ночі при кімнатній температурі. С успензію фільтрують і промивають фільтрат водою. Органічний шар екстрагують, використовуючи 20%-ну НСI, і потім водний шар підлуговують 8 Η розчином NaOH, після чого екстрагують етилацетатом. Органічний шар промивають водою, висушують над безводним Na2SO4 і упарюють. Отриману маслянисту речовину (4,50г) очищають колонковою хроматографією (силікагель, хлороформ/етанол/аміак у співвідношенні 225:8:1), оде 25 85541 ржуючи при цьому 2,25г (6,73ммоль) (вихід 33%) чистої сполуки, структура якої підтверджується даними 1Н-ЯМР. 1 Н-ЯМР(300МГц, ДМСО-d 6): δ 1,20-1,40 (m, 1H), 1,45-1,72 (m, 11Н), 1,89 (bs, 1H), 2,45-2,62 (m, 5H), 3,03-3,10 (m, 1H), 4,22 (bs, 1H), 4,50-4,63 (m, 3H), 6,93-6,99 (m, 2H), 7,38 (m, 1H); мас-спектроскопія, [М+1]+: 335. Приклад 3 Одержання 1-азабіцикло[2.2.1]гепт-4-илового складного ефіру бензилфенілкарбамінової кислоти У двогорлу колбу в атмосфері азоту поміщають 3мл ТГФ і 150мг (1,33ммоль) 4-гідрокси-1азабіцикло[2.2.1]гептану. Отриману суспензію охолоджують до -60°С і додають по краплях 0,7мл (1,46ммоль) LDA. Після додавання температурі дають підвищитися до 0°С і витримують протягом двох годин. Додають протягом 30 хвилин розчин 295мг (1,20ммоль) бензилфенілкарбамоїлхлориду в 2мл ТГФ. Реакційній суміші дають повільно нагрітися до кімнатної температури і перемішують протягом 18 годин. Суспензію фільтрують і фільтрат концентрують при зниженому тиску. Отриманий залишок екстрагують дихлорметаном і водою. Органічний шар екстрагують 2Н розчином НСI і потім водний шар підлуговують, використовуючи 8 Η розчин NaOH, після чого екстрагують дихлорметаном. Органічні шари висушують над безводним Na2SO4 і упарюють. Отриману маслянисту речовину (162мг) очищають за допомогою РХВР-МС, одержуючи при цьому 4,86мг (0,015ммоль), 1,3% чистої сполуки у вигляді форміату, стр уктура якого підтверджується даними 1H-ЯМР. 1 H-ЯМР (300МГц, ДМС О-d6): δ 1,86 (m, 4H), 2,65 (s, 2H), 2,77 (bs, 2H), 3,03 (bs, 2Н), 4,84 (s, 2Н), 7,14-7,32 (m, 10Н). 8,19 (s, 1H); мас-спектроскопія [М-НСОО]+: 323. Приклад 4 Одержання (3R)-1-азабіцикло[2.2.2]окт-3илового складного ефіру м-толіл-(2,4,5трифторбензил)карбамінової кислоти До 140мл сухого толуолу додають 0,69г (30ммоль) натрію (невеликими порціями). Суспензію кип'ятять зі зворотним холодильником при інтенсивному перемішуванні. Після того, як весь натрій розчиниться, додають 3,78г (29,73ммоль) (3R)-3-гідрокси-1-азабіцикло[2.2.2]октану, у п'ять прийомів, і отриману суміш кип'ятять зі зворотним холодильником протягом 2 годин, за цей час весь натрій вступає в реакцію з утворенням при цьому алкоголяту. Потім повільно додають розчин 8,11г (25,85ммоль) м-толіл-(2,4,5трифторбензил)карбамоїлхлориду (проміжна сполука 1-3) у 60мл толуолу. Отриману суміш кип'я тять зі зворотним холодильником протягом 3 годин, і потім перемішують при кімнатній температурі протягом ще 64 годин. Після закінчення цього часу реакційну суміш фільтрують і отриманий розчин екстрагують, використовуючи 2Η розчин НСI (2´125мл). Водні шари об'єднують, підлуговують твердим K2СО3 і екстрагують, використовуючи СНСІ3. Органічний шар висушують над безводним MgSO4, фільтрують і упарюють. Отриману маслянисту речовину (6,30г) очищають колонковою хроматографією (силікагель, суміш хлоро 26 форм/етанол у співвідношенні 5:1), одержуючи при цьому 3,05г (29,2%) чистої сполуки у вигляді маслянистої речовини, структура якої підтверджується даними 1Н-ЯМР. 1 Н-ЯМР (CDCI3): δ 1,22-1,40 (m, 1Н), 1,40-1,60 (m, 2H), 1,60-1,75 (m, 1H), 2,0 (m, 1H), 2,32 (s, 3H), 2,60-2,90 (m, 5H), 3,17-3,26 (m, 1H), 4,78-4,83 (m, 1H), 4,86 (s, 2H), 6,82-7,0 (m, 3H), 7,03-7,07 (m, 1H), 7,15-7,25 (m, 2H); мас-спектроскопія, [М+1]+: 405. Приклад 5 Одержання (3R)-1-азабіцикло[2.2.2]окт-3илового складного ефіру [2-(4-фторфеніл)етил]-(3метилтіофен-2-ілметил)карбамінової кислоти Суміш 0,7г (0,018моль) гідриду натрію (60%-на дисперсія в мінеральному маслі) і 1,8г (0,014моль) (3R)-3-гідрокси-1-азабіцикло[2.2.2]октану в 70мл толуолу кип'ятять зі зворотним холодильником протягом двох годин для того, щоб одержати алкоголят. Одержують суспензію білої твердої речовини. Потім повільно додають розчин 4,5г (0,014моль) [2-(4-фторфеніл)етил]-(3метилтіофен-2-ілметил)карбамоїлхлориду в 30мл толуолу. Отриману суміш кип'ятять зі зворотним холодильником протягом 2 годин і потім перемішують при кімнатній температурі протягом ще 64 годин. Після цього реакційну суміш охолоджують до 0-5°С і обережно при перемішуванні додають 75мл води. Органічну фазу відокремлюють і екстрагують, використовуючи 2Η розчин НСI (2´75мл). Водні фази об'єднують, підлуговують, використовуючи 2Н розчин NaOH, і екстрагують толуолом (2´75мл). Органічні шари об'єднують і концентрують розчин досуха. Отриману маслянисту речовину (1,80г) об'єдн ують з 0,3г продукту, о триманого на попередній стадії й очищають колонковою хроматографією (силікагель, як елюент використовують суміш CH2Cl2/MeOH/NH 4OH у співвідношенні 90:10:1), одержуючи при цьому 1,1г (сумарний вихід 13,7%) вказаної в заголовку сполуки у вигляді маслянистої речовини, структура цієї сполуки підтверджується даними 1Н-ЯМР. 1 Н-ЯМР (ДМСО-d6): δ 1,33 (m, 1H), 1,48 (m, 1H), 1,60 (m, 2H), 1,89 (m, 1H), 2,18 (s, 3H), 2,352,85 (m, 7H), 3,07 (m, 1H), 3,20-3,45 (m, 2H), 4,454,65 (m, 3H), 6,84 (m, 1H), 7,05-7,30 (m, 4H), 7,33 (m, 1H). мас-спектроскопія [М+1]+: 403. [2-(4-Фторфеніл)етил]-(3-метилтіофен-2ілметил)карбамоїлхлорид одержують відповідно до способу (б), використовуючи як вихідну сполуку відповідний амін. Спосіб (б) Карбамоїлхлориди загальної формули (III) одержують відповідно до методики, описаної в літературі: [М. Saraswati et al. Drug Development Research (1994), 31, 142-146; G. M. Shutske et al. J. Heterocycl. Chem. (1990), 27, 1617; GB 1246606; US 2762796]. Підготовчий приклад 1 Проміжна сполука 1-1 - одержання бутилфенілкарбамоїлхлориду. До розчину 6,72г (45ммоль) бутилфеніламіну в 50мл метиленхлориду, охолодженому до 10°С, повільно додають при перемішуванні 6,67г 27 85541 (22,5ммоль) трифосгену в 40мл метиленхлориду. Взаємодію продовжують при кімнатній температурі протягом 27 годин. Розчинник упарюють і отриманий залишок двічі екстрагують н-гексаном. Органічний розчин концентрують у вакуумі, одержуючи при цьому 9,11г (43,03ммоль) жовтої маслянистої речовини (вихід 96%). 1Н-ЯМР (CDCI3) : δ 0,9 (m, 3Н), 1,3 (m, 2H), 1,6 (m, 2H), 3,7 (m, 2H), 7,2-7,4 (m, 5H). Підготовчий приклад 2 Проміжна сполука 1-2 - одержання циклопентилтіофен-2-ілметилкарбамоїлхлориду До розчину 5,0г (27,58ммоль) циклопентилтіофен-2-ілметиламіну в 40мл метиленхлориду при 10°С повільно додають при перемішуванні 4,09г (13,79ммоль) трифосгену в 35мл метиленхлориду. Взаємодію здійснюють, продовжуючи перемішування при кімнатній температурі протягом 64 годин, кип'я тять зі зворотним холодильником протягом 4 годин і додатково витримують протягом 25 годин при кімнатній температурі. Розчинник упарюють і отриманий залишок екстрагують нгексаном. Органічний розчин концентрують з одержанням при цьому 4,96г (20,34ммоль) коричневої маслянистої речовини (вихід 74%). 1Н-ЯМР (CDCI3): δ 1,4 (m, 8Н), 4,2 (bs, 1Н), 4,5 (m, 2H), 6,87,3 (m, 3H). Підготовчий приклад 3 Проміжна сполука 1-3 - одержання м-толіл(2,4,5-трифторбензил)карбамоїлхлориду До розчину 6,5г (25,87ммоль) м-толіл-(2,4,5трифторбензил)аміну (проміжна сполука 1-7) у 45мл метиленхлориду, о холодженому при -10°С, повільно додають при перемішуванні розчин 3,84г (12,94ммоль) трифосгену в 25мл метиленхлориду. Реакційній суміші дають нагрітися до кімнатної температури, перемішують при цій температурі протягом 2 годин і потім кип'ятять зі зворотним холодильником протягом 10 годин. Після закінчення цього часу тверда речовина, яка утворилася при проведенні процесу, розчиняється. Розчинник упарюють і отриманий залишок обробляють нгексаном при -25°С. Розчинну частину відокремлюють і фільтрують. Фільтрат концентрують у вакуумі, одержуючи при цьому 8,2г маслянисті речовини. Структур у сполуки підтверджують даними 1 Н-ЯМР. 1 H-ЯМР (CDCI3): δ 2,30 (s, 3Н), 4,85 (s, 2Н), 6,70-7,10 (m, 3Н), 7,10-7,40 (m, 3Н). Підготовчий приклад 4 Проміжна сполука 1-4 - одержання 3фтор феніл-(3,4,5трифторбензил)карбамоїлхлориду До розчину 3,4г (13,30ммоль) 3-фторфеніл(3,4,5-трифторбензил)аміну (проміжна сполука 18) у 25мл метиленхлориду, о холодженому при 10°С, повільно додають при перемішуванні розчин 2,0г (6,70ммоль) трифосгену в 15мл метиленхлориду. Реакційній суміші дають нагрітися до кімнатної температури і при цій температурі перемішують протягом 17 годин. Після цього тверду речовину, яка утворилася при проведенні процесу, відфільтровують і потім фільтрат концентрують у вакуумі. Отриманий залишок обробляють нгексаном при -25°С. Розчинну частину відокрем 28 люють і фільтрують. Фільтрат концентрують у вакуумі досуха, одержуючи при цьому 2,65г (вихід 62,8%) вказаної в заголовку сполуки у вигляді маслянистої речовини. Структуру сполуки підтверджують даними 1Н-ЯМР. 1 Н-ЯМР (CDCI3): δ 4,80 (s, 2Н), 6,70-7,0 (m, 4Н), 7,0-7,20 (m, 1H), 7,25-7,45 (m, 1H). Підготовчі приклади 5-12 Прикладами деяких інших сполук формули (III), які одержують відповідно до даного винаходу відповідно до способу (б), є наступні сполуки: (3-фторбензил)-(3фтор феніл)карбамоїлхлорид; циклогексилметил-(2фтор феніл)карбамоїлхлорид; [2-(3,4-диметоксифеніл)етил]-(5-метилфуран2-ілметил)карбамоїлхлорид; (5-бромтіофен-2-ілметил)-(2,4,5трифторфеніл)карбамоїлхлорид; (4-фтор-2-метилфеніл)-(3-метилтіофен-2ілметил)карбамоїлхлорид; (3-фтор-4-метоксифеніл)тіофен-3ілметилкарбамоїлхлорид; (4,5-диметилфуран-2-ілметил)-(5-метилфуран2-ілметил)карбамоїлхлорид; [2-(4-фторфеніл)етил]-(3-метилтіофен-2ілметил)карбамоїлхлорид. Підготовчий приклад 13 Проміжна сполука 1-5 - одержання [2-(3,4диметоксифеніл)етил]-(5-метилфуран-2ілметил)аміни До розчину 4,82г (26,6ммоль) 2-(3,4диметоксифеніл)етиламіну і 3,0г (27,2ммоль) 5метилфуран-2-карбальдегіду в 65мл ЕtOН додають 18,3г молекулярних сит (0,3нм) і отриману суміш кип'ятять зі зворотним холодильником протягом 4 годин. Після цього реакційну суміш охолоджують до кімнатної температури і фільтрують. Отриманий розчин концентрують у вакуумі з одержанням при цьому маслянистої речовини. Цю маслянисту речовину розчиняють у 65мл МеОН і додають невеликими порціями 1,01г (26,6ммоль) NaBH 4, підтримуючи температуру реакційної суміші на рівні кімнатної температури. Отриману суміш перемішують при цій температурі додатково протягом 16 годин. Після цього розчинник упарюють у вакуумі й отриманий залишок обробляють 150мл води і потім двічі екстрагують ефіром. Органічні шари об'єднують, промивають насиченим розчином солі, висушують над безводним MgSO4, фільтрують і упарюють досуха, одержуючи при цьому 6,05г (вихід 82,6%) вказаної в заголовку сполуки у вигляді маслянистої речовини. Mac-спектроскопія, [М+1]+: 276; 1 Н-ЯМР (CDCI3) : δ 2,25 (s, 3Н), 2,70-2,95 (m, 4Н), 3,75 (s, 2Н), 3,85 (два синглети, 6Н), 5,85 (m, 1Н), 6,02 (m, 1H), 6,70-6,85 (m, 3Н). Підготовчий приклад 14 Проміжна сполука 1-6 - одержання (5бромтіофен-2-ілметил)-(2,4,5-трифторфеніл)аміну До розчину 2г (13,6ммоль) 2,4,5трифторфеніламіну і 2,66г (13,9ммоль) 5бромтіофен-2-карбальдегіду в 30мл ЕtOН, додають 9,4г молекулярних сит (0,3нм) і отриману суміш кип'ятять зі зворотним холодильником протя 29 85541 гом 20 годин. Після цього реакційну суміш охолоджують до кімнатної температури, фільтрують і упарюють розчинник у вакуумі. Отриману маслянисту речовину розчиняють у 30мл МеОН і додають невеликими порціями 0,51г (13,6ммоль) NaBH4, підтримуючи температуру реакційної суміші на рівні кімнатної температури. Отриману суміш перемішують при цій температурі додатково протягом 20 годин. Після цього розчинник упарюють у вакуумі й отриманий залишок обробляють, використовуючи 100мл води, і потім двічі екстрагують ефіром. Органічні шари об'єднують, промивають насиченим розчином солі, висушують над безводним MgSO4, фільтрують і упарюють досуха, одержуючи при цьому 3,2г маслянисті речовини. Ці 3,2г об'єднують з 3,5г, отриманими на наступній стадії, і сумарний отриманий продукт (6,7г) очищають хроматографією на силікагелі, використовуючи як елюент суміш гексан/AcOEt у співвідношенні 5:1→1:1. Відповідні фракції об'єднують, одержуючи при цьому 0,95г вказаної в заголовку сполуки у вигляді маслянистої речовини (сумарний вихід 8,2%). Mac-спектроскопія [М+1]+: 321,323; 1 Н-ЯМР (CDCI3): δ 4,10 (bs, NH, 1H), 4,40 (s, 2H), 6,40-6,65 (m, 1H), 6,75-7,10 (m, 3H). Підготовчий приклад 15 Проміжна сполука 1-7 - одержання м-толіл(2,4,5-трифторбензил)аміну До розчину м-толіламіну (3,26г, 3,27мл, 30,5ммоль) і 2,4,5-трифторбензальдегіду (5,0г, 31,2ммоль) у 60мл ЕtOН, додають 21г молекулярних сит (0,3нм) і отриману суміш кип'ятять зі зворотним холодильником протягом З годин. Після цього реакційну суміш охолоджують до кімнатної температури і фільтрують. Отриманий розчин концентрують у вакуумі, одержуючи при цьому маслянисту речовину. Цю маслянисту речовину розчиняють у 60мл МеОН і додають невеликими порціями 1,15г (30,5ммоль) NaBH4, підтримуючи температуру реакційної суміші на рівні кімнатної температури. Реакційну суміш перемішують при цій температурі протягом додатково 16 годин. Після цього розчинник упарюють у вакуумі й отриманий залишок обробляють, використовуючи 100мл води, потім двічі екстрагують ефіром. Органічні шари об'єднують, промивають насиченим розчином солі, висушують над безводним MgSO4, фільтрують і концентрують у вакуумі досуха, одержуючи при цьому 6,5г (вихід 84,8%) вказаної в заголовку сполуки у вигляді маслянистої речовини (яка твердне при низькій температурі). Структуру сполуки підтверджують даними ^-RMN і масспектроскопії. ГХ/МС: [М]+: 251; 1 H-ЯМР (CDCI3) : δ 2,25 (s, 3Н), 4,0 (bs, 1Н), 4,35 (s, 2H), 6,35-6,65 (m, 3H), 6,85-7,40 (m, 3H). Підготовчий приклад 16 Проміжна сполука 1-8 - одержання (3фтор феніл)-(3,4,5-трифторбензил)аміну Суміш 3,7г (3,2мл, 33,3ммоль) 3фтор феніламіну, 2,5г (11,1ммоль) 5-(бромметил)1,2,3-трифторбензолу і 1,53г (11,1ммоль) K2СО3 у 30 30мл толуолу, кип'ятять зі зворотним холодильником протягом 5 год і перемішують при кімнатній температурі ще протягом 16 годин. Після цього реакційну суміш фільтрують і отриману тверду речовину промивають толуолом. Толуольні розчини об'єднують, промивають водою і насиченим розчином солі, висушують над MgSO4 і концентрують у вакуумі досуха, одержуючи при цьому 5,0г маслянистого залишку. Цю маслянисту речовину обробляють діетиловим ефіром, потім отриману тверду речовину відокремлюють фільтруванням і викидають. Фільтрат концентрують досуха й очищають, використовуючи тр убку з кульовим розширенням, перегонкою при зниженому тиску. Після відгону надлишку 3-фторфеніламіну (0,15мм Hg, нагрівання при 100°С) відганяють 2,40г (вихід 84,8%) вказаної в заголовку сполуки (0,15мм Hg, нагрівання 175-200°С). Структура сполуки підтверджується даними мас-спектроскопії і 1H-RMN. ГХ/МС: [M]+: 255; 1 Н-ЯМР (CDCI3): δ 4,30 (s, 2Н), 4,0-4,50 (bs, 1Н), 6,20-6,55 (m, 3H), 6,80-7,25 (m, 3H). 3-Фторфеніл-(3,4,5-трифторбензил)амін також одержують відновним алкілуванням, використовуючи як вихідні сполуки 3,4,5-трифторбензальдегід і 3-фторфеніламін. Підготовчі приклади 17-22 Деякі інші приклади отриманих сполук формули (V) згідно із даним винаходом включають: (3-фторбензил)-(3-фторфеніл)амін; циклогексилметил-(2-фторфеніл)амін; (4-фтор-2-метилфеніл)-(3-метилтіофен-2ілметил)амін; (3-фтор-4-метоксифеніл)тіофен-3-ілметиламін; (4,5-диметилфуран-2-ілметил)-(5-метилфуран2-ілметил)амін; [2-(4-фторфеніл)етил]-(3-метилтіофен-2ілметил)амін. Спосіб (в) Приклад 6 Одержання (3R)-3-(біс-тіофен-2ілметилкарбамоїлокси)-1-(3-тіофен-2-ілпропіл)-1азоніабіцикло[2.2.2]октану, броміду. Змішують 0,54г (1,5ммоль) (3R)-1азабіцикло[2.2.2]окт-3-илового складного ефіру біс-тіофен-2-ілметилкарбамінової кислоти, 7,5мл тетрагідрофурану і 0,46г (2,25ммоль) 2-(3бромпропіл)тіофену. Отриманий розчин кип'ятять зі зворотним холодильником протягом 4 годин і потім перемішують при кімнатній температурі ще 116 годин. Додають ефір і отриману суміш перемішують протягом 30хв. Розчинник екстрагують і додають додаткову кількість ефіру. Цю процедуру повторюють декілька разів для того, щоб видалити алкілувальний агент. На закінчення суспензію фільтрують і отриманий залишок висушують у вакуумній шафі. Вихід становить 0,69г (1,22ммоль) (81%). 1 H-ЯМР (ДМСО-d6): 1,78-2,10 (m, 6H), 2,34 (bs, 1H), 2,82 (m, 2H), 3,21-3,46 (m, 7H), 3,89 (m, 1H), 4,54 (m, 4H), 5,06 (m, 1H), 6,95-7,01 (m, 4H), 7,077,11 (m, 2H), 7,38-7,49 (m, 3H); мас-спектроскопія [M-Br]+: 487; т. пл.: 143°С. 31 85541 Приклад 7 Одержання (3R)-1-(2-феноксіетил)-3-[м-толіл(2,4,5-трифторбензил)карбамоїлокси]-1азоніабіцикло[2.2.2]октану, броміду Змішують 0,300г (0,742ммоль) (3R)-1азабіцикло[2.2.2]окт-3-илового складного ефіру мтоліл-(2,4,5-трифторбензил)карбамінової кислоти, 7,0мл тетрагідрофурану і 0,253г (1,258ммоль) (2брометокси)бензолу. Отриманий розчин кип'ятять зі зворотним холодильником протягом 55 годин і залишають при перемішуванні при кімнатній температурі ще протягом 16 годин. Після цього розчинник упарюють у вакуумі. Додають ефір і отриману суміш перемішують, одержуючи при цьому тверду речовину. Цю тверду речовину обробляють декілька разів ефіром для того, щоб видалити алкілувальний агент, що залишився. На закінчення суспензію фільтрують і отриману тверду речовину промивають ефіром і висушують. Вихід становить 0,34г (75,5%). Т. пл.: 137,3-139,1°С; мас-спектроскопія [М-Вr]+: 525; 1 Н-ЯМР (ДМСО-d6): δ 1,40-1,70 (m, 1Н), 1,702,05 (m, 3Н), 2,20 (m, 1H), 2,25 (s, 3H), 3,25-3,40 (m, 1H), 3,40-3,80 (m, 6H), 3,95-4,10 (m, 1H), 4,44 (m, 2H), 4,90 (m, 2H), 5,01 (m, 1H), 6,95-7,30 (m, 7H), 7,30-7,60 (m, 4H). Приклад 8 Одержання (3R)-1-аліл-3-[[2-(3,4диметоксифеніл)етил]-(5-метилфуран-2ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октану, броміду 0,300г (0,7ммоль) (3R)-1-азабіцикло[2.2.2]окт3-илового складного ефіру [2-(3,4диметоксифеніл)етил]-(5-метилфуран-2ілметил)карбамінової кислоти розчиняють у 5мл СНСІ3 і 3,5мл ацетонітрилу. До цього розчину додають 0,30мл (0,423г, 3,5ммоль) алілброміду й отриману суміш перемішують протягом 21 години при кімнатній температурі в атмосфері N2. Розчинники упарюють. Отриманий залишок обробляють декілька разів ефіром, одержуючи при цьому маслянисту речовину, яку перерозчиняють у СНСІ3 і упарюють досуха з одержанням при цьому 0,365г (вихід 94,8 %) вказаної в заголовку сполуки. Mac-спектроскопія [М-Вr]+: 469. Спосіб (г) Приклад 9 Одержання (3R)-1-гептил-3-(фенілтіофен-3ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октану, трифторацетату 30мг (0,08ммоль) (3R)-1-азабіцикло[2.2.2]окт3-илового складного ефіру фенілтіофен-3ілметилкарбамінової кислоти розчиняють у 1мл ДМСО. До цього розчину додають 75мг (0,40ммоль) гептилброміду. Після перемішування протягом ночі при кімнатній температурі отриману суміш очищають твердофазною екстракцією з використанням катіонообмінного картриджа «Mega Bond Elut cartridge», попередньо обробленого при рН=7,5 з використанням 0,1Μ МаН2РО4-буфера. Реакційну суміш наносять на картридж і промивають спочатку, використовуючи 2мл ДМСО, і потім три рази, використовуючи 5мл CH3CN, відмиваючи 32 при цьому усі вихідні речовини. Амонієві похідні елюють, використовуючи 5мл 0,03Μ розчину ТФК у суміші СН3СN:СНСl3 (у співвідношенні 2:1). Цей розчин нейтралізують, використовуючи 300мг полі(4-вінілпіридину), фільтрують і упарюють досуха. Вихід вказаної в заголовку сполуки становить 12мг (34%). 1 Н-ЯМР (ДМСО-d6): δ 0,88 (m, 3Н), 1,28 (m, 8Н), 1,60-2,19 (m, 7Н), 3,00-3,41 (m, 7Н), 3,83 (m, 1Н), 4,88 (s, 2H), 5,99 (m, 1H), 7,01 (m, 1H), 7,217,39 (m, 6H), 7,49-7,52 (m, 1H); мас-спектроскопія [M-CF3COO]+: 441. В обсяг даного винаходу також входять фармацевтичні композиції, які включають як активний інгредієнт принаймні одне похідне хінуклідину загальної формули (І) або (II) у сполученні з фармацевтично прийнятним носієм або розріджувачем. Переважно, композицію готують у формі, прийнятній для перорального введення. Фармацевтично прийнятні носій або розріджувачі, які змішують з активною сполукою або сполуками, з одержанням при цьому композиції згідно із даним винаходом, добре відомі самі по собі, і вибір конкретно використовуваних допоміжних речовин залежить, зокрема, від способу введення композиції. Композиції згідно із даним винаходом переважно застосовують для перорального введення. У цьому випадку композиції для перорального введення можуть бути представлені у вигляді таблеток, таблеток із плівковим покриттям, рідких засобів для інгаляції, порошкових інгаляцій і аерозолів для інгаляції; які містять одну або декілька сполук згідно із даним винаходом; такі препарати можуть бути о тримані способами, добре відомими з попереднього рівня техніки. Розріджувачі, які можуть бути використані для приготування препаратів, включають такі рідкі і тверді розріджувачі, які сумісні з активним інгредієнтом, разом з агентами, які підфарбовують, або агентами, які поліпшують смак і запах, якщо це потрібно. Таблетки або таблетки з плівковим покриттям можуть підходяще містити від 0,1мг до 500мг, переважно, від 0,5 до 200мг активного інгредієнта. Композиції для інгаляцій можуть містити від 1мкг до 1000мкг, переважно, від 10 до 800мкг активного інгредієнта. При терапевтичному лікуванні людини доза сполуки загальної формули (І) або (II) буде залежати від потрібного ефекту і тривалості лікування; дози для дорослих звичайно становлять від 0,5мг до 300мг у день при прийомі у вигляді таблеток і від 10мкг до 800мкг у день для інгаляційних засобів. Сполуки згідно із даним винаходом, або фармацевтичні композиції, які містять їх, можуть бути використані разом з β2-агоністом, стероїдом, протиалергічним лікарським засобом і/або інгібітором фосфодіестерази IV для одночасного, окремого або послідовного використання при лікуванні респіраторного захворювання. Фармакологічна дія Наступні приклади наведені для демонстрації високої фармацевтичної активності сполук згідно із даним винаходом. Результати зв'язування з му 33 85541 скариновим рецептором людини і тестування на бронхоспазм у морських свинок отримані таким чином, як описано нижче. Дослідження зв'язування з мускариновим рецептором людини Зв'язування [3H]-N MS з мускариновими рецепторами проводили відповідно до методики, описаної в статті: [Waelbroeck et al (1990), Моl. Pharmacol., 38: 267-273]. Дослідження проводять при температурі 25°С. Використовують препарати мембран стабільно трансфектованих К1-клітин яєчників китайських хом'яків (СНО), які експреують гени для мускаринових рецепторів людини. Для визначення ІС50 препарати мембран суспендують у DPBS до кінцевої концентрації 89мкг/мл для М3 підтипу. Суспензію мембран інкубують з міченою тритієм сполукою протягом 60хв. Після інкубування фракцію мембран відокремлюють за допомогою фільтрації і визначають радіоактивність зв'язаних з мембраною сполук. Неспецифічне зв'язування визначають за допомогою додавання 10-4Μ атропіну. Дослідження проводять у відношенні принаймні шести концентрацій, здійснюючи паралельно по два вимірювання, з побудовою індивідуальних кривих заміщення. Отримані результати свідчать про те, що сполуки згідно із даним винаходом мають високу спорідненість по відношенню до мускаринових М3 рецепторів. Переважні сполуки згідно із даним винаходом характеризуються величиною ІС 50 (нМ) для М3 рецепторів, що становить менше, ніж 35нМ, найбільше переважно, менше ніж 10нМ. Переважні сполуки згідно із даним винаходом також мають високу селективність по відношенню до М3 рецепторів у порівнянні із селективністю у відношенні М2 рецепторів. Так, співвідношення ІС50 M2/ІС50 М3 становить більше, ніж 5, переважно, більше, ніж 10, найбільш переважно, більше ніж 15. Тестування на бронхоспазм у морських свинок Дослідження проводили відповідно до методики, описаної в статті: [Н. Konzett, F. Rossler (1940), Arch. Exp. Path. Pharmacol. 195, 71-74]. З водних розчинів агентів, які піддаються тестуванню, одержують аерозоль і вводять його за допомогою інгаляції підданим анестезії примусово вентильованим самцям морських свинок (лінія «DunkinHartley»). Бронхіальний відклик на внутрішньовенне введення ацетилхоліну визначали до і після введення лікарського засобу, зміни легеневого опору для декількох точок у часі виражають у вигляді відсотка інгібування бронхоспазму. Сполуки згідно із даним винаходом виявляють високу бронходилаторну активність і мають тривалу дію. Виходячи з описаних ви ще результатів досліджень, фахівець у даній галузі те хніки може легко зрозуміти, що сполуки згідно із даним винаходом мають значну антимускаринову активність (М3) і внаслідок цього можуть бути використані для лікування захворювань, перебіг яких зв'язаний з мускариновим М3 рецептором, включаючи респіраторні захворювання, такі як хронічне обструктивне захворювання легень, бронхіт, астма, бронхіальна гіперреактивність і риніт; захворювання сечового 34 міхура, такі як мимовільне сечовипускання і нетримання сечі, полакіурія (прискорене сечовипускання), неврогенна дисфункція сечового міхура, нічне нетримання сечі, нестабільне функціонування сечового міхура, цистоспазм і хронічний цистит; шлунково-кишкові захворювання, такі як синдром подразненого кишечнику, спастичний коліт, дивертикуліт і пептична виразка; а також захворювання серцево-судинної системи, такі як вагусно індукована синусова брадикардія. Наприклад, сполуки згідно із даним винаходом можуть бути використані для лікування респіраторних захворювань, таких як хронічне обструктивне захворювання легень, хронічний бронхіт, астма і риніт; урологічних захворювань, таких як мимовільне сечовипускання і нетримання сечі, прискорене сечовипускання при полакіурії нервового походження, нейрогенний сечовий міхур, нічний енурез, нестабільне функціонування сечового міхура, цистоспазм і хронічний цистит; а також шлунково-кишкових захворювань, таких як синдром подразненого кишечнику, спастичний коліт і дивертикуліт. Даний винахід також стосується сполук формули (І) або (II) або фармацевтично прийнятної композиції, яка включає сполуку формули (І) або (II), для використанні при здійсненні способу лікування людини або тварини за допомогою терапії, зокрема, для лікування респіраторних, урологічних або шлунково-кишкових захворювань. Даний винахід також стосується застосування сполуки формули (І) або (II) або фармацевтично прийнятної композиції, яка включає сполуку формули (І) або (II) для одержання лікарського засобу, призначеного для лікування респіраторних, урологічних або шлунково-кишкових захворювань. Крім того, сполуки формули (І) або (II) і фармацевтичні композиції, які включають сполуку формули (І) або (II), можуть бути використані при здійсненні способу лікування респіраторного, урологічного або шлунково-кишкового захворювання, такий спосіб включає введення пацієнту - людині або тварині, яка потребує такого лікування, ефективної кількості сполуки формули (І) або (II) або фармацевтичної композиції, яка включає сполуку формули (І) або (II). Крім того, сполуки формули (І) або (II) і фармацевтичні композиції, які включають сполуку формули (І) або (II) можуть бути використані в сполученні з іншими лікарськими засобами, ефективними при лікуванні цих захворювань. Наприклад, у сполученні з β2 агоністами, стероїдами, протиалергічними лікарськими засобами, інгібіторами фосфодіестерази IV і/або інгібіторами лейкотриєну D4 (LTD4), для одночасного, окремого або послідовного використання при лікуванні респіраторного захворювання. Таким чином, даний винахід стосується набору продуктів, який включає (і) сполуку згідно із даним винаходом; і (іі) іншу сполук у, е фективну при лікуванні респіраторного, урологічного або шлунково-кишкового захворювання, порушення або розладу для одночасного, окремого або послідовного використання. 35 85541 Сполука (іі), яка ефективна при лікуванні респіраторного, урологічного або шлунково-кишкового захворювання, порушення або розладу може являти собою β2-агоніст, стероїд, протиалергічний лікарський засіб, інгібітор фосфодіестерази IV і/або антагоніст лейкотриєну D4 (LTD4). Переважно, набір продуктів призначений для їх одночасного, окремого або послідовного використання при лікуванні респіраторного захворювання. Далі даний винахід буде проілюстрований наступними прикладами. Приклади наводяться тільки для ілюстрації і їх не слід розглядати як такі, що обмежують обсяг винаходу. Приклад 10 (3R)-1-Азабіцикло[2.2.2]окт-3-иловий складний ефір (3-фторбензил)-(3-фторфеніл)карбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід становить 3,0г, 39,1%. Mac-спектроскопія [М+1]+: 373; 1 Н-ЯМР (CDCI3): δ 1,20-1,35 (m, 1H), 1,35-1,50 (m, 1H), 1,50-1,60 (m, 1H), 1,60-1,75 (m, 1H), 2,0 (m, 1H), 2,55-2,85 (m, 5H), 3,18-3,27 (m, 1H), 4,79-4,90 (m, 1H), 4,90 (s, 2H), 6,85-7,10 (m, 5H), 1,22-1,2,5 (m, 3H). Приклад 11 (3R)-3-[(3-Фторбензил)-(3фтор феніл)карбамоїлокси]-1-(2-феноксіетил)-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способів (а) і (в). Вихід на заключній стадії становить 0,32г, 69,2%. Т. пл.: 142,8-143,6°С; мас-спектроскопія [М-Вr]+: 493; 1 Н-ЯМР (ДМСО-d6): δ 1,50-1,70 (m, 1H), 1,701,85 (m, 1H), 1,85-2,05 (m, 2H), 2,23 (m, 1H), 3,253,40 (m, 1H), 3,40-3,75 (m, 6H), 3,95-4,10 (m, 1H), 4,44 (m, 2H), 4,90-5,10 (m, 3H), 6,90-7,25 (m, 8H), 7,25-7,45 (m, 5H). Приклад 12 (3R)-3-[(3-Фторбензил)-(3фтор феніл)карбамоїлокси]-1-(3-фенілпропіл)-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способів (а) і (в). Вихід на заключній стадії становить 0,24г, 52,1%. Т.пл: 64,5-66,0°С; мас-спектроскопія [М-Вr]+: 491; 1H-ЯМР (ДМСО-d6): δ 1,50-1,65 (m, 1Н), 1,651,80 (m, 1H), 1,80-2,10 (m, 4H), 2,20 (m, 1H), 2,60 (t, 2H), 3,05-3,55 (m, 7H), 3,80-3,90 (m, 1H), 4,90-5,10 (m, 3H), 7,05-7,45 (m, 13H). Приклад 13 (3R)-1-(3-Фенілпропіл)-3-[м-толіл-(2,4,5трифторбензил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способів (а) і (в). Вихід на заключній стадії становить 0,32г, 72,5%. Т.пл: 113,1-114,8°С; мас-спектроскопія [М-Вr]+: 523; 1 H-ЯМР (ДМСО-d6): δ 1,40-1,60 (m, 1H), 1,601,80 (m, 1H), 1,80-2,10 (m, 4H), 2,18 (m, 1H), 2,26 (s, 3Н), 2,60 (t, 2H), 3,05-3,55 (m, 7H), 3,80-3,90 (m, 36 1H), 4,90 (m, 2H), 4,98 (m, 1H), 7,0-7,15 (m, 2H), 7,15-7,40 (m, 7H), 7,40-7,60 (m, 2H). Приклад 14 (3R)-1-Азабіцикло[2.2.2]окт-3-иловий складний ефір (3-фтор феніл)-(3,4,5трифторбензил)карбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід становить 0,33г, 8,8%. Мас-спектроскопія [М+1]+: 409; 1 H-ЯМР (CDCl3): 61,20-1,80 (m, 4H), 2,02 (m, 1H), 2,60-3,05 (m, 5H), 3,25-3,40 (m, 1H), 4,70-4,82 (m, 2H), 4,85-4,90 (m, 1H), 6,80-7,10 (m, 4H), 7,207,40 (m, 2H). Приклад 15 (3R)-3-[(3-Фторфеніл)-(3,4,5трифторбензил)карбамоїлокси]-1-(2-феноксіетил)1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способів (а) і (в). Вихід на заключній стадії становить 0,16г, 75%. Т.пл: 173,9-175,5°С; мас-спектроскопія [М-Вr]+: 529; 1 Н-ЯМР (ДМСО-d6): δ 1,50-2,05 (m, 4Н), 2,24 (m, 1Н), 3,25-3,85 (m, 7Н), 4,03 (m, 1H), 4,45 (m, 2Н), 4,95 (m, 2Н), 5,04 (m, 1H), 6,95-7,15 (m, 4Н), 7,20-7,45 (m, 7Н). Приклад 16 (3R)-1-Азабіцикло[2.2.2]окт-3-иловий складний ефір циклогексилметил-(2фтор феніл)карбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід становить 3,15г, 42,3%. Мас-спектроскопія [М+1]+: 361; 1 H-ЯМР (СDСІ3): δ 0,80-1,05 (m, 2Н), 1,05-1,80 (m, 13Н), 2,0 (m, 1H), 2,55-3,05 (m, 5Н), 3,15-3,30 (m, 1H), 3,40-3,60 (m, 2H), 4,70-4,85 (m, 1H), 7,057,35 (m, 4H). Приклад 17 (3R)-3-[Циклогексилметил-(2фтор феніл)карбамоїлокси]-1-(2-феноксіетил)-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способів (а) і (в). Вихід на заключній стадії становить 0,38г, 81,4%. Т.пл: 73,1-74,5°С; мас-спектроскопія [М-Вr]+: 481; 1 Н-ЯМР (ДМСО-d6): δ 0,80-1,0 (m, 2Н), 1,0-1,20 (m, 3Н), 1,20-1,45 (m, 1H), 1,45-1,80 (m, 6Н), 1,802,20 (m, 4Н), 3,05-3,20 (m, 1H), 3,30-3,85 (m, 8Н), 3,90-4,10 (m, 1H), 4,35-4,50 (m, 2Н), 4,90-5,10 (m, 1Н), 6,95-7,10 (m, 3Н), 7,20-7,55 (m, 6H). Приклад 18 (3R)-3-[Циклогексилметил-(2фтор феніл)карбамоїлокси]-1-(3-фенілпропіл)-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способів (а) і (в). Вихід на заключній стадії становить 0,34г, 73 %. Т.пл: 73,3-74,1°С; мас-спектроскопія [М-Вr]+: 479; 1 Н-ЯМР (ДМСО-d6): δ 0,80-1,45 (m, 6H), 1,502,20 (m, 12Н), 2,57 (m, 2H), 2,90-3,0 (m, 1Н), 3,10 37 85541 3,65 (m, 8H), 3,75-3,95 (m, 1H), 4,90-5,05 (m, 1H), 7,20-7,55 (m, 9H). Приклад 19 (3R)-1-Азабіцикло[2.2.2]окт-3-иловий складний ефір [2-(3,4-диметоксифеніл)етил]-(5-метилфуран2-ілметил) карбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід становить 3,5г, 61,2%. Мас-спектроскопія [М+1]+: 429; 1 H-ЯМР (СDСІ3): δ 1,34-1,50 (m, 1Н), 1,50-1,64 (m, 1H), 1,64-1,78 (m, 1H), 1,78-1,94 (m, 1H), 2,05 (m, 1H), 2,27 (два синглети, 3Н), 2,64-2,84 (m, 5H), 2,84-2,98 (m, 2H), 3,20-3,30 (m, 1H), 3,35-3,60 (m, 2H), 3,82 (s, 6H), 4,28 (m, 1H), 4,36 (m, 1H), 4,7 (m, 1H), 5,89 (m, 1H), 6,03-6,13 (m, 1H), 6,60-6,82 (m, 3H). Приклад 20 (3R)-3-[[2-(3,4-Диметоксифеніл)етил]-(5метилфуран-2-ілметил)-карбамоїлокси]-1-(4етоксикарбонілбутил)-1-азоніабіцикло[2.2.2]октан, форміат Вказану в заголовку сполуку синтез ують відповідно до способів (а) і (в). Алкілувальний агент, який використовують відповідно до способу (в), являє собою етиловий ефір 5-бромпентанової кислоти. Порцію отриманого продукту масою 270мг очищають препаративною РХВР/МС, одержуючи при цьому 53мг чистої сполуки у вигляді форміату. Мас-спектроскопія [М-НСОО-]+: 557; 1 Н-ЯМР (ДМСО-d6): δ 1,16-1,23 (m, 3Н), 1,451,75 (m, 4H), 1,75-2,10 (m, 4H), 2,14-2,28 (m, 1H), 2,24 (s, 3Н), 2,38 (m, 2H), 2,68 (m, 2H), 3,0-3,90 (m, ЮН), 3,71 і 3,73 (два синглети, 6Н), 4,03-4,10 (m, 2Н), 4,31-4,48 (m, 2Н), 4,80-5,0 (m, 1Н), 6,03 (m, 1Н), 6,27 (m, 1H), 6,64-6,88 (m, 3Н), 8,34 (s, 1H). Умови проведення очищення з використанням методу РХВР-МС: колонка: симетричний С18,100 А, 5мкм 19´100мм, «Waters», рухома фаза: А (Н2О 0,1% HCOONH 4, рН=3) і В (AcN 0,1% HCOONH4, pH=3), В: 19%→34%. Приклад 21 (3R)-1-Азабіцикло[2.2.2]окт-3-иловий складний ефір (5-бромтіофен-2-ілметил)-(2,4,5трифторфеніл)карбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Порцію отриманого продукту масою 158мг очищають препаративною РХВР/МС, одержуючи при цьому 16мг чистої сполуки у вигляді форміату. Mac-спектроскопія [М+1]+: 475,477. Умови проведення очищення з використанням методу РХВР/МС: колонка: симетричний С18,100 А, 5мкм, 19´100мм, «Waters»; рухома фаза: А (Н2О 0,1% HCOONH 4, рН=3) і В (AcN 0,1% HCOONH4, рН=3), В: 10%→35%. Приклад 22 (3R)-1-Азабіцикло[2.2.2]окт-3-иловий складний ефір (4-фтор-2-метилфеніл)-(3-метилтіофен-2ілметил)карбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 0,8г, 10,8%. Mac-спектроскопія [М+1]+: 389; 38 1 H-ЯМР (CDCI3): δ 1,10-1,25 (m, 2Н), 1,45-1,70 (m, 2Н), 1,70-1,85 (m, 1Н), 1,87 (s, 3H), 2,0-2,05 (два синглети, 3Н), 2,40-3,0 (m, 5Н), 3,10-3,40 (m, 1Н), 4,65-5,0 (m, 3H), 6,72 (m, 1H), 6,80-6,95 (m, 3H), 7,12 (m, 1H). Приклад 23 (3R)-3-[(4-Фтор-2-метилфеніл)-(3-метилтіофен2-ілметил)карбамоїлокси]-1-(2-феноксіетил)-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способів (а) і (в). Вихід на заключній стадії становить 0,5г, 84,7%. Mac-спектроскопія [М-Вr]+: 509; 1 Н-ЯМР (ДМСО-d6): δ 1,15-1,45 (m, 1H), 1,602,20 (m, 10Н), 2,90-3,10 (m, 1H), 3,30-3,85 (m, 6H), 3,90-4,20 (m, 1H), 4,30-4,55 (m, 2H), 4,75-5,15 (m, 3H), 6,78 (m, 1H), 6,90-7,20 (m, 6H), 7,35 (m, 3H). Приклад 24 (3R)-1-Азабіцикло[2.2.2]окт-3-иловий складний ефір (3-фтор-4-метоксифеніл)тіофен-3ілметилкарбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 1,9г, 25,7%. Мас-спектроскопія [М+1]+: 391; 1 H-ЯМР (CDCI3): δ 1,20-1,90 (m, 4Н), 2,01 (m, 1H), 2,55-2,90 (m, 5H), 3,22 (m, 1H), 3,88 (s, 3Н), 4,70-4,90 (m, 3Н), 6,70-6,95 (m, 3Н), 6,95-7,15 (m, 2Н), 7,26 (m, 1Н). Приклад 25 (3R)-3-[(3-Фтор-4-метоксифеніл)тіофен-3ілметилкарбамоїлокси]-1-(3-фенілаліл)-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способів (а) і (в). Вихід на заключній стадії становить 1,9г, 97,1% . Мас-спектроскопія [М-Вr]+: 507; 1 Н-ЯМР (ДМСО-d6): δ 1,40-1,65 (m, 1H), 1,652,05 (m, 3Н), 2,10-2,30 (m, 1H), 3,10-3,30 (m, 1H), 3,30-3,60 (m, 4H), 3,78 (s, 3H), 3,80-3,95 (m, 1H), 3,95-4,10 (m, 2H), 4,80 (m, 2H), 5,0 (m, 1H), 6,42 (m, 1H), 6,85 (m, 1H), 6,90-7,15 (m, 3H), 7,20-7,50 (m, 7H), 7,58 (m, 1H). Приклад 26 (3R)-1-Азабіцикло[2.2.2]окт-3-иловий складний ефір (4,5-диметилфуран-2-ілметил)-(5метилфуран-2-ілметил)карбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а); 200мг отриманого продукту очищають колонковою хроматографією (силікагель, як елюент суміш СНСІ3/EtOH у співвідношенні 5:1), одержуючи при цьому 34мг чистої сполуки. Мас-спектроскопія [М+1]+: 373; 1 Н-ЯМР (CDCI3): δ 1,20-1,40 (m, 1Н), 1,40-1,55 (m, 1H), 1,55-1,70 (m, 1H), 1,70-1,80 (m, 1H), 1,852,05 (m, 1H), 1,90 (s, 3H), 2,16 (s, 3H), 2,25 (s, 3H), 2,70-3,05 (m, 5H), 3,25-3,32 (m, 1H), 4,20-4,50 (m, 4H), 4,85 (m, 1H), 5,85-6,15 (m, 3H). Приклад 27 (3R)-1-Аліл-3-[2-(4-фторфеніл)етил]-(3метилтіофен-2-ілметил)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способів (а) і (в). Вихід на заключній стадії становить 0,4г, 51,3%. 39 85541 Мас-спектроскопія [М-Вr]+: 443; 1 Н-ЯМР (ДМСО-d 6): δ 1,80-2,10 (m, 4Н), 2,20 (s, 3Н), 2,25-2,30 (m, 1Н), 2,77 (m, 2H), 3,15-3,70 (m, 7H), 3,82 (m, 1H), 3,90 (m, 2H), 4,45-4,65 (m, 2H), 4,85-5,05 (m, 1H), 5,56-5,66 (m, 2H), 5,90-6,10 (m, 1H), 6,87 (m, 1H), 7,10-7,30 (m, 4H), 7,36 (m, 1H). Приклад 28 1-Азабіцикло[2.2.2]окт-3-(R)иловий складний ефір бензилфенілкарбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 1000мг, 18%. 1 Н-ЯМР (CDCI3): δ 1,3-1,7 (m, 4Н), 1,9 (s, 1H), 2,5-2,8 (m, 5H), 3,2 (m, 1H), 4,8 (m, 1H), 4,9 (s, 2H), 7,1-7,4 (m, 10H); мас-спектроскопія [М+1]+: 337. Приклад 29 3-(R)(Бензилфенілкарбамоїлокси)-1-метил-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 20мг, 34%. 1 Н-ЯМР (ДМСО-d 6): δ 1,54-1,90 (m, 4H), 2,17 (s, 1Н), 2,95 (s, 3Н), 3,22-3,52 (m, 5H), 3,84 (m, 1H), 4,92 ( s, 2H), 4,99 (m, 1H), 7,12-7,37 (m, 10Н); мас-спектроскопія [M-CF3COO]+: 351. Приклад 30 3-(R)(Бензилфенілкарбамоїлокси)-1-(4метилпент-3-еніл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 18мг, 25%. Мас-спектроскопія [M-CF3COO]+: 419. Приклад 31 3-(R)(Бензилфенілкарбамоїлокси)-1-(3феноксипропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 21мг, 26%. 1 H-ЯМР (ДМСО-d6): δ 1,56-1,91 (m, 4H), 2,112,20 (m, 3Н), 3,12 (m, 1H), 3,34-3,51 (m, 6H), 3,86 (m, 1H), 4,06 (m, 2H), 4,93 ( s, 2H), 5,02 (m, 1H), 6,97 (m, 3H), 7,20-7,38 (m, 12H); мас-спектроскопія [M-CF3COO]+: 471. Приклад 32 3-(R)(Бензилфенілкарбамоїлокси)-1-(3фенілаліл)-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 220мг, 70%. 1 Н-ЯМР (ДМСО-d 6): δ 1,55-1,92 (m, 4Н), 2,21 (s, 1H), 3,15 (m, 1H), 3,34-3,50 (m, 5H), 3,90 (m, 1H), 4,1 (m, 2 H), 4,02 (s, 2 H), 5,05 (m, 1H), 6,49 (m, 1H), 6,85-6,90 (d, 1H), 7,20-7,59 (m, 12H), 7,59-7,61 (m, 2H); мас-спектроскопія [M-Br]+: 453; т. пл.: 129°С. Приклад 33 1-Аліл-3-(R)(бензилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 230мг, 85%. 40 1 Н-ЯМР (ДМСО-d 6): δ 1,58-1,91 (m, 4Н), 2,20 (s, 1H), 3,10 (m, 1H), 3,27-3,41 (m, 4H), 3,79-3,90 (m, 3H), 4,92 (s, 2H), 5,03 (m, 1H), 5,61 (m, 2H), 5,98 (m, 1H), 7,20-7,38 (m, 10H); мас-спектроскопія [M-Br]+: 377; т. пл.: 70°С. Приклад 34 3-(R)(Бензилфенілкарбамоїлокси)-1-(2гідроксіетил)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 19%. Мас-спектроскопія [M-CF3COO]+: 381. Приклад 35 3-(R)(Бензилфенілкарбамоїлокси)-1-ізопропіл1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 17мг, 26%. 1 H-ЯМР (ДМСO-d6): δ 1,24 (m, 6Н), 1,64-1,89 (m, 4Н), 2,20 (s, 1H), 2,78 (m, 1Н), 3,23-3,32 (m, 4Η), 3,50 (m, 1H), 3,76 (m, 1H), 4,92 (s, 2H), 5,06 (m, 1H), 7,20-7,38 (m,10H); мас-спектроскопія [M-CF3COO]+: 379. Приклад 36 3-(R)(Бензилфенілкарбамоїлокси)-1-пропіл-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 16мг, 25%. 1 H-ЯМР (ДМСО-d6): δ 0,88 (m, 3Н), 1,57-1,68 (m, 4Н), 1,89 (m, 2Н), 2,18 (s, 1Н), 2,99-3,14 (m, 3Н), 3,26-3,40 (m, 4H), 3,83 (m, 1H), 4,92 (s, 2H), 5,01 (m, 1H), 7,20-7,37 (m, 10Н); мас-спектроскопія [MCF3COO]+: 379. Приклад 37 3-(R)(Бензилфенілкарбамоїлокси)-1-(3ціанопропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 19% 1 Н-ЯМР (ДМСО-d 6): δ 1,67-2,07 (m, 6Н), 2,19 (s, 1Н), 2,60 (m, 2H), 3,07 (m, 1H), 3,21-3,48 (m, 6H), 3,85 (m, 1H), 4,92 (s, 2H), 5,01 (m, 1H), 7,20-7,37 (m, 10); мас-спектроскопія [M-CF3COO]+: 404. Приклад 38 3-(R)(Бензилфенілкарбамоїлокси)-1циклопропілметил-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 9мг, 14%. Мас-спектроскопія [МСF3СОО]+: 391. Приклад 39 3-(R)(Бензилфенілкарбамоїлокси)-1-(2етоксіетил)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 22мг, 32%. 1 H-ЯМР (ДМСО-d6): δ 1,12 (m, 3Н), 1,58-1,90 (m, 4Н), 2,19 (s, 1H), 3,12-3,15 (m, 1Н), 3,28-3,53 (m, 8H), 3,75 (m, 2H), 3,90 (m, 1H), 4,91 (s, 2H), 5,02 41 85541 (m, 1H), 7,20-7,37 (m, 10Н); мас-спектроскопія [MCF3COO]+: 409. Приклад 40 3-(R)(Бензилфенілкарбамоїлокси)-1-(4етоксикарбонілбутил)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 14мг, 18%. 1 H-ЯМР (ДМСО-d6): δ 1,19 (m, 3Н), 1,50-1,67 (m, 4H), 1,85-1,88 (m, 2H), 2,18 (s, 1H), 2,38 (m, 2Н), 3,99 (m, 1Н), 3,16-3,42 (m, 8H), 3,82 (m, 1H), 4,06 (m, 2H), 4,92 (s, 2H), 5,02 (m, 1H), 7,19-7,37 (m, 10Н); мас-спектроскопія [M-CF3COO]+: 465. Приклад 41 3-(R)(Бензилфенілкарбамоїлокси)-1-(4фенілбутил)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 14мг, 18%. 1 H-ЯМР (ДМСО-d6): δ 1,57-1,65 (m, 6Н), 1,88 (m, 2Н), 2,18 (s, 1H), 2,63 (m, 2H), 3,00 (m, 1H), 3,18-3,42 (m, 6H), 3,79-3,86 (m, 1H), 4,94 (s, 2H), 5,00 (m, 1H), 7,18-7,37 (m, 15H); мас-спектроскопія [M-CF3COO]+: 469. Приклад 42 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(4фтор фенокси)пропіл]-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 21мг, 25%. 1 H-ЯМР (ДМСО-d6): δ 1,55-1,91 (m, 4Н), 2,102,20 (m,3H), 3,10 (m, 1H), 3,28-3,50 (m, 6H), 3,88 (m, 1H), 4,02 (m, 2H), 4,93 (s, 2H), 5,02 (m, 1H), 6,95-7,12 (m, 2H), 7,12-7,38 (m,12H); мас-спектроскопія [M-CF3COO]+: 489. Приклад 43 3-(R)(Бензилфенілкарбамоїлокси)-1-(3гідроксипропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 18%. 1 H-ЯМР (ДМСО-d 6): δ 1,54-1,88 (m, 6Н), 2,18 (s, 1Н), 3,09 (m, 1H), 3,23-3,49 (m, 8H), 3,85 (m, 1H), 4,84 (m,0H), 4,92 (s, 2H), 5,02 (m, 1H), 7,19-7,37 (m, 10Н); мас-спектроскопія [M-CF3COO]+: 395. Приклад 44 1-(4-Ацетоксибутал)-3(R)(бензилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 9мг, 12%. 1 H-ЯМР (ДМСО-d6): δ 1,40-1,70 (m, 5Н), 1,811,91 (m, 3Н), 2,02 (m, 3Н), 2,19 (s, 1H), 3,03 (m, 1H), 3,19 (m, 2H), 3,26-3,46 (m, 4H), 3,80-3,84 (m, 1H), 4,04 (m, 2H), 4,92 (s, 2H), 5,01-5,02 (m, 1H), 7,197,37 (m, 10Н); мас-спектроскопія [M-CF3COO]+: 451. Приклад 45 42 3-(R)(Бензилфенілкарбамоїлокси)-1-(4-оксо-4тіофен-2-ілбутил)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 16мг, 19%. 1 H-ЯМР (ДМСО-d6): δ 1,55-1,69 (m, 2H), 1,872,05 (m, 4Н), 2,19 (s, 1H), 3,09 (m, 3Н), 3,22 (m, 2Н), 3,29-3,46 (m, 4Н), 3,88 (m, 1Н), 4,93 (s, 2H), 5,02 (m, 1H), 7,19-7,38 (m, 11H), 7,98-8,06 (m, 2H); масспектроскопія [М-CF3COO]+: 489. Приклад 46 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(3гідроксифенокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 17мг, 21%. 1 Н-ЯМР (ДМСО-d6): δ 1,57-1,68 (m, 2H), 1,90 (m, 2Н), 2,08-2,19 (m, 3Н), 3,11 (m, 1Н), 3,28-3,50 (m, 6H), 3,88 (m, 1H), 3,97 (m, 2H), 4,93 (s, 2H), 5,02 (m, 1H), 6,33-6,40 (m, 3H), 7,04 (m, 1H), 7,20-7,38 (m, 10H), 9,5 (s, OH); мас-спектроскопія [M-CF3COO]+: 487. Приклад 47 3-(R)(Бензилфенілкарбамоїлокси)-1-гептил-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 17мг, 23%. 1 H-ЯМР (ДМСО-d6): δ 0,88 (m, 3Н), 1,28 (m, 8H), 1,62 (m, 4H), 1,85-1,88 (m, 2Н), 2,18 (s, 1Н), 3,02 (m, 1H), 3,15 (m, 2H), 3,26-3,40 (m, 4H), 3,83 (m, 1H), 4,92 (s, 2H), 5,01 (m, 1H), 7,20-7,37 (m, 10Н); мас-спектроскопія [M-CF3COO]+: 435. Приклад 48 1-(2-Бензилоксіетил)-3(R)(бензилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 20мг, 25%. 1 Н-ЯМР (ДМСО-d 6): δ 1,54-1,94 (m, 4Н), 2,20 (s, 1H), 3,17 (m, 1H), 3,28-3,55 (m, 6H), 3,85 (m, 2H), 9,92-3,99 (m, 1H), 4,53 (s, 2H), 4,91 (s, 2H), 5,02 (m, 1H), 7,18-7,40 (m, 15H); мас-спектроскопія [M-CF3COO]+: 471. Приклад 49 1-Азабщикло[2.2.2]окт-3-(R)иловий складний ефір бензил-(4-фторфеніл)карбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 1110мг, 13%. 1 H-ЯМР (ДМСО-d 6): δ 1,16-1,52 (m, 4Н), 1,81 (s, 1Н), 2,42-2,57 (m, 5H), 2,99-3,07 (m, 1H), 4,63 (m, 1H), 4,84 (s, 2H), 7,10-7,32 (m, 9H); мас-спектроскопія [М+1]: 355. Приклад 50 1-Аліл-3-(R)[бензил-(4фтор феніл)карбамоїлокси]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії 43 85541 становить 10мг, 23%. Mас-спектроскопія [МСF3СОО]+: 395. Приклад 51 3-(R)[Бензил-(4-фторфеніл)карбамоїлокси]-1(3-фенілпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 25%. Мас-спектроскопія [МСFзСОО]+: 473. Приклад 52 1-Азабіцикло[2.2.2]окт-3-(R)иловий складний ефір бензил-n-толілкарбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 1070мг, 11%. 1 H-ЯМР (ДМСО-d6): δ 1,18-1,30 (m, 2Н), 1,451,55 (m, 2Н), 1,83 (s, 1H), 2,25 (s, 3H), 2,43-2,59 (m, 5H), 3,01-3,10 (m, 1H), 4,64 (m, 1H), 4,85 (s, 2H), 7,12-7,34 (m, 9H); мас-спектроскопія [М+1]+: 351. Приклад 53 1-Аліл-3-(R)(бензил-n-толіл-карбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 9мг, 19%. мас-спектроскопія [MCF3COO]+: 391. Приклад 54 3-(R)(Бензил-n-толілкарбамоїлокси)-1-(3фенілпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 25%. Мас-спектроскопія [МСF3СОО]+: 469. Приклад 55 3-(R)(Бензилфенілкарбамоїлокси)-1-[2-(2метоксіетокси)етил]-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 390мг, 84%. 1 H-ЯМР (ДМСО-d6): δ 1,55-1,75 (m, 2 Η), 1,88 (m, 2Η), 2,17 (s, 1H), 3,14 (m, 1H), 3,22 (s, 3H), 3,293,55 (m, 10H), 3,78 (m, 2H), 3,90 (m, 1H), 4,89 (s, 2H), 4,99 (m, 1H), 7,17-7,35 (m, 10Н); мас-спектроскопія [M-Br]+: 439. Приклад 56 3-(R)(Бензилфенілкарбамоїлокси)-1-фенетил1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 200мг, 65%. 1 Н-ЯМР (ДМСО-d6): δ 1,55-1,75 (m, 2Н), 1,90 (m, 2Н), 2,19 (s, 1Н), 3,00 (m, 2H), 3,10 (m, 1H), 3,31-3,51 (m, 6H), 3,90 (m, 1H), 4,91 (s, 2H), 5,04 (m, 1H), 7,18-7,37 (m, 15H); мас-спектроскопія [M-Br]+: 441; т. пл. 81°С. Приклад 57 3-(R)(Бензилфенілкарбамоїлокси)-1-(3-тіофен2-ілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 970мг, 82%. 44 1 H-ЯМР (ДМСО-d6): δ 1,55-1,69 (m, 2Н), 1,852,04 (m, 4Н), 2,18 (s, 1Н), 2,83 (m, 2H), 3,01 (m, 1H), 3,20-3,44 (m, 6H), 3,85 (m, 1H), 4,92 (s, 2H), 5,00 (m, 1H), 6,94-7,00 (m, 2 H), 7,19-7,40 (m, 11H); мас-спектроскопія [M-Br]+: 461; т. пл. 95°C. Приклад 58 3-(R)(Бензилфенілкарбамоїлокси)-1-(3фенілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 880мг, 79%. 1 H-ЯМР (ДМСО-d6): δ 1,55-1,69 (m, 2Н), 1,852,00 (m, 4Н), 2,18 (s, 1H), 2,59 (m, 2H), 3,04 (m, 1H), 3,23-3,44 (m, 6H), 3,85 (m, 1H), 4,92 (s, 2H), 5,02 (m, 1H), 7,18-7,36 (m, 15H).); мас-спектроскопія [M-Br]+: 455; т. пл. 101°С. Приклад 59 3-(R)(Бензилфенілкарбамоїлокси)-1-(2феноксіетил)-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 360мг, 67%. 1 Н-ЯМР (ДМСО-d6): δ 1,5-1,73 (m, 2Н), 1,89 (m, 2Н), 2,20 (s, 1Н), 3,23 (m, 1H), 3,46-3,72 (m, 6H), 4,02 (m, 1H), 4,43 (m, 2H), 4,92 (s, 2H), 5,03 (m, 1H), 7,01 (m, 3H), 7,17-7,38 (m, 12H); мас-спектроскопія [M-Br]+: 457; т. пл. 117°С. Приклад 60 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(3ціанофенокси)пропіл]-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 16мг, 36%; мас-спектроскопія [М-СF3СОО]+: 496. Приклад 61 3-(R)(Бензилфенілкарбамоїлокси)-1-[3(нафталін-1-илокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 10мг, 21%; мас-спектроскопія [M-CF3COO]+: 521. Приклад 62 3-(R)(Бензилфенілкарбамоїлокси)-1-[3(метилфеніламіно)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 28%; мас-спектроскопія [M-CF3COO]+: 484. Приклад 63 3-(R)(Бензилфенілкарбамоїлокси)-1-(3фенілсульфанілпропіл)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 8мг, 18%; 1 Н-ЯМР (ДMCO-d6): δ 1,45-2,00 (m, 6Н), 2,17 (bs, 1H), 3,00 (m, 2H), 3,28-3,41 (m, 7H), 3,83 (m, 1H), 4,91 (s, 2H), 4,98 (m, 1H), 7,18-7,41 (m, 15H); мас-спектроскопія [M-CF3COO]+: 487. 45 85541 Приклад 64 3-(R)(Бензилфенілкарбамоїлокси)-1-(4-оксо-4фенілбутил)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 10мг, 23%; 1 H-ЯМР (ДМСО-d6): δ 1,50-2,06 (m, 6H), 2,20 (bs, 1Н), 3,13-3,47 (m, 9H), 3,89 (m, 1H), 4,93 (s, 2H), 5,02 (m, 1H), 7,19-7,38 (m, 10H), 7,54-7,70 (m, 3H), 7,98-8,00 (m, 2H); мас-спектроскопія [M-CF3COO]+: 483. Приклад 65 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(2,4,6триметилфенокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 14мг, 30%; 1 Н-ЯМР (ДМСО-d 6): δ 1,50-2,20 (m, 7H), 2,19 (s, 9Н), 3,16-3,52 (m, 7Н), 3,73 (m, 2Н), 3,92 (m, 1H), 4,93 (s, 2Н), 5,03 (m, 1Н), 6,83 (s, 2H), 7,19-7,38 (m, 10Н); мас-спектроскопія [M-CF3COO]+: 513. Приклад 66 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(2хлорфенокси)пропіл]-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 14мг, 31%; мас-спектроскопія [M-CF3COO]+: 506. Приклад 67 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(3трифторметилфенокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 14мг, 29%; 1 H-ЯМР (ДМСО-d6): δ 1,50-2,00 (m, 4H), 2,082,20 (m, 3Н), 3,12-3,50 (m, 7Н), 3,90 (m, 1H), 4,14 (m, 2Н), 4,93 (s, 2Н), 5,03 (m, 1H), 7,19-7,38 (m, 13Н), 7,54-7,59 (m, 1H); мac-спектроскопія, [M-CF3COO]+: 539. Приклад 68 3-(R)(Бензилфенілкарбамоїлокси)-1-[3(біфеніл-4-ілокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 24%; 1 Н-ЯМР (ДМСО-d6): δ 1,50-2,20 (m, 7H), 3,14 (bs, 1H), 3,28-3,52 (m, 6 Η), 3,91 (m, 1H), 4,10 (m, 2H), 4,93 (s, 2H), 5,03 (m, 1H), 7,03-7,08 (m, 2H), 7,18-7,47 (m,13H), 7,61-7,65 (m, 4H); мас-спектроскопія [M-CF3COO]+: 547. Приклад 69 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(2,4дифторфенокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 10мг, 22%; 46 1 H-ЯМР (ДМСО-d6): δ 1,50-2,19 (m, 7H), 3,10 (bs, 1Н), 3,28-3,51 (m,6H), 3,90 (m, 1H), 4,10 (m, 2H), 4,93 (s, 2H), 5,02 (m, 1H), 7,02-7,09 (m, 1H), 7,19-7,37 (m, 12H); мас-спектроскопія [M-CF3COO]+: 507. Приклад 70 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(4метоксифенокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 10мг, 22%; 1 Н-ЯМР (ДМСО-d6): 1,50-2,19 (m, 7H), 3,11 (bs, 1H), 3,28-3,51 (m, 6H), 3,70 (s,3H), 3,89 (m, 1H), 3,94-3,99 (m, 2H), 4,93 (s, 2H), 5,02 (m, 1H), 6,856,92 (m, 4H), 7,19-7,38 (m, 10Н); мас-спектроскопія [M-CF3COO]+: 501. Приклад 71 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(5,6,7,8тетрагідронафталін-2-илокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 10мг, 21%; 1 Н-ЯМР (ДМСО-d6): δ 1,50-1,71 (m, 6H), 1,872,19 (m, 5Н), 2,63-2,68 (m, 4Н), 3,10 (bs, 1Н), 3,283,50 (m, 6H), 3,88 (m, 1H), 3,98 (m, 2H), 4,93 (s, 2H), 5,02 (m, 1H), 6,63-6,70 (m, 2H), 6,95-6,98 (d, 1H), 7,19-7,38 (m, 10H); мас-спектроскопія [М-СF3СОО]+: 525. Приклад 72 1-[3-(Бензо[1.3]діоксол-5-ілокси)пропіл]-3(R)(бензилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 26%; мас-спектроскопія [М-СF3СОО]+: 515. Приклад 73 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(2карбамоїлфенокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 10мг, 22%; 1 H-ЯМР (ДМСО-d6): δ 1,50-2,27 (m, 7H), 3,09 (bs, 1Н), 3,28-3,48 (m, 6H), 3,88 (m, 1H), 4,14 (m, 2H), 4,93 (s, 2H), 5,04 (m, 1H),7,02-7,15 (m, 2H), 7,19-7,38 (m, 10H), 7,44-7,50 (m, 1H), 7,55(bs, NH2), 7,69-7,72 (dd, 1H); мас-спектроскопія [М-СF3СОО]+: 514. Приклад 74 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(3диметиламінофенокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 26%; мас-спектроскопія [М-СF3СОО]+: 514. Приклад 75 1-[3-(4-Ацетиламінофенокси)пропіл]-3(R)(бензилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат 47 85541 Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 25%; 1 Н-ЯМР (ДМСO-d 6): δ 1,50-1,92 (m, 4H), 2,01 (s, 3Н), 2,04-2,20 (m, 3Н), 3,12 (bs, 1H), 3,28-3,51 (m, 6H), 3,89 (m, 1H), 4,00 (m, 2H), 4,93 (s, 2H), 5,02 (m, 1H), 6,86-6,91 (m, 2H), 7,19-7,38 (m, 10H), 7,48-7,53 (m. 2H), 9,85 (s, NH); мас-спектроскопія [M-CF3COO]+: 528. Приклад 76 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(4метоксикарбонілфенокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 25%; 1 H-ЯМР (ДМСО-d6): δ 1,50-2,20 (m, 7H), 3,12 (bs, 1Н), 3,29-3,51 (m, 6H), 3,82 (s, 3Н), 3,87-3,93 (m, 1H), 4,14 (m, 2H), 4,93 (s, 2H), 5,03 (m, 1H), 7,04-7,09 (m, 2H), 7,19-7,38 (m, 10H), 7,92-7,96 (m, 2H); мас-спектроскопія [M-CF3COO]+: 529. Приклад 77 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(4нітрофенокси)пропіл]-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 26%; 1 Н-ЯМР (ДМСО-d6): δ 1,50-2,27 (m, 7H), 3,12 (bs, 1H), 3,29-3,51 (m, 6Н), 3,87-3,94 (m, 1Н), 4,21 (m, 2H), 4,93 (s, 2H), 5,03 (m, 1H), 7,14-7,38 (m, 12H), 8,22-8,28 (m, 2H); мас-спектроскопія [M-CF3COO]+: 516. Приклад 78 3-(R)(Бензилфенілкарбамоїлокси)-1-[3-(4гідроксиметилфенокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 10мг, 22%; мас-спектроскопія [M-CF3COO]+: 501. Приклад 79 1-Азабіцикло[2.2.2]окт-3-(S)иловий складний ефір бензилфенілкарбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 1000мг, 23%; 1 H-ЯМР (ДМСО-d6): δ 1,14-1,57 (m, 4H), 1,83 (bs, 1Н), 2,43-2,61 (m, 5H), 2,61-3,01 (m, 1H), 4,64 (m, 1H), 4,89 (s, 2H), 7,16-7,35 (m, 10Н); мас-спектроскопія [М+1]+: 337. Приклад 80 3-(S)(Бензилфенілкарбамоїлокси)-1-(3фенілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 660мг, 83%; 1 Н-ЯМР (ДМСО-d6): δ 1,40-2,00 (m, 6H), 2,18 (bs, 1Н), 2,59 (m, 2H), 2,95-3,44 (m, 7H), 3,84 (m, 1H), 4,92 (s, 2H), 5,00 (m, 1H), 7,19-7,36 (m, 15H); мас-спектроскопія [M-Br]+: 455; т. пл.: 64°С. Приклад 81 3-(R)(Бутилфенілкарбамоїлокси)-1-метил-1азоніабіцикло[2.2.2]октан, трифторацетат 48 Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 16мг, 30%; мас-спектроскопія [М-СF3СОО]+: 317. Приклад 82 3-(R(Бутилфенілкарбамоїлокси)-1-(4метилпент-3-еніл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 18мг, 27%; мас-спектроскопія, [M-CF3COO]+: 385. Приклад 83 3-(R)(Бутилфенілкарбамоїлокси)-1-(3феноксипропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 21мг, 28%; мас-спектроскопія, [М-СF3СОО]+: 437. Приклад 84 3-(R)(Бутилфенілкарбамоїлокси)-1-(3фенілаліл)-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 182мг, 48%; 1 H-ЯМР (ДМСО-d6): δ 0,84 (m, 3Н), 1,25 (m, 2Н), 1,40 (m, 2Н), 1,70-1,91 (m, 4Н), 2,20 (s, 1Н), 3,2-3,4 (m, 6 Η), 3,64 (m, 2H), 3,88 (m, 1H), 3,884,07 (d, 2H), 4,97 (m, 1H), 6,45 (m, 1H), 6,83-6,88 (d, 1H), 7,23-7,45 (m, 7H), 7,60 (m, 2H); мас-спектроскопія, [M-Br]+: 419; т. пл.: 144°С. Приклад 85 1-Аліл-3-(R)(бутилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 200мг, 72%; 1 H-ЯМР (ДМСО-d6): δ 0,85 (m, 3Н), 1,21-1,34 (m, 3Н), 1,40-1,45 (m, 2H), 1,70-2,18 (m, 4H), 3,153,40 (m,5H), 3,61-3,67 (m, 2H), 3,82 (m, 1H), 3,923,94 (m, 2H), 4,95 (m, 1H), 5,62 (m, 2H), 5,97-6,01 (m, 1H), 7,26-7,44 (m, 5H); мас-спектроскопія, [M-Br]+: 343; т. пл.: 141°С. Приклад 86 3-(R)(Бутилфенілкарбамоїлокси)-1-(2гідроксіетил)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 19%; мас-спектроскопія, [M-CF3COO]+: 347. Приклад 87 3-(R)(Бутилфенілкарбамоїлокси)-1-ізопропіл-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 20мг, 29%; мас-спектроскопія, [M-CF3COO]+: 345. Приклад 88 3-(R)(Бутилфенілкарбамоїлокси)-1-пропіл-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 16мг, 23%; 49 85541 мас-спектроскопія, [M-CF3COO]+: 345. Приклад 89 3-(R)(Бутилфенілкарбамоїлокси)-1-(3ціанопропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 15мг, 20%; мас-спектроскопія, [М-СF3СОО]+: 370. Приклад 90 3-(R)(Бутилфенілкарбамоїлокси)-1циклопропілметил-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 2мг, 3%; мас-спектроскопія, [M-CF3COO]+: 357. Приклад 91 3-(R)(Бутилфенілкарбамоїлокси)-1-(2етоксіетил)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 19мг, 25%; мас-спектроскопія, [M-CF3COO]+: 375. Приклад 92 3-(R)(Бутилфенілкарбамоїлокси)-1-(4етоксикарбонілбутил)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 14%; мас-спектроскопія, [M-CF3COO]+: 431. Приклад 93 3-(R)(Бутилфенілкарбамоїлокси)-1-(3гідроксипропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 17%; мас-спектроскопія, [M-CF3COO]+: 361. Приклад 94 3-(R)(Бутилфенілкарбамоїлокси)-1-(3-пірол-1илпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадіїстановить 19мг, 23%; мас-спектроскопія, [M-CF3COO]+: 410. Приклад 95 1-(4-ацетоксибутил)-3(R)(бутилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 10мг, 12 ас-спектроскопія, [M-CF3COO]+: 417. Приклад 96 3-(R)(Бутилфенілкарбамоїлокси)-1-(4-оксо-4тіофен-2-ілбутил)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 17мг, 19%; мас-спектроскопія, [M-CF3COO]+: 455. 50 Приклад 97 3-(R)(Бутилфенілкарбамоїлокси)-1-(4фенілбутил)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 17мг, 20%; мас-спектроскопія, [M-CF3COO]+: 435. Приклад 98 3-(R)(Бутилфенілкарбамоїлокси)-1-[3-(3гідроксифенокси)пропіл]-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 21мг, 23%; мас-спектроскопія, [M-CF3COO]+: 453. Приклад 99 3-(R)(Бутилфенілкарбамоїлокси)-1-гептил-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 17мг, 21%; мас-спектроскопія, [M-CF3COO]+: 401. Приклад 100 1-(2-Бензилоксіетил)-3(R)(бутилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 22мг, 25%; мас-спектроскопія, [М-СF3СОО]+: 437. Приклад 101 3-(R)(Бутилфенілкарбамоїлокси)-1-фенетил-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 330мг, 82%; 1 Н-ЯМР (ДМСО-d6): δ 0,83 (m, 3Н), 1,27-1,34 (m, 2Н), 1,41-1,48 (m, 3Н), 1,60-2,23 (m, 4H), 2,963,47 (m, 7H), 3,57-3,71 (m, 4H), 3,92 (m, 1H), 4,98 (m, 1H), 7,25-7,45 (m, 10Н); мас-спектроскопія, [М-Вr]+: 407; т. пл.: 139°С Приклад 102 3-(R)(Бутилфенілкарбамоїлокси)-1-[2-(2метоксіетокси)етил]-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 520мг, 81%; 1 Н-ЯМР (ДМСО-d6): δ 0,82 (m, 3Н), 1,24-1,31 (m, 2Н), 1,39-1,47 (m, 2Н), 1,70-2,20 (m, 5 Η), 3,26 (s, 3Н), 3,35-3,70 (m, 13H), 3,82-3,86 (m, 3Н), 4,94 (m, 1H), 7,26-7,44 (m, 5 Η); мас-спектроскопія, [МВr]+: 405. Приклад 103 1-Азабіцикло[2.2.2]окт-3-(R)-иловий складний ефір бутил-(4-фтор феніл)-карбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 1650мг, 24%; 1 Н-ЯМР (ДМСО-d6): δ 0,82 (m, 3Н), 1,20-1,54 (m, 8Н), 1,83 (m, 1H), 2,49-2,70) (m, 5Н), 3,02-3,09 (m, 1H), 3,36-3,63 (m, 2H), 4,59 (m, 1H), 7,19-7,35 (m, 4H); мас-спектроскопія, [М+1]+: 321. 51 85541 Приклад 104 3-(R)(Бутилфенілкарбамоїлокси)-1-[3-(4фтор фенокси)пропіл]-1-азоніабіцикло[2.2.2]октан; хлорид Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 390мг, 75%; 1 H-ЯМР (ДМСО-d6): δ 0,82 (m, 3Н), 1,26-1,31 (m, 2Н), 1,40-1,48 (m, 2Н), 1,70-2,17 (m,5H), 3,203,7 (m, 11Н), 3,86 (m, 1H), 4,02 (m, 2H), 4,94 (m, 1H), 6,95-7,00 (m, 2H), 7,12-7,18 (m, 2H), 7,26-7,44 (m, 5H); мас-спектроскопія, [M-Cl]+: 455; т. пл.: 126°C. Приклад 105 3-(R)(Бутилфенілкарбамоїлокси)-1-(2феноксіетил)-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 260мг, 53%; 1 Н-ЯМР (ДМСО-d6): δ 0,84 (m, 3Н), 1,23-1,30 (m, 2Н), 1,39-1,48 (m, 2Н), 1,70-2,20 (m, 5Н), 3,203,72 (m, 9Н), 3,99 (m, 1Н), 4,44 (m, 2H), 4,95 (m, 1H), 7,01 (m, 3Н), 7,24-7,40 (m, 7H); мас-спектроскопія, [M-Br]+: 423; т. пл.: 153°С. Приклад 106 3-(R)(Бутилфенілкарбамоїлокси)-1-(3-тіофен2-ілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 1100мг, 62%; 1 Н-ЯМР (ДМСО-d6): δ 0,84 (m, 3Н), 1,24-1,31 (m, 2H), 1,42 (m, 2H), 1,60-2,21 (m, 7H), 2,85 (m, 2H), 3,0-3,50 (m, 7H), 3,60-3,69 (m, 2Н), 3,85 (m, 1H), 4,93 (m, 1H), 6,95-7,00 (m, 2H), 7,28-7,43 (m, 6H); мас-спектроскопія, [M-Br]+: 427; т. пл.: 127°С. Приклад 107 3-(R)(Бутилфенілкарбамоїлокси)-1-(3фенілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 280мг, 56%; 1 Н-ЯМР (ДМСО-d6): δ 0,84 (m, 3Н), 1,23-1,33 (m, 2Н), 1,43 (m, 2Н), 1,60-2,20 (m, 7Н), 2,59 (m, 2Н), 3,00-3,78 (m, 9Н), 3,84 (m, 1Н), 4,92 (m, 1H), 7,20-7,42 (m, 10Н); мас-спектроскопія, [M-Br]+: 421; т. пл.: 120°С. Приклад 108 1-Азабіцикло[2.2.2]окт-3-(R)-иловий складний ефір фенілтіофен-2-ілметилкарбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 310мг, 10%; 1 Н-ЯМР (ДМСО-d6): δ 1,10-1,60 (m, 4 Η), 1,87 (s, 1H), 2,46-2,63 (m, 5H), 3,04-3,33 (m, 1H), 4,66 (m, 1H), 5,01 (s, 2H), 6,87-6,94 (m, 2H), 7,20-7,43 (m, 6H); мас-спектроскопія, [М+1]+: 343. Приклад 109 1-Метил-3-(R)(фенілтіофен-2ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 160мг, 80%; 52 1 Н-ЯМР (ДМСО-d 6): 1,65-2,00 (m, 4H), 2,20 (s, 1 Η), 2,98 (s, 3Н), 3,32-3,52 (m, 5Н), 3,85-3,92 (m, 1Н), 4,98-5,04 (m, 3Н), 6,94 (m, 2H), 7,24-7,45 (m, 6H).; мас-спектроскопія, [M-Br]+: 357. Приклад 110 1-(3-Феноксипропіл)-3-(R)(фенілтіофен-2ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 16мг, 42%; мас-спектроскопія, [M-CF3COO]+: 477. Приклад 111 1-(3-Фенілпропіл)-3-(R)(фенілтіофен-2ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 35%; 1 H-ЯМР (ДМСО-d6): δ 1,72-2,3 (m, 7H), 2,58 (m, 2Н), 3,00-3,48 (m, 7Н), 3,84 (m, 1Н), 5,04 (m, 3Н), 6,92-6,94 (m, 2H), 7,20-7,43 (m, 11Н); мас-спектроскопія, [M-CF3COO]+: 461. Приклад 112 1-(3-Фенілаліл)-3-(R)(фенілтіофен-2ілметилкарбамоїлокси)-1азоніабщикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 4мг, 11%; мас-спектроскопія, [M-CF3COO]+: 459. Приклад 113 1-(2-Бензилоксіетил)-3-(R)(фенілтіофен-2ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 14мг, 37%; мас-спектроскопія, [M-CF3COO]+: 477. Приклад 114 1-[3-(3-Гідроксифенокси)пропіл]-3(R)(фенілтіофен-2-ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 11мг, 28%; мас-спектроскопія, [M-CF3COO]+: 493. Приклад 115 1-Гептил-3-(R)(фенілтіофен-2ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 37%; мас-спектроскопія, [M-CF3COO]+: 441. Приклад 116 3-(R)(фенілтіофен-2-ілметилкарбамоїлокси)-1(3-тіофен-2-ілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 140мг, 48%; 1 H-ЯМР (ДМСО-d6): δ 1,40-2,30 (m, 7H), 2,83 (m, 2Н), 3,00-3,60 (m, 7Н), 3,88 (m, 1H), 5,04 (m, 3Н), 6,93-6,99 (m, 4H), 7,28-7,43 (m, 7Н); 53 85541 мас-спектроскопія, [М-Вr]+: 467. Приклад 117 1-(2-Феноксіетил)-3-(R)(фенілтіофен-2ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 510мг, 80%; 1 Н-ЯМР (ДМСО-d6): δ 1,40-2,30 (m, 5H), 3,203,73 (m, 7H), 4,05 (m, 1H), 4,44 (bs, 2H), 5,04 (m, 3H), 6,91-7,04 (m, 5H), 7,24-7,41 (m, 8H); мас-спектроскопія, [M-Br]+: 463; т. пл.: 133°С. Приклад 118 1-Аліл-3-(R)(фенілтіофен-2ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 360мг, 66%; 1 Н-ЯМР (ДМСО-d6): δ 1,40-2,30 (m, 5H), 3,003,41 (m, 5Н), 3,81-3,92 (m, 3Н), 5,04 (m, 3Н), 5,61 (m, 2Н), 5,93-6,05 (m, 1Н), 6,93-6,96 (m, 2H), 7,247,46 (m, 6H); мас-спектроскопія, [M-Br]+: 383; т. пл.: 110°С. Приклад 119 1-Азабіцикло[2.2.2]окт-3-(R)иловий складний ефір фенетилфенілкарбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 1400мг, 17%; 1 Н-ЯМР (ДМСО-d 6): δ 1,10-1,60 (m, 4H), 1,83 (s, 1H), 2,40-2,70 (m, 5Н), 2,78 (m, 2Н), 3,00-3,08 (m, 1Н), 3,87 (m, 2H), 4,58 (m, 1H), 7,16-7,40 (m, 10Н); мас-спектроскопія, [М+1]+: 351. Приклад 120 1-Метил-3-(R)(фенетилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 140мг, 73%; 1 H-ЯМР (ДМСО-d6): δ 1,40-2,30 (m, 5H), 2,80 (m, 2Н), 2,94 (s, 3Н), 3,10-3,50 (m, 5Н), 3,78-3,95 (m, 3Н), 4,89 (m, 1H), 7,16-7,41 (m, 10Н); мас-спектроскопія, [М-Вr]+: 365; т. пл.: 203°С. Приклад 121 1-Аліл-3-(R)(фенетилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 11мг, 35%; мас-спектроскопія, [M-CF3COO]+: 391. Приклад 122 3-(R)(Фенетилфенілкарбамоїлокси)-1-(3феноксипропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 16мг, 41%; мас-спектроскопія, [M-CF3COO]+: 485. Приклад 123 3-(R)(Фенетилфенілкарбамоїлокси)-1-(2феноксіетил)-1-азоніабіцикло[2.2.2]октан, трифторацетат 54 Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 15мг, 40%; 1 H-ЯМР (ДМСО-d6): δ 1,45-2,18 (m, 5H), 2,81 (m, 2Н), 3,28-3,70 (m, 7Н), 3,80-4,02 (m, 3Н), 4,43 (m, 2Н), 4,95 (m, 1H), 6,98-7,04 (m, 2Н), 7,16-7,40 (m, 13H); мас-спектроскопія, [M-CF3COO]+: 471. Приклад 124 3-(R)(Фенетилфенілкарбамоїлокси)-1-(3фенілпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 14мг, 37%; 1 H-ЯМР (ДМСО-d6): δ 1,45-2,20 (m, 7H), 2,59 (m, 2Н), 2,81 (m, 2Н), 3,05-3,5 (m, 7Н), 3,78-3,89 (m, 3Н), 4,91 (m, 1H), 7,17-7,42 (m, 15Н); мас-спектроскопія, [M-CF3COO]+: 469. Приклад 125 3-(R)(Фенетилфенілкарбамоїлокси)-1-(3фенілаліл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 4мг, 11%; мас-спектроскопія, [M-CF3COO]+: 467. Приклад 126 1-(2-Бензилоксіетил)-3(R)(фенетилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 14мг, 36%; мас-спектроскопія, [M-CF3COO]+: 485. Приклад 127 1-[3-(3-Гідроксифенокси)пропіл]-3(R)(фенетилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 14мг, 35%; 1 Н-ЯМР (ДМСО-d6): δ 1,45-2,20 (m, 7H), 2,82 (m, 2H), 3,05-3,50 (m, 7H), 3,83-3,99 (m, 5H), 4,94 (m, 1H), 6,33-6,39 (m, 3Н), 7,04-7,09 (m, 1H), 7,187,44(m, 10H), 9,49 (s, OH); мас-спектр [M-CF 3COO]+: 501. Приклад 128 1-Гептил-3-(R)(фенетилфенілкарбамоїлокси)1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 15мг, 42%; 1 Н-ЯМР (ДМСО-d6): δ 0,88 (m, 3Н), 1,28 (m, 8Н), 1,55-2,20 (m, 7Н), 2,82 (m, 2Н), 3,00-3,50 (m, 7Н), 3,68-3,89 (m, 3Н), 4,92 (m, 1Н), 7,18-7,43 (m, 10Н); мас-спекгроскопія, [M-CF3COO]+: 449. Приклад 129 3-(R)(Фенетилфенілкарбамоїлокси)-1-(3тіофен-2-ілпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 15мг, 39%; 55 85541 мас-спектроскопія, [M-CF3COO]+: 475. Приклад 130 1-Азабіцикло[2.2.2]окт-3-(R)иловий складний ефір пентилфенілкарбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 620мг, 9%; 1 H-ЯMP (ДМСО-d6): δ 0,83 (m, 3Н), 1,22-1,30 (m, 5Н), 1,43-1,56 (m, 5Н), 1,83 (s, 1Н), 2,42-2,65 (m, 5H), 3,01-3,06 (m, 1H), 3,59-3,65 (m, 2H), 4,49 (m, 1H), 7,22-7,41 (m, 5 H); мас-спектроскопія, [М+1]+: 317. Приклад 131 1-Метил-3-(R)(пентилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 130мг, 68%; 1 Н-ЯМР (ДМСО-d6): δ 0,81 (m, 3Н), 1,21 (m, 5Н), 1,45-2,20 (m, 6Н), 2,93 (s, 3Н), 3,10-3,70 (m, 7Н), 3,80 (m, 1 Η), 4,88 (m, 1Η), 7,24-7,41 (m, 5H); мас-спектроскопія, [М-Вr]+: 331. Приклад 132 1-Аліл-3-(R)(пентилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 10мг, 35%; 1 Н-ЯМР (ДМСО-d6): δ 0,83 (m, 3Н), 1,21-1,28 (m, 4H), 1,46 (m, 3Н), 1,54-1,91 (m, 3Н), 2,30 (m, 1H), 3,28-3,41 (m, 5H), 3,78-3,92 (m, 5H), 4,94 (m, 1H), 5,54-5,64 (m, 2H), 5,98 (m, 1H), 7,26-7,43 (m, 5H); мас-спекіроскопія, [M-CF3COO]+: 357. Приклад 133 3-(R)(Пентилфенілкарбамоїлокси)-1-(3феноксипропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 36%; мас-спектроскопія, [M-CF3COO]+: 451. Приклад 134 3-(R)(Пентилфенілкарбамоїлокси)-1-(2феноксіетил)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 14мг, 40%; 1 Н-ЯМР (ДМСО-d6): δ 0,82 (m, 3Н), 1,23 (m, 4Н), 1,46 (m, 3Н), 1,54-1,91 (m, 3Н), 2,25 (s, 1Н), 3,28-3,70 (m, 9H), 3,98 (m, 1H), 4,43 (m, 2H), 4,95 (m, 1H), 6,98-7,04 (m, 3H), 7,23-7 r,4 (m, 7H); мас-спектроскопія, [М-CF3COO]+: 437. Приклад 135 3-(R)(Пентилфенілкарбамоїлокси)-1-(3фенілпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 37%; 1 Н-ЯМР (ДМСО-d6): δ 0,82 (m, 3Н), 1,20-1,25 (m, 5Н), 1,44 (m, 3Н), 1,68-2,13 (m, 7H), 2,58 (m, 2H), 3,00-3,41 (m, 5H), 3,54-3,69 (m, 2Н), 3,79-3,85 (m, 1Н), 4,92 (m, 1H), 7,20-7,42 (m, 10Н); 56 мас-спектроскопія, [М-CF3COO]+: 435. Приклад 136 3-(R)(Пентилфенілкарбамоїлокси)-1-(3фенілаліл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 4мг, 12%; мас-спектроскопія, [M-CF3COO]+: 433. Приклад 137 1-(2-Бензилоксіетил)-3(R)(пентилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 15мг, 42%; мас-спектроскопія, [M-CF3COO]+: 451. Приклад 138 1-[3-(3-Гідроксифенокси)пропіл]-3(R)(пентилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 32%; мас-спектроскопія, [M-CF3COO]+: 467. Приклад 139 1-Гептил-3-(R)(пентилфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 15мг, 45%; мас-спектроскопія, [М-СF3СОО]+: 415. Приклад 140 3-(R)(Пентилфенілкарбамоїлокси)-1-(3-тіофен2-ілпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 37%; 1 Н-ЯМР (ДМСО-d6): δ 0,82 (m, 3Н), 1,22-1,26 (m, 5Н), 1,46 (m, 3Н), 1,60-2,14 (m, 7H), 2,82 (m, 2H), 3,20-3,41 (m, 5H), 3,50-3,70 (m, 2Н), 3,82 (m, 1Н), 4,92 (m, 1H), 6,93-6,99 (m, 2 Η), 7,25-7,43 (m, 6H); мас-спектроскопія, [М-СF3СОО]+: 441. Приклад 141 1-Азабіцикло[2.2.2]окт-3-(R)иловий складний ефір пент-4-енілфенілкарбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 690мг, 14%; 1 H-ЯМР (ДМСО-d6): δ 1,10-1,60 (m, 6 Η), 1,84 (bs, 1H), 1,97-2,04 (m, 2H), 2,45-2,65 (m, 5H), 3,023,10 (m, 1H), 3,29-3,66 (m, 2H), 4,59 (m, 1H), 4,615,00 (m, 2H), 5,70-5,84 (m, 1H), 7,22-7,42 (m, 5H); мас-спектроскопія, [M+1]+:315. Приклад 142 1-Аліл-3-(R)(пент-4-енілфенілкарбамоїлокси)1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполук синтезують відповідно до способу (г). Вихід на заключній стадії становить 10мг, 35%; мас-спектроскопія, [M-CF3COO]+: 355. 57 85541 Приклад 143 3-(R)(Пент-4-енілфенілкарбамоїлокси)-1-(3феноксипропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 15мг, 42%; 1 Н-ЯМР (ДМСО-d6): δ 1,50-2,20 (m, 1H), 3,233,47 (m, 7H), 3,56-3,73 (m, 2H), 3,87 (m, 1H), 4,03 (m, 2H), 4,92-4,95 (m, 2H), 5,00 (m, 1H), 5,70-5,82 (m, 1H), 6,93-6,99 (m, 2H), 7,26-7,44 (m, 8H); мас-спектроскопія, [М-CF3COO]+: 449. Приклад 144 3-(R)(Пент-4-енілфенілкарбамоїлокси)-1-(2феноксіетил)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 37%; 1 H-ЯМР (ДМСО-d6): δ 1,55 (m, 2H), 1,65-2,20 (m, 7Н), 3,28-3,75 (m, 9Н), 3,98 (m, 1H), 4,43 (bs, 2H), 4,92-4,99 (m, 3Н), 5,70-5,83 (m, 1H), 6,98-7,04 (m, 3Н), 7,24-7,40 (m, 7H); мас-спектроскопія, [M-CF3COO]+: 435. Приклад 145 3-(R)(Пент-4-енілфенілкарбамоїлокси)-1-(3фенілпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 37%; 1 Н-ЯМР (ДМСО-d6): δ 1,56 (m, 3Н), 1,70-2,14 (m, 8Н), 2,58 (m, 2Н), 3,19-3,41 (m, 7Н), 3,56-3,71 (m, 2Н), 3,81 (m, 1H), 4,92-4,99 (m, 3Н), 5,70-5,83 (m, 1H), 7,20-7,43 (m, 10Н); мас-спектроскопія, [M-CF3COO]+: 433. Приклад 146 3-(R)(Пент-4-енілфенілкарбамоїлокси)-1-(3фенілаліл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 4мг, 12%; мас-спектроскопія, [M-CF3COO]+: 431. Приклад 147 1-(2-Бензилоксіетил)-3-(R)пент-4енілфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 16мг, 44%; мас-спектроскопія, [M-CF3COO]+: 449. Приклад 148 1-[3-(3-Гідроксифенокси)пропіл]-3-(R)(пент-4енілфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 32%; мас-спектроскопія, [M-CF3COO]+: 465. Приклад 149 1-Гептил-3-(R)(пент-4енілфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат 58 Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 3мг, 9%; мас-спектроскопія, [M-CF3COO]+: 413. Приклад 150 1-Метил-3-(R)(пент-4енілфенілкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 49%; мас-спектроскопія, [M-CF3COO]+: 429. Приклад 151 3-(R)(Пент-4-енілфенілкарбамоїлокси)-1-(3тіофен-2-ілпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 15мг, 43%; 1 Н-ЯМР (ДМСО-d6): δ 1,40-2,20 (m, 11H), 2,82 (m, 2H), 3,05-3,5 (m, 7H), 3,58-3,86 (m, 3Н), 4,924,95 (m, 2H) 5,00 (m, 1H), 5,70-5,84 (m, 1H), 6,937,00 (m, 2H), 7,26-7,44 (m, 6H); мас-спектроскопія, [M-CF3COO]+: 439. Приклад 152 1-Азабіцикло[2.2.2]окт-3-(R)иловий складний ефір фенілтіофен-3-ілметилкарбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 2000мг, 15%; 1 Н-ЯМР (ДМСО-d6): δ 1,10-1,60 (m, 4H), 1,84 (bs, 1Н), 2,46-2,62 (m, 5H), 3,02-3,10 (m, 1H), 4,624,67 (m, 1H), 4,84 (s, 2H), 6,99 (m, 1H), 7,18-7,36 (m, 6H), 7,47-7,50 (m, 1H); мас-спектроскопія, [М+1]+: 343. Приклад 153 1-Аліл-3-(R)(фенілтіофен-3ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 8мг, 26%; 1 Н-ЯМР (ДМСО-d6): δ 1,45-2,00 (m, 4H), 2,21 (bs, 1H), 3,04-3,42 (m, 5Н), 3,78-3,91 (m, 3Н), 4,87 (s, 2Н), 5,02 (m, 1H), 5,54-5,64 (m, 2H), 5,91-6,02 (m, 1H), 7,00-7,02 (m, 1H), 7,22-7,39 (m, 6H), 7,507,52 (m, 1H); мас-спектроскопія, [M-CF3COO]+: 383. Приклад 154 1-(3-Феноксипропіл)-3-(R)(фенілтіофен-3ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 31%; мас-спектроскопія, [М-СF3СОО]+: 477. Приклад 155 1-(3-Фенілпропіл)-3-(R)(фенілтіофен-3ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 15мг, 41%; 59 1 85541 Н-ЯМР (ДМСО-d6): δ 1,45-2,18 (m, 7H), 2,59 (m, 2Н), 3,02-3,44 (m, 7Н), 3,84 (m, 1H), 4,87 (s, 2H), 4,99 (m, 1H), 7,00 (m, 1H), 7,21-7,38 (m, 11H), 7,477,50 (m, 1H); мас-спектроскопія, [M-CF3COO]+: 461. Приклад 156 1-(3-Фенілаліл)-3-(R)(фенілтіофен-3ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 4мг, 11%; мас-спектроскопія, [M-CF3COO]+: 459. Приклад 157 1-(2-Бензилоксіетил)-3-(R)(фенілтіофен-3ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 16мг, 42%; мас-спектроскопія, [M-CF3COO]+: 477. Приклад 158 1-[3-(3-Гідроксифенокси)пропіл]-3(R)(фенілтіофен-3-ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 33%; мас-спектроскопія, [M-CF3COO]+: 493. Приклад 159 1-Метил-3-(R)(фенілтіофен-3ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 12мг, 42%; мас-спектроскопія, [M-CF3COO]+: 357. Приклад 160 3-(R)(Фенілтіофен-3-ілметилкарбамоїлокси)-1(3-тіофен-2-ілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 500мг, 78%; 1 H-ЯМР (ДМСО-d6): δ 1,45-2,19 (m, 7H), 2,83 (m, 2Н), 3,04-3,13 (m, 1H), 3,19-3,46 (m, 6H), 3,833,90 (m, 1H), 4,88 (s, 2H), 4,99 (m, 1H), 6,94 (m, 3H), 7,20-7,40 (m, 7H), 7,49 (m, 1H); мас-спектроскопія, [M-Br]+: 467; т. пл.: 110°С. Приклад 161 3-(R)(Фенілтіофен-3-ілметилкарбамоїлокси)-1(2-феноксіетил)-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 350мг, 63%; 1 Н-ЯМР (ДМСО-d6): δ 1,45-2,20 (m, 5H), 3,27 (m, 1H), 3,40-3,80 (m, 6Н), 4,00-4,06 (m, 1H), 4,44 (bs, 2Н), 4,87 (s, 2Н), 5,02 (m, 1Н), 6,99-7,04 (m, 4H), 7,20-7,38 (m, 8H), 7,48 (m, 1H); мас-спектроскопія, [M-Br]+: 463; т. пл.:131°С. Приклад 162 Бутилтіофен-2-ілметилкарбамінової кислоти 1азабіцикло[2.2.2]окт-3-(R)иловий складний ефір 60 Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 1300мг, 29%; 1 Н-ЯМР (ДМСО-d6): δ 0,85 (m, 3Н), 1,19-1,68 (m, 8Н), 1,92 (m, 1Н), 2,49-2,64 (m, 5Н), 3,05-3,22 (m, 3Н), 4,56-4,62 (m, 3Н), 6,95-7,04 (m, 2Н), 7,427,44 (m, 1Н); мас-спектроскопія, [М+1]+: 323. Приклад 163 1-Аліл-3-(R)(бутилтіо фен-2ілметилкарбамоїлокси)-1азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 10мг, 23%; 1 H-ЯМР (ДМСО-d6): δ 0,86 (m, 3Н), 1,20-1,26 (m, 2Н), 1,42-1,49 (m, 2Н), 1,58-2,05 (m, 4Н), 2,32 (bs, 1H), 3,20-3,41 (m, 7H), 3,74-3,94 (m, 3H), 4,514,72 (m, 2H), 4,99 (m, 1H), 5,55-5,64 (m, 2H), 5,876,10 (m, 1H), 6,99 (m, 1H), 7,08 (m, 1H), 7,46 (m, 1H); мас-спектроскопія, [M-CF3COO]+: 363. Приклад 164 3-(R)(Бутилтіофен-2-ілметилкарбамоїлокси)-1(3-фенілпропіл)-1-азоніабіцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 13мг, 25%; 1 Н-ЯМР (ДМСО-d6): δ 0,85 (m, 3Н), 1,19-1,26 (m, 2Н),1,41-1,50 (m, 2Н), 1,75-2,10 (m, 6Н), 2,30 (bs, 1H), 2,59 (m, 2H), 3,10-3,50 (m, 9Н), 3,83 (m, 1 Η), 4,50-4,74 (m, 2H),4,97 (m, 1H), 6,97 (m, 1H), 7,07 (m, 1H), 7,20-7,35 (m, 5H), 7,43 (m, 1H); мас-спектроскопія, [M-CF3COO]+: 441. Приклад 165 1-Азабііщкло[2.2.2]окт-3-(R)иловий складний ефір біс-тіофен-2-ілметилкарбамінової кислоти Вказану в заголовку сполуку синтез ують відповідно до способу (а). Вихід на заключній стадії становить 340мг, 7%; 1 Н-ЯМР (ДМСО-d6): δ 1,28-1,31 (m, 1H), 1,451,72 (m, 3Н), 1,94-1,97 (m, 1H), 2,49-2,71 (m, 5H), 3,06-3,14 (m, 1H), 4,50-4,57 (m, 4H),4,62-4,69 (m, 1H), 6,96-7,06 (m, 4H), 7,44-7,46 (m, 2H); мас-спектроскопія, [М+1]+: 363. Приклад 166 1-Аліл-3-(R)(біс-тіофен-2ілметилкарбамоїлокси)-1азоніабїцикло[2.2.2]октан, трифторацетат Вказану в заголовку сполуку синтез ують відповідно до способу (г). Вихід на заключній стадії становить 9мг, 19%; 1 H-ЯМР (ДМСО-d6): δ 1,70-2,06 (m, 4H), 2,35 (bs, 1Н), 3,25-3,50 (m, 5H), 3,80-3,94 (m, 3H), 4,544,71 (m, 4H), 5,10 (m, 1H), 5,55-5,65 (m, 2H), 5,876,10 (m, 1H), 6,98-7,01 (m, 2H), 7,06-7,10 (m, 2H), 7,47-7,48 (m, 2H); мас-спектроскопія, [M-CF3COO]+: 403. Приклад 167 3-(R)(біс-тіофен-2-ілметилкарбамоїлокси)-1-(3фенілпропіл)-1-азоніабіцикло[2.2.2]октан, бромід Вказану в заголовку сполуку синтез ують відповідно до способу (в). Ви хід на заключній стадії становить 690мг, 82%;
ДивитисяДодаткова інформація
Назва патенту англійськоюQuinuclidine carbamate derivatives and pharmaceutical compositions containing the same
Автори англійськоюPrat Quinones Maria, Buil Albero Maria Antonia, Fernandez Forner Maria Dolors
Назва патенту російськоюКарбаматные производные хинуклидина и фармацевтическая композиции, которая содержит эти соединения
Автори російськоюПрат Киньонес Мария, Буил Альберо Мария Антония, Фернандес Форнер Мария Долорс
МПК / Мітки
МПК: A61P 13/02, A61P 43/00, A61P 11/08, C07D 453/00, A61P 1/08, A61P 25/00, A61P 1/00, C07D 487/08, A61P 9/00, A61K 45/00, A61P 1/04, A61P 29/00, A61K 31/439, A61P 11/00, A61P 13/00, A61P 11/06, A61P 13/10, A61P 11/02, A61P 9/06
Мітки: похідні, композиція, містить, яка, фармацевтична, сполуки, карбаматні, хінуклідину
Код посилання
<a href="https://ua.patents.su/33-85541-karbamatni-pokhidni-khinuklidinu-i-farmacevtichna-kompoziciya-yaka-mistit-ci-spoluki.html" target="_blank" rel="follow" title="База патентів України">Карбаматні похідні хінуклідину і фармацевтична композиція, яка містить ці сполуки</a>
Попередній патент: Пристрій для електроплазмолізу сировини рослинного походження
Наступний патент: Лікарські засоби, що містять тригідрат гідрохлориду варденафілу та спосіб їх виготовлення
Випадковий патент: Спосіб підготовки посадкового матеріалу картоплі до посадки





































