Гетероциклічні сполуки, придатні для лікування дисліпідемії
Номер патенту: 113053
Опубліковано: 12.12.2016
Автори: Калапатапу Ві. Ві. Ем. Саірам, Пінгалі Харікісхор, Макадіа Панкадж, Пандія Враджеш, Джаін Мукул Ар.
Формула / Реферат
1. Сполуки формули (І)
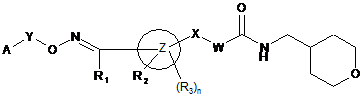 (І)
(І)
їх таутомерні форми, їх стереоізомери, їх фармацевтично прийнятні солі, де А позначає необов'язково заміщену одиночну або конденсовану групу, вибрану з арильних, гетероциклічних або циклоалкільних груп;
Y позначає зв'язок або заміщені чи незаміщені лінійні чи розгалужені (C1-C6)-алкільні, (С2-С6)-алкенільні групи, або групи, представлені -U(CH2)m-, де U позначає О, S(O)o, NR4; m позначає ціле число від 2 до 4, о позначає ціле число від 0 до 2, і R4 позначає Н, заміщений чи незаміщений лінійний чи розгалужений (C1-C6)-алкіл; Z позначає необов'язково заміщену одиночну або конденсовану групу, вибрану з арильних, гетероциклічних або циклоалкільних груп; X позначає зв'язок або є вибраним з О, S(O)o чи NR4; де R4 має вказані вище значення; W позначає заміщені чи незаміщені лінійні чи розгалужені (C1-C6)-алкіл, (С2-С6)-алкенільні групи; R1 позначає водень, необов'язково заміщені (C1-C6)-алкільні, (С3-С6)-циклоалкільні, алкоксіалкільні, гідроксіалкільні, аміноалкільні, арильні, гетероциклічні, аралкільні, гетероциклілалкільні групи; R2 позначає водень або групи, вибрані з (C1-C6)-алкілу, арилу, гетероциклілу, аралкілу, гетероциклілалкілу, (C1-C6)-алкокси, гідроксіалкілу, тіо-(C1-C6)-алкілу, аміно, аміноалкілу, алкіламіно, кожен з яких може бути необов'язково заміщеним; або R1 та R2, коли це можливо, можуть разом утворювати 4-7-членне насичене або частково насичене кільце, яке містить 0-2 додаткових гетероатоми, вибрані з групи, що включає N, О, та S(O)o; R3 у кожному випадку присутності незалежно позначає водень, галоген, (С1-С3)-алкіл, галоїд-(С1-С3)-алкіл, (С1-С3)-алкокси, тіо-(С1-С3)-алкіл, сульфенільні похідні, сульфонільні похідні; n позначає ціле число, вибране з 0-3.
2. Сполуки за п. 1, де А вибирають з необов'язково заміщених арильних або гетероциклічних груп.
3. Сполуки за п. 1 та 2, де А позначає арильну групу, арильні групи вибирають з заміщених чи незаміщених моноциклічних або біциклічних ароматичних груп.
4. Сполука за п. 3, де арильна група є необов'язково заміщеною фенільною групою.
5. Сполука за п. 1, де А позначає гетероциклічну групу, гетероциклічну групу вибирають з одиночних або конденсованих моно-, бі- або трициклічних ароматичних або неароматичних груп, що містять один чи декілька гетероатомів, вибраних з О, N або S.
6. Сполука за п. 5, яка відрізняється тим, що гетероциклічну групу вибирають з піридильної, тієнільної, фурильної, піролільної, оксазолільної, тіазолільної, ізотіазолільної, імідазолільної, ізоксазолільної, оксадіазолільної, тіадіазолільної, триазолільної, тетразолільної, бензофуранільної, бензотієнільної, індолінільної, індолільної, азаіндолільної, азаіндолінільної, піразолопіримідинільної, азахіназолінільної, піридофуранільної, піридотієнільної, тієнопіримідильної, хінолінільної, піримідинільної, піразолільної, хіназолінільної, піридазинільної, триазинільної, бензимідазолільної, бензотриазолільної, фталазинільної, нафтиридинільної, пуринільної, карбазолільної, фенотіазинільної, феноксазинільної, бензоксазолільної, бензотіазолільної, тіазепінільної, оксазолідинільної, тіазолідинільної, дигідротіофенової, дигідропіранової, дигідрофуранової, дигідротіазольної, бензопіранільної, бензопіранонільної, бензодигідрофуранільної, бензодигідротієнільної, піразолопіримідонільної, азахіназоліноїльної, тієнопіримідонільної, хіназолонільної, піримідонільної, бензохазинільної, бензоксазинонільної, бензотіазинільної, бензотіазинонільної, тієнопіперидинільної груп.
7. Сполука за п. 1, де Z позначає необов'язково заміщені арильні або гетероциклічні групи.
8. Сполука за п. 7, де арильну групу вибирають з заміщених чи незаміщених моноциклічних або біциклічних ароматичних груп.
9. Сполука за п. 8, де арильна група є необов'язково заміщеною фенільною групою.
10. Сполука за п. 7, де гетероциклічну групу вибирають з одиночних або конденсованих моно- або біциклічних ароматичних груп, що містять один чи декілька гетероатомів, вибраних з О, N або S.
11. Сполука за п. 10, де ароматичну гетероциклічну групу вибирають з піридильної, тієнільної, фурильної, піролільної, оксазолільної, тіазолільної, ізотіазолільної, імідазолільної, ізоксазолільної, оксадіазолільної, тіадіазолільної, триазолільної, тетразолільної, бензофуранільної, бензотієнільної, індолінільної, індолільної, азаіндолільної, азаіндолінільної, піразолопіримідинільної, азахіназолінільної, піридофуранільної, піридотієнільної, тієнопіримідильної, хінолінільної, піримідинільної, піразолільної, хіназолінільної, піридазинільної, триазинільної, бензимідазолільної, бензотриазолільної, фталазинільної, нафтиридинільної, пуринільної, карбазолільної, фенотіазинільної, феноксазинільної, бензоксазолільної, бензотіазолільної груп.
12. Сполуки за п. 1, де сполуки вибрані з:
N-((тетрагідро-2Н-піран-4-іл)метил)-2-(4-(1-(((4-(трифторметил)бензил)оксі)іміно)-пропіл)феноксі)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)-етил)піридин-2-іл)оксі)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)-етил)піридин-2-іл)аміно)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-((4-(1-(((4-(трифторметил)бензил)оксі)іміно)-пропіл)феніл)аміно)ацетаміду;
2,2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)етил)оксазол-2-іл)азанедіїл)біс-(N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду);
N-((тетрагідро-2Н-піран-4-іл)метил)-2-((1-(4-(трифторметил)бензил)-3-((((4-(трифторметил)бензил)оксі)іміно)метил)-1Н-індол-5-іл)оксі)ацетаміду;
2-(2-метил-4-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(2-феніл-1-(((3-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(2-(піридин-4-іл)-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(2-морфоліно-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-(4-(2-тіоморфоліно-1-(((4-(трифторметил)-бензил)оксі)іміно)етил)феноксі)ацетаміду;
2-(2-метил-4-(2-(тіофен-3-іл)-1-(((4-(трифторметил)бензил)оксі)іміно)етил)-фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-(4-((((4-(трифторметил)бензил)оксі)іміно)-метил)феноксі)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-(4-(1-(((4-(трифторметил)бензил)оксі)іміно)-етил)феноксі)ацетаміду;
N-((тeтpaгiдpo-2H-пipaн-4-iл)мeтил)-2-((5-((((4-(тpифтopмeтил)бeнзил)oкci)iмiнo)-метил)піридин-2-іл)оксі)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-((4-(1-(((4-(трифторметил)бензил)оксі)іміно)-етил)феніл)аміно)ацетаміду;
2-((5-(1-(((4-ціанобензил)оксі)іміно)етил)піридин-2-іл)окси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)-пропіл)піридин-2-іл)оксі)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)-пропіл)піридин-2-іл)аміно)ацетаміду;
2-((5-(1-((бензилоксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2Н-піран-4-іл)-метил)ацетаміду;
2-((5-(1-(((4-метилбензил)оксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-((5-(1-(((4-метоксибензил)оксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-((5-(1-(((4-фторбензил)оксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-((5-(1-(((4-ціанобензил)оксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(2-метил-4-(1-(((4-(трифторметил)бензил)оксі)іміно)бутил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(2-метокси-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(2-гідрокси-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(2-метил-4-(1-(((4-метилбензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(1-(((4-метилбензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(1-(((4-фторбензил)оксі)іміно)-2-фенілетил)-2-метилфенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(1-(((4-фторбензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(1-(((4-хлорбензил)оксі)іміно)-2-фенілетил)-2-метилфенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(1-(((4-хлорбензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(2-метил-4-(2-феніл-1-(((4-(трифторметокси)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(2-феніл-1-(((4-(трифторметокси)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(1-(((4-метоксибензил)оксі)іміно)-2-фенілетил)-2-метилфенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(1-(((4-метоксибензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(1-(((4-(метилсульфоніл)бензил)оксі)іміно)пропіл)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(2-феніл-1-((піридин-2-ілметоксі)іміно)етил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(1-((2-(1Н-індол-1-іл)етоксі)іміно)пропіл)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(1-(((5-етилпіримідин-2-іл)оксі)іміно)пропіл)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(1-(((5-метил-2-фенілоксазол-4-іл)метоксі)іміно)пропіл)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(1-(((3-(трет-бутил)-1-(п-толіл)-1Н-піразол-5-іл)метоксі)іміно)пропіл)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-((5-(((4-(трифторметил)бензил)оксі)іміно)-5,6,7,8-тетрагідронафталін-2-іл)оксі)ацетаміду;
2-((5-(((4-хлорбензил)оксі)іміно)-5,6,7,8-тетрагідронафталін-2-іл)окси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-((5-(((4-ціанобензил)оксі)іміно)-5,6,7,8-тетрагідронафталін-2-іл)окси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-((5-(((4-метоксибензил)оксі)іміно)-5,6,7,8-тетрагідронафталін-2-іл)окси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
метил-3-((((6-(2-оксо-2-(((тетрагідро-2Н-піран-4-іл)метил)аміно)етокси)-3,4-дигідронафталін-1(2Н)-іліден)аміно)окси)метил)бензоату;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)-етил)хінолін-8-іл)оксі)ацетаміду;
2-метил-N-((тетрагідро-2Н-піран-4-іл)метил)-2-(4-(1-(((4-(трифторметил)бензил)-оксі)іміно)пропіл)фенокси)пропанаміду;
2-метил-N-((тетрагідро-2Н-піран-4-іл)метил)-2-(4-(1-(((4-(трифторметил)бензил)-оксі)іміно)етил)фенокси)пропанаміду;
2-(4-(1-(((тетрагідро-2Н-піран-4-іл)метоксі)іміно)етил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-(4-(1-((циклогексилметоксі)іміно)етил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)-метил)ацетаміду;
2-(4-(1-((нафталін-2-ілметоксі)іміно)етил)фенокси)-N-((тетрагідро-2Н-піран-4-іл)-метил)ацетаміду;
2-((5-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)окси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
2-((5-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)аміно)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-((3-((((4-(трифторметил)бензил)оксі)іміно)-метил)-1Н-індол-5-іл)оксі)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-((3-(1-(((4-(трифторметил)бензил)оксі)іміно)-етил)-1Н-індол-5-іл)оксі)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-((3-(1-(((4-(трифторметил)бензил)оксі)іміно)-пропіл)-1Н-індол-5-іл)оксі)ацетаміду;
2-((3-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)-1Н-індол-5-іл)окси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-3-(5-(1-(((4-(трифторметил)бензил)оксі)іміно)-етил)піримідин-2-іл)пропанаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-3-(5-(1-(((4-(трифторметил)бензил)оксі)іміно)-пропіл)піримідин-2-іл)пропанаміду;
3-(5-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піримідин-2-іл)-N-((тетрагідро-2Н-піран-4-іл)метил)пропанаміду;
N-((тетрагідро-2Н-піран-4-іл)метил)-2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)-пропіл)хінолін-8-іл)оксі)ацетаміду;
2-((5-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)хінолін-8-іл)окси)-N-((тетрагідро-2Н-піран-4-іл)метил)ацетаміду.
Текст
Реферат: O A Y O N Z R1 R2 X (R3)n W N H O Даний винахід стосується сполук загальної формули (І), їх таутомерних форм, їх стереоізомерів, їх фармацевтично прийнятних солей, фармацевтичних композицій, що їх містять, способів їх одержання, застосування цих сполук у медицині та проміжних сполук, використовуваних при їх одержанні. Даний винахід стосується сполук, які можуть бути використані для лікування таких хвороб, як гіперліпідемія, а також позитивно впливає на холестерин. UA 113053 C2 (12) UA 113053 C2 UA 113053 C2 Область техніки Даний винахід стосується сполук загальної формули (I), їх таутомерних форм, їх стереоізомерів, їх фармацевтично прийнятних солей, фармацевтичних композицій, що їх містять, способів їх одержання, застосування цих сполук у медицині та проміжних сполук, використовуваних при їх одержанні. Даний винахід стосується сполук, які можуть бути використані для лікування хвороб, таких як гіперліпідемія, а також позитивно впливає на холестерин. Сполуки загальної формули (I) знижують глюкозу крові, знижують чи модулюють рівні тригліцеридів та/або рівні холестерину та/або ліпопротеїнів низької густини (LDL) та підвищують рівні у плазмі ліпопротеїнів високої густини (HDL), і тому є корисними для боротьби з різними медичними станами, при яких таке зниження (і підвищення) є цілющим. Таким чином, вони можуть бути використані у лікуванні та/або профілактиці ожиріння, гіперліпідемії, гіперхолестеринемії, гіпертензії, епізодів атеросклеротичної хвороби, рестенозу судин, діабету та багатьох інших споріднених станів. Сполуки загальної формули (I) є корисними для запобігання або зниження ризику розвитку атеросклерозу, який призводить до таких хвороб та станів, як артеріосклеротичні серцевосудинні хвороби, інсульт, коронарні хвороби серця, цереброваскулярні хвороби, хвороби периферичних судин та споріднені розлади. Ці сполуки загальної формули (I) є корисними для лікування та/або профілактики метаболічних розладів, широко визначених як синдром X. Характерні ознаки синдрому X включають початкову інсулінорезистентність з подальшими гіперінсулінемією, дисліпідемією та порушеною толерантністю до глюкози. Непереносність глюкози може призводити до інсуліннезалежного цукрового діабету (NIDDM, діабет типу 2), що характеризується гіперглікемією, яка за відсутності контролю може призводити до діабетичних ускладнень або метаболічних розладів, спричинюваних інсулінорезистентністю. Діабет вже не вважають асоційованим лише з метаболізмом глюкози, і він впливає на анатомічні та фізіологічні параметри з інтенсивністю, що змінюється у залежності від стадій/тривалості та тяжкості діабетичного стану. Сполуки за даним винаходом також є корисними для запобігання, зупинення чи уповільнення розвитку, або зниження ризику вищезгаданих розладів, разом із спричинюваними вторинними хворобами, такими як серцево-судинні хвороби, як то артеріосклероз, атеросклероз; діабетична ретинопатія, діабетична невропатія та хвороба нирок, включаючи діабетичну нефропатію, гломерулонефрит, гломерулосклероз, нефротичний синдром, гіпертензивний нефросклероз та ниркові хвороби кінцевої стадії, такі як мікроальбумінурія та альбумінурія, які можуть бути наслідком гіперглікемії або гіперінсулінемії. Сполуки за даним винаходом можуть бути корисними як інгібітори альдозоредуктази; для поліпшення когнітивних функцій при деменції, та при лікуванні та/або профілактиці розладів, таких як псоріаз, синдром полікістозу яєчніків (PCOS), рак, остеопороз, лептинорезистентність, запалення та запальні хвороби кишечнику, загоєння ран, ксантома, панкреатит, міотонічна дистрофія, дисфункція ендотеліальних клітин та гіперліпідемія. Відомий рівень техніки Вищі рівні холестерину LDL у плазмі підвищують серцево-судинні ризики, а зниження рівнів LDL буде зменшувати ризик серцево-судинних хвороб (CVD) на порівняний процент (PNAS, 2009, 106, 9546-9547). Кліренс холестерину LDL з плазми відбувається завдяки дії рецепторів LDL у печінці, і рецептори LDL є глікопротеїнами клітинної поверхні, що зв'язуються з аполіпопротеїном B100 (апоB100) на частинках LDL з високою афінністю та медіюють їх ендоцитозне поглинання (Journal of Biological Chemistry, 2009, 284, 10561-10570). Порушення кліренсу печінкового холестерину та підвищені рівні холестерину LDL плазми, спричинені мутаціями, викликають сімейну гіперхолестеринемію. Такі мутації були ідентифіковані в людському рецепторі LDL та пізніше в аполіпопротеїні B (Nature Structural and Molecular Biology, 2007, 14, 413-419). Нещодавно було знайдено, що мутації у певних субтипах гена пропротеїнконвертази/субтилізину, таких як субтип дев'ять (тут та надалі "ген") є третім класом 1 UA 113053 C2 мутацій, асоційованих з аутосомно-домінантною гіперхолестеринемією (ADH). Відкриття, етіологія та функції цього субтипу гена детально описані у Nature Genetics, 2003, 34, 154-156, Trends in Biochemical Sciences, 2008, 33, 426-434 і т.д. Декілька місенс-мутацій (S127R, D129G, F216L, D374H, D374Y) асоційовані з гіперхолестеринемією та передчасним атеросклерозом (J Lipid Res. 2008, 49, 1333-1343). Мутації втрати функції (R46L, L253F, A433T) призводять до підвищеної копійності рецептора, посилення кліренса холестерину LDL з циркуляції та зниження серцево-судинного ризику (Nature Structural and Molecular Biology, 2007, 14, 413-419). Детальні молекулярні механізми, що пояснюють асоціацію LDLR і конкретного субтипу гена та деградацію LDLR, залишаються точно невідомими (Drug News Perspectives, 2008, 21, 323330). Внаслідок інгібування рециркуляції LDLR, число рецепторів LDL на клітинній поверхні зменшується, і це збільшує рівні LDL у плазмі (PNAS, 2009, 106, 9546-9547). Були описані різноманітні підходи до інгібування цього конкретного субтипу гена, включаючи глушення гена за допомогою кіРНК (siRNA) або антисмислових олігонуклеотидів, моноклонального антитіла (mAb), яке порушує білок-білкові взаємодії, або пептидами; усі вищезгадані стратегії продемонстрували зниження холестерину LDL, що може бути ефективною терапією для лікування гіперхолестеринемії (Biochemical Journal, 2009, 419, 577-584; PNAS, 2008, 105, 11915-11920; Journal of Lipid Research, 2007, 48, 763-767; PNAS, 2009, 106, 98209825). Однак, повідомлялося про дуже незначний успіх при спробах інгібування цього субтипу гена за допомогою малих молекул. Такі інгібітори на основі малих молекул мають очевидні клінічні та терапевтичні переваги порівняно з іншими підходами, описаними вище. Ми розкриваємо тут нові малі молекули, які продемонстрували здатність інгібувати цей конкретний ген в in vitro дослідженнях і тому забезпечують альтернативний корисний підхід до лікування пацієнтів, що потребують такої терапії. Кращі варіанти втілення винаходу Важливою задачею даного винаходу є створення нових заміщених оксимінових похідних, представлених загальною формулою (I), їх таутомерних форм, їх стереоізомерів, їх фармацевтично прийнятних солей та фармацевтичних композиції, що їх містять, або їх сумішей. У варіанті втілення даного винаходу пропонується спосіб одержання нових заміщених оксимінових похідних та їх похідних, представлених загальною формулою (I), їх таутомерних форм, їх стереоізомерів, їх фармацевтично прийнятних солей. В наступному варіанті втілення даного винаходу пропонуються фармацевтичні композиції, що містять сполуки загальної формули (I), їх таутомерні форми, їх стереоізомери, їх фармацевтично прийнятн солі, або їх суміші у поєднанні з придатними носіями, розчинниками, розріджувачами та іншими середовищами, звичайно використовуваними при виготовленні таких композицій. В наступному варіанті втілення даного винаходу пропонується спосіб лікування хвороб, таких як дисліпідемія, гіперліпідемія і т.д., шляхом забезпечення терапевтично ефективної кількості сполук формули (I) або їх фармацевтично прийнятних солей або їх придатних фармацевтичних композицій. Вищеописані та інші варіанти втілення представлені детальніше нижче. Детальний опис винаходу Таким чином, даний винахід стосується сполук загальної формули (I), їх таутомерних форм, їх стереоізомерів, їх фармацевтично прийнятних солей та фармацевтичних композицій, що їх містять, де A позначає необов'язково заміщену одиночну або конденсовану групу, вибрану з арильної, гетероциклічної або циклоалкільної груп; У кращому варіанті втілення, A вибирають з необов'язково заміщених арильних або гетероциклічних груп; У додатковому кращому варіанті втілення, арильна група може бути вибрана із заміщених чи незаміщених моноциклічних або біциклічних ароматичних груп; У ще кращому варіанті втілення, арильна група є необов'язково заміщеною фенільною групою. 2 UA 113053 C2 У варіанті втілення, коли A позначає гетероциклічну групу, гетероциклічна група може бути вибрана з одиночних або конденсованих моно-, бі- або трициклічних ароматичних чи неароматичних груп, що містять один чи декілька гетероатомів, вибраних з O, N або S; У кращому варіанті втілення, гетероциклічна група може бути вибрана з піридилу, тієнілу, фурилу, піролілу, оксазолілу, тіазолілу, ізотіазолілу, імідазолілу, ізоксазолілу, оксадіазолілу, тіадіазолілу, триазолілу, тетразолілу, бензофуранілу, бензотієнілу, індолінілу, індолілу, азаіндолілу, азаіндолінілу, піразолопіримідинілу, азахіназолінілу, піридофуранілу, піридотієнілу, тієнопіримідилу, хінолінілу, піримідинілу, піразолілу, хіназолінілу, піридазинілу, триазинілу, бензимідазолілу, бензотриазолілу, фталазинілу, нафтиридинілу, пуринілу, карбазолілу, фенотіазинілу, феноксазинілу, бензоксазолілу, бензотіазолілу, тіазепінілу, оксазолідинілу, тіазолідинілу, дигідротіофену, дигідропірану, дигідрофурану, дигідротіазолу, бензопіранілу, бензопіранонілу, бензодигідрофуранілу, бензодигідротієнілу, піразолопіримідонілу, азахіназоліноїлу, тієнопіримідонілу, хіназолонілу, піримідонілу, бензоxазинілу, бензоксазинонілу, бензотіазинілу, бензотіазинонілу, тієнопіперидинілу тощо; Y позначає зв'язок або заміщені чи незаміщені лінійні чи розгалужені (C1-C6)-алкільні, (C2C6)-алкенільні групи або групи, представлені -U(CH2)m-, де U позначає O, S(O)o, NR4; m позначає ціле число від 2 до 4, o позначає ціле число від 0 до 2, і R4 позначає H, заміщений чи незаміщений лінійний чи розгалужений (C1-C6)-алкіл; Z позначає необов'язково заміщену одиночну або конденсовану групу, вибрану з арильних, гетероциклічних або циклоалкільних груп; У кращому варіанті втілення, Z вибирають з необов'язково заміщених арильних або гетероциклічних груп; У додатковому кращому варіанті втілення, арильна група може бути вибрана із заміщених чи незаміщених моноциклічних або біциклічних ароматичних груп; У ще кращому варіанті втілення, арильна група є необов'язково заміщеною фенільною групою. Якщо Z позначає гетероциклічну групу, то гетероциклічна група може бути вибрана з одиночних або конденсованих моно- або біциклічних ароматичних груп, що містять один чи декілька гетероатомів, вибраних з O, N або S; У ще кращому варіанті втілення, коли Z позначає гетероароматичну групу, гетероароматична група може бути вибрана з піридильної, тієнільної, фурильної, піролільної, оксазолільної, тіазолільної, ізотіазолільної, імідазолільної, ізоксазолільної, оксадіазолільної, тіадіазолільної, триазолільної, тетразолільної, бензофуранільної, бензотієнільної, індолінільної, індолільної, азаіндолільної, азаіндолінільної, піразолопіримідинільної, азахіназолінільної, піридофуранільної, піридотієнільної, тієнопіримідильної, хінолінільної, піримідинільної, піразолільної, хіназолінільної, піридазинільної, триазинільної, бензимідазолільної, бензотриазолільної, фталазинільної, нафтиридинільної, пуринільної, карбазолільної, фенотіазинільної, феноксазинільної, бензоксазолільної, бензотіазолільної груп. X позначає зв'язок або може бути вибраний з O, S(O)o чи NR4; де R4 має вказані вище значення; W позначає заміщені чи незаміщені лінійні чи розгалужені (C1-C6)-алкільні, (C2-C6)алкенільні групи; R1 позначає водень, необов'язково заміщені (C1-C6)-алкільні, (C3-C6)-циклоалкільні, алкоксіалкільні, гідроксіалкільні, аміноалкільні, арильні, гетероциклічні, аралкільні, гетероциклілалкільні групи; R2 позначає водень або групи, вибрану з (C1-C6)-алкілу, арилу, гетероциклілу, аралкілу, гетероциклілалкілу, (C1-C6)-алкокси, гідроксіалкілу, тіо(C1-C6)-алкілу, аміно, аміноалкілу, алкіламіно, кожен з яких може бути необов'язково заміщеним; Альтернативно, R1 та R2, коли це можливо, можуть разом утворювати 4-7-членне насичене або частково насичене кільце, яке містить 0-2 додаткових гетероатомів, вибраних з групи, що складається з N, O, та S(O)o; R3 у кожному випадку присутності незалежно позначає водень, галоген, (C1-C3)-алкіл, галоїд-(C1-C3)-алкіл, (C1-C3)-алкокси, тіо-(C1-C3)-алкіл, сульфенільні похідні, сульфонільні похідні; n позначає ціле число, вибране з 0-3; Якщо A, R1, R2, R3 або R4 є заміщеними, замісники у кожному випадку присутності можуть бути незалежно вибраними з гідроксилу, оксо, галоїду, тіолу, нітро, аміно, ціано, формілу, або заміщених чи незаміщених груп, вибраних з амідино, алкілу, галоїдалкілу, пергалоїдалкілу, алкокси, галоїдалкокси, пергалоїдалкокси, алкенілу, алкінілу, циклоалкілу, циклоалкенілу, біциклоалкілу, біциклоалкенілу, алкокси, алкенокси, циклоалкокси, арилу, арилокси, аралкілу, аралкокси, гетероциклілу, гетероциклілалкілу, гетероциклокси, гетероциклілалкокси, 3 UA 113053 C2 гетероциклілалкоксиацилу, ацилу, ацилокси, ациламіно, монозаміщеного або дизаміщеного аміно, ариламіно, аралкіламіно, карбонової кислоти та її похідних, таких як складні ефіри та аміди, карбоніламіно, гідроксіалкілу, аміноалкілу, алкоксіалкілу, арилоксиалкілу, аралкоксіалкілу, алкілтіо, тіоалкілу, циклоалкілтіо, арилтіо, гетероциклілтіо, алкілсульфінілу, циклоалкілсульфінілу, арилсульфінілу, гетероциклілсульфінілу, алкілсульфонілу, циклоалкілсульфонілу, арилсульфонілу, гетероциклілсульфонілу, алкілсульфоніламіно, циклоалкілсульфоніламіно, арилсульфоніламіно, гетероциклілсульфоніламіно, алкілсульфонілокси, циклоалкілсульфонілокси, арилсульфонілокси, гетероциклілсульфонілокси, алкоксикарбоніламіно, арилоксикарбоніламіно, аралкілоксикарбоніламіно, амінокарбоніламіно, алкіламінокарбоніламіно, алкоксиаміно, гідроксиламіно, сульфінільних похідних, сульфонільних похідних, сульфонової кислоти та її похідних. Якщо замісники на A, R1, R2, R3 або R4 є додатково заміщеними, замісники можуть бути вибрані з однієї чи декількох груп, описаних вище. Різні групи, радикали та замісники, згадувані будь-де в даному описі винаходу, описані далі. У додатковому кращому варіанті втілення групи, радикали, описані вище, можуть бути вибрані з таких: - "алкільна" група, використовувана сама по собі або у поєднанні з іншими радикалами, позначає лінійний чи розгалужений радикал, який містить від одного до шести атомів вуглецю, вибраний з метилу, етилу, н-пропілу, ізопропілу, н-бутилу, втор-бутилу, трет-бутилу, амілу, тамілу, н-пентилу, н-гексилу тощо; - "алкенільну" групу, використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з радикала, що містить від двох до шести атомів вуглецю, краще, з груп, вибраних з вінілу, алілу, 2-бутенілу, 3-бутенілу, 2-пентенілу, 3-пентенілу, 4-пентенілу, 2-гексенілу, 3гексенілу, 4-гексенілу тощо; "алкенільна" група включає дієни та триєни з лінійними та розгалуженими ланцюгами; - "циклоалкільну" або "аліциклічну" групу, використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з циклічного радикала, що містить від трьох до шести атомів вуглецю, краще, циклопропілу, циклобутилу, циклопентилу, циклогексилу тощо; - "циклоалкенільну" групу, використовувану саму по собі або у поєднанні з іншими радикалами, краще вибирають з циклопропенілу, 1-циклобутенілу, 2-циклобутенілу, 1циклопентенілу, 2-циклопентенілу, 3-циклопентенілу, 1-циклогексенілу, 2-циклогексенілу, 3циклогексенілу тощо; термін "біциклоалкеніл" означає декілька циклоалкенільних груп, сконденсованих одна з одною; - групу "алкокси", використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з групи, що включає алкільний радикал, як визначено вище, приєднаний безпосередньо до атома кисню, краще, з груп, вибраних з метокси, етокси, н-пропокси, ізопропокси, н-бутокси, т-бутокси, ізобутокси, пентилокси, гексилокси тощо; - групу "циклоалкокси", використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з циклічного радикала, що містить від трьох до семі атомів вуглецю, краще, циклопропілокси, циклобутилxoy, циклопентилокси, циклогексилокси тощо; термін "біциклоалкілокси" означає декілька циклоалкільних груп, сконденсованих одна з одною; - групу "алкенокси", використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з групи, що включає алкенільний радикал, як визначено вище, приєднаний до атома кисню, краще, вибирають з вінілокси, алілокси, бутенокси, пентенокси, гексенокси тощо; - "галоїдалкільну" групу вибирають з алкільного радикала, як визначено вище, придатно заміщеного одним чи декількома галогенами; такого як пергалоїдалкіл, краще, перфтор(C1C6)алкіл, такий як фторметил, дифторметил, трифторметил, фторетил, дифторетил, трифторетил, моно- або полігалоїд-заміщених метильної, етильної, пропільної, бутильної, пентильної або гексильної груп; - групу "галоїдалкокси" вибирають з придатного галоїдалкілу, як визначено вище, безпосередньо приєднаного до атома кисню, краще, з груп, вибраних з фторметокси, хлорметокси, фторетокси, хлоретокси тощо; - "арильну" або "ароматичну" групу, використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з придатної ароматичної системи, що включає одно, два чи три кільця, причому такі кільця можуть бути з'єднані одне з одним через місточкові зв'язки або можуть бути сконденсованими, краще, групи вибирають з фенілу, нафтилу, тетрагідронафтилу, індану, біфенілу тощо; - групу "арилокси", використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з групи, що включає арильний радикал, як визначено вище, приєднаний 4 UA 113053 C2 безпосередньо до атома кисню, краще, з груп, вибраних з фенокси, нафтилокси, тетрагідронафтилокси, біфенілокси тощо; - "гетероцикліл" або "гетероциклічну" групу, використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з придатних ароматичних або неароматичних радикалів, що містять один чи декілька гетероатомів, вибраних з O, N або S. Неароматичні радикали можуть бути насиченими, частково насиченими або ненасиченими моно-, бі- або трициклічними радикалами, що містять один чи декілька гетероатомів, вибраних з азоту, сірки та кисню, краще, вибирають з азиридинілу, азетидинілу, піролідинілу, імідазолідинілу, піперидинілу, піперазинілу, 2-оксопіперидинілу, 4-оксопіперидинілу, 2-оксопіперазинілу, 3-оксопіперазинілу, морфолінілу, тіоморфолінілу, 2-оксоморфолінілу, азепінілу, діазепінілу, оксапінілу, тіазепінілу, оксазолідинілу, тіазолідинілу, дигідротіофену, дигідропірану, дигідрофурану, дигідротіазолу, бензопіранілу, бензопіранонілу, бензодигідрофуранілу, бензодигідротієнілу, піразолопіримідонілу, азахіназоліноїлу, тієнопіримідонілу, хіназолонілу, піримідонілу, бензоxазинілу, бензоксазинонілу, бензотіазинілу, бензотіазинонілу, тієнопіперидинілу тощо; ароматичні радикали можуть бути вибрані з придатних одиночних або конденсованих моно-, бі- або трициклічних ароматичних гетероциклічних радикалів, що містять один чи декілька гетероатомів, вибраних з O, N або S, краще, групи вибирають з піридилу, тієнілу, фурилу, піролілу, оксазолілу, тіазолілу, ізотіазолілу, імідазолілу, ізоксазолілу, оксадіазолілу, тіадіазолілу, триазолілу, тетразолілу, бензофуранілу, бензотієнілу, індолінілу, індолілу, азаіндолілу, азаіндолінілу, піразолопіримідинілу, азахіназолінілу, піридофуранілу, піридотієнілу, тієнопіримідилу, хінолінілу, піримідинілу, піразолілу, хіназолінілу, піридазинілу, триазинілу, бензимідазолілу, бензотриазолілу, фталазинілу, нафтиридинілу, пуринілу, карбазолілу, фенотіазинілу, феноксазинілу, бензоксазолілу, бензотіазолілу тощо; - групи "гетероциклокси", "гетероциклілалкокси" вибирають з придатних гетероциклічних, гетероциклілалкільних груп, відповідно, як визначено вище, приєднаних до атома кисню; - "ацильну" групу, використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з радикала, що містить від одного до восьми атомів вуглецю, краще, вибирають з формілу, ацетилу, пропаноїлу, бутаноїлу, ізобутаноїлу, пентаноїлу, гексаноїлу, гептаноїлу, бензоїлу тощо, які можуть бути заміщеними; - групу "ацилокси", використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з придатної ацильної групи, як визначено вище, безпосередньо приєднаної до атома кисню, краще, такі групи вибирають з ацетилокси, пропіонілокси, бутаноїлокси, ізобутаноїлокси, бензоїлокси тощо; - групу "ациламіно", використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з придатної ацильної групи, як визначено вище, приєднаної до радикала аміно, краще, такі групи вибирають з CH3CONH, C2H5CONH, C3H7CONH, C4H9CONH, C6H5CONH тощо, які можуть бути заміщеними; - група "монозаміщений аміно", використовувана сама по собі або у поєднанні з іншими радикалами, позначає аміногрупу, заміщену однією групою, вибраною з (C1-C6)алкільної, заміщеної алкільної, арильної, заміщеної арильної або арилалкільної груп, як визначено вище, краще, такі групи вибирають з метиламіну, етиламіну, н-пропіламіну, н-бутиламіну, нпентиламіну тощо; - група "дизаміщений аміно", використовувана сама по собі або у поєднанні з іншими радикалами, позначає аміногрупу, заміщену двома радикалами, які можуть бути однаковими чи різними, вибраними з (C1-C6)алкільної, заміщеної алкільної, арильної, заміщеної арильної або арилалкільної групи, як визначено вище, краще, групи вибирають з диметиламіно, метилетиламіно, діетиламіно, фенілметиламіно тощо; - "ариламіно", використовуваний сам по собі або у поєднанні з іншими радикалами, позначає арильну групу, як визначено вище, приєднану через аміногрупу, що має вільний валентний зв'язок на атомі азоту, краще, групи вибирають з феніламіно, нафтиламіно, N-метиланіліно тощо; - "оксо" або "карбонільна" група, використовувана сама по собі (-C=O-) або у поєднанні з іншими радикалами, такими як алкіл, описаними вище, наприклад, "алкілкарбоніл", позначає карбонільний радикал (-C=O-), заміщений алкільним радикалом, описаним вище, такий як ацил або алканоїл; - група "карбонової кислоти", використовувана сама по собі або у поєднанні з іншими радикалами, позначає -COOH групу, та включає похідні карбонової кислоти, такі як складні ефіри та аміди; - "складноефірна" група, використовувана сама по собі або у поєднанні з іншими радикалами, позначає -COO- групу, та включає похідні карбонової кислоти, краще, 5 UA 113053 C2 складноефірні фрагменти вибирають з алкоксикарбонілу, такого як метоксикарбоніл, етоксикарбоніл тощо, які необов'язково можуть бути заміщені; арилоксикарбонільної групи, такої як феноксикарбоніл, нафтилоксикарбоніл тощо, які необов'язково можуть бути заміщені; аралкоксикарбонільної групи, такої як бензилоксикарбоніл, фенетилоксикарбоніл, нафтилметоксикарбоніл тощо, які необов'язково можуть бути заміщені; гетероарилоксикарбонілу, гетероаралкоксикарбонілу, де гетероарильна група є такою, як визначено вище, які необов'язково можуть бути заміщені; гетероциклілоксикарбонілу, де гетероциклічна група була визначена вище, який необов'язково може бути заміщеним; - "амідна" група, використовувана сама по собі або у поєднанні з іншими радикалами, позначає амінокарбонільний радикал (H2N-C=O), у якому аміногрупа є моно- або дизаміщеною чи незаміщеною, краще, групи вибирають з метиламіду, диметиламіду, етиламіду, діетиламіду тощо; - "амінокарбонільна" група, використовувана сама по собі або у поєднанні з іншими радикалами, може бути вибрана з амінокарбонілу, амінокарбонілалкілу, н- алкіламінокарбонілу, N-ариламінокарбонілу, Ν,Ν-діалкіламінокарбонілу, N-алкіл-N-ариламінокарбонілу, N-алкіл-Nгідроксиамінокарбонілу та N-алкіл-N-гідроксиамінокарбонілалкілу, кожен з яких є необов'язково заміщеним. Терміни N-алкіламінокарбоніл та Ν,Ν-діалкіламінокарбоніл позначають амінокарбонільні радикали, як визначено вище, які були заміщені одним алкільним радикалом та двома алкільними радикалами, відповідно. Кращим є "нижчий алкіламінокарбоніл", який має нижчі алкільні радикали, як описано вище, приєднані до амінокарбонільного радикала. Терміни "N-ариламінокарбоніл" та "N-алкіл-N-ариламінокарбоніл" позначають амінокарбонільні радикали, заміщені, відповідно, одним арильним радикалом, або одним алкільним та одним арильним радикалами. Термін "амінокарбонілалкіл" включає алкільні радикали, заміщені амінокарбонільними радикалами; - "гідроксіалкільну" групу, використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з алкільної групи, як визначено вище, заміщеної одним чи декількома гідроксильними радикалами, краще, групи вибирають з гідроксиметилу, гідроксіетилу, гідроксипропілу, гідроксибутилу, гідроксипентилу, гідроксигексилу тощо; - "аміноалкільна" група, використовувана сама по собі або у поєднанні з іншими радикалами, позначає фрагмент аміно (-NH2), приєднаний до алкільного радикала, як визначено вище, який може бути заміщеним, наприклад, моно- та дизаміщеним аміноалкілом. Термін "алкіламіно" у використовуваному тут значенні, сам по собі або у поєднанні з іншими радикалами, позначає алкільний радикал, як визначено вище, приєднаний до аміногрупи, яка може бути заміщеною, наприклад, моно- та дизаміщений алкіламіно; - "алкоксіалкільна" група, використовувана сама по собі або у поєднанні з іншими радикалами, позначає алкоксигрупу, як визначено вище, приєднану до алкільної групи, як визначено вище, краще, групи можуть бути вибрані з метоксиметилу, етоксиметилу, метоксіетилу, етоксіетилу тощо; - група "алкілтіо", використовувана сама по собі або у поєднанні з іншими радикалами, позначає лінійний або розгалужений або циклічний одновалентний замісник, який включає алкільну групу, як визначено вище, приєднаний через двовалентний атом сірки, що має вільний валентний зв'язок на атомі сірки, краще, групи можуть бути вибрані з метилтіо, етилтіо, пропілтіо, - "тіоалкільна" група, використовувана сама по собі або у поєднанні з іншими радикалами, позначає алкільну групу, як визначено вище, приєднану до групи формули -SR", where R" позначає водень, алкільну або арильну групу, наприклад, тіометил, метилтіометил, фенілтіометил тощо, які можуть бути необов'язково заміщеними. - групу "алкоксикарбоніламіно", використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з придатної алкоксикарбонільної групи, як визначено вище, приєднаної до аміногрупи, краще, метоксикарбоніламіно, етоксикарбоніламіно тощо; - група "арилтіо", використовувана сама по собі або у поєднанні з іншими радикалами, включає арильну групу, як визначено вище, приєднану через двовалентний атом сірки, що має вільний валентний зв'язок на атомі сірки, краще, групи можуть бути вибрані з фенілтіо, нафтилтіо, тетрагідронафтилтіо, індантіо, біфенілтіо тощо; - група "гетероциклілтіо", використовувана сама по собі або у поєднанні з іншими радикалами, включає гетероциклічну групу, як визначено вище, приєднану через двовалентний атом сірки, що має вільний валентний зв'язок на атомі сірки, краще, групи можуть бути вибрані з азиридинілтіо, азетидинілтіо, піролідинілтіо, імідазолідинілтіо, піперидинілтіо, піперазинілтіо, 2оксопіперидинілтіо, 4-оксопіперидинілтіо, 2-оксопіперазинілтіо, 3-оксопіперазинілтіо, морфолінілтіо, тіоморфолінілтіо, 2-оксоморфолінілтіо, азепінілтіо, діазепінілтіо, оксапінілтіо, 6 UA 113053 C2 тіазепінілтіо, оксазолідинілтіо, тіазолідинілтіо, дигідротіофентіо, дигідропірантіо, дигідрофурантіо, дигідротіазолтіо, бензопіранілтіо, бензопіранонілтіо, бензодигідрофуранілтіо, бензодигідротієнілтіо, піразолопіримідонілтіо, азахіназоліноїлтіо, тієнопіримідонілтіо, хіназолонілтіо, піримідонілтіо, бензоxазинілтіо, бензоксазинонілтіо, бензотіазинілтіо, бензотіазинонілтіо, тієнопіперидинілтіо, піридилтіо, тієнілтіо, фурилтіо, піролілтіо, оксазолілтіо, тіазолілтіо, ізотіазолілтіо, імідазолілтіо, ізоксазолілтіо, оксадіазолілтіо, тіадіазолілтіо, триазолілтіо, тетразолілтіо, бензофуранілтіо, бензотієнілтіо, індолінілтіо, індолілтіо, азаіндолілтіо, азаіндолінілтіо, піразолопіримідинілтіо, азахіназолінілтіо, піридофуранілтіо, піридотієнілтіо, тієнопіримідилтіо, хінолінілтіо, піримідинілтіо, піразолілтіо, хіназолінілтіо, піридазинілтіо, триазинілтіо, бензимідазолілтіо, бензотриазолілтіо, фталазинілтіо, нафтиридинілтіо, пуринілтіо, карбазолілтіо, фенотіазинілтіо, феноксазинілтіо, бензоксазолілтіо, бензотіазолілтіо тощо; - групу "алкоксикарбоніламіно", використовувану саму по собі або у поєднанні з іншими радикалами, вибирають з придатної алкоксикарбонільної групи, як визначено вище, приєднаної до аміногрупи, краще, метоксикарбоніламіно, етоксикарбоніламіно тощо; - групи "амінокарбоніламіно", "алкіламінокарбоніламіно", "діалкіламінокарбоніламіно", використовувані самі по собі або у поєднанні з іншими радикалами, позначають групу карбоніламіно (-CONH2), приєднану до аміно (NH2), алкіламіногрупи або діалкіламіногрупи, відповідно, де алкільна група є такою, як визначено вище; - група "амідино", використовувана сама по собі або у поєднанні з іншими радикалами, позначає радикал -C(=NH)-NH2; група "алкіламідино" позначає алкільний радикал, як описано вище, приєднаний до групи амідино; - група "алкоксиаміно", використовувана сама по собі або у поєднанні з іншими радикалами, позначає придатну алкоксигрупу, як визначено вище, приєднану до аміногрупи; - група "гідроксиаміно", використовувана сама по собі або у поєднанні з іншими радикалами, позначає фрагмент -NHOH і може бути необов'язково заміщеною придатними групами, вибраними з описаних вище; - "сульфенільна" група або "сульфенільні похідні", використовувані самі по собі або у поєднанні з іншими радикалами, позначають бівалентну групу -SO- або RxSO, де Rx є необов'язково заміщеною алкільною, арильною, гетероарильною, гетероциклічною групою, вибраною з описаних вище; - "сульфонільна" група або "сульфонові похідні", використовувані самі по собі або у поєднанні з іншими радикалами, з іншими термінами, такими як алкілсульфоніл, позначає двовалентний радикал -SO2- або RxSO2-, де Rx є таким, як визначено вище. Краще, групи можуть бути вибрані з "алкілсульфонілу", у якому придатні алкільні радикали, вибрані з визначених вище, приєднані до сульфонільного радикала, такого як метилсульфоніл, етилсульфоніл, пропілсульфоніл тощо, "арилсульфонілу", у якому арильний радикал, як визначено вище, приєднаний до сульфонільного радикала, такого як фенілсульфоніл тощо. - Термін "комбінована терапія" означає введення двох чи більше терапевтичних агентів для лікування терапевтичного стану або розладу, описаних в даному документі. Таке введення охоплює спільне введення цих терапевтичних агентів по суті одночасно, наприклад, в одній капсулі, що містить фіксоване співвідношення активних інгредієнтів, або в численних окремих капсулах для кожного активного інгредієнта. Крім того, таке введення також охоплює використання кожного типу терапевтичного агента у заданій послідовності. В будь-якому випадку, схема лікування буде забезпечувати корисні ефекти комбінації лікарських засобів при лікуванні станів або розладів, описаних тут. - Фраза "терапевтично ефективний" призначена для того, щоб охарактеризувати кількість активних інгредієнтів, використовуваних при лікуванні хвороби чи розладу. Ця кількість буде забезпечувати досягнення мети, що полягає у зменшенні чи усуненні зазначеної хвороби або розладу. - Термін "терапевтично прийнятний" стосується сполук (або солей, проліків, таутомерів, цвітеріонних форм і т.д.), які є придатними для використання у контакті з тканинами пацієнтів без надмірної токсичності, подразнення та алергічної реакції, мають відповідне розумне співвідношення користь/ризик, та ефективні при їх передбачуваному застосуванні. - У використовуваному тут значенні, посилання на "лікування" пацієнта має включати профілактику. Термін "пацієнт" означає усіх ссавців, включаючи людей. Приклади пацієнтів включають людей, велику рогату худобу, собак, кішок, кіз, овець, свиней та кролів. Краще, пацієнт є людиною. Придатні групи та замісники на групах можуть бути вибрані з описаних будь-де в даному описі винаходу. 7 UA 113053 C2 Особливо корисні сполуки можуть бути вибрані з: N-((тетрагідро-2H-піран-4-іл)метил)-2-(4-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)феноксі)ацетаміду; N-((тетрагідро-2H-піран-4-іл)метил)-2-((5-(1-(((4(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)оксі)ацетаміду; N-((тетрагідро-2H-піран-4-іл)метил)-2-((5-(1-(((4(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)аміно)ацетаміду; N-((тетрагідро-2H-піран-4-іл)метил)-2-((4-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)феніл)аміно)ацетаміду; 2,2'-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)етил)оксазол-2-іл)азанедіїл)біс(N((тетрагідро-2H-піран-4-іл)метил)ацетаміду); N-((тетрагідро-2H-піран-4-іл)метил)-2-((1-(4-(трифторметил)бензил)-3-((((4(трифторметил)бензил)оксі)іміно)метил)-1H-indol-5-іл)оксі)ацетаміду; 2-(2-метил-4-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро2H-піран-4-іл)метил)ацетаміду; 2-(4-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2H-піран4-іл)метил)ацетаміду; 2-(4-(2-феніл-1-(((3-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2H-піран4-іл)метил)ацетаміду; 2-(4-(2-(піридин-4-іл)-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро2H-піран-4-іл)метил)ацетаміду; 2-(4-(2-морфоліно-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетаміду; N-((тетрагідро-2H-піран-4-іл)метил)-2-(4-(2-тіоморфоліно-1-(((4(трифторметил)бензил)оксі)іміно)етил)феноксі)ацетаміду; 2-(2-метил-4-(2-(тіофен-3-іл)-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N((тетрагідро-2H-піран-4-іл)метил)ацетаміду; N-((тетрагідро-2H-піран-4-іл)rnетил)-2-(4-((((4(трифторметил)бензил)оксі)іміно)метил)феноксі)ацетаміду; N-((тетрагідро-2H-піран-4-іл)метил)-2-(4-(1-(((4(трифторметил)бензил)оксі)іміно)етил)феноксі)ацетаміду; N-((тетрагідро-2H-піран-4-іл)метил)-2-((5-((((4(трифторметил)бензил)оксі)іміно)метил)піридин-2-іл)оксі)ацетаміду; N-((тетрагідро-2H-піран-4-іл)метил)-2-((4-(1-(((4(трифторметил)бензил)оксі)іміно)етил)феніл)аміно)ацетаміду; 2-((5-(1-(((4-ціанобензил)оксі)іміно)етил)піридин-2-іл)окси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; N-((тетрагідро-2H-піран-4-іл)метил)-2-((5-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)піридин-2-іл)оксі)ацетаміду; N-((тетрагідро-2H-піран-4-іл)метил)-2-((5-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)піридин-2-іл)аміно)ацетаміду; 2-((5-(1-((бензилоксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро2H-піран-4іл)метил)ацетаміду; 2-((5-(1-(((4-метилбензил)оксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-((5-(1-(((4-метоксибензил)оксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-((5-(1-(((4-фторбензил)оксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-((5-(1-(((4-ціанобензил)оксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-(2-метил-4-(1-(((4-(трифторметил)бензил)оксі)іміно)бутил)фенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетаміду; 2-(4-(2-метокси-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетаміду; 2-(4-(2-гідрокси-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетамід; 2-(2-метил-4-(I-(((4-метилбензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 8 UA 113053 C2 2-(4-(1-(((4-метилбензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-(4-(1-(((4-фторбензил)оксі)іміно)-2-фенілетил)-2-rnетилфенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-(4-(1-(((4-фторбензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-(4-(1-(((4-хлорбензил)оксі)іміно)-2-фенілетил)-2-метилфенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-(4-(1-(((4-хлорбензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-(2-метил-4-(2-феніл-1-(((4-(трифторметокси)бензил)оксі)іміно)етил)фенокси)-N((тетрагідро-2H-піран-4-іл)метил)ацетаміду; 2-(4-(2-феніл-1-(((4-(трифторметокси)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетаміду; 2-(4-(1-(((4-метоксибензил)оксі)іміно)-2-фенілетил)-2-метилфенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетаміду; 2-(4-(1-(((4-метоксибензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-(4-(1-(((4-(метилсульфоніл)бензил)оксі)іміно)пропіл)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-(4-(2-феніл-1-((піридин-2-ілметоксі)іміно)етил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-(4-(1-((2-(1H-індол-1-іл)етоксі)іміно)пропіл)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-(4-(1-(((5-етилпіримідин-2-іл)оксі)іміно)пропіл)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-(4-(1-(((5-метил-2-фенілоксазол-4-іл)метоксі)іміно)пропіл)фенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетаміду; 2-(4-(1-(((3-(трет-бутил)-1-(п-толіл)-1H-піразол-5-іл)метоксі)іміно)пропіл)фенокси)-N((тетрагідро-2H-піран-4-іл)метил)ацетаміду; N-((тетрагідро-2H-піран-4-іл)метил)-2-((5-(((4-(трифторметил)бензил)оксі)іміно)-5,6,7,8тетрагідронафталін-2-іл)оксі)ацетаміду; 2-((5-(((4-хлорбензил)оксі)іміно)-5,6,7,8-тетрагідронафталін-2-іл)окси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетаміду; 2-((5-(((4-ціанобензил)оксі)іміно)-5,6,7,8-тетрагідронафталін-2-іл)окси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетаміду; 2-((5-(((4-метоксибензил)оксі)іміно)-5,6,7,8-тетрагідронафталін-2-іл)окси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетаміду; метил-3-((((6-(2-оксо-2-(((тетрагідро-2H-піран-4-іл)метил)аміно)етокси)-3,4-дигідронафталін1(2H)-іліден)аміно)окси)метил)бензоату; N-((тетрагідро-2H-піран-4-іл)метил)-2-((5-(1-(((4(трифторметил)бензил)оксі)іміно)етил)хінолін-8-іл)оксі)ацетаміду; 2-метил-N-((тетрагідро-2H-піран-4-іл)метил)-2-(4-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)фенокси)пропанаміду; 2-метил-N-((тетрагідро-2H-піран-4-іл)метил)-2-(4-(1-(((4(трифторметил)бензил)оксі)іміно)етил)фенокси)пропанаміду; 2-(4-(1-(((тетрагідро-2H-піран-4-іл)метоксі)іміно)етил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-(4-(1-((циклогексилметоксі)іміно)етил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-(4-(1-((нафталін-2-ілметоксі)іміно)етил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетаміду; 2-((5-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)окси)-N-((тетрагідро2H-піран-4-іл)метил)ацетаміду; 2-((5-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)аміно)-N((тетрагідро-2H-піран-4-іл)метил)ацетаміду; N-((тетрагідро-2H-піран-4-іл)метил)-2-((3-((((4-(трифторметил)бензил)оксі)іміно)метил)-1Hіндол-5-іл)оксі)ацетаміду; N-((тетрагідро-2H-піран-4-іл)метил)-2-((3-(1-(((4-(трифторметил)бензил)оксі)іміно)етил)-1Hіндол-5-іл)оксі)ацетаміду; 9 UA 113053 C2 N-((тетрагідро-2H-піран-4-іл)метил)-2-((3-(1-(((4-(трифторметил)бензил)оксі)іміно)пропіл)-1Hіндол-5-іл)оксі)ацетаміду; 2-((3-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)-1H-індол-5-іл)окси)-N((тетрагідро-2H-піран-4-іл)метил)ацетаміду; N-((тетрагідро-2H-піран-4-іл)метил)-3-(5-(1-(((4(трифторметил)бензил)оксі)іміно)етил)піримідин-2-іл)пропанаміду; N-((тетрагідро-2H-піран-4-іл)метил)-3-(5-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)піримідин-2-іл)пропанаміду; 3-(5-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піримідин-2-іл)-N-((тетрагідро-2Hпіран-4-іл)метил)пропанаміду; N-((тетрагідро-2H-піран-4-іл)метил)-2-((5-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)хінолін-8-іл)оксі)ацетаміду; 2-((5-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)хінолін-8-іл)окси)-N-((тетрагідро2H-піран-4-іл)метил)ацетаміду; Даний винахід також розкриває певні нові проміжні сполуки, придатні для одержання сполук формули (I). Конкретніше, даний винахід розкриває: 2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)оксі)оцтову кислоту; 2,2'-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)етил)оксазол-2-іл)азанедіїл)діоцтову кислоту; 2-((1-(4-(трифторметил)бензил)-3-((((4-(трифторметил)бензил)оксі)іміно)метил)-1H-індол-5іл)оксі)оцтову кислоту; 2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)етил)хінолін-8-іл)оксі)оцтову кислоту; 2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)аміно)оцтову кислоту; 2-((5-((((4-(трифторметил)бензил)оксі)іміно)метил)піридин-2-іл)оксі)оцтову кислоту; 2-((5-(1-(((4-ціанобензил)оксі)іміно)етил)піридин-2-іл)оксі)оцтову кислоту; 2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)пропіл)піридин-2-іл)оксі)оцтову кислоту; 2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)пропіл)піридин-2-іл)аміно)оцтову кислоту; 2-((5-(1-((бензилоксі)іміно)пропіл)піридин-2-іл)оксі)оцтову кислоту; 2-((5-(1-(((4-метилбензил)оксі)іміно)пропіл)піридин-2-іл)оксі)оцтову кислоту; 2-((5-(1-(((4-метоксибензил)оксі)іміно)пропіл)піридин-2-іл)оксі)оцтову кислоту; 2-((5-(1-(((4-фторбензил)оксі)іміно)пропіл)піридин-2-іл)оксі)оцтову кислоту; 2-((5-(1-(((4-ціанобензил)оксі)іміно)пропіл)піридин-2-іл)оксі)оцтову кислоту; 2-((5-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)оксі)оцтову кислоту; 2-((5-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)аміно)оцтову кислоту; 2-((3-((((4-(трифторметил)бензил)оксі)іміно)метил)-1H-індол-5-іл)оксі)оцтову кислоту; 2-((3-(1-(((4-(трифторметил)бензил)оксі)іміно)етил)-1H-індол-5-іл)оксі)оцтову кислоту; 2-((3-(1-(((4-(трифторметил)бензил)оксі)іміно)пропіл)-1H-індол-5-іл)оксі)оцтову кислоту; 2-((3-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)-1H-індол-5-іл)оксі)оцтову кислоту; 3-(5-(1-(((4-(трифторметил)бензил)оксі)іміно)етил)піримідин-2-іл)пропіонову кислоту; 3-(5-(1-(((4-(трифторметил)бензил)окси)iraino)пропіл)піримідин-2-іл)пропіонову кислоту; 3-(5-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піримідин-2-іл)пропіонову кислоту; 2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)пропіл)хінолін-8-іл)оксі)оцтову кислоту; 2-((5-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)хінолін-8-іл)оксі)оцтову кислоту. Нові сполуки за даним винаходом можуть бути одержані з використанням реакцій та методик, зображених на схемі нижче та описаних в даному розділі. Реакції проводять у розчинниках, придатних для роботи з використовуваними реагентами та матеріалами та для здійснюваних перетворень. Кваліфікованим фахівцям в цій області техніки зрозуміло, що природа та порядок наведених стадій синтезу можуть змінюватися з метою оптимізації утворення сполук за даним винаходом. Також добре зрозуміло, що один чи декілька реагентів можуть бути захищені та звільнені від захисту для спрощення синтезу методами, відомими кваліфікованим фахівцям. Слід також розуміти, що одна чи декілька сполук за даним винаходом можуть існувати у стереоізомерній та/або діастереомерній формах. Такі стереоізомери та/або діастереоізомери, а також їх оптичні антиподи повинні вважатися такими, що входять до складу даного винаходу. Також має бути зрозуміло, що одна чи декілька цих сполуки можуть бути перетворені на їх солі та інші похідні в залежності від конкретних груп, присутніх у сполуках, як добре відомо кваліфікованим фахівцям. Такі солі та/або інші похідні, залежно від обставин, також повинні вважатися такими, що входять до обсягу даного винаходу. 10 UA 113053 C2 Схема I: Сполуки загальної формули (I), у яких усі символи мають вказані вище значення, можуть бути одержані за допомогою реакцій, указаних на схемі I нижче, яка включає: i. Сполуки загальної формули VI, у якій R6 позначає C1-C6 лінійний чи розгалужений алкіл або аралкіл, і решта символів мають вказані вище значення, можуть бути одержані шляхом сполучення сполук загальної формули II, у якій всі символи мають вказані вище значення, та сполуки загальної формули IV, де L позначає придатну відхідну групу, і решта символів мають вказані вище значення, з використанням придатної основи та придатного реакційного середовища, за допомогою способів, доступних з літератури для стандартної реакції нуклеофільного заміщення; ii.. Альтернативно, сполуки загальної формули VI, у якій всі символи були визначені вище, можуть бути одержані шляхом сполучення сполук формули III, у якій усі символи мають вказані вище значення, та сполук загальної формули V, у якій решта символів були визначені, з використанням придатної основи та придатного реакційного середовища, за допомогою способів, доступних з літератури для стандартної реакції нуклеофільного заміщення; iii. Сполуки загальної формули VII, у якій усі символи мають вказані вище значення, можуть бути одержані шляхом проведення реакції сполук загальної формули VI, у якій усі символи мають вказані вище значення, з гідроксиламіну гідрохлоридом в присутності придатної основи та придатних розчинників; iv. Сполуки формули IX, у якій всі символи мають вказані вище значення, можуть бути одержані шляхом сполучення сполук формули VII, у якій усі символи мають вказані вище значення, та сполук загальної формули VIII, у якій L позначає придатну відхідну групу і решта символів мають вказані вище значення, з використанням придатної основи та придатного реакційного середовища; v. Сполуки загальної формули X, у якій усі символи мають вказані вище значення, можуть бути одержані шляхом гідролізу сполук загальної формули IX, у якій усі символи мають вказані вище значення, в придатних умовах; vi. Сполуки формули (I), у якій усі символи мають вказані вище значення, можуть бути одержані шляхом сполучення сполук формули X, у якій всі символи мають вказані вище значення, та (тетрагідро-2H-піран-4-іл)метанаміну (XI), де всі символи є такими, як визначено, з використанням придатних способів, доступних з літератури, для стандартного пептидного сполучення; 11 UA 113053 C2 Схема 2: Альтернативно, сполуки загальної формули (I), у якій усі символи мають вказані вище значення, можуть бути одержані за допомогою реакцій, указаних на схемі 2 нижче, яка включає: i. Сполуки загальної формули XII, у якій усі символи мають вказані вище значення, можуть бути одержані шляхом гідролізу сполук загальної формули VI, у якій усі символи мають вказані вище значення, в придатних умовах; ii. Сполуки формули XIII, у якій усі символи мають вказані вище значення, можуть бути одержані шляхом сполучення сполук формули XII, у якій всі символи є такими, як визначено вище, та (тетрагідро-2H-піран-4-іл)метанаміну (XI), де усі символи мають вказані вище значення, за допомогою придатних способів, доступних з літератури, для стандартного пептидного сполучення; iii. Сполуки загальної формули XIV, у якій всі символи мають вказані вище значення, можуть бути одержані шляхом проведення реакції сполук загальної формули XIII, у якій всі символи мають вказані вище значення, з гідроксиламіну гідрохлоридом в присутності придатної основи та придатних розчинників; iv. Сполуки формули (I), у якій усі символи мають вказані вище значення, можуть бути одержані шляхом сполучення сполук формули XIV, у якій усі символи мають вказані вище значення, та сполук загальної формули VIII, у якій усі символи є такими, як визначено вище, з використанням придатної основи та придатного реакційного середовища. Метод A: Сполуки формули VI, IX та (I), у якій усі символи мають вказані вище значення, можуть бути одержані з придатних вихідних матеріалів, як вказано на Схемі 1 та Схемі 2, з використанням придатної неорганічної основи (основ), такої як NaOH, KOH, K2CO3, Cs2CO3 тощо, або органічної основи (основ), такої як піридин, триетиламін, діізопропілетиламін тощо. Реакція може бути проведена без розведення або в присутності придатного протонного розчинника (розчинників), такого як метанол, етанол, бутанол тощо, або придатного апротонного розчинника (розчинників), такого як диметилформамід, тетрагідрофуран, дихлорметан тощо, або їх придатних сумішей. Реакція може бути проведена при температурі в інтервалі від 0 °C до температури кипіння зі зворотним холодильником використовуваного розчинника (розчинників), і час реакції може становити від 1 до 48 годин. Метод B: Сполуки формули VI, у якій усі символи мають вказані вище значення, можуть бути одержані з використанням придатних вихідних матеріалів, як вказано на схемі I, із застосуванням придатної неорганічної основи (основ), такої як NaOH, KOH, K2CO3, Cs2CO3 тощо, або придатної органічної основи (основ), такої як піридин, триетиламін, діізопропілетиламін тощо. Альтернативно, сполуки формули VI, у якій усі символи мають вказані вище значення, також можуть бути одержані шляхом використання придатного каталізатора на основі паладію, такого як ацетат паладію, Pd(Ph3P)4 тощо, та з органічним лігандом, таким як BINAP тощо, чи без нього. Реакція може бути проведена без розведення або в присутності придатного протонного розчинника (розчинників), такого як метанол, етанол, бутанол тощо, або придатного апротонного розчинника (розчинників), такого як диметилформамід, толоул, тетрагідрофуран, дихлорметан тощо, або їх сумішей. Реакція може бути проведена при температурі в інтервалі від 0 °C до температури кипіння зі зворотним холодильником використовуваного розчинника (розчинників), а час реакції може змінюватися від 1 до 48 годин. 12 UA 113053 C2 Метод C: Сполуки формул VII та XIV, у яких усі символи мають вказані вище значення, можуть бути одержані шляхом проведення реакції придатних кетонів, як показано на Схемі 1 та Схемі 2, з гідроксиламіну гідрохлоридом в присутності основи (основ), такої як NaOH, NaOAc, піридин тощо. Реакція може бути проведена в присутності придатного розчинника (розчинників), такого як метанол, етанол, бутанол, вода тощо, або їх придатних сумішей. Реакція може бути проведена при температурі в інтервалі від 0 °C до температури кипіння зі зворотним холодильником використовуваного розчинника (розчинників), а час реакції може складати від 1 до 48 годин. Метод D: Сполуки формул X та XII, у яких усі символи мають вказані вище значення, можуть бути одержані шляхом гідролізу відповідних складних ефірів, як показано на Схемі 1 та Схемі 2, з використанням придатної основи (основ), наприклад, NaOH, LiOH, KOH тощо. Реакція може бути проведена у придатному розчиннику (розчинниках), такому як метанол, етанол, ТГФ, вода тощо, або їх сумішах. Реакція може бути проведена при температурі в інтервалі від 20 °C до температури кипіння зі зворотним холодильником використовуваного розчинника (розчинників), а час реакції може складати від 1 до 48 годин. Метод E: Сполуки формул (I) та XIII, у яких усі символи мають вказані вище значення, можуть бути одержані за реакцією сполучення придатної кислоти та придатного аміну, як показано на Схемі 1 та Схемі 2, в придатних умовах, таких як описані у Tetrahedron, 2005, 61(46), 10827-10852, з придатними модифікаціями та змінами, як добре відомо кваліфікованому фахівцю. Реакція може бути проведена в присутності реагенту (реагентів), такого як N-(3диметиламінопропіл)-N'- етилкарбодііміду гідрохлорид (EDCl) та 1-гідроксибензотриазол (HOBT)тощо. Реакція може бути проведена у придатному розчиннику (розчинниках), такому як диметилформамід, тетрагідрофуран, дихлорметан тощо, або їх сумішах. Реакція може бути проведена при температурі в інтервалі від 0 °C до температури кипіння зі зворотним холодильником використовуваного розчинника (розчинників), а час реакції може становити від 1 до 48 годин. Фармацевтична композиція забезпечується шляхом використання звичайних методик. Краще, композиція має вигляд дозованої лікарської форми, що містить ефективну кількість активного компонента, тобто, сполуки формули (I) відповідно до даного винаходу. Кількість активного компонента, тобто, сполуки формули (I) відповідно до даного винаходу, у фармацевтичній композиції та її дозованій лікарській формі може змінюватися чи регулюватися у широких межах в залежності від конкретного способу застосування, активності конкретної сполуки та бажаної концентрації. Загалом, кількість активного компонента буде знаходитися в інтервалі значень від 0,5 % до 90 % від ваги композиції. Винахід пояснюється більш детально у наведених нижче прикладах, які приводяться лише для ілюстрації і тому не повинні тлумачитися як такі, що обмежують обсяг винаходу. Спектральні дані 1H ЯМР, представлені у прикладах (див. нижче) були зареєстровані за допомогою 400 МГц спектрометра (Bruker AVANCE-400) та наводяться за шкалою δ. Якщо не зазначене інше, то розчинником, використовуваним для ЯМР, є CDCl3, з використанням тетраметилсилану як внутрішнього стандарту. Приклад 1 N-((Тетрагідро-2H-піран-4-іл)метил)-2-(4-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)феноксі)ацетамід Стадія 1: Етил-2-(4-пропіонілфеноксі)ацетат До розчину 1-(4-гідроксифеніл)пропан-1-ону (33 г, 0,2200 моль) в ДМФ (165 мл) додавали карбонат калію (60,7 г, 0,4400 моль) та етилбромацетат (40,6 г, 0,2420 моль) та реакційну суміш перемішували при 50 °C протягом 3 годин. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 49 г (94 %) продукту у вигляді в'язкої рідини. 1H ЯМР: ДМСО-d6 δ 1,06 (т, J=7,2 Гц, 3H), 1,20 (т, J=4,8 Гц, 3H), 2,96 (кв, J=7,4 Гц, 2H), 4,14 (кв, J=3,6 Гц, 2H), 4,88 (с, 2H), 7,02 (дд, J=2,0 та 6,8 Гц, 2H), 7,92 (дд, J=2,0 та 6,8 Гц, 2H). Стадія 2: Етил-2-(4-(1-(гідроксііміно)пропіл)феноксі)ацетат До розчину продукту стадії 1 (49 г, 0,2076 моль) в метанолі (343 мл), додавали гідроксиламіну гідрохлорид (28,6 г, 0,4152 моль) та розчин ацетату натрію (34 г, 0,4152 моль) у воді (147 мл) і реакційну суміш нагрівали до кипіння зі зворотним холодильником протягом 1 години. Розчинники випарювали при зниженому тиску. Залишок розчиняли у воді та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 40 г (76 %) продукту у вигляді твердої речовини. 13 UA 113053 C2 1H ЯМР: ДМСО-d6 δ 1,01 (т, J=7,4 Гц, 3H), 1,21 (т, J=7,0 Гц, 3H), 2,66 (кв, J=7,6 Гц, 2H), 4,16 (кв, J=7,2 Гц, 2H), 4,79 (с, 2H), 6,93 (дд, J=5,2 та 2,8 Гц, 2H), 7,56 (дд, J=6,8 та 2,0 Гц, 2H), 10,93 (с, 1H). Стадія 3: Етил-2-(4-(1-(((4-(трифторметил)бензил)оксі)іміно)пропіл)феноксі)ацетат До розчину продукту стадії 2 (18 г, 0,0723 моль) в ДМФ (54 мл) додавали карбонат цезію (47 г, 0,1446 моль) та 4-(трифторметил)бензилбромід (19 г, 0,0795 моль) і реакційну суміш перемішували при 25 °C протягом 3 годин. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 28 г (95 %) продукту у вигляді в'язкої рідини. 1H ЯМР: ДМСО-d6 δ 1,05 (т, J=7,4 Гц, 3H), 1,19 (т, J=7,0 Гц, 3H), 2,73 (кв, J=7,6 Гц, 2H), 4,16 (кв, J=7,2 Гц, 2H), 4,80 (с, 2H), 5,26 (с, 2H), 6,93 (дд, J=7,2 та 2,4 Гц, 2H), 7,56 (дд, J=6,8 та 2,0 Гц, 2H), 7,59 (д, J=8,0 Гц, 2H), 7,72 (д, J=8,0 Гц, 2H). Стадія 4: 2-(4-(1-(((4-(Трифторметил)бензил)оксі)іміно)пропіл)феноксі)оцтова кислота До розчину продукту стадії 3 (28 г, 0,0683 моль) у ТГФ (140 мл) додавали розчин гідроксиду літію (4,3 г, 0,1024 моль) у воді (140 мл) і реакційну суміш перемішували при 25 °C протягом 3 годин. Розчинники випарювали при зниженому тиску. Залишок розчиняли у воді, підкислювали 1N HCl та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 23 г (88 %) продукту у вигляді твердої речовини. 1H ЯМР: ДМСО-d6 δ 1,05 (т, J=7,4 Гц, 3H), 2,73 (кв, J=7,4 Гц, 2H), 4,69 (с, 2H), 5,26 (с, 2H), 6,92 (дд, J=2 та 6,8 Гц, 2H), 7,55 (дд, J=2,4 та 7,2 Гц, 2H), 7,59 (д, J=8 Гц, 2H), 7,72 (д, J=8 Гц, 2H). Стадія 5: N-((Тетрагідро-2H-піран-4-іл)метил)-2-(4-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)феноксі)ацетамід До розчину продукту стадії 4 (23 г, 0,0602 моль) в ДМФ (69 мл) додавали (тетрагідро-2Hпіран-4-іл)метанамін (7,6 г, 0,0662 моль), HOBT (50 мг, каталітична кількість), EDC∙HCl (17,5 г, 0,0903 моль) та DMAP (50 мг, каталітична кількість) і реакційну суміш перемішували при 25 °C протягом 16 годин. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску. Сировий продукт очищали хроматографією на колонці, використовуючи етилацетат: гексан (1:1) як елюент, одержуючи 16,5 г (57 %) продукту у вигляді білої твердої речовини. 1H ЯМР: ДМСО-d6 δ 1,10 (т, J=6,6 Гц, 3H), 1,13-1,16 (м, 2H), 1,46-1,49 (м, 2H), 1,61-1,70 (м, 1H), 2,74 (кв, J=7,6 Гц, 2H), 3,01 (т, J=6,6 Гц, 2H), 3,17-3,23 (м, 2H), 3,78-3,81 (дд, J=11,4 та 2,6 Гц, 2H), 4,51 (с, 2H), 5,26 (с, 2H), 6,96 (дд, J=6,8 та 2,0 Гц, 2H), 5,57-5,61 (м, 4H), 7,72 (д, J=8,0 Гц, 2H), 8,10 (т, J=6,0 Гц, NH). Приклад 2 2-((5-(1-(((4-(Трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)оксі)оцтова кислота Стадія 1: Етил-2-((5-ацетилпіридин-2-іл)оксі)ацетат До розчину 1-(6-хлорпіридин-3-іл)етанону (4,0 г, 0,0257 моль) в ДМФ (15 мл) додавали карбонат цезію (16,8 г, 0,051 моль), а потім додавали метил-2-гідроксіацетат (8,0 мл, 0,103 ммоль) при 25 °C під атмосферою азоту і реакційну суміш перемішували при 80-90 °C протягом 18 год. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску. Сировий продукт очищали хроматографією на колонці (елюент: 16 % етилацетату в гексані), одержуючи 1,25 г (23 %) продукту у вигляді білуватої твердої речовини. 1H ЯМР: ДМСО-d6 δ 2,55 (с, 3H), 3,67 (с, 3H), 5,02 (с, 2H), 7,04 (дд, J=8,8 та 0,4 Гц, 1H), 8,20 (дд, J=8,8 та 2,4 Гц, 1H), 8,78 (д, J=2,0 Гц, 1H). Стадія 2: Метил-2-((5-(1-(гідроксііміно)етил)піридин-2-іл)оксі)ацетат До розчину метил-2-((5-ацетилпіридин-2-іл)оксі)ацетату (1,23 г, 0,059 моль) в етанолі (10 мл) додавали розчин ацетату натрію (0,942 г, 0,0117 моль) та гідроксиламонію хлорид (1,2 г, 0,0117 моль) у воді (5 мл) і реакційну суміш нагрівали до кипіння зі зворотним холодильником протягом 1 год. Реакційну суміш охолоджували до кімнатної температури та розчинник випаровували під вакуумом. Залишок розводили охолодженою льодом водою і тверду речовину, що утворилася, фільтрували, промивали водою та осушали над P2O5 під вакуумом, одержуючи 1,15 г (88 %) названого у заголовку продукту у вигляді білуватої твердої речовини. 1H ЯМР: ДМСО-d6 δ 2,12 (с, 3H), 3,66 (с, 3H), 4,94 (с, 2H), 6,95 (д, J=8,8 Гц, 1H), 8,02 (дд, J=8,4 та 2,4 Гц, 1H), 8,34 (д, J=2,0 Гц, 1H). 14 UA 113053 C2 Стадія 3: Метил-2-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)оксі)ацетат До розчину 1-(бромметил)-4-(трифторметил)бензолу (0,87 мл, 5,6 ммоль) в ДМФ (10 мл) додавали карбонат цезію (3,35 г, 10,2 ммоль), після чого додавали метил-2-((5-(1(гідроксііміно)етил)піридин-2-іл)оксі)ацетат (1,15 г, 5,1 ммоль) при 25 °C під атмосферою азоту і реакційну суміш перемішували при такій саме температурі протягом 12 год. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 2,0 г (94 %) продукту у вигляді в'язкої рідини. 1H ЯМР: ДМСО-d6 δ 2,24 (с, 3H), 3,65 (с, 3H), 4,94 (с, 2H), 5,29 (с, 2H), 6,94 (д, J=8,8 Гц, 1H), 7,60 (д, J=8,0 Гц, 2H), 7,73 (д, J=8,0 Гц, 2H), 8,00 (дд, J=8,8 та 2,4 Гц, 1H), 8,36 (д, J=2,4 Гц, 1H). Стадія 4: 2-((5-(1-(((4-(Трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)оксі)оцтову кислоту До розчину продукту стадії 3 (2,0 г, 5,2 ммоль) у суміші ТГФ (12 мл), метанолу (4 мл) та води (4 мл) додавали гідроксид літію (440 мг, 10,5 ммоль) і реакційну суміш перемішували при ambient температура протягом 4 годин. Розчинники випарювали при зниженому тиску. Залишок розчиняли у воді, підкислювали 1N HCl та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 1,7 г (88 %) названого у заголовку продукту у вигляді білої твердої речовини. 1H ЯМР: ДМСО-d6 δ 2,24 (с, 3H), 4,84 (с, 2H), 5,29 (с, 2H), 6,93 (д, J=8,8 Гц, 1H), 7,60 (д, J=8,0 Гц, 2H), 7,73 (д, J=8,0 Гц, 2H), 7,98 (дд, J=8,8 та 2,8 Гц, 1H), 8,36 (д, J=2,4 Гц, 1H). Приклад 3 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((5-(1-(((4(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)оксі)ацетамід До розчину сполуки, одержаної у прикладі 3 (2,0 г, 5,43 ммоль) в ДМФ (10 мл) додавали (тетрагідро-2H-піран-4-іл)метанамін (625 мг, 5,43 ммоль), HOBT (1,09 г, 8,14 ммоль), EDC∙HCl (1,25 г, 6,52 ммоль) та N-етилморфолін (2,05 мл, 16,29 ммоль) і реакційну суміш перемішували при 25 °C протягом 5 годин під атмосферою азоту. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску. Сировий продукт тритурували з гексаном, одержуючи 2,8 г (72 %) продукту у вигляді білої твердої речовини. 1H ЯМР: ДМСО-d6 δ 1,07-1,11 (м, 2Η), 1,45-1,49 (м, 2Η), 1,58-1,64 (м, 1H), 2,24 (с, 3Η), 2,96 (т, J=6,8 Гц, 2Η), 3,17-3,23 (м, 2Η), 3,22 (дд, J=11,4 та 2,6 Гц, 2Η), 4,72 (с, 2H), 5,29 (с, 2H), 6,91 (д, J=8,8 Гц, 1H), 7,60 (д, J=8,0 Гц, 2H) 7,72 (д, J=8,0 Гц, 2H), 7,98-7,99 (м, 1H), 8,33 (д, J=2,0 Гц, 1H). Приклад 4 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((5-(1-(((4(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)аміно)ацетамід Стадія 1: Етил-2-((5-ацетилпіридин-2-іл)аміно)ацетат До суміші 1-(6-амінопіридин-3-іл)етанону (700 мг, 5,15 ммоль) та перхлорної кислоти (1,4 мл) додавали розчин гліоксалю (0,24 мл, 5,15 ммоль) в метанолі (14 мл) і реакційну суміш нагрівали до кипіння зі зворотним холодильником протягом 48 год. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску. Сировий продукт очищали хроматографією на колонці (елюент: 1,5 % метанолу у хлороформі), одержуючи 350 мг (33 %) продукту у вигляді білуватої твердої речовини. 1H ЯМР: ДМСО-d6 δ 2,43 (с, 3H), 3,63 (с, 3H), 4,12 (д, J=6,0 Гц, 2H), 6,62 (дд, J=8,8 Гц, 1H), 7,86 (дд, J=8,8 та 2,4 Гц, 1H), 8,34 (д, J=2,0 Гц, 1H). Стадія 2: 2-((5-Ацетилпіридин-2-іл)аміно)оцтова кислота До розчину продукту стадії 1 (1,1 г, 5,3 ммоль) у суміші ТГФ (12 мл), метанолу (4 мл) та води (4 мл) додавали гідроксид літію (444 мг, 10,6 ммоль) і реакційну суміш перемішували при температурі навколишнього середовища протягом 4 годин. Розчинники випарювали при зниженому тиску. Залишок розчиняли у воді, підкислювали 1N HCl та випаровували під вакуумом. Залишок розводили етилацетатом, перемішували протягом 30 хв. та фільтрували. Фільтрат концентрували під вакуумом, одержуючи 1,0 г (98 %) названого у заголовку продукту у вигляді білуватої твердої речовини. 1H ЯМР: CD3OD: δ 2,48 (с, 3H), 4,08 (с, 2H), 6,59 (дд, J=8,8 Гц, 1H), 7,86 (дд, J=8,8 та 2,0 Гц, 1H), 8,65 (д, J=2,4 Гц, 1H). Стадія 3: N-((Тетрагідро-2H-піран-4-іл)метил)-2-((5-(1-(((4(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)аміно)ацетамід 15 UA 113053 C2 До розчину продукту стадії 2 (1,4 г, 7,2 ммоль) в ДМФ (10 мл) додавали (тетрагідро-2H-піран4-іл)метанамін (1,2 г, 7,94 ммоль), HOBT (1,48 г, 10,8 ммоль), EDC∙HCl (1,16 г, 8,66 ммоль) та Nетилморфолін (2,75 мл, 21,6 ммоль) і реакційну суміш перемішували при 25 °C протягом 2 годин під атмосферою азоту. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 1,0 г сирового продукту у вигляді маслянистої рідини. Сировий продукт розчиняли в етанолі (10 мл) і додавали розчин ацетату натрію (0,564 г, 6,8 ммоль) та гідроксиламонію хлориду (0,615 г, 6,8 ммоль) у воді (5 мл) і реакційну суміш нагрівали до кипіння зі зворотним холодильником протягом 1 год. Реакційну суміш охолоджували до кімнатної температури та розчинник випаровували під вакуумом. Залишок розводили охолодженою льодом водою та екстрагували етилацетатом. Етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випаровували під вакуумом, одержуючи 420 мг продукту у вигляді маслянистої рідини. До розчину одержаного вище продукту (450 мг, 1,47 ммоль) в ДМФ (5 мл) додавали карбонат цезію (959 мг, 2,94 ммоль), а потім додавали 1-(бромметил)-4-(трифторметил)бензол (350 мг, 1,47 ммоль) при 25 °C під атмосферою азоту і реакційну суміш перемішували при такій саме температурі протягом 12 год. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт was промивали водою та розсолом, осушали над сульфатом натрію і випарювали при зниженому тиску, одержуючи 135 мг (58 %) продукту у вигляді білуватої твердої речовини. 1H ЯМР: ДМСО-d6 δ 1,22-1,25 (м, 2H), 1,47-1,50 (м, 2H), 1,57-1,62 (м, 1H), 2,17 (с, 3H), 2,95 (т, J=6,4 Гц, 2H), 3,16-3,22 (м, 2H), 3,78-3,81 (дд, J=2,8 та 11,2 Гц, 2H), 3,85 (д, J=6,0 Гц, 2H), 5,23 (с, 2H), 6,55 (д, J=9,2 Гц, 1H), 7,11 (т, J=5,8 Гц, 1H), 7,59 (д, J=8,0 Гц, 2H), 7,65-7,68 (дд, J=2,4 та 8,8 Гц, 1H), 7,73 (д, J=8,4 Гц, 2H), 7,83 (т, J=6,0 Гц, -NH), 8,19 (с, 1H). Приклад 5 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((4-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)феніл)аміно)ацетамід Стадія 1: N-(4-(1-(((4-(Трифторметил)бензил)оксі)іміно)пропіл)феніл)ацетамід До розчину N-(4-(1-(гідроксііміно)пропіл)феніл)ацетаміду (6 г, 0,0291 моль) в ДМФ (60 мл) додавали карбонат цезію (18,9 г, 0,0582 моль) та 4- (трифторметил)бензилбромід (6,96 г, 0,0291 моль) і реакційну суміш перемішували при 25 °C протягом 3 годин. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 10 г (94 %) продукту у вигляді твердої речовини. 1H ЯМР: ДМСО-d6 δ 1,06 (т, J=7,4 Гц, 3H), 2,04 (с, 3H), 2,75 (кв, J=7,6 Гц, 2H), 5,27 (с, 2H), 7,55-7,61 (м, 6H), 7,73 (д, J=8 Гц, 2H), 10,07 (с, 1H). Стадія 2: 1-(4-Амінофеніл)пропан-1-он-O-(4-(трифторметил)бензил)оксим До розчину продукту стадії 1 (10 г, 0,0275 моль) в етанолі (70 мл) додавали розчин гідроксиду калію (6,15 г, 0,1098 моль) у воді (30 мл) і реакційну суміш перемішували при 8090 °C протягом 36 годин. Реакційну суміш виливали в охолоджену льодом воду та екстрагували дихлорметаном. Об'єднаний дихлорметановий екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 7,5 г (84 %) продукту у вигляді рідини. 1H ЯМР: ДМСО-d6 δ 1,03 (т, J=3,8 Гц, 3H), 2,66 (кв, J=7,6 Гц, 2H), 5,21 (с, 2H), 5,42 (с, 2H), 6,51-6,56 (м, 2H), 7,30-7,35 (м, 2H), 7,57 (д, J=8 Гц, 2H), 7,72 (д, J=8,4 Гц, 2H). Стадія 3: Етил-2-((4-(1-(((4-(трифторметил)бензил)оксі)іміно)пропіл)феніл)аміно)ацетат До розчину продукту стадії 2 (3,5 г, 0,0097 моль) в ДМФ (35 мл) додавали карбонат калію (4 г, 0,0291 моль) та етилбромацетат (1,8 г, 0,0107 моль) і реакційну суміш перемішували при 100 °C протягом ночі. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 2,2 г (55 %) продукту у вигляді твердої речовини. 1H ЯМР: ДМСО-d6 δ 1,04 (т, J=7,6 Гц, 3H), 1,19 (т, J=7,2 Гц, 3H), 2,67 (кв, J=7,6 Гц, 2H), 3,90 (д, J=6,4 Гц, 2H), 4,10 (кв, J=7,2 Гц, 2H), 5,22 (с, 2H), 6,37 (т, J=6,4 Гц, 1H), 6,52 (д, J=8,8 Гц, 2H), 7,37 (д, J=8,8 Гц, 2H), 7,58 (д, J=8,4 Гц, 2H), 7,72 (д, J=8 4 Гц, 2H). Стадія 4: 2-((4-(1-(((4-(Трифторметил)бензил)оксі)іміно)пропіл)феніл)аміно)оцтова кислота До розчину продукту стадії 3 (2,2 г, 5,39 ммоль) у ТГФ (10 мл) додавали розчин гідроксиду літію (0,45 г, 10,77 ммоль) у воді (10 мл) і реакційну суміш перемішували при 25 °C протягом 3 16 UA 113053 C2 годин. Розчинники випаровували при зниженому тиску. Залишок розчиняли у воді та нейтралізували до pH 6 за допомогою 1N HCl. Тверду речовину, що утворилася, фільтрували, промивали водою та осушали над CaCl2 під вакуумом, одержуючи 1,64 г (82 %) названого у заголовку продукту. 1H ЯМР: ДМСО-d6 δ 1,04 (т, J=7,6 Гц, 3H), 2,66-2,71 (м, 2H), 3,80 (с, 2H), 5,21 (с, 2H), 6,52 (д, J=8,8 Гц, 2H), 7,37 (д, J=8,8 Гц, 2H), 7,58 (д, J=8 Гц, 2H), 7,72 (д, J=8,4 Гц, 2H). Стадія 5: N-((Тетрагідро-2H-піран-4-іл)метил)-2-((4-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)феніл)аміно)ацетамід До розчину продукту стадії 4 (6,5 г, 0,0171 моль) в ДМФ (40 мл) додавали (тетрагідро-2Hпіран-4-іл)метанаміну гідрохлорид (2,6 г, 0,0171 моль), HOBT (2,31 г, 0,0171 моль), EDC∙HCl (4,24 г, 0,0222 моль) та N-етилморфолін (5,9 г, 0,0513 моль) і реакційну суміш перемішували при 25 °C протягом 5 годин під атмосферою азоту. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску. Сировий продукт очищали хроматографією на колонці, використовуючи 1 % MeOH у хлороформі як елюент, одержуючи 1,22 г (15 %) продукту у вигляді білої твердої речовини. 1H ЯМР: ДМСО-d6 δ 1,03 (т, J=7,6 Гц, 3H), 1,06-1,10 (м, 2H), 1,44 (д, J=12,8 Гц, 2H), 1,58-1,61 (м, 1H), 2,69 (кв, J=7,6 Гц, 2H), 2,96 (т, J=6,4 Гц, 2H), 3,15-3,22 (м, 2H), 3,64 (д, J=6 Гц, 2H), 3,77 (дд, J=11,6 та 2,8 Гц, 2H), 5,21 (с, 2H), 6,25 (т, J=6 Гц, 1H), 6,51 (д, J=8,8 Гц, 2H), 7,37 (д, J=8,8 Гц, 2H), 7,57 (д, J=8,0 Гц, 2H), 7,72 (д, J=8,0 Гц, 2H), 7,89 (т, J=6:0 Гц, 1H). Приклад 6 2,2'-((5-(1-(((4-(Трифторметил)бензил)оксі)іміно)етил)оксазол-2-іл)азанедіїл)діоцтова кислота Стадія 1: Діетил-2,2'-((5-ацетилоксазол-2-іл)азанедіїл)діацетат До розчину 1-(2-амінооксазол-5-іл)етанону (300 мг, 2,38 ммоль) в ДМФ (2 мл) додавали карбонат цезію (1,16 г, 3,57 ммоль), а потім додавали етилбромацетат (794 мг, 4,76 ммоль) при 25 °C під атмосферою азоту, і реакційну суміш перемішували при такій саме температурі протягом 18 год. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 310 мг (44 %) продукту у вигляді в'язкої рідини. 1H ЯМР: δ 1,27 (т, J=7,0 Гц, 6Η), 2,33 (с, 3Η), 4,20-4,27 (м, 4Η), 4,37 (с, 4Η), 7,57 (с, 1Η). Стадія 2: Діетил-2,2'-((5-(1-(гідроксііміно)етил)оксазол-2-іл)азанедііл)діацетат До розчину діетил-2,2'-((5-ацетилоксазол-2-іл)азанедіїл)діацетату (300 мг, 1,01 ммоль) в етанолі (6 мл) додавали розчин ацетату натрію (165 мг, 2,01 ммоль) та гідроксиламонію хлориду (139 мг г, 2,01 ммоль) у воді (2 мл), і реакційну суміш нагрівали до кипіння зі зворотним холодильником протягом 1 год. Реакційну суміш охолоджували до кімнатної температури та розчинник випаровували під вакуумом. Залишок розводили охолодженою льодом водою та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 252 мг (80 %) названого у заголовку продукту у вигляді в'язкої рідини. 1H ЯМР: δ 1,25-1,37 (м, 6H), 2,45 (с, 3H), 4,18-4,29 (м, 4H), 4,37 (с, 4H), 7,57 (с, 1H). Стадія 3: Діетил-2,2'-((5-(1-(((4-(трифторметил)бензил)оксі)іміно)етил)оксазол-2іл)азанедіїл)діацетат До розчину 1-(бромметил)-4-(трифторметил)бензолу (200 мг, 0,84 ммоль) в ДМФ (2 мл) додавали карбонат цезію (408 мг, 1,26 ммоль), а потім додавали діетил 2,2'-((5-(1(гідроксііміно)етил)оксазол-2-іл)азанедіїл)діацетат (262 мг, 0,84 ммоль) при 25 °C під атмосферою азоту і реакційну суміш перемішували при такій саме температурі протягом 18 год. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску. Сировий продукт очищали хроматографією на колонці (елюент: 15 % етилацетату у гексані), одержуючи 295 мг (75 %) продукту у вигляді в'язкої рідини. 1H ЯМР: δ 1,25-1,36 (м, 6H), 2,04 (с, 3H), 4,19 (кв, J=12 Гц, 4H), 4,32 (с, 4H), 5,22 (с, 2H), 6,99 (с, 1H), 7,47 (д, J=8,0 Гц, 2H), 7,60 (д, J=8,4 Гц, 2H). Стадія 4: 2,2'-((5-(1-(((4-(Трифторметил)бензил)оксі)іміно)етил)оксазол-2іл)азанедіїл)діоцтова кислота До розчину продукту стадії 3 (295 мг, 0,62 ммоль) у суміші ТГФ (6 мл), метанолу (2 мл) та води (2 мл) додавали гідроксид літію (105 мг, 1,25 ммоль) і реакційну суміш перемішували при температурі навколишнього середовища протягом 4 годин. Розчинники випарювали при 17 UA 113053 C2 зниженому тиску. Залишок розчиняли у воді та підкислювали 1N HCl. Білу тверду речовину, що утворилася, фільтрували та промивали водою і осушали над P2O5 під вакуумом, одержуючи 250 мг (82 %) названого у заголовку продукту у вигляді білуватої твердої речовини. 1H ЯМР: ДМСО-d6 δ 2,06 (с, 3H), 4,16 (с, 4H), 5,23 (с, 2H), 7,31 (с, 1H), 7,58 (д, J=8,0 Гц, 2H), 7,72 (д, J=8,4 Гц, 2H). Приклад 7 2,2'-((5-(1-(((4-(Трифторметил)бензил)оксі)іміно)етил)оксазол-2-іл)азанедіїл)біс-(N((тетрагідро-2H-піран-4-іл)метил)ацетамід) До розчину сполуки, одержаної у прикладі 6 (250 мг, 0,60 ммоль) в ДМФ (2 мл) додавали (тетрагідро-2H-піран-4-іл)метанамін (138 мг, 1,20 ммоль), HOBT (121 мг, 0,90 ммоль), EDC∙HCl (138 мг, 0,72 ммоль) та N-етилморфолін (227 мкл, 1,80 ммоль) і реакційну суміш перемішували при 25 °C протягом 2-5 годин під атмосферою азоту. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску. Сировий продукт тритурували з гексаном, одержуючи 180 мг (49 %) продукту у вигляді білої твердої речовини. 1H ЯМР: ДМСО-d6 δ 1,04-1,14 (м, 4H), 1,47-1,50 (м, 4H), 1,58-1,62 (м, 2H), 2,04 (с, 3H), 2,96 (т, J=6,2 Гц, 4H), 3,18 (т, J=10,8 Гц, 4H), 3,76 (дд, J=11,0 Гц та 3,0 Гц, 4H), 4,08 (с, 4H), 5,20 (с, 2H), 7,28 (с, 1H), 7,58 (д, J=8,0 Гц, 2H), 7,72 (д, J=8,4 Гц, 2H). Приклад 8 2-((1-(4-(Трифторметил)бензил)-3-((((4-(трифторметил)бензил)оксі)іміно)метил)-1H-індол-5іл)оксі)оцтова кислота Стадія 1: Етил-2-((1H-індол-5-іл)оксі)ацетат До розчину 5-гідроксііндолу (4,56 г, 0,034 моль) в ДМФ (20 мл) додавали карбонат калію (9,43 г, 0,068 моль), етилбромацетат (6,29 г, 0,0377 моль) і реакційну суміш перемішували при температурі навколишнього середовища протягом 12 годин. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 6,2 г (82 %) продукту у вигляді твердої речовини. 1H ЯМР: ДМСО-d6 δ 1,20 (т, J=3,6 Гц, 3H), 4,13 (кв, J=8,6 Гц, 2H), 4,70 (с, 2H), 6,31 (д, J=2,0 Гц, 1H), 6,74 (дд, J=8,8 та 2,4 Гц, 1H), 6,99 (д, J=2,4 Гц, 1H), 1,21 (дд, J=5,6 та 2,8 Гц, 2H), 10,95 (шир.с, 1H). Стадія 2: Етил-2-((3-((гідроксііміно)метил)-7H-індол-5-іл)оксі)ацетат До ДМФ (1,74 г, 0,023 моль), охолодженого до 0 °C під атмосферою азоту, додавали порціями оксихлорид фосфору (3,5 г, 0,022 моль) та перемішували протягом 15 хв. До цієї суміші додавали розчин продукту стадії 1 (2,5 г, 0,011 моль) у дихлоретані (18 мл) при 0 °C та нагрівали до 80 °C протягом 2 год. Розчинники випарювали при зниженому тиску. Залишок розчиняли у воді, підлуговували за допомогою NaOH та екстрагували етилацетатом. Етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску. Сировий продукт очищали хроматографією на колонці (елюент: 40 % EtOAC у гексані), одержуючи 900 мг (31 %) продукту у вигляді твердої речовини. 1H ЯМР: ДМСО-d6 δ 1,22 (т, J=1,82 Гц, 3H), 4,15 (кв, J=7,2 Гц, 2H), 4,77 (с, 2H), 6,91 (дд, J=8,8 та 2,8 Гц, 1H), 7,41 (д, J=8,8 Гц, 1H), 7,52 (д, J=2,4 Гц, 1H), 8,23 (д, J=2,8 Гц, 1H), 9,88 (д, J=4,4 Гц, 1H), 12,06 (шир.с, 1H). Стадія 3: Етил-2-((3-((гідроксііміно)метил)-1H-індол-5-іл)оксі)ацетат До розчину продукту стадії 2 (880 мг, 3,56 ммоль) в метанолі (6 мл) та воді (3 мл) додавали гідроксиламіну гідрохлорид (491 мг, 7,12 ммоль), ацетат натрію (584 мг, 7,12 моль) і реакційну суміш нагрівали при 70 °C протягом 2 годин. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, Сировий продукт очищали хроматографією на колонці, використовуючи 40 % EtOAC у гексані як елюент, одержуючи 280 мг (27 %) продукту у вигляді твердої речовини. 1H ЯМР: δ 1,21 (т, J=4,0 Гц, 3H), 4,14 (кв, J=7,0 Гц, 2H), 4,70 (с, 2H), 6,83 (дд, J=8,8 та 2,4 Гц, 1H), 7,31 (д, J=8,8 Гц, 1H), 7,43 (д, J=2,4 Гц, 1H), 7,58 (д, J=2,8 Гц, 1H), 8,22 (с, 1H), 10,46 (с, 1H), 11,30 (шир.с, 1H). Стадія 4: Етил-2-((1-(4-(трифторметил)бензил)-3-((((4(трифторметил)бензил)оксі)іміно)метил)-1H-індол-5-іл)оксі)ацетат До розчину продукту стадії 3 (280 мг, 1,068 ммоль) в ДМФ (2 мл) додавали карбонат цезію (1,0 г, 3,2 ммоль), 4-трифторметилбензилбромід (510 мг, 2,13 ммоль) і реакційну суміш перемішували при 25 °C протягом 2 годин. Реакційну суміш виливали в охолоджену льодом 18 UA 113053 C2 воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, Сировий продукт очищали хроматографією на колонці, використовуючи 15 % EtOAC у гексані як елюент, одержуючи 350 мг (56 %) продукту у вигляді твердої речовини. 1H ЯМР: δ 1,16 (т, J=7,0 Гц, 3H), 4,11 (кв, J=6,9 Гц, 2H), 4,69 (с, 2H), 5,23 (с, 2H), 5,54 (с, 2H), 6,85 (дд, J=8,8 та 2,4 Гц, 1H), 7,35-7,40 (м, 4H), 7,68 (д, J=2,4 Гц, 4H), 7,74 (д, J=8,0 Гц, 2H), 7,85 (с, 1H), 8,44 (с, 1H). Стадія 5: 2-((1-(4-(Трифторметил)бензил)-3-((((4-(трифторметил)бензил)оксі)іміно)метил)1H-індол-5-іл)оксі)оцтова кислота До розчину продукту стадії 4 (350 мг, 0,605 ммоль) у ТГФ (2 мл), воді (2 мл) додавали гідроксид літію моногідрат (38 мг, 0,908 ммоль) і реакційну суміш перемішували при 25 °C протягом 3 годин. Реакційну суміш виливали в охолоджену льодом воду, підкислювали розб.HCl та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску, одержуючи 250 мг (77 %) продукту у вигляді твердої речовини. 1H ЯМР: δ 4,61 (с, 2H), 5,21 (с, 2H), 5,53 (с, 2H), 6,84 (дд, J=9,2 та 2,8 Гц, 1H), 7,36 (т, 3H), 7,42 (д, J=2,4 Гц, 1H), 7,67 (д, J=8,4 Гц, 4H), 7,74 (д, J=8,4 Гц, 2H), 7,84 (с, 1H), 8,42 (с, 1H), 12,98 (д, J=4,4 Гц, 1H). Приклад 9 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((1-(4-(трифторметил)бензил)-3-((((4(трифторметил)бензил)оксі)іміно)метил)-1H-індол-5-іл)оксі)ацетамід До розчину сполуки, одержаної у прикладі 8 (250 мг, 0,454 ммоль), в ДМФ (2 мл) додавали (тетрагідро-2H-піран-4-іл)метанаміну гідрохлорид (83 мг, 0,545 ммоль), HOBT (каталізатор), EDC∙HCl (130 мг, 0,681 ммоль) та N-етилморфолін (0,173 мл, 1,362 ммоль) і реакційну суміш перемішували при 25 °C протягом 5 годин під атмосферою азоту. Реакційну суміш виливали в охолоджену льодом воду та екстрагували етилацетатом. Об'єднаний етилацетатний екстракт промивали водою та розсолом, осушали над сульфатом натрію та випарювали при зниженому тиску. Сировий продукт очищали хроматографією на колонці, одержуючи 200 мг (68 %) продукту у вигляді білої твердої речовини. 1H ЯМР: δ 1,01-1,11 (м, 2H), 1,42 (д, J=12,8 Гц, 2H), 1,61-1,67 (м, 1H), 2,67 (т, J=1,8 Гц, 2H), 2,98-3,15 (м, 2H), 3,71 (дд, J=14,0 та 2,8 Гц, 2H), 4,45 (с, 2H), 5,23 (с, 2H), 5,53 (с, 2H), 6,89 (дд, J=8,8 та 2,4 Гц, 1H), 7,34 (д, J=8,0 Гц, 2H), 7,38 (д, J=9,2 Гц, 1H), 7,46 (д, J=2,4 Гц, 1H), 7,68 (т, J=8,2 Гц, 4H), 7,75 (д, J=8,0 Гц, 2H), 7,84 (с, 1H), 8,08 (т, J=6,0 Гц, 1H), 8,42 (с, 1H). Приклад 10 2-(2-Метил-4-(2-феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро2H-піран-4-іл)метил)ацетамід 1H ЯМР: δ 1,2 (м, 2H), 1,5 (м, 2H), 1,7 (м, 1H), 2,2 (с, 3H), 3,2 (т, J=6,4 Гц, 2H), 3,3 (т, J=11,4 Гц, 2H), 3,9 (дд, J=11,6 та 3,6 Гц, 2H), 4,1 (с, 2H), 4,6 (с, 2H), 5,2 (с, 2H), 6,6 (т, NH), 6,7 (д, J=8,4 Гц, 1H), 7,1-7,2 (м, 5H), 7,3 (м, 3H), 7,5 (с, 1H), 7,6 (д, J=8,0 Гц, 2H). Приклад 11 2-(4-(2-Феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2H-піран4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,02-1,13 (м, 2H), 1,43-1,46 (м, 2H), 1,58-1,65 (м, 1H), 2,97 (т, J=6,4 Гц, 2H), 3,15-3,20 (м, 2H), 3,75 (дд, J=11,4 та 2,6 Гц, 2H), 4,17 (с, 2H), 4,47 (с, 2H), 5,31 (с, 2H), 6,89 (д, J=9,2 Гц, 2H), 7,12-7,16 (м, 3H), 7,20-7,24 (м, 2H), 7,55-7,61 (м, 4H), 7,71 (д, J=8,0 Гц, 2H), 8,80 (т, NH). Приклад 12 2-(4-(2-Феніл-1-(((3-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2H-піран4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,11-1,06 (м, 2H), 1,46-1,43 (м, 2H), 1,64-1,59 (м, 1H), 2,99 (т, J=12,8 Гц, 2H), 3,19 (т, J=21,6 Гц, 2H), 3,78 (д, 2H), 4,16 (с, 2H), 4,47 (с, 2H), 5,31 (с, 2H), 6,91 (д, J=8,8 Гц, 2H), 7,15 (т, J=3,8 Гц, 3H), 7,22 (д, J=6 Гц, 2H),7,60 (т, J=8,8 Гц, 3H), 7,67 (с, 1H), 7,70 (с, 2H), 8,10 (т, J=11,6 Гц, 1H). Приклад 13 2-(4-(2-(Піридин-4-іл)-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро2H-піран-4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,05-1,10 (м, 2H), 1,45 (д, J=12,8 Гц, 2H), 1,65-1,71 (м, 1H), 2,98 (т, J=6,4 Гц, 2H), 3,14-3,20 (м, 2H), 3,75-3,78 (м, 2H), 4,20 (с, 2H), 4,47 (с, 2H), 5,30 (с, 2H), 6,92 (д, J=8,8 Гц, 2H), 7,14 (д, J=6,0 Гц, 2H), 7,55 (д, J=8,0 Гц, 2H), 7,61 (д, J=8,8 Гц, 2H), 7,71 (д, J=8,0 Гц, 2H), 8,07 (с, -NH), 8,40 (д, J=4,4 Гц, 2H). 19 UA 113053 C2 Приклад 14 2-(4-(2-Морфоліно-1-(((4-(трифторrnетил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,05-1,16 (м, 2H), 1,48 (д, J=13,2 Гц, 2H), 1,62-1,68 (м, 1H), 2,36 (шир.с, 4H), 3,01 (т, J=6,4 Гц, 2H), 3,20 (т, J=11,0 Гц, 2H), 3,46 (м, 4H), 3,64 (с, 2H), 3,78-3,81 (дд, J=11,6 та 2,4 Гц, 2H), 4,51 (с, 2H), 5,27 (с, 2H), 6,93 (д, J=8,8 Гц, 2H), 7,61 (д, J=8,0 Гц, 2H), 7,67 (д, J=8,8 Гц, 2H), 7,74 (д, J=8,4 Гц, 2H), 8,11 (т, NH). Приклад 15 N-((Тетрагідро-2H-піран-4-іл)метил)-2-(4-(2-тіоморфоліно-1-(((4(трифторметил)бензил)оксі)іміно)етил)феноксі)ацетамід 1H ЯМР: ДМСО-d6 δ 1,09-1,18 (м, 2H), 1,46-1,49 (м, 2H), 1,60-1,65 (м, 1H), 2,47-2,49 (м, 4H), 2,61-2,63 (м, 4H), 2,99 (т, J=6,6 Гц, 2H), 3,17-3,23 (м, 2H), 3,67 (с, 2H), 3,78-3,81 (м, 2H), 4,50 (с, 2H), 5,26 (с, 2H), 6,92 (дд, J=7,0 та 1,8 Гц, 2H), 7,59-7,65 (м, 4H), 7,73 (д, J=8,0 Гц, 2H), 8,09 (т, NH). Приклад 16 2-(2-Метил-4-(2-(тіофен-3-іл)-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N((тетрагідро-2H-піран-4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,04-1,14 (м, 2H), 1,44 (д, J=12,8 Гц, 2H), 1,58-1,67 (м, 1H), 2,19 (с, 3H), 2,98 (т, J=6,4 Гц, 2H), 3,15-3,21 (м, 2H), 3,76-3,79 (м, 2H), 4,11 (с, 2H), 4,50 (с, 2H), 5,31 (с, 2H), 6,77 (д, J=8,8 Гц, 1H), 6,89 (м, 1H), 7,11 (с, 1H), 7,38-7,40 (м, 1H), 7,43 (дд, J=8,6 та 1,8 Гц, 1H), 7,51 (с, 1H), 7,55 (д, J=8,0 Гц, 2H), 7,70 (д, J=8,4 Гц, 2H), 7,90 (т, NH). Приклад 17 N-((Тетрагідро-2H-піран-4-іл)метил)-2-(4-((((4(трифторметил)бензил)оксі)іміно)метил)феноксі)ацетамід 1H ЯМР: ДМСО-d6 δ 1,05-1,16 (м, 2H), 1,46-1,49 (м, 2H), 1,62-1,98 (м, 1H), 2,99 (т, J=6,4 Гц, 2H), 3,17-3,24 (м, 2H), 3,78-3,81 (м, 2H), 4,51 (с, 2H), 5,23 (с, 2H), 6,97-6,99 (dd. J=2,0 та 8,8 Гц, 2H), 7,54 (дд, J=2,0 та 8,8 Гц, 2H),7,60 (д, J=8,0 Гц, 2H), 7,73 (д, J=8,0 Гц, 2H), 8,12 (т, NH), 8,29 (с, 1H). Приклад 18 N-((Тетрагідро-2H-піран-4-іл)метил)-2-(4-(1-(((4(трифторметил)бензил)оксі)іміно)етил)феноксі)ацетамід 1H ЯМР: ДМСО-d6 δ 1,12-1,07 (м, 2H), 1,45-1,44 (м, 2H), 1,48 (м, 1H), 2,21 (с, 3H), 2,99 (т, J=6,4 Гц, 2H), 3,22-3,16 (м, 2H), 3,80-3,77 (м, 2H), 4,49 (с, 2H), 5,26 (с, 2H), 6,96-6,93 (дд, J=2,0 та 6,8 Гц, 2H), 7,60-7,56 (м, 4H), 7,71 (д, J=8,0 Гц, 2H), 8,10 (т, J=5,6 Гц, 1H). Приклад 19 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((5-((((4(трифторметил)бензил)оксі)іміно)метил)піридин-2-іл)оксі)ацетамід 1H ЯМР: δ 1,24-1,35 (м, 2H), 1,54-1,58 (м, 2H), 1,73-1,81 (м, 1H), 3,21 (т, J=6,6 Гц, 2H), 3,313,37 (м, 2H), 3,93-3,97 (м, 2H), 4,85 (с, 2H), 5,23 (с, 2H), 6,42 (шир.с, NH), 6,83 (д, J=8,4 Гц, 1H), 7,49 (д, J=8,0 Гц, 2H), 7,61 (д, J=8,0 Гц, 2H), 7,95 (дд, J=8,4 та 2,4 Гц, 1H), 8,12 (с, 1H), 8,20 (д, J=2,4 Гц, 1H). Приклад 20 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((4-(1-(((4(трифторметил)бензил)оксі)іміно)етил)феніл)аміно)ацетамід 1H ЯМР: ДМСО-d6 δ 1,06-1,15 (м, 2H), 1,44 (д, J=12,8 Гц, 2H), 1,60 (м, 1H), 2,16 (с, 3H), 2,94 (т, J=6,4 Гц, 2H), 3,16-3,22 (м, 2H), 3,64 (д, J=6,0 Гц, 2H), 3,77-3,80 (м, 2H), 5,22 (с, 2H), 6,23 (т, J=6,0 Гц, 1H), 6,51 (д, J=8,4 Гц, 2H), 7,38 (д, J=8,4 Гц, 2H), 7,58 (д, J=8 Гц, 2H), 7,71 (д, J=8,0 Гц, 2H), 7,88 (т, J=5,8 Гц, 1H). Приклад 21 2-((5-(1-(((4-Ціанобензил)оксі)іміно)етил)піридин-2-іл)окси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,06-1,10 (м, 2H), 1,44-1,47 (м, 2H), 1,62-1,68 (м, 1H), 2,24 (с, 3H), 2,95 (т, J=6,4 Гц, 2H), 3,15-3,22 (м, 2H), 3,76-3,80 (дд, J=2,8 та 11,6 Гц, 2H), 4,71 (с, 2H), 5,27 (с, 2H), 6,91 (д, J=8,8 Гц, 1H), 7,57 (д, J=8,0 Гц, 2H), 7,83 (д, J=6,4 Гц, 2H), 7,95-8,01 (м, 2H), 8,32 (с, 1H). Приклад 22 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((5-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)піридин-2-іл)оксі)ацетамід 1H ЯМР: δ 1,14 (т, J=7,6 Гц, 3H), 1,24-1,34 (м, 2H), 1,55-1,58 (м, 2H), 1,72-1,82 (м, 1H), 2,76 (кв, J=7,6 Гц, 2H), 3,23 (т, J=6,4 Гц, 2H), 3,30-3,37 (м, 2H), 3,93-3,97 (м, 2H), 4,85 (с, 2H), 5,25 (с, 20 UA 113053 C2 2H), 6,44 (шир.с, NH), 6,81 (д, J=8,8 Гц, 1H), 7,48 (д, J=8,0 Гц, 2H), 7,61 (д, J=8,0 Гц, 2H), 7,94 (дд, J=8,6 та 2,2 Гц, 1H), 8,35 (д, J=2,4 Гц, 1H). Приклад 23 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((5-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)піридин-2-іл)аміно)ацетамід 1H ЯМР: δ 1,03 (т, J=7,6 Гц, 3Η), 1,07-1,11 (м, 2Η), 1,47-1,51 (м, 2Η), 1,57-1,63 (м, 1H), 2,68 (кв, J=7,6 Гц, 2H), 2,94 (т, J=6,4 Гц, 2H), 3,16-3,23 (м, 2H), 3,78 (дд, J=11,2 та 2,4 Гц, 2H), 3,86 (д, J=6,0 Гц, 2H), 5,23 (с, 2H), 6,55 (д, J=8,8 Гц, 1H), 7,12 (т, J=6,0 Гц, NH), 7,58 (д, J=8,0 Гц, 2H) 7,64 (дд, J=9,0 та 2,6 Гц, 1H), 7,72 (д, J=8,0 Гц, 2H), 7,83 (т, J=6,0 Гц, NH), 8,18 (д, J=2,0 Гц, 1H). Приклад 24 2-((5-(1-((Бензилоксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: δ 1,11 (т, J=7,6 Гц, 3H), 1,24-1,35 (м, 2H), 1,54-1,58 (м, 2H), 1,72-1,82 (м, 1H), 2,72 (кв, J=7,6 Гц, 2H), 3,21 (т, J=6,6 Гц, 2H), 3,31-3,37 (м, 2H), 3,93-3,96 (м, 2H), 4,84 (с, 2H), 5,21 (с, 2H), 6,45 (шир.с, NH), 6,80 (дд, J=8,8 та 0,4 Гц, 1H), 7,29-7,41 (м, 5H), 7,96 (дд, J=8,8 та 2,4 Гц, 1H), 8,35 (д, J=2,0 Гц, 1H). Приклад 25 2-((5-(1-(((4-Метилбензил)оксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: δ 1,10 (т, J=7,2 Гц, 3H), 1,25-1,36 (м, 2H), 1,56-1,59 (м, 2H), 1,73-1,84 (м, 1H), 2,36 (с, 3H), 2,72 (кв, J=7,2 Гц, 2H), 3,22 (т, J=6,6 Гц, 2H), 3,32-3,38 (м, 2H), 3,94-3,98 (м, 2H), 4,85 (с, 2H), 5,27 (с, 2H), 6,47 (шир.с, NH), 6,82 (д, J=8,4 Гц, 1H), 7,17 (д, J=7,6 Гц, 2H), 7,29 (д, J=8,0 Гц, 2H), 7,98-8,00 (м, 1H), 8,35 (д, J=2,0 Гц, 1H). Приклад 26 2-((5-(1-(((4-Метоксибензил)оксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: δ 1,10 (т, J=7,6 Гц, 3H), 1,24-1,35 (м, 2H), 1,54-1,56 (м, 2H), 1,73-1,80 (м, 1H), 2,69 (кв, J=7,6 Гц, 2H), 3,21 (т, J=6,6 Гц, 2H), 3,31-3,37 (м, 2H), 3,81 (с, 3H), 3,93-3,96 (м, 2H), 4,84 (с, 2H), 5,13 (с, 2H), 6,45 (шир.с, NH), 6,81 (д, J=8,8 Гц, 1H), 6,88-6,91 (м, 2H), 7,31-7,35 (м, 2H), 7,96 (дд, J=8,8 та 2,4 Гц, 1H), 8,34 (д, J=2,0 Гц, 1H). Приклад 27 2-((5-(1-(((4-Фторбензил)оксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: δ 1,11 (т, J=7,6 Гц, 3H), 1,24-1,35 (м, 2H), 1,54-1,58 (м, 2H), 1,73-1,81 (м, 1H), 2,71 (кв, J=7,6 Гц, 2H), 3,21 (т, J=6,6 Гц, 2H), 3,31-3,37 (м, 2H), 3,93-3,96 (м, 2H), 4,84 (с, 2H), 5,16 (с, 2H), 6,45 (шир.с, NH), 6,81 (дд, J=8,8 та 0,4 Гц, 1H), 7,01-7,07 (м, 2H), 7,34-7,39 (м, 2H), 7,95 (дд, J=8,8 та 2,4 Гц, 1H), 8,34 (д, J=2,0 Гц, 1H). Приклад 28 2-((5-(1-(((4-Ціанобензил)оксі)іміно)пропіл)піридин-2-іл)окси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: δ 1,16 (т, J=7,6 Гц, 3H), 1,25-1,35 (м, 2H), 1,55-1,59 (м, 2H), 1,72-1,81 (м, 1H), 2,75 (кв, J=7,6 Гц, 2H), 3,21 (т, J=6,6 Гц, 2H), 3,31-3,38 (м, 2H), 3,93-3,97 (м, 2H), 4,85 (с, 2H), 5,26 (с, 2H), 6,44 (шир.с, NH), 6,82 (дд, J=8,8 Гц, 1H), 7,47 (д, J=8,0 Гц, 2H), 7,65 (д, J=8,4 Гц, 2H), 7,93 (дд, J=8,4 та 2,4 Гц, 1H), 8,35 (д, J=2,0 Гц, 1H). Приклад 29 2-(2-Метил-4-(1-(((4-(трифторметил)бензил)оксі)іміно)бутил)фенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 0,87 (т, J=7,4 Гц, 3H), 1,07-1,15 (м, 2H), 1,41-1,48 (м, 4H), 1,60-1,67 (м, 1H), 2,21 (с, 3H), 2,72 (т, J=7,6 Гц, 2H), 3,00 (т, J=6,4 Гц, 2H), 3,16-3,22 (т, J=12,0 Гц, 2H), 3,773,80 (дд, J=11,2 та 11,2 Гц, 2H), 4,51 (с, 2H), 5,24 (с, 2H), 6,80 (д, J=8,4 Гц, 1H), 7,36-7,38 (дд, J=8,8 та 8,4 Гц, 1H), 7,43 (д, J=1,6 Гц, 1H), 7,58 (д, J=8,0 Гц, 2H), 7,72 (д, J=8,0 Гц, 2H), 7,93 (т, J=5,8 Гц, 1H). Приклад 30 2-(4-(2-Метокси-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,07-1,04 (м, 2H), 1,15-1,13 (м, 2H), 1,66-1,62 (м, 1H), 3,00 (т, 2H), 3,163,17 (м, 2H), 3,19 (с, 3H), 3,80-3,77 (м, 2H), 4,49 (с, 2H), 4,58 (с, 2H), 5,27 (с, 2H), 6,95-6,93 (дд, J=2 та 7,2 Гц, 2H), 7,55-7,52 (м, 2H), 7,59 (д, J=8 Гц, 2H), 7,72 (д, J=8,0 Гц, 2H), 8,09 (т, J=5,9 Гц, 1H). Приклад 31 21 UA 113053 C2 2-(4-(2-Гідрокси-1-(((4-(трифторметил)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,05-1,15 (м, 2H), 1,46 (д, J=12,8 Гц, 2H), 1,62-1,68 (м, 1H), 2,99 (т, J=6,4 Гц, 2H), 3,17 (т, J=10,8 Гц, 2H), 3,77-3,81 (м, 2H), 4,49 (с, 2H), 4,60 (д, J=5,6 Гц, 2H), 5,15 (т, J=5,6 Гц, 1H), 5,25 (с, 2H), 6,93 (д, J=8,8 Гц, 2H), 7,55 (д, J=8,8 Гц, 2H), 7,59 (д, J=8 Гц, 2H), 7,71 (д, J=8 Гц, 2H), 8,09 (т, J=5,6 Гц, 1H). Приклад 32 2-(2-Метил-4-(1-(((4-метилбензил)окси)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2H-піран4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,03-1,16 (м, 2H), 1,43 (м, 2H), 1,58-1,66 (м, 1H), 2,18 (с, 3H), 2,28 (с, 3H), 2,97 (т, J=6,6 Гц, 2H), 3,1-3,20 (м, 2H), 3,75-3,79 (м, 2H), 4,10 (с, 2H), 4,48 (с, 2H), 5,15 (с, 2H), 6,74 (д, J=8,8 Гц, 1H), 7,10-7,16 (м, 5H), 7,18-7,21 (м, 2H), 7,24 (д, J=8,0 Гц, 2H), 7,40 (дд, J=8,6 та 2,2 Гц, 1H), 7,50 (д, J=1,6 Гц, 1H), 7,91 (т, J=6,0 Гц, NH). Приклад 33 2-(4-(1-(((4-Метилбензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,06-1,16 (м, 2H), 1,43 (д, J=12,8 Гц, 2H), 1,59-1,66 (м, 1H), 2,28 (с, 3H), 2,96 (т, J=6,4 Гц, 2H), 3,14 (м, 2H), 3,75-3,78 (м, 2H), 4,11 (с, 2H), 4,46 (с, 2H), 5,16 (с, 2H), 6,89 (д, J=8,8 Гц, 2H), 7,11-7,16 (м, 5H), 7,18-7,22 (м, 2H), 7,24 (д, J=8,0 Гц, 2H), 7,59 (д, J=8,8 Гц, 2H), 8,07 (т, J=5,8 Гц, NH). Приклад 34 2-(4-(1-(((4-Фторбензил)оксі)іміно)-2-фенілетил)-2-метилфенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,21-1,36 (м, 2H), 1,54-1,57 (м, 2H), 1,72-1,79 (м, 1H), 2,25 (с, 3H), 3,23 (т, J=6,4 Гц, 2H), 3,31-3,37 (м, 2H), 3,93 (дд, J=11,2 та 3,6 Гц, 2H), 4,11 (с, 2H), 4,48 (с, 2H), 5,20 (с, 2H), 6,68 (д, J=8,8 Гц, 2H), 6,98 (т, J=8,8 Гц, 2H), 7,13-7,32 (м, 7H), 7,39 (дд, J=8,8 та 2,0 Гц, 1H), 7,52 (с, 1H). Приклад 35 2-(4-(1-(((4-Фторбензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: δ 1,24-1,35 (м, 2H), 1,54-1,57 (м, 2H), 1,71-1,80 (м, 1H), 3,23 (т, J=6,2 Гц, 2H), 3,293,36 (м, 2H), 3,92-3,96 (м, 2H), 4,12 (с, 2H), 4,47 (с, 2H), 5,20 (с, 2H), 6,58 (с, 1H), 6,85 (д, J=12 Гц, 2H), 6,98-7,03 (м, 2H), 7,13-7,24 (м, 5H), 7,29-7,32 (м, 2H), 7,58-7,61 (м, 2H). Приклад 36 2-(4-(1-(((4-Хлорбензил)оксі)іміно)-2-фенілетил)-2-метилфенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,03-1,14 (м, 2H), 1,43 (д, J=12,8 Гц, 2H), 1,59-1,65 (м, 1H), 2,18 (с, 3H), 2,97 (т, J=6,4 Гц, 2H), 3,15-3,20 (м, 2H), 3,75-3,79 (м, 2H), 4,12 (с, 2H), 4,49 (с, 2H), 5,19 (с, 2H), 6,75 (д, J=8,8 Гц, 1H), 7,12-7,15 (м, 3H), 7,19-7,22 (м, 2H), 7,35-7,43 (м, 5H), 7,58 (д, J=1,2 Гц, 1H), 7,90 (т, J=5,8 Гц, NH). Приклад 37 2-(4-(1-(((4-Хлорбензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,05-1,13 (м, 2H), 1,43 (д, J=11,6 Гц, 2H), 1,61-1,63 (м, 1H), 2,96 (т, J=6,4 Гц, 2H), 3,14 (т, J=10,8 Гц, 2H), 3,75-3,78 (м, 2H), 4,13 (с, 2H), 4,46 (с, 2H), 5,20 (с, 2H), 6,89 (д, J=8,8 Гц, 2H), 7,12-7,15 (м, 3H), 7,19-7,23 (м, 2H), 7,36-7,42 (м, 4H), 7,58 (д, J=8,8 Гц, 2H), 8,06 (т, J=5,8 Гц, NH). Приклад 38 2-(2-Метил-4-(2-феніл-1-(((4-(трифторметокси)бензил)оксі)іміно)етил)фенокси)-N((тетрагідро-2H-піран-4-іл)метил)ацетамід 1H ЯМР: δ 1,25-1,37 (м, 2H), 1,57 (м, 2H), 1,71-1,80 (м, 1H), 2,25 (с, 3H), 3,25 (т, J=6,6 Гц, 2H), 3,31-3,37 (м, 2H), 3,93-3,97 (м, 2H), 4,13 (с, 2H), 4,48 (с, 2H), 5,23 (с, 2H), 6,58 (с, 1H), 6,70 (д, J=8,8 Гц, 1H), 7,14-7,24 (м, 7H), 7,33 (д, J=8,8 Гц, 2H), 7,39-7,42 (м, 1H), 7,51 (д, J=7,6 Гц, 1H). Приклад 39 2-(4-(2-Феніл-1-(((4-(трифторметокси)бензил)оксі)іміно)етил)фенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,02-1,13 (м, 2H), 1,43 (д, J=12,8 Гц, 2H), 1,58-1,65 (м, 1H), 2,96 (т, J=6,4 Гц, 2H), 3,14-3,20 (м, 2H), 3,75-3,78 (м, 2H), 4,14 (с, 2H), 4,47 (с, 2H), 5,24 (с, 2H), 6,89 (д, J=8,8 Гц, 2H), 7,13-7,14 (м, 3H), 7,18-7,22 (м, 2H), 7,33 (д, J=8,4 Гц, 2H), 7,47 (д, J=8,8 Гц, 2H), 7,59 (д, J=8,8 Гц, 2H), 8,06 (т, J=5,8 Гц, NH). 22 UA 113053 C2 Приклад 40 2-(4-(1-(((4-Метоксибензил)оксі)іміно)-2-фенілетил)-2-метилфенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,03-1,14 (м, 2H), 1,43-1,47 (м, 2H), 1,59-1,64 (м, 1H), 2,18 (с, 3H), 2,97 (т, J=6,4 Гц, 2H), 3,14-3,20 (м, 2H), 3,73 (с, 3H), 3,75-3,79 (м, 2H), 4,08 (с, 2H), 4,48 (с, 2H), 5,12 (с, 2H), 6,74 (д, J=8,8 Гц, 1H), 6,88-6,92 (м, 2H), 7,10-7,13 (м, 3H), 7,17-7,21 (м, 2H), 7,29-7,32 (м, 2H), 7,40 (дд, J=8,6 та 2,2 Гц, 1H), 7,50 (д, J=1,6 Гц, 1H), 7,91 (т, J=6,0 Гц, NH). Приклад 41 2-(4-(1-(((4-Метоксибензил)оксі)іміно)-2-фенілетил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,03-1,13 (м, 2H), 1,43-1,46 (м, 2H), 1,59-1,65 (м, 1H), 2,96 (т, J=6,4 Гц, 2H), 3,14-3,20 (м, 2H), 3,73 (с, 3H), 3,75-3,78 (м, 2H), 4,10 (с, 2H), 4,46 (с, 2H), 5,13 (с, 2H), 6,89 (дд, J=8,8 та 2,0 Гц, 4H), 7,10-7,13 (м, 3H), 7,18-7,21 (м, 2H), 7,29 (дд, J=11,2 та 2,8 Гц, 2H), 7,58 (д, J=10,0 Гц, 2H), 8,06 (т, J=6,0 Гц, NH). Приклад 42 2-(4-(1-(((4-(Метилсульфоніл)бензил)оксі)іміно)пропіл)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: δ 1,04-1,16 (м, 5H), 1,45-1,49 (м, 2H), 1,61-1,70 (м, 1H), 2,72 (кв, J=7,6 Гц, 2H), 2,99 (т, J=6,4 Гц, 2H), 3,17-3,23 (м, 5H), 3,77-3,81 (дд, J=11,4 та 2,6 Гц, 2H), 4,51 (с, 2H), 5,28 (с, 2H), 6,95-6,98 (м, 2H), 7,55-7,59 (м, 2H), 7,62 (д, J=8,0 Гц, 2H), 7,91 (дд, J=6,8 та 1,6 Гц, 2H), 8,08 (т, J=5,8 Гц, NH). Приклад 43 2-(4-(2-Феніл-1-((піридин-2-ілметоксі)іміно)етил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: δ 1,27-1,35 (м, 2H), 1,53-1,57 (м, 2H), 1,72-1,79 (м, 1H), 3,21 (т, J=6,6 Гц, 2H), 3,293,36 (м, 2H),3,92 (дд, J=11,0 та 3,4 Гц, 2H), 4,21 (с, 2H), 4,47 (с, 2H), 5,39 (с, 2H), 6,58 (шир.с, NH), 6,82-6,86 (м, 2H), 7,16-7,28 (м, 7H), 7,60-7,64 (м, 3H), 8,56-8,58 (м, 1H). Приклад 44 2-(4-(1-((2-(1H-Індол-1-іл)етоксі)іміно)пропіл)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 0,83 (т, J=7,4 Гц, 3H), 1,08-1,12 (м, 2H), 1,45-1,49 (м, 2H), 1,60-1,68 (м, 1H), 2,49-2,53 (м, 2H), 3,00 (т, J=6,4 Гц, 2H), 3,20 (т, J=11,6 Гц, 2H), 3,78-3,81 (дд, J=11,4 та 2,6 Гц, 2H), 4,36-4,38 (т, J=5,0 Гц, 2H), 4,48-4,51 (м, 4H), 6,41 (д, J=3,2 Гц, 1H), 6,94 (д, J=8,8 Гц, 2H), 6,97-7,01 (м, 1H), 7,08 (т, J=7,0 Гц, 1Η), 7,30 (д, J=2,8 Гц, 1H), 7,44 (д, J=8,0 Гц, 1H), 7,51-7,56 (м, 3H), 8,10 (т, NH). Приклад 45 2-(4-(1-(((5-Етилпіримідин-2-іл)оксі)іміно)пропіл)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,07-1,20 (м, 8H), 1,47-1,50 (дд, J=12,8 та 12,8 Гц, 2H), 1,65-1,66 (м, 1H), 2,56-2,61 (кв, 2H), 2,86-2,92 (кв, 2H), 3,02 (т, J=6,4 Гц, 2H), 3,18-3,28 (м, 2H), 3,78-3,81 (дд, J=11,2 та 11,2 Гц, 2H), 4,55 (с, 2H), 7,03-7,06 (м, 2H), 7,73-7,76 (м, 2H), 8,13 (т, J=5,8 Гц, 1H), 8,54 (с, 2H). Приклад 46 2-(4-(1-(((5-Метил-2-фенілоксазол-4-іл)метоксі)іміно)пропіл)фенокси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетамід 1H ЯМР: δ 1,07 (т, J=7,6 Гц, 3H), 1,25-1,37 (м, 2H), 1,56-1,64 (м, 2H), 1,75-1,81 (м, 1H), 2,47 (с, 3H), 2,71 (кв, J=7,6 Гц, 2H), 3,23 (т, J=6,6 Гц, 2H), 3,32 (т, J=11,8 Гц, 2H), 3,94 (дд, J=11,0 та 3,8 Гц, 2H), 4,51 (с, 2H), 5,12 (с, 2H), 6,62 (шир.с, NH), 6,88-6,92 (м, 2H), 7,40-7,45 (м, 3H), 7,59-7,63 (м, 2H), 7,99-8,02 (м, 2H). Приклад 47 2-(4-(1-(((3-(трет-Бутил)-1-(п-толіл)-1H-піразол-5-іл)метоксі)іміно)пропіл)фенокси)-N((тетрагідро-2H-піран-4-іл)метил)ацетамід 1H ЯМР: δ 1,06 (т, J=7,6 Гц, 3H), 1,27-1,34 (м, 2H), 1,36 (с, 9H), 1,58-1,60 (м, 2H), 1,78-1,80 (м, 1H), 2,37 (с, 3H), 2,69 (кв, J=7,4 Гц, 2H), 3,24 (т, J=6,6 Гц, 2H), 3,32 (т, J=11,6 Гц, 2H), 3,94 (дд, J=11,0 та 3,4 Гц, 2H), 4,52 (с, 2H), 5,11 (с, 2H), 6,37 (с, 1H), 6,62 (с, NH), 6,90 (д, J=8,8 Гц, 2H), 7,21 (д, J=8,0 Гц, 2H), 7,44 (д, J=8,0 Гц, 2H), 7,58 (д, J=8,8 Гц, 2H). Приклад 48 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((5-(((4-(трифторметил)бензил)оксі)іміно)-5,6,7,8тетрагідронафталін-2-іл)оксі)ацетамід 23 UA 113053 C2 1H ЯМР: ДМСО-d6 δ 1,08 (т, J=6,6 Гц, 2H), 1,44 (д, J=12,8 Гц, 2H), 1,48 (м, 1H), 1,75 (т, J=5,8 Гц, 2H), 2,66 (т, J=5,6 Гц, 2H), 2,98 (т, J=6,6 Гц, 2H), 3,01 (т, J=6,4 Гц, 2H), 3,16-3,21 (м, 2H), 3,80 (д, J=2,4 Гц, 2H), 4,47 (с, 2H), 5,24 (с, 2H), 6,74 (д, J=2,4 Гц, 1H), 6,77-6,80 (дд, J=2,8 та 8,8 Гц, 1H), 7,58 (д, J=8 Гц, 2H), 7,69-7,73 (дд, J=4 та 8 Гц, 3H), 8,09 (т, J=5,6 Гц, 1H). Приклад 49 2-((5-(((4-Хлорбензил)оксі)іміно)-5,6,7,8-тетрагідронафталін-2-іл)окси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1-09-1,15 (м, 2H), 1,45 (д, J=12,8 Гц, 2H), 1,61-1,69 (м, 1H), 1,69-7,75 (м, 2H), 2,63-2,68 (м, 4H), 2,99 (т, J=6,4 Гц, 2H), 3,15-3,22 (м, 2H), 4,47 (с, 2H), 5,12 (с, 2H), 6,73 (д, J=2,4 Гц, 1H), 6,78-6,81 (дд, J=2,8 та 8,8 Гц, 1H), 7,38 (д, J=8 Гц, 4H), 7,71 (д, J=8,8 Гц, 1H), 8,08 (т, J=6,0 Гц, 1H). Приклад 50 2-((5-(((4-Ціанобензил)оксі)іміно)-5,6,7,8-тетрагідронафталін-2-іл)окси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,07-1,30 (м, 2H), 1,44-1,48 (м, 2H), 1,64 (м, 1H), 1,72-1,75 (м, 2H), 2,66 (т, J=6,0 Гц, 2H), 2,69-2,72 (м, 2H), 2,99 (т, J=6,4 Гц, 2H), 3,16-3,22 (м, 2H), 3,76-3,80 (кв, J=2,6 Гц, 2H), 4,47 (с, 2H), 5,23 (с, 2H), 6,74 (д, J=2,8 Гц, 1H), 6,77-6,8 (дд, J=2,4 та 8,4 Гц, 1H), 7,54 (д, J=8,4 Гц, 2H), 7,68 (д, J=8,8 Гц, 1H), 7,81 (д, J=1,6 Гц, 2H), 8,08 (т, J=6,0 Гц, 1H). Приклад 51 2-((5-(((4-Метоксибензил)оксі)іміно)-5,6,7,8-тетрагідронафталін-2-іл)окси)-N-((тетрагідро-2Hпіран-4-іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,09-1,16 (м, 2H), 1,46-1,49 (дд, J=1,6 та 12,8 Гц, 2H), 1,64-1,74 (м, 3H), 2,61-2,66 (м, 4H), 2,99 (т, J=6,4 Гц, 2H), 3,18-3,24 (м, 2H), 3,74 (с, 3H), 3,78-3,82 (дд, J=2,4 та 11,2 Гц, 2H), 4,48 (с, 2H), 5,06 (с, 2H), 6,75 (д, J=2,4 Гц, 1H), 6,80-6,83 (дд, J=2,8 та 8,8 Гц, 1H), 6,92 (д, J=8,4 Гц, 2H), 7,34 (д, J=8,4 Гц, 2H), 7,77 (д, J=8,8 Гц, 1Η), 8,08 (т, J=6,0 Гц, 1H). Приклад 52 Метил-3-((((6-(2-оксо-2-(((тетрагідро-2H-піран-4-іл)метил)аміно)етокси)-3,4-дигідронафталін1(2H)-іліден)аміно)окси)метил)бензоат 1H ЯМР: ДМСО-d6 δ 1,08-1,15 (м, 2H),1,45-1,49 (дд, J=1,6 та 12,8 Гц, 2H), 1,64-1,66 (м, 1H), 1,72 (т, J=6,0 Гц, 2H), 2,65-2,71 (м, 4H), 2,99 (т, J=6,4 Гц, 2H), 3,17-3,20 (м, 2H), 3,78-3,81 (дд, J=2,4 та 11,2 Гц, 2H), 3,85 (с, 3H), 4,48 (с, 2H), 5,22 (с, 2H), 6,75 (д, J=2,8 Гц, 1H), 6,79-6,82 (дд, J=2,8 та 8,8 Гц, 1H), 7,50 (т, J=7,6 Гц, 1H), 7,68 (д, J=7,6 Гц, 1H), 7,74 (д, J=8,8 Гц, 1H), 7,88-7,91 (м, 1H), 7,98 (с, 1H), 8,06 (т, J=6,0 Гц, 1H). Приклад 53 2-((5-(1-(((4-(Трифторметил)бензил)оксі)іміно)етил)хінолін-8-іл)оксі)оцтова кислота 1H ЯМР: ДМСО-d6 δ 2,36 (с, 3H), 4,78 (с, 2H), 5,32 (с, 2H), 7,23 (д, J=7,6 Гц, 1H), 7,41-7,44 (м, 1H), 7,55-7,58 (м, 1H), 7,64-7,66 (м, 2H), 7,77 (д, J=8,4 Гц, 2H), 8,40 (д, J=8,8 Гц, 1H), 8,86 (д, J=2,8 Гц, 1H). Приклад 54 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((5-(1-(((4(трифторrnетил)бензил)оксі)іміно)етил)хінолін-8-іл)оксі)ацетамід 1H ЯМР: ДМСО-d6 δ 1,09-1,16 (м, 2H), 1,44 (д, J=12,8 Гц, 2H), 1,61-1,64 (м, 1H), 2,36 (с, 3H), 3,04 (т, J=6,4 Гц, 2H), 3,16-3,23 (м, 2H), 3,77 (дд, J=2,8 та 11,6 Гц, 2H), 4,77 (с, 2H), 5,33 (с, 2H), 7,24 (д, J=8,4 Гц, 1H), 7,43 (дд, J=4,4 та 8,8 Гц, 1H), 7,58 (д, J=8,4 Гц, 1H), 7,64 (д, J=8 Гц, 2H), 7,77 (д, J=8 Гц, 2H), 8,34 (т, J=5,8 Гц, 1H), 8,39 (дд, J=1,6 та 8,8 Гц, 1H), 8,89 (дд, J=1,6 та 4,0 Гц, 1H). Приклад 55 2-Метил-N-((тетрагідро-2H-піран-4-іл)метил)-2-(4-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)фенокси)пропанамід 1H ЯМР: δ 1,14 (т, J=7,6 Гц, 3H), 1,23-1,34 (м, 2H), 1,50-1,51 (м, 2H), 1,57 (с, 6H), 1,72-1,77 (м, 1H), 2,74 (кв, J=7,6 Гц, 2H), 3,17 (т, J=6,6 Гц, 2H), 3,29-3,36 (м, 2H), 3,91-3,95 (м, 2H), 5,25 (с, 2H), 6,68 (т, J=5,8 Гц, NH), 6,86-6,90 (м, 2H), 7,49-7,55 (м, 4H), 7,60 (д, J=8,4 Гц, 2H). Приклад 56 2-Метил-N-((тетрагідро-2H-піран-4-іл)метил)-2-(4-(1-(((4(трифторметил)бензил)оксі)іміно)етил)фенокси)пропанамід 1H ЯМР: δ 1,23-1,34 (м, 2H), 1,51-1,56 (сложн, 8H), 1,71-1,77 (м, 1H), 2,26 (с, 3H), 3,17 (т, J=6,6 Гц, 2H), 3,29-3,36 (м, 2H), 3,92-3,95 (м, 2H), 5,26 (с, 2H), 6,71 (т, J=5,6 Гц, NH), 6,86-6,90 (м, 2H), 7,49-7,55 (м, 4H), 7,60 (д, J=8,0 Гц, 2H). Приклад 57 24 UA 113053 C2 2-(4-(1-(((Тетрагідро-2H-піран-4-іл)метоксі)іміно)етил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: ДМСО δ 1,09-1,16 (м, 2H), 1,23-1,31 (м, 2H), 1,50 (дд, J=12,8 та 1,6 Гц, 2H), 1,61 (дд, J=12,8 та 2 Гц, 2H), 1,62-1,66 (м, 1H), 1,67-1,96 (м, 1H), 2,15 (с, 3H), 3,01 (т, J=6,4 Гц, 2H), 3,183,24 (м, 2H), 3,26-3,29 (м, 2H), 3,78-3,86 (м, 4H), 3,97 (д, J=6,4 Гц, 2H), 4,51 (с, 2H), 6,97 (дд, J=7,2 та 2,4 Гц, 2H), 7,60 (дд, J=6,8 та 2,0 Гц, 2H), 8,12 (т, J=5,8 Гц, 1H). Приклад 58 2-(4-(1-((Циклогексилметоксі)іміно)етил)фенокси)-N-((тетрагідро-2H-піран-4іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 0,95-0,98 (м, 2H), 1,09-1,21 (м, 5H), 1,48 (дд, J=12,8 та 1,6 Гц, 2H), 1,641,74 (м, 7H), 2,14 (с, 3H), 3,01 (т, J=6,6 Гц, 2H), 3,18-3,24 (м, 2H), 3,82 (дд, J=11,2 та 2,4 Гц, 2H), 3,92 (д, J=6,4 Гц, 2H), 4,51 (с, 2H), 6,94-6,98 (м, 2H), 7,57-7,60 (м, 2H), 8,12 (т, J=6 Гц, 1H). Приклад 59 2-(4-(1-((Нафталін-2-ілметоксі)іміно)етил)фенокси)-N-((тетрагідро2H-піран-4іл)метил)ацетамід 1H ЯМР: ДМСО-d6 δ 1,05-1,16 (м, 2H), 1,46 (д, J=13,2 Гц, 2H), 1,63-1,68 (м, 1H), 2,22 (с, 3H), 3,01 (т, J=6,4 Гц, 2H), 3,16-3,23 (м, 2H), 3,78-3,82 (дд, J=11,2 та 2,4 Гц, 2H), 4,50 (с, 2H), 5,33 (с, 2H), 6,97 (д, J=7,2 Гц, 2H), 7,49-7,52 (м, 2H), 7,54-7,56 (дд, J=8,8 та 1,6 Гц, 1H), 7,59-7,61 (дд, J=6,8 та 1,6 Гц, 2H), 7,89-7,93 (м, 4H), 8,11 (т, J=5,8 Гц, 1H). Наступні сполуки можуть бути одержані за процедурою, подібною до описаних вище, з відповідними варіантами реакцій, реакційних умов та кількостей реагентів, які є відомими кваліфікованим фахівцям в даній області техніки. Приклад 60 2-((5-(1-(((4-(Трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)аміно)оцтова кислота Приклад 61 2-((5-((((4-(Трифторметил)бензил)оксі)іміно)метил)піридин-2-іл)оксі)оцтова кислота Приклад 62 2-((5-(1-(((4-Ціанобензил)оксі)іміно)етил)піридин-2-іл)оксі)оцтова кислота Приклад 63 2-((5-(1-(((4-(Трифторметил)бензил)оксі)іміно)пропіл)піридин-2-іл)оксі)оцтова кислота Приклад 64 2-((5-(1-(((4-(Трифторметил)бензил)оксі)іміно)пропіл)піридин-2-іл)аміно)оцтова кислота Приклад 65 2-((5-(1-((Бензилоксі)іміно)пропіл)піридин-2-іл)оксі)оцтова кислота Приклад 66 2-((5-(1-(((4-Метилбензил)оксі)іміно)пропіл)піридин-2-іл)оксі)оцтова кислота Приклад 67 2-((5-(1-(((4-Метоксибензил)оксі)іміно)пропіл)піридин-2-іл)оксі)оцтова кислота Приклад 68 2-((5-(1-(((4-Фторбензил)оксі)іміно)пропіл)піридин-2-іл)оксі)оцтова кислота Приклад 69 2-((5-(1-(((4-Ціанобензил)оксі)іміно)пропіл)піридин-2-іл)оксі)оцтова кислота Приклад 70 2-((5-(2-Феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)оксі)оцтова кислота Приклад 71 2-((5-(2-Феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)окси)-N-((тетрагідро2H-піран-4-іл)метил)ацетамід Приклад 72 2-((5-(2-Феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)аміно)оцтова кислота Приклад 73 2-((5-(2-Феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піридин-2-іл)аміно)-N((тетрагідро-2H-піран-4-іл)метил)ацетамід Приклад 74 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((3-((((4-(трифторметил)бензил)оксі)іміно)метил)-1Hіндол-5-іл)оксі)ацетамід Приклад 75 2-((3-((((4-(Трифторметил)бензил)оксі)іміно)метил)-1H-індол-5-іл)оксі)оцтова кислота Приклад 76 25 UA 113053 C2 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((3-(1-(((4-(трифторметил)бензил)оксі)іміно)етил)-1Hіндол-5-іл)оксі)ацетамід Приклад 77 2-((3-(1-(((4-(Трифторметил)бензил)оксі)іміно)етил)-1H-індол-5-іл)оксі)оцтова кислота Приклад 78 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((3-(1-(((4-(трифторметил)бензил)оксі)іміно)пропіл)1H-індол-5-іл)оксі)ацетамід Приклад 79 2-((3-(1-(((4-(Трифторметил)бензил)оксі)іміно)пропіл)-1H-індол-5-іл)оксі)оцтова кислота Приклад 80 2-((3-(2-Феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)-1H-індол-5-іл)окси)-N((тетрагідро-2H-піран-4-іл)метил)ацетамід Приклад 81 2-((3-(2-Феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)-1H-індол-5-іл)оксі)оцтова кислота Приклад 82 N-((Тетрагідро-2H-піран-4-іл)метил)-3-(5-(1-(((4(трифторметил)бензил)оксі)іміно)етил)піримідин-2-іл)пропанамід Приклад 83 3-(5-(1-(((4-(Трифторметил)бензил)оксі)іміно)етил)піримідин-2-іл)пропіонова кислота Приклад 84 N-((Тетрагідро-2H-піран-4-іл)метил)-3-(5-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)піримідин-2-іл)пропанамід Приклад 85 3-(5-(1-(((4-(Трифторметил)бензил)оксі)іміно)пропіл)піримідин-2-іл)пропіонова кислота Приклад 86 3-(5-(2-Феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піримідин-2-іл)-N-((тетрагідро-2Hпіран-4-іл)метил)пропанамід Приклад 87 3-(5-(2-Феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)піримідин-2-іл)prdpanoic acid Приклад 88 N-((Тетрагідро-2H-піран-4-іл)метил)-2-((5-(1-(((4(трифторметил)бензил)оксі)іміно)пропіл)хінолін-8-іл)оксі)ацетамід Приклад 89 2-((5-(1-(((4-(Трифторметил)бензил)оксі)іміно)пропіл)хінолін-8-іл)оксі)оцтова кислота Приклад 90 2-((5-(2-Феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)хінолін-8-іл)окси)-N-((тетрагідро2H-піран-4-іл)метил)ацетамід Приклад 91 2-((5-(2-Феніл-1-(((4-(трифторметил)бензил)оксі)іміно)етил)хінолін-8-іл)оксі)оцтова кислота Сполуки за даним винаходом знижували LDL (ліпопротеїди низької густини), тригліцериди та загальний холестерин (ТС). Це було продемонстровано в in vitro, а також in vivo експериментах на тваринах. A) Демонстрація in vitro ефективності сполук Аналіз зв'язування in vitro, описаний тут, є кількісним твердофазовим аналізом зв'язування для визначення ефективності сполук. На планшети заздалегідь наносили покриття з рекомбінантного домену LDLR-AB, який зв'язується з геном пропротеїнконвертази субтипу девять. Досліджувану сполуку в різних концентраціях додавали до субтипу гена та додавали до LDLR, іммобілізованого у лунках. Кількість зв'язаного гена вимірювали шляхом його зв'язування з біотинільованим анти-His-міченим моноклональним антитілом, з подальшим зв'язуванням з пероксидазою хрону, кон'югованою із стрептавідиновим субстратом. Забарвлення кількісно вимірювали за допомогою планшет-ридера для ELISA на 450 нм, що відповідає відносній кількості "гена", який зв'язується з LDLR в присутності інгібітора та без нього. Значення EC50 розраховували шляхом нелінійного регресійного аналізу, використовуючи прикладну програму Graph Pad Prism. Кожна точка концентрацій відповідає результату двох паралельних дослідів. Приклад № 1 Концентрація, (мкМ) 1 10 100 % інгібування 29 35 57 26 UA 113053 C2 Приклад № 3 4 5 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 Концентрація, (мкМ) 1 10 100 1 10 100 1 10 100 1 5 10 100 1 5 10 100 1 10 100 1 10 100 1 10 100 1 10 100 1 5 10 100 1 10 100 1 10 100 10 100 1 10 100 100 1 10 100 1 10 100 1 10 100 1 10 100 % інгібування 28 41 54 34 39 51 34 40 50 3 18 35 51 20 23 49 61 19 55 79 22 32 48 15 31 41 25 37 39 10 21 35 61 13 19 44 16 38 63 40 46 20 34 57 15 29 46 46 30 42 47 24 1 28 52 28 34 50 27 UA 113053 C2 Приклад № 26 27 28 30 31 32 33 34 35 36 37 38 39 40 41 42 43 48 49 Концентрація, (мкМ) 1 10 100 1 10 100 100 100 1 10 100 1 10 100 1 10 100 1 10 100 1 10 100 1 10 100 1 10 100 10 100 10 100 10 100 1 100 10 100 10 100 1 10 100 10 100 % інгібування 45 45 52 10 15 29 23 36 15 20 29 14 35 48 10 10 28 7 ' 13 32 22 13 25 6 9 36 20 26 28 19 38 33 42 20 47 10 19 9 51 15 27 17 42 64 7 11 B) Здатність до зниження LDL-C у мишей C57 на раціоні з високим вмістом жирів Зниження LDL-C (холестерин ліпопротеїдів низької густини) in vivo досліджуваними сполуками тестували на мишах C57, яких утримували на кормі з високим вмістом жирів протягом 4 тижнів і брали кров методом пункції ретроорбітального синуса під легкою анестезією ефіром в день 0 (перед початком експерименту). Тварин ділили на групи за рівнями LDL-C, після чого протягом 4-6 тижнів проводили дослідження із введенням раз на день носія або досліджуваної сполуки в дозі 30 мг/кг (mpk). Після завершення досліджень в день 28 брали кров для вимірювання рівнів LDL-C. Розраховували процент змін LDL-C у групі, що отримувала досліджувану сполуку, у порівнянні з групою, що отримувала носій. 28
ДивитисяДодаткова інформація
Назва патенту англійськоюHeterocyclic compounds suitable for the treatment of dyslipidemia
Автори англійськоюPengali, Harikishore, Makadia, Pankaj, Pandya, Vrajesh, Kalapatapu, V. V. M. Sairam, Jain, Mukul R.
Автори російськоюПингали Харикисхор, Макадиа Панкадж, Пандия Враджеш, Калапатапу Ви. Ви. Эм. Саирам, Джаин Мукул Ар.
МПК / Мітки
МПК: C07D 309/06, A61K 31/35, C07D 413/12, C07D 409/12, C07D 407/12
Мітки: дисліпідемії, лікування, сполуки, гетероциклічні, придатні
Код посилання
<a href="https://ua.patents.su/35-113053-geterociklichni-spoluki-pridatni-dlya-likuvannya-dislipidemi.html" target="_blank" rel="follow" title="База патентів України">Гетероциклічні сполуки, придатні для лікування дисліпідемії</a>
Попередній патент: Спосіб ферментного синтезу (7s)-1-(3,4-диметоксибіцикло[4.2.0]окта-1,3,5-триєн-7-іл)-n-метилметанаміну та використання в синтезі івабрадину та його солей
Наступний патент: Спосіб поверхневої обробки пігменту з діоксиду титану
Випадковий патент: Вогнетривкий склад для приклеювання волокнистих матеріалів












