Спільні кристали і солі інгібіторів ccr3
Номер патенту: 109290
Опубліковано: 10.08.2015
Автори: Сантагостіно Марко, Анрі Мануель, Хеберле Ханс, Вертманн Ульріке, Требінг Томас, Франк Маркус, Пахур Торстен, Штерц Уве
Формула / Реферат
1. Співкристали сполук формули 1
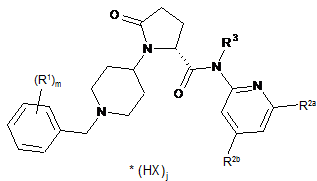 , 1
, 1
в якій
R1 означає С1-С6-алкіл, С1-С6-галогеналкіл, О-С1-С6-галогеналкіл, галоген;
m дорівнює 1, 2 або 3;
R2а і R2b всі незалежно вибрані з групи, що включає Н, С1-С6-алкіл, С1-С6-алкеніл, С1-С6-алкініл, С3-С6-циклоалкіл, СОО-С1-С6-алкіл, О-С1-С6-алкіл, CONR2b.1R2b.2, галоген;
R2b.1 означає Н, С1-С6-алкіл, С0-С4-алкіл-С3-С6-циклоалкіл, С1-С6-галогеналкіл;
R2b.2 означає Н, С1-С6-алкіл;
або R2b.1 і R2b.2 разом означають С3-С6-алкіленову групу, що утворює разом з атомом азоту гетероциклічне кільце, де один атом вуглецю в кільці необов'язково замінений на атом кисню;
R3 означає Н, С1-С6-алкіл;
X означає аніон, вибраний із групи, що включає хлорид, бромід, йодид, сульфат, фосфат, метансульфонат, нітрат, малеат, ацетат, бензоат, цитрат, саліцилат, фумарат, тартрат, дибензоїлтартрат, оксалат, сукцинат і п-толуолсульфонат;
j дорівнює 0, 0,5, 1, 1,5 або 2;
з речовиною, що створює співкристали, вибраною з групи, що включає оротову кислоту, гіпурову кислоту, L-піроглутамінову кислоту, D-піроглутамінову кислоту, нікотинову кислоту, L-(+)-аскорбінову кислоту, сахарин, піперазин, 3-гідрокси-2-нафтойну кислоту, муцинову (галактарову) кислоту, памоєву (ембонову) кислоту, стеаринову кислоту, холеву кислоту, дезоксихолеву кислоту, нікотинамід, ізонікотінамід, сукцинамід, урацил, L-лізин, L-пролін, D-валін, L-аргінін, гліцин.
2. Співкристали сполук формули 1 за п. 1, в якій
R2a означає Н, С1-С6-алкіл, С1-С6-алкеніл, С1-С6-алкініл, С3-С6-циклоалкіл, О-С1-С6-алкіл, CONR2a.1R2a.2;
R2a.l означає Н, С1-С6-алкіл, С1-С6-галогеналкіл;
R2а.2означає Н, С1-С6-алкіл;
R2b означає Н, С1-С6-алкіл, С1-С6-алкеніл, С1-С6-алкініл, С3-С6-циклоалкіл, СОО-С1-С6-алкіл, О-С1-С6-алкіл, CONR2b.lR2b.2, галоген;
R2b.1 означає Н, С1-С6-алкіл, С0-С4-алкіл-С3-С6-циклоалкіл, С1-С6-галогеналкіл;
R2b.2 означає Н, С1-С6-алкіл;
або R2b.1 і R2b.2 разом означають С3-С3-алкіленову групу, що утворює разом з атомом азоту гетероциклічне кільце, де один атом вуглецю в кільці необов'язково замінений на атом кисню.
3. Співкристали сполук формули 1 за одним з пп. 1 або 2, в якій
R1 означає С1-С6-алкіл, С1-С6-галогеналкіл, О-С1-С6-галогеналкіл, галоген;
m дорівнює 1 або 2;
R2а означає Н, С1-С4-алкіл;
R2b означає H, CONR2b.1R2b.2;
R2b.1 означає С1-С4-алкіл, С0-С4-алкіл-С3-С6-циклоалкіл, С1-С4-галогеналкіл;
R2b.2 означає Н, С1-С4-алкіл;
або R2b.1 і R2b.2 разом означають С3-С6-алкіленову групу, що утворює разом з атомом азоту гетероциклічне кільце, де один атом вуглецю в кільці необов'язково замінений на атом кисню;
R3 означає Н, С1-С6-алкіл;
X означає аніон, вибраний із групи, що включає хлорид або дибензоїлтартрат;
j дорівнює 1 або 2.
4. Співкристали сполук формули 1 за одним з пп. 1-3, в якій
R2a означає Н, С1-С4-алкіл;
R2b означає Н, CONR2b.1R2b.2;
R2b.1 означає С1-С4-алкіл;
R2b.2 означає С1-С4-алкіл.
5. Співкристали сполук формули 1 за одним з пп. 1-4, в якій
R2а означає Н, С1-С4-алкіл;
R2b означає Н, CONR2b.1R2b.2;
R2b.1 означає С0-С4-алкіл-С3-С6-циклоалкіл;
R2b.2 означає Н, С1-С4-алкіл.
6. Співкристали сполук формули 1 за одним з пп. 1-5, в якій
R2a означає Н, С1-С4-алкіл;
R2b означає Н, CONR2b.1R2b.2;
R2b.1 означає С1-С4-галогеналкіл;
R2b.2 означає Н, С1-С4-алкіл.
7. Співкристали сполук формули 1 за одним з пп. 1-6, в якій R2b.1 і R2b.2 разом означають С3-С6-алкіленову групу, що утворює разом з атомом азоту гетероциклічне кільце, де один атом вуглецю в кільці необов'язково замінений на атом кисню.
8. Співкристали сполук формули 1 за одним з пп. 1-7, де речовину, що утворює співкристали, вибрано з групи, що включає аскорбінову кислоту, памоєву кислоту, сукцинамід, нікотинову кислоту, нікотинамід, ізонікотінамід, L-лізин, L-пролін або їх гідрати, або гідрохлориди.
9. Солі сполук формули 1
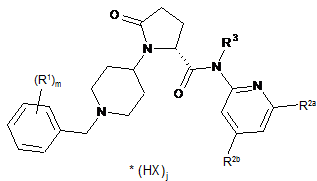 , 1
, 1
в якій R1, m, R2a, R2b, R3 є такими, як визначено в одному з пп. 1-8, і
X означає аніон, вибраний з групи, що включає хлорид, бромід, йодид, сульфат, фосфат, метансульфонат, нітрат, малеат, ацетат, бензоат, цитрат, саліцилат, фумарат, тартрат, дибензоїлтартрат, оксалат, сукцинат і п-толуолсульфонат;
j дорівнює 0, 0,5, 1, 1,5 або 2.
10. Солі сполук формули 1 за п. 9, в якій R1, m, R2a, R2b, R3 є такими, як визначено в одному з пп. 1-8, і
X означає аніон, вибраний з групи, що включає хлорид або дибензоїлтартрат;
j дорівнює 1 або 2.
11. Солі за п. 9 або 10, що застосовуються для одержання співкристалу за одним з пп. 1-8.
12. Сполуки формули І13, що застосовуються для одержання співкристалу або солі сполуки формули 1 за одним з пп. 1-10
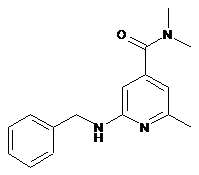 , I13.
, I13.
13. Сполуки формули І14, що застосовуються для одержання співкристалу або солі сполуки формули 1 за одним з пп. 1-10
 , I14.
, I14.
14. Сполуки формули І3'-Ме, що застосовуються для одержання співкристалу або солі сполуки формули 1 за одним з пп. 1-10
 , I3'-Me.
, I3'-Me.
15. Фармацевтична композиція, що містить щонайменше один співкристал або сіль сполуки формули 1 за будь-яким з пп. 1-10, і фармацевтично прийнятний носій.
16. Співкристал або сіль сполуки формули 1 за одним з пп. 1-10 як лікарський засіб.
17. Застосування співкристалу або солі сполуки формули 1 за одним з пп. 1-10 для попередження або лікування самих різних запальних, інфекційних та імунорегуляторних порушень і захворювань, включаючи астму та алергічні захворювання, хронічне обструктивне захворювання легень, інфікування патогенними мікробами (включаючи віруси), аутоімунні патології, такі як ревматоїдний артрит і атеросклероз, а також вікова дегенерація жовтої плями (ВДП), діабетична ретинопатія і діабетичний набряк жовтої плями.
Текст
Реферат: У заявці описані спільні кристали і солі інгібіторів CCR3 формули (1) UA 109290 C2 (12) UA 109290 C2 O R N 3 N (R1)m N O R2a N * (HX)j R2b , (1) фармацевтичні композиції, що їх містять, і їх застосування як засобів, призначених для лікування і/або попередження захворювань, пов'язаних з рецептором CCR3. O N H N N UA 109290 C2 5 10 15 20 25 30 35 40 45 50 55 60 Галузь техніки, до якої належить винахід Даний винахід належить до спільних кристалів і солей інгібіторів CCR3, які містять одну з цих речовин фармацевтичних композицій і до способів їх застосування в якості засобів, призначених для попередження та / або лікування самих різних запальних, інфекційних та імунорегуляторних порушень і захворювань, включаючи астму та алергічні захворювання, хронічного обструктивного захворювання легень, інфікування патогенними мікробами (включаючи віруси), аутоімунних патологій, таких як ревматоїдний артрит і атеросклероз, а також вікової дегенерації жовтої плями (ВДП), діабетичної ретинопатії і діабетичного набряку жовтої плями. Рівень техніки Хемокіни є хемотаксичними цитокінами, що мають молекулярну масу, що дорівнює 6-15 кДа, які вивільняються самими різними клітинами і, разом з іншими типами клітин, притягують і активують макрофаги, T-і B-лімфоцити, еозинофіли, базофіли і нейтрофіли (огляди наведені у публікаціях Luster, New Eng. J Med., 338, 436-445 (1998); Rollins, Blood, 90, 909-928 (1997); Lloyd, Curr Opin Pharmacol., 3, 443-448 (2003); Murray, Current Drug Targets., 7, 579-588 (2006); Smit, Eur J Pharmacol., 533,277-88 (2006). Існують два основні класи хемокінів, CXC і CC, що розрізняються тим, чи розділені перші два цистеїна амінокислотної послідовності однієї амінокислотою (CXC) або вони є сусідніми (CC). CXC хемокіни, такі як інтерлейкін-8 (IL-8), активований нейтрофілом білок 2 (NAP2) і білок, що стимулює активність зростання меланоми (MGSA) є хемотаксичними в першу чергу для нейтрофілів і T-лімфоцитів, тоді як CC хемокіни, такі як RANTES, MIP-la, MIP-1, моноцитарні хемотоксичні білки (MCP-1, MCP-2, MCP-3, MCP-4 і MCP-5) і еотаксіни (-1, -2 і -3) є хемотаксичними, поряд з іншими типами клітин, для макрофагів, T-лімфоцитів, еозинофілів, мастоцитів, дендритних клітин і базофілів. Також існують хемокіни лімфотактін-1, лімфотактін-2 (обидва є C хемокінів) і фракталкін (CXXXC хемокін), які не входять в ці основні підродини хемокінів. Хемокіни зв'язуються зі специфічними рецепторами поверхні клітини, що відносяться до сімейства пов'язаних з білком G семи білків трансмембранного домену (огляди наведені у публікаціях Horuk, Trends Pharm. Sci., 15, 159-165 (1994); Murphy, Pharmacol Rev., 54 (2) :227229 (2002); Allen, Annu. Rev. Immunol., 25, 787-820 (2007)), які називаються "хемокіновими рецепторами". При зв'язуванні зі своїми спорідненими лігандами хемокінові рецептори перетворюють внутрішньоклітинний сигнал за допомогою асоційованих тримерного білків G, що призводить, поряд з іншими відповідями, до швидкого збільшення концентрації кальцію всередині клітини, активації білків G, змін форми клітини, посиленню експресії молекул клітинної адгезії, дегрануляції, стимулювання міграції клітин, виживанню і проліферації. Існують щонайменше одинадцять хемокінових рецепторів людини, які зв'язуються з CC хемокінами або реагують на них, які мають наступні характеристичні особливості: CCR-1 (або "CKR-1" або "CCCKR-1") [MIP-la, MCP-3, MCP-4, RANTES] (Ben-Barruch, et al., Cell, 72, 415-425 (1993), Luster, New Eng. J. Med., 338, 436-445 (1998)); CCR-2A і CCR-2B (або "CKR-2A" / "CKR-2B" або "CCCKR-2A" / "CC-CKR-2B") [MCP-1, MCP2, MCP-3, MCP-4, MCP-5] (Charo et al., Proc. Natl. Acad. Sci. USA, 91, 2752-2756 (1994), Luster, New Eng. J. Med., 338, 436-445 (1998)); CCR3 (або "CKR3" або "CC-CKR-3") [еотаксін-1, еотаксін-2, RANTES, MCP-3, MCP-4] (Combadiere, et al., J. Biol. Chem., 270, 16491-16494 (1995), Luster, New Eng. J. Med., 338, 436-445 (1998)); CCR-4 (або "CKR-4" або "CC-CKR-4") [TARC, MIP-la, RANTES, MCP-1] (Power et al., J. Biol. Chem., 270, 19495-19500 (1995), Luster, New Eng. J. Med., 338, 436-445 (1998)); CCR-5 (або "CKR-5" або "CCCKR-5") [MIP-la, RANTES, MIP-lp] (Sanson, et al., Biochemistry, 35, 3362-3367 (1996)); CCR-6 (або "CKR-6" або "CC-CKR-6") [LARC] (Baba et al., J. Biol. Chem., 272, 14893-14898 (1997)); CCR7 (або "CKR-7 "або" CC-CKR-7 ") [ELC] (Yoshie et al., J. Leukoc. Biol. 62, 634-644 (1997)); CCR-8 (або" CKR-8 "або" CC-CKR-8 ") [1-309, TARC, MIP-1p] (Napolitano et al., J. Immunol., 157, 27592763 (1996), Bernardini et al., Eur. J. Immunol., 28, 582-588 (1998)); CCR-10 (або "CKR-10" або "CC-CKR-10") [MCP-1, MCP-3] (Bonini et al, DNA and Cell Biol., 16, 1249-1256 (1997)); і CCR31 (або "CKR-11" або "CC-CKR-11") [MCP-1, MCP-2, MCP-4] (Schweickart et al., J Biol Chem, 275 9550-9556 (2000)). На додаток до хемокінових рецепторів ссавців рецептори Decoy CCX-CKR, D6 і DARC / Duffy, а також білки, що експресуються цитомегаловірусами ссавців, вірусами герпесу і поксвірусів, здатні зв'язуватися з хемокіновими рецепторами (огляди наведені у публікаціях Wells and Schwartz, Curr. Opin. Biotech., 8, 741-748 (1997); Comerford, Bioessays., 29 (3):237-47 (2007)). Хемокіни CC людини, такі як RANTES і MCP-3, можуть призвести до швидкої мобілізації кальцію з допомогою цих кодуємих вірусами рецепторів. Експресія рецептора може забезпечити інфікування, порушуючи що проводиться імунною системою нормальний контроль і відповідь на 1 UA 109290 C2 5 10 15 20 25 30 35 40 45 50 інфекцію. Крім того, хемокінові рецептори людини, такі як CXCR-4, CCR2, CCR3, CCR5 і CCR8, можуть виступати в якості сорецепторов інфікування клітин ссавців мікробами, наприклад, вірусами імунодефіциту людини (ВІЛ). Відзначено, що хемокінові рецептори є важливими медіаторами запальних, інфекційних та імунорегуляторних порушень і захворювань, включаючи астму та алергічні захворювання, а також аутоімунних патологій, такі як ревматоїдний артрит, дифузний токсичний зоб, хронічне обструктивне захворювання легень і атеросклероз. Наприклад, хемокіновий рецептор CCR3 експресується, зокрема, еозинофілами, базофілами, клітинами TH2, альвеолярними макрофагами, мастоцитами, епітеліальними клітинами, клітинами мікроглії, астроцитами і фібробластами. CCR3 грає головну роль у тяжінні еозинофілів до центрів алергічного запалення з наступною активацією цих клітин. Хемокінові ліганди CCR3 індукують швидке збільшення внутрішньоклітинної концентрації кальцію, посилений GTP обмін білків G, посилене фосфорилювання ERK, посилену інтерналізацію рецептора, зміна форми еозінофілу, посилену експресію молекул клітинної адгезії, дегрануляцію клітин і стимулювання міграції. Тому засоби, які інгібують хемокінові рецептори повинні бути корисні при таких порушеннях і захворюваннях. Крім того, засоби, які інгібують хемокінові рецептори, також повинні бути корисні при інфекційних захворюваннях, наприклад, для блокування інфікування експресуючих CCR3 клітин за допомогою ВІЛ або для попередження змін імунних відповідей клітин вірусами, такими як цитомегаловіруси. Тому CCR3 є важливою мішенню і антагонізм по відношенню до CCR3, ймовірно, ефективний при лікуванні запальних, еозинофільних, імунорегуляторних та інфекційних порушень і захворювань (Wegmann, Am J Respir Cell Mol Biol., 36(1):61-67 (2007); Fryer J Clin Invest., 116(1):228-236 (2006); De Lucca, Curr Opin Drug Discov Devel., 9(4):516-524 (2006). Тому в основу даного винаходу була покладена задача отримання антагоністів CCR3, переважно що характеризуються меншою кількістю побічних ефектів, які не тільки є активними інгібіторами CCR3, але також застосовні для приготування лікарського засобу, призначеного для попередження та / або лікування захворювань, при яких грає роль активність рецептора CCR3. Згідно винаходу неочікувано було встановлено, що заміщені піперидини формули 1 є вельми відповідні для використання в якості антагоністів CCR3, мають меншу кількість побічних ефектів, наприклад, інгібують норепінефрин (NET), допамін (DAT) або переносники зворотного захоплення серотоніну (5-HTT), як це описано в публікації Watson PS, Bioorg Med Chem Lett., 16 (21):5695-5699 (2006), або інгібують рецептори 5HT2A, 5HT2C або допаміну D2, як це описано в публікації De Lucca, J Med Chem., 48 (6):2194-2211 (2005), або інгібують канал hERG, як це описано в публікації De Lucca, Curr Opin Drug Discov Devel., 9 (4):516-524 (2006), або інгібують альфа-1B-адренергічний рецептор. Однак такі сполуки є основами і тому їх важко використовувати для приготування лікарського засобу, оскільки їх фізичні характеристики можуть викликати труднощі при виборі підходящої фармацевтичної форми. Це можуть бути труднощі, пов'язані зі структурою, такі як стабільність, чутливість до світла або затуманюючі за рахунок поглинання вологи, а також труднощі, пов'язані з фізичними характеристиками, наприклад, якщо сполука нерозчинна або не є підходящою для звичайних методик обробки, таких як розмел. Згідно винаходу неочікувано було встановлено, що заявлені спільні кристали або солі сполук формули 1 в достатній мірі задовольняють описаним вище критеріям використання у фармацевтиці для приготування лікарського засобу, наприклад, вони мають достатню стабільність, регульоване розпливання за рахунок поглинання вологи, розчинність, достатню для можливості застосування в якості лікарського засобу, та перебувають у твердому стані, необхідному для звичайних методик обробки, або у досить певній кристалічній формі. Детальний опис винаходу Об'єктом даного винаходу є спільні кристали сполук формули 1 O 3 R N N 1 (R )m N O * (HX)j 2 2a R N 2b R 1 UA 109290 C2 5 10 15 20 25 30 35 40 45 50 55 60 в якій 1 R означає C1-C6-алкіл, C1-C6-галогеналкіл, O-C1-C6-галогеналкіл, галоген; m дорівнює 1, 2 або 3; бажано 1 або 2; 2a 2b R і R всі незалежно вибрані із групи, що включає H, C1-C6-алкіл, C1-C6-алкеніл, C1-C62b.1 2b.2 алкініл, C3-C6-циклоалкіл, COO-C1-C6-алкіл, O-C1-C6-алкіл, CONR R , галоген; 2b.1 R означає H, C1-C6-алкіл, C0-C4-алкіл-C3-C6-циклоалкіл, C1-C6-галогеналкіл; 2b.2 R означає H, C1-C6-алкіл; 2b.1 2b.2 або R і R разом означають C3-C6-алкіленову групу, утворює разом з атомом азоту гетероциклічне кільце, де один атом вуглецю в кільці необов'язково замінений на атом кисню; 3 R означає H, C1-C6-алкіл; X означає аніон, вибраний із групи, що включає хлорид, бромід, йодид, сульфат, фосфат, метансульфонат, нітрат, малеат, ацетат, бензоат, цитрат, саліцилат, фумарат, тартрат, дибензоілтартрат, оксалат, сукцинат, бензоат і п-толуолсульфонат; бажано хлорид або дибензоілтартрат; j дорівнює 0, 0,5, 1, 1,5 або 2; бажано 1 або 2; з речовиною, що створює спільні кристали, вибраним з групи, що включає оротову кислоту, гіпурову кислоту, L-піроглутамінову кислоту, D-піроглутамінову кислоту, нікотинову кислоту, L(+)-аскорбінову кислоту, сахарин, піперазин, 3-гідрокси-2-нафтойну кислоту, муцинову (галактарову) кислоту, памоеву (ембонову) кислоту, стеаринову кислоту, холеву кислоту, дезоксихолеву кислоту, нікотинамід, ізонікотінамід, сукцінамід, урацил, L-лізин, L-пролін, Dвалін, L-аргінін, гліцин, переважно аскорбінову кислоту, муцинову кислоту, памоеву кислоту, сукцінамід, нікотинову кислоту, нікотинамід, ізонікотінамід, L-лізин, L-пролін. Ці спільні кристали застосовні для приготування лікарського засобу, призначеного для попередження та / або лікування захворювань, при яких грає роль активність рецептора CCR3. Іншим об'єктом даного винаходу є спільні кристали сполук формули 1, в якій 2a R означає H, C1-C6-алкіл, C1-C6-алкеніл, C1-C6-алкініл, C3-C6-циклоалкіл, O-C1-C6-алкіл, 2a.1 2a.2 CONR R ; 2a.1 R означає H, C1-C6-алкіл, C1-C6-галогеналкіл; 2a.2 R означає H, C1-C6-алкіл; 2b R означає H, C1-C6-алкіл, C1-C6-алкеніл, C1-C6-алкініл, C3-C6-циклоалкіл, COO-C1-C6-алкіл, 2b.1 2b.2 O-C1-C6-алкіл, CONR R , галоген; 2b.1 R означає H, C1-C6-алкіл, C0-C4-алкіл-C3-C6-циклоалкіл, C1-C6-галогеналкіл; 2b.2 R означає H, C1-C6-алкіл; 2b.1 2b.2 або R і R разом означають C3-C6-алкіленову групу, утворює разом з атомом азоту гетероциклічне кільце, де один атом вуглецю в кільці необов'язково замінений на атом кисню;і решта залишків є такими, як визначено вище. Іншим об'єктом даного винаходу є спільні кристали сполук формули 1, в якій 2a 2a.1 2a.2 R означає H, C1-C6-алкіл, C1-C6-алкініл, C3-C6-циклоалкіл, O-C1-C6-алкіл, CONR R ; 2a.1 R означає C1-C6-алкіл; 2a.2 R означає H; 2b 2b.1 2b.2 R означає H, C1-C6-алкіл, O-C1-C6-алкіл, CONR R ; 2b.1 R означає C1-C6-алкіл, C0-C4-алкіл-C3-C6-циклоалкіл, C1-C6-галогеналкіл; 2b.2 R означає H, C1-C6-алкіл; 2b.1 2b.2 або R іR разом означають C3-C6-алкіленову групу, що утворює разом з атомом азоту гетероциклічне кільце, де один атом вуглецю в кільці необов'язково замінений на атом кисню; і решта залишків є такими, як визначено вище. Іншим об'єктом даного винаходу є спільні кристали сполук формули 1, в якій 2a 2a.1 2a.2 R означає H, C1-C4-алкіл, C1-C4-алкініл, C3-C6-циклоалкіл, O-C1-C4-алкіл, CONR R ; 2a.1 R означає C1-C4-алкіл; 2a.2 R означає H; 2b 2b.1 2b.2 R означає H, C1-C4-алкіл, O-C1-C4-алкіл, CONR R ; 2b.1 R означає C1-C4-алкіл, C0-C4-алкіл-C3-C6-циклоалкіл, C1-C4-галогеналкіл; 2b.2 R означає H, C1-C4-алкіл; 2b.1 2b.2 або R іR разом означають C3-C6-алкіленову групу, що утворює разом з атомом азоту гетероциклічне кільце, де один атом вуглецю в кільці необов'язково замінений на атом кисню; і решта залишків є такими, як визначено вище. Іншим об'єктом даного винаходу є спільні кристали сполук формули 1, в якій 2a R означає H, C1-C4-алкіл, 2b 2b.1 2b.2 R означає H, CONR R ; 3 UA 109290 C2 2b.1 5 10 15 20 25 30 35 40 45 R означає C1-C4-алкіл, C0-C4-алкіл-C3-C6-циклоалкіл, C1-C4-галогеналкіл; 2b.2 R означає H, C1-C4-алкіл; 2b.1 2b.2 або R іR разом означають C3-C6-алкіленову групу, що утворює разом з атомом азоту гетероциклічне кільце, де один атом вуглецю в кільці необов'язково замінений на атом кисню; і решта залишків є такими, як визначено вище. Іншим об'єктом даного винаходу є спільні кристали сполук формули 1, в якій 1 R означає C1-C6-алкіл, C1-C6-галогеналкіл, O-C1-C6-галогеналкіл, галоген; m дорівнює 1 або 2; 2a R означає H, C1-C4-алкіл; 2b 2b.1 2b.2 R означає H, CONR R ; 2b.1 R означає C1-C4-алкіл, C0-C4-алкіл-C3-C6-циклоалкіл, C1-C4-галогеналкіл; 2b.2 R означає H, C1-C4-алкіл; 2b.1 2b.2 або R іR разом означають C3-C6-алкіленову групу, що утворює разом з атомом азоту гетероциклічне кільце, де один атом вуглецю в кільці необов'язково замінений на атом кисню; 3 R означає H, C1-C6-алкіл; X означає аніон, вибраний із групи, що включає хлорид або дибензоилтартрат; j дорівнює 1 або 2. Іншим об'єктом даного винаходу є спільні кристали сполук формули 1, в якій 2a R означає H, C1-C4-алкіл; бажано метил, етил, пропіл; 2b 2b.1 2b.2 R означає H, CONR R ; 2b.1 R означає C1-C4-алкіл; бажано метил, етил, пропіл; 2b.2 R означає C1-C4-алкіл; бажано метил, етил, пропіл; і решта залишків є такими, як визначено вище. Іншим об'єктом даного винаходу є спільні кристали сполук формули 1, в якій 2a R означає H, C1-C4-алкіл; бажано метил, етил, пропіл; 2b 2b.1 2b.2 R означає H, CONR R ; 2b.1 R означає C0-C4-алкіл-C3-C6-циклоалкіл; 2b.2 R означає H, C1-C4-алкіл; бажано H, метил, етил, пропіл; і решта залишків є такими, як визначено вище. Іншим об'єктом даного винаходу є спільні кристали сполук формули 1, в якій 2a R означає H, C1-C4-алкіл; бажано метил, етил, пропіл; 2b 2b.1 2b.2 R означає H, CONR R ; 2b.1 R означає C1-C4-галогеналкіл; 2b.2 R означає H, C1-C4-алкіл; бажано H, метил, етил, пропіл; і решта залишків є такими, як визначено вище. Іншим об'єктом даного винаходу є спільні кристали сполук формули 1, в якій 2b.1 2b.2 R і R разом означають C3-C6-алкіленову групу, що утворює разом з атомом азоту гетероциклічне кільце, де один атом вуглецю в кільці необов'язково замінений на атом кисню; і решта залишків є такими, як визначено вище. 1 2a 2b Іншим об'єктом даного винаходу є спільні кристали сполук формули 1, в якій R , m, R , R , 3 R , X і j є такими, як визначено вище, і речовину, що утворює спільні кристали, вибрано з групи, що включає аскорбінову кислоту, памоеву кислоту, сукцінамід, нікотинову кислоту, нікотинамід, ізонікотінамід, L-лізин, L-пролін або їх гідрати, або гідрохлориди. 2a 2b 3 Іншим об'єктом даного винаходу є спільні кристали сполук формули 1a, в якій R , R , R , X і j є такими, як визначено вище O N H N N O Cl N * (HX)j 50 2a R 2b R 1a. Іншим об'єктом даного винаходу є спільні кристали сполук формули 1a, в якій 2a R означає H, C1-C4-алкіл; бажано метил, етил, пропіл; 2b 2b.1 2b.2 R означає H, CONR R ; 2b.1 R означає C1-C4-алкіл; бажано метил, етил, пропіл; 2b.2 R означає C1-C4-алкіл; бажано метил, етил, пропіл; і решта залишків є такими, як визначено вище. 4 UA 109290 C2 5 10 15 20 25 30 Іншим об'єктом даного винаходу є спільні кристали сполук формули 1a, в якій 2a R означає H, C1-C4-алкіл; бажано метил, етил, пропіл; 2b 2b.1 2b.2 R означає H, CONR R ; 2b.1 R означає C0-C4-алкіл-C3-C6-циклоалкіл; 2b.2 R означає H, C1-C4-алкіл; бажано H, метил, етил, пропіл; і решта залишків є такими, як визначено вище. Іншим об'єктом даного винаходу є спільні кристали сполук формули 1a, в якій 2a R означає H, C1-C4-алкіл; бажано метил, етил, пропіл; 2b 2b.1 2b.2 R означає H, CONR R ; 2b.1 R означає C1-C4-галогеналкіл; 2b.2 R означає H, C1-C4-алкіл; бажано H, метил, етил, пропіл; і решта залишків є такими, як визначено вище. Іншим об'єктом даного винаходу є спільні кристали сполук формули 1a, в якій 2b.1 2b.2 R і R разом означають C3-C6-алкіленову групу, що утворює разом з атомом азоту гетероциклічне кільце, де один атом вуглецю в кільці необов'язково замінений на атом кисню; і решта залишків є такими, як визначено вище. Вільні основи сполук формули 1 (j=0) часто є аморфними сполуками і їх використовують в способі отримання спільних кристалів, проте солі сполук формули 1 є бажаними для способу отримання спільних кристалів. Тому іншим об'єктом даного винаходу є солі сполук формули 1, в 1 2a 2b 3 якій R , m, R , R , R є такими, як визначено вище для спільних кристалів, іX означає аніон, вибраний з групи, що включає хлорид, бромід, йодид, сульфат, фосфат, метансульфонат, нітрат, малеат, ацетат, бензоат, цитрат, саліцилат, фумарат, тартрат, дібензоілтартрат, оксалат, сукцинат, бензоат і п-толуолсульфонат; бажано хлорид або дібензоілтартрат; j дорівнює 0, 0,5, 1, 1,5 або 2; бажано 1 або 2. 1 2a 2b 3 Іншим об'єктом даного винаходу є солі сполук формули 1, в якій R , m, R , R , R є такими, як визначено вище для спільних кристалів, іX означає аніон, вибраний з групи, що включає хлорид або дибензоілтартрат; j дорівнює 1 або 2. 1 2a 2b 3 Іншим об'єктом даного винаходу є солі сполук формули 1, в якій R , m, R , R , R є такими, як визначено вище для солей, і X означає хлорид і j дорівнює 2. 1 2a 2b 3 Іншим об'єктом даного винаходу є солі сполук формули 1, в якій R , m, R , R , R є такими, як визначено вище для солей, і X означає дибензоілтартрат і j дорівнює 1. 2a 2b 3 Іншим об'єктом даного винаходу є солі сполук формули 1a, в якій R , R , R , X і j є такими, як визначено вище O N H N N O Cl 35 40 45 50 * (HX)j 2a R N 2b R 1a. Іншим об'єктом даного винаходу є солі сполук формули 1a, в якій 2a R означає H, C1-C4-алкіл; бажано метил, етил, пропіл; 2b 2b.1 2b.2 R означає H, CONR R ; 2b.1 R означає C1-C4-алкіл; бажано метил, етил, пропіл; 2b.2 R означає C1-C4-алкіл; бажано метил, етил, пропіл; і решта залишків є такими, як визначено вище. Іншим об'єктом даного винаходу є солі сполук формули 1a, в якій 2a R означає H, C1-C4-алкіл; бажано метил, етил, пропіл; 2b 2b.1 2b.2 R означає H, CONR R ; 2b.1 R означає C0-C4-алкіл-C3-C6-циклоалкіл; 2b.2 R означає H, C1-C4-алкіл; бажано H, метил, етил, пропіл; і решта залишків є такими, як визначено вище. Іншим об'єктом даного винаходу є солі сполук формули 1a, в якій 2a R означає H, C1-C4-алкіл; бажано метил, етил, пропіл; 2b 2b.1 2b.2 R означає H, CONR R ; 2b.1 R означає C1-C4-галогеналкіл; 2b.2 R означає H, C1-C4-алкіл; бажано H, метил, етил, пропіл; 5 UA 109290 C2 5 10 15 20 25 30 35 40 і решта залишків є такими, як визначено вище. Іншим об'єктом даного винаходу є солі сполук формули 1a, в якій 2b.1 2b.2 R і R разом означають C3-C6-алкіленову групу, що утворює разом з атомом азоту гетероциклічне кільце, де один атом вуглецю в кільці необов'язково замінений на атом кисню; і решта залишків є такими, як визначено вище. 1 2a 2b 3 Іншим об'єктом даного винаходу є солі сполук формули 1a, в якій R , m, R , R , R є такими, як визначено вище для солей, і X означає хлорид і j дорівнює 2. 1 2a 2b 3 Іншим об'єктом даного винаходу є солі сполук формули 1a, в якій R , m, R , R , R є такими, як визначено вище для солей, і X означає дибензоілтартрат і j дорівнює 1. Іншим 1 2a 2b 3 об'єктом даного винаходу є солі сполук формули 1a, в якій R , m, R , R , R є такими, як визначено вище для солей, і X означає (S) - (S) - (+) -2,3-дибензоілтартрат і j дорівнює 1. Зазначені вище солі також застосовні для приготування лікарського засобу, призначеного для попередження та / або лікування захворювань, при яких грає роль активність рецептора CCR3. Іншим об'єктом даного винаходу є спільні кристали або солі сполук прикладів 1-36, наведених нижче у розділі "Синтез сполук прикладів" з кислотою (HX) j, де X означає аніон, вибраний з групи, що включає хлорид, бромід, йодид, сульфат, фосфат, метансульфонат, нітрат, малеат, ацетат, бензоат, цитрат, саліцилат, фумарат, тартрат, дибензоілтартрат, оксалат, сукцинат, бензоат і п-толуолсульфонат; бажано хлорид або дибензоілтартрат, і j дорівнює 0, 0,5, 1, 1,5 або 2; бажано 1 або 2; і, у разі спільних кристалів, з речовиною, що створює спільні кристали, вибраним з групи, що включає оротову кислоту, гіпурову кислоту, Lпіроглутамінову кислоту, D-піроглутамінову кислоту, нікотинову кислоту, L-(+) -аскорбінову кислоту, сахарин, піперазин, 3-гідрокси-2-нафтойну кислоту, муцинову (галактарову) кислоту, памоеву (ембонову) кислоту, стеаринову кислоту, холеву кислоту, дезоксихолеву кислоту, нікотинамід, ізонікотінамід, сукцінамід, урацил, L-лізин, L-пролін, D-валін, L-аргінін, гліцин, бажано аскорбінову кислоту, муцинову кислоту, памоеву кислоту, сукцінамід, нікотинову кислоту, нікотинамід, ізонікотінамід, L-лізин, L-пролін. Іншим об'єктом даного винаходу є спільні кристали або солі сполук прикладів 1-36, наведених нижче у розділі "Синтез сполук прикладів" з кислотою (HX) j, де X означає аніон, вибраний з групи, що включає хлорид або дибензоілтартрат, і j дорівнює 1 або 2; і, у разі спільних кристалів, з речовиною, що створює спільні кристали, вибраним з групи, що включає аскорбінову кислоту, муцинову кислоту, памоеву кислоту, сукцінамід, нікотинову кислоту, нікотинамід, ізонікотінамід, L-лізин, L-пролін. Дигідрохлорид і (S) - (S) - (+) -2,3-дибензоілтартрат сполуки формули 1, 1a або сполук прикладів 1-36, наведених нижче у розділі "Синтез сполук прикладів", є переважними прикладами сполук, пропонованих у даному винаході, які застосовні для отримання / приготування описаних вище спільних кристалів і / або для приготування лікарського засобу, призначеного для попередження та / або лікування захворювань, при яких грає роль активність рецептора CCR3. Якщо в контексті даного винаходу вказаний дибензоілтартрат, то бажаним енантіомером дибензоілтартрату завжди є (S) - (S) - (+) -2,3-дибензоілтартрат. Іншим об'єктом даного винаходу є нові проміжні продукти для отримання сполук формули 1. Ці проміжні продукти можна отримати з наявних у продажу едуктів так, як описано нижче в експериментальному розділі. 45 N O Cl N O N O N N H I12 I13 6 N H2N N I14 UA 109290 C2 COOMe MeOOC O NH N Cl 10 15 20 25 30 35 40 45 O COOMe N COOH N N Cl Cl I3'-Me 5 N I4' A' У цьому контексті апостроф (') вказує на відміну назви певної структури, представленої в експериментальному розділі, від назви нового проміжного продукту. Відмінність полягає в тому, що R1 означає тільки Cl і Me і m дорівнює 1. Терміни та визначення, що використовуються Термінам, спеціально не визначеними у цьому винаході, слід надавати значення, які їм повинен надавати фахівець у даній галузі техніки відповідно з розкриттям і контекстом. Однак, якщо не вказано інше, то при використанні в описі наведені нижче терміни мають зазначеними значеннями і прийнята зазначена нижче номенклатура. У групах, радикалах або фрагментах, визначених нижче, кількість атомів вуглецю часто вказується перед групою, наприклад, C1-C6-алкіл означає алкільну групу або радикал, що містить від 1 до 6 атомів вуглецю. Зазвичай в групах, що містять дві або більшу кількість підгрупи, перша названа група є місцем приєднання радикала, наприклад, замісник "C1-C3алкіларил" означає арильну групу, яка пов'язана з C1-C3-алкільного групою, остання з яких пов'язана з ядром або групою, до якої приєднано замісник. У випадку, якщо сполука, пропонована в даному винаході, описана за допомогою хімічного назви і у вигляді формули, то разі будь-яких відмінностей визначальною є формула. Знак зірочки можна використовувати в субформулах для позначення зв'язку, яка з'єднана з ядром молекули, як це визначено. Якщо спеціально не вказано інше, то в описі і прикладеній формулі винаходу певна хімічна формула або назва сполуки включає його таутомери і всі стереоізомери, оптичні та геометричні ізомери (наприклад, енантіомери, діастереоізомери, E / Z-ізомери і т. п.) і рацемати, а також суміші окремих енантіомерів у різних співвідношеннях, суміші діастереоізомери, або суміші будь-яких описаних вище форм, в яких існують такі ізомери та енантіомери, а також його солі, включаючи її фармацевтично прийнятні солі та її сольвати, такі як, наприклад, гідрати, включаючи сольвати вільних сполук або сольвати солей сполуки. Термін "галоген" зазвичай означає фтор, хлор, бром і йод. Термін "C1-Cn-алкіл", де n є цілим числом, що дорівнює від 2 до n, окремо або в комбінації з іншим радикалом, означає ациклічний, насичений, що має розгалужений або лінійний ланцюг вуглеводневий радикал, що містить від 1 до n атомів C. Наприклад, термін C 1-С5-алкіл включає радикали H3C-, H3C-CH2-, H3C-CH2-CH2-, H3C-CH(CH3)-, H3C-CH2-CH2-CH2-, H3C-CH2-CH(CH3)-, H3C-CH(CH3)-CH2-, H3C-C(CH3)2-, H3C-CH2-CH2-CH2-CH2-, H3C-CH2-CH2-CH(CH3)-, H3C-CH2CH(CH3)-CH2-, H3C-CH(CH3)-CH2-CH2-, H3C-CH2-C(CH3)2-, H3C-C(CH3)2-CH2-, H3C-CH(CH3)CH(CH3)- і H3C-CH2-CH(CH2CH3)-. Термін "C1-Cn-галогеналкіл", де n є цілим числом, що дорівнює від 2 до n, окремо або в комбінації з іншим радикалом, означає ациклічний, насичений, що має розгалужену або лінійну ланцюгом вуглеводневий радикал, що містить від 1 до n атомів C, в якому один або більшу кількість атомів водню замінені атомом галогену, вибраним з групи, що включає фтор, хлор або бром, бажано фтор і хлор, особливо бажано фтор. приклади включають: CH 2F, CHF2, CF3. Термін "C1-Cn-алкілен", де n є цілим числом, що дорівнює від 2 до n, окремо або в комбінації з іншим радикалом, означає ациклічний що має лінійний або розгалужений ланцюг двовалентний алкільний радикал, що містить від 1 до n атомів вуглецю. Наприклад, термін C 1C4-алкілен включает -CH2-, -CH2-CH2-, -CH(CH3)-, -CH2-CH2-CH2-, -C(CH3)2-, CH(CH2CH3)-, CH(CH3)-CH2-, -CH2-CH(CH3)-, -CH2-CH2-CH2-CH2-, -CH2-CH2-CH(CH3)-, -CH(CH3)-CH2-CH2-, -CH2CH(CH3)-CH2-, -CH2-C(CH3)2-, -C(CH3)2-CH2-, -CH(CH3)-CH(CH3)-, -CH2-CH(CH2CH3)-, CH(CH2CH3)-CH2-, CH(CH2CH2CH3)-, -CH(CH(CH3))2- і -C(CH3)(CH2CH3)-. Термін "C2-Cn-алкеніл" використовують для позначення групи, визначеної у визначенні для "C1-Cn-алкілу", яка містить щонайменше 2 атоми вуглецю, якщо щонайменше 2 з цих атомів вуглецю зазначеної групи пов'язані один з одним подвійним зв'язком. 7 UA 109290 C2 5 10 15 Термін "C2-Cn-алкініл" використовують для позначення групи, визначеної у визначенні для "C1-Cn-алкілу", яка містить щонайменше 2 атоми вуглецю, якщо щонайменше 2 з цих атомів вуглецю зазначеної групи пов'язані один з одним потрійним зв'язком. Термін "C3-Cn-циклоалкіл", де n є цілим числом, що дорівнює від 4 до n, окремо або в комбінації з іншим радикалом, означає циклічний, насичений, що має нерозгалужений ланцюг вуглеводневий радикал, що містить від 3 до n атомів C. Наприклад, термін C3-С7-циклоалкіл включає циклопропіл, циклобутил, циклопентил, циклогексил і циклогептіл. Отримання Отримання сполук формули 1 Сполуки прикладів, запропоновані в даному винаході, представлені загальною структурою 1, 1 2a 2b можна синтезувати за наведеними нижче методиками 1-6, де m, R , R і R є такими, як визначено вище, і Xs означає хлор або бром і Y означає метил або етил. У цих методиках прямо або побічно використовують проміжний продукт A, який синтезують у відповідності зі схемою I. Якщо не вказано інше, вихідні речовини є у продажу. Схема I BuO 2tC CO 2Me HO 2C CO 2Me 1 (R ) m X s O 1 (R ) m NH Стадія 2 Стадія 1 N O N (R ) m CO 2Me N 1 1 N (R ) m I2 I1 Стадія 4 N 1 (R ) m NH Стадія 3 I3 O N (R ) m CO 2H N Стадія 5 1 Проміжний продукт A I4 Методика 1 O N CO 2NH 2 Стадія 1 Проміжний продукт A O H N 1 N O 1 (R ) m I5 CO 2Y N I6 8 X N Стадія 2 (R ) m N s UA 109290 C2 Стадія 3 H N O N R N Стадія 4 O O N R 2a Стадія 5 N O CO 2Y N 1 (R ) m H N 2a N 1 (R ) m Сполуки прикладів C O 2H I8 I7 Методика 2 Стадія 1 Проміжний продукт A Стадія 2 Стадія 3 I7 Сполуки прикладів I8 Методика 3A Стадія 1 Проміжнийй продукт A 5 Сполуки прикладів Методика 3B Стадія 2 Стадія 1 Проміжний продукт A Сполуки прикладів I11 Методика 4 O Стадія 1 H N N X N O O Стадія 2 H N N N X Стадія 3 O I6 1 (R ) m CO 2H N 1 (R ) m I10 I9 10 R 2b N Методика 5 Стадія 1 I5 Стадія 2 Стадія 3 I7 I8 Методика 6 9 Сполуки прикладів Сполуки прикладів UA 109290 C2 O Стадія 1 H N SiMe 3 N N Стадія 2 O I6 1 (R ) m CO 2Y N I15 1 5 10 15 20 25 30 35 40 45 Синтез проміжного продукту A (як приклад R означає 4-хлор-3-метил) Стадія 1: 4-Хлор-3-метилбензилбромід (20 г) [синтезують по літературній методиці: JL Kelley, J.A. Linn, J.W.T. Selway, J. Med. Chem. 1989, 32 (8), 1757-1763], 4-піперідон (22 г), K2CO3 (26 г) в ацетонітрилі (300 мл) нагрівають при 50° C протягом 14 год. Суспензію фільтрують і фільтрат концентрують у вакуумі. Залишок очищають за допомогою флеш-хроматографії (циклогексан / EtOAc 1:1) і отримують проміжний продукт I1 (17,4 г). Стадія 2: Проміжний продукт I1 (10 г) і DH-Glu (OtBu)-OMe (10,8 г) розчиняють у ДМФ (N, Nдиметилформамід) (200 мл) і HOAc (5 мл). Потім додають молекулярні сита (1,0 г, 4Ǻ, порошкоподібні) і суспензію перемішують протягом ночі. Додають триацетоксиборогідрид натрію (37,5 г) і суспензію перемішують до завершення перетворення утвореного проміжного іміну. Шляхом повільного додавання водного розчину NaHCO3 середовище підлужують, потім додатково додають воду і дихлорметан (500 мл). Органічну фазу відокремлюють і водну фазу екстрагують дихлорметаном (500 мл). Органічну фазу промивають розсолом, сушать і концентрують у вакуумі і отримують проміжний продукт I2 (19,5 г). Стадія 3: Проміжний продукт I2 (19,5 г, чистота 74 %) розчиняють у дихлорметані (40 мл) і трифтороцтовій кислоті (ТФК, 20 мл). Розчин перемішують при 25° C протягом 14 год., потім додатково додають ТФК (40 мл) і розчин продовжують перемішувати протягом ще 7 г. Потім реакційну суміш концентрують у вакуумі, розчиняють у толуолі і повторно концентрують і отримують проміжний продукт I3 (29,5 г). Стадія 4: Проміжний продукт I3 (29 г, чистота 55 %) розчиняють в суміші дихлорметану (100 мл) і ДІПЕА (діізопропілетіламін) (22 мл). Додають TBTU (O-(бензотриазол-1-іл)-N, N,N',N'тетраметилуронійтетрафторборат) (15 г) і розчин перемішують протягом 30 хв. Потім додають дихлорметан (150 мл), воду (100 мл) і насичений розчин NaHCO3 (100 мл), органічну фазу відокремлюють і водну фазу один раз екстрагують дихлорметаном (100 мл). Органічну фазу сушать і концентрують і отримують масло, яке потім фракционируют за допомогою ВЕРХ (високоефективна рідинна хроматографія) з оберненою фазою. Шукані фракції концентрують у вакуумі, потім середовище підлужують шляхом додавання розчину NaHCO3 і продукт екстрагують дихлорметаном і отримують проміжний продукт I4 (8,1 г). Стадія 5: Проміжний продукт I4 (7 г) розчиняють у діоксані (50 мл). Додають LiOH (2,5 M водний розчин, 23 мл) і воду (20 мл) і перемішують при кімнатній температурі протягом ночі. Розчин підкислюють 4 н. водним розчином HCl і потім концентрують у вакуумі. Залишок розчиняють у воді, ацетонітрилі і невеликій кількості діоксану і ліофілізують і отримують проміжний продукт A (10,4 г, чистота 71 %). 1 Альтернативний шлях синтезу проміжного продукту A (як приклад R означає 4-хлор-3метил) Стадія 1: 4-Хлор-3-метилбензилхлорид (85,7 г), гідрат 4-піперидонгідрохлориду (80,5 г) і K2CO3 (141,8 г) в суміші діоксану / вода складу 1:1 (600 мл) кип'ятять із зворотним холодильником протягом 3,5 г. Суспензію охолоджують до кімнатної температури і додають воду (200 мл). Потім суміш екстрагують толуолом (2400 мл). Об'єднані органічні фази промивають розсолом (2400 мл), сушать над Na2SO4 і фільтрують. Після випарювання насухо отримують проміжний продукт I1 [110,8 г, Rf=0,27 (ТШХ (тонкошарова хроматографія), діоксид кремнію, ПЕ (петролейний ефір) / EtOAc=7:3)] і. Стадія 2+3+4: D-H-Glu(OMe)-OMeHCl (11,4 г) і проміжний продукт I1 (11,4 г) розчиняють у ДМФ (35 мл) і перемішують при кімнатній температурі протягом 2 г. Потім при температурі нижче 15° C додають розчин NaBH (OAc) 3 (36,8 г) в ДМФ (40 мл). Суміш нагрівають до кімнатної температури і перемішують протягом 30 хв. Після цього сполуку формули I3'-Me 10 UA 109290 C2 COOMe MeOOC NH N Cl 5 10 15 20 25 30 35 40 45 50 I3'-Me можна виділити або проміжний продукт не виділяють і додають AcOH (0,3 мл) і суміш нагрівають при 105° C протягом 1,5 г. Суміш охолоджують до кімнатної температури і додають холодну воду (188 мл). Значення pH доводять до дорівнюєго 8 шляхом додавання NaOH (50 % розчин у воді). На закінчення суміш екстрагують трет-бутилметиловим ефіром (375 мл), об'єднані органічні фази промивають розсолом (150 мл), Сушать над Na2SO4 і фільтрують. Після випарювання насухо отримують проміжний продукт I4 [15,9 г, ЕІ = 98,3 %, Rf=0,30 (ТШХ, діоксид кремнію, толуол /EtOH=85:15)]. Стадія 5: Проміжний продукт I4 (150,3 г) розчиняють у MeOH (526 мл), додають 4 н. розчин NaOH (145,7 мл) і суміш кип'ятять із зворотним холодильником протягом 2 г. Потім MeOH відганяють і додають воду (500 мл). Суміш екстрагують трет-бутилметиловим ефіром (2300 мл). Водну фазу розбавляють водою (402 мл) і значення pH доводять до дорівнюєго 6,5 шляхом додавання 4 н. розчину HCl. Суспензію охолоджують до 5° C і перемішують протягом ще 2 г. На закінчення суміш фільтрують, залишок промивають водою і сушать і отримують проміжний продукт A [107,8 г, ЕІ (енантіомерний надлишок) ≥ 99,0 %, tпл температура плавлення): 260±3° C, Rf=0,2 (ТШХ, діоксид кремнію, толуол/EtOH=9:1]). Синтез сполук прикладів 1 2a Синтез сполук прикладів за методикою 1 (як приклад R означає 4-хлор-3-метил; R 2b S означає етил; R означає N, N-диметилкарбоксамідну групу; X означає бром; Y означає метил). Стадія 1: Проміжний продукт A у вигляді її солі з N, N-діізопропілетіламіном (500 мг) в інертній атмосфері суспендується в сухому ДМФ (7 мл) і додають TBTU (836 мг), потім N, Nдіізопропілетіламін (0,53 мл). Після перемішування при кімнатній температурі протягом 1 год. додають гексаметілдісілазан (0,44 мл) і суміш перемішують протягом 6 г. Додають ще порції TBTU (334 мг) і гексаметілдісілазану (0,22 мл) і реакційну суміш перемішують протягом ще 18 год.. Розчинник випарюють при зниженому тиску і залишок піддають розподілу між насиченим водним розчином NaHCO3 і EtOAc. Шари розділяють і водну фазу екстрагують за допомогою EtOAc. Об'єднані органічні екстракти промивають розсолом, сушать над Na 2SO4, фільтрують і розчинник випарюють при зниженому тиску. Неочищену речовину очищають за допомогою флеш-хроматографії (картридж Isolute ® з силікагелем, 20 г; елюент: діхлорметан/MeOH/NH4OH 95/5/0, 5) і отримують сполуку I5 (295 мг). НВРХ (рідинна хроматографія надвисокого тиску) (Rt) = 1,24 хв (методика M) Стадія 2: При перемішуванні до розчину цітразінової кислоти (15 г) додають оксиброміди фосфору (45 г) і суміш нагрівають до 140° C. Через 14 год. суміш охолоджують до 0° C і при енергійному перемішуванні обережно додають MeOH (100 мл). Потім суміш виливають в охолоджений (0° C) водний розчин карбонату натрію (1M, 500 мл) і додають хлороформ (500 мл). Двофазну суміш фільтрують і органічний шар відокремлюють. Після фільтрування через деревне вугілля розчин концентрують у вакуумі. Залишок очищають за допомогою РХСТ (рідинна хроматографія середнього тиску) (дихлорметан: MeOH від 100:3 до 100:6) і отримують метил 2,6-дібромізонікотінат (13,7 г). ВЕРХ (Rt) = 1,62 (методика D). При перемішуванні в атмосфері аргону до розчину сполуки I5 (2,6 г) у діоксані (30 мл) додають метил 2,6-дібромізонікотінату (2,2 г), ацетат паладію (167 мг), Xanthphos (432 мг) і Cs2CO3 (5,6 г) і суміш кип'ятять із зворотним холодильником протягом 1 г. Суміші дають охолонути до кімнатної температури і потім додають до води і екстрагують за допомогою EtOAc. Органічні екстракти промивають розсолом, сушать над Na2SO4, фільтрують і розчинник випарюють при зниженому тиску. Неочищений продукт очищають за допомогою ВЕРХ (методика E) і отримують I6 (0,6 г). Стадія 3: При перемішуванні до розчину сполуки I5 (500 мг) в діоксані (10 мл) в атмосфері аргону додають 1,1 '-біс (дифенілфосфіно) ферроцендіхлорпалладій (II) (65 мг) і діетілцинк (1M розчин в гексані, 1, 1 мл). Суміш кип'ятять із зворотним холодильником протягом 2 год., потім їй 11 UA 109290 C2 5 10 15 20 25 30 35 40 45 50 55 60 дають охолонути до КТ (кімнатна температура). Потім реакцію зупиняють водним розчином NH4Cl і суміш екстрагують за допомогою EtOAc. Органічні екстракти промивають розсолом, сушать над Na2SO4, фільтрують і розчинник випарюють при зниженому тиску і отримують сполуку I7. Стадія 4: (Використовують методику, описану на стадії 5 методики синтезу проміжного продукту A, реакцію проводять при температурі 50 °C). Отримують сполуку I8 (137 мг). ВЕРХ (Rt) = 1,32 хв (методика D). Стадія 5: При перемішуванні до розчину сполуки I8 (800 мг) в ДМФ (10 мл) додають TBTU (772 мг), ДІПЕА (0,7 мл) і диметиламин (0,36 г). Через 2 год. реакцію зупиняють водою і суміш екстрагують за допомогою EtOAc. Органічні екстракти промивають розсолом, сушать над Na2SO4, фільтрують, і розчинник випарюють при зниженому тиску і отримують сполуку прикладу 25 (410 мг). ВЕРХ (Rt) = 1,32 хв (методика D). 1 2a Синтез сполук прикладів за методикою 2 (як приклад R означає 4-хлор-3-метил; R 2b означає водень; R означає N-метилкарбоксамідну групу; Y означає етил). Стадія 1: При перемішуванні до розчину проміжного продукту A (0,48 г) у дихлорметані (5 мл) додають оксалілхлорид (2M розчин у дихлорметані, 2,5 мл). Через 2 год. реакційну суміш концентрують при зниженому тиску. До реакційної суміші додають суспензію етилового ефіру 2аміноізонікотінової кислоти (0,51 г) у піридині (1 мл) і діоксані (2 мл) і цю суміш перемішують протягом 10 хв. Суміш концентрують при зниженому тиску і отримують сполуку I7 (0,3 г). ВЕРХ (Rt) = 1,37 хв (методика D). Стадія 2: (Використовують методику, описану на стадії 5 методики синтезу проміжного продукту A). Отримують сполуку I8 (55 мг). ВЕРХ (Rt) = 1,23 хв (методика D). Стадія 3: При перемішуванні до розчину сполуки I8 (55 мг) при кімнатній температурі додають ГАТУ (60 мг), ДМФ (1 мл) і ДІПЕА (0,07 мл). Через 5 хв додають метиламін (2M розчин в ТГФ (тетрагідрофуран), 0,2 мл). Ще через 5 хв додають воду і суміш підкислюють за допомогою ТФК. Неочищений продукт очищають за допомогою ВЕРХ і отримують сполуку прикладу 8 (50 мг). ВЕРХ (Rt) = 1,22 хв (методика D). Метиловий ефір 2-аміно-6-метілізонікотінової кислоти, який також є відповідним для використання на стадії 1, одержують у такий спосіб: Стадія a: 2-Хлор-6-метілізонікотінову кислоту (9 г), водний розчин аміаку (44 мл), Cu(II) SO4 (0,9 г) і сульфід натрію (0,32 г) поміщають в автоклав і нагрівають при 155° C протягом ночі. Неочищений продукт суспендують у воді і отримують 2-аміно-6-метилізонікотинову кислоту (3,6 г). ВЕРХ: Rt=0,37 хв (методика D) Стадія b: У 50 мл MeOH при кімнатній температурі по краплях додають ацетилхлорид (3 мл). Через 15 хв додають 2-аміно-6-метілізонікотінову кислоту (2,3 г) і суміш перемішують при 50° C протягом ночі. Після концентрування розчину отриманий залишок суспендують в ацетоні і потім фільтрують і сушать при 50° C у вакуумі і отримують метиловий ефір 2-аміно-6метілізонікотінової кислоти (4,1 г). ВЕРХ: Rt=0,91 хв (методика D) 1 2a Синтез сполук прикладів за методикою 3A (в якості прикладу R означає 4-хлор-3-метил; R 2b означає метил; R означає N, N-диметилкарбоксамідну групу). Стадія 1: Проміжний продукт A (8,30 г), 2-аміно-6, N, N-триметилізонікотинамід (4,24 г) і NEt3 (43 мл) змішують в абсолютному ТГФ (66 мл) і нагрівають до 55° C. Додають T3P (ангідрид пропілфосфонової кислоти) (50 % розчин у EtOAc, 56 мл) і реакційну суміш перемішують протягом 1 г. Після охолодження до кімнатної температури додають EtOAc (66 мл) і воду (50 мл). Фази розділяють і водну фазу екстрагують за допомогою EtOAc (1'50 мл). Об'єднані органічні фази промивають розсолом і сушать над Na2SO4. Після фільтрування, розчинник видаляють у вакуумі і отримують сполуку прикладу 11 [9,78 г, Rf=0,55 (ТШХ, діоксид кремнію, толуол/EtOH=3:2)]. Синтез дибензоілтартрату Сполуку прикладу 11 (200 мг), EtOH (0,8 мл) і воду (0,4 мл) змішують і нагрівають до 70° C. Додають розчин (S) - (S) - (+) -2,3-дибензоілвинної кислоти (175 мг) в EtOH (0,6 мл) і воді (0,6 мл). Після охолодження до кімнатної температури осад відфільтровують, промивають за допомогою EtOH/H2O (7:3) і сушать і отримують (S) - (S) - (+) -2,3-дибензоілтартрат сполуки прикладу 11 (200 мг). 1 2a Синтез сполук прикладів за методикою 3B (як приклад R означає 4-хлор-3-метил; R 2b означає метил; R означає N, N-диметилкарбоксамідну групу). Стадія 1: Проміжний продукт A (73,3 г) і NEt3 (117 мл) змішують в сухому ТГФ (440 мл) і додають T3P (50 % розчин у EtOAc, 246 мл). Суміш нагрівають при 50° C протягом 30 хв і додають метиловий ефір 2-аміно-6-метілізонікотінової кислоти (34,7 г). Після перемішування 12 UA 109290 C2 5 протягом ночі реакційну суміш охолоджують до кімнатної температури і додають воду (440 мл) і 4 н. розчин NaOH (52 мл). Фази розділяють і водну фазу екстрагують за допомогою iPrOAc (2220 мл). Об'єднані органічні фази промивають водою (2220 мл), сушать над Na2SO4, фільтрують і випарюють досуха і отримують проміжний продукт I11. [99,1 г, tпл: 155±3° C, Rf=0,29 (ТШХ, діоксид кремнію, толуол/EtOH=85:15)]. O O O O N N H N N Cl 10 15 20 25 30 35 I11 Стадія 2: Проміжний продукт I11 (138,6 г) суспендують у iPrOH (415 мл) і додають NaOH (50 % розчин у воді, 14,5 мл). Суміш нагрівають при 55° C протягом 1 г. Потім розчинник видаляють у вакуумі і залишок переганяють з iPrOH (2200 мл) и Me-ТГФ (1500 мл). Потім додають сухий Me-ТГФ (701 мл), Me2NH (2M розчин в ТГФ, 208 мл) і NEt3 (117 мл) і суміш нагрівають до 50° C. Додають T3P (50 % розчин у EtOAc, 327,4 мл) і реакційну суміш перемішують при 50° C протягом ще 1,5 г. Після охолодження до кімнатної температури додають воду (818 мл). Фази розділяють і водну фазу екстрагують за допомогою iPrOAc (2281 мл). Об'єднані органічні фази промивають водою (2'281 мл), сушать над Na2SO4, фільтрують і випарюють досуха. Залишок (неочищена сполука прикладу 11) розчиняють в ацетоні (1,46 л) і порціями додають HCl (2,98 M розчин в EtOAc, 240 мл). Суспензію перемішують при кімнатній температурі протягом 1 г. Осад відфільтровують, промивають ацетоном (100 мл) і суспендують у суміші ацетону (1,53 л) і абсолютного EtOH (180 мл) при 50° C протягом 30 хв. Потім суспензію охолоджують до 10° C і перемішують протягом 30 хв. Осад відфільтровують, промивають холодним ацетоном (200 мл) і ретельно сушать і отримують сполуку прикладу 11 у вигляді дигідрохлориду (117 г, ЕІ ≥ 99,9 %, tпл: 194±5° C), продукт також необов'язково може перебувати у вигляді гідрату дигідрохлориду сполуки прикладу 11, не володіє певною температурою плавлення. Синтез 2-аміно-6,N, N-триметилізонікотинаміду Стадія 1: 2-Хлор-6-метилізонікотинову кислоту [публікація: Sperber et al., JACS 1959, 81, 704-707] (96,1 г) суспендують у толуолі (480 мл) і додають ДМФ (0,5 мл). Після нагрівання до 85° C порціями додають SOCl2 (61,5 мл). Реакційну суміш кип'ятять із зворотним холодильником протягом 1,5 год. і потім охолоджують до кімнатної температури. Після видалення розчинника і надлишку реагенту у вакуумі залишок переганяють з толуолом (2200 мл) і на закінчення розчиняють у толуолі (300 мл). Потім отриманий вище розчин при температурі нижче 10° C додають до суміші Me2NH (2M розчин в ТГФ, 336 мл) і NEt3 (94 мл). Суміш нагрівають до кімнатної температури і перемішують протягом ще 30 хв. Додають воду (300 мл) і суміш екстрагують толуолом (3'200 мл). Об'єднані органічні фази промивають розсолом (1200 мл), сушать над Na2SO4, фільтрують і випарюють. Маслоподібними залишок обробляють нгептаном (288 мл) і додають затравочние кристали. Після перемішування при кімнатній температурі протягом 30 хв осад відфільтровують, промивають і сушать у вакуумі і отримують проміжний продукт I12 [93,7 г, tпл: 85±3 °C, Rf=0,22 (ТШХ, діоксид кремнію, ПЕ/EtOAc=1:1)]. 40 N O Cl N 13 I12 UA 109290 C2 5 Стадія 2: Проміжний продукт I12 (26,7 г), Cs2CO3 (70 г), Pd (OAc) 2 (302 мг) і (2-біфеніл)-дітрет-бутілфосфін (0,92 г) змішують в абсолютному діоксані (270 мл) і додають бензиламінів (22,3 мл). Реакційну суміш нагрівають при 100° C протягом ночі, охолоджують до кімнатної температури і фільтрують. Додають водний розчин HCl (2M розчин, 100 мл) і суміш екстрагують трет-бутилметиловим ефіром (70 мл). До водній фазі додають NaOH (4 н. Розчин, 55 мл). Після екстракції трет-бутилметиловим ефіром (370 мл) об'єднані органічні фази промивають розсолом, сушать над Na2SO4, фільтрують і випарюють досуха і отримують проміжний продукт I13 [23,0 г, tпл: 124±3° C, Rf=0,20 (ТШХ, діоксид кремнію, ПЕ /EtOAc=2:3)]. N O N H N 10 15 I13 Стадія 3: Проміжний продукт I13 (37,0 г) і Pd (OH) 2 / C суспендують в абсолютному EtOH 2 (185 мл) і AcOH (16 мл). Суміш гідрують при 70° C і тиску, дорівнює 60 фунт-сила/дюйм , до повного витрачення вихідних речовин. Суміш фільтрують і фільтрат випарюють досуха. Отриманий залишок розчиняють у дихлорметані (250 мл), промивають розчином Na2CO3 (10 % розчин у воді, 150 мл) і сушать над Na2SO4. Після фільтрування та випарювання виділяють 2аміно-6, N, N-триметилізонікотинамід I14 [22,2 г, t пл: 168±3 °C, Rf=0,15 (ТШХ, діоксид кремнію, інактивований за допомогою NEt3/ПЕ, EtOAc)]. N O 20 25 30 35 40 H2N N I14 Альтернативна методика: Проміжний продукт I12 (26,6 г), Cs2CO3 (48,9 г), бензофенонімін (25,0 г), Pd (OAc) 2 (0,60 г) і рацемічний БІНАФ (2,2 '-біс (дифенілфосфіно) -1,1 '-бінафтіл) (4,52 г) суспендують у толуолі (266 мл) і нагрівають при 100° C протягом 2 днів. Суміш охолоджують до кімнатної температури і фільтрують. До фільтрату додають 4 н. розчин HCl (67 мл) і суміш перемішують при кімнатній температурі протягом 30 хв. Додають воду (67 мл) і фази розділяють. Органічну фазу екстрагують водою (50 мл). Об'єднані водні фази промивають толуолом (100 мл). Після додавання 4 н. розчину NaOH (70 мл) лужну водну фазу екстрагують за допомогою CH2Cl2 (4100 мл). Об'єднані органічні фази промивають розсолом (100 мл), сушать над Na2SO4 і фільтрують. Після випарювання насухо виділяють 2-аміно-6, N, Nтриметилізонікотинамід I14 [22,1 г, Rf=0,15 (ТШХ, діоксид кремнію, інактивований за допомогою NEt3/ПЕ, EtOAc)]. Замість бензиламіну (використовується на стадії 1) або бензофеноніміну (використовується в альтернативній методиці), описаних вище, для синтезу 2-аміно-6, N, Nтриметилізонікотінаміду можна використовувати інше джерело N, таке як CH3CONH2 або CF3CONH2. 1 2a Синтез сполук прикладів за методикою 4 (як приклад R означає 3-метил-4-хлор; R 2b означає циклопропіл; R означає N, N-диметилкарбоксамідну групу; X означає бром і Y означає метил). Стадія 1: При перемішуванні до розчину сполуки I6 (90 мг) в ТГФ (3 мл) при кімнатній температурі додають LiOH (10 % водний розчин; 0,05 мл). Через 1 год. реакційну суміш нагрівають до 30° C і ще через 30 хв концентрують при зниженому тиску і отримують сполука I9 (110 мг). ВЕРХ (Rt) = 1,34 хв (методика D). Стадія 2: При перемішуванні до розчину сполуки I9 (80 мг) в дихлорметані (5 мл), що містить 14 UA 109290 C2 5 10 15 20 25 30 35 40 45 кілька крапель ДМФ, при кімнатній температурі додають ГАТУ (110 мг). Через 45 хв додають диметиламин (0,014 мл) і суміш перемішують протягом 2 г. Додатково додають ГАТУ (110 мг) і диметиламін (1 мл) і через 2 год. реакційну суміш додають до суміші вода / дихлорметан і фази розділяють з використанням картриджа Isolute HMN. Органічну фазу сушать над Na2SO4, фільтрують і розчинник випарюють при зниженому тиску. Очищення залишку за допомогою ВЕРХ дає сполуку I10 (20 мг). ВЕРХ (Rt) = 1,32 хв (методика D). Стадія 3: При перемішуванні до розчину бромціклопропану (0,039 мл) у ТГФ в атмосфері аргону при -78° C по краплях додають трет-бутиллітій (0,056 мл). Через 25 хв додають циклопропілбромід цинку (0,5 M розчин в ТГФ, 0,096 мл) і суміші дають нагрітися до КТ. Через 1 год. додають сполуку I10 (23 мг) і 1,1 '-біс (дифенілфосфіно) ферроцендіхлорпалладій (II) (3 мг). Ще через 35 хв додатково додають ціклопропілбромід цинку (0,5 M розчин в ТГФ, 0,096 мл) і ще через 1 год. додатково додають ціклопропілбромід цинку (0,5 M розчин в ТГФ, 0,096 мл) і суміш перемішують протягом ночі. Додатково додають ціклопропілбромід цинку (0,5 M розчин в ТГФ, 0,24 мл) і через 4 год. суміш розбавляють за допомогою ТГФ і фільтрують. Очищення за допомогою ВЕРХ дає сполуку прикладу 32 (7 мг). ВЕРХ (R t) = 1,34 хв (методика D). 1 2a Синтез сполук прикладів за методикою 5 (якприклад R означає 4-хлор-3-метил; R 2b означає метоксигрупу; R означає N, N-диметилкарбоксамідну групу; Y означає метил). Стадія 1: Розчин метоксиду натрію (375 мг) і метил-2,6-дібромізонікотінату (1,0 г) у MeOH (20 мл) нагрівають в мікрохвильовій печі при 130° C протягом 30 хв. Потім додатково додають метоксид натрію (281 мг) і нагрівання продовжують при 130° C протягом ще 15 хв. Потім до реакційної суміші додають концентровану сірчану кислоту (1,86 мл) і отриману суспензію нагрівають при 80-85° C протягом 4 г. Після охолодження до кімнатної температури суміш виливають в охолоджений льодом водний розчин карбонату натрію (100 мл) і екстрагують дихлорметаном (100 мл). Органічний шар відокремлюють, сушать над Na2SO4 і концентрують у вакуумі. Залишок очищають за допомогою РХСТ (дихлорметан: MeOH = від 100:3 до 100:5) і отримують 710 мг суміші 2-бром-6-метоксіізонікотіната (497 мг) і відповідної тріметілцітразіновой кислоти (213 мг) складу 7:3. ВЕРХ (Rt) = 1,66 хв (методика D). Потім цю суміш використовують у реакції, аналогічної описаній на стадії 2 методики 1. Стадії 2+3: (Проводять аналогічно стадіям 2,3 методики 2 відповідно) Отримують сполуку прикладу 26 (7 мг). ВЕРХ (Rt) = 1,29 хв (методика D). 1 2a Синтез сполук прикладів за методикою 6 (як приклад R означає 4-хлор-3-метил; R 2b означає етиніл; R означає N, N-диметилкарбоксамідну групу; X означає бром; Y означає метил). Стадія 1: До розчину сполуки I6 (3,5 г) у ТГФ (20 мл) в атмосфері аргону при кімнатній температурі додають ТЕА (тріетіламін) (2 мл), біс (трифенілфосфін) палладійхлорід (219 мг) та йодид міді (I) (59 мг), потім триметилсилілацетілен (1 мл). Після перемішування протягом ночі суміш додають до води з льодом і екстрагують за допомогою EtOAc. Органічний шар відокремлюють, сушать над Na2SO4 і концентрують у вакуумі. Флеш-хроматографія (95:5 дихлорметан: MeOH) дає сполуку I15 (3 г). Rf (95:5 дихлорметан: MeOH) 0,22. Стадія 2: При перемішуванні до розчину сполуки I15 (3 г) в діоксані (30 мл) при кімнатній температурі додають LiOH (1M водний розчин, 10,4 мл). Через 2 год. додають HCl (1M водний розчин) до утворення нейтрального середовища і отриману суспензію фільтрують і сушать. 2a Очищення за допомогою ВЕРХ дає сполуку I8 (в якому R означає етиніл) (2,3 г). ВЕРХ (Rt) = 1,31 хв (методика D) Стадія 3: (Проводять аналогічно стадії 3 методики 2). Отримують сполуку прикладу 34 (210 мг). ВЕРХ (Rt) = 1,23 хв (методика E) Наведені нижче сполуки прикладів можна синтезувати за описаними вище методиками: Приклад № Методика синтезу Структура Методика ВЕРХ ВЕРХ, Rt O N O 1 Cl N 2 HN NH N O 15 D 1,24 UA 109290 C2 Приклад № Методика синтезу Структура O ВЕРХ, Rt O N HN 2 Методика ВЕРХ N 3 B 1,49 3 B 1,36 3 B 1,37 3 B 1,50 3 N D 1,25 Cl O O N HN 3 O N N Cl O O N HN 4 N N Cl Cl N 5 NH N N O O O O N HN O NH N 6 N Cl 16 UA 109290 C2 Приклад № Методика синтезу Структура ВЕРХ, Rt O O O Методика ВЕРХ N NH HN N 7 2 D 1,26 2 D 1,22 2 D 1,29 2 D 1,26 3 D 1,28 2 D 1,32 N Cl O N O 8 Cl HN N N N O O N O 9 Cl HN N N N O O N O O 10 Cl HN N N N O O N O 11 Cl HN N N N O O N O 12 Cl N HN N N O 17 UA 109290 C2 Приклад № Методика синтезу Структура Методика ВЕРХ ВЕРХ, Rt O N O O 13 2 1,24 D 1,27 2 D 1,38 2 N D 3 Cl B 1,53 2 HN B 1,66 N N O O O N N N 14 N Cl O N O 15 Cl HN N H N N O O O O N N HN N 16 N Cl O O O H N N HN N 17 N Cl 18 UA 109290 C2 Приклад № Методика синтезу Структура H N N HN N 18 ВЕРХ, Rt O O O Методика ВЕРХ F 2 B 1,60 2 B 1,65 2 B 1,65 2 F N D 1,34 2 D 1,36 Cl O O O H N N HN N 19 N Cl O O O N N HN N 21 N Cl O N O 22 Cl HN N N N O O N O 23 Cl N HN H N N O 19 UA 109290 C2 Приклад № Методика синтезу Структура O O Методика ВЕРХ ВЕРХ, Rt O N N HN N 24 2 D 1,28 1 D 1,31 5 D 1,29 4 D 1,41 2 D 1,26 N Br O N O O N N H N 25 N Cl O N O O N N H N 26 O N Cl O N O O N N H N 27 N Cl O O O N N HN N 28 N Cl Cl 20 UA 109290 C2 Приклад № Методика синтезу Структура Методика ВЕРХ ВЕРХ, Rt O N O O N N H N 29 1 D 1,36 3 D 1,21 3 D 1,30 4 D 1,34 3 D 1,30 N Cl O O O N N HN N 30 N F O O O N N HN N 31 F N F F Cl O N O O N N H N 32 N Cl O O O N N HN N 33 N Cl 21 UA 109290 C2 Приклад № Методика синтезу Структура Методика ВЕРХ ВЕРХ, Rt O N O O N N H N 34 6 E 1,23 3 D 1,31 2 E 1,24 N Cl O O O N N HN N 35 N Cl O O O N N HN N 36 N Cl 5 10 15 20 25 Приклади спільних кристалів Інші особливості та переваги даного винаходу стануть зрозумілі з наведених нижче більш докладно описаних прикладів, які в якості прикладу ілюструють основні положення даного винаходу. Синтез спільних кристалів з використанням в якості вихідних речовин дигідрохлоріду сполук формули 1: Еквімолярні кількості дигідрохлориду одного з сполук формули 1, бажано однієї зі сполук прикладів 1-36, наведених вище, та відповідної речовини, що утворює спільні кристали (вибране з групи, що включає оротову кислоту, гіпурову кислоту, L-піроглутамінову кислоту, Dпіроглутамінову кислоту, нікотинову кислоту, L-(+)-аскорбінову кислоту, сахарин, піперазин, 3гідрокси-2-нафтойну кислоту, муцинову (галактарову) кислоту, памоеву (ембонову) кислоту, стеаринову кислоту, холеву кислоту, дезоксихолеву кислоту, нікотинамід, ізонікотінамід, сукцінамід, урацил, L-лізин, L-пролін, D-валін, L-аргінін, гліцин), при 80-50° C об'єднують у відповідному розчиннику (вибраному з групи, що включає, наприклад, 2-бутанон, ацетон, ацетонітрил, ізопропілацетат). Після перемішування протягом 10-60 хв реакційну суміш охолоджують до кімнатної температури, при необхідності для полегшення перемішування суміші додають додаткову кількість розчинника. На закінчення тверду речовину виділяють фільтруванням, промивають підходящим органічним розчинником і потім сушать у вакуумі і отримують відповідний спільний кристал. Синтез спільних кристалів з використанням в якості вихідних речовин вільних основ сполук формули 1: Еквімолярні кількості вільного заснування однієї зі сполук формули 1, бажано однієї зі сполук прикладів 1-36, наведених вище, та відповідної речовини, що утворює спільні кристали (вибрану із групи, що включає оротову кислоту, гіпурову кислоту, L-піроглутамінову кислоту, D 22 UA 109290 C2 5 10 15 20 піроглутамінову кислоту, нікотинову кислоту, L-(+)-аскорбінову кислоту, сахарин, піперазин, 3гідрокси-2-нафтойну кислоту, муцинову (галактарову) кислоту, памоеву (ембонову) кислоту, стеаринову кислоту, холеву кислоту, дезоксихолеву кислоту, нікотинамід, ізонікотінамід, сукцінамід, урацил, L-лізин, L-пролін, D-валін, L-аргінін, гліцин), і хлористоводневу кислоту (1,5-2 екв.) об'єднують у відповідному розчиннику (вибраному з групи, що включає, наприклад, 2 бутанон, ацетон, ацетонітрил, ізопропілацетат) і температуру суміші встановлюють таку, що дорівнює 80-50 °C. Після перемішування протягом 10-60 хв суміш охолоджують до кімнатної температури, при необхідності для полегшення перемішування суміші додають додаткову кількість розчинника. На закінчення тверду речовину виділяють фільтруванням, промивають підходящим органічним розчинником і потім сушать у вакуумі і отримують відповідний спільний кристал. Аналіз наведених як приклади спільних кристалів і солей Кристалічні форми спільних кристалів і солей досліджували за допомогою порошкової рентгенографії; рентгенограми, які знімали з використанням випромінювання CuKα, містили піки при певних значеннях градусів 2θ (0,05 градусів 2θ). В обсязі даного винаходу знімали порошкові рентгенограми в режимі пропускання на дифрактометрі STOE-STADI P, забезпеченому позиційним детектором (OED) і анодом Cu в якості джерела рентгенівського випромінювання (випромінювання CuKα, λ = 1,54056 Å, 40 кВ, 40 мА). Таблиця 4 Найбільш інтенсивних характеристичних піка на порошкових рентгенограмах спільних кристалів, отриманих із сполуки прикладу 11, та відповідної речовини, що утворює спільні кристали (РУСК) Використовувана Співвідношення сполуку 4 Найбільш інтенсивних характеристичних піка на РУСК прикладу 11: РУСК порошкової рентгенограмі, 2-тета [°] аскорбінова кислота 1:0,5 10,75 16,04 17,26 19,41 муцинова кислота 1:0,5-2 10,73 16,14 19,61 30,71 памоева кислота 1:1,25 9,45 15,63 26,27 29,90 сукцинамід 1:1-2 16,16 18,39 19,83 22,24 нікотинова кислота 1:1,1-1,2 6,29 14,64 18,71 26,66 нікотинамід 1:1-1,1 14,68 18,58 24,11 26,51 ізоникотинамід 1:1-1,1 13,30 14,70 17,46 18,60 гідратований 1:0,8-1 11,32 14,69 18,61 21,99 L-лізин гідратований 1:0,8-1 13,30* 23,98* 24,62* 31,45* L-лізин* L-пролін 1:1,1 16,39 17,69 18,71 21,55 * спільний кристал з гідратованим L-лізином, отриманий після експерименту з динамічної сорбції парів з використанням спільного кристала з L-лізин (витримування при відносній вологості, що складає 10-90 %) 25 Таблиця 4 Найбільш інтенсивних характеристичних піка на порошкових рентгенограмах солей сполуки прикладу 11 Сіль (S)-(S)-(+)-2,3-дибензоілтартрат дигідрохлорид дигідрохлорид1,5 H2O дигідрохлоридМІБК* 30 * МБІК = метилізобутилкетон Фармакологічна частина В іншому варіанті здійснення 4 Найбільш інтенсивних характеристичних піка на порошкової рентгенограмі, 2-тета [°] 3,72 13,60 16,89 16,02 16,86 19,45 5,10 10,67 16,07 5,08 15,97 16,81 даний винахід 23 можна використовувати 19,34 19,71 25,13 18,56 для оцінки UA 109290 C2 5 10 15 20 25 30 35 40 45 50 55 60 передбачуваних специфічних агоністів або антагоністів пов'язаного з білком G рецептора. Даний винахід належить до застосування цих сполук для приготування препаратів для досліджень і проведення скринінгових досліджень сполук, які модулюють активність хемокінових рецепторів. Крім того, сполуки, запропоновані в даному винаході, застосовні для встановлення або визначення центру зв'язування інших сполук з хемокіновими рецепторами, наприклад, шляхом конкурентного гальмування або в якості стандартів при дослідженнях, проведених для порівняння сполуки з відомою активністю зі сполукою з невідомою активністю. При розробці нових досліджень або методик сполуки, запропоновані в даному винаході, можна використовувати для оцінки їх ефективності. Зокрема, такі сполуки можна готувати у вигляді наборів що продаються, наприклад, для використання у фармацевтичних дослідженнях, включаючи дослідження для описаних вище захворювань. Сполуки, запропоновані в даному винаході, також застосовні для оцінки передбачуваних специфічних модуляторів хемокінових рецепторів. Крім того, сполуки, запропоновані в даному винаході, можна використовувати для вивчення специфічності пов'язаних з білком G рецепторів, що не вважаються хемокіновими рецепторами, шляхом використання в якості прикладів сполук, що не зв'язуються з ними, або в якості структурних варіантів сполук, активних по відношенню до цих рецепторів, що може допомогти визначенню центрів специфічної взаємодії. Дослідження зв'язування рецептора CCR3 засноване на використанні лінії клітин K562 (бластні клітини мієлолейкозу), трансфікованих хемокіновим рецептором людини CCR3 (клітини hCCR3-C1). Клітинні мембрани отримували шляхом руйнування клітин hCCR3-C1 шляхом розкладання азотом. Препарат центрифугували при 400 g, при 4° C протягом 30 хв. Супернатант переносили в чисті пробірки і другий раз центрифугували при 48000 g, при 4° C протягом 1 г. Мембрани повторно суспендованих в інкубаційному буфері для ПСА (проксимальний сцинтиляційний аналіз) (25 мМ HEPES (4 - (2-гідроксіетіл) -1 піперазінетансульфоновая кислота), 25 мМ MgCl2 6 H2O, 1 мМ CaCl2 2 H2O), не містить бичачий сироватковий альбумін, і гомогенізували шляхом пропускання через одноразову голку (Terumo, 23Gx1''). Мембрани зберігали у вигляді аліквот при -80 °C. Дослідження зв'язування рецептора CCR3 проводили за методикою проксимального сцинтиляційного аналізу (ПСА) з радіолігандом 125I - рекомбінантний еотаксін-1 людини. Мембрани клітин hCCR3 C1 повторно гомогенізували шляхом пропускання через одноразову голку (Terumo, 23Gx1'') і розводили в інкубаційному буфері для ПСА до відповідних концентрацій (0,5-10 мкг білка / лунка) у 96-лункових мікропланшетах для титрування (1450-514, Perkin Elmer). Дослідження за допомогою ПСА проводили в інкубаційному буфері для ПСА при кінцевому об'ємі, дорівнює 200 мкл, і кінцевою концентрації, що становить 25 мМ HEPES, 25 мМ MgCl2 6H2O, 1 мМ CaCl2 2H2O і 0,1 % бичачого сироваткового альбуміну. Суміш для дослідження за допомогою ПСА містила 60 мкл суспензії мембран, 80 мкл гранул PVT, на які нанесено аглютинін із зародків пшениці (органічний сцинтилятор, GE Healthcare, RPNQ-0001, 0,2 мг / лунка), 40 мкл 125I - рекомбінантний еотаксін-1 людину (Biotrend), розведеній в буфері для ПСА до кінцевої концентрації, таку, що дорівнює 30000 розпадів / хв на лунку, і 20 мкл досліджуваної сполуки (розчиненого у розведеннях у ДМСО (диметилсульфоксид)). Суміш для дослідження за допомогою ПСА інкубували при кімнатній температурі протягом 2 г. Радіоактивність пов'язаного речовини визначали сцинтиляційним лічильником (Micro Beta "Trilux", Wallac). Використовували контрольні зразки для повного зв'язування (ПС, без додавання витискувача) і неспецифічного зв'язування (НСС) з додаванням неміченого рекомбінантного еотаксіна-1 людини (Biotrend, Cat # 300-21) або еталонної сполуки. Спорідненість досліджуваної Сполука розраховувалі, віднімаючі значення для неспеціфічного зв'язування (НСС) Із значення для полного зв'язування (ПС) або зв'язування в прісутності досліджуваної сполуки (B) при даній концентрації Сполука. Значення НСС відповідало інгібуванню на 100 %. Значення ПС-НСС відповідало інгібуванню на 0 %. Константу диссоциації Ki розраховували шляхом итеративной апроксимації експериментальних даних, отриманих при декількох концентраціях сполуки в діапазоні доз від 0,1 до 10000 нМ за допомогою програми "easy sys", яка заснована на законі дії мас (Schittkowski, Num Math 68, 129-142 (1994)). Застосовність сполук, пропонованих у даному винаході, в якості інгібіторів активності хемокиновогорецептора можна продемонструвати за методикою, відомою в даній галузі техніки, такий як дослідження зв'язування ліганда CCR3, описане в публікаціях Ponath et al., J. Exp. Med., 183,2437-2448 (1996) і Uguccioni et al., J. Clin. Invest., +100,11371143 (1997). Лінії клітин, що експресують розглянутий рецептор, включають ті, які самі експресують хемокінових рецептор, такі як EOL-3 або THP-1, в яких індукується експресія хемокиновогорецептора 24 UA 109290 C2 5 10 шляхом додавання хімічних реагентів або білків, такі як клітини HL-60 або AML14.3D10, оброблені, наприклад, олійною кислотою з додаванням інтерлейкіну-5, або клітини, яким за допомогою генної інженерії додана здатність експресувати рекомбінантний хемокіновий рецептор, такі як клітини L1.2, K562, CHO або HEK-293. Крім того, в таких дослідженнях можна використовувати клітини крові або тканин, наприклад, еозинофіли периферичної крові людини, виділені за методиками, описаним у публікації Hansel et al., J. Immunol. Methods, 145,105-110 (1991). Зокрема, за даними описаних вище досліджень сполуки, запропоновані в даному винаході, мають активність при зв'язуванні з рецептором CCR3 та інгібують активацію CCR3 лігандами CCR3, включаючи еотаксін-1, еотаксін-2, еотаксін-3, MCP-2, MCP-3, MCP-4 або RANTES. При використанні в даному винаході "активна" означає сполука, за даними описаних вище досліджень приводить до інгібування на 50 % при концентрації 1 мкМ або вище. Такий результат вказує на власну активність сполук, як інгібіторів активності рецептора CCR3. Значення Ki наведені нижче (еотаксін-1 людини на рецепторі CCR3 людини): 15 № 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 20 hCCR3, Ki (нM) 23,4 69,6 46,5 67,5 196,6 72,0 10,4 8,5 0,9 6,0 3,2 4,7 19,1 1401,6 3,5 6,8 4,3 4,6 4,0 121,5 5,2 2,3 4,2 5,8 8,3 231,6 413,8 17,8 4,1 70,3 87,2 2,3 7,9 7,9 61,3 1,7 Показання Спільні кристали і солі сполук формули 1, описані вище, застосовні для приготування лікарського засобу, призначеного для попередження та / або лікування захворювань, при яких грає роль активність рецептора CCR3. Кращим є приготування лікарського засобу, призначеного для попередження та / або лікування самих різних запальних, інфекційних та імунорегуляторних порушень і захворювань 25 UA 109290 C2 5 10 15 20 25 30 35 40 45 50 55 60 дихальних шляхів або шлунково-кишкового тракту, запальних захворювань суглобів і алергічних захворювань носоглотки, очей і шкіри, включаючи астму та алергічні захворювання, еозинофільних захворювань, інфікування патогенними мікробами (які за визначенням включають віруси), а також аутоімммунних патологій, таких як ревматоїдний артрит і атеросклероз, а також захворювань, пов'язаних з аномально посиленою неоваскуляризацією, таких як вікова дегенерація жовтої плями (ВДП), діабетична ретинопатія і діабетичний набряк жовтої плями. Вікова дегенерація жовтої плями є головною причиною сліпоти в усьому світі. Більшість випадків сліпоти при ВДП обумовлено інвазією сітківки внаслідок неоваскуляризации судинної оболонки ока. У пацієнтів, які страждають ВДП, CCR3 специфічно експресується в ендотеліальних клітинах неоваскулярізірованной судинної оболонки ока. В часто використовується модель ВДП на мишах спричинена пошкодженням лазером неоваскуляризация судинної оболонки ока була зменшена шляхом генетичного зменшення кількості лігандів CCR3 або CCR3, а також шляхом лікування мишей антитілами до CCR3 або антагоністом CCR3 (Takeda et al, Nature 2009, 460(7252):225-30). Найбільш кращим є приготування лікарського засобу, призначеного для попередження та / або лікування, наприклад, запальних або алергічних захворювань і патологічних станів, включаючи респіраторні алергічні захворювання, такі як астма, цілорічний і сезонний алергічний риніт, алергічний кон'юнктивіт, алергічні захворювання легень, гіперчутливий пневмоніт, еозинофільний целюліт (наприклад, синдром Велла), еозинофільні пневмонії (наприклад, синдром Леффлера, хронічна еозинофільна пневмонія), атонічний фасциит (наприклад, синдром Шульмана), гіперчутливість сповільненого типу, інтерстиціальні захворювання легень (ІЗЛ) (наприклад, ідіопатичний фіброз легень або ІЗЛ, пов'язане з ревматоїдним артритом, системний червоний вовчак, анкілозуючийспондиліт, системний склероз, синдром Шегрена, поліміозит або дерматоміозит); неалергічна астма; викликаний фізичним навантаженням бронхостеноз; загальна анафілактична реакція або реакції гіперчутливості, лікарські алергії (наприклад, на пеніцилін, цефалоспорини), еозинофільна міалгія, викликана споживанням забрудненої триптофану, алергічні реакції на укус комахи; аутоімунні захворювання, такі як ревматоїдний артрит, псоріатичний артрит, розсіяний склероз, системний червоний вовчак, злоякісна міастенія, імунна тромбоцитопенія (ІТП) (ІТП дорослих, тромбоцитопенія новонароджених, ІТП у дітей), імунна гемолітична анемія (аутоімунна і викликана лікарським засобом), синдром Еванса (тромбоцитарная і еритроцитарна імунні цитопенії), гемолітична анемія новонароджених з Rhg-фенотипом, синдром Гудпасчера (відкладення антитіл до базальної мембрани клубочків нирок), захворювання черевної порожнини, аутоімунна кардіоміопатія, юнацький діабет; гломерулонефрит, аутоімунний тиреоїдит, хвороба Бехчета; відторгнення трансплантата (наприклад, при трансплантації), включаючи відторгнення алотрансплантату або реакцію "трансплантат проти хазяїна"; запальні захворювання кишечника, такі як хвороба Крона і виразковий коліт; спондилоартропатии; склеродермія; псоріаз (включаючи опосредуемий T-клітинами псоріаз) і запальні дерматози, такі як дерматит, екзема, атопічний дерматит, алергічний контактний дерматит, уртікарія; васкуліт (наприклад, некротичний, шкірний і алергічний васкуліт); нодозная еритема; еозинофільний міозит, атонічний фасциит; ракові захворювання з інфільтрацією лейкоцитів у шкіру або органи; хронічне обструктивне захворювання легень, вікову дегенерацію жовтої плями (ВДП), діабетичну ретинопатію і діабетичний набряк жовтої плями. Спосіб лікування Відповідно до цього даний винахід належить до спільних кристалів і солей сполук формули 1, описаним вище, які застосовні для попередження та / або лікування самих різних запальних, інфекційних та імунорегуляторних порушень і захворювань, включаючи астму та алергічні захворювання, хронічного обструктивного захворювання легень, інфікування патогенними мікробами (які за визначенням включають віруси), аутоімммунних патологій, таких як ревматоїдний артрит і атеросклероз, а також вікової дегенерації жовтої плями (ВДП), діабетичної ретинопатії і діабетичного набряку жовтої плями. Наприклад, спільний кристал або сіль сполуки, що пропонується в даному винаході, яка інгібує одну або більшу кількість функцій хемокінового рецептора ссавців (наприклад, хемокінового рецептора людини), можна вводити для інгібування (тобто ослаблення або попередження) запалення, інфекційних захворювань або аномально посиленою неоваскуляризації. У результаті пригнічується один або більшу кількість запальних процесів, таких як еміграція лейкоцитів, адгезія, хемотаксис, екзоцитоз (наприклад, ферментів, факторів росту, гістаміну) або вивільнення запального медіатора, виживання або проліферація експресуючих CCR3 клітин. Наприклад, способом, запропонованим у даному винаході, можна придушити інфільтрацію еозинофілів в центри запалення (наприклад, при астмі або алергічному 26 UA 109290 C2 5 10 15 20 25 30 35 40 45 50 55 60 риніті). Зокрема, за даними зазначених вище досліджень спільний кристал або сіль, зазначена в наведених нижче прикладах володіє активністю, що забезпечує блокування активації і міграції клітин, що експресують рецептор CCR3 з використанням відповідних хемокінів. В іншому випадку можна інгібувати ендотеліальну проліферацію і неоваскуляризації (тобто послабити або попередити). У результаті пригнічується аномально посилена неоваскуляризация, тобто сітківки. На додаток до приматів, таким як люди, способом, запропонованим у даному винаході можна лікувати різних інших ссавців. Наприклад, можна лікувати ссавців, включаючи, але не обмежуючись лише ними, корів, овець, кіз, коней, собак, кішок, морських свинок, щурів або інших видів бичачих, овечих, кінських, собачих, котячих, гризунів або мишачих. Однак спосіб також можна використовувати для лікування інших видів, таких як види птахів. Суб'єктом, якого лікують зазначеними вище способами, є ссавець, самець або самка, для якого бажано інгібування активності хемокінового рецептора. Захворювання або патологічні стани людей або інших видів, які можна лікувати інгібіторами функції хемокінового рецептора, включають, але не обмежуються тільки ними: запальні або алергічні захворювання і патологічні стани, включаючи респіраторні алергічні захворювання, такі як астма, алергічний риніт, алергічні захворювання легень, гіперчутливий пневмоніт, еозинофільний целюліт (наприклад, синдром Велла), еозинофільні пневмонії (наприклад, синдром Леффлера, хронічна еозинофільна пневмонія), атонічний фасциит (наприклад, синдром Шульмана), гіперчутливість сповільненого типу, інтерстиціальні захворювання легень (ІЗЛ) (наприклад, ідіопатичний фіброз легень або ІЗЛ, пов'язане з ревматоїдним артритом, системний червоний вовчак, анкілозуючийспондиліт, системний склероз, синдром Шегрена, поліміозит або дерматоміозит); хронічне обструктивне захворювання легень (включаючи загострення, викликані риновірусом); загальна анафілактична реакція або реакції гіперчутливості, лікарські алергії (наприклад, на пеніцилін, цефалоспорини), еозинофільна міалгія, викликана споживанням забрудненої триптофану, алергічні реакції на укус комахи; аутоімунні захворювання, такі як ревматоїдний артрит, псоріатичний артрит, розсіяний склероз, системний червоний вовчак, злоякісна міастенія, юнацький діабет; гломерулонефрит, аутоімунний тиреоїдит, хвороба Бехчета; відторгнення трансплантата (наприклад, при трансплантації), включаючи відторгнення алотрансплантату або реакція "трансплантат проти хазяїна"; запальні захворювання кишечника, такі як хвороба Крона і виразковий коліт; спондилоартропатии; склеродермія; псоріаз (включаючи опосредуемий T-клітинами псоріаз) і запальні дерматози, такі як дерматит, екзема, атопічний дерматит, алергічний контактний дерматит, уртікарія; васкуліт (наприклад, некротичний, шкірний і алергічний васкуліт); еозинофільний міозит, атонічний фасциит; ракові захворювання з інфільтрацією лейкоцитів у шкіру або органи. Інші захворювання або патологічні стани, які можна лікувати, пригнічуючи небажані запальні реакції, включають, але не обмежуються тільки ними, реперфузійне ураження, атеросклероз, деякі злоякісні захворювання крові, викликане цитокіном токсичну прояв (наприклад, септичний шок, ендотоксичний шок), поліміозит, дерматоміозит. Інфекційні захворювання або патологічні стани людей або інших видів, які можна лікувати інгібіторами функції хемокінового рецептора, включають, але не обмежуються тільки ними, ВІЛ. Крім того, можна лікувати захворювання, пов'язаних з аномально посиленою неоваскуляризацією, такі як вікова дегенерація жовтої плями (ВДП), діабетична ретинопатія і діабетичний набряк жовтої плями. В іншому варіанті здійснення даний винахід можна використовувати для оцінки передбачуваних специфічних агоністів або антагоністів пов'язаного з білком G рецептора. Даний винахід належить до застосування цих сполук для приготування препаратів для досліджень і проведення скринінгових досліджень сполук, які модулюють активність хемокінових рецепторів. Крім того, сполуки, запропоновані в даному винаході, застосовні для встановлення або визначення центру зв'язування інших сполук з хемокіновими рецепторами, наприклад, шляхом конкурентного гальмування або в якості стандартів при дослідженнях, проведених для порівняння сполуки з відомою активністю зі сполукою з невідомою активністю. При розробці нових досліджень або методик сполуки, запропоновані в даному винаході, можна використовувати для оцінки їх ефективності. Зокрема, такі сполуки можна готувати у вигляді що продаються наборів, наприклад, для використання у фармацевтичних дослідженнях, включаючи дослідження для описаних вище захворювань. Сполуки, запропоновані в даному винаході, також застосовні для оцінки передбачуваних специфічних модуляторів хемокінових рецепторів. Крім того, сполуки, запропоновані в даному винаході, можна використовувати для вивчення специфічності пов'язаних з білком G рецепторів, що не вважаються хемокіновими рецепторами, шляхом 27 UA 109290 C2 5 10 15 20 25 30 35 40 45 50 55 60 використання в якості прикладів сполук, що не зв'язуються з ними, або в якості структурних варіантів сполук, активних по відношенню до цих рецепторів, що може допомогти визначенню центрів специфічної взаємодії. Комбінації Спільні кристали і солі сполук формули 1, описані вище, можна використовувати окремо або в комбінації з іншими активними сполуками формули 1, запропонованими в даному винаході. Сполуки загальної формули 1 також необов'язково можна об'єднувати з іншими фармакологічно активними речовинами. Вони включають агоністи ß2-адренорецептора (короткочасної і тривалої дії), антіхолінергетиків (короткочасної і тривалої дії), протизапальні стероїди (кортикостероїди для перорального та місцевого введення), хромоглікат, метилксантин, диссоційовані глюкокортікоідміметікі, інгібітори PDE3, інгібітори PDE4, інгібітори PDE7, антагоністи LTD4, інгібітори EGFR, агоністи допаміну, антагоністи PAF, похідні ліпоксіна A4, модулятори FPRL1, антагоністи рецептора LTB4 (BLT1, BLT2), антагоністи гістамінових рецепторів H1, антагоністи гістамінових рецепторів H4, подвійні антагоністи гістамінових рецепторів H1/H3а, інгібітори кінази PI3, інгібітори нерецепторних тирозинкіназ, таких як, наприклад, LYN, LCK, SYK, ZAP-70, FYN, BTK або ITK, інгібітори кіназ MAP, таких як, наприклад, p38, ERK1, ERK2, JNK1, JNK2, JNK3 або SAP, інгібітори сигнального шляху NF-κ B, такі як, наприклад, інгібітори кінази IKK2, інгібітори iNOS, інгібітори MRP4, інгібітори біосинтезу лейкотрієну, такі як, наприклад, інгібітори 5-ліпоксигенази (5-LO), інгібітори cPLA2, інгібітори лейкотрієн-A4-гідролази або інгібітори FLAP, нестероїдні протизапальні засоби (НСПВС), антагоністи CRTH2, модулятори рецептора DP1, антагоністи тромбоксанового рецептора, антагоністи CCR3, антагоністи CCR4, антагоністи CCR1, антагоністи CCR5, антагоністи CCR6, антагоністи CCR7, антагоністи CCR8, антагоністи CCR9, антагоністи CCR30, антагоністи CXCR3, антагоністи CXCR4, антагоністи CXCR2, антагоністи CXCR1, антагоністи CXCR5, антагоністи CXCR6, антагоністи CX3CR3, антагоністи нейрокініна (NK1, NK2), модулятори сфингозин-1-фосфатного рецептора, інгібітори сфингозин1-фосфатліази, модулятори аденозинові рецептора, такі як, наприклад, агоністи A2a, модулятори пуринергічних рецепторів, такі як, наприклад, інгібітори P2 × 7, активатори гістондезацетілази (HDAC), антагоністи брадикініну (BK1, BK2), інгібітори TACE, модулятори PPAR-гамма, інгібітори кінази Rho, інгібітори інтерлейкін 1-бета-конвертуючого ферменту (ICE), модулятори Toll-подібного рецептора (TLR), інгібітори HMG-CoA редуктази, антагоністи VLA-4, інгібітори ICAM-1, агоністи SHIP, антагоніст рецептора GABAa, інгібітори ENaC, модулятори меланокортинового рецептора (MC1R, MC2R, MC3R, MC4R, MC5R), антагоністи CGRP, антагоністи ендотеліну, антагоністи TNF α, антитіла до TNF, антитіла до GM-CSF, антитіла до CD46, антитіла до IL-1, антитіла до IL-2, антитіла до IL-4, антитіла до IL-5, антитіла до IL-13, антитіла до IL-4/IL-13, антитіла до TSLP, антитіла до OX40, мукорегулятори, імунотерапевтичні засоби, сполуки, що перешкоджають набряку дихальних шляхів, протикашльові сполуки, інгібітори VEGF, а також комбінації двох або трьох активних речовин. Бажаними є бета-міметики, антіхолінергетиків, кортикостероїди, інгібітори PDE4, антагоністи LTD4, інгібітори EGFR, інгібітори CRTH2, інгібітори 5-LO, антагоністи гістамінових рецепторів та інгібітори SYK, а також комбінації двох або трьох активних речовин, тобто: - Бета-міметики з кортикостероїдами, інгібіторами PDE4, інгібіторами CRTH2 або антагоністами LTD4, - Антіхолінергетіки з бета-міметиками, кортикостероїдами, інгібіторами PDE4, інгібіторами CRTH2 або антагоністами LTD4, - Кортикостероїди з інгібіторами PDE4, інгібіторами CRTH2 або антагоністами LTD4, - Інгібітори PDE4 з інгібіторами CRTH2 або антагоністами LTD4, - Інгібітори CRTH2 з антагоністами LTD4. Фармацевтичні форми Препарати, які підходять для введення спільних кристалів або солей сполук формули 1 включають наприклад, таблетки, капсули, супозиторії, розчини та порошки і т. п. Вміст фармацевтично активної сполуки (сполук) має перебувати в діапазоні від 0,05 до 90 мас. %, бажано від 0,1 до 50 мас. % у перерахунку на композицію в цілому. Відповідні таблетки можна виготовити, наприклад, шляхом змішування активної речовини (речовин) з відомими інертними наповнювачами, наприклад, інертними розчинниками, такими як карбонат кальцію, фосфат кальцію або лактоза, розпушувачами, такими як кукурудзяний крохмаль або альгінова кислота, єднальними, такими як крохмаль або желатин, змащуючими речовинами, такими як стеарат магнію або тальк і / або агентами для уповільнення вивільнення, такими як карбоксиметилцелюлоза, ацетат-фталат целюлози або полівінілацетат. Таблетки також можуть містити кілька шарів. Таблетки з покриттям можна виготовити шляхом нанесення на ядра, отримані аналогічно 28
ДивитисяДодаткова інформація
Назва патенту англійськоюCo-crystals and salts of ccr3-inhibitors
Автори англійськоюFrank, Markus, Haeberle, Hans, Henry, Manuel, Pachur, Thorsten, Santagostino, Marco, Stertz, Uwe, Trebing, Thomas, Werthmann, Ulrike
Автори російськоюФранк Маркус, Хеберле Ханс, Анри Мануель, Пахур Торстен,Сантагостино Марко, Штерц Увэ, Требинг Томас, Вертманн Ульрике
МПК / Мітки
МПК: C07D 213/81, A61K 31/454, C07D 401/04, C07D 401/14, C07D 211/58, A61P 31/00
Мітки: спільні, кристали, інгібіторів, солі
Код посилання
<a href="https://ua.patents.su/37-109290-spilni-kristali-i-soli-ingibitoriv-ccr3.html" target="_blank" rel="follow" title="База патентів України">Спільні кристали і солі інгібіторів ccr3</a>
Попередній патент: Застосування 4,3′-спіро[(2-аміно-3-ціано-4,5-дигідропірано[3,2-c]хромен-5-он)-5-метил-2′-оксиндолу] з метою профілактики та лікування ішемічного ураження печінки
Наступний патент: Механічний безмуфтовий прес
Випадковий патент: Крутопохилий сепаратор












