4-оксо-1-(3-заміщені феніл)-1,4-дигідро-1,8-нафтиридин-3-карбоксаміди як інгібітори фосфодіестерази-4
Номер патенту: 82208
Опубліковано: 25.03.2008
Автори: Дюб Лоранс, Дюб Даніель, Галлан Мішель, Жирар Ів, Лякомб Патрік, Аспіотіс Рене, Макдональд Дуайт
Формула / Реферат
1. Сполука формули (І):
 (I)
(I)
або її фармацевтично прийнятна сіль, де
Аr являє собою феніл, тієніл або його оксид;
Y являє собою -COOR4, С1-6алкіл (С1-4алкіл)n-СООR4, -С3-4циклоалкіл (С1-4алкіл)m-СООR4, де -С1-6алкіл і С3-4циклоалкіл необов'язково заміщені галогеном, алкокси, гідрокси або нітрилом, і (С1-4алкіл) замісники необов'язково зв'язані з утворенням С3-4циклоалкілу; де n має значення 0, 1, 2, 3 або 4, m має значення 0, 1 або 2;
R і R4 кожний незалежно вибраний з Н і -С1-6алкілу;
R1 являє собою Н або -С1-6алкіл, -С3-6циклоалкіл, необов'язково заміщені 1-3 замісниками, незалежно вибраними з галогенС1-6алкілу, -С1-6алкілу, -С1-6алкокси, ОН, аміно, -(С0-6алкіл)-SOр-(С1-6алкіл), нітро, CN, =N-O-С1-6алкілу, -О-N=С1-6алкілу або галогену, де р має значення 0, 1 або 2, або R1 являє собою -С3-6циклоалкіл, заміщений фенілом;
R2 являє собою Н, галоген або -С1-6алкіл;
R3 вибраний з Н або галогену.
2. Сполука формули (І):
 (I)
(I)
або її фармацевтично прийнятна сіль, де
Аr являє собою феніл, тієніл або його оксид;
Y являє собою -СООН, С1-6алкіл(С1-4алкіл)n-СООН, -С3-4циклоалкіл (С1-4алкіл)m-СООН, де -С1-6алкіл і С3-4циклоалкіл необов'язково заміщені галогеном, алкокси, гідрокси або нітрилом, і (С1-4алкіл) замісники необов'язково зв'язані з утворенням С3-4циклоалкілу; де n має значення 0, 1, 2, 3 або 4, m має значення 0, 1 або 2;
R являє собою Н або -С1-6алкіл;
R1 являє собою Н або -С1-6алкіл або -С3-6циклоалкіл, необов'язково заміщений незалежно 1-3 замісниками, вибраними з галогенС1-6алкілу, -С1-6алкілу, -С1-6алкокси, ОН, аміно, -(С0-6алкіл)-SOр-(С1-6алкіл), нітро, CN, =N-О-С1-6алкілу, -О-N=С1-6алкілу або галогену, де р має значення 0, 1 або 2;
R2 являє собою Н, галоген або С1-6алкіл;
R3 вибраний з Н або галогену.
3. Сполука за п. 2 або її фармацевтично прийнятна сіль, де
Y являє собою -С3-4циклоалкіл(С1-4алкіл)m-СООН, де С3-4циклоалкіл необов'язково заміщений галогеном, алкокси, гідрокси або нітрилом, і (С1-4алкіл) замісники необов'язково зв'язані з утворенням С3-4циклоалкілу;
де n має значення 0, 1, 2, 3 або 4,
m має значення 0, 1 або 2.
4. Сполука за п. 2 або її фармацевтично прийнятна сіль, де
Y являє собою циклопропіл-СООН; і
Аr являє собою феніл.
5. Сполука за п. 4 або її фармацевтично прийнятна сіль, де
R1 являє собою -С1-6алкіл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з -С1-6алкілу, -С1-6алкокси, ОН, аміно, -(С0-6алкіл)-SОр-(С1-6алкіл), нітро, CN, =N-O-С1-6алкілу, -О-N=С1-6алкілу або галогену.
6. Сполука за п. 4 або її фармацевтично прийнятна сіль, де
R1 являє собою -С3-6циклоалкіл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з -С1-6алкілу, -С1-6алкокси, ОН, аміно, -(С0-6алкіл)-SОр-(С1-6алкіл), нітро, CN, =N-O-С1-6алкілу, -О-N=С1-6алкілу або галогену.
7. Сполука за п. 4 або її фармацевтично прийнятна сіль, де
R являє собою водень.
8. Сполука за п. 4 або її фармацевтично прийнятна сіль, де R2 являє собою водень або -С1-3алкіл.
9. Сполука за п. 4 або її фармацевтично прийнятна сіль, де
R1 являє собою -С3-6циклоалкіл, необов'язково заміщений метилом або галогеном; і
R являє собою водень.
10. Сполука за п. 4 або її фармацевтично прийнятна сіль, де
R1 являє собою циклопропіл, необов'язково заміщений метилом або галогеном; і
R і R2 являє собою водень.
11. Сполука за п. 2 або її фармацевтично прийнятна сіль, де
R і R3 являють собою водень;
R1 являє собою -С3-6циклоалкіл, необов'язково заміщений метилом або галогеном, або -С1-6алкіл, необов'язково заміщений 1-3 галогенами; і
Аr являє собою феніл.
12. Сполука за п. 11, де
R2 являє собою водень або галоген; і
Y являє собою -СН2-С3-4циклоалкіл-СООН або -С3-4циклоалкіл-СООН.
13. Сполука за п. 2, яка являє собою
2-(транс)-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
2-(транс)-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-3-іл}циклопропанкарбонову кислоту;
2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-3-іл}-2-метилпропанову кислоту;
2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}-2-метилпропанову кислоту;
3-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}-3-метилбутанову кислоту;
{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}(гідроксі)оцтову кислоту;
1-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
2-(цис)-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
5-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}-2,2-диметил-1,3-діоксолан-4-карбонову кислоту;
1-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-3-іл}циклопропанкарбонову кислоту;
1-ціано-3-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}-2,2-диметилциклопропанкарбонову кислоту;
2-(транс)-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-3-фтор-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
(цис)-2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-3-іл}циклопропанкарбонову кислоту;
2-(транс)-{3'-бром-5'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
2-(транс)-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-3-метил-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
2-(транс)-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-2-метил-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
2-(транс)-{3-хлор-3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
2-(цис)-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-3-фтор-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-карбонову кислоту;
2-(транс)-{3'-[3-(морфолін-4-ілкарбоніл)-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
2-(транс)-{3'-[4-оксо-3-({[5-(трифторметил)-1,3,4-тіадіазол-2-іл]аміно}карбоніл)-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
2-(транс)-{3'-[3-({[2-(метилтіо)етил]аміно}карбоніл)-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
2-(транс)-{3'-[3-({[2-(метилсульфоніл)етил]аміно}карбоніл)-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
2-(транс)-{3'-[4-оксо-3-{[(2,2,2-трифторетил)аміно]карбоніл}-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
2-(транс)-(5-{3-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]феніл}тієн-2-іл)циклопропанкарбонову кислоту;
2-(транс)-{3'-[3-{[(циклопропілметил)аміно]карбоніл}-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту;
2-(транс)-{3'-[3-{[(1-ціаноциклопропіл)аміно]карбоніл}-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту або
3-{3'-[3-[(ізопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}-3-метилбутанову кислоту;
14. Сполука за п. 1, що являє собою
(+)-(транс)-2-{3-фтор-3'-[4-оксо-3-{[(2,2,2-трифторетил)аміно]карбоніл}-1,8-нафтиридин-1(4Н)-іл]біфеніл-4-іл}циклопропанкарбонову кислоту;
1-({3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}метил)циклобутанкарбонову кислоту;
(транс)-2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-2-метилциклопропанкарбонову кислоту;
(транс)-2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-2-іл}циклопропанкарбонову кислоту;
3-метил-3-{3'-[4-оксо-3-{[(2,2,2-трифторетил)аміно]карбоніл}-1,8-нафтиридин-1(4Н)-іл]біфеніл-4-іл}бутанову кислоту;
(транс)-2-{3'-[4-оксо-3-{[(2,2,2-трифторетил)аміно]карбоніл}-1,8-нафтиридин-1(4Н)-іл]біфеніл-2-іл}циклопропанкарбонову кислоту;
(транс)-2-{3'-[4-оксо-3-{[(2,2,3,3,3-пентафторпропіл)аміно]карбоніл}-1,8-нафтиридин-1(4Н)-іл]біфеніл-4-іл}циклопропанкарбонову кислоту;
(транс)-2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-1-фторциклопропанкарбонову кислоту;
(+)-(транс)-2-{3-хлор-3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}циклопропанкарбонову кислоту;
(-)-(транс)-2-{3'-[4-оксо-3-{[(2,2,2-трифторетил)аміно]карбоніл}-1,8-нафтиридин-1(4Н)-іл]біфеніл-4-іл}циклопропанкарбонову кислоту;
(+)-(транс)-етил 2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}циклопропанкарбоксилат;
(+)-(транс)-ізопропіл 2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}циклопропанкарбоксилат;
трет-бутил 3-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-2,2-диметилпропаноат;
3-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-2,2,-диметилпропанову кислоту;
3-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-3-іл}-2,2-диметилпропанову кислоту;
1-({3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-3-іл}метил)циклобутанкарбонову кислоту;
3-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-2-іл}-2,2-диметипропанову кислоту;
1-({3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-2-іл}метил)циклобутанкарбонову кислоту;
(+)-(транс)-2-{3'-[3-[(трет-бутиламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}циклопропанкарбонову кислоту;
(+)-(транс)-2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}циклопропанкарбонову кислоту;
3-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}біцикло[1.1.1]пентан-1-карбонову кислоту;
4-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-4-гідроксипентанову кислоту;
(транс)-2-{3'-[3-{[(±)-цис-(2-фторциклопропіл)аміно]карбоніл}-4-оксо-1,8-нафтиридин-1(4Н)-іл]-(+)-біфеніл-4-іл}циклопропанкарбонову кислоту;
(+)-(транс)-2-{3'-[3-{[(дициклопропілметил)аміно]карбоніл}-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-циклопропанкарбонову кислоту;
4-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-2,2-диметилбутанову кислоту;
(+)-(транс)-2-{3'-[3-{[(1-гідроксициклопропіл)аміно]карбоніл}-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}циклопропанкарбонову кислоту;
(+)-(транс)-2-{3'-[4-оксо-3-{[(1-фенілциклопропіл)аміно]карбоніл}-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}циклопропанкарбонову кислоту;
4-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-3,3-диметилбутанову кислоту;
(+)-(транс)-2-{3'-[3-{[(1-циклопропіл-1-метилетил)аміно]карбоніл}-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}циклопропанкарбонову кислоту;
1-({3'-[4-оксо-3-{[(2,2,2-трифторетил)аміно]карбоніл}-1,8-нафтиридин-1(4Н)-іл]біфеніл-4-іл}метил)циклобутанкарбонову кислоту;
(+)-(транс)-2-{3'-[3-{[(циклопропілметил)аміно]карбоніл}-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-циклопропанкарбонову кислоту;
(-)-(транс)-2-{3-фтор-3'-[3-{[(1-гідроксициклопропіл)аміно]карбоніл}-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}циклопропанкарбонову кислоту;
(транс)-2-{3'-[4-оксо-3-{[((±)-2,2,2-трифтор-1-метилетил)аміно]карбоніл}-1,8-нафтиридин-1(4Н)-іл]-(+)-біфеніл-4-іл}циклопропанкарбонову кислоту;
(+)-(транс)-2-{3'-[3-{[(1-метилциклопропіл)аміно]карбоніл}-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-циклопропанкарбонову кислоту;
2,2-диметил-4-{3'-[4-оксо-3-{[(2,2,2-трифторетил)аміно]карбоніл}-1,8-нафтиридин-1(4Н)-іл]біфеніл-4-іл}бутанову кислоту;
2,2-диметил-3-{3'-[4-оксо-3-{[(2,2,2-трифторетил)аміно]карбоніл}-1,8-нафтиридин-1(4Н)-іл]біфеніл-4-іл}пропанову кислоту;
(-)-(транс)-2-{3-хлор-3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}циклопропанкарбонову кислоту або
(+)-(транс)-2-{3'-[4-оксо-3-{[(2,2,2-трифторетил)аміно]карбоніл}-1,8-нафтиридин-1(4Н)-іл]біфеніл-4-іл}циклопропанкарбонову кислоту.
15. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки за будь-яким з пп. 1-14 або її фармацевтично прийнятної солі і фармацевтично прийнятний носій.
16. Фармацевтична композиція за п. 15, що додатково містить антагоніст рецепторів лейкотриєну, інгібітор біосинтезу лейкотриєну, антагоніст М2/М3, кортикостероїд, антагоніст рецепторів Н1 або агоніст бета-2 адренорецепторів.
17. Фармацевтична композиція за п. 15, що додатково містить селективний інгібітор СОХ-2, статин або NSAID.
18. Спосіб лікування або профілактики астми, хронічного бронхіту, хронічного обструктивного захворювання легенів (COPD), еозинофільної гранульоми, псоріазу і інших доброякісних або злоякісних проліферативних шкірних захворювань, ендотоксичного шоку (і пов'язаних з цим станів, таких як ламініт і коліки у коней), септичного шоку, виразкового коліту, хвороби Крона, реперфузійного ураження міокарда і мозку, запального артриту, остеопорозу, хронічного гломерулонефриту, атонічного дерматиту, кропивниці, респіраторного дистрес-синдрому у дорослих, респіраторного дистрес-синдрому у дітей, хронічного обструктивного захворювання легенів у тварин, нецукрового діабету, алергічного риніту, алергічного кон'юнктивіту, весняного кон'юнктивіту, рестенозу артерій, атеросклерозу, нейрогенного запалення, болю, кашлю, ревматоїдного артриту, анкілозуючого спондиліту, відторгнення трансплантата і захворювання "трансплантат проти хазяїна", підвищеної секреції шлункової кислоти, сепсису або септичного шоку бактерійного, грибкового або вірусного типу, запалення і опосередкованої цитокінами хронічної дегенерації тканини, остеоартриту, раку, кахексії, м'язової гіпотрофії, депресії, погіршення пам'яті, монополярної депресії, гострого і хронічного нейродегенеративного захворювання із запальними компонентами, хвороби Паркінсона, хвороби Альцгеймера, травми спинного мозку, травми голови, розсіяного склерозу, росту пухлини і інвазії ракової пухлини в нормальні тканини, що включає стадію введення терапевтично ефективної кількості або профілактично ефективної кількості сполуки за п. 1 або її фармацевтично прийнятної солі.
19. Спосіб поліпшення пізнавальної здатності у здорового суб'єкта, що включає введення безпечної, поліпшуючої пізнавальну здатність кількості сполуки за п. 1 або її фармацевтично прийнятної солі.
20. Спосіб за п. 18, де використовують кількість сполуки, що не викликає у вказаного суб'єкта блювотної реакції.
21. Спосіб за п. 18, де суб'єкт є людиною віком 55 років або старше.
22. Сполука за п. 2, де Y являє собою -С3-6циклоалкіл(С1-4алкіл)m-СООН, де С3-6циклоалкіл необов'язково заміщений галогеном, алкокси, гідрокси або нітрилом, і (С1-4алкіл) замісники необов'язково зв'язані з утворенням С3-6циклоалкілу;
де n має значення 0, 1,2,3 або 4, m має значення 0, 1.
23. Застосування сполуки формули (І) за будь-яким з пп. 1-14 або 22 для отримання лікарського засобу для лікування або профілактики захворювання за п. 18 або поліпшення пізнавальної здатності у здорового суб'єкта.
24. Сполука формули (І) за будь-яким з пп. 1-14 або 22 для лікування або профілактики захворювання за п. 18 або поліпшення пізнавальної здатності у здорового суб'єкта.
25. Фармацевтична композиція інгібітора фосфодіестерази-4, що містить прийнятну інгібуючу фосфодіестеразу-4 кількість сполуки формули (І) за будь-яким з пп. 1-14 або 22 в поєднанні з фармацевтично прийнятним носієм.
26. (-)-2-(Транс)-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8-нафтиридин-1(4Н)-іл]-3-фтор-1,1'-біфеніл-4-іл}циклопропанкарбонова кислота формули
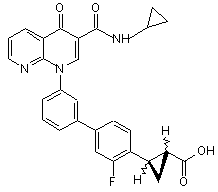 .
.
27. Фармацевтична композиція, інгібуюча фосфодіестеразу-4, що містить інгібуючу фосфодіестеразу-4 кількість сполуки за п. 26 в поєднанні з фармацевтично прийнятним носієм.
Текст
1. Сполука формули (І): O O 2 3 m має значення 0, 1 або 2. 4. Сполука за п. 2 або її фармацевтично прийнятна сіль, де Y являє собою циклопропіл-СООН; і Аr являє собою феніл. 5. Сполука за п. 4 або її фармацевтично прийнятна сіль, де R1 являє собою -С1-6алкіл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з -С1-6алкілу, -С1-6алкокси, ОН, аміно, -(С0-6алкіл)SОр-(С1-6алкіл), нітро, CN, =N-O-С1-6алкілу, -ОN=С1-6алкілу або галогену. 6. Сполука за п. 4 або її фармацевтично прийнятна сіль, де R1 являє собою -С3-6циклоалкіл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з -С1-6алкілу, -С1-6алкокси, ОН, аміно, -(С0-6алкіл)-SОр-(С1-6алкіл), нітро, CN, =N-O-С1-6алкілу, -О-N=С1-6алкілу або галогену. 7. Сполука за п. 4 або її фармацевтично прийнятна сіль, де R являє собою водень. 8. Сполука за п. 4 або її фармацевтично прийнятна сіль, де R2 являє собою водень або -С13алкіл. 9. Сполука за п. 4 або її фармацевтично прийнятна сіль, де R1 являє собою -С3-6циклоалкіл, необов'язково заміщений метилом або галогеном; і R являє собою водень. 10. Сполука за п. 4 або її фармацевтично прийнятна сіль, де R1 являє собою циклопропіл, необов'язково заміщений метилом або галогеном; і R і R2 являє собою водень. 11. Сполука за п. 2 або її фармацевтично прийнятна сіль, де R і R3 являють собою водень; R1 являє собою -С3-6циклоалкіл, необов'язково заміщений метилом або галогеном, або -С1-6алкіл, необов'язково заміщений 1-3 галогенами; і Аr являє собою феніл. 12. Сполука за п. 11, де R2 являє собою водень або галоген; і Y являє собою -СН2-С3-4циклоалкіл-СООН або -С3-4циклоалкіл-СООН. 13. Сполука за п. 2, яка являє собою 2-(транс)-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонову кислоту; 2-(транс)-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-3іл}циклопропанкарбонову кислоту; 2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-3-іл}-2метилпропанову кислоту; 2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}-2метилпропанову кислоту; 3-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}-3метилбутанову кислоту; 82208 4 {3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}(гідроксі)оцтову кислоту; 1-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонову кислоту; 2-(цис)-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонову кислоту; 5-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}-2,2диметил-1,3-діоксолан-4-карбонову кислоту; 1-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-3іл}циклопропанкарбонову кислоту; 1-ціано-3-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}2,2-диметилциклопропанкарбонову кислоту; 2-(транс)-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-3-фтор-1,1'-біфеніл4-іл}циклопропанкарбонову кислоту; (цис)-2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-3іл}циклопропанкарбонову кислоту; 2-(транс)-{3'-бром-5'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонову кислоту; 2-(транс)-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-3-метил-1,1'біфеніл-4-іл}циклопропанкарбонову кислоту; 2-(транс)-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-2-метил-1,1'біфеніл-4-іл}циклопропанкарбонову кислоту; 2-(транс)-{3-хлор-3'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонову кислоту; 2-(цис)-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-3-фтор-1,1'-біфеніл-4іл}циклопропанкарбонову кислоту; 3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-карбонову кислоту; 2-(транс)-{3'-[3-(морфолін-4-ілкарбоніл)-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонову кислоту; 2-(транс)-{3'-[4-оксо-3-({[5-(трифторметил)-1,3,4тіадіазол-2-іл]аміно}карбоніл)-1,8-нафтиридин1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту; 2-(транс)-{3'-[3-({[2-(метилтіо)етил]аміно}карбоніл)4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонову кислоту; 2-(транс)-{3'-[3-({[2(метилсульфоніл)етил]аміно}карбоніл)-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонову кислоту; 2-(транс)-{3'-[4-оксо-3-{[(2,2,2трифторетил)аміно]карбоніл}-1,8-нафтиридин1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонову кислоту; 2-(транс)-(5-{3-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]феніл}тієн-2іл)циклопропанкарбонову кислоту; 5 2-(транс)-{3'-[3{[(циклопропілметил)аміно]карбоніл}-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонову кислоту; 2-(транс)-{3'-[3-{[(1ціаноциклопропіл)аміно]карбоніл}-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонову кислоту або 3-{3'-[3-[(ізопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}-3метилбутанову кислоту; 14. Сполука за п. 1, що являє собою (+)-(транс)-2-{3-фтор-3'-[4-оксо-3-{[(2,2,2трифторетил)аміно]карбоніл}-1,8-нафтиридин1(4Н)-іл]біфеніл-4-іл}циклопропанкарбонову кислоту; 1-({3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4іл}метил)циклобутанкарбонову кислоту; (транс)-2-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-2метилциклопропанкарбонову кислоту; (транс)-2-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-2іл}циклопропанкарбонову кислоту; 3-метил-3-{3'-[4-оксо-3-{[(2,2,2трифторетил)аміно]карбоніл}-1,8-нафтиридин1(4Н)-іл]біфеніл-4-іл}бутанову кислоту; (транс)-2-{3'-[4-оксо-3-{[(2,2,2трифторетил)аміно]карбоніл}-1,8-нафтиридин1(4Н)-іл]біфеніл-2-іл}циклопропанкарбонову кислоту; (транс)-2-{3'-[4-оксо-3-{[(2,2,3,3,3пентафторпропіл)аміно]карбоніл}-1,8-нафтиридин1(4Н)-іл]біфеніл-4-іл}циклопропанкарбонову кислоту; (транс)-2-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-1фторциклопропанкарбонову кислоту; (+)-(транс)-2-{3-хлор-3'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4іл}циклопропанкарбонову кислоту; (-)-(транс)-2-{3'-[4-оксо-3-{[(2,2,2трифторетил)аміно]карбоніл}-1,8-нафтиридин1(4Н)-іл]біфеніл-4-іл}циклопропанкарбонову кислоту; (+)-(транс)-етил 2-{3'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4іл}циклопропанкарбоксилат; (+)-(транс)-ізопропіл 2-{3'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4іл}циклопропанкарбоксилат; трет-бутил 3-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-2,2диметилпропаноат; 3-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-2,2,диметилпропанову кислоту; 3-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-3-іл}-2,2диметилпропанову кислоту; 82208 6 1-({3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-3іл}метил)циклобутанкарбонову кислоту; 3-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-2-іл}-2,2диметилпропанову кислоту; 1-({3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-2іл}метил)циклобутанкарбонову кислоту; (+)-(транс)-2-{3'-[3-[(трет-бутиламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4іл}циклопропанкарбонову кислоту; (+)-(транс)-2-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-біфеніл-4іл}циклопропанкарбонову кислоту; 3-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4іл}біцикло[1.1.1]пентан-1-карбонову кислоту; 4-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-4гідроксипентанову кислоту; (транс)-2-{3'-[3-{[(±)-цис-(2фторциклопропіл)аміно]карбоніл}-4-оксо-1,8нафтиридин-1(4Н)-іл]-(+)-біфеніл-4іл}циклопропанкарбонову кислоту; (+)-(транс)-2-{3'-[3{[(дициклопропілметил)аміно]карбоніл}-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4-іл}циклопропанкарбонову кислоту; 4-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-2,2диметилбутанову кислоту; (+)-(транс)-2-{3'-[3-{[(1гідроксициклопропіл)аміно]карбоніл}-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4іл}циклопропанкарбонову кислоту; (+)-(транс)-2-{3'-[4-оксо-3-{[(1фенілциклопропіл)аміно]карбоніл}-1,8нафтиридин-1(4Н)-іл]-біфеніл-4іл}циклопропанкарбонову кислоту; 4-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4-іл}-3,3диметилбутанову кислоту; (+)-(транс)-2-{3'-[3-{[(1-циклопропіл-1метилетил)аміно]карбоніл}-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4іл}циклопропанкарбонову кислоту; 1-({3'-[4-оксо-3-{[(2,2,2трифторетил)аміно]карбоніл}-1,8-нафтиридин1(4Н)-іл]біфеніл-4-іл}метил)циклобутанкарбонову кислоту; (+)-(транс)-2-{3'-[3{[(циклопропілметил)аміно]карбоніл}-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4-іл}циклопропанкарбонову кислоту; (-)-(транс)-2-{3-фтор-3'-[3-{[(1гідроксициклопропіл)аміно]карбоніл}-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4іл}циклопропанкарбонову кислоту; (транс)-2-{3'-[4-оксо-3-{[((±)-2,2,2-трифтор-1метилетил)аміно]карбоніл}-1,8-нафтиридин-1(4Н)іл]-(+)-біфеніл-4-іл}циклопропанкарбонову кислоту; (+)-(транс)-2-{3'-[3-{[(1метилциклопропіл)аміно]карбоніл}-4-оксо-1,8 7 нафтиридин-1(4Н)-іл]-біфеніл-4-іл}циклопропанкарбонову кислоту; 2,2-диметил-4-{3'-[4-оксо-3-{[(2,2,2трифторетил)аміно]карбоніл}-1,8-нафтиридин1(4Н)-іл]біфеніл-4-іл}бутанову кислоту; 2,2-диметил-3-{3'-[4-оксо-3-{[(2,2,2трифторетил)аміно]карбоніл}-1,8-нафтиридин1(4Н)-іл]біфеніл-4-іл}пропанову кислоту; (-)-(транс)-2-{3-хлор-3'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-біфеніл-4іл}циклопропанкарбонову кислоту або (+)-(транс)-2-{3'-[4-оксо-3-{[(2,2,2трифторетил)аміно]карбоніл}-1,8-нафтиридин1(4Н)-іл]біфеніл-4-іл}циклопропанкарбонову кислоту. 15. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки за будь-яким з пп. 1-14 або її фармацевтично прийнятної солі і фармацевтично прийнятний носій. 16. Фармацевтична композиція за п. 15, що додатково містить антагоніст рецепторів лейкотриєну, інгібітор біосинтезу лейкотриєну, антагоніст М2/М3, кортикостероїд, антагоніст рецепторів Н1 або агоніст бета-2 адренорецепторів. 17. Фармацевтична композиція за п. 15, що додатково містить селективний інгібітор СОХ-2, статин або NSAID. 18. Спосіб лікування або профілактики астми, хронічного бронхіту, хронічного обструктивного захворювання легенів (COPD), еозинофільної гранульоми, псоріазу і інших доброякісних або злоякісних проліферативних шкірних захворювань, ендотоксичного шоку (і пов'язаних з цим станів, таких як ламініт і коліки у коней), септичного шоку, виразкового коліту, хвороби Крона, реперфузійного ураження міокарда і мозку, запального артриту, остеопорозу, хронічного гломерулонефриту, атонічного дерматиту, кропивниці, респіраторного дистрессиндрому у дорослих, респіраторного дистрессиндрому у дітей, хронічного обструктивного захворювання легенів у тварин, нецукрового діабету, алергічного риніту, алергічного кон'юнктивіту, весняного кон'юнктивіту, рестенозу артерій, атеросклерозу, нейрогенного запалення, болю, кашлю, ревматоїдного артриту, анкілозуючого спондиліту, відторгнення трансплантата і захворювання "трансплантат проти хазяїна", підвищеної секреції шлункової кислоти, сепсису або септичного шоку бактерійного, грибкового або вірусного типу, запалення і опосередкованої цитокінами хронічної дегенерації тканини, остеоартриту, раку, кахексії, м'язової гіпотрофії, депресії, погіршення пам'яті, монополярної депресії, гострого і хронічного нейродегенеративного захворювання із запальними компонентами, хвороби Паркінсона, хвороби Альцгеймера, травми спинного мозку, травми голови, розсіяного склерозу, росту пухлини 82208 8 і інвазії ракової пухлини в нормальні тканини, що включає стадію введення терапевтично ефективної кількості або профілактично ефективної кількості сполуки за п. 1 або її фармацевтично прийнятної солі. 19. Спосіб поліпшення пізнавальної здатності у здорового суб'єкта, що включає введення безпечної, поліпшуючої пізнавальну здатність кількості сполуки за п. 1 або її фармацевтично прийнятної солі. 20. Спосіб за п. 18, де використовують кількість сполуки, що не викликає у вказаного суб'єкта блювотної реакції. 21. Спосіб за п. 18, де суб'єкт є людиною віком 55 років або старше. 22. Сполука за п. 2, де Y являє собою -С36циклоалкіл(С 1-4алкіл)m-СООН, де С3-6циклоалкіл необов'язково заміщений галогеном, алкокси, гідрокси або нітрилом, і (С1-4алкіл) замісники необов'язково зв'язані з утворенням С36циклоалкілу; де n має значення 0, 1,2,3 або 4, m має значення 0, 1. 23. Застосування сполуки формули (І) за будь-яким з пп. 1-14 або 22 для отримання лікарського засобу для лікування або профілактики захворювання за п. 18 або поліпшення пізнавальної здатності у здорового суб'єкта. 24. Сполука формули (І) за будь-яким з пп. 1-14 або 22 для лікування або профілактики захворювання за п. 18 або поліпшення пізнавальної здатності у здорового суб'єкта. 25. Фармацевтична композиція інгібітора фосфодіестерази-4, що містить прийнятну інгібуючу фосфодіестеразу-4 кількість сполуки формули (І) за будь-яким з пп. 1-14 або 22 в поєднанні з фармацевтично прийнятним носієм. 26. (-)-2-(Транс)-{3'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-3-фтор-1,1'-біфеніл-4іл}циклопропанкарбонова кислота формули O O NH N N H OH F H O . 27. Фармацевтична композиція, інгібуюча фосфодіестеразу-4, що містить інгібуючу фосфодіестеразу-4 кількість сполуки за п. 26 в поєднанні з фармацевтично прийнятним носієм. 9 Даний винахід стосується 4-оксо-1(3заміщених феніл-1,4-дигідро-1,8-нафтиридин-3карбоксамідів, придатних як інгібітори фосфодіестерази-4. Гормони являють собою сполуки, що впливають різним чином на клітинну активність. У багатьох відношеннях, гормони діють як месенджери для запуску специфічних клітинних відповідей і активності. Багато які ефекти, що виробляються гормонами, однак, викликані не тільки окремим ефектом саме цього гормону. Навпаки, гормон спочатку зв'язується з рецептором, спричиняючи, таким чином, вивільнення другої сполуки, яка продовжує впливати на клітинну активність. У цьому випадку гормон називають першим месенджером, тоді як сполуку називають другим месенджером. Циклічний аденозинмонофосфат (аденозин 3',5'циклічний монофосфат,"сАМР" або "циклічний AMP") відомий як другий месенджер для гормонів, що включають епінефрин, глюкагон, кальцитонін, кортикотрофін, ліпотропін, лютеїнізуючий гормон, норепінефрин, паратиреоїдний гормон, тироїдстимулюючий гормон і вазопресин. Таким чином, сАМР опосередковує клітинні відповіді на гормони. Циклічний AMP також опосередковє клітинні відповіді на різні нейротрансмітери. Фосфодіестерази ("PDE") являють собою сімейство ферментів, які метаболізують 3',5' циклічні нуклеотиди до 5' нуклеозидмонофосфатів, припиняючи, таким чином, активність сАМР як другого месенджера. Конкретна фосфодіестераза, фосфодіестераза-4 ("PDE4", також відома як "PDE-IV"), яка являє собою PDE типу IV і володіє високою спорідненістю і специфічністю до сАМР, викликала інтерес як потенційна мішень для розробки нових антиастматичних і протизапальних сполук. Відомо, що PDE4 існує у вигляді, щонайменше, чотирьох ізоферментів, кожний з яких кодується окремим геном. Кожний з чотирьох відомих генних продуктів PDE4, як вважають, відіграє різну роль в алергічних і/або запальних відповідях. Тому вважається, що інгібування PDE4, зокрема конкретних специфічних ізоформ PDE4, які виробляють несприятливі відповіді, може сприятливо діяти на алергічні і запальні симптоми. Було б бажано отримати нові сполуки і композиції, що інгібують активність PDE4. Основним недоліком застосування інгібіторів PDE4 є побічний блювотний ефект, що спостерігається у випадку деяких сполуккандидатів, як описано в [C.Bumouf et al., ("BurnouP), Ann.Rep.In.Med.Chem., 33: 91109(1998). B.Hughes et al., Br.J.Pharmacol., 118: 1183-1191(1996); M.J.Perry et al., Cell Biochem. Biophys., 29: 113-132(1998); S.B.Christensen et al., J.Med.Chem., 41: 821-835(1998); і Burnouf описує різну міру тяжкості небажаних побічних ефектів, що інгібуються різними сполуками. Як описано в M.D.Houslay et al., Adv.In Pharmacol., 44: 225342(1998) and D.Spina et al., Adv.In Pharmacol., 44: 33-89(1998), існує значний інтерес, і проводяться дослідження терапевтичних інгібіторів PDE4. 82208 10 Міжнародна патентна публікація WO 9422852 описує хіноліни як інгібітори PDE4. Міжнародна патентна публікація WO 9907704 описує похідні 1арил-1,8-нафтилідин-4-ону як інгібітори PDE4. [А.Н.Соок, і інш., J.Chem.Soc, 413-417(1943)] описує гамма-піридилхіноліни. Інші хінолінові сполуки описані в [Kei Manabe і інш., J.Org.Chem., 58(24): 6692-6700(1993); Kei Manabe і інш., J.Am.Chem.Soc, 115(12): 5324-5325 (1993); Kеі Manabe і інш., J.Am.Chem.Soc, 114(17):69406941(1992)]. Сполуки, що включають кільцеві системи, описані різними дослідниками як ефективні для різних терапевтичних цілей і застосувань. Наприклад, Міжнародна патентна публікація [WO 98/25883] описує кетобензаміди як інгібітори калпаїну, [Європейська патентна публікація №ЕР 811610 і патенти США №№5679712, 5693672 і 5747541] описують заміщені бензоїлгуанідини як блокатори натрієвих каналів, [патент США №5736297] описує кільцеві системи, корисні як світлочутлива композиція. [Патенти США №№5491147, 5608070, 5622977, 5739144, 5776958, 5780477, 5786354, 5798373, 5849770, 5859034, 5866593, 5891896 і Міжнародна патентна публікація WO 95/35283] описують інгібітори PDE4, що є тризаміщеними похідними арил- або гетероарилфенілів. [Патент США №5580888] описує інгібітори PDE4, що є похідними стиролу. [Патент США №5550137] описує інгібітори PDE4, що є похідними феніламінокарбонілів. [Патент США №5340827] описує інгібітори PDE4, що є похідними фенілкарбоксамідів. [Патент США №5780478] описує інгібітори PDE4, що є тетразаміщеними фенільними похідними. [Міжнародна патентна публікація WO 96/00215] описує похідні оксиму як інгібітори PDE4. [Патент США №5633257] описує інгібітори PDE4, що є цикло(алкіл і алкеніл)фенілалкеніл(арил і гетероарил) похідними. Однак залишається потреба в нових сполуках і композиціях, які терапевтично інгібують PDE4 з мінімальними побічними ефектами. Даний винахід спрямований на біарилзаміщені 1,8-нафтиридин-4(1Н)-они, представлені загальною формулою (І): (I) або їх фармацевтично прийнятні солі, які є інгібіторами фосфодіестерази-4. Даний винахід також стосується фармацевтичної композиції, яка включає ефективну кількість нових біарилзаміщених 1,8нафтиридин-4(1Н)-онів і фармацевтично прийнятного носія. Даний винахід також пропонує 11 82208 спосіб лікування у ссавців, наприклад, астми, хронічного бронхіту, хронічного обструктивного захворювання легенів (COPD), еозинофільної гранульоми, псоріазу і інших доброякісних або злоякісних проліферативних шкірних захворювань, ендотоксичного шоку (і пов'язаних з цим станів, таких як ламініт і коліки у коней), септичного шоку, виразкового коліту, хвороби Крона, реперфузійного ураження міокарда і мозку, запального артриту, остеопорозу, хронічного гломерулонефриту, атопічного дерматиту, кропивниці, респіраторного дистрес-синдрому у дорослих, респіраторного дистрес-синдрому у дітей, хронічного обструктивного захворювання легенів у тварин, нецукрового діабету, алергічного риніту, алергічного кон'юнктивіту, весняного кон'юнктивіту, рестенозу артерій, атеросклерозу, нейрогенного запалення, болю, кашлю, ревматоїдного артриту, анкілозуючого спондиліту, відторгнення трансплантату і захворювання "трансплантат проти хазяїна", підвищеної секреції шлункової кислоти, сепсису або септичного шоку бактерійного, грибкового або вірусного типу, запалення і опосередкованої цитокінами хронічної дегенерації тканини остеоартриту, раку, кахексії, м'язової гіпотрофії, депресії, погіршення пам'яті монополярної депресії, гострого і хронічного нейродегенеративного захворювання із запальними компонентами, хвороби Паркінсона, хвороби Альцгеймера, травми спинного мозку, травми голови, розсіяного склерозу, росту пухлини і інвазії ракової пухлини в нормальні тканини шляхом введення ефективної кількості сполук формули (І) або сполуки-попередника, що утворює в in vivo умовах сполуки формули (І), які є інгібіторами фосфодіестерази-4. Даний винахід, крім того, пропонує спосіб поліпшення пізнавальної здатності у здорових людей. В одному варіанті здійснення даний винахід спрямований на сполуки, представлені формулою (І): (I) і їх фармацевтично прийнятні солі, де Аr являє собою феніл, піридил, піримідил, індоліл, хінолініл, тієніл, піридоніл, оксазоліл, оксадіазоліл, тіадіазоліл або імідазоліл; або їх оксиди, коли Аг являє собою гетероарил; Υ являє собою -СООН, С1-4алкій (С1-4алкіл)пСООН, -Сз^циклоалкіл (С1-44алкіл)т-СООН, де -С16алкіл і С3-4циклоалкіл необов'язково заміщені галогеном, алкокси, гідрокси або нітрилом, і (С1замісники необов'язково пов'язані з 4алкіл) утворенням С3-4циклоалкілу; де n має значення 0, 1, 2, 3 або 4, m має значення 0, 1 або 2; R являє собою H або - С1-6алкіл; 12 R1 являє собою H або -С1-6алкіл, -С3-С1-6лкокси, -С2-6алкеніл, С3-6алкініл, гетероарил або гетероцикл, необов'язково заміщений незалежно 1-3 замісниками, вибраними з галогенС1-6алкілу, -С1-6алкілу, -С1-6алкокси, ОН, аміно, -(С0-6алкіл)-SОр-(С1-6алкіл), нітро, CN, =N-ОС1-6алкілу, -О-N=С1-6алкілу або галогену, де p має значення 0, 1 або 2; R2 являє собою Н, галоген, -CN, -ΝΟ2, -С16алкіл, -С3-6циклоалкіл, -О-С3-6циклоалкіл, О-С1О-С3-6циклоалкіл-С 1-6алкіл(С36алкіл, 6циклоалкіл)(С3-6циклоалкіл), -С1-6алкокси, феніл, гетероарил, гетероцикл, аміно, -С(О)-С1-6алкіл, С(О)-О-С1-6алкіл, -С1-6алкіл (=N-OH), -C(N=NOH)С16алкіл, -С0-6алкіл(окси)С1-6алкіл-феніл, SОk NН(С06алкіл) або -(С0-6алкіл)-SОк-(С1-6алкіл), де феніл, гетероарил або гетероцикл необов'язково заміщені галогеном, -С1-6алкілом, -С1-6алкокси, гідрокси, аміно або -С(О)-О-С1-6алкілом, і де алкіл або циклоалкіл необов'язково заміщені 1-6 замісниками, незалежно вибраними з атомів галогенів або -ОН, і де k має значення 0, 1 або 2; R3 вибраний з Н, галогену, CN, -С1-6алкілу, -С36циклоалкілу, нітро, -С(О)-С1-6алкілу, -С(О)-О-С06алкілу, -SOn'NH(C0-6алкіл) або -(С0-6алкіл)SОn'-(С16алкіл), О-С1-6алкілу, -О-С3-6циклоалкілу, де n' має значення 0, 1 або 2, і де алкіл і циклоалкіл необов'язково заміщені 1-6 замісниками, незалежно вибраними з галогену або ОН; В альтернативному варіанті група Y: 6циклоалкіл, або -С3-6циклоалкіл(С1-4алкіл)m-СООН, де С3необов'язково заміщений галогеном, алкокси, гідрокси або нітрилом, і (С1-4алкіл) замісники необов'язково пов'язані з утворенням С36циклоалкілу; де n має значення 0, 1, 2, 3 або 4; m має значення 0, 1. В об'єм цього варіанту винаходу входить група сполук або їх фармацевтично прийнятні солі, де: Υ являє собою -С3-4циклоалкіл (С1-4алкіл)mСООН, де С3-4циклоалкіл необов'язково заміщений галогеном, алкокси, гідрокси або нітрилом, і (С1замісники необов'язково пов'язані з 4алкіл) утворенням С3-4циклоалкілу; де n має значення 0,1,2, 3 або 4, m має значення 0,1 або 2. В об'єм цього варіанту винаходу входить також ще одна група сполук або їх фармацевтично прийнятні солі, де: Υ являє собою циклопропіл-СООН; і Аr являє собою феніл. Ця група охоплює також підгрупу сполук або їх фармацевтично прийнятні солі, де: R1 являє собою -С1-6алкіл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з -С1-6алкілу, -С1-6алкокси, ОН, аміно, -(С0-6алкіл)SОр-(С1-6алкіл), нітро, CN, =N-О-С1-6алкілу, -ОN=С1-6алкілу або галогену. Ця група охоплює також підгрупу сполук або їх фармацевтично прийнятні солі, де: 6циклоалкіл 13 R1 являє собою -С3-6циклоалкіл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з -С1-6алкілу, -С1-6алкокси, ОН, аміно, -(С0-6алкіл)SOр-(С1-6алкіл), нітро, CN, =N-О-С1-6алкілу, -ON=С1-6алкілу або галогену. Ця група охоплює ще одну підгрупу сполук або їх фармацевтично прийнятні солі, де: R являє собою водень. Ця група охоплює також ще одну підгрупу сполук або їх фармацевтично прийнятні солі, де: R2 являє собою водень або -С1-3залкіл або галоген. R3 являє собою водень або галоген. Ця група охоплює також ще одну підгрупу сполук або їх фармацевтично прийнятні солі, де: R1 являє собою –С3-6циклоалкіл, необов'язково заміщений метилом або галогеном; і R являє собою водень. Ця група охоплює також ще одну підгрупу сполук або їх фармацевтично прийнятні солі, де: R1 являє собою циклопропіл, необов'язково заміщений метилом або галогеном; і R і R2 являють собою водень; R3 являє собою водень або галоген. В іншому аспекті, в об'єм варіанту винаходу, описаного вище, входить ще одна група сполук або їх фармацевтично прийнятні солі, де: Υ являє собою циклопропіл-СООН; і Аr являє собою піридил, піримідил або їх оксид. Ця група охоплює підгрупу сполук або їх фармацевтично прийнятні солі, де: R1 являє собою -С1-6алкіл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з -С1-6алкілу, -С1-6алкокси, ОН, аміно, -(С0-6алкіл)SОр-(С1-6алкіл), нітро, CN, =N-O-С1-6алкілу, -ОN=С1-6алкілу або галогену. Ця група охоплює іншу підгрупу сполук або їх фармацевтично прийнятні солі, де: R1 являє собою -С3-6циклоалкіл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з -С1-6алкілу, -С1-6алкокси, ОН, аміно, -(С0-6алкіл)SОр-(С1-6алкіл), нітро, CN, =N-O-С1-6алкілу, -ОN=С1-6алкілу або галогену. Ця група охоплює ще одну підгрупу сполук або їх фармацевтично прийнятні солі, де: R являє собою водень. Ця група охоплює також ще одну підгрупу сполук або їх фармацевтично прийнятні солі, де: R2 являє собою водень або -С1-6залкіл; R3 являє собою водень або галоген. Ця група охоплює також ще одну підгрупу сполук або їх фармацевтично прийнятні солі, де: R1 являє собою -С3-6циклоалкіл, необов'язково заміщений метилом або галогеном; і R являє собою водень. Ця група охоплює також ще одну підгрупу сполук або їх фармацевтично прийнятні солі, де: R1 являє собою циклопропіл, необов'язково заміщений метилом або галогеном; і R і R2 являють собою водень; R3 являє собою водень або галоген. Прикладами сполук згідно з даним винаходом є наступні: 82208 14 2-(транс)-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонова кислота; 2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонова кислота; 2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-3іл}метилпропанова кислота; 2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}метил пропанова кислота; 3-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-іл}-3метилбутанова кислота; {3'-[3-[(циклопропі ламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4іл}(гідрокси)оцтова кислота; 1-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4іл}циклопропанкарбонова кислота; 2-(цис)-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4іл}циклопропанкарбонова кислота; 5-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-іл}-2,2диметил-1,3-діоксолан-4-карбонова кислота; 1-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-3іл}циклопропанкарбонова кислота; 1-ціано-3-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}2,2-диметилциклопропанкарбонова кислота; 2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-3-фтор-1,1'-біфеніл-4іл}циклопропанкарбонова кислота; (цис)-2-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-3іл}циклопропанкарбонова кислота; 2-{3'-бром-5'-[3-[(циклопротламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4іл}циклрпропанкарбонова кислота; 2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-3-метил-1,1'-біфеніл-4іл}циклопропанкарбонова кислота; 2-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-2-метил-1,1'-біфеніл-4іл}циклопропанкарбонова кислота; 2-{3-хлор-3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонова кислота; 2-(цис)-{3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-3-фтор-1,1'-біфеніл4-іл}циклопропанкарбонова кислота; 3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-карбонова кислота; 2-{3'-[3-(морфолін-4-ілкарбоніл)-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонова кислота; 2-{3'-[4-оксо-3-({[5-(трифторметил)-1,3,4тіадіазол-2-іл]аміно}карбоніл)-1,8-нафтиридин1(4Н)-іл]-1,1’-біфеніл-4-іл}циклопропанкарбонова кислота; 15 82208 2-{3'-[3-({[2-(метилтіо)етил]аміно}карбоніл)-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонова кислота; 2-{3'-[3-({[2(метилсульфоніл)етил]аміно}карбоніл)-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонова кислота; 2-{3'-[4-оксо-3-{[2,2,2трифторетил)аміно]карбоніл}-1,8-нафтиридин1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонова кислота; 2-(5-{3-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]феніл}тієн-2іл)циклопропанкарбонова кислота; 2-{3'-[3-{[(циклопропілметил)аміно]карбоніл}-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонова кислота; 2-{3'-[3-{[(1-ціаноциклопропіл)аміно]карбоніл}4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонова кислота; 3-{3'-[3-[(ізопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}-3метилбутанова кислота; і їх фармацевтично прийнятні солі. В іншому варіанті здійснення даний винахід стосується сполук, представлених формулою (І): (I) і їх фармацевтично прийнятні солі, де Аr являє собою феніл, піридил, піримідил, індоліл, хінолініл, тієніл, піридоніл, оксазоліл, оксадіазоліл, тіадіазоліл або імідазоліл; або їх оксиди, якщо Аr являє собою гетероарил; Υ являє собою -COOR4, С1-6алкіл (С1-6алкіл)nСООR4, -С3-4циклоалкіл(С1-4алкіл)m-СОOR4, де -С16алкіл і С3-4циклоалкіл необов'язково заміщені галогеном, алкокси, гідрокси або нітрилом, і (С1замісники необов'язково пов'язані з 4алкіл) утворенням С3-4циклоалкілу; де n має значення 0, 1, 2, 3 або 4, m має значення 0, 1 або 2; R і R4 кожний незалежно вибраний з N або -С16алкілу; R1 являє собою N або -С1-6алкіл, -С36циклоалкіл, -С1-6алкокси, -С2-6алкеніл, С3-6алкініл, гетероарил або гетероцикл, необов'язково заміщений 1-3 замісниками, незалежно вибраними з галогенС1-6алкілу, -С1-6алкілу, -С1-6алкокси, ОН, аміно, -(С0-6алкіл)-SOр-(С1-6алкіл), нітро, CN, =N-ОС1-6алкілу, -О-N=С1-6алкілу або галогену, де p має значення 0, 1 або 2, або R1 являє собою -С1-6алкіл, моно-або дизаміщений замісниками, вибраними з фенілу і -С3-6циклоалкілу; R2 являє собою Н, галоген, -CN, -NO2s -С16алкіл, -С3-6циклоалкіл, -О-С3-6циклоалкіл, О-С16алкіл, О-С3-6циклоалкіл-С^балкіл (С3-6циклоалкіл) (С3-6циклоалкіл), -С1-6алкокси, феніл, гетероарил, гетероцикл, аміно, -С(О)-С1-6алкіл, -С(О)-О-С1 6алкіл, 16 -С1-6алкіл(=N-ОН), -C(N=NOH) С1-6алкіл, -С0SОкNН(С0-6алкіл) або (С0-6алкіл)-SОk-С1-6алкіл), де феніл, гетероарил або гетероцикл необов'язково заміщені галогеном, -С1-6алкілом, -С1-6алкокси, гідрокси, аміно або С(О)-О-С1-6алкілом, і де алкіл або циклоалкіл необов'язково заміщені 1-6 замісниками, незалежно вибраними з атомів галогенів або -ОН, і де k має значення 0,1 або 2; R3 вибраний з Н, галогену, CN, -С1-6алкілу, -С3циклоалкілу, нітро, -С(О)-С1-6алкілу, -С(O)-O-С06 6алкілу, -SОn'NН(С0-6алкіл) або -(С0-6алкіл)SОn'-(С16алкіл), О-С1-6алкілу, -О-С3-6циклоалкілу, де n' має значення 0, 1 або 2, і де алкіл і циклоалкіл необов'язково заміщені 1 - 6 замісниками, незалежно вибраними з галогену або ОН. В одному аспекті сполуки згідно з даним винаходом є корисними для лікування дефіциту пізнавальної здатності (такого як погіршення пам'яті, як вказано в даному описі) через психологічну дисфункцію, неврологічного розладу (такого як удар) або психіатричної дисфункції. В іншому аспекті даний винахід спрямований на спосіб поліпшення пізнавальної здатності у здорового суб'єкта, що включає введення безпечної, поліпшуючої пізнавальну здатність кількості інгібітору фосфодіестерази-4. Зокрема, даний винахід спрямований на спосіб поліпшення пам'яті, запам'ятовування, втримання в пам'яті, здатності згадувати, упевненості і розсудливості у здорових суб'єктів, що включає введення безпечної і ефективної кількості інгібітору фосфодіестерази-4 формули І. В об'ємі даної заявки як суб'єкт мається на увазі суб'єкт, що володіє пізнавальною здатністю в нормальних межах для суб'єктів цього віку або іншої класифікації. Пізнавальна здатність здорової людини, а також поліпшення її пізнавальної здатності показана з приведенням випробувань сполук у водному лабіринті Морріса (Morris), описаному McNamara and Skelton, Psychobiology, 1993, 21, 101-108. Більш детально відповідна методика описана в [WO 96/25948]. Інші методи визначення поліпшення пізнавальної здатності включають, але не обмежуються цим, "Т" критерій Maze; тест витягнутої руки Maze; уповільнений непарний і уповільнений парний критерій; процедуру пасивного уникнення; 5-вибіркове випробування, розкриті в [WO 01/87281 А2, опублікованої 22 листопада 2001р.]. У даному описі класи здорових суб'єктів включають підлітків, дорослих і людей старшого віку із середньою пізнавальною здатністю; підлітків, дорослих і людей старшого віку з пізнавальною здатністю вище середньої; і підлітків, дорослих і людей старшого віку з пізнавальною здатністю нижче середньої. У даному описі підлітки визначаються як люди молодші 18 років. В описі дорослі визначаються як люди віку 18 років і старше. Цей клас охоплює людей від 18 до 40 років. У даному описі люди старшого віку визначаються як люди віку 40 років і старше. Цей клас охоплює людей віку від 55 років і старше, віку від 65 років і старше, віку від 70 років і старше. 6алкіл(окси)С1-6алкілфеніл, 17 Як повинно бути зрозуміло фахівцям, починаючи від 25 років пізнавальна здатність у здорових людей знижується з швидкістю, яку можна виміряти і відтворити, наприклад, наступними описаними методами: [Cambridge Neurophysiological Test Automated Battery (CANTAB, de Jager CA, Milwain E, Budge Μ. Early detection of isolated memory deficits in the eldery: the need for more sensitive neurophysiological tests. Psycol Med 2002 Apr;32(3): 483-91); Cognitive Drug research Battery (CDR, Barker A, Jones R, Simpson P, Wesnes K. (1995). Scopolamine induced cognitive impairment as a predictor of cognitive decline in healthy elderly volunteers. International Journal of Geriatric Psychiatry 10: 1059-1062)]. Таким чином, після досягнення віку 40 років пізнавальна здатність істотно знижується, і її можна поліпшити способом, поліпшуючим пізнавальну здатність. У даному описі "алкіл", а також інші групи, що мають префікс "алк", наприклад такі, як алкокси, алканоїл, алкеніл,. алкініл і т.п., означають вуглецеві ланцюги, які можуть бути лінійними або розгалуженими, або їх поєднання. Приклади алкільних груп включають метил, етил, пропіл, бутил, втор-і трет-бутил, пентил, гексил, гептил і т.п. "Алкеніл", "алкініл" і подібні терміни включають вуглецеві ланцюги, що містять, щонайменше, один ненасичений С-С зв'язок. Термін "галогеналкіл", наприклад, "галогенС16алкіл", означає алкіл, заміщений однією або декількома групами галогенів. Термін "циклоалкіл" означає карбоцикли, що не містять гетероатомів, і включає моно-, бі- і трициклічні насичені карбоцикли, а також конденсовані кільцеві системи. Такі конденсовані кільцеві системи можуть включати одне кільце, що є частково або повністю ненасиченим, таке як бензольне кільце, для утворення конденсованої кільцевої системи, такої як бензоконденсовані карбоцикли. Циклоалкіл включає такі конденсовані кільцеві системи, як спіроконденсовані кільцеві системи. Приклади циклоалкілу включають циклопропіл, циклобутан, циклопентан, циклогексил, декагідронафталін, адамантан, інданіл, інденіл, флуореніл, 1,2,3,4тетрагідронафталін і т.п. Аналогічним чином, "циклоалкеніл" означає карбоцикли, що не містять гетероатомів і що містять, щонайменше, один неароматичний подвійний С-С зв'язок, і включають моно-, бі- і трициклічні частково насичені карбоцикли, а також бензоконденсовані циклоалкани. Приклади циклоалкенілу включають циклогексеніл, інденіл і т.п. Термін "циклоалкокси", якщо конкретно не вказано інше, включає циклоалкільну групу, сполучену зі зв'язуючим атомом окси. Термін "алкокси", якщо конкретно не вказано інше, включає алкільну групу, сполучену зі зв'язуючим атомом окси. Термін "арил", якщо конкретно не вказано інше, включає багатокільцеві системи, а також системи з одним кільцем, наприклад, такі як феніл або нафтил. 82208 18 Термін "арилокси", якщо конкретно не вказано інше, включає багатокільцеві системи, а також системи з одним кільцем, наприклад, такі як феніл або нафтил, сполучені в місці приєднання через зв'язуючий атом окси. Термін "С0-6алкіл", включає алкіли, що містять 6, 5, 4, 3, 2, 1 або 0 атомів вуглецю. Алкіл, що не містить атомів вуглецю, являє собою водневий замісник або простий зв'язок - в залежності від того, чи є алкіл кінцевою групою або місточковою групою. Термін "гетеро", якщо конкретно не вказано інше, включає один або декілька атомів О, S або N. Наприклад, гетероциклоалкіл і гетероарил включають кільцеві системи, що містять один або декілька атомів О, S або N в кільці, включаючи комбінації таких атомів. Гетроатоми заміняють кільцеві атоми вуглецю. Так, наприклад, гетероциклоС5алкіл являє собою п'ятичленне кільце, що містить від 5 до 0 атомів вуглецю. Приклади гетероарилу включають, наприклад, піридиніл, хінолініл, ізохінолініл, піридазиніл, піримідиніл, піразиніл, хіноксалініл, фурил, бензофурил, дибензофурил, тієніл, бензотієніл, піроліл, індоліл, піразоліл, індазоліл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, імідазоліл, бензімідазоліл, оксадіазоліл, тіадіазоліл, триазоліл, тетразоліл. Термін "гетероарилокси", якщо конкретно не вказано інше, включає гетероарильну групу, сполучену через зв'язуючий атом окси з місцем приєднання. Приклади гетероарил(С1-6)алкілу включають, наприклад, фурилметил, фурилетил, тієнілметил, тієнілетил, піразолілметил, оксазолілметил, оксазолілетил, ізоксазолілметил, тіазолілметил, тіазолілетил, імідазолілметил, імідазолілетил, бензімідазолілметил, оксадіазолілметил, оксадіазолілетил, тіадіазолілметил, тіадіазолілетил, триазолілметил, триазолілетил, тетразолілметил, тетразолілетил, піридинілметил, піридинілетил, піридазинілметил, піримідинілметил, піразинілметил, хінолінілметил, ізохінолінілметил і хіноксалініл метил. Приклади гетероциклоС3-7алкілу включають, наприклад, азетидиніл, піролідиніл, піперидиніл, піперазиніл, морфолінил, тетрагідрофураніл, імідазолініл, піролідин-2-он, піперидин-2-он і тіоморфолініл. Приклади арил(С1-6)алкілу включають, наприклад, феніл(С1-6)алкіл і нафтил(С1-6)алкіл. Приклади гетероциклоС3-7алкілкарбоніл(С1включають, наприклад, азетидиніл 6)алкілу карбоніл(С1-6)алкіл, піролідиніл карбоніл(С 1-6)алкіл, піперидиніл карбоніл(С1-6)алкіл, піперазиніл карбоніл(С1-6)алкіл, морфолініл карбоніл(С1-6)алкіл і тіоморфолініл карбоніл(С1-6)алкіл. Термін "амін", якщо конкретно не вказано інше, включає первинні, вторинні і третинні аміни. Термін "карбамоїл", якщо не вказано інше, включає -NHC(O)OC1-C4алкіл і -ОС(О)NНС1C4алкіл. Термін "галоген" включає атоми фтору, хлору, брому і йоду. 19 Термін "необов'язково заміщений" означає і заміщений і незаміщений. Так, наприклад, необов'язково заміщений арил може являти собою пентафторфеніл або фенільне кільце. Крім того, заміщення може бути зроблене по будь-якій з груп. Наприклад, заміщений арил(С1-6)алкіл включає заміщення по арильній групі, а також заміщення по алкільній групі. Термін "оксид" гетероарильних груп використовується в його звичайному, широко відомому хімічному значенні і включає, наприклад, N-оксиди гетероатомів азоту. Описані в даний заявці сполуки містять один або декілька подвійних зв'язків і можуть, таким чином, утворювати цис/транс ізомери, а також інші конформаційні ізомери. Даний винахід включає всі такі можливі ізомери, а також суміші таких ізомерів. Описані в даний заявці сполуки можуть містити один або декілька центрів асиметрії і можуть, таким чином, утворювати діастереомери, а також оптичні ізомери. Даний винахід включає все такі можливі діастереомери, а також їх рацемічні суміші, їх по суті чисті розділені енантіомери, всі можливі геометричні ізомери і їх фармацевтично прийнятні солі. Наведена вище формула І показана без певної стереохімії в певних положеннях. Даний винахід включає всі стереоізомери формули І і їх фармацевтично прийнятні солі. Крім того, включені суміші стереоізомерів, а також виділені конкретні стереоізомери. У ході стадій синтезу, що використовуються для отримання таких сполук, або при використанні стадій рацемізації або епімеризації, які відомі фахівцям в даній галузі, продуктами таких стадій можуть бути суміші стереоізомерів. Термін "фармацевтично прийнятні солі" відноситься до солей, отриманих з фармацевтично прийнятних нетоксичних основ або кислот. Якщо сполука згідно з даним винаходом є кислотною, її відповідну сіль можна отримати з фармацевтично прийнятних нетоксичних основ, включаючи неорганічні основи і органічні основи. Солі, отримані з таких неорганічних основ включають солі алюмінію, амонію, кальцію, міді (одновалентної і двовалентної), двовалентного заліза, одновалентного заліза, літію, магнію, марганцю (одновалентного і двовалентного), калію, натрію, цинку і т.п. Особливо переважні солі амонію, кальцію, магнію, калію і натрію. Солі, отримані з фармацевтично прийнятних нетоксичних органічних основ, включають солі первинних, вторинних і третинних амінів, а також циклічних амінів і заміщених амінів, таких як природні і синтетично отримані заміщені аміни. Інші фармацевтично прийнятні нетоксичні органічні основи, з яких можуть бути утворені солі, включають іонообмінні смоли, такі як, наприклад, аргінін, бетаїн, кафеїн, холін, Ν,Ν'дибензилетилендіамін, діетиламін, 2діетиламіноетанол, 2-диметиламіноетанол, етаноламін, етилендіамін, N-етилморфолін, Nетилпіперидин, глюкамін, глюкозамін, гістидин, 82208 20 гідрабамін, ізопропіламін, лізин, метилглюкамін, морфолін, піперазин, піперидин, поліамінові смоли, прокаїн, пурини, теобромін, триетиламін, триметиламін, трипропіламін, трометамін і т.п. Якщо сполука згідно з даним винаходом є основною, її відповідну сіль можна отримати з фармацевтично прийнятних нетоксичних кислот, включаючи органічні і неорганічні кислоти. Такі кислоти включають, наприклад, оцтову, бензолсульфонову, бензойну, камфорсульфонову, лимонну, етансульфонову, фумарову, глюконову, глутамінову, бромистоводневу, хлористоводневу, ізетіонову, молочну, малеїнову, мигдалеву, метансульфонову, слизеву, азотну, памову, пантотенову, фосфорну, янтарну, сірчану, винну, п-толуолсульфонову кислоту і т.п. Особливо переважними є бензолсульфонова, лимонна, бромистоводнева, хлористоводнева, малеїнова, фосфорна, сірчана і винна кислоти. Фармацевтичні композиції згідно з даним винаходом включають сполуку, представлену формулою І (або її фармацевтично прийнятні солі), як активний інгредієнт, фармацевтично прийнятний носій і, необов'язково, інші терапевтичні інгредієнти або ад'юванти. Такі додаткові терапевтичні інгредієнти включають, наприклад, і) антагоністи рецепторів лейкотрієну, іі) інгібітори біосинтезу лейкотрієну, ііі) кортикостероїди, iv) антагоністи рецепторів НІ, ν) агоністи бета 2 адренорецептора, vi) селективні інгібітори СОХ-2, vii) статини, viii) нестероїдні протизапальні лікарські засоби ("NSAID") і iх) антагоністи М2/М3. Композиції включають композиції, придатні для перорального, ректального, місцевого і парентерального (включаючи підшкірне, внутрішньом'язове і внутрішньовенне) введення, хоча найбільш відповідне введення для будь-якого конкретного випадку залежить від конкретного пацієнта, природи і тяжкості стану, для лікування якого вводять даний активний інгредієнт. Фармацевтичні композиції можна отримати у вигляді стандартної лікарської форми, і вони можуть бути отримані будь-яким способом, добре відомим в галузі фармацевтики. Для місцевого застосування можна використати креми, мазі, желе, розчини або суспензії, що містять сполуку формули І. Місцеве застосування відповідно до даного винаходу охоплює полоскання для порожнини рота і полоскання для горла. Для лікування таких станів, як і) легеневих захворювань, наприклад, астми, хронічного бронхіту, хронічного обструктивного захворювання легенів (COPD), респіраторного дистрес-синдрому у дорослих, респіраторного дистрес-синдрому у дітей, кашлю, хронічного обструктивного захворювання легенів у тварин, іі) шлунковокишкових розладів, наприклад, виразкового коліту, хвороби Крона і підвищеної секреції шлункової кислоти, ііі) інфекційних захворювань, наприклад, сепсису або септичного шоку бактерійного, грибкового або вірусного типу, ендотоксичного шоку (і пов'язаних з цим станів, таких як ламініт і коліки у коней) і септичного шоку, iv) неврологічних 21 захворювань, наприклад, травми спинного мозку, травми голови, нейрогенного запалення, болю і реперфузійного ураження головного мозку, ν) запальних захворювань, наприклад, псоріатичного артриту, ревматоїдного артриту, анкілозуючого спондиліту, остеоартриту, запалення і опосередкованої цитокінами хронічної дегенерації тканини, vi) алергічних захворювань, наприклад, алергічного риніту, алергічного кон'юнктивіту і еозинофільної гранульоми, vii) психіатричних захворювань, наприклад, депресії, погіршення пам'яті і монополярної депресії, vii) нейродегенеративних захворювань, наприклад, хвороби Паркінсона, хвороби Альцгеймера, гострого і хронічного розсіяного склерозу, іх) дерматологічних захворювань, наприклад, псоріазу і інших доброякісних або злоякісних проліферативних шкірних захворювань, атопічного дерматиту і кропивниці, х) онкологічних захворювань, наприклад, раку, росту пухлини і інвазії ракової пухлини в нормальні тканини, хі) метаболічних розладів, наприклад, нецукрового діабету, хіі) кісткових захворювань, наприклад, остеопорозу, хііі) серцево-судинних розладів, наприклад, рестенозу артерій, атеросклерозу, реперфузійного ураження міокарда, і xiv) інших захворювань, наприклад, хронічного гломерулонефриту, весняного кон'юнктивіту, відторгнення трансплантату і захворювання "трансплантат проти хазяїна" і кахексії, що є чутливими до інгібування PDE4, корисними є дози в межах від близько 0,001мг/кг до близько 140мг/кг маси тіла, або альтернативно, від близько 0,5мг до близько 2,7г на пацієнта в день. Крім того, повинно бути зрозуміло, що сполуку згідно з даним винаходом, яка інгібує PDE4, можна вводити в профілактично ефективних дозах для профілактики вищеперелічених станів. Кількість активного інгредієнта, яку можна поєднувати з матеріалом носія для отримання одиниці лікарської форми, варіюється в залежності від суб'єкта, що підлягає лікуванню, і від конкретного способу введення. Наприклад, композиція, призначена для перорального введення людині, може містити від близько 0,5мг до близько 5г активної речовини, сполученої з відповідною і зручною кількістю матеріалу носія, яка може варіювати від близько 5 до близько 95 процентів від загальної маси композиції. Стандартні лікарські форми звичайно містять від близько 0,01мг до близько 1000мг активного інгредієнта, типово, 0,01мг, 0,05мг, 0,25мг, 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг, 500мг, 600мг, 800мг або 1000мг. Однак повинно бути зрозуміло, що конкретний рівень дозування для будь-якого конкретного пацієнта залежить від різних факторів, включаючи вік, масу тіла, загальний стан здоров'я, стать, раціон харчування, час введення, шлях введення, швидкість виведення з організму, комбінацію лікарських засобів і тяжкість конкретного захворювання, яке лікують. На практиці сполуки, представлені формулою І, або їх фармацевтично прийнятні солі згідно з даним винаходом можна об'єднувати як активний 82208 22 інгредієнт в суміші з фармацевтичним носієм відповідно до традиційних методів отримання фармацевтичних композицій. Носій може бути в різноманітних формах в залежності від форми препарату, яка бажана для введення, наприклад, пероральної або парентеральної (включаючи внутрішньовенну). Так, фармацевтичні композиції згідно з даним винаходом можуть надаватися у вигляді окремих дозованих одиниць, відповідних для перорального введення, таких як капсули, саше або таблетки, кожна з яких містить заздалегідь визначену кількість активного інгредієнта. Крім того, композиції можуть бути приготовані в формі порошку, гранул, розчину, суспензії у водній рідині, у вигляді неводної рідини, у вигляді емульсії масло-в-воді або емульсії водав-маслі. Крім звичайних лікарських форм, описаних вище, сполука, представлена формулою І, або її фармацевтично прийнятні солі також можна вводити за допомогою засобів і/або пристроїв доставки з вивільненням, що контролюється. Композиції можуть бути отримані будь-яким з способів, що застосовуються в фармацевтиці. Як правило, такі способи включають стадію поєднання активного інгредієнта з носієм, що складається з одного або декількох необхідних інгредієнтів. Як правило, композиції отримують однорідним і рівномірним змішуванням активного інгредієнта з рідкими носіями або тонко подрібненими твердими носіями або і тим і іншим. Потім продукту надають зручну форму з отриманням бажаного зовнішнього вигляду препарату. Таким чином, фармацевтичні композиції згідно з даним винаходом можуть включати фармацевтично прийнятний носій і сполуку або фармацевтично прийнятну сіль формули І. Сполуки формули І або їх фармацевтично прийнятні солі можна також включати в фармацевтичні композиції в поєднанні з однією або декількома іншими терапевтично активними сполуками. Фармацевтичний носій, який використовують, може являти собою, наприклад, тверду речовину, рідину або газ. Приклади твердих носіїв включають лактозу, білу глину, сахарозу, тальк, желатин, агар, пектин, аравійську камедь, стеарат магнію і стеаринову кислоту. Прикладами рідких носіїв є цукровий сироп, арахісова олія, оливкова олія і вода. Приклади газоподібних носіїв включають діоксид вуглецю і азот. При отриманні композицій для пероральної лікарської форми можна використати будь-які зручні фармацевтичні середовища. Наприклад, воду, гліколі, масла, спирти, віддушки, консерванти, барвники і т.п. можна використати для отримання пероральних рідких препаратів, таких як суспензії, еліксири і розчини; тоді як носії, такі як крохмаль, цукор, мікрокристалічна целюлоза, розріджувачі, гранулювальні речовини, змазки, зв'язуючі, розпушувачі і т.п. можна використати для отримання пероральних твердих препаратів, таких як порошки, капсули і таблетки. Через простоту введення таблетки і капсули є переважними разовими дозами пероральної 23 лікарської форми, при цьому використовують тверді фармацевтичні носії. Таблетки необов'язково можуть мати покриття, нанесене стандартним водним або неводним способом. Таблетку, що містить композицію згідно з даним винаходом, можна отримати пресуванням або формуванням, необов'язково з одним або декількома допоміжними інгредієнтами або ад'ювантами. Пресовані таблетки можна отримати пресуванням у відповідній машині активного інгредієнта у вільно текучій формі, такій як порошок або гранули, необов'язково змішаний зі зв'язуючою, мастильною речовиною, інертним розріджувачем, поверхнево-активною речовиною або диспергуючим агентом. Формовані таблетки можна отримати формуванням у відповідній машині суміші порошкоподібної сполуки, змоченої рідким інертним розріджувачем. Кожна таблетка переважно містить від близько 0,1мг до близько 500мг активного інгредієнта, а кожні саше або капсула переважно містить від близько 0,1мг до близько 500мг активного інгредієнта. Фармацевтичні композиції згідно з даним винаходом, придатні для парентерального введення, можуть бути приготовані у вигляді розчинів або суспензій активних сполук у воді. Може бути додана відповідна поверхнево-активна речовина, така як, наприклад, гідроксипропілцелюлоза. Дисперсії також можуть бути приготовані в гліцерині, рідких поліетиленгліколях і їх сумішах в маслах. Крім того, може бути доданий консервант для запобігання шкідливому росту мікроорганізмів. Фармацевтичні композиції згідно з даним винаходом, придатні для введення шляхом ін'єкції, включають стерильні водні розчини або дисперсії. Крім того, композиції можуть знаходитися в формі стерильних порошків для приготування таких розчинів або дисперсій для негайного введення. У всіх випадках готова форма для ін'єкції повинна бути стерильною і досить рідкою для забезпечення легкого введення через шприц. Фармацевтичні композиції повинні бути стабільними в умовах виготовлення і зберігання; тому вони, переважно, повинні бути захищені від забруднюючої дії мікроорганізмів, таких як бактерії і гриби. Носій може являти собою розчинник або дисперсійне середовище, що містить, наприклад, воду, етанол, поліол (наприклад, гліцерин, пропіленгліколь і рідкий поліетиленгліколь), рослинні олії і відповідні суміші цих речовин. Фармацевтичні композиції згідно з даним винаходом можуть знаходитися в формі, придатній для місцевого застосування, такій як, наприклад, аерозоль, крем, мазь, лосьйон, тонкоподрібнений порошок і т.п. Крім того, композиції можуть знаходитися в формі, придатній для черезшкірного використання. Такі композиції можуть бути отримані з використанням сполуки формули І згідно з даним винаходом або її фармацевтично прийнятних солей із застосуванням традиційних способів переробки. Як приклад, крем або мазь отримують змішуванням гідрофільної речовини і води разом з 5% мас. -10% мас. сполуки з 82208 24 отриманням крему або мазі, що мають бажану консистенцію. Фармацевтичні композиції згідно з даним винаходом можуть знаходитися в формі, придатній для ректального введення, де носій являє собою тверду речовину. Переважно, щоб суміш утворювала стандартні одиниці лікарської форми, такої як супозиторії. Відповідні носії включають масло какао і інші речовини, широко відомі в галузі техніка. Супозиторії можна зручним чином отримувати спочатку змішуванням композиції з розм'якшеним або розплавленим носієм(ями), з подальшим охолоджуванням і формуванням в спеціальних формах. Крім вищеперелічених інгредієнтів носія фармацевтичні композиції, описані вище, можуть включати, якщо це є відповідним, один або декілька додаткових інгредієнтів носія, наприклад, розріджувачі, буфери, віддушки, зв'язуючі, поверхнево-активні речовини, загусники, змащувальні речовини, консерванти (включаючи антиоксиданти) і т.п. Крім того, можуть бути включені інші ад'юванти для надання композиції ізотонічності з кров'ю передбачуваного реципієнта. Композиції, що містять сполуку формули І або її фармацевтично прийнятні солі, можна отримувати в формі порошку або рідкого концентрату. Було виявлено, що сполуки і фармацевтичні композиції згідно з даним винаходом виявляють біологічну активність як інгібітори PDE4. Відповідно, наступний аспект даного винаходу включає лікування у ссавців, наприклад, і) легеневих захворювань, наприклад, астми, хронічного бронхіту, хронічного обструктивного захворювання легенів (COPD), респіраторного дистрес-синдрому у дорослих, респіраторного дистрес-синдрому у дітей, кашлю, хронічного обструктивного захворювання легенів у ссавців, іі) шлунково-кишкових розладів, наприклад, виразкового коліту, хвороби Крона і підвищеної секреції шлункової кислоти, ііі) інфекційних захворювань, наприклад, сепсису або септичного шоку бактерійного, грибкового або вірусного типу, ендотоксичного шоку (і пов'язаних з цим станів, таких як ламініт і коліки у коней) і септичного шоку, iv) неврологічних захворювань, наприклад, травми спинного мозку, травми голови, нейрогенного запалення, болю і реперфузїйного ураження головного мозку, ν) запальних захворювань, наприклад, псоріатичного артриту, ревматоїдного артриту, анкілозуючого спондиліту, остеоартриту, запалення і опосередкованої цитокінами хронічної дегенерації тканини, vi) алергічних захворювань, наприклад, алергічного риніту, алергічного кон'юнктивіту і еозинофільної гранульоми, vii) психіатричних захворювань, наприклад, депресії, погіршення пам'яті і монополярної депресії, vii) нейродегенеративних захворювань, наприклад, хвороби Паркінсона, хвороби Альцгеймера, гострого і хронічного розсіяного склерозу, іх) дерматологічних захворювань, наприклад, псоріазу і інших доброякісних або злоякісних проліферативних шкірних захворювань, атонічного дерматиту і кропивниці, х) онкологічних захворювань, наприклад, раку, росту пухлини і 25 інвазії ракової пухлини в нормальні тканини, хі) метаболічних розладів, наприклад, нецукрового діабету, хіі) кісткових захворювань, наприклад, остеопорозу, хііі) серцево-судинних розладів, наприклад, рестенозу артерій, атеросклерозу, реперфузїйного ураження міокарда, і xiv) інших захворювань, наприклад, хронічного гломерулонефриту, весняного кон'юнктивіту, відторгнення трансплантату І захворювання "трансплантат проти хазяїна" і кахексії захворювань, які піддаються лікуванню шляхом інгібування ізоферменту PDE4 і підвищення, внаслідок цього, рівнів сАМР - шляхом введення ефективної кількості сполук згідно з даним винаходом. Термін "ссавці" включає людину, а також інших ссавців, таких як, наприклад, собаки, кішки, коні, свині і корови. Відповідно, повинно бути зрозуміло, що лікування ссавців, відмінних від людини, являє собою лікування захворювань, клінічно відповідних тим, які приводилися як приклад вище як таких, що відносяться до захворювань людини. Крім того, як описано вище, сполуку згідно з даним винаходом можна використати в поєднанні з іншими терапевтичними сполуками. Зокрема, можна використати комбінації сполуки-інгібітора PDE4 з і) антагоністами рецепторів лейкотрієну, іі) інгібіторами біосинтезу лейкотрієну, ііі) селективними інгібіторами СОХ-2, iv) статинами, v) NSAID, vi) антагоністами М2/МЗ, vii) кортикостероїдами, viii) антагоністами рецепторів НІ (гістаміну) і іх) агоністами бета 2 адренорецептора. Так наприклад, легеневі захворювання, такі як астма, хронічний бронхіт, хронічне обструктивне захворювання легенів (COPD), респіраторний дистрес-синдром у дорослих, респіраторний дистрес-синдром у дітей, кашель, хронічне обструктивне захворювання легенів у ссавців, зручно лікувати з використанням капсул, саше або таблеток, кожна з яких містить 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг або 500мг активного інгредієнта - сполуки згідно з даним винаходом або її фармацевтично прийнятної солі, які вводять один, два або три рази на день. Шлунково-кишкові розлади, такі як виразковий коліт, хвороба Крона і підвищена секреція шлункової кислоти, зручно лікувати з використанням капсул, саше або таблеток, кожна з яких містить 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг або 500мг активного інгредієнта сполуки згідно з даним винаходом або її фармацевтично прийнятної солі, які вводять один, два або три рази на день. Інфекційні захворювання, такі як сепсис або септичний шок бактерійного, грибкового або вірусного типу, ендотоксичний шок (і пов'язані з цим стани, такі як ламініт і коліки у коней), і септичний шок, зручно лікувати з використанням капсул, саше або таблеток, кожна з яких містить 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг або 500мг активного інгредієнта -сполуки згідно з даним винаходом або її фармацевтично прийнятної солі, які вводять один, два або три рази на день. 82208 26 Неврологічні захворювання, такі як травма спинного мозку, травма голови, нейрогенне запалення, біль і реперфузійне ураження головного мозку, зручно лікувати з використанням капсул, саше або таблеток, кожна з яких містить 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг або 500мг активного інгредієнта - сполуки згідно з даним винаходом або її фармацевтично прийнятної солі, які вводять один, два або три рази на день. Запальні захворювання, такі як псоріатичний артрит, ревматоїдний артрит, анкілозуючий спондиліт, остеоартрит, запалення і опосередкована цитокінами хронічна дегенерація тканини, зручно лікувати з використанням капсул, саше або таблеток, кожна з яких містить 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг або 500мг активного інгредієнта - сполуки згідно з даним винаходом або її фармацевтично прийнятної солі, які вводять один, два або три рази на день. Алергічні захворювання, такі як алергічний риніт, алергічний кон'юнктивіт і еозинофільна гранульома, зручно лікувати з використанням капсул, саше або таблеток, кожна з яких містить 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг або 500мг активного інгредієнта - сполуки згідно з даним винаходом або її фармацевтично прийнятної солі, які вводять один, два або три рази на день. Психіатричні захворювання, такі як депресія, погіршення пам'яті і монополярна депресія, зручно лікувати з використанням капсул, саше або таблеток, кожна з яких містить 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг або 500мг активного інгредієнта - сполуки згідно з даним винаходом або її фармацевтично прийнятної солі, які вводять один, два або три рази на день. Нейродегенеративні захворювання, такі як хвороба Паркінсона, хвороба Альцгеймера, гострий і хронічний розсіяний склероз, зручно лікувати з використанням капсул, саше або таблеток, кожна з яких містить 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг або 500мг активного інгредієнта - сполуки згідно з даним винаходом або її фармацевтично прийнятної солі, які вводять один, два або три рази на день. Дерматологічні захворювання, такі як псоріаз і інші доброякісні або злоякісні проліферативні шкірні захворювання, атонічний дерматит і кропивниця, зручно лікувати з використанням капсул, саше або таблеток, кожна з яких містить 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг або 500мг активного інгредієнта -сполуки згідно з даним винаходом або її фармацевтично прийнятної солі, які вводять один, два або три рази на день. Онкологічні захворювання, такі як рак, ріст пухлини і інвазія ракової пухлини в нормальні тканини, зручно лікувати з використанням капсул, саше або таблеток, кожна з яких містить 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг або 500мг активного інгредієнта - сполуки згідно з даним винаходом або її фармацевтично прийнятної солі, які вводять один, два або три рази на день. 27 Метаболічні розлади, такі як нецукровий діабет, зручно лікувати з використанням капсул, саше або таблеток, кожна з яких містить 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг або 500мг активного інгредієнта - сполуки згідно з даним винаходом або її фармацевтично прийнятної солі, які вводять один, два або три рази на день. Кісткові захворювання, такі як остеопороз, серцево-судинні розлади, такі як рестеноз артерій, атеросклероз, реперфузійне ураження міокарда, і інші захворювання, така як хронічний гломерулонефрит, весняний кон'юнктивіт, відторгнення трансплантату і захворювання "трансплантат проти хазяїна" і кахексія, зручно лікувати з використанням капсул, саше або таблеток, кожна з яких містить 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг або 500мг активного інгредієнта - сполуки згідно з даним винаходом або її фармацевтично прийнятної солі, які вводять один, два або три рази на день. Для поліпшення пізнавальної здатності (наприклад, поліпшення пам'яті, здатності до запам'ятовування, втримання в пам'яті, здатності згадувати, упевненості і розсудливості) корисними є дози від близько 0,0001мг/кг до близько 50мг/кг маси тіла на день, або від близько 0,005мг до близько 2,5г на пацієнта в день. Альтернативно, дози від близько 0,001мг до 10мг сполуки на кілограм маси тіла на день, або альтернативно, від близько 0,05мг до близько 500мг на пацієнта в день. Кількість активного інгредієнта, яку можна об'єднувати з матеріалом носія з отриманням одиниці лікарської форми, варіює в залежності від підлягаючого лікуванню хазяїна і конкретного шляху введення. Наприклад, зручно, якщо композиція, призначена для перорального введення людині, містить від близько 0,005мг до близько 2,5г активної речовини в поєднанні з відповідною і зручною кількістю матеріалу носія. Стандартні лікарські форми звичайно містять від близько 0,005мг до близько 1000мг активного інгредієнта, звичайно, 0,005, 0,01мг, 0,05мг, 0,25мг, 1мг, 5мг, 25мг, 50мг, 100мг, 200мг, 300мг, 400мг, 500мг, 600мг, 800мг або 1000мг, при введенні один, два або три рази на день. Абревіатури, що використовуються в даний заявці мають значення, вказані в таблиці нижче. Абревіатури, які не вказані в таблиці, мають загальноприйняті значення, якщо не вказано інше. 82208 28 4 Аналізи, що демонструють біологічну активність LPS і FMLP-індуковані TNF-α і LTB4 аналізи з використанням цільної крові людини З цільної крові отримують білок і збагачене клітинами середовище, відповідне для дослідження біохімічної ефективності протизапальних сполук, таких як селективні інгібітори PDE4. Нормальна, нестимульована кров людини не містить детектовані рівні TNF-α і LTB4. При стимуляції за допомогою LPS активовані моноцити експресують і секретують TNF-αаж до 8 годин, і рівні вмісту в плазмі залишаються стабільними протягом 24 годин. Опубліковані результати досліджень показали, що інгібування TNF-αшляхом підвищення внутрішньоклітинного сАМР в результаті інгібування PDE4 і/або підвищеній активності аденілілциклази відбувається на рівні транскрипції. Синтез LTB4 також чутливий до рівнів внутрішньоклітинного сАМР і може бути повністю інгібований селективними інгібіторами PDE4. Оскільки 29 протягом 24 годин LPS-стимуляції цільної крові продукується невелика кількість LTB4, для синтезу LTB4 активованими нейтрофілами необхідна додаткова LPS-стимуляція з подальшою fMLPстимуляцією цільної крові. Таким чином, використовуючи одну і ту ж пробу крові, можна визначити активність сполуки на двох сурогатних маркерах активності PDE4 в цільній крові з використанням методики, описаної нижче. Свіжу кров брали з вени здорових людей (чоловіків і жінок), що добровільно беруть участь у випробуванні, і збирали в гепаринізовані пробірки. У цих добровольців не було ніяких явно виражених запальних станів, і вони не приймали ніяких NSAID протягом, щонайменше, 4 днів до взяття крові. 500-мкл аліквоти крові заздалегідь інкубували або з 2мкл носія (DMSO), або з 2мкл сполуки, що випробовується, в різних концентраціях протягом 15 хвилин при 37°С. Потім додавали або 10мкл носія (PBS) у вигляді контрольного розчину, або 10мкл LPS (кінцева концентрація 1мкг/мл, #L-2630 (Sigma Chemical Co., St.Louis, MO) з E.coli, серотип 0111:В4; розбавлений в 0,1% мас/об. BSA (в PBS)). Після 24 годин інкубації при 37°С до крові додавали ще 10мкл PBS (контроль) або 10мкл LPS (кінцева концентрація 1мкг/мл) і інкубували протягом ЗО хвилин при 37°С. Потім кров стимулювали або 10мкл 'PBS (контроль), або 10мкл fMLP (кінцева концентрація 1мкМ, #F-3560 (Sigma); розбавлений в 0,1% мас/об. BSA (в PBS)) протягом 15 хвилин при 37°С. Зразки крові центрифугували при 1500xg протягом 10 хвилин при 4°С з отриманням плазми. 50-мкл аліквоту плазми змішували з 200мкл метанолу для осадження білка і центрифугували, як описано вище. Супернатант аналізували на LTB4 з використанням набору для імуноферментного аналізу (#520111 від Cyaman Chemical Co., Ann Arbor, MI) відповідно до процедури виробника. TNF-α аналізували в розбавленій плазмі (в PBS), використовуючи набір ELISA (Cistron Biotechnology, Pine Brook, NJ), відповідно до процедури виробника. Отримані в прикладах значення ІК50 звичайно знаходилися в межах від 0,075мкМ до 25мкМ. Протиалергічна активність in vivo Сполуки згідно з даним винаходом були перевірені на їх дію відносно IgEопосередкованого алергічного легеневого 82208 30 запалення, індукованого у сенсибілізованих морських свинок вдиханням антигену. Морських свинок спочатку сенсибілізували до овальбуміну при слабкій циклофосфамід-індукованій імуносупресії шляхом внутрішньочеревинної ін'єкції антигену в поєднанні з гідроксидом алюмінію і коклюшевою вакциною. Через два і чотири тижні вводили бустерні дози антигену. Після шести тижнів тварин стимулювали овальбуміном в формі аерозолю під захистом антигістамінного засобу (мепіраміну), який вводили внутрішньочеревинно. Ще через 48 годин здійснювали бронхіальний альвеолярний лаваж (BAL) і підраховували кількість еозинофілів і інших лейкоцитів в BAL рідинах. Також видаляли легені для гістологічного дослідження на запальне ураження. Введення сполук даного винаходу (0,001-10мг/лп в/ч або п/о) до трьох разів протягом 48 годин з подальшою стимуляцією антигеном приводило до значного зниження еозинофілії і накопичення інших запальних лейкоцитів. Також спостерігалася менш запальне ураження в легенях тварин, оброблених сполуками згідно з даним винаходом. Протокол аналізу активності PDE з використанням SPA Здійснювали відбір сполук, які інгібують гідроліз сАМР до AMP за допомогою сАМРспецифічної фосфодіестерази типу IV, в форматі 96-ямкового планшета таким чином: У 96-ямковий планшет при 30°С додавали сполуку, що випробовується (розчинену в 2мкл DMSO), 188мл субстратного буферу, що містить [2,8-3Н]аденозин 3',5'-циклофосфат (сАМР, від 100нМ до 5мкМ), 10мМ MgCl2, 1мМ 4 EDTA, 50мМ Тріс, рН7,5. Реакцію ініціювали додаванням 10мл людської рекомбінантної PDE4 (кількість контролювали так, щоб за 10хв. утворилося -10% продукту). Через 10 хвилин реакцію зупиняли додаванням 1мг PDE-SPA гранул (Amersham, Pharmacia Biotech, Inc., Piscataway, NJ). Визначали кількість утвореного продукту AMP на лічильнику для 96-ямкових планшетів Wallac Microbeta® (FG&G Wallac Co., Gaithersburg, MD). Сигнал відсутності ферменту визначали як фоновий. 100% активність визначали по детектованому сигналу в присутності ферменту і DMSO за вирахуванням фонового сигналу. Відповідно розраховували процент інгібування. Значення ІК50 апроксимували методом нелінійної регресії з використанням рівняння стандартні 4 параметра/множинні дільниці зв'язування на основі даних титрування по десяти точках. Значення ІК50 прикладів, розкриті нижче, визначали при 100нМ сАМР, використовуючи очищений злитий білок GST людської рекомбінантної фосфодіестерази IVb (met-248), отриманий з системи експресії бакуловірус/Sf-9-. Значення ІК50 прикладів, розкриті нижче, знаходяться в межах від 0,01нМ до 2300нМ. 31 Приведені нижче приклади призначені для ілюстрації деяких переважних варіантів виконання винаходу, і не призначені для якого-небудь обмеження даного винаходу. Якщо конкретно не вказане інше, експерименти здійснювали в наступних умовах. Всі операції здійснювали при кімнатній температурі або при температурі навколишнього середовища, тобто при температурі в межах 1825°С. Випарювання розчинника здійснювалина роторному випарнику при зниженому тиску (6004000Па: 4,5-30мм рт.ст.) при температурі бані до 60°С. Хід реакції відстежували методом тонкошарової хроматографії (ТШХ), і час реакції приводиться тільки з метою ілюстрації. Точки плавлення нескориговані, і "d" означає розкладання. Вказані точки плавлення були визначені для речовин, отриманих, як описано нижче. У деяких прикладах отримання при виділенні речовин з різними точками плавлення може мати місце поліморфізм. Структуру і чистоту всіх кінцевих продуктів підтверджували, щонайменше, одним з наступних методів: ТШХ, мас-спектрометрія, ядерний магнітний резонанс (ЯМР) або мікроаналітичні дані. Якщо вказаний вихід продукту, ці дані представлені виключно в ілюстративних цілях. Якщо представлені дані ЯМР, вони представлені в формі дельта (δ) одиниць для основних діагностичних протонів, виражені в мільйонних частках (ррт) відносно тетраметилсилану (TMS) як внутрішній стандарт, отримані при 300МГц, 400МГц або 500МГц з використанням вказаного розчинника. Загальноприйняті абревіатури, що використовуються для позначення форми сигналу, наступні: s - синглет; d - дублет; t - триплет; m мультиплет; br - уширений; і т.д. Крім того, "Аr" означає ароматичний сигнал. Хімічні символи мають їх звичайні значення; також використали наступні абревіатури: об. (об'єм), мас. (маса), b.р. (точка кипіння), m.р. (точка плавлення), л (літр(и)), мл (мілілітри),г (грам(и)),мг (міліграм(и)), моль (молі), ммоль (мілімолі),екв. (еквівалент(и)). Способи синтезу Сполуки згідно з даним винаходом можна отримати відповідно до наступних способів. Замісники - ті ж, що і в Формулі І, за винятком випадків, якщо вказано інше. 1-(3-бромфеніл)-1,4-дигідро-[1,8]нафтиридин4-он-3-карбоксамід загальної формули VII 82208 32 отримували відповідно до загального способу, представленого на Схемі 1. Спочатку 2хлорнікотиноїлхлорид формули II конденсували з триетилортоформіатом в присутності оцтового ангідриду з отриманням 2-хлорнікотиноїлакрилату формули III. Після додання відповідно заміщеного галогенарил аміну формули IV отримували 3ариламіноакрилат типу V. Циклізацію сполуки V до 1-галогенарил-1,4-дигідро-[1,8]нафтиридин-4-онкарбоксилату формули VI здійснювали в присутності надмірної кількості сильної основи при кімнатній температурі. Альтернативно, проміжну сполуку VI можна отримати способом, здійснюваним в одній посудині, з використанням, наприклад, 2-хлорнікотиноїлхлориду і етил N,Nдиметиламіноакрилату і галогенариламіну IV в присутності основи, такої як триетиламін, в розчиннику, такому як ацетонітрил. Гідроліз VI і подальше поєднання отриманої карбонової кислоти з аміном (RR'NH2) з використанням HATU і основи Hunig дає бажану ключову проміжну сполуку - арилбромід VII. Сполуки формули І отримували, використовуючи будь-який з описаних нижче загальних підходів. Каталізоване паладієм поєднання Suzuki-Miaura між арилбромідом типу VII і відповідно заміщеним арилпінаколборонатом типу VIII може привести до утворення бажаної сполуки І або відповідного складного алкілового ефіру IX. Складноефірна сполука IX може бути гідролізована за допомогою LiOH в ТГФ/МеОН з отриманням бажаної кислоти І. Альтернативно, арилбромід VII можна перетворити в пінаколборонат XI шляхом каталізованого паладієм поєднання з пінаколдибораном. Описана вище реакція Suzuki-Miyaura між сполукою XI і арилбромідом типу XII може привести до утворення кислоти І або відповідного складного алкілового ефіру IX. На закінчення, реакція поєднання Stille між арилбромідом типу VII і відповідно заміщеним арилстаннаном типу X 33 82208 34 також приводить до отримання бажаної кислоти формули І. коричної кислоти XVIII, використовуючи описану вище процедуру дiазометан/Рd(Ас)2. Цис-складний ефір коричної кислоти XVIII можна отримати модифікованим способом олефінування HornerEmmons з використанням біс(трифторетил)фосфонового ефіру і сильної основи [Still et al. Tetrahedron Lett, 1983, 24,4405]. І складний ефір боронату типу VIII і станнан типу X (Схема 3) можна отримати з проміжної сполуки арилброміду XII шляхом каталізованого паладієм поєднання з використанням, відповідно, пінаколдиборану і гексаалкілдіолова. Цис-і транс-хіральні циклопропанові проміжні сполуки типу XIV і XVII, відповідно, також можна отримати наступними двома способами. Коричну кислоту XIII в присутності GDI перетворюють в ацил-імідазол XIX, який в лужних умовах взаємодіє з оптично чистим оксазолідиноном XX, з утворенням хірального цинамат-оксазолідинону XXI. Циклопропанування сполуки XXI відповідно до описаного вище способу, дає суміш (>5 до 1) діастереоізомерів XXII, яку можна розділити (кристалізація, SiO2). В результаті гідролізу отримують бажаний хіральний циклопропіл XIV. Аналогічним чином, рацемічну суміш циклопропілу типу XIV (XVII) можна перетворити в дві стадії в 1:1 діастереоізомерну суміш описаного вище цинамат-оксазолідинону XXI. Проміжні сполуки типу XII, в яких Υ являє собою циклопропан, як в сполуці формули XIV, можна отримати з використанням будь-якої з наступних чотирьох загальних процедур (Схема 4). Складний ефір коричної кислоти типу XIII, комерційно доступний або отриманий реакцією Horner-Emmons з відповідного альдегіду XV, можна перетворити в циклопропанову сполуку з використанням діазометану в присутності каталітичної кількості діацетату паладія. Отриманий транс-циклопропановий складний ефір XIV можна розділити методом ВЕРХ на колонці Chiral-Pak з отриманням двох окремих енантіомерів. У другому підході, альдегід XV можна перетворити у відповідний стирол XVI за допомогою реакції Wittig з подальшим енантіоселективним циклопропануванням, використовуючи комплекс біс-оксазоліновий хіральний ліганд/мідь і діазоацетат [Evans et al. J.Am.Chem.Soc. 1991, 113, 726]. Отриману, суміш транс XIV і цис XVII циклопропану можна розділити методом селективного гідролізу в лужних умовах (тип гідролізу: тран>цис). Індивідуальні енантіомери (XIV або XVII) можна отримати, використовуючи або R, або S хіральний ліганд. Цис циклопропановий складний ефір XIV також можна отримати з цис-складного ефіру Проміжні сполуки типу XXV (Схема 6) можна отримати депротонуванням складного ефіру типу XXIV з використанням надмірної кількості сильної основи в присутності алкілуючого агента, такого як R5I. Кількість основи і алкілуючого агента по відношенню до початкового складного ефіру співвідноситься з рівнем заміщення (моно vs. біс). Для пропіонових аналогів типу XXVII третбутиловий складний ефір XXVI можна 35 депротонувати з використанням просторово ускладеної основи. Додання алкілуючого агента приводить до суміші моно-і біс-алкілованої сполуки. При повторі цієї процедури отримують, в основному, складний ефір типу XXVII. Циклопропіловий аналог типу XXX можна отримати в дві стадії з відповідного арилацетонітрилу XXVIII. Реакція фазового перенесення з використанням нітрилу XXVIII і 2хлорброметану у водному розчині сильної основи дає циклопропілнітрил XXIX [Org. Prep. & Рrос. 1995, 27, 355]. Гідроліз з використанням NaOH в киплячому етанолі дає бажану кислоту XXX. (1,1диметил)етиларил типу XXXIII можна отримати в три стадії. (2-Хлор-1,1-диметилетил)арил типу XXXI можна перетворити у відповідний складний ефір XXXII спочатку шляхом гасіння солі Гріньяра XXXI діоксидом вуглецю з подальшою етерифікацією отриманої кислоти діазометаном. Електрофільне заміщення складного арилового ефіру XXXIL в середовищі, що генерує катіон йодонію, дає бажаний йодарил XXXIII [J. Am. Chem. Soc. 1948, 70, 370.]. Заміщений циклопропіл типу XXXV можна отримати в дві стадії (Схема 7). Адукт Knoevenagel XXXIV, отриманий конденсацією альдегіду XV і етилціаноацетату, можна перетворити в циклопропіл XXXV в присутності 2-нітропропану і основи в киплячому етанолі [Tetrahedron Lett. 1985, 26, 1923]. На завершення, проміжні циклічні ацеталеві сполуки типу XXXVII можна отримати в дві стадії з цинамату XIII. Біс-гідроксилювання цинамату XIII з використанням умов, розроблених [Sharpless et al. (AD-mix. J. Org. Chem. 1992, 57, 2768)], після конденсації з ацетоном в присутності каталітичної кількості кислоти діолу XXXVI, дає бажаний хіральний ацеталь XXXVII. 82208 36 Нафтиридинон 1 N-Ізопропіл-1-(3-бромфеніл)-1,4дигідро[1,8]нафтиридин-4-он-3-карбоксамід Стадія 1: Етил 3-(3-броманіліно)-2-(2хлорнікотиноїл)акрилат Суміш етил 2-хлорнікотиноїлацетату (отриманого відповідно до способу, описаного в [J. het. Chem., 30, 855. 1993] (1екв.), триетилортоформіату (1,5екв.) і оцтового ангідриду (5екв.) нагрівали при 130°С протягом 2,5 годин. Леткі компоненти відганяли і залишок двічі випарювали разом з ксилолом. Маслянистий залишок розчиняли в метиленхлориді і повільно додавали 3-броманілін (1,2екв.). Отриманий розчин перемішували при кімнатній температурі протягом 18 годин і випарювали розчинник. Отриману иеочищену сполуку використали без очищення на наступній стадії. Стадія 2: Етил 1-(3-бромфеніл)-1,4дигідро[1,8]нафтиридин-4-он-3-карбоксилат Неочищену сполуку зі стадії 1 розчиняли в тетрагідрофурані (0,3М), розчин охолоджували до 0°С і по порціях додавали гідрид натрію (60% дисперсія в маслі, 1,3екв.). Після перемішування при 0°С протягом 1 години суміші давали нагрітися до кімнатної температури. Через 2 години до суспензії додавали воду і нерозчинну тверду речовину відфільтровували і промивали водою у великій кількості. Після висихання тверду речовину перемішували в простому ефірі при кімнатній температурі протягом 24 годин і фільтрували з отриманням вказаної в заголовку сполуки у вигляді твердої речовини кремового кольору. 1 Н ЯМР (Ацетон-d6) δ 1,32 (т, 3Н), 4,29 (кв, 2Н), 7,54-7,63 (м, 2Н), 7,69 (дд, 1Н), 7,78 (дд, 1H), 7,93 (с, 1Н), 8,66-8,71 (м, 3Н). Альтернативно, для стадій 1-2 можна використати наступний спосіб. Суміш 2-хлорнікотиноїлхлориду (1екв.), триетиламіну (4екв.) і етил 3,3диметиламіноакрилату (1,5екв.) в ацетонітрилі (0,5М) нагрівали до температури кипіння із зворотним холодильником протягом 3 годин, охолоджували до 40-50°С і додавали 3-броманілін (1екв.). Реакційну суміш нагрівали до температури кипіння із зворотним холодильником протягом ночі, охолоджували до кімнатної температури, розбавляли водою (2 об'єми). Продукт виділяли 37 фільтруванням і промивали водою, простим ефіром або сумішшю ацетонітрил-вода (1:1). Стадія 3: 1-(3-бромфеніл)-1,4дигідро[1,8]нафтиридин-4-он-3-карбонова кислота Суспензію етил 1-(3-бромфеніл)-1,4дигідро[1,8]нафтиридин-4-он-3-карбоксилату зі стадії 2 (1екв.) в суміші тетрагідрофуран-метанол (0,15М) і 1н водний розчин гідроксиду натрію (2екв.) нагрівали приблизно при 50°С протягом 20 хвилин при перемішуванні. Після охолоджування суміш розбавляли водою і підкисляли 1н водним розчином НСI. Після перемішування протягом 45 хвилин осад відфільтровували, ретельно промивали водою і сушили з отриманням вказаної в заголовку кислоти у вигляді твердої речовини кремового кольору. 1 Н ЯМР (Ацетон-d6) δ 7,65 (т, 1Н), 7,76 (м, 2Н), 7,84 (д, 1H), 7,99 (с, 1Н), 8,87 (м, 2Н), 9,01 (с, 1H). Стадія 4: N-ізопропіл-1-(3-бромфеніл)-1,4дигідро[1,8]нафтиридин-4-он-3-карбоксамід До суспензії 1-(3-бромфеніл)-1,4дигідро[1,8]нафтиридин-4-он-3-карбонової кислоти зі стадії 3 (1екв.) і триетиламіну (3екв.) в тетрагідрофурані (0,08М) при 0°С додавали ізобутилхлорформіат (1,8екв.). Після перемішування при 0°С протягом 2 годин додавали ізопропіламін (5екв.) і суміші давали нагрітися до кімнатної температури і перемішували протягом ночі. Потім суміш розподіляли між етилацетатом і водою, органічну фазу сушили і упарювали до отримання твердої речовини, яку перемішували в простому ефірі при кімнатній температурі протягом 3 годин і фільтрували з отриманням N-ізопропіл-1-(3бромфеніл)-1,4-дигідро[1,8]нафтиридин-4-он-3карбоксаміду у вигляді білої твердої речовини. 1 Н ЯМР (Ацетон-d6) δ 1,25 (д, 6Н), 4,17 (м, 1Н), 7,59-7,63 (м, 2Н), 7,70 (д, 1H), 7,80 (д, 1H), 7,94 (с, 1H), 8,73 (м, 1Н), 8,78 (д, 1H), 8,85 (с, 1H), 9,61 (ушир, ΝH). Нафтиридинон 2 N-Циклопропіл-1-(3бромфеніл)-1,4-дигідро[1,8]нафтиридин-4-он-3карбоксамід Слідуючи способу отримання нафтиридинону 1, але замінюючи на стадії 4 ізопропіламін циклопропіламіном, отримували вказану в заголовку сполуку у вигляді рихлої білої твердої речовини. 1 H ЯМР (Ацетон-d6) δ 0,59 (м, 2Н), 0,80 (м, 2Н), 2,96 (м, 1Н), 7,59-7,68 (м, 2Н), 7,72 (дд, 1H), 7,82 (дд, 1H), 7,97 (с, 1H), 8,72-8,81 (м, 2Н), 8,89 (с, 1H), 9,70 (ушир., ΝN). Нафтиридинон 3 N-Циклопропіл-4-оксо-1-[3-(4,4,5,5тетраметил-1,3,2-діоксаблоролан-2-іл)феніл]-1,4дигідро-1,8-нафтиридин-3-карбоксамід 82208 38 Суміш нафтиридинону 2 (1,0екв.), пінаколдиборану (1,5екв.), КОАс (4екв.) і PdCl2(dppf) (0,05екв.) в DMF (0,2М) перемішували при 70-80°С протягом 3 годин. Суміш охолоджували до кімнатної температури, розбавляли ЕtOАс і розчином NH4CI. Органічні екстракти промивали H2J, насиченим сольовим розчином, сушили над MgSO4, фільтрували і концентрували. Після кристалізації з простого ефіру і флеш-хроматографії (СН2Сl2: ЕtOАс, 50:50) маточного розчину отримували вказану в заголовку сполуку у вигляді білої твердої речовини. 1 Н ЯМР (500МГц, Ацетон-d6): 9,78 (с, 1Н), 8,90 (с, 1Н), 8,79 (дд, 1Н), 8,72 (дд, 1Н), 7,94 (д, 1H), 7,91 (с, 1Н), 7,80 (д, 1H), 7,69 (т, 1H), 7,62 (дд, 1H), 2,9 (м, 1Н), 1,38 (с, 12Н), 0,80 (м, 2Н), 0,60 (м, 2Н). Нафтиридинон 4 Отримували відповідно до способу, описаного для отримання нафтиридинону 3, але використовуючи нафтиридинон 1 як вихідну речовину. Приклад 1 2-(транс)-{3'-[3-[(Циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонова кислота Стадія 1: Етил 2-(транс)-(4бромфеніл)циклопропанкарбоксилат До суміші етил 4-бромцинамату і Pd(OAc)2 (0,05екв.) в метиленхлориді (1М) при 0°С 39 додавали по краплях розчин CH2N2 в простому ефірі доти, поки за даними ЯМР реакція не завершувалася. Суміш фільтрували через шар силікагелю і концентрували з отриманням вказаної в заголовку сполуки у вигляді масла. Стадія 2: Етил 2-(транс)-[4-(4,4,5,5тетраметил-1,3,2-діоксаборолан-2іл)феніл]циклопропанкарбоксилат Суміш броміду зі стадії 1 (1,0екв.), пінаколдиборанового ефіру (1.4екв.), КОАс (3,5екв.) і PdCl2(dppf) (0,03екв.) в DMF (0,14М) перемішували при 60°С протягом 24 годин. Отриману суміш охолоджували до кімнатної температури, розбавляли ЕtOАстексаном (1:1). Органічну фазу промивали водою, насиченим сольовим розчином, сушили над MgSO4, фільтрували і концентрували. Флешхроматографія (гексан:ЕtOАс; 90:10) давала вказанув заголовку сполуку. Стадія 3: 2-(транс)-[4-(4,4,5,5-тетраметил1,3,2-діоксаборолан-2іл)феніл]циклопропанкарбонова кислота Суміш складного ефіру зі стадії 2 і NaOH (20%, 30мл) нагрівали до 100°С протягом 1,5 годин, охолоджували до кімнатної температури, підкисляли 10% НСI і екстрагували ЕtOАс. Органічний екстракт сушили над Na2SO4 і випарювали розчинник з отриманням вказаної в заголовку сполуки. Стадія 4: 2-(транс)-{3'-[3[(Циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонова кислота Суміш нафтиридинону 2 (1,0екв.), кислоти зі стадії 3 (1,5екв.), Na2CO3 (3,5екв., 2М в Н2О), Pd(OAc)2 (0,05екв.) і PPh3 (0,15екв.) або PdCl2dppf (0,05екв.) в н-пропанолі-DMF (1:1, 0,1М) перемішували при 70°С протягом 2 годин. Суміш охолоджували до кімнатної температури, гасили АсОН і розбавляли ЕtOАс. Об'єднані органічні екстракти промивали насиченим сольовим розчином, сушили над Na2SO4, фільтрували і концентрували. Флеш-хроматографія (CH2Cl2:EtОAc; 60:40, 2% АсОН) давала вказану в заголовку сполуку у вигляді білої твердої речовини. 1 Н ЯМР (500МГц, CDCI 3): δ 9,9 (д, 1H), 9,08 (с, 1Н), 8,77 (дд, 1H), 8,69 (дд, 1H), 7,71 (д, 1H), 7,60 (м, 2Н), 7,52 (д, 2Н), 7,45 (м, 1H), 7,38 (д, 1H), 7,13 (д, 2Н), 2,97 (м, 1Н), 2,54 (м, 1H), 1,87 (м, 1H), 1,60 (м, 1Н), 1,35 (м, 1H), 0,85 (м, 2Н), 0,65 (м, 2Н). МС (H-): 464,2. Оптично активні ізомери прикладу 1 можуть бути виділені окремо методом хроматографії з використанням хіральної колонки; наприклад, Chiral Pak AD, елююючи гексаном:ЕtOН або гексаном.іРrОН, що містить 0,2% TFA. Альтернативно, розділення можна здійснити на проміжній сполуці (транс)-2-(4бромфеніл)циклопропанкарбоновій кислоті (транс)-2-(4бромфеніл)циклопропанкарбонова кислота До розчину складного ефіру зі стадії 1 в ТГФМеОН (4:1, 0,5М) додавали LiOH (3екв., 2М) і суміш перемішували при 50°С протягом 1 години. Органічний розчинник випарювали, водну фазу 82208 40 підкисляли 1н розчином НСI і кислоту екстрагували EtOAc (3X). Органічну фазу промивали насиченим сольовим розчином, сушили і випарювали розчинник з отриманням 2(4-бромфеніл)циклопропанкарбонової кислоти. Оптично активні попередники отримували розділенням на хіральній колонці (Chiral Pak AD), елююючи гексаном:ЕtOН або гексаном.iРrOН, що містить 0,2% TFA. Наступна альтернатива являє собою використання хіральної допоміжної сполуки, як описано нижче. Стадія 1: (транс)-3-(4-Бромфеніл)-1-імідазол1-ілпропенон До розчину (транс)-3-(4-бромфеніл)акрилової кислоти (1,0екв.) в толуолі (0,2М) додавали CDI (1,5екв.). Суміш перемішували при кімнатній температурі протягом 3 годин. Отриманий залишок виділяли фільтруванням з отриманням вказаної в заголовку сполуки у вигляді білої твердої речовини. Стадія 2: (транс)-3-[3-(4-бромфеніл)-акрилоїл]4-метил-5-фенілоксазолідин-2-он Суміш 3-(4-бромфеніл)-1-імідазол-1ілпропенону (1,05екв.) зі стадії 1, (4R, 5S)-(+)-4метил-5-феніл-2-оксазолідинону (1,0екв.) або (-)ізомеру і Et3N (1,2екв.) в CH3CN (0,2Μ) кип'ятили із зворотним холодильником протягом ночі. Отриману суміш охолоджували до кімнатної температури, фільтрували через шар силікагелю і концентрували. Кристалізація в гексані: Et2O давала вказану в заголовку сполуку у вигляді білої твердої речовини. Стадія 3: (транс)-3-[2-(4бромфеніл)циклопропанкарбоніл]-4-метил-5фенілоксазолідин-2-он До розчину (транс)-3-[3-(4бромфеніл)акрилоїл]-4-метил-5-фєнілоксазолідин2-ону з Стадії 2 і Pd(OAc)2 (0,05екв.) в ТГФ (0,2М) по порціях додавали CH2 N2 до завершення реакції. Реакцію відстежували шляхом аналізу аліквот методом ЯМР. Отриману суміш концентрували і піддавали флеш-хроматографії (гексан:ЕtOАс; 362) з отриманням двох окремих діастереоізомерів. Кожний діастереоізомер окремо піддавали описаним нижче процедурам з отриманням (+) і (-) енантіомерів прикладу 1. Стадія 4: 2-(транс)-(4бромфеніл)циклопропанкарбонова кислота До розчину аміду зі стадії 3 в ТГФ-ЕtOН-Н2О (4:1:1, 0,1М) додавали LiOH (2,4екв., 2М) і суміш перемішували при кімнатній температурі протягом 2 годин. Суміш нейтралізували до рН7 за допомогою 1н розчину НСI, органічний розчинник випарювали і отриманий залишок розчиняли в простому ефірі. Органічну фазу промивали 1н розчином NaOH (2X). Об'єднані водні шари підкисляли і екстрагували простим ефіром (3Х). Органічний екстракт промивали насиченим сольовим розчином, сушили і випарювали розчинник з отриманням (+) або (-)-(транс)-2-(4бромфеніл)циклопропанкарбонової кислоти у вигляді білої твердої речовини. Стадія 5: 2-(транс)-{3'-[3[(Циклопропіламіно)карбоніл]-4-оксо-1,8 41 нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}циклопропанкарбонова кислота Суміш нафтиридинону 3 (1,0екв.), 2-(транс)-(4бромфеніл)циклопропанкарбонової кислоти (1,2екв.) зі стадії 4, Na2CO3 (3,5екв., 2М в Н2О), Pd(OAc)2 (0,05екв.) і PPh3 (0,15екв.) в н-пропанолі (0,1М) перемішували при 70°С протягом 4 годин. Суміш охолоджували до кімнатної температури, виливали у воду і екстрагували ЕtOАс (2´). Об'єднані органічні екстракти промивали насиченим сольовим розчином, сушили над Na2SO4, фільтрували і концентрували. Флешхроматографія (СН2Сl2:ЕtOАс; 50:50, 2% АсОН) давала вказану в заголовку сполуку у вигляді білої твердої речовини. Ще одна альтернатива являє собою енантіоселективне циклопропанування з використанням, наприклад, комплексу бісоксазоліновий хіральний ліганд/мідь і діазоацетату [Evans et al., J. Am. Chem. Soc. 1991, 113, 726] для отримання оптично активного етил 2-(транс)-(4бромфеніл)циклопропанкарбоксилату з 4бромстиролу. Селективний гідроліз суміші цис- і транс ізомеру з використанням LiOH (1екв. з розрахунку на транс-ефір) давав 2-(транс)-(4бромфеніл)циклопропанкарбонову кислоту і етил 2-(цис)-(4-бромфеніл)циклопропанкарбоксилат, який можна використати в прикладі 8. Приклад 2 2-{3'-[3-[(Циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-3іл}циклопропанкарбонова кислота Стадія 1: Метил 2-(транс)-(3бромфеніл)циклопропанкарбоксилат До суміші 3бромкоричної кислоти і Pd(OAc)2 (0,05екв.) в метиленхлориді (1М) при 0°С додавали по краплях розчин CH2N2 в простому ефірі доти, поки за даними ЯМР реакція не завершувалася. Суміш фільтрували через шар силікагелю і концентрували з отриманням вказаної в заголовку сполуки. Стадія 2: 2-(3бромфеніл)циклопропанкарбонова кислота До розчину складного ефіру зі стадії 1 в ТГФ-МеОН (4:1, 0,5М) додавали LiOH (3екв., 2М) і суміш перемішували при 50°С протягом 1 години. Органічний розчинник випарювали, водну фазу підкисляли 1н розчином НСI і кислоту екстрагували EtOAc (3X). Органічну фазу промивали насиченим сольовим розчином, сушили і випарювали розчинник з отриманням 2(3-бромфеніл)циклопропанкарбонової кислоти. t Стадія 3: 2-(транс)-{3'-[3[(Циклопропіламіно)карбоніл]-4-оксо-1,8 82208 42 нафтиридин-1(4Н)-іл]-1,1'-біфеніл-3іл}циклопропанкарбонова кислота Суміш нафтиридинону 3 (1,0екв.), кислоти зі стадії 2 (1,2екв.), Na2CO3 (3,5екв., 2М в Н2О), PdCl2 (dppf) (0,05екв.) в н-пропанолі (0,1М) перемішували при 90°С протягом 3 годин. Суміш охолоджували до кімнатної температури, гасили за допомогою НСI і розбавляли EtOAc. Об'єднані органічні екстракти промивали насиченим сольовим розчином, сушили над MgSO4, фільтрували і концентрували. Флешхроматографія (CH2Cl2:EtOAc:NH4OH; 75:25:2,5) давала вказану в заголовку сполуку у вигляді білої твердої речовини. 1 Н ЯМР (500МГц, Ацетон-d6) δ м.ч. 0,61 (м, 2 Н) 0,80 (м, 2Н) 1,45 (м, 1Н) 1,52 (м, 1Н) 2,01 (м, 1Н) 2,54 (м, 1H) 2,97 (дт, J=11,35, 3,47Гц, 1H) 7,25 (д, J=8,20Гц, 1H) 7,43 (т, J=7,57Гц, 1Н) 7,63 (м, 4Н) 7,75 (т, J=7,88Гц, 1Н) 7,95 (д, J=8,20Гц, 1Н) 8,04 (с, 1H) 8,75 (дд, J=4,41, 1,89Гц, 1Н) 8,80 (дд, 7=8,20, 1,89Гц, 1H) 8,96 (с, 1Н) 9,76 (с, 1H). Приклад 3 2-{3'-[3-[(Циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-3-іл}-2метилпропанова кислота Стадія 1: Метил 2-(3-бромфеніл)-2метилпропаноат До розчину LiHMDS (1Μ, ТГФ, 2,1екв.) в ТГФ (0,06Μ) додавали метил 3-бромфенілацетат (1екв.). Через 15 хвилин додавали Mel (4екв.) і реакційну суміш повільно нагрівали до кімнатної температури і перемішували протягом 18 годин. Суміш гасили 10% розчином НСI, розбавляли ЕtOАс, промивали 10% розчином НСI, насиченим сольовим розчином, сушили і випарювали розчинник. Флеш-хроматографія (гексан:ЕtOАс; 95:5) давала вказану в заголовку сполуку. Стадія 2: 2-(3-бромфеніл) метилпропанова кислота До розчину складного ефіру зі стадії 1 в ТГФМеОН (4:1, 0,5М) додавали LiOH (3екв., 2М) і суміш перемішували при 50°С протягом 1 години. Органічний розчинник випарювали, водну фазу підкисляли 1н розчином НСI і кислоту екстрагували ЕtOАс (3Х). Органічну фазу промивали насиченим сольовим розчином, сушили і випарювали розчинник з отриманням вказаної кислоти. Стадія 3: 2-{3'-[3-[(Циклопропіламіно)карбоніл]4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-3-іл}2-метилпропанова кислота Суміш нафтиридинону 3 (1,0екв.), кислоти зі стадії 2 (1,5екв.), Na2CO3 (3,5екв., 2М в Н2О) і Pd(Ph3)4 або PdCl2 (dppf) або Pd(OAc)2 (Ph3P) з 43 (0,05екв.) в н-пропанолі (0,1М) перемішували при 70-90°С протягом 3 годин. Суміш охолоджували до кімнатної температури, гасили за допомогою НСI і розбавляли EtOAc. Об'єднані органічні екстракти промивали насиченим сольовим розчином, сушили над MgSO4, фільтрували і концентрували. Флеш-хроматографія (СН2Сl2:МеOН; 99:1) давала вказану в заголовку сполуку у вигляді білої твердої речовини. 1 Н ЯМР (500МГц, Ацетон-d6): δ 11,0 (с, ОН), 9,76 (с, ΝH), 8,95 (с, 1H), 8,74 (дд, 1Н), 8,71 (дд, 1Н), 8,02 (с, 1Н), 7,88 (д, 1H), 7,81 (с, 1H), 7,72 (т, 1H), 7,65 (м, 2Н), 7,58 (дд, 1H), 7,46 (д, 1Н), 2,94 (м, 1H), 1,61 (с, 6Н), 0,77 (м, 2Н), 0,58 (м, 2Н). MC+ECI Q1 (M+1) 468,3. Приклад 4 2-{3'-[3-[(Циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-іл}-2метилпропанова кислота Отримували відповідно до способу, описаного в прикладі 3, але використовуючи як вихідну речовину 4-бромфенілацетат. Флешхроматографія (CH2Cl2:EtOAc, 40:60, 2% АсОН) давала вказану в заголовку сполуку у вигляді білої твердої речовини. 1 Н ЯМР (500МГц, ДМСО-d6): δ 9,75 (д, 1H), 8,81 (с, 1Н), 8,77 (м, 1Н), 8,71 (д, 1Н), 7,92 (с, 1H), 7,86 (д, 1Н), 7,70 (д, 2Н), 7,70-7,55 (м, 3Н), 7,45 (д, 2Н), 2,88 (м, 1Н), 1,50 (с, 6Н), 0,77 (м, 2Н), 0,55 (м, 2Н). Приклад 5 3-{3'-[3-[(Циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл -4-іл}-3метилбутанова кислота Отримували відповідно до способу, описаного в прикладі 3, стадія 2 і 3, але використовуючи як вихідну речовину метиловий ефір 3-(4-йодфеніл)3-метилмасляної кислоти (отриманий відповідно до способу, описаного в [J. Am. Chem. Soc. 1948, 70, 370]). Флеш-хроматографія (CH2Cl2:EtOAc, 82208 44 40:60, 2% AcOH) давала вказану в заголовку сполуку у вигляді білої твердої речовини. 1 Н ЯМР (500МГц, ДМСО-d6): δ 9,75 (д, 1H), 8,82 (с, 1H), 8,78 (дд, 1Н), 8,72 (дд, 1H), 7,94 (с, 1Н), 7,86 (д, 1Н), 7,68-7,60 (м, 2Н), 7,66 (д, 2Н), 7,57 (д, 1Н), 7,49 (д, 2Н), 2,88 (м, 1H), 2,60 (с, 2Н), 1,40 (с, 6Н), 0,76 (м, 2Н), 0,55 (м, 2Н). Приклад 6 {3'-[3-[(Циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4іл}(гідрокси)оцтова кислота Отримували відповідно до способу, описаного в прикладі 3, стадія 3, але використовуючи як вихідну речовину 4-броммигдальну кислоту. Флеш-хроматографія (СН2СІ 2:Ме0Н, від 9:1 до 8:2) з подальшим інтенсивним перемішуванням залишку в СНгСУефір і виділенням шляхом фільтрування давала вказану в заголовку сполуку у вигляді білої твердої речовини. 1 Н ЯМР (500МГц, Ацетон-d6): δ 9,75 (д, 1H), 8,83 (с, 1H), 8,79 (дд, 1H), 8,74 (дд, 1H), 7,97 (с, 1Н), 7,89 (д, 1H), 7,73 (д, 2Н), 7,70 (т, 1H), 7,65 (дд, 1Н), 7,61 (д, 1Н), 7,52 (д, 2Н), 5,03 (с, 1Н), 2,92-2,90 (м, 1Н), 0,80-0,77 (м, 2Н), 0,59-0,56 (м, 2Н). Приклад 7 1-{3'-[3-[(Циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1'-біфеніл-4-іл}циклопропанкарбонова кислота Стадія 1: 1-(4бромфеніл)циклопропанкарбонітрил Суміш 4-бромфенілацетонітрилу (1екв.), 1,2бромхлоретану (1,5екв.), бензилтриетиламонійхлориду (0,14екв.) в 50% розчині NaOH (4Μ) нагрівали до 50°С протягом 18 годин. Суміш охолоджували до кімнатної температури, гасили 5% розчином НСI і розбавляли простим ефіром. Об'єднані органічні екстракти промивали насиченим сольовим розчином, сушили над MgSO4, фільтрували і концентрували. Флеш-хроматографія 45 (гексан:ЕtOАс; 95:5) давала вказану в заголовку сполуку. Стадія 2: 1-(4бромфеніл)циклопропанкарбонова кислота Суміш нітрилу (1екв.) зі стадії 1, 25% розчину NaOH (12екв.) в ЕtOН (0,5Μ) нагрівали до 100°С протягом 5 годин. Суміш охолоджували до кімнатної температури, гасили АсОН і розбавляли простим ефіром. Об'єднані органічні екстракти промивали насиченим сольовим розчином, сушили над MgSO4, фільтрували і концентрували. Флеш-хроматографія (гексан:ЕtOАс, від 90:10 до 50:50) давала вказану в заголовку сполуку. Стадія 3: 1-{3'-[3-[(Циклопропіламіно)карбоніл]4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4іл}циклопропанкарбонова кислота Отримували відповідно до способу, описаного в прикладі 3, стадія 3, але використовуючи як вихідну речовину кислоту зі стадії 2. Флешхроматографія (СН2СІ2:МеОН, 98:2) давала вказану в заголовку сполуку у вигляді білої твердої речовини. 1 H ЯМР (500МГц, Ацетон-d6): δ 9,92 (д, 1H), 9,77 (д, 1Н), 8,96 (с, 1Н), 8,79 (дд, 1Н), 8,74 (дд, 1Н), 8,00 (с, 1Н), 7,76-7,72 (м, 3Н), 7,65 (дд, 1H), 7,61 (дд, 1Н), 7,52 (д, 2Н), 2,98-2,94 (м, 1Н), 1,601,58 (м, 2Н), 1,25-1,22 (м, 2Н), 0,82-0,78 (м, 2Н), 0,62-0,59 (м, 2Н). Приклад 8 2-(цис)-{3'-[3-[(Циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4іл}циклопропанкарбонова кислота Стадія 1: Метил 2-(цис)-3-(4-бромфеніл)проп2-еноат До розчину біс(трифторетил)(метоксикарбонілметил)фосфона ту і 18-краун-6 (5екв.) в ТГФ (0,05М) при -78°С додавали KHMDS (1екв., 0,5М, толуол), а потім 4бромбензальдегід (1екв.). Реакційну суміш перемішували при -78°С протягом 1 години, гасили насиченим розчином хлориду амонію і розбавляли простим ефіром. Об'єднані органічні екстракти промивали насиченим сольовим розчином, сушили « над Na2SO4, фільтрували і концентрували. Флеш-хроматографія (гексан:ЕtOАс, від 9:1 до 7:3) давала вказану в заголовку сполуку. Стадія 2: Метил 2-(цис)-(4бромфеніл)циклопропанкарбоксилат Суміш складного ефіру зі стадії 1 і Pd(OAc)2 (0,05екв.) в метиленхлориді (1М) при 0°С додавали по краплях, розчин CH2N2 в простому ефірі доти, поки за даними ЯМР аналізу реакція не завершувалася. Флеш-хроматографія 82208 46 (гексан:EtOAc, від 100:0 до 90:10) давала вказану в заголовку сполуку. Стадія 3: Метил 2-{3'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-іл}циклопропанкарбоксилат Отримували відповідно до способу, описаного в прикладі 3, стадія 3, але використовуючи як вихідну речовину складний ефір з прикладу 8, стадія 2. Продукт очищали флеш-хроматографією (гексан:ЕtOАс, 60:40) з подальшим інтенсивним перемішуванням залишку в гексані/ефірі і виділенням шляхом фільтрування з отриманням вказаної в заголовку сполуки у вигляді білої твердої речовини. Стадія 4: 2-(цис)-{3'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-іл}циклопропанкарбонова кислота До розчину складного ефіру в ТГФ-ЕtOН (1:1, 0,05М) додавали LiOH (5екв., 2М) і суміш перемішували при 60°С протягом 4 годин. Суміш охолоджували до кімнатної температури, екстрагували простим ефіром. Водну фазу підкисляли 1н розчином НСI і кислоту екстрагували ЕtOАс (3Х). Органічну фазу промивали насиченим сольовим розчином, сушили і випарювали розчинник. Залишок інтенсивно перемішували в суміші СН2Сl2/гексан/ацетон і виділяли фільтруванням з отриманням вказаної в заголовку сполуки у вигляді не зовсім білої твердої речовини. 1 Н ЯМР (500МГц, ДМСО-d6): δ 11,88 (ушир, с, 1H), 9,75 (д, 1H), 8,80 (с, 1Н), 8,79 (дд, 1H), 8,74 (дд, 1Н), 7,95 (с, 1Н), 7,87 (д, 1H), 7,63-7,70 (м, 4Н), 7,59 (д, 1Н), 7,35 (д, 2Н), 2,89-2,93 (м, 1H), 2,62 (дд, 1Н), 2,04-2,09 (м, 1H), 1,31-1,35 (м, 1H), 0,770,87 (м, 2Н), 0,56-0,59 (м, 2Н). Оптично активні діастереоізомери прикладу 8 можна виділити окремо методом хроматографії з використанням хіральної колонки; наприклад, Chiral Pak AD, елююючи гексаном:ЕtOН або гексаном:іРrOН, що містить 0,2% TFA. Альтернативно, оптично активна проміжна сполука може бути отримана, як описано нижче. (цис)-2-(4-Бромфеніл)циклопропанкарбонова кислота До розчину складного ефіру зі стадії 2 в ТГФМеОН (4:1, 0,05М) додавали LiOH (3екв., 2М) і суміш перемішували при 50°С протягом 4 годин. Органічний розчинник випарювали, водний шар підкисляли 1н розчином НСI і кислоту екстрагували EtOAc (3Х). Об'єднані органічні екстракти промивали насиченим сольовим розчином, сушили і упарювали з отриманням 2-(4бромфеніл)циклопропанкарбонової кислоти. Оптично активні проміжні сполуки отримували розділенням на хіральній колонці (Chiral Pak AD) з використанням гексану:ЕtOН (90:10 з 0,2% TFA). Інша альтернатива являє собою використання хіральної допоміжної сполуки, як описано нижче. Стадія 1: (цис)-1-{[2-(4Бромфеніл)циклопропіл]карбоніл}-1H-імідазол До розчину (цис)-2-(4бромфеніл)циклопропанкарбонової кислоти 47 (1,0екв.) в толуолі (0,2М) додавали CDI (1,5екв.). Суміш перемішували при 50°С протягом 18 годин. Розчинник випарювали і залишок інтенсивно перемішували в суміші гексан/СН2Сl, фільтрували і фільтрат упарювали з отриманням вказаної в заголовку сполуки у вигляді білої твердої речовини. Стадія 2: (цис)-3-{[2-(4Бромфеніл)циклопропіл]карбоніл}-4-метил-5феніл-1,3-оксазолідин-2-он Суміш (цис)-1-{[2-(4бромфеніл)циклопропіл]карбоніл}-1Н-імідазолу (1екв.) зі стадії 1, (4R, 5S)-(+)-4-метил-5-феніл-2оксазолідинону (1,2екв.) або (-)-ізомеру і DBU (що додається при 0°С, 1.2екв.) в CH3CN (0,2Μ) перемішували при 0°С протягом 4 годин. Розчинник випарювали і залишок очищали флешхроматографією (гексан:EtOAc, від 100:0 до 80:20) з отриманням кожного діастереоізомеру. Стадія 3: (цис)-2-(4бромфеніл)циклопропанкарбонова кислота До розчину аміду (або (+), або (-) ізомер) зі стадії 2, описаної вище) в ТГФ-Н2О (4:1, 0,5М) при 0°С додавали LiOH (1,6екв., 2М) і Н2О2 (35%, 4екв.). Суміш перемішували при 0°С протягом 4 годин. Органічний розчинник випарювали і суміш екстрагували СН2Сl2, водну фазу підкисляли 1н розчином НСI і кислоту екстрагували EtOAc (3X). Об'єднані органічні екстракти промивали насиченим сольовим розчином, сушили і розчинник випарювали з отриманням або (+), або (-) оптично активної (цис)-2-(4бромфеніл)циклопропанкарбонової кислоти. Ще одна альтернатива являє собою енантіоселективне циклопропанування з використанням, наприклад, комплексу бісоксазоліновий хіральний ліганд/мідь і діазоацетату [Evans et al., J. Am. Chem. Soc. 1991, 113, 726] для отримання оптично активного етил 2-(цис)-(4бромфеніл)циклопропанкарбоксилату з 4бромстиролу. Селективний гідроліз суміші цис і транс ізомеру з використанням LiOH (1екв. з розрахунку на транс-ізомер) давав 2-(транс)-(4бромфеніл)циклопропанкарбонову кислоту (що використовується в Прикладі 1) і бажаний етил-2(цис)-(4-бромфеніл)циклопропанкарбоксилат. Приклад 9 5-{3'-[3-[(Циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-іл}-2,2диметил-1,3-диоксолан-4-карбонова кислота Стадія 1: Етил 3-(4-бромфеніл)-2,3дигідроксипропаноат Слідували методиці, описаній в [J. Org. Chem., 1992, 57, 2768], з використанням етил-4 82208 48 бромцинамату як вихідної речовини. Залишок очищали флеш-хроматографією (гексан:ЕtOАс, 50:50) з отриманням вказаної в заголовку сполуки. Стадія 2: Етил 5-(4-бромфеніл)-2,2-диметил1,3-діоксолан-4-карбоксилат Розчин діолу зі стадії 1(1екв.) в ацетоні (0,2М), диметоксипропану (8екв.) і pTsOH (0,05екв.) перемішували при кімнатній температурі протягом 4 годин. Розчинник випарювали, залишок розчиняли в ЕtOАс і промивали водним розчином NaHCO3. Органічний екстракт промивали насиченим сольовим розчином, сушили над Na2SO4, фільтрували і концентрували. Флешхроматографія (гексан:EtOAc, від 95:5 до 85:15) давала вказану в заголовку сполуку. Стадія 3: Етил 5-{3'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-іл}-2,2диметил-1,3-діоксолан-4-карбоксилат Суміш нафтиридинону 3 (1,0екв.), складного ефіру зі стадії 2 (1,2екв.), Na2CO3 (2,5екв., 2М в Н2О) і Pd(OAc)2 (Ph3P) з (0,05екв.) в DMF-H2O (0,3Μ) перемішували при 80°С протягом 4 годин. Суміш охолоджували до кімнатної температури, розбавляли ЕtOАс і фільтрували через целіт (промивали EtOAc). Органічні екстракти промивали насиченим сольовим розчином, сушили над MgSO4, фільтрували і концентрували. Флеш-хроматографія (гексан:ЕtOАс, 30:70) давала вказану в заголовку сполуку у вигляді білої твердої речовини. Стадія 4: 5-{3'-[3-[(циклопропіламіно)карбоніл]4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-іл}2,2-диметил-1,3-діоксолан-4-карбонова кислота До розчину складного ефіру зі стадії 3 в ТГФМеОН (1:1, 0,05М) додавали LiOH (3екв., 2М) і суміш перемішували при 50°С протягом 15 хвилин. Органічний розчинник випарювали, водну фазу підкисляли 1н розчином НСI і кислоту екстрагували EtOAc (3X). Об'єднаний органічний екстракт промивали насиченим сольовим розчином, сушили і випарювали розчинник, залишок розтирали в порошок в суміші гексан/простий ефір і виділяли фільтруванням з отриманням вказаної в заголовку сполуки. 1 Н ЯМР (500МГц, ацетон-4): δ 11,4 (ушир, с, 1H), 9,76 (д, 1H), 8,97 (с, 1H), 8,79 (дд, 1H), 8,75 (дд, 1H), 8,02 (т, 1H), 7,94 (д, 1H), 7,83 (д, 2Н), 7,76 (т, 1H), 7,6 ПРО-7,68 (м, 4Н), 5,27 (д, 1Н), 4,40 (д, 1Н), 2,95-2,99 (м, 1Н), 1,58 (с, 3Н), 1,53 (с, 3Н), 0,79-0,82 (м, 2Н), 0,59-0,63 (м, 2Н). Приклад 10 1-{3'-[3-[(Циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-3-іл}циклопропанкарбонова кислота 49 82208 50 Отримували відповідно до способу, описаного в прикладі 7, але використовуючи як вихідну речовину 3-бромфенілацетонітрил. Залишок очищали флеш-хроматографією (СН2Сl2:Ме0Н, 96:4), розтирали в порошок в гексані/СН2Сl2 і потім виділяли шляхом фільтрування з отриманням вказаної в заголовку сполуки у вигляді білої твердої речовини. 1 Н ЯMP (500МГц, CDCI 3): δ 9,88 (д, 1H), 9,06 (с, 1Н), 8,79 (дд, 1Н), 8,69 (дд, 1Н), 7,70 (д, 1H), 7,60-7,52 (м, 3Н), 7,49 (д, 1Н), 7,44 (дд, 1Н), 7,397,30 (м, 3Н), 2,95 (м, 1H), 1,65 (м, 2Н), 1,25 (м, 2H), 0,82 (м, 2Н), 0,65 (м, 2Н). Приклад 11 1-Ціано-3-{3'-[3-[(циклопропіламіно)карбоніл]4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-іл}2,2-диметилциклопропанкарбонова кислота Складний ефір зі стадії 3 (1екв.) в CH2Cl2-TFADMS (3:2:1, 0,02Μ) перемішували при кімнатній температурі протягом 48 годин. Леткі речовини випарювали, залишок розтирали з ефіром і потім виділяли фільтруванням з отриманням вказаної в заголовку сполуки у вигляді білої твердої речовини. 1 Н ЯМР (500МГц, Ацетон-d6): δ 9,73 (с, 1H), 8,94 (с, 1Н), 8,77 (дд, 1H), 8,72 (дд, 1H), 8,01 (т, 1H), 7,92 (д, 1H), 7,81 (д, 2Н), 7,73 (т, 1H), 7,64 (дд, 1H), 7,59 (дд, 1H), 7,51 (д, 2Н), 2,93 (м, 1Н), 2,9 (ушир, с, ОН), 1,52 (с, 3Н), 1,36 (с, 3Н), 0,78 (м, 2Н), 0,58 (м, 2Н). Приклад 12 2-{3'-[3-[(Циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-3-фтор-1,1’-біфеніл-4іл}циклопропанкарбонова кислота Стадія 1:трет-бутил (2Е)-3-(4-бромфеніл)-2ціанопроп-2-еноат Суміш 4-бромбензальдегіду (1екв.), третбутилціаноацетату (1екв.) і NH4OAс (1екв.) в бензолі (1М) кип'ятили із зворотним холодильником протягом 4 годин, видаляючи при цьому воду за допомогою пастки Діна-Старка. Суміш охолоджували до кімнатної температури, розбавляли гексаном і розтирали в порошок. Вказану в заголовку сполуку виділяли після фільтрування у вигляді білої твердої речовини. Стадія 2: трет-Бутил 3-(4-бромфеніл)-1-ціано2,2-диметилциклопропанкарбоксилат Слідуючи методиці, описаній в Tetrahedron Lett. 1985, 1923, суміш 2-нітропропану (1екв.), K2СО3 (1екв.) і складного ефіру зі стадії 1 (1екв.) в ЕtOН (1,2М) перемішували при 100°С в закритому бутлі протягом 3 годин. Суміш охолоджували до кімнатної температури, розбавляли ЕtOАс, промивали розчином NH4CI, насиченим сольовим розчином, сушили над MgSO4, фільтрували і концентрували. Флеш-хроматографія (гексан:ЕtOАс, 95:5) давала вказану в t заголовку сполуку у вигляді масла. Стадія 3: трет-Бутил 1-ціано-3-{3'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-іл}-2,2диметилциклопропанкарбоксилат Отримували відповідно до способу, описаного в прикладі 7, стадія 3, але використовуючи як вихідну речовину складний ефір зі стадії 2. Залишок очищали флеш-хроматографією (гексан:ЕtOАс, від 60:40 до 30:70). Стадія 4: 1-Ціано-3-{3'-[3[(Циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-іл}-2,2диметилциклопропанкарбонова кислота Стадія 1: Метил 2-(4-бром-2фторфеніл)циклопропанкарбоксилат До суміші 4-бром-2-фторкоричної кислота і Pd(OAc)2 (0,05екв.) в метиленхлориді (1М) при 0°С додавали по краплях розчин CH2N2 в простому ефірі доти, поки за даними ЯМР реакція не завершувалася. Залишок очищали флешхроматографією (гексан:ЕtOАс, від 100:0 до 70:30). Стадія 2: Метил 2-{3'-[3[(Циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-3-фтор-1,1’-біфеніл-4іл}циклопропанкарбоксилат Суміш нафтиридинону 3 (1,0екв.), складного ефіру зі стадії 1 (1,3екв.), Na2CO3 (3,5екв., 2М в Н2О), Pd(OAc)2 (0,05екв.) і PPh3 (0,15екв.) або PdCl2 dppf (0,05екв.) в н-пропанолі (0,1М) перемішували при 60-80°С протягом 1-3 годин. Суміш охолоджували до кімнатної температури, виливали у воду і екстрагували EtOAc (2´). Об'єднані органічні екстракти промивали насиченим сольовим розчином, сушили над Na2SO4, фільтрували і концентрували. Флешхроматографія (СН2СІ 2:ЕtOАс; 90:10) давала вказану в заголовку сполуку. Стадія 3: 2-(транс)-{3'-[3[Циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-3-фтор-1,1’-біфеніл-4-іл} циклопропанкарбонова кислота До розчину складного ефіру зі стадії 2 в ТГФМеОН (2:1, 0,2М) додавали LiOH (5екв., 2М) і суміш перемішували при кімнатній температурі протягом 6 годин. Органічний розчинник випарювали, водну фазу підкисляли АсОН і кислоту екстрагували EtOAc (3X). Органічний шар промивали насиченим сольовим розчином, сушили і випарювали розчинник. Залишок розтирали в порошок в СН2Сl2/ефірі і потім 51 виділяли фільтруванням з отриманням вказаної в заголовку сполуки у вигляді твердої речовини. 1 Н ЯМР (500МГц, CDCI 3): δ 9,85 (д, 1H), 9,08 (с, 1H), 8,80 (дд, 1H), 8,70 (дд, 1Н), 7,71 (д, 1Н), 7,63 (т, 1N), 7,60 (с, 1H), 7,46 (дд, 1H), 7,40 (д, 1H), 7,28 (м, 2Н), 7,01 (т, 1H), 2,97 (м, 1H), 2,66 (м, 1Н), 1,93 (м, 1H), 1,62 (м, 1Н), 1,40 (м, 1H), 0,84 (м, 2Н), 0,66 (м, 2Н). Оптично активну (+) або (-)-(транс)-2-{3'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-3-фтор-1,1’-біфеніл-4іл}циклопропанкарбонову кислоту можна отримати, використовуючи оптично активний (+) або (-)-(транс)-метил 2-(4-бром-2фторфеніл)циклопропанкарбоксилат, отриманий відповідно до способу, описаного в прикладі 29, стадії 5-8. Приклад 13 (цис)2-{3'-[3-[(Циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-3іл}циклопропанкарбонова кислота Отримували відповідно до способу, описаного в прикладі 8, але використовуючи 3бромбензальдегід як вихідну речовину. 1 Н ЯМР (500МГц, Ацетон-d6): δ 9,78 (ушир, с, 1Н), 8,96 (с, 1H), 8,79 (д, 1Н), 8,76 (д, 1H), 7,97 (с, 1H), 7,91 (д, 1H), 7,75 (т, 1Н), 7,7 (с, 1H), 7,59-7,65 (м, 3Н), 7,34-7,40 (м, 2Н), 2,69 (дд, 1Н), 2,12-2,15 (м, 1H), 1,67 (дд, 1H), 1,35-1,39 (м, 1Н), 0,79-0,83 (м, 2Н), 0,61 (ушир, с, 2Н). Приклад 14 2-{3'-Бром-5'-[3-[(циклопропіламiно)карбоніл]4-оксо-1,8-нафтиридин-1(4Н)-iл]-1,1’-біфеніл-4іл}циклопропанкарбонова кислота Стадія 1: N-Циюіопропіл-1-(3,5-дибромфеніл)4-оксо-1,4-дигідро-1,8-нафтиридин-3-карбоксамід Отримували відповідно до способу, описаного для отримання нафтиридинону 2, але використовуючи 3,5-диброманілін як вихідну речовину. Стадія 2: Етил 2-[4(триметилстанніл)феніл]циклопропанкарбоксилат Суміш етил 2-(транс)-(4бромфеніл)циклопропанкарбоксилату з прикладу 82208 52 1, стадія 1, гексаметилдіолова (3,5екв.) в 1,4діоксані (0,2М) перемішували при 60°С протягом 18 годин, розчинник випарювали і залишок очищали флеш-хроматографією (гексан:ЕtOАс; 95:5) з отриманням вказаної в заголовку сполуки. Стадія 3: Етил 2-{3'-бром-5'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4іл}циклопропанкарбоксилат Суміш складного ефіру зі стадії 2 (1,7екв.), дибром сполуки зі стадії 1 (1екв.), Pd2(dba)3 (0,05екв.) і трифеніларсину (0,25екв.) в DMF (0,05М) нагрівали при 80°С протягом 2 годин. Суміш охолоджували до кімнатної температури, розбавляли EtOAc і водою, органічний шар промивали насиченим сольовим розчином, сушили і випарювали розчинник. Залишок очищали флеш-хроматографією (СН2Сl2:МеOН, від 99:1 до 90:10) з отриманням вказаної в заголовку сполуки. Стадія 4: 2-(транс)-{3'-Бром-5'-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4іл}циклопропанкарбонова кислота До розчину складного ефіру зі стадії 3 в ТГФМеОН-Н2О (2:1:0,5, 0,1М) додавали LiOH (5екв., 2М) і суміш перемішували при 50°С протягом 4 годин. Органічний розчинник випарювали, водну фазу підкисляли АсОН і кислоту екстрагували EtOAc (3X). Органічну фазу промивали насиченим сольовим розчином, сушили і випарювали розчинник. Залишок очищали флешхроматографією (СН2Сl2:МеOН, від 99:1 до 90:10) з отриманням вказаної в заголовку сполуки. 1 Н ЯМР (500МГц, ДМСО-d6): δ 9,71 (д, 1H), 8,84 (с, 1H), 8,80 (дд, 1Н), 8,72 (дд, 1H), 8,08 (с, 1H), 8,01 (с, 1Н), 7,91 (с, 1H), 7,71 (д, 2Н), 7,65 (дд, 1H), 7,29 (д, 2Н), 2,91-2,89 (м, 1Н), 2,46-2,43 (м, 1Н), 1,88-1,85 (м, 1H), 1,47-1,45 (м, 1Н), 1,43-1,38 (м, 1H), 0,81-0,77 (м, 2Н), 0,57-0,56 (м, 2Н). Оптично активні попередники отримували розділенням на хіральній колонці (Chiral Pak AD), елююючи гексаном:ЕtOН (35:65), який містить 0,2% TFA. Приклад 15 2-{3'-[3-[(Циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-3-метил-1,1’-біфеніл-4іл}циклопропанкарбонова кислота Стадія 1: Етил (2Е)-3-(4-бром-2метилфеніл)проп-2-еноат До розчину 4-бром-2-метилбензальдегіду (1екв.) і триетилфосфоноацетату (1,1екв.) в ТГФ (0,3М) при кімнатній температурі додавали по краплях трет-бутоксид калію (1,1екв., 1М, ТГФ). Реакційну суміш перемішували при кімнатній 53 температурі протягом 3 годин, гасили 10% розчином НСl, розбавляли простим ефіром, промивали розчином NaHCO3, насиченим сольовим розчином, сушили над MgSO4, фільтрували і концентрували. Флешхроматографія (гексан:ЕtOАс, від 90:10 до 70:30) давала вказану в заголовку сполуку. Стадія 2: 2-(транс)-{3'-[3[(Циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-3-метил-1,1’-біфеніл-4іл}циклопропанкарбонова кислота Отримували відповідно до способу, описаного в прикладі 12, але використовуючи як вихідну речовину складний ефір зі стадії 1. 1 Н ЯМР (500МГц, CDCI 3): δ 9,82 (д, 1H), 9,10 (с, 1H), 8,80 (дд, 1H), 8,70 (дд, 1Н), 7,60 (м, ЇЙ), 7,48 (м, 2H), 7,40 (м, 2Н), 7,22 (д, 1Н), 7,02 (с, 1H), 6,97 (м, 1Н), 2,98 (м, 1H), 2,55 (м, 1Н), 2,30 (с, 3Н), 1,95 (м, 1H), 1,65 (м, 1Н), 1,40 (м, 1Н), 0,85 (м, 2Н), 0,65 (м, 2Н). Приклад 16 2-{3'-[3-[(Циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-2-метил-1,1’-біфеніл-4іл}циклопропанкарбонова кислота Отримували відповідно до способу, описаного в прикладі 15, але використовуючи 4-бром-Зметилбензальдегід як вихідну речовину. Отримували вказану в заголовку сполуку 2(транс)-{3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-2-метил-1,1’-біфеніл-4іл}циклопропанкарбонову кислоту. 1 H ЯМР (500МГц, CDCI 3): δ 9,88 (с, 1H), 9,10 (с, 1H), 8,80 (д, 1H), 8,70 (д, 1Н), 7,72 (д, 1Н), 7,60 (м, 2Н), 7,45 (дд, 1H), 7,40 (м, 3Н), 7,05 (д, 1H), 2,98 (м, 1Н), 2,55 (м, 1Н), 2,45 (с, 3Н), 1,78 (м, 1Н), 1,60 (м, 1H), 1,40 (м, 1Н), 0,85 (м, 2Н), 0,75 (м, 2Н). Приклад 17 2-{3-3'-[3-[(циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]-1,1-біфеніл-4іл}циклопропанкарбонова кислота 82208 54 Отримували відповідно до способу, описаного в прикладі 15, але використовуючи 4-бром-2хлорбензальдегід як вихідну речовину. 1 Н ЯМР (500МГц, CDCI 3): δ 9,88 (с, 1H), 9,10 (с, 1H), 8,80 (д, 1Н), 8,70 (д, 1H), 7,72 (д, 1H), 7,65 (м, 3Н), 7,45 (м, 3Н), 7,05 (д, 1Н), 2,95 (м, 1Н), 2,70 (м, 1Н), 1,80 (м, 1H), 1,65 (м, 1H), 1,35 (м, 1Н), 0,85 (м, 2Н), 0,65 (м, 2Н). Отримували вказану в заголовку сполуку - 2(транс)-{3-хлор-3'-[3-[(циклопропіламіно)карбоніл]4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4іл}циклопропанкарбонову кислоту. Приклад 18 2-(цис)-{3'-[3-[(Циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-3-фтор-1,1’-біфеніл4-іл}циклопропанкарбонова кислота Отримували відповідно до способу, описаного в прикладі 8, але використовуючи 4-бром-2фторбензальдегід як вихідну речовину. 1 Н ЯМР (500МГц, ДМСО-d6): δ 11,91 (ушир, с, 1H), 9,75 (д, 1H), 8,83 (с, 1H), 8,79 (дд, 1Н), 8,74 (дд, 1H), 8,02 (с, 1Н), 7,93 (д, 1H), 7,70 (т, 1H), 7,627,66 (м, 2Н), 7,57 (д, 1H), 7,54 (д, 1Н), 7,36 (т, 1H), 2,88-2,94 (м, 1Н), 2,55 (кв, 1Н), 2,08-2,13 (м, 1Н), 1,53 (дд, 1Н), 1,36-1,40 (м, 1Н), 0,77-0,81 (м, 2Н), 0,56-0,59 (м, 2Н). Приклад 19 3'-[3-[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин1(4Н)-іл]-1,1’-біфеніл-4-карбонова кислота 55 Стадія 1: Етил 3-[3[(циклопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-карбоксилат Суміш нафтиридинону 3 (1екв.), етил 4бромбензоату (3екв.), Na2CO3 (3,5екв., 2М в Н2О), Pd(PPh3)4 (0,15екв.) в н-пропанолі-DMF (1:1, 0,1М) перемішували при 80°С протягом 2 годин. Суміш охолоджували до кімнатної температури, гасили насиченим сольовим розчином і розбавляли EtOAc. Органічні екстракти промивали насиченим сольовим розчином, сушили над Na2SO4, фільтрували і концентрували. Залишок розтирали в порошок в простому ефірі/ЕtOАс і потім виділяли фільтруванням з отриманням вказаної в заголовку сполуки у вигляді білої твердої речовини. Стадія 2: 3'-[3-[(циклопропіламіно)карбоніл]-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4карбонова кислота До розчину складного ефіру зі стадії 2 в ТТФМеОН-СН2Сl2 (2:2:0,5, 0,2М) додавали LiOH (5екв., 2М) і суміш перемішували при кімнатній температурі протягом 6 годин. Органічний розчинник випарювали, водну фазу підкисляли 1н розчином НСI і кислоту екстрагували EtOAc (3X). Органічний шар промивали насиченим сольовим розчином, сушили і випарювали розчинник. Флешхроматографія (СН2Сl2:МеOН, 80:20 з NH3) давала вказану в заголовку сполуку. 1 Н ЯМР (500МГц, ДМСО-d6): δ 11,2 (с, ОН), 9,75 (с, ΝH), 8,77 (дд, 1Н), 8,73 (дд, 1Н), 8,13 (д, 2Н), 8,07 (с, 1Н), 7,98 (д, 1H), 7,91 (д, 2Н), 7,77 (т, 2Н), 7,70 (д, 1H), 7,60 (дд, 1H), 2,94 (м, 1Н), 0,78 (м, 2Н), 0,57 (м, 2Н). МС+ESI Q1 (M+1) 426,2. Приклад 20 2-{3'-[3-[(Морфолін-4-ілкарбоніл)4-оксо-1,8-нафтиридин-1(4Н)]-іл]-1,1’-біфеніл-4іл}циклопропанкарбонова кислота Стадія 1: 1-(3-Бромфеніл)-3-(морфолін-4ілкарбоніл]-1,8-нафтиридин-1(4Н)-він До розчину кислоти прикладу отримання нафтиридинону 1, стадія 3 (1екв.), в ТГФ (0,1М) додавали оксалілхлорид (1,5екв.) і 2 краплі DMF. Суміш нагрівали до температури кипіння із зворотним холодильником протягом 1 години, охолоджували до кімнатної температури і переносили в розчин морфоліну (3екв., депротонований за допомогою NaH в ТГФ при 0°С). Суміш перемішували при кімнатній температурі протягом 18 годин, гасили розчином NH4CI і розбавляли EtOAc. Органічний шар промивали насиченим сольовим розчином, сушили і випарювали розчинник. Залишок розтирали в порошок в простому ефірі/ЕtOАс і 82208 56 потім виділяли фільтруванням з отриманням вказаної в заголовку сполуки. Стадія 2: Етил 2-[4-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)феніл] циклопропанкарбоксилат Отримували відповідно до методики, описаної для отримання нафтиридинону 3, але використовуючи як вихідну речовину етил 2(транс)-(4-бромфеніл)циклопропанкарбоксилат з прикладу 1, стадія 1. Стадія 3: Етил 2-[4-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)феніл] циклопропанкарбонова кислота До розчину складного ефіру зі стадії 2 в ТГФН2О (0,2М) додавали LiOH (3екв., 2М) і суміш перемішували при кімнатній температурі протягом 18 годин. Органічний розчинник випарювали, водну фазу підкисляли 1н розчином НСI і кислоту екстрагували ЕtOАс (3Х). Органічний шар промивали насиченим сольовим розчином, сушили і випарювали розчинник з отриманням вказаної в заголовку карбонової кислоти. Стадія 4: 2-(транс)-{3'-[3-[(Морфолін-4ілкарбоніл)-4-оксо-1,8-нафтиридин-1(4Н)]-іл]-1,1’біфеніл-4-іл}циклопропанкарбонова кислота Суміш кислоти зі стадії 2 (1екв.), аміду зі стадії 1 (1екв.), Na2CO3 (3,5екв.; 2М в Н2О), Pd(PPh3)4 (0,15екв.) в н-пропанолі-DMF (1:1, 0,1М) перемішували при 80°С протягом 2 годин. Суміш охолоджували до кімнатної температури, гасили насиченим сольовим розчином, і розбавляли EtOAc. Органічний екстракт промивали насиченим сольовим розчином, сушили над Na2SO4, фільтрували і концентрували. Залишок очищали флеш-хроматографією (СНСl3:ТГФ, 50:50), розтирали в порошок в простому ефірі/ацетоні і потім виділяли фільтруванням з отриманням вказаної в заголовку сполуки у вигляді твердої речовини. 1 H ЯΜΡ (500МГц, CDCI 3): δ 10,5 (с, ΝH), 8,80 (дд, 1H), 8,71 (дд, 1H), 8,37 (с, 1Н), 7,73 (д, 1H), 7,68 (с, 1Н), 7,63 (т, 1H), 7,55 (д, 2Н), 7,45 (м, 2Н), 7,17 (д, 2Н), 3,83 (ушир, с, 6Н), 3,53 (ушир, с, 2Н), 2,59 (м, 1H), 1,93 (м, 1H), 1,65 (м, 1Н), 1,38 (м, 1Н). MC+ESI Q1(M+1) 496,1. Приклад 21 2-{3'-[4-оксо-3-({[5(трифторметил)-1,3,4-тіадіазол-2іл]аміно}карбоніл)-1,8-нафтиридин-1(4Н)]-іл]-1,1’біфеніл-4-іл}циклопропанкарбонова кислота Стадія 1: 1-(3-Бромфеніл)-4-оксо-N-[5(трифторметил)-1,3,4-тіадіазол-2-іл]-1,4-дигідро1,8-нафтиридин-3-карбоксамід 57 До розчину кислоти прикладу отримання нафтиридинону 1, стадія 3 (1екв.) в DMF (0,1М) додавали НАTU (4екв.), діізопропілетиламін (8екв.), а потім 5-(трифторметил)-1,3,4-тіадіазол-2амін (4екв.). Суміш перемішували при кімнатній температурі протягом 12 годин і потім нагрівали до 80°С протягом 2 годин, охолоджували до кімнатної температури і розбавляли водою. Залишок потім виділяли фільтруванням, промивали простим ефіром, розтирали в порошок в ацетоні з отриманням вказаної в заголовку сполуки. Стадія 2: 2-(транс)-{3'-[4-оксо-3-({[5(трифторметил)-1,3,4-тіадіазол-2іл]аміно}карбоніл)-1,8-нафтиридин- 1(4Н)]-іл]-1,1’біфеніл-4-іл} циклопропанкарбонова кислота Отримували відповідно до способу, описаного в прикладі 20, стадії 2, 3 і 4, але використовуючи амід зі стадії 1 як вихідну речовину. Очищали за допомогою Флеш-хроматографії (СНСl3:МеОН, 80:20 з NH3). 1 Н ЯМР (500МГц, ДМСО-d6): δ 13,8 (с, ОН), 9,95 (с, ΝH), 9,10 (с, 1H), 8,83 (м, 2Н), 7,98 (с, 1H), 7,88 (д, 1Н), 7,71 (д, 2Н), 7,69 (м, 2Н), 7,64 (д, 1H), 7,28 (д, 2Н), 2,43 (м, 1H), 1,86 (м, 1H), 1,46 (м, 1Н), 1,38 (м, 1Н). MC+ESI Q1 (M+1) 578,2. Приклад 22 2-{3'-[3-({[2-(Метилтіо)етил]аміно}карбоніл)-4оксо-1,8-нафтиридин-1(4Н)]-іл]-1,1’-біфеніл-4іл}циклопропанкарбонова кислота Стадія 1: 1-(3-Бромфеніл)-N-[2(метилтіо)етил]-4-оксо-1,4-дигідро-1,8нафтиридин-3-карбоксамід Отримували відповідно до способу, описаного в прикладі 21, стадія 1, але використовуючи як вихідну речовину 2-(метилтіо)етанамід. Стадія 2: Етил 2-{3'-[3-({[2(метилтіо)етил]аміно}карбоніл)-4-оксо-1,8нафтиридин-1(4Н)]-іл]-1,1’-біфеніл-4-іл} циклопропанкарбоксилат Суміш аміду зі стадії 1 (1екв.), етил 2-(транс)(4-бромфеніл)циклопропанкарбоксилату з прикладу 1 стадія 1 (1екв.), Na2CO3 (3,5екв.; 2М в Н2О), Pd(PPh3)4 (0,05екв.) в н-пропанолі (0,1М) перемішували при 80°С протягом 3 годин. Суміш охолоджували до кімнатної температури, гасили насиченим сольовим розчином, і розбавляли ЕtOАс. Органічні екстракти промивали насиченим сольовим розчином, сушили над Na2SO4, фільтрували і концентрували. Залишок розтирали 82208 58 в порошок в простому ефірі/МеОН, виділяли фільтруванням і промивали простим ефіром з отриманням вказаної в заголовку сполуки у вигляді твердої речовини. Стадія 3: 2-(транс)-{3'-[3-({[2(Метилтіо)етил]аміно}карбоніл)-4-оксо-1,8нафтиридин-1(4Н)]-іл]-1,1’-біфеніл-4іл}циклопропанкарбонова кислота До розчину складного ефіру зі стадії 2 в ТГФМеОН-Н2О (2:1:0,5, 0,1М) додавали LiOH (5екв., 2М) і суміш перемішували при кімнатній температурі протягом 18 годин. Органічний розчинник випарювали, водну фазу підкисляли 1н розчином НСI і кислоту екстрагували ЕtOАс (3Х). Органічний шар промивали насиченим сольовим розчином, сушили і випарювали розчинник. Залишок розтирали в порошок з простим ефіром/МеОН і потім виділяли фільтруванням з отриманням вказаної в заголовку сполуки у вигляді твердої речовини. 1 Н ЯМР (500МГц, CDCI 3): δ 10,21 (с, ОН), 9,16 (с, ΝH), 8,89 (дд, 1H), 8,76 (дд, 1H), 7,78 (д, 1H), 7,65 (т, 1H), 7,63 (с, 1H), 7,53 (д, 2Н), 7,51 (дд, 1H), 7,43 (д, 1Н), 7,20 (д, 2Н), 3,76 (тд, 2Н), 2,82 (т, 2Н), 2,60 (м, 1H), 2,21 (с, 3Н), 1,96 (м, 1Н), 1,66 (м, 1H), 1,42 (м, 1H). MC+ESI Q1 (M+1) 500,2. Приклад 23 2-{3'-[3-({[2(Метилсульфоніл)етил]аміно}карбоніл)-4-оксо-1,8нафтиридин-1(4Н)]-іл]-1,1’-біфеніл-4іл}циклопропанкарбонова кислота До розчину сполуки прикладу 22 (1екв.) в ТГФМеОН-Н2О (2:1:1, 0,1М) додавали оксон (2екв.). Суміш перемішували при кімнатній температурі протягом 18 годин і розбавляли водою. Залишок виділяли фільтруванням, промивали простим ефіром з отриманням вказаної в заголовку сполуки у вигляді твердої речовини. 1 Н ЯМР (500МГц, ДМСО-d6): δ 12,4 (с, ОН), 9,97 (с, ΝH), 8,83 (с, 1H), 8,78 (дд, 1H), 8,75 (дд, 1H), 7,95 (с, 1H), 7,87 (д, 1Н), 7,66 (д, 2Н), 7,64 (м, 2Н), 7,59 (д, 1H), 7,28 (д, 2Н), 3,82 (тд, 2Н), 3,42 (т, 2Н), 3,05 (с, 3Н), 2,44 (м, 1H), 1,87 (м, 1Н), 1,46 (м, 1Н), 1,40 (с, 1H). MC+ESI Q1 (M+1) 532,1. Отримували вказану в заголовку сполуку 2(транс)-{3'-[3-({[2(метилсульфоніл)етил]аміно}карбоніл)-4-оксо-1,8нафтиридин-1(4Н)]-іл]-1,1’-біфеніл-4іл}циклопропанкарбонова кислота 59 82208 60 оксо-1,8-нафтиридин-1(4Н)-іл]феніл}тієн-2іл)циклопропанкарбонову кислоту. Приклад 26 2-{3'-[3-{[(Циклопропілметіл)аміно]карбоніл}-4оксо-1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4іл}циклопропанкарбонова кислота Приклад 24 2-{3'-[4-оксо-3-{[2,2,2трифторетил)аміно]карбоніл}-1,8-нафтиридин1(4Н)-іл]-1,1’-біфеніл-4-іл}циклопропанкарбонова кислота Отримували відповідно до способу, описаного в прикладі 22, але використовуючи як вихідну речовину 2,2,2-трифторетанамід. 1 Н ЯМР (500МГц, CDCI 3): δ 11,3 (с, ОН), 10,34 (с, ΝH), 9,11 (с, 1H), 8,88 (дд, 1Н), 8,77 (дд, 1H), 7,78 (д, 1Н), 7,68 (т, 1Н), 7,65 (с, 1Н), 7,56 (д, 2Н), 7,52 (дд, 1Н), 7,44 (дд, 1Н), 7,22 (д, 2Н), 4,21 (ушир, квт, 2Н), 2,62 (м, 1Н), 1,97 (м, 1H), 1,70 (м, 1Н), 1,45 (м, 1H). MC+ESI Q1 (M+1) 508,1. Отримували вказану в заголовку сполуку 2(транс)-{3'-[4-оксо-3-{[2,2,2трифторетил)аміно]карбоніл}-1,8-нафтиридин1(4Н)-іл]-1,1’-біфеніл-4-іл}циклопропанкарбонову кислоту. Приклад25 2-(5-{3-[3-[(Циклопропіламіно)карбоніл]-4-оксо1,8-нафтиридин-1(4Н)-іл]феніл}тієн-2іл)циклопропанкарбонова кислота Отримували відповідно до способу, описаного в прикладі 15, але використовуючи як вихідну речовину 5-бромтіофен-2-карбальдегід. 1 Н ЯМР (500МГц, CDCI 3): δ 10,21 (с, ОН), 9,77 (с, ΝH), 9,04 (с, 1Н), 8,79 (дд, 1Н), 8,69 (дд, 1Н), 7,66 (д, 1Н), 7,54 (м, 2Н), 7,45 (дд, 1Н), 7,28 (д, 1H), 7,13 (дд, 1Н), 6,77 (дд, 1H), 2,97 (м, 1H), 2,68 (м, 1Н), 1,93 (м, 1H), 1,65 (м, 1H), 1,36 (м, 1Н), 0,83 (м, 2Н), 0,66 (м, 2Н). МС +ESI Q1 (M+1) 472,2. Отримували вказану в заголовку сполуку 2(транс)-(5-{3-[3-[(циклопропіламіно)карбоніл]-4 Отримували відповідно до способу, описаного в прикладі 22, але використовуючи як вихідну речовину 1-циклопропілметанамін. 1 Н ЯМР (500МГц, ДМСО-d6): δ 9,83 (с, ΝH), 8,82 (с, 1H), 8,79 (дд, 1H), 8,75 (дд, 1H), 7,96 (с, 1H), 7,87 (д, 1Н), 7,65 (м, 3Н), 7,57 (д, 2Н), 7,28 (д, 2Н), 3,38 (т, 2Н), 2,45 (м, 1Н), 1,87 (м, 1H), 1,47 (м, 1H), 1,40 (м, 1Н), 1,08 (м, 1Н), 0,49 (м, 2Н), 0,26 (м, 2Н). MC+ESI Q1 (M+1) 480,1. Отримували вказану в заголовку сполуку 2(транс)-{3'-[3-{[(циклопропілметил)аміно]карбоніл}4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4іл}циклопропанкарбонову кислоту. Приклад 27 2-{3'-[3-{[(1-Ціаноциклопропіл)аміно]карбоніл}4-оксо-1,8-нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4іл}циклопропанкарбонова кислота Отримували відповідно до способу, описаного в прикладі 21, але використовуючи як вихідну речовину 1-аміноциклопропанкарбонітрил. 1 H ЯМР (500МГц, CDCI 3): δ 11,51 (с, ОН), 10,36 (с, ΝH), 9,11 (с, 1Н), 8,84 (дд, 1Н), 8,76 (дд, 1H), 7,78 (д, 1Н), 7,67 (т, 1Н), 7,63 (с, 1Н), 7,57 (д, 2Н), 7,53 (дд, 1Н), 7,41 (д, 1Н), 7,22 (д, 2Н), 2,67 (м, 1Н), 1,98 (м, 1Н), 1,74 (м, 1Н), 1,66 (м, 2Н), 1,45 (м, 1H), 1,40 (м, 2Н). MC+ESI Q1 (M+1) 519,2. Отримували вказану в заголовку сполуку 2(транс)-{3'-[3-{[(1ціаноциклопропіл)аміно]карбоніл}-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-іл} циклопропанкарбонову кислоту. Приклад 28 3-{3'-[3-[(Ізопропіламіно)карбоніл]-4-оксо-1,8нафтиридин-1(4Н)-іл]-1,1’-біфеніл-4-іл}-3метилбутанова кислота
ДивитисяДодаткова інформація
Назва патенту англійською4-oxo-1-(3-substituted phenyl)-1,4-dihydro-1,8-naphthyridine-3-carboxamide phosphodiesterase-4 inhibitors
Автори англійськоюDube, Daniel, Gallant Michel, Lacombe Patrick, Aspiotis Renee, Dube Laurence, Girard Yves, Macdonald Dwight
Назва патенту російською4-оксо-1-(3-замещенные фенил)-1,4 дигидро-1,8-нафтиридин- 3-карбоксамиды как ингибиторы фосфодиэстеразы- 4
Автори російськоюДюб Даниэль, Галлан Мишель, Лякомб Патрик, Аспиотис Рене, Дюб Лоранс, Жирар Ив, Макдональд Дуайт
МПК / Мітки
МПК: A61P 25/00, C07D 471/04
Мітки: інгібітори, фосфодіестерази-4, 4-оксо-1-(3-заміщені, феніл)-1,4-дигідро-1,8-нафтиридин-3-карбоксаміди
Код посилання
<a href="https://ua.patents.su/37-82208-4-okso-1-3-zamishheni-fenil-14-digidro-18-naftiridin-3-karboksamidi-yak-ingibitori-fosfodiesterazi-4.html" target="_blank" rel="follow" title="База патентів України">4-оксо-1-(3-заміщені феніл)-1,4-дигідро-1,8-нафтиридин-3-карбоксаміди як інгібітори фосфодіестерази-4</a>
Попередній патент: Опалювальний газовий апарат
Наступний патент: Спосіб і пристрій для виконання корекції тонкого частотного зсуву після швидкого перетворення фур’є
Випадковий патент: Спосіб одержання альдегідів, які використовують при синтезі сполук, цінних як антифолати












