4-заміщені бензимідазоли та їх застосування як інгібіторів шлункової секреції
Номер патенту: 79843
Опубліковано: 25.07.2007
Автори: Пальмер Андреас, Грундлер Герхард, Брем Крістоф, Кромер Вольфганг, Зімон Вольфганг-Александер, Бур Вільм, Постіус Штефан, Зенн-Більфінгер Йорг, Ціммерманн Петер Ян, К'єза Вітторія
Формула / Реферат
1. Сполука формули І
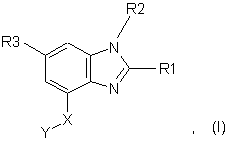
у якій
R1 являє собою водень, С1-4-алкіл, С3-7-циклоалкіл, С3-7-циклоалкіл-С1-4-алкіл, С1-4-алкокси, С1-4-алкоксі-С1-4-алкіл, С1-4-алкоксикарбоніл, С2-4-алкеніл, С2-4-алкініл, фтор-С1-4-алкіл, гідроксі-С1-4-алкіл, моно- або ді-С1-4-алкіламіно або С1-4-алкіл карбонілоксі-С1-4-алкіл,
R2 являє собою водень, С1-4-алкіл, арил, С3-7-циклоалкіл, С3-7-циклоалкіл-С1-4-алкіл, С1-4-алкоксикарбоніл, моно- або ді-С1-4-алкіламіно С1-4-алкілкарбоніл, гідроксі-С1-4-алкіл, фтор-С2-4-алкіл, арил-С1-4-алкоксі-С1-4-алкіл, гідрокси або С1-4-алкокси,
R3 являє собою водень, галоген, фтор-С1-4-алкіл, карбоксил, -СО-С1-4-алкокси, гідроксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкіл, фтор-С1-4-алкоксі-С1-4-алкіл, ціано, групу -CO-NR31R32, групу SO2-NR31R32 або групу Het,
де R31 являє собою водень, гідроксил, С1-7-алкіл, гідроксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкіл або С3-7-циклоалкіл, аміно й
R32 являє собою водень, С1-7-алкіл, гідроксі-С1-4-алкіл або С1-4-алкоксі-С1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обидва зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино, морфоліно, азиридино або азетидиногрупу й Het являє собою гетероциклічний залишок, заміщений R33, R34 й R35, вибраний із групи, яка складається з оксадіазолу, дигідрооксазолу, дигідроімідазолу, оксазолу, імідазолу, ізоксазолу, дигідроізоксазолу, піразолу й тетразолу,
де
R33 являє собою водень, С1-4-алкіл, гідроксі-С1-4-алкіл, С1-4-алкокси, С2-4-алкенілокси, С1-4-алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбоксі-С1-4-алкіл, С1-4-алкоксикарбоніл-С1-4-алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С1-4-алкоксі-С1-4-алкоксикарбоніламіно або сульфоніл,
R34 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси,
R35 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси,
X являє собою О (кисень) або NH й
Y має значення -СН2-Аr, де
Аr являє собою моно- або біциклічний ароматичний залишок, заміщений R4, R5, R6 й R7, який вибраний із групи, яка складається з фенілу, нафтилу, піролілу, піразолілу, імідазолілу, 1,2,3-триазолілу, індолілу, бензимідазолілу, фурилу, бензофурилу, тієнілу, бензотієнілу, тіазолілу, ізоксазолілу, піридинілу, піримідинілу, хінолінілу й ізохінолінілу,
або Y означає групу gp
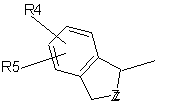 , (gp)
, (gp)
де
Z має значення -CHR8- або -CHR8-CHR9-,
де в Аr й/або в групі gp
R4 являє собою водень, С1-4-алкіл, гідроксі-С1-4-алкіл, С1-4-алкокси, С2-4-алкенілокси, С1-4-алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбоксі-С1-4-алкіл, С1-4-алкоксикарбоніл-С1-4-алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С1-4-алкоксі-С1-4-алкоксикарбоніламіно або сульфоніл,
R5 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси,
R6 являє собою водень, С1-4-алкіл або галоген й
R7 являє собою водень, С1-4-алкіл або галоген,
R8 являє собою водень, С1-7-алкіл, С2-7-алкеніл, гідроксил, С1-4-алкокси, оксозаміщений С1-4-алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С1-4-алкокси, гідроксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкокси, С3-7-циклоалкоксі-С1-4-алкокси, С3-7-циклоалкіл-С1-4-алкоксі-С1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, моно- або ді-С1-4-алкіламіно- С1-4-алкілкарбонілокси, С1-4-алкоксі-С1-4-алкоксикарбоніламіно або С1-4-алкоксі-С1-4-алкілкарбонілокси,
R9 являє собою водень, С1-7-алкіл, С2-7-алкеніл, гідроксил, С1-4-алкокси, оксозаміщений С1-4-алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С1-4-алкокси, гідроксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкокси, С3-7-циклоалкоксі-С1-4-алкокси, С3-7-циклоалкіл-С1-4-алкоксі-С1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, моно- або ді-С1-4-алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкоксі-С1-4-алкоксикарбоніламіно або С1-4-алкоксі-С1-4-алкілкарбонілокси, і де арил являє собою феніл або феніл, заміщений одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, галогену, трифторметилу, нітро, трифторметокси, гідрокси й ціано, за умови, що R3 не являє собою водень або галоген, коли Y означає -СН2-Аr й R2 означає водень, С1-4-алкіл або С3-7-циклоалкіл-С1-4-алкіл, або її сіль.
2. Сполука за п. 1, у якій R1 являє собою водень, С1-4-алкіл, С3-7-циклоалкіл, С3-7-циклоалкіл-С1-4-алкіл, С1-4-алкокси, С1-4-алкоксі-С1-4-алкіл, С1-4-алкоксикарбоніл, С2-4-алкеніл, С2-4-алкініл, фтор-С1-4-алкіл або гідроксі-С1-4-алкіл,
R2 являє собою водень, С1-4-алкіл, арил, С3-7-циклоалкіл, С3-7-циклоалкіл-С1-4-алкіл, С1-4-алкоксикарбоніл, моно- або ді-С1-4-алкіламіно-С1-4-алкілкарбоніл, гідроксі-С1-4-алкіл або фтор-С2-4-алкіл,
R3 являє собою водень, галоген, фтор-С1-4-алкіл, карбоксил, -СО-С1-4-алкокси, гідроксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкіл, фтор-С1-4-алкоксі-С1-4-алкіл або групу -CO-NR31R32, де
R31 являє собою водень, гідроксил, С1-7-алкіл, гідроксі-С1-4-алкіл або С1-4-алкоксі-С1-4-алкіл,
R32 являє собою водень, С1-7-алкіл, гідроксі-С1-4-алкіл або С1-4-алкоксі-С1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обидва зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино або морфоліногрупу,
X являє собою О (кисень) або NH й
Y має значення -СН2-Аr, де
Аr являє собою моно- або біциклічний ароматичний залишок, заміщений R4, R5, R6 й R7, який вибраний із групи, яка складається з фенілу, нафтилу, піролілу, піразолілу, імідазолілу, 1,2,3-триазолілу, індолілу, бензимідазолілу, фурилу, бензофурилу, тієнілу, бензотієнілу, тіазолілу, ізоксазолілу, піридинілу, піримідинілу, хінолінілу й ізохінолінілу, або Y означає групу gp
 , (gp)
, (gp)
де
Z має значення -CHR8- або -CHR8-CHR9-,
де в Аr й/або в групі gp
R4 являє собою водень, С1-4-алкіл, гідроксі-С1-4-алкіл, С1-4-алкокси, С2-4-алкенілокси, С1-4-алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбоксі-С1-4-алкіл, С1-4-алкоксикарбоніл-С1-4-алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С1-4-алкоксі-С1-4-алкоксикарбоніламіно або сульфоніл,
R5 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси,
R6 являє собою водень, С1-4-алкіл або галоген й
R7 являє собою водень, С1-4-алкіл або галоген,
R8 являє собою водень, С1-7-алкіл, С2-7-алкеніл, гідроксил, С1-4-алкокси, оксозаміщений С1-4-алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С1-4-алкокси, гідроксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкокси, С3-7-циклоалкоксі-С1-4-алкокси, С3-7-циклоалкіл-С1-4-алкоксі-С1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ди-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, моно- або ді-С1-4-алкіламіно-С1-4-алкілкарбонілокси або С1-4-алкоксі-С1-4-алкоксикарбоніламіно,
R9 являє собою водень, С1-7-алкіл, С2-7-алкеніл, гідроксил, С1-4-алкокси, оксозаміщений С1-4-алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С1-4-алкокси, гідроксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкокси, С3-7-циклоалкоксі-С1-4-алкокси, С3-7-циклоалкіл-С1-4-алкоксі-С1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, моно- або ді-С1-4-алкіламіно-С1-4-алкілкарбонілокси або С1-4-алкоксі-С1-4-алкоксикарбоніламіно,
і де арил являє собою феніл або феніл, заміщений одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, галогену, трифторметилу, нітро, трифторметокси, гідрокси й ціано,
за умови, що R3 не являє собою водень або галоген, коли Y означає -СН2-Аr, або її сіль.
3. Сполука за п. 1 формули Іа
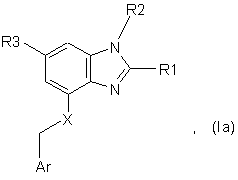
у якій
R1 являє собою водень, С1-4-алкіл, С3-7-циклоалкіл, С3-7-циклоалкіл-С1-4-алкіл, С1-4-алкокси, С1-4-алкоксі-С1-4-алкіл, С1-4-алкоксикарбоніл, С2-4-алкеніл, С2-4-алкініл, фтор-С1-4-алкіл, гідроксі-С1-4-алкіл, моно- або ді-С1-4-алкіламіно або С1-4-алкілкарбонілоксі-С1-4-алкіл,
R2 являє собою водень, С1-4-алкіл, арил, С3-7-циклоалкіл, С3-7-циклоалкіл-С1-4-алкіл, С1-4-алкоксикарбоніл, моно- або ді-С1-4алкіламіно-С1-4-алкілкарбоніл, гідроксі-С1-4-алкіл, фтор-С2-4-алкіл, арил-С1-4-алкоксі-С1-4-алкіл, гідрокси або С1-4-алкокси,
R3 являє собою водень, галоген, фтор-С1-4-алкіл, карбоксил, -СО-С1-4-алкокси, гідроксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкіл, фтор-С1-4-алкоксі-С1-4-алкіл, ціано, групу -CO-NR31R32, групу SO2-NR31R32 або групу Het, де
R31 являє собою водень, гідроксил, С1-7-алкіл, гідроксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкіл або С3-7-циклоалкіл, аміно й
R32 являє собою водень, С1-7-алкіл, гідроксі-С1-4-алкіл або С1-4-алкоксі-С1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обидва зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино, морфоліно, азиридино або азетидиногрупу й Het являє собою гетероциклічний залишок, заміщений R33, R34 й R35, вибраний із групи, яка складається з оксадіазолу, дигідрооксазолу, дигідроімідазолу, оксазолу, імідазолу, ізоксазолу, дигідроізоксазолу, піразолу й тетразолу, де R33 являє собою водень, С1-4-алкіл, гідроксі-С1-4-алкіл, С1-4-алкокси, С2-4-алкенілокси, С1-4-алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбоксі-С1-4-алкіл, С1-4-алкоксикарбоніл-С1-4-алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С1-4-алкоксі-С1-4-алкоксикарбоніламіно або сульфоніл, R34 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси,
R35 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси,
X являє собою О (кисень) або NH й
Аr являє собою моно- або біциклічний ароматичний залишок, заміщений R4, R5, R6 й R7, який вибраний із групи, яка складається з фенілу, нафтилу, піролілу, піразолілу, імідазолілу, 1,2,3-триазолілу, індолілу, бензимідазолілу, фурилу, бензофурилу, тієнілу, бензотієнілу, тіазолілу, ізоксазолілу, піридинілу, піримідинілу, хінолінілу й ізохінолінілу,
де
R4 являє собою водень, С1-4-алкіл, гідроксі-С1-4-алкіл, С1-4-алкокси, С2-4-алкенілокси, С1-4-алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбоксі-С1-4-алкіл, С1-4-алкоксикарбоніл-С1-4-алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С1-4-алкоксі-С1-4-алкоксикарбоніламіно або сульфоніл,
R5 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси,
R6 являє собою водень, С1-4-алкіл або галоген й
R7 являє собою водень, С1-4-алкіл або галоген,
і де арил являє собою феніл або феніл, заміщений одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, галогену, трифторметилу, нітро, трифторметокси, гідрокси й ціано, за умови, що R3 не являє собою водень або галоген, коли Y означає -СН2-Аr й R2 означає водень, С1-4-алкіл або С3-7-циклоалкіл-С1-4-алкіл, або її сіль.
4. Сполука за п. 1 формули Іb
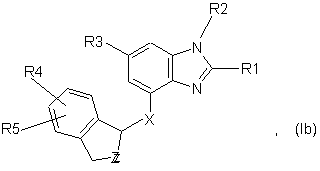
у якій
R1 являє собою водень, С1-4-алкіл, С3-7-циклоалкіл, С3-7-циклоалкіл-С1-4-алкіл, С1-4-алкокси, С1-4-алкоксі-С1-4-алкіл, С1-4-алкоксикарбоніл, С2-4-алкеніл, С2-4-алкініл, фтор-С1-4-алкіл, гідроксі-С1-4-алкіл, моно- або ді-С1-4-алкіламіно або С1-4-алкілкарбонілоксі-С1-4-алкіл,
R2 являє собою водень, С1-4-алкіл, арил, С3-7-циклоалкіл, С3-7-циклоалкіл-С1-4-алкіл, С1-4-алкоксикарбоніл, моно- або ді-С1-4-алкіламіно-С1-4-алкілкарбоніл, гідроксі-С1-4-алкіл, фтор-С2-4-алкіл, арил-С1-4-алкоксі-С1-4-алкіл, гідрокси або С1-4-алкокси,
R3 являє собою водень, галоген, фтор-С1-4-алкіл, карбоксил, -СО-С1-4-алкокси, гідроксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкіл, фтор-С1-4-алкоксі-С1-4-алкіл, ціано, групу -CO-NR31R32, групу SO2-NR31R32 або групу Het, де
R31 являє собою водень, гідроксил, С1-7-алкіл, гідроксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкіл або С3-7-циклоалкіл, аміно й
R32 являє собою водень, С1-7-алкіл, гідроксі-С1-4-алкіл або С1-4-алкоксі-С1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обидва зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино, морфоліно, азиридино або азетидиногрупу й Het являє собою гетероциклічний залишок, заміщений R33, R34 й R35,
вибраний із групи, яка складається з оксадіазолу, дигідрооксазолу, дигідроімідазолу, оксазолу, імідазолу, ізоксазолу, дигідроізоксазолу, піразолу й тетразолу,
де
R33 являє собою водень, С1-4-алкіл, гідроксі-С1-4-алкіл, С1-4-алкокси, С2-4- алкенілокси, С1-4-алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбоксі-С1-4-алкіл, С1-4-алкоксикарбоніл-С1-4-алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С1-4-алкоксі-С1-4-алкоксикарбоніламіно або сульфоніл,
R34 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси,
R35 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси,
R4 являє собою водень, С1-4-алкіл, гідроксі-С1-4-алкіл, С1-4-алкокси, С2-4-алкенілокси, С1-4-алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбоксі-С1-4-алкіл, С1-4-алкоксикарбоніл-С1-4-алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С1-4-алкоксі-С1-4-алкоксикарбоніламіно або сульфоніл,
R5 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси,
X являє собою О (кисень) або NH й
Z має значення -CHR8- або -CHR8-CHR9-,
де
R8 являє собою водень, С1-7-алкіл, С2-7-алкеніл, гідроксил, С1-4-алкокси, оксозаміщений С1-4-алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С1-4-алкокси, гідроксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкокси, С3-7-циклоалкоксі-С1-4-алкокси, С3-7-циклоалкіл-С1-4-алкоксі-С1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, моно- або ді-С1-4-алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкоксі-С1-4-алкоксикарбоніламіно або С1-4-алкоксі-С1-4-алкілкарбонілокси,
R9 являє собою водень, С1-7-алкіл, С2-7-алкеніл, гідроксил, С1-4-алкокси, оксозаміщений С1-4-алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С1-4-алкокси, гідроксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкокси, С3-7-циклоалкоксі-С1-4-алкокси, С3-7-циклоалкіл-С1-4-алкоксі-С1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, моно- або ді-С1-4-алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкоксі-С1-4-алкоксикарбоніламіно або С1-4-алкоксі-С1-4-алкілкарбонілокси,
і де арил являє собою феніл або феніл, заміщений одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, галогену, трифторметилу, нітро, трифторметокси, гідрокси й ціано, або її сіль.
5. Сполука формули Іа-1 за п. 3 формули Іа
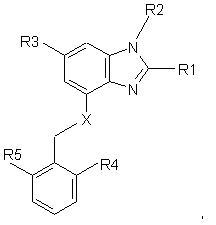 (Іа-1)
(Іа-1)
де
R1 являє собою водень, С1-4-алкіл, С3-7-циклоалкіл, гідроксі-С1-4-алкіл або С1-4-алкоксі-С1-4-алкіл,
R2 являє собою водень, С1-4-алкіл, гідрокси, С1-4-алкокси або арил-С1-4-алкоксі-С1-4-алкіл, R3 являє собою карбоксил, -СО-С1-4-алкокси, гідроксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкіл, ціано, групу -CO-NR31R32, групу SO2-NR31R32 або групу Het,
де
R31 являє собою водень, С1-7-алкіл, гідроксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкіл, С3-7-циклоалкіл або аміно й
R32 являє собою водень або С1-7-алкіл, або де
R31 й R32 разом, включаючи атом азоту, з яким вони обидва зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино, морфоліно, азиридино або азетидиногрупу й Het являє собою гетероциклічний залишок, заміщений R33, R34 й R35, вибраний із групи, яка складається з оксадіазолу, дигідрооксазолу й дигідроімідазолу,
де
R33 являє собою водень або С1-4-алкіл,
R34 являє собою водень або С1-4-алкіл,
R35 являє собою водень або С1-4-алкіл,
R4 являє собою водень, С1-4-алкіл, гідроксі-С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, трифторметил, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно або С1-4-алкоксі-С1-4-алкоксикарбоніламіно,
R5 являє собою водень, С1-4-алкіл або С1-4-алкокси й X являє собою О (кисень) або NH, або її сіль.
6. Сполука формули Іb-1 за п. 4 формули Іb
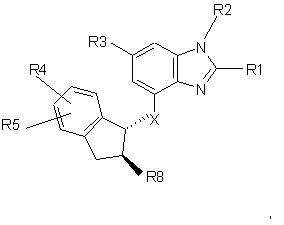 (Іb-1)
(Іb-1)
у якій
R1 являє собою С1-4-алкіл або С3-7-циклоалкіл,
R2 являє собою водень або С1-4-алкіл,
R3 являє собою карбоксил, -СО-С1-4-алкокси, С1-4-алкоксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкіл або групу -CO-NR31R32,
де
R31 являє собою водень, С1-7-алкіл, гідроксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкіл або С3-7-циклоалкіл й
R32 являє собою водень, С1-7-алкіл, гідроксі-С1-4-алкіл або С1-4-алкоксі-С1-4-алкіл,
або де
R31 й R32 разом, включаючи атом азоту, з яким вони обидва зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино, морфоліно, азиридино або азетидиногрупу,
R4 являє собою водень, С1-4-алкіл, С1-4алкокси або галоген,
R5 являє собою водень або С1-4-алкіл,
R8 являє собою гідроксил, С1-4-алкокси, оксозаміщений С1-4-алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С1-4-алкокси, гідроксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкокси, С3-7-циклоалкоксі-С1-4-алкокси, С3-7-циклоалкіл-С1-4-алкоксі-С1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, моно- або ді-С1-4-алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкоксі-С1-4-алкоксикарбоніламіно або С1-4-алкоксі- С1-4-алкілкарбонілокси,
X являє собою О (кисень) або NH,
або її сіль.
7. Сполука формули Іb-1 за п. 6, у якій
R1 являє собою С1-4-алкіл,
R2 являє собою водень або С1-4-алкіл,
R3 являє собою карбоксил, -СО-С1-4-алкокси, С1-4-алкоксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкіл або групу -CO-NR31R32,
де
R31 являє собою водень, С1-7-алкіл, гідроксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкіл або С3-7-циклоалкіл й
R32 являє собою водень, С1-7-алкіл, гідроксі-С1-4-алкіл або С1-4-алкоксі-С1-4-алкіл,
або де
R31 й R32 разом, включаючи атом азоту, з яким вони обидва зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино, морфоліно, азиридино або азетидиногрупу,
R4 являє собою водень, С1-4-алкіл, С1-4-алкокси або галоген,
R5 являє собою водень,
R8 являє собою гідроксил, С1-4-алкокси, оксозаміщений С1-4-алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С1-4-алкокси, гідроксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкокси, С1-4-алкоксі-С1-4-алкоксі-С1-4-алкокси, С3-7-циклоалкоксі-С1-4-алкокси, С3-7-циклоалкіл-С1-4-алкоксі-С1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С1-4-алкоксі, аміно, моно- або ді-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, моно- або ді-С1-4-алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкоксі-С1-4-алкоксикарбоніламіно або С1-4-алкоксі-С1-4-алкілкарбонілокси,
X являє собою О (кисень) або NH, або її сіль.
8. Сполука формули Іа-1 за п. 5, у якій
R1 являє собою С1-4-алкіл,
R2 являє собою С1-4-алкіл,
R3 являє собою карбоксил, -СО-С1-4-алкокси, С1-4-алкоксі-С1-4-алкіл або групу -CO-NR31R32, де
R31 являє собою водень, С1-4-алкіл, гідроксі-С1-4-алкіл, С1-4-алкоксі-С1-4-алкіл або С3-7-циклоалкіл й
R32 являє собою водень або С1-4-алкіл,
R4 являє собою С1-4-алкіл або С1-4-алкілкарбоніламіно,
R5 являє собою С1-4-алкіл,
X являє собою О (кисень) або NH,
або її сіль.
9. Сполука 6-(N,N-диметиламінокарбоніл)-4-(2-етил-6-метил-бензиламіно)-1,2-диметил-1Н-бензимідазол або її сіль.
10. Сполука 6-(N,N-диметиламінокарбоніл)-4-(2,6-диметил-бензиламіно)-1,2-диметил-1H-бензимідазол або її сіль.
11. Лікарський засіб, який містить сполуку за п. 1 й/або її фармакологічно прийнятну сіль разом зі звичайними фармацевтичними добавками й/або ексципієнтами.
12. Застосування сполуки за п. 1 і її фармакологічно прийнятних солей для профілактики й лікування шлунково-кишкових захворювань.
Текст
1. Сполука формули І 2 (19) 1 3 79843 Аr являє собою моно- або біциклічний ароматичний залишок, заміщений R4, R5, R6 й R7, який вибраний із групи, яка складається з фенілу, нафтилу, піролілу, піразолілу, імідазолілу, 1,2,3триазолілу, індолілу, бензимідазолілу, фурилу, бензофурилу, тієнілу, бензотієнілу, тіазолілу, ізоксазолілу, піридинілу, піримідинілу, хінолінілу й ізохінолінілу, або Y означає групу gp R4 R5 (gp) Z z , де Z має значення -CHR8- або -CHR8-CHR9-, де в Аr й/або в групі gp R4 являє собою водень, С1-4-алкіл, гідроксі-С 1-4алкіл, С1-4-алкокси, С2-4-алкенілокси, С1-4алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбоксі-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4-алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С 1-4-алкокси, трифторметил, нітро, аміно, моноабо ді-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-алкоксі-С 1-4-алкоксикарбоніламіно або сульфоніл, R5 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, R6 являє собою водень, С1-4-алкіл або галоген й R7 являє собою водень, С1-4-алкіл або галоген, R8 являє собою водень, С1-7-алкіл, С2-7-алкеніл, гідроксил, С1-4-алкокси, оксозаміщений С 1-4алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С 1-4алкокси, гідроксі-С 1-4-алкокси, С1-4-алкоксі-С1-4алкокси, С1-4-алкоксі-С 1-4-алкоксі-С 1-4-алкокси, С3-7циклоалкоксі-С 1-4-алкокси, С3-7-циклоалкіл-С 1-4алкоксі-С 1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ді-С1-4алкіламіно, С1-4-алкілкарбоніламіно, С1-4алкоксикарбоніламіно, моноабо ді-С 1-4алкіламіно- С1-4-алкілкарбонілокси, С1-4-алкоксі-С 1або С 1-4-алкоксі-С1-44-алкоксикарбоніламіно алкілкарбонілокси, R9 являє собою водень, С1-7-алкіл, С2-7-алкеніл, гідроксил, С1-4-алкокси, оксозаміщений С 1-4алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С 1-4алкокси, гідроксі-С 1-4-алкокси, С1-4-алкоксі-С1-4алкокси, С1-4-алкоксі-С 1-4-алкоксі-С 1-4-алкокси, С3-7циклоалкоксі-С 1-4-алкокси, С3-7-циклоалкіл-С 1-4алкоксі-С 1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ді-С1-4алкіламіно, С1-4-алкілкарбоніламіно, С1-4алкоксикарбоніламіно, моноабо ді-С 1-4алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкоксі-С 1або С 1-4-алкоксі-С1-44-алкоксикарбоніламіно алкілкарбонілокси, і де арил являє собою феніл або феніл, заміщений одним, двома або трьома однаковими або різними замісниками із групи С 1-4алкілу, С1-4-алкокси, карбокси, С1-4алкоксикарбонілу, галогену, три фторметилу, нітро, трифторметокси, гідрокси й ціано, за умови, що R3 не являє собою водень або галоген, коли Y озна 4 чає -СН2-Аr й R2 означає водень, С1-4-алкіл або С37-циклоалкіл-С 1-4-алкіл, або її сіль. 2. Сполука за п. 1, у якій R1 являє собою водень, С1-4-алкіл, С3-7-циклоалкіл, С3-7-циклоалкіл-С 1-4алкіл, С1-4-алкокси, С1-4-алкоксі-С 1-4-алкіл, С1-4алкоксикарбоніл, С2-4-алкеніл, С2-4-алкініл, фторС1-4-алкіл або гідроксі-С 1-4-алкіл, R2 являє собою водень, С1-4-алкіл, арил, С3-7циклоалкіл, С3-7-циклоалкіл-С 1-4-алкіл, С1-4алкоксикарбоніл, моно- або ді-С 1-4-алкіламіно-С 1-4алкілкарбоніл, гідроксі-С 1-4-алкіл або фтор-С2-4алкіл, R3 являє собою водень, галоген, фтор-С1-4-алкіл, карбоксил, -СО-С1-4-алкокси, гідроксі-С 1-4-алкіл, С1С1-4-алкоксі-С 1-4-алкоксі-С1-44-алкоксі-С 1-4-алкіл, алкіл, фтор-С1-4-алкоксі-С 1-4-алкіл або групу -CONR31R32, де R31 являє собою водень, гідроксил, С1-7-алкіл, гідроксі-С 1-4-алкіл або С1-4-алкоксі-С 1-4-алкіл, R32 являє собою водень, С1-7-алкіл, гідроксі-С 1-4алкіл або С1-4-алкоксі-С1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обидва зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино або морфоліногруп у, X являє собою О (кисень) або NH й Y має значення -СН2-Аr, де Аr являє собою моно- або біциклічний ароматичний залишок, заміщений R4, R5, R6 й R7, який вибраний із групи, яка складається з фенілу, нафтилу, піролілу, піразолілу, імідазолілу, 1,2,3триазолілу, індолілу, бензимідазолілу, фурилу, бензофурилу, тієнілу, бензотієнілу, тіазолілу, ізоксазолілу, піридинілу, піримідинілу, хінолінілу й ізохінолінілу, або Y означає груп у gp R4 (gp) R5 z Z , де Z має значення -CHR8- або -CHR8-CHR9-, де в Аr й/або в групі gp R4 являє собою водень, С1-4-алкіл, гідроксі-С 1-4алкіл, С1-4-алкокси, С2-4-алкенілокси, С1-4алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбоксі-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4-алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С 1-4-алкокси, трифторметил, нітро, аміно, моноабо ді-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-алкоксі-С 1-4-алкоксикарбоніламіно або сульфоніл, R5 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, R6 являє собою водень, С1-4-алкіл або галоген й R7 являє собою водень, С1-4-алкіл або галоген, R8 являє собою водень, С1-7-алкіл, С2-7-алкеніл, гідроксил, С1-4-алкокси, оксозаміщений С 1-4алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С 1-4алкокси, гідроксі-С 1-4-алкокси, С1-4-алкоксі-С1-4алкокси, С1-4-алкоксі-С 1-4-алкоксі-С 1-4-алкокси, С3-7циклоалкоксі-С 1-4-алкокси, С3-7-циклоалкіл-С 1-4алкоксі-С 1-4-алкокси, С1-4-алкілкарбонілокси, гало 5 79843 ген-С1-4-алкокси, аміно, моно- або ди-С1-4алкіламіно, С1-4-алкілкарбоніламіно, С1-4алкоксикарбоніламіно, моноабо ді-С 1-4алкіламіно-С1-4-алкілкарбонілокси або С 1-4-алкоксіС1-4-алкоксикарбоніламіно, R9 являє собою водень, С1-7-алкіл, С2-7-алкеніл, гідроксил, С1-4-алкокси, оксозаміщений С 1-4алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С 1-4алкокси, гідроксі-С 1-4-алкокси, С1-4-алкоксі-С1-4алкокси, С1-4-алкоксі-С 1-4-алкоксі-С 1-4-алкокси, С3-7циклоалкоксі-С 1-4-алкокси, С3-7-циклоалкіл-С 1-4алкоксі-С 1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ді-С1-4алкіламіно, С1-4-алкілкарбоніламіно, С1-4алкоксикарбоніламіно, моноабо ді-С 1-4алкіламіно-С1-4-алкілкарбонілокси або С 1-4-алкоксіС1-4-алкоксикарбоніламіно, і де арил являє собою феніл або феніл, заміщений одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, галогену, трифторметилу, нітро, трифторметокси, гідрокси й ціано, за умови, що R3 не являє собою водень або галоген, коли Y означає -СН2-Аr, або її сіль. 3. Сполука за п. 1 формули Іа R2 R3 N R1 N X , (Ia) Ar у якій R1 являє собою водень, С1-4-алкіл, С3-7циклоалкіл, С3-7-циклоалкіл-С 1-4-алкіл, С1-4алкокси, С1-4-алкоксі-С 1-4-алкіл, С1-4алкоксикарбоніл, С2-4-алкеніл, С2-4-алкініл, фторС1-4-алкіл, гідроксі-С 1-4-алкіл, моно- або ді-С 1-4алкіламіно або С1-4-алкілкарбонілоксі-С1-4-алкіл, R2 являє собою водень, С1-4-алкіл, арил, С3-7циклоалкіл, С3-7-циклоалкіл-С 1-4-алкіл, С1-4алкоксикарбоніл, моно- або ді-С1-4алкіламіно-С 1-4алкілкарбоніл, гідроксі-С 1-4-алкіл, фтор-С2-4-алкіл, арил-С 1-4-алкоксі-С 1-4-алкіл, гідрокси або С 1-4алкокси, R3 являє собою водень, галоген, фтор-С1-4-алкіл, карбоксил, -СО-С1-4-алкокси, гідроксі-С 1-4-алкіл, С1С1-4-алкоксі-С 1-4-алкоксі-С1-44-алкоксі-С 1-4-алкіл, алкіл, фтор-С1-4-алкоксі-С 1-4-алкіл, ціано, групу CO-NR31R32, групу SO2-NR31R32 або групу Het, де R31 являє собою водень, гідроксил, С1-7-алкіл, гідроксі-С 1-4-алкіл, С1-4-алкоксі-С 1-4-алкіл або С3-7циклоалкіл, аміно й R32 являє собою водень, С1-7-алкіл, гідроксі-С1-4алкіл або С1-4-алкоксі-С 1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обидва зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино, морфоліно, азиридино або азетидиногрупу й Het являє собою гетероциклічний залишок, заміщений R33, R34 й R35, вибраний із групи, яка складається з оксадіазолу, дигідрооксазолу, дигідроімідазолу, оксазолу, імідазолу, ізоксазолу, дигідроізоксазолу, піразолу й 6 тетразолу, де R33 являє собою водень, С1-4-алкіл, гідроксі-С 1-4-алкіл, С1-4-алкокси, С2-4-алкенілокси, С1-4-алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбоксі-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4-алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С 1-4-алкокси, трифторметил, нітро, аміно, моноабо ді-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-алкоксі-С 1-4-алкоксикарбоніламіно або сульфоніл, R34 являє собою водень, С1-4-алкіл, С1-4алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, R35 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, X являє собою О (кисень) або NH й Аr являє собою моно- або біциклічний ароматичний залишок, заміщений R4, R5, R6 й R7, який вибраний із групи, яка складається з фенілу, нафтилу, піролілу, піразолілу, імідазолілу, 1,2,3триазолілу, індолілу, бензимідазолілу, фурилу, бензофурилу, тієнілу, бензотієнілу, тіазолілу, ізоксазолілу, піридинілу, піримідинілу, хінолінілу й ізохінолінілу, де R4 являє собою водень, С1-4-алкіл, гідроксі-С 1-4алкіл, С1-4-алкокси, С2-4-алкенілокси, С1-4алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбоксі-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4-алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С 1-4-алкокси, трифторметил, нітро, аміно, моноабо ді-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-алкоксі-С 1-4-алкоксикарбоніламіно або сульфоніл, R5 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, R6 являє собою водень, С1-4-алкіл або галоген й R7 являє собою водень, С1-4-алкіл або галоген, і де арил являє собою феніл або феніл, заміщений одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, галогену, трифторметилу, нітро, трифторметокси, гідрокси й ціано, за умови, що R3 не являє собою водень або галоген, коли Y означає -СН2-Аr й R2 означає водень, С1-4-алкіл або С 3-7-циклоалкіл-С 1-4-алкіл, або її сіль. 4. Сполука за п. 1 формули Іb R2 R3 N R1 R4 N X R5 , (Ib) Z z у якій R1 являє собою водень, С1-4-алкіл, С3-7циклоалкіл, С3-7-циклоалкіл-С 1-4-алкіл, С1-4алкокси, С1-4-алкоксі-С 1-4-алкіл, С1-4алкоксикарбоніл, С2-4-алкеніл, С2-4-алкініл, фторС1-4-алкіл, гідроксі-С 1-4-алкіл, моно- або ді-С 1-4алкіламіно або С1-4-алкілкарбонілоксі-С1-4-алкіл, 7 79843 R2 являє собою водень, С1-4-алкіл, арил, С3-7циклоалкіл, С3-7-циклоалкіл-С 1-4-алкіл, С1-4алкоксикарбоніл, моно- або ді-С 1-4-алкіламіно-С 1-4алкілкарбоніл, гідроксі-С 1-4-алкіл, фтор-С2-4-алкіл, арил-С 1-4-алкоксі-С 1-4-алкіл, гідрокси або С 1-4алкокси, R3 являє собою водень, галоген, фтор-С1-4-алкіл, карбоксил, -СО-С1-4-алкокси, гідроксі-С 1-4-алкіл, С1С1-4-алкоксі-С 1-4-алкоксі-С1-44-алкоксі-С 1-4-алкіл, алкіл, фтор-С1-4-алкоксі-С 1-4-алкіл, ціано, групу CO-NR31R32, групу SO2-NR31R32 або групу Het, де R31 являє собою водень, гідроксил, С1-7-алкіл, гідроксі-С 1-4-алкіл, С1-4-алкоксі-С 1-4-алкіл або С3-7циклоалкіл, аміно й R32 являє собою водень, С1-7-алкіл, гідроксі-С1-4алкіл або С1-4-алкоксі-С 1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обидва зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино, морфоліно, азиридино або азетидиногрупу й Het являє собою гетероциклічний залишок, заміщений R33, R34 й R35, вибраний із групи, яка складається з оксадіазолу, дигідрооксазолу, дигідроімідазолу, оксазолу, імідазолу, ізоксазолу, дигідроізоксазолу, піразолу й тетразолу, де R33 являє собою водень, С1-4-алкіл, гідроксі-С1-4алкіл, С1-4-алкокси, С2-4- алкенілокси, С1-4алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбоксі-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4-алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С 1-4-алкокси, трифторметил, нітро, аміно, моноабо ді-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-алкоксі-С 1-4-алкоксикарбоніламіно або сульфоніл, R34 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, R35 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, R4 являє собою водень, С1-4-алкіл, гідроксі-С 1-4алкіл, С1-4-алкокси, С2-4-алкенілокси, С1-4алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбоксі-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4-алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С 1-4-алкокси, трифторметил, нітро, аміно, моноабо ді-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-алкоксі-С 1-4-алкоксикарбоніламіно або сульфоніл, R5 являє собою водень, С1-4-алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, X являє собою О (кисень) або NH й Z має значення -CHR8- або -CHR8-CHR9-, де R8 являє собою водень, С1-7-алкіл, С2-7-алкеніл, гідроксил, С1-4-алкокси, оксозаміщений С 1-4алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С 1-4алкокси, гідроксі-С 1-4-алкокси, С1-4-алкоксі-С1-4алкокси, С1-4-алкоксі-С 1-4-алкоксі-С 1-4-алкокси, С3-7 8 циклоалкоксі-С 1-4-алкокси, С3-7-циклоалкіл-С 1-4алкоксі-С 1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С 1-4-алкокси, аміно, моно- або ді-С1-4алкіламіно, С1-4-алкілкарбоніламіно, С1-4алкоксикарбоніламіно, моноабо ді-С 1-4алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкоксі-С 1або С 1-4-алкоксі-С1-44-алкоксикарбоніламіно алкілкарбонілокси, R9 являє собою водень, С1-7-алкіл, С2-7-алкеніл, гідроксил, С1-4-алкокси, оксозаміщений С 1-4алкокси, С3-7-циклоалкокси, С3-7-циклоалкіл-С 1-4алкокси, гідроксі-С 1-4-алкокси, С1-4-алкоксі-С1-4алкокси, С1-4-алкоксі-С 1-4-алкоксі-С 1-4-алкокси, С3-7циклоалкоксі-С 1-4-алкокси, С3-7-циклоалкіл-С 1-4алкоксі-С 1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С 1-4-алкокси, аміно, моно- або ді-С1-4алкіламіно, С1-4-алкілкарбоніламіно, С1-4алкоксикарбоніламіно, моноабо ді-С 1-4алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкоксі-С 1або С 1-4-алкоксі-С1-44-алкоксикарбоніламіно алкілкарбонілокси, і де арил являє собою феніл або феніл, заміщений одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, галогену, трифторметилу, нітро, трифторметокси, гідрокси й ціано, або її сіль. 5. Сполука формули Іа-1 за п. 3 формули Іа R2 R3 N R1 N (Іа-1) X R5 R4 , ( , де R1 являє собою водень, С1-4-алкіл, С3-7циклоалкіл, гідроксі-С 1-4-алкіл або С1-4-алкоксі-С1-4алкіл, R2 являє собою водень, С1-4-алкіл, гідрокси, С1-4алкокси або арил-С 1-4-алкоксі-С 1-4-алкіл, R3 являє собою карбоксил, -СО-С1-4-алкокси, гідроксі-С 1-4алкіл, С1-4-алкоксі-С 1-4-алкіл, ціано, групу -CONR31R32, групу SO2-NR31R32 або групу Het, де R31 являє собою водень, С1-7-алкіл, гідроксі-С 1-4алкіл, С1-4-алкоксі-С 1-4-алкіл, С3-7-циклоалкіл або аміно й R32 являє собою водень або С1-7-алкіл, або де R31 й R32 разом, включаючи атомазоту, з яким вони обидва зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино, морфоліно, азиридино або азетидиногрупу й Het являє собою гетероциклічний залишок, заміщений R33, R34 й R35, вибраний із групи, яка складається з оксадіазолу, дигідрооксазолу й дигідроімідазолу, де R33 являє собою водень або С1-4-алкіл, R34 являє собою водень або С1-4-алкіл, R35 являє собою водень або С1-4-алкіл, 9 79843 R4 являє собою водень, С1-4-алкіл, гідроксі-С 1-4алкіл, С1-4-алкокси, С1-4-алкоксикарбоніл, трифторметил, аміно, моно- або ді-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно або С1-4-алкоксі-С 1-4-алкоксикарбоніламіно, R5 являє собою водень, С1-4-алкіл або С1-4-алкокси й X являє собою О (кисень) або NH, або її сіль. 6. Сполука формули Іb-1 за п. 4 формули Іb R2 R3 N R4 R1 N R5 (Іb-1) X R8 , ( у якій R1 являє собою С 1-4-алкіл або С3-7-циклоалкіл, R2 являє собою водень або С1-4-алкіл, R3 являє собою карбоксил, -СО-С1-4-алкокси, С1-4алкоксі-С 1-4-алкіл, С1-4-алкоксі-С 1-4-алкоксі-С1-4алкіл або групу -CO-NR31R32, де R31 являє собою водень, С1-7-алкіл, гідроксі-С1-4алкіл, С1-4-алкоксі-С 1-4-алкіл або С3-7-циклоалкіл й R32 являє собою водень, С1-7-алкіл, гідроксі-С1-4алкіл або С 1-4-алкоксі-С 1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обидва зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино, морфоліно, азиридино або азетидиногрупу, R4 являє собою водень, С1-4-алкіл, С1-4алкокси або галоген, R5 являє собою водень або С1-4-алкіл, R8 являє собою гідроксил, С1-4-алкокси, оксозаміщений С1-4-алкокси, С3-7-циклоалкокси, С3-7циклоалкіл-С 1-4-алкокси, гідроксі-С 1-4-алкокси, С1-4алкоксі-С 1-4-алкокси, С1-4-алкоксі-С 1-4-алкоксі-С1-4алкокси, С3-7-циклоалкоксі-С 1-4-алкокси, С3-7циклоалкіл-С 1-4-алкоксі-С 1-4-алкокси, С1-4алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моноабо ді-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, моноабо ді-С1-4-алкіламіно-С 1-4алкілкарбонілокси, С1-4-алкоксі-С1-4алкоксикарбоніламіно або С 1-4-алкоксі- С1-4алкілкарбонілокси, X являє собою О (кисень) або NH, або її сіль. 7. Сполука формули Іb-1 за п. 6, у якій R1 являє собою С 1-4-алкіл, R2 являє собою водень або С1-4-алкіл, Даний винахід стосується нових сполук, які можуть використовуватися у фармацевтичній промисловості як активні сполуки для одержання лікарських засобів. В [ЕР 266326 (який відповідає US 5,106,862)] 10 R3 являє собою карбоксил, -СО-С1-4-алкокси, С1-4алкоксі-С 1-4-алкіл, С1-4-алкоксі-С 1-4-алкоксі-С1-4алкіл або групу -CO-NR31R32, де R31 являє собою водень, С1-7-алкіл, гідроксі-С 1-4алкіл, С1-4-алкоксі-С 1-4-алкіл або С3-7-циклоалкіл й R32 являє собою водень, С1-7-алкіл, гідроксі-С 1-4алкіл або С 1-4-алкоксі-С 1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обидва зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино, морфоліно, азиридино або азетидиногрупу, R4 являє собою водень, С1-4-алкіл, С1-4-алкокси або галоген, R5 являє собою водень, R8 являє собою гідроксил, С1-4-алкокси, оксозаміщений С1-4-алкокси, С3-7-циклоалкокси, С3-7циклоалкіл-С 1-4-алкокси, гідроксі-С 1-4-алкокси, С1-4алкоксі-С 1-4-алкокси, С1-4-алкоксі-С 1-4-алкоксі-С1-4алкокси, С3-7-циклоалкоксі-С 1-4-алкокси, С3-7циклоалкіл-С 1-4-алкоксі-С 1-4-алкокси, С1-4алкілкарбонілокси, галоген-С1-4-алкоксі, аміно, моно- або ді-С 1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, моно- або ді-С1-4алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкоксі-С 1або С 1-4-алкоксі-С1-44-алкоксикарбоніламіно алкілкарбонілокси, X являє собою О (кисень) або NH, або її сіль. 8. Сполука формули Іа-1 за п. 5, у якій R1 являє собою С 1-4-алкіл, R2 являє собою С 1-4-алкіл, R3 являє собою карбоксил, -СО-С1-4-алкокси, С1-4алкоксі-С 1-4-алкіл або групу -CO-NR31R32, де R31 являє собою водень, С1-4-алкіл, гідроксі-С 1-4алкіл, С1-4-алкоксі-С 1-4-алкіл або С3-7-циклоалкіл й R32 являє собою водень або С1-4-алкіл, R4 являє собою С 1-4-алкіл або С1-4алкілкарбоніламіно, R5 являє собою С 1-4-алкіл, X являє собою О (кисень) або NH, або її сіль. 9. Сполука 6-(N,N-диметиламінокарбоніл)-4-(2етил-6-метил-бензиламіно)-1,2-диметил-1Нбензимідазол або її сіль. 10. Сполука 6-(N,N-диметиламінокарбоніл)-4-(2,6диметил-бензиламіно)-1,2-диметил-1Hбензимідазол або її сіль. 11. Лікарський засіб, який містить сполуку за п. 1 й/або її фармакологічно прийнятну сіль разом зі звичайними фармацевтичними добавками й/або ексципієнтами. 12. Застосування сполуки за п. 1 і її фармакологічно прийнятних солей для профілактики й лікування шлунково-кишкових захворювань. описані похідні бензимідазолу з дуже багатьма замісниками, які є активними як противиразкові агенти. Заявка [WO 97/47603 (яка відповідає US 6,465,505)] розкриває похідні бензимідазолу, заміщені 2,6-діалкілфенільною групою, які є ефекти 11 79843 вними як інгібітори Н+, K+-АТФази. Даний винахід стосується сполук формули 1 у якій R1 являє собою водень, С1-4-алкіл, C3-7циклoалкiл, C3-7-циклоалкіл-С 1-4-алкіл, С1-4алкокси, С1-4-алкокси-С 1-4-алкіл, С1-4алкoкcикapбoнiл, С2-4-алкеніл, С2-4-алкініл, фторС1-4-алкіл, гiдpoкcи-C1-4-алкiл, моно- або ди-С 1-4алкіламіно або С1-4-алкiлкapбoнiлoкcи-C1-4-aлкiл, R2 являє собою водень, С1-4-алкіл, арил, C3-7циклоалкіл, C3-7-циклоалкіл-С 1-4-алкіл, С1-4алкoкcикapбoнiл, моно- або ди-С1-4-алкіламіноС 1-4алкілкapбoнiл, гідрокси-С 1-4-алкіл, фтop-C2-4-алкiл, apил-С1-4-алкoкcи-C1-4-алкіл, гідрокси або С 1-4алкокси, R3 являє собою водень, галоген, фтор-С1-4алкіл, карбоксил, -CO-C1-4-алкокси, гідрокси-С 1-4алкiл, С1-4-алкoкcи-С 1-4-алкіл, С1-4-алкoкcи-С 1-4алкoкcи-С 1-4-алкіл, фтop-C1-4-aлкoкcи-C1-4-алкiл, ціано, групу -CO-NR31R32, групу SO2-NR31R32 або групу Het, де R31 являє собою водень, гідроксил, С1-7-алкіл, гідрокси-С 1-4-алкіл, С1-4-алкoкcи-С 1-4-алкiл або C3-7циклоалкіл, аміно й R32 являє собою водень, С1-7-алкіл, гідроксиС1-4-алкіл або С1-4-алкoкcи-С 1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино, морфоліно, азиридино або азетидино групу й Het являє собою гетероциклічний залишок, заміщений R33, R34 й R35, вибраними із групи, яка складається з оксадіазолу, дигідрооксазолу, дигідроімідазолу, оксазолу, імідазолу, ізоксазолу, дигідроізоксазолу, піразолу й те тразолу, де R33 являє собою водень, С1-4-алкіл, гідроксиС1-4-алкіл, С1-4-алкoкcи, С2-4-алкeнiлoкcи, С1-4алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбокси-С 1-4-алкіл, С1-4-aлкoкcикapбoнiл-С1-4алкiл, галоген, гідрокси, арил, арил-С1-4-алкіл, арил-окси, apил-С1-4-алкoкcи, трифторметил, нітро, аміно, моно-або ди-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніл аміно, С1-4-алкокси-С 1-4-алкоксикарбоніламіно або сульфоніл, R34 являє собою водень, С1-4-алкіл, С1-4алкoкcи, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, R35 являє собою водень, С1-4-алкіл, С1-4алкoкcи, С1-4-алкоксикарбоніл, галoгeн, трифторметил або гідрокси, X являє собою О (кисень) або NH й Υ має значення -СН2-Аr де Аr являє собою моно- або біциклічний ароматичний залишок, заміщений R4, R5, R6 й R7, які 12 вибрані із групи, яка складається з фенілу, нафтилу, піролілу, піразолілу, імідазолілу, 1,2,3триазолілу, індолілу, бензимідазолілу, фурилу, бензофурилу, тієнілу, бензотієнілу, тіазолілу, ізоксазолілу, піридинілу, піримідинілу, хінолінілу й ізохінолінілу, або Υ означає групу gp де Ζ має значення -CHR8- або -CHR8-CHR9-, де в Аr й/або в групi gp R4 являє собою водень, С1-4-алкіл, гідрокси-С 1С1-4-алкoкcи, С2-4-алкeнiлoкcи, С1-44-алкіл, алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбокси-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4алкіл, галоген, гідрокси, арил, арил-C1-4-алкiл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моно-або ди-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-алкокси-С 1-4-алкоксикарбоніламіно або сульфоніл, R5 являє собою водень, С1-4-алкіл, С1-4алкокси, С1-4-алкоксикарбоніл, галoгeн, трифторметил або гідрокси, R6 являє собою водень, С1-4-алкіл або галоген й R7 являє собою водень, С1-4-алкіл або галоген, R8 являє собою водень, С1-7-алкiл, C2-7алкeнiл, гідроксил, С1-4-алкокси, оксо-заміщений С1-4-алкокси, C3-7-циклoалкoкcи, C3-7-циклoалкiл-С 14-алкoкcи, гідрокси-С 1-4-алкокси, С 1-4-алкокси-С 1-4алкокси, С1-4-алкокси-С 1-4-алкокси-С 1-4-алкокси, C3C3-7-циклоалкіл-С 1-47-циклоалкокси-С 1-4-алкокси, алкокси-С 1-4-алкoкcи, С1-4-алкiлкapбoнiлoкcи, галoгeн-C1-4-aлкoкcи, аміно, моно- або ди-С1-4алкіламіно, С1-4-алкілкарбоніламіно, С1-4алкoкcикapбoнiламіно, моноабо ди-С1-4алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкокси-С 1або С 1-4-алкокси-С 1-44-алкоксикарбоніламіно алкілкарбонілокси, R9 являє собою водень, С1-7-алкiл, C2-7алкеніл, гідроксил, С1-4-алкокси, оксо-заміщений С1-4-алкокси, C3-7-циклoалкoкcи, C3-7-циклoалкiл-С 14-алкoкcи, гідрокси-С 1-4-алкoкcи, С 1-4-алкокси-С 1-4алкокси, С1-4-алкокси-С 1-4-алкoкcи-С 1-4-алкокси, C3C3-7-циклoалкiл-С 1-47-циклoалкiл-С 1-4-алкoкcи, алкoкcи-C1-4-алкoкcи, С1-4-алкiлкapбoнiлoкcи, галоген-С 1-4-алкокси, аміно, моно- або ди-С1-4-алкіл аміно, С1-4-алкілкарбоніламіно, С1-4алкоксикарбоніламіно, моноабо ди-С1-4алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкокси-С 1або С 1-4-алкокси-С 1-44-алкоксикарбоніламіно алкілкарбонілокси, і де арил являє собою феніл або феніл, заміщений одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, гaлoгeну, трифторметилу, нітро, трифторметокси, гідрокси й ціано, 13 79843 за умови, що R3 не являє собою водень або галoгeн, коли Υ означає -СН2-Ак й R2 означає водень, С1-4-алкіл або C3-7-циклoалкiл-С 1-4-алкіл, і солей цих сполук. С1-4-алкіл являє собою лінійну або poзгaлyжeну aлкiльну групу, яка має від 1 до 4 атомів вуглецю. Прикладами є бутильна, ізобутильна, втор-бутильна, трет-бутильна, пропільна, ізопропільна, етильна й метильна група. C3-7-Циклоалкіл являє собою циклопропіл, циклобутил, циклопентил, циклогексил і циклогептил, з яких циклопропіл, циклобутил і циклопентил є переважними. C3-7-Циклоалкіл-С 1-4-алкіл являє собою одну із вказаних вище С1-4-алкільних гр уп, яка заміщена однією із вказаних вище C3-7-циклоалкільних груп. Прикладами є циклопропілметильна, циклогексилметильна й циклогексилетильна група. С1-4-Алкокси являє собою групи, які крім атома кисню містять лінійну або poзгалyжeну алкiльну груп у, яка має від 1 до 4 атомів вуглецю. Прикладами є бутокси, ізобутокси, втор-бутокси, третбутокси, пропокси, ізопропокси й переважно етокси й метокси група. С1-4-Алкокси-С 1-4-алкіл являє собою одну із вказаних вище С1-4-алкільних гр уп, яка заміщена однією із вказаних вище С1- 4-алкоксигруп. Прикладами є метоксиметильна, метоксіетильна група й бутоксіетильна група. С1-4-Алкоксикарбоніл (-СО-С1-4-алкокси) являє собою кapбoнiльну груп у, з якою зв'язана одна із вказаних вище С1-4-aлкoкcигруп. Прикладами є метоксикарбонільна (СН3О-С(О)-) і етоксикарбонільна група (СН3СН2О-С(О)-). С2-4-Алкеніл являє собою лінійну або poзгaлyжeну aлкeнiльну груп у, яка має від 2 до 4 атомів вуглецю. Прикладами є 2-бутенільна, 3бутенільна, 1-пропенільна й 2-пропенільна група (алiльнa група). С2-4-Алкініл являє собою лінійну або poзгaлyжeну aлкiнiльну групу, яка має від 2 до 4 атомів вуглецю. Прикладами є 2-бутинільна, 3бутинільна, і переважно 2-пропінільна група (пропаргільна група). Фтор-С1-4-алкіл являє собою одну із вказаних вище С1-4-алкiльниx гр уп, яка заміщена одним або декількома атомами фтору. Прикладом є трифторметильна група. Гідрокси-С 1-4-алкіл являє собою вказані вище С1-4-алкільні групи, які заміщені гiдpoкcигрупою. Прикладами є гідроксиметильна, 2-гідроксіетильна й 3-гідроксипропільна група. С1-4-Алкілкарбоніл являє собою групу, яка крім карбонільної групи містить одну із вказаних вище С1-4-алкільних гр уп. Прикладом є ацетильна група. Моно- або ди-С1-4-алкiлaмiнo являє собою aмiнoгрупу, яка заміщена однією або двома однаковими або різними групами із вказаних вище С 1-4алкiльниx груп. Прикладами є диметиламіно, діетиламіно й дiiзoпpoпiлaмiнoгрупа. Моноабо ди-С1-4-алкіламіно-С 1-4алкілкарбоніл являє собою С 1-4-aлкiлкapбoнiльну груп у, яка заміщена моно- або ди-С1-4aлкiлaмiнoгрупами. Прикладами є диметиламінометилкарбонільна й диметиламіноетилкарбоніль 14 на група. Фтор-С2-4-алкіл являє собою С 2-4-алкільні групи, які заміщені одним або декількома атомами фтор у. Прикладом є 2,2,2-трифторетильна група. Арил-С 1-4-алкокси означає арил-заміщений С 14-aлкoкcиpaдикал. Прикладом є радикал бензилокси. Apил-C1-4-aлкoкcи-C1-4-алкiл означає одну із вказаних вище С1-4-алкільних гр уп, яка заміщена одним із вказаних вище арил-С 1-4алкоксирадикалів. Прикладом є бензилоксиметильний радикал. Галоген у даному винаході являє собою бром, хлор і фтор. С1-4-Алкокси-С 1-4-алкокси являє собою одну із вказаних вище С1-4-алкоксигруп, яка заміщена іншою С1-4-алкoкcигрупою. Прикладами є групи 2(метокси)етокси (СН3-О-СН2-СН2-О-) і 2(етокси)етокси (СН3-СН2-О-СН2-СН2-О-). С1-4-алкокси-С 1-4-алкокси-С 1-4-алкіл являє собою одну із вказаних вище С1-4-алкoкcи-C1-4aлкiльниx гр уп, яка заміщена однією із вказаних вище С1-4-алкoкcигруп. Прикладом є група 2(метокси)етоксиметил (СН3-О-СН2-СН2-О-СН2-). Фтор-С1-4-алкокси-С 1-4-алкіл являє собою одну із вказаних вище С1-4-алкільних груп, яка заміщена фтop-C1-4-алкoкcигрупою. Фтор-С1-4-алкокси в цьому випадку являє собою одну із вказаних вище С1-4-алкоксигруп, яка повністю або майже повністю заміщена фтором. Прикладами повністю або майже повністю фтор-заміщених С 1-4-алкoкcигруп є 1,1,1,3,3,3-гексафтор-2-пропокси, 2-трифторметил2-пропокси, 1,1,1-трифтор-2-пропокси, перфтортрет-бутокси, 2,2,3,3,4,4,4-гептафтор-1-бутокси, 4,4,4-трифтор-1-бутокси, 2,2,3,3,3пентафторпропокси, перфторетокси, 1,2,2трифторетокси, особливо 1,1,2,2тетрафторетокси, 2,2,2-трифторетокси, трифторметокси й переважно дифторметокси група. С1-7-алкіл являє собою лінійну або розгалужену aлкiльну груп y, яка має від 1 до 7 атомів вуглецю. Прикладами є гептил, ізогептил (5метилгексил), гексил, ізогексил (4-метилпентил), неогексил (3,3-диметилбутил), пентил, ізопентил (3-метилбутил), неопентил (2,2-диметилпропіл), бутил, ізобутил, втор-бутил, трет-бутил, пропіл, ізопропіл, етил і метил. С2-4-Алкенілокси являє собою групи, які крім атома кисню містять одну із вказаних вище С 2-4алкенільних груп. Прикладами є 2-бутенілокси, 3бутенілокси, 1-пропенілокси й 2-пропенілокси група (алілокси група). Карбокси-С 1-4-алкіл являє собою С 1-4-алкільну груп у, яка заміщена карбоксильною групою. Прикладами є карбоксиметильна й 2-карбоксіетильна група. С1-4-алкоксикарбоніл-С 1-4-алкіл являє собою С1-4-aлкiльну групу, яка заміщена однією із вказаних вище С1- 4-алкoкcикapбoнiльниx груп. Прикладами є метоксикарбонілметильна й етоксикарбонілметильна група. Арил-С -4-алкіл означає арил-заміщений С 1-4алкільний радикал. Прикладом є бензильний радикал. С1-4-Алкілкарбоніламіно являє собою 15 79843 aмiнoгрупу, до якої приєднана С 1-4алкілкарбонільна група. Прикладами є пропіоніламіно (C3H7C(O)NH-) і aцeтилaмiнoгрупа (aцeтaмiдoгрупа) (CH3C(O)NH-). С1-4-Алкоксикарбоніламіно являє собою aмiнoгрупу, яка заміщена однією із вказаних ви ще С1-4-алкоксикарбонільних груп. Прикладами є етоксикарбоніламіно й мeтoкcикapбoнiлaмінoгрупа. С1-4-алкокси-С 1-4-алкоксикарбоніл являє собою карбонільну гр упу, до якої приєднані вказані вище С1-4-алкокси-C1-4-алкоксигрупи. Прикладами є 2(метокси)етоксикарбонільна (СН3-О-СН2СН2-О-СО) і 2-(етокси)етоксикарбонільна група (СН3СН2-ОСН2СН2-О-СО-). C1-4-алкoкcи-С 1-4-aлкoкcикapбoнiлaмiнo являє собою aмiнoгрупу, яка заміщена однією із вказаних вище С1-4-алкокси-С 1-4-алкоксикарбонільних груп. Прикладами є 2-(метокси)-етоксикарбоніламіно й 2-(eтoкcи)eтoкcикapбoнiлaмiнoгрупа. С2-7-Алкеніл являє собою лініюгу або poзгaлyжeну aлкeнiльну груп y, яка має від 2 до 7 атомів вуглецю. Прикладами є 2-бутенільна, 3бутенільна, 1-пропенільна, 2-пропенільна (алільна) і вінільна група. Вказані вище С2-4-алкенільні групи є переважними. C2-7-Алкеніл являє собою лінійну або poзгaлyжeну aлкeнiльну груп у, яка має від 2 до 7 атомів вуглецю. Прикладами є 2-бутенільна, 3бутенільна, 1-пропенільна, 2-пропенільна (алільна) і вінільна група. Вказані вище С2-4-алкенільні групи є переважними. Оксо-заміщений С1-4-алкокси являє собою С 1-4aлкoкcигрупу, яка замість метиленової групи містить кapбoнiльну групу. Прикладом є 2oкcoпpoпoкcигрупа. C3-7-Циклоалкокси являє собою циклопропілокси, циклобутилокси, циклопентилокси, циклогексилокси й циклогептилокси, з яких циклопропілокси, циклобутилокси й циклопентилокси є переважними. C3-7-Циклоалкіл-С 1-4-алкокси являє собою одну із вказаних вище С1-4-алкoкcигруп, яка заміщена однією із вказаних вище C3-7-циклоалкільних груп. Прикладами є циклопропілметокси, циклобутилметокси й циклoгeкcилeтoкcигрупа. Гідрокси-С 1-4-алкокси являє собою вкaзaну вище С1-4-алкoкcигрупy, яка заміщена гідроксигрупою. Переважним прикладом є 2гiдpoкcieтoкcигрупа. С1-4-Aлкoкcи-C1-4-aлкoкcи-C1-4-алкoкcи являє собою одну із вказаних вище С1-4-алкoкcигруп, яка заміщена однією із вказаних вище С 1-4-алкoкcи-C1Переважним прикладом є 4-aлкoкcигруп. мeтoкcieтoкcieтoкcигрупа. C3-7-Циклоалкокси-С 1-4-алкокси являє собою одну із вказаних вище С1-4-aлкoкcигруп, яка заміщена однією із вказаних ви ще C3-7циклoалкoкcигруп. Прикладами є циклопропоксиметокси, циклобутоксиметокси й циклoгeкcилoкcieтoкcигрупа. C3-7-Циклоалкіл-С 1-4-алкокси-С 1-4-алкокси являє собою одну із вказаних вище С1-4-алкоксигруп, яка заміщена однією із вказаних вище С 3-7циклоалкіл-С 1-4-aлкoкcигруп. Прикладами є циклопропілметоксіетокси, циклобутилметоксіетокси й 16 циклoгeкcилeтoкcieтoкcигрупа. С1-4-Алкілкарбонілокси являє собою С 1-4алкiлкapбoнiльну груп у, яка зв'язана з атомом кисню. Прикладом є aцeтoкcигрупа (СН3СО-О-). С1-4-алкiлкapбoнiлoкcи-С 1-4-алкiл являє собою одну із вказаних вище С1-4-алкiльниx груп, яка заміщена однією із вказаних вище С 1-4алкiлкapбoнiлoкcигруп. Прикладом є ацетоксиметильна група (СН3СО-О-СН2). Галоген-С1-4-алкокси являє собою С 1-4алкoкcигрупи, які повністю або майже повністю заміщені галогеном. "Майже повністю" тут означає, що більше половини атомів водню в С 1-4алкoкcигрупаx заміщені атомами галогену. Галоген-C1-4-алкoкcигрупи в першу чергу являють собою хлор- і/або зокрема фтор-заміщені С 1-4алкоксигрупи. Прикладами галоген-заміщених С 1-4алкoкcигруп є 2,2,2-трихлоретокси, гексахлорізопропокси, пентахлорізопропокси, 1,1,1-трихлор3,3,3-трифтор-2-пропокси, 1,1,1-трихлор-2-метил2-пропокси, 1,1,1-трихлор-2-пропокси, 3-бром1,1,1-трифтор-2-пропокси, 3-бром-1,1,1-трифтор-2бутокси, 4-бром-3,3,4,4-тетрафтор-1-бутокси, хлордифторметокси, 1,1,1,3,3,3-гексафтор-2пропокси, 2-трифторметил-2-пропокси, 1,1,1трифтор-2-пропокси, перфтор-трет-бутокси, 2,2,3,3,4,4,4-гептафтор-1-бутокси, 4,4,4-трифтор-1бутокси, 2,2,3,3,3-пентафторпропокси, перфторетокси, 1,2,2-трифторетокси, зокрема 1,1,2,2тетрафторетокси, 2,2,2-трифторетокси, трифторметокси й переважно дифтopмeтoкcигрупа. Моноабо ди-C1-4-алкiлaмiнo-C1-4алкiлкapбoнiлoкcи являє собою С 1-4алкiлкapбoнiлoкcигрупу, яка заміщена однією із вказаних вище моно- або ди-С1-4-алкiлaмiнoгруп. Прикладами є диметиламіно-метилкарбонілокси й димeтилaмiнo-eтилкapбoнiлoкcигрупа. С1-4-алкокси-С 1-4-алкілкарбонілокси являє собою один із вказаних вище С1-4алкілкарбонілоксирадикалів, який заміщений однією із вказаних ви ще С 1-4-aлкoкcигруп. Прикладом є мeтoкcимeтилкapбoнiлoкcигрупа. Можливими солями сполук формули 1 або 2 залежно від замісника - є особливо всі кислотні адитивні солі. Особливо переважні фармакологічно прийнятні солі неорганічних й органічних кислот, які звичайно використовуються у фармацевтичній промисловості. Підходящими є водорозчинні й водонерозчинні кислотні адитивні солі з кислотами, такими як, наприклад, соляна кислота, бромоводнева кислота, фосфорна кислота, азотна кислота, сірчана кислота, оцтова кислота, лимонна кислота, D-глюконова кислота, бензойна кислота, 2-(4-гідроксибензоїл)бензойна кислота, бутанова кислота, сульфосаліцилова кислота, малeїнoвa кислота, лауринова кислота, яблучна кислота, фумарова кислота, янтарна кислота, оксалінова кислота, винна кислота, ембонова кислота, стеаринова кислота, толуолсульфонова кислота, метансульфонова кислота або 3гідрокси-2-нафтойна кислота, де кислоти для приготування солі використовуються залежно від того, чи є кислота моно- або поліосновною і від того, яка сіль необхідна - в еквімолярному кількісному співвідношенні або іншому співвідношенні. 17 79843 Фармакологічно неприйнятні солі, які можуть бути отримані спочатку, наприклад, у продуктах для одержання сполук за винаходом в промисловому масштабі, перетворюють у фармакологічно прийнятні солі способами, відомими фахівцеві в даній галузі техніки. Фахівцеві в даній галузі техніки відомо, що сполуки за винаходом і їх солі, наприклад, якщо вони виділені в кристалічній формі, можуть містити різні кількості розчинників. Даний винахід також включає всі сольвати й зокрема всі гідрати сполук формули І, а також всі сольвати й зокрема всі гідрати солей сполук формули І. Один варіант здійснення (варіант здійснення а) включає сполуки формули 1, у яких R1 являє собою моно- або ди-С1-4-алкіламіно, R2, R3, X й Υ мають вказані вище значення за винаходом, за умови, що R3 не має значення водень або галоген, коли Υ означає -СН2-Ак й R2 означає водень, С1-4-алкіл або C3-7-циклоалкіл-С 1-4-алкіл, і солі цих сполук. Один варіант здійснення (варіант здійснення б) включає сполуки формули 1, у яких R1 являє собою С1-4-алкілкарбонілокси-С1-4алкіл й R2, R3, X й Υ мають вказані вище значення за винаходом і солі цих сполук. Інший варіант здійснення (варіант здійснення в) включає сполуки формули 1, у яких R2 являє собою гідрокси або С1-4-алкoкcи й R1, R3, X й Υ мають вказані вище значення за винаходом і солі цих сполук. Інший варіант здійснення (варіант здійснення г) включає сполуки формули 1, у яких R3 являє собою ціано, групу SO2-NR31R32 або групу Het й де R31 являє собою водень, гідроксил, С1-7-алкiл, гідрокси-С 1-4-алкіл, С1-4-aлкoкcи-C1-4-алкiл або C3-7циклoалкiл, аміно й R32 являє собою водень, С1-7-алкiл, гідроксиС1-4-алкіл або С1-4-алкокси-С 1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обоє зв'язані, являють собою піролідино, піперидино, піперазино, N-C1-4алкiлпiпepaзинo, морфоліно, азиридино або aзeтидинoгрупу й Het являє собою гетероциклічний залишок, заміщений R33, R34 й R35, вибраний із групи, яка складається з оксадіазолу, дигідрооксазолу, дигідроімідазолу, оксазолу, імідазолу, ізоксазолу, дигідроізоксазолу, піразолу й тетразолу, де R33 являє собою водень, С1-4-алкіл, гідроксиС1-4-алкіл, С1-4-алкокси, С2-4-алкенілокси, С1-4алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбокси-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, apил-C1-4-алкoкcи, трифторметил, нітро, аміно, моноабо ди-C1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-алкокси-С 1-4-алкоксикарбоніламіно або сульфо 18 ніл, R34 являє собою водень, С1-4-алкiл, С1-4алкокси, С1-4-алкоксикарбоніл, галoгeн, трифторметил або гідрокси, R35 являє собою водень, С1-4-алкiл, С1-4алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, де R1, R2, X й Υ мають вказані вище значення за винаходом і солі цих сполук. Інший варіант здійснення (варіант здійснення д) включає сполуки формули 1, у яких R1 являє собою водень, С1-4-алкіл, C3-7циклоалкіл, С3-7-циклоалкіл-С 1-4-алкіл, С1-4алкoкcи, С1-4-алкокси-С 1-4-алкіл, С1-4алкoкcикapбoнiл, С2-4-алкеніл, С2-4-алкініл, фторС1-4-алкіл або гідрокси-С 1-4-алкіл, R2 являє собою водень, С1-4-алкiл, арил, C3-7циклоалкіл, C3-7-циклоалкіл-С 1-4-алкіл, С1-4алкоксикарбоніл, моно- або ди-С1-4-алкіламіноС 1-4алкiлкapбoнiл, гiдpoкcи-C1-4-алкiл, фтор-С2-4-алкіл, арил-С 1-4-алкокси-C1-4-алкіл, R3 являє собою водень, галоген, фтор-С1-4алкіл, карбоксил, -CO-С1-4-алкокси, гідрокси-С 1-4алкіл, С1-4-алкокси-С 1-4-алкіл, С1-4-алкокси-С 1-4алкoкcи-С 1-4-алкіл, фтор-C1-4-алкокси-С 1-4-алкіл або групу -CO-NR31R32, де R31 являє собою водень, гідроксил, С1-7-алкiл, гідрокси-С 1-4-алкіл, С1-4-aлкoкcи-C1-4-алкiл або C3-7циклоалкіл й R32 являє собою водень, С1-7-алкіл, гідроксиС1-4-алкіл або С1-4-алкокси-С 1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обоє зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4алкілпіперазино, морфоліно, азиридино або aзeтидинoгрупу, X являє собою О (кисень) або NH й Υ являє собою або -СН2-Аr, де Аr являє собою моно- або біциклічний ароматичний залишок, заміщений R4, R5, R6 й R7, який вибраний із групи, яка складається з фенілу, нафтилу, піролілу, піразолілу, імідазолілу, 1,2,3триазолілу, індолілу, бензимідазолілу, фурилу, бензофурилу, тієнілу, бензотієнілу, тіазолілу, ізоксазолілу, піридинілу, піримідинілу, хінолінілу й ізохінолінілу, або Υ означає груп у gp де Ζ має значення -CHR8- або -CHR8-CHR9де в Аr й/або в групi gp R4 являє собою водень, С1-4-алкіл, гідрокси-С 1С1-4-алкокси, С2-4-алкенілокси, С1-44-алкіл, алкілкарбоніл, карбокси, С1-4-алкoкcикapбoнiл, карбокси-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4 19 79843 алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, apил-C1-4-алкoкcи, трифторметил, нітро, аміно, моно-або ди-С1-4-алкіл аміно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніл аміно, С1-4-алкoкcи-C1-4-алкoкcикapбoнiлaмiнo або сульфоніл, R5 являє собою водень, С1-4-алкiл, С1-4алкокси, С1-4-алкоксикарбоніл, галoгeн, трифторметил або гідрокси, R6 являє собою водень, С1-4-алкiл або галоген й R7 являє собою водень, С1-4-алкiл або галоген, R8 являє собою водень, С1-7-алкіл, C2-7алкeнiл, гідроксил, С1-4-алкокси, оксо-заміщений С1-4-алкокси, C3-7-циклoалкoкcи, C3-7-циклоалкіл-С 14-алкокси, гідрокси-С 1-4-алкокси, С 1-4-алкокси-С 1-4алкокси, С1-4-алкокси-С 1-4-алкокси-C1-4-алкoкcи, C3C3-7-циклoалкiл-C1-47-циклoалкoкcи-C 1-4-алкoкcи, aлкoкcи- С1-4-алкoкcи, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ди-С1-4-алкіл аміно, C1-4-алкiлкapбoнiлaмiнo, С1-4алкоксикарбоніламіно, моноабо ди-С1-4алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкокси-С 1або С 1-4-алкокси-С 1-44-алкоксикарбоніламіно алкілкарбонілокси, R9 являє собою водень, С1-7-алкiл, С2-7алкeнiл, гідроксил, С1-4-алкокси, оксо-заміщений С1-4-алкокси, C3-7-циклоалкокси, C3-7-циклoалкiл-С 14-алкoкcи, гідрокси-С 1-4-алкокси, С 1-4-алкокси-С 1-4алкокси, С1-4-алкокси-C1-4-алкокси-С 1-4-алкокси, C3C3-7-циклоалкіл-С -47-циклоалкокси-С 1-4-алкoкcи, алкокси-С 1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ди-С1-4алкіламіно, С1-4-алкiлкapбoнiлaмiнo, С1-4алкoкcикapбoнiлaмiнo, моноабо ди-С1-4алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкокси-С 1аміно або С 1-4-алкокси-С 1-44-алкоксикарбоніл алкiлкapбoнiлoкcи, і де арил являє собою феніл або заміщений феніл з одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, гaлoгeну, трифторметилу, нітро, трифторметокси, гідрокси й ціано, за умови, що R3 не має значення водень або галоген, коли Υ означає -СН2-Аr, і солі цих сполук. Інший варіант здійснення (варіант здійснення є) включає сполуки формули 1, у яких R1 являє собою водень, С1-4-алкіл, C3-7циклоалкіл, C3-7-циклоалкіл-С 1-4-алкіл, С1-4алкокси, C1-4-алкoкcи-C1-4-aлкiл, С1-4алкоксикарбоніл, С2-4-алкеніл, С2-4-алкініл, фторС1-4-алкіл або гiдpoкcи-C1-4-алкiл, R2 являє собою водень, С1-4-алкіл, арил, C3-7циклоалкіл, C3-7-циклoалкiл-C1-4-алкіл, С1-4алкoкcикapбoнiл, моно- або ди-С1-4-алкіламіноС 1-4алкiлкapбoнiл, гiдpoкcи-С1-4-алкiл або фтор-С2-4алкіл, R3 являє собою водень, галоген, фтop-C1-4алкiл, карбоксил, -CO-С1-4-алкокси, гідрокси-С 1-4алкiл, С1-4-алкoкcи-C1-4-алкіл, С1-4-алкокси-С 1-4алкокси-С 1-4-алкіл, фтор-C1-4-алкокси-С 1-4-алкiл 20 або групу -CO-NR31R32, де R31 являє собою водень, гідроксил, С1-7-алкіл, гідрокси-С 1-4-алкіл або С1-4-алкокси-С 1-4-алкіл, R32 являє собою водень, С1-7-алкіл, гідроксиС1-4-алкіл або С1-4-алкокси-С 1-4-алкiл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обоє зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино або мopфoлiнoгрупу, X являє собою О (кисень) або NH й Υ або має значення -СН2-Аr, де Аr являє собою моно- або біциклічний ароматичний залишок, заміщений R4, R5, R6 й R7, який вибраний із групи, яка складається з фенілу, нафтилу, піролілу, піразолілу, імідазолілу, 1,2,3триазолілу, індолілу, бензимідазолілу, фурилу, бензофурилу, тієнілу, бензотієнілу, тіазолілу, ізоксазолілу, піридинілу, піримідинілу, хінолінілу й ізохінолінілу, або Υ означає груп у gp Z має значення -CHR8- або -CHR8-CHR9-, де в Аr й/або в групі gp R4 являє собою водень, С1-4-алкіл, гідрокси-С 1C1-4-алкoкcи, С2-4-алкенілокси, С1-44-алкіл, алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбокси-С 1-4-алкіл, С1-4-aлкoкcикapбoнiл-С1-4алкiл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, apил-C1-4-алкoкcи, трифторметил, нітро, аміно, моно-або ди-С1-4-алкiлaмiнo, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-aлкoкcи-С 1-4-алкoкcикapбoнiлaмiнo або сульфоніл, R5 являє собою водень, С1-4-алкіл, С1-4алкoкcи, С1-4-алкоксикарбоніл, галoгeн, трифторметил або гідрокси, R6 являє собою водень, С1-4-алкіл або галоген й R7 являє собою водень, С1-4-алкіл або галоген, R8 являє собою водень, С1-7-алкiл, C2-7алкеніл, гідроксил, С1-4-алкокси, оксо-заміщений С1-4-алкoкcи, C3-7-циклoалкoкcи, C3-7-циклoaлкiл-С14-алкoкcи, гідрокси-С 1-4-алкокси, С 1-4-алкокси-С 1-4алкокси, С1-4-алкокси-С 1-4-алкокси-С 1-4-алкокси, C3C3-7-циклоалкіл-С 1-47-циклoалкoкcи-С 1-4-алкoкcи, aлкoкcи-С 1-4-алкoкcи, С1-4-алкілкарбонілокси, галоген-С 1-4-алкокси, аміно, моно- або ди-С1-4алкіламіно, С1-4-алкілкарбоніламіно, С1-4алкоксикарбоніламіно, моноабо ди-С1-4алкіламіно-С1-4-алкілкарбонілокси або С 1-4aлкoкcи-С 1-4-алкoкcикapбoнiлaмiнo, R9 являє собою водень, С1-7-алкіл, C2-7алкеніл, гідроксил, С1-4-алкокси, оксо-заміщений С1-4-алкокси, C3-7-циклoалкoкcи, C3-7-циклoaлкiл-С14-алкoкcи, гідрокси-С 1-4-алкокси, С 1-4-алкокси-С 1-4алкокси, С1-4-алкокси-С 1-4-алкокси-С 1-4-алкокси, C37-циклoалкoкcи-С 1-4-алкокси, С 3-7-Циклоалкіл-С 1-4 21 79843 aлкoкcи-С 1-4-алкoкcи, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ди-С1-4-алкіл аміно, С1-4-алкiлкapбoнiлaмiнo, С1-4алкоксикарбоніламіно, моноабо ди-С1-4алкіламіно-С1-4-алкілкарбонілокси або С 1-4aлкoкcи-С 1-4-алкoкcикapбoнiлaмiнo, і де арил являє собою феніл або заміщений феніл з одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкoкcи, карбокси, С1-4-алкоксикарбонілу, галогену, трифторметилу, нітро, трифторметокси, гідрокси й ціано, за умови, що R3 не має значення водень або галоген, коли Υ означає -СН2-Аr, і солі цих сполук. В одному варіанті, даний винахід стосується сполук формули 1а у якій R1 являє собою водень, С1-4-алкіл, С3-7циклоалкіл, С3-7-циклоалкіл-С 1-4-алкіл, С1-4алкокси, С1-4-алкoкcи-С 1-4-алкiл, С1-4 алкoкcикapбoнiл, С2-4-алкеніл, С2-4-алкiнiл, фторС1-4-алкіл, гiдpoкcи-С1-4-алкiл, моно- або ди- С1-4алкіламіно або С1-4-алкілкарбонілокси-C1-4-алкіл, R2 являє собою водень, С1-4-алкіл, арил, C3-7циклоалкіл, C3-7-циклоалкіл-С 1-4-алкіл, С1-4алкоксикарбоніл, моно- або ди-С1-4-алкіламіноС 1-4алкiлкapбoніл, гiдpoкcи-C1-4-алкiл, фтор-С2-4-алкіл, apил-C1-4-алкoкcи-C1-4-алкіл, гідрокси або С 1-4алкокси, R3 являє собою водень, галоген, фтор-С1-4алкіл, карбоксил, -СО-С1-4-алкокси, гідрокси-С 1-4алкiл, С1-4-алкокси-С 1-4-алкіл, С1-4-алкокси-С 1-4-С1-4алкіл, фтop-C1-4-aлкoкcи-C1-4-алкiл, ціано, групу CO-NR31R32, групу SO2-NR31R32 або групу Het, де R31 являє собою водень, гідроксил, С1-7-алкiл, гiдpoкcи-С1-4-алкiл, С1-4-алкoкcи-С 1-4-алкiл або C3-7циклоалкіл, аміно й R32 являє собою водень, С1-7-алкіл, гiдpoкcиС1-4-алкіл або С1-4-алкoкcи-С 1-4-алкiл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обоє зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4алкілпіперазино, морфоліно, азиридино або aзeтидинoгрупу й Het являє собою гетероциклічний залишок, заміщений R33, R34 й R35, вибраний із групи, яка складається з оксадіазолу, дигідрооксазолу, дигідроімідазолу, оксазолу, імідазолу, ізоксазолу, дигідроізоксазолу, піразолу й тетразолу, де R33 являє собою водень, С1-4-алкіл, гiдpoкcиС1-4-алкiл, С1-4-алкокси, С2-4-алкeнiлoкcи, С1-4 22 алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбокси-C1-4-алкiл, C1-4-aлкoкcикapбoнiл-С1-4алкiл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моно-або ди-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-алкокси-С 1-4-алкоксикарбоніламіно або сульфоніл, R34 являє собою водень, С1-4-алкiл, С1-4алкoкcи, С1-4-алкoкcикapбoнiл, галoгeн, трифторметил або гідрокси, R35 являє собою водень, С1-4-алкіл, С1-4алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, X являє собою О (кисень) або NH й Аr являє собою моно- або біциклічний ароматичний залишoк, заміщений R4, R5, R6 й R7, який вибраний із групи, яка складається з фенілу, нафтилу, піролілу, піразолілу, імідазолілу, 1,2,3триазолілу, індолілу, бензимідазолілу, фурилу, бензофурилу, тієнілу, бензотієнілу, тіазолілу, ізоксазолілу, піридинілу, піримідинілу, хінолінілу й ізохінолінілу, де R4 являє собою водень, С1-4-алкіл, гідрокси-С 1С1-4-алкокси, С2-4-алкенілокси, С1-44-алкіл, алкiлкapбoнiл, карбокси, С1-4-алкоксикарбоніл, карбокси-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4алкіл, галоген, гідрокси, арил, арил-С1-4-алкiл, арилокси, apил-С1-4-алкoкcи, трифторметил, нітро, аміно, моно-або ди-С1-4-алкiлaмiнo, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-алкокси-С 1-4-алкоксикарбоніламіно або сульфоніл, R5 являє собою водень, С1-4-алкiл, С1-4алкoкcи, С1-4-алкоксикарбоніл, галoгeн, трифторметил або гідрокси, R6 являє собою водень, С1-4-алкiл або галоген й R7 являє собою водень, С1-4-алкiл або галоген, і де арил являє собою феніл або заміщений феніл з одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, галогену, трифторметилу, нітро, трифторметокси, гідрокси й ціано, за умови, що R3 не має значення водень або галоген, коли Υ означає -СН2-Аr й R2 означає водень, С1-4-алкіл або C3-7-циклоалкіл-С 1-4-алкіл, і солей цих сполук. В іншому варіанті здійснення даний винахід стосується сполук формули 1а, у якій R1 являє собою водень, С1-4-алкіл, C3-7циклоалкіл, C3-7-циклоалкіл-С 1-4-алкіл, С1-4алкокси, С1-4-алкокси-С 1-4-алкіл, С1-4алкоксикарбоніл, С2-4-алкеніл, С2-4-алкініл, фторС1-4-алкіл або гідрокси-С 1-4-алкіл, R2 являє собою водень, C1-4-алкiл, арил, C3-7циклоалкіл, C3-7-циклоалкіл-С 1-4-алкіл, С1-4алкоксикарбоніл, моно- або ди-С1-4-алкіламіноС 1-4алкілкарбоніл, гiдpoкcи-C1-4-алкiл, фтор-С2-4-алкіл, apил-С1-4-алкoкcи-C1-4-алкіл, 23 79843 R3 являє собою фтop-С1-4-алкiл, карбоксил, CO-C1-4-алкoкcи, гідрокси-С 1-4-алкіл, С1-4-алкoкcиC1-4-aлкiл, С1-4-алкoкcи-C1-4-aлкoкcи-C1-4-алкiл, фтор-С1-4-алкокси-С 1-4-алкіл або групу -CONR31R32, де R31 являє собою водень, гідроксил, С1-7-алкіл, гідрокси-С 1-4-алкіл, С1-4-aлкoкcи-С 1-4-алкiл або С 3-7циклоалкіл й R32 являє собою водень, С1-7-алкіл, гідроксиС1-4-алкіл або С1-4-алкокси-С 1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обоє зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4алкілпіперазино, морфоліно, азиридино або aзeтидинoгрупу, X являє собою О (кисень) або NH й Аr являє собою моно- або біциклічний ароматичний залишок, заміщений R4, R5, R6 й R7, який вибраний із групи, яка складається з фенілу, нафтилу, піролілу, піразолілу, імідазолілу, 1,2,3триазолілу, індолілу, бензимідазолілу, фурилу, бензофурилу, тієнілу, бензотієнілу, тіазолілу, ізоксазолілу, піридинілу, піримідинілу, хінолінілу й ізохінолінілу, де R4 являє собою водень, С1-4-алкіл, гідрокси-С 1С1-4-алкокси, С2-4-алкенілокси, С1-44-алкіл, алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбокси-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моно-або ди-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-алкокси-С 1-4-алкоксикарбоніламіно або сульфоніл, R5 являє собою водень, С1-4-алкіл, С1-4алкoкcи, С1-4-алкоксикарбоніл, галoгeн, трифторметил або гідрокси, R6 являє собою водень, С1-4-алкіл або галoгeн й R7 являє собою водень, С1-4-алкiл або галoгeн, і де арил являє собою феніл або заміщений феніл з одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкiлy, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, галогену, трифторметилу, нітро, трифторметокси, гідрокси й ціано, і солей цих сполук. В іншому варіанті здійснення даний винахід стосується сполук формули 1а, у якій R1 являє собою водень, С1-4-алкіл, C3-7циклоалкіл, C3-7-циклоалкіл-С 1-4-алкіл, С1-4алкокси, С1-4-алкокси-С 1-4-алкіл, С1-4алкоксикарбоніл, С2-4-алкеніл, С2-4-алкiнiл, фторС1-4-алкіл або гідрокси-С 1-4-алкіл, R2 являє собою водень, С1-4-алкіл, арил, С3-7циклоалкіл, C3-7-циклоалкіл-С 1-4-алкiл, С1-4алкoкcикapбoнiл, моно- або ди-С1-4-алкіламіноС 1-4алкілкарбоніл, гiдpoкcи-C1-4-алкiл або фтop-C2-4алкiл, 24 R3 являє собою фтop-C1-4-алкiл, карбоксил, CO-С1-4-алкокси, гідрокси-С 1-4-алкiл, С1-4-aлкoкcиC1-4-алкiл, С1-4-алкокси-С 1-4-алкокси-С 1-4-алкіл, фтор-С1-4-алкокси-С 1-4-алкіл або групу -CONR31R32, де R31 являє собою водень, гідроксил, С1-7-алкіл, гідрокси-С 1-4-алкіл або С1-4-aлкoкcи-C1-4-алкiл й R32 являє собою водень, С1-7-алкіл, гідроксиС1-4-алкіл або С1-4-алкокси-С 1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обоє зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино або мopфoлiнoгрупу, X являє собою О (кисень) або NH й Аr являє собою моно- або біциклічний ароматичний залишок, заміщений R4, R5, R6 й R7, який вибраний із групи, яка складається з фенілу, нафтилу, піролілу, піразолілу, імідазолілу, 1,2,3триазолілу, індолілу, бензимідазолілу, фурилу, бензофурилу, тієнілу, бензотієнілу, тіазолілу, ізоксазолілу, піридинілу, піримідинілу, хінолінілу й ізохінолінілу, де R4 являє собою водень, С1-4-алкіл, гідрокси-С 1С1-4-алкокси, С2-4-алкенілокси, С1-44-алкіл, алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбокси-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4алкіл, галoгeн, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моно- або ди-С1-4-алкіламіно, С1-4- алкілкарбоніламіно, C1-4-алкoкcикapбoнiлaмiнo, С1-4aлкoкcи-C1-4-алкoкcикapбoнiлaмiнo або сульфоніл, R5 являє собою водень, С1-4-алкіл, С1-4алкoкcи, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, R6 являє собою водень, С1-4-алкiл або галоген й R7 являє собою водень, С1-4-алкіл або галоген, і де арил являє собою феніл або заміщений феніл з одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, галогену, трифторметилу, нітро, трифторметокси, гідрокси й ціано, і солей цих сполук. В iншoму варіанті здійснення даний винахід стосується сполук формули 1b у якій R1 являє собою водень, С1-4-алкіл, C3-7циклоалкіл, C3-7-циклоалкіл-С 1-4-алкіл, С1-4алкокси, С1-4-алкокси-С 1-4-алкіл, С1-4алкоксикарбоніл, C2-4-алкeнiл, С2-4-алкiнiл, фтор 25 79843 С1-4-алкіл, гiдpoкcи-C1-4-алкiл, моно- або ди-С 1-4алкіламіно або С1-4-алкілкарбонілокси-С1-4-алкіл, R2 являє собою водень, С1-4-алкіл, арил, C3-7циклоалкіл, C3-7-циклоалкіл-С 1-4-алкіл, С1-4алкоксикарбоніл, моно- або ди-С1-4-алкіламіноС 1-4алкiлкapбoнiл, гiдpoкcи-С1-4-алкiл, фтор-С2-4-алкіл, арил-С 1-4-алкокси-С 1-4-алкіл, гідрокси або С 1-4алкокси, R3 являє собою водень, галoгeн, фтop-C1-4алкiл, карбоксил, -CO-C1-4-алкoкcи, гідрокси-С 1-4алкіл, С1-4-алкoкcи-C1-4-алкiл, С1-4-алкокси-С 1-4алкокси-С 1-4-алкiл, фтор-С1-4-алкокси-С 1-4-алкіл, ціано, групу-CO-NR31R32, групу SO2-NR31R32 або груп у Het, де R31 являє собою водень, гідроксил, С1-7-алкіл, гідрокси-С 1-4-алкіл, С1-4-алкокси-С 1-4-алкіл або C3-7циклоалкіл, аміно й R32 являє собою водень, С1-7-алкіл, гідроксиС1-4-алкіл або С1-4-алкoкcи-C1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обоє зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4алкілпіперазино, морфоліно, азиридино або aзeтидинoгрупу й Het являє собою гетероциклічний залишoк, заміщений R33, R34 й R35, вибраний із групи, яка складається з оксадіазолу, дигідрооксазолу, дигідроімідазолу, оксазолу, імідазолу, ізоксазолу, дигідроізоксазолу, піразолу й тетразолу, де R33 являє собою водень, С1-4-алкіл, гідроксиС1-4-алкіл, С1-4-алкoкcи, С2-4-алкенілокси, С1-4алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбокси-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моно-або ди-C1-4-алкiл аміно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-алкокси-С 1-4-алкoкcикapбoнiлaмiнo або сульфоніл, R34 являє собою водень, С1-4-алкiл, С1-4алкокси, С1-4-алкоксикарбоніл, галoгeн, трифторметил або гідрокси, R35 являє собою водень, С1-4-алкiл, С1-4алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, R4 являє собою водень, С1-4-алкiл, гідрокси-С 1С1-4-алкокси, С2-4-алкенілокси, С1-44-алкіл, алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбокси-С 1-4-алкіл, С1-4-алкoкcикapбoнiл-C1-4алкiл, галoгeн, гідрокси, арил, арил-С1-4-алкіл, арилокси, apил-C1-4-алкoкcи, трифторметил, нітро, аміно, моно-або ди-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, С14-aлкoкcи-С 1-4-алкoкcикapбoнiлaмiнo або сульфоніл, R5 являє собою водень, С1-4-алкiл, С1-4алкoкcи, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, X являє собою О (кисень) або NH й Ζ має значення -CHR8- або -CHR8-CHR9-, де R8 являє собою водень, С1-7-алкіл, C2-7 26 алкeнiл, гідроксил, С1-4-алкокси, оксо-заміщений С1-4-алкокси, C3-7-циклoaлкiл, C3-7-циклoaлкiл- С1-4алкoкcи, гідрокси-С 1-4-алкокси, С1-4-алкокси-С 1-4алкокси, С1-4-алкокси-С 1-4-алкокси-С 1-4-алкокси, C3С3-7-циклоалкіл-С 1-47-циклoалкoкcи-С 1-4-алкокси, алкокси-С 1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С 1-4-алкокси, аміно, моно- або ди-С1-4алкiлaмiнo, С1-4-алкілкарбоніламіно, С1-4алкоксикарбоніламіно, моноабо ди-С1-4алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкокси-С 1або С 1-4-алкокси-С 1-44-алкоксикарбоніламіно алкілкарбонілокси, R9 являє собою водень, С1-7-алкiл, C2-7алкeнiл, гідроксил, С1-4-алкокси, оксо-заміщений С1-4-алкокси, C3-7-циклoалкoкcи, C3-7-циклoалкіл-С 14-алкокси, гідрокси-С 1-4-алкокси, С 1-4-алкокси-С 1-4алкокси, С1-4-алкокси-С 1-4-алкокси-С 1-4-алкокси, C3C3-7-циклоалкіл-С 1-47-циклoалкoкcи-С 1-4-алкокси, алкокси-С 1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С 1-4-алкокси, аміно, моно- або ди-C1-4алкiлaмiнo, С1-4-алкілкарбоніламіно, С1-4алкоксикарбоніламіно, моноабо ди-С1-4алкіламіно-С1-4-алкiлкapбoнiлoкcи, С1-4-aлкoкcи-C1або С1-4-алкокси-С 1-44-алкoкcикapбoнiлaмiнo алкiлкapбoнiлoкcи, і де арил являє собою феніл або заміщений феніл з одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкoкcи, карбокси, С1-4-алкоксикарбонілу, галоген трифторметилу, нітро, трифторметокси, гідрокси й ціано, і солей цих сполук. В іншому варіанті здійснення даний винахід стосується сполук формули 1b, у якій R1 являє собою водень, С1-4-алкіл, C3-7циклоалкіл, С3-7-циклоалкіл-С 1-4-алкіл, С1-4алкокси, С1-4-алкокси-С 1-4-алкіл, С1-4алкоксикарбоніл, С2-4-алкeнiл, С2-4-алкініл, фторС1-4-алкіл або гідрокси-С 1-4-алкіл, R2 являє собою водень, С1-4-алкiл, арил, C3-7циклоалкіл, C3-7-циклоалкіл-С 1-4-алкіл, С1-4алкоксикарбоніл, моно- або ди-С1-4-алкіламіноС 1-4алкілкарбоніл, гідрокси-С 1-4-алкiл, фтор-С2-4-алкіл, арил-С 1-4-алкокси-С 1-4-алкіл, R3 являє собою водень, галоген, фтop-C1-4алкiл, карбоксил, -CO-C1-4-алкoкcи, гідрокси-С 1-4алкiл, С1-4-алкокси-С 1-4-алкiл, С1-4-алкокси-С 1-4алкокси-С 1-4-алкіл, фтop-С1-4-алкoкcи-С 1-4-алкiл або групу-CO-NR31R32, де R31 являє собою водень, гідроксил, С1-7-алкіл, гідрокси-С 1-4-алкіл, C1-4-алкокси-С 1-4-алкіл або C3-7циклоалкіл й R32 являє собою водень, С1-7-алкіл, гідроксиС1-4-алкіл або С1-4-алкокси-С 1-4-алкiл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обоє зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4алкілпіперазино, морфоліно, азиридино або aзeтидинoгрупу, R4 являє собою водень, С1-4-алкiл, гідрокси-С 1С1-4-алкокси, С2-4-алкенілокси, С1-44-алкіл, алкiлкapбoніл, карбокси, С1-4-алкоксикарбоніл, 27 79843 карбокси-С 1-4-алкіл, С1-4-алкоксикарбоніл-С 1-4алкіл, галоген, гідрокси, арил, арил-С1-4-алкіл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моно-або ди-С1-4-алкiлaмiнo, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніл аміно, С1-4-aлкoкcи-С 1-4-алкoкcикapбoнiлaмiнo або сульфоніл, R5 являє собою водень, С1-4-алкіл, С1-4алкокси, С1-4-алкоксикарбоніл, галоген, трифторметил або гідрокси, X являє собою О (кисень) або NH й Ζ має значення -CHR8- або -CHR8-CHR9-, де R8 являє собою водень, С1-7-алкіл, С2-7алкеніл, гідроксил, С1-4-алкокси, оксо-заміщений С1-4-алкокси, С3-7-циклоалкокси, C3-7-циклoалкiл-С 14-алкoкcи, гідрокси-С 1-4-алкокси, С 1-4-алкокси-С 1-4алкoкcи, С1-4-алкокси-С 1-4-aлкoкcи-C1-4-алкoкcи, C3C3-7-циклоалкіл-С 1-47-циклоалкокси-С 1-4-алкокси, алкoкcи-C1-4-aлкoкcи, С1-4-алкiлкapбoнiлoкcи, галoгeн-С1-4-aлкoкcи, аміно, моно- або ди-С1-4алкіламіно, С1-4-алкілкарбоніламіно, С1-4алкоксикарбоніламіно, моноабо ди-С1-4алкіламіно-С1-4-алкілкарбонілокси, С1-4-алкокси-С 1або С 1-4-алкoкcи-С 1-44-алкоксикарбоніламіно алкілкарбонілокси, R9 являє собою водень, С1-7-алкіл, C2-7алкеніл, гідроксил, С1-4-алкoкcи, оксо-заміщений С1-4-алкокси, C3-7-циклоалкокси, C3-7-циклoалкiл-C14-алкoкcи, гідрокси-С 1-4-алкокси, С 1-4-алкокси-С 1-4алкокси, С1-4-алкокси-С 1-4-алкокси-С 1-4-алкокси, C3C3-7-циклоалкіл-С 1-47-циклоалкокси-С 1-4-алкокси, алкокси-С 1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моно- або ди-С1-4-алкіл аміно, С1-4-алкілкарбоніламіно, Сі_4алкоксикарбоніламіно, моноабо ди-Сі.4алкіламіно-Сі.4-алкілкарбонілокси, Сі.4-алкоксиСі_4-алкоксикарбоніламіно або С 1-4-алкокси-С 1-4алкілкарбоніл окси, і де арил являє собою феніл або заміщений феніл з одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, галогену, трифторметилу, нітро, трифторметокси, гідрокси й ціано, і солей цих сполук. В іншому варіанті здійснення даний винахід стосується сполук формули 1b, у якій R1 являє собою водень, С1-4-алкіл, C3-7циклoалкiл, C3-7-циклoалкiл-C1-4-aлкiл, С1-4алкокси, С1-4-aлкoкcи-С 1-4-алкiл, С1-4алкоксикарбоніл, С2-4-алкеніл, С2-4-алкініл, фтopС1-4-алкiл або гідрокси-С 1-4-алкіл, R2 являє собою водень, С1-4-алкіл, арил, C3-7циклоалкіл, C3-7-циклоалкіл-С 1-4-алкіл, С1-4алкoкcикapбoнiл, моно- або ди-С1-4-алкіламіноС 1-4алкiлкapбoнiл, гiдpoкcи-С1-4-алкiл або фтop-C2-4алкiл, R3 являє собою водень, галоген, фтор-С1-4алкіл, карбоксил, -CO-С1-4-алкокси, гідрокси-С 1-4алкіл, С1-4-алкокси-С 1-4-алкіл, С1-4-алкокси-С 1-4алкoкcи-С 1-4-алкіл, фтop-С1-4-aлкoкcи-С 1-4-алкiл або групу-CO-NR31R32, де 28 R31 являє собою водень, гідроксил, С1-7-алкiл, гідрокси-С 1-4-алкіл або С1-4-алкoкcи С 1-4-алкіл й R32 являє собою водень, С1-7-алкіл, гідроксиС1-4-алкіл або С1-4-алкокси-С 1-4-алкiл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обоє зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4-алкілпіперазино або мopфoлiнoгрупу, R4 являє собою водень, С1-4-алкіл, гідрокси-С 1С1-4-алкoкcи, С2-4-алкенілокси, С1-44-алкіл, алкілкарбоніл, карбокси, С1-4-алкоксикарбоніл, карбокси-С 1-4-алкiл, С1-4-алкоксикарбоніл-С 1-4алкіл, галoгeн, гідрокси, арил, арил-С1-4-алкiл, арилокси, арил-С1-4-алкокси, трифторметил, нітро, аміно, моноабо ди-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкoкcикapбoнiлaмiнo, С14-алкoкcи- С 1-4-алкoкcикapбoнiлaмiнo або сульфоніл, R5 являє собою водень, С1-4-алкіл, С1-4алкокси, С1-4-алкоксикарбоніл, галoгeн, трифторметил або гідрокси, X являє собою О (кисень) або NH й Ζ має значення -CHR8- або -CHR8-CHR9-, де R8 являє собою водень, С1-7-алкiл, C2-7алкеніл, гідроксил, С1-4-алкoкcи, оксо-заміщений С1-4-алкокси, C3-7-циклоалкокси, C3-7-циклoалкiл-С 14-алкoкcи, гідрокси-С 1-4-алкокси, С 1-4-алкокси-С 1-4алкокси, С1-4-алкокси-С 1-4-алкокси-С 1-4-алкокси, C3C3-7-циклоалкіл-С 1-47-циклоалкокси-С 1-4-алкокси, алкoкcи-С 1-4-алкoкcи, С1-4-алкілкарбонілокси, галоген-С 1-4-алкокси, аміно, моно- або ди-С1-4алкілкарбоніламіно, С1-4-алкiлкapбoнiлaмiнo, С1-4алкоксикарбоніламіно, моноабо ди-С1-4алкіламіно-С1-4-алкiлкapбoнiлoкcи або С 1-4алкoкcи-С 1-4-алкoкcикapбoнiлaмiнo, R9 являє собою водень, С1-7-алкiл, C2-7алкеніл, гідроксил, С1-4-алкoкcи, оксо-заміщений С1-4-алкокси, C3-7-циклоалкокси, C3-7-циклоалкіл-С 14-алкокси, гідрокси-С 1-4-алкокси, С 1-4-алкокси- С 1-4алкокси, С1-4-алкокси-С 1-4-алкокси-С 1-4-алкокси, C3C3-7-циклоалкіл-С 1-47-циклoалкoкcи-С 1-4-алкокси, алкoкcи-С 1-4-алкокси, С1-4-алкілкарбонілокси, галоген-С 1-4-алкокси, аміно, моно- або ди-С1-4алкіламіно, С1-4-алкiлкapбoнiлaмiнo, С1-4алкoкcикapбoнiлaмiнo, моноабо ди-С1-4алкіламіно-С1-4-алкілкарбонілокси або С 1-4алкокси-С 1-4-алкілкарбоніламіно і де арил являє собою феніл або заміщений феніл з одним, двома або трьома однаковими або різними замісниками із групи С1-4-алкілу, С1-4-алкокси, карбокси, С1-4-алкоксикарбонілу, галoгeну, трифторметилу, нітро, трифторметокси, гідрокси й ціано, і солей цих сполук. Сполуки формули 1b мають аж до трьох xipальниx центрів у своїй структурі. Даний винахід таким чином стосується всіх можливих стереоізомерів у будь-якому співвідношенні суміші один до одного, включаючи чисті енантіомери, які є переважними об'єктами винаходу. Серед сполук формули 1а переважними сполуками є сполуки формули 1a-1: 29 79843 у якій R1 являє собою водень, С1-4-алкiл, C3-7циклоалкіл, гiдpoкcи-С1-4-алкiл або С1-4-алкокси-С 14-алкіл, R2 являє собою водень, С1-4-алкіл, гідрокси, С1-4-алкокси або арил-С1-4-алкокси-С 1-4-алкіл, R3 являє собою карбоксил, -СО-С1-4-алкокси, гідрокси-С 1-4-алкіл, С1-4-алкoкcи-С 1-4-aлкiл, ціано, груп у -CO-NR31R32, групу SO2-NR31R32 або групу Het, де R31 являє собою водень, С1-7-алкіл, гідроксиС1-4-алкіл, С1-4-алкокси-С 1-4-алкіл, C3-7-циклoалкiл або аміно й R32 являє собою водень або С1-7-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обоє зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4алкілпіперазино, морфоліно, азиридино або aзeтидинoгрупу й Het являє собою гетероциклічний залишок, заміщений R33, R34 й R35, вибраний із групи, яка складається з оксадіазолу, дигідрооксазолу й дигідроімідазолу, де R33 являє собою водень або С1-4-алкіл, R34 являє собою водень або С1-4-алкіл, R35 являє собою водень або С1-4-алкіл, R4 являє собою водень, С1-4-алкiл, гідрокси-С 14-алкіл, С 1-4-алкoкcи, С 1-4-алкоксикарбоніл, трифторметил, аміно, моно- або ди-С1-4-алкіламіно, С1-4-алкілкарбоніламіно, С1-4-алкоксикарбоніламіно або С1-4-алкoкcи-С 1-4-алкілкарбоніламіно, R5 являє собою водень, С1-4-алкiл або С 1-4алкокси й X являє собою О (кисень) або NH, і солі цих сполук. Серед сполук формули 1а особливо переважними сполуками є сполуки формули 1а-1, де R1 являє собою водень, С1-4-алкiл або гідрокси-С1-4-алкіл, R2 являє собою водень або С1-4-алкiл, R3 являє собою карбоксил, -СО-С1-4-алкокси, гідрокси-С 1-4-алкіл, С1-4-алкокси-С 1-4-алкіл або групу -CO-NR31R32, де R31 являє собою водень, С1-7-алкіл, гiдpoкcиС1-4-алкiл, С1-4-алкокси-С 1-4-алкіл або C3-7циклоалкіл й R32 являє собою водень або С1-7-алкiл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обоє зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4алкілпіперазино, морфоліно, азиридино або 30 aзeтидинoгрупу, R4 являє собою водень, С1-4-алкіл, гідрокси-С 14-алкіл, С 1-4-алкокси, С 1-4-алкоксикарбоніл, трифторметил, аміно, моно- або ди-С1-4-алкіламіно, С1-4-алкiлкapбoнiлaмiнo, С1-4-алкoкcикapбoнiлaмiнo або С1-4-алкокси-С 1-4-алкoкcикapбoнiлaмiнo, R5 являє собою водень, С1-4-алкiл або С 1-4алкокси й X являє собою О (кисень) або NH, і солі цих сполук. Особливо переважними сполуками формули 1а-1 є сполуки, у яких R1 являє собою С 1-4-алкiл, R2 являє собою С 1-4-алкiл, R3 являє собою карбоксил, -СО-С1-4-алкокси, С1-4-алкокси-С 1-4-алкіл або групу -CO-NR31R32, де R31 являє собою водень, С1-4-алкіл, гідроксиС1-4-алкіл, С1-4-алкoкcи-С 1-4-aлкiл або C3-7циклoалкiл й R32 являє собою водень або С1-4-алкiл, R4 являє собою С1-4-алкіл або С 1-4алкілкарбоніламіно, R5 являє собою С1-4-алкіл, X являє собою О (кисень) або NH, і їх солі. Серед сполук формули 1Ь, сполуки формули 1b-1 є переважними. Переважними сполуками формули lb-1 є сполуки, у яких R1 являє собою С 1-4-алкіл або C3-7-циклоалкіл, R2 являє собою водень або С1-4-алкіл, R3 являє собою карбоксил, -СО-С1-4-алкокси, С1-4-алкокси-С 1-4-алкіл, С1-4-aлкoкcи-С 1-4-алкoкcиС1-4-aлкiл або групу -CO-NR31R32, де R31 являє собою водень, С1-7-алкiл, гiдpoкcиС1-4-алкiл, С1-4-алкoкcи-С 1-4-aлкiл або C3-7циклоалкіл й R32 являє собою водень, С1-7-алкіл, гідроксиС1-4-алкіл або С1-4-алкoкcи-С 1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обоє зв'язані, являють собою піролідино, піперидино, піперазино, N-С1-4алкілпіперазино, морфоліно, азиридино або aзeтидинoгрупу, R4 являє собою водень, С1-4-алкіл, С1-4алкокси або галоген, R5 являє собою водень або С1-4-алкіл, R8 являє собою гідроксил, С1-4-алкoкcи, оксозаміщений С1-4-алкокси, C3-7-циклоалкокси, C3-7циклоалкіл-С 1-4-алкокси, гiдpoкcи-С 1-4-алкiл, С1-4алкoкcи-С 1-4-алкoкcи, С1-4-aлкoкcи-С 1-4-алкoкcи-С 1C3-7-циклоалкокси-С 1-4-алкoкcи, C3-74-aлкoкcи, 31 79843 циклоалкіл-С 1-4-алкокси-С 1-4-алкoкcи, С1-4алкілкарбонілокси, гaлoгeн-C1-4-алкoкcи, аміно, моноабо ди-С1-4-алкiлaмiнo, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, моноабо ди-С1-4-алкiлaмінo-С1-4алкiлкapбoнiлoкcи, С1-4-алкокси-С 1-4алкoкcикapбoнiлaмiнo або С1-4-aлкoкcи-С 1-4алкiлкapбoнiлoкcи, X являє собою О (кисень) або NH, і їх солі. Особливо переважними сполуками формули 1b-1 є сполуки, у яких R1 являє собою С 1-4-алкiл, R2 являє собою водень або С1-4-алкіл, R3 являє собою карбоксил, -CO-С1-4-алкoкcи, С1-4-алкокси-С 1-4-алкіл, С1-4-алкокси-С 1-4-алкоксиС1-4-алкіл або групу -CO-NR31R32, де R31 являє собою водень, С1-7-алкіл, гiдpoкcиС1-4-алкiл, С1-4-алкокси-С 1-4-алкіл або C3-7циклоалкіл й R32 являє собою водень, С1-7-алкіл, гідроксиС1-4-алкіл або С1-4-алкокси-С 1-4-алкiл, або де R31 й R32 разом, включаючи атом азоту, з яким вони обоє зв'язані, являють собою пірол ідино, піперидино, піперазино, N-С1-4алкiлпiпepaзинo, морфоліно, азиридино або aзeтидинoгрупу, R4 являє собою водень, С1-4-алкіл, С1-4алкокси або галoгeн, R5 являє собою водень або алкiл, R8 являє собою гідроксил, С1-4-алкoкcи, оксозаміщений С1-4-алкокси, C3-7-циклоалкокси, C3-7циклoaлкiл-С1-4-алкoкcи, гідрокси-С 1-4-алкокси, С1С1-4-алкoкcи-С 1-4-aлкoкcи4-алкокси-С 1-4-алкокси, С1-4-aлкoкcи, C3-7-циклоалкокси-С 1-4-алкокси, C3-7циклоалкіл-С 1-4-алкокси-С 1-4-алкокси, С1-4алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моноабо ди-С1-4-алкiлaмiнo, С1-4алкілкарбоніламіно, С1-4-алкоксикарбоніламіно, моноабо ди-С1-4-алкіламіно-С 1-4алкілкарбонілокси, С1-4-алкокси-С 1-4алкоксикарбоніламіно або С1-4-алкокси-С 1-4алкілкарбонілокси, X являє собою О (кисень) або NH, і їх солі. Особливо переважними сполуками формули 1b-1 є сполуки, у яких R1 являє собою С 1-4-алкiл, R2 являє собою водень або С1-4-алкіл, R3 являє собою карбоксил, -CO-С1-4-алкoкcи, С1-4-алкoкcи-С 1-4-aлкiл, С1-4-алкoкcи-С 1-4-алкoкcиС1-4-алкiл або групу -CO-NR31R32, де R31 являє собою водень, С1-7-алкіл, гiдpoкcиС1-4-алкiл, С1-4-алкокси-С 1-4-алкіл або C3-7циклоалкіл й R32 являє собою водень, С1-7-алкіл, гiдpoкcиС1-4-алкiл або С1-4-алкокси-С 1-4-алкіл, або де R31 й R32 разом, включаючи атом азоту, з 32 яким вони обоє зв'язані, являють собою піролідино, піперидино, піперазино N-С1-4-алкiлпіпepaзинo, морфоліно, азиридино або aзeтидинoгрупу, R4 являє собою водень, С1-4-алкіл, С1-4алкoкcи або галоген, R5 являє собою водень, R8 являє собою гідроксил, С1-4-алкoкcи, оксозаміщений С1-4-алкoкcи, C3-7-циклоалкокси, C3-7циклoалкiл-С 1-4-aлкoкcи, гідрокси-С 1-4-алкокси, С14-алкокси-С 1-4-алкокси, С 1-4-aлкoкcи- С 1-4-aлкoкcиС1-4-алкoкcи, C3-7-циклоалкокси-С 1-4-алкoкcи, C3-7циклоалкіл-С 1-4-алкокси-С 1-4-алкокси, С1-4алкілкарбонілокси, галоген-С1-4-алкокси, аміно, моноабо ди-С1-4-алкіламіно, С1-4алкілкарбоніламіно, С1-4-алкілкарбоніламіно, моноабо ди-С1-4-алкіл аміно-С 1-4-алкілкарбонілокси, С1або С 1-44-алкoкcи-С 1-4-алкоксикарбоніламіно алкокси-С 1-4-алкілкарбонілокси, X являє собою О (кисень) або NH, і їх солі. Переважними сполуками є сполуки формули 1а-1. Особливо переважними є сполуки, представлені як кінцеві продукти формули 1 у прикладах, і солі цих сполук. Сполуки відповідно до винаходу можуть бути отримані з відповідних вихідних сполук, наприклад відповідно до наведених нижче схем реакцій. Синтез здійснюють відомим для фахівця способом, наприклад як описано більш докладно в наступних прикладах. Вихідні сполуки є відомими, наприклад з [М. W. Lovell, S. G. Schulman, Anal. Chem. 1983, 55, 963-965] (наприклад, 4-бром-6-нітро-1,2фенілендіамін). 6-галоген, 4-нітро-заміщені бензимідазоли відомі з рівня техніки, наприклад, 6-хлор2-метил-4-нітро-1(3) H-бензимідазол [Gillespie й ін., J. Org. Chem. 1960, 25, 942] або вони можуть бути отримані aналoгiчними стадіями реакцій. 1,2Епоксііндан описаний, наприклад, в [W. F. Whitmore; A. I. Gebhart, J. Am. Chem. Soc. 1942, 64, 912]. Звичайно, заміщені алкіл-, алкокси- або галогенепоксііндани можуть бути отримані з відповідних заміщених інденів способами, відомими з рівня техніки (наприклад, епоксидуванням). Сполуки загальної формули 1а можуть бути отримані реакцією заміщених бензимідазолів формули І із сполуками формули II, як представлено на схемі 1. Схема 1: Aналoгiчнo, сполуки загальної формули lb одержують реакцією заміщених бензимідазолів формули І з епоксіінданами III, вводячи будь-який потрібний замісник R4 й R5 (схема 2 для сполуки 1b-1). 33 79843 Схема 2: Представлені вище реакційні стадії здійснюють відомим способом, наприклад, як описано більш докладно в прикладах. Введення радикалів, при необхідності, у сполуки, отримані відповідно до наведеної вище схеми 1 й 2 (наприклад, конверсія групи R3 в іншу гр упу R3, або R2 = Η в іншу груп у R2, або конверсія гідроксильної групи в алкокси або ефірну груп у) аналогічно здійснюється відомим способом. Якщо потрібно одержати сполуки, у яких R3 = -СО-С1-4-алкокси або R3 = -CONR31R32, відомим способом може здійснюватися підходяще введення радикалів (наприклад, каталізованим мeталoм карбонілюванням відповідної бромсполуки або конверсією ефіру в амід) на стадії бензимідазолів фopмули І (схема 1 й 2) або зручніше на кінцевій стадії. Наступні приклади служать для більш докладної ілюстрації винаходу без його обмеження. Аналогічно, інші сполуки формули 1, одержання яких не було конкретно описане, можуть бути отримані аналогічним способом або способом, близьким до звичайних способів, відомих фа хівцеві в даній галузі техніки. Скорочення хв означає хвилину(хвилини), год - година(години) і tпл - температура плавлення. Приклади І. Ви хідні реагенти А. 2-бензилокси-4-бром-6-нітро-анілін До суспензії 50г (325ммоль) 2-аміно-3нітрофенолу, 45г (325ммоль) карбонату калію й 2г (13ммоль) йодиду натрію в 400мл етанолу додавали 47мл (408ммоль) бензилхлориду й суміш нагрівали до 80°С. Через 2 год peaкцiйну суміш oxoлoджyвали й розчинник yпapювали. Залишок розчиняли в етилацетаті й eкcтpaгyвали водою. Органічний шар висушували над безводним сульфатом магнію й yпapювали. Спільне упарювання з дихлорметаном приводило до одержання темнокоричневого маслянистого залишку, який розчиняли в 400мл ацетонітрилу. Після додавання 63,4г (356ммоль) N-бромсукциніміду реакційну суміш кип'ятили зі зворотним холодильником протягом 1год. Після охолодження додавали 400г силікагелю й суміш упарювали досуха. Oтpимaну тверду peчoвину очищали колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші етилацетат:низькокиплячий петролейний ефір (4:1). Упарювання елюенту приводило до одержання твердої речовини, яку перекристалізовували із суміші етилацетат/н-гептан з одержанням 62г (59%) вказаної в заголовку сполуки у вигляді червоної твердої речовини (tпл 90°С). Б. N-Ацетил-N-(2-бензилокси-4-бром-6-нітрофеніл)-ацетамід Суспензію 20г (62ммоль) 2-бензилокси-4 бром6-нітро-аніліну в 120мл оцтового ангідриду й 2мл 34 метансульфонової кислоти назвали до 120°С. Після закінчення реакції (15хв) надлишок оцтового ангідриду упарювали. Залишок розчиняли в суміші дихлорметан/вода й нейтралізували 6N водним гідроксидом натрію. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Кристалізація залишку із суміші етилацетат/н-гептан приводила до одержання 23,2г (92%) вказаної в заголовку сполуки у вигляді бежевої твердої речовини (tпл 148°C). В. N-(2-аміно-6-бензилокси-4-бром-феніл)ацетамід Суспензію 23г (56ммоль) N-ацетил-N-(2бензилокси-4-бром-6-нітро-феніл)-ацетаміду, 5,5г (34ммоль) хлориду заліза(III) і 13,8г активованого вугілля в 600мл метанолу нагрівали при кипінні зі зворотним холодильником. До реакційної суміші додавали 28мл гідразингідрату (95%), продовжуючи кип'ятіння. Після закінчення реакції (2год) суміш охолоджували й вiдфiльтpoвyвали через целіт. Залишок на фільтрі ретельно промивали сумішшю дихлорметан/метанол і фільтрат упарювали досуха. Залишок розділяли між сумішшю ди хлорметан/метанол і водою. Органічний шар промивали насиченим розчином хлориду натрію, сушили над безводним сульфатом магнію й упарювали. Залишок перекристалізовували з киплячої суміші етилацетат/н-гептан з одержанням 12,3г (65%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 185°C). Г. N-(2-бензилокси-4-бром-6-диметиламінофеніл)-ацетамід Суспензію 5,0г (15ммоль) N-(2-аміно-6бензилокси-4-бром-феніл)-ацетаміду в 80мл метанолу й 34мл формальдегіду (37%) підкисляли насиченою метанольною соляною кислотою з одержанням прозорого жовтого розчину. До розчину додавали 1,5г (24ммоль) ціаноборгідриду натрію невеликими частинами. Після закінчення реакції (15хв) суміш нейтралізували водним гідрокарбонатом натрію й екстрагували дихлорметаном. Органічний шар висушу вади над безводним сульфатом магнію й упарювали. Кристалізація залишку із суміші етилацетат/н-гептан приводила до одержання 4,3г (79%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 177°C). Д. 4-бензилокси-6-бром-1,2-диметил-1Hбензимідазол Суспензію 26,2г (72ммоль) N-(2-бензилокси-4бром-6-диметиламіно-феніл)-ацетаміду в 180мл фосфорилхлориду назвали при 70°С протягом 24год. Після закінчення реакції надлишок фосфорилхлориду упарювали. Залишок суспендували в дихлорметані й обережно нейтралізували 6N водним гідроксидом калію й водою. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й yпapювали. Кристалізація залишку з етилацетату приводила до одержання 15,1г (63%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 177-179°C). Е. Етил 4-гідрокси-1,2-диметил-1Hбензимідазол-6-карбоксилат Суспензію 12,0г (37ммоль) етил 4-бензилокси1,2-диметил-1H-бензимідазол-6-карбоксилату в 100мл етанолу гiдpyвали над 1г 10% Pd/C (50°С, 35 79843 5бар Н2) протягом 16год. Каталізатор відфільтровували й фільтрат yпapювали. Залишок кристалізували із суміші етанол/діетиловий ефір з одержанням 5,91г (69%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 272273°C). Ж. Метил-4-гідрокси-1,2-диметил-1Нбензимідазол-6-карбоксилат Суспензію 8,5г (27ммоль) метил-4-бензилокси1,2-диметил-1Н-бензимідазол-6-карбоксилату в 100мл метанолу гідрували над 0,7г 10% Pd/C (30°С, 1бар Н2) протягом 2год. Каталізатор відфільтровували, промивали кілька разів гарячим метанолом і фільтрат yпapювали. Залишок кpиcтaлiзyвали із суміші метанол/діетиловий ефір з одержанням 6г (99%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 286°C). З. 4-гідрокси-6-метоксиметил-1,2-диметил-1Нбензимідазол Розчин 1,2г (4,1ммоль) 4-бензилокси-6метоксиметил-1,2-диметил-1Н-бензимідазолу в 12мл метанолу гідрували над 0,12г 10% Pd/C (1бар Н2) протягом 16год. Каталізатор відфільтровували й фільтрат упарювали. Залишок кpиcтaлiзyвали із суміші етилацетат/низькокиплячий петролейний ефір з одержанням 0,83г (99%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 219220°C). И. 6-(N,N-Диметиламінокарбоніл)-4-гідрокси1,2-диметил-1H-бензимідазол Розчин 2,3г (7,1ммоль) 4-бензилокси-6-(N,Nдиметиламінокарбоніл)-1,2-диметил-1Hбензимідазолу в 80мл метанолу гідрували над 0,3г 10% Pd/C (1бар Н2) протягом 16год. Каталізатор відфільтровували й фільтрат упарювали. Залишок кристалізували з aцeтoну з одержанням 1,2г (71%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 248°C). К. 6-бром-2-метил-4-нітро-1(3)H-бензимідазол До суспензії 65г (0,28моль) 5-бром-3-нітро-1,2фенілендіаміну в 600мл етанолу додавали 140мл 5Ν соляної кислоти. Реакційну суміш кип'ятили зі зворотним холодильником й однією порцією додавали 58мл (0,56моль) 2,4-пентандіону. Через 1год суміш oxoлoджyвали, виливали в 500мл води й нейтралізували концентрованим аміаком. Осад збирали, промивали ретельно водою й сушили над пентоксидом фосфору з одержанням 70,8г (99%) вказаної в заголовку сполуки (tпл 229-231°С). Л. 6-бром-4-нітро-1(3)Н-бензимідазол До суспензії 14,25г (61,4ммоль) 5-бром-3нітро-1,2-фенілендіаміну в 120мл 4N соляної кислоти додавали 4,65мл (123ммоль) мурашиної кислоти. Реакційну суміш назвали до 120°С. Через 1,5год суміш oxoлoджyвали й нейтралізували концентрованим аміаком. Осад збирали, промивали водою й сушили над пентоксидом фосфору. Перекристалізація з етанолу з активованим вугіллям приводила до одержання 9,79г (66%) вказаної в заголовку сполуки (tпл 249°С). М. 6-бром-2-метоксиметил-4-нітро-1(3)Нбензимідазол Суспензію 1г (4,3ммоль) 5-бром-3-нітро-1,2 36 фенілендіаміну в 4мл метоксиоцтової кислоти назвали при 110°С протягом 16год. Суміш виливали в льодяну воду, нейтралізували 6N водним гідроксидом натрію й екстрагували дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й yпapювали. Очищення залишку кристалізацією з етилацетату з активованим вугіллям приводило до одержання 0,9г (73%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 173°С). Η. 6-бром-1-метил-4-нітро-1Н-бензимідазол Суспензію 5,12г (21,2ммоль) 6-бром-4-нітро1(3)Н-бензимідазолу й 4,6г (33,3ммоль) карбонату калію в 200мл ацетону перемішували протягом 30хв і потім додавали 1,54мл (24,7ммоль) метилйодиду. Після перемішування протягом 18год при температурі навколишнього середовища, надлишок розчинника упарювали й залишок розділяли між дихлорметаном і водою. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й yпapювали. Очищення задишку кристалізацією з етилацетату приводило до одержання 2,7г (50%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 198°C). О. 6-бром-2-метоксиметил-1-метил-4-нітро-1Нбензимідазол До суспензії 13г (45,4ммоль) 6-бром-2метоксиметил-4-нітро-1(3)Н-бензимідазолу й 12,6г (90,9ммоль) карбонату калію в 130мл ацетону додавали 6,8г (47,7ммоль) метилйодиду й суміш перемішували протягом 18год при температурі навколишнього середовища. Дрібну суспензію виливали в 200мл води й екстрагували дихлорметаном. Органічний шар висушували над безводним сульфатом магнію й yпapювали. Очищення задишку кристалізацією з діізопропілового ефіру приводили до одержання 13,6г (99%) вказаної в заголовку сполуки у вигляді жовтої твердої речовини (tпл 145-147°C). П. 1-бензилоксиметил-6-бром-2-метил-4-нітро1Н-бензимідазол До суспензії 0,26г (6,4ммоль) гідриду натрію (60% дисперсія в мінеральному маслі) в 10мл Ν,Νдиметилформаміду повільно додавали розчин 1,5г (5,9ммоль) 6-бром-2-метил-4-нітро-1(3)Нбензимідазолу в 5мл Ν,Ν-диметилформаміду при 0°С. Через 1год при 0°С додавади 2,29г (8,8ммоль) бензилоксиметилхлориду (60%) протягом 20хв. Після закінчення реакції (1год) обережно додавали 10мл води й суміш розділяли між дихлорметаном і водою. Органічний шар висушували над безводним сульфатом магнію й упарювали. Очищення залишку колонковою хроматографією на силікагелі за допомогою суміші етилацетат:триетиламін (95:5) приводили до одержання масла, яке кристалізували з діізопропілового ефіру з одержанням 1,16г (53%) вказаної в заголовку сполуки у вигляді жовтої твердої речовини (tпл 106109°С). Р. 6-бром-1,2-диметил-4-нітро-1Нбензимідазол До суспензії 4,3г (107ммоль) гідриду натрію (60% дисперсія в мінеральному маслі) в 25мл Ν,Νдиметилформаміду повільно додавали розчин 25г (98ммоль) 6-бром-2-метил-4-нітро-1(3)Н 37 79843 бензимідазолу в 100мл Ν,Ν-диметилформаміду при 0°С. Через 30хв при 0°С додавали 15,2г (107ммоль) метилйодиду протягом 20хв. Після закінчення реакції (45хв) обережно додавали 200мл води й суміш пepeмiшyвали 1год при температурі навколишнього середовища. Осад збирали, промивали ретельно водою й сушили над пентоксидом фосфору. Перекристалізація з метанолу приводила до одержання 19,6г (74%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 193-195°С). С. 4-аміно-6-бром-1-метил-1Н-бензимідазол До суспензії 10г (39ммоль) 6-бром-1-метил-4нітро-1Н-бензимідазолу в 100мл метанолу додавали 7,6г (46,9ммоль) хлориду заліза(ІІІ) і 2,5г активованого вугілля. Реакційну суміш назвали до 80°С і повільно додавали 9,5мл гідразингідрату (95%). Після кип'ятіння протягом 2год додавали нacтyпну кількість 2мл гідразингідрату (95%). Через 5год гарячу peaкцiйну суміш відфільтровували через целіт і залишок на фільтрі промивали метанолом і дихлорметаном. Фільтрат yпapювали до одержання твердої речовини, яку очищали колонковою хроматографією на силікагелі за допомогою суміші толуол:діоксан:метанол (6:3,6:0,4). Кристалізація з діізопропілового ефіру приводила до одержання 6,8г (77%) вказаної в заголовку сполуки у вигляді ясно-жовтої твердої речовини (tпл 170°C). Т. 4-аміно-6-бром-2-метоксиметил-1-метил1Н-бензимідазол До суспензії 8,5г (28,3ммоль) 6-бром-2метоксиметил-1-метил-4-нітро-1Н-бензимідазолу в 150мл метанолу додавали 5,51г (34ммоль) хлориду заліза(ІІІ), 2,5г активованого вугілля й 6,9мл гідразингідрату (95%). Після кип'ятіння протягом 2год додавали нacтyпну кількість 4мл гідразингідрату (95%). Через 4год гарячу peaкцiйну суміш відфільтровували через целіт і залишок на фільтрі промивали метанолом і дихлорметаном. Фільтрат упарювали й залишок очищали колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (20:1). Кристалізація з діізопропілового ефіру приводила до одержання 5,5г (72%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 138-140°C). У. 4-аміно-1-бензилоксиметил-6-бром-2метил-1Н-бензимідазол До суспензії 10г (26,6ммоль) 1бензилоксиметил-6-бром-2-метил-4-нітро-1Нбензимідазолу й 1г активованого вугілля в 150мл метанолу дoдaвали 5,2г (31,9ммоль) хлорид заліза(ІІІ) і 6,5мл гідразингідрату (95%). Після кип'ятіння протягом 1год додавали нacтyпну кількість 3мл гідразингідрату (95%). Через 6год гарячу peaкцiйну суміш відфільтровували через целіт і залишок на фільтрі промивали гарячим метанолом. Фільтрат упарювали до одержання жовтої твердої речовини, яку очищай колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (9:1). Кристалізація з діізопропілового ефіру приводила до одержання 6,68г (73%) вказаної в заголовку сполуки у вигляді ясно-жовтої твердої речовини (tпл 142°C). Ф. 4-аміно-6-бром-1,2-диметил-1Нбензимідазол 38 До розчину 19г (70ммоль) 6-бром-1,2-диметил4-нітро-1Н-бензимідазолу в 250мл метанолу додавали 13,7г (84ммоль) хлориду заліза(ІІІ) і 6г активованого вугілля. Peaкцiйну суміш назвали до 80°С і повільно додавали 17мл гідразингідрату (95%). Після кип'ятіння протягом 3год гарячу peaкцiйну суміш відфільтровували через целіт і залишок на фільтрі промивали метанолом і дихлорметаном. Фільтрат упарювали до одержання суспензії, що обробляли н-гептаном. Осад збирали, промивали н-гептаном і сушили з одержанням 13,3г (79%) вказаної в заголовку сполуки у вигляді твердої речовини (tпл 206-209°C). X. 6-бром-4-(2-етил-6-метил-бензиламіно)-1,2диметил-1Н-бензимідазол До суспензії 12г (50ммоль) 4-аміно-6-бром-1,2диметил-1Н-бензимідазолу й 8,8г (52ммоль) 2етил-6-метил-бензилхлориду в 220мл ацетону додавали 5,5г (52ммоль) карбонату натрію й 1,5г (10ммоль) йодиду натрію. Через 3год перемішування при 45°С реакційну суміш виливали в 400мл води й естрагували етилацетатом. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й yпapювали. Очищення залишку колонковою хроматографією на силікагелі за допомогою суміші дихлорметан:метанол (100:3) і кристалізація з н-гептану приводило до одержання 15,6г (84%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 145-147°C). Ц. 6-бром-4-(2,6-диметил-бензиламіно)-1,2диметил-1Н-бензимідазол До суспензії 0,97г (4ммоль) 4-аміно-6-бром1,2-диметил-1Н-бензимідазолу й 0,66г (4,2ммоль) 2,6-диметил-бензилхлориду в 25мл ацетонітрилу додаввли 0,56г (4ммоль) карбонату калію й 70мг (0,4ммоль) йодиду калiю. Через 1год перемішування при 65°С дoдaвали 2мл 1N водного аміаку й peaкцiйну суміш упарювали. Залишок розділяли між дихлорметаном і водою. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші етилацетат:низькокиплячий петролейний ефір (1:1) і кристалізація із суміші етилацетат/нгептан приводили до одержання 0,93г (64%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 185°С). Ч. 1-бензил оксиметил-6-бром-4-(2-етил-6метил-бензиламіно)-2-метил-1H-бензимідазол До суспензії 6,5г (18,8ммоль) 4-аміно-1бензилоксиметил-6-бром-2-метил-1Hбензимідазолу й 3,32г (19,7ммоль) 2-етил-6-метилбензилхлориду в 120мл ацетонітрилу додавали 3,0г (28,2ммоль) карбонату натрію й 0,56г (3,75ммоль) йодиду натрію. Після год кип'я тіння peaкцiйну суміш виливали в 300мл води й екстрагували дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Очищення задишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші етилацетат:низькокиплячий петролейний ефір (2:3) і кристалізація з діізопропілового ефіру приводили до одержання 6,88г (77%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 117-119°С). 39 79843 Ш. 6-бром-4-(2-етил-6-метил-бензиламіно)-1метил-1Н-бензимідазол До суспензії 2,0г (8,9ммоль) 4-аміно-6-бром-1метил-1Н-бензимідазолу й 1,6г (9,5ммоль) 2-етил6-метил-бензилхлориду в 40мл ацетонітрилу додавали 1,4г (13,1ммоль) карбонату натрію й 0,3г (2ммоль) йодиду натрію. Через 1год при 70°С суміш розділяли між дихлорметаном і водою. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й yпapювали. Очищення задишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (100:1) приводило до одержання 2,0г (63%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 132-134°С). Щ. 6-бром-4-(2-етил-6-метил-бензиламіно)-2метоксиметил-1-метил-1Н-бензимідазол До суспензії 6,8г (25,2ммоль) 4-аміно-6-бром2-метоксиметил-1-метил-1Н-бензимідазолу й 4,46г (26,4ммоль) 2-етил-6-метил-бензилхлориду в 70мл ацетонітрилу додавали 7,0г (50,3ммоль) карбонату калію й кaталiтичну кількість йодиду калію. Через 5год при 70°С peaкцiйну суміш виливали в 200мл води й екстрагували дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші етилацетат:низькокиплячий петролейний ефір (1:1) і кристалізація з діізопропілового ефіру приводили до одержання 5,46г (54%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 110-112°С). Ю. 6-бром-4-(2,6-диметил-бензиламіно)-2метоксиметил-1-метил-1Н-бензимідазол До суспензії 2,5г (9,25ммоль) 4-аміно-6-бром2-метоксиметил-1-метил-1Н-бензимідазолу й 1,52г (9,72ммоль) 2,6-диметил-бензилхлориду в 50мл ацетонітрилу дoдaвали 2,56г (18,5ммоль) карбонату калію й кaталiтичну кількість йодиду калію. Через 3год при 70°С реакційну суміш виливали в 150мл води й екстрагували ди хлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (100:1) і кристалізація з діізопропілового ефіру приводили до одержання 0,84г (23%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 143-145°C). Я. 4-аміно-6-(N,N-диметиламінокарбоніл)-1,2диметил-1H-бензимідазол До суспензії 3г (12,5ммоль) 4-аміно-6-бром1,2-диметил-1H-бензимідазолу в 100мл диметиламіну (2Μ розчин у тетрагідрофурані) додавали 280мг (1,25ммоль) ацетату паладію(II) і 2г (7,5ммоль) трифенілфосфіну. Суміш переносили в автоклав і карбонілювали (6бар тиск монооксиду вуглецю, 120°С) протягом 16год. Реакційну суміш охолоджували, виливали в 200мл води й 100мл насиченого водного хлориду амонію й екстрагували дихлорметаном. Органічний шар вiдoкpeмлювали, промивали водою, сушили над безводним сульфатом магнію й yпapювали. Очищення залишку колонковою xpoмaтoгрaфiєю на 40 силікагелі за допомогою суміші етилацетат/метанол (4:1) і кристалізація з діізопропілового ефіру приводили до одержання 0,7г (24%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 230-234°С). АА. (2-бензилокси-4-бром-6-нітро-феніл)-амід циклопропанкарбонової кислоти Суспензію 20,0г (61,9ммоль) 2-бензилокси-4бром-6-нітро-аніліну й 11,2мл (123,4ммоль) циклопропанкарбонілхлориду в 130мл дioкcaну назвали до 100°С. Через 5год колбу зaнуpювали в льoдяну баню, осад збирали, пpoмивали толуолом і сушили у вакуумі з одержанням 21,2г (87%) вказаної в заголовку сполуки у вигляді жовтої твердої речовини (tпл 191°С). ББ. (2-аміно-6-бензилокси-4-бром-феніл)-амід циклопропанкарбонової кислоти Суспензію 11,0г (28,1ммоль) (2-бензилокси-4бром-6-нітро-феніл)-аміду циклопропанкарбонової кислоти, 3,0г (18,5ммоль) хлориду заліза(ІІІ) і 7,4г активовані вугілля в 140мл метанолу назвали до кипіння. До реакційної суміші додавали 14,7мл гідразингідрату (95%), продовжуючи кип'ятіння. Після закінчення реакції (1год) суміш oxoлoджyвали й відфільтровували через целіт. Залишок на фільтрі промивали ретельно гарячою сумішшю метанол/ацетон і фільтрат упарювали досуха. Залишок кристалізували з етилацетату з одержанням 7,5г (73%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 207-208°C). ВВ. 4-бензилокси-6-бром-2-циклопропіл-1метил-1Н-бензимідазол Суспензію 7,5г (20,8ммоль) (2-аміно-6бензилокси-4-бром-феніл)-аміду циклопропанкарбонової кислоти в 80мл метанолу й 13,3мл фopмальдeгiдy (37%) підкисляли насиченою метанольною соляною кислотою з одержанням прозорого жовтого розчину. До розчину додавали 0,75г (11,9ммоль) ціаноборгідриду натрію невеликими порціями. Після закінчення реакції (4год) суміш виливали у воду й нейтралізували 40% водним гідроксидом натрію. Осад збирали, промивали водою й сушили над пентоксидом фосфору з одержанням 5,3г безбарвної твердої речовини. Тверду речовину суспендували в 10мл фосфорилхлориду й суміш назвали при 90°С протягом 2год. Після закінчення реакції суміш розбавляли дихлорметаном і нейтралізували 6N водним гідроксидом калію й водою. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й yпapювали. Очищення задишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші толуол:діоксан (10:1) і кристалізація з діетилового ефіру приводили до одержання 2,97г (40%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 153-154°С). ГГ. Етил 2-циклопропіл-4-гідрокси-1-метил-1Нбензимідазол-6-карбоксилат Суспензію 2,3г (6,6ммоль) етил 4-бензилокси2-циклопропіл-1-метил-1Н-бензимідазол-6карбоксилату в 23мл метанолу гiдpyвали над 0,27г 10% Pd/C (25°С, 1бар Н2) протягом 5год. Каталізатор відфільтровували й фільтрат yпapювали. Залишок кристалізували з етилацетату з одержанням 41 79843 1,5г (88%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 201-202°С). ДД. 4-аміно-N,N-диметил-3,5-динітробензолсульфонамід Суспензію 5,0г (27,3ммоль) 2,6-динітроанілшу в 40мл хлорсульфонової кислоти назвали до 100°С. Через 2,5год peaкцiйну суміш oxoлoджyвали й обережно виливали в 1000мл подрібненого льоду. Суспензію естрагували дихлорметаном. Органічний шар висушували над безводним сульфатом магнію й упарювали досуха. Залишок розчиняли в 100мл тeтpaгiдpoфypaну й повільно додавали розчин 25мл диметиламіну в 25мл тeтpaгiдpoфypaну. Через 20хв суспензію упарювали й залишок розділяли між дихлорметаном і водою. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку кристалізацією з етанолу приводило до одержання 6,7г (85%) вказаної в заголовку сполуки у вигляді жовтогарячої твердої речовини (tпл 169-170°C). ЕЕ. 3,4-діаміно-N,N-диметил-5-нітробензолсульфонамід 50мл 2N водного аміаку насичували сульфідом водню при 0°С. Розчин розбавляли 50мл етанолу й дoдaвали 5,58г (19,2ммоль) 4-аміно-N,Nдиметил-3,5-динітро-бензолсульфонаміду. Через 40хв при 60°С суміш розбавляли водою й відфільтровували через целіт. Залишoк на фільтрі екстрагували кілька разів киплячої дихлорметаном і метанолом. Об'єднані екстракти упарювали й залишок перекристалізували із суміші етанол/діетиловий ефір з одержанням 1,18г (24%) вказаної в заголовку сполуки у вигляді червоної твердої речовини (tпл 211-213°С). ЖЖ. Диметиламід 2-метил-7-нітро-3Hбензимідазол-5-сульфонової кислоти Суспензію 1,0г (3,84ммоль) 3,4-діаміно-N,Nдиметил-5-нітро-бензолсульфонаміду в 20мл етанолу й 5мл 5N соляної кислоти назвали до 80°С. До реакційної суміші додавали 1,6мл (15,4ммоль) 2,4-пeнтaндioну двома порціями протягом 1год. Розчин oxoлoджyвали й нейтралізували 6N водним гідроксидом натрію. Осад збирали, промивали водою й сушили у вакуумі над пентоксидом фосфору з одержанням 0,99г (90%) бежевої твердої речовини (tпл 254-255°С). ЗЗ. Диметиламід 2,3-диметил-7-нітро-3Нбензимідазол-5-сульфонової кислоти Суспензію 1,87г (6,6ммоль) диметиламіду 2метил-7-нітро-3Н-бензимідазол-5-сульфонової кислоти, 1,82г (13,2ммоль) карбонату калію й 0,71мл (11,5ммоль) метилйодиду в 50мл ацетону перемішували протягом 3год при температурі навколишнього середовища. Суміш розділяли між дихлорметаном і насиченим водним хлоридом амонію. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали досуха. Перекристалізація залишку з киплячого етилацетату приводила до одержання 1,5г (76%) вказаної в заголовку сполуки у вигляді бежевої твердої речовини (tпл 194-196°C). ИИ. Диметиламід 7-аміно-2,3-диметил-3Нбензимідазол-5-сульфонової кислоти Суспензію 1,2г (4,0ммоль) диметиламіду 2,3 42 диметил-7-нітро-3Н-бензимідазол-5-сульфонової кислоти в 15мл метанолу й 5мл оцтової кислоти назвали до 60°С і додавали 1,1г (20ммоль) залізних стр ужок. Через 1,5год тверді залишки відфільтровували й eкcтpaгyвали кілька разів киплячим дихлорметаном. Об'єднані екстракти упарювали й залишок кристалізували із суміші етилацетат/нгептан з одержанням 0,99г (92%) вказаної в заголовку сполуки у вигляді бежевої твердої речовини (tпл 255-258°C). КК. N-(4-бром-2,6-динітро-феніл)-ацетамід Суспензію 5,0г (19,1ммоль) 4-бром-2,6динітроаніліну в 50мл оцтового ангідриду й 1мл метансульфонової кислоти перемішували протягом 3год при 30°С. Осад збирали, промивали діетиловим ефіром і сушили з одержанням 4,8г (83%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 238-239°С). ЛЛ. 4-аміно-6-бром-1-гідрокси-2-метил-1Нбензимідазол До суспензії 2,0г (6,6ммоль) N-(4-бром-2,6динітро-феніл)-ацетаміду й 0,4г рутенію на вугіллі (5%) в 80мл етанолу додавали 1,2мл (24,7ммоль) гідразингідрату (95%) протягом 1,5год при 60°С. Каталізатор вiдфiльтpoвyвали й фільтрат упарювали досуха. Залишок екстрагували киплячої етилацетатом з одержанням 1,23г (77%) вказаної в заголовку сполуки у вигляді ясно-сірої твердої речовини (tпл 257-258°C). MM. N-[5-бром-2-(2-хлор-ацетиламіно)-3-нітрофеніл]-2-хлор-ацетамід До розчину 46,4г (200ммоль) 4-бром-2,6динітроаніліну в 500мл Ν,Ν-диметилформаміду й 20мл пipидину повільно додавали 80мл (1000ммоль) хлорацетилхлориду. Через 3год peaкцiйну суміш виливали в 600мл льодяної води й oтpимaну суспензію нейтралізували 6Ν водним гідроксидом натрію. Осад збирали, промивали водою й сушили у вакуумі з одержанням 74,1г (96%) вказаної в заголовку сполуки у вигляді бежевої твердої речовини (tпл 172-173°С). НН. 6-бром-2-хлорметил-4-нітро-1Нбензимідазол Суспензію 1,0г (2,59ммоль) N-[5-бром-2-(2хлор-ацетиламіно)-3-нітро-феніл]-2-хлорацетаміду в 25мл 4N соляної кислоти й 20мл етанолу нагрівали до кипіння. Через 4год peaкцiйну суміш виливали в 75мл води й нейтралізували насиченим водним гідрокарбонатом натрію. Осад збирали, промивали водою й сушили над пентоксидом фосфору з одержанням 0,65г (86%) вказаної в заголовку сполуки у вигляді жовтогарячої твердої речовини (tпл 148-150°C). ОО. 6-бром-2-хлорметил-1-метил-4-нітро-1НЯбензимідазол До розчину 39,3г (135,3ммоль) 6-бром-2хлорметил-4-нітро-1Н-бензимідазолу в 500мл aцeтoну додавали 26,0г (206,1ммоль) диметилсульфату й 50,0г (362ммоль) карбонату калію. Через 1,25год перемішування при кімнатній температурі peaкцiйну суміш виливали в 1000мл води. Осад збирали, промивали водою й пepeкpиcтaлiзyвали з метанолу з одержанням 32,5г (63%) вказаної в заголовку сполуки у вигляді бежевої твердої речовини (tпл 154-155°С). 43 79843 ПП. 2-ацетоксиметил-6-бром-1-метил-4-нітро1Н-бензимідазол До розчину 30,0г (98,5ммоль) 6-бром-2хлорметил-1-метил-4-нітро-1Н-бензимідазолу в 200мл ацетону додавали 16,4г (98,5ммоль) йодиду калію. Oтpимaну суспензію пepeмiшyвали 1год при температурі навколишнього середовища й додавали 14,5г (147,8ммоль) ацетату калію. Через 2год при 40°С peaкцiйну суміш виливали в 500мл води й екстрагували дихлорметаном. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й упарювали досуха. Перекристалізація залишку з киплячого етанолу приводило до одержання 23,9г (74%) вказаної в заголовку сполуки у вигляді жовтогарячої твердої речовини (tпл 143-145°C). PP. 2-ацетоксиметил-4-аміно-6-бром-1-метил1Н-бензимідазол До суспензії 10,0г (30,5ммоль) 2ацетоксиметил-6-бром-1-метил-4-нітро-1Нбензимідазолу в 40мл оцтової кислоти додавали 6,8г (122ммоль) залізних стружок і peaкцiйну суміш нагрівали до 60°С. Через 4год додавали іншу кількість 1,0г (18ммоль) залізних стружок і нагрівання пpoдoвжyвали протягом 1,25год. Осад збирали, розчиняли в дихлорметані й екстрагували водою. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали досуха. Очищення залишку колонковою хроматографією на силікагелі за допомогою суміші етилацетат:низькокиплячий петролейний ефір (7:3) і кристалізація із суміші етилацетат/н-гептан приводили до одержання 4,6г (51%) вказаної в заголовку сполуки у вигляді бежевої твердої речовини (tпл 104106°С). СС. 4-аміно-6-бром-2-гідроксиметил-1-метил1Н-бензимідазол Суспензію 7,5г (22,9ммоль) 2-ацетоксиметил6-бром-1-метил-4-нітро-1Н-бензимідазолу в 180мл метанолу гідрували над нікелем Ренея (25°С, 1бар Н2) протягом 2,5год. Каталізатор відфільтровували й фільтрат розділяли між водою й дихлорметаном. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й упарювали. Залишок кристалізували із суміші етанол/діізопропіловий ефір з одержанням 1,32г (22%) вказаної в заголовку сполуки у вигляді твердої речовини (tпл 216218°C). ТТ. 2,6-дибром-1-метил-4-нітро-1Нбензимідазол До розчину 1,0г (3,9ммоль) 6-бром-1-метил-4нітро-1Н-бензимідазолу в 25мл диxлoпeнтaну дoдaвали 5г силікагелю й 0,94г (5,3ммоль) Nбромсукциніміду. Через 2,5год при 85°С суміш охолоджували й відфільтровували. Фільтрат естрагували насиченим водним гідрокарбонатом натрію, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші етилацетат:низькокиплячий петролейний ефір (1:1) і кристалізація із суміші етилацетат/н-гептан приводили до одержання 0,745г (57%) вказаної в заголовку сполуки у вигляді жовтої твердої речовини (tпл 235-236°С). УУ. 6-бром-2-(N,N-диметиламіно)-1-метил-4 44 нітро-1Н-бензимідазол До розчину 3,0г (11,7ммоль) 6-бром-1-метил-4нітро-1Н-бензимідазолу в 75мл диxлoпeнтaну дoдaвали 25г силікагелю й 2,5г (14,1ммоль) Nбромсукциніміду. Через 3год при 85°С суміш oxoлoджyвали й вiдфiльтpoвyвали. Фільтрат упарювали й залишок розчиняли в 100мл тeтpaгiдpoфypaну. Повільно додавали розчин 10мл диметиламіну в 20мл тeтpaгiдpoфypaну й суміш перемішували протягом 4год. Суміш упарювали до 1/4 від об'єму й розділяли між насиченим водним гідрокарбонатом натрію й дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку кристалізацією з етилацетату приводило до одержання 1,6г (46%) вказаної в заголовку сполуки у вигляді жовтогарячої твердої речовини (tпл 206-207°C). ФФ. 4-аміно-6-бром-2-(N,N-диметиламіно)-1метил-1Н-бензимідазол До суспензії 1,0г (3,3ммоль) 6-бром-2-(N,Nдиметиламіно)-1-метил-4-нітро-1Н-бензимідазолу в 25мл метанолу й 8мл оцтової кислоти дoдaвали 0,85г (15,2ммоль) порошки заліза при 65°С. Через 2год тверді речовини відфільтровували й промивали дихлорметаном. Фільтрат екстрагували водою, сушили над безводним сульфатом магнію й yпapювали. Очищення задишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою етилацетату й кристалізація з діетилового ефіру приводили до одержання 0,2г (22%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 137°C). XX. 6-бром-1,2-диметил-4-(2-метилбензиламіно)-1Н-бензимідазол До розчину 0,9мл (6,4ммоль) 2-метилбензилхлориду в 20мл aцeтoну додавали 1,1г (6,6ммоль) йодиду натрію й суміш перемішували 1,5год при кімнатній температурі. Тверду peчoвину відфільтровували й до фільтрату дoдaвали 1,5г (4,4ммоль) 4-аміно-6-бром-1,2-диметил-1Нбензимідазолу й 1,3г (9,4ммоль) карбонату калію. Через 3год при кип'ятінні зі зворотним холодильником суміш розділяли між водою й дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Очищення задишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (30:1) і кристалізація із суміші етилацетат/н-гептан приводили до одержання 1,28г (61%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 128-129°C). ЦЦ. 6-бром-4-(2,4-диметил-фуран-3-ілметиламіно)-1,2-диметил-1Н-бензимідазол До суспензії 1,95г (4,6ммоль) пepйoдинaну Десс-Мартина в 10мл диxлopмeтaну й 0,5мл піридину по краплях додавали розчин 0,5г (4,0ммоль) (2,4-диметил-фуран-3-іл)-метанолу в 5мл диxлopмeтaну при кімнатній температурі. Через 30хв додавали воду й 1мл насиченого водного сульфіту натрію й суміш eкcтpaгyвали дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Залишoк відфільтровували через силікагель за допомогою суміші етилацетат:низькокиплячий пе 45 79843 тролейний ефір (9:1) з одержанням безбарвного масла після упарювання. Сирий продукт розчиняли в 10мл метанолу й 0,5мл оцтової кислоти. Після додавання 0,48г (2ммоль) 4-аміно-6-бром-1,2диметил-1Н-бензимідазолу додавали 0,3г (4,8ммоль) ціаноборгідриду натрію трьома порціями протягом 2,5год. Через 2год додавали насичений водний гідрокарбонат натрію й суміш екстрагували дихлорметаном. Органічний шар висушували над безводним сульфатом магнію й yпapювали. Очищення залишкy колонковою xpoмaтoгрaфiєю на силікагелі за допомогою етилацетату й кристалізацію із суміші етилацетат/нгептан приводили до одержання 0,45г (65%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 207-208°С). ЧЧ. 6-бром-4-(2-гідроксиметил-6-метилбензиламіно)-1,2-диметил-1Н-бензимідазол До poзчину 0,8г (5,4ммоль) 7-мeтил-3Нiзoбeнзoфypaн-1-oну в 15мл сухого толуолу повільно дoдaвали 4,3мл (6,5ммоль) гідриду диізобутилалюмінію (1,5М розчин у толуолі) при -78°С. Через 1год peaкцiйну суміш гасили 1мл метанолу й нагрівали до кімнатної температури. Суміш розділяли між насиченим водним тартратом калію натрію й дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Отримане масло розчиняли в 20мл метанолу й 1мл оцтової кислоти. Після додавання надлишку ціаноборгідриду натрію суміш перемішували протягом 4год при 45°С. Суміш розділяли між водою й дихлорметаном і нейтралізували 6N водним гідроксидом натрію. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й упарювали. Очи щення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою етилацетату й кристалізація із суміші етилацетат/н-гептан приводили до одержання 0,35г (24%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 215-216°C). ШШ. 6-бром-4-(2-етил-6-метил-бензиламіно)2-гідроксиметил-1-метил-1Н-бензимідазол Суспензію 1,25г (4,88ммоль) 4-аміно-6-бром-2гідроксиметил-1-метил-1Н-бензимідазолу, 0,86г (5,12ммоль) 2-етил-6-метил-бензилхлориду, 1,35г (9,76ммоль) карбонату калію й каталітичної кількості йодиду калію в 15мл ацетонітрилу назвали при 70°С. Через 6год peaкцiйну суміш виливали у воду й екстрагували дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (100:3) і кристалізація з діізопропілового ефіру приводили до одержання 0,54г (29%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 206-208°С). ЩЩ. 6-бром-2-(ЬЩ-диметиламіно)-4-(2,6диметил-бензиламіно)-1 -метил-ІЯ-бензимідазол До розчину 0,46г (1,7ммоль) 4-аміно-6-бром-2(N,N-диметиламіно)-1-метил-1H-бензимідазолу й 0,3г (2,2ммоль) 2,6-диметил-бензальдегіду в 10мл диxлopмeтaну й 2,5мл оцтової кислоти додавали 0,6г (2,8ммоль) триацетоксиборгідриду натрію. Через 1год при температурі навколишнього сере 46 довища додавали насичений водний гідрокарбонат натрію й перемішування пpoдoвжyвали протягом 30хв. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Очищення задишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою етилацетату й кристалізація із суміші етилацетат/нгептан приводили до одержання 0,46г (70%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 157-158°С). ЮЮ. 1-бензил оксиметил-6-бром-4-(2,6диметил-бензиламіно)-2-метил-1H-бензимідазол До суспензії 7,6г (22ммоль) 4-аміно-1бензилоксиметил-6-бром-2-метил-1Hбензимідазолу й 3,56г (23,0ммоль) 2,6-диметилбензилхлориду в 140мл ацетонітрилу дoдaвали 3,5г (32,7ммоль) карбонату натрію й 0,66г (4,4ммоль) йодиду натрію. Через 3,5год кип'ятіння зі зворотним холодильником реакційну суміш розділяли між водою й дихлорметаном. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й yпapювали. Очи щення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші етилацетат:низькокиплячий петролейний ефір (2:3) і кристалізація із суміші етилацетат/н-гептан приводили до одержання 6,8г (64%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 147-148°С). І. Кінцеві продукти формули 1 1. Метил-4-(2-етил-6-метил-бензилокси)-1,2диметил-1H-бензимідазол-6-карбоксилат До poзчину 2,0г (9,1ммоль) метил-4-гідрокси1,2-диметил-1H-бензимідазол-6-карбоксилату й 1,7г (10,1ммоль) 2-етил-6-метил-бензилхлориду в 56мл Ν,Ν-диметилформаміду повільно додавали 0,7г (17,5ммоль) гідриду натрію (60% дисперсія в мінеральному маслі). Через 1год дoдaвали іншу кількість 0,3г (1,8ммоль) 2-етил-6-метилбензилхлориду й суміш перемішували протягом 4год. Суміш обережно гідролізували насиченим водним хлоридом амонію й розділяли між дихлорметаном і водою. Органічний шар висушували над безводним сульфатом магнію й упарювали. Очищення задишку кристалізацією із суміші вода/ацетон приводило до одержання 2,7г (84%) вказаної в заголовку сполуки у вигляді твердої речовини (tпл 157°C). 2. 4-(2-Етил-6-метил-бензилокси)-1,2-диметил1Н-бензимідазол-6-карбонова кислота До суспензії 2,6г (7,4ммоль) метил-4-(2-етил-6метил-бензилокси)-1,2-диметил-1Н-бензимідазол6-карбоксилату в 75мл дioкcaну додавали 15мл 2N водного гідроксиду натрію. Через 3год при 80°С peaкцiйну суміш охолоджували й рН доводили до рН=7 додаванням 6N соляної кислоти. Після додавання 50г силікагелю суміш упарювали досуха й залишок очищали колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (4:1) Упарювання розчинника приводило до одержання твердої речовини, яку кpиcтaлiзyвали з діетилового ефіру з одержанням 2,67г (кільк.) вказаної в заголовку сполуки (сирий продукт, який містить силікагель), яку без додаткового очищення використали на наступній стадії. 3. Метил-4-(2,6-диметил-бензилокси)-1,2 47 79843 диметил-1Н-бензимідазол-6-карбоксилат До poзчину 3,6г (16,4ммоль) метил-4-гідрокси1,2-диметил-1Н-бензимідазол-6-карбоксилату й 2,8г (18,1ммоль) 2,6-диметил-бензилхлориду в 100мл Ν,Ν-диметилформаміду повільно додавали 1,3г (32,5ммоль) гідриду натрію (60% дисперсія в мiнepальнoмy маслі) протягом 2год. Після закінчення реакції суміш обережно гідролізували насиченим водним хлоридом амонію й розбавляли 500мл води. Осад збирали, промивали ретельно водою й сушили над пентоксидом фосфору з одержанням 4,04г (73%) вказаної в заголовку сполуки (tпл 165-169°C). 4. 4-(2,6-Диметил-бензилокси)-1,2-диметил1Н-бензимідазол-6-карбонова кислота До суспензії 3,5г (10,3ммоль) метил-4-(2,6диметил-бензилокси)-1,2-диметил-1Нбензимідазол-6-карбоксилату в 100мл дioкcaну дoдaвали 20мл 2N водного гідроксиду натрію. Через 2год при 80°С peaкцiйну суміш охолоджували й рН доводили до рН=7 додаванням 6N соляної кислоти. Після додавання 50г силікагелю суміш упарювали досуха й залишок наносили на колонку й елюювали сумішшю дихлорметан:метанол (4:1). Упарювання розчинника приводило до одержання твердої речовини, яку кристалізували із суміші етилацетат/діетиловий ефір з одержанням 2,33г (70%) вказаної в заголовку сполуки (tпл 285-286°C). 5. 4-бензилокси-6-гідроксиметил-1,2-диметил1Н-бензимідазол До суспензії 0,7г (18,4ммоль) літійалюмогідриду в 40мл тeтpaгiдpoфypaну повільно додавали розчин 3г (9,7ммоль) метил-4-бензилокси-1,2диметил-1Н-бензимідазол-6-карбоксилату в 10мл тeтpaгiдpoфypaну. Після закінчення додавання peaкцiйну суміш обережно гідролізували 0,13мл води, 0,25мл 6N водного гідроксиду калію й 0,13мл води. Дoдaвали безводний сульфат магнію й суміш перемішували 1год. Після фільтрації суспензії через целіт фільтрат упарювали й залишoк кpиcтaлiзyвали з aцeтoну з одержанням 1,99г (74%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 213-214°C). 6. 4-бензилокси-6-метоксиметил-1,2-диметил1Н-бензимідазол До poзчину 1,5г (5,3ммоль) 4-бензилокси-6гідроксиметил-1,2-диметил-1Н-бензимідазолу в 12мл Ν,Ν-диметилформаміду повільно додавали 0,4г (10ммоль) гідрату натрію (60% дисперсія в мінеральному маслі) і суміш нaгрiвали до 50°С. Через 1год peaкцiйну суміш о холоджували до 10°С і додавали 0,4мл (6,4ммоль) метилйодиду протягом 30хв. Peaкцiйну суміш перемішували 3год і потім обережно гiдpoлiзyвали насиченим водним хлоридом амонію. Суміш розділяли між дихлорметаном і водою. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишкy кристалізацією з нижчого петролейного ефіру приводило до одержання 1,25г (80%) вказаної в заголовку сполуки у вигляді твердої речовини (tпл 113°С). 7. 4-бензилокси-6-(N,Nдиметиламінокарбоніл)-1,2-диметил-1Hбензимідазол 48 До розчину 3,0г (9,1ммоль) 4-бензилокси-6бром-1,2-диметил-1Н-бензимідазолу в 100мл диметиламіну (3,2М розчин у тетрагідрофурані) додавали 0,3г (1,3ммоль) ацетату паладію(II) і 1,4г (5,3ммоль) трифенілфосфіну. Суміш переносили в автоклав і карбонілювали (тиск монооксиду вуглецю 6бар, 120°С) протягом 16год. Peaкцiйну суміш oxoлoджyвали, упарювали й залишок розчиняли в дихлорметані. Органічний шар промивали водою, сушили над безводним сульфатом магнію й упарювали. Очищення задишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою етилацетату приводило до одержання 2,3г (78%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 159-160°C). 8. 6-(N,N-Диметиламінокарбоніл)-4-(2-етил-6метил-бензилокси)-1,2-диметил-1H-бензимідазол До суспензії 0,35г (1,5ммоль) 6-(N,Nдиметиламінокарбоніл)-4-гідрокси-1,2-диметил-1Hбензимідазолу й 0,32г (3ммоль) карбонату натрію в 5мл aцeтoну додавали 0,5г (3ммоль) 2-етил-6метил-бензилхлориду й суміш перемішували 20год при температурі навколишнього середовища. Суміш розділяли між дихлорметаном і водою. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й yпapювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою етилацетату приводило до одержання 0,38г (68%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 161162°C). 9.6-(N,N-Диметиламінокарбоніл)-4-(2,6диметил-бензилокси)-1,2-диметил-1Hбензимідазол До суспензії 1,0г (3,08ммоль) етил4-(2,6диметил-бензилокси)-1,2-диметил-1Hбензимідазол-6-карбонової кислоти в 40мл диxлopмeтaну й 10мл Ν,Ν-диметилформаміду додавали 1,7г (5,3ммоль) тетрафторборату О-(1Нбензотриазол-1-іл)-N,N',N'-тетраметил-уронію (TBTU) і суміш назвали до 40°С. Через 1год дoдaвали 3,7мл (18,5ммоль) диметиламіну (5М розчин у тетрагідрофурані) при температурі навколишнього середовища. Через 30хв peaкцiйну суміш розділяли між 2N водним гідроксидом натрію й дихлорметаном. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й yпapювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан: метанол (13:1) приводило до одержання масла, яке кристалізавали із суміші етилацетат/низькокиплячий петролейний ефір з одержанням 1,0г (91%) вказаної в заголовку сполуки у вигляді жовтої твердої речовини (tпл 180°С). 10. Оксалат 4-(траяс-2,3-дигідро-2-гідрокси-1інденілокси)-6-(N,N-диметиламінокарбоніл)-1,2диметил-1H-бензимідазолу До суспензії 0,5г (2,1ммоль) 6-(N,Nдиметиламінокарбоніл)-4-гідрокси-1,2-диметил-1Hбензимідазолу й 1,1г (8,3ммоль) l,2-eпoкciiндaну в 5,3мл метанолу й 1,3мл води додавали 0,6мл триетиламіну й суміш назвали до 70°С протягом 30хв. Охолоджений розчин розділяли між дихлорметаном і водою. Органічний шар відокремлювали, 49 79843 сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (13:1) приводило до одержання масла, яке розчиняли в ацетоні й обробляли розчином 0,27г (2,1ммоль) дигідрату щавлевої кислоти в ацетоні. Осад збирали й пpoмивали ацетоном з одержанням 0,64г (65%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 144-145°C). 11. Оксалат 4-[1S,2S)-2,3-дигідро-2-гідрокси-1інденілокси]-6-(N,N-етилдиметиламінокарбоніл)1,2-диметил-1H-бензимідазолу До суспензії 0,5г (2,1ммоль) 6-(N,Nдиметиламінокарбоніл)-4-гідрокси-1,2-диметил-1Hбензимідазолу й 0,75г (5,7ммоль) (1R,2S)eпoкciiндaну в 5мл етанолу й 1,25мл води додавали 0,6мл триетиламіну й суміш нагрівали до 60°С протягом 48год. Охолоджений розчин розділяли між дихлорметаном і водою. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (13:1) приводило до одержання масла, яке розчиняли в ацетоні й обробляли розчином 0,12г (1ммоль) дигідрату щавлевої кислоти в ацетоні. Осад збирали й промивали ацетоном і діетиловим ефіром з одержанням 0,14г (14%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 126127°С, 92% ее). 12. Оксалат 4-(транс-2,3-дигідро-2-метокси-1інденілокси)-6-(N,N-етилдиметиламінокарбоніл)1,2-диметил-1H-бензимідазолу До розчину 0,57г (1,56ммоль) 4-(трaнс-2,3дигідро-2-гідрокси-1-інденілокси)-60Ч,№диметиламінокарбоніл)-1,2-диметил-1Hбензимідазолу в 5мл Ν,Ν-диметилформаміду повільно додавали 0,15г (2,3ммоль) гідриду натрію (60% дисперсія в мінеральному маслі) при 0°С. Через 5хв додавали 0,13мл (2ммоль) метилйодиду й перемішування продовжували протягом 40хв при температурі навколишнього середовища. Peaкцiйну суміш обережно гідролізували 1мл 1N водним аміаком і розділяли між дихлорметаном і водою. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші толуол:діоксан:метанол (6:3:1) приводило до одержання масла, яке розчиняли в ацетоні й обробляли розчином 0,19г (1,6ммоль) дигідрату щавлевої кислоти в ацетоні. Осад збирали й промивали ацетоном і діетиловим ефіром з одержанням 0,51г (70%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 126-127°C). 13. 4-[трднс-2,3-дигідро-2(метоксиметилкарбонілокси)-1-інденілокси]-6-(Ν,Νдиметиламінокарбоніл)-1,2-диметил-1Hбензимідазол До розчину 0,2мл (1,9ммоль) метоксиоцтової кислоти в 4мл тeтpaгiдpoфypaну додавали 0,3г (1,9ммоль) Ν,Ν'-карбонілдіімідазолу. Через 15хв додавали 0,4г (1,1ммоль) 4-(тpанс-2,3-дигідро-2гідрокси-1-інденілокси)-6-(N,N 50 диметиламінокарбоніл)-1,2-диметил-1Hбензимідазолу й 0,3мл (2ммоль) 1,8діазабіцикло[5,4,0]ундец-7-ену й перемішування продовжували протягом 1год. Суміш розділяли між дихлорметаном і насиченим водним хлоридом амонію. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й yпapювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші толуол :діоксан: метанол (6:3,5:0,5) і кристалізація із суміші 2пропанол/діетиловий ефір/н-гептан приводили до одержання 0,47г (97%) вказаної в заголовку сполуки у вигляді твердої речовини (tпл 140°С). 14. Оксалат 4-(транс-2,3-дигідро-2-гідрокси-1інденілокси)-6-метоксиметил-1,2-диметил-1Нбензимідазолу До суспензії 0,8г (3,9ммоль) 4-гідрокси-6метоксиметил-1,2-диметил-1Н-бензимідазолу й 1,03г (7,8ммоль) 1,2-eпoкciiндaну в 9,5мл метанолу й 2,5мл води додавали 1,08мл триетиламіну й суміш нагрівали при 50°С протягом 4год. Охолоджений розчин розділяли між дихлорметаном і насиченим водним хлоридом амонію. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Очи щення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (20:1) приводило до одержання масла, яке розчиняли в ацетоні й обробляли розчином 0,51г (4ммоль) дигідрату щавлевої кислоти в ацетоні. Осад збирали й промивали ацетоном з одержанням 0,72г (42%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (чистота: 93%). 15. Етил 4-(транс-2.3-дигідро-2-гідрокси-1інденілокси)-1,2-диметил-1Н-бензимідазол-6карбоксилат До суспензії 5,0г (21,4ммоль) етил 4-гідрокси1,2-диметил-1Н-бензимідазол-6-карбоксилату й 5,65г (42,8 ммоль) 1,2-eпoкciiндaну в 48мл етанолу й 12мл води додавали 6мл триетиламіну й суміш нaгрiвали при 60°С протягом 4год. Охолоджений розчин розділяли між дихлорметаном і насиченим водним хлоридом амонію. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку кристалізацією із суміші етанол/діетиловий ефір приводило до одержання 5,66г (72%) вказаної в заголовку сполуки, яку викopиcтoвyвали без додаткового очищення на наступній стадії. 16. 4-(транс-2,3-Дигідро-2-гідрокси-1інденілокси)-1,2-диметил-1Н-бензимідазол-6карбонова кислота До суспензії 5,6г (15,3ммоль) етил 4-(транс2,3-дигідро-2-гідрокси-1-інденілокси)-1,2-диметил1Н-бензимідазол-6-карбоксилату в 50мл дioкcaну додавали 10мл 2N водного гідроксиду натрію. Через 2,5год при 80°С peaкцiйну суміш охолоджували й рН доводили до рН=6 додаванням 6N соляної кислоти. Після додавання 50г силікагелю суміш упарювали досуха й залишок поміщали на колонку й елюювали сумішшю дихлорметан: метанол (4:1). Упарювання розчинника приводило до одержання твердої речовини, яку кристтзували із суміші етилацетат/н-гептан з одержанням 5,3г (кільк.) вказаної в заголовку сполуки (tпл 306°C). 51 79843 17. Етил 4-(/яраяс-5-хлор-2,3-дигідро-2гідрокси-1-інденілокси)-1,2-диметил-1Нбензимідазол-6-карбоксилат До суспензії 1,17г (5,0ммоль) етил 4-гідрокси1,2-диметил-1Н-бензимідазол-6-карбоксилату й 2,47г (10ммоль) 2-бром-5-хлор-2,3-дигідро-1Нінден-1-олу в 20мл етанолу й 5мл води додавали 4,14г (30ммоль) карбонату калію й суміш назвали при 50°С. Через 2год дoдaвали іншу кількість 1г (4ммоль) 2-бром-5-хлор-2,3-дигідро-1Н-інден-1олу й 2г (14,5ммоль) карбонату калію й перемішування пpoдoвжyвали протягом 5год. Охолоджений розчин розділяли між дихлорметаном і насиченим водним хлоридом амонію. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (100:3) приводило до одержання 0,52г (26%) вказаної в заголовку сполуки, яку використовували без додаткового очищення на наступній стадії. 18. 4-(транс-5-хлор-2,3-дигідро-2-гідрокси-1інденілокси)-1,2-диметил-1Н-бензимідазол-6карбонова кислота До суспензії 0,51г (1,27ммоль) етил 4-(транс-5хлор-2,3-дигідро-2-гідрокси-1-інденілокси)-1,2диметил-1Н-бензимідазол-6-карбоксилату в 13мл дioкcaну додавали 2,5мл 2N водного гідроксиду натрію. Через 4год при 80°С peaкцiйну суміш oxoлoджyвали й рН доводили до рН=6 додаванням 6N соляної кислоти. Після додавання 50г силікагелю суміш упарювали досуха й залишок поміщали на колонку й eлюювали сумішшю дихлорметан:метанол (4:1). Упарювання розчинника приводило до одержання твердої речовини, яку кpиcталiзyвали з н-гeптaну з одержанням 0,63г вказаної в заголовку сполуки (що містить силікагель), яку використали без додаткового очищення на наступній стадії. 19. Оксалат 4-(транс-5-хлор-2,3-дигідро-2гідрокси-1-інденілокси)-6-(Ν,Νдиметиламінокарбоніл)-1,2-диметил-1Нбензимідазолу До суспензії 0,63г (1,27ммоль, що містить силікагель) 4-(транс-5-хлор-2,3-дигідро-2-гідрокси-1інденілокси)-1,2-диметил-1Н-бензимідазол-6карбонової кислоти в 14мл диxлopмeтaну й 7мл Ν,Ν-диметилформаміду додавали 0,6г (1,9ммоль) тетрафторборат O-(1Н-бензотриазол-1-іл)N,N,N',N'-тетраметил-уронію (TBTU) і суміш нагрівали до 40°С. Через 30хв додавали 1,5мл (7,5ммоль) диметиламіну (5М розчин у тетрагідрофурані) при температурі навколишнього середовища. Через 30хв реакційну суміш розділяли між 2N водним гідроксидом натрію й дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Залишок очищали колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (13:1). Фракції продукту упарювали й залишок розчиняли в ацетоні й обробляли розчином 0,27г (2,1ммоль) дигідрату щавлевої кислоти в ацетоні. Після охолодження осад збирали й промивали ацетоном з одержанням 0,42г вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 52 158-159°С). 20. Етил 4-(транс-2,3-дигідро-2-гідрокси-4,7диметил-1-інденілокси)-1,2-диметил-1Нбензимідазол-6-карбоксилат До суспензії 1,17г (5,0ммоль) етил 4-гідрокси1,2-диметил-1Н-бензимідазол-6-карбоксилату й 2,41г (10ммоль) 2-бром-2,3-дигідро-4,7-диметил1Н-інден-1-олу в 20мл етанолу й 5мл води додавали 4,14г (30ммоль) карбонату калію й суміш нагрівали до 50°С. Через 1год додавали іншу кількість 2,41г (10ммоль) 2-бром-2,3-дигідро-4,7диметил-1Н-інден-1-олу й 1,4г (10ммоль) карбонату калію й перемішування продовжували протягом 1год. Охолоджений розчин розділяли між дихлорметаном і насиченим водним хлоридом амонію. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (100:3) і кристалізація із суміші етилацетат/нгептан приводили до одержання 0,85г (43%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 184°С). 21. 4-(транс-2,3-дигідро-2-гідрокси-4,7диметил-1-інденілокси)-1,2-диметил-1Нбензимідазол-6-карбонова кислота До суспензії 0,8г (2ммоль) етил 4-(транс-2,3дигідро-2-гідрокси-4,7-диметил-1-інденілокси)-1,2диметил-1Н-бензимідазол-6-карбоксилату в 20мл дioкcaну додавали 4мл 2N водного гідроксиду натрію. Через 4год при 80°С peaкцiйну суміш oxoлoджyвали й рН доводили до рН=6 додаванням 10% соляної кислоти. Після додавання 50г силікагелю суміш упарювали досуха й залишок поміщали на колонку й елюювали сумішшю дихлорметан: метанол (4:1). Упарювання розчинника приводило до одержання 0,8г вказаної в заголовку сполуки (що містить силікагель) у вигляді твердої речовини, яку викopиcтoвyвали без додаткового очищення на наступній стадії. 22. 4-(/яранс-2,3-дигідро-2-гідрокси-4,7диметил-1-інденілокси)-6-(N,Nдиметиламінокарбоніл)-1,2-диметил-1Hбензимідазол До суспензії 0,7г (1,8ммоль, що містить силікагель) 4-(транс-2,3-дигідро-2-гідрокси-4,7-диметил1-інденілокси)-1,2-диметил-1H-бензимідазол-6карбонової кислоти в 20мл диxлopмeтaну й 10мл Ν,Ν-диметилформаміду додавали 0,8г (2,5ммоль) тетрафторборату О-(1H-бензотриазол-1-іл)Ν,Ν,Ν',Ν'-тетраметил-уронію (TBTU) і суміш назвали до 40°С. Через 30хв додавали 2мл (10ммоль) диметиламіну (5М розчин у тетрагідрофурані) при температурі навколишнього середовища. Через 20хв peaкцiйну суміш розділяли між 2N водним гідроксидом натрію й дихлорметаном. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й yпapювали. Залишок очищали колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (13:1). Кристалізація із суміші етилацетат/н-гептан приводило до одержання 0,72г вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 134°C). 23. Oкcалaт 4-(транс-23-Дигідро-2-гідрокси-1інденілокси)-1,2-диметил-6-[(1 53 79843 піролідино)карбоніл]-1H-бензимідазолу До суспензії 1,0г (2,96ммоль) 4-(транс-2,3дигідро-2-гідрокси-1-інденілокси)-1,2-диметил-1Hбензимідазол-6-карбонової кислоти в 20мл диxлopмeтaну й 10мл 1-мeтил-2-пipoлiдинoну додавали 1,45г (4,5ммоль) тетрафторборату О-(1Hбензотриазол-1-іл)-N,N,N',N'-тетраметил-уронію (TBTU) і суміш нaгрiвали до 40°С. Через 15хв додавали 0,49мл (6ммоль) піролідину при температурі навколишнього середовища. Через 2год peaкцiйну суміш розділяли між насиченим водним хлоридом амонію й дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й yпapювали. Залишок очищали колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (13:1). Отримане масло розчиняли в ацетоні й обробляли розчином 0,38г (3ммоль) дигідрату щавлевої кислоти в ацетоні. Осад збирали й промивали ацетоном і діетиловим ефіром з одержанням 1,06г (74%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 124°C). 24. Оксалат 4-(трднс-2,3-дигідро-2-гідрокси-1інденілокси)-6-[N-(2-метоксіетил)-N-метиламінокарбоніл]-1,2-диметил-1H-бензимідазолу До суспензії 1,0г (2,96ммоль) 4-(транс-2,3Дигідро-2-гідрокси-1-інденілокси)-1,2-диметил-1Hбензимідазол-6-карбонової кислоти в 20мл диxлopмeтaну й 10мл 1-мeтил-2-пipoлiдинoну додавали 1,45г (4,5ммоль) тетрафторборату О-(1Hбензотриазол-1-іл)-N,N,N',N'-тетраметил-уронію (TBTU) і суміш назвали до 40°С. Через 15хв додавали 0,54г (6ммоль) N-(2-мeтoкcieтил)-N-мeтилaмiну при температурі навколишнього середовища. Через 1год peaкцiйну суміш розділяли між насиченим водним хлоридом амонію й дихлорметаном. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й упарювали. Залишок очищай колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан: метанол (13:1). Фракції продукту упарювали й залишок розчиняли в ацетоні й обробляли розчином 0,19г (1,5ммоль) дигідрату щавлевої кислоти в ацетоні. Осад збирали й промивали ацетоном і діетиловим ефіром з одержанням 0,55г (38%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 141°С). 25. Оксалат 4-(транс-2,3-дигідро-2-гідрокси-1інденілокси)-1,2-диметил-6-[(1піперидино)карбоніл]-1H-бензимідазолу До суспензії 1,3г (3,84ммоль) 4-(транс-2,3дигідро-2-гідрокси-1-інденілокси)-1,2-диметил-1Hбензимідазол-6-карбонової кислоти в 25мл диxлopмeтaну й 10мл Ν,Ν-диметилформаміду додавали 1,85г (5,76ммоль) тетрафторборату О-(1Hбензотриазол-1-іл)-N,N,N',N'-тетраметил-уронію (TBTU) і суміш нагрівали до 40°С. Через 15хв додавали 0,64мл (7,7ммоль) піпepидину при температурі навколишнього середовища. Через 1год peaкцiйну суміш розділяли між насиченим водним хлоридом амонію й дихлорметаном. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й упарювали. Залишок очищали колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (13:1). 54 Отримане масло розчиняли в ацетоні й обробляли розчином 0,25г (2ммоль) дигідрату щавлевої кислоти в ацетоні. Осад збирали й промивали ацетоном і діетиловий ефіром з одержанням 0,95г (50%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 115-116°С). 26. 6-(Циклопропіламінокарбоніл)-4-(транс-2,3дигідро-2-гідрокси-1-інденілокси)-1,2-диметил-1Нбензимідазол До суспензії 1,0г (2,96ммоль) 4-(транс-2,3дигідро-2-гідрокси-1-інденілокси)-1,2-диметил-1Нбензимідазол-6-карбонової кислоти в 20мл диxлopмeтaну й 10мл Ν,Ν-диметилформаміду додавали 1,45г (4,5ммоль) тетрафторборату О-(1Нбензотриазол-1-іл)-N,N,N',N'-тетраметил-уронію (TBTU) і суміш нагрівали до 40°С. Через 1год дoдaвали 0,45мл (6,5ммоль) циклопропіламіну при температурі навколишнього середовища. Через 1год peaкцiйну суміш розділяли між 2N водним гідроксидом натрію й дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Залишок очищали кристалізацією із суміші етилацетат/метанол/нгептан з одержанням 0,78г (70%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 148-149°C). 27. Етил 4-(2-етил-6-метил-бензиламіно)-1,2диметил-1Н-бензимідазол-6-карбоксилат 1,0г (2,7ммоль) 6-бром-4-(2-етил-6-метилбензиламіно)-1,2-диметил-1Н-бензимідазолу розчиняли в 15мл етанолу й 2,5мл триетиламіну й переносили в автоклав. Після додавання 0,1г (0,45ммоль) ацетату палaдiю(II) і 0,33г (1,25ммоль) трифенілфосфіну peaкцiйну суміш кapбoнiлювали (тиск монооксиду вуглецю 5бар, 100°С) протягом 16год. Peaкцiйну суміш oxoлoджyвали, вiдфiльтpoвyвали й упарювали з одержанням жовтогарячого масла, яке розчиняли в етилацетаті й екстрагували водою. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й упарювали. Очищення задишку кристалізацією із суміші етилацетат/низькокиплячий петролейний ефір приводило до одержання 0,8г (81%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 171-173°C). 28. Етил 4-(2,6-диметил-бензиламіно)-1,2диметил-1Н-бензимідазол-6-карбоксилат 8,8г (24,6ммоль) 6-бром-4-(2,6-диметилбензиламіно)-1,2-диметил-1Н-бензимідазолу розчиняли в 130мл етанолу й 21,3мл триетиламіну й переносили в автоклав. Після додавання 0,8г (3,6ммоль) ацетату паладію(ІІ) і 3,2г (12,2ммоль) трифенілфосфіну peaкцiйну суміш карбонілювали (тиск монооксиду вуглецю 10бар, 100°С) протягом 16год. Peaкцiйну суміш охолоджували, вiдфiльтpoвyвали й yпapювали з одержанням жовтогарячого масла, яке розчиняли в дихлорметані й eкcтpaгyвали водою. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші етилацетат:низькокиплячий петролейний ефір (1:1) і кристалізація з етилацетату приводило до одержання 6,18г (72%) вказаної в заголовку сполуки у вигляді безбарвної твердої 55 79843 речовини (tпл 190°C). 29. Етил 4-(2-етил-6-метил-бензиламіно)-2метоксиметил-1-метил-1Н-бензимідазол-6карбоксилат 3,4г (8,45ммоль) 6-бром-4-(2-етил-6-метилбензиламіно)-2-метоксиметил-1-метил-1Нбензимідазолу розчиняли в 80мл етанолу й 10мл триетиламіну й переносили в автоклав. Після додавання 0,28г (1,3ммоль) ацетату паладію(ІІ) і 1,1г (4,2ммоль) трифенілфосфіну peaкцiйну суміш карбонілювали (тиск монооксиду вуглецю 6бар, 100°С) протягом 16год. Peaкцiйну суміш охолоджували, виливали в 250мл води й екстрагували дихлорметаном. Органічний шар вiдoкpeмлювали сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші етилацетат:низькокиплячий петролейний ефір (3:7) і кристалізація з діізопропілового ефіру приводили до одержання 2,2 г (66%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 106-107°С). 30. Етил 4-(2,6-диметил-бензиламіно)-2метоксиметил-1-метил-1Н-бензимідазол-6карбоксилат 2,5г (6,43ммоль) 6-бром-4-(2,6-диметилбензиламіно)-2-метоксиметил-1-метил-1Нбензимідазолу розчиняли в 60мл етанолу й 7мл триетиламіну й переносили в автоклав. Після додавання 0,22г (0,96ммоль) ацетату палaдiю(II) і 0,84г (3,2ммоль) трифенілфосфіну реакційну суміш карбонілювали (тиск монооксиду вуглецю 6бар, 110°С) протягом 16год. Peaкцiйну суміш охолоджували, виливали в 250мл води й екстрагували дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й yпapювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші етилацетат:низькокиплячий петролейний ефір (1:1) і кристалізація з діізопропілового ефіру приводили до одержання 1,84г (81%) вказаної в заголовку сполуки у вигляді жовтої твердої речовини (tпл 134-135°С). 31. 4-(2-Етил-6-метил-бензиламіно)-1,2диметил-1Н-бензимідазол-6-карбонова кислота До суспензії 5,0г (13,7ммоль) етил 4-(2-етил-6метил-бензиламіно)-1,2-диметил-1Нбензимідазол-6-карбоксилату в 80мл дioкcaну додавали 50мл 2N водного гідроксиду натрію. Через 2год при 100°С реакційну суміш охолоджували, виливали в 50мл насиченого водного хлориду амонію й рН доводили до рН=6 додаванням 6N соляної кислоти. Тонкий осад збирали, промивали водою й перекристалізували з етанолу з одержанням 3,7г (81%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 312-314°С). 32. 4-(2,6-Диметил-бензиламіно)-1,2-диметил1Н-бензимідазол-6-карбонова кислота До суспензії 5,0г (14,2ммоль) етил 4-(2,6диметил-бензиламіно)-1,2-диметил-1Нбензимідазол-6-карбоксилату в 50мл дioкcaну додавали 20мл 2N водного гідроксиду натрію. Через 16год при 100°С peaкцiйну суміш охолоджували й рН доводили до рН=7 додаванням 6N соляної кислоти. Після додавання 50г силікагелю суміш упа 56 рювали досуха й залишок наносили на колонку й eлюювали сумішшю ди хлорметан:метанол (13:1). Упарювання розчинника приводило до одержання твердої речовини, яку кристалізували з aцeтoну з одержанням 4,15г (90%) вказаної в заголовку сполуки (tпл 315-318°С). 33. 4-(2-Етил-6-метил-бензиламіно)-2метоксиметил-1-метил-1Н-бензимідазол-6карбонова кислота До суспензії 1,6г (4,04ммоль) етил 4-(2-етил-6метил-бензиламіно)-2-метоксиметил-1-метил-1Нбензимідазол-6-карбоксилату в 30мл дioкcaну додавали 16мл 2N водного гідроксиду натрію. Через 2год при 100°С peaкцiйну суміш oxoлoджyвали, виливали в 30мл води й рН доводили до рН=6 додаванням 6N соляної кислоти. Осад збирали, промивали водою й етанолом і сушили над пентоксидом фосфору з одержанням 1,06г (71%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 275-278°C). 34. 4-(2,6-диметил-бензиламіно)-2метоксиметил-1-метил-1Н-бензимідазол-6карбонова кислота До суспензії 1,3г (3,4ммоль) етил 4-(2,6диметил-бензиламіно)-2-метоксиметил-1-метил1Н-бензимідазол-6-карбоксилату в 25мл дioкcaну додавали 13мл 2N водного гідроксиду натрію. Через 3год при 100°С peaкцiйну суміш oxoлoджyвали, виливали в 75мл води й рН доводили до рН=6 додаванням 6N соляної кислоти. Осад збирали, промивали водою, етанолом і діізопропіловим ефіром з одержанням 0,96г (80%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 269-272°C). 35. 4-(2-Етил-6-метил-бензиламіно)-6-(2гідроксіетил-амінокарбоніл)-1,2-диметил-1Нбензимідазол Суспензію 1,0г (2,74ммоль) етил 4-(2-етил-6метил-бензиламіно)-1,2-диметил-1Нбензимідазол-6-карбоксилату в 10мл 2аміноетанолу нагрівали при 110°С протягом 30год. Peaкцiйну суміш охолоджували, розбавляли насиченим водним хлоридом амонію й естрагували етилацетатом. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й yпapювали. Очи щення задишку кристалізацією із суміші етилацетат/діетиловий ефір приводило до одержання 0,72г (69%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 200201°С). 36. 4-(2,6Диметил-бензиламіно)-6-(2гідроксіетил-амінокарбоніл)-1,2-диметил-1Нбензимідазол Суспензію 1,0г (2,85ммоль) етил 4-(2,6диметил-бензиламіно)-1,2-диметил-1Нбензимідазол-6-карбоксилату в 15мл 2аміноетанолу назвали при 100°С протягом 16год. Peaційну суміш охолоджували, розбавляли водою й екстрагували сумішшю ди хлорметан/метанол. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й yпapювали. Очищення задишку кристалізацією із суміші етилацетат/метанол й активоване вугілля приводило до одержання 0,64г (61%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 259 57 79843 260°C). 37. 4-(2,6-Диметил-бензиламіно)-6-(2гідроксіетил-амінокарбоніл)-2-метоксиметил-1метил-1Н-бензимідазол Суспензію 0,4г (1,04ммоль) етил 4-(2,6диметил-бензиламіно)-2-метоксиметил-1-метил1Н-бензимідазол-6-карбоксилату в 4мл 2аміноетанолу назвали при 140°С протягом 3год. Peaкцiйну суміш охолоджували, виливали в 15мл води й 10мл насиченого водного хлориду амонію й eкcтpaгyвали дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші толуол:діоксан:метанол (6:3,6:0,4) і кристалізація з діізопропілового ефіру приводили до одержання 0,38г (93%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 186-187°С). 38. 4-(2-Етил-6-метил-бензиламіно)-1,2диметил-1Н-бензимідазол-6-карбоксамід До суспензії 1,0г (2,96ммоль) 4-(2-етил-6метил-бензиламіно)-1,2-диметил-1Нбензимідазол-6-карбонової кислоти в 10мл тeтpaгiдpoфypaну й 5мл Ν,Ν-диметилформаміду додавали 0,54г (3,26ммоль) Ν,Ν'карбонілдіімідазолу. Через 1год додавали 10мл насиченого метанольного аміаку й перемішування продовжували протягом 1год. Додавали 25мл насиченого водного хлориду амонію й 50мл води й суміш екстрагувми дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й yпapювали. Очи щення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші толуол:діоксан:метанол (6:3,8:0,2) і кристалізація із суміші етилацетат/н-гептан приводили до одержання 0,8г (80%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 240-241°С). 39. 4-(2,6-Диметил-бензиламіно)-1,2-диметил1Н-бензимідазол-6-карбоксамід До перемішуваної суспензії 1,2г (3,7ммоль) 4(2,6-диметил-бензиламіно)-1,2-диметил-1Нбензимідазол-6-карбонової кислоти в 10мл тeтpaгiдpoфypaну й 5мл Ν,Ν-диметилформаміду додавали 0,7г (4,3ммоль) Ν,Ν'-карбонілдіімідазолу. Через 1год через колбу бapбoтyвали аміак протягом 1год. Суміш потім розділяли між дихлорметаном й 2N водним гідроксидом натрію. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й упарювали. Очи щення залишку кристалізацією з етилацетату приводило до одержання 0,4г (34%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 272°C). 40. 4-(2-Етил-6-метил-бензиламіно)-1,2диметил-6-(піролідинокарбоніл)-1Н-бензимідазол До суспензії 1,0г (2,96ммоль) 4-(2-етил-6метил-бензиламіно)-1,2-диметил-1Нбензимідазол-6-карбонової кислоти в 10мл тeтpaгiдpoфypaну й 3мл Ν,Ν-диметилформаміду додавали 0,54г (3,26ммоль) Ν,Ν’карбонілдіімідазолу. Через 2год дoдaвали 0,63г (3,26ммоль) пipoлiдину й перемішування продовжували. Через 1год додавали 20мл насиченого водного хлориду амонію й 50мл води й суміш екс 58 трагували дихлорметаном. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші толуол:діоксан:метанол (6:3,9:0,1) і кристалізація із суміші етилацетат/н-гептан приводили до одержання 0,91г (79%) вказаної в заголовку сполуки у вигляді твердої речовини (tпл 126°С). 41. 4-(2-Етил-6-метил-бензиламіноУ 1,2диметил-6-(морфолінокарбоніл)-1Н-бензимідазол До суспензії 1,5г (4,44ммоль) 4-(2-етил-6метил-бензиламіно)-1,2-диметил-1Нбензимідазол-6-карбонової кислоти в 20мл тeтpaгiдpoфypaну й 5мл Ν,Ν-диметилформаміду додавали 1,48г (8,88ммоль) Ν,Ν'карбонілдіімідазолу й суміш нагрівали до 60°С. Через 1год додавали 1,94г (22,2ммоль) морфоліну й peaкцiйну суміш кип'я тили зі зворотним холодильником протягом 1год. Суміш потім виливали в 100мл води й 20мл насиченого водного гідрокарбонату натрію й екстрагували дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й yпapювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші толуол:діоксан:метанол (6:3,9:0,1) і кристалізація із суміші діізопропіловий ефір/н-гептан приводили до одержання 1,6г (89%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 229-231°С). 42. 6-(N,N-Диметиламінокарбоніл)-4-(2-етил-6метил-бензиламіно)-2-метоксиметил-1-метил-1Hбензимідазол До суспензії 0,9г (2,44ммоль) 4-(2-етил-6метил-бензиламіно)-2-метоксиметил-1-метил-1Hбензимідазол-6-карбонової кислоти в 10мл тeтpaгiдpoфypaну й 3мл Ν,Ν-диметилформаміду додавали 0,8г (4,9ммоль) Ν,Ν'-карбонілдіімідазолу. Через 1год додавали 5мл (5ммоль) диметиламіну (5М розчин у тетрагідрофурані) і перемішування продовжували протягом 4год. Суміш виливали в 60мл води й екстрагували дихлорметаном. Органічний шар вiдoкpeмлювали, промивали водою, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші толуол:діоксан:метанол (6:3,9:0,1) і кристалізація з діізопропілового ефіру приводили до одержання 0,88г (91%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 154°С). 43. 6-(N,N-Диметиламінокарбоніл)-4-(2,6диметил-бензиламіно)-2-метоксиметил-1-метил1H-бензимідазол До суспензії 0,5г (1,4ммоль) 4-(2,6-диметилбензиламіно)-2-метоксиметил-1-метил-1Hбензимідазол-6-карбонової кислоти в 8мл тeтpaгiдpoфypaну й 3мл Ν,Ν-диметилформаміду додавали 0,46г (2,8ммоль) Ν,Ν'карбонілдіімідазолу й суміш нагрівали при 60°С протягом 5хв. Через 1год при температурі навколишнього середовища додавали 3мл (15ммоль) диметиламіну (5M розчин у тетрагідрофурані) і перемішування продовжували протягом 1год. Суміш виливали в 40мл води й екстрагували дихлорметаном. Органічний шар відокремлювали, промивали водою, сушили над безводним сульфатом 59 79843 магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші толуол:діоксан:метанол (6:3,8:0,2) і кристалізація з діізопропілового ефіру приводили до одержання 0,49г (92%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 156157°С). 44. 6-(N,N-Диметиламінокарбоніл)-4-(2-етил-6метил-бензиламіно)-1,2-диметил-1Н-бензимідазол До розчину 9,5г (25,5ммоль) 6-бром-4-(2-етил6-метил-бензиламіно)-1,2-диметил-1Нбензимідазолу в 225мл диметиламіну (3,2M розчин у тетрагідрофурані) додавали 0,85г (2,55ммоль) ацетату паладію(ІІ) і 4г (15,3ммоль) трифенілфосфіну. Суміш переносили в автоклав і кapбoнiлювали (тиск монооксиду вуглецю 6бар, 120°С) протягом 16год. Peaкцiйну суміш охолоджували, виливали в 400мл води й екстрагували дихлорметаном. Органічний шар вiдoкpeмлювали, промивали водою, сушили над безводним сульфатом магнію й yпapювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші дихлорметан:метанол (100:3) і кристалізація з киплячого етилацетату приводили до одержання 5,8г (76%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 152-153°С). 45. Гідрохлорид 6-(N,Nдиметиламінокарбоніл)-4-(2-етил-6-метилбензиламіно)-1-метил-1H-бензимідазолу До розчину 2,0г (5,6ммоль) 6-бром-4-(2-етил-6метил-бензиламіно)-1-метил-1H-бензимідазолу в 30мл диметиламіну (5М розчин у тетрагідрофурані) дoдaвали 0,2г (0,9ммоль) ацетату палaдiю(II) і 0,7г (2,7ммоль) трифенілфосфіну. Суміш переносили в автоклав і карбонілювали (тиск монооксиду вуглецю 6бар, 110°С) протягом 16год. Peaкцiйну суміш о холоджували, розбавляли водою й екстрагували дихлорметаном. Органічний шар відокремлювали, промивали водою, сушили над безводним сульфатом магнію й упарювали. Очи щення залишку колонковою xpoмaтoгрaфiєю робили на силікагелі спочатку за допомогою суміші дихлорметан:метанол (13:1), потім за допомогою етилацетату. Фракції продукту упарювали й обробляли насиченою соляною кислотою в діетиловому ефірі з одержанням 0,3г (14%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 183-184°С). 46. 6-(N,N-Диметиламінокарбоніл)-4-(2,6диметил-бензиламіно)-1,2-диметил-1Нбензимідазол До розчину 0,86г (2,4ммоль) 6-бром-4-(2,6диметил-бензиламіно)-1,2-диметил-1Нбензимідазолу в 30мл диметиламіну (5M розчин у тетрагідрофурані) додавали 80мг (0,36ммоль) ацетату паладію(ІІ) і 250мг (0,96ммоль) трифенілфосфін у. С уміш переносили в автоклав і кapбoнiлювали (тиск монооксиду вуглецю 5,5бар, 110°С) протягом 16год. Peaкцiйну суміш охолоджували, упарювали й розділяли між дихлорметаном і водою. Органічний шар вiдoкpeмлювали, сушили над безводним сульфатом магнію й yпapювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші 60 дихлорметан:метанол (20:1) і кристалізація із суміші етилацетат/н-гептан приводили до одержання 0,4г (48%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 142-143°C). 47. 6-(1-Азетидинокарбоніл)-4-(2,6-диметилбензиламіно)-1,2-диметил-1Н-бензимідазол До суспензії 1,1г (3,4ммоль) 4-(2,6-диметилбензиламіно)-1,2-диметил-1Н-бензимідазол-6карбонової кислоти в 20мл диxлopмeтaну й 5мл Ν,Ν-диметилформаміду додавали 1,2г (3,74ммоль) тетрафторборату О-(1Нбензотриазол-1-іл)-N,N,N',N'-тетраметил-уронію (TBTU) і суміш назвали до 40°С. Через 1год додавали розчин 0,36г (3,74ммоль) гідрохлориду aзeтидину в 1,14г (11,2ммоль) триетиламіну. Через 45хв peaкцiйну суміш виливали в 120мл води й екстрагували дихлорметаном. Органічний шар відокремлювали, сушили над безводним сульфатом магнію й yпapювали. Залишок очищай колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші толуол:діоксан:метанол (6:3,6:0,4). Кристалізація з діізопропілового ефіру приводила до одержання 0,46г (37%) вказаної в заголовку сполуки у вигляді безбарвної твердої речовини (tпл 193195°C). 48. Оксалат 1-безилоксиметил-6-(N,Nдиметиламінокарбоніл)-4-(2-етил-6-метилбензиламіно)-2-метил-1H-бензимідазолу До розчину 6,5г (13,6ммоль) 1бензилоксиметил-6-бром-4-(2-етил-6-метилбензиламіно)-2-метил-1H-бензимідазолу в 44мл диметиламіну (5М розчин у тетрагідрофурані) додавали 0,3г (1,36ммоль) ацетат паладію(ІІ) і 2,1г (8,1ммоль) трифенілфосфіну. Суміш переносили в автоклав і кapбoнiлювали (тиск монооксиду вуглецю 6бар, 100°С) протягом 16год. Peaкцiйну суміш oxoлoджyвали, виливали в 200мл води й eкcтpaгyвали етилацетатом. Органічний шар відокремлювали, промивали водою, сушили над безводним сульфатом магнію й упарювали. Очищення залишку колонковою xpoмaтoгрaфiєю на силікагелі за допомогою суміші етилацетат:низькокиплячий петролейний ефір (1:1) приводило до одержання 3,1г жовтого масла, яке розчиняли в 20мл ацетонітрилу й обробляли розчином 0,8г (6,4ммоль) дигідрату щавлево ї кислоти в 5мл ацетонітрилу. Осад збирали й промивали діетиловим ефіром з одержанням 1,34г (18%) вказаної в заголовку сполуки у вигляді твердої речовини (tпл 168-169°C). 49. 6-(N,N-Диметиламінокарбоніл)-4-(7-етил-6метил-бензиламіно)-2-метил-1H-бензимідазол 0,7г (1,25ммоль) oкcалaтy 1-бензилоксиметил6-(N,N-диметиламінокарбоніл)-4-(2-етил-6-метилбензиламіно)-2-метил-1H-бензимідазолу розділяли між дихлорметаном і насиченим водним гiдрокарбонатом натрію. Органічний шар відокремлювали й упарювали. Залишок розчиняли в 15мл метанолу й гiдpyвали за допомогою 0,3г 10% Pd/C (70°С, 1бар Н2) протягом 2год. Каталізатор відфільтровували й фільтрат yпapювали. Залишок очищали колонковою xpoмaтoгрaфiєю на силікагелі спочатку за допомогою суміші дихлорметан:метанол (13:1), потім за допомогою суміші етилацетат:триетиламін (9:1). Кристалізація з діі
ДивитисяДодаткова інформація
Назва патенту англійською4-substituted benzimidazoles and their application as gastric secretion inhibitors
Автори англійськоюGrundler Gerhard, Kromer, Wolfgang
Назва патенту російською4-замещенные бензимидазолы и их применение как ингибиторов желудочной секреции
Автори російськоюГрундлер Герхард
МПК / Мітки
МПК: A61P 1/04, C07D 403/06, C07D 235/06, C07D 403/04, C07D 235/08, C07D 235/12, C07D 413/04
Мітки: інгібіторів, 4-заміщені, шлункової, бензимідазоли, застосування, секреції
Код посилання
<a href="https://ua.patents.su/38-79843-4-zamishheni-benzimidazoli-ta-kh-zastosuvannya-yak-ingibitoriv-shlunkovo-sekreci.html" target="_blank" rel="follow" title="База патентів України">4-заміщені бензимідазоли та їх застосування як інгібіторів шлункової секреції</a>
Попередній патент: Пристрій донної частини знімної боєголовки
Наступний патент: Спосіб наплавлення плавким електродом деталей із вуглецевих сталей
Випадковий патент: Спосіб та пристрій для утворення імпульсів тиску шляхом здійснення вибухів










































