Уретани, сечовини, аміди та родинні інгібітори фактора xа
Номер патенту: 107106
Опубліковано: 25.11.2014
Автори: Тарасов Дмітрій Ніколаєвіч, Товбін Дмітрій Гєннадьєвіч, Малахов Дмітрій Вікторовіч
Формула / Реферат
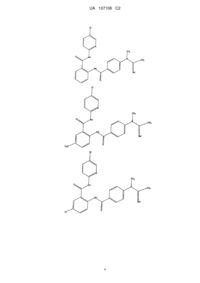
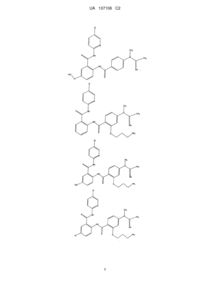
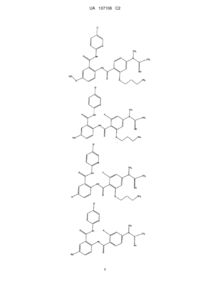
1. Сполука формули І
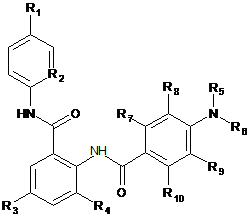 ,
,
де
R1 вибраний з H, -Cl, -F, -Вr, -ОН, -Me, -OMe;
R2 вибраний з СН і N;
R3 і R4 кожний незалежно вибраний з Н, -Сl, -F, -Br, -OH, -Me, -OMe;
R5 вибраний з Н або С1-6алкілу, який при необхідності заміщений гідроксилом або карбоксилом;
R6 вибраний з
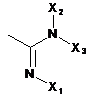 ,
, 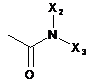 ,
,
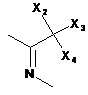 ,
, 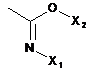 ,
,
де X1, X2, X3 і Х4 кожний незалежно вибраний з Н або С1-6алкілу, який при необхідності заміщений гідроксилом або карбоксилом;
R8, R9 і R10 кожний незалежно вибраний з Н, -Сl, -F, -Br, -OH, -Me, -OMe;
R7 вибраний з Н, -Сl, -F, -Br, -OH, -Me, -OMe або з наступних груп:
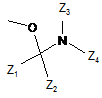 ,
, 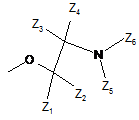 ,
,  ,
,
 ,
, 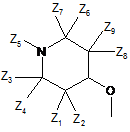 ,
,
де Z1, Z2, Z3, Z4, Z5, Z6, Z7, Z8, Z9 і Z10 кожний незалежно являє собою Н або С1-6алкіл, який при необхідності заміщений гідроксилом або карбоксилом;
або сполука, що має наступну структуру:
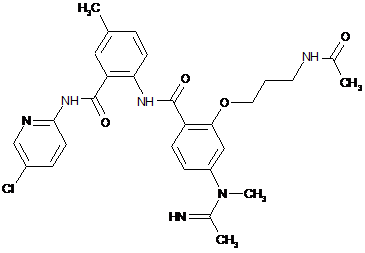 ,
,
або її фармацевтично прийнятна сіль, гідрат або сольват.
2. Сполука за п. 1, що має наступну структуру:
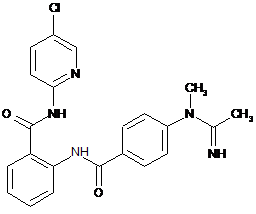 .
.
3. Сполука за п. 1, що має наступну структуру:
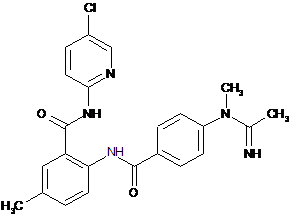 .
.
4. Сполука за п. 1, що має наступну структуру:
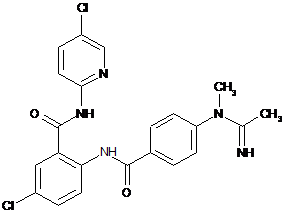 .
.
5. Сполука за п. 1, що має наступну структуру:
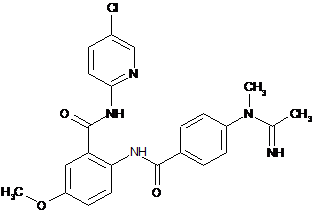 .
.
6. Сполука за п. 1, що має наступну структуру:
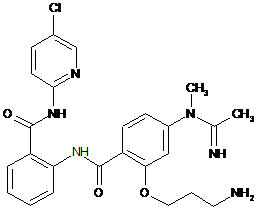 .
.
7. Сполука за п. 1, що має наступну структуру:
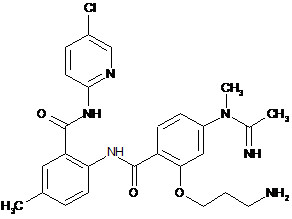 .
.
8. Сполука за п. 1, що має наступну структуру:
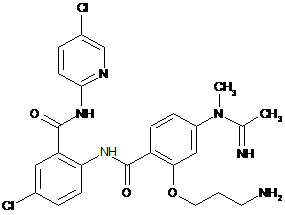 .
.
9. Сполука за п. 1, що має наступну структуру:
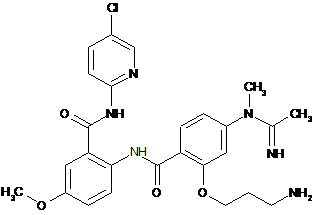 .
.
10. Сполука за п. 1, що має наступну структуру:
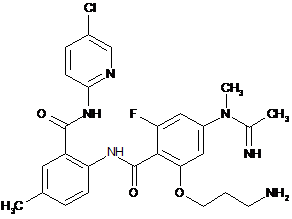 .
.
11. Сполука за п. 1, що має наступну структуру:
 .
.
12. Сполука за п. 1, що має наступну структуру:
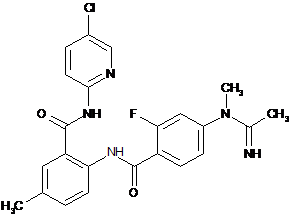 .
.
13. Сполука за п. 1, що має наступну структуру:
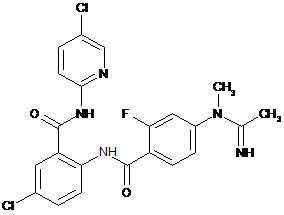 .
.
14. Сполука за п. 1, що має наступну структуру:
 .
.
15. Сполука за п. 1, що має наступну структуру:
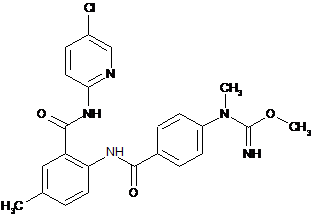 .
.
16. Сполука за п. 1, що має наступну структуру:
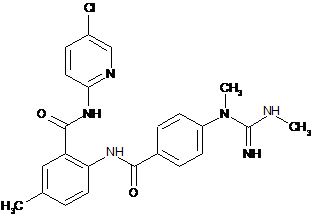 .
.
17. Сполука за п. 1, що має наступну структуру:
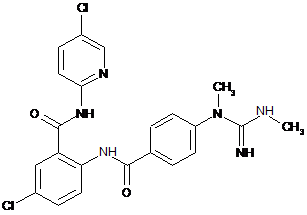 .
.
18. Сполука за п. 1, що має наступну структуру:
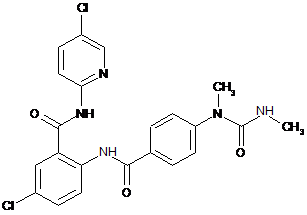 .
.
19. Сполука за п. 1, що має наступну структуру:
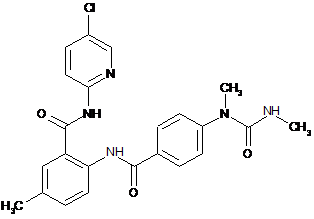 .
.
20. Сполука за п. 1, що має наступну структуру:
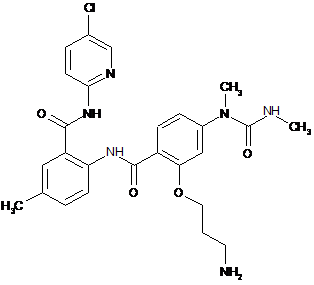 .
.
21. Сполука за п. 1, що має наступну структуру:
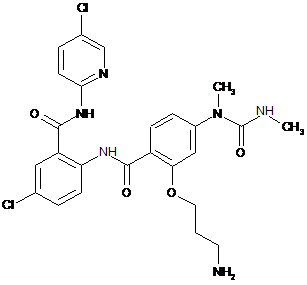 .
.
22. Фармацевтична композиція для профілактики або лікування стану ссавця, який характеризується небажаним тромбозом, що містить терапевтично ефективну кількість сполуки за будь-яким з пунктів 1-21.
23. Спосіб профілактики або лікування стану ссавця, який характеризується небажаним тромбозом, при здійсненні якого вводять терапевтично ефективну кількість сполуки за будь-яким з пунктів 1-21.
24. Спосіб за пунктом 23, де зазначений стан являє собою гострий коронарний синдром, інфаркт міокарда, нестабільну стенокардію, рефрактерну стенокардію, тромбози, спричинені післятромболітичною терапією або коронарною ангіопластикою, гострий ішемічний цереброваскулярний синдром, емболічний інсульт, тромботичний інсульт, ішемічні приступи, що минають, венозний тромбоз, глибокий венозний тромбоз, легеневий ембол, коагулопатію, розсіяну внутрішньосудинну коагуляцію, тромбоцитопенічний акроангіотромбоз, облітеруючий тромбангіїт, тромбозні захворювання, пов'язані з гепариноіндукованою тромбоцитопенією, тромбічні ускладнення, пов'язані зі штучним кровообігом, тромбічні ускладнення, пов'язані з протезними пристроями.
25. Спосіб впливу на коагуляцію крові або плазми за допомогою інгібування фактора Xa, при здійсненні якого в зразок вводять сполуку за будь-яким з пунктів 1-21.
Текст
Реферат: Даний винахід стосується нового класу сполук, їх фармацевтично прийнятних солей і їх фармацевтично прийнятних композицій, які ефективні як селективні інгібітори фактора Хa як в ізольованому стані, так і в комплексі з іншими білками. Нові сполуки, описані у даному винаході, можуть використовуватися для лікування та профілактики хвороб, таких як гострий коронарний синдром, інфаркт міокарда, нестабільна стенокардія, рефрактерна стенокардія, тромбози, спричинені післятромболітичною терапією або коронарною ангіопластикою, гострий ішемічний цереброваскулярний синдром, емболічний інсульт, тромболітичний інсульт і ряд інших хвороб, у людини та ссавців, пов'язаних зі зсілістю крові. UA 107106 C2 (12) UA 107106 C2 UA 107106 C2 5 10 15 20 25 30 35 40 45 50 55 60 Область техніки, до якої відноситься винахід Даний винахід відноситься до нового класу речовин, ефективних і селективних інгібіторів фактора Xa, як в ізольованому стані, так і в комплексі з іншими білками. Даний винахід так само відноситься до нового класу речовин, їх фармацевтично прийнятним солям, їх фармацевтично прийнятним композиціям, які можуть бути використані як ефективні та селективні інгібітори згортаємості крові у людини та інших ссавців. Даний винахід так само відноситься до нових методів використання нових класів речовин, для лікування хвороб, пов'язаних з порушенням згортаємості крові в людини та інших ссавців. Рівень техніки Контроль над кровотечею здійснюється або хірургічними методами, або впливом на фізіологічний стан кровоносних судин, або на згортаємость крові. Даний винахід стосується згортаємості крові і її ролі в підтримці працездатності людського організму при ушкодженнях, запаленнях, хворобах, природних дефектах, дисфункціях і інших проблемах. Тромбін - ключовий білок у процесі згортаємості крові. Тромбін відіграє головну роль у процесі тромбоутворення завдяки своїй можливості каталізувати перетворення фібриногену у фібрин. Прямі та непрямі інгібітори тромбіну донедавна були об'єктами різних підходів до контролю згортаємості крові. Claeson, G., "Synthetic Peptides and Peptidomimetics as Substrates and Inhibitors of Thrombm and Other Proteases in the Blood Coagulation System", Blood Coag. Fibrinol. 5, 411-436 (1994). Деякі класи ліків антикоагулянтів, використовуваних у клінічній практиці, є прямими та непрямими інгібіторами тромбіну (гепарин, низькомолекулярний гепарин, кумарини і т.д.). Протромбіназний комплекс, що включає в себе білок (фактор) Xa, перетворює профермент протромбін в активований тромбін. Фактор Xa відноситься до класу серинових протеаз і утворюється активацією з білка (фактора) X. На відміну від тромбіну, який діє на безліч білківсубстратів і специфічних рецепторів, білок Xa, очевидно, діє тільки на єдиний субстрат, а саме на протромбін. Оскільки одна молекула білка Xa здатна генерувати до 138 молекул тромбіну, то прямі інгібітори білка Xa, як інгібітори утворення тромбіну, можуть бути використані як ефективний спосіб контролю згортаємості крові. Тому, цілком очевидно, що речовини, які селективно інгібують білок Xa можуть бути використані для діагностики згортаємості крові "in vitro", а так само в якості ліків при захворюваннях, пов'язаних зі згортаємостю крові. Відомо, що поліпептиди, отримані із крові деяких паразитів, можуть бути ефективними та селективними інгібіторами фактора Xa. Патент США 4588587 описує антикоагулянтну активність слини мексиканської п'явки, Haementeria officinalis. Основна активна речовина слини цієї п'явки поліпептид антистатин, інгібітор фактора Xa. Інший ефективний і селективний інгібітор фактора Xa, що називається кліщовий антикоагулянтний пептид (ТАР), був отриманий з екстракту тулуба м'якого кліща ornithidoros moubata. Інгібітори білка Xa, які не являються поліпептидами, були отримані різними групами дослідників: Tidwell, R. R. et al., "Strategies for Anticoagulation With Synthetic Protease Inhibitors. Xa Inhibitors Versus Thrombin Inhibitors", Thromb. Res., 19, 339-349 (1980); Turner, A. D. et al.,"pamidino Esters as Irreversible Inhibitors of Factor Ixa and Xa and Thrombin", Biochemistry, 25, 49294935 (1986); Hitomi, Y. et al.,"Inhibitory Effect of New Synthetic Protease Inhibitor (FUT-175) on the Coagulation System", Haemostasis, 15, 164-168 (1985); Sturzebecher, J. et al., "Synthetic Inhibitors of Bovine Factor Xa and Thrombin. Comparison of Their Anticoagulant Efficiency", Thromb. Res., 54, 245-252 (1989); Kam, C. M. et al.,"Mechanism Based Isocoumarin Inhibitors for Trypsin and Blood Coagulation Serine Proteases: New Anticoagulants", Biochemistry, 27, 2547-2557 (1988); Hauptmann, J. et al.,"Conzparisofz of the Anticoagulant and Antithrombotic Effects of Synthetic Thrombin and Factor Xa Inhibitors", Thromb. Haemost, 63, 220-223 (1990); і т.д. Інші групи дослідників одержали інгібітори фактора Xa, які є невеликими органічними молекулами, такими як азотовмісні гетероцикли, що мають у своєму складі заміщені амідинові групи із двома функціональними групами, здатні зв'язуватися з білком Xa у двох активних сайтах білка. Наприклад, WO 98/28269 описує піразол з кінцевими C(=NH)-NH2 групами; WO 97/21437 описує бензамідазол, заміщений групами, які з'єднані з нафталіновою групою прямо або через ланцюг алкілів і, -С(=0) або -S(=0)2 групи; WO 99/10316 описує сполуки, що мають 4феніл n-алкіламідино-піперидин, з'єднаний з 3-амідинофенільною групою через карбоксіалкіленаміно групу; a EP 798295 описує сполуки, що мають у своєму складі 4-феноксі-nалкіламідино-піперидинову групу, з'єднану з амідиновою групою через заміщені або не заміщені сульфонаміди. Дотепер існує необхідність в ефективних активних агентах, що регулюють процес згортаємості крові для запобігання та лікування формування тромбів і інших патологічних 1 UA 107106 C2 5 10 процесів у кровоносних судинах, обумовлених формуванням тромбіну, таких як запалення та звуження судин. На практиці, як і раніше, існує гостра необхідність у сполуках, які будуть селективно інгібувати білок Xa. Сполуки, які зв'язуються з білком Xa сильніше, чим з білком тромбіном, особливо переважно, якщо ці сполуки мають гарну біодоступність та розчинність. Суть винаходу Таким чином, першим аспектом винаходу є нові сполуки загальної формули І Де R1 вибраний з H, -Cl, -F, -Br, -OH, -Me, -OMe; R2 вибраний з CH і N; R3 і R4 кожний незалежно вибраний з H, -Cl, -F, -Br, -OH, -Me, -OMe; R5 вибраний з H або С1-С6 алкілу, який також може містити гідроксильні, карбоксильні або складноефірні групи; R6 вибраний з 15 2 UA 107106 C2 де X1, Х2, Х3 і Х4 кожний незалежно вибраний з H або С1-С6 алкілу, який також може містити гідроксильні, карбоксильні або складноефірні групи; R8, R9 і R10 кожний незалежно вибраний з H, -Cl, -F, -Br, -OH, -Me, -OMe; R7 вибраний з H, -Cl, -F, -Br, -OH, -Me, -OMe або з наступних груп: 5 де Z1, Z2, Z3, Z4, Z5, Z6, Z7, Z8, Z9 і Ζ10 кожний незалежно являє собою H або С1-С6 алкіл, який також може містити гідроксильні, карбоксильні або складноефірні групи; або їх фармацевтично прийнятний ізомер, сіль, гідрат, сольват і пролікарська похідна. Особливо переважними сполуками є сполуки, обрані із групи, що містить: 3 UA 107106 C2 4 UA 107106 C2 5 UA 107106 C2 6 UA 107106 C2 7 UA 107106 C2 8 UA 107106 C2 5 10 15 20 25 Наступним аспектом винаходу є фармацевтична композиція для профілактики або лікування стану ссавця, який характеризується небажаним тромбозом, що містить терапевтично ефективну кількість сполуки за винаходом. Фармацевтична композиція крім активного інгредієнта, яким є сполука загальної формули (І), містить фармацевтично прийнятний носій, розчинник або розріджувач, якими, зокрема, можуть бути ті, що зазначені в Ремінгтон "Наукова та практична фармацевтика" (Remington's "The Science and Practice of Pharmacy"), Кірк Отмер "Енциклопедія хімічної технології" (Kirk Othmer's "Encyclopedia of Chemical Technology"), монографія "Фармакологічні основи терапії" ("The Pharmacological Basis of Therapeutics", 3 видання). Ще одним аспектом винаходу є спосіб профілактики або лікування стану ссавця, який характеризується небажаним тромбозом, що включає введення терапевтично ефективної кількості сполуки формули (І). Стани ссавця, які характеризуються небажаним тромбозом, є добре відомими, зокрема вони являють собою гострий коронарний синдром, інфаркт міокарда, нестабільну стенокардію, рефрактерну стенокардію, тромбози, спричинені посттромболітичною терапією або коронарною ангіопластикою, гострий ішемічний цереброваскулярний синдром, емболічний інсульт, тромботичний інсульт, ішемічні приступи, що минають, венозний тромбоз, глибокий венозний тромбоз, легеневий ембол, коагулопатію, розсіяну внутрішньосудинну коагуляцію, тромбоцитопенічний акроангіотромбоз, облітеруючий тромбангіїт, тромбозні захворювання, пов'язані з гепариніндукованою тромбоцитопенією, тромбічні ускладнення, пов'язані зі штучним кровообігом, тромбічні ускладнення, пов'язані з протезними пристроями. Нарешті, ще одним аспектом винаходу є спосіб інгібування коагуляції біологічних зразків, що включає стадію введення в зразок сполуки формули (І). Розкриття винаходу Синтез хімічних речовин Сполуки, описані загальною формулою (І), можуть бути синтезовані будь-яким підходящим методом, наприклад, приєднанням відповідного аміну (II) до похідної відповідної карбонової кислоти (III) 9 UA 107106 C2 5 10 15 у присутності підходящих агентів поєднання, таких як 1,1'-карбонілдиімідазол (CDI), дициклогексилкарбодиімід (DCC), N-(3-диметиламінооприл)-N'-етилкарбодиімід гідрохлорид (EDCI), або інших подібних реагентів. Формування амідного зв'язку може бути так само забезпечено взаємодією хлорангідридів (IV) з амінами (II). Хлорангідриди (IV) можуть бути отримані з відповідних карбонових кислот (III) обробкою підходящим реагентом, таким як SOCl2 або POCl3. Хлорангідрид (IV) відповідної карбонової кислоти легко реагує з амінами (II), даючи на виході цільову сполуку (І). Аміни (II) можуть бути отримані відновленням відповідних нітросполук (V) при підходящих умовах. У якості агентів, що відновлюють, можна використовувати, наприклад, SnCl2 або гідрування в присутності нікелю Ренея. Нітросполуки (V) можуть бути синтезовані з відповідних амінів (VI) і нітрозаміщених карбонових кислот (VII). 10 UA 107106 C2 5 10 15 Карбонові кислоти (VII) перетворюються у відповідні хлорангідриди (VIII) обробкою підходящим реагентом, таким як SOCl2 або POCl3. Хлорангідриди (VIII) потім гладко реагують із амінами (VI), утворюючи нітросполуки (V). Альтернативним методом синтезу амідного зв'язку може також бути реакція карбонової кислоти (VII) з аміном (VI) у присутності підходящих агентів поєднання, таких як DCC, EDCI, CDI. У більшості випадків згадані вище реакції, відбуваються без проблем з гарним виходом. Проте, заміщені карбонові кислоти з деякими радикалами R5 і R6 (III) не реагують із амінами (II). У цьому випадку для формування амідного зв'язку слід використовувати відповідні захисні групи, при цьому замісники R5 і R6 вводяться в молекулу вже після здійснення формування амідного зв'язку. Заміщені похідні сечовин (IIIa) можуть бути синтезовані шляхом обробки відповідних метилових або етилових ефірів аміноарилкарбонової кислоти (XI) CDI і аміну X2X3NH. Потім етиловий або метиловий ефіри гідролізуються в лужному середовищі, що приводить до утворення бажаних сполук: Альтернативним методом амінокислота (IIIb) може бути перетворена у відповідну похідну сечовини IIIc шляхом взаємодії з відповідним ізоціанатом або ціанатом натрію (при Х2=Н). 20 Слід зазначити, що у випадку, коли X2=H відповідна похідна сечовини (IIIс) не взаємодіє з аміном (II) при дії DCC, CDI і EDCI, тому для формування амідного зв'язку необхідно спочатку синтезувати захищений амін (Ia) із захисною групою Y. 11 UA 107106 C2 5 10 У якості захисної можна використовувати, наприклад, трифторацетильну групу. Захищений амін (Ia) може бути синтезований з відповідної захищеної амінокислоти (IIId) взаємодією з аміном (II) у присутності підходящого зв'язуючого агента. Зняття захисної групи може здійснюватися під дією підходящих реагентів, у випадку трифторацетильної групи для цих цілей можна використовувати лужний гідроліз. Амін (Ib) потім може бути трансформований у відповідну похідну сечовини (Ic) підходящим способом, наприклад, послідовною обробкою аміну (Ib) реагентом CDI і аміном X2X3NH або у випадку, коли Х3=Н, обробкою відповідним ізоціанатом OCN-Z2. Амін (Ib) може бути перетворений в амідин (Id) взаємодією з нітрилом NC-CZ2Z3Z4 у присутності сухої газоподібної HCl. Амідин (Id) може бути в подальшому алкілований або 12 UA 107106 C2 арилований до амідину (Ie) відповідним алкіл- або арил-галогенідом X1-HaI або іншим реагентом з підходящою групою, що відходить. 5 10 15 20 25 30 Приклад 1 Реакція 1 1,9 г 2-нітробензойної кислоти кип'ятиться в 20 мл SOCl2 зі зворотним холодильником із хлоркальцієвою трубкою протягом 4-х годин, після чого отриманий розчин охолоджується, упарюється на роторному випарнику, двічі повторно упарюється з безводним ТГФ, залишок розчиняється в 10 мл ТГФ, отриманий розчин протягом 30 хвилин краплинно додається до розчину, що перемішується, 1,5 г 2-аміно-5-хлорпіридину в 20 мл ТГФ. Через 5 годин реакційна суміш упарюється, залишок розчиняється в 30 мл хлороформу, промивається насиченим водяним розчином NaHCO3, хлороформний екстракт упарюється, залишок наноситься на колонку 40x150 мм, наповнену 30-50 мкм силікагелем. Продукт елююється хлороформом. Детектування здійснюється за допомогою УФ-комірки, на довжині хвилі 280 нм. Поглинаючі УФ випромінювання фракції збираються, чистота продукту контролюється методом тонкошарової хроматографії в хлороформі. Rf продукту становить 0,4, Rf вихідного 2-аміно-5-хлорпіридину становить 0,7. 2-нітробензойна кислота в хлороформі залишається на старті (Rf
ДивитисяДодаткова інформація
Назва патенту англійськоюUrethanes, ureas, amidines and related inhibitors of factor xa
Автори англійськоюTovbin, Dmitry Gennadievich, Tarasov, Dmitry Nikolaevich, Malakhov, Dimitry Viktorovich
Автори російськоюТовбин Дмитрий Геннадьевич, Тарасов Дмитрий Николаевич, Малахов Дмитрий Викторович
МПК / Мітки
МПК: C07D 213/75, A61K 31/16, A61K 31/44, A61K 31/17, A61P 7/02
Мітки: фактора, уретани, інгібітори, аміди, сечовини, родинні
Код посилання
<a href="https://ua.patents.su/39-107106-uretani-sechovini-amidi-ta-rodinni-ingibitori-faktora-xa.html" target="_blank" rel="follow" title="База патентів України">Уретани, сечовини, аміди та родинні інгібітори фактора xа</a>
Попередній патент: Спосіб визначення орієнтації рухомого об’єкта та пристрій для його реалізації
Наступний патент: Спосіб лікування хворих з синдромом “діабетична стопа”
Випадковий патент: Спосіб визначення струму витоку