Протигрибкові похідні 5,6-дигідро-4-[(дифторетил)феніл]-4н-піроло[1,2-a][1,4]бензодіазепіну і 4-(дифторетил)феніл-6н-піроло[1,2-a][1,4]бензодіазепіну
Номер патенту: 107963
Опубліковано: 10.03.2015
Автори: Меерпоель Лівен, де Віт Келлі, Мес Луї Жюль Роже Марі
Формула / Реферат
1. Сполука формули (І)
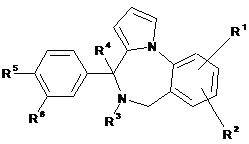 (I)
(I)
або її стереоізомерна форма, де
R1 є воднем, хлором або фтором;
R2 є воднем, хлором, фтором або метилом;
R3 і R4 є воднем;
або R3 і R4, узяті разом, утворюють зв'язок;
R5 є 1,1-дифторетилом, і R6 є воднем або фтором;
або R5 є воднем або фтором, і R6 є 1,1-дифторетилом;
або її фармацевтично прийнятна сіль або сольват.
2. Сполука за п. 1, де R1 є хлором або фтором.
3. Сполука за п. 1, де R1 є хлором або фтором; і де R2 є хлором, фтором або метилом.
4. Сполука за п. 1, де R1 є хлором або фтором;
R2 є воднем, хлором, фтором або метилом;
R3 і R4, узяті разом, утворюють зв'язок;
R5 є 1,1-дифторетилом, і R6 є воднем або фтором;
або R5 є воднем або фтором, і R6 є 1,1-дифторетилом.
5. Сполука за п. 1, де R1 є хлором або фтором;
R2 є воднем;
R3 і R4, узяті разом, утворюють зв'язок;
R5 є 1,1-дифторетилом;
R6 є воднем.
6. Сполука за п. 1, де
R1 знаходиться в 7-ому положенні і є хлором або фтором; і
R2 знаходиться з будь-яких інших положеннях і є воднем, хлором, фтором або метилом.
7. Сполука за п.1, де сполука є 7-хлор-4-[4-(1,1-дифторетил)феніл]-6Н-піроло[1,2-а][1,4]бензодіазепіном.
8. Фармацевтична композиція, що містить фармацевтично прийнятний носій і, як активний інгредієнт, терапевтично ефективну кількість сполуки, вказаної у будь-якому з пп. 1-7.
9. Сполука, вказана в будь-якому з пп. 1-7, для застосування як лікарського засобу.
10. Сполука, вказана в будь-якому з пп. 1-7, для застосування при лікуванні або профілактиці грибкової інфекції.
11. Сполука для застосування за п. 10, де грибкова інфекція викликана одним або декількома грибами, вибраними з групи, що складається з Candida spp.; Aspergillus spp.; Cryptococcus neoformans; Sporothrix schenckii, Epidermophyton floccosum; Microsporum spp.; Trichophyton spp.; Fusarium spp.; Rhizomucor spp.; Mucor circinelloides; Rhizopus spp.; Malassezia furfur; Acremonium spp.; Paecilomyces; Scopulariopsis; Arthrographis spp.; Scytalidium; Scedosporium spp.; Trichoderma spp.; Penicillium spp.; Penicillium marneffei і Blastoschizomyces.
12. Сполука для застосування за п. 10, де грибкова інфекція викликана одним або декількома грибами, вибраними з групи, що складається з Candida parapsilosis; Aspergillus spp.; Cryptococcus neoformans; Sporothrix schenckii; Epidermophyton floccosum; Microsporum spp.; Trichophyton spp.; Fusarium spp.; Rhizomucor spp.; Mucor circinelloides; Rhizopus spp.; Acremonium spp.; Paecilomyces; Scopulariopsis; Arthrographis spp.; Scytalidium; Scedosporium spp.; Trichoderma spp.; Penicillium spp.; Penicillium marneffei і Blastoschizomyces.
13. Сполука для застосування за п. 10, де грибкова інфекція викликана одним або декількома грибами, вибраними з групи, що складається з Microsporum canis, Trichophyton mentagrophytes, Trichophyton rubrum і Aspergillus fumigatus.
Текст
Реферат: Даний винахід стосується нових сполук формули (І) UA 107963 C2 (12) UA 107963 C2 R R R 1 N 4 5 N R 1 6 R 2 3 4 3 R 5 6 2 , (I) де R , R , R , R , R і R мають значення, визначені в пунктах формули винаходу. Сполуки за даним винаходом активні головним чином відносно дерматофітів і системних грибкових інфекцій. Крім того, винахід стосується способів отримання таких нових сполук, фармацевтичних композицій, що містять вказані сполуки як активний інгредієнт, а також застосування вказаних сполук як лікарського засобу. UA 107963 C2 5 10 15 20 25 30 35 40 45 50 55 60 ОБЛАСТЬ ТЕХНІКИ Даний винахід відноситься до нових протигрибкових похідних 5,6-дигідро-4[(дифторетил)феніл]-4H-пірроло[1,2-а][1,4]бензодіазепіна і 4-(дифторетил)феніл-6H-пірроло[1,2а][1,4]бензодіазепіна, головним чином активним відносно дерматофітів і системних грибкових інфекцій. Крім того, винахід відноситься до способів отримання таких нових сполук, фармацевтичних композицій, що містять вказані сполуки як активний інгредієнт, а також до застосування вказаних сполук як лікарського засобу. РІВЕНЬ ТЕХНІКИ Дерматофіт є загальною назвою для групи з 3 видів грибів, що зазвичай викликають шкірні захворювання у тварин і людини. Це анаморфні гриби (безстатеві або недосконалі гриби) родів: Microsporum, Epidermophyton і Trichophyton. Існує близько 40 видів цих 3 родів. Дерматофіти викликають шкірні інфекції, інфекції волосся і нігтів через їх здатність отримувати живильні речовини з ороговілого матеріалу. Організми колонізують кератинові тканини, і запалення викликається відповіддю господаря на метаболічні побічні продукти. Вони, як правило, обмежені роговим шаром епідермісу через їх нездатність проникати в життєздатні тканини імунокомпетентного господаря. Проте, інколи організми проникають у підшкірні тканини, призводячи до розвитку керіона. Інвазія викликає відповідну реакцію господаря, в діапазоні від легкої до сильної. За наявними даними, кислотні протеїнази, еластаза, кератинази і інші протеїнази, виступають як чинники вірулентності. Системні грибкові інфекції (SFI) є небезпечними для життя захворюваннями, які найчастіше вражають пацієнтів з послабленим імунітетом, зазвичай у результаті терапевтичного втручання при лікуванні злоякісних захворювань. Кількість SFI в сучасних лікарнях продовжує зростати, а кількість різних грибів, залучених в SFI, є значною і продовжує зростати. Не дивлячись на безліч випадків інвазивного кандидозу і аспергілезу спостерігається підвищена частота інфекцій, викликаних іншими плісневими грибами, такими як Scedosporium apiospermum, Fusarium spp. і Zygomycetes, Rhizopus і Mucor spp. Ефективність терапевтичних засобів для лікування всіх цих інфекцій дуже висока, відповідно, необхідно мати дуже широкий спектр активності. В останні декілька десятиліть для лікування SFI використовували ітраконазол, флуконазол, кетоконазол і внутрішньовенний або ліпосомальний Амфотерицин В, і всі ці засоби мають свої обмеження відносно спектру, безпеки і простоти введення. Зовсім нещодавно було випробуване і представлене на ринку третє покоління азолів, що поліпшують лікування у відділеннях інтенсивної терапії. Вориконазол (Vfend™) і позаконазол (Noxafil™) показали значне поліпшення при лікуванні інвазивної SFI, що загрожувала життю, такої як кандидоз, аспергілез і інфекцій, викликаних видами Fusarium, у клінічних відповідних дозах. Крім того, позаконазол показав ефективність відносно інфекцій, викликаних Zygomycetes spp, що розвивається. Ехінокандіни, такі як анідулафунгін, каспофунгін і мікафунгін, які не є конкурентними інгібіторами синтезу 1,3-β-глюкана у клітинних стінках грибів, проявляють високу ефективність відносно Candida spp. і Aspergillus spp., але не активні відносно Cryptococcus, Fusarium або Zygomycetes spp. Зі всіх протигрибкових засобів, азоли як і раніше є унікальним класом сполук, що демонструють широкий протигрибковий спектр, шляхом інгібування 14-α-деметилази, ферменту, що має істотне значення для біосинтезу ергостерину в грибах. Оніхомікоз є найбільш поширеним захворюванням нігтів і складає близько половини всіх захворювань нігтів. Поширеність оніхомікозу складає близько 6-8 % у дорослого населення. Збудники оніхомікозу включають дерматофіти, Candida і плісневі гриби, що не відносяться до дерматофітів. Дерматофіти є грибами, що найчастіше викликають оніхомікоз у західних країнах з помірним кліматом, тоді як Candida і плісневі гриби, що не відносяться до дерматофітів, частіше викликають захворювання в тропіках і субтропіках. Trichophyton rubrum є найбільш поширеним дерматофітом, що викликає оніхомікоз. Іншими дерматофітами, які можуть викликати захворювання, є Trichophyton interdigitale, Epidermophyton floccosum, Trichophyton violaceum, Microsporum gypseum, Trichophyton tonsurans, Trichophyton soudanense і Trichophyton verrucosum. Інші збудники включають Candida і плісневі гриби, що не відносяться до дерматофітів, зокрема, покоління плісневих грибів Scytalidium (також Neoscytalidium), Scopulariopsis і Aspergillus. 5,6-дігідро-4H-пірроло[1,2-а][1,4]бензодіазепіни були описані в J. Chem. Soc.(C), 2732-2734 (1971); J. Heterocyclic Chem., 13, 711-716 (1976); і J. Heterocyclic Chem., 16, 241-244 (1979). Сполуки, описані в цих посиланнях, усі мають різні заміщення у фенільній групі в 4-му положенні і, крім того, ні в одному з цих посилань не повідомлялось про біологічні активності. У WO02/34752 описані 4-заміщені 5,6-дигідро-4H-пірроло[1,2-а][1,4]бензодіазепіни як новий клас протигрибкових сполук. Проте, у WO02/34752 конкретно не описаний даний приклад заміщення у фенільній групі в 4-му положенні. 1 UA 107963 C2 5 10 15 20 25 30 35 40 45 50 Багато лікарських сполук, маючи при цьому бажаними терапевтичними властивостями, використовуються неефективно внаслідок їх поганої розчинності у воді. Так, наприклад, у разі, коли такі сполуки вводять перорально, лише невелика частина препарату потрапляє в кров під час проходження через шлунково-кишковий тракт. Як результат, для досягнення необхідного поглинання лікарського препарату може виявитись потрібним введення високих доз лікарської сполуки, щоб продовжити період прийому препарату, або здійснення частих ведень лікарської сполуки. Дійсно, погана розчинність і, відповідно, низька біодоступність лікарського препарату можуть стати причиною використання альтернативного лікарського препарату, можливо, препарату з небажаними побічними ефектами або препарату, що вимагає інвазивного введення (наприклад, шляхом ін'єкції або інфузії), які будуть використовуватись замість погано розчинного препарату. Тому метою даного винаходу є отримання більш біодоступних сполук з широким протигрибковим спектром або отримання придатних альтернативних сполук з досить високою терапевтичною ефективністю і достатньо низькими токсичністю або іншими побічними ефектами. Несподівано виявлено, що протигрибкові сполуки за даним винаходом або частина сполук за даним винаходом можуть мати покращені властивості метаболічної стабільності, покращеними PK (фармакокінетичними) властивостями, підвищеною розчинністю, зменшеною потребою в цитохромі Р450 або підвищеною біодоступністю в порівнянні із сполуками, описаними у відомому рівні техніки. Сполуки за даним винаходом можуть бути використані як інгібітори скваленепоксидази. Відповідно, об'єктом даного винаходу є нові сполуки з протигрибковою дією для подолання або поліпшення, принаймні, одного з недоліків попереднього рівня техніки, або їх придатна альтернатива. СУТЬ ВИНАХОДУ Було виявлено, що сполуки за даним винаходом можуть бути використані як протигрибкові сполуки. Даний винахід відноситься до нових сполук формули (I): і їх стереоізомерним формам, де 1 R є воднем, хлором або фтором; 2 R є воднем, хлором, фтором або метилом; 3 4 R і R є воднем; 3 4 або R і R , взяті разом, утворюють зв'язок; 5 6 R є 1,1-дифторетил, і R є воднем або фтором; 5 6 або R є воднем або фтором, і R є 1,1-дифторетилом; і їх фармацевтично прийнятним солям і сольватам. Даний винахід також відноситься до способів отримання сполук формули (I) і фармацевтичних композицій, що містять ці сполуки. Дані сполуки є ефективними засобами для боротьби з грибками in vivo. Нові сполуки, описані в даному винаході, можуть бути використані при лікуванні і профілактиці інфекцій, викликаних дерматофітами, системними грибковими інфекціями і оніхомікозом. Нові сполуки, описані в даному винаході, можуть бути активні відносно широкого спектру грибів, таких як Candida spp., наприклад, Candida albicans, Candida glabrata, Candida krucei, Candida parapsilosis, Candida kefyr, Candida tropicalis; Aspergillus spp., наприклад, Aspergillus fumigatus, Aspergillus niger, Aspergillus flavus; Cryptococcus neoformans; Sporothrix schenckii; Epidermophyton floccosum; Microsporum spp., наприклад, Microsporum canis, Microsporum gypseum; Trichophyton spp., наприклад, Trichophyton mentagrophytes, Trichophyton rubrum, Trichophyton quinckeanum, Trichophyton tonsurans, Trichophyton verrucosum, Trichophyton violaceum, Trichophyton interdigitale, Trichophyton soudanense; Fusarium spp., наприклад, Fusarium solani, Fusarium oxysporum, Fusarium proliferatum, Fusarium verticillioides; Rhizomucor 2 UA 107963 C2 5 10 15 20 25 30 35 40 45 50 spp., наприклад, Rhizomucor miehei, Rhizomucor pusillus; Mucor circinelloides; Rhizopus spp., наприклад, Rhizopus oryzae, Rhizopus microspores; Malassezia furfur; Acremonium spp.; Paecilomyces; Scopulariopsis; Arthrographis spp.; Scytalidium; Scedosporium spp., наприклад, Scedosporium apiospermum, Scedosporium prolificans; Trichoderma spp.; Penicillium spp.; Penicillium marneffei; Blastoschizomyces. Зважаючи на вищезгадану фармакологію сполук за даним винаходом, витікає, що вони придатні для застосування як лікарський засіб. Крім того, винахід відноситься до сполуки, що відповідає загальній формулі (I), її стереоізомерним формам і фармацевтично прийнятним аддитивним солям і сольватам, для використання при лікуванні і профілактиці грибкових інфекцій. Однією з переваг сполук або частини сполук за даним винаходом може бути їх підвищена біодоступність, покращені властивості метаболічної стабільності, покращені фармакокінетичні властивості, знижене інгібування каналу HERG або знижена потреба в цитохромі Р450 у порівнянні із сполуками, описаними в попередньому рівні техніки. Даний винахід описаний далі. У подальших розділах винаходу різні аспекти винаходу визначені детальніше. Кожен визначений таким чином аспект може бути об'єднаний з будь-яким іншим аспектом або аспектами, якщо конкретно не вказане інше. Зокрема, будь-яка ознака, вказана як бажана або вигідна, може бути об'єднана з будь-якою іншою ознакою або ознаками, позначеними як бажані або вигідні. ДЕТАЛЬНИЙ ОПИС Хімічні назви сполук за даним винаходом були дані відповідно до правил номенклатури, погоджених з Chemical Abstracts Service (Хімічна реферативна служба), використовуючи номенклатурне програмне забезпечення (ACD/Name product version 10,01; Build 15494, 1 Dec 2006) компанії Advanced Chemical Development, Inc. У разі таутомерних форм повинно бути зрозуміло, що інші, не описані таутомерні форми, також включені в обсяг даного винаходу. Атоми в трициклических системах пронумеровані, як показано на наступній формулі (XX): Слід мати на увазі, що деякі із сполук формули (I) і їх фармацевтично прийнятні солі і сольвати можуть мати один або декілька центрів хіральності і існують у вигляді стереоізомерних форм. Вище і далі термін "сполуки формули (I)" має на увазі включення аддитивних солей, сольватів і стереоізомерів. Термін "стереоізомери", "стереоізомерні форми" або "стереохімічно ізомерні форми", вище або далі в цьому документі, використовуються взаємозамінно. Винахід включає всі стереоізомери сполуки формули (I), або у вигляді чистих стереоізомерів, або у вигляді суміші двох або більше стереоізомерів. Енантіомери є стереоізомерами, які є дзеркальними відображеннями один одного, що не накладаються. Суміш 1:1 пари енантіомерів є рацематом або рацемічною сумішшю. Діастереомери (або діастереоізомери) є стереоізомерами, які не є енантіомерами, тобто вони не є дзеркальними відображеннями один одного. Якщо сполука містить подвійний зв'язок, то замісники можуть бути в E або Z конфігурації. Якщо сполука містить дизаміщену циклоалкільну групу, замісники можуть знаходитись у цис- або транс-конфігурації. Таким чином, винахід включає енантіомери, діастереомери, рацемати, E-ізомери, Z-ізомери, цис-ізомери, транс-ізомери і їх суміші, коли це хімічно можливо. Абсолютна конфігурація визначається відповідно до системи Кана-Інгольда-Прелога. Конфігурацію асиметричного атома позначають як R або S. Індивідуальні сполуки, абсолютна конфігурація яких невідома, можуть бути позначені як (+) або (-), залежно від напрямку, в якому вони обертають площину поляризованого світла. Коли конкретний стереоізомер визначений, це означає, що вказаний стереоізомер, по суті, вільний, тобто має відношення до менше ніж 50 %, бажано, менше 20 %, бажаніше менше ніж 10 %, ще бажаніше менше ніж 5 %, зокрема, менше ніж 2 %, і найбажаніше менше ніж 1 % інших 3 UA 107963 C2 5 10 15 20 25 30 35 40 45 50 55 60 ізомерів. Таким чином, коли сполука формули (I), наприклад, вказана як (R), це означає, що сполука, в основному, не містить (S)-ізомер; коли сполука формули (I), наприклад, вказана як E, це означає, що сполука, в основному, не містить Z-ізомер, коли сполука формули (I), наприклад, вказана як цис, це означає, що сполука, в основному, не містить транс-ізомер. Солі сполук формули (I) для терапевтичного застосування є солями, в яких протиіон є фармацевтично прийнятним. Проте солі кислот і основ, які не є фармацевтично прийнятними, також можуть знайти застосування, наприклад, при отриманні або очищенні фармацевтично прийнятної сполуки. Всі солі, незалежно від того, чи є фармацевтично прийнятними чи ні, включені в обсяг даного винаходу. Аддитивні солі фармацевтично прийнятних кислот і основ, як вказувалось вище або далі в цьому документі, включають терапевтично активні форми аддитивних солей нетоксичної кислоти і основи, які здатні утворювати сполуки формули (I). Аддитивні солі фармацевтично прийнятної кислоти можуть бути отримані загальноприйнятим способом обробки сполуки у формі основи такою прийнятною кислотою. Прийнятні кислоти включають, наприклад, неорганічні кислоти, такі як галогенводневі кислоти, наприклад, хлористоводневу або бромистоводневу кислоту, сірчану, азотну, фосфорну і подібні кислоти, або органічні кислоти, такі як, наприклад, оцтову, пропіонову, гідроксиоцтову, молочну, піровиноградну, щавлеву (тобто етандіову), малонову, бурштинову (тобто бутандіову кислоту), малеїнову, фумарову, яблучну, винну, лимонну, метансульфонову, етансульфонову, бензолсульфонову, птолуолсульфонову, цикламову, саліцилову, п-аміносаліцилову, памову і тому подібні кислоти. З іншого боку, вказані сольові форми можна перетворити у форму вільної основи обробкою прийнятною основою. Сполуки формули (I), що містять кислотний протон, також можна перетворити в їх нетоксичні форми аддитивних солей металу або аміну обробкою прийнятними органічними і неорганічними основами. Прийнятні сольові форми основи включають, наприклад, солі аммонію, солі лужних або лужноземельних металів, наприклад, солі літію, натрію, калію, магнію, кальцію і тому подібні; солі з органічними основами, наприклад, солі первинних, вторинних і третинних аліфатичних і ароматичних амінів, таких як метиламін, етиламін, пропіламін, ізопропіламін, чотири бутиламінових ізомерів, диметиламін, діетиламін, діетаноламін, дипропіламін, діізопропіламін, ди-н-бутиламін, пірролідин, піперидин, морфолін, триметиламін, триетиламін, трипропіламін, хінуклідин, піридин, хінолін і ізохінолін; бензатин, N-метил-Dглюкамін, гідрабамін, і солі з амінокислотами, такими як, наприклад, аргінін, лізин і тому подібні. І, навпаки, сольова форма може бути перетворена шляхом обробки кислотою у форму вільної кислоти. Термін "сольват" включає гідрати і форми додавання розчинника, які здатні утворювати сполуки формули (I), а також їх солі. Прикладами таких форм є, наприклад, гідрати, алкоголяти і тому подібне. Сполуки формули (I), отримані способами, описаними нижче, можуть бути синтезовані у вигляді сумішей енантіомерів, зокрема, рацемічних сумішей енантіомерів, які можуть бути відокремлені один від одного відповідно до відомих способів розділення. Спосіб розділення енантіомерних форм сполук формули (I) включає рідинну хроматографію з використанням хіральної нерухомої фази. Вказані стереохімічно чисті ізомерні форми також можуть бути отримані з відповідних стереохімічно чистих ізомерних форм прийнятних первинних речовин, за умови, що реакція протікає стереоспецифічно. Бажано, якщо потрібний певний стереоізомер, вказана сполука може бути синтезована стереоспецифічними способами отримання. У даних способах, бажано, використовують енентіомерно чисті первинні речовини. В рамках даної заявки, сполука за даним винаходом, по суті, включає всі ізотопні поєднання її хімічних елементів. У рамках даної заявки, хімічний елемент, зокрема, коли він вказаний у зв'язку із сполукою формули (I), включає всі ізотопи і ізотопні суміші цього елементу. Наприклад, 1 2 3 коли вказаний водень, повинно бути зрозуміло, що він відноситься до H, H, H і їх сумішам. Відповідно, сполука за даним винаходом, по суті, включає сполуку з одним або декількома ізотопами одного або декількох елементів і їх суміші, включаючи радіоактивну сполуку, яка також називається сполукою, міченою радіоактивним ізотопом, в якій один або декілька нерадіоактивних атомів було замінено одним з їх радіоактивних ізотопів. Під терміном "сполука, мічена радіоактивним ізотопом", розуміється будь-яка сполука формули (I) або її фармацевтично прийнятна сіль, яка містить, щонайменше, один радіоактивний атом. Наприклад, сполука може бути мічена позитроном або гаммавипромінюючими радіоактивними 3 125 ізотопами. Для способів зв'язування з радіолігандом, H-атом або I-атом є атомом, вибраним для заміни. Для отримання зображення найширше використовують позитронно-емітуючі (PET) 11 18 15 13 радіоактивні ізотопи, що є C, F, O і N, кожен з яких отриманий за допомогою 4 UA 107963 C2 5 10 15 20 25 30 35 40 45 50 прискорювача і має період напіврозпаду 20, 100, 2 і 10 хвилин, відповідно. Оскільки періоди напіврозпаду цих радіоактивних ізотопів дуже короткі, то їх використання практично можливе лише в інститутах, які мають прискорювач для їх отримання, і ця обставина, відповідно, 18 99m 201 123 обмежує їх застосування. Найширше використовуваними з цих ізотопів є F, Tc, Tl і I. Поводження з такими радіоактивними ізотопами, їх отримання, виділення і введення в молекулу добре відомі фахівцям у даній галузі техніки. Зокрема, радіоактивний атом вибраний з групи, що включає водень, вуглець, азот, сірку, 3 11 18 122 кисень і галоген. Зокрема, радіоактивний ізотоп вибраний з групи, що включає H, C, F, I, 123 125 13 75 76 77 82 I, I, 1I, Br, Br, Br і Br. Як використовується в описі і формулі винаходу, що додається, форми однини іменників також включають множину, якщо в контексті явно не вказане інше. Наприклад, "сполука" означає одну сполуку або декілька сполук. Терміни, описані вище, та інші, використані в описі, добре відомі фахівцям у даній галузі. Бажані властивості сполук за даним винаходом описані в даній заявці. Даний винахід відноситься до нових сполук формули (I): і їх стереоізомерним формам, де 1 R є воднем, хлором або фтором; 2 R є воднем, хлором, фтором або метилом; 3 4 R і R є воднем; 3 4 або R і R , узяті разом, утворюють зв'язок; 5 6 R є 1,1-дифторетилом, і R є воднем або фтором; 5 6 або R є воднем або фтором, і R є 1,1-дифторетилом; і їх фармацевтично прийнятним солям і сольватам. В одному з варіантів здійснення, винахід відноситься до сполук стереоізомерних формам, де 1 R є хлором або фтором; 2 R є воднем, хлором, фтором або метилом; 3 4 R і R є воднем; 3 4 або R і R , узяті разом, утворюють зв'язок; 5 6 R є 1,1-дифторетилом, і R є воднем або фтором; 5 6 або R є воднем або фтором, і R є 1,1-дифторетилом; і їх фармацевтично прийнятним солям і сольватам. В одному з варіантів здійснення, винахід відноситься до сполук стереоізомерних формам, де 1 R є хлором або фтором; 2 R є хлором, фтором або метилом; 3 4 R і R є воднем; 3 4 або R і R , взяті разом, утворюють зв'язок; 5 6 R є 1,1-дифторетилом, і R є воднем або фтором; 5 6 або R є воднем або фтором, і R є 1,1-дифторетилом; і їх фармацевтично прийнятним солям і сольватам. В одному з варіантів здійснення, винахід відноситься до сполук стереоізомерних форм, де 1 R є хлором або фтором; 2 R є воднем, хлором, фтором або метилом; 3 4 R і R , узяті разом, утворюють зв'язок; 5 6 R є 1,1-дифторетилом, і R є воднем або фтором; 5 6 або R є воднем або фтором, і R є 1,1-дифторетилом; і їх фармацевтично прийнятним солям і сольватам. У іншому варіанті здійснення, винахід відноситься до сполук стереоізомерних форм, де 5 формули (I) і їх формули (I) і їх формули (I) і їх формули (I) і їх UA 107963 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 R є хлором або фтором; 2 R є воднем; 3 4 R і R , взяті разом, утворюють зв'язок; 5 R є 1,1-дифторетилом; 6 R є воднем; і їх фармацевтично прийнятним солям і сольватам. У наступному варіанті здійснення, винахід відноситься до будь-якого з інших варіантів 5 здійснення або будь-якому поєднанню з інших варіантів здійснення, де R є 1,1-дифторетилом, і 6 R є воднем або фтором. У ще одному варіанті здійснення, винахід відноситься до будь-якого з інших варіантів 5 здійснення або будь-якому поєднанню з інших варіантів здійснення, де R є воднем або фтором 6 і R є 1,1-дифторетилом. У наступному варіанті здійснення, винахід відноситься до будь-якого з інших варіантів 1 здійснення або будь-якому поєднанню з інших варіантів здійснення, де, щонайменше, один з R 2 і R є іншим, ніж водень. У конкретному варіанті здійснення, винахід відноситься до будь-якого з інших варіантів 2 здійснення або будь-якому поєднанню з інших варіантів здійснення, де R є воднем, хлором або фтором. У іншому варіанті здійснення, винахід відноситься до будь-якого з інших варіантів здійснення 3 4 або будь-якому поєднанню з інших варіантів здійснення, де R і R є воднем. У іншому варіанті здійснення, винахід відноситься до будь-якого з інших варіантів здійснення 1 2 або будь-якому поєднанню з інших варіантів здійснення, де R або R знаходиться в 7положенні і є іншим, ніж водень. У іншому варіанті здійснення, винахід відноситься до будь-якого з інших варіантів здійснення 1 або будь-якому поєднанню з інших варіантів здійснення, де R знаходиться в 7-положенні і є 1 хлором або фтором, зокрема, R знаходиться в 7-положенні і є хлором. У іншому варіанті здійснення винахід відноситься до будь-якого з інших варіантів здійснення або будь-якому поєднанню з інших варіантів здійснення, де 1 1 R знаходиться в 7-положенні і є хлором або фтором, зокрема, R знаходиться в 7положенні і є хлором, і 2 R знаходиться в будь-якому іншому положенні і є воднем, хлором, фтором або метилом, зокрема, хлором, фтором або метилом; конкретніше, хлором або фтором, і, навіть конкретніше, хлором. У іншому варіанті здійснення винахід відноситься до будь-якого з інших варіантів здійснення 2 або будь-якому поєднанню з інших варіантів здійснення, де R знаходиться в 7-положенні і є хлором, фтором або метилом. У іншому варіанті здійснення винахід відноситься до будь-якого з інших варіантів здійснення або будь-якому поєднанню з інших варіантів здійснення, де 2 R знаходиться в 7-положенні і є хлором, фтором або метилом, і 1 R знаходиться в будь-яких інших положеннях і є воднем, хлором або фтором, зокрема, хлором або фтором, конкретніше, хлором. У ще одному варіанті здійснення, винахід відноситься до будь-якого з інших варіантів 3 4 здійснення або будь-якому поєднанню з інших варіантів здійснення, де R і R , взяті разом, утворюють зв'язок. У наступному варіанті здійснення винаходу, сполука формули (I) вибрана з групи, що включає: 7-хлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін, 7-хлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін·НСl, (4S)-7-хлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін, (4S)-7-хлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін·НСl, (4R)-7-хлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін, (4R)-7-хлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін·НСl, 8,10-дихлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін, 8,10-дихлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін·НСl, 8,10-дихлор-4-[4-(1,1-дифторетил)феніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, 7,8-дихлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін, 7,8-дихлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін·НСl, 7,10-дихлор-4-[4-(1,1-дифторетил)феніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, 7,9-дихлор-4-[4-(1,1-дифторетил)феніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, 7,8-дихлор-4-[4-(1,1-дифторетил)феніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, 6 UA 107963 C2 5 10 15 20 25 30 35 40 7,10-дихлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін, 7,10-дихлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін·НСl, 7,9-дихлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін 7,9-дихлор-4-[4-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін·НСl, 7-хлор-4-[4-(1,1-дифторетил)феніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, 7-хлор-4-[3-(1,1-дифторетил)феніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, 4-[4-(1,1-дифторетил)феніл]-7-фтор-6H-пірроло[1,2-а][1,4]бензодіазепін, 9-хлор-4-[4-(1,1-дифторетил)феніл]-7-метил-6H-пірроло[1,2-а][1,4]бензодіазепін, 9-хлор-4-[4-(1,1-дифторетил)феніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, 4-[4-(1,1-дифторетил)феніл]-7,9-дифтор-6H-пірроло[1,2-а][1,4]бензодіазепін, 10-хлор-4-[4-(1,1-дифторетил)феніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, 4-[3-(1,1-дифторетил)-4-фторфеніл]-7-фтор-6H-пірроло[1,2-а][1,4]бензодіазепін, 7-хлор-4-[3-(1,1-дифторетил)-4-фторфеніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, 9,10-дихлор-4-[4-(1,1-дифторетил)феніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, 4-[3-(1,1-дифторетил)-4-фторфеніл]-7,9-дифтор-6H-пірроло[1,2-а][1,4]бензодіазепін, 7-хлор-4-[4-(1,1-дифторетил)феніл]-9-фтор-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін, 7-хлор-4-[4-(1,1-дифторетил)феніл]-9-фтор-5,6-дигідро-4Н-пірроло[1,2а][1,4]бензодіазепін·НСl, 7,9-дихлор-4-[3-(1,1-дифторетил)-4-фторфеніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, 7-хлор-4-[3-(1,1-дифторетил)-4-фторфеніл]-9-фтор-6H-пірроло[1,2-а][1,4]бензодіазепін, 7-хлор-4-[4-(1,1-дифторетил)феніл]-9-фтор-6H-пірроло[1,2-а][1,4]бензодіазепін, 10-хлор-4-[4-(1,1-дифторетил)феніл]-7-метил-6H-пірроло[1,2-а][1,4]бензодіазепін, 7-хлор-4-[3-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін, 7-хлор-4-[3-(1,1-дифторетил)феніл]-5,6-дигідро-4Н-пірроло[1,2-а][1,4]бензодіазепін·НСl, 7-хлор-4-[4-(1,1-дифторетил)-3-фторфеніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, 4-[4-(1,1-дифторетил)-3-фторфеніл]-7-фтор-6H-пірроло[1,2-а][1,4]бензодіазепін, 7-хлор-4-[4-(1,1-дифторетил)-3-фторфеніл]-9-фтор-6H-пірроло[1,2-а][1,4]-ензодіазепін, 9-хлор-4-[4-(1,1-дифторетил)феніл]-7-фтор-6H-пірроло[1,2-а][1,4]бензодіазепін, 4-[4-(1,1-дифторетил)-3-фторфеніл]-7,9-дифтор-6H-пірроло[1,2-а][1,4]бензодіазепін, 9-хлор-4-[3-(1,1-дифторетил)-4-фторфеніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, 10-хлор-4-[3-(1,1-дифторетил)-4-фторфеніл]-6H-пірроло[1,2-а][1,4]бензодіазепін, включаючи будь-яку стереохімічно ізомерну форму і їх фармацевтично прийнятні солі і сольвати. У ще іншому варіанті здійснення винаходу, сполука формули (I) є 7-хлор-4-[4-(1,1дифторетил)феніл]-6H-пірроло[1,2-а][1,4]бензодіазепіном. Усі можливі поєднання вище вказаних варіантів, що цікавлять, вважаються включеними в обсяг даного винаходу. Даний винахід охоплює також способи отримання сполук формули (I) і їх підгруп. Сполуки формули (I) і їх підгрупи можуть бути отримані послідовністю стадій, як описано нижче. Сполуки, як правило, отримують з первинних продуктів, які є або комерційно доступними, або отриманими стандартними засобами, очевидними для фахівців у даній галузі. Сполуки за даним винаходом також можуть бути отримані з використанням стандартних способів синтезу, зазвичай використовуємих фахівцями в галузі органічної хімії. Сполуки за даним винаходом можуть бути отримані згідно схемі 1: 45 7 UA 107963 C2 3 5 10 15 4 Сполуки формули (I), де R і R , взяті разом, утворюють додатковий зв'язок, тобто сполуки, представлені формулою (I-b), можуть бути отримані із сполук, представлених формулою (I-а), відповідно до відомих реакцій окислення аміну до іміна. Ці реакції окислення можуть бути проведені шляхом здійснення взаємодії сполуки формули (I-а) з окислювачем, таким як, наприклад, тетраацетат свинцю або діоксид марганцю, в реакційно інертному розчиннику, такому як галогеновані вуглеводні, наприклад, дихлорметан (DCM) або трихлорметан. Швидкість реакції може бути підвищена шляхом перемішування і, можливо, нагрівання реакційної суміші. Альтернативно, сполуки формули (I-b) можуть бути отримані шляхом внутрішньомолекулярної циклізації проміжної сполуки формули (II). У присутності кислоти, такої як, наприклад, POCl3, амід проміжної сполуки формули (II) може діяти як C-електрофіл, призводячи до замикання кільця. Реакція може бути проведена у прийнятному розчиннику, такому як, наприклад, DCM. Перемішування і нагрівання можуть підвищити швидкість реакції. Сполука формули (I-а) може бути отримана виходячи з проміжної сполуки формули (IV) + шляхом перетворення її в сіль (III) шляхом взаємодії з кислотою H X формули (XI), і взаємодією 8 UA 107963 C2 5 10 15 20 25 30 35 40 45 50 55 60 вказаної солі формули (III) з альдегідом формули (XII) у прийнятному розчиннику, такому як спирт, наприклад, метанол (MеOH), етанол (EtOH), ізопропанол, при підвищеній температурі, бажано, при температурі кипіння. Альтернативно, проміжна сполука формули (IV) спочатку може бути піддана взаємодії з альдегідом формули (XII), і отриманий таким чином імін може бути циклізований у присутності + кислоти H X формули (XI) до сполуки формули (I-а). Альтернативно, сполука формули (I-а) може бути отримана шляхом відновлення сполуки формули (I-b), використовуючи способи, добре відомі фахівцям у даній галузі. Проміжна сполука формули (II) може бути отримана за допомогою реакції конденсації проміжної сполуки формули (III) і (XIII). Вказана реакція може бути здійснена у присутності конденсуючих агентів, таких як загальновідомий 1-гідрокси-1H-бензотриазол (HOBt) і моногідрохлорид N'-(етилкарбонімідоїл)-N,N-диметил-1,3-пропандіаміна (EDCI). Реакція може бути проведена у присутності основи, такої як триетиламін (Et3N), і прийнятного розчинника, такого як, наприклад, DCM. Альтернативно, похідне хлорангідрида кислоти (XIII) або його реакційноспроможне складноефірне похідне (XIII) також можуть бути використані в реакції цього типа для отримання проміжної сполуки формули (II). Проміжна сполука формули (XIII) або її хлорангідрид кислоти або складноефірне похідне легко можуть бути отримані фахівцями у даній галузі. Проміжні сполуки формули (III) і (IV) отримують шляхом відновлення 1-(2ціанофеніл)піррольного похідного формули (V). Для відновлення нітрильної функціональної групи можуть бути використані деякі способи, добре відомі фахівцям у даній галузі, такі як, наприклад: 1. LiAlH4/ТГФ [S. Raines, S.Y. Chai and F.P. Palopoli, J. Heterocyclic Chem., 13, 711-716 (1976)]. ® 2. i. біс(2-метоксиетокси)алюмінат натрію (Red-Al ) 70 % мас/мас толуол, кімнатна температура: ii. NaOH 10 %, кімнатна температура [G.W.H. Cheeseman and S.G. Greenberg; J. Heterocyclic Chem., 16, 241-244 (1979)] 3а. i. KBH4/CF3COOH, ТГФ, ii. H2O, iii. НСl [P. Trinka, P. Slegel and J. Reiter; J. Prakt. Chem., 338, 675-678 (1996)] 3b. Боран-диметілсульфід (1:1), ТГФ 4а. RaNi (нікель Ренея) /H2 4b. RaNi/раствор тіофена/(MeOH/NH3) Також можуть бути використані навіть інші відомі способи відновлення нітрильної функціональної групи. Проміжна сполука формули (V), у свою чергу, є комерційно доступною або, альтернативно, може бути легко отримана, наприклад, обробкою 2-амінобензонітрильного похідного формули (VI) тетрагідро-2,5-диметоксифураном в інертному розчиннику, такому як діоксан або тетрагідрофуран (ТГФ), у присутності кислоти, такої як гідрохлорид 4-хлорпіридина, або в кислотному розчиннику, такому як крижана оцтова кислота, при підвищеній температурі, бажано, при температурі кипіння. Альтернативно, проміжна сполука формули (V) також може бути отримана виходячи з проміжної сполуки формули (X). Як правило, проміжну сполуку формули (X), де Halo визначається як Br, I, Cl або F, піддають взаємодії з пірролом у присутності основи, такої як, наприклад, Cs2CO3 або NaH, у прийнятному розчиннику, такому як, зазвичай, ДМФ. Альтернативно, проміжна сполука формули (IV) може бути отримана шляхом обробки проміжної сполуки формули (VII) боран-диметилсульфідом (1:1) у прийнятному розчиннику, такому як, наприклад, ТГФ. Зазвичай реакція може бути здійснена у присутності кислоти, такої як НСl. Після того, як реакція завершувалась, реакційна суміш може бути підлужена прийнятною основою, такию як NaOH. Реакція може бути здійснена при підвищеній температурі, бажано, при температурі кипіння. Проміжна сполука формули (VII) може бути отримана виходячи з проміжної сполуки формули (VIII). Проміжна сполука формули (VIII) може бути піддана взаємодії з джерелом азоту, таким як NH3·H2O у присутності HOBt і EDCI. Цей тип реакції зазвичай може бути здійснений у прийнятному розчиннику, подібному ДМФ. Перемішування реакційної суміші може підвищити швидкість реакції. Проміжна сполука формули (VIII) може бути легко отримана шляхом обробки проміжної сполуки формули (IX) тетрагідро-2,5-диметоксифураном в інертному розчиннику, такому як діоксан, у присутності кислоти, такої як гідрохлорид 4-хлорпіридина, при підвищеній температурі, бажано, при температурі кипіння. Крім того, в реакції цього типа для отримання 9 UA 107963 C2 5 10 15 20 25 30 35 40 45 50 55 проміжної сполуки формули (VIII) також може бути використано реакційноспроможне похідне ефіру (IX). Усі первинні матеріали є комерційно доступними або можуть бути легко отримані фахівцями у даній галузі. У всіх цих отриманнях продукти реакції можуть бути виділені з реакційного середовища і, при необхідності, додатково очищені відповідно до методик, які широко відомі у даній галузі, такими як, наприклад, екстракція, кристалізація, розтирання і хроматографія. Зокрема, стереоізомери можуть бути виділені хроматографічно з використанням стаціонарної хіральної ® ® фази, такої як, наприклад, Chiralpak AD (3,5-диметилфенілкарбамат амілози) або Chiralpak AS, обидві від фірми Daicel Chemical Industries, Ltd, Японія. Чисті стереоізомерні форми сполук і проміжних сполук за даним винаходом можуть бути отримані шляхом використання відомих способів. Енантіомери можуть бути відокремлені один від одного шляхом селективної кристалізації їх діастереомерних солей за допомогою оптично активних кислот. Альтернативно, енантіомери можуть бути розділені хроматографічними способами з використанням хіральних стаціонарних фаз. Указані чисті стереоізомерні форми можуть бути також отримані з відповідних чистих форм стереоізомерних форм відповідних первинних продуктів, за умови, що реакція протікає стереоселективно або стереоспецифічно. Переважно, якщо бажаний конкретний стереоізомер, вказану сполуку синтезували шляхом стереоселективного або стереоспецифічного способів отримання. У цих способах доцільно використовувати хірально чисті первинні продукти. Стереоізомерні форми сполук формули (I), що очевидно, призначені для включення в обсяг винаходу. Хірально чисті форми сполук формули (I) утворюють бажану групу сполук. У зв'язку з цим, хірально чисті форми проміжних сполук і їх сольові форми особливо можуть бути використані при отриманні хірально чистих сполук формули (I). Також енентіомерні суміші проміжних сполук можуть бути використані при отриманні сполук формули (I) з відповідною конфігурацією. Сполуки формули (I) і їх стереоізомерні форми, і фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активними відносно диморфних патогенних мікроорганізмів, дерматофітів, зигоміцетів, гіалінових гіфоміцетів, демацієвих гіфоміцетів, дріжджів і дріжджеподібних організмів. Сполуки формули (I) і їх стереоізомерні форми, і фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно диморфних патогенних мікроорганізмів, дріжджів і дріжджеподібних організмів. Сполуки формули (I) і їх стереоізомерні форми, і фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно плісневих грибів. Сполуки формули (I) і їх стереоізомерні форми, і фармацевтично прийнятні солі і сольвати, можуть бути активні відносно широкого спектру грибів, таких як Candida spp., наприклад, Candida albicans, Candida glabrata, Candida krucei, Candida parapsilosis, Candida kefyr, Candida tropicalis; Aspergillus spp., наприклад, Aspergillus fumigatus, Aspergillus niger, Aspergillus flavus; Cryptococcus neoformans; Sporothrix schenckii; Epidermophyton floccosum; Microsporum spp., наприклад, Microsporum canis, Microsporum gypseum; Trichophyton spp., наприклад, Trichophyton mentagrophytes, Trichophyton rubrum, Trichophyton quinckeanum, Trichophyton tonsurans, Trichophyton verrucosum, Trichophyton violaceum, Trichophyton interdigitale, Trichophyton soudanense; Fusarium spp., наприклад, Fusarium solani, Fusarium oxysporum, Fusarium proliferatum, Fusarium verticillioides; Rhizomucor spp., наприклад, Rhizomucor miehei, Rhizomucor pusillus; Mucor circinelloides; Rhizopus spp., наприклад, Rhizopus oryzae, Rhizopus microspores; Malassezia furfur; Acremonium spp.; Paecilomyces; Scopulariopsis; Arthrographis spp.; Scytalidium; Scedosporium spp., наприклад, Scedosporium apiospermum, Scedosporium prolificans; Trichoderma spp.; Penicillium spp.; Penicillium marneffei; Blastoschizomyces. Сполуки формули (I) і їх стереоізомерні форми, і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно широкого спектру грибів, таких як Candida parapsilosis; Aspergillus spp., наприклад, Aspergillus fumigatus, Aspergillus niger, Aspergillus flavus; Cryptococcus neoformans; Sporothrix schenckii; Epidermophyton floccosum; Microsporum spp., наприклад, Microsporum canis, Microsporum gypseum; Trichophyton spp., наприклад, Trichophyton mentagrophytes, Trichophyton rubrum, Trichophyton quinckeanum, Trichophyton tonsurans, Trichophyton verrucosum, Trichophyton violaceum, Trichophyton interdigitale, Trichophyton soudanense; Fusarium spp., наприклад, Fusarium solani, Fusarium oxysporum, Fusarium proliferatum, Fusarium verticillioides; Rhizomucor spp., наприклад, Rhizomucor miehei, Rhizomucor pusillus; Mucor circinelloides; Rhizopus spp., наприклад, Rhizopus oryzae, Rhizopus microspores; Acremonium spp.; Paecilomyces; Scopulariopsis; Arthrographis spp.; Scytalidium; Scedosporium 10 UA 107963 C2 5 10 15 20 25 30 35 40 45 50 55 60 spp., наприклад, Scedosporium apiospermum, Scedosporium prolificans; Trichoderma spp.; Penicillium spp.; Penicillium marneffei; Blastoschizomyces. Сполуки формули (I) і їх стереоізомерні форми, і фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні проти широкого спектру грибків, таких як Candida parapsilosis; Aspergillus spp., наприклад, Aspergillus fumigatus, Aspergillus niger, Aspergillus flavus; Cryptococcus neoformans; Epidermophyton floccosum; Microsporum spp., наприклад, Microsporum canis, Microsporum gypseum; Trichophyton spp., наприклад, Trichophyton mentagrophytes, Trichophyton rubrum, Trichophyton quinckeanum, Trichophyton tonsurans, Trichophyton verrucosum, Trichophyton violaceum, Trichophyton interdigitale, Trichophyton soudanense; Fusarium spp., наприклад, Fusarium solani, Fusarium oxysporum, Fusarium proliferatum, Fusarium verticillioides; Rhizomucor spp., наприклад, Rhizomucor miehei, Rhizomucor pusillus; Mucor circinelloides; Rhizopus spp., наприклад, Rhizopus oryzae, Rhizopus microspores; Acremonium spp.; Paecilomyces; Scopulariopsis; Arthrographis spp.; Scytalidium; Scedosporium spp., наприклад, Scedosporium apiospermum, Scedosporium prolificans; Trichoderma spp.; Penicillium spp.; Penicillium marneffei; Blastoschizomyces; зокрема Aspergillus spp., наприклад, Aspergillus fumigatus, Aspergillus niger, Aspergillus flavus; Cryptococcus neoformans; Epidermophyton floccosum; Microsporum spp., наприклад, Microsporum canis, Microsporum gypseum; Trichophyton spp., наприклад, Trichophyton mentagrophytes, Trichophyton rubrum, Trichophyton quinckeanum, Trichophyton tonsurans, Trichophyton verrucosum, Trichophyton violaceum, Trichophyton interdigitale, Trichophyton soudanense; Fusarium spp., наприклад, Fusarium solani, Fusarium oxysporum, Fusarium proliferatum, Fusarium verticillioides; Rhizomucor spp., наприклад, Rhizomucor miehei, Rhizomucor pusillus; Mucor circinelloides; Rhizopus spp., наприклад, Rhizopus oryzae, Rhizopus microspores; Acremonium spp.; Paecilomyces; Scopulariopsis; Arthrographis spp.; Scytalidium; Scedosporium spp., наприклад, Scedosporium apiospermum, Scedosporium prolificans; Trichoderma spp.; Penicillium spp.; Penicillium marneffei; Blastoschizomyces. Сполуки формули (I) і стереоізомерні форми, і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно Candida parapsilosis B66126, Aspergillus fumigatus B42928, Cryptococcus neoformans B66663, Sporothrix schenckii B62482, Microsporum canis B68128, Trichophyton mentagrophytes B70554, Trichophyton rubrum B68183, Scedosporium apiospermum IHEM3817 і Scedosporium prolificans IHEM21157. Сполуки формули (I) і їх стереоізомерні форми і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно Candida parapsilosis B66126, Aspergillus fumigatus B42928, Cryptococcus neoformans B66663, Sporothrix schenckii B62482, Microsporum canis B68128, Trichophyton mentagrophytes B70554, Trichophyton rubrum B68183, Scedosporium apiospermum IHEM3817, Scedosporium prolificans IHEM21157, Rhizopus oryzae IHEM5223, Rhizomucor miehei IHEM13391 і Mucor circinelloides IHEM21105. Сполуки формули (I) і їх стереоізомерні форми і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно Candida parapsilosis, Aspergillus fumigatus, Cryptococcus neoformans, Sporothrix schenckii, Microsporum canis, Trichophyton mentagrophytes, Trichophyton rubrum, Scedosporium apiospermum, Scedosporium prolificans, Rhizopus oryzae, Rhizomucor miehei і Mucor circinelloides. Сполуки формули (I) і стереоізомерні форми, і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно Candida parapsilosis, Aspergillus fumigatus, Cryptococcus neoformans, Sporothrix schenckii, Microsporum canis, Trichophyton mentagrophytes, Trichophyton rubrum, Scedosporium apiospermum і Scedosporium prolificans; зокрема Aspergillus fumigatus, Microsporum canis, Trichophyton mentagrophytes, Trichophyton rubrum, Scedosporium apiospermum і Scedosporium prolificans. Сполуки формули (I) і стереоізомерні форми, і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні проти широкого спектру грибків, таких як Candida parapsilosis; Aspergillus spp.; Cryptococcus neoformans; Sporothrix schenckii; Microsporum spp.; Fusarium spp.; Scedosporium spp.; зокрема, Candida parapsilosis; Aspergillus spp.; Cryptococcus neoformans; Microsporum spp; Fusarium spp; Scedosporium spp.; конкретніше, Aspergillus spp.; Cryptococcus neoformans; Microsporum spp.; Fusarium spp.; Scedosporium spp. Сполуки формули (I) і стереоізомерні форми, і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні проти широкого спектру грибків, таких як Candida parapsilosis; Aspergillus spp. Cryptococcus neoformans; Trichophyton spp.; Sporothrix schenckii; Microsporum spp.; Fusarium spp.; Scedosporium spp., зокрема, Aspergillus spp.; Microsporum spp.; Trichophyton spp. Сполуки формули (I) і стереоізомерні форми, і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно грибів, таких як Candida parapsilosis; Aspergillus spp., 11 UA 107963 C2 5 10 15 20 25 30 35 40 45 50 55 60 наприклад, Aspergillus fumigatus, Aspergillus niger, Aspergillus flavus; Cryptococcus neoformans; Sporothrix schenckii; Epidermophyton floccosum; Microsporum canis; Trichophyton spp., наприклад, Trichophyton mentagrophytes, Trichophyton rubrum, Trichophyton quinckeanum; зокрема, Candida parapsilosis; Aspergillus spp., наприклад, Aspergillus fumigatus, Aspergillus niger, Aspergillus flavus; Cryptococcus neoformans; Epidermophyton floccosum; Microsporum canis; Trichophyton spp., наприклад, Trichophyton mentagrophytes, Trichophyton rubrum, Trichophyton quinckeanum; конкретніше Aspergillus spp., наприклад, Aspergillus fumigatus, Aspergillus niger, Aspergillus flavus; Cryptococcus neoformans; Epidermophyton floccosum; Microsporum canis; Trichophyton spp., наприклад, Trichophyton mentagrophytes, Trichophyton rubrum, Trichophyton quinckeanum. Сполуки формули (I) і стереоізомерні форми, і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно грибів, таких як Candida parapsilosis; Aspergillus spp.; Cryptococcus neoformans; Microsporum spp.; Trichophyton spp.; Scedosporium spp. Сполуки формули (I) і їх стереоізомерні форми і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно Candida parapsilosis, Aspergillus fumigatus, Cryptococcus neoformans, Sporothrix schenckii, Microsporum canis, Trichophyton mentagrophytes, Trichophyton rubrum, Scedosporium apiospermum і Scedosporium prolificans; зокрема, Candida parapsilosis, Aspergillus fumigatus, Cryptococcus neoformans, Microsporum canis, Trichophyton mentagrophytes, Trichophyton rubrum, Scedosporium apiospermum і Scedosporium prolificans; конкретніше Aspergillus fumigatus, Cryptococcus neoformans, Microsporum canis, Trichophyton mentagrophytes, Trichophyton rubrum, Scedosporium apiospermum і Scedosporium prolificans. Сполуки формули (I) і їх стереоізомерні форми, і фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні проти різних грибків, які вражають шкіру, волосся і нігті, а також проти підшкірних і системних грибкових збудників. Сполуки формули (I) і їх стереоізомерні форми і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно 3 родів дерматофітів: Trichophyton, Microsporum і Epidermophyton, зокрема, відносно Trichophyton і Microsporum. Сполуки формули (I) і їх стереоізомерні форми і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно дерматофітів і Aspergillus spp.; зокрема, Microsporum canis, Trichophyton mentagrophytes, Trichophyton rubrum і Aspergillus fumigatus; конкретніше, Microsporum canis, Trichophyton mentagrophytes і Trichophyton rubrum. Сполуки формули (I) і їх стереоізомерні форми, і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно Trichophyton mentagrophytes, Trichophyton rubrum і Aspergillus spp.; зокрема Trichophyton mentagrophytes, Trichophyton rubrum і Aspergillus fumigatus. Сполуки формули (I) і їх стереоізомерні форми і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно Trichophyton mentagrophytes; Trichophyton rubrum; Aspergillus spp., наприклад, Aspergillus fumigatus; Fusarium spp.; Mucor spp.; Zygomycetes spp.; Scedosporium spp.; Microsporum canis; Sporothrix schenckii; Cryptococcus neoformans і Candida parapsilosis. Сполуки формули (I) і їх стереоізомерні форми і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно дерматофітів. Сполуки формули (I) і їх стереоізомерні форми і їх фармацевтично прийнятні аддитивні солі і сольвати, можуть бути активні відносно Aspergillus fumigatus. Сполуки формули (I) і їх стереоізомерні форми, і їх фармацевтично прийнятні аддитивні солі, і сольвати можуть бути активні відносно широкого спектру грибів, наприклад, одного або декількох вказаних вище грибів. Сполуки формули (I) і їх стереоізомерні форми, і фармацевтично прийнятні аддитивні солі, і сольвати є ефективними протигрибковими препаратами при пероральному або місцевому введенні. Сполуки за даним винаходом можуть бути використані як інгібітори синтезу ергостерола. Враховуючи корисність сполуки формули (I), запропонований спосіб лікування теплокровних тварин, включаючи людину, страждаючих на, або спосіб профілактики теплокровних тварин, включаючи людину, страждаючих на будь-які захворювання, вказані вище. Таким чином, сполуки формули (I) призначені для застосування як лікарського засобу. Також запропоновано застосування сполуки формули (I) при отриманні лікарського засобу, що використовується в лікуванні грибкових інфекцій. Інші сполуки формули (I) запропоновані для застосування при лікуванні грибкових інфекцій. Термін "лікування", що використовується в цьому документі, позначає всі процеси, в яких може бути уповільнення, порушення, придушення або зупинка розвитку інфекції, але не обов'язково означає повне усунення всіх симптомів. 12 UA 107963 C2 5 10 15 20 25 30 35 40 45 50 55 60 Винахід відноситься до сполуки, яка відповіднає загальній формулі (I), її стереоізомерним формам і аддитивним солям фармацевтично прийнятної кислоти або основи, і сольватам, для застосування як лікарський засіб. Крім того, винахід відноситься до сполуки, яка відповідає загальній формулі (I), її стереоізомерним формам і аддитивним солям фармацевтично прийнятної кислоти або основи, і сольватам, для лікування або профілактики грибкових інфекцій, зокрема, грибкових інфекцій, викликаних одним або декількома з вищезгаданих грибів. Крім того, винахід відноситься до сполуки, що відповідає загальній формулі (I), її стереоізомерним формам і аддитивним солям фармацевтично прийнятної кислоти або основи, і сольватам, для лікування грибкових інфекцій, зокрема, грибкових інфекцій, викликаних одним або декількома з вищезгаданих грибів. Крім того, винахід відноситься до сполуки, що відповідає загальній формулі (I), її стереоізомерним формам і аддитивним солям фармацевтично прийнятної кислоти або основи, і сольватам, для застосування при лікуванні і профілактиці грибкових інфекцій, зокрема, грибкових інфекцій, викликаних одним або декількома з вищезгаданих грибів. Крім того, винахід відноситься до сполуки, що відповідає загальній формулі (I), її стереоізомерним формам і аддитивним солям фармацевтично прийнятної кислоти або основи, і сольватам, для застосування при лікуванні або профілактиці, зокрема, лікування грибкових інфекцій; зокрема, грибкових інфекцій, викликаних одним або декількома з грибів, вибраних з групи, що складається з вищезгаданих грибів. Крім того, винахід відноситься до сполуки, що відповідає загальній формулі (I), її стереоізомерним формам і аддитивним солям фармацевтично прийнятної кислоти або основи, і сольватам, для застосування при лікуванні грибкових інфекцій, зокрема грибкових інфекцій, викликаних одним або декількома з вищезгаданих грибів. Крім того, винахід відноситься до сполуки, що відповідає загальній формулі (I), її стереоізомерним формам і аддитивним солям фармацевтично прийнятної кислоти або основи, і сольватам, для застосування при лікуванні і профілактиці грибкових інфекцій, зокрема, грибкових інфекцій, викликаних одним або декількома з вищезгаданих грибів. Крім того, винахід відноситься до сполуки, що відповідає загальній формулі (I), її стереоізомерним формам і аддитивним солям фармацевтично прийнятної кислоти або основи і сольватам, для застосування при лікуванні і профілактиці грибкових інфекцій, в якій грибкова інфекція викликана одним або декількома з грибів, вибраних з групи, що складається з Candida spp.; Aspergillus spp.; Cryptococcus neoformans; Sporothrix schenckii; Epidermophyton floccosum; Microsporum spp.; Trichophyton spp; Fusarium spp.; Rhizomucor spp.; Mucor circinelloides; Rhizopus spp.; Malassezia furfur; Acremonium spp.; Paecilomyces; Scopulariopsis; Arthrographis spp.; Scytalidium; Scedosporium spp.; Trichoderma spp.; Penicillium spp.; Penicillium marneffei; і Blastoschizomyces; зокрема, в якому грибкова інфекція викликана одним або декількома з грибів, вибраних з групи, що складається з Candida parapsilosis; Aspergillus spp.; Cryptococcus neoformans; Sporothrix schenckii; Epidermophyton floccosum; Microsporum spp.; Trichophyton spp.; Fusarium spp.; Rhizomucor spp.; Mucor circinelloides; Rhizopus spp.; Acremonium spp.; Paecilomyces; Scopulariopsis; Arthrographis spp. Scytalidium; Scedosporium spp.; Trichoderma spp.; Penicillium spp.; Penicillium marneffei; і Blastoschizomyces. ще конкретніше, де грибкова інфекція викликана одним або декількома з грибів, вибраних з групи, що складається з Microsporum Canis, Trichophyton mentagrophytes, Trichophyton rubrum і Aspergillus fumigatus. Нові сполуки, описані в даному винаході, можуть бути використані при лікуванні або профілактиці захворювань або станів, вибраних з групи, що складається з інфекцій, викликаних дерматофітами, системними грибковими інфекціями і оніхомікозом. Нові сполуки, описані в даному винаході, можуть бути використані при лікуванні або профілактиці захворювань або станів, таких як, наприклад, інфекції, викликані дерматофітами, системними грибковими інфекціями або оніхомікозом. Винахід також відноситься до застосування сполуки відповідно до загальної формули (I), її стереоізомерних форм і аддитивних солей фармацевтично прийнятної кислоти або основи, і сольватів при отриманні лікарського засобу. Винахід також відноситься до застосування сполуки відповідно до загальної формули (I), її стереоізомерних форм і аддитивних солей фармацевтично прийнятної кислоти або основи, і сольватів, при отриманні лікарського засобу для лікування або профілактики, зокрема лікування, грибкових інфекцій, зокрема грибкових інфекцій, викликаних одним або декількома з вищезгаданих грибів. 13 UA 107963 C2 5 10 15 20 25 30 35 40 45 50 55 60 Сполуки за даним винаходом можуть бути введені ссавцям, бажано людині, для лікування або профілактики, зокрема лікування, грибкових інфекцій, зокрема грибкових інфекцій, викликаних одним або декількома з вищезгаданих грибів. Враховуючи корисність сполук формули (I), запропонований спосіб лікування хворих теплокровних тварин, включаючи людину, або спосіб профілактики теплокровних тварин, включаючи людину, страждаючих від грибкових інфекцій, зокрема грибкових інфекцій, викликаних одним або декількома з вищезгаданих грибів. Вказані способи включають введення, тобто системне або місцеве введення, бажано, пероральне введення, ефективної кількості сполуки формули (I), її стереоізомерної форми і його фармацевтично прийнятної солі або сольвата, теплокровним тваринам, включаючи людину. Фахівці з лікування таких захворювань можуть визначити ефективну терапевтичну добову кількість з результатів досліджень, наведених нижче. Ефективна терапевтична добова кількість складатиме приблизно від 0,005 мг/кг до 50 мг/кг, зокрема, 0,01 мг/кг до 50 мг/кг маси тіла, бажаніше, від 0,01 мг/кг до 25 мг/кг маси тіла, бажано, від близько 0,01 мг/кг до близько 15 мг/кг, бажаніше, від близько 0,01 мг/кг до близько 10 мг/кг, ще бажаніше, від близько 0,01 мг/кг до 1 мг/кг, найбажаніше, від близько 0,05 мг/кг до 1 мг/кг маси тіла. Кількість сполуки відповідно до даного винаходу, також названу в цьому документі як активний інгредієнт, яка необхідна для досягнення терапевтичного ефекту, буде, звичайно, змінюватись у кожному конкретному випадку, наприклад, залежно від конкретної сполуки, способу введення, віку і стану реципієнта, і конкретного розладу або захворювання, яке піддають лікуванню. Спосіб лікування може також включати введення активного інгредієнта за схемою від одного до чотирьох прийомів на день. У цих способах лікування сполуки відповідно до винаходу, бажано, отримують перед введенням. Як описано нижче, прийнятні фармацевтичні препарати отримують відомими способами з використанням добре відомих і легко доступних інгредієнтів. Хоча цілком можливо введення лише активного інгредієнта, бажано отримувати його у вигляді фармацевтичної композиції. Даний винахід також відноситься до композицій для лікування або профілактики грибкових інфекцій, що включає терапевтично ефективну кількість сполуки формули (I) і фармацевтично прийнятний носій або розчинник. Носій або розчинник має бути "прийнятним" у сенсі сумісності з іншими інгредієнтами композиції і не спричиняти шкідливої дії на його одержувачів. Сполуки за даним винаходом, які є прийнятними для лікування або профілактики грибкових інфекцій, можна вводити окремо або у поєднанні з одним або декількома іншими терапевтичними засобами. Комбінована терапія включає введення окремої фармацевтичної дозованої композиції, яка містить сполуку формули (I) і один або декілька додаткових терапевтичних засобів, а також введення сполуки формули (I) і будь-яких додаткових терапевтичних засобів у вигляді окремої фармацевтичної дозованої композиції. Наприклад, сполука формули (I) і терапевтичний засіб можуть бути введені пацієнтові разом у вигляді однієї дозованої композиції для перорального введення, такої як пігулки або капсули, або кожен засіб може бути введений у вигляді окремих дозованих композицій для перорального введення. З урахуванням корисних фармакологічних властивостей, для забезпечення цілей введення сполуки, що розглядаються, можуть бути отримані у вигляді різних фармацевтичних форм. Сполука відповідно до винаходу, зокрема, сполука формули (I), її аддитивна сіль фармацевтично прийнятної кислоти або основи, її стереохімічно ізомерна форма, або будь-яка підгрупа або їх поєднання, можуть бути отримана у вигляді різних фармацевтичних форм для забезпечення цілей введення. Як прийнятні композиції можуть бути наведені всілякі композиції, що зазвичай використовуються для лікарських засобів, що системно вводяться. Для отримання фармацевтичних композицій за даним винаходом, ефективну кількість конкретної сполуки, необов'язково у формі аддитивної солі, як активного інгредієнта, об'єднують в однорідній суміші з фармацевтично прийнятним носієм, який може мати найрізноманітніші форми залежно від форми препарату, потрібної для введення. Такі фармацевтичні композиції бажані в лікарській формі для однократного введення, прийнятній, зокрема, для перорального, ректального, підшкірного, парентерального введення або введення шляхом інгаляції. Наприклад, при отриманні композицій у лікарській формі для перорального введення, можна використовувати будь-яке звичайне фармацевтичне середовище, таке як, наприклад, вода, гліколі, масла, спирти і тому подібне, в разі рідких препаратів для перорального введення, таких як суспензії, сиропи, еліксири, емульсії і розчини; або тверді носії, такі як крохмалі, цукри, каолін, розчинники, змащуючі речовини, зв'язуючі речовини, розпушуючі речовини і тому подібне, в разі порошків, пілюль, капсул і пігулок. Зважаючи на легкість введення пігулки і 14 UA 107963 C2 5 10 15 20 25 30 35 40 45 50 55 60 капсули є найбільш бажаними стандартними лікарськими формами для перорального введення, при цьому, що вочевидь, використовують тверді фармацевтичні носії. Для парентеральних композицій носій зазвичай включає стерильну воду, принаймні, в значній мірі, хоча можуть бути включені і інші інгредієнти, наприклад, речовини для підвищення розчинності. Наприклад, можуть бути отримані розчини для ін'єкцій, в яких носій містить фізіологічний розчин, розчин глюкози або суміш фізіологічного розчину і розчину глюкози. Наприклад, можуть бути отримані розчини для ін'єкцій, в яких носій містить фізіологічний розчин, розчин глюкози або суміш фізіологічного розчину і розчину глюкози. Розчини для ін'єкцій, що містять сполуки формули (I), можуть бути отримані в олії, для пролонгованої дії. Відповідними оліями для цієї мети є, наприклад, арахісова олія, кунжутна олія, бавовняна олія, кукурудзяна олія, соєва олія, синтетичні ефіри гліцерину і довголанцюжкових жирних кислот і суміші цих і інших олій. Також можуть бути отримані суспензії для ін'єкцій, і в цьому випадку можуть бути використані прийнятні рідкі носії, суспендуючі агенти і тому подібне. Також включені тверді форми препаратів, які призначені для перетворення в рідкі форми безпосередньо перед застосуванням. У композиціях, прийнятних для підшкірного введення, носій необов'язково включає засіб для посилення проникності та⁄або прийнятний зволожуючий агент, необов'язково, у поєднанні з прийнятними добавками будь-якої природи в незначних кількісних співвідношеннях, які не спричиняють істотної шкідливої дії на шкіру. Такі добавки можуть сприяти введенню в шкіру та⁄або можуть бути використані для отримання бажаної композиції. Ці композиції можуть бути введені різними способами, наприклад, у вигляді трансдермального пластиру, у вигляді нанесення плям, у вигляді мазі. Солі приєднання кислоти або основи сполук формули (I) у зв'язку з їх підвищеною розчинністю у воді в порівнянні з їх відповідною формою основи або кислоти, є більш прийнятними для отримання водних композицій. Композиції для введення через ніготь існують у вигляді розчину, і носій необов'язково включає речовину, що підсилює проникність, який сприяє проникненню протигрибкового засобу в і через ороговілий шар нігтя. Середовище розчинника включає воду, змішану з допоміжним розчинником, таким як спирт, що має від 2 до 6 атомів вуглецю, наприклад, етанол. Для підвищення розчинності та⁄або стабільності сполук формули (I) у фармацевтичних композиціях, можуть бути переважно використані α-, β- і γ-циклодекстрини або їх похідні, зокрема, гідроксиалкіл заміщені циклодекстрини, наприклад, 2-гідроксипропіл-β-циклодекстрин або сульфобутил-β-циклодекстрин. Також допоміжні розчинники, такі як спирти, можуть покращити розчинність та⁄або стабільність сполук за винаходом у фармацевтичних композиціях. Відношення активного інгредієнта до циклодекстрину може змінюватись у широких межах. Наприклад, може бути застосоване співвідношення 1/100-100/1. Бажане співвідношення активного інгредієнта до циклодекстрину знаходиться в інтервалі від близько 1/10 до 10/1. Бажаніше співвідношення активного інгредієнта до циклодекстрину знаходиться в інтервалі від близько 1/5 до 5/1. Залежно від способу введення фармацевтична композиція бажано міститиме від 0,05 до 99 % по масі, бажаніше, від 0,1 до 70 % по масі, ще бажаніше, від 0,1 до 50 % по масі сполуки формули (I), і від 1 до 99,95 % по масі, бажаніше, від 30 до 99,9 % по масі, ще бажаніше, від 50 до 99,9 % по масі фармацевтично прийнятного носія, де всі відсотки приведені від загальної маси композиції. В разі парентеральних композицій, можуть бути включені також інші інгредієнти, сприяючі розчиненню, наприклад, циклодекстрини. Відповідними циклодекстринами є α-, β- і γциклодекстрини або прості ефіри і змішані прості ефіри, в яких одна або декілька гідроксильних груп ангідроглюкозних одиниць циклодекстрина заміщені C1-6алкілом, зокрема, метилом, етилом або ізопропілом, наприклад, випадковим чином метилованим β-CD; гідроксиC1-6алкілом, зокрема, гідроксиетилом, гідроксипропілом або гідроксибутилом; карбоксиC 1-6алкілом, зокрема, карбоксиметилом або карбоксиетилом; C1-6алкілкарбонилом, зокрема, ацетилом. Особливо слід зазначити, що комплексоутворювачами та⁄або солюбілізаторами є β-CD, випадковим чином метилований β-CD, 2,6-диметил-β-CD, 2-гідроксиетил-β-CD, 2-гідроксиетил-β-CD, 2гідроксипропіл-β-CD і (2-карбоксиметокси)пропіл-β-CD, і, зокрема, 2-гідроксипропіл-β-CD (2-HPβ-CD). Термін "змішаний ефір" позначає похідні циклодекстрина, де, принаймні, дві циклодекстрин гідроксигрупи перетворені на простий ефір за допомогою різних груп, таких як, наприклад, гідроксипропіл і гідроксиетил. Середнє молярне заміщення (M.S.) використовують як міру середнього числа молей алкоксильних груп на моль ангідроглюкози. Середня міра заміщення (D.S.) відноситься до середнього числа заміщених гідроксильних груп на одиницю ангідроглюкози. Значення M.S. і D.S. може бути визначено різними аналітичними способами, такими як ядерний магнітний 15 UA 107963 C2 5 10 15 20 25 30 35 40 45 50 55 60 резонанс (ЯМР), мас-спектрометрія (MS) і інфрачервона спектроскопія (ІК). Залежно від способу, що використовується, можуть бути отримані злегка різні значення для одного даного похідного циклодекстрина. Бажано, як визначено за допомогою мас-спектрометрії, M.S. знаходиться в діапазоні від 0,125 до 10 і D.S. знаходиться в діапазоні від 0,125 до 3. Інші прийнятні композиції для перорального або ректального введення включають частки, що складаються з твердої дисперсії, що містить сполуки формули (I) і одного або більше відповідних фармацевтично прийнятних водорозчинних полімерів. Використовуємий надалі термін "тверда дисперсія" позначає систему в твердому стані (на відміну від рідкого або газоподібного стану), що містить, принаймні, два компоненти, в даному випадку, сполуку формули (I) і водорозчинний полімер, в якій один компонент диспергований практично рівномірно в іншому компоненті або компонентах (у разі додаткових фармацевтично прийнятних речовин для отримання лікарського препарату, як правило, відомих у даній галузі, включаючих, наприклад, пластифікатори, консерванти і тому подібне). Коли вказана дисперсія компонентів така, що система є хімічно і фізично повністю однорідною або гомогенною, або складається з однієї фази, як це визначається в термодинаміці, така тверда дисперсія називатиметься "твердий розчин". Тверді розчини є бажаними фізичними системами, оскільки компоненти в них, як правило, є біологічно легко доступними для організмів, яким вони вводяться. Цей ефект, ймовірно, можна пояснити легкістю, з якою вказані тверді розчини можуть утворювати рідкі розчини при контакті з рідким середовищем, таким як шлунковокишкові соки. Легкість розчинення може бути пов'язана з тим, принаймні частково, що енергія, необхідна для розчинення компонентів з твердого розчину, менше, ніж потрібний для розчинення компонентів з кристалічної або мікрокристалічної твердої фази. Термін "тверда дисперсія" також включає дисперсії, які є менш гомогенними, ніж тверді розчини. Такі дисперсії не є хімічно і фізично гомогенними або містять більше однієї фази. Наприклад, термін "тверда дисперсія" також відноситься до системи, що має зони або невеликі області, де аморфна мікрокристалічна або кристалічна сполука формули (I), або аморфний мікрокристалічний або кристалічний водорозчинний полімер, або обидва, дисперговані практично рівномірно в іншій фазі, що містить водорозчинний полімер або сполуку формули (I), або твердий розчин, що містить сполуки формули (I) і водорозчинний полімер. Вищезгадані зони є областями в твердій дисперсії, виразно помітними за деякою фізичною ознакою (властивістю), невеликими за розміром і рівномірно і у випадковому порядку розподіленими по твердій дисперсії. Крім того, може бути придатним отримання протигрибкових сполук за даним винаходом у формі наночасток, які мають модифікатор поверхні, адсорбований на їх поверхні, в кількості, достатній для підтримки ефективного середнього розміру часток менше 1000 нм. Модифікатори поверхні, що використовуються, як вважають, включають такі модифікатори поверхні, які фізично адгезуються на поверхні протигрибкового засобу, але хімічно не зв'язуються з протигрибковим засобом. Прийнятні модифікатори поверхні, бажано, можуть бути вибрані з відомих органічних і неорганічних фармацевтичних наповнювачів. Такі наповнювачі включають різні полімери, низькомолекулярні олігомери, природні речовини і поверхнево-активні речовини. Бажані модифікатори поверхні включають неіонні і аніонні поверхнево-активні речовини. Ще один спосіб отримання сполук за даним винаходом, що представляє інтерес, включає фармацевтичну композицію, в якій протигрибкові засоби за даним винаходом включені в гідрофільні полімери, і нанесення цієї суміші як плівкового покриття на безліч невеликих гранул, із отриманням, таким чином, композиції, яка може бути легко оброблена, і яка є прийнятною для отримання фармацевтичних лікарських форм для перорального введення. Вказані гранули містять розташоване в середині ядро круглої або сферичної форми, плівкове покриття з гідрофільного полімеру, протигрибковий засіб і шар захисного покриття. Безліч речовин є придатними для застосування як ядра в гранулах, за умови, що вказані речовини є фармацевтично прийнятними і мають відповідні розміри і щільність. Прикладами таких речовин є полімери, неорганічні речовини, органічні речовини і сахариди, і їх похідні. Для простоти введення і одноманітності доз, зокрема, особливо бажано готувати вищезгадані фармацевтичні композиції у вигляді стандартної лікарської форми. Лікарська форма, використана в описі і формулі винаходу, відноситься до фізично дискретних одиниць, прийнятних як одиничні дози, кожна одиниця містить певну кількість активного інгредієнта, розраховану для отримання бажаного терапевтичного ефекту, у поєднанні з необхідним фармацевтичним носієм. Прикладами таких стандартних лікарських форм є пігулки (включаючи пігулки з насічкою або пігулки, вкриті оболонкою), капсули, пілюлі, супозиторії, пакетовані 16 UA 107963 C2 5 10 15 20 25 30 35 40 45 порошки, облатки, розчини, що ін'єктуються, або суспензії, чайні ложки, столові ложки і тому подібне, і їх окрема кратна кількість. Оскільки сполуки відповідно до винаходу є ефективними сполуками для перорального введення, фармацевтичні композиції, що містять вказані сполуки для перорального введення, є особливо бажаними. Наступні приклади ілюструють даний винахід. Експериментальна частина Тут і далі, термін "DCM" позначає дихлорметан; "MeOH" позначає метанол; "LCMS" позначає рідинну хроматографію/мас спектрометрію; "ВЕРХ" позначає високоефективну рідинну хроматографію; "к.т." позначає кімнатну температуру; "т.пл." позначає точку плавлення; "хв" позначає хвилину(и); "год." позначає годину(и); "вн.д." позначає внутрішній діаметр; "EtOAc" позначає етилацетат; "Et3N" позначає триетиламін; "EtOH" позначає етанол; "екв." позначає еквівалент; "р.с." позначає реакційну(і) суміш(і); "q.s." скільки потрібно; "НФХ" позначає надкритичну флюїдну хроматографію; "ТГФ" позначає тетрагідрофуран; "HOAc" позначає оцтову кислоту; "DEA" позначає діетиламін, "HOBt" позначає 1-гідрокси-1H-бензотриазол; "Me2S" позначає диметилсульфід; "Pd(PPh 3)2Cl2" позначає дихлорбіс(трифенілфосфін)палладій; і "EDCI" позначає моногідрохлорид N’-(етилкарбонімідоїл)-N, N-диметил-1,3-пропандіаміна. A. Отримання проміжних сполук Приклад A1 a-1) Отримання проміжної сполуки 1 2-хлор-6-(1H-піррол-1-іл)бензонітрил (50 г, 0,2467 міль) розчиняли в ТГФ (500 мл). У цей розчин при кімнатній температурі додавали по краплях 10,0M розчин BH 3 в Me2S (27,1 мл, 0,2714 моль). Реакційну суміш далі перемішували і кип'ятили із зворотним холодильником протягом 12 год. Потім суміш охолоджували до кімнатної температури і додавали по краплях розчин 6н HCl (47 мл). Реакційну суміш нагрівали при температурі кипіння протягом 30 хв. Прозорий розчин охолоджували до температури 0 °C і додавали NaOH (55,5 г). Суміш екстрагували за допомогою EtOAc і насиченого сольового розчину. Органічний шар сушили (MgSO4), фільтрували, і розчинник упарювали, отримуючи 46,5 г продукту у вигляді вільної основи. Потім продукт підкислювали за допомогою суміші HCl/діоксан (q.s.) із отриманням 55 г проміжної сполуки 1 (97 %-вий вихід; ·HCl). a-2) Альтернативний спосіб отримання проміжної сполуки 1 Суміш 2-хлор-6-(1H-піррол-1-іл)бензонітрилу (0,08 моль) у MeOH/NH3 (250 мл) гідрували при температурі 14 °C за допомогою нікелю Ренея (2 г) як каталізатора, у присутності 4 %-ного розчину тіофена в MeOH (2 мл). Після обробки H2 (2 екв.), каталізатор фільтрували і фільтрат упарювали. Далі додавали 6н розчин 2-пропанол/HCl (14 мл). Потім розчинник упарювали, отримуючи суміш 2-(1H-піррол-1-іл)бензолметанаміна і проміжної сполуки 1 у вигляді HCl-соли (·HCl). Дану суміш використовували на наступній стадії реакції як таку без додаткового очищення. Приклад A2 Отримання проміжної сполуки 2 4-(1,1-дифторетіл)бензойну кислоту (5,05 г, 27,1 ммоль) розчиняли в DCM (100 мл). У цей розчин додавали Et3N (10 мл, 60,9 ммоль), HOBt (3,6 г, 27,1 ммоль), EDCI (5,18 г, 27,1 ммоль) і проміжну сполуку 1 (6,0 г, 24,7 ммоль), і реакційну суміш перемішували протягом ночі. Потім додавали воду (q.s.), і суміш екстрагували за допомогою DCM. Відокремлений органічний шар сушили (Na2SO4), фільтрували, і розчинник упарювали. Залишок очищали шляхом хроматографії на колонці (петролейний ефір/EtOAc, градієнтне елюювання від 15/1 до 10/1). 17 UA 107963 C2 Фракції продукту збирали, і розчинник упарювали у вакуумі, отримуючи 8,2 г проміжної сполуки 2 (88,6 %-вий вихід). Приклад A3 a) Отримання проміжної сполуки 3 5 10 15 20 25 30 35 Суміш 2-аміно-4,6-дифторбензойної кислоти (60 г, 346 ммоль), тетрагідро-2,5диметоксифурана (45,7 г, 346 ммоль) і гідрохлорида піридина (1:1) (40 г, 346 ммоль) у діоксані (500 мл) нагрівали при кипінні із зворотним холодильником протягом ночі. Потім розчинник упарювали, і залишок розчиняли в EtOAc (100 мл). Даний розчин промивали насиченим сольовим розчином і водою. Органічний шар відділяли, сушили (MgSO 4), фільтрували, і розчинник упарювали. Вихід: 70 г сирої проміжної сполуки 3, яку використовували як таку на наступній стадії реакції. b) Отримання проміжної сполуки 4 До розчину проміжної сполуки 3, HOBt (47 г, 346 ммоль) і EDCI (70 г, 346 ммоль) у ДМФ (300 мл) додавали NH3·H2O (100 мл). Реакційну суміш перемішували протягом ночі. Потім розчинник упарювали, і залишок розчиняли в EtOAc. Цей органічний розчин спочатку промивали насиченим сольовим розчином і водою, потім сушили (MgSO4) і фільтрували, і в кінці розчинник упарювали. Вихід: 55 г сирої проміжної сполуки 4, яку використовували як таку на наступній стадії реакції. c) Отримання проміжної сполуки 5 До суміші проміжної сполуки 4 (45 г, 202,5 ммоль) у ТГФ (500 мл) додавали BH3·Me2S (10 M розчин; 40,5 мл, 405 ммоль). Реакційну суміш кип'ятили із зворотним холодильником протягом ночі в атмосфері N2. Далі суміш охолоджували на бані крига-вода і додавали 6н розчин HCl (10 мл). Суміш знову кип'ятили із зворотним холодильником протягом 30 хвилин. Суміш охолоджували на бані крига-вода і додавали твердий NaOH до pH>9. Суміш екстрагували за допомогою DCM (2 рази по 300 мл). Органічні шари відділяли, об'єднували, сушили (MgSO 4), фільтрували, і розчинник упарювали. Залишок коричневого кольору перетворювали в HCl сольову форму (1:1) за допомогою суміші HCl/2-пропанол, отримуючи 35 г проміжної сполуки 5 (71 %-вий вихід). d) Отримання проміжної сполуки 6 4-(1,1-дифторетіл)бензойну кислоту (1,17 г, 6,13 ммоль) розчиняли в DCM (50 мл). До розчину додавали Et3N (7,3 мл), HOBt (0,828 г, 6,13 ммоль), EDCI (1,17 г, 6,13 ммоль) і проміжну 18 UA 107963 C2 5 10 15 20 25 30 35 сполуку 5 (1,5 г, 6,13 ммоль), і реакційну суміш перемішували протягом ночі при кімнатній температурі. Потім розчинник упарювали, і до залишку додавали воду. Водну суміш екстрагували за допомогою DCM. Органічний шар відділяли, сушили (Na 2SO4), фільтрували, і розчинник упарювали. Вихід: 1,4 г проміжної сполуки 6 (60 %-вий вихід). Приклад A4 a) Отримання проміжної сполуки 7 3-ацетил-4-фторбензонітрил (11,0 г, 67,4 ммоль) розчиняли в трифториді (диетиламіно)сірки (25 мл) у потоці N2. Розчин нагрівали при температурі 50 °C протягом 16 год. і потім виливали в розчин NaHCO3 (q.s.). Отриману суміш екстрагували за допомогою EtOAc. Органічний шар відділяли, сушили (Na2SO4), фільтрували, і розчинник упарювали при зниженому тиску. Залишок очищали шляхом хроматографії на колонці з силікагелем (елюент: петролейний ефір/EtOAc від 30/1 до 20/1). Бажані фракції збирали, і розчинник упарювали у вакуумі. Вихід: 10,5 г проміжної сполуки 7 (84 %-вий вихід). b) Отримання проміжної сполуки 8 Суміш проміжної сполуки 7 (8,2 г, 5,7 ммоль) у 20 %-вому розчині NaOH (50,0 мл) і EtOH (20,0 мл) кип'ятили із зворотним холодильником і перемішували протягом ночі. Потім суміш концентрували у вакуумі. HCl додавали до pH 2, і утворювався осад. Осад фільтрували і сушили у вакуумі. Твердий продукт використовували як такий на наступній стадії реакції. Вихід: 9,2 г проміжної сполуки 8. c) Отримання проміжної сполуки 9 Суміш проміжної сполуки 1 (1,0 г, 4,2 ммоль), проміжної сполуки 8 (1,0 г, 5,0 ммоль), Et3N (5,0 мл, 36 ммоль), HOBt (0,62 г) і EDCI (0,96 г) у DCM (40 мл) перемішували протягом ночі при кімнатній температурі. Отриману суміш промивали водою (3 рази по 100 мл), сушили (MgSO 4), фільтрували, і розчинник упарювали при зниженому тиску. Залишок очищали шляхом хроматографії на колонці з силікагелем (елюент: петролейний ефір/EtOAc від 20/1 до 10/1). Бажані фракції збирали, і розчинник упарювали у вакуумі. Вихід: 0,9 г проміжної сполуки 9 (59,6 %-вий вихід). Приклад A5 a) Отримання проміжної сполуки 10 У суспензію CuCN (21,5 г, 242 ммоль) у CH3CN (500 мл) додавали трет-бутил нітрит (25 г, 242 ммоль). Суміш нагрівали при температурі 70 °C і перемішували протягом 15 хв. Потім додавали суміш 2-хлор-4-фтор-6-нітробензоламіна (23 г, 121 ммоль) і CH3CN (q.s.), і отриманий 19 UA 107963 C2 5 10 15 20 25 30 35 розчин коричневого кольору нагрівали протягом ночі при температурі 70 °C. Розчинник видаляли у вакуумі. До залишку додавали воду (q.s.), і водну суміш екстрагували за допомогою EtOAc. Відокремлений органічний шар сушили (MgSO 4), фільтрували, і розчинник упарювали. Залишок очищали шляхом хроматографії на колонці з силікагелем (елюент: EtOAc/петролейний ефір 1/4). Бажані фракції збирали, і розчинник упарювали. Вихід: 10 г проміжної сполуки 10 (41 %-вий вихід; твердий продукт жовтого кольору). b) Отримання проміжної сполуки 11 До розчину проміжної сполуки 10 (10 г, 50 ммоль) у HOAc (250 мл) по частинах додавали Fe (11,6 г, 200 ммоль). Реакційну суміш нагрівали при температурі 70 °C протягом 1 години і потім охолоджували до кімнатної температури. Твердий продукт фільтрували, і розчинник упарювали. Залишок розчиняли в EtOAc, промивали водним розчином NaHCO 3 і водою. Органічний шар сушили (MgSO4), фільтрували, і розчинник упарювали. Вихід: 6,2 г проміжної сполуки 11, яку використовували як таку на наступній стадії реакції. c) Отримання проміжної сполуки 12 Розчин проміжної сполуки 11 (6 г, 35 ммоль) і тетрагідро-2,5-диметоксифурана (4,66 г, 35 ммоль) у HOAc (50 мл) нагрівали при температурі кипіння протягом 6 год. Потім розчинник упарювали, і залишок очищали шляхом хроматографії на колонці з силікагелем (елюент: DCM). Бажані фракції збирали і розчинник упарювали. Вихід: 4,6 г проміжної сполуки 12 (90 %-ний вихід). d) Отримання проміжної сполуки 13 До суміші проміжної сполуки 12 (4,4 г, 20 ммоль) у ТГФ (50 мл) додавали 10M розчин BH3·Me2S (2 мл; 20 ммоль). Реакційну суміш кип'ятили із зворотним холодильником протягом ночі в атмосфері N2. Далі суміш охолоджували на бані крига-вода, і до суміші обережно додавали 6н розчин HCl (10 мл). Розчин потім знову кип'ятили із зворотним холодильником протягом 30 хв, і потім знову охолоджували на бані крига-вода. Додавали тверді NaOH до pH>9. Суміш екстрагували за допомогою DCM (2 рази по 300 мл). Відокремлений органічний шар сушили (MgSO4), фільтрували, і розчинник упарювали. Залишок коричневого кольору перетворювали на HCl сіль (1:1) за допомогою суміші HCl/2-пропанол. Вихід: 5 г проміжної сполуки 13 (96 %-вий вихід). Приклад A6 a) Отримання проміжної сполуки 14 Реакцію проводили в атмосфері N2: Суміш 4-бром-3-фторбензонітрила (6,0 г, 30,00 ммоль) і (1-етоксиетеніл)трибутилолова (11,2 мл, 33,00 ммоль) у толуолі (100 мл) перемішували при кімнатній температурі. До суміші додавали Pd(PPh 3)2Cl2 (0,72 г, 1,03 ммоль), і реакційну суміш 20 UA 107963 C2 5 10 15 20 25 30 35 нагрівали при кип'ятинні із зворотним холодильником і перемішували протягом ночі. Суміш охолоджували, і до суміші при перемішуванні додавали 2н розчин KF (50 мл). Через 30 хв до суміші додавали 6н розчин HCl (100 мл), і суміш нагрівали при температурі 70 °C і перемішували протягом 2 год. Нерозчинні речовини фільтрували, і фільтрат екстрагували за допомогою EtOAc (3 рази по 80 мл). Об'єднані органічні шари промивали насиченим сольовим розчином, сушили (MgSO4), фільтрували, і розчинник упарювали у вакуумі. Вихід: 4,3 г проміжної сполуки 14 (88 %-вий вихід). Проміжна сполука 14 може бути далі піддана взаємодії аналогічно методиці реакції, описаній у прикладі A4, з отриманням сполуки 29. Приклад A7 a) Отримання проміжної сполуки 15 Суміш 4-хлор-2,6-дифторбензонітрила (1,66 г, 9,56 ммоль), пірролу (0,67 г, 10 ммоль) і Cs2CO3 (3,7 г, 12 ммоль) у ДМФ (20 мл) перемішували протягом ночі. Далі твердий продукт фільтрували, і розчинник видаляли при зниженому тиску. Залишок очищали шляхом хроматографії на колонці з силікагелем (елюент: суміш EtOAc/петролейний ефір 10/1). Бажані фракції збирали, і розчинник упарювали. Вихід: 1,1 г проміжної сполуки 15 (15 %-вий вихід; твердий продукт білого кольору). Проміжна сполука 15 може бути далі піддана взаємодії аналогічно методиці реакції, описаній у прикладі A1, з отриманням сполуки 32. B. Отримання сполук Приклад B1 a) Отримання сполуки 1 Суміш проміжної сполуки 1 (9,5 г, 39,2 ммоль) і 4-(1,1-дифторетил)бензальдегіда (8,0 г, 47,0 ммоль) в EtOH (15 мл) перемішували і кип'ятили із зворотним холодильником протягом 4 год. Потім суміш охолоджували і кристалізували протягом ночі. Осад фільтрували, промивали ізопропіловим ефіром і сушили у вакуумі. Вихід: 8,0 г сполуки 1 (52,2 %-вий вихід). b) Отримання сполуки 2 і сполуки 3 Сполука 2: S енантіомер; Сполука 3: R енантіомер Сполуку 1 виділяли у вигляді її енантіомерів за допомогою хіральної НФХ (Колонка AD 300 мм*50 мм, 20 мкМ; Рухома фаза: CO2/MeOH(0,2 % DEA) 60/40; Потік: 200 мл/хв). Дві різні фракції збирали, і обидві фракції перетворювали на форму HCl солі за допомогою суміші HCl/EtOH 1/1. Вихід: 3,2 г сполуки 2 (20,8 %-вий вихід; S конфігурація). Вихід: 3,0 г сполуки 3 (19,6 %-вий вихід; R конфігурація). Приклад B2 a) Отримання сполуки 4 21 UA 107963 C2 5 10 15 20 25 30 35 Суміш сполуки 1 (0,334 г, 0,0009 моль) і MnO2 (2,6 г, 0,0299 моль) у DCM (15 мл) перемішували протягом 96 год. при кімнатній температурі. Далі осад фільтрували через діатомову землю, і фільтрат упарювали. Залишок очищали за допомогою препаративної ВЕРХ, отримуючи 0,19 г сполуки 4 (59 %). b) Альтернативне отримання сполуки 4 Проміжну сполуку 2 (4,0 г, 10,67 ммоль) розчиняли в POCl3 (12 мл). Суміш перемішували і кип'ятили із зворотним холодильником протягом ночі. Далі суміш охолоджували і виливали у воду. Водну суміш нейтралізували за допомогою NaOH до pH 7, і потім екстрагували за допомогою DCM. Відокремлений органічний шар сушили (Na 2SO4), фільтрували, і розчинник упарювали. Залишок кристалізували з EtOH, отримуючи сполуку 4 (56,3 %-вий вихід). Приклад B3 a) Отримання сполуки 18 Проміжну сполуку 6 (1,4 г, 3,71 ммоль) розчиняли в POCl3 (10 мл). Суміш перемішували і кип'ятили із зворотним холодильником протягом ночі. Потім суміш охолоджували і виливали у воду. Водну суміш нейтралізували за допомогою NaOH до pH 7, і потім екстрагували DCM. Органічний шар відділяли, сушили (MgSO 4), фільтрували і концентрували. Залишок очищали шляхом колонкової флеш хроматографії на силікагелі (елюент: суміш петролейний ефір/EtOAc 4/1). Фракції продукту збирали і розчинник упарювали з виходом 150 мг сполуки 118 (21,6 %-вий вихід). Приклад B4 a) Отримання сполуки 21 Проміжну сполуку 9 (0,80 г, 2,0 ммоль) розчиняли в POCl3 (3 мл). Суміш перемішували протягом ночі при температурі 100 °C. Потім реакційну суміш виливали в крижану воду. Додавали NaOH до pH 8-9. Суміш потім екстрагували за допомогою DCM. Органічні шари відділяли, сушили (Na2SO4), фільтрували, і розчинник упарювали у вакуумі. Залишок очищали шляхом хроматографії на колонці з силікагелем (елюент: суміш петролейний ефір/EtOAc від 10/1 до 5/1). Бажані фракції збирали, і розчинник упарювали у вакуумі. Вихід: 0,510 г сполуки 21 (вихід 68 %). Приклад B5 a) Отримання сполуки 24 Розчин проміжної сполуки 13 (0,52 г, 2 ммоль) і 4-(1,1-дифторетил)бензальдегіда (0,374 г, 2 ммоль) в EtOH (5 мл) нагрівали при кипінні із зворотним холодильником протягом 4 годин. Потім 22 UA 107963 C2 5 10 суміш охолоджували до кімнатної температури, і твердий продукт збирали і сушили. Вихід: 0,6 г сполуки 24 (80 %-вий вихід; ·HCl). Використовуючи аналогічні методики реакції, описані в наступних прикладах, були отримані наступні сполуки. "Спол. №" позначає номер сполуки. "Сп." відноситься до номера прикладу, відповідно до якого здійснювали спосіб отримання сполуки. У разі, коли сольова форма не 3 4 вказана, сполука була отримана у формі вільної основи. Сполуки, де R і R є воднем, і для яких у таблиці 1 не вказана конкретна стереохімія, були отримані у вигляді сумішей енантіомерів. У разі, коли цільова сполука, отримана з використанням аналогічних методик, як описано в B1 або B5, не перетворюється повністю у форму HCl солі, сполуку перетворювали у форму HCl солі, використовуючи способи, відомі фахівцеві у даній галузі. Згідно типовому способу, сполуки розчиняли в розчиннику, такому як, наприклад, 2-пропанол, і потім поступово по краплях додавали розчин HCl у розчиннику, такому як, наприклад, 2-пропанол. Перемішування протягом певного періоду часу, звичайно близько 10 хвилин, може підвищити швидкість реакції. 15 23 UA 107963 C2 24 UA 107963 C2 5 10 15 20 C. Результати аналізів LCMS Виміри ВЕРХ здійснювали з використанням модуля Agilent 1100, що містить насос, діодноматричний детектор (DAD) (використовуєма довжина хвилі 220 нм), колонковий нагрівач і колонку, як вказано у відповідних методиках нижче. Потік з колонки розділяли на Agilent MSD Series G1946C і G1956A. MS детектор був налагоджений з API-ES (іонізація електророзпилюванням при атмосферному тиску). Мас-спектри були отримані шляхом сканування від 100 до 1000. Напруга капілярної голки була 2500 В для позитивного і 3000 В для негативного режиму іонізації. Напруга фрагментації була 50 В. Температуру осушуючого газу підтримували при 350 °C при потоці 10 л/хв. Обернено фазову ВЕРХ проводили на YMC-Pack ODS-AQ, 50 × 2,0 мм 5 мкм колонка із швидкістю потоку 0,8 мл/хв. Використовували 2 рухомих фази (рухома фаза A: вода з 0,1 % ТФУ; рухома фаза B: CH3CN з 0,05 % ТФУ). Спочатку, 90 % A і 10 % B проводили протягом 0,8 хв. Потім застосовували градієнт 20 % A і 80 % B в 3,7 хв і проводили протягом 3 хв. Використовували типові об'єми ін'єкцій у 2 мкл. Температура печі була 50 °C. (полярність MS: позитивна). Точки плавлення Для ряду сполук, точки плавлення (т.пл.) визначали за допомогою приладу для визначення точок плавлення WRS-2A від фірми Shanghai Precision and Scientific Instrument Co. Ltd. Точки плавлення визначали при лінійному нагріванні із швидкістю 0,2-5,0 °C/хв. Представлені значення є інтервалами плавлення. Максимальна температура була 300 °C. Результати аналітичних визначень показані в таблиці 2. 25 UA 107963 C2 Таблиця 2 + Час утримування (Rt) у хв, пік [M+H] (протонована молекула) і т.пл. (точка плавлення в°C). ("н.в." означає не визначалось; "розкл." позначає розкладалось) + Спол. № Rt [M+H] 1 3,57 359 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 3,38 3,33 3,59 4,00 4,03 3,95 3,99 4,03 4,03 4,04 н.в. 4,11 3,51 3,27 3,97 359 359 357 393 391 393 391 391 391 393 н.в. 393 357 341 371 17 3,53 357 18 3,31 359 т.пл. (°C) Rt [M+H] н.в. 19 3,52 357 206,7-207,6 206,3-206,8 215,2-217,6 н.в. 132,1-134,2 253,5-254,2 162,3-163,5 н.в. н.в. 188,5-191,1 н.в. 233,9-235,0 106,9-109,7 н.в. 89,6-91,2 115,3 розкл. н.в. 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 3,46 3,56 3,84 3,48 3,53 3,77 3,53 3,84 3,71 3,44 3,25 3,44 3,31 3,23 3,95 359 375 391 377 377 409 393 375 371 375 359 393 375 377 375 т.пл. (°C) 247,5 розкл. н.в. н.в. 140,9-142,1 143,2-144,3 240,0-240,7 124,2-125,4 84,9-85,9 н.в. 139,3-141,2 186,3-186,6 170,8-171,5 162,5-164,8 145,3-147,4 158,2-161,3 н.в. 35 3,97 375 н.в. 1 5 10 15 20 25 30 + Спол. № H ЯМР 1 Для ряду сполук спектр H ЯМР визначали на спектрометрі Bruker DPX-300 або Bruker DPX400 із стандартною послідовністю імпульсів, що працюють при 300 Мгц і 400 Мгц, відповідно, використовуючи як розчинники ХЛОРОФОРМ-d (дейтерований хлороформ, CDCl3) або ДМСО-d6 (дейтерований ДМСО, диметил-d6 сульфоксид). Хімічні зрушення (δ) представлені в мільйонних долях (м.д.) відносно тетраметилсилана (ТМС), який використовували як внутрішній стандарт. Сполука № 1: (300 Мгц, ДМСО-d6) δ м.д. 2,01 (т, J=18,9 Гц, 3 H) 3,87 (д, J=14,3 Гц, 1H) 4,57 (д, J=13,9 Гц, 1H) 5,35 (ушир. с, 1H) 5,84 (ушир. с, 1H) 6,30 (т, J=3,2 Гц, 1H) 7,43 (ушир. с, 1H) 7,57-7,77 (м, 5 H) 7,90 (д, J=8,1 Гц, 2H) 10,45 (ушир. с, 2H). Сполука № 2: (300 Мгц, ДМСО-d6) δ м.д. 2,01 (т, J=18,93 Гц, 3 H) 3,88 (д, J=14,32 Гц, 1H) 4,58 (д, J=13,94 Гц, 1H) 5,35 (ушир. с, 1H) 5,84 (ушир. з, 1H) 6,31 (т, J=3,20 Гц, 1H) 7,44(ушир. с, 1H) 7,57-7,78 (м, 5 H) 7,90 (д, J=8,10 Гц, 2H) 10,45 (ушир. с, 2H). Сполука № 3: (300 Мгц, ДМСО-d6) δ м.д. 2,01 (т, J=18,93 Гц, 3Н) 3,88 (д, J=14,13 Гц, 1H) 4,58 (д, J=13,94 Гц, 1H) 5,35 (ушир. с, 1H) 5,84 (д, J=2,64 Гц, 1H) 6,31 (т, J=3,20 Гц, 1H) 7,43 (дд, J=2,64, 1,51 Гц, 1H) 7,56-7,79 (м, 5Н) 7,90 (д, J=7,91 Гц, 2H) 10,40 (ушир. с, 2H). Сполука № 4: (300 Мгц, CDCl3) δ м.д. 1,84 (т, J=18,08 Гц, 3Н) 4,13 (ушир. с, 1H) 5,44 (ушир. с, 1H) 6,25-6,54 (м, 2H) 7,19-7,24 (м, 2H) 7,25-7,35 (м, 2H) 7,42 (м, J=8,29 Гц, 2H) 7,69 (м, J=8,10 Гц, 2H). Сполука № 5: (400 Мгц, ДМСО-d6) δ м.д. 2,01 (т, J=18,97 Гц, 3Н) 3,62 (д, J=13,32 Гц, 1H) 4,39 (д, J=13,32 Гц, 1H) 5,41 (ушир. с, 1H) 5,88 (д, J=2,83 Гц, 1H) 6,30 (т, J=3,23 Гц, 1H) 7,40 (дд, J=3,03, 1,41 Гц, 1H) 7,70 (м, J=8,07 Гц, 2H) 7,80 (д, J=2,42 Гц, 1H) 7,91 (м, J=8,07 Гц, 2H) 8,07 (д, J=2,42 Гц, 1H) 10,26 (ушир. с, 1H) 10,66 (ушир. с, 1H). Сполука № 6: (400 Мгц, CDCl3) δ м.д. 1,93 (т, J=18,1 Гц, 3Н) 4,28 (д, J=11,0 Гц, 1H) 4,87 (д, J=11,0 Гц, 1H) 6,47 (ушир. с, 1H) 6,57 (ушир. с, 1H) 7,41-7,66 (м, 5Н) 7,88 (д, J=7,8 Гц, 2H). Сполука № 8: (400 Мгц, CDCl3) δ м.д. 1,92 (т, J=18,2 Гц, 3Н) 4,08 (д, J=11,3 Гц, 1H) 5,46 (д, J=11,3 Гц, 1H) 6,38-6,46 (м, 1H) 6,51 (д, J=2,5 Гц, 1H) 7,34 (д, J=8,5 Гц, 1H) 7,39 (д, J=8,5 Гц, 1H) 7,46-7,58 (м, 3Н) 7,87 (д, J=8,3 Гц, 2H). Сполука № 9: (400 Мгц, CDCl3) δ м.д. 1,92 (т, J=18,2 Гц, 3Н) 4,16 (ушир. с, 1H) 5,49 (ушир. с, 1H) 6,38-6,57 (м, 2H) 7,30 (д, J=2,0 Гц, 1H) 7,34 (ушир. с, 1H) 7,41 (д, J=1,8 Гц, 1H) 7,51 (м, J=8,3 Гц, 2H) 7,76 (м, J=8,3 Гц, 2H). 26 UA 107963 C2 5 10 15 20 25 30 35 40 45 50 55 60 Сполука № 10: (400 Мгц, CDCl3) δ м.д. 1,95 (т, J=18,3 Гц, 3Н) 4,46 (ушир. с, 1H) 5,82 (ушир. с, 1H) 6,80 (дд, J=4,3, 2,8 Гц, 1H) 7,04 (дд, J=4,3, 1,5 Гц, 1H) 7,29 (д, J=8,8 Гц, 1H) 7,66 (д, J=8,5 Гц, 1H) 7,69 (д, J=8,3 Гц, 2H) 7,79-7,85 (м, 1H) 7,90 (д, J=8,3 Гц, 2H). Сполука № 11: (300 Мгц, ДМСО-d6) δ м.д. 2,01 (т, J=18,8 Гц, 3Н) 3,59 (д, J=14,3 Гц, 1H) 4,57 (д, J=14,3 Гц, 1H) 5,44 (ушир. с, 1H) 5,91 (ушир. с, 1H) 6,32 (т, J=3,2 Гц, 1H) 7,42 (ушир. с, 1H) 7,65-7,79 (м, 3Н) 7,83 (д, J=7,9 Гц, 2H) 7,89 (д, J=8,7 Гц, 1H). Сполука № 13: (300 Мгц, ДМСО-d6) δ м.д. 2,01 (т, J=19,0 Гц, 3Н) 3,83 (д, J=14,3 Гц, 1H) 4,53 (д, J=13,9 Гц, 1H) 5,42 (ушир. с, 1H) 5,83 (ушир. с, 1H) 6,30 (т, J=3,0 Гц, 1H) 7,49 (ушир. с, 1H) 7,70 (д, J=7,9 Гц, 2H) 7,77-7,94 (м, 4Н) 10,42 (ушир. с, 2H). Сполука № 14: (300 Мгц, CDCl3) δ м.д. 1,90 (т, J=18,1 Гц, 3Н) 4,17 (ушир. с, 1H) 5,50 (ушир. с, 1H) 6,43-6,55 (м, 2H) 7,22-7,30 (м, 2H) 7,30-7,45 (м, 3Н) 7,56 (д, J=7,5 Гц, 1H) 7,76 (д, J=7,9 Гц, 1H) 7,84 (с, 1H). Сполука № 15: (400 Мгц, CDCl3) δ м.д. 1,92 (т, J=18,2 Гц, 3Н) 4,74 (с, 2H) 6,43-6,51 (м, 1H) 6,53 (дд, J=3,8, 1,5 Гц, 1H) 7,09 (т, J=8,3 Гц, 1H) 7,18 (д, J=8,3 Гц, 1H) 7,35 (тд, J=8,1, 5,9 Гц, 1H) 7,39-7,43 (м, 1H) 7,52 (м, J=8,3 Гц, 2H) 7,78 (м, J=8,3 Гц, 2H). Сполука № 16: (300 Мгц, CDCl3) δ м.д. 1,93 (т, J=18,18 Гц, 3Н) 2,60 (с, 3Н) 4,13 (ушир. с, 1H) 5,17 (ушир. с, 1H) 6,42-6,53 (м, 2H) 7,20 (д, J=1,88 Гц, 1H) 7,24 (д, J=1,88 Гц, 1H) 7,33-7,40 (м, 1H) 7,52 (м, J=8,29 Гц, 2H) 7,75 (м, J=8,29 Гц, 2H). Сполука № 18: (400 Мгц, CDCl3) δ м.д. 1,92 (т, J=18,1 Гц, 3Н) 4,69 (ушир. с, 2H) 6,45-6,49 (м, 1H) 6,49-6,53 (м, 1H) 6,84 (тд, J=9,0, 2,4 Гц, 1H) 6,95 (дт, J=9,0, 1,9 Гц, 1H) 7,33 (дд, J=2,8, 1,5 Гц, 1H) 7,51 (м, J=8,3 Гц, 2H) 7,75 (м, J=8,3 Гц, 2H). Сполука № 20: (400 Мгц, CDCl3) δ м.д. 2,00 (т, J=18,6 Гц, 3Н) 4,77 (ушир. с, 2H) 6,53 (ушир. с, 1H) 6,59 (ушир. с, 1H) 7,06-7,26 (м, 3Н) 7,33-7,44 (м, 1H) 7,47 (ушир. с, 1H) 7,90 (ушир. с, 1H) 7,95 (д, J=6,5 Гц, 1H). Сполука № 21: (300 Мгц, CDCl3) δ м.д. 2,01 (т, J=18,6 Гц, 3Н) 4,24 (ушир. с, 1H) 5,62 (ушир. с, 1H) 6,50-6,79 (м, 2H) 7,16-7,33 (м, 2H) 7,38 (т, J=7,9 Гц, 1H) 7,43-7,62 (м, 2H) 7,85-8,15 (м, 2H). Сполука № 22: (400 Мгц, CDCl3) δ м.д. 1,92 (т, J=18,1 Гц, 3Н) 4,24 (д, J=11,3 Гц, 1H) 4,82 (д, J=11,3 Гц, 1H) 6,39-6,46 (м, 1H) 6,49 (дд, J=3,9, 1,4 Гц, 1H) 7,37 (д, J=8,0 Гц, 1H) 7,44 (д, J=8,3 Гц, 1H) 7,51 (м, J=8,3 Гц, 2H) 7,55 (дд, J=2,8, 1,5 Гц, 1H) 7,83 (м, J=8,5 Гц, 2H). Сполука № 23: (400 Мгц, CDCl3) δ м.д. 2,00 (т, J=18,6 Гц, 3Н) 5,03 (ушир. с, 2H) 6,45-6,52 (м, 2H) 6,85 (тд, J=9,0, 2,4 Гц, 1H) 6,95 (д, J=9,3 Гц, 1H) 7,07-7,18 (м, 1H) 7,33 (т, J=2,1 Гц, 1H) 7,697,81 (м, 1H) 7,92 (дд, J=7,3, 2,0 Гц, 1H). Сполука № 24: (400 Мгц, ДМСО-d6) δ м.д. 2,01 (т, J=18,97 Гц, 3Н) 3,83 (д, J=14,13 Гц, 1H) 4,54 (д, J=14,13 Гц, 1H) 5,41 (ушир. с, 1H) 5,85 (ушир. с, 1H) 6,32 (т, J=3,43 Гц, 1H) 7,46 (ушир. с, 1H) 7,65 (дд, J=9,28, 2,42 Гц, 1H) 7,67-7,74 (м, 3Н) 7,85 (д, J=807,00 Гц, 2H) 10,15 (ушир. з, 1H) 10,44 (ушир. с, 1H). Сполука № 25: (400 Мгц, CDCl3) δ м.д. 1,99 (т, J=18,4 Гц, 3Н) 4,14 (ушир. с, 1H) 5,45 (ушир. с, 1H) 6,44-6,55 (м, 2H) 7,05-7,17 (м, 1H) 7,30 (д, J=2,0 Гц, 1H) 7,34 (т, J=2,3 Гц, 1H) 7,41 (д, J=2,0 Гц, 1H) 7,71-7,83 (м, 1H) 7,91 (дд, J=7,3, 2,3 Гц, 1H). Сполука № 26: (400 Мгц, CDCl3) δ м.д. 1,99 (т, J=18,3 Гц, 3Н) 4,12 (ушир. с, 1H) 5,44 (ушир. с, 1H) 6,42-6,55 (м, 2H) 7,05 (дд, J=8,9, 2,4 Гц, 1H) 7,09-7,20 (м, 2H) 7,33 (т, J=2,1 Гц, 1H) 7,72-7,83 (м, 1H) 7,92 (дд, J=7,3, 2,3 Гц, 1H). Сполука № 27: (400 Мгц, CDCl3) δ м.д. 1,92 (т, J=18,2 Гц, 3Н) 4,16 (ушир. с, 1H) 5,47 (ушир. с, 1H) 6,42-6,55 (м, 2H) 7,04 (дд, J=8,9, 2,4 Гц, 1H) 7,16 (дд, J=8,3, 2,5 Гц, 1H) 7,29-7,36 (м, 1H) 7,51 (м, J=8,3 Гц, 2H) 7,76 (м, J=8,0 Гц, 2H). Сполука № 28: (300 Мгц, CDCl3) δ м.д. 1,91 (т, J=18,2 Гц, 3Н) 2,59 (с, 3Н) 4,04 (д, J=11,1 Гц, 1H) 5,11 (д, J=11,1 Гц, 1H) 6,33-6,44 (м, 1H) 6,44-6,53 (м, 1H) 7,12 (д, J=8,3 Гц, 1H) 7,33 (д, J=8,1 Гц, 1H) 7,45-7,58 (м, 3Н) 7,84 (д, J=8,1 Гц, 2H). Сполука № 29: (300 Мгц, CDCl3) δ м.д. 2,00 (т, J=18,9 Гц, 3Н) 4,20 (ушир. с, 1H) 5,53 (ушир. с, 1H) 6,42-6,50 (м, 1H) 6,50-6,56 (м, 1H) 7,28-7,35 (м, 2H) 7,37 (дд, J=2,8, 1,7 Гц, 1H) 7,38-7,43 (м, 1H) 7,46-7,63 (м, 3Н). Сполука № 30: (400 Мгц, CDCl3) δ м.д. 2,00 (т, J=18,6 Гц, 3H) 4,73 (ушир. с, 2H) 6,42-6,49 (м, 1H) 6,50-6,57 (м, 1H) 7,09 (т, J=8,5 Гц, 1H) 7,18 (д, J=8,0 Гц, 1H) 7,31-7,41 (м, 2H) 7,47-7,61 (м, 3Н). Сполука № 31: (400 Мгц, CDCl3) δ м.д. 2,00 (т, J=18,4 Гц, 3H) 4,14 (ушир. с, 1H) 5,48 (ушир. с, 1H) 6,44-6,51 (м, 1H) 6,51-6,59 (м, 1H) 7,04 (дд, J=8,9, 2,4 Гц, 1H) 7,17 (дд, J=8,3, 2,3 Гц, 1H) 7,34 (дд, J=2,8, 1,5 Гц, 1H) 7,54 (д, J=3,3 Гц, 3Н). Сполука № 32: (300 Мгц, CDCl3) δ м.д. 1,92 (т, J=18,1 Гц, 3H) 4,70 (ушир. с, 2H) 6,43-6,55 (м, 2H) 7,11 (дд, J=8,6, 1,8 Гц, 1H) 7,18-7,23 (м, 1H) 7,31-7,39 (м, 1H) 7,51 (м, J=8,3 Гц, 2H) 7,74 (м, J=8,1 Гц, 2H). 27 UA 107963 C2 5 10 15 20 25 30 Сполука № 33: (400 Мгц, ДМСО-d6) δ м.д. 2,02 (т, J=18,97 Гц, 3Н) 4,57 (ушир. с, 2H) 6,55 (т, J=3,23 Гц, 1H) 6,59 (дд, J=3,84, 1,41 Гц, 1H) 7,36 (тд, J=9,49, 2,42 Гц, 1H) 7,40-7,48 (м, 1H) 7,517,58 (м, 2H) 7,62 (т, J=7,87 Гц, 1H) 7,81 (дд, J=2,62, 1,41 Гц, 1H). Сполука № 34: (400 Мгц, CDCl3) δ м.д. 1,88-2,10 (м, 3H) 4,42 (ушир. с, 1H) 4,78 (ушир. с, 1H) 6,45-6,50 (м, 2H) 7,12 (дд, J=10,0, 8,8 Гц, 1H) 7,29 (дд, J=8,0, 2,0 Гц, 1H) 7,36 (т, J=2,3 Гц, 1H) 7,40 (д, J=2,0 Гц, 1H) 7,42 (д, J=8,0 Гц, 1H) 7,69-7,79 (м, 1H) 7,93 (дд, J=7,4, 2,1 Гц, 1H). Сполука № 35: (400 Мгц, CDCl3) δ м.д. 1,93-2,06 (м, 3H) 4,27 (д, J=11,3 Гц, 1H) 4,86 (д, J=11,0 Гц, 1H) 6,39-6,45 (м, 1H) 6,49 (дд, J=3,6, 1,4 Гц, 1H) 7,13 (дд, J=10,2, 8,9 Гц, 1H) 7,24 (т, J=8,0 Гц, 1H) 7,41-7,46 (м, 1H) 7,48 (дд, J=8,2, 1,4 Гц, 1H) 7,59 (дд, J=2,6, 1,4 Гц, 1H) 7,79-7,89 (м, 1H) 8,03 (дд, J=7,3, 2,3 Гц, 1H). D. Фармакологічні приклади Приклад D.1: Вимір протигрибкової активності in vitro Стандартне дослідження сприйнятливості проводили на 96-лункових планшетах (U-образне дно, Greiner Bio-One). Серійні розведення (2-кратне або 4-кратне) 20 мМ первинних розчинів сполуки виконували в 100 % ДМСО, потім проміжну стадію розведення у воді. Далі ці серійні розведення (10 мкл) наносили на тест-пластини, які можуть зберігатись у темряві при 4 °C протягом не більше 2 тижнів. Прийнятний широкий діапазон доз був включений з 64 мкМ як найвища концентрація в тесті. До культурального середовища RPMI-1640 додавали L-глютамін, 2 % глюкозу і буферували 3-(N-морфоліно)пропансульфоновою кислотою (MOPS) при рН 7,0±0,1. Різні види грибів/ізолятів (таблиця 3а) кріоконсервували і розбавляли 1/1000 в середовищі безпосередньо перед використанням. Потім в кожну лунку додавали 200 мкл стандартного 3 інокулума, що містить 10 колонієутворюючих одиниць (КОЕ). Позитивний контроль (100 %-ве зростання = грибкові культури без протигрибкової) і негативний контроль (0 % зростання = середовище RPMI-MOPS) включали в кожен планшет. Оптимальний час інкубації і температура залежали від вигляду грибів і змінювались від 24 год. для дріжджів (37 °C) до одного тижня або більше для дерматофітів (27 °C). Інгібування зростання грибів вимірювали після додавання 10 мкл 0,005 % (маса/об'єм) Resazurin (Sigma Aldrich) у кожну лунку, грунтуючись на принципі, що живі клітини перетворять нефлуоресцентний синій резазурин у рожевий і флуоресцентний резофурин, що дозволяє здійснити флуориметричне зчитування (λex 550 нм і λeм 590 нм) після додаткового інкубаційного періоду (час "Resa", наведений у таблиці 3а). Результати представлені в таблиці 3b у вигляді значень pIC50. Таблиця 3а Умови інкубації для різних видів грибів. "Resa time" відповідає додатковому часу інкубації після додавання резазурина до тест-системи Види Microsporum canis Trichophyton mentagrophytes Trichophyton rubrum Scedosporium apiospermum Scedosporium prolificans Sporothrix schenkii Aspergillus fumigatus Candida parapsilosis Cryptococcus neoformans Rhizopus oryzae Rhizomucor miehei Mucor circinelloides Температура (°C) 27 27 27 37 37 27 27 37 37 37 37 27 Час 9 днів 7 днів 7 днів 48 год. 48 год. 4 днів 48 год. 24 год. 24 год. 24 год. 48 год. 48 год. 35 28 Час інкубації після додавання резазурина 24 год. 24 год. 24 год. 17 год. 17 год. 24 год. 17 год. 4 год. 4 год. 6 год. 17 год. 17 год.
ДивитисяДодаткова інформація
Назва патенту англійськоюNovel antifungal 5,6-dihydro-4-[(difluoroethyl)phenyl]-4h-pyrrolo[1,2-a][1,4]benzodiazepine and 4-(difluoroethyl)phenyl-6h-pyrrolo[1,2-a][1,4]benzodiazepine derivatives
Автори англійськоюMeerpoel, Lieven, Maes, Louis, Jules, Roger, Marie, de Wit, Kelly
Автори російськоюМеерпоэль Ливен, Мес Луи Жюль Роже Мари, де Вит Келли
МПК / Мітки
МПК: A61P 31/10, C07D 487/04, A61K 31/5517
Мітки: 4-(дифторетил)феніл-6н-піроло[1,2-a][1,4]бензодіазепіну, 5,6-дигідро-4-[(дифторетил)феніл]-4н-піроло[1,2-a][1,4]бензодіазепіну, протигрибкові, похідні
Код посилання
<a href="https://ua.patents.su/39-107963-protigribkovi-pokhidni-56-digidro-4-diftoretilfenil-4n-pirolo12-a14benzodiazepinu-i-4-diftoretilfenil-6n-pirolo12-a14benzodiazepinu.html" target="_blank" rel="follow" title="База патентів України">Протигрибкові похідні 5,6-дигідро-4-[(дифторетил)феніл]-4н-піроло[1,2-a][1,4]бензодіазепіну і 4-(дифторетил)феніл-6н-піроло[1,2-a][1,4]бензодіазепіну</a>
Попередній патент: Курильний виріб з термостійким листовим матеріалом
Наступний патент: Вогнезахисна полімерна композиція
Випадковий патент: Шлаколужний цемент для бетонів і будівельних розчинів












