N -(3-трифторметилфеніл)-2-(2-оксо-3,5a,6,11b-тетрагідро-2н,5н-хромено[4′,3′:4,5]тіопірано[2,3- d][1,3]тіазол-3-іл)ацетамід, що проявляє протипухлинну активність
Номер патенту: 49340
Опубліковано: 26.04.2010
Автори: Крищишин Анна Петрівна, Зіменковський Борис Семенович, Лесик Роман Богданович
Формула / Реферат
N-(3-трифторметилфеніл)-2-(2-оксо-3,5а,6,11b-тетрагідро-2H,5H-xpoмено[4',3':4,5]тioпipaнo[2,3-d][1,3]тiaзол-3-іл)aцетамід, формули
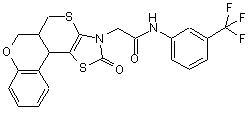 ,
,
що проявляє протипухлинну активність.
Текст
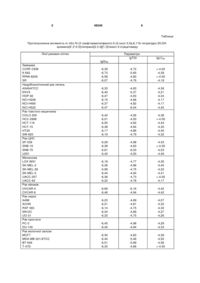
N-(3-трифторметилфеніл)-2-(2-оксо3,5а,6,11b-тетрагідро-2H,5H xpoмено[4',3':4,5]тioпipaнo[2,3-d][1,3]тiaзол-3іл)aцетамід, формули F S F H N F N O O S O Корисна модель стосується синтезу органічних сполук і фармації, зокрема одержання біологічно активного N-(3-трифторметилфеніл)-2-(2-оксо3,5а,6,11b-тетрагідро-2H,5Hxpoмено[4',3':4,5]тioпipaнo[2,3-d][1,3]тiaзол-3іл)aцетаміду, що проявляє протипухлинну активність і може бути використаний в клінічній медицині як протипухлинний лікарський засіб. Серед похідних тіопірано[2,3-d]тіазолу, синтетичними прекурсорами яких є біологічно активні 5іліден-4-тіазолідони, ідентифіковано ряд сполук з протипухлинною активністю. Зокрема, для ряду похідних характерне селективне інгібування клітинних ліній лейкемії, меланоми, недрібноклітинного раку легень, раку нирок і молочної залози, епітеліального раку [Roman Lesyk, Borys Zimenkovsky, Dmytro Atamanyuk, Frank Jensen, Katarzyna Kiec-Kononowicz and Andrzej Gzella. Anticancer thiopyrano[2,3-d][1,3]thiazol-2-ones with norbomane moiety. Synthesis, cytotoxicity, physicochemical properties, and computational studies, Bioorganic & Medicinal Chemistry, 2006, 14(15), 5230-5240; Dmytro Atamanyuk, Borys Zimenkovsky & Roman Lesyk. Synthesis and anticancer activity of novel thiopyrano[2,3-d][1,3]thiazole based compounds containing norbomane moiety, Journal of Sulfur Chemistry, 2007, 29(2), 151-162]. Враховуючи наведене пошук нових синтетичних протипухлинних засобів із групи похідних тіопірано[2,3d]тіазолу є актуальним для сучасної фармацевтичної і медичної хімії. Відомі лікарські засоби з протипухлинною активністю, наприклад, метотрексат [Машковский М.Д. Лекарственные средства. В двух томах. Т.2. Изд. 14-е, новое. - Москва: Новая волна, 2002. - С. 423]. Метотрексат за структурою близький до фолеатної кислоти і є її антиметаболітомантагоністом. Він діє в S-фазу клітинного циклу, механізм протиракового ефекту пов'язаний з інгібуванням синтезу пуринових нуклеотидів і тимідилату шляхом незворотного зв'язування з дигідрофолатредуктазою, що перешкоджає відновленню дигідрофолату в активний тетрагідрофолат. Даний лікарський засіб є активним відносно клітин, що швидко ростуть, і володіє необхідними лікувальними властивостями, проте характеризується значними побічними ефектами: найчастіше - нудота, блювота, дисфагія, стоматит, фарингіт, лейкопенія і тромбоцитопенія; можливі - еритема, кропивниця, гіперпігментація, телеангіектазії, акне, фурункульоз, анемія, септицемія, анорексія, діарея, мелена, кровотечі; при довготривалому прийомі - гостра дистрофія печінки, цироз, анурія, азотемія, гематурія, олігоспермія і порушення менструаль , (19) UA (11) 49340 (13) U що проявляє протипухлинну активність. 3 ного циклу, легеневі інфільтрати, пневмосклероз, імуносупресія, метаболічні порушення, остеопороз. Відома також сполука формули N N P N S O CH3 , яка є похідною тіазолідину і застосовується для лікування хворих еритремією [Машковский М.Д. Лекарственные средства. В двух томах. Т. 2. Изд. 14-е, новое. - Москва: Новая волна, 2002. - С. 417]. Описаний лікарський засіб відомий під назвою іміфос. Однак і цей лікарський засіб має ряд недоліків, зокрема, при його застосуванні можуть розвиватись лейкопенія і тромбоцитопенія. Іміфос протипоказаний для хворих з різким виснаженням, анемією, лейкопенією та тромбоцитопенією. В основу корисної моделі поставлене завдання створення ефективного протипухлинного засобу з меншими побічними явищами та прийнятним токсикологічним профілем. Поставлене завдання вирішується тим, що синтезований N-(3-трифторметилфеніл)-2-(2-оксо3,5а,6,11b-тетрагідро-2H,5Hхромено[4',3':4,5]тіопірано[2,3-d][1,3]тіазол-3іл)ацетамід, формули F S F H N F N O O S O , який проявляє протипухлинну активність. Синтезована сполука є білими кристалічним порошком, розчинним в ДМФА, малорозчинним в оцтовій кислоті, спиртах і нерозчинним в етері та воді. Для підтвердження складу і структури синтезованої сполуки були використані відомі фізикохімічні методи, зокрема 1H-ЯМР-спектроскопія та елементний аналіз. Одержані результати свідчать про відповідність синтезованої сполуки заявленій. Заявлений N-(3-трифторметилфеніл)-2-(2оксо-3,5а,6,11b-тетрагідро-2H,5Hxpoмено[4',3':4,5]тioпipaнo[2,3-d][1,3]тiaзол-3іл)aцетамід одержують у декілька стадій, що включають синтез в умовах «доміно»-реакції Кньовенагеля-гетеро-Дільса-Альдера 2-оксо-3,5а,6,11b 49340 4 тетрагідро-2H,5H-хромено[4',3':4,5]тіопірано[2,3d][1,3]тіазол, який через стадію одержання Nкалійної солі алкілюють відповідним хлорацетамідом, що приводить до утворення цільового продукту. Визначення протипухлинної активності N-(3трифторметилфеніл)-2-(2-оксо-3,5а,6,11bтетрагідро-2H,5H-xpoмено[4',3':4,5]тioпipaнo[2,3d][1,3]тiaзол-3-іл)aцетаміду проведено in vitro на 57 лініях ракових клітин при дії речовин в концентраціях 10-4-10-8М згідно зі стандартною процедурою оцінки протипухлинної активності сполук в Національному інституті раку США (National Cancer Institute of National Institute of Health, USA), в рамках Development Therapeutic Program (згідно з договором між вказаною установою та Львівським національним медичним університетом імені Данила Галицького). У результаті проведених експериментальних досліджень одержано 3 дозозалежні параметри: lgGI50 - логарифм концентрації досліджуваної речовини, яка пригнічує ріст 50% клітин, lgTGI - логарифм концентрації досліджуваної речовини, яка повністю пригнічує ріст клітин, lgLC50 - логарифм концентрації досліджуваної речовини, яка спричиняє загибель 50% клітин [Alley M.C., Scudiero D.A., Monks P.A. et al, Feasibility of Drug Screening with Panels of Human Tumor Cell Lines Using a Microculture Tetrazolium Assay, Cancer Research., 1988, Vol. 48, P. 589-601; Boyd M.R., Paull K.D., Drug Development Research., 1995, Vol. 34, P. 91-109; Grever M.R., Schepartz S.A., Chabner B.A., Seminars in Oncology, 1992. - Vol. 19, № 6. - P.622-638; A. Monks, D. Scudiero, P. Skehan, R. Shomaker, K. Paull, D. Vistica, C. Hose, J. Langley, P. Cronise, A. Vaigro-Wolff, M. GrayGoodrich, H. Campbell, J. Mayo, M. Boyd, J. Nat. Cancer. Inst., 1991, 83, P. 757-766]. В умовах експерименту, результати якого наведені у таблиці, заявлений N-(3трифторметилфеніл)-2-(2-оксо-3,5а,6,11bтетрагідро-2H,5H-xpoмено[4',3':4,5]тioпipaнo[2,3d][1,3]тiaзол-3-іл)aцетамід виявив високу протипухлинну активність. Сполука, що заявляється, проявила помітне інгібування росту майже всіх ліній ракових клітин. Найменші ефективні значення концентрацій N-(3трифторметилфеніл)-2-(2-оксо-3,5а,6,11bтетрагідро-2H,5H-xpoмено[4',3':4,5]тioпipaнo[2,3d][1,3]тiaзол-3-іл)aцетаміду спостерігалися при дії на лінію лейкемії К-562 (lgGI50 =-6,73), лінію раку товстого кишечника НСТ-116 (lgGI50 =-6,55), лінію раку ЦНС SNB-75 (lgGI50 =-6,61), лінію раку яйників OVCAR-4 (lgGI50 =-6,69), лінію раку молочної залози ВТ-549 (lgGI50= -6,51). 5 49340 6 Таблиця Протипухлинна активність in vitro N-(3-трифторметилфеніл)-2-(2-оксо-3,5а,6,11b-тетрагідро-2H,5Hxpoмено[4',3':4,5]тioпipaнo[2,3-d][1,3]тiaзол-3-іл)aцетаміду Лінії ракових клітин Параметри lgTGI lgLC50 lgGI50 Лейкемія CCRF-CEM К-562 RPMI-8226 SR Недрібноклітинний рак легень А549/АТСС EKVX НОР-92 NCI-H226 NCI-H460 NCI-H522 Рак товстого кишечника COLO 205 НСС-2998 НСТ-116 НСТ-15 НТ29 SW-620 Рак ЦНС SF-539 SNB-19 SNB-75 U251 Меланома LOX IMVI SK-MEL-2 SK-MEL-28 SK-MEL-5 UACC-257 UACC-62 Рак яйників OVCAR-4 OVCAR-8 Рак нирок А498 ACHN RXF 393 SN12C UO-31 Рак простати РС-3 DU-145 Рак молочної залози MCF7 MDA-MB-321/ATCC ВТ-549 T-47D -6,39 -6,73 -6,58 -6,07 -4,72 -5,65 -4,80 -4,76 >-4.00 -4,39 >-4.00 -4,18 -6,33 -6,40 -6,47 -6,15 -6,37 -6,47 -4,83 -5,37 -4,93 -4,66 -4,82 -6,04 -4,36 -4,21 -4,34 -4,17 -4,17 -4,42 -6,42 -6,01 -6,55 -6,38 -6,17 -6,19 -4,95 -4,50 -4,92 -4,84 -4,86 -4,79 -4,38 >-4.00 -4,44 -4,30 -4,40 -4,32 -6,29 -6,38 -6,61 -6,42 -4,98 -4,63 -6,03 -4,93 -4,43 >-4.00 -4,53 -4,46 -6,18 -6,36 -5,99 -6,44 -6,36 -6,22 -4,77 -4,96 -4,75 -4,94 -4,73 -4,78 -4,35 -4,40 -4,22 -4,41 >-4.00 -4,17 -6,69 -6,46 -6,16 -4,94 -4,42 -4,42 -6,23 -6,21 -6,14 -6,34 -6,33 -4,69 -4,81 -4,75 -4,89 -4,75 -4,07 -4,32 -4,32 -4,27 -4,26 -6,45 -6,42 -4,98 -4,94 -4,29 -4,33 -6,30 -6,44 -6,51 -6,33 -4,83 -5,46 -5,89 -4,66 -4,39 -4,52 -4,56 >-4.00 7 49340 Таким чином, заявлена сполука виявляє високу протипухлинну дію і є перспективним протипухлинним засобом. Для розуміння даної корисної моделі нижче наведено приклад одержання N-(3трифторметилфеніл)-2-(2-оксо-3,5а,6,11bтетрагідро-2H,5H-xpoмено[4',3':4,5]тioпipaнo[2,3d][1,3]тiaзол-3-іл)aцетаміду. Сполуку синтезують наступним чином. 1. Синтез 2-оксо-3,5а,6,11b-тетрагідро-2H,5Hхромено[4',3':4,5]тіопірано[2,3-d][1,3]тіазолу. У круглодонну колбу поміщають по 0,01 моль 2алілоксибензальдегіду та 4-тіоксо-2-тіазолідинону, додають 20мл льодяної оцтової кислоти та нагрівають на водяній лазні зі зворотнім холодильником протягом 3 год. Після охолодження реакційної суміші утворений осад відфільтровують і перекристалізовують з діоксану. Вихід 80%. Жовтий кристалічний порошок. Ттопл=230-231°С. C13H11NO2S2, Знайдено, %: N 5,00, S 23,30; Вирахувано, %: N 5,05, S 23,12. ЯМР 1Н (400МГц, DMSO-d6), , м.ч.: 2,22-2,36 (м, 1Н, 5-Н), 3,00-3,08 (м, 1Н, 5-Н), 3,15 (дд, 1Н, J=3,6, 12,0Гц, 5-Н), 3,82-4,00 (м, 1Н, 6-Н), 3,97 (д, 1Н, J = 10,5Гц, 11b-H), 4,39 (дд, 1Н, J= 3,6, 10,3Гц, 6-Н), 6,85 (д, 1Н, J = 7,6Гц, 8-Н), 6,95 (т, 1Н, J=7,8Гц, 10-Н), 7,17 (т, 1Н, J=7,6Гц, 9-Н), 7,43 (д, 1Н, J=7,8Гц, 11-Н), 11,50 (с, 1Н, NH). 2. Синтез калійної солі 2-оксо-3,5а,6,11bтетрагідро-2H,5H-хромено[4',3':4,5]тіопірано[2,3d][1,3]тіазолу. У плоскодонну колбу поміщають 0,01 моль 2-оксо-3,5а,6,11b-тетрагідро-2H,5Hхромено[4',3':4,5]тіопірано[2,3-d][1,3]тіазолу та суспендують у 30мл етанолу. До отриманої суспензії Комп’ютерна верстка А. Крулевський 8 додають розчин 0,01 моль гідроксиду калію в 15мл етанолу. Реакційну суміш перемішують при кімнатній температурі протягом 1 год. Утворену калійну сіль відфільтровують, промивають етанолом, ефіром та використовують у подальших перетвореннях без додаткової очистки. 3. Синтез N-(3-трифторметилфеніл)-2-(2-оксо3,5а,6,11b-тетрагідро-2H,5Hxpoмено[4',3':4,5]тioпipaнo[2,3-d][1,3]тiaзол-3іл)aцетаміду. У круглодонну колбу із зворотнім холодильником поміщають по 0,01 моль N-калійної солі 2-оксо-3,5а,6,11b-тетрагідро-2H,5Hхромено[4',3':4,5]тіопірано[2,3-d][1,3]тіазолу та N(3-трифторметилфеніл)-ацетаміду, додають 15мл ДМФА, каталітичну кількість йодиду та карбонату калію. Реакційну суміш кип'ятять протягом 3 год. Продукт реакції відфільтровують після повного охолодження реакційної суміші. Промивають водою та ефіром. Перекристалізовують з суміші ДМФА-етанол (1:1). Вихід 47%. Білий кристалічний порошок. Ттопл=240-242°С. C22H16F3N2O3S2, Знайдено, %: N 5,97, S 13,34; Вирахувано, %: N 5,85, S 13,40. ЯМР 1Н (400МГц, DMSO-d6), , м.ч.: 2,222,40 (м, 1H, 5а-Н), 3,00-3,08 (м, 1H, 5-Н), 3,20 (дд, 1H, J=3,8, 12,2Гц, 5-Н), 3,80-3,98 (м, 1H, 6-Н), 4,00 (д, 1Н, J=10,4Гц, 11b-H), 4,56 (дд, 1Н, J=3,6, 10,3Гц, 6-Н), 6,86 (д, 1H, J=7.8Гц, 8-Н), 7,00 (т, 1H, J=7.8Гц, 10-Н), 7,21 (т, 1Н, J=7,6Гц, 9-Н), 7,42-7,48 (м, 2Н, 11-Н; 4-Н, 3-CF3-C6H4), 7,49 (т, 1Н, J=7.8Гц, 5-Н, 3-CF3-C6H4), 7,73 (д, 1Н, J=7.8Гц, 6-Н, 3-CF3C6H4), 8,09 (с, 1Н, 2-Н, 3-CF3-C6H4), 11,78 (с, 1H, NH). Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюN-(3-trifluoromethylphenyl)-2-(2-oxo-3,5a,6,11b-tetrahydro-2h,5h-chromeno[4',3':4,5]thiopyrano[2,3-d][1,3] thiazole-3-yl)acetamid exhibiting anticancer activity
Автори англійськоюKryshyshyn Anna Petrivna, Lesyk Roman Bohdanovych, Zimenkovskyi Borys Semenovych
Назва патенту російськоюN-( 3-трифторметилфенил)-2-(2-оксо-3,5а,6,11b-тетрагидро-2н,5н-хромено[4',3':4,5]тиопирано[2,3- d][1,3]тиазол-3-ил)ацетамид, который проявляет противоопухолевая активность
Автори російськоюКрищишин Анна Петровна, Лесик Роман Богданович, Зименковский Борис Семенович
МПК / Мітки
МПК: C07D 233/00, A61P 31/00
Мітки: протипухлинну, проявляє, активність, d][1,3]тіазол-3-іл)ацетамід, 3-трифторметилфеніл)-2-(2-оксо-3,5a,6,11b-тетрагідро-2н,5н-хромено[4',3':4,5]тіопірано[2,3
Код посилання
<a href="https://ua.patents.su/4-49340-n-3-triftormetilfenil-2-2-okso-35a611b-tetragidro-2n5n-khromeno4345tiopirano23-d13tiazol-3-ilacetamid-shho-proyavlyaeh-protipukhlinnu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">N -(3-трифторметилфеніл)-2-(2-оксо-3,5a,6,11b-тетрагідро-2н,5н-хромено[4′,3′:4,5]тіопірано[2,3- d][1,3]тіазол-3-іл)ацетамід, що проявляє протипухлинну активність</a>
Попередній патент: Пристрій для наведення засувки на гирло фонтануючої свердловини
Наступний патент: Спосіб каталізу
Випадковий патент: Спосіб тренінгу ламп розжарювання