Спосіб одержання 5-аміно-1-арил-3-ціанопіразолів, проміжна сполука для їх одержання та спосіб одержання проміжної сполуки
Номер патенту: 57729
Опубліковано: 15.07.2003
Автори: Хаукінс Девід Віл'ям, Робертс Девід Алан, Вілкінсон Джон Харрі, Клавел Жан-Луіс
Формула / Реферат
1. Спосіб одержання сполуки формули (І):
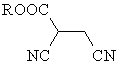 ,
,
(I)
де R являє собою алкіл з нормальним або розгалуженим ланцюгом, що містить від 1 до 18 атомів вуглецю, або його солі, що включає реакцію ціанацетату формули (II):
RO2C-CH2CN,
(II)
де R визначений вище,
з сіллю ціанистоводневої кислоти та формальдегідом або джерелом останнього.
2. Спосіб за п. 1, який відрізняється тим, що сіль ціанистоводневої кислоти являє собою сіль лужного або лужноземельного металу.
3. Спосіб за п. 2, який відрізняється тим, що сіль ціанистоводневої кислоти являє собою ціанистий натрій або ціанистий калій.
4. Спосіб за пп. 1, 2 або 3, який відрізняється тим, що R являє собою алкіл з нормальним або розгалуженим ланцюгом, що має від 1 до 6 атомів вуглецю.
5. Спосіб за будь-яким з пп. 1-4, який відрізняється тим, що сполука формули (II) являє собою етилціаноацетат.
6. Спосіб за будь-яким з пп. 1-5, який відрізняється тим, що джерелом формальдегіду є параформальдегід.
7. Спосіб за будь-яким з пп. з 1-6, який відрізняється тим, що реакцію проводять у присутності розчинника, що являє собою спиртове середовище.
8. Спосіб за будь-яким з попередніх пп. 1-7, який відрізняється тим, що реакцію проводять при температурі приблизно від 0 °С до 120 °С.
9. Спосіб за будь-яким з попередніх пп. 1-8, який відрізняється тим, що реакцію проводять, використовуючи біля 1 молярного еквівалента сполуки формули (II), приблизно від 0,95 до 1,0 молярного еквівалента солі ціанистоводневої кислоти і біля 1 молярного еквівалента формальдегідної сполуки.
10. Спосіб за будь-яким з попередніх пп. 1-9, який відрізняється тим, що реакційну суміш підкислюють після реакції ціаноацетату формули (II) з сіллю ціанистоводневої кислоти і формальдегідом.
11. Спосіб за будь-яким з попередніх пп. 1-10, який відрізняється тим, що реакцію проводять в основному у безводних умовах.
12. Спосіб одержання сполуки формули (III):
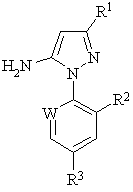 ,
,
(III)
де R1 являє собою ціаногрупу, W являє собою азот або -CR4, R2 і R4 незалежно являють собою галоген, і R3 являє собою галоген, галоїдалкіл, галоїдалкокси або SF5, який включає:
а) взаємодію ціанацетату формули (II)
RO2C-CH2CN,
(II)
де R являє собою алкіл з нормальним або розгалуженим ланцюгом, що містить від 1 до 18 атомів вуглецю, з сіллю ціанистоводневої кислоти і формальдегідом або його джерелом з отриманням сполуки формули (І), як визначено у п. 1, і
б) взаємодію одержаної таким чином сполуки формули (І) з сіллю діазонію сполуки формули (IV):
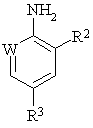 ,
,
(IV)
де W, R2 і R3 визначені вище; з одержанням сполуки формули (V):
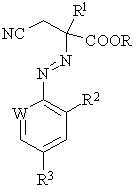 ,
,
(V)
де W, R, R1, R2 і R3 визначені вище; з наступною циклізацією вказаної сполуки формули (V).
13. Спосіб за п. 12, який відрізняється тим, що сполуку стадії (а) реакції оброблюють спиртовим розчином кислоти, переважно неорганічної кислоти.
14. Спосіб за п. 12 або п. 13, який відрізняється тим, що молярне співвідношення сполук формул (II):(IV) складає приблизно від 1,5:1 до 1:4, переважно, приблизно від 1,3:1 до 1:1.
15. Спосіб за п. 12, п. 13 або п. 14, який відрізняється тим, що стадію (а) реакції проводять в основному у безводних умовах.
16. Спосіб за будь-яким з пп. 12-15, який відрізняється тим, що циклізацію здійснюють завдяки гідролізу сполуки формули (V).
17. Сполука формули (V):
 ,
,
(V)
де R визначений вище, R1 являє собою ціаногрупу, W являє собою азот або -CR4, R2 і R4 незалежно являють собою галоген, і R3 являє собою галоген, галоїдалкіл, галоїдалкокси або SF5.
Текст
1 Спосіб одержання сполуки формули (І) ROOC > \ (І) NC CN де R являє собою алкіл з нормальним або розгалуженим ланцюгом, що містить від 1 до 18 атомів вуглецю, або його солі, що включає реакцію ціанацетату формули (II) RO2C-CH2CN (II) де R визначений вище, з сіллю ціанистоводневої кислоти та формальдегідом або джерелом останнього 2 Спосіб за п 1, який відрізняється тим, що сіль ціанистоводневої кислоти являє собою сіль лужного або лужноземельного металу 3 Спосіб за п 2, який відрізняється тим, що сіль ціанистоводневої кислоти являє собою ціанистий натрій або ціанистий калій 4 Спосіб за пп 1, 2 або 3, який відрізняється тим, що R являє собою алкіл з нормальним або розгалуженим ланцюгом, що має від 1 до 6 атомів вуглецю 5 Спосіб за будь-яким з пп 1-4, який відрізняється тим, що сполука формули (II) являє собою етилціаноацетат 6 Спосіб за будь-яким з пп 1-5, який відрізняється тим, що джерелом формальдегіду є параформальдегід 7 Спосіб за будь-яким з пп 1-6, який відрізняється тим, що реакцію проводять у присутності розчинника, що являє собою спиртове середовище 8 Спосіб за будь-яким з попередніх пп 1-7, який відрізняється тим, що реакцію проводять при температурі приблизно від 0 °С до 120 °С 9 Спосіб за будь-яким з попередніх пп 1-8, який відрізняється тим, що реакцію проводять, використовуючи біля 1 молярного еквівалента сполуки формули (II), приблизно від 0,95 до 1,0 молярного еквівалента солі ціанистоводневої кислоти і біля 1 молярного еквівалента формальдегідної сполуки 10 Спосіб за будь-яким з попередніх пп 1-9, який відрізняється тим, що реакційну суміш підкислюють після реакції ціаноацетату формули (II) з сіллю ціанистоводневої кислоти і формальдегідом 11 Спосіб за будь-яким з попередніх пп 1-10, який відрізняється тим, що реакцію проводять в основному у безводних умовах 12 Спосіб одержання сполуки формули (III) R1 О HJST (III) о> де R являє собою ціаногрупу, W являє собою азот або -CR4, R2 і R4 незалежно являють собою галоген, і R3 являє собою галоген, галоідалкіл, галоїдалкокси або SFs, який включає а) взаємодію ціанацетату формули (II) RO2C-CH2CN (II) де R являє собою алкіл з нормальним або розгалуженим ланцюгом, що містить від 1 до 18 атомів вуглецю, з сіллю ціанистоводневої кислоти і формальдепдом або його джерелом з отриманням сполуки формули (І), як визначено у п 1, і б) взаємодію одержаної таким чином сполуки формули (І) з сіллю діазонію сполуки формули (IV) ІО р — ^ _^ ^ J 5Г — 57729 NH (IV) де\Л/, R iR визначені вище, з одержанням сполуки формули (V) R COOR (II) (IV) складає приблизно від 1,5 1 до 1 4, переважно, приблизно від 1,3 1 до 1 1 15 Спосіб за п 12, п 13 або п14, який відрізняється тим, що стадію (а) реакції проводять в основному у безводних умовах 16 Спосіб за будь-яким з пп 12-15, який відрізняється тим, що циклізацію здійснюють завдяки гідролізу сполуки формули (V) 17 Сполука формули (V) R COOR (V) 1 2 (V) 3 де W, R, R , R і R визначені вище, з наступною циклізацією вказаної сполуки формули (V) 13 Спосіб за п 12, який відрізняється тим, що сполуку стадії (а) реакції оброблюють спиртовим розчином кислоти, переважно неорганічної кислоти 14 Спосіб за п 12 або п 13, який відрізняється тим, що молярне співвідношення сполук формул Цей винахід відноситься до способу отримання певних похідних ціанметилпропана та використанню цих сполук у синтезі пестицидів та проміжних сполук (штермедіатів) для пестицидів В W094/21606 описано використання диціанпропюната, що приймає участь у реакції з похідними пара-8Р5-аншна з утворенням в результаті подальшої реакції ціанпіразолів Вперше етил 2,3-диціанпропюнат був отриманий та охарактеризований Гігсон і Торпе (Higson і Thorpe) (JChemSoc 89, 1460 (1906)), які отримали сполуку з гарним виходом (70-81%) завдяки реакції формальдегід ціангідрину з натрієвою сіллю етилового ефіру ціаноцтової кислоти Дикінсон (Dickinson) (J Am Chem Soc 82, 6132 (I960)) повторив цю роботу Цей спосіб отримання дищанпропюнату має серйозний недолік, який заключається у тому, що спочатку необхідно виділити проміжний формальдегід ціангідрин Цей добре розчинний у воді ціангідрин, що отриманий в результаті тривалої безперервної екстракції, характеризується обмеженою стабільністю, часто сильно розкладається при перегонці Окрім того, цю реакцію необхідно проводити з обережністю, оскільки існує ризик утворення димерних побічних продуктів Отримання диціанпропюнатів також описано Вайтлі та Маріанеллі (Whiteley і МапапеІІі) (Synthesis (1978), 392) способом, який дозволяє отримати 2,3-дизаміщені динітрили бурштинової кислоти із ціанацетату, альдепда (алкілальдегід, що містить від 1 до 3 атомів вуглецю, або бензальдегід) та ціаністого калія через 3-заміщені -2,3диціанпропюнати (які не були виділені) Однак, вихід різко зменшується від ізомасляного альдепда до оцтового альдепда Сміт та Горвітц (Smith і Horwitz) (J Am Chem Soc 1949, 71, 3418) описали 1 де R визначений вище, R являє собою ціаногрупу, 4 2 4 W являє собою азот або -CR , R і R незалежно 3 являють собою галоген, і R являє собою галоген, галоідалкіл, галоідалкокси або SFs ідентичну реакцію з кетоном з виходом 70% Ці ВІДОМОСТІ, що ВІДОМІ з рівня техніки, вказують, що вихід покращується із збільшенням розміру групи, що суміжна з карбонільною групою З однієї сторони, даний винахід призначений для створення способу отримання похідних ціанметилпропана, що задовольняє одне або більше з наступних критеріїв запобігти використанню формальдегід ціанпдрина, запобігти побічної реакції димеризацм, отримати цільову сполуку безпосередньо з високим виходом та високим ступенем чистоти Таким чином, даний винахід пропонує спосіб отримання сполуки формули (1) Де R представляє собою алкіл з нормальним або розгалудженим ланцюгом, що має майже до 18 атомів вуглецю, або його сіль, що включає реакцію ціаноацетата формули (II) RO2C-CH2CN (II) де R визначено вище, з сіллю ціаністоводневої кислоти і формальдегідом або джерелом формальдепда Переважно R представляє собою алкіл з нормальним або розгалудженим ланцюгом, що містить від 1 до 6 атомів вуглецю, та найбільш переважно R представляє собою етил Прийнятні солі ціаністоводневої кислоти включають солі металів та органічні солі (наприклад, ціаніди тетра-алкіламонія, такі як ціанід тетрабу 57729 тиламонія) Переважно ціаноацетат формули (II) де Ri представляє собою ціано, W представреагує з лужною або лужноземельною сіллю ціаніляє собою азот або -CR4, R2 і R4 незалежно предстоводневої кислоти, причому солі лужних металів ставляють собою галоген, і R3 представляє собою ціаністоводневої кислоти особливо прийнятні для галоген, галоідалкіл (переважно, трифторметил), використання у даному винаході, особливо ціанісгалоідалкокси (переважно, трифторметокси) або тий натрій Продукт легко може бути виділений у SF5, що включає вигляді солі лужноземельних металів або лужних а) реакцію ціаноацетата формули (II), як виметалів Альтернативно, реакційну суміш підкисзначено вище, із сіллю ціаністоводневої кислоти люють, наприклад, неорганічною кислотою, такою та формальдегідом або джерелом формальдегіду, як сірчаста або хлорводнева кислота, для того, з отриманням формули (І), як визначено вище, і щоб отримати сполуку формули (І) Коли бажаним б) взаємодію отриманої таким чином сполуки є вищезгадана сполука формули (І) (скоріше, ніж формули (І) з діазонієвою сіллю сполуки формули його сіль), ВИСОКИЙ ВИХІД звичайно отримують, ко(IV) ли реакційну суміш підкислюють без додавання води Хоча у реакції можна використати сам формальдегід, він більш зручний для застосування у полімеризованій формі, що відома як параформальдегід, [(НСОН)п], що доступний, наприклад, в (IV) Aldnch Chemical Company Реакцію звичайно проводять, використовуючи 1 молярний еквівалент сполуки формули (II), біля 0 95 до 1 0 молярного еквівалента солі ціаністоводневої кислоти, і біля 1 молярного еквівалента сполуки формальдегіда (відносно сполуки формальдегіда) Реакцію можна проводити у присутності розчинника Переважно, реакцію здійснюють у середовищі розчинника, яка звичайно представляє собою спиртове середовище або диметилформамід (DMF, ДЬФ), N-метилпіролідон (NMP, НМЛ), диоксан, тетрапдрофуран (THF, ТГФ) або диметоксиетан Особливо прийнятними розчинниками є Сі-С6 спирти, такі, як метанол, або більш переважно, безводний етанол Хоча температура реакції не є критичним фактором, реакцію звичайно проводять при температурі від біля 0° до біля 120°С або при темпратурі розчинника, що кипить із зворотнім холодильником Звичайно найкращі результати отримують при введенні формальдепдвмісної сировини після того, як ІНШІ реагенти об'єднані Звичайно реакція протікає за змістом у безводних умовах (треба розуміти, що реакція протікає з утворенням одного еквівалента води), оскільки при тривалій витримці у водних умовах існує ризик, що складно-ефірна група сполуки формули (І) підпаде гідролізу (внаслідок основних умов, що проявляються під час реакції") до відповідної кислоти формули (І) (у якій R замінений воднем) і потім декарбоксилюванню з утворенням 1,2-диціанетану Сполука формули (І) придатна для отримання пестицидно-активних сполук, наприклад, як описано у European Patent Publication Nos 0295117 і 0234119, IW093/06089 Зокрема, спосіб за винаходом може складати частину отримання in situ іншої проміжної сполуки пестицида та іншим аспектом винаходу є спосіб отриманнясполуки формули (III) (in) де W, R2 і R3 мають значення, що визначені вище, з отриманням сполуки формули (V) CO2R (V) де W, R, R-і, R2 і R3 визначені вище, з наступною циклізацією вказаної вище сполуки формули (V) Вищезгадані сполуки формули (V) містять хіральний центр, що дає початок різним енантюмерам, та можуть існувати також у вигляді різних геометричних ізомерів або суміші їх Даний винахід включає усі такі форми У цьому способі сполука (а)- стадії реакції звичайно підкисляють спиртовим розчином неорганічної кислоти, переважно, розчином хлористоводневої кислоти в етанолі Це також забезпечує те, що любий кислий побічний продукт (а)-стадм реакції (що приводить до відповідної сполуки формули (І), у якій R замінений воднем) реестерифікується По цим причинам також є прийнятним те, що у цьому способі (а)-стадія реакції протікає за змістом у безводних умовах (б)-стадію реакції звичайно здійснюють у присутності інертного розчинника, наприклад, води, ацетонітрила, дихлорметану або ДМФ, або, більш переважно, спиртового розчинника (наприклад, метанола або етанола), і необов'язково буферованого (наприклад, ацетатом натрія) Сіль діазонія сполуки формули (IV) отримують, використовуючи діазотуючі агенти, що ВІДОМІ В літературі, і звичайно готують в еквімолярному співвідношенні нітрату натрія та неорганічної кислоти (наприклад, хлористоводневої або сірчастої кислоти) При температурі від біля -10°С до біля 50°С, більш переважно, від біля 0°с до біля 5°С Сіль діазонія сполуки формули (IV) звичайно готують in situ, оскільки розчинники, такі як спирти, мають тенденцію швидко відновлювати солі діазонія У даній реакції солі 57729 сполуки формули (IV) з отриманням вищезгаданої сполуки формули (V) звичайно відбувається швидше, ніж відновлення солі діазонія Наступний гідроліз, переважно, з використанням м'яких умов з основою, такою як водний гідроокис натрія, вуглекислий натрій або амоній, може бути необхідний для ефективності циклізації сполуки формули (V) до сполуки формули (III) Молярне співвідношення сполук формули (II) (IV) звичайно складає від біля 1 5 Ідо біля 1 4, переважно, від біля 1 3 1 до біля 1 1, більш переважно, 1 1 1 Вищезгадані сполуки формул (III) і (IV) описані у літературі, наприклад, див ЕР-А1-0295117 Вищезгадані сполуки формули (V) є новими і, таким чином, складають ще одну ознаку даного винахоДУ Наступні приклади ілюструють винахід Приклад 1 Отримання етил 2,3-дищанпропюната Ціаністий калій (13 0г, 0 2М) перемішують в абсолютному етанолі та додають етил ціаноацетат (22 6г, 0 2М) і параформальдегід (6 0г, 0 2М) при кімнатній температурі Через 5 хвилин білу суспензію нагрівають при КИП'ЯТІННІ ІЗ зворотнім холодильником на протязі 12 хвилин, і жовтогарячий розчин випарюють до сухого стану під вакуумом при температурі нижче 25°С для отримання блідожовтої твердої речовини Речовину (калієва сіль) розчиняють у воді (400мл), підкисляють до рН5 2М розчином хлористоводневої кислоти з отриманням червоного масла (23 5г), 'н ЯМР (CDCI3) d 4 3(2Н, q), 3 95(1 Н, t), З 0(2Н, d), 1 35(ЗН, t), ідентичного з аутентичним зразком Перегнана сполука має точку кипіння 132 - 136°С при 0 5мм нд ВИХІД 77% Порівняльний приклад ВІДПОВІДНО J Chem Soc 89, 1460(1906) Розчин етилата натрія [приготований із натрія (25 2г, 1 15М) і абсолютного етанолу (650мл)] перемішують в інертній атмосфері та оброблюють етилціаноацетатом (127 7мл, 1 2М) понад 20 хвилин Розчин охолоджують до температури нижче 10°С та потім повільно додають до розчину формальдепда ціаногідрин (щойно приготованого, 70г, 0 2М) в абсолютному етиловому спирті (200мл) при 5°С понад 55 хвилин Після витримки на протязі ночі суміш виливають у крижану воду (1л) та підкислюють до рН1 - 2 концентрованою хлористоводневою кислотою Суміш екстрагують дихлорметаном, сушать над безводним сульфатом маг Комп'ютерна верстка С Волобуєв 8 нія та випарюють, отримуючи темно-жовтогаряче масло (150 6г) Залишок переганяють у вакуумі, збираючи названу сполуку (73 6г) у вигляді безкольорового масла, точка кипіння 144 - 148°С/1мбар Вихід 40% Перевага способа винаходу, таким чином, чітко продемонстрована Приклад 2 Спосіб отримання 5-амшо-3-ціан-1-(2,6дихлор-4-трифторметил-феніл) піразола Ціаністий натрій (20г, 0 408М) і етил ціаноацетат (46г, 0 408М) розчиняють в абсолютному етанолі (300 мл) в інертній атмосфері Додають параформальдегід (12 2г, 0 408М), що викликає екзотермію, і температуру підтримують нижче 50°С Потім реакційну суміш перемішують при кімнатній температурі на протязі від 5 до 7 годин, охолоджують до 0° - 5°С і додають спиртовий розчин, що містить хлористий водень (0 45М), підтримуючи температуру нижче 5°С Реакційну суміш залишають на всю ніч і до отриманої таким чином суспензії додають 111 мл розчину хлористоводневої кислоти (0 73М) в етиловому спирті при 5°С При цій температурі додають 2,6-дихлор-4трифторметил-анілін (84 44г, 0 367М) з наступним додаванням нітрату натрія (35 84г, 0 514М), що приводить до утворенняетил-2,3-Диціан-2-[2,6дихлор-4-трифторметилфеніл)азо] пропюната, який можна виділити завдяки колонковій хроматогрфм, еліюючи сумішшю пентан/розчин ефіру, і/або хроматографією в оберненій фазі з розчином ацетонітрил-вода, або видалення етанолу перегонкою, розчинення реакційної суміші в толуолі, промивання розчину толуола водою та випарювання толуола до сухого стану 'н ЯМР (CDCI3) 1 37 (t, ЗН), 3 55 (s, 2H), 4 34 (q, 2H), 7 65 (s, 2H) Газоподібний аміак (9 6г, 0 56М) потім барботують в реакційну суміш при 0°С Етанол випарюють з реакційної суміші при пониженому тиску та концентровану рідину поглинають сумішшю толуолу і етилацетату Цей розчин промивають водою та після концентрування фази толуола при 80°С розчин охолоджують, щоб отримати сполуку у вигляді твердих кристалів, а рідини концентрують та охолоджують для отримання другого збору рекристалізованої сполуки, точка плавління 141 - 142°С (об'єднана вага названої сполуки 87 54г, вихід, відносно вихідного матеріалу - похідного аніліна, складає 78%) Підписано до друку 05 08 2003 Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ТОВ "Міжнародний науковий комітет", вул Артема, 77, м Київ, 04050, Україна
ДивитисяДодаткова інформація
Назва патенту англійськоюA process for preparing 5-amino-1-aryl-3-cyanopyrazoles, an intermediary compound for preparing thereof and a process for preparing the intermediary compound
Автори англійськоюROBERTS David Alan
Назва патенту російськоюСпособ получения 5-амино-1-арил-3-цианопиразолов, промежуточное соединение для их получения и способ получения промежуточного соединения
Автори російськоюРобертс Дэвид Алан
МПК / Мітки
МПК: C07D 231/38, C07D 213/76, C07C 255/19, C07D 213/77, C07C 253/00, C07C 255/65, C07D 401/04, C07C 253/04
Мітки: сполука, проміжної, 5-аміно-1-арил-3-ціанопіразолів, проміжна, одержання, сполуки, спосіб
Код посилання
<a href="https://ua.patents.su/4-57729-sposib-oderzhannya-5-amino-1-aril-3-cianopirazoliv-promizhna-spoluka-dlya-kh-oderzhannya-ta-sposib-oderzhannya-promizhno-spoluki.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 5-аміно-1-арил-3-ціанопіразолів, проміжна сполука для їх одержання та спосіб одержання проміжної сполуки</a>
Попередній патент: Закупорювальний пристрій
Наступний патент: Закупорювальний пристрій
Випадковий патент: Привід круглов`язальної машини








