Похідні 6-метил-2,4-дигідроксипіримідин-5-сульфонаміду і спосіб їх одержання
Номер патенту: 75516
Опубліковано: 17.04.2006
Автори: Потапенко Едуард Володимирович, Ісак Олександр Дем'янович, Погорєлова Ірина Петрівна
Формула / Реферат
1. Похідні 6-метил-2,4-дигідроксипіримідин-5N-сульфонаміду загальної формули
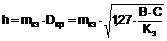 ,
,
де R - 2-СН3 (Іа); 3-СН3 (Іb); 4-СН3 (Іс); 2-СН3О (Id); 4-СН3О (Іе); 4-С3Н5О (If); 4-Сl (Ig); 4-Br (Ih); 4-F (Ii); 4-(C2H5)2N (Ij); 2-COOH (Ik); 2-СООСН3 (Іl); 4-NH2SO2 (Im); 2-СF3 (Іn); 3-СF3 (Іо); 4-СF3 (Ір); 4-СН3-3-СF3 (Iq); 4-NO2-3-СF3 (Ir); 2-NO2 (Is); 3-NO2 (It); 4-NO2 (Iu).
2. Спосіб одержання похідних 6-метил-2,4-дигідроксипіримідин-5-сульфонаміду, при якому проводять взаємодію 6-метил-2,4-дигідроксипіримідин-5-сульфохлориду з аміном у розчиннику в присутності основи при перемішуванні, який відрізняється тим, що основу для нейтралізації хлороводню додають після закінчення взаємодії реагентів, як аміни використовують толуїдини, анізидини, фенетидини, n-діетиламіноанілін, нітроаніліни, галогенаніліни, трифторметиланіліни, а взаємодію 6-метил-2,4-дигідроксипіримідин-5-сульфохлориду з амінами проводять у водному середовищі або в органічному розчиннику.
3. Спосіб за п. 2, який відрізняється тим, що як основи використовують, наприклад, гідроксид натрію, поташ, піридин, ацетат натрію.
Текст
1. Похідні 6-метил-2,4-дигідроксипіримідин5N-сульфонаміду загальної формули 2 C2 1 3 75516 4 де R= 2-СН3 (Іа); 3-СН3 (Ib); 4-СН3 (Іс); 2-СН3О рою. (Id); 4-СН3О (Ie); 4-C2H5O (If); 4-С1 (Ig); 4-Br (Ih); 4Проведення реакції в органічному розчиннику F (Ii); 4-(C2H5)2N (Ij); 2-COOH (Ik); 2-СООСН3 (Іl); 4має перевагу ще і в тому, що органічний розчинник NH2SO2 (Im); 2-СF3 (In); 3-СF3 (Ιο); 4-СF3 (Ір); 4легко регенерується і його можна повторно викоСН3-3-СF3 (Iq); 4-NO2-3-СF3 (Іr); 2-NO2 (Is); 3-NO2 ристовувати в подальшому синтезі. Цим самим (It); 4-NO2 (Iu); зменшується кількість стічних вод виробництва. Отримують сполуки I (a-u) за схемою: Будова отриманих сполук підтверджена даними елементного аналізу (Таблиця 1) та ПМРHO N CH R HO N CH спектрами, а їх індивідуальність та чистота визнаOH O + O N чалася за допомогою тонкошарової хроматографії t C N S HN S N Cl HO O H з використанням сілуфолу. HO O Запропоновані нові сульфонаміди містять у II III (a-u) I (a-u) своєму складі залишок 6-метил-2,4дигідроксипіримідину (6-метилурацилу), циклічна Взаємодію 6-метил-2,4-дигідроксипіримідин-5частина якого входить до складу нуклеїнових киссульфохлориду (II) з амінами (ІІІа-u) проводять у лот і тому для живих організмів він не є токсичним. водному середовищі, або в середовищі органічних Приклади, які ілюструють винахід. розчинників. У випадку використання рідких амінів Приклад 1 (прототип). 6-Метил-2,4(анілін, о-толуїдин, м-толуїдін, n-фенетидин, nдигідроксипіримідин-5-сульфоніланілід. фторанілін, метиловий ефір антранілової кислоти В 10 мл 20%-ного розчину поташу старанно та ін.) взаємодію сульфохлориду з амінами проворозмішують 1,4 г (0,015 моль) аніліну. До отримадять, як у водному середовищі при температурі 5ної емульсії при розмішуванні придають 2,24 г 10°С, так і в органічному розчиннику при темпера(0,010 моль) 2,4-дигідрокси-6-метил-5турі 25-30°С, а потім для завершення реакції реакпіримідинсульфохлориду (ІІ). Через 30 хвилин роційну масу нагрівають протягом 30-45 хвилин на змішування розчин фільтрують і знебарвлюють водяній бані при температурі 75-80°С. З іншими активованим вугіллям. При підкисленні отриманого амінами, що не розчинні у воді, взаємодію сульрозчину виділяють 0,80 г (28%) 6-Метил-2,4фохлориду II з амінами III проводять переважно дигідроксипіримідин-5-сульфоніланіліду, Тпл 237при температурі 75-85°С в органічному розчинни23 С (після перекристалізації із суміші метанолку. Проведення синтезу у воді при пониженій тембензол). пературі (5-10°С) дає змогу уникнути прискореного Приклад 2. N5-(2-Метилфеніл}-2,4-дигідроксигідролізу вихідного сульфохлориду і таким чином 6-метил-5-піримідинсульфонамід (Іа). підвищити вихід кінцевого продукту. В ролі органіВ 25 мл води вносять 1,2 мл (1,2 г, 0,011 моля) чних розчинників використовують, наприклад, ацесвіжоперегнанного о-толуїдину (ІІІа). До отриманої тон, діоксан, метилетилкетон, ДМСО, ДМФА, бенемульсії протягом 30 хвилин при температурі 0зол, толуол, хлорбензол, піридин, 5°С і інтенсивному розміщуванні невеликими портетрагідрофуран, оцтову кислоту та ін. ціями придають 2,25 г (0,010 моля) 2,4-дигідроксиДля зв'язування хлороводню, що виділяється 6-метил-5-піримідинсульфохлориду (ІІ). Потім реапід час взаємодії сульфохлориду з амінами викокційну масу розмішують при кімнатній температурі ристовують основи, наприклад, гідроксид калію протягом 45-60 хвилин до зникнення сульфохлоабо натрію, поташ, ацетат натрію, кальціновану риду. Під кінець витримки до реакційної маси присоду, піридин та ін. Основи додають у еквівалентдають 0,76 г (0,0055 моля) поташу для зв'язування ній кількості до реакційної маси тільки після зникхлороводню, що виділився під час реакції онення вихідного сульфохлориду. Такий порядок толуїдину і 2,4-дигідрокси-6-метил-5введення реагентів (з метою уникнення гідролізу піримідинсульфохлориду. При охолоджені в бані з сульфохлориду) збільшує вихід цільового продукту льодом і сіллю випадають білі кристали, які відфів 2-3 рази у порівнянні з відомим способом. льтровують, промивають спиртом і сушать. ОтриКінець реакції контролюють за допомогою тонмано 2,37 г (91,3% теоретичного) N5-(2-метилкошарової хроматографії на сілуфолі у системах: феніл)]-2,4-дигідрокси-6-метил-5етилацетат, етанол, хлороформ : метанол - 10:1, піримідинсульфонамід (Іа). Тпл 238-239°С ( з води) або по зникненню з реакційної маси вихідного . ароматичного аміну, використовуючи реакцію діаЕлементний аналіз та фізико-хімічні властивозотування та азосполучення (проба на витік). сті (Іа) наведено в таблиці 1. Після закінчення реакції масу розбавляють 2В аналогічних умовах отримано: 3-хкратною кількістю води (у випадку використання N5-(3-Meтилфeніл)-2,4-дигiдpoкcи-6-мeтил-5розчинників, що змішуються з водою - ацетон, діопіримідин-cyлъфoнамiд (Іb); ксан, ДМСО, ДМФА, N-метилпіролідон, піридин, N5-(3-Meтоксифeніл)-2,4-дигiдpoкcи-6-мeтилоцтова кислота). При використанні органічних роз5-піримідин-cyлъфoнамiд (Іd); чинників, що не змішуються з водою (дихлоретан, N5-(3-Діетиламінофeніл)-2,4-дигiдpoкcи-6хлороформ, бензол, толуол, хлорбензол, омeтил-5-піримідин-cyлъфoнамiд (Іj); дихлорбензол), після закінчення реакції масу підФізико-хімічні властивості та елементний анакислюють соляною або оцтовою кислотою до рН 5ліз отриманих сполук наведено в табл. 1. 6 і розчинник відганяють з водяною парою. НерозПриклад 3. 6-Метил-2,4-дигідрокситримідин-5чинені у воді сульфонаміди відділяють фільтру(N-n-толіл)сульфоніламід (Іс). ванням, а розчинені сульфонаміди - частковим В 25 мл діоксану розчиняють 1.34 г (0,0125 випаруванням водного розчину, що утворився пісмоля) свіжоперегнанного n-толуїдину (ІІІс) (Ткип ля відгонки органічного розчинника з водяною па3 3 2 5 75516 6 100-102°С/25 мм.рт.ст.). До отриманого розчину трифторметиланіліну (ІІІn) (0,012 моля) і придають аміну (ІІІd) невеликими порціями протягом 30-40 2,25 г (0,010 моля) (II). Реакційну масу нагрівають хвилин придають 2,25 г (0,010 моля) 2,4до 75 С, придають 0,95 г (0,012 моля) розтертого в дигідрокси-6-метил-5-піримідинсульфохлориду (І). порошок безводного ацетату натрію. Реакційну Реакційну масу розмішують 30-40 хвилин при кіммасу при розмішуванні нагрівають протягом 2,5-3 натній температурі (до відсутності метилурацилгод. при температурі 75-80°C (до зникнення сульсульфохлориду (І) по хроматограмі на сілуфолі). фохлориду по хроматограмі на силуфолі, система Після закінчення витримки реакційну масу протя- етилацетат). Після закінчення витримки реакційгом 15-20 хвилин нагрівають на водяній бані при ну масу розбавляють рівним об'ємом води. Насту90-95°С. Під кінець витримки до реакційної маси пного дня відфільтровують осадок (In). придають розчин 0,95 г (0,012 моля) безводного Отримано 3,28 г In (94,0% теоретичного), безацетату натрію в 5 мл води. Після охолодження барвні іголчаті кристали. Тпл 283-284°С (з АсОН). відфільтровують кристали 6-метил-2,4В аналогічних умовах отримано: дигідроксипіримідин-5-(N-n-толіл)сульфаніламіду N5-(2-метоксикарбонілфеніл)-2,4-дигідрокси-6(Іс), що випали, промивають декілька раз невелиметил-5-піримідинсульфонамід (Il); кими порціями води, потім спиртом і висушують. N5-(3-трифторметилфеніл)-2,4-дигідрокси-6Отримано 2,61 г Іс (88,5 % теоретичного), Тпл метил-5-піримідинсульфонамід (Iо); 245-246°С (з води). N5-(4-трифторметилфеніл)-2,4-дигідрокси-6Елементний аналіз та фізико-хімічні властивометил-5-піримідинсульфонамід (Iр); сті Іс наведено в таблиці 1. N5-(3-трифторметил-4-нітрофеніл)-2,4В аналогічних умовах отримано: дигідрокси-6-метил-5-піримідинсульфонамід (Ir). N5-(4-Meтoкcифeніл)-2,4-дигiдpoкcи-6-мeтилФізико-хімічні властивості та елементний ана5-піримідинcyльфoнaмiд (Іе); ліз отриманих сполук наведено в табл. 1. N5-(4-Етоксифeніл)-2,4-дигiдpoкcи-6-мeтил-5Приклад 6. N5-(о-Карбоксифеніл)-6-метил-2,4піримідинcyльфoнaмiд (Іf); дигідроксипіримідии-5-сульфонамід (Іk). N5-(4-Діетиламінофeніл)-2,4-дигiдpoкcи-6В 20 мл безводного тетрагідрофурану розчимeтил-5-піримідинcyльфoнaмiд (Іj); няють 1,5 г (0,012 моля) антранілової кислоти (ІІк) і N5-(2-метоксикарбоніл)-2,4-дигiдpoкcи-62,25 г (0,010 моль) сульфохлориду (І). Реакційну мeтил-5-піримідинcyльфoнaмiд (Іl). масу розмішують протягом 3,5-5 год. при кімнатній Фізико-хімічні властивості та елементний анатемпературі (до зникнення сульфохлориду по тонліз отриманих сполук наведено в табл. 1. кошаровій хроматографії на сілуфолі, система: Приклад 4. N5-(4-хлорфеніл)-6-метилурацилетилацетат, етиловий спирт-ректифікат). Наступ5-сульфонамід (Ig). ного дня реакційну масу розбавляють рівним об'єВ 20 мл сухого піридину розчиняють 1,35 г мом води, піридин відганяють з водяною парою. (0,0106 моля) n-хлораніліну. Розчин охолоджують Осадок відфільтровують, промивають 50%-ним до 0-3°С. До отриманого розчину протягом 30-40 етиловим спиртом (2-3 рази по 5 мл спирту) і вихвилин невеликими порціями при інтенсивному сушують. перемішуванні придають 2,25 г (0,010 моль) 2,4Отримано 2,40 г Ік (74,4% теоретичного), дигідрокси-6-метил-5-піримідинсульфохлориду (І), Тпл>350°С (з АсОН). підтримуючи температуру в межах 0-5°С. Потім Фізико-хімічні властивості та елементний анареакційну масу протягом 30-40 хвилин нагрівають ліз отриманих сполук наведено в табл. 1. на водяній бані (до зникнення вихідного метилураПриклад 7. N5-{4-нiтpoфeнiл)-6-Meтил-2,4цилсульфохлориду по хроматограмі на сілуфолі). дигiдpoкcипіpимiдин-5-сульфонамід (Ιu) Після закінчення витримки реакційну масу охолоВ 30 мл ледяної оцтової кислоти розчиняють джують до 10-15°С , розбавляють 4-хкратною кіль1,45 г (0,015 моля) n-нітроаніліну (IIu) і 2,25 г (0,010 кістю води, розчин знебарвлюють активованим моля) метилурацилсульфохлориду (11). Вміст ковугіллям і випаровують до об'єму 15 мл. Наступнолби при розмішуванні нагрівають на паровій бані го дня відфільтровують осадок (Ig), промивають протягом 4,5-5 год. (до зникнення сульфохлориду декілька раз водою і висушують. по хроматограмі на сілуфолі). По закінченні виОтримано 2,1 г безбарвних кристалів Ig (74,8% тримки до реакційної маси придають 0,90 г безвотеоретичного), Тпл 276-277°С (з оцтової кислоти). дного ацетату натрію, або еквівалентну кількість Елементний аналіз та фізико-хімічні властивопоташу. Розчин розбавляють водою (до появи сті Ig наведено в таблиці 1. В аналогічних умовах помутніння розчину) і залишають для повільного отримано: охолодження та кристалізації. Наступного дня віN5-(4-Бромфеніл)-2,4-дигідрокси-6-метил-5дфільтровують кристали, промивають декілька раз піримідинcyльфoнaмiд (Ib), водою і отриманий осадок (Iu) висушують. N5-(4-Фторфеніл)-2,4-дигідрокси-6-метил-5Отримано 2,94 г Ιu (88,0% теоретичного), світпіримідинcyльфoнaмiд (Iі), ло-жовті іголчаті кристали, Tпл 242-243°С (з АсОН). 4-(2,4-Дигідрокси-6-метил-5В аналогічних умовах отримано: піримідинcyльфoнaмiдо)-1-бензолсульфонамід N5-(2-нитpoфeніл}-2,4-дигiдpoкcи-6-мeтил-5(Im). піримiдинcyльфoнамiд (Іо); Фізико-хімічні властивості та елементний анаN5-(3-нитpoфeніл}-2,4-дигiдpoкcи-6-мeтил-5ліз отриманих сполук наведено в табл. 1. піримiдинcyльфoнамiд (Іо); Приклад 5. N5-{2-трифторметилфеніл)-2,4N5-(4-метил-2-трифторметилфeніл}-2,4дигідрокси-6-метил-5-піримідинсульфонамід (Іn). дигiдpoкcи-6-мeтил-5-піримiдинcyльфoнамiд (Іq). В 15 мл ДМСО розчиняють 1,15 г оФізико-хімічні властивості та елементний ана 7 75516 8 ліз отриманих сполук наведено в табл. 1. вують до об'єму 10 мл і залишають для охолоПриклад 8. N5-(4-Етоксифеніл)-6-Метил-2,4дження. Кристали (If), що випали в осад, фільтрудигідроксипіримідин-5-сульфонамід (If) ють, добре відсмоктують і сушать. В 50 мл сухого бензолу (хлорбензолу) розчиОтримано 2,84 г (86,5% теоретичного) (If), няють 2,25 г (0,010 моля) І. До отриманого розчину безбарвні іголчаті кристали, Тпл 237-238°С (з водсульфохлориду при охолодженні (5-10°С) невелиного спирту). кими порціями при розмішуванні придають 1,45 г ( В аналогічних умовах отримано: 0,011 моля) n-фенетидину (ІІІf). Вміст колби розN5-(4-метоксифеніл)-2,4-дигідрокси-6-метил-5мішують 1,5-2 години на холоду. Потім отриману піримідинсульфонамід (Іе), реакційну масу протягом 30-45 хвилин нагрівають N5-(3-нитрофеніл)-2,4-дигідрокси-6-метил-5при 70-75°С. По закінченню витримки до реакційпіримідинсульфонамід (Іо), ної маси придають розчин ацетату натрію (0,95 г N5-(4-метил-2-трифторметилфеніл)-2,4безводного ацетату натрію, або еквівалентну кільдигідрокси-6-метил-5-піримідинсульфонамід (Іq). кість тригідрату в 10 мл води). Розчинник відганяФізико-хімічні властивості та елементний анають з водяною парою. Отриманий розчин випароліз отриманих сполук наведено в табл. 1. Таблиця 1 Фізико-хімічні властивості 6-метилурацил-(N-арил)сульфонамидов Сполука Іа Іb Іс Id Ie If Іg Ih Іі Ij Ik Il Im In Ιο ip Iq Ir Is It lu Вихід, % 2-СН3 3-СН3 4-СН3 2-ОСН3 4-ОСН3 4-OC2H5 4-Сl 4-Вr 4-F 4-(С2Н5)2Н 2-СООН 2-СООСН3 4-H2NSO2 2-CF3 3-CF3 4-СF3 4-СН3-2-СF3 4-NO2-3-CF3 2-NO2 3-NO2 4-NO2 Τпл, С 91,3 76,4 88,5 94,6 90,3 86,5 74,8 82,5 72,1 89,6 74,4 89,7 68,8 94,0 89,5 92,1 80,0 64,8 84,8 92,5 88,0 238-239 201-202 245-246 224-225 267-268 237-238 276-277 327-328 279-280 286-287 >350 305-307 >350 283-284 225-226 195-196 292-293 251-252 275-278 266-267 242-243 Комп’ютерна верстка М. Клюкін С 48,71 48,84 48,68 46,25 46,17 48,16 41,63 36,89 44,01 51,08 44,13 45,89 36,42 41,05 41,12 41,08 42,71 36,82 40,28 40,32 40,61 Знайдено Η N 4,02 14,35 4,15 14,15 4,00 14,24 3,81 13,69 3,71 13,74 4,73 13,19 4,78 13,17 2,68 11,75 3,45 14,25 5,61 16,18 3,51 13,14 3,92 12,54 3,24 15,71 2,81 12,23 2,75 11,93 2,81 12,18 3,24 11,74 2,47 14,09 3,01 17,26 3,11 17,34 3,03 19,29 S 11,02 11,12 11,04 10,54 10,62 10,09 10,34 9,14 11,06 10,06 10,11 9,25 17,98 9,36 9,45 9,27 9,05 8,58 10,18 10,10 10,15 Формула C12H12N3O4S C12H12N3O4S C12H12N3O4S C12H12N3O5S C12H12N3O5S C13H15N3O5S C11H10ClN3O4S C11H10BrN3O4S C11H10FN3O4S C15H20N4O4S C12H11N3O6S C13H13N3O6S C11H12N4O6S2 C12H10F3N3O4S C12H10F3N3O4S C12H10F3N3O4S C13H12F3N3O4S C12H9F3N4O6S C11H10N4O6S C11H10N4O6S C11H10N4O6S Підписне С 48,97 48,97 48,97 46,45 46,45 48,29 41,84 36,68 44,15 51,27 44,31 46,02 36,66 41,26 41,26 41,26 42,98 36,55 40,49 40,49 40,49 Вирахувано Η N 4,11 14,27 4,11 14,27 4,11 14,27 3,89 13,54 3,89 13,54 4,67 12,99 3,19 13,31 2,80 11,67 3,37 14,04 5,73 15,94 3,41 12,92 3,86 12,38 3,36 15,55 2,88 12,03 2,88 12,03 2,88 12,03 3,33 11,56 2,30 14,21 3,09 17,17 3,09 17,17 3,09 17,17 Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 S 10,89 10,89 10,89 10,33 10,33 9,91 10,15 8,90 10,71 9,12 9,85 9,45 17,79 9,18 9,18 9,18 8,82 8,31 9,82 9,82 9,82
ДивитисяДодаткова інформація
Назва патенту англійською6-methyl-2,4-dihydroxypyrimidine -5-sulfonamide derivatives and a method for the preparation thereof
Автори англійськоюPohorielova Iryna Petrivna, Isak Oleksandr Demianovych
Назва патенту російськоюПроизводные 6-метил-2,4-дигидроксипиримидин-5-сульфонамида и способ их получения
Автори російськоюПогорелова Ирина Петровна, Исак Александр Демьянович
МПК / Мітки
МПК: A61P 31/12, A61K 31/505, A61P 31/04, C07D 239/69
Мітки: спосіб, 6-метил-2,4-дигідроксипіримідин-5-сульфонаміду, похідні, одержання
Код посилання
<a href="https://ua.patents.su/4-75516-pokhidni-6-metil-24-digidroksipirimidin-5-sulfonamidu-i-sposib-kh-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Похідні 6-метил-2,4-дигідроксипіримідин-5-сульфонаміду і спосіб їх одержання</a>
Попередній патент: Спосіб сумісного визначення параметрів капілярних сил на межі розділу фаз
Наступний патент: Шлакоутворююча суміш
Випадковий патент: Двигун внутрішнього згоряння








