Спосіб синтезу (2s)-індолін-2-карбонової кислоти і застосування у синтезі периндоприлу
Формула / Реферат
1. Спосіб синтезу (2S)-індолін-2-карбонової кислоти формули (І):
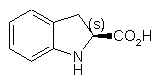 , (I)
, (I)
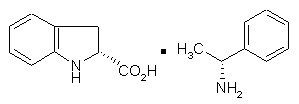
який відрізняється тим, що рацемічну індолін-2-карбонову кислоту формули (IIІ):
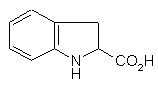 , (III)
, (III)
піддають реакції з хіральним аміном з тим, щоб одержати сіль формули (IV):
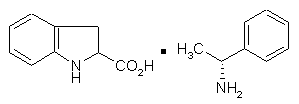 , (IV)
, (IV)
яку відфільтровують, і виділяють:
з одного боку, (2S) ізомер формули (IVa):
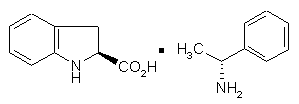 , (IVa)
, (IVa)
у формі кристалів,
сполуку формули (IVa) потім обробляють хлористоводневою кислотою з тим, щоб одержати сполуку формули (І),
і з іншого боку, суміш (2S) ізомеру формули (IVa) і (2R) ізомеру формули (IVb), в якій (2R) ізомер переважає:
 , (IVb)
, (IVb)
шляхом випаровування фільтрату,
суміш потім обробляють хлористоводневою кислотою з тим, щоб одержати суміш (2R)-індолін-2-карбонової кислоти і (2S)-індолін-2-карбонової кислоти, в якій (2R) кислота переважає,
яку рацемізують реакцією з розчином гідроксиду натрію,
при температурі від 140 до 200°С,
під тиском від 5 до 15 бар,
з тим, щоб одержати, після виділення, сполуку формули (III), з якою повторюють ряд операцій, які описуються вище,
потім, після проведення від 2 до 6 циклів, всі складові одержання сполуки формули (І), об'єднують.
2. Спосіб синтезу (2S)-індолін-2-карбонової кислоти формули (І):
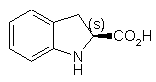 , (I)
, (I)
який відрізняється тим, що піддають реакції (2R)-індолін-2-карбонову кислоту формули (V):
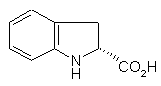 , (V)
, (V)
яку рацемізують реакцією з розчином гідроксиду натрію,
при температурі від 140 до 200°С,
під тиском від 5 до 15 бар,
з тим, щоб одержати, після виділення, сполуку формули (III):
 , (III)
, (III)
яку піддають реакції з хіральним аміном з тим, щоб одержати сіль формули (IV):
 , (IV)
, (IV)
яку відфільтровують, і виділяють:
з одного боку, (2S) ізомер формули (IVa):
 , (IVa)
, (IVa)
у формі кристалів,
сполуку формули (IVa) потім обробляють хлористоводневою кислотою, з тим, щоб одержати сполуку формули (І),
і з іншого боку, суміш (2S) ізомеру формули (IVa) і (2R) ізомеру формули (IVb), в якій (2R) ізомер переважає:
 , (IVb)
, (IVb)
шляхом випаровування фільтрату,
суміш потім обробляють хлористоводневою кислотою, з тим, щоб одержати суміш (2R)-індолін-2-карбонової кислоти і (2S)-індолін-2-карбонової кислоти, в якій (2R) кислота переважає,
з якою повторюють, якщо бажано, ряд операцій, описаних вище,
потім, після проведення від 1 до 6 циклів, всі складові, одержані зі сполуки формули (І), об'єднують.
3. Спосіб синтезу за п. 1 або 2, який відрізняється тим, що хіральний амін являє собою (R) – a – метилбензиламін .
4. Спосіб синтезу периндоприлу або його фармацевтично прийнятних солей, починаючи зі сполуки формули (І), який відрізняється тим, що вказану сполуку формули (І) одержують відповідно до способу за будь-яким з пп. 1-3.
Текст
1. Спосіб синтезу (2S)-індолін-2-карбонової кислоти формули (І): 3 N H 80040 (III) CO2H , яку піддають реакції з хіральним аміном з тим, щоб одержати сіль формули (IV): N H CO2H . H 3C (IV) NH 2 , яку відфільтровують, і виділяють: з одного боку, (2S) ізомер формули (IVa): N H . CO 2H H 3C (IVa) NH2 , у формі кристалів, сполуку формули (IVa) потім обробляють хлористоводневою кислотою, з тим, щоб одержати сполуку формули (І), і з іншого боку, суміш (2S) ізомеру формули (IVa) і (2R) ізомеру формули (IVb), в якій (2R) ізомер переважає: Даний винахід відноситься до способу синтезу (2S)-індолін-2-карбонової кислоти, і до застосування у синтезі периндоприлу і його фармацевтично прийнятних солей. Більш конкретно, даний винахід відноситься до нового способу промислового синтезу (2S)індолін-2-карбонової кислоти формули (І): (I) Сполука формули (І), одержана відповідно до способу за даним винаходом, є корисною у синтезі периндоприлу формули (II): (II) і у синтезі його фармацевтично прийнятних солей. Периндоприл і його солі володіють цінними фармакологічними властивостями. Їх головною властивістю є інгібування ангіотензин І перетворюючого ферменту (або кіназа II), що дозволяє, з одного боку, запобігти перетворенню декапептид ангіотензину І на октапептид ангіотензин II (вазоконстриктор) і, з іншого боку, запобігти деградації брадикініну (вазодилататор) до пасивного пептиду. 4 N H CO2H . H 3C (IVb) NH 2 , шляхом випаровування фільтрату, суміш потім обробляють хлористоводневою кислотою, з тим, щоб одержати суміш (2R)-індолін-2карбонової кислоти і (2S)-індолін-2-карбонової кислоти, в якій (2R) кислота переважає, з якою повторюють, якщо бажано, ряд операцій, описаних вище, потім, після проведення від 1 до 6 циклів, всі складові, одержані зі сполуки формули (І), об'єдн ують. 3. Спосіб синтезу за п. 1 або 2, який відрізняється тим, що хіральний амін являє собою (R) – a – метилбензиламін . 4. Спосіб синтезу периндоприлу або його фармацевтично прийнятних солей, починаючи зі сполуки формули (І), який відрізняється тим, що вказану сполуку формули (І) одержують відповідно до способу за будь-яким з пп. 1-3. Ці дві дії сприяють корисним впливам периндоприлу на серцево-судинні захворювання, більш конкретно на артеріальну гіпертензію і параліч серця. Периндоприл, його одержання і його застосування у лікуваннях розкриті [в описі Європейського патенту ЕР 0 049 658]. Беручи до уваги фармацевтичне значення цієї сполуки, було важливим спромогтись одержати проміжну сполуку формули (І) ефективним способом синтезу, який дозволяє одержати (S) енантіомер селективно з дуже хорошим виходом і з відмінною чистотою. Деякі способи для одержання сполуки формули (І) вже відомі. Так, [патентні описи ЕР 0 308 339 і ЕР 0 308 341] розкривають одержання (2S)-індолін-2карбонової кислоти шляхом розщеплення рацемічної індолін-2-карбонової кислоти, використовуючи (R)-a-метилбензиламін. (R)-a-метилбензиламінна сіль (2S)-індолін-2-карбонової кислоти виділяють фракційною кристалізацією, потім окислюють з тим, щоб одержати сполуку формули (І). Такий спосіб має перевагу використання вихідного матеріалу і реагентів, які мають розумну ціну і дуже легко доступні. З іншого боку, ви хід сполуки формули (І), використовуючи такий спосіб, складає тільки 35%. Заявник на даний момент розробив спосіб синтезу сполуки формули (І), в якій (2R) ізомер, який утворюється протягом протікання реакції розщеплення, використовують повторно. Спосіб, розроблений таким чином, робить можливим одержання сполуки формули (І) з виходом, починаючи з рацемічної індолін-2-карбонової кислоти, що знахо 5 80040 диться в діапазоні від 50% до 70%, відповідно до кількості операцій повторного використання, які проводяться. Більш конкретно, даний винахід відноситься до способу синтезу сполуки формули (І), який відрізняється тим, що рацемічну індолін-2-карбонову кислоту формули (III): (III) 6 (VI) дозволяє одержати периндоприл формули (II) з дуже задовільною чистотою і виходом. Даний винахід відноситься також до варіанту вищезазначеного способу, в якому піддають реакції (2R)-індолін-2-карбонову кислоту формули (V): піддають реакції з хіральним аміном з тим, щоб одержати сіль формули (IV): (V) (IV) яку відфільтровують, і виділяють: - з одного боку, (2S) ізомер формули (IVa): яку рацемізують реакцією з розчином гідроксиду натрію, при температурі від 140 до 200°С, під тиском від 5 до 15 бар, з тим, щоб одержати, після виділення, сполуку формули (III): (IVa) у формі кристалів, сполуку формули (IVa) потім обробляють хлористоводневою кислотою з тим, щоб одержати сполуку формули (І), - і з іншого боку, суміш (2S) ізомеру формули (IVa) і (2R) ізомеру формули (IVb), в якій (2R) ізомер переважає: (IVb) шляхом випаровування фільтрату, суміш потім обробляють хлористоводневою кислотою з тим, щоб одержати суміш (2R)-iндoлiн2-кapбoнoвoї кислоти і (2S)-індолін-2-карбонової кислоти, в якій (2R) кислота переважає, яку рацемізують реакцією з розчином гідроксиду натрію, при температурі від 140 до 200°С, під тиском від 5 до 15 бар, з тим, щоб одержати, після виділення, сполуку формули (III), з якою повторюють ряд операцій, які описуються вище, потім, після проведення від 2 до 6 циклів, всі складові, одержані зі сполуки формули (І), об'єднують. Сполуку формули (І) таким чином одержують з виходом, що варіює від 50% до 70%, відповідно до кількості проведених циклів. Її хімічна і енантіомерна чистота дуже хороша, що робить її застосування у синтезі периндоприлу формули (II) особливо переважним. З метою ілюстрації, каталітична гідрогенізація сполуки формули (І), одержаної відповідно до способу винаходу, з наступним зв'язуванням (2S,3aS,7aS)-пергідроіндол-2-карбонової кислоти, одержаної таким чином, зі сполукою формули (VI): (III) яку піддають реакції з хіральним аміном з тим, щоб одержати сіль формули (IV): (IV) яку відфільтровують, і виділяють: - з одного боку, (2S) ізомер формули (IVa): (IVa) у формі кристалів, сполуку формули (IVa) потім обробляють хлористоводневою кислотою, з тим, щоб одержати сполуку формули (І), - і з іншого боку, суміш (2S) ізомеру формули (IVa) і (2R) ізомеру формули (IVb), в якій (2R) ізомер переважає: (IVb) шляхом випаровування фільтрату, суміш потім обробляють хлористоводневою кислотою, з тим, щоб одержати суміш (2R)-iндoлiн2-кapбoнoвoї кислоти і (2S)-індолін-2-карбонової, в якій (2R) кислота переважає, з якою повторюють, якщо бажано, ряд операцій, описаних вище, потім, після проведення від 1 до 6 циклів, всі складові, одержані зі сполуки формули (І), об'єднують. Серед хіральних амінів, які можуть бути використані у способі відповідно до даного винаходу, 7 80040 або можуть бути згадані їх варіанти, без будьякого обмеження, (R)-a-метилбензиламін, 1-(1нафтил)-етиламін, ефедрин, a-хімотрипсин, вторбутиламін, 1-аміно-2-метилбутан, Ν,Ν-диметил-1фенілетиламін, 1-циклогексилетиламін, циклосерин, 2-(метоксиметил)-піролідин, a-диметиламіноє -капролактам, ізобороніламін, 1-(4-нітрофеніл)етиламін, a-аміно- є -капролактам, 2-аміно-1бутанол, 1-аміно-2-пропанол, цинхонідин, цилхонін, N-метил-ефедрин, фенілаланінол, хінідин, валінол, феніл-гліцинол, лейцинол. Переважним хіральним аміном є (R)-aметилбензиламін. "Суміш, в якій (2R) переважає", як повинно бути зрозумілим, означає суміш (2R) і (2S) ізомерів, в якій (2R) ізомер складає більшу частин у суміші. Приклад, наведений нижче, ілюструє винахід. Приклад: (2S)-індолін-2-карбонова кислота Стадія А: Розщеплення рацемічної індолін-2карбонової кислоти 3,7кг (R)-a-метилбензиламіну додають до розчину 5кг індолін-2-карбонової кислоти в етанолі і потім суміш перемішують протягом 2год. і фільтрують. Стадія А1: (2S)-індолін-2-карбонова кислота Білий осад, зібраний на Стадії А, перекристалізовують з ізопропанолу і потім розчиняють в 13 літрах води, і додають 12 літрів розчину 1N хлористоводневої кислоти. Після перемішування протягом 2год., осад відфільтровують і потім промивають і сушать з тим, щоб одержати (2S)-індолін-2карбонову кислоту ("перша складова") у формі кристалів (1,80кг) з хімічною чистотою 98% і енантіомерною чистотою більшою, ніж 99,5%. Стадія А2: Індолін-2-карбонова кислота (суміш, в якій (2R) переважає) Фільтрат, зібраний на Стадії А, випаровують і одержаний залишок розчиняють в 13 літрах води і потім додають 12 літрів розчину 1N хлористоводневої кислоти. Після перемішування протягом Комп’ютерна в ерстка Т. Чепелев а 8 2год., осад відфільтровують і потім промивають і сушать з тим, щоб одержати індолін-2-карбонову кислоту у формі суміші (2R) і (2S) енантіомерів (2,6кг), в якій (2R) енантіомер переважає. Стадія В: Рацемізація В автоклав вміщують осад, одержаний на Стадії А2, (2,6кг), і потім 12 літрів води і 3,1 літрів розчину 8,65N гідроксиду натрію, потім нагрівають при 170°С протягом 3год. під тиском 7 бар. Реакційну суміш згодом доводять до температури навколишнього середовища і потім переносять в реактор, і згодом додають концентровану хлористоводневу кислоту, доки не досягнуть рН3,4, підтримуючи температуру між 20 і 25°С. Суміш потім перемішують протягом 1 год. і осад згодом відфільтровують, промивають і висушують з тим щоб одержати рацемічну індолін-2карбонову кислоту з ви ходом 90% (2,34кг). Стадія С: Повторне використання індолін-2карбонової кислоти Рацемічну індолін-2-карбонову кислоту, одержану на Стадії В, (2,34кг) розчиняють відповідно до методики на Стадії А. (R)-a-метилбензиламінну сіль (2S)-індолін-2карбонової кислоти, утворену таким чином, виділяють і потім обробляють хлористоводневою кислотою відповідно до методики на Стадії А1 з тим, щоб одержати (2S)-індолін-2-карбонову кислоту ("друга складова") у формі кристалів (0,84кг), що має хімічну чистоту 98% і енантіомерну чистоту більшу, ніж 99,5%. Першу складову, одержану на Стадії А1, і др угу складову, одержану на Стадії С, потім об'єднують. (2S)-індолін-2-карбонову кислоту таким чином одержують з повним виходом 52,8%, хімічною чистотою 98,% і енантіомерною чистотою більшою, ніж 99,5%. Підписне Тираж 26 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюNormal;heading 1;heading 2;process for the synthesis of (2s)-indoline-2-carboxylic acid and use thereof in the synthesis of perindopril
Автори англійськоюSouvie Jean-Claude, LECOUVE JEAN-PIERRE
Назва патенту російськоюСпособ синтеза (2s)- индолин-2-карбоновой кислоты и применение в синтезе периндоприла
Автори російськоюСувье Жан-Клод, Лекув Жан-Пьер
МПК / Мітки
МПК: C07D 209/42, C07K 5/06
Мітки: кислоти, 2s)-індолін-2-карбонової, периндоприлу, синтезу, спосіб, застосування, синтезі
Код посилання
<a href="https://ua.patents.su/4-80040-sposib-sintezu-2s-indolin-2-karbonovo-kisloti-i-zastosuvannya-u-sintezi-perindoprilu.html" target="_blank" rel="follow" title="База патентів України">Спосіб синтезу (2s)-індолін-2-карбонової кислоти і застосування у синтезі периндоприлу</a>








