Спосіб одержання 1-ціклопропіл-7-хлор-6-фтор-1,4-дігідро-4-оксо-3-хінолінкарбонової кислоти
Формула / Реферат
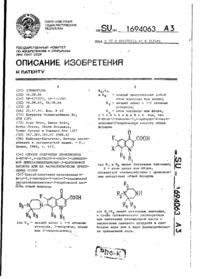
1. Способ получения 1-циклопропил-7-хлор-6-фтор-1,4-дигидро-4-оксо-3-хинолин-карбоновой кислоты формулы I
взаимодействием соединения формулы II
с соединением общей формулы III
где R1 и R3 одинаковы или различны и означают низший алкил, при нагревании в среде инертного низкокипящего органического растворителя в присутствии основания с последующим взаимодействием полученного при этом продукта с циклопропиламином формулы IV
в среде инертного органического растворителя при 70-100°С, циклизацией полученного при этом продукта в среде инертного органического растворителя при нагревании в присутствии основания с последующим омылением и осаждением целевого продукта с помощью кислоты, отличающийся тем, что, с цеяьто интенсификации процесса при сохранении высокого выхода целевого продукта, взаимодействие соединений формул (II) и (III) осуществляют добавлением соединения формулы (II) к смеси соединения формулы (III), инертного низкокипящего органического растворителя и основания при 90-110°С или температуре ее кипения, а циклизацию проводят в среде инертного высококипящего органического растворителя при 135-145°С, причем все стадии проводят без выделения соответствующего продукта реакции.
2. Способ по п. 1, отличающийся тем, что низкокипящий растворитель удаляют перед добавлением циклопропиламина.
3. Способ по п. 1, отличающийся тем, что низкокипящий растворитель удаляют после реакции с циклопропиламином.
4. Способ по п. 3, отличающийся тем, что удаление осуществляют путем нагревания до температуры циклизации после добавления инертного высоко-кипящего органического растворителя.
5. Способ по п. 1, отличающийся тем, что перед омылением реакционную смесь охлаждают до температуры порядка 90-100°С.
Текст
Изобретение касается гетероциклических веществ, в частности получения 1-циклопропил-7-хлор-6-фтор-1,4-дигидро-4-оксо-3-хинолинкарбоновой кислоты - полупродукта для синтеза активных веществ. Цель -интенсификация процесса при сохранении высокого выхода целевого вещества. Синтез ведут реакцией 2,4-дихлор-5-фторбензоилхлорида с соединением ф-лы, R2R3N-CH-CH-C(O)-ORi, где Ri-R3 (одина ковы или различны) - алкил (низший), которое в виде смеси с инертным органическим растворителем и основанием добавляют к указанному бензоилхлориду Процесс ведут при 90-110°С или температуре кипения реакционной смеси Затем ведут обработку полученного продукта пропиламином (для циклизации) в среде органического растворителя при 135-145°С При этом лучше удалять низкокипящий растворитель перед добавлением циклопропиламина или после реакции с ним Удаление растворителя ведут нагреванием до температуры циклизации после добавления инертного высококипящего растворителя Далее ведут омыление полученного продукта с предварительным охлаждением реакционной смеси до 90-100°С и выделение целевого продукта осаждением с помощью кислоты При этом все стадии процесса ведут без выделения промежуточных веществ Эти условия сокращают длительность 1-й стадии с 5 ч до 75 мин и циклизации со 180 до 90 мин при аналогичном с известным выходе целевого продукта 4 з.п ф-лы. so Изобретение относится к способам получения 1-циклопропил-7-хлор-6-фтор-1,4дигидро-4-оксо-З-хинолинкарбоновой кислоты (і), которая используется в качестве промежуточного продукта в синтезе фармацевтически активных хинолинкарбоновых кислот. Цель изобретения - интенсификация процесса при сохранении высокого выхода целевого продукта. Поставленная цель достигается взаимодействием 2,4-дихлор~5-фторбензоилх/шрида (!!) с соединением CH-COORi где R1-R3 одинаковы или различны и означают низший алкил, в среде низкокипящего органического растворителя в присутствии 1660582 основания при 9D-110°C или температуре кипения реакционной смеси с последующим взаимодействием полученного промежуточного продукта с циклопропиламином в среде инертного органического раствори- 5 теля при 70-90°С с последующей циклизацией полученного промежуточного продукта в среде инертного высококипящего органического растворителя при 135145°С в присутствии основания с 10 последующим омылением и осаждением целевого продукта с помощью кислоты, причем процесс проводят без выделения промежуточных продуктов реакций. П р и м е р 1. 28,8 г сложного этилового 15 эфира ї\І,ї\І-диметиламиноакриловай кислоты и 26 г Ы,М~дмметилбензиламина в среде 71 мл толуола нагревают до 90°С и при этой температуре каплями добавляют в течение 60мин40г2,4-дихлор-5-фторбензоилхлори- 20 да. Затем дополнительно перемешивают в течение 15 мин и выпавший гидрохлорид N.N-диметиленбензиламина отделяют на нутч-фильтре. Фильтрат упаривают в вакууме и остаток смешивают с 80 мл бутилглико- 25 ля. При 70-75°С добавляют каплями в течение 30 мин 13 г циклопропиламина и после добавления температуру реакционной смеси поддерживают при 100°С в течение 1 ч до конца выделения газа. К 30 реакционной смеси добавляют 27,9 г поташа и 100 мл бутилгликоля и медленно нагревают до 135-145°С. При этом отгоняют около 40 мл низкокипящих компонентов. Температуру поддерживают в течение 1,5 ч, 35 Затем охлаждают до 100-120°С и к реакционной смеси добавляют 130мл воды. Дополнительно перемешивают в течение 15 мин при 90°С и при этой температуре добавляют каплями в течение 15 мин 27 мл уксусной кислоты. Содержимое колбы охлаждают и 40 твердое вещество отделяют на нутч-фильтре. Продукт промывают 27 мл воды и 50 мл метанола, отсасывают досуха и сушат в вакууме при 70°С в течение 24 ч. Получают 37 г (74,9% в пересчете на исходный бензоил- 45 хлорид) 1-циклопропил-7-хлор-6-фтор-1,4дигидро-4-оксо-З-хинолинкарбоновой кислоты, т.пл. 240-241°С. лопропиламина, после чего нагревают до 100°С до конца выделения газа. Затем добавляют 42 г поташа и 270 мл бутилгликоля и медленно нагревают до 135-145°С. При этом отгоняют около 180 мл толуола и низкокипящих компонентов. В течение 1,5 ч поддерживают температуру на уровне 135-145°С и после охлаждения реакционной смеси до 100°С добавляют 200 мл воды. Через 15 мин при 90°С добавляют каплями 40,5 мл уксусной кислоты и выпавшее твердое вещество отсасывают на нутч-фильтре, Продукт дополнительно промывают 140 мл воды и 75 мл метанола, отсасывают досуха и сушат в вакууме в течение 24 ч при 70°С. Получают 58,5 г (79% в пересчете на исходный бензоилхлорид) 1-циклопропил~7-хлорб-фтор-М-дмгидро-4-оксо-З-хинолинкарбовой кислоты. П р и м е р з . 44,7 сложного этилового эфира Ы,Ы-диметиламиноакриловой кислоты и 17,1 г М.МЧциметилпиперазина в 95 мл циклогексана нагревают с обратным холодильником. В течение 1 ч каплями добэвляют 62 г 2,4-дихлор-5-фторбензоилхлорида. Выпавший гидрохлорид диметилбензиламина отделяют на нухч-фильтре и фильтрат упаривают досуха в вакууме. Остаток растворяют в 125 мл бутилгликоля и к раствору каплями добавляют 20,2 циклопропиламина при 90°С. После окончания выделения газа добавляют 43,4 поташа и 165 мл бутилгликоля и нагревают до 145°С в течение 1.5 ч. При этом сначала отгоняют незначительное количество низкокипящих компонентов. Через 1,5 ч. охлаждают до 100°С, реакционную смесь смешивают с 205 мл воды и дополнительно перемешивают в течение 15 мин при 95°С. Затем каплями добавляют 42 г уксусной кислоты, охлаждают до 30°С и выпавшее твердое вещество отгоняют на нутч-фильтре. Фильтровальный осадок промывают 180 мл воды и 80 мл 80%-ного изопропанола и сушат в вакууме в течение ночи при 70°С. Получают 60,1 г (78,1 % в пересчете на исходный бензоилхлорид) 1-циклопропил-7-хлор-6-фтор-1,4~дигидро-4-оксо-3-хинолинкарбоновой кислоты. П р и м е р 4. 33,7 г сложного метилоП р и м е р 2. 43,2 г сложного этилового 50 вого эфира М,!Ч-диметиламиноакриловой эфира Г\і,М-диметиламиноакриловой кислокислоты и 40,5 г Ы,М-диметил6ензилачина ты в 84 мл толуола нагревают до 100°С и в 95 мл толуола нагревают до 110°С. При добавляют 40 мл триэтиламина. температуре флегмы в течение 1 ч каплями добавляют 62 г 2,4-дихлор-5-фторбензоилПри температуре флегмы каплями добавляют в течение 30 мин 60 г 2,4-дихлор-5- 55 хлорида и затем выпавший гидрохлорид фторбензоилхлорида и затем выпавший диметилбензиламина отделяют на нутчгидрохлорид триэтиламина отделяют на фильтре. нутч-фильтре. Дополнительно промывают Растворитель отгоняют в вакууме, до55 мл толуола и каплями добавляют к фильбавляют 130 мл бутилгликоля и каплями трату в течение 20 мин при 70°С 16,2 г цикдобавляют в течение 20 мин при 90°С 20,2 г 1660582 циклопропиламмна, После окончания выделения газа реакционную смесь смешивают с 43,4 г поташа и 150 мл бутилгликоля и медленно нагревают до 140°С, при этом отгоняют незначительное количество низко- 5 кипящего растворителя. Затем дополнительно перемешивают в течение 1,5ч при 140°С. После охлаждения до 100°С к реакционной смеси добавляют 205 мл воды и перемешивают в течение 15 мин при 10 90°С. При слабом охлаждении добавляют 100 мп 30%-ной серной кислоты, твердое вещество отсасывают на нутч-фильтре и промывают 200 мл воды и 200 мл изопропанола. Твердое вещество сушат в вакууме 15 при 70°С в течение ночи. Получают 59,4 £ (77,2% в пересчете на исходный бензоилхлорид) 1 -циклоп ропил-7-хлор-6-фтор-1,4дигидро-4-оксо-З-хинолинкарбоновой кислоты. 20 П р и м е р 5. К 44,7 г сложного этилового эфира ІМ.КІ-диметиламиноакриловой кислоты в 95 мл циклогексэна добавляют 55,6 трибутиламина и в течение 1 ч при 85~95°С каплями добавляют 62 г 2,4-дихлор-5-фтор- 25 бензоилхлорида Затем к реакционной смеси добавляют 250 мл воды и отделяют водную солевую фазу. Водную фазу перемешивают вместе с 50 мл циклогексана и соединенные органические фазы упаривают 30 досуха в вакууме, получаемом при помощи водоструйного насоса. Остаток поглощают в 125 мл бутилгликоля, нагревают до 70°С и в течение 15 мин каплями добавляют 20,2 г циклопропиламина. После окончания выде- 35 ления газа добавляют следующие 160 мл бутилгликоля и 44 г поташа и реакционную смесь медленно нагревают до 140°С. После достижения 140°С дополнительно перемешивают в течение 1,5 ч, затем охлаждают до 40 100°С и к реакционной смеси добавляют 205 мл зоды. По истечении 15 мин каплями добавляют 42 г уксусной кислоты в течение 10 мин и охлаждают до комнатной температуры. Осадок отделяют на нутч-фильтре и 45 промывают водой и изолропанолом. После сушки в вакууме при 50°С в течение ночи получают 54,6 (71% в пересчете на исходный бензилхлорид) 1-циклопропил-7-хлор6-фтор-1,4-дигидро-4-оксо-3-хинолинкарбо- 50 новой кислоты, П р и м е р 6. 105 г трибутиламина и 86 г сложного метилового эфира ММ-диметиламиноакриловой кислоты в 148 мл толуола нагревают до 105°С и в течение 1 ч каплями добавляют 124 г2,4-дихлор-5-фторбензоилхлорида. После охлаждения реакционной смеси до 50°С экстрагируют два раза водой по 250 мл. Органическую фазу сгущают в вакууме, получаемом при помо щи водоструйного насоса, и к остатку каплями добавляют 7,5 г циклопропиламина при внутренней температуре 70- 75°С При этом до конца реакции выделяется газообразный диметилзмин Реакционную смесь смешивают с 86,8 г поташа и 500 мл бутилгликоля и медленно нагревают до 135-145°С. При этом отгоняют незначительное количество низкокипящего растворителя В течение 1,5 ч поддерживают температуру на уровне 135-145°С, а затем охлаждают до 100°С и добавляют 535 мл 10%-ной уксусной кислоты. Полученную суспензию охлаждают до комнатной температуры, твердое вещество отгоняют на нутч-фильтре и промывают 175 мл воды и 200 мл 80%-ного изопропанола. Продукт суша г в течение ночи в вакууме при 70°С Получают 220 г (78,1% в пересчете на исходный бензоилхлорид) 1циклопропил-7-хлор-6-фтор-1,4-дигидро-4 -оксо-3-хинолинкзрбоновой кислоты. Целевой продукт по примерам і^б имеет т пл. 240-241°С, т. е. является высоко чистым. Первую стадию способа можно проводить в течение не более 75 мин (вместо 5 ч по известному способу) без ухудшения выхода конечного продукта благодаря тому, что бензоилхлорид добавляют к смеси сложного эфира акриловой кислоты, инертного низкокипящего органического растворителя и основания при 90-110°С или температуре ее кипения, Этот признак является существенным, так как при добавлении сложного эфира акриловой кислоты к смеси, содержащей бензоилхлорид, выход конечного продукта существенно снижается, Так, например, при повторении примера 1, за исключением того, что сложный этиловый эфир М,Г\!-диметиламиноакриловой кислоты добавляют к нагретой до 90°С смеси, содержащей 2,4-дихлор-5-фторбензоилхлорид, выход целевого продукта составляет лишь 67,5%. Следовательно, суметом исключения по предлагаемому способу потерь промежуточных веществ выход целевого продукта практически ниже уровня по известному способу. Дальнейшая интенсификация процесса обеспечивается за счет проведения стадии циклизации при 135-145°С в среде высококипящего органического растворителя При этом циклизацию можно проводить в течение 90 мин, тогда как по известному способу 55 она требует 180 мин, Формула изобретения 1. Способ получения 1-циклолропил-7хлор-6-фтор-1,4-дигидро-4~оксо-3-хинолин карбоновой кислоты формулы I 1660582 COOH взаимодействием соединения формулы II 5 F СІ СІ, с соединением общей формулы III 10 CH-COORi 3 z. где Ri и Яз одинаковы или различны и озна- 15 чают низший алкил, при нагревании в среде инертного низкокипящего органического растворителя в присутствии основания с последующим взаимодействием полученного при этом продукта с циклопропиламином формулы IV 20 8 щ и й ся тем, что, с целью интенсификации процесса при сохранении высокого выхода целевого продукта, взаимодействие соединений формул (II) и (І! І) осуществляют добавлением соединения формулы (II) к смеси соединения формулы (III), инертного низкокипящего органического растворителя и основания при 90-110°С или температуре ее кипения, а циклизацию проводят в среде инертного высококипящего органического растворителя при 135-145°С. причем все стадии проводят без выделения соответствующего продукта реакции. 2. Способ по п. 1, о т л и ч а ю щ и й с я тем, что низкокипящий растворитель удаляют перед добавлением циклопропиламина. 3. Способ по п. 1, о т л и ч а ю щ и й с я тем, что низкокипящий растворитель удаляют после реакции с циклопропиламином. 4. Способ по п. 3, о т л и ч а ю щ и й с я тем, что удаление осуществляют путем нагревания до температуры циклизации после добавления инертного высококипящего органического растворителя. в среде инертного органического раствори- 25 теля при70-100°С, циклизацией полученно5. Способ по п.1, о т л и ч а ю щ и й с я го при этом продукта в среде инертного тем, что перед омылением реакционную органического растворители при нагревасмесь охлаждают до температуры порядка нии в присутствии основания с последующим омылением и осаждением целевого 30 90-100°С. продукта с помощью кислоты, о т л и ч а ю Редактор А.Огар Составитель А.Свиридова Техред М.Моргентал Корректор Т.Малец Заказ 1859 Тираж 247 Подписное ВНИИПИ Государственного комитета по изобретениям и открытиям при ГКНТ СССР 113035, Москва, Ж-35, Раушская наб., 4/6 Производственно-издательский комбинат "Патент", г. Ужгород, ул.Гагарина, 101
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 1-cyclopropyl-7-chloro-6-fluoro-1,4-dihydro-4-oxo-3-quinoline carboxylic acid
Назва патенту російськоюСпособ получения 1-циклопропил-7-хлор-6-фтор-1,4-дигидро-4-оксо-3-хинолинкарбоновой кислоты
МПК / Мітки
МПК: C07D 215/56
Мітки: спосіб, 1-ціклопропіл-7-хлор-6-фтор-1,4-дігідро-4-оксо-3-хінолінкарбонової, кислоти, одержання
Код посилання
<a href="https://ua.patents.su/4-8018-sposib-oderzhannya-1-ciklopropil-7-khlor-6-ftor-14-digidro-4-okso-3-khinolinkarbonovo-kisloti.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 1-ціклопропіл-7-хлор-6-фтор-1,4-дігідро-4-оксо-3-хінолінкарбонової кислоти</a>
Попередній патент: Спосіб одержання заміщених 1-(1-фенілціклобутіл)-алкіламінів або їх фармакологічно припущених солей
Наступний патент: Спосіб одержання харчової води “екстра біо n4″
Випадковий патент: Комбінована дозована форма, що містить тамсулозин та інгібітор тестостерон-5a-редуктази