Складні арилалкілові ефіри 4-аміно-6-(заміщений феніл)піколінатів і їх застосування як гербіцидів
Номер патенту: 108922
Опубліковано: 25.06.2015
Автори: Лоу Крістіан Т., Йєркс Карла Н., Еккельбарджер Джозеф Д., Шмітцер Пол Р., Гюнтенспбергер Катеріне А., Епп Джеффрі Б., Сіддалл Томас Л.
Формула / Реферат
1. Сполука формули IB:
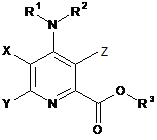 , IB
, IB
де
X являє собою Н або F;
Y являє собою галоген, С1-С8-алкіл, С3-С6-циклоалкіл або феніл, заміщений 1-4 замісниками, незалежно вибраними з галогену, С1-С3-алкілу, С3-С6-циклоалкілу, С1-С3-алкокси, С1-С3-галогеналкілу, С1-С3-галогеналкокси, ціано, нітро, NR1R2, або де два суміжні замісники, взяті разом, являють собою -О(СН2)nО-або -О(СН2)n-, де n=1 або 2;
Z являє собою галоген або С2-С4-алкеніл;
R1 і R2 незалежно являють собою Н, С1-С6-алкіл або С1-С6-ацил;
R3 являє собою незаміщений або заміщений С7-С11-арилалкіл.
2. Сполука за п. 1, де X являє собою Н.
3. Сполука за п. 1, де X являє собою F.
4. Сполука за п. 1, де Y являє собою заміщений феніл.
5. Сполука за п. 1, де Z являє собою Сl.
6. Сполука за п. 1, де R1 і R2 являють собою Н.
7. Сполука за п. 1, де R3 являє собою бензил.
8. Сполука за п. 1, де R3 являє собою незаміщений або орто-, мета- або пара-монозаміщений бензил.
9. Гербіцидна композиція, що містить гербіцидно ефективну кількість сполуки формули IB за п. 1, в суміші з прийнятним з точки зору сільського господарства допоміжним засобом або носієм.
10. Спосіб боротьби з небажаною рослинністю, що включає приведення в контакт рослинності або її локусу за допомогою нанесення на листя або шляхом поливу, або шляхом внесення в ґрунт або воду для запобігання появі рослинності гербіцидно ефективної кількості сполуки формули IB за п. 1.
11. Спосіб вибіркової боротьби з небажаною рослинністю на післясходовій стадії в присутності рису, пшениці або кормових рослин, який включає застосування до вказаної небажаної рослинності гербіцидно ефективної кількості сполуки формули IB за п. 1 або їх гербіцидної композиції.
Текст
Реферат: Складні арилалкілові ефіри 4-амінопіколінових кислот формули (IB) являють собою гербіциди для боротьби з бур'янами, особливо з тими видами, які, як правило, зустрічаються в системах для вирощування рису і пшениці і в програмах поліпшення пасовищ. R 1 N X Y R 2 Z O N R O 3 (IB) UA 108922 C2 UA 108922 C2 5 10 15 20 25 30 35 Даний винахід стосується конкретних нових складних ефірів 4-аміно-6-(заміщений феніл)піколінових кислот і 6-аміно-2-(заміщений феніл)-4-піримідинкарбонових кислот і застосування цих сполук як гербіцидів для боротьби з бур'янами, особливо з тими видами, які, як правило, зустрічаються в системах для вирощування рису і пшениці і в програмах поліпшення пасовищ. Багато які піколінові кислоти і їх пестицидні властивості описані в галузі техніки. Патент США 6784137 B2 і патент США 7314849 B2 розкривають сімейство 4-аміно-6-арилпіколінових кислот і їх похідні і їх застосування як гербіцидів вибіркової дії, зокрема, для рису і зернових злаків, таких як пшениця і ячмінь. WO 2005/063721 A1, WO 2007/082076 A1, патент США 7863220 B2, патент США 7300907 B2, патент США 7642220 B2 і патент США 7786044 B2 розкривають конкретні 6-аміно-2-заміщені-4-піримідинкарбонові кислоти і їх похідні і їх застосування як гербіцидів. У цей час виявлено, що певні складні ефіри 4-аміно-6-(заміщений феніл)піколінових кислот і 6-аміно-2-(заміщений феніл)-4-піримідинкарбонових кислот можуть забезпечувати чудову боротьбу з бур'янами, особливо, в системах для вирощування рису і пшениці і в програмах поліпшення пасовищ. Певні складні арилалкілові ефіри 4-аміно-6-(заміщений феніл)піколінових кислот і 6-аміно-2(заміщений феніл)-4-піримідинкарбонових кислот є чудовими гербіцидами з широким спектром боротьби з широколистими, трав'янистими і осоковими бур'янами, особливо в системах для вирощування рису і пшениці і в програмах поліпшення пасовищ. Сполуки додатково мають чудові токсикологічні або екологічні профілі. Даний винахід включає сполуки формули IA: , де Y являє собою С1-C8-алкіл, C3-C6-циклоалкіл або феніл, заміщений 1-4 замісниками, незалежно вибраними з галогену, C1-C3-алкілу, C3-C6-циклоалкілу, C1-C3-алкокси, C1-C31 2 галогеналкілу, C1-C3-галогеналкокси, ціано, нітро, NR R , або де два суміжні замісники, взяті разом, являють собою -O(CH2)nO- або -O(CH2)n-, де n=1 або 2; Z являє собою галоген, C1-C3-алкокси або C2-C4-алкеніл; 1 2 R і R незалежно один від одного являють собою Н, C1-C6-алкіл або C1-C6-ацил; 3 R являє собою незаміщений або заміщений C7-C11-арилалкіл. Переважні сполуки включають такі, в яких Y являє собою заміщений феніл, Z являє собою 1 2 3 Cl, -CH=CH2 або OCH3, R і R являють собою Н, R являє собою незаміщений або орто-, метаабо пара-монозаміщений бензил. Даний винахід також включає сполуки формули IB: , де X=Н або F; Y являє собою галоген, C1-C8-алкіл, C3-C6-циклоалкіл або феніл, заміщений 1-4 замісниками, незалежно вибраними з галогену, C1-C3-алкілу, C3-C6-циклоалкілу, C1-C3-алкокси, C1-C3 1 UA 108922 C2 1 5 10 15 20 25 30 35 40 45 50 2 галогеналкілу, C1-C3-галогеналкокси, ціано, нітро, NR R або де два суміжні замісники, взяті разом, являють собою -O(CH2)nO- або -O(CH2)n-, де n=1 або 2; Z являє собою галоген або C2-C4-алкеніл; 1 2 R і R незалежно являють собою Н, C1-C6-алкіл або C1-C6-ацил; 3 R являє собою незаміщений або заміщений C7-C11-арилалкіл. Переважні сполуки включають такі, в яких X являє собою Н або F, Y являє собою заміщений 1 2 3 феніл, Z являє собою Cl, R і R являють собою Н, R являє собою незаміщений або орто-, мета- або пара-монозаміщений бензил. Даний винахід включає гербіцидні композиції, що містять гербіцидно ефективну кількість сполук формули IA або IB в суміші з прийнятним з точки зору сільського господарства допоміжним засобом або носієм. Даний винахід також включає спосіб застосування сполук і композицій за даним винаходом для знищення або боротьби з небажаною рослинністю шляхом застосування гербіцидної кількості сполуки до рослинності або до локусу рослинності, а також до ґрунту до появи рослинності або до поливної або заливної води до або після появи сходів. Даний винахід додатково включає спосіб вибіркової боротьби з небажаною рослинністю на післясходовій стадії в присутності рису, пшениці або кормових рослин, що включає застосування до вказаної небажаної рослинності гербіцидно ефективної кількості сполуки за даним винаходом. Даний винахід також включає спосіб отримання сполук за даним винаходом. Гербіцидні сполуки за даним винаходом є складними арилалкіловими ефірами 4-аміно-6(заміщений феніл)піколінових кислот і 6-аміно-2-(заміщений феніл)-4-піримідинкарбонових кислот і їх похідних. Піколінові кислоти, з яких отримують складні ефіри формули IB, являють собою новий клас сполук, які мають гербіцидну дію. Багато які сполуки піколінових кислот описані в патенті США 6784137 B2 і патенті США 7314849 B2, включаючи inter alia, 4-аміно-3хлор-6-(4-хлор-2-фтор-3-метокси-феніл)піколінову кислоту, 4-аміно-3-хлор-5-фтор-6-(4-хлор-2фтор-3-метоксифеніл)піколінову кислоту і 4-аміно-3-хлор-6-(2,4-дихлор-3метоксифеніл)піколінову кислоту. Піримідинкарбонові кислоти, такі, із яких отримують складні ефіри формули IA, також являють собою новий клас сполук, які мають гербіцидну дію. Багато які сполуки піримідинкарбонових кислот описані в WO 2005/063721 A1, WO 2007/082076 A1, патенті США 7863220 B2, патенті США 7300907 B2, патенті США 7642220 B2 і патенті США 7786044 B2. Ці піколінові і піримідинкарбонові кислоти діють проти однорічних трав'янистих бур'янів, широколистих бур'янів і осокових бур'янів в рисі і пшениці, але складні арилалкілові ефіри за даним винаходом демонструють більш ефективну дію, ніж відомі складні ефіри, особливо проти бур'янів, що зустрічаються в системах для вирощування рису і пшениці і в програмах поліпшення пасовищ. Переважними складноефірними групами є ті, які забезпечують більший рівень боротьби з бур'янами в порівнянні з нормою внесення складних метилових ефірів в еквіваленті кислоти. Переважні складноефірні групи включають незаміщений складний бензиловий ефір і орто-, мета- і пара-монозаміщені складні бензилові ефіри. Складні арилалкілові ефіри 6-аміно-2-(заміщений феніл)-4-піримідинкарбонових кислот можуть бути отримані шляхом реакції піримідинкарбонових кислот з арилалкілгалогенідом в присутності основи. Схема 1 . Складні арилалкілові ефіри піколінових кислот можуть бути отримані шляхом зв’язування піколінової кислоти зі спиртом із застосуванням будь-якого з числа придатних активаторів, таких як застосовуються для зв’язування пептидів, таких як дициклогексилкарбодіімід (DCC) або карбонілдіімідазол (CDI), або шляхом реакції відповідної кислоти з відповідним арилалкіловим спиртом в присутності кислотного каталізатора. Альтернативно, складні арилалкілові ефіри можуть бути отримані шляхом реакції піколінової кислоти з арилалкілгалогенідом в присутності основи. 2 UA 108922 C2 Схема 2 5 10 15 20 25 30 35 40 45 50 . Вважається, що деякі реагенти і умови реакції, розкриті в даному описі або в хімічній літературі з отриманням сполуки формули IA або IB, можуть не бути сумісними з певними функціональними властивостями, властивими проміжним продуктам. У цих випадках введення блокуючих/знімання блокуючих послідовностей або взаємне перетворення функціональних груп в ході синтезу буде сприяти отриманню бажаних продуктів. Застосування і вибір блокуючих груп будуть очевидні фахівцеві галузі хімічного синтезу. Терміни "алкіл", "алкеніл" і "алкініл", а також похідні терміни, такі як "алкокси", "ацил" і "алкілтіо", як використовується в даному описі, охоплюють фрагменти з прямим і розгалуженим ланцюгом. Якщо не указано інакше, кожний з них може бути незаміщеним або заміщеним одним або більше замісниками, вибраними з, але не обмежуючись ними, галогену, алкокси, алкілтіо або аміноалкілу, за умови, що замісники є стерично сумісними, і дотримуються умови утворення хімічного зв'язку і енергії деформації. Терміни "алкеніл" і "алкініл" призначені для позначення включення одного або більше ненасичених зв'язків. Термін "арилалкіл", як використовується в даному описі, стосується фенілзамещеної алкільної групи, що містить загалом 7-11 вуглецевих атомів, такої як бензил (-CH2C6H5), 2метилнафтил(-CH2C10H7) і 1- або 2-фенетил (-CH2CH2C6H5 або -CH(CH3)C6H5). Фенільна група може бути сама по собі незаміщеною або заміщеною одним або більше замісниками, незалежно вибраними з галогену, нітро, ціано, C1-C6-алкілу, C1-C6-алкокси, галогенованого C1C6-алкілу, галогенованої C1-C6-алкокси, C1-C6-алкілтіо, С(О)OC1-C6-алкілу, або де два суміжні замісники, взяті разом, являють собою -О(CH2)nO-, де n=1 або 2, за умови, що замісники є стерично сумісними, і дотримуються умов утворення хімічного зв'язку і енергії деформації. Якщо інакше конкретно не обмежено, термін "галоген" включає фтор, хлор, бром і йод. Виявлено, що сполуки формули IA або IB є придатними як передсходові і післясходові гербіциди в системах для вирощування рису і зернових злаків і для програм поліпшення пасовищ. Термін "гербіцид" використовується в даному описі для позначення активного інгредієнта, знищувального, регулюючого або іншим чином несприятливо модифікуючого ріст рослин. Гербіцидно ефективною або регулюючою ріст рослинності кількістю активного інгредієнта є кількість, яка викликає несприятливий модифікуючий ефект, що включає відхилення від природного розвитку, знищення, регулювання, висушування, затримку росту і т. п. Терміни "рослини" і "рослинність" включають проростаюче насіння, сходи, що з'являються, надземні і підземні частини рослин, такі як пагони, коріння, бульби, ризоми і т. п. і сталу рослинність. Гербіцидна дія, яка демонструється сполуками за даним винаходом, при їх застосуванні безпосередньо до рослини або до локусу рослини на будь-якій стадії росту або до посадки або появи сходів. Спостережуваний ефект залежить від видів рослин, з якими необхідно боротися, стадії росту рослини, параметрів розведення для застосування і розміру крапель, які розбризкуються, величини часток твердих компонентів, умов навколишнього середовища під час застосування, конкретної сполуки, що застосовується, конкретних допоміжних засобів і носіїв, які застосовуються, типу ґрунту, якості води і т. п., а також від кількості застосовуваного хімікату. Ці і інші фактори можуть бути відрегульовані так, як відомо в галузі техніки, для посилення вибіркової гербіцидної дії. Загалом, для досягнення максимального результату боротьби з бур'янами переважно застосування сполук формули IA або IB на післясходовій стадії шляхом розбризкування або з поливною водою до відносно незрілої небажаної рослинності. Норми внесення 1-500 грам на гектар (г/га), загалом, застосовують при листових і водних обробках на післясходовій стадії. Переважні норми внесення становлять 10-300 г/га. Для застосувань на досходовій стадії, загалом, застосовують норми внесення 5-500 г/га. Переважні норми внесення становлять 30-300 г/га. Більш високі вказані норми внесення, загалом, 3 UA 108922 C2 5 10 15 20 25 30 35 40 45 50 55 60 приводять до невибіркової боротьби з широким спектром небажаної рослинності. Більш низькі норми внесення, як правило, приводять до вибіркової боротьби і можуть бути застосовані до локусів сільськогосподарських культур. Гербіцидні сполуки за даним винаходом часто застосовують разом з одним або більше іншими гербіцидами для боротьби з більш широким спектром небажаної рослинності. При застосуванні разом з іншими гербіцидами, представлені в даному описі сполуки можуть бути складені в композицію з іншим гербіцидом або гербіцидами, змішані з іншим гербіцидом або гербіцидами в резервуарі або застосовані послідовно з іншим гербіцидом або гербіцидами. Деякі гербіциди, які можуть бути застосовані разом із сполуками за даним винаходом, включають: солі 2,4-Д, складні ефіри і аміни, ацетохлор, ацифлуорфен, алахлор, амідосульфурон, амінопіралід, амінотриазол, тіоціатат амонію, аніліфос, атразин, азимсульфурон, бенфуресат, бенсульфурон-метил, бентазон, бентіокарб, бензобіциклон, бензофенап, біфенокс, біспірибак-натрій, бромбутид, бутахлор, кафенстрол, карфентразонетил, клодинафоп-пропаргіл, хлоримурон, хлорпрофам, циносульфурон, клетодим, кломазон, кломепроп, клопіралід, клорансулам-метил, циклосульфамурон, циклоксидим, цигалофопбутил, кумілурон, даімурон, диклосулам, дифлуфенікан, дифлуфензопір, димепіперат, диметаметрин, дикват, дитіопір, EK2612, EPTC, еспрокарб, ET-751, етоксисульфурон, етбензанід, феноксапроп, феноксапроп-етил, феноксапроп-етил + ізоксадифен-етил, фентразамід, флазасульфурон, флорасулам, флуазифоп, флуазифоп-Р-бутил, флуцетосульфурон, флуфенацет, флуфенпір-етил, флуметсулам, флуміоксазин, флупірсульфурон, флуроксипір, фомесафен, форамсульфурон, глуфосинат, глуфосинат-Р, гліфосат, галосульфурон-метил, галоксифоп-метил, галоксифоп-R, галоксифоп-R-метил, імазаметабенз, імазамокс, імазапік, імазапір, імазаквін, імазетапір, імазосульфурон, інданофан, іоксиніл, іпфенкарбазон, ізоксабен, MCPA, MCPB, мефенацет, мезосульфурон, мезотріон, метаміфоп, метазосульфурон, метолахлор, метосулам, метсульфурон, молінат, моносульфурон, MSMA, ортосульфамурон, оризалін, оксадіаргіл, оксадіазон, оксацикломефон, оксифлуорфен, паракват, пендиметалін, пеноксулам, пентоксазон, петоксамід, піклорам, піперофос, претилахлор, профоксидим, прогексадіон-кальцій, пропахлор, пропаніл, пропізохлор, пропізамід, пропірисульфурон, просульфурон, пірабутикарб, піраклоніл, піразогіл, піразолінат, піразосульфурон-етил, піразоксифен, пірибензоксим, піридат, пірифталід, піримінобак-метил, піримісульфан, примісульфурон, піроксулам, квінокламін, квінклорак, квізалофоп-Р-етил, S-3252, сентоксидим, симазин, симетрин, s-метолахлор, сулькотріон, сулфентразон, сульфосат, тефурилтріон, тенілхлор, тіазопір, тіобенкарб, триклопір, складні ефіри і аміни триклопіру, трифлуралін, тринексапак-етил, тритосульфурон і інші 4-аміно-6(заміщений феніл)піколінати і 6-аміно-2-(заміщений феніл)-4-піримідинкарбоксилати і їх солі і складні ефіри. Сполуки за даним винаходом можуть бути додатково застосовані для боротьби з небажаною рослинністю в багатьох сільськогосподарських культурах, яким додали стійкість до або резистентність до цих або інших гербіцидів шляхом генетичної модифікації або шляхом мутації і селекції. Гербіцидні сполуки за даним винаходом можуть бути додатково застосовані разом з гліфосатом, глуфосинатом, дикамбою, імідазолінонами, арилоксифеноксипропіонатами або 2,4-Д до сільськогосподарських культур стійких до гліфосату, глуфосинату, дикамби, імідазолінону, арилоксифеноксипропіонату або 2,4-Д. Загалом, переважне застосування сполук за даним винаходом в комбінації з гербіцидами, які є вибірковими відносно сільськогосподарської культури, яка обробляється, і які доповнюють спектр бур'янів, що контролюються цими сполуками, при застосовуваній нормі внесення. Додатково, загалом, переважне застосування сполук за даним винаходом і інших додаткових гербіцидів одночасно, або у вигляді комбінованого складу, або у вигляді танкової суміші. Аналогічні гербіцидні сполуки за даним винаходом можуть бути застосовані разом з ацетолактатсинтазними (ALS) інгібіторами до сільськогосподарських культур, стійких до ацетолактатсинтазних інгібіторів, або з інгібіторами 4-гідроксифенілпіруватдіоксигенази (HPPD) до сільськогосподарських культур, стійких до інгібіторів 4-гідроксифенілпіруватдіоксигенази. Сполуки за даним винаходом можуть бути, загалом, застосовані в комбінації з відомими гербіцидними антидотами, такими як беноксакор, бентіокарб, брасинолід, клоквінтоцет (мексил), ціометриніл, ципросульфамід, даімурон, дихлормід, дициклонон, діетолат, димепіперат, дисулфотон, фенхлоразол-етил, фенклорим, флуразол, флуксофенім, фурилазол, білок гарпін, ізоксадифен-етил, мефенпір-діетил, мефенат, MG 191, MON 4660, нафталіновий ангідрид (NA), оксабетриіл, R29148 і аміди N-фенілсульфонілбензойної кислоти, для збільшення їх селективності. Вони можуть бути додатково застосовані для боротьби з небажаною рослинністю в багатьох сільськогосподарських культурах, яким додали стійкість або 4 UA 108922 C2 5 10 15 20 25 30 35 40 45 50 55 60 резистентність до цих або інших гербіцидів шляхом генетичної модифікації або шляхом мутації і селекції. Наприклад, можна обробляти кукурудзу, пшеницю, рис, сою, цукровий буряк, бавовну, канолу і інші сільськогосподарські культури, яким додали стійкість або резистентність до сполук, які є інгібіторами ацетолактатсинтази у чутливих рослин. Багато які стійкі до гліфосату і глуфосинату сільськогосподарські культури можна також обробляти цими гербіцидами окремо або в комбінації. Деяким сільськогосподарським культурам додали стійкість до ауксинових гербіцидів і гербіцидів на основі АССази, таких як 2,4-(дихлорфеноксі)оцтова кислота (2,4-Д) і дикамба і арилоксифеноксипропіонати. Ці гербіциди можуть бути застосовані для обробки подібних стійких сільськогосподарських культур або інших стійких до ауксину сільськогосподарських культур. Деяким сільськогосподарським культурам додали стійкість до гербіцидів, інгібуючих 4-гідроксифенілпіруватдіоксигеназу, і ці гербіциди можуть бути застосовані для обробки подібних стійких сільськогосподарських культур. У той час як сполуки формули IA або IB можна напряму застосовувати як гербіциди, переважно їх застосування в сумішах, що містять гербіцидно ефективну кількість сполуки разом із щонайменше одним прийнятним з точки зору сільського господарства допоміжним засобом або носієм. Придатні допоміжні засоби або носії не повинні бути фітотоксичними для цінних сільськогосподарських культур, особливо, в концентраціях, які використовуються при застосуванні композицій для вибіркової боротьби з бур'янами в присутності сільськогосподарських культур, і не повинні реагувати хімічно із сполуками формули IA або IB або іншими інгредієнтами композиції. Такі суміші можуть бути розроблені для застосування безпосередньо до бур'янів або їх локусів або можуть являти собою концентрати або композиції, які, як правило, розбавляються додатковими носіями і допоміжними засобами перед застосуванням. Вони можуть являти собою тверді частинки, такі як, наприклад, пудри, гранули, дисперговані у воді гранули або змочувані порошки або рідини, такі як, наприклад, емульговані концентрати, розчини, емульсії або суспензії. Вони також можуть бути надані у вигляді готових сумішей або танкових сумішей. Придатні сільськогосподарські допоміжні засоби і носії, які є придатними при отриманні гербіцидних сумішей за даним винаходом, відомі фахівцям в галузі техніки. Деякі із цих допоміжних засобів включають, але не обмежені ними, концентрат олії сільськогосподарської культури (мінеральне масло (85%) + емульгатори (15%)); нонілфенолетоксилат; бензилкокоалкілдиметилову четвертинну амонієву сіль; суміш нафтових вуглеводнів, алкіловані складні ефіри, органічну кислоту і аніоногенну поверхнево-активну речовину; C9-C11алкілполіглікозид; фосфатований етоксилат спирту; етоксилат природного первинного спирту (C12-C16); блок-співполімер ди-втор-бутилфенол ЕО-ПО; полісилоксан-метилову кінцеву групу; нонілфенолетоксилат + сечовинно-амонієвий нітрат; емульгована метилована олія насіння; тридециловий спирт (синтетичний) етоксилат (8 ЕО); талового аміну етоксилат (15 ЕО); ПЕГ (400) діолеат-99. Рідкі носії, які можуть бути застосовані, включають водні і органічні розчинники. Застосовувані органічні розчинники, як правило, включають, але не обмежені ними, фракції нафти або вуглеводні, такі як мінеральне масло, ароматичні розчинники, парафінові масла і т. п.; рослинні олії, такі як соєва олія, ріпакова олія, оливкова олія, рицинова олія, олія насіння соняшнику, кокосова олія, кукурудзяна олія, бавовняна олія, льняна олія, пальмова олія, арахісова олія, сафлорова олія, кунжутна олія, тунгова олія і т. п.; складні ефіри вищезгаданих рослинних олій; складні ефіри одноатомних спиртів або двоатомних, триатомних або інших нижчих багатоатомних спиртів (які містять 4-6 гідроксильні групи), такі як 2-етилгексилстеарат, н-бутилолеат, ізопропілміристат, пропіленгліколю діолеат, діоктилсукцинат, дибутиладипат, діокілфталат і т. п.; складні ефіри моно-, ди- і полікарбонових кислот і т. п. Конкретні органічні розчинники включають толуол, ксилол, бензинолігроїнову фракцію, олію сільськогосподарської культури, ацетон, метилетилкетон, циклогексанон, трихлоретилен, перхлоретилен, етилацетат, амілацетат, бутилацетат, монометиловий ефір пропіленгліколю і монометиловий ефір діетиленгліколю, метиловий спирт, етиловий спирт, ізопропіловий спирт, аміловий спирт, етиленгліколь, пропіленгліколь, гліцерин, N-метил-2-піролідинон, N,N-диметилалкіламіди, диметилсульфоксид, рідкі добрива і т. п. Вода, загалом, є переважним носієм для розбавлення концентратів. Придатні тверді носії включають тальк, пірофілітову глину, кварц, атапульгітову глину, каолінову глину, кізельгур, крейду, діатоміт, вапно, карбонат кальцію, бентонітову глину, Фулерову землю, лушпиння насіння бавовнику, пшеничне борошно, соєве борошно, пемзу, деревне борошно, борошно зі шкаралупи волоського горіха, лігнін і т. п. Звичайно бажане включення одного або більше поверхнево-активних агентів в композиції за даним винаходом. Такі поверхнево-активні агенти вигідно застосовуються як в твердих, так і в 5 UA 108922 C2 5 10 15 20 25 30 35 40 45 50 рідких композиціях, особливо в таких, які розроблені для розбавлення носієм перед застосуванням. Поверхнево-активні агенти можуть бути аніоногенними, катіоногенними або неіоногенними за природою і можуть бути застосовані як емульгуючі агенти, змочувальні агенти, суспендуючі агенти або в інших цілях. Поверхнево-активні речовини, які традиційно застосовуються в галузі складання препаративних форм, і які також можуть бути застосовані в композиціях за даним винаходом, описані, inter alia, в "McCutcheon's Detergents and Emulsifiers Annual" MC Publishing Corp., Ріджвуд, Нью-Джерсі, 1998 і в "Encyclopedia of Surfactants" Том I-III, Chemical Publishing Co., Нью-Йорк, 1980-81. Типові поверхнево-активні агенти включають солі алкілсульфатів, такі як діетаноламонію лаурилсульфат; алкілурилсульфонатні солі, такі як додецилбензолсульфонат кальцію; продукти приєднання алкілфенолу і алкіленоксиду, такі як нонілфенол-С18-етоксилат; продукти приєднання спирту і алкіленоксиду, такі як тридециловий спирт-С16-етоксилат; мила, такі як стеарат натрію; алкілнафталенсульфонатні солі, такі як дибутил-нафталенсульфонат натрію; складні діалкілові ефіри сульфосукцинатних солей, такі як ди(2-етилгексил)сульфосукцинат натрію; складні ефіри сорбіту, такі як сорбітолеат; четвертинні аміни, такі як лаурилтриметиламонію хлорид; складні поліетиленгліколеві ефіри жирних кислот, такі як поліетиленглікольстеарат; блок-співполімери етиленоксиду і пропіленоксиду; солі складних моно- і діалкілових фосфатних ефірів; олії з рослин або насіння, такі як соєва олія, ріпакова/канолова олія, оливкова олія, рицинова олія, олія із насіння соняшнику, кокосова олія, кукурудзяна олія, бавовняна олія, льняна олія, пальмова олія, арахісова олія, сафлорова олія, кунжутна олія, тунгова олія і т. п.; і складні ефіри вищезгаданих рослинних олій, зокрема, складні метилові ефіри. Часто, деякі з цих матеріалів, такі як рослинні олії або олії з насіння і їх складні ефіри, можуть бути застосовані взаємозамінно як сільськогосподарський допоміжний засіб, як рідкий носій або як поверхнево-активний агент. Інші добавки, які, як правило, застосовуються в сільськогосподарських композиціях, включають агенти поліпшуючі сумісність, протиспінюючі агенти, зв’язувальні агенти, нейтралізуючі агенти і буфера, інгібітори корозії, фарби, віддушки, агенти, поліпшуючі розтікання, поліпшуючі проникнення, клейкі агенти, диспергуючі агенти, загусники, агенти, які знижують температуру замерзання, протимікробні агенти і т. п. Композиції також можуть містити інші сумісні компоненти, наприклад, інші гербіциди, регулятори росту рослин, фунгіциди, інсектициди і т. п., і можуть бути складені в композицію з рідкими добривами або твердими, дисперсними носіями добрив, такими як нітрат амонію, сечовина і т. п. Концентрація активних інгредієнтів в гербіцидних композиціях за даним винаходом, загалом, складає від 0,001 до 98 процентів за вагою. Часто застосовують концентрації від 0,01 до 90 процентів за вагою. У композиціях, розроблених для застосування у вигляді концентратів, активні інгредієнти, загалом, присутні в концентрації від 5 до 98 вагових процентів, переважно, 10-90 вагових процентів. Такі композиції, як правило, розбавляють інертним носієм, таким як вода, перед застосуванням. У розбавлених композиціях, які застосовуються, як правило, до бур'янів або їх локусів, загалом, вміст активного інгредієнта складає від 0,0001 до 1 вагового процента і переважно складає від 0,001 до 0,05 вагового процента. Композиції за даним винаходом можуть бути застосовані до бур'янів або їх локусів за допомогою традиційних наземних або повітряних розпилювачів, розбризкувачів і пристроїв внесення гранул шляхом внесення в іригаційну воду або воду для заливання в чеки і іншими традиційними засобами, відомими фахівцям в галузі техніки. Наступні приклади наведені для ілюстрації різних аспектів даного винаходу і не повинні бути розглянуті як обмежуючі формулу винаходи. Приклади Загальне: Мікрохвильове нагрівання проводили із застосуванням мікрохвильового реактора Biotage Initiator™. Реакції з мікрохвильовим нагріванням проводили в закритих реакторах з перемішуванням магнітною мішалкою і з контролем температури за допомогою інфрачервоного (ІЧ) датчика. Приклад 1. Отримання бензил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3-метоксифеніл)-5фторпіколінату (сполука 1) 6 UA 108922 C2 5 10 15 20 25 30 . До розчину 4-аміно-3-хлор-6-(4-хлор-2-фтор-3-метоксифеніл)-5-фторпіколінової кислоти (отриманої способами, описаними в патенті США 7314849 B2; 100 міліграм (мг), 0,29 мілімоль (ммоль) в тетрагідрофурані (ТГФ; 1 мілілітр (мл), додавали карбонілдіімідазол (51 мг, 0,32 ммоль). Реакційну суміш перемішували при температурі навколишнього середовища протягом 30 хвилин (хв.) до припинення виділення діоксиду вуглецю (CO 2). Додавали бензиловий спирт (62 мг, 0,58 ммоль), і реакційну суміш нагрівали в настільній мікрохвильовій печі при 90°С протягом 20 хвилин. Реакційну суміш очищали хроматографією на силікагелі (вводили безпосередньо в колонку RediSep® розміром 40 грам (г) Isco, із елююванням градієнтом 0-100% простого діетилового ефіру (Et2O) в гексані) із отриманням білої твердої речовини (147 мг, 78%): 1 температура плавлення 132-133°С, H-ЯМР (400 МГц, ДМСО-d6) δ 7,50-7,33 (м, 6H), 7,29 (дд, + J=8,5, 7,1 Гц, 1H), 7,13 (с, 2H), 5,37 (с, 2H), 3,92 (с, 3H); ESIMS m/z 439 ([M+Н] ). Приклад 2. Отримання 4-хлорбензил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3-метоксифеніл)-5фторпіколінату (сполука 2) . Суспензію 4-аміно-3-хлор-6-(4-хлор-2-фтор-3-метоксифеніл)-5-фторпіколінової кислоти (150 мг, 0,43 ммоль), 1-(бромметил)-4-метилбензолу (159 мг, 0,86 ммоль), карбонату калію (K2CO3; 118 мг, 0,86 ммоль) і іодиду натрію (NaI; 6 мг, 0,04 ммоль) в N,N-диметилформаміді (ДМФ; 1 мл) нагрівали в настільній мікрохвильовій печі при 100°С протягом 5 хвилин. Потім реакційну суміш розбавляли за допомогою Et2O, промивали сольовим розчином, висушували над сульфатом натрію (Na2SO4) і концентрували у вакуумі. Залишок очищали хроматографією на силікагелі (елюювали за допомогою градієнта 0-70% етилацетату (EtOAc)/гексан) з отриманням білої 1 твердої речовини (148 мг, 73%): температура плавлення 143°С; H-ЯМР (400 МГц, ДМСО-d6) δ 7,50-7,42 (м, 5H), 7,28 (дд, J=8,5, 7,1 Гц, 1H), 7,08 (с, 2H), 5,37 (с, 2H), 3,93 (д, J=0,8 Гц, 3H); + ESIMS m/z 475 ([M+Н] ). Сполуки 3-16 в таблиці 1 синтезували так, як в прикладі 2. Приклад 3. Отримання 2,4-дихлорбензил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3метоксифеніл)піколінату (сполука 17) . 4-Аміно-3-хлор-6-(4-хлор-2-фтор-3-метоксифеніл)піколінову кислоту (отриману способами, описаними в патенті США 7314849 B2; 828 мг, 2,5 ммоль) розчиняли в ДМФ (4 мл). Порціями додавали гідрид натрію (NaH, 60% дисперсія в мінеральному маслі; 154 мг, 3,85 ммоль). До 7 UA 108922 C2 5 10 15 20 25 30 35 суміші додавали 2,4-дихлор-1-(хлорметил)бензол (586 мг, 3,0 ммоль). Реакційну суміш залишали перемішуватися протягом 24 годин (год.). У реакційну суміш додавали воду, і водну фазу екстрагували за допомогою EtOAc (×3). Об'єднані органічні екстракти промивали сольовим розчином, висушували над Na2SO4, фільтрували і концентрували. Внаслідок очищення хроматографією з нормальними фазами отримували білу тверду речовину (440 мг, 35%): 1 температура плавлення 165-168°С, H-ЯМР (400 МГц, CDCl3) δ 7,68 (дд, J=8,6, 7,8 Гц, 1H), 7,54 (д, J=8,3 Гц, 1H), 7,43 (д, J=2,1 Гц, 1H), 7,28 (д, J=2,1 Гц, 1H), 7,23 (д, J=1,8 Гц, 1H), 7,21 (д, J=1,6 Гц, 1H), 5,50 (с, 2H), 4,83 (с, 2H), 3,97 (д, J=0,8 Гц, 3H); ESIMS m/z 489 ([M-H]). Сполуки 18 і 19 в таблиці 1 синтезували так, як в прикладі 3. Приклад 4. Отримання 4-трифторметоксибензил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3метоксифеніл)-5-фторпіколінату (сполука 20) . Суспензію 4-аміно-3-хлор-6-(4-хлор-2-фтор-3-метоксифеніл)-5-фторпіколінової кислоти (200 мг, 0,573 ммоль), 1-(бромметил)-4-(трифторметокси)бензолу (161 мг, 0,630 ммоль) і K2CO3 (119 мг, 0,859 ммоль) в ДМФ (2 мл) нагрівали при 50°С протягом ночі. Потім реакційну суміш концентрували під вакуумом. Залишок очищали хроматографією на силікагелі (елюювали градієнтом 0-80% EtOAc/гексан) з отриманням білої твердої речовини (154 мг, 51,4%): 1 температура плавлення 155-156°С; H-ЯМР (400 МГц, ДМСО-d6) δ 7,60 (д, J=8,7 Гц, 2H), 7,47 (дд, J=8,5, 1,5 Гц, 1H), 7,41 (д, J=8,0 Гц, 2H), 7,29 (дд, J=8,5, 7,1 Гц, 1H), 7,14 (с, 2H), 5,41 (с, 2H), + 3,95-3,90 (м, 3H); ESIMS m/z 523 ([M+Н] ), 521 ([M-H] ). Сполуки 21-34 в таблиці 1 синтезували так, як в прикладі 4. Приклад 5. Отримання бензил-6-аміно-2-(4-хлор-2-фтор-3-метоксифеніл)-5-вінілпіримідин-4карбоксилату (сполука 35) . 6-Аміно-2-(4-хлор-2-фтор-3-метоксифеніл)-5-вінілпіримідин-4-карбонову кислоту (отриману способами, описаними в патенті США 7786044 B2; 0,150 г, 0,463 ммоль), (бромметил)бензол (0,103 г, 0,602 ммоль) і карбонат літію (Li2CO3; 0,044 г, 0,602 ммоль) об'єднували в ДМФ (1,5 мл) і нагрівали при 60°С протягом ночі. Охолоджену реакційну суміш концентрували і потім розділяли між EtOAc і водою. Органічну фазу висушували, концентрували і очищали колонковою хроматографією (елюювали за допомогою градієнта EtOAc/гексани) з отриманням бензил-6-аміно-2-(4-хлор-2-фтор-3-метоксифеніл)-5-вінілпіримідин-4-карбоксилату у вигляді 1 білої твердої речовини (0,154 г, 80%): температура плавлення 119-121°С; H-ЯМР (400 МГц, CDCl3) δ 7,67 (дд, J=8,5, 7,5 Гц, 1H), 7,49-7,42 (м, 2H), 7,42-7,32 (м, 3H), 7,21 (дд, J=8,6, 1,7 Гц, 1H), 6,70 (дд, J=17,8, 11,6 Гц, 1H), 5,60 (дд, J=7,7, 1,0 Гц, 1H), 5,57 (с, 1H), 5,39 (с, 2H), 5,35 (с, + 2H), 4,00 (д, J=0,8 Гц, 3H); ESIMS m/z 414 ([M+Н] ). Приклад 6. Отримання 4-метоксибензил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3метоксифеніл)піколінату (сполука 36) 8 UA 108922 C2 5 10 15 20 25 30 . До розчину 4-аміно-3-хлор-6-(4-хлор-2-фтор-3-метоксифеніл)піколінової кислоти (600 мг, 1,81 ммоль) в ТГФ (10 мл) додавали трифенілфосфін (475 мг, 1,81 ммоль), діетилазодикарбоксилат (0,29 мл, 1,81 ммоль) і 4-метоксибензиловий спирт (0,34 мл, 2,72 ммоль). Реакційну суміш перемішували протягом 48 год. У реакційну суміш додатково додавали трифенілфосфін (475 мг, 1,81 ммоль) і перемішували протягом 24 год. Реакційну суміш концентрували досуха і очищали хроматографією на силікагелі (елюювали градієнтом 0-100% EtOAc/гексан) з отриманням не зовсім білої твердої речовини (170 мг, 26%): температура 1 плавлення 73-83°С; H-ЯМР (400 МГц, CDCl3) δ 7,66 (дд, J=8,6, 7,8 Гц, 1H), 7,45-7,38 (м, 2H), 7,22 (дд, J=8,7, 1,8 Гц, 1H), 7,16 (д, J=1,7 Гц, 1H), 6,94-6,87 (м, 2H), 5,38 (с, 2H), 4,80 (с, 2H), 3,96 + (д, J=0,8 Гц, 3H), 3,81 (с, 3H); ESIMS m/z 451 ([M+Н] ), 449 ([M-H] ). Сполуку 37 в таблиці 1 синтезували так, як в прикладі 6. Приклад 7. Отримання бензил-4-аміно-3-хлор-6-(2,4-дихлор-3-метоксифеніл)піколінату (сполука 38) . Метил-4-аміно-3-хлор-6-(2,4-дихлор-3-метоксифеніл)піколінат (сполука С, отримана способами, описаними в патенті США 7314849 B2; 500 мг, 1,4 ммоль) розчиняли в бензиловому спирті (10 мл), обробляли ізопропілатом титану(IV) (приблизно 100 мкл) і нагрівали при 85-90°С. Через 2 год. додавали ще порцію ізопропілату титану(IV) (100 мкл), і нагрівання продовжували ще протягом 18 год. Летючі компоненти видаляли під високим вакуумом, і залишок очищали хроматографією на силікагелі (елюювали 5% Et 2O - 30% дихлорметан (CH2Cl2) - 65% гексан). Речовину додатково очищали оберненофазовою високоефективною рідинною хроматографією (ОФ-ВЕРХ; елюювали 70% ацетонітрилом) із отриманням сполуки, вказаної в заголовку (375 мг, 1 61%): температура плавлення 107-108°С; H-ЯМР (400 МГц, CDCl3) δ 7,50-7,26 (м, 8H), 6,97 (с, + 1H), 5,42 (с, 2H), 4,85 (с, 2H), 3,91 (с, 3H); ESIMS m/z 437 ([M+Н] ). Сполуку 39 в таблиці 1 синтезували так, як в прикладі 7. Приклад 8. Отримання бензил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3-(1-фторетил)феніл)-5фторпіколінату (сполука 40) Стадія А. Метил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3-(1-фторетил)феніл)-5-фторпіколінат (сполука Н). 2-(4-Хлор-2-фтор-3-(1-фторетил)феніл)-4,4,5,5-тетраметил-1,3,2-діоксаборолан (510 мг, 1,7 ммоль, 1,0 еквівалент (екв.)) і метил-4-аміно-3,6-дихлор-5-фторпіколінат (отриманий 9 UA 108922 C2 5 10 15 20 25 30 35 40 45 50 способами, описаними в патенті США 6784137 B2; 400 мг, 1,7 ммоль, 1,0 екв.) послідовно додавали в посудину із мікрохвильовим опроміненням Biotage об'ємом на 5 мл з подальшим додаванням фториду цезію (CsF; 510 мг, 3,3 ммоль, 2,0 екв.), ацетату паладію(II) (19 мг, 0,084 ммоль, 0,05 екв.) і 3,3',3''-фосфінтриїлтрибензолсульфонату натрію (95 мг, 0,17 ммоль, 0,10 екв.). Додавали суміш вода-ацетонітрил 3:1 (3,2 мл), і отриману коричневу суміш нагрівали в настільній мікрохвильовій печі при 150°С протягом 5 хвилин. Охолоджену реакційну суміш розбавляли водою (150 мл) і екстрагували за допомогою CH2Cl2 (4×50 мл). Об'єднані органічні екстракти висушували над сульфатом магнію (MgSO 4), безнапорно фільтрували і концентрували на роторному випарнику. Залишок очищали оберненофазовою колонковою хроматографією (елюювали за допомогою градієнта ацетонітрилу від 5% до 100%) з отриманням необхідного продукту, метил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3-(1фторетил)феніл)-5-фторпіколінату у вигляді жовто-коричневої напівтвердої речовини (220 мг, -1 1 35%): ІЧ (тонкоплівковий) 3475, 3353 (м), 3204, 3001, 2955, 1738 (с), 1711 (с), 1624 (с) см ; HЯМР (300 МГц, CDCl3) δ 7,50 (м, 1H), 7,30 (м, 1H), 7,21 (д, J=2 Гц, 1H), 6,16 (дкв, J=46, 7 Гц, 1H), + 4,96 (ушир.с, 2H), 3,97 (с, 3H), 1,75 (дд, J=23, 7 Гц, 3H); ESIMS m/z 379 ([M+Н] ). Стадія В. 4-Аміно-3-хлор-6-(4-хлор-2-фтор-3-(1-фторетил)феніл)-5-фторпіколінова кислота. 2 Молярний (M) розчин гідроксиду натрію у воді (NaOH; 580 мкл, 1,2 ммоль, 4,0 екв.) додавали до перемішуваної суспензії метил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3-(1-фторетил)феніл)-5фторпіколінату (110 мг, 0,29 ммоль, 1,0 екв.) в метиловому спирті (1,9 мл) при 23°С. Отриманий світло-жовтий гомогенний розчин перемішували при 23°С протягом 20 год. Реакційну суміш доводили до приблизно pH=4 шляхом додавання по краплях концентрованої соляної кислоти (HCl) і концентрували на роторному випарнику. Залишок суспендували у воді і фільтрували з вакуумним насосом з отриманням необхідного продукту, 4-аміно-3-хлор-6-(4-хлор-2-фтор-3-(1фторетил)феніл)-5-фторпіколінової кислоти у вигляді білого порошку (55 мг, 50%): ІЧ -1 1 (тонкоплівковий) 3319 (м), 3193, 2983, 1719 (м), 1629 (с) см ; H-ЯМР (300 МГц, ДМСО-d6) δ 7,58 (т, J=9 Гц, 1H), 7,49 (д, J=9 Гц, 1H), 6,99 (ушир.с, 2H), 6,15 (дкв, J=44, 7 Гц, 1H), 1,71 (дд, J=23, 7 + Гц, 3H); ESIMS m/z 365 ([M+Н] ). Стадія С. Бензил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3-(1-фторетил)феніл)-5-фторпіколінат. Триетиламін (190 мкл, 1,4 ммоль, 2,0 екв.) і бензилбромід (120 мкл, 1,0 ммоль, 1,5 екв.) послідовно додавали до переміщуваного розчину 4-аміно-3-хлор-6-(4-хлор-2-фтор-3-(1фторетил)феніл)-5-фторпіколінової кислоти (0,25 г, 0,69 ммоль, 1,0 екв.) в ТГФ (3,4 мл) при 23°С. Отриманий блідий світло-жовтий розчин перемішували при 23°С протягом 18 год. Реакційну суміш розбавляли водою (150 мл) і екстрагували за допомогою CH 2Cl2 (3×70 мл). Об'єднані органічні шари висушували (MgSO4), безнапорно фільтрували і концентрували на роторному випарнику. Залишок очищали оберненофазовою колонковою хроматографією (елюювали за допомогою градієнта ацетонітрилу від 5% до 100%) з отриманням необхідного продукту, бензил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3-(1-фторетил)феніл)-5-фторпіколінату у вигляді жовтої напівтвердої речовини (160 мг, 52%): ІЧ (тонкоплівковий) 3485 (м), 3393 (м), 3196, -1 1 3035, 2983, 1737 (с), 1622 (с) см ; H-ЯМР (300 МГц, CDCl3) δ 7,23-7,57 (м, 7H), 6,18 (дкв, J=45, 6 + Гц, 1H), 5,45 (с, 2H), 4,94 (ушир.с, 2H), 1,78 (ддд, J=23, 7, 1 Гц, 3H); ESIMS m/z 453 ([M+Н] ). Приклад 9. Отримання бензил-4-аміно-3-хлор-6-(4-хлор-3-етокси-2-фторфеніл)-5фторпіколінату (сполука 41) . Стадія А. Метил-4-аміно-3-хлор-6-(4-хлор-3-етокси-2-фторфеніл)-5-фторпіколінат (сполука А). 2-(4-Хлор-3-етокси-2-фторфеніл)-4,4,5,5-тетраметил-1,3,2-діоксаборолан (500 мг, 1,7 ммоль, 1,0 екв.) і метил-4-аміно-3,6-дихлор-5-фторпіколінат (400 мг, 1,7 ммоль, 1,0 екв.) послідовно додавали в ємність для мікрохвильової печі Biotage об'ємом на 5 мл, з подальшим додаванням CsF (510 мг, 3,3 ммоль, 2,0 екв.), ацетату паладію(II) (19 мг, 0,084 ммоль, 0,05 екв.) і 3,3',3''фосфінтриїлтрибензолсульфонату натрію (95 мг, 0,17 ммоль, 0,10 екв.). Додавали суміш водаацетонітрил 3:1 (3,2 мл), і отриману коричневу суміш нагрівали в настільній мікрохвильовій печі 10 UA 108922 C2 5 10 15 20 25 30 35 40 45 50 при 150°С протягом 5 хвилин. Охолоджену реакційну суміш розбавляли водою (150 мл) і екстрагували за допомогою CH2Cl2 (4×50 мл). Об'єднані органічні екстракти висушували (MgSO4), безнапорно фільтрували і концентрували на роторному випарнику. Залишок очищали колонковою хроматографією силікагелю (елюювали 33% EtOAc/гексан) з отриманням необхідного продукту, метил-4-аміно-3-хлор-6-(4-хлор-3-етокси-2-фторфеніл)-5-фторпіколінату у вигляді жовто-коричневого порошку (450 мг, 63%): температура плавлення 170-172°С; ІЧ -1 1 (тонкоплівковий) 3485 (м), 3380 (с), 2951, 1739 (с), 1610 (с) см ; H-ЯМР (300 МГц, CDCl3) δ 7,207,30 (м, 2H), 4,95 (ушир.с, 2H), 4,19 (кв, J=7 Гц, 2H), 3,98 (с, 3H), 1,43 (т, J=7 Гц, 3H); ESIMS m/z + 377 ([M+Н] ). Стадія В. 4-Аміно-3-хлор-6-(4-хлор-3-етокси-2-фторфеніл)-5-фторпіколінова кислота. 2 М розчин водного NaOH (900 мкл, 1,8 ммоль, 4,0 екв.) додавали до перемішуваної суспензії метил-4-аміно-3-хлор-6-(4-хлор-3-етокси-2-фторфеніл)-5-фторпіколінату (170 мг, 0,45 ммоль, 1,0 екв.) в метиловому спирті (3,0 мл) при 23°С. Отриману гетерогенну білу суміш перемішували при 23°С протягом 4 год. Реакційну суміш доводили до приблизно pH=4 шляхом додавання по краплях концентрованої HCl і потім концентрували на роторному випарнику. Залишок суспендували у воді і фільтрували з вакуумним насосом з отриманням необхідного продукту, 4аміно-3-хлор-6-(4-хлор-3-етокси-2-фторфеніл)-5-фторпіколінової кислоти у вигляді білого порошку (140 мг, 88%): температура плавлення 163-165°С; ІЧ (тонкоплівковий) 3486 (м), 3377 -1 1 (с), 3155, 2981, 2935, 1718 (с), 1614 (с) см ; H-ЯМР (300 МГц, ДМСО-d6) δ 7,45 (дд, J=9, 2 Гц, 1H), 7,28 (дд, J=9, 7 Гц, 1H), 7,01 (ушир.с, 2H), 4,15 (кв, J=7 Гц, 2H), 1,33 (т, J=7 Гц, 3H); ESIMS + m/z 363 ([M+Н] ). Стадія С. Бензил-4-аміно-3-хлор-6-(4-хлор-3-етокси-2-фторфеніл)-5-фторпіколінат. Триетиламін (290 мкл, 2,1 ммоль, 2,0 екв.) і бензилбромід (190 мкл, 1,6 ммоль, 1,5 екв.) послідовно додавали до перемішуваного розчину 4-аміно-3-хлор-6-(4-хлор-3-етокси-2фторфеніл)-5-фторпіколінової кислоти (0,38 г, 1,1 ммоль, 1,0 екв.) в ТГФ (7,0 мл) при 23°С. Отриманий блідо-коричневий розчин перемішували при 23°С протягом 18 год. Реакційну суміш розбавляли водою (150 мл) і екстрагували за допомогою CH2Cl2 (3×70 мл). Об'єднані органічні екстракти висушували (MgSO4), безнапорно фільтрували і концентрували на роторному випарнику. Залишок очищали за допомогою ОФ-ВЕРХ (елюювали за допомогою градієнта ацетонітрилу від 5% до 100%) з отриманням необхідного продукту, бензил-4-аміно-3-хлор-6-(4хлор-3-етокси-2-фторфеніл)-5-торпіколінату у вигляді білого порошку (230 мг, 49%): температура плавлення 122-124°С; ІЧ (тонкоплівковий) 3477 (с), 3372 (с), 3194, 3036, 2992 (м), -1 1 2943, 2900, 1729 (с), 1616 (с) см ; H-ЯМР (300 МГц, CDCl3) δ 7,49-7,32 (м, 5H), 7,29-7,21 (м, 2H), + 5,43 (с, 2H), 4,91 (ушир.с, 2H), 4,19 (кв, J=7 Гц, 2H), 1,43 (т, J=7 Гц, 3H); ESIMS m/z 453 ([M+Н] ), Приклад 10. Отримання бензил-4-аміно-3-хлор-6-(4-циклопропілфеніл)-5-фторпіколінату (сполука 42) . Стадія А. Етил-4-аміно-3-хлор-6-(4-циклопропілфеніл)-5-фторпіколінат. 4Циклопропілфенілборонову кислоту (250 мг, 1,5 ммоль, 1,2 екв.) і метил-4-аміно-3,6-дихлор-5фторпіколінат (300 мг, 1,3 ммоль, 1,0 екв.) послідовно додавали в ємність для мікрохвильової печі Biotage об'ємом на 5 мл з подальшим додаванням CsF (380 мг, 2,5 ммоль, 2,0 екв.), ацетату паладію(II) (14 мг, 0,063 ммоль, 0,05 екв.) і 3,3',3''-фосфінтриїлтрибензолсульфонату натрію (71 мг, 0,13 ммоль, 0,10 екв.). Додавали суміш 3:1 вода-ацетонітрил (2,5 мл), і отриману коричневу суміш нагрівали в настільній мікрохвильовій печі при 150°С протягом 5 хвилин. Охолоджену реакційну суміш розбавляли водою (150 мл) і екстрагували за допомогою CH 2Cl2 (4×50 мл). Об'єднані органічні екстракти висушували (MgSO4), безнапорно фільтрували і концентрували на роторному випарнику. Залишок очищали за допомогою ОФ-ВЕРХ (елюювали за допомогою градієнта ацетонітрилу від 5% до 100%) з отриманням необхідного продукту, метил-4-аміно-3-хлор-6-(4-циклопропілфеніл)-5-фторпіколінату у вигляді білого порошку (310 мг, 78%): температура плавлення 116-119°С; ІЧ (тонкоплівковий) 3475 (с), 3357 (с), 3089, 3013, -1 1 2954, 1724 (м), 1607 (м) см ; H-ЯМР (300 МГц, CDCl3) δ 7,81 (м, 2H), 7,15 (м, 2H), 4,85 (ушир.с, + 2H), 3,98 (с, 3H), 1,94 (м, 1H), 1,01 (м, 2H), 0,74 (м, 2H); ESIMS m/z 321 ([M+Н] ). 11 UA 108922 C2 5 10 15 20 25 30 35 40 45 50 Стадія В. 4-Аміно-3-хлор-6-(4-циклопропілфеніл)-5-фторпіколінова кислота. 2 М розчин водного NaOH (600 мкл, 1,2 ммоль, 2,0 екв.) додавали до перемішуваної суспензії метил-4аміно-3-хлор-6-(4-циклопропілфеніл)-5-фторпіколінату (190 мг, 0,59 ммоль, 1,0 екв.) в метиловому спирті (3,0 мл) при 23°С. Отриману гетерогенну білу суміш перемішували при 23°С протягом 3 год. Реакційну суміш доводили до приблизно pH=4 шляхом додавання по краплях концентрованої HCl і потім концентрували на роторному випарнику. Залишок суспендували у воді і фільтрували з вакуумним насосом з отриманням необхідного продукту, 4-аміно-3-хлор-6(4-циклопропілфеніл)-5-фторпіколінової кислоти у вигляді білого порошку (170 мг, з виходом 94%): температура плавлення 147-149°С; ІЧ (тонкоплівковий) 3463 (с), 3339 (с), 3202 (м), 3084, -1 1 3007, 1721 (м), 1630 (с) см ; H-ЯМР (300 МГц, ДМСО-d6) δ 7,70 (м, 2H), 7,17 (м, 2H), 6,81 + (ушир.с, 2H), 1,96 (м, 1H), 0,99 (м, 2H), 0,71 (м, 2H); ESIMS m/z 307 ([M+Н] ). Стадія С. Бензил-4-аміно-3-хлор-6-(4-циклопропілфеніл)-5-фторпіколінат. Триетиламін (220 мкл, 1,6 ммоль, 2,0 екв.) і бензилбромід (140 мкл, 1,2 ммоль, 1,5 екв.) послідовно додавали до переміщуваного розчину 4-аміно-3-хлор-6-(4-хлор-3-етокси-2-фторфеніл)-5-фторпіколінової кислоти (0,24 г, 0,78 ммоль, 1,0 екв.) в ТГФ (5,2 мл) при 23°С. Отриманий блідий світло-жовтий розчин перемішували при 23°С протягом 72 год. Реакційну суміш розбавляли водою (150 мл) і екстрагували за допомогою CH2Cl2 (3×70 мл). Об'єднані органічні екстракти висушували (MgSO4), безнапорно фільтрували і концентрували на роторному випарнику. Залишок очищали за допомогою ОФ-ВЕРХ (елюювали за допомогою градієнта ацетонітрилу від 5% до 100%) з отриманням необхідного продукту, бензил-4-аміно-3-хлор-6-(4-циклопропілфеніл)-5фторпіколінату у вигляді білого порошку (180 мг, 58%): температура плавлення 129-131°С; ІЧ -1 1 (тонкоплівковий) 3389 (с), 3229, 3194, 3083, 3068, 3033, 3008, 1737 (с), 1616 (с) см ; H-ЯМР (300 МГц, CDCl3) δ 7,83 (м, 2H), 7,48 (м, 2H), 7,33-7,42 (м, 3H), 7,15 (м, 2H), 5,43 (с, 2H), 4,82 + (ушир.с, 2H), 1,94 (м, 1H), 1,01 (м, 2H), 0,75 (м, 2H); ESIMS m/z 497 ([M+Н] ). Приклад 11: Отримання бензил-4-аміно-3-бром-6-(4-хлор-2-фтор-3-метоксифеніл)-5фторпіколінату (сполука 43) . Стадія А. Суміш метил-4,5,6-трихлорпіколінату (отриманого способами, описаними в патенті США 6784137 B2; 25 г, 0,10 моль (моль) і бензилового спирту (100 г, 0,2 моль) в тригорловій круглодонній колбі на 250 мл нагрівали в атмосфері азоту при 100°С. Додавали ізопропілат титану (0,6 г, 0,02 моль). Через 4 год. при 100°С майже безбарвний розчин охолоджували і переносили в одногорлову круглодонну колбу на 250 мл. Надлишок бензилового спирту видаляли під вакуумом з отриманням майже білої твердої речовини (31 г, 94%): температура 1 плавлення 125-126,5°С; H-ЯМР (400 МГц, CDCl3) δ 8,08 (с, 1H, пірідин Н), 7,42 (м, 2H, феніл), 13 1 7,31 (м, 3H, феніл), 5,40 (с, 2H, CH2Ph); C{ H}-ЯМР (101 МГц, CDCl3) δ 162,0 (CO2R), 150,4, 145,0, 144,9, 134,7, 133,1, 128,3 (феніл CH), 125,4 (пірідин CH), 67,88 (CH 2Ph). Стадія В. Тригорлову колбу на 250 мл, обладнану зворотним холодильником і входом для подачі азоту (N2), заповнювали бензил-4,5,6-трихлорпіколінатом (17,77 г, 56,10 ммоль), 2-(4хлор-2-фтор-3-метоксифеніл)-1,3,2-діоксаборинаном (19,20 г, 79,0 ммоль) і CsF (17,04 г, 112,0 ммоль). Додавали ацетонітрил (100 мл) і воду (30 мл). Атмосферу над реакційною сумішшю розряджали за допомогою вакуумного насоса/заповнювали N 2 (5×). Додавали твердий дихлорбіс(трифенілфосфін)паладій(II) (Pd(PPh 3)2Cl2; 1,724 г, 2,456 ммоль). Атмосферу над розчином розряджали за допомогою вакуумного насоса/заповнювали N 2 (5×) і потім перемішували із зворотним холодильником протягом 90 хвилин. При охолоджуванні до кімнатної температури випадав білий твердий осад. Тверду речовину фільтрували, промивали 1 водою і висушували на повітрі (18,66 г, 75%): H-ЯМР (400 МГц, CDCl3) δ 8,23 (с, 1H, пірідин Н), 7,52-7,32 (м, 5H, феніл), 7,27 (дд, JH-H=8,4 Гц, JF-H=1,7 Гц, 1H, ароматичного ряду), 7,10 (дд, JHH=8,4 Гц, JF-H=6,8 Гц, 1H, ароматичного ряду), 5,44 (с, 2H, CH 2Ph), 3,98 (д, JF-H=1,3 Гц, 3H, OMe); 13 1 C{ H}-ЯМР (101 МГц, CDCl3) δ 163,0, 153,7, 153,5 (д, JF-C=253 Гц, C2'), 146,0, 144,5 (д, JF-C=13 Гц), 144,1, 135,0, 134,2, 129,9 (д, JF-C=3 Гц), 128,5, 126,1, 125,8 (д, JF-C=14 Гц), 125,3 (д, JF-C=3 Гц), 124,9 (д, JF-C=2 Гц), 67,9 (CH2), 61,5 (д, JF-C=4 Гц, OMe), Аналітично розраховано для C20H13Cl3FNO3: С, 54,51; Н, 2,97; N, 3,18; виявлено: С, 54,60; Н, 3,08; N, 3,16. 12 UA 108922 C2 5 10 15 20 25 30 35 40 45 Стадія С. Тригорлова колба на 250 мл була обладнана дефлегматором, входом для N 2, механічною мішалкою і термопарою. Колбу заповнювали CsF (21,07 г, 139,0 ммоль). Додавали безводний ДМСО (100 мл), і над суспензією атмосферу за допомогою вакуумного насоса розряджали/заповнювали N2 (5×). Суспензію нагрівали при 80°С протягом 30 хвилин, ДМСО (30 мл) відганяли під вакуумом для видалення будь-якої залишкової води. Додавали твердий бензил-4,5-дихлор-6-(4-хлор-2-фтор-3-метоксифеніл)піколінат (15,34 г, 34,8 ммоль) і атмосферу над розчином розряджали за допомогою вакуумного насоса/заповнювали N 2 (5×). Реакційну суміш нагрівали до 105°С в атмосфері N2. Через 6 год. при 105°С аналіз аліквоти зразка шляхом ГХ не показував піка для монофторозаміщеного проміжного продукту. Реакційну суміш залишали охолоджуватися до кімнатної температури. Реакційну суміш виливали у воду з льодом (400 г) і екстрагували за допомогою EtOAc (3×200 мл). Об'єднані органічні екстракти промивали насиченим (насищ.) розчином NaHCO 3, водою (5×100 мл) і сольовим розчином. Екстракти висушували (MgSO4) і концентрували при зниженому тиску з отриманням жовтокоричневої твердої речовини (12,97 г). Тверду речовину очищали за допомогою флешхроматографії (330 г колонка із силікагелем; градієнт EtOAc 0-20%) з отриманням білої твердої 1 речовини (9,95 г; 70%): температура плавлення 114-116°С; H-ЯМР (400 МГц, CDCl3) δ 8,01 (дд, JF-H=9,4, 5,5 Гц, 1H, пірідин Н), 7,53-7,20 (м, 7H, феніл), 5,44 (с, 2H, CH2Ph), 3,99 (д, JF-H=1,2 Гц, 13 3H, OMe); C-ЯМР (101 МГц, CDCl3) δ 162,8 (д, JF-C=3 Гц, CO2Bn), 156,2 (дд, JF-C=267, 12 Гц), 153,9 (д, JF-C=255 Гц), 148,0 (дд, JF-C=269, 11 Гц), 145,4 (т, JF-C=7 Гц), 144,7 (д, JF-C=13 Гц), 144,6 (дд, JF-C=13, 2 Гц), 135,2 (с), 130,6 (д, JF-C=3 Гц), 125,6 (д, JF-C=4 Гц), 125,4 (д, JF-C=2 Гц), 122,0 (д, 19 1 JF-C=14 Гц), 115,0 (д, JF-C=16 Гц), 67,9 (с, CH2Ph), 61,6 (д, JF-C=5 Гц, OMe); F{ H}-ЯМР (376 МГц, CDCl3) δ -123,90 (д, JF-F=19,7 Гц, F4), -128,37 (д, JF-F=33,5 Гц, F2'), -139,64 (дд, JF-F=33,5, 19,7 Гц, F5), Аналітично розраховано для C20H13ClF3NO3: С, 58,91; Н, 3,21; N, 3,43; виявлено: С, 59,03; Н, 3,20; N, 3,39. Стадія D. Бензил-4,5-дифтор-6-(4-хлор-2-фтор-3-метоксифеніл)піколінат (4,99 г, 12,2 ммоль) суспендували в ДМСО (100 мл). Аміак барботували через розчин протягом 30 хвилин. Після перемішування протягом ночі, реакційну суміш виливали у воду з льодом (500 мл). Продукт екстрагували в EtOAc (3×150 мл). Об'єднані органічні екстракти промивали водою (5×100 мл) і сольовим розчином, висушували (MgSO4) і концентрували при зниженому тиску з отриманням 1 білої твердої речовини (4,99 г, 101%); H-ЯМР (400 МГц, CDCl3) δ 7,52 (д, JF-H=6,5 Гц, 1H, пірідин H3), 7,45-7,38 (м, 2H), 7,37-7,17 (м, 5H), 5,38 (с, 2H, CH2Ph), 4,67 (ушир.с, 2Н, NH2), 3,94 (д, JF13 1 С{ H}-ЯМР (101 МГц, CDCl3) 164,4 (CO2R), 153,9 (д, JF-C=254 Гц), 147,6 (д, H=1,1 Гц, 3H, OMe); JF-C=256 Гц), 144,4 (д, JF-C=14 Гц), 144,0 (д, JF-C=5 Гц), 142,2 (д, JF-C=12 Гц), 140,4 (д, JF-C=15 Гц), 135,6 (с), 129,5 (д, JF-C=3 Гц), 128,5 (CH), 128,3 (CH), 128,3 (CH), 125,6 (д, J F-C=3 Гц, CH), 125,2 (д, JF-C=4 Гц, CH), 123,3 (дд, JF-C=14, 4 Гц), 113,1 (д, JF-C=4 Гц, C3), 67,3 (с, CH2Ph), 61,5 (д, JF-C=4 19 1 Гц, OMe); F{ H}-ЯМР (376 МГц, CDCl3) δ -128,54 (дд, J=30,7, 5,2 Гц, F2'), -141,84 (дд, J=30,8, + 6,5 Гц, F5), HRMS-ESI (m/z) [М] розраховано для C20H15ClF2N2O3 404,0739; виявлено 404,0757. Стадія Е. N-бромсукцинімід (NBS; 580 мг, 3,3 ммоль, 1,1 екв.) додавали до перемішуваної суспензії бензил-4-аміно-6-(4-хлор-2-фтор-3-метоксифеніл)-5-фторозаміщеного піколінату (1,2 г, 3,0 ммоль, 1,0 екв.) в 1,2-дихлоретані (15 мл) при 23°С. Отриману яскраво-жовту суміш перемішували при 23°С протягом 72 год. Коричневу реакційну суміш концентрували в потоку N 2, і залишок очищали колонковою хроматографією із силікагелем (елюювали 29% EtOAc/гексан) з отриманням необхідного продукту, бензил-4-аміно-3-бром-6-(4-хлор-2-фтор-3-метоксифеніл)-5фторпіколінату, у вигляді жовто-коричневого порошку (1,3 г, 93%): температура плавлення 144-1 146°С; ІЧ (тонкоплівковий) 3370 (с), 3225, 3190, 3093, 3066, 3037, 2948, 1731 (с), 1616 (с) см ; 1 H-ЯМР (400 МГц, CDCl3) δ 7,47 (м, 2H), 7,41-7,33 (м, 3H), 7,26-7,22 (м, 2H), 5,42 (с, 2H), 4,98 + (ушир.с, 2H), 3,96 (д, J=1 Гц, 3H); ESIMS m/z 485 ([M+Н] ). Приклад 12: Отримання (Е)-бензил-4-аміно-6-(4-хлор-2-фтор-3-метоксифеніл)-3-(2хлорвініл)-5-фторпіколінату (сполука 44) . 50 13 UA 108922 C2 5 10 15 20 25 30 35 Стадія А. Гідрид трибутилолова (2,0 мл, 7,3 ммоль, 1,0 екв.) і етинілтриметилсилан (2,1 мл, 15 ммоль, 2,0 екв.) об'єднували, додавали 2,2'-азобіс-(2-метилпропіонітрил) (AIBN; 60 мг, 0,36 ммоль, 0,05 екв.), і отриманий безбарвний бездомішковий розчин нагрівали до 80°С. При нагріванні спостерігали екзометермічну реакцію, яка підвищувала температуру до ~110°С. Реакційну суміш охолоджували зворотно до 80°С і перемішували протягом 20 год. Реакційну суміш охолоджували до 23°С з отриманням необхідного сирого продукту, (Е)-триметил(2(трибутилстаніл)вініл)силану, у вигляді блідо-жовтого масла (2,8 г, вихід сирого продукту 99%): 1 H-ЯМР (400 МГц, CDCl3) δ 6,96 (д, J=22,5 Гц, 1H), 6,60 (д, J=22,5 Гц, 1H), 1,54-1,44 (м, 6H), 1,351,23 (м, 6H), 0,91-0,82 (м, 15H), 0,03 (с, 9H). Стадія В. (Е)-Триметил(2-(трибутилстаніл)вініл)силан (1,1 г, 2,7 ммоль, 1,1 екв.) додавали до перемішуваної суміші бензил-4-аміно-3-бром-6-(4-хлор-2-фтор-3-метоксифеніл)-5фторпіколінату (сполука 43; 1,2 г, 2,5 ммоль, 1,0 екв.) і тетракіс(трифенілфосфін)паладію(0) (290 мг, 0,25 ммоль, 0,10 екв.) в ДМФ (8,3 мл) при 23°С. Реакційну суміш нагрівали до 90°С з отриманням гомогенного темно-жовтого розчину, і реакційну суміш перемішували протягом 20 год. Охолоджену реакційну суміш розбавляли водою (400 мл) і екстрагували за допомогою Et 2O (4×100 мл). Органічний шар висушували (MgSO 4), безнапорно фільтрували і концентрували на роторному випарнику. Залишок очищали оберненофазовою колонковою хроматографією (градієнтом від 5% ацетонітрилу до 100% ацетонітрилу) з отриманням необхідного продукту, (Е)-бензил-4-аміно-6-(4-хлор-2-фтор-3-метоксифеніл)-5-фтор-3-(2(триметилсиліл)вініл)піколінату, у вигляді світло-коричневого масла (460 мг, 38%): ІЧ -1 1 (тонкоплівковий) 3483, 3376 (м), 3206, 3069, 2955 (с), 2897, 1732 (с), 1619 (с) см ; H-ЯМР (400 МГц, CDCl3) δ 7,44-7,27 (м, 7H), 6,94 (д, J=20 Гц, 1H), 6,28 (д, J=20 Гц, 1H), 5,33 (с, 2H), 4,62 + (ушир.с, 2H), 3,95 (д, J=1 Гц, 3H), 0,09 (с, 9H); ESIMS m/z 503 ([M+Н] ). Стадія С. N-Хлорсукцинімід (NCS; 190 мг, 1,4 ммоль, 2,0 екв.), додавали до перемішуваного розчину (Е)-бензил-4-аміно-6-(4-хлор-2-фтор-3-метоксифеніл)-5-фтор-3-(2(триметилсиліл)вініл)піколінату (350 мг, 0,70 ммоль, 1,0 екв.) в ДМФ (7,0 мл) при 23°С. Гомогенний блідо-зелений розчин нагрівали до 50°С і перемішували протягом 24 год. Охолоджену реакційну суміш розбавляли водою (400 мл) і екстрагували за допомогою Et 2O (4×100 мл). Об'єднані органічні шари висушували (MgSO 4), безнапорно фільтрували і концентрували на роторному випарнику. Залишок очищали оберненофазовою колонковою хроматографією (градієнт від 5% ацетонітрилу до 100% ацетонітрилу) з отриманням необхідного продукту, (Е)-бензил-4-аміно-6-(4-хлор-2-фтор-3-метоксифеніл)-3-(2-хлорвініл)-5фторпіколінату, у вигляді жовто-коричневого порошку (70 мг, з виходом 22%): температура плавлення 133-135°С; ІЧ (тонкоплівковий) 3486 (с), 3345 (с), 3215, 3069, 3037, 2953, 1719 (с), -1 1 1616 (с) см ; H-ЯМР (400 МГц, CDCl3) δ 7,47-7,43 (м, 2H), 7,41-7,33 (м, 3H), 7,27 (м, 2H), 6,89 (д, J=14 Гц, 1H), 6,45 (д, J=14 Гц, 1H), 5,37 (с,2H), 4,62 (ушир.с, 2H), 3,97 (д, J=1 Гц, 3H); ESIMS m/z + 465 ([M+Н] ). 14 UA 108922 C2 Таблиця 1 Структури сполук в прикладах 15 UA 108922 C2 16 UA 108922 C2 17 UA 108922 C2 18 UA 108922 C2 19 UA 108922 C2 20 UA 108922 C2 Таблиця 2 Аналітичні дані для сполук в таблиці 1 1 Номер сполуки Зовнішній вигляд Т.пл. (°С) ESIMS m/z 3 Біла тверда речовина 139 453 ([M+Н] ) + 21 H-ЯМР (напруженість поля, розчинник) (400 MГц, ДМСО-d6) δ 7,45 (дд, J=8,5, 1,6 Гц, 1H), 7,34 (д, J=8,0 Гц, 2H), 7,28 (дд, J=8,5, 7,1 Гц, 1H), 7,20 (д, J=7,9 Гц, 2H), 7,07 (с, 2H), 5,32 (с, 2H), 3,92 (д, J=0,8 Гц, 3H), 2,30 (с, 3H) Інші дані ЯМР UA 108922 C2 Продовження таблиці 2 1 Номер сполуки Зовнішній вигляд Т.пл. (°С) ESIMS m/z 4 Біла тверда речовина 151 464 ([M+Н] ) 5 Біла тверда речовина 183-184 469 ([M+Н] ), 467 ([M-H] ) 6 Біла тверда речовина 118-119 507 ([M+Н] ), 505 ([M-H] ) 7 Жовта тверда речовина 170-175 449 ([M+Н] ), 447 ([M-H] ) 8 Біла тверда речовина 135 453 ([M+Н] ), 451 ([M-H] ) 9 Біла тверда речовина 183-184 474 ([M+Н] ), 472 ([M-H] ) 10 Біла тверда речовина 135-136 469 ([M+Н] ) + + + + + + + 22 H-ЯМР (напруженість поля, розчинник) (400 MГц, ДМСО-d6) δ 7,92-7,84 (м, 2H), 7,65 (д, J=8,5 Гц, 2H), 7,47 (дд, J=8,5, 1,6 Гц, 1H), 7,30 (дд, J=8,5, 7,1 Гц, 1H), 7,10 (с, 2H), 5,48 (с, 2H), 3,93 (д, J=0,9 Гц, 3H) (400 MГц, ДМСО-d6) δ 7,43 (д, J=8,4 Гц, 1H), 7,29-7,12 (м, 4H), 6,88 (д, J=8,7 Гц, 2H), 4,59 (д, J=4,4 Гц, 2H), 3,90 (с, 3H), 3,71 (с, 3H) (400 MГц, ДМСО-d6) δ 7,79 (д, J=8,2 Гц, 2H), 7,68 (д, J=8,1 Гц, 2H), 7,47 (дд, J=8,5, 1,5 Гц, 1H), 7,31 (дд, J=8,5, 7,1 Гц, 1H), 7,15 (с, 2H), 5,49 (с, 2H), 3,93 (д, J=0,7 Гц, 3H) (400 MГц, CDCl3) δ 8,037,94 (м, 2H), 7,70-7,59 (м, 2H), 7,51 (дд, J=10,6, 4,8 Гц, 2H), 7,22 (дд, J=7,7, 1,6 Гц, 2H), 5,63 (с, 2H), 4,95 (с, 2H), 3,96 (д, J=0,8 Гц, 3H) (400 MГц, ДМСО-d6) δ 7,50-7,38 (м, 2H), 7,337,18 (м, 4H), 7,13 (с, 2H), 5,39 (с, 2H), 3,92 (д, J=0,7 Гц, 3H), 2,35 (с, 3H) (400 MГц, ДМСО-d6) δ 7,62 (дд, J=7,0, 2,3 Гц, 1H), 7,57-7,37 (м, 4H), 7,30 (дд, J=8,5, 7,1 Гц, 1H), 7,14 (с, 2H), 5,45 (с, 2H), 3,92 (с, 3H) (400 MГц, ДМСО-d6) δ 7,46 (дд, J=8,5, 1,5 Гц, 1H), 7,43-7,33 (м, 2H), 7,29 (дд, J=8,5, 7,1 Гц, 1H), 7,11 (с, 2H), 7,05 (д, J=8,0 Гц, 1H), 6,96 (тд, J=7,4, 0,9 Гц, 1H), 5,34 (с, 2H), 3,92 (д, J=0,5 Гц, 3H), 3,81 (с, 3H) Інші дані ЯМР UA 108922 C2 + 11 Біла тверда речовина 150 453 ([M+Н] ), 451 ([M-H] ) 12 Біла тверда речовина 147-148 474 ([M+Н] ), 472 ([M-H] ) 13 Біла тверда речовина 164-165 469 ([M+Н] ), 467 ([M-H] ) 14 Безбарвне масло 15 Біла тверда речовина 84-85 453 ([M+Н] ), 451 ([M-H] ) 16 Біла тверда речовина 182 498 ([M+Н] ), 496 ([M-H] ) 18 Біла тверда речовина 100-108 457 ([M+Н] ), 455 ([M-H] ) + + + 453 ([M+Н] ), 451 ([M-H] ) + + + 23 (400 MГц, ДМСО-d6) δ 7,46 (дд, J=8,5, 1,5 Гц, 1H), 7,32-7,21 (м, 4H), 7,17 (д, J=7,2 Гц, 1H), 7,13 (с, 2H), 5,34 (с, 2H), 3,92 (д, J=0,7 Гц, 3H), 2,31 (с, 3H) (400 MГц, ДМСО-d6) δ 7,55 (с, 1H), 7,51-7,39 (м, 4H), 7,30 (дд, J=8,5, 7,1 Гц, 1H), 7,15 (с, 2H), 5,40 (с, 2H), 3,93 (д, J=0,7 Гц, 3H) (400 MГц, ДМСО-d6) δ 7,47 (дд, J=8,5, 1,5 Гц, 1H), 7,36-7,25 (м, 2H), 7,14 (с, 2H), 7,02 (д, J=7,4 Гц, 2H), 6,96-6,88 (м, 1H), 5,35 (с, 2H), 3,93 (д, J=0,7 Гц, 3H), 3,74 (с, 3H) 19 (400 MГц, ДМСО-d6) δ F-ЯМР (376 7,50-7,43 (м, 3H), 7,41- MГц, ДМСО7,35 (м, 2H), 7,35-7,26 d6) δ -129,03 (м, 2H), 7,07 (с, 2H), (д, J=28,1 6,08 (кв, J=6,5 Гц, 1H), Гц), -137,77 3,93 (д, J=0,9 Гц, 3H), (д, J=28,1 1,61 (д, J=6,6 Гц, 3H) Гц) (400 MГц, ДМСО-d6) δ 7,47 (дд, J=8,5, 1,6 Гц, 1H), 7,36-7,18 (м, 6H), 7,05 (с, 2H), 4,53 (т, J=6,8 Гц, 2H), 3,93 (д, J=1,0 Гц, 3H), 3,02 (т, J=6,8 Гц, 2H) (400 MГц, ДМСО-d6) δ 8,02-7,95 (м, 2H), 7,59 (д, J=8,5 Гц, 2H), 7,46 (дд, J=8,5, 1,6 Гц, 1H), 7,30 (дд, J=8,5, 7,1 Гц, 1H), 7,09 (с, 2H), 5,47 (с, 2H), 3,93 (д, J=1,0 Гц, 3H), 3,86 (с, 3H) (400 MГц, CDCl3) δ 7,64 (дд, J=8,6, 7,8 Гц, 1H), 7,44-7,32 (м, 4H), 7,22 (дд, J=8,7, 1,8 Гц, 1H), 7,17 (д, J=1,6 Гц, 1H), 5,40 (с, 2H), 4,85 (с, 2H), 3,96 (д, J=0,9 Гц, 3H) UA 108922 C2 19 Біла тверда речовина 110-113 21 Біла тверда речовина 207-208 22 Біла тверда речовина 107-108 23 Біла тверда речовина 160-161 24 Біла тверда речовина 143-144 25 Біла тверда речовина 169 26 Біла тверда речовина 133-134 (400 MГц, CDCl3) δ 7,71 (дд, J=8,6, 7,8 Гц, 1H), 7,49 (дд, J=5,4, 3,4 Гц, 2H), 7,40-7,34 (м, 2H), 7,33-7,28 (м, 1H), 7,23 + 435 ([M+Н] ), 433 (дд, J=8,7, 1,7 Гц, 1H), ([M-H] ) 7,18 (д, J=1,6 Гц, 1H), 6,21 (кв, J=6,6 Гц, 1H), 4,80 (с, 2H), 3,97 (д, J=0,8 Гц, 3H), 1,72 (д, J=6,6 Гц, 3H) (400 MГц, ацетон-d6) δ 8,33-8,25 (м, 2H), 7,857,77 (м, 2H), 7,40 (ддд, + 484 ([M+Н] ), J=15,3, 8,5, 4,1 Гц, 2H), 482([M-H] ) 6,52 (с, 1H), 5,59 (с, 2H), 3,99 (д, J=1,1 Гц, 3H) (400 MГц, ДМСО-d6) δ 7,48 (дд, J=8,5, 1,6 Гц, 1H), 7,34 (с, 4H), 7,27 (дд, J=8,5, 7,1 Гц, 1H), 485 ([M-H] ) 7,09 (с, 2H), 4,52 (т, J=6,6 Гц, 2H), 3,93 (д, J=0,8 Гц, 3H), 3,01 (т, J=6,6 Гц, 2H) (400 MГц, ДМСО-d6) δ 7,50-7,41 (м, 2H), 7,34457 ([M+Н]+), 7,26 (м, 3H), 7,20 (с, 455 ([M-H] ) 1H), 7,14 (с, 2H), 5,40 (с, 2H), 3,92 (д, J=0,6 Гц, 3H) (400 MГц, ДМСО-d6) δ 7,55-7,50 (м, 2H), 7,46 (дд, J=8,5, 1,5 Гц, 1H), + 457 ([M+Н] ) 7,31-7,20 (м, 3H), 7,13 (с, 2H), 5,36 (с, 2H), 3,92 (с, 3H) (400 MГц, ДМСО-d6) δ 7,57 (дт, J=9,4, 4,7 Гц, 1H), 7,45 (ддд, J=9,4, + 457 ([M+Н] ), 455 4,6, 1,7 Гц, 2H), 7,26 ([M-H] ) (ддд, J=15,6, 7,3, 2,8 Гц, 3H), 7,13 (с, 2H), 5,42 (с, 2H), 3,92 (д, J=0,5 Гц, 3H) (400 MГц, ДМСО-d6) δ 7,84-7,69 (м, 3H), 7,61 (т, J=7,5 Гц, 1H), 7,48 + 507 ([M+Н] ), 505 (дд, J=8,5, 1,5 Гц, 1H), ([M-H] ) 7,29 (дд, J=8,5, 7,1 Гц, 1H), 7,15 (с, 2H), 5,53 (с, 2H), 3,92 (д, J=0,6 Гц, 3H) 24 UA 108922 C2 + 27 Біла тверда речовина 75-76 481 ([M+Н] ), 479 ([M-H] ) 28 Біла тверда речовина 142-143 489 ([M+Н] ), 487 ([M-H] ) 29 Біла тверда речовина 144-145 497 ([M+Н] ), 495 ([M-H] ) 30 Біла тверда речовина 167-168 485 ([M-H] ) 31 Біла тверда речовина 145 485 ([M+Н] ), 483 ([M-H] ) 32 Безбарвна тверда речовина 161 497 ([M+Н] ), 495 ([M-H] ) 33 Біла тверда речовина 145-147 417 ([M+Н] ) + + + + + 25 (400 MГц, ДМСО-d6) δ 7,46 (дд, J=8,5, 1,5 Гц, 1H), 7,37 (д, J=8,1 Гц, 2H), 7,32-7,23 (м, 3H), 7,12 (с, 2H), 5,32 (с, 2H), 3,92 (д, J=0,7 Гц, 3H), 2,88 (дт, J=13,7, 6,8 Гц, 1H), 1,19 (д, J=6,9 Гц, 6H) (400 MГц, ацетон-d6) δ 8,06 (с, 1H), 8,00-7,90 (м, 3H), 7,65 (дд, J=8,5, 1,7 Гц, 1H), 7,59-7,51 (м, 2H), 7,40 (ддд, J=15,3, 8,5, 4,1 Гц, 2H), 6,49 (с, 2H), 5,61 (с, 2H), 4,00 (д, J=1,1 Гц, 3H) (400 MГц, ацетон-d6) δ 8,19 (дд, J=1,7, 1,2 Гц, 1H), 8,01 (дт, J=7,8, 1,4 Гц, 1H), 7,79 (ддд, J=7,7, 1,7, 1,2 Гц, 1H), 7,58 (т, J=7,7 Гц, 1H), 7,43 (дд, J=8,5, 1,5 Гц, 1H), 7,37 (дд, J=8,5, 6,7 Гц, 1H), 6,50 (с, 2H), 5,53 (с, 2H), 4,00 (д, J=1,1 Гц, 3H), 3,90 (с, 3H) (400 MГц, ацетон-d6) δ 7,51 (д, J=8,2 Гц, 1H), 7,43 (дд, J=8,5, 1,6 Гц, 1H), 7,37-7,30 (м, 2H), 7,26 (дд, J=8,1, 2,0 Гц, 1H), 6,49 (с, 2H), 5,43 (с, 2H), 4,00 (д, J=1,1 Гц, 3H) (400 MГц, ацетон-d6) δ 7,50-7,39 (м, 3H), 7,33 (ддд, J=8,4, 7,9, 4,4 Гц, 3H), 6,48 (с, 2H), 5,38 (с, 2H), 4,00 (д, J=1,1 Гц, 3H) (400 MГц, ацетон-d6) δ 8,02 (дд, J=7,8, 1,3 Гц, 1H), 7,78 (дд, J=7,8, 0,6 Гц, 1H), 7,65 (тд, J=7,6, 1,4 Гц, 1H), 7,54-7,35 (м, 3H), 6,50 (с, 1H), 5,82 (с, 2H), 4,01 (д, J=1,1 Гц, 3H), 3,91 (с, 3H) (400 MГц, CDCl3) δ 7,657,15 (м, 9H), 5,45 (д, 19 F ЯМР (376 J=4,1 Гц, 2H), 5,40 (с, MГц, CDCl3) 2H), 3,99 (д, J=1,0 Гц, δ -129,38 (с) 3H), 3,81 (д, J=7,2 Гц, 3H) UA 108922 C2 34 37 10 15 20 25 30 35 Жовте масло 39 5 Прозоре масло Білі кристали 90-91,5 (400 MГц, CDCl3) δ 7,59 (дд, J=8,6, 7,5 Гц, 1H), 19 7,35-7,15 (м, 6H), 5,63 F ЯМР (376 + 431 ([M+Н] ) (с, 2H), 4,63 (тд, J=7,0, MГц, CDCl3) 4,0 Гц, 2H), 3,98 (д, δ -129,46 (с) J=0,9 Гц, 3H), 3,75 (с, 3H), 3,15-3,07 (м, 2H) (400 MГц, CDCl3) δ 7,67 (дд, J=8,6, 7,9 Гц, 1H), 7,29 (дд, J=15,8, 3,6 Гц, 4H), 7,25-7,20 (м, 2H), + 435 ([M+Н] ), 433 7,19 (д, J=1,6 Гц, 1H), ([M-H] ) 4,81 (с, 2H), 4,62 (т, J=7,2 Гц, 2H), 3,97 (д, J=0,7 Гц, 3H), 3,12 (т, J=7,1 Гц, 2H) (400 MГц, CDCl3) δ 7,737,11 (м, 9H), 5,45 (с, + 421 ([M+Н] ) 2H), 4,81 (с, 2H), 3,97 (д, J=0,6 Гц, 3H) Приклад 13. Оцінка загальної гербіцидної дії на післясходовій стадії Насіння або горішки бажаних видів тестованих рослин, висівали в суміш для вирощування Sun Gro Metro-Mix® 360, як правило, ту, що має pH від 6,0 до 6,8 і вміст органічної речовини 30 2 процентів, в пластмасових горщиках з площею поверхні 84,6 квадратних сантиметрів (см ). Коли потрібна гарантія хорошого проростання і здорових рослин, застосовують обробки фунгіцидами і/або інші хімічні або фізичні обробки. Рослини вирощували протягом 7-31 днів (д) в оранжереї з фотоперіодом приблизно 15 годин (год.), при якому підтримували температуру 23-29°С протягом дня і 22-28°С протягом ночі. Регулярно додавали поживні речовини і воду, і додаткове освітлення, по мірі необхідності, забезпечувало верхніми метало-галогеновими лампами потужністю 1000 Вт. Рослини брали участь у випробуванні тоді, коли вони досягали стадії розвитку першого або другого справжнього листка. Обробки складалися із складних ефірів сполук 33 і 39 і F і G. Сполука F являє собою метил6-аміно-2-(4-хлор-2-фтор-3-метоксифеніл)-5-метоксипіримідин-4-карбоксилат; і сполука G являє собою метил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3-метоксифеніл)піколінат. Зважену кількість, визначену найбільшою тестованою нормою внесення кожної тестованої сполуки, вміщували в скляну пробірку на 25 мл і розчиняли в 4 мл 97:3 об./об. (об'єм/об'єм) суміш ацетону і диметилсульфоксиду (ДМСО) з отриманням концентрованих маточних розчинів. Якщо тестована сполука легко не розчинялася, то суміш підігрівали і/або обробляли ультразвуком. Отримані концентровані маточні розчини розбавляли 20 мл водної суміші, що містить ацетон, воду, ізопропіловий спирт, ДМСО, концентрат олії сільськогосподарської культури Atplus 411F і поверхнево-активну речовину Triton® X-155 у відношенні 48,5:39:10:1,5:1,0:0,02 об./об., з отриманням розчинів для розбризкування з найвищими нормами внесення. Додаткові норми внесення отримували серійним розведенням 12 мл розчину з високою нормою внесення до розчину, що містить 2 мл 97:3 об./об. (об'єм/об'єм) суміш ацетону і ДМСО і 10 мл водної суміші, що містить ацетон, воду, ізопропіловий спирт, ДМСО, концентрат олії сільськогосподарської культури Atplus 411F і поверхнево-активну речовину Triton® X-155 у співвідношенні 48,5:39:10:1,5:1,0:0,02 об./об., з отриманням 1/2×, 1/4×, 1/8× і 1/16× від високої норми внесення. Вимоги до сполук засновані на об'ємі внесення 12 мл при нормі внесення 187 літрів на гектар (л/га). Складені в композицію сполуки застосовували до рослинного матеріалу за допомогою верхнього машинного розбризкувача Mandel, обладнаного форсунками 8002E, каліброваними 2 для доставки 187 л/га на території застосування 0,503 квадратних метрів (м ) з висотою розбризкування 18 дюймів (43 см) над середнім рівнем листового покриву. Контрольні рослини оббризкували таким же чином чистим розчинником. Оброблені рослини і контрольні рослини вміщували в оранжерею, як описано вище, і поливали внутрішньоґрунтовим зрошуванням для запобігання змивання сполук. Через 14 д стан тестованих рослин в порівнянні з таким необроблених рослин визначали візуально і оцінювали за шкалою від 0 до 100 процентів, де 0 відповідає відсутності пошкодження і 100 відповідає повному знищенню. 26 UA 108922 C2 Деякі тестовані сполуки, застосовувані норми внесення, тестовані види рослин і результати наведені в таблицях 3 і 4. Таблиця 3 Дія гербіцидних сполук на післясходовій стадії при різних нормах внесення (14 днів після застосування (DAA)) Норма внесення (г аі/га) 35 17,5 8,75 35 17,5 8,75 Номер сполуки G G G 39 39 39 Візуальне пошкодження (%) IPOHE 65 50 40 80 75 70 Таблиця 4 Дія гербіцидних сполук при застосуванні на післясходовій стадії (70 г аі/га на 14 DAA) Номер сполуки F 33 ORYSA 75 30 Візуальне пошкодження (%) TRZAS IPOHE VIOTR 70 80 80 45 100 100 STEME 90 100 IPOHE = Ipomoea hederacea (Іпомея ранкове сяйво), ORYSA = Oryza sativa (Рис), STEME = Stellaria media (Зірочник польовий), TRZAS = Triticum aestivum (Яра пшениця), VIOTR = Viola tricolor (Фіалка триколірна), г аі/га = грам активного інгредієнта на гектар, DAA = днів після застосування. 5 10 15 20 25 30 Приклад 14. Оцінка гербіцидної дії на післясходовій стадії в зернових сільськогосподарських культурах Насіння необхідних видів рослин, що тестуються, висівали в суміш для вирощування Sun Gro Metro-Mix® 360, яка, як правило, має pH від 6,0 до 6,8 і вміст органічної речовини 30 2 процентів, в пластмасових горщиках з площею поверхні 84,6 см . За необхідності для забезпечення хорошого проростання і здорових рослин, застосовують обробку фунгіцидами і/або інші хімічні або фізичні обробки. Рослини вирощували протягом 7-36 д в оранжереї з фотоперіодом приблизно 14 год., при якому підтримували 18°С протягом дня і 17°С протягом ночі. Регулярно додавали поживні речовини і воду, і додаткове освітлення, по мірі необхідності, забезпечувало верхніми метало-галогеновими лампами потужністю 1000 Вт. Рослини брали участь у випробуванні тоді, коли вони досягали стадії розвитку другого або третього справжнього листка. Обробки складалися із складних ефірів сполук 33, 34, 39, 40 і 42 і В, F, G і Н. Сполука В являє собою метил-4-аміно-3-хлор-6-(4-циклопропілфеніл)-5-фторпіколінат; сполука F являє собою метил-6-аміно-2-(4-хлор-2-фтор-3-метоксифеніл)-5-метоксипіримідин-4-карбоксилат; сполука G являє собою метил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3-метоксифеніл)піколінат і сполука Н являє собою метил-4-аміно-3-хлор-6-(4-хлор-2-фтор-3-(1-фторетил)феніл)-5фторпіколінат. Зважену кількість, визначену найбільшою тестованою нормою внесення кожної тестованої сполуки, вміщували в скляну пробірку на 25 мл і розчиняли в 8 мл суміші ацетону і ДМСО у співвідношенні 97:3 об./об. з отриманням концентрованих маточних розчинів. Якщо тестована сполука легко не розчиняється, то суміш підігрівали і/або обробляли ультразвуком. Отримані концентровані маточні розчини розбавляли 16 мл водної суміші, що містить ацетон, воду, ізопропіловий спирт, ДМСО, концентрат олії сільськогосподарської культури Agri-dex і поверхнево-активну речовину Triton® X-77 у співвідношенні 64,7:26,0:6,7:2,0:0,7:0,01 об./об., з отриманням розчинів для розбризкування з найвищими нормами внесення. Додаткові норми внесення отримували серійним розведенням 12 мл розчину з високою нормою внесення до 27 UA 108922 C2 5 10 15 розчину, що містить 4 мл суміші ацетону і ДМСО в співвідношенні 97:3 об./об. і 8 мл водної суміші, що містить ацетон, воду, ізопропіловий спирт, ДМСО, концентрат олії сільськогосподарської культури Agri-dex і поверхнево-активну речовину Triton® X-77 у співвідношенні 48,5:39,0:10,0:1,5:1,0:0,02 об./об., з отриманням норм, рівних 1/2×, 1/4×, 1/8× і 1/16× від самої високої норми внесення. Вимоги до сполук засновані на об'ємі внесення, рівному 12 мл, при нормі внесення 187 л/м. Складені в композицію сполуки застосовували до рослинного матеріалу за допомогою верхнього машинного розбризкувача Mandel, обладнаного 2 форсункою 8002E, каліброваною для доставки 187 л/га на території площею 0,503 м з висотою розбризкування 18 дюймів (43 см) над середнім рівнем листового покриву. Контрольні рослини оббризкували таким же чином чистим розчинником. Оброблені рослини і контрольні рослини вміщували в оранжерею, як описано вище, і поливали внутрішньоґрунтовим зрошуванням для запобігання змивання тестованих сполук. Через 20-22 д стан рослин в порівнянні з таким необроблених рослин визначали візуально і оцінювали за шкалою від 0 до 100 процентів, де 0 відповідає відсутності пошкодження, і 100 відповідає повному знищенню. Деякі тестовані сполуки, застосовувані норми внесення, тестовані види рослин і результати наведені в таблицях 5-10. Таблиця 5 Дія гербіцидних сполук в системах вирощування пшениці (35 г ек/га і 21 DAA) Візуальне пошкодження (%) POLCO SINAR 62 70 95 93 Номер сполуки B 42 Таблиця 6 Дія гербіцидних сполук в системах вирощування пшениці (35 г ек/га і 21 DAA) Номер сполуки G 39 SINAR 80 95 Візуальне пошкодження (%) KCHSC SASKR MATCH 87 80 75 95 90 95 POLCO 85 95 20 Таблиця 7 Дія гербіцидних сполук в системах вирощування пшениці при різних нормах внесення (21 DAA) Номер сполуки G G 39 39 Норма внесення (г ек/га) 17,5 8,75 17,5 8,75 Візуальне пошкодження (%) CIRAR 80 70 95 90 Таблиця 8 Дія гербіцидних сполук в системах вирощування пшениці (8,75 г ек/га і 21 DAA) Номер сполуки H 40 SINAR 87 98 Візуальне пошкодження (%) VERPE 80 95 28 PESGL 0 65
ДивитисяДодаткова інформація
Назва патенту англійськоюArylalkyl esters of 4-amino-6-(substituted phenyl)picolinates and 6-amino-2-(substituted phenyl)-4-pyrimidinecarboxylates and their use as herbicides
Автори англійськоюYerkes, Carla N., Lowe, Christian T., Eckelbarger, Joseph, D., Epp, Jeffrey, B., Guenthenspberger, Katharine A., Siddall, Thomas L., Schmitzer, Paul R.
Автори російськоюЙеркс Карла Н., Лоу Кристиан Т., Эккельбарджер Джозеф Д., Эпп Джеффри Б., Гюнтенспбергер Катерине А., Сиддалл Томас Л., Шмитцер Пол Р.
МПК / Мітки
МПК: A01P 13/00, C07D 213/79, A01N 43/90
Мітки: складні, арилалкілові, застосування, ефіри, 4-аміно-6-(заміщений, гербіцидів, феніл)піколінатів
Код посилання
<a href="https://ua.patents.su/40-108922-skladni-arilalkilovi-efiri-4-amino-6-zamishhenijj-fenilpikolinativ-i-kh-zastosuvannya-yak-gerbicidiv.html" target="_blank" rel="follow" title="База патентів України">Складні арилалкілові ефіри 4-аміно-6-(заміщений феніл)піколінатів і їх застосування як гербіцидів</a>
Попередній патент: Магазин штурмової гвинтівки калібру 5,45х39
Наступний патент: Спусковий механізм пістолета
Випадковий патент: Очисник головок коренеплодів