Похідні b-арил-a
Номер патенту: 82835
Опубліковано: 26.05.2008
Автори: Ікбал Джавед, Дас Сайбал Кумар, Мадхаван Гуррам Ранга, Бхунія Дебназ, Вікрамадізіан Рееба Каннімел, Чакрабарті Ранджан
Формула / Реферат
1. Сполука формули (І)
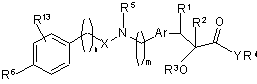 , (I)
, (I)
де R1 - гідроген, гідроксил, галоген, лінійний чи розгалужений (С1-С12)-алкіл, лінійний чи розгалужений (С1-С12)-алкокси, заміщений чи незаміщений арилалкіл,
R2 - гідроген, галоген, лінійний чи розгалужений (С1-С12)-алкіл, лінійний чи розгалужений (С1-С12)-алкокси, (С1-С12)-алканоїл, ароїл, арилалканоїл, заміщений чи незаміщений арилалкіл,
R3 - гідроген, заміщений чи незаміщений лінійний чи розгалужений (С1-С12)-алкіл, циклоалкіл, циклоалкілалкіл, циклоалкеніл, арил, (С1-С12)-алканоїл, ароїл, арилалкіл, арилалканоїл, одновалентний гетероцикл, гетероарил, гетероарилалкіл, алкоксіалкіл, алкоксикарбоніл, арилоксикарбоніл, алкіламінокарбоніл чи ариламінокарбоніл,
R4 - гідроген або заміщений чи незаміщений лінійний чи розгалужений (С1-С12)-алкіл, циклоалкіл, арил, арилалкіл, одновалентний гетероцикл, гетероарил чи гетероарилалкіл,
Y - оксиген,
R5 - гідроген або заміщений чи незаміщений алкіл, алкеніл, циклоалкіл, циклоалкілалкіл, арил чи арилалкіл,
Аr - заміщений чи незаміщений двовалентний фенілен, нафтилен, піридил, хінолініл, бензофурил, дигідробензофурил, бензопіраніл, дигідробензопіраніл, індоліл, індолініл, азаіндоліл, азаіндолініл, піразоліл, бензотіазоліл чи бензоксазоліл,
X - -C(=S)-O, -C(=O)-O-, -C(=O)-S-, -C(=S)-O-, -O-(CH2)d-, -NH-(CH2)d-, де d знаходиться в інтервалі 1-4, -О-С(=О)-, -CRa=CRb-CH2-, де Ra та Rb є однаковими чи різними і позначають гідроген чи (С1-С6)-алкіл, або X позначає зв'язок,
R6 - заміщений чи незаміщений арилоксикарбоніл, арилалкоксикарбоніл, алкілкарбонілокси, алкоксикарбоніламіно, арилоксикарбоніламіно, арилалкоксикарбоніламіно, флуоренілметоксикарбоніл (Fmoc), флуоренілметоксикарбоніламіно (N-Fmoc), -OSO2R8, -OCONR8R9, NR8COOR9, -NR8COR9, -NR8SO2R9, NR8CONR9R10, -NR8CSNR8R9, -SO2R8, -SOR8, -SR8, -SO2NR8R9, -SO2OR8, -COOR9, -COR9 чи -CONR8R9, де R8, R9 та R10 є однаковими чи різними і незалежно позначають гідроген або заміщений чи незаміщений алкіл, арил, арилалкіл, алкоксикарбоніл чи арилалкоксикарбоніл, або R6 позначає гідроген, якщо R13 знаходиться у положенні 3 фенільного кільця і не позначає гідроген,
R13 - гідроген, галоген, нітрогрупа, ціаногрупа, аміногрупа, галоїдалкіл, гідроксил або заміщений чи незаміщений лінійний чи розгалужений (С1-С12)-алкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, одновалентний гетероциклічний радикал, алкоксигрупа, моноалкіламіногрупа, діалкіламіногрупа, алкоксикарбоніл, арилоксикарбоніл, арилалкоксикарбоніл, арилоксигрупа, арилалкоксигрупа, алкілкарбонілоксигрупа, алкоксикарбоніламіногрупа, арилоксикарбоніламіногрупа, арилалкоксикарбоніламіногрупа, флуоренілметоксикарбоніл (Fmoc), флуоренілметоксикарбоніламіногрупа (N-Fmoc), -OSO2R8, -OCONR8R9, NR8COOR9, -NR8COR9, -NR8R9, -NR8SO2R9, NR8CONR9R10, -NR8CSNR8R9, -SO2R8, -SOR8, -SR8, -SO2NR8R9, -SO2OR8, -COOR9, -COR9, -CONR8R9, де R8, R9 та R10 є однаковими чи різними і незалежно позначають гідроген або заміщений чи незаміщений алкіл, арил, арилалкіл, алкоксикарбоніл чи арилалкоксикарбоніл, n має значення від 1 до 6 і m має значення від 0 до 6,
та її таутомерні форми, її стереоізомери, її поліморфи, її фармацевтично прийнятні солі, її фармацевтично прийнятні сольвати.
2. Сполука за п. 1, вибрана з:
етил-2-метокси-3-[4-{3-(4-метансульфонілоксифеніл)пропіламіно}феніл]пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
етил-2-етокси-3-[4-{3-(4-метансульфонілоксифеніл)пропіламіно}феніл]пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
етил-2-етокси-3-[4-{3-(4-метансульфонілоксифеніл)пропілоксикарбоніламіно}-феніл]пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
етил-2-етокси-3-[4-{3-(3-метансульфонілоксифеніл)пропіламіно}феніл]пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
етил-2-етокси-3-[4-{3-(4-(толуол-4-сульфонілокси)феніл)пропіламіно}феніл]пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
етил-2-етокси-3-[3-{3-(4-метансульфонілоксифеніл)пропіламіно}феніл]пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
етил-2-ізопропокси-3-[4-{3-(4-метансульфонілоксифеніл)пропіламіно}феніл]пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
етил-2-етокси-3-[4-(4-метилсульфонілоксифенетиламіно)феніл]пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
етил-2-етокси-3-{4-[(Е)-3-(4-метилсульфонілоксифеніл)-2-пропеніламіно]феніл}пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
метил-2-етокси-3-[4-(4-метансульфонілоксибензиламіно)феніл]пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
2-метокси-3-[4-{3-(4-метансульфонілоксифеніл)пропіламіно}феніл]пропіонової кислоти
чи її солей у формі окремих енантіомерів чи рацемату,
2-етокси-3-[4-{3-(4-метансульфонілоксифеніл)пропіламіно}феніл]пропіонової кислоти
чи її солей у формі окремих енантіомерів чи рацемату,
2-етокси-3-[4-{3-(4-метансульфонілоксифеніл)пропілоксикарбоніламіно}феніл]пропіонової кислоти
чи її солей у формі окремих енантіомерів чи рацемату,
2-етокси-3-[4-{3-(3-метансульфонілоксифеніл)пропіламіно}феніл]пропіонової кислоти
чи її солей у формі окремих енантіомерів чи рацемату,
2-етокси-3-[4-{3-(4-(толуол-4-сульфонілокси)феніл)пропіламіно}феніл]пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
2-етокси-3-[3-{3-(4-метансульфонілоксифеніл)пропіламіно}феніл]пропіонової кислоти
чи її солей у формі окремих енантіомерів чи рацемату,
2-ізопропокси-3-[4-{3-(4-метансульфонілоксифеніл)пропіламіно}феніл]пропіонової кислоти
чи її солей у формі окремих енантіомерів чи рацемату,
2-етокси-3-[4-(4-метансульфонілоксибензиламіно)феніл]пропіонової кислоти
чи її солей у формі окремих енантіомерів чи рацемату,
2-етокси-3-[4-(4-метилсульфонілоксифенетиламіно)феніл]пропіонової кислоти
чи її солей у формі окремих енантіомерів чи рацемату,
2-етокси-3-{4-[(Е)-3-(4-метилсульфонілоксифеніл)-2-пропеніламіно]феніл}пропіонової кислоти
чи її солей у формі окремих енантіомерів чи рацемату,
етил-2-етокси-3-[4-{3-(4-трет-бутокси-4-метилсульфонамідофеніл)пропіламіно}феніл]пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
2-етокси-3-[4-{3-(4-трет-бутокси-4-метилсульфонамідофеніл)пропіламіно}феніл]пропіонової кислоти
чи її солей у формі окремих енантіомерів чи рацемату,
етил-2-метокси-3-[4-{(Е)-3-(4-метилсульфонілоксифеніл)-2-пропеніламіно}феніл]пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
2-метокси-3-[4-{(Е)-3-(4-метилсульфонілоксифеніл)-2-пропеніламіно}феніл]пропіонової кислоти
чи її солей у формі окремих енантіомерів чи рацемату,
етил-2-метокси-3-[4-{3-(3-метансульфонілоксифеніл)пропіламіно}феніл]пропіонату
чи його солей у формі окремих енантіомерів чи рацемату,
2-метокси-3-[4-{3-(3-метансульфонілоксифеніл)пропіламіно}феніл]пропіонової кислоти
чи її солей у формі окремих енантіомерів чи рацемату.
3. Сполука за п. 1, у якій фармацевтично прийнятна сіль вибрана з групи, що складається з солей Li, Na, К, Са, Mg, Fe, Cu, Zn, Al, Mn, N,N'-діацетилетилендіаміну, бетаїну, кофеїну, 2-діетиламіноетанолу, 2-диметиламіноетанолу, н-етилморфоліну, н-етилпіперидину, глюкаміну, глюкозаміну, гідрабаміну, ізопропіламіну, метилглюкаміну, морфоліну, піперазину, піперидину, прокаїну, теоброміну, валінолу, діетиламіну, триетиламіну, триметиламіну, трипропіламіну, трометаміну, адамантиламіну, діетаноламіну, меглуміну, етилендіаміну, N,N'-дифенілетилендіаміну, N,N'-дибензилетилендіаміну, N-бензилфенілетиламіну, холіну, холіну гідроксиду, дициклогексиламіну, метформіну, бензиламіну, фенілетиламіну, діалкіламіну, триалкіламіну, тіаміну, амінопіримідину, амінопіридину, пурину, піримідину, спермідину, алкілфеніламіну, етаноламіну, фенілетаноламіну, гліцину, аланіну, валіну, лейцину, ізолейцину, норлейцину, тирозину, цистину, цистеїну, метіоніну, проліну, гідроксипроліну, гістидину, орнітину, лізину, аргініну, серину, треоніну, фенілаланіну, неприродних амінокислот, D-ізомерів чи заміщених амінокислот, солей кислотних амінокислот, вибраних з аспарагінової кислоти чи глутамінової кислоти, гуанідину, заміщеного гуанідину, у якому замісники вибрані з нітрогрупи, аміногрупи, алкілу, алкенілу чи алкінілу, амонію, заміщених амонієвих солей, сульфатів, нітратів, фосфатів, перхлоратів, боратів, гідрогалогенідів (НСl, НВr, Нl), ацетатів, тартратів, малеатів, цитратів, сукцинатів, пальмоатів, метансульфонатів, бензоатів, саліцилатів, гідроксинафтоатів, бензолсульфонатів, аскорбатів, гліцерофосфатів чи кетоглутаратної солі.
4. Фармацевтична композиція, яка включає сполуку формули (І)
 , (I)
, (I)
визначену у будь-якому з пп. 1-3, та фармацевтично прийнятний носій, розріджувач, ексципієнт чи сольват.
Текст
1. Сполука формули (І) C2 2 (19) 1 3 82835 алкіл, арил, арилалкіл, гетероарил, гетероарилалкіл, одновалентний гетероциклічний радикал, алкоксигрупа, моноалкіламіногрупа, діалкіламіногрупа, алкоксикарбоніл, арилоксикарбоніл, арилалкоксикарбоніл, арилоксигрупа, арилалкоксигрупа, алкілкарбонілоксигрупа, алкоксикарбоніламіногрупа, арилоксикарбоніламіногрупа, арилалкоксикарбоніламіногрупа, флуоренілметоксикарбоніл (Fmoc), флуоренілметоксикарбоніламіногрупа (N-Fmoc), -OSO2R8, OCONR8R9, NR8COOR9 , -NR8COR9, -NR8R9, NR8SO2R9, NR8CONR9R10, -NR8CSNR8R9, -SO2R 8, SOR8, -SR8, -SO2NR8R9 , -SO2OR8 , -COOR 9, -COR 9, -CONR8R9, де R8, R9 та R10 є однаковими чи різними і незалежно позначають гідроген або заміщений чи незаміщений алкіл, арил, арилалкіл, алкоксикарбоніл чи арилалкоксикарбоніл, n має значення від 1 до 6 і m має значення від 0 до 6, та її та утомерні форми, її стереоізомери, її поліморфи, її фармацевтично прийнятні солі, її фармацевтично прийнятні сольвати. 2. Сполука за п. 1, вибрана з: етил-2-метокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонату чи його солей у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонату чи його солей у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-{3-(4метансульфонілоксифеніл)пропілоксикарбоніламіно}-феніл]пропіонату чи його солей у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-{3-(3метансульфонілоксифеніл)пропіламіно}феніл]пропіонату чи його солей у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-{3-(4-(толуол-4сульфонілокси)феніл)пропіламіно}феніл]пропіонату чи його солей у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[3-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонату чи його солей у формі окремих енантіомерів чи рацемату, етил-2-ізопропокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонату чи його солей у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-(4метилсульфонілоксифенетиламіно)феніл]пропіонату чи його солей у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-{4-[(Е)-3-(4метилсульфонілоксифеніл)-2пропеніламіно]феніл}пропіонату 4 чи його солей у формі окремих енантіомерів чи рацемату, метил-2-етокси-3-[4-(4метансульфонілоксибензиламіно)феніл]пропіонату чи його солей у формі окремих енантіомерів чи рацемату, 2-метокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонової кислоти чи її солей у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонової кислоти чи її солей у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-{3-(4метансульфонілоксифеніл)пропілоксикарбоніламіно}феніл]пропіонової кислоти чи її солей у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-{3-(3метансульфонілоксифеніл)пропіламіно}феніл]пропіонової кислоти чи її солей у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-{3-(4-(толуол-4сульфонілокси)феніл)пропіламіно}феніл]пропіонату чи його солей у формі окремих енантіомерів чи рацемату, 2-етокси-3-[3-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонової кислоти чи її солей у формі окремих енантіомерів чи рацемату, 2-ізопропокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонової кислоти чи її солей у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-(4метансульфонілоксибензиламіно)феніл]пропіонової кислоти чи її солей у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-(4метилсульфонілоксифенетиламіно)феніл]пропіонової кислоти чи її солей у формі окремих енантіомерів чи рацемату, 2-етокси-3-{4-[(Е)-3-(4-метилсульфонілоксифеніл)2-пропеніламіно]феніл}пропіонової кислоти чи її солей у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-{3-(4-трет-бутокси-4метилсульфонамідофеніл)пропіламіно}феніл]пропіонату чи його солей у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-{3-(4-трет-бутокси-4метилсульфонамідофеніл)пропіламіно}феніл]пропіонової кислоти 5 82835 6 чи її солей у формі окремих енантіомерів чи рацемату, етил-2-метокси-3-[4-{(Е)-3-(4метилсульфонілоксифеніл)-2пропеніламіно}феніл]пропіонату чи його солей у формі окремих енантіомерів чи рацемату, 2-метокси-3-[4-{(Е)-3-(4метилсульфонілоксифеніл)-2пропеніламіно}феніл]пропіонової кислоти чи її солей у формі окремих енантіомерів чи рацемату, етил-2-метокси-3-[4-{3-(3метансульфонілоксифеніл)пропіламіно}феніл]пропіонату чи його солей у формі окремих енантіомерів чи рацемату, 2-метокси-3-[4-{3-(3метансульфонілоксифеніл)пропіламіно}феніл]пропіонової кислоти чи її солей у формі окремих енантіомерів чи рацемату. 3. Сполука за п. 1, у якій фармацевтично прийнятна сіль вибрана з групи, що складається з солей Li, Na, К, Са, Mg, Fe, Cu, Zn, Al, Mn, N,N'діацетилетилендіаміну, бетаїн у, кофеїн у, 2діетиламіноетанолу, 2-диметиламіноетанолу, нетилморфоліну, н-етилпіперидину, глюкаміну, глюкозаміну, гідрабаміну, ізопропіламіну, метилглюкаміну, морфоліну, піперазину, піперидину, прокаїну, теоброміну, валінолу, діетиламіну, триетиламіну, триметиламіну, трипропіламіну, трометаміну, адамантиламіну, діетаноламіну, меглуміну, етилендіаміну, N,N'-дифенілетилендіаміну, N,N'-дибензилетилендіаміну, Nбензилфенілетиламіну, холіну, холіну гідроксиду, дициклогексиламіну, метформіну, бензиламіну, фенілетиламіну, діалкіламіну, триалкіламіну, тіаміну, амінопіримідину, амінопіридину, пурину, піримідину, спермідину, алкілфеніламіну, етаноламіну, фенілетаноламіну, гліцину, аланіну, валіну, лейцину, ізолейцину, норлейцину, тирозину, цистину, цистеїн у, метіоніну, проліну, гідроксипроліну, гістидину, орнітину, лізину, аргініну, серину, треоніну, фенілаланіну, неприродних амінокислот, Dізомерів чи заміщених амінокислот, солей кислотних амінокислот, вибраних з аспарагінової кислоти чи глутамінової кислоти, гуанідину, заміщеного гуанідину, у якому замісники вибрані з нітрогрупи, аміногрупи, алкілу, алкенілу чи алкінілу, амонію, заміщених амонієвих солей, сульфатів, нітратів, фосфа тів, перхлоратів, боратів, гідрогалогенідів (НСl, НВr, Нl), ацетатів, тартратів, малеатів, цитратів, сукцинатів, пальмоатів, метансульфонатів, бензоатів, саліцилатів, гідроксинафтоатів, бензолсульфонатів, аскорбатів, гліцерофосфатів чи кетоглутаратної солі. 4. Фармацевтична композиція, яка включає сполуку формули (І) Даний винахід стосується нових антидіабетичних, гіполіпідемічних, гіпохолестеринемічних сполук та засобів проти ожиріння формули (І), їхніх похідних, їхніх аналогів, їхніх таутомерних форм, їхні х стереоізомерів, їхніх поліморфів, їхні х фармацевтично прийнятних солей, їхніх фармацевтично прийнятних сольватів та фармацевтично прийнятних композицій, що їх містять. Конкретніше, даний винахід стосується сполук загальної формули (і), які є переважно агоністами PPARα, їхніх похідних, їхніх аналогів, їхніх та утомерних форм, їхніх стереоізомерів, їхні х поліморфів, їхні х фармацевтично прийнятних шлей,- їхніх фармацевтично прийнятних сольватів та фармацевтично прийнятних композицій, що їх містять їл, арилалканоїл, заміщений чи незаміщений арилалкіл, або R2 утворює зв'язок разом з R1; R3 позначає атом гідрогену або заміщені чи незаміщені групи, вибрані з лінійної чи розгалуженої (С1-С12)-алкільної, циклоалкільної, циклоалкілалкільної, циклоалкенільної, арильної, (С1-С12)алканоїльної, ароїльної, арилалкільної, арилалканоїльної, одновалентної гетероциклічної, гетероарильної, гетероарилалкільної, алкоксиалкільної, алкоксикарбонільної, арилоксикарбонільної, алкіламінокарбонільної чи ариламінокарбонільної груп; 4 R позначає гідроген або заміщені чи незаміщені групи, вибрані з лінійної чи розгалуженої (С1С12)-алкільної, циклоалкільної, арильної, арилалкільної, одновалентної гетероциклічної, гетероарильної чи гетероарилалкільної груп; Y позначає оксиген або NR7 чи N(R7)O, де R7 позначає гідроген або заміщені чи незаміщені групи, вибрані з лінійної чи розгалуженої (С1-С12)-алкільної, арильної, арилалкільної, гідроксіалкільної, алканоїльної, ароїльної, арилалканоїльної, одновалентної гетероциклічної, гетероарильної, гетероарилалкільної, алкоксикарбонільної чи арилалкоксикарбонільної груп; R4 та R7 разом можуть утворювати заміщену чи незаміщену 5- чи 6-членну циклічну стр уктур у, що містить атоми карбону, атом нітрогену, яка може додатково містити один чи кілька додаткових (I) де R1 позначає гідроген, гідроксильну групу, галоген, лінійний чи розгалужений (С1-С12)-алкіл, лінійну чи розгалужену (С1-С12)-алкоксильну гр упу, заміщену чи незаміщену арилалкільну групу, або утворює зв'язок разом із сусідньою групою R2; R2 позначає гідроген; галоген, лінійний чи розгалужений (С1-С12)-алкіл, лінійну чи розгалужену (С1-С12)-алкоксильну груп у, (С1-С12)-алканоїл, аро R5 R13 nX N Ar m R6 R1 R2 O Y R4 R 3O , (I) визначену у будь-якому з пп. 1-3, та фармацевтично прийнятний носій, розріджувач, ексципієнт чи сольват. 7 82835 гетероатомів, вибраних з оксигену, сульфуру чи нітрогену; R5 позначає гідроген або заміщені чи незаміщені групи, вибрані з алкільної, алкенільної, циклоалкільної, циклоалкілалкільної, арильної, арилалкільної, ароїльної чи аралканоїльної груп; Ar позначає заміщені чи незаміщені групи, вибрані з двовалентного фенілену, нафтилену, піридилу, хінолінілу, бензофурилу, дигідробензофурилу, бензопіранілу, дигідробензопіранілу, індолілу, індолінілу, азаіндолілу, азаіндолінілу, піразолілу, бензотіазолілу, бензоксазолілу і т.п., X позначає -С(=О)-, -C(=S)-, -C(=S)-O, -C(=O)O-, -C(=O)-S-, -O-(CH 2)d-, -NH-(CH2)d-, -O-C(=O)-, C(O)CH2-, -CRa=CRb-CH2-; -CRa=CRb-CO-, де Ra та Rb можуть бути однаковими чи різними і позначають гідроген чи (СгС6)-алкіл, d позначає ціле число від 1 до 4, або X позначає зв'язок; R6 позначає заміщену чи незаміщену гр упу, вибрану з арилоксикарбонілу, арилалкоксикарбонілу, алкілкарбонілоксигрупи, алкоксикарбоніламіногрупи, арилоксикарбоніламіногрупи, арилалкоксикарбоніламіногрупи, флуоренілметоксикарбонілу (Fmoc), флуоренілметоксикарбоніламіногрупи (N-Fmoc), -OSO2R8, OCONR8R9, NR8COOR9, -NR8COR9, -NR8SO2R9, NR8CONR9R10, -NR8CSNR8R9, -SO2R8, -SOR 8, -SR8, -SO2NR8R9, -SO2 OR8, -COOR 9, -COR 9 чи CONR8R9, де R8, R9 та R10 можуть бути однаковими чи різними і незалежно позначають гідроген або заміщений чи незаміщений алкіл, арил, арилалкіл, алкоксикарбоніл чи арилалкоксикарбоніл; R8 та R9, коли вони знаходяться на атомі нітрогену, можуть разом утворювати 5- чи 6-членну циклічну стр уктур у, що містить атоми карбону та один чи кілька гетероатомів, вибраних з оксигену, сульфур у чи нітрогену. R6 позначає гідроген, якщо R13 знаходиться у положенні 3 фенільного кільця і не позначає гідроген; R13 позначає гідроген, галоген, нітрогрупу, ціаногрупу, аміногрупу, галоїдалкіл, гідроксильну групу або заміщену чи незаміщену групу, вибрану з лінійного чи розгалуженого (С1-С12)-алкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, одновалентного гетероциклічного радикала, алкоксигрупи, моноалкіламіногрупи, діалкіламіногрупи, алкоксикарбонілу, арилоксикарбонілу, арилалкоксикарбонілу, арилоксигрупи, арилалкоксигрупи, алкілкарбонілоксигрупи, алкоксикарбоніламіногрупи, арилоксикарбоніламіногрупи, арилалкоксикарбоніламіногрупи, флуоренілметоксикарбонілу (Fmoc), флуоренілметоксикарбоніламіногрупи (NFmoc), -OSO2R8, -OCONR 8R9, NR8COOR9 , NR8COR9, -NR8R9, -NR8SO2R9, NR8CONR9R10, NR8CSNR8R9, -SO2R8, -SOR 8, -SR8 , -SO2NR8R9 , SO2OR8 , -COOR 9 , -COR 9 , -CONR8R9, де R8, R9 та R10 можуть бути однаковими чи різними і незалежно позначають гідроген або заміщений чи незаміщений алкіл, арил, арилалкіл, алкоксикарбоніл чи арилалкоксикарбоніл; R8 та R9, коли вони знаходяться на атомі нітрогену, разом можуть утворювати 5- чи 6-членну циклічну структур у, що містить атоми карбону та один чи кілька гетероатомів, вибраних з оксигену, сульфуру чи нітрогену; m по 8 значає ціле число від 0 до 6 і n позначає ціле число від 0 до 6. Даний винахід також стосується способу одержання зазначених вище сполук, їхніх аналогів, їхні х !похідних, їхніх таутомерних форм, їхніх стереоізомерів, їхніх поліморфів, їхніх фармацевтично прийнятних солей, їхні х фармацевтично прийнятних сольватів та фармацевтичних композицій, що їх містять. Даний винахід також стосується нових проміжних сполук, способів їхнього одержання, їхнього використання у синтезі сполук формули (І) та їхнього використання як антидіабетичних, гіполіпідемічних, гіпохолестеринемічних сполук та засобів проти ожиріння. Сполуки за даним винаходом знижують глюкозу, тригліцериди, інсулін плазми, знижують загальний холестерин (TC) та підвищують ліпопротеїди високої густини (HDL) і знижують ліпопротеїди низької густини (LDL), що має корисний ефект при ішемічній хворобі серця та атеросклерозі. Сполуки за даним винаходом є корисними для зниження ваги тіла та для лікування та/або профілактики хвороб, таких як атеросклероз, інсульт, периферичні судинні хвороби та споріднені розлади. Ці сполуки є придатними для лікування гіперліпідемії, гіперглікемії, гіперхолестеринемії, зниження атерогенних ліпопротеїдів, VLDL (ліпопротеїди дуже низької густини) та LDL. Сполуки за даним винаходом можуть бути використані для лікування ниркових хвороб, включаючи гломерулонефрит, гломерулосклероз, нефротичний синдром, гіпертензивний нефросклероз та нефропатію. Сполуки загальної формули (І) є також придатними для лікування та/або профілактики лептинорезистентності, порушеної толерантності до глюкози, розладів, споріднених із синдромом X, таких як гіпертензія, ожиріння, інсулінорезистентність, ішемічна хвороба серця та інші серцево-судинні розлади. Ці сполуки можуть також бути корисними як інгібітори альдозоредуктази, для поліпшення пізнавальних функцій при деменції, лікування діабетичних ускладнень, розладів, пов'язаних з активацією ендотеліальних клітин, псоріазу, синдрому полікістозних яєчників (PCOS), запальних хвороб кишечнику, остеопорозу, міотонічної дистрофії, панкреатиту, артеріосклерозу, ретинопатії, ксантоми, розладів харчування, запалення та для лікування раку. Сполуки заданим винаходом є також корисними при лікуванні та/або профілактиці вищезгаданих хвороб у комбінації/супутно з одним чи кількома інгібіторами HMG СоА-редуктази, інгібітором всмоктування холестерину, засобом проти ожиріння, засобом для лікування ліпопротеїдних розладів, гіпоглікемічним агентом, інсуліном, бігуанідом, сульфонілсечовиною, тіазолідиндіоном, подвійним агоністом PPARα та у чи їхньою сумішшю. Атеросклероз та інші периферичні судинні хвороби впливають на якість життя мільйонів людей. Тому значна увага приділяється вивченню етіології гіперхолестеринемії та гіперліпідемії і розробці ефективних терапевтичних стратегій. Гіперхолестеринемія визначається як рівень холестерину в плазмі, який перевищує значення, 9 82835 довільно назване "нормальним" рівнем. Нещодавно було визнано, що "ідеальні" рівні холестерину в плазмі є набагато нижчими за "нормальний" рівень холестерину у загальній популяції, і що ризик хвороби коронарних артерій (CAD) зростає з підвищенням рівню холестерину вище "оптимального" (або "ідеального") значення. Існує безсумнівний причинно-наслідковий зв'язок між гіперхолестеринемією та CAD, особливо для осіб з численними факторами ризику. Більша частина холестерину знаходиться у етерифікованих формах з різними ліпопротеїдами, такими як ліпопротеїди низької густини (LDL), ліпопротеїди проміжної густини (IDL), ліпопротеїди високої густини (HDL) і, частково, ліпопротеїди дуже низької густини (VLDL). Дослідження чітко вказують на наявність зворотного співвідношення між CAD та атеросклерозом і концентраціями HDL-холестерину у сироватці [Stampfer et аl, N. Engl. J. Med., 325 (1991), 373381]. Ризик CAD зростає з підвищенням рівнів LDL та VLDL. При CAD звичайно спостерігаються "жирові смужки" у сонній, коронарній та мозковій артеріях, які складаються переважно з вільного та етерифікованого холестерину. Miller et аl [Br. Med. J., 282 (1981), 1741-1744] показали, що підвищення кількості частинок HDL може зменшити кількість ділянок стенозу у коронарних артеріях людини, а високий рівень HDL-холестерину може запобігати розвитку атеросклерозу. [Picardo et аl, Arteriosclerosis 6 (1986) 434-441], показали в експериментах in vitro, що HDL є здатним видаляти холестерин з клітин. Вони припустили, що HDL може очищати тканини від надлишку вільного холестерину та переносити його до печінки, що відомо як зворотний транспорт холестерину [Macikinnon et аl, J. Віоі Chem. 261 (1986), 25482552]. Таким чином, агенти, що підвищують рівень холестерину HDL, будуть мати терапевтичну значущість для лікування гіперхолестеринемії та ішемічної хвороби серця (CHD). Ожиріння є хворобою, дуже поширеною у суспільствах з високим достатком та у країнах, що розвиваються, і є важливою причиною захворюваності та смертності. Воно є станом накопичення в організмі надлишкового жиру. Причини ожиріння точно невідомі. Вважається, що воно має генетичну природу або промотується взаємодією між генотипом та навколишнім середовищем. Незалежно від причини, результатом є відкладання жиру внаслідок дисбалансу між споживанням енергії та витрачанням енергії. Частиною курсу лікування ожиріння є дієта, фізичні вправи та пригнічення апетиту. Існує потреба в ефективній терапії для боротьби з цією хворобою, оскільки вона може спричинювати ішемічну хворобу серця, діабет, інсульт, гіперліпідемію, подагру, остеоартрит, знижену фертильність та багато інших психологічних та соціальних проблем. Діабет та інсулінорезистентність є іншою хворобою, що сильно впливає на якість життя великої кількості людей у світі. Інсулінорезистентність є зменшеною здатністю інсуліну виявляти свою біологічну дію в широкому інтервалі концентрацій, При інсулінорезистентності організм секретує 10 аномально високу кількість інсуліну для компенсації цього дефекту; при неспроможності досягти цього, концентрація глюкози в плазмі неминучо підвищується та призводить до розвитку діабету. У країнах, що розвиваються, цукровий діабет є дуже поширеною проблемою; він асоційований з різними аномаліями, включаючи ожиріння, гіпертензію, гіперліпідемію [J. Clin. Invest, 75 (1985) 809-817; N. Engl. J. Med., 317 (1987) 350-357; J. Clin. Endocrinol. Metab., 66 (1988) 580-583; J. Clin. Invest, 68 (1975) 957-969] та інші ниркові ускладнення [патентна публікація №WO 95/21608]. Зараз дедалі більшого визнання набуває думка про те, що інсулінорезистентність та відносна гіперінсулінемія відіграють певну роль в ожирінні, гіпертензії, атеросклерозі та цукровому діабеті типу 2. Зв'язок інсулінорезистентності з ожирінням, гіпертензією та стенокардією був описаний як синдром, центральною патогенною ланкою якого є інсулінорезистентність - синдром X. Гіперліпідемія єголовною причиною серцевосудинних захворювань (CVD) та інших хвороб периферичних судин. Високий ризик CVD пов'язаний з підвищеними значеннями LDL (ліпопротеїди низької густини) та VLDL (ліпопротеїди дуже низької густини), що. спостерігаються при гіперліпідемії. Пацієнти з нестерпністю до глюкози/інсулінорезистентністю, на додаток до гіперліпідемії мають підвищений ризик CVD. Численні дослідження у минулому показали, що зниження тригліцеридів плазми та загального холестерину, зокрема, LDL та VLDL, і підвищення холестерину HDL допомагає запобіганню серцево-судинних хвороб. Рецептори, активовані проліфератором пероксисом (PPAR), є сиротськими рецепторами, які належать до надсімейства стероїдних/ретиноїдних рецепторів ліганд-активованих факторів транскрипції [Wilson T. M. and Wahli W., Curr. Opin. Chem. Biol., 1997, Vol.1, 235-241]. Були виділені три рецептора, що активуються проліфератором пероксисом (PPAR), названі PPAR-α, PPAR-γ та PPAR-δ. Ці PPAR регулюють експресію цільових генів шляхом зв'язування з елементами послідовностей ДНК. Було визнано, що деякі сполуки, які активують чи у інший спосіб взаємодіють з одним чи кількома з PPAR, беруть участь у регулюванні рівнів тригліцеридів та холестерину у тваринних моделях [патенти США №№5847008, 5859051 та публікації PCTWO 97/28149, WO 99/04815]. Існує величезна кількість інформації про вплив агоністів PPARα на профіль серцево-судинного ризику, наприклад, сполуки класу фібратів, які є слабкими агоністами PPAR-α, коригують атерогенну дисліпопротеїнемію. Кілька випробувань ангіографічного втручання продемонстрували корисну дію цих ліків на розвиток атеросклеротичних ушкоджень, а результати випробувань з первинної та вторинної профілактики виявили зниження частоти серцево-судинних явищ [Ricote M. and Glass C. K.; Trends in Pharmacological Sciences; 2001; 22(9); 441-443]. Незважаючи на той факт, що фібрати, які є слабкими активаторами PPAR-α, знижують рівні 11 82835 тригліцеридів плазми і одночасно підвищують рівні HDL-C, вони не є кращими лікарськими засобами через низьку ефективність, що потребує використання великих доз, можливість виникнення міозиту та наявність протипоказань для пацієнтів з порушеннями ниркової та печінкової функцій і вагітних та жінок, що годують. Однак, відбувався швидкий прогрес у розумінні ролі PPAR-α при різних патофізіологічних станах, на додаток до добре документованих сприятливих ефектів на ліпідний профіль. Запальна активація гладких клітин м'язів аорти, яка є характерною ознакою атеросклерозу, по-видимому, інгібується дією PPAR-α [Vamecq J. and Latruffe N; Lancet; 1999; 354; 141-148]. Нещодавно одержані дані дозволяють припустити роль рецепторів PPAR-α у поліпшенні чутливості до інсуліну. Було продемонстровано, що за рахунок зниження ліпідів у кровообігу та м'язах у інсулінорезистентних моделей гризунів, таких як щури Zucker з ожирінням, миші, яких годують кормом з високим вмістом жиру, та щури, яких годують сахарозою-лярдом, ліганди PPAR-α поліпшують чутливість до інсуліну та стан при ожирінні. Крім того, було виявлено взаємодію ліпідзнижувальної активності статинів з рецепторами PPAR-α на додаток до обмеженої доступності холестерину. Деякі клінічні випробування виявили поліпшення показників чутливості до інсуліну при застосуванні фібратів [Guerre-MiIIo M, Rounalt C. and Poulain P; Diabetes; 2001; 50; 2809-2814, Muoio D. M., Wa y J. M. and Tanner C. J.; Diabetes; 2002; 51; 901-909, Ye J, Doyle P. J. and lglesias M. A.; Diabetes; 2001; 50; 411-417, та Roglans N, Sanguino E. and Peris C; JPET; 2002; 302; 232-239]. Таким чином, існують цікаві свідчення того, що агоністи PPAR-α можуть бути використані для контролю ліпідів і, за останніми даними, навіть для поліпшення чутли вості до інсуліну. Обмеження існуючих зараз засобів лікарської терапії у поєднанні із зростаючим поширенням ліпідних аномалій в усьому світі вимагають вмявлення більш сильнодіючих та безпечних агоністів PPAR-α. У продовження наших досліджень агоністів PPAR [патенти США №№5885997, 6054453, 6265401; заявка РСТ/ІВ02/04275] з метою задоволення цих потреб, було синтезовано ряд сполук, які розкриті у даному винаході. Було описано декілька алкілкарбонових кислот, їхніх похідних та їхніх аналогів, придатних для використання у лікуванні гіперглікемії та гіперхолестеринемії. Деякі з таких сполук, описаних у відомому рівні техніки, вказані нижче: і) [Пат. США №5306726, WO 91/19702], розкривають кілька похідних 3-арил-2-оксипропіонової кислоти загальних формул (llа) та (llb) як гіполіпідемічні та гіпоглікемічні агенти. 12 (Ilc) (Ild) іі) [Міжнародні публікації №№WO 95/03038 та WO 96/04260] розкривають сполуки формули (llе) (Ile) Приклад цих сполук представлений ормулою (Ilf) (Ilf) Ні) [Міжнародні публікації №№WO 94/13650, WO 94/01420 та WO 95/17394] розкривають сполуки загальної формули (Ilg) (Ilg) Приклад цих сполук представлений формулою (Il п) (Ilh) iv) [Міжнародна публікація №WO 00/49005] розкриває сполуки загальної формули (Ilі) (Ili) Приклад цих сполук представлений формулою (Ilj) (Ilj) v) [Міжнародна публікація №WO 94/12181] розкриває сполуки загальної формули (Ilk) (Ilk) Приклад цих сполук представлений формулою (Il І) (Ill) vi) [Міжнародна публікація №WO 93/16697 та патент США №5227490] розкривають сполуки загальної формули (Ilm) (Ilm) Приклади цих сполук представлені формулами (llc) та (lld) Приклад цих сполук представлений формулою (Iln) (Iln) 13 82835 vii) [Міжнародні публікація №WO 99/62871] розкриває сполуки загальної формули (Ilо) (Ilo) де А знаходиться у орто-, мета- чи параположенні і позначає 14 ристовувалися як проміжні сполуки для синтезу цільових молекул. Деякі з таких сполук, описаних у відомому рівні техніки, вказані нижче: і) [Європейська патентна заявка ЕРО 816316] розкриває сполуку формули (va) (va) Сполуку формули (va) далі перетворюють на 1,2-етандіольне похідне формули (vb) Приклад цих сполук представлений формулою (Ilр) (vb) (Ilp) viii) [Міжнародна публікація №WO 00/64888] розкриває сполуки загальної формули (llq) Ці 1,2-етандіольні похідні є корисними проміжними сполуками для фармацевтичних та сільськогосподарських хімікатів. іі) [Патентна заявка Японії JP 10017540] розкриває сполуку формули (vc) (Ilq) (vc) Приклад цих сполук представлений формулою Сполуку формули (vc) далі перетворюють на сполуку формули (vd) (llr) (Ilr) іх) [Міжнародна публікація №WO 99/62872] розкриває сполуки формули (lls) (Ils) х) [Міжнародна публікація №WO 00/63153] розкриває сполуки формули (llt) (Ilt) (llu) Приклад цих сполук представлений формулою (Ilu) хі) [Міжнародна публікація №WO 01/55085] розкриває сполуки формули (llv) (Ilv) Приклад цих сполук представлений формулою (llw) (Ilw) Були описані кілька похідних (β-феніл-αгідроксизаміщеної пропіонової кислоти, що вико (vd) Метою даного винаходу є створення нових сполук загальної формули (I), які мають переважно PPARα-агоністичну активність з істотно зниженою токсичністю, асоційованою з PPARγактивацією, придатних для зниження глюкози крові, рівнів ліпідів, зниження холестерину та зменшення ваги тіла з корисними ефектами при лікуванні та/або профілактиці хвороб, пов'язаних з підвищеними рівнями ліпідів, атеросклерозу, захворювань коронарної артерії, синдрому X, порушеної толерантності до глюкози, інсулінорезистентності, інсулінорезистентності, що приводить до діабету типу 2 та його діабетичних ускладнень, для лікування хвороб, патофізіологічним механізмом яких є інсулінорезистентність, та для лікування гіпертензії, з кращою ефективністю, дієвістю та меншою токсичністю, для чого ми зосередили наші дослідження на розробці нових сполук, ефективних для лікування вищезгаданих хвороб. Зусилля в цьому напрямку привели до створення сполук, що мають загальну формулу (І). Таким чином, головним аспектом даного винаходу є створення нових алкілкарбонових кислот загальної формули (І), їхні х похідних, їхні х аналогів, їхніх та утомерних форм, їхніх стереоізомерів, їхні х поліморфів, їхніх фармацевтично прийнятних солей, їхніх фармацевтично прийнятних сольватів та фармацевтичних композицій, що їх містять, чи їхні х сумішей. Іншим аспектом даного винаходу є створення нових алкілкарбонових кислот, їхніх похідних, їхніх аналогів, їхніх та утомерних форм, їхніх стереоізо 15 82835 мерів, їхніх поліморфів, їхніх фармацевтично прийнятних солей, їхніх фармацевтично прийнятних сольватів та фармацевтичних композицій, що їх містять, чи їхніх сумішей, які можуть мати агоністичну активність по відношенню до PPARα та/або PPAR γ і, необов'язково, інгібувати HMG СоАредуктазу, на додаток до наявності агоністичної активності по відношенню до PPARα та/або PPAR γ. Ще іншим аспектом даного винаходу є створення способу одержання алкілкарбонових кислот формули (І), їхні х похідних, їхніх аналогів, їхніх таутомерних форм, їхніх стереоізомерів, їхніх поліморфів, їхні х фармацевтично прийнятних солей та їхніх фармацевтично прийнятних сольватів. Ще іншим аспектом даного винаходу є створення фармацевтичних композицій, що містять сполуки загальної формули (І), їхні аналоги, їхні похідні, їхні таутомери, їхні стереоізомери, їхні поліморфи, їхні солі, сольвати чи їхні суміші у комбінації з придатними носіями, розчинниками, розріджувачами та іншими середовищами, звичайно використовуваними для виготовлення таких композицій. Іншим аспектом даного винаходу є створення нових проміжних сполук, способу їхнього одержання та використання проміжних сполук у способах одержання алкілкарбонових кислот формули (І), їхні х похідних, їхні х аналогів, їхні х та утомерів, їхні х стереоізомерів, та їхнє використання як антидіабетичних, гіполіпідемічних, гіпохолестеринемічних сполук та засобів проти ожиріння. Нові β-арил-α-оксизаміщені протонові кислоти загальної формули (І) (I) їхні похідні, їхні аналоги, їхні таутомерні форми, їхні стереоізомери, їхні поліморфи, їхні фармацевтично прийнятні солі, їхні фармацевтично прийнятні сольвати, де: R1 позначає гідроген, гідроксильну гр упу, галоген, лінійний чи розгалужений (С1-С12)-алкіл, лінійну чи розгалужену (С1-С12)алкоксигрупу, заміщену чи незаміщену арилалкільну груп у або утворює зв'язок разом із сусідньою групою R2; R2 позначає гідроген, галоген, лінійний чи розгалуженмй (С1-С12)-алкіл, лінійну чи розгалужену (С1-С12)-алкоксигрупу, (С1-С12)-алканоїл, ароїл, арилалканоїл, заміщений чи незаміщений арилалкіл, або R2 утворює зв'язок разом з R1; R3 позначає атом гідрогену або заміщені чи незаміщені групи, вибрані з лінійної чи розгалуженої (С1С12)-алкільної, циклоалкільної, циклоалкілалкільної, циклоалкенільної, арильної, (С1-С12)алканоїльної, ароїльної, арилалкільної, арилалканоїльної, одновалентної гетероциклічної, гетероарильної, гетероарилалкільної, алкоксіалкільної, алкоксикарбонільної, арилоксикарбонільної, алкіламінокарбонільної чи ариламінокарбонільної груп; R4 позначає гідроген або заміщені чи незаміщені групи, вибрані з лінійної чи розгалуженої (С1С12)-алкільної, циклоалкільної, арильної, арилалкільної, одновалентної гетероциклічної, гетероари 16 льної чи гетероарилалкільної груп; Y позначає оксиген або NR7 чи N(R7)O, де R7 позначає гідроген або заміщені чи незаміщені групи, вибрані з лінійної чи розгалуженої (С1-С12)-алкільної, арильної, арилалкільної, гідроксіалкільної, алканоїльної, ароїльної, арилалканоїльної, одновалентної гетероциклічної, гетероарильної, гетероарилалкільної, алкоксикарбонільної чи арилалкоксикарбонільної груп; R4 та R7 разом можуть утворювати заміщену чи незаміщену 5- чи б-членну циклічну стр уктур у, що містить атоми карбону, атом нітрогену, яка може додатково містити один чи кілька додаткових гетероатомів, вибраних з оксигену, сульфуру чи нітрогену; R5 позначає гідроген або заміщені чи незаміщені групи, вибрані з алкільної, алкенільної, циклоалкільної, циклоалкілалкільної, арильної, арилалкільної, ароїльної чи аралканоїльної груп; n та m є цілими числами в інтервалі 0-6; Ar позначає заміщені чи незаміщені групи, вибрані з двовалентного фенілену, нафтилену, піридилу, хінолінілу, бензофурилу, дигідробензофурилу, бензопіранілу, дигідробензопіранілу, індолілу, індолінілу, азаіндолілу, азаіндолінілу, піразолілу, бензотіазолілу, бензоксазолілу і т.п. Замісники на групі, позначеній Ar, можуть бути вибрані з лінійного чи розгалуженого, необов'язково, галогенованого (С1-С6)-алкілу, необов'язково галогенованої (С1С3)-алкоксигрупи, галогену, ацилу, такого як ацетил, COC2H5, бутаноїлу, пентаноїлу, пропіонілу, бензоїлу і т.п., аміногруп, ациламіногруп, таких як NHCOCH3, NHCOC2H5, NHCOC3H7 and NHCOC6H5 і т.п.; тіо- чи карбонових чи сульфонових кислот та їхні х похідних. Похідні карбонової кислоти та сульфонової кислоти включають аміди, хлорангідриди, складні ефіри та ангідриди карбонової кислоти та сульфонової кислоти. X позначає -С(=O)-, -C(=S)-, -C(=S)-O, -С(=O)O-, -C(=O)-S-, -O-(CH 2)d-, -NH-(CH2)d-, -O-С(=O)-, C(O)CH2-, -CRa=CRb-CH2-; -CRa=CRb-CO-, де Ra та Rb можуть бути однаковими чи різними і позначають гідроген чи (С1-С6)-алкіл; d має значення від 1 до 4; або X позначає зв'язок; R6 позначає заміщену чи незаміщену гр упу, вибрану з арилоксикарбонілу, арилалкоксикарбонілу, алкілкарбонілоксигрупи, алкоксикарбоніламіногрупи, арилоксикарбоніламіногрупи, арилалкоксикарбоніламіногрупи, флуоренілметоксикарбонілу (Fmoc), флуоренілметоксикарбоніламіногрупи (N-Fmoc), -OSO2R8, OCONR8R9, NR8COOR9, -NR8COR9, -NR8SO 2R9, NR8CONR9R10, -NR8CSNR8R9, -SO2R8, -SOR 8, -SR8, -SO2NR8R9, -SO2OR 8, -COOR 9, -COR 9 , -CONR8R9, де R8, R9 та R10 можуть бути однаковими чи різними і незалежно позначають гідроген або заміщений чи незаміщений алкіл, арил, арилалкіл, алкоксикарбоніл чи арилалкоксикарбоніл; R8 та R9, коли вони знаходяться на атомі нітрогену, разом можуть утворювати 5- чи 6-членну циклічну стр уктуру, що містить атоми карбону та один чи кілька гетероатомів, вибраних з оксигену, сульфуру чи нітрогену. R6 позначає гідроген, якщо R13 знаходиться у положенні 3 фенільного кільця і не позначає гідроген. R13 позначає гідроген, галоген, нітрогрупу, цізногрупу, аміногрупу, галоїдалкіл, гідроксильну гру 17 82835 пу або заміщену чи незаміщену групу, вибрану з лінійного чи розгалуженого (С1-С12)-алкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, одновалентного гетероциклічного радикала, алкоксигрупи, моноалкіламіногрупи, діалкіламіногрупи, алкоксикарбонілу, арилоксикарбонілу, арилалкоксикарбонілу, арилоксигрупи, арилалкоксигрупи, алкілкарбонілоксигрупи, алкоксикарбонілу, аміногрупи, арилоксикарбоніламіногрупи, арилалкоксикарбоніламіногрупи, флуоренілметоксикарбонілу (Fmoc), флуоренілметоксикарбоніламіногрупи (NFmoc), -OSO2R8, -OCONR 8R9, NR8COOR9 , NR8COR9, -NR8R9, -NR8SO2R9, -NR8CONR9R10, NR8CSNR8R9, -SO2R8, -SOR 8, -SR8 , -SO2NR8R9 , SO2OR8 , -COOR 9 , -COR 9 , -CONR8R9, де R8, R9 та R10 можуть бути однаковими чи різними і незалежно позначають гідроген або заміщений чи незаміщений алкіл, арил, арилалкіл, алкоксикарбоніл чи арилалкоксикарбоніл; R8 та R9, коли вони знаходяться на атомі нітрогену, разом можуть утворювати 5- чи 6-членну циклічну структур у, що містить атоми карбону та один чи кілька гетероатомів, вибраних з оксигену, сульфур у чи нітрогену. Придатні групи, представлені R1, можуть бути вибрані з гідрогену, гідроксигрупи, галогену, лінійної чи розгалуженої (С1-С12)-алкільної групи, краще, (Сі-Сб)-алкільних груп, таких як метил, етил, пропіл, ізопропіл чи трет-бутил; лінійної чи розгалуженої (С1-С12)-алкоксигрупи, краще, лінійної чи розгалуженої (Сі-Сб)-алкоксигрупи, такої як метоксигрупа, етоксигрупа, пропоксигрупа, ізопропоксигрупа і т.п.; заміщеного чи незаміщеного арилалкілу, такого як бензил, фенетил і т.п., або R1 разом з R2 можуть утворювати зв'язок. Арилалкіл може бути заміщеним (Сі-Сб)-алкільною, (СгСб)алкоксильною чи гідроксильною групою. Придатні групи, представлені R2, можуть бути вибрані з гідрогену, галогену, лінійних чи розгалужених (С1-С12)-алкільних, краще, лінійних чи розгалужених (С1-С6)-алкільних груп, таких як метил, етил, пропіл, ізопропіл чи т-бутил; лінійних чи розгалужених (С1-С12)-алкоксигруп, краще, лінійних чи розгалужених (С1-С6)-алкоксигруп, таких як метоксигрупа, етоксигрупа, пропоксигрупа, ізопропоксигрупа і т.п.; (С1-С12)-алканоїлу, такого як ацетил, пропаноїл, бутаноїл, пентаноїл і т.п.; ароїлу, такого як бензоїл і т.п.; арилалканоїлу, такого як фенілацетил, фенілпропаноїл і т.п. або заміщеного чи незаміщеного арилалкілу, такого як бензил, фенетил і т.п., або R2 разом з R1 можуть утворювати зв'язок. Арилалкіл може бути заміщеним (С1-С6)алкілом, (С1-С6)-алкоксигрупою чи гідроксильною групою. Придатні групи, представлені R3, можуть бути вибрані з гідрогену, заміщеної чи незаміщеної, лінійної чи розгалуженої (С1-С12)-алкільної групи, такої як метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, т-бутил, пентил, гексил, гептил, октил і т.п.; заміщеної чи незаміщеної (С1-С12)алканоїльної групи, краще, (C2-C8)-алканоїльної групи, ткої як ацетил, пропаноїл, бутаноїл, пентаноїл і т.п.; ароїльної фупи, такої як бензоїл і т.п., яка може бути заміщеною; арилалканоїльної групи, такої як фенілацетил, фенілпропаноїл і т.п., яка може бути заміщеною; (С3-С7)-циклоалкільної 18 групи, такої як циклопропіл, циклобутил, циклопентил, циклогексил, і т.п., причому циклоалкільна група може бути заміщеною; (С3-С7)циклоалкілалкільної групи, такої як циклогексилметил, циклогексилетил, циклогексилпропіл, циклогексилбутил і т.п., яка може бути заміщеною; (С3-С7)-циклоалкенільної групи, такої як циклопропеніл, циклобутеніл, циклопентеніл, циклосексеніл і т.п., причому циклоалкенільна група може бути заміщеною; арильної групи, такої як феніл, нафтил і т.п., причому арильна група може бути заміщеною; арилалкілу, такого як бензил, фенетил, С6Н5СН2СН2СН2, нафтилметил і т.п., причому арилалкільна група може бути заміщеною; групи одновалентного гетероциклічного радикала, такого як азиридиніл, піролідиніл, піперидиніл і т.п., причому група одновалентного гетероциклічного радикала може бути заміщеною; гетероарильної групи, такої як піридил, тієніл, фурил і т.п., причому гетероарильна група може бути заміщеною; гетероарилалкільної групи, такої як фуранметил, піридинметил, оксазолметил, оксазолетил і т.п., причому гетероарилалкільна група може бути заміщеною; (С1-С6)-алкоксі-(С1-С6)-алкільної групи, такої як метоксиметил, етоксиметил, метоксіетил, етоксипропіл і т.п., причому алкоксіалкільна група може бути заміщеною; (С1-С6)-алкоксикарбонілу, такого як метоксикарбоніл, етоксикарбоніл, пропоксикарбоніл і т.п., який може бути заміщеним; арилоксикарбонілу, такого як феноксикарбоніл, нафтилоксикарбоніл і т.п., який може бути заміщеним; (С1-С6)-алкіламінокарбонілу, такого як метиламінокарбоніл, етиламінокарбоніл, пропіламінокарбоніл і т.п., який може бути заміщеним; і ариламінокарбонілу, такого як PhNHCO, нафтиламінокарбоніл і т.п., який може бути заміщеним. Замісники на групі, представленій R3, можуть бути вибрані з галогену, гідроксильної групи, ціаногрупи чи нітрогрупи або заміщених чи незаміщених гр уп, вибраних з алкілу, циклоалкілу, алкоксигрупи, циклоалкоксигрупи, такої як циклопропілоксигрупа, циклобутилоксигрупа, циклопентилоксигрупа, циклогексилоксигрупа і т.п.; арилалкоксіалкілу, такого як бензилокси-СН 2-, бензилокси-СН 2-СН2, нафтилокси-СН2-, 2-фенетилокси-СН 2-і т.п.; арилу, арилалкілу, одновалентного гетероциклічного радикала, гетероарилу, гетероарилалкілу, ацилу, ацилоксигрупи, такої як OCOMe, OCOEt, OCOPh і т.п.; гідроксіалкілу, аміногрупи, ациламіногрупи, такої як NHCOCH3, NHCOC2H5 і т.п.; ариламіногрупи, такої як HNC6H5, NCH3(C6H5), NHC6H4CH3, NHC6H4-HaI і т.п.; аміноалкілу, арилоксигрупи, алкоксикарбонілу, алкіламіногрупи, такої як NHCH3, NHC 2H5, NHC3H7, N(CH3J2, NCH3(C2H5), N(C2H5)2 і т.п.; алкоксіалкілу, алкілтіогрупи, такої як метилтіогрупа, ( етилтіогрупа, пропілтіогрупа, ізопропілтіогрупа і т.п.; тіоалкілу, такого як тіометил, тіоетил, тіопропіл і т.п.; карбонової кислоти чи її похідних або сульфонової кислоти чи її похідних. Похідні карбонової кислоти та сульфонової кислоти включають аміди, хлорангідриди, складні ефіри та ангідриди карбонової кислоти та сульфонової кислоти. Придатні групи, представлені R4, можуть бути вибрані з гідрогену, заміщеної чи незаміщеної лінійної чи розгалуженої (С1-С12)-алкільної групи, 19 82835 такої як метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, пентил, гексил, гептил, октил і т.п.; (С3С7)-циклоалкілу, такого як циклопропіл, циклопентил, циклогексил і т.п., причому циклоалкільна група може бути заміщеною; арильної групи, такої як феніл, нафтил і т.п., причому арильна група може бути заміщеною; арилалкільної групи, такої як бензил та фенетил, причому арилалкільна група може бути заміщеною; групи одновалентного гетероциклічного радикала, такої як азиридиніл, піролідиніл, піперидиніл і т.п., причому група одновалентного гетероциклічного радикала може бути заміщеною; гетероарильної групи, такої як піридил, тієніл, фурил і т.п., причому гетероарильна група може бути заміщеною; гетероарилалкільної групи, такої як фуранметил, піридинметил, оксазолметил, оксазолетил і т.п., причому гетероарилалкільна група може бути заміщеною. Замісниками на групі, представленій R4, можуть бути такі групи, як циклопропілоксигрупа, циклобутилоксигрупа, циклопентилоксигрупа, циклогексилоксигрупа і т.п.; арилалкоксіалкіл, такий як бензилокси-СН 2-, бензилокси-СН 2-СН2, нафтилокси-СН 2-, 2-фенетилокси-СН 2- і т.п.; арил, арилалкіл, одновалентний гетероциклічний радикал, гетероарил, гетероарилалкіл, ацил, ацилоксигрупа, така як OCOMe, OCOEt, OCOPh і т.п.; гідроксіалкіл, аміногрупа, ациламіногрупа, така як NHCOCH3, NHCOC2H5 і т.п.; ариламіногрупа, така як HNC6H5, NCH3(C6H5), NHC6H4CH3, NHC6H4-HaI і т.п.; аміноалкіл, арилоксигрупа, алкоксикарбоніл, алкіламіногрупа, така як NHCH3, NHC2H5, NHC3H7, N(CH3J2, NCH3(C2H5), N(C2H5)2 і т.п.; алкоксіалкіл, алкілтіогрупа, така як метилтіогрупа, етилтіогрупа, пропілтіогрупа, ізопропілтіогрупа і т.п.; тіоалкіл, такий як тіометил, тіоетил, тіопропіл і т.п., карбонова кислота чи її похідні або сульфонова кислота чи її похідні. Придатні групи, представлені R5, можуть бути вибрані з гідрогену, заміщеної чи незаміщеної лінійної чи розгалуженої (С1-С16)-алкільної, краще, (С1-С12)-алкільної групи, такої як метил, етил, нпропіл, ізопропіл, н-бутил, ізобутил, пентил, гексил, гептил, октил і т.п.; заміщеного чи незаміщеного лінійного чи розгалуженого (С2-С8)-алкенту, такого як етеніл, н-пропеніл, н-бутеніл, ізобутеніл, н-пентеніл, гексеніл, гептеніл і т.п.; (С3-С7)циклоалкільної групи, такої як циклопропіл, циклобутил, циклопентил, іциклогексил і т.п., причому циклоалкільна група може бути заміщеною; (С3С7)-циклоалкіл-(С1-С10)-алкільної групи, такої як циклогексилметил, циклогексилетил, циклогексилпропіл, циклогексилбутил і т.п., яка може бути заміщеною; арильної групи, такої як феніл, нафтил і т.п., причому арильна група може бути заміщеною; арилалкілу, такого як бензил, фенетил, C6H5CH2CH2CH2, нафтилметил і т.п., причому арилалкільна група може бути заміщеною; ароїлу, такого як бензоїл і т.п., який може бути заміщеним; аралканоїлу, такого як фенілацетил, фенілпропаноїл і т.п., який може бути заміщеним. Замісники на групі, представленій R5, можуть бути вибрані з галогену, гідроксильної групи, , нітрогрупи, алкілу, циклоалкілу, алкоксигрупи, арилу, арилалкілу, арилалкоксіалкілу, такого як C6H5CH2OCH2-, 20 С6Н5СН2ОСН2СН2-, С6Н5СН2СН2ОСН2СН2-, C6H5CH2CH2OCH2- і т.п.; одновалентного гетероциклічного радикала, гетероарилу та аміногрупи. Придатні групи, представлені R6, можуть бути вибрані з незаміщеної чи заміщеної арилоксикарбонільної групи, такої як феноксикарбоніл, нафтилоксикарбоніл і т.п.; арилалкоксикарбонільної групи, такої як бензилоксикарбоніл, фенетилоксикарбоніл, нафтилметоксикарбоніл і т.п., яка може бути заміщеною; алкілкарбонілоксигрупи, такої як метилкарбонілоксигрупа, етилкарбонілоксигрупа, пропілкарбонілоксигрупа і т.п., яка може бути заміщеною; алкоксикарбоніламіногрупи, такої як метоксикарбоніламіногрупа, етоксикарбоніламіногрупа, пропоксикарбоніламіногрупа, бутоксикарбоніламіногрупа, тбутоксикарбоніламіногрупа і т.п., яка може бути заміщеною; арилоксикарбоніламіногрупи, такої як NHCOOC6H5, N(CH3)COOC 6H5, N(C2H5)COOC 6H5, NHCOOC6H4CH3, NHCOOC 6H4OCH3 і т.п., яка може бути заміщеною; арилалкоксикарбоніламіногрупи, такої як NHCOOCH 2C6H5, NHCOOCH2CH2C6H5, N(CH3)COOCH2C6H5, N(C2H5)COOCH2C6H5, NHCOOCH2C6H4CH3, NHCOOCH2C6H4OCH3 і т.п., яка може бути заміщеною; флуоренілметоксикарбонілу (Fmoc), флуоренілметоксикарбоніламіногрупи (N-Fmoc), OSO2R8 , -OCONR 8R9, NR8COOR 9, -NR8COR9, NR8SO2R9, NR8CONR9R10, -NR8CSNR8R9, -SO2R 8, SOR8, -SR8 , -SO 2NR8R9, -SO2OR8 , -COOR 9, -COR 9 чи -CONR8R9. R6 позначає гідроген, якщо R13 знаходиться у положенні 3 фенільного кільця і не позначає гідроген. Якщо групи, представлені R6, є заміщеними, замісники можуть бути вибрані з галогену, гідроксильної групи, нітрогрупи, алкілу, циклоалкілу, алкоксигрупи, арилу, арилалкілу чи аміногрупи. Придатні групи, представлені R13, можуть бути вибрані з гідрогену, атома галогену, такого як флюор, хлор, бром чи йод; гідроксильної групи, аміногрупи, нітрогрупи, ціаногрупи або незаміщеної чи заміщеної лінійної чи розгалуженої (С1-С12)алкільної групи, такої як метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, т-бутил, пентил, гексил, гептил, октил і т.п.; галоїдалкілу, такого як трифлюорметил і т.п.; (С1-С6)-алкоксигрупи, такої як метоксигрупа, етоксигрупа, пропоксигрупа і т.п., яка може бути заміщеною; арильної групи, такої як феніл, нафтил і т.п., причому арильна група може бути заміщеною; арилалкілу, такого як бензил, фенетил,- C6H5CH2CH2CH2, нафтилметил і т.п., причому арилалкільна група може бути заміщеною»; гетероарильної групи, такої як піридил, тієніл, фурил, піроліл, оксазоліл, тіазоліл, імідазоліл, оксадіазоліл, тетразоліл, бензопіраніл, бензофураніл і т.п., причому гетероарильна група може бути заміщеною; гетероарилалкільних груп, таких як фуранметил, піридинметил, оксазолметил, оксазолетил і т.п., причому гетероарилалкільна група може бути заміщеною; груп одновалентного гетероциклічного радикала, таких як азиридиніл, піролідиніл, морфолініл, піперидиніл, піперазиніл і т.п., причому група одновалентного гетероциклічного радикала може бути заміщеною; моноалкіламіногрупи, такої як NHCH3, NHC2H5, NHC 3H7, 21 82835 NHC6H13 і т.п., яка може бути заміщеною; діалкіламіногрупи, такої як N(CH3)2, NCH3(C2H5), N(C2H5)2 і т.п., яка може бути заміщеною; алкоксикарбонілу, такого як метоксикарбоніл, етоксикарбоніл, пропоксикарбоніл, бутоксикарбоніл, тбутоксикарбоніл і т.п., який може бути заміщеним; арилоксикарбонільної групи, такої як феноксикарбоніл, нафтилоксикарбоніл і т.п., яка може бути заміщеною; арилалкоксикарбонільної групи, такої як бензилоксикарбоніл, фенетилоксикарбоніл, нафтилметоксикарбоніл і т.п., яка може бути заміщеною; арилоксигрупи, такої як феноксигрупа, нафтилоксигрупа і т.п., причому арилоксигрупа може бути заміщеною; арилалкоксигрупи, такої як бензилоксигрупа, фенетилоксигрупа, нафтилметилоксигрупа, фенілпропілоксигрупа і т.п., причому арилалкоксигрупа може бути заміщеною; алкілкарбонілоксигрупи, такої як метилкарбонілоксигрупа, етилкарбонілоксигрупа, пропілкарбонілоксигрупа і т.п., яка може бути заміщеною; алкоксикарбоніл аміногрупи, такої як метоксикарбоніламіногрупа, етоксикарбоніламіногрупа, пропоксикарбоніламіногрупа, бутоксикарбоніламіногрупа, т-бутоксикарбоніламіногрупа і т.п., яка може бути заміщеною; арилоксикарбоніламіногрупи, такої як NHCOOC6H5, N(CH3)COOC 6H5, N(C2H5)COOC 6H5, NHCOOC 6H4CH3, NHCOOC6H4OCH3 і т.п., яка може бути заміщеною; арилалкоксикарбоніламіногрупи, такої як NHCOOCH2C6H5, NHCOOCH2CH2C6H5, N(CH3)COOCH2C6H5, N(C2H5)COOCH2C6H5, NHCOOCH2C6H4CH3, NHCOOCH2C6H4OCH3 і т.п., яка може бути заміщеною; флуоренілметоксикарбонілу (Fmoc), флуоренілметоксикарбоніламіногрупи (N-Fmoc), -OSO2R8, -OCONR 8R9, 8 9 8 9 8 9 NR COOR , -NR COR , -NR R , -NR8SO 2R9, 8 9 10 8 8 9 NR CONR R , -NR CSNR R , -SO2R8, -SOR 8, -SR8, -SO2NR8R9, -SO2 OR8, -COOR 9, -COR 9, -CONR 8R9 . Якщо групи, представлені R13, є заміщеними, замісники можуть бути вибрані з галогену, гідроксильної групи, нітрогрупи, алкілу, циклоалкілу, алкоксигрупи, арилу, арилалкілу чи аміногрупи. Придатні групи, представлені R8, R9, R10, можуть бути вибрані з гідрогену, незаміщеної, лінійної чи розгалуженої (С1-С12)-алкільної групи, такої як метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, т-бутил, пентил, гексил, октил і т.п.; арильної групи, такої як феніл, нафтил і т.п., причому арильна група може бути заміщеною; арилалкілу, такого як бензил, фенетил, C6H5CH2CH2CH2, нафтилметил і т.п., причому арилалкільна група може бути заміщеною; алкоксикарбонільної групи, такої як т-бутилоксикарбоніл (BOC) і т.п.; арилалкоксикарбонільних груп, таких як бензилоксикарбоніл (CBZ) і т.п. R8 та R9, коли вони знаходяться на атомі нітрогену, разом можуть утворювати 5- чи 6членну циклічну кільцеву систему, що містить атоми карбону, щонайменше один нітроген і, необов'язково, один чи кілька гетероатомів, вибраних з оксигену, суль фуру чи нітрогену, причому циклічна кільцева система може містити один чи два подвійних зв'язків або може бути ароматичною. Замісники на групах, представлених R8 , R9 та R 10, можуть бути вибрані з галогену, гідроксильної групи, алкоксигрупи, ціаногрупи, нітрогрупи, алкілу, 22 циклоалкілу, арилу, арилалкілу, ацилу, ацилоксигрупи, гідроксіалкілу, аміногрупи, арилоксигрупи, алкілтіогрупи чи тіоалкільної групи. Придатні групи, представлені R7, можуть бути вибрані з гідрогену або заміщеного чи незаміщеного, лінійного чи розгалуженого (С1-С12)-алкілу; арильної групи, такої як феніл, нафтил і т.п., причому арильна група може бути заміщеною; гідроксі-(С1-С6)-алкілу, який може бути заміщеним; арилалкільної групи, такої як бензил та фенетил і т.п., яка може бути заміщеною; групи одновалентного гетероциклічного радикала, такого як азиридиніл, піролідиніл, піперидиніл і т.п., яка може бути заміщеною; гетероарильної групи, такої як піридил, тієніл, фурил і т.п., яка може бути заміщеною; гетероарилалкільної групи, такої як фуранметил, піридинметил, оксазолметил, оксазолетил і т.п., яка може бути заміщеною; лінійної чи розгалуженої (С2-С8)-алканоїльної групи, такої як ацетил, пропаноїл, бутаноїл, пентаноїл і т.п., яка може бути заміщеною; ароїльної групи, такої як бензоїл і т.п., яка може бути заміщеною; арилалканоїльної групи, такої як фенілацетил, фенілпропаноїл і т.п., яка може бути заміщеною; алкоксикарбонільної групи, такої як т-бутилоксикарбоніл і т.п.; арилалкоксикарбонільних груп, таких як бензилоксикарбоніл і т.п. Замісники групи, представленої R7, можуть бути вибрані з галогену, гідроксильної групи, алкоксигрупи, ціаногрупи, нітрогрупи, алкілу, циклоалкілу, арилу, арилалкілу, ацилу, ацилоксигрупи, гідроксіалкілу, аміногрупи, арилоксигрупи, алкілтіогрупи чи тіоалкільної групи. Придатні кільцеві структури, утворені R4 та R7 разом, можуть бути вибрані з піролідинілу, піперидинілу, морфолінілу, піперазинілу, оксазолінілу і т.п. Придатні замісники на циклічній структурі, утвореній взятими разом R4 та R7, можуть бути вибрані з гідроксильної групи, алкілу, оксогрупи, арилалкілу і т.п. Придатні групи, представлені Ar, можуть бути вибрані із заміщеної чи незаміщеної двовалентної феніленової, нафтиленової, бензофурильної, індолільної, індолінільної, хінолінільної, азаіндолільної, азаіндолінільної, бензотіазолільної чи бензоксазолільної груп, які можуть бути незаміщеними чи заміщеними алкільними, галоїдалкільними, метоксильними чи галоїдалкоксильними групами. Придатні n та m є цілими числами в інтервалі значень 0-6. Придатні X позначають -С(=О)-, -O(CH2)d (де d позначає ціле число від 1 до 4), -C(=S)-, O-C(=O)-, -C(O)CH2-, -CH=CH-CH2-, -CHNCH-CO-, або X позначає зв'язок. Кращими сполуками за даним винаходом є такі сполуки формули (I)1 у яких: R1 позначає гідроген, лінійну чи розгалужену (С1-С8)-алкільну груп у або утворює зв'язок з R2. R2 позначає гідроген, лінійну чи розгалужену (С1-С6)-алкільну груп у або утворює зв'язок з R1. R3 позначає гідроген, лінійний чи розгалужений (С1-С12)-алкіл, (С3-С7)-циклоалкільну гр упу, арильну групу, таку як феніл, нафтил, або арилалкільну груп у. 23 82835 R4 позначає гідроген, лінійний чи розгалужений (С1-С12)-алкіл, (С3-С7)-циклоалкільну гр упу, арильну групу, таку як феніл, нафтил, або арилалкільну груп у. R5 позначає гідроген, (С1-С12)-алкільну чи (С3С7)-циклоалкільну гр упу. R6 позначає флуоренілметоксикарбоніл (Fmoc), флуоренілметоксикарбоніламіногрупу (NFmoc), -OSO2R8, -OCONR 8R9, NR8COOR9 , NR8COR9 чи -NR 8SO2R9 . R8 позначає гідроген, лінійний чи розгалужений (С1-С6)-алкіл або арильну гр упу, яка може бути заміщеною. R9 позначає гідроген, лінійний чи розгалужений (С1-С6^алкіл, т-бутилоксикарбонільну чи бензилоксикарбонільну гр упу. R13 позначає гідроген чи -OSO2R8 . X позначає -С(=O)-, O-С(=O)-, -O(CH2)d (де d позначає ціле число від 1 до 4), -C(=S)-, -CH=CHCH2-, -CH=CH-CO-, або X позначає зв'язок. Y позначає оксиген чи NR7. R7 позначає гідроген, заміщений чи незаміщений, лінійний чи розгалужений (С1-С12)-алкіл або арильну групу, причому арильна група може бути заміщеною; d позначає ціле число в інтервалі 1-4. m позначає ціле число від O дo 1. n позначає ціле число від O дo 2. Ще кращими сполуками за даним винаходом є такі сполуки формули (І), у яких: R1 позначає гідроген або утворює зв'язок з R 2. R2 позначає гідроген або утворює зв'язок з R 1. R3 позначає гідроген, лінійну чи розгалужену (С1-С12)-алкільну гр упу. R4 позначає гідроген, лінійну чи розгалужену (С1-С12)-алкільну гр упу. R5 позначає гідроген чи (С1-С12)-алкільну гр упу. R6 позначає -OSO2R8 чи -NR8SO2R9 . R5 позначає лінійний чи розгалуженмй (С1-С6)алкіл або заміщену арильну групу, у якій замісник є лінійною чи розгалуженою (С1-С6)-алкільною групою. R9 позначає лінійний чи розгалужений (С1-С6)алкіл, т-бутилоксикарбонільну чи бензилоксикарбонільну груп у. R13 позначає гідроген чи -OSO2R8 . X позначає -С(=О)-, О-С(-О)-, -O(CH2) d (d дорівнює 1-4), -CH=CH-CH 2-; -CH=CH-CO-, або X позначає зв'язок. Y позначає оксиген. Фармацевтично прийнятні солі, що утворюють частину даного винаходу, включають солі, утворені неорганічними основами, такими як Li, Na, K, Ca, Mg, Fe, Cu, Zn, Al, Mn; солі органічних основ, таких як N,N'-діацетилетилендіамін, бетаїн, кофеїн, 2діетиламіноетанол, 2-диметиламіноетанол, нетилморфолін, н-етилпіперидин, глюкамін, глюкозамін, гідрабамін, ізопропіламін, метилглюкамін, морфолін, піперазин, піперидин, прокаїн, теобромін, валінол, діетиламін, триетиламін, триметиламін, трипропіламін, трометамін, адамантиламін, діетаноламін, меглумін, етилендіамін, N,N'дифенілетилендіамін, N,N'-дибензилетилендіамін, н-бензилфенілетиламін, холін, холіну гідроксид, 24 дициклогексиламін, метформін, бензиламін, фенілетиламін, діалкіламін, триалкіламін, тіамін, амінопіримідин, амінопіридин, пурин, піримідин, спермідин і т.п.; хіральних основ, таких як алкілфеніламін, етаноламін, фенілетаноламін і т.п., солі природних амінокислот, таких як гліцин, аланін, валін, лейцин, ізолейцин, норлейцин, тирозин, цистин, цистеїн, метіонін, пролін, гідроксипролін, гістидин, орнітин, лізин, аргінін, серии, треонін, фенілаланін; неприродних амінокислот, таких як D-ізомери чи заміщені амінокислоти; солі кислотних амінокислот, таких як аспарагінова кислота, глутамінова кислота; гуанідину, заміщеного гуанідину, де замісники вибрані з нітрогрупи, аміногрупи, алкілу, алкенілу, алкінілу, амонієвих чи заміщених амонієвих солей. Солі можуть включати у належних випадках кислотно-адитивні солі, які можуть бути сульфа тами, нітратами, фосфатами, перхлоратами, боратами,' гідрогалогенідами (HCI, HBr, НІ), ацетатами, тартратами, малеатами, цитратами, сукцинатами, пальмоатами, метансульфонатами, бензоатами, саліцилатами, гідроксинафтоатами, бензолсульфонатами, аскорбатами, гліцерофосфатами, кетоглутаратами і т.п. Фармацевтично прийнятні сольвати можуть бути гідратами або включати інші розчинники кристалізації, такі як спирти. Особливо корисні сполуки за даним винаходом включають: етил-2-метокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонат чи його солі у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонат чи його солі у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-{3-(4етансульфонілоксифеніл)пропілоксикарбоніламіно}феніл]-пропіонат чи його солі у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-{3-(3метансульфонілоксифеніл)пропіламіно}феніл]пропіонат чи його солі у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-{3-(4-(толуол-4сульфонілокси)феніл)пропіламіно}феніл]пропіонат чи його солі у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[3-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонат чи його солі у формі окремих енантіомерів чи рацемату, етил-2-ізопропокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонат чи його солі у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-(4метилсульфонілоксифенетиламіно)феніл]пропіонат чи його солі у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-{4-[(E)-3-(4метилсульфонілоксифеніл)-2 25 пропеніламіно]феніл}-пропіонат чи його солі у формі окремих енантіомерів чи рацемату, метил-2-етокси-3-[4-(4метансульфонілоксибензиламіно)феніл]пропіонат чи його солі у формі окремих енантіомерів чи рацемату, 2-метокси-3-[4-{3-(4етансульфонілоксифеніл)пропіламіно}феніл]пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-{3-(4метансульфонілоксифеніл)пропілоксикарбоніламіно}феніл]-пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-{3-(3метансульфонілоксифеніл)пропіламіно}феніл]пропіонову кислоту чиїї солі у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-{3-(4-(толуол-4сульфонілокси)феніл)пропіламіно}феніл]пропіонат чи його солі у формі окремих енантіомерів чи рацемату, 2-етокси-3-[3-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, 2-ізопропокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-(4метансульфонілоксибензиламіно)феніл]пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-(4метилсульфонілоксифенетиламіно)феніл]пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, 2-етокси-3-{4-[(Е)-3-(4метилсульфонілоксифеніл)-2пропеніламіно]феніл}-пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-(4метилсульфонілоксибензилкарбоксамідо)феніл]пропіонат чи його солі у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-(4метилсульфонілоксибензилкарбоксамідо)феніл]пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-{3-(4-трет-бутокси-4метилсульфонамідофеніл)пропіламіно}феніл]пропіонат чи його солі у формі окремих енантіомерів чи рацемату, 82835 26 2-етокси-3-[4-{3-(4-трет-бутокси-4метилсульфонамідофеніл)пропіламіно}феніл]пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-(4-[(Е)-2-(4метилсульфонілоксифеніл)-1-етенілкарбоксамідо]феніл}пропіонат чи його солі у формі окремих енантіомерів чи рацемату, 2-етокси-3-{4-[(E)-2-(4метилсульфонілоксифеніл)-1етенілкарбоксамідо]феніл}-пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-[4-(4метилсульфонілоксифенетилкарбоксамідо)феніл]пропіонат чи його солі у формі окремих енантіомерів чи рацемату, 2-етокси-3-[4-(4метилсульфонілоксифенетенілкарбоксамідо)феніл]пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, етил-2-метокси-3-[4-{(E)-3-(4метилсульфонілоксифеніл)-2пропеніламіно}феніл]-пропіонат чи його солі у формі окремих енантіомерів чи рацемату, 2-метокси-3-[4-{(Е)-3-(4метилсульфонілоксифеніл)-2пропеніламіно}феніл]-пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, етил-2-метокси-3-[4-{3-(3метансульфонілоксифеніл)пропіламіно}феніл]пропіонат чи його солі у формі окремих енантіомерів чи рацемату, 2-метокси-3-[4-{3-(3метансульфонілоксифеніл)пропіламіно}феніл]пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, етил-2-етокси-3-{4-[(E)-3-(4метилсульфонілоксифеніл)-2пропеніл(феніл)карбокс-амідо]феніл}пропіонат чи його солі у формі окремих енантіомерів чи рацемату, 2-етокси-3-{4-[(Е)-3-(4метилсульфонілоксифеніл)-2пропеніл(феніл)карбоксамідо]-феніл]пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату, метил-2-метокси-3-{4-[(E)-3-(4метилсульфонілоксифеніл)-2-пропеніл(феніл)карбоксамідо]феніл}пропіонат чи його солі у формі окремих енантіомерів чи рацемату, 2-метокси-3-{4-[(E)-3-(4метилсульфонілоксифеніл)-2пропеніл(феніл)карбокс-амідо]феніл}пропіонову кислоту чи її солі у формі окремих енантіомерів чи рацемату. Згідно з даним винаходом, сполука загальної формули (І), де R1, R2, R3, R 4, R5 , R6 , R13, X1 Y, n, m та Ar мають вказані вище значення, може бути одержана будь-яким з таких шляхів, зображених на Схемі І нижче. 27 82835 Шлях (1): Реакція сполуки загальної формули (llIa), у якій всі символи мають вказані вище значення, зі сполукою формули (Illb), у якій Y має вказані вище значення, за винятком NH, R11 позначає лінійний чи розгалужений (С1-С6)-алкіл, а всі інші символи мають вказані вище значення, з одержанням сполуки загальної формули (І), де Y має вказані вище значення, за винятком NH, а всі інші символи мають вказані вище значення, може бути проведена у присутності основи, такої як гідриди лужних металів, такі як NaH чи KH; літійорганічні сполуки, такі як CH3Li, BuLi, LDA, TMEDA і т.п.; алкоксиди, такі як NaOMe, NaOEt, K+BuO- і т.п. чи їхні суміші. Реакція може бути проведена у присутності розчинників, таких як діетиловий ефір, ТГФ, діоксан, ДМФ, ДМСО, DME (диметиловий ефір етиленгліколю), толуол, бензол і т.п. чи їхні суміші. Як співрозчинник може бути використаний HMPA (гексаметилфосфорамід). Температура реакції може змінюватися в інтервалі від -78°C до 50°C, краще, в інтервалі температур від -10°C до 30°C. Реакція проходить більш ефективно у безводних умовах. Сполука загальної формули (llIb) може бути одержана за реакцією Арбузова (Annalen. Chemie, 1996, 53,699). За іншим варіантом втілення, сполука формули (І) може бути одержана шляхом проведення реакції сполуки формули (llIa), у якій всі символи мають вказані вище значення, з реагентами Віттіга, такими як Hal-Ph3P+CH-(OR3)CO2R4, за реакційних умов, аналогічних до описаних вище, де R3 та R4 мають вказані вище значення. Шлях (2): Реакція сполуки формули (llId), де R6 має вказані вище значення, NR8R9, Y має вказані вище значення, за винятком NH, а всі інші символи мають вказані вище значення, зі сполукою формули (llIc), де R3 має вказані вище значення, за винятком гідрогену, a L1 позначає відхідну гр упу, таку як атом галогену, п-толуолсульфонат, метансульфонат, трифлюорметансульфонат і т.п., з одержанням сполуки формули (І), може бути проведена у присутності розчинників, таких як діетиловий ефір, ТГФ, ДМФ, ДМСО, D ME, толуол, бензол і т.п. 28 Може підтримуватися інертна атмосфера шляхом використання інертних газів, таких як N2, Ar, Не і т.п. Реакція може бути проведена у присутності основи, такої як KOH, NaOH, NaOMe, t-BuO-K+, NaH, KH, LDA, NaHMDS, K2CO3, Na2CO3 і т.п. Може бути використаний каталізатор фазового перенесення, такий як галогеніди чи гідроксиди чи бісульфати тетраалкіламонію. Температура реакції може змінюватися в інтервалі від -20°C до 200°C, краще, в інтервалі температур від 0°C до 150°C. Тривалість реакції може змінюватися від 1 до 72 годин, краще, від 1 до 12 годин. Реакція може також бути проведена з використанням алкілувальних агентів, таких як діалкілсульфати, наприклад, діетилсульфат чи диметилсульфат; алкілгалогенідів, наприклад, метилйодиду, метилброміду, етилйодиду, етилброміду і т.п. Шлях (3): Реакція сполуки загальної формули (llla), у якій всі символи мають вказані вище значення, зі сполукою формули (llIe), де R 2 позначає атом гідрогену, Y має вказані вище значення, за винятком NH, а всі інші символи мають вказані вище значення, може бути проведена у присутності основи. Природа основи не є • критичною. Може бути використана будь-яка основа, що звичайно використовується для реакції альдольної конденсації; можуть бути використані такі основи, як гідрид металу, наприклад, NaH, KH, алкоксиди металів, такі як NaOMe, т-BuO-K+, NaOEt, аміди металів, такі як LiNH2, LiN(iPr)2. Можуть бути використані апротонні розчинники, такі як ТГФ, діетиловий ефір, діоксан. Реакція може бути проведена у інертній атмосфері, яка може підтримуватися шляхом використання інертних газів, таких як N2, Ar чи Не, причому реакція проходить більш ефективно у безводних умовах. Може бути використана температура в інтервалі від -80°C до 35°C. Одержаний спочатку р-гідроксилований продукт може бути дегідратований при звичайних умовах дегідратації, таких як обробка п-TSA у розчинниках, таких як бензол чи толуол. Природа розчинника та агента дегідратації є некритичними. Може бути використана температура в інтервалі від 20°C до 29 82835 температури кипіння зі зворотним холодильником використаного розчинника, краще, температура кипіння зі зворотним холодильником розчинника, при безперервному видаленні води за допомогою водяного сепаратора Діна-Старка. Шлях (4): Реакція сполуки формули (Illg), де R6, R13, X, n мають вказані вище значення, і L1 позначає відхідну групу, таку як атом галогену, наприклад, хлор чи бром чи йод, п-толуолсуль фонат, метансульфонат, трифлюорметансульфонат і т.п., краще, атом галогену, зі сполукою формули (llIf), де R1 та R2 разом позначають зв'язок, а всі інші символи мають вказані вище значення, з утворенням сполуки формули (І), визначеної вище, може бути проведена у присутності апротонних розчинників, таких як діетиловий ефір, ТГФ, ДМФ, ДМСО, DME, толуол, бензол, ацетон, ацетонітрил і т.п. чи їхні суміші. Реакція може бути проведена у інертній атмосфері, яка може підтримуватися шляхом використання інертних газів, таких як N2, Ar, Не і т.п. Реакція може бути проведена у присутності основи, такої як K2СО3, Na2CO3 чи NaH або їхні суміші. Температура реакції може змінюватися в інтервалі -20°C - 120°C, краще, в інтервалі температур 0°C - 120°C. Тривалість реакції може змінюватися від 1 до 48 годин. Може бути використаний каталізатор фазового перенесення, такий як галогеніди чи гідроксиди чи бісульфати тетраалкіламонію. Шлях (5): Реакція сполуки загальної формули (llIh), де R6, R13, X, n мають вказані вище значення, зі сполукою загальної формули (llIi), де R1 та R2 разом позначають зв'язок, R5 позначає гідроген, а всі інші символи мають вказані вище значення, може бути проведена з використанням придатних агентів сполучення, таких як ізобутилхлорформіат чи етилхлорформіат/Et3N, півалоїлхлорид/Еt3N, дициклогексилсечовина, триарилфосфін/діалкілазадикарбоксилат, наприклад, PPh3/DEAD і т.п. Реакція може бути проведена у присутності розчинників, таких як ТГФ, DME, 30 CH2CI2, СНСІ3, толуол, ацетонітрил, чотирихлоритий вуглець і т.п. Може підтримуватися інертна атмосфера шляхом використання інертних газів, таких як N2, Ar, Не і т.п. Реакція може бути проведена у присутності D MAP (диметиламінопіридин), HOBt (гідрат 1-гідроксибензотриазолу), які можуть бути використані у кількості від 0,05 до 2 еквівалентів, краще, від 0,25 до 1 еквівалента. Температура реакції може знаходитися в інтервалі від 0°C до 100°C, краще, в інтервалі від 20°C до 80°C. Тривалість реакції може змінюватися від 0,5 до 48 годин, краще, від 03 дo 24 годин. Шлях 6: Реакція сполуки формули (llIi), у якій всі символи мають вказані вище значення, зі сполукою формули (llIj), де Y позначає оксиген, R3=R4 і мають вказані вище значення, за винятком гідрогену, з утворенням сполуки формули (І), де R1 та R2 разом позначають зв'язок, Y позначає атом оксигену, може бути проведена без розведення у присутності основи, такої як гідриди лужних металів, наприклад, NaH, KH, чи літійорганічні реагенти, наприклад, СН3Li, BuLi і т.п., чи алкоксиди, такі як NaOMe, NaOEt, т-ВuО-K+ і т.п., чи їхні суміші. Реакція може бути проведена у присутності апротонних розчинників, таких як ТГФ, діоксан, ДМФ, ДМСО, D ME і т.п. чи їхні суміші. Як співрозчинник може бути використаний HMPA. Температура реакції може змінюватися в інтервалі від -78°C до 100°C, краще, в інтервалі від -10°C до 50°C. Тривалість реакції може змінюватися від 1 до 48 годин. За ще іншим варіантом втілення даного винаходу, сполука загальної формули (I), де R1 позначає атом гідрогену, гідроксильну груп у, алкоксигрупу, галоген, нижчий алкіл, заміщену чи незаміщену арилалкільну групу; R2 позначає гідроген, галоген, нижчий алкіл, алканоїл, ароїл, арилалканоїл, заміщений чи незаміщений арилалкіл; R3, R4, R5, R6, R13 , X, Y, Ar, m та n мають вказані вище значення, може бути одержана одним чи кількома способами, зображеними на Схемі Il нижче. 31 82835 Шлях 7: Відновлення сполуки формули (IVa), яка позначає сполуку формули (І), де R1 та R2 разом позначають зв'язок, Y позначає атом оксигену, а всі інші символи мають вказані вище значення, одержаної, як описано вище (Схема І), з утворенням сполуки загальної формули (І), де R1 та R2 позначають кожний атом гідрогену, і всі символи мають вказані вище значення, може бути проведене у присутності газоподібного гідрогену та каталізатора, такого як Pd/C, Rh/C, Pt/C і т.п. Можуть бути використані суміші каталізаторів. Реакція може також бути проведена у присутності розчинників, таких як діоксан, оцтова кислота, етилацетат, спирт, такий як метанол, етанол і т.п. Може бути використаний тиск від атмосферного тиску до 276552кПа (40-80psi). Каталізатором може бути, краще, 5-10% Pd/C, а кількість використаного каталізатора може знаходитися в інтервалі 5-100% мас/мас. Реакція може також бути проведена шляхом відновлення металом у розчиннику, наприклад, магнієм чи самарієм у спирті або амальгамою натрію у спирті, краще, метанолі. Гідрування може бути проведене у присутності металевих каталізаторів, що містять хіральні ліганди, для одержання сполуки формули (І) у оптично активній формі. Металевий каталізатор може містити родій, рутеній, індій і т.п. Хіральні ліганди можуть, краще, бути хіральними фосфінами, такими як оптично чисті енантіомери 2,3-біс(дифенілфосфіно)бутану, 2,3-ізопропіліден-2,3-дигідрокси-1,4біс(дифенілфосфіно)бутану і т.п. Може бути використаний будь-який придатний хіральний каталізатор, який забезпечує бажану оптичну чистоту продукту (І) [ди в.: Principles of Asymmetric Synthesis, Tetrahedron Series, Vol.14, pp.311-316, Ed. Baldwin J. E.]. Шлях 8: Реакція сполуки формули (IVb), де R6 має вказані вище значення; R4 має вказані вище значення, за винятком гідрогену, а всі інші символи мають вказані вище значення і L1 позначає відхідну гр упу, таку як атом галогену, наприклад, хлор, бром чи йод; метансульфонат, птолуолсульфонат, трифлюорметансульфонат, зі спиртом загальної формули (IVc), де R3 має вказані вище значення, за винятком гідрогену, з утворенням сполуки формули (І), визначеної вище, може бути проведена у присутності розчинників, таких як діетиловий ефір, ТГФ, ДМФ, ДМСО, D ME, діетиловий ефір, толуол, бензол і т.п. чи їхні суміші. Реакція може бути проведена у інертній атмосфері, яка може підтримуватися шляхом використання інертних газів, таких як N2, Ar, Не і т.п. Реакція може бути проведена у присутності основи, такої як KOH, NaOH, NaOMe, NaOEt, т-ВuО-K+, NaH, KH чи їхні суміші. Можуть бути використані каталізатори фазового перенесення, такі як галогеніди, бісульфати чи гідроксиди тетраалкіламонію. Температура реакції може знаходитися в інтервалі від -20°C до 120°C, краще, в інтервалі від 0°C до 100°C. Тривалість реакції може змінюватися від 1 до 48 годин, краще, від 1 до 24 годин. Шлях 9: Реакція сполуки формули (llIg), визначеної раніше, зі сполукою формули (llIf), у якій всі символи мають вказані вище значення, з утворен 32 ням сполуки формули (І), визначеної вище, може бути проведена у присутності розчинників, таких як діетиловий ефір, ТГФ, ДМФ, ДМСО, DME, толуол, бензол, ацетон, ацетонітрил і т.п. чи їхні суміші. Реакція може бути проведена у інертній атмосфері, яку підтримують шляхом використання інертних газів, таких як N2, Ar, Не і т.п. Реакція може бути проведена у присутності основи, такої як K2СО3, Na2CO3, NaH і т.п. чи їхні суміші. Температура реакції може змінюватися в інтервалі від -20°C до 12O°C, краще, в інтервалі температур 0°C 12O°C. Тривалість реакції може змінюватися від 1 до 48 годин, краще, від 1 до 24 годин. Може бути використаний каталізатор фазового перенесення, такий як галогеніди чи гідроксиди тетраалкіламонію. Шлях 10: Реакція сполуки загальної формули (llIh) визначеної раніше, зі сполукою загальної формули (llIf), де всі символи мають вказані вище значення, може бути проведена з використанням придатних агентів сполучення, таких як ізобутилхлорформіат, етилхлорформіат/Еt3N чи півалоїлхлорид/Еt3N, дициклогексилсечовина, триарилфосфін/діалкілазадикарбоксилат, наприклад, РРh3/DEAD і т.п. Реакція може бути проведена у присутності розчинників, таких як ТГФ, DME, СН2Сl2, СНСІ3, толуол, ацетонітрил, чотирихлоритий вуглець і т.п. Може підтримуватися інертна атмосфера шляхом використання інертних газів, таких як N2, Ar, Не і т.п. Реакція може бути проведена у присутності DMAP, HOBt, які можуть бути використані у кількості від 0,05 до 2 еквівалентів, краще, від 0,25 до 1 еквівалента. Температура реакції може знаходитися в інтервалі від 0°C до 100°C, краще, в інтервалі від 20°C до 80°C. Тривалість реакції може змінюватися від 0,5 до 48 годин, краще, від 6 до 24 годин. Шлях 11: Реакція сполуки формули (llld), яка позначає сполуку формули (І), де всі символи мають вказані вище значення, зі сполукою формули (llIc), де R3 має вказані вище значення, за винятком гідрогену, і L1 позначає відхідну груп у, таку як атом галогену, наприклад, хлор, бром чи йод; метансульфонат, п-толуолсульфонат, трифлюорметансульфонат і т.п., може бути проведена у присутності розчинників, таких як діетиловий ефір, ТГФ, ДМФ, ДМСО, D ME, толуол, бензол, ацетон, ацетонітрил і т.п. Може підтримуватися інертна атмосфера шляхом використання інертних газів, таких як N2, Ar, Не і т.п. Реакція може бути проведена у присутності основи, такої як KOH, NaOH, NaOMe, t-BuO-K+, NaH, KH, LDA, NaHMDS, K2СО3, Na2CO3 і т.п. Може бути використаний каталізатор фазового перенесення, такий як галогеніди чи гідроксиди чи бісульфати тетраалкіламонію. Температура реакції може змінюватися в інтервалі від -20°C до 200°C, краще, в інтервалі від 0°C до 150°C. Тривалість реакції може змінюватися від 1 до 72 годин, краще, від 1 до 12 годин. Реакція може також бути проведена з використанням алкілувальних агентів, таких як діалкілсульфати, наприклад, діетилсульфат чи диметилсульфат; алкілгалогеніди, наприклад, метилйодид, метилбромід, етилйодид, етилбромід і т.п. 33 82835 Шлях 12: Реакція сполуки загальної формули (INa), визначеної раніше, зі сполукою формули (llIe), де R2 позначає атом гідрогену, Y має вказані вище значення, за винятком NH, а всі інші символи мають вказані вище значення, може бути проведена в звичайних умовах. Може бути використана будь-яка основа, що звичайно використовується для реакції альдольної конденсації, наприклад, гідрид металу, такий як NaH чи KH; алкоксиди металів, такі як NaOMe, т-BuO-K+ чи NaOEt; аміди металів, такі як LiNH2, LiN(iPr)2. Можуть бути використані апротонні розчинники, такі як ТГФ, ДМФ чи діетиловий ефір. Може бути використана інертна атмосфера, така як аргон, причому реакція проходить більш ефективно у безводних умовах. Можуть бути використана температура в інтервалі від -80°C до 25°C. (β-Гідроксилований альдольний продукт може бути дегідроксилований звичайними методами, зручно, з використанням методу іонного гідрування, такого як шляхом обробки триалкілсиланом у присутності кислоти, такої як трифлюороцтова кислота. Може бути використаний розчинник, такий як CH2Cl2. Краще, реакція проводиться при 25°C. Якщо реакція проходить повільно, то може бути використана вища температура. Дегідроксилювання може також бути проведене з використанням процедури деоксигенування за Бартоном (Barton) [див.: D.H.R. Barton et al., J. Chem. Soc, Perkin Trans. I, 1975, 1574; F.S. Martin et al., Tetrahedron Lett, 1992, 33, 1839]. Шлях 13: Перетворення сполуки формули (IVd), у якій всі символи мають вказані вище значення, на сполуку формули (І), де Y позначає атом оксигену і всі інші символи мають вказані вище значення, може бути проведене у присутності основи чи кислоти, причому вибір основи чи кислоти не є критичним. Може бути використана будь-яка основа, що звичайно використовується для гідролізу нітрилу до кислоти, наприклад, гідроксиди металів, такі як NaOH чи KOH, у водному розчиннику, або може бути використана будь-яка кислота, що звичайно використовується для гідролізу нітрилу до складного ефіру, така як HCI, у надлишку спирту, такого як метанол, етанол, пропанол і т.д. Реакція може бути проведена в інтервалі температур від 0°C до температури кипіння зі зворотним холодильником використаного розчинника, краще, в інтервалі температур від 25°C до температури кипіння зі зворотним холодильником використаного розчинника. Тривалість реакції може змінюватися від 0,25 до 48год. Шлях 14: Реакція сполуки формули (IVe), де R4 має вказані вище значення, за винятком гідрогену, і всі символи мають вказані вище значення, зі сполукою формули (IVc), де R3 має вказані вище значення, за винятком гідрогену, з утворенням сполуки формули (І) (за реакцією вклинення, медійованою карбеноїдом родію) може бути проведена у присутності солей родію(ІІ), таких як ацетат родію(ІІ). Реакція може бути проведена у присутності розчинників, таких як бензол, толуол, діоксан, діетиловий ефір, ТГФ і т.п. чи їхня комбінація або, якщо це можливо, у присутності R3OH як розчинника при будь-якій температурі, що забезпечує зручну швидкість утворення бажаного продукту, 34 загалом, при підвищеній температурі, наприклад, при температурі кипіння розчинника зі зворотним холодильником. Може підтримуватися інертна атмосфера шляхом використання інертних газів, таких як N2, Ar, Не і т.п. Тривалість реакції може змінюватися від 0,5 до 24год., краще, від 0,5 до 6год. Шлях 15: Реакція сполуки формули (IVg) зі сполукою формули (IVf), де G1 та G2 є різними і незалежно позначають NH2 чи CHO, q позначає ціле число в інтервалі 0-6, а всі інші символи мають вказані вище значення, з утворенням сполуки формули (І), де R5 позначає гідроген, а всі інші символи мають вказані вище значення, може бути проведена у дві стадії, першою з яких є утворення іміну, а потім відновлення. Утворення іміну може бути проведене у розчинниках, таких як MeOH, EtOH, і-РrOН і т.п. Реакція може бути проведена у присутності основи, такої як NaOAc, KOAc і т.п. чи їхні суміші. Температура реакції може змінюватися в інтервалі від кімнатної температури до температури кипіння зі зворотним холодильником використаного розчинника. Час реакції може складати від 2год. до 24год., краще, від 2год. до 12год. Імін може бути також одержаний за реакцією сполуки загальної формули (IVg) зі сполукою формули (IVf), де G 1 та G 2 є різними і незалежно позначають NH2 чи CHO, q позначає ціле число в інтервалі 0-6, а всі інші символи мають вказані вище значення, з використанням розчинників, таких як CH2CI2, CHCl3, хлорбензол, бензол, ТГФ, у присутності каталізатора, такого як птолуолсульфонова кислота, метансульфонова кислота, TFA, TfOH, BF 3-OEt2 і т.п. Реакція може також бути проведена у присутності активованихмолекулярних сит. Температура реакції може змінюватися в інтервалі від 10°C до 100°C, краще, в інтервалі від 10°C до 60°C. Час реакції може складати від 1год. до 48год. Одержаний, як описано вище, іміновий продукт може бути відновлений за допомогою Na(CN)BH3-HCI [див.: Hutchins, R. O. et al. J. Org. Chem. 1983, 48, 3433], NaBH4, H2-Pd/C, H 2-Pt/C, H 2Rh/C і т.п. у розчинниках, таких як метанол, етанол і т.п. Сполука формули (І), де R5 позначає гідроген, може бути також одержана за допомогою одностадійної процедури з використанням сполуки формули (IVg) та (IVf), де всі символи мають вказані вище значення, шляхом відновного амінування з використанням гідрогену як відновника. Сполуки формул (IVg) та (IVf) при конденсації під тиском у присутності гідрогену можуть утворювати сполуку формули (І). Тиск може змінюватися в інтервалі від 69 до 620кПа (10-90psi), "краще, від 138 до 414кПа (20-60psi). Як розчинник може бути вибраний один з MeOH, EtOH, EtOAc, діоксан, толуол і т.п. Температура може змінюватися в інтервалі від кімнатної температури до 50°C, краще, в інтервалі від кімнатної температури до 40°C. Може бути використаний каталізатор, такий як Pd/C, Rh/C, Pt/C і т.п. Сполука загальної формули (І), де R4 позначає атом гідрогену, може бути одержана шляхом гідролізу, з використанням звичайних методів, сполу 35 82835 ки формули (І), де R 4 позначає всі визначені раніше гр упи, за винятком гідрогену. Гідроліз може бути проведений у присутності основи, такої як Nа2СО3, K2СО3 , NaOH, KOH, LiOH і т.п., та придатного розчинника, такого як метанол, етанол, вода і т.п. чи їхні суміші. Реакція може бути проведена в інтервалі температур 20 - 120°C. Час реакції може складати від 2 до 48год., краще, від 2 до 12год. Сполука загальної формули (І), де Y позначає оксиген і R4 позначає гідроген чи нижчу алкільну груп у, може бути перетворена на сполуку формули (І), де Y позначає NR7, за реакцією з відповідними амінами формули NHR4R7, де R4 та R7 мають вказані вище значення, з утворенням сполуки формули (І), де Y позначає NR7, а всі інші символи мають вказані вище значення. За іншим варіантом втілення, сполука формули» (І), де YR4 позначає OH, може бути перетворена на галоїдангідрид кислоти, краще, YR4=Cl, шляхом проведення реакції з відповідними реагентами, такими як оксалілхлорид, тіонілхлорид і т.п., з наступною обробкою амінами формули NHR4R7, де R4 та R7 мають вказані вище значення. За іншим варіантом втілення, змішані ангідриди можуть бути одержані зі сполуки формули (І), де YR4 позначає OH, а всі інші символи мають вказані вище значення, шляхом обробки галоїдангідридами кислот, такими як ацетилхлорид, ацетилбромід, півалоїлхлорид, дихлорбензоїлхлорид і т.п. Реакція може бути проведена у присутності піридину, триетиламіну, діізопропілетиламіну і т.п. Для активації кислоти можуть бути також використані агенти сполучення, такі як DCC/DMAP, DCC/HOBt, EDCI/HOBT, е тилхлорформіат, ізобутилхлорформіат. Можуть бути використані розчинники, такі як галогеновані вуглеводні, наприклад, СНСІ3 чи СН 2Сl2; вуглеводні, такі як бензол, толуол, ксилол і т.п. Реакція може бути проведена в інтервалі температур від -40°C до 40°C, краще, при температурі в інтервалі від 0°C до 20°C. Галоїдангідрид кислоти чи змішаний ангідрид чи активована кислота, одержана за допомогою агентів сполучення, як описано вище, можуть бути оброблені далі відповідними амінами формули NHR4R7, де R4 та R7 мають вказані вище значення, з утворенням сполуки формули (І), де Y позначає NR7, а всі інші символи мають вказані вище значення. Ще інший варіант втілення даного винаходу передбачає нову проміжну сполуку формули (llIa) (Illa) її похідні, її аналоги, її таутомерні форми, її стереоізомери, її солі, її сольвати, де R5 позначає гідроген або заміщену чи незаміщену групу, вибрану з алкільної, алкенільної, циклоалкільної, циклоалкілалкільної, арильної чи арилалкільної груп; n та m є цілими чилами в інтервалі 0 - 6; Ar позначає заміщені чи незаміщені групи, вибрані з двовалентного фенілену, нафтилену, піридилу, хінолінілу, бензофурилу, дигідробензофурилу, 36 бензопіранілу, дигідробензопіранілу, індолілу, індолінілу, азаіндолілу, азаіндолінілу, піразолілу, бензотіазолілу, бензоксазолілу і т.п.; X позначає C=O, C=S, -C(O)CH 2-, -CH=CH-CH2-; -CH=CH-COабо X позначає зв'язок; R6 позначає заміщену чи незаміщену гр упу, вибрану з арилоксикарбонілу, арилалкоксикарбонілу, алкіл карбонілоксигрупи, алкоксикарбоніламіногрупи, арилоксикарбоніламіногрупи, арилалкоксикарбоніламіногрупи, флуоренілметоксикарбонілу (Fmoc), флуоренілметоксикарбоніламіногрупи (N-Fmoc), OSO2R8, -OCONR 8R9, NR8COOR9, -NR8COR9, -NR8SO2R 9, NR8CONR9R10, -NR8CSNR8R9, -SO2R8,. -SOR 8 , -SR8 , -SO 2NR8R9, SO2OR8 , -COOR 9, -COR 9 чи -CONR8R9, де R8, R9 та R10 можуть бути однаковими чи різними і незалежно позначають гідроген або заміщений чи незаміщений алкіл, арил, арилалкіл, алкоксикарбоніл чи арилалкоксикарбоніл; R8 та R9, коли вони знаходяться на атомі нітрогену, можуть разом утворювати 5- чи 6-членну циклічну структур у, що містить атоми карбону та один чи кілька гетероатомів, вибраних з оксигену, сульфур у чи нітрогену, або R6 позначає гідроген, якщо R13 знаходиться у положенні 3 фінільного кільця і не позначає гідроген. R13 позначає гідроген, галоген, нітрогрупу, ціаногрупу, аміногрупу, галоїдалкіл, гідроксил або заміщену чи незаміщену групу, вибрану з лінійного чи розгалуженого (С1-С12)-алкілу, арилу, арилалкілу, гетероарилу, гетероарилалкілу, одновалентного гетероциклічного радикала, алкоксигрупи, моноалкіламіногрупи, діалкіламіногрупи, алкоксикарбонілу, арилоксикарбонілу, арилалкоксикарбонілу, арилоксигрупи, арилалкоксигрупи, алкілкарбонілоксигрупи, алкоксикарбоніламіногрупи, арилоксикарбоніламіногрупи, арилалкоксикарбоніламіногрупи, флуоренілметоксикарбонілу (Fmoc), флуоренілметоксикарбоніламіногрупи (NFmoc), -OSO2R8, -OCONR 8R9, NR8COOR9 , NR8COR9, -NR8R9, -NR8SO2R9, NR8CONR9R10, NR8CSNR8R9, -SO2R8, -SOR 8, -SR8 , -SO2NR8R9 , SO2OR8 , -COOR 9 , -COR 9 , -CONR8R9, де R8, R9 та R10 можуть бути однаковими чи різними і незалежно позначають гідроген або заміщений чи незаміщений алкіл, арил, арилалкіл, алкоксикарбоніл чи арилалкоксикарбоніл; R8 та R9, коли вони знаходяться на атомі нітрогену, можуть разом утворювати 5- чи 6-членну циклічну структур у, що містить атоми карбону та один чи кілька гетероатомів, вибраних з оксигену, сульфур у чи нітрогену. Замісники груп, представлених Ar, R 5, R6 , R8 , 9 R , R10 та R13 , мають значення, вказані для сполуки формули (І). m позначає ціле число від 0 до 6, і п позначає ціле число від 0 до 6. За ще іншим варіантом втілення даного винаходу, сполука формули (Illa), де R5 позначає гідроген; X позначає C(O)CH2-, -CH=CH-CH2-; або X позначає зв'язок; m дорівнює O, Ar позначає феніл, а всі інші символи мають вказані вище значення, може бути одержана у спосіб, описаний на Схемі III нижче: 37 82835 Реакція сполуки формули (llIk), де всі символи визначені вище, зі сполукою формули (III I), де R12 позначає гідроген чи (С1-С6)-алкільну групу, з утворенням сполуки формули (llIm), у якій всі символи мають вказані вище значення, може бути проведена у дві стадії - першою стадією є утворення іміну, а потім відновлення. Утворення іміну може бути проведене у розчинниках, таких як MeOH, EtOH, і-РrOН і т.п. Реакція може бути проведена у присутності промотора, такого як NaOAc, KOAc і т.п. чи їхніх сумішей. Температура реакції може змінюватися в інтервалі від кімнатної температури до температури кипіння зі зворотним холодильником використаного розчинника. Час реакції може складати від 2год. до 24год., краще, від 2год. до 12год. Імін може бути також одержаний за реакцією сполуки загальної формули (llIk) зі сполукою формули (llІ І) з використанням розчинників, таких як СН2СІ2, CHCI3, хлорбензол, бензол, ТГФ, у присутності каталізатора, такого як п-толуолсульфонова кислота, метансульфонова кислота, TFA, TfOH1 BF3-OEt 2 і т.п. Реакція може також бути проведена у присутності активованихмолекулярних сит. Температура реакції може змінюватися в інтервалі від 10°C до 100°C, краще, в-інтервалі від 10°C до 60°C. Час реакції може складати від 1год. до 48год. Iміновий продукт, одержаний, як описано вище, може бути відновлений за допомогою Na(CN)BH3-HCI (див.: Hutchins, R. O. et al., J. Org. Chem. 1983, 48, 3433), NaBH4, Н2-Р0УС, Нг-Pt/C, Нг-Rh/C і т.п. у розчинниках, таких як метанол, етанол і т.п. Гідроліз сполуки формули (Illm), у якій всі символи мають вказані вище значення, з утворенням сполуки формули (llIa), може бути проведений у присутності основи чи кислоти, причому вибір основи чи кислота не є критичним. Можуть бути використані такі основи, як гідроксиди металів, наприклад, NaOH чи KOH, у водному розчиннику чи кислотах, таких як водна HCI чи TFA у розчинниках, таких як СН2СІ2, ТГФ, ацетон, метанол, етанол, пропанол, вода і т.д. Реакція може бути проведена в інтервалі температур від 0°C до температури кипіння зі зворотним холодильником використаного розчинника, краще, в інтервалі температур від 0°C до температури кипіння зі зворотним холодильником використаного розчинника. Тривалість реакції може змінюватися від 0,25 до 48год. 38 За ще іншим варіантом втілення даного винаходу, сполука формули (Illa), де R5 позначає гідроген чи алкільну групу; m дорівнює 0, а всі інші символи мають вказані вище значення, може бути одержана у спосіб, який включає проведення реакції сполуки формули (llIg) (Illg) де всі символи мають вказані вище значення, зі сполукою формули (llIn) (Illn) де R12 позначає гідроген чи алкільну груп у, і R5 має вказані вище значення, m позначає ціле число в інтервалі 0 - 6. Реакція сполуки формули (lllg) зі сполукою формули (Illn) може бути проведена у присутності розчинників, таких як ТГФ, ДМФ, ДМСО, DME, толуол, бензол, ацетон, ацетонітрил і т.п. чи їхніх сумішей. Реакція може бути проведена у інертній атмосфері, яку підтримують шляхом використання інертних газів, таких як N2, Ar, Не і т.п. Реакція може бути проведена у присутності основи, такої як K2CO3, Na2CO3 , NaH і т.п. чи їхні х сумішей. Температура реакції може змінюватися в інтервалі від 20°C до 120°C, краще, в інтервалі 30°C - 80°C. Тривалість реакції може змінюватися від 1 до 24 годин, краще, від 1 до 12 годин. Проміжна сполука (llIf) за даним винаходом та спосіб її одержання є предметом нашої [заявки PCT №РСТ/ІВ02/04274]. Передбачається, що в будь-якій із зазначених вище реакцій, будь-яка реакційноздатна група у молекулі субстрата може бути захищена згідно до звичайної хімічної практики. Придатними захисними групами у будь-якій із згаданих вище реакцій є трет-бутилдиметилсиліл, метоксиметил, трифенілметил, бензилоксикарбоніл, THP і т.д. для захисту гідроксильної чи фенольної гідроксильної групи; н-Вос, н-Cbz, N-Fmoc, бензофенонімін і т.д., для захисту аміногрупи чи аніліногрупи, ацетальний захист для альдегіду, кетальний захист для кетону і т.п. Способи утворення та видалення таких захисних груп є звичайними способами, які залежать від молекули, що потребує захисту. Фармацевтично прийнятні солі одержують шляхом проведення реакції сполуки формули (І) з 39 82835 1 - 4 еквівалентами основи, такої як гідроксид натрію, метоксид натрію, гідрид натрію, гідроксид калію, т-бутоксид калію, гідроксид кальцію, гідроксид магнію і т.п., у розчинниках, таких як діетиловий ефір, ТГФ, метанол, т-бутанол, діоксан, ізопропанол, етанол і т.д. Можуть бути використані суміші розчинників. Можуть бути використані також органічні основи, такі як лізин, аргінін, діетаноламін, холін, гуанідин, трометамін та їхні похідні і т.д. За іншим варіантом, у належних випадках одержують кислотно-адитивні солі шляхом обробки кислотами, такими як хлористоводнева кислота, бромистоводнева кислота, азотна кислота, сірчана кислота, фосфорна кислота, п-толуолсульфонова кислота, метансульфонова кислота, оцтова кислота, лимонна кислота, малеїнова кислота, фумарова кислота, саліцилова кислота, оксинафтойна кислота, аскорбінова кислота, пальмітинова кислота, бурштинова кислота, бензойна кислота, бензолсульфонова кислота, винна кислота і т.п., у розчинниках, таких як етилацетат, діетиловий ефір, спирти, ацетон, ТГФ, діоксан і т.д. Можуть бути використані також суміші розчинників. Стереоізомери сполук, що утворюють частину даного винаходу, можуть бути одержані шляхом використання у способі, якщо це можливо, реагентів у формі окремих енантіомерів, або шляхом проведення реакції у присутності реагентів чи каталізаторів у формі їхніх окремих енантіомерів, або шляхом розділення суміші стереоізомерів звичайними методами. Деякі з кращих методів включають використання мікробного розділення, розділення діастереомерних солей, утворених з хіральними кислотами, такими як мигдалева кислота, камфорсульфонова кислота, винна кислота, молочна кислота і т.п., якщо це можливо, або з хіральними основами, такими як бруцин, алкалоїди хінного дерева та їхні похідні і т.п. Звичайно використовувані методи описані [Jaques et al. у книзі "Enantiomers, Racemates and Resolution" (Wiley lnterscience, 1981)]. Конкретніше, сполука формули (І), де YR10 позначає OH, може бути перетворена на 1:1 суміш діастереомерних амідів шляхом обробки хіральними амінами, амінокислотами, аміноспиртами, похідними від амінокислот; для перетворення кислоти на амід можуть бути використані звичайні умови реакції; діастереомери можуть бути розділені за допомогою фракційної кристалізації чи хроматографії, і стереоізомери сполуки формули (І) можуть бути одержані шляхом гідролізу чистого діастереомерного аміду. Різні поліморфи сполуки загальної формули (І), що утворюють частину даного винаходу, можуть бути одержані шляхом кристалізації сполуки формули (І) в різних умовах. Наприклад, використовують для перекристалізації звичайно використовувані розчинники чи їхні суміші; проводять кристалізацію при різних температурах; використовують різні режими охолодження, від дуже швидкого до дуже повільного охолодження під час кристалізації. Поліморфи можуть бути одержані також шляхом нагрівання чи плавління сполуки з наступним поступовим чи швидким охолодженням. Присутність поліморфів може бути визначена методами твердофазової ЯМР 40 спектроскопії, ІЧ-спектроскопії, диференційної скануючої калориметрії, порошкової рентгенівської дифракції чи іншими подібними методами. Даний винахід пропонує фармацевтичну композицію, що містить сполуки загальної формули (І), визначеної вище, їхні похідні, їхні аналоги, їхні таутомерні форми, їхні стереоізомери, їхні поліморфи, їхні фармацевтично прийнятні солі чи їхні фармацевтично прийнятні сольвати у комбінації із звичайними фармацевтично застосовними носіями, розріджувачами і т.п., придатну для лікування та/або профілактики хвороб, таких як гіпертензія, ішемічна хвороба серця, атеросклероз, інсульт, периферичні судинні захворювання та споріднені розлади. Ці сполуки є придатними для лікування сімейної гіперхолестеринемії, гіпертригліцеридемії, зниження атерогенних ліпопротеїдів, VLDL та LDL. Сполуки за даним винаходом можуть бути використані для лікування деяких • ниркових захворювань, включаючи гломерулонефрит, гломерулосклероз, нефротичний синдром, гіпертензивний нефросклероз, нефропатію. Сполуки загальної формули (І) є також придатними для лікування/профілактики інсулінорезистентності (діабет типу II), порушеної толерантності до глюкози, лептинорезистентності, дисліпідемії, розладів, пов'язаних із синдромом X, таких як гіпертензія, ожиріння, інсулінорезистентність, ішемічна хвороба серця, та інших серцево-судинних розладів. Сполуки за даним винаходом можуть також бути корисними як інгібітори альдозоредуктази, для поліпшення пізнавальних функцій при деменції, як запальні агенти, для лікування діабетичних ускладнень, розладів, пов'язаних з активацією ендотеліальних клітин, псоріазу, синдрому полікістозних яєчників (PCOS), запальних хвороб кишечнику, остеопорозу, міотонічної дистрофії, панкреатиту, ретинопатії, артеріосклерозу, ксантоми та для лікування раку. Сполуки за даним винаходом є придатними для лікування та/або профілактики вказаних ви ще хвороб у комбінації/суп утно з одним чи кількома інгібіторами HMG СоА-редуктази; інгібіторами всмоктування холестерину; засобами для лікування ожиріння; засобами для лікування ліпопротеїдних розладів; гіпоглікемічними агентами: інсуліном; бігуанідом; сульфонілсечовиною; тіазолідиндіоном; подвійними агоністами PPARα та у чи їхньою сумішшю. Сполуки за даним винаходом у комбінації з інгібіторами HMG СоА-редуктази, інгібіторами всмоктування холестерину, засобами для лікування ожиріння, гіпоглікемічними агентами можуть вводитися одночасно чи протягом такого періоду часу, щоб забезпечити їхню синергічну дію. Даний винахід пропонує також фармацевтичну композицію, яка містить сполуки загальної формули (І), визначеної вище, їхні похідні, їхні аналоги, їхні та утомерні форми, їхні стереоізомери, їхні поліморфи, їхні фармацевтично прийнятні солі чи їхні фармацевтично прийнятні сольвати та один чи кілька інгібіторів HMG СоА-редуктази; інгібіторів всмоктування холестерину; засобів проти ожиріння; засобів для лікування ліпопротеїдних розладів; гіпоглікемічних агентів; інсулін; бігуанід; сульфоні 41 82835 лсечовину; тіазолідиндіон; подвійні PPARα та у чи їхню суміш у комбінації із звичайними фармацевтично застосовними носіями, розріджувачами і т.п. Фармацевтична композиція може знаходитися у звичайно застосовуваних формах, таких як таблетки, капсули, порошки, сиропи, розчини, суспензії і т.п., може містити смакові агенти, підсолоджувачі і т.д. у придатних твердих чи рідких носіях чи розріджувачах, чи у придатному стерильному середовищі для утворення розчинів чи суспензій для ін'єкцій. Такі композиції типово містять від 1 до 20%, краще, від 1 до 10% мас., активної сполуки, а решта композиції складається з фармацевтично прийнятних носіїв, розріджувачів чи розчинників. Придатні фармацевтично прийнятні носії включають тверді наповнювачі чи розріджувачі та стерильні водні чи органічні розчини. Активний інгредієнт входить до складу таких фармацевтичних композицій у кількості, достатній для забезпечення бажаної дози в указаному вище інтервалі значень. Так, для орального введення, сполука формули (І) може бути поєднана з придатним твердим чи рідким носієм чи розріджувачем з утворенням капсул, таблеток, порошків, сиропів, розчинів, суспензій і т.п. Фармацевтичні композиції можуть, якщо бажано, містити додаткові компоненти, такі як смакові агенти, підсолоджувачі, ексципієнти і т.п. Для парентерального введення, сполуки можуть бути поєднані зі стерильним водним чи органічним середовищем для одержання розчинів чи суспензій для ін'єкцій. Наприклад, можуть бути використані розчини у кунжутній чи арахісовій олії, водному пропіленгліколі і т.п., а також водні розчини водорозчинних фармацевтично прийнятних кислотно-адитивних солей чи солей основних форм сполук. У розчинах для ін'єкцій можуть також бути використані водні розчини з активними інгредієнтом, розчиненим у полігідроксилованій рициновій олії. Розчини для ін'єкцій, виготовлені у такий спосіб, можуть бути потім введені внутрішньовенно, внутрішньочеревинно, підшкірно чи внутрішньом'язово, причому кращим для людей є внутрішньом'язове введення. Для назального введення, препарат може містити сполуки за даним винаходом, розчинені чи суспендовані у рідкому носії, зокрема, у водному носії, для аерозольного застосування. Носій може містити добавки, такі як солюбілізатори, наприклад, пропіленгліколь, поверхнево-активні речовини, засоби, що посилюють всмоктування, такі як лецитин (фосфатидилхолін) чи циклодекстрин, або консерванти, такі як парабени. Особливо придатними для будь-якого орального застосування є таблетки, драже чи капсули, що містять зв'язуючий носій на основі тальку та/або вуглеводу і т.п. Краще, носії для таблеток, драже чи капсул включають лактозу, кукурудзяний крохмаль та/або картопляний крохмаль. У випадках, коли може бути застосований підсолоджений носій, можуть бути використані сироп чи еліксир. Сполуку (сполуки) формули (І), визначеної вище, клінічно вводять ссавцям, включаючи людину, оральним чи парентеральним шляхами. Кращим є введення оральним шляхом, як більш зручне та таке, що дозволяє уникнути болю та 42 подразнення, можливих при ін'єкції. Однак, якщо пацієнт не може проковтнути лікарський засіб або при порушеному всмоктуванні після орального введення, наприклад, внаслідок хвороби чи іншої аномалії, лікарський засіб має бути введений парентерально. При будь-якому шляху введення, дозу, що знаходиться в інтервалі від близько 0,01 до близько 100мг/кг ваги тіла суб'єкта на добу, чи, краще, від близько 0,01 до близько 50мг/кг ваги тіла на добу, вводять як разову чи кратні дози. Однак, оптимальну схему дозування для кожного суб'єкта, що отримує лікування, визначає особа, відповідальна за лікування, причому звичайно спочатку вводять менші дози, які потім поступово збільшують для визначення найбільш придатної дози. Сполуки за даним винаходом знижують рівень цукру крові у довільний момент часу, тригліцериди, загальний холестерин, LDL, VLDL і підвищують HDL за агоністичним механізмом. Це можна продемонструвати експериментами на тваринах як in vitro, так і in vivo. Винахід пояснюється детальніше у наведених нижче прикладах, які даються лише для ілюстрації і тому не повинні тлумачитися як такі, що обмежують обсяг винаходу. Синтез 1 4-(3Метансуль фонілоксипропіл)фенілметансульфонат Стадія (і) До суспензії LAH (22,1г, 2,5екв., 583ммоль) у сухому ТГФ (1,0л), додають по краплях розчин метил-3-(4-гідроксифеніл)пропіонату (21г, 1,0екв., 116ммоль) у ТГФ (50мл) при кімнатній температурі. Реакційну суміш нагрівають до кипіння зі зворотним холодильником протягом 4 - 5год. її доопрацьовують шляхом гасіння надлишком етилацетату з наступним доданням води (23мл), 15%-ного водн. NaOH (23мл) та води (70мл) при контрольованому перемішуванні та підтримуванні кімнатної температури. До доопрацьованої суміші додають конц. HCI для доведення рН до 7,0. Потім її фільтрують крізь целіт та промивають етилацетатом. Об'єднаний фільтрат осушають (Na2SO 4) та конденсують. Одержаний залишок піддають хроматографії (етилацетат/гексани), одержуючи 3-(4гідроксифеніл)пропанол (17г, 100%) у вигляді білої твердої речовини. Т.пл.: 52-54°C. 1 H ЯМР (CDCI3 , 200МГц) δ: 1,78-1,86 (м, 2Н); 2,63 (т, J=7,9Гц, 2Н); 3,67 (т, J=6,3Гц, 2Н); 6,74 (д, J=8,8Гц, 2Н); 7,05 (д, J=8,8Гц, 2Н). ІЧ (чиста речовина) см -1: 3485, 3029, 2940, 1505. Маса m/z (Cl) (хімічна Іонізація): 152 [М+1]. Стадія (іі) До розчину 3-(4-гідроксифеніл)пропанолу (17г, 1,0екв., 111,8ммоль), одержаного на стадії (і), та триетиламіну (93,3мл, 6,0екв., 670,8ммоль) у ДХМ (550мл) додають по краплях метансульфонілхлорид (26мл, 3,0екв., 335,4ммоль) при 0°C. Реакційну суміш перемішують при кімнатній температурі протягом 16год., після чого її доопрацьовують 43 82835 шляхом розведення надлишком ДХМ та промивання органічного шару розв. HCI, водою та розсолом. Органічний шар осушають (Na2SO4) та концентрують. Бажаний продукт очищають з сирової маси перекристалізацією з діізопропілового ефіру. Решту маточного розчину конденсують та піддають хроматографії (етилацетат/гексани), одержуючи додаткову кількість бажаної сполуки (загальний вихід 20,8г, 61%) у вигляді білої твердої речовини. Т.пл.: 60-62°C. 1 H ЯМР (CDCI3 , 200МГц): δ 2,00-2,18 (м, 2Н); 2,77 (т, J=7,8Гц, 2Н); 3,00 (с, 3Н); 3,13 (с, 3Н); 4,23 (т, J=6,3Гц, 2Н); 7,22 (ароматичне ядро, 4Н): ІЧ (чиста речовина) см -1: 3029, 2935, 1504. Маса m/z (Cl): 309 [М+1]. Синтез 2 3-(3Метансуль фонілоксипропіл)фенілметансульфонат Одержують за типовою процедурою Синтезу 1. Стадія (і) З метил-3-гідроксифенілпропіонату одержують 3-(3-гідроксифеніл)пропанол у вигляді рідкої маси (100%). 1 H ЯМР (CDCI3 , 200МГц): δ 1,80-1,88 (м, 2Н); 2,64 (т, J=7,9Гц, 2Н); 3,49 (шир.с, -OH); 3,67 (т, J=6,5Гц, 2Н); 6,65-6,76 (ароматичне ядро, 3Н); 7,09-7,17 (ароматичне ядро, 1Н). ІЧ (чиста речовина) см-1: 3353, 2932, 2859, 1590. Маса m/z (Cl): 152 [М+1]. Стадія (іі) З 3-(3-гідроксифеніл)пропанолу (900мг, 1,0екв., 5,92ммоль), одержаного на стадії (і), одержують 3-(3метансульфонілоксипропіл)фенілметансульфонат (52%) у вигляді білої твердої речовини. Т.пл.: 6062°C. 1 H ЯМР (CDCI3 , 200МГц): δ 2,00-2,18 (м, 2Н); 2,79 (т, J=7,8Гц, 2Н); 3,00 (с, 3Н); 3,15 (с, 3Н); 4,22 (т, J=6,4Гц, 2Н); 7,10-7,20 (ароматичне ядро, 3Н); 7,21-7,40 (м, 1Н). ІЧ (чиста речовина) см"1: 3030, 2941,1586. Macam/z(CI):309[M+1]. Синтез 3 4-(3-(Толуол-4сульфонілокси)пропіл)фенілтолуол-4-сульфонат До розчину 3-(4-гідроксифеніл)пропанолу (2,5г, 1,0екв., 16,44ммоль), одержаного на стадії (і) Синтезу 1 у ДХМ (82мл) та триетиламіні (11,4мл, 5,0екв., 82,2ммоль), додають по краплях толуол-4сульфонілхлорид (9,4г, 3,0екв., 49,3ммоль) при 0°C Реакційну суміш перемішують при кімнатній температурі протягом 16год., після чого її доопрацьовують шляхом розведення надлишком ДХМ та промивання органічного шару водою та розсолом. Сировий залишок, одержаний після сушіння 44 (Na2SO4) та конденсування, піддають хроматографії (етилацетат/гексани), одержуючи бажану сполуку (5,1г, 67,7%) у ви гляді в'язкої рідини. 1 H ЯМР (CDCI3, 200МГц): δ 1,90 (квінтет, J=7,9Гц, 2Н); 2,44 (с, 6Н); 2,61 (т, J=6,8Гц, 2Н); 3,98 (т, J=6,3Гц, 2Н); 6,83 (д, J=8,8Гц, 2Н); 6,97 (д, J=8,8Гц, 2Н); 7,32 (т, J=7,5Гц, 2Н); 7,67 (д, J=8,3Гц, 2Н); 7,76 (д, J=8,3Гц, 2Н). ІЧ (чиста речовина) см -1: 2926,1597, 1502, 1364. Маса m/z (Cl): 461 [М+1]. Синтез 4 2-(4-Нітрофенокси)етилбромід Суміш 4-нітрофенолу (1,0г, 1,0екв., 7,19ммоль), 1,2-диброметану (3,85мл, 6,0екв., 43,1ммоль) та безводного K2СО3 (3,0г, 3екв., 21,5ммоль) у сухому ацетоні (36мл) перемішують при кімнатній температурі протягом 16год. Реакційну суміш фільтрують і фільтрат конденсують. Конденсовану масу знов розчиняють у етилацетаті та промивають водн. розчином бікарбонату натрію. Органічний шар осушають (Nа2SО4 конденсують і залишок піддають хроматографії з використанням етилацетату та гексанів, одержуючи названу у заголовку сполуку у вигляді твердої речовини (540мг, 32%). Т.пл.: 168°C. 1 H ЯМР (CDCI3, 200МГц): δ 3,67 (т, J=6,1Гц, 2Н); 4,38 (т, J=6,1Гц, 2Н); 6,97 (д, J=8,7Гц, 2Н); 8,20 (д, J=8,7Гц, 2Н). ІЧ (чиста речовина) см-1: 2925, 1592, 1511, 1330. Маса m/z (Cl): 245 [M(79Br)], 246 [M( 79Br)+1], 247 [M(81Br)], 248 [М( 81Вг)+1]. Синтез 5 Етил-2-етокси-3-(4-амінофеніл)пропіонат Стадія (і) Готують сіль Віттіга з триетил-2етоксифосфоноацетату (26,5г, 1,5екв., 99,3ммоль) та NaH (50% у маслі) (5,3г, 2екв., 132,4ммоль) у ТГФ (350мл) при 0°C. Додають до неї порціями твердий 4-нітробензальдегід (10г, 1екв., 66,2ммоль) при 0°C і одержаний розчин перемішують при кімнатній температурі протягом 16год. Реакційну суміш розводять етилацетатом та промивають водним NH4CI. Сировий продукт містить етил-п-нітро-2-етоксицинамат у формі Z- та Eстереоізомерів (11г). Стадія (іі) Етил-п-нітро-2-етоксицинамат, одержаний на стадії (і), гідрують з використанням 10% Pd-C - H2 (414кПа) (60psi) (11г) у етилацетаті (150мл) при кімнатній температурі та піддають хроматографії з використанням етилацетату/гексану, одержуючи названу у заголовку сполуку у вигляді в'язкої маслянистої рідини (9,41г, 60%). 1 H ЯМР (CDCI3, 200МГц): δ 1,16 (т, J=7,0Гц, 3H), 1,22 (т, J=7,0Гц, 3H), 2,90 (д, J=6,3Гц, 2Н), 3,30 (шир.с, 2Н, NH2), 3,35 (м, 1Н), 3,55 (м, 1Н), 45 82835 3,94 (т, J=6,3Гц, 1Н), 4,15 (кв. J=7,0Гц, 2Н), 6,62 (д, J=8,3Гц, 2Н), 7,03 (д, J=8,0Гц, 2Н). ІЧ (чиста речовина) см -1: 3372,1738. Маса m/z (Cl): 238 (М+1), 192 (M - OC 2H5). Синтез 6 Метил-2-етокси-3-(4-амінофеніл)пропіонат Стадія (і) Готують сіль Віттіга з триетил-2етоксифосфоноацетату (34,3мл, 2екв., 132ммоль) та NaH (50% у маслі) (6,28г, 2екв., 132ммоль) у ТГФ (350мл) при 0°C. Додають до неї твердий пнітробензальдегід (10г, 1екв., 66ммоль) порціями при 0°C. Одержаний розчин перемішують при кімнатній температурі протягом 16год. Реакційну суміш розводять етилацетатом та промивають водним NH4CI. Сировий продукт містить етил-п-нітро2-етоксицинамат у формі Z- та E- стереоізомерів (15г, 86%). Стадія (іі) Сирову сполуку (15г, 1екв., 56,6ммоль), одержану на стадії (і), розчиняють у метанолі (250мл). Додають до неї форміат амонію (35,6г, 10екв., 566ммоль) та 10% Pd-C (40г) і реакційну суміш перемішують при кімнатній температурі протягом 16год. Каталізатор відокремлюють на фільтрі і фільтрат конденсують на обертовому випарнику. Залишок розводять етилацетатом та промивають водою і розсолом. Сирову масу піддають хроматографії, одержуючи етил-2-етокси-п-аміноцинамат у формі (E)- та (Z)-ізомерів (10г, 75%). Стадія (ііі) Етил-2-етокси-п-аміноцинамат (10г, 1екв., 42,5ммоль), одержаний на стадії (іі), обробляють магнієм (20,4г, 20екв., 850ммоль) та сухим метанолом (500мл). Реакційну суміш нагрівають до кипіння зі зворотним холодильником протягом 23год., та залишають при перемішуванні при кімнатній температурі протягом 16год. Реакційну суміш розводять етилацетатом та гасять холодним водним хлоридом амонію. Органічний шар промивають водою та розсолом. Залишок піддають хроматографії з використанням етилацетату та гексану, одержуючи названу у заголовку сполуку у вигляді в'язкої рідини (8,06г, 80%). 1 H ЯМР (200МГц, CDCI3): δ 1,64 (т, J=6,8Гц, 3H), 2,90 (д, J=6,3Гц, 2H)1 3,22-3,42 (м, 1Н), 3,423,65 (м, 2Н), 3,70 (с, 3H), 3,96 (т, J=6.8Гц, 1Н), 6,61 (д, J=8,3Гц, 2Н); 7,00 (д, J=8,3Гц, 2Н). ІЧ (чиста речовина) см -1: 3350 (шир.), 1735. Maca m/z(CI):224[M+1] Синтез 7 Етил-2-етокси-3-(3-амінофеніл)пропіонат Починаючи з 3-нітробензальдегіду та використовуючи типову процедуру Синтезу 5, одержують названу у заголовку сполуку у вигляді в'язкої маслянистої рідини (60% для двох стадій). 1 H ЯМР (200МГц, CDCI3): δ 1,17 (т, J=7Гц, 3H); 1,22 (т, J=7Гц, 3H); 2,91 (д, J=6,7Гц, 2Н); 3,30-3,48 (м, 1Н); 3,48-3,62 (м, 1Н); 4,00 (т, J=6,7Гц, 1Н); 4,17 46 (кв, J=7Гц, 2Н); 6,50-6,70 (ароматичне ядро, 3H); 7,06 (т, J=7,5Гц, 1Н). ІЧ (чиста речовина) см-1: 3374, 2978, 1738, 1606. Маса m/z (Cl): 238 [М+1]. Синтез 8 Етил-2-ізопропокси-3-(4-нітрофеніл)пропіонат Стадія (і) 4-Нітрофенілаланін (5г, 1екв., 23,788ммоль) додають порціями до розчину сухого етанолу (50мл) та тіонілхлориду (5мл) при -5°C. Суміш перемішують при цій температурі протягом ще години, а потім перемішують при кімнатній температурі протягом 16год. Реакційну суміш конденсують на обертовому випарнику, піддають азеотропній перегонці з толуолом, а потім висушують за допомогою високовакуумної помпи, одержуючи хлористоводневу сіль етилового складного ефіру 4нітрофенілаланіну у вигляді білої твердої речовини (кількісний вихід). Стадія (ii) Хлористоводневу сіль етилового складного ефіру 4-нітрофенілаланіну (2г, 1,0екв., 7,28ммоль), одержану на стадії (і), розчиняють у етилацетаті (150мл). Додають до неї Na2СО3 (386мг, 0,5екв., 3,64ммоль) і перемішують протягом 15хв. Реакційну суміш промивають водн. NaHCO3. Органічний шар осушають кімнатній температурі протягом 3 4год. Бажаний продукт виділяють після фільтрації реакційної суміші та концентрування фільтрату при зниженому тиску. Хроматографія на колонці сирової маси з використанням етилацетату та гексанів дає бажану сполуку етил-2-ізопропокси-3-(4амінофеніл)пропіонат (1,16г, загальний вихід 86%). 1 H ЯМР (200МГц, CDCI3) δ: 0,97 (д, J=5,8Гц, 3H)1 1,15 (д, J=5,8Гц, 3H), 1,23 (т, J=7,0Гц, 3H), 2,80-2,95 (м, 2H), 3,49 (квінтет, 1H), 3,98 (дд, J=8,1 та 5,7Гц, 1Н), 4,16 (KB, J=7,0Гц, 2Н), 6,61 (д, J=8,3Гц, 2Н), 7,03 (д, J=8,3Гц, 2Н). ІЧ (чиста речовина) см-1: 3455, 3371, 2975, 2929, 1737, 1626, 1519. Maca.m/z (Cl): 252 [М+1]. Синтез 10 4-Метансульфонілоксибензальдегід Суміш 4-гідроксибензальдегіду (5,0г, 1,0екв., 40,98ммоль), безводного K2CO3 (17г, 3екв., 123ммоль) та метансульфонілхлориду (4,76мл, 1,5екв., 61,37ммоль) у сухому ДМФ (200мл) перемішують при кімнатній температурі протягом 16год. Реакційну суміш розводять етилацетатом (200мл) та промивають водою і розсолом. Органічний шар осушають (Na2SO4), конденсують, і одержаний залишок піддають хроматографії з використанням етилацетату та гексанів, одержуючи названу у заголовку сполук у у вигляді білої твердої речовини (2,0г, 25%). Т.пл.: 60-62°C. 47 82835 1 H ЯМР (CDCI3, 200МГц) δ: 3,21 (с, 3Н); 7,45 (д, J=8,8Гц, 2Н); 7,95 (д, J=8,8Гц, 2Н); 10,01 (с, 1Н). ІЧ (чиста речовина) см-1: 3024, 2932, 1701, 1591, 1502. Маса m/z (Cl): 201 [М+1]. Синтез 11 2-(4-Гідроксифеніл)-1-етанол Розчин метил-2-(4-гідроксифеніл)ацетату (3,0г, 18,07ммоль) у ТГФ (20мл) додають до перемішуваної суспензії LAH (0,89г, 23,49ммоль) у ТГФ (20мл) при 0°C. Перемішування продовжують при кімнатній температурі протягом 4год. Надлишок LAH гасять насиченим розчином Na2SO4 і осад, що утворюється, збирають на фільтрі. Фільтрат екстрагують етилацетатом і органічний екстракт промивають розсолом, осушають (Na2SO4) та упарюють до сухого залишку. Очи щення на колонці з використанням 50% етилацетату-петролейного ефіру дає названу у заголовку сполуку (1,1г, 44%) у вигляді білої твердої речовини. Т.пл.: 88-92°C. 1 H ЯМР (200МГц, CDCl3+ДMCO-d6): δ 2,75 (т, J=7,1Гц, 2Н); 3,75 (т, J=6,3Гц, 2Н); 6,75 (д, J=8,3Гц, 2Н); 7,03 (д, J=8,3Гц, 2Н). Маса m/z (Cl): 138 [M]. Синтез 12 4-(2Метилсульфонілоксіетил)фенілметансульфонат Названу у заголовку сполуку (2г, 94%) одержують з 2-(4-гідроксифеніл)-1-етанолу (1,0г, 7,25ммоль), одержаного у Синтезі 11, у ДХМ (20мл) з використанням триетиламіну (2,52мл, 16,1ммоль) та метансульфонілхлориду (0,83мл, 15,9ммоль) при кімнатній температурі протягом 2год. у відповідності до процедури, аналогічної до описаної у Синтезі 1, стадія (іі). 1 H ЯМР (200МГц, CDCI3): δ 2,91 (с, 3H); 3,08 (т, J=6,8Гц, 2Н); 3,15 (с, 3H); 4,42 (т, J=6,8Гц, 2Н); 7,20-7,34 (м, 4Н). Маса m/z (Cl): 199 [M - OSO 2 Me]. Синтез 13 Метил-2-(4-метилсульфонілоксифеніл)ацетат Названу у заголовку сполуку (1,7г, 77%) одержують з метил-2-(4-гідроксифеніл)ацетату (1,5г, 9,04ммоль) у ДХМ (20мл) з використанням триетиламіну (3,14мл, 22,59ммоль) та метансульфонілхлориду (0,84мл, 10,84ммоль) при кімнатній температурі протягом 2год. у відповідності до процедури, аналогічної до описаної у Синтезі 1, стадія (іі). 1 H ЯМР (200МГц, CDCI3): δ 3,14 (с, 3H); 3,64 (с, 2Н); 3,71 (с, 3H); 7,24 (д, J=8,8Гц, 2Н); 7,34 (д, J=8,8Гц, 2Н). Маса m/z: 244 [M]. Синтез 14 48 2-(4-Метилсульфонілоксифеніл)оцтова кисло та До розчину метил-2-(4метилсульфонілоксифеніл)ацетату (0,95г, 3,89ммоль), одержаного у Синтезі 13, у метанолі (10мл) додають Nа2СО3 (2,06г, 19,48ммоль) у воді (5мл) і реакційну суміш перемішують при кімнатній температурі протягом 24год. Метанол упарюють і залишок розводять у воді та промивають етилацетатом для видалення з нього домішок, якщо вони є. Водний шар підкислюють до рН -2, після чого виділяють названу у заголовку сполуку (0,55г, 61,4%) у вигляді білої твердої речовини. Т.пл.: 158-162°C. 1 H ЯМР (200МГц, ДМСО-d6): δ 3,32 (с, 3Н); 3,62 (с, 2Н); 7,28 (д, J=8,9Гц, 2Н); 7,37 (д, J=8,6Гц, 2Н). Маса m/z (Cl): 231 [М+1]; 230 [M]. Синтез 15 Метил-4-нітроцинамат Розчин 4-нітрокоричної кислоти (3г, 15,54ммоль) у метанолі (50мл) охолоджують до 10°C, повільно додають конц. H2SO4 (1мл), а потім нагрівають до кипіння зі зворотним холодильником протягом 30год. Метанол упарюють при зниженому тиску. Додають до залишку етилацетат (150мл) і розчин промивають водою, насич. розчином NаНСО3, водою та розсолом, відповідно. Органічний шар осушають (Na2SO4) та упарюють, одержуючи названу у заголовку сполуку (3г, 93%) у вигляді білуватої твердої речовини. Т.пл.: 158-160°C. 1 H ЯМР (200МГц, CDCI3): δ 3,84 (с, 3Н); 6,56 (д, J=15,9Гц, 1Н); 7,64-7,78 (м, 3H); 8,25 (д, J=8,9Гц, 2Н). Маса m/z (Cl): 208 [М+1]; 194 [M - CH 3]. Синтез 16 Метил-3-(4-амінофеніл)пропіонат До розчину метил 4-нітроцинамату, одержаного у Синтезі 15 (1,5г, 7,25ммоль), у діоксані (25мл) додають 10% Pd-C (0,6г) та гідрують при кімнатній температурі при 414кПа (60psi) протягом 20год. Реакційну суміш фільтрують крізь целіт та концентрують при зниженому тиску. Сировий залишок очищають хроматографією на колонці з використанням 50% ЕtOАс-петролейного ефіру, одержуючи чисту названу у заголовку сполуку (1,07г, 82,5%) у вигляді білуватої твердої речовини. Т.пл.: 142-144°C. 1 H ЯМР (200МГц, CDCI3): δ 2,57 (т, J=7,5Гц, 2Н); 2,85 (т, J=7,8Гц, 2Н); 3,66 (с, 3Н); 6,64 (д, J=8,3Гц, 2Н); 7,00 (д, J=8,3Гц, 2Н). Маса m/z (Cl): 180 [М+1]. Синтез 17 3-(4-Амінофеніл)-1-пропанол 49 82835 50 Синтез 20 Метил-4-гідроксицинамат Холодний розчин метил-3-(4амінофеніл)пропіонату (0,48г, 2,7ммоль), одержаного у Синтезі 16, у ТГФ (10мл) повільно додають по краплях до суспензії LAH (132мг, 3,49ммоль) у ТГФ (10мл) при 0°C і перемішують протягом ночі при кімнатній температурі. Непрореагований LAH гасять насич. розчином Na2SO4 та фільтр ують крізь целіт, а шар фільтруючого матеріалу ретельно промивають етилацетатом. Фільтрат та промивну рідину об'єднують і органічний шар осушають (Na2SO4) та упарюють. Залишок дає після очищення названу у заголовку сполуку (0,27г, 66,7%) у вигляді твердої речовини жовтого кольору. Т.пл.: 54-56°C. 1 H ЯМР (200МГц, CDCI3): δ 1,88-1,92 (м, 2Н); 2,60 (т, J=7,5Гц, 2Н); 3,66 (т, J=6,3Гц, 2Н); 6,63 (д, J=8,1Гц, 2Н); 6,99 (д, J=8,1Гц, 2Н). Маса m/z (Cl): 152 [М+1]. Синтез 18 3-(4-Аміно-4-трет-бутоксифеніл)-1-пропанол До охолодженого (0°C) розчину 3-(4амінофеніл)-1-пропанолу, одержаного у Синтезі 17 (0,5г, 3,3ммоль), у дихлорметані (15мл) додають Et3N (1,4мл), а потім Вос-ангідрид (0,84мл, 3,64ммоль) і суміш перемішують протягом 72год. при кімнатній температурі. Реакційну суміш розводять ДХМ (50мл) і органічний шар промивають водою та розсолом, осушають (Na2SO 4) та упарюють до сухого залишку. Хроматографія залишку на колонці дає названу у заголовку сполуку (0,4г, 48%) у вигляді безбарвної маслянистої рідини. 1 H ЯМР (200МГц, CDCI3): δ 1,44-1,53 (м, 9Н); 1,78-1,93 (м, 2Н); 2,64 (т, J=7,6Гц, 2Н); 3,64 (т, J=6,6Гц, 2Н); 6,41 (шир.с, 1H, D2O-обмінний); 7,10 (д, J=8,3Гц, 2Н); 7,25 (д, J=8,3Гц, 2Н). Маса m/z (Cl): 252 [М+1]; 152 [M - Вос]. Синтез 19 3-(4-трет-Бутокси-4метилсульфонамідофеніл)пропілметансульфонат До охолодженого (0°C) розчину 3-(4-аміно-4трет-бутоксифеніл)-1-пропанолу, одержаного у Синтезі 18 (0,5г, 3,3ммоль), у дихлорметані (10мл) додають Et3N (1,4мл), а потім мезилхлорид (0,27мл, 3,5ммоль) і суміш перемішують протягом 4год. при кімнатній температурі. Реакційну суміш розводять ДХМ (50мл) і органічний шар промивають водою та розсолом, осушають (Na2SO4) та упарюють до сухого залишку, одержуючи названу у заголовку сполук у (0,61г, 94%). 1 H ЯМР (200МГц, CDCI3): δ 1,50 (с, 9Н); 1,952,10 (м, 2Н); 2,68 (т, J=7,5Гц, 2Н); 2,97 (с, 3H); 3,13 (с, 1Н); 3,66 (с, 2Н); 4,19 (т, J=6,3Гц, 2Н); 7,08 (д, J=8,3Гц, 2Н); 7,27 (д, J=8,3Гц, 2Н). Маса m/z (Cl): 329 [M - SO 2 Me]. Названу у заголовку сполуку одержують у вигляді твердої речовини коричневого кольору з 4оксикоричної кислоти (2г, 12,18ммоль) з використанням метанолу (25мл) та конц. H2SO4 (0,8мл) протягом 20год. за такою саме процедурою, як описано у Синтезі 15. Т.пл.: 144-146°C. 1 H ЯМР (200МГц, CDCI3): δ 3,80 (с, 3Н); 5,69 (шир.с, D2O обмінний); 6,30 (д, J=15,8Гц, 1Н); 6,85 (д, J=8,6Гц, 2Н); 7,43 (д, J=8,6Гц, 2Н); 7,64 (д, J=16,1Гц, 1Н). Маса m/z (Cl): 179 [М+1]. Синтез 21 (E)-3-(4-Гідроксифеніл)-2-пропен-1-ол Розчин метил-4-гідроксицинамату, одержаного у Синтезі 20 (1,5г, 8,43ммоль), у ТГФ (15мл) додають по краплях до суспензії LAH (416 мг) у сухому ТГФ (10мл) при 0°C і реакційну суміш перемішують при кімнатній температурі протягом 2год. Надлишок LAH гасять насич. розчином Na2SO4. С уміш фільтрують крізь шар целіту і фільтрат осушають (Na2SO4) та упарюють до сухого залишку. Залишок очищають хроматографією на колонці, використовуючи 20% EtOAc у петролейному ефірі, одержуючи названу у заголовку сполуку (0,4г, 31,6%) у вигляді білуватої твердої речовини. Т.пл.: 116-118°C. 1 H ЯМР (200МГц, CD3OD) δ: 4,17 (д, J=5,9Гц, 2Н); 6,15 (тд, J=5,9 та 15,8Гц, 1Н); 6,50 (д, J=5,9Гц, 1Н); 6,71 (д, J=8,3Гц, 2Н); 7,23 (д, J=8,6Гц, 2Н). Маса m/z (Cl): 151 [М+1]. Синтез 22 4-[(E)-3-Хлор-1пропеніл]фенілметансульфонат Названу у заголовку сполуку одержують (0,47г, 64%) з (E)-3-(4-гідроксифеніл)-2-пропен-1-олу, одержаного у Синтезі 21 (0,36г, 2,4ммоль), ДХМ (10мл), Et3N (0,83мл) та метансульфонілхлориду (0,41мл) у такий саме спосіб, як описано у Синтезі 19. 1 H ЯМР (200МГц, CDCI3): δ 3,14 (с, 3Н); 4,24 (д, J=7,0Гц, 2Н); 6,21-6,4 (м, 1Н); 6,65 (д, J=15,8Гц, 1Н); 7,25 (д, J=8,6Гц, 2Н); 7,43 (д, J=8,8Гц, 2Н). Маса m/z (Cl): 247 [М+1]. Синтез 23 (Е)-3-(4-Метилсульфонілоксифеніл)-2пропенова кислота Названу у заголовку сполуку одержують (0,53г, 36%) з (E)-4-оксикоричної кислоти (1,0г, 6,1ммоль), ДХМ (20мл), Et3N (2,12мл, 15,24ммоль) та мета 51 82835 нсульфонілхлориду (0,57мл, 7,32ммоль) у такий саме спосіб, як описано у Синтезі 19. 1 H ЯМР (200МГц, CDCI3): δ 3,20 (с, 3Н); 6,51 (д, J=15,8Гц, 1Н); 7,36 (д, J=8,6Гц, 2Н); 7,64 (д, J=8,3Гц, 2Н); 7,81 (д, J=15,8Гц, 1Н). Маса m/z (Cl): 243 [М+1]. Синтез 24 3-(4-Метилсульфонілоксифеніл)пропіонова кислота Названу у заголовку сполуку одержують (1,02г, 69,4%) з 3-(4-гідроксифеніл)пропіонової кислоти (1,0г, 6,02ммоль), ДХМ (15мл), Et3N (2,1мл, 15,06ммоль) та метансульфонілхлориду (0,56мл, 7,23ммоль) у такий саме спосіб, як описано у Синтезі 19. 1 H ЯМР (200МГц, CDCI3): δ 2,74 (т, J=7,4Гц, 2Н); 3,00-3,09 (м, 2Н); 3,14 (с, 3H); 7,14-7,37 (M, 4Н). Маса m/z (Cl): 245 [М+1]. Синтез 25 Етил-(2S)-3-(4-амінофеніл)-2-етоксипропіонат та етил-(2R)-3-(4-амінофеніл)-2-етоксипропіонат Стадія (і): Етил-3-(4-дибензиламінофеніл)-2етоксипропіонат До охолодженого розчину етил-2-етокси-3-(4амінофеніл)пропіонату (2,0г, 8,44ммоль), одержаного у Синтезі 5, у сухому ДМФ (30мл) додають Na2CO3 (2,68г, 25,3ммоль) і перемішують протягом 15хв. Потім до розчину додають по краплях бензилбромід (2,0мл, 16,88ммоль) і реакційну суміш перемішують протягом 16год. при кімнатній тем До охолодженого розчину сполуки, одержаної на стадії (іі) (1,0г, 2,57ммоль), у сухому ДХМ додають 5-гідроксибензотриазол (172мг, 1,286ммоль) та 1-(3-(диметиламіно)пропіл)-3етилкарбодіімід (EDCI) (592мг, 3,08ммоль) і реакційну суміш перемішують при 0°С протягом 30хв. (поки вона не стане прозорим розчином). Додають до розчину 2-L-фенілетаноламін (0,37г, 2,69ммоль) і перемішують при кімнатній температурі протягом 16год. Реакційну суміш розводять ДХМ (25мл), промивають водою (3´25мл), осушають (Na2SO4) та концентрують. Діастереомери 52 пературі. Реакційну суміш розводять водою (50мл) і екстрагують етилацетатом (3´50мл). Об'єднані органічні шари промивають розсолом, осушають (Na2SO4) та упарюють до сухого залишку, одержуючи названу у заголовку сполуку у вигляді жовтої маслянистої рідини (3,42г, 97%), яку використовують на наступній стадії без очищення. 1 H ЯМР (200МГц, CDCI3): δ 1,06-1,32 (м, 6H), 2,89 (д, J=6,4Гц, 2H); 3,28-3,48 (м, 1H); 3,52-3,70 (м, 1H); 3,95 (т, J=6,6Гц, 1H); 4,12 (кв, J=7,0Гц, 2H); 4,63 (с, 4H); 6,67 (д, J=7,0Гц, 2H); 7,03 (д, J=8,3Гц, 2H); 7,15-7,43 (м, 10Н). Маса m/z (Cl): 418 [М+1]. Стадія (іі): 3-(4-ДибензиламіноФеніл)-2етоксипропіонова кислота До розчину сполуки, одержаної на стадії (і) (0,5г, 1,2ммоль), у метанолі (10мл) додають Nа2СО3 (380мг, 3,6ммоль) у воді (2мл) і реакційну суміш перемішують протягом 3 днів при кімнатній температурі. Потім метанол видаляють і реакційну суміш розводять водою (10мл). Водний шар екстрагують етилацетатом для видалення будь-яких небажаних неполярних домішок. Потім водний шар підкислюють за допомогою 2Н розчину HCI до рН ~4 та екстрагують етилацетатом. Об'єднані етилацетатні шари промивають розсолом (3´10мл), осушають (Na2SO4) та концентрують, одержуючи названу у заголовку сполуку (0,340г, 74%). 1H ЯМР (200МГц, CDCI3): δ 1,17 (т, J=7,1Гц, 3H); 2,82-3,05 (м, 2Н); 3,29-3,67 (м, 2Н); 3,97-4,09 (м, 1Н); 4,63 (с, 4Н); 6,67 (д, J=8,8Гц, 2Н); 7,03 (д, J=8,3Гц, 2Н); 7,13-7,42 (м, 10Н). Маса m/z (Cl): 390 [М+1]. Стадія (III): N1-[(1S)-1-Фенілпропіл]-(2S)-3-(4дибензиламінофеніл)-2-етоксипропанамід (іііа) та N1-[(1S)-1-Фенілпропіл]-(2R)-3-(4дибензиламінофеніл)-2-етоксипропанамід (iiib) розділяють на колонці з силікагелем, використовуючи 10-45% етилацетату у петролейному ефірі. Вихід іііа: 420мг (32%); біла тверда речовина, т.пл.: 110-112°C. Вихід iiib: 380мг (29%). іііа: 1H ЯМР (200МГц, CDCI3): δ 1,18 (т, J=7,1Гц, 3H); 2,74-3,12 (м, 2Н); 3,46-3,64 (м, 2Н); 3,87 (д, J=5,4Гц, 2Н); 3,98 (дд, J=6,9 та 3,7Гц, 1Н); 4,64 (с, 4Н); 4,93-5,05 (м, 1Н); 6,64 (д, J=8,4Гц, 2Н); 7,02 (д, J=8,3Гц, 2Н); 7,12-7,46 (м, 15Н). Маса m/z (Cl): 509 [М+1]. iiib: 1H ЯМР (200МГц, CDCI3): δ 1,13 (т, J=7,6Гц, 3H); 2: 80-3,16 (м, 2Н); 3,39-3,68 (м, 4Н); 53 82835 3,96 (дд, J=3,9 та 5,5Гц, 1Н); 4,64 (с, 4Н); 4,85-5,00 (м, 1Н); 6,67 (д, J=6,8Гц, 2Н); 6,97 (д, J=6,8Гц, 2Н); 7,06 (д, J=8,3Гц, 2Н); 7,12-7,42 (м, 13Н). Маса m/z (Cl): 509 [М+1]. Стадія (іv): (2S)-3-(4-Дибензиламінофеніл)-2етоксипропіонова кислота (iva) До розчину сполуки іііа (410мг, 0,8ммоль) у діоксані (6мл) додають 1М Н2SО4 (4мл) і реакційну суміш нагрівають до кипіння зі зворотним холодильником протягом 24год. Діоксан видаляють при зниженому тиску і залишок розводять водою (10мл). Водний шар екстрагують етилацетатом (3´25мл) і об'єднані органічні шари промивають розсолом, осушають (Na2SO4) та упарюють до сухого залишку. Сирову масу очи щають на силікагелі, використовуючи 40% етилацетату у петролейному ефірі, одержуючи названу у заголовку сполуку (180мг, 58%). [α]D25=1,8° (с 0,5, MeOH). 1 H ЯМР (200МГц, CDCI3): δ 1,16 (т, J=7,6Гц, 3H); 2,80-3,07 (м, 2Н); 3,43-3,68 (м, 2Н); 4,16 (дд, J=7,3 та 4,4Гц, 1Н); 4,61 (с, 4Н); 6,65 (д, J=8,3Гц, 2Н); 7,04 (д, J=8,8Гц, 2Н); 7,12-7,39 (м, 10Н). Маса m/z (Cl): 390 [М+1]. (2R)-3-(4-Дибензиламінофеніл)-2етоксипропіонова кислота (ivb) Сполуку ivb одержують (152мг, 60%) зі сполуки iiib (0,5г, 0,98ммоль), використовуючи 1 М H2SO4 (5мл) у діоксані при кип'ятінні зі зворотним холодильником протягом 24год. з використанням такої саме процедури, як описано для синтезу сполуки iva. 1 H ЯМР (200МГц, CDCI3): δ 1,18 (т, J=7,0Гц, 3H); 2,83-3,05 (м, 2Н); 3,40-3,67 (м, 2Н); 4,03 (дд, J=7,3 та 4,3Гц, 1Н); 4,63 (с, 4Н); 6,67 (д, J=8,6Гц, 2Н); 7,03 (д, J=8,6Гц, 2Н); 7,15-7,40 (м, 10Н). Маса m/z (Cl): 390 [М+1]. Стадія (v): Етил-(25)-3-(4дибензиламіноФеніл)-2-етоксипропіонат (va) До охолодженого розчину сполуки iva (1,2г, 3,08ммоль) у сухому ДМФ (30мл) додають K2CO3 (1,277г, 9,25ммоль) і перемішують протягом 15хв. при низькій температурі. Додають етилйодид (0,75мл, 9,25ммоль) і реакційну суміш залишають при перемішуванні на 3год. при кімнатній темепратурі. Додають воду і реакційну суміш екстрагують етилацетатом (3*30мл). Об'єднані органічні шари промивають (розеол), осушають (Na2SO4) та концентрують, одержуючи названу у заголовку сполуку (1,1г, 85%). 54 1 H ЯМР (200 3МГц, CDCI3): δ 1,09-1,30 (м, 6Н); 2,90 (д, J=6,5Гц, 2Н); 3,27-3,67 (м, 2Н); 3,96 (т, J=6,7Гц, 1Н); 4,14 (кв, J=7,3Гц, 2Н); 4,63 (с, 4Н); 6,65 (д, J=8,6Гц, 2Н); 7,03 (д, J=8,3Гц, 2Н); 7,157,42 (м, 10Н). Маса m/z (Cl): 418 [М+1]. Етил (2R)-3-(4-ДибензиламіноФеніл)-2етоксипропіонат (vb) Сполуку vb (120мг, 74%) одержують зі сполуки ivb (150мг, 0,39ммоль), K2CO3 (156мг, 1,17ммоль), етилйодиду (0,09мл, 1,17ммоль) у сухому ДМФ з використанням такої саме процедури, як описано для синтезу va. 1 H ЯМР (200МГц, CDCI3): δ 1,08-1,30 (м, 6Н); 2,89 (д, J=6,4Гц, 2Н); 3,28-3,67 (м, 2Н); 3,95 (T, J=10Гц, 1Н); 4,13 (кв, J=7,0Гц, 2Н); 4,62 (с, 4Н); 6,64 (д, J=8,6Гц, 2Н); 7,02 (д, J=8,6Гц, 2Н); 7,197,40 (м, 10Н). Маса m/z (Cl): 418 [М+1]. Стадія (vі): Етил-(2S)-3-(4-амінофеніл)-2етоксипропіонат (via) До розчину va (1,0г, 2,4ммоль) у метанолі (20мл) додають 10% Pd-C (0,2г, 20% мас/мас.) і суміш гідрують у гідрогенізаторі Parr при 414кПа (60psi) протягом 24год. при кімнатній температурі. Реакційну суміш фільтр ують крізь целіт та промивають фільтрувальний шар метанолом. Об'єднані шари упарюють до сухого залишку і залишок очищають на силікагелі з використанням 20% EtOAc у петролейному ефірі, одержуючи названу у заголовку сполуку (300мг, 53%). 1 H ЯМР (200МГц, CDCI3): δ 1,17 (т, J=6,8Гц, 3H); 1,23 (т, J=7,0Гц, 3H); 2,91 (д, J=6,8Гц, 2Н); 3,25-3,79 (м, 2Н); 3,95 (т, J=6,8Гц, 1Н); 4,13 (кв, J=7,6Гц, 2Н); 6,62 (д, J=8,3Гц, 2Н); 7,03 (д, J=8,3Гц, 2Н). Маса m/z (Cl): 238 [М+1]. Етил-(2R)-3-(4-аміноФеніл)-2етоксипропіонат(vіb) Сполуку vib одержують (1,6г, 84%) зі сполуки vb (1,6г, 3,89ммоль), використовуючи 10% Pd-C (0,32г, 20% мас/мас.) у метанолі (20мл) протягом 24год. з використанням такої саме процедури, як описано для синтезу сполуки via. 1 H ЯМР (200МГц, CDCI3): δ 1,17 (т, J=7,0Гц, 3H); 1,23 (т, J=7,0Гц, 3H); 2,90 (д, J=6,7Гц, 2H); 3,25-3,80 (м, 2H); 3,94 (т, J=6,7Гц, 1H); 4,16 (кв, J=7,1Гц, 2H); 6,61 (д, J=8,3Гц, 2H); 7,03 (д, J=8,1Гц, 2H). Маса m/z (Cl): 238 [М+1]. Синтез 26 (S)-Етил-2-етокси-3-(4-амінофеніл)пропіонат 55 82835 56 1 Стадія (і) До розчину (S)-(4-нітрофеніл)гліцину (10г, 47,6ммоль) у суміші води (50мл), H2SO4 (1 M, 60мл) та ацетону (150мл) при -5°C додають по краплях при перемішуванні розчин нітриту натрію (9,85г, 142,8ммоль) у воді (40мл) протягом 30хв. Реакційну суміш перемішують при температурі від -5 до 0°C протягом ще 1,5год., а потім перемішують при кімнатній температурі протягом 16год. Ацетон видаляють, а реакційну суміш розводять 500мл етилацетату. Органічний шар промивають розсолом, осушають над безводним Na2SO4 та концентрують. Сирову масу очищають кристалізацією з ізопропілацетату (9,0г, 96%). Т.пл.: 134-136°C. [α]D: -25 °(с 1,0, MeOH). 1 H ЯМР (CDCI3): δ 3,04 (дд, J=14, 7,8Гц, 1Н), 3,24 (дд, J=14, 4,Гц, 1Н), 4,39 (дд, J=7,3, 4,1Гц, 1Н), 7,42 (д, J=8,7Гц, 2Н), 8,16 (д, J=8,7Гц, 2Н). ІЧ (чиста речовина) см-1: 3485, 3180, 2927, 1715, 1515, 1343. Маса m/z (Cl): 212 (М+1). Стадія (іі) (S)-2-Окси-3-(4-нітрофеніл)пропіонову кислоту (9,0г, 42,6ммоль), одержану на стадії (і) вище, розчиняють у сухому EtOH (300мл). До цього розчину додають конц. H 2SO4 (326 мкл, 5,9ммоль), та кип'ятять зі зворотним холодильником протягом 56год. Реакційну суміш нейтралізують водним бікарбонатом натрію. Етанол конденсують на обертовому випарнику, і залишок розчиняють у етилацетаті. Органічний шар промивають водним бікарбонатом натрію, водою, розсолом, а потім осушають над безводним Na2SO4 та концентрують. Бажаний продукт одержують з сирової маси кристалізацією з діізопропілового ефіру (8,0г, 78,5%). Т.пл.: 74-76°C. [α]D:-13° (с 1,0, MeOH). 1 H ЯМР (CDCI3): δ 1,30 (т, J=7Гц, 3H), 3,06 (дд, J=14, 7,Гц, 1H), 3,25 (дд, J=14, 4,3,Гц, 1Н), 4,25 (кв. J=7Гц, 2Н), 4,25 (дд, J=7, 4,3Гц, 1Н), 7,42 (д, J=8,7Гц, 2H), 8,16 (д, J=8,7Гц, 2Н). ІЧ (чиста речовина) см-1: 3432, 2924, 1736, 1518, 1347. Маса m/z (Cl): 240-(М+1). Стадія (ііі) До суміші (S)-етил-2-гідрокси-3-(4нітрофеніл)пропіонату (4,77г, 19,95ммоль), одержаного на стадії (іі) вище, молекулярних сит (4A) (5,0г) та порошкоподібного Аg2О (13,8г, 59,8ммоль) у сухому ацетонітрилі (100мл) додають етилйодид (6,4мл, 79,8ммоль) при кімнатній температурі. Реакційну суміш нагрівають при 60°C протягом 16год. Реакційну суміш фільтрують крізь целіт та концентрують. Сирову масу піддають хроматографії з використанням етилацетату та гексанів, одержуючи бажаний продукт у вигляді в'язкої рідини (3,5г, вихід окремої стадії 67%). Видобувають непрореагований вихідний матеріал (900мг), який може бути використаний повторно. [α]D: -26° (с 1,0, MeOH). H ЯМР (CDCI3): δ 1,15 (т, J=7Гц, 3H); 1,26 (т, J=7,1Гц, 3H); 3,10 (д, J=3,8Гц, 1Н); 3,13 (с, 1Н); 3,16-3,35 (м, 1Н); 3,45-3,65 (м, 1Н); 4,03 (дд, J=7,5, 5,4Гц, 1Н); 4,21 (кв. J=7,2Гц, 2Н); 7,43 (д, J=8,6Гц, 2Н); 8,15 (д, J=8,6Гц, 2Н). ІЧ (чиста речовина) см-1: 2980, 1747, 1604, 1521, 1347. Маса m/z (Cl): 268 (М+1). Стадія (іv) (S)-Етил-2-етокси-3-(4-нітрофеніл)пропіонат (6,0, 25,3ммоль), одержаний на стадії (ііі) вище, розчиняють у сухому метанолі (100мл). До цього розчину додають 10% Pd/C (2,0г) і гідрують з використанням газоподібного водню (138кПа, 20psi) протягом 3 - 4год. Реакційну суміш фільтр ують крізь целіт і фільтрат концентрують, одержуючи сиропоподібну масу. Продукт одержують з кількісним виходом. [α]D:-14,2° (с 1,0, MeOH). Хіральна ВЕРХ: е.н. (енантіомерний надлишок) >98%. 1 H ЯМР (CDCI3): δ 1,16 (т, J=7,0Гц, 3H), 1,22 (т, J=7,0Гц, 3H), 2,90 (д, J=6,3Гц, 2H)1 3,30 (шир.с, 2Н, NH2), 3,24-3,42 (м, 1H), 3,50-3,70 (м, 1H), 3,94 (т, J=6,3Гц, 1H), 4,15 (кв. J=7,0Гц, 2H), 6,62 (д, J=8,3Гц, 2H), 7,03 (д, J=8,0Гц, 2H). ІЧ (чиста речовина) см -1: 3372, 1738. Маса m/z (Cl): 238 (М+1), 192 (M - OC 2H5). Синтез 27 (S)-Етил-2-метокси-3-(4-амінофеніл)пропіонат Стадія (і) До суміші (S)-етил-2-гідрокси-3-(4нітрофеніл)пропіонату (12,5г, 52,3ммоль), одержаного на стадії (іі) Синтезу 26, та порошкоподібного Ag2O (36,3г, 157ммоль) у сухому ацетонітрилі (260мл) додають метил йодид (13мл, 209,2ммоль) при кімнатній температурі. Додають активованімолекулярні сита (4A) (12,5г), а потім реакційну суміш перемішують при кімнатній температурі протягом 16год. Реакційну суміш фільтрують крізь целіт та концентрують. Сирову масу піддають хроматографії з використанням етилацетату та гексанів, одержуючи бажаний продукт у вигляді в'язкої рідини (10,0г, 75%). [α]D:-30,1° (с 1,0, MeOH). 1 H ЯМР (CDCI3): δ 1,24 (т, J=7,1Гц, 3H); 3,09 (д, J=5,4Гц, 1Н); 3,12 (д, J=2,7Гц, 1Н); 3,35 (с, 3H); 3,96 (дд, J=7,5, 5,1Гц, 1Н); 4,19 (кв, J=7,1Гц, 2Н); 7,39 (д, J=8,6Гц, 2Н); 8,13 (д, J=8,6Гц, 2Н). ІЧ (чиста речовина) см-1: 2995, 1747, 1604, 1521, 1343. Маса m/z (Cl): 254 (М+1). Стадія (іі) (S)-Етил-2-метокси-3-(4-нітрофеніл)пропіонат (8,0, 31,6ммоль), одержаний на стадії (і) вище, розчиняють у сухому метанол (200мл). До цього розчину додають 10% Pd/C (2,5г) та гідрують з використанням газоподібного водню (138кПа, 20psi) протягом 3 - 4год. Реакційну суміш фільтрують крізь целіт та концентрують до сиропоподібної маси. Після хроматографії на колонці з викорис 57 82835 танням етилацетату/гексанів виділяють бажаний продукт у вигляді в'язкої рідини (7,0г, кількісний вихід). [α]D:-14,1° (с 1,0, MeOH). Хіральна ВЕРХ: е.н. >98%. 1 H ЯМР (CDCI3): δ 1,23 (т, J=7,2Гц, 3H), 2,91 (д, J=6,1Гц, 2Н), 3,30 (шир.с, 2Н, NH2), 3,34 (с, 3H), 3,88 (т, J=6,2Гц, 1Н), 4,17 (кв, J=7,2Гц, 2H)1 6,62 (д, J=8,3Гц, 2Н), 7,01 (д, J=8,1Гц, 2Н). ІЧ (чиста речовина) см-1: 3372, 2985, 2932, 1739, 1627, 1519. Маса m/z (Cl): 223 (M), 234 (М+1), 192 (M OMe). Синтез 28 (S)-Етил2-етокси-3-(4-амінофеніл)пропіонат Стадія (і) (S)-Етил-2-гідрокси-3-(4-нітрофеніл)пропіонат (9,6г, 40,1ммоль), одержаний на стадії (іі) Сийтезу 26, розчиняють у етилацетаті (250мл). До цього розчину додають 10% Pd/C (7,0г) та гідрують з використанням газоподібного водню (138кПа, 20psi) протягом 3 - 4год. Реакційну суміш фільтрують крізь целіт та концентрують, одержуючи сиропоподібну масу. Після хроматографіє на колонці з використанням етилацетату/гексанів виділяють бажаний продукт у вигляді в'язкої рідини (6,1г, 72%). [α]D: +6,5° (с 1,0, MeOH). 1 H ЯМР (CDCI3): δ 1,25 (т, J=7,2Гц, 3H), 2,83 (дд, J=14, 6,5Гц, 1H)1 2,98 (дд, J=14, 4,6Гц, 1Н), 3,35 (шир.с, 2Н, NH2), 4,17 (кв, J=7,2Гц, 2Н), 4.33 (дд, J=6,5, 4,6Гц, 1Н), 6,58 (д, J=8,4Гц, 2Н), 6,97 (д, J=8,1Гц, 2Н). ІЧ (чиста речовина) см-1: 3372, 2985, 2932, 1739, 1627, 1519. Маса m/z (Cl): 209 [M] 1 210 [М+1]. Стадія (іі) Суміш (S)-етил-2-гідрокси-3-(4амінофеніл)пропіонату (4,0г, 19,1ммоль), одержаного на стадії (і) вище, бензилброміду (4,7мл, 40,19ммоль) та безводного Na2CO3 (6,07г, 57,3ммоль) у сухому ДМФ (100мл) перемішують при кімнатній температурі протягом 16год. Реакційну суміш розводять етилацетатом (300мл), промивають 10%-ною водною лимонною кислотою, осушають над безводним Na2SO4 та концентрують. Після хроматографії на колонці з використанням етилацетату/гексанів виділяють бажаний продукт у вигляді в'язкої рідини (4,5г, 61%). [α]D:-12° (с 0,1, MeOH). 1 H ЯМР (CDCI3): δ 1,25 (т, J=7,2Гц, 3H), 2,16 (с, ОН); 2,84 (дд, J=14, 6,5,Гц, 1Н), 2,99 (дд, J=14, 4ДГц, 1Н), 4,19 (кв, J=7,2Гц, 2Н), 4,31-4,37 (м, 1Н), 4,62 (с, 4Н), 6,66 (д, J=8.8Н2, 2Н), 7,01 (д, J=8,8Гц, 2Н); 7,21-7,35 (ароматичне ядро, 10Н). ІЧ (чиста речовина) см-1: 3497, 3062, 3028, 1733, 1615, 1521. Маса m/z (CI): 390 [М+1]. Стадія (ііі) (S)-Етил-2-гідрокси-3-(4дибензиламінофеніл)пропіонат (4,5г, 1,0екв., 58 11,57ммоль), одержаний на стадії (іі) вище, гідролізують у МеОН-ТГФ-воді за допомогою LiOH×H2O (972мг, 2екв., 23,1ммоль) при кімнатній температурі. Реакційну суміш концентрують і доводять до рН3. Бажана кислота випадає до осаду, який потім збирають на фільтрі (4,0г, вихід 96 %). Т.пл.: 114-116°C. 1 H ЯМР (CDCI3): δ 2,83 (дд, J=14, 7Гц, 1Н); 3,09 (дд, J=14, 3,5Гц, 1Н), 4,35-4,44 (м, 1Н), 4,62 (с, 4Н); 6,68 (д, J=8,3Гц, 2Н), 7,03 (д, J=8,3Гц, 2Н); 7,21-7,35 (ароматичне ядро, 10Н). ІЧ (чиста речовина) см-1: 3450, 3028, 2923, 1725, 1615, 1521. Маса m/z (Cl): 362 [М+1]. Стадія (iv) До розчину (S)-2-окси-3-(4дибензиламінофеніл)пропіонової кислоти (4,0г, 11,1ммоль), одержаної на стадії (ііі), у сухому ДМФ (56мл) додають порціями NaH (60% у маслі, 886мг, 22,2ммоль) при кімнатній температурі. Одержану суміш перемішують при 50°C протягом 2год. Реакційну суміш знов охолоджують до кімнатної температури і додають етилйодид (2,67мл, 33,3ммоль). Одержану суміш перемішують при кімнатній температурі протягом 16год. Реакційну суміш розводять етилацетатом та промивають водою та розсолом. Органічний шар осушають над безводним Na2SO4 та концентрують. Залишок очищають хроматографією на колонці з використанням етилацетату/гексанів, одержуючи бажаний продукт у вигляді в'язкої рідини (2,65г, вихід 57%). [α]D:-3,5° (с 1,0 MeOH). 1 H ЯМР (CDCI3): δ 1,18 (т, J=7,0Гц, 3H), 1,20 (т, J=7,3Гц, 3H), 2,91 (д, J=6,7Гц, 2Н), 3,30-3,48 (M, 1Н), 3,52-3,70 (м, 1Н), 3,97 (т, J=6,7Гц, 1Н), 4,15 (кв, J=7,2Гц, 2H), 4,62 (с, 4Н), 6,67 (д, J=8,3Гц, 2H)1 7,04 (д, J=8,0Гц, 2H), 7,23-7,36 (ароматичне ядро, 10Н). ІЧ (чиста речовина) см-1: 3027, 2978, 1744, 1616, 1521. Маса m/z (Cl): 418 (М+1). Стадія (v) (S)-Етил-2-етокси-3-(4дибензиламінофеніл)пропіонат, одержаний на стадії (iv) вище, гідр ують за допомогою Pd/C (10%) та газоподібного водню (138-207кПа, 20-30psi) у етилацетатному розчиннику протягом 3 - 4год. Бажаний продукт одержують з реакційної суміші концентруванням фільтрату одразу після відокремлення каталізатора фільтрацією. [α]D:-14,2° (с 1,0, MeOH). Хіральна ВЕРХ: е.н. >98%. 1 H ЯМР (CDCI3): δ 1,16 (т, J=7,0Гц, 3H), 1,22 (т, J=7,0Гц, 3H), 2,90 (д, J=6,3Гц, 2Н), 3,30 (шир.с, 2Н, NH2), 3,24-3,42 (м, 1Н), 3,50-3,70 (м, 1Н), 3,94 (т, J=6,3Гц, 1Н), 4,15 (кв. J=7,0Гц, 2Н), 6,62 (д, J=8,3Гц, 2H)1 7,03 (д, J=8,0Гц, 2Н). ІЧ (чиста речовина) см -1: 3372, 1738. Маса m/z (Cl): 238 (М+1), 192 (M - OC 2H5). Приклад 1 (S)-Етил-2-метокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонат 59 82835 Суміш 4-(3метансульфонілоксипропіл)фенілметансульфонату (5,5г, 1,0екв., 17,9ммоль), одержаного у Синтезі 1, (S)-етил-2метокси-3-(4-амінофеніл)пропіонату (4,0г, 1,0екв., 17,9ммоль), одержаного у Синтезі 27, тетрабутиламонійброміду (2,8г, 0,5екв., 9,0ммоль) та безводного K2СО3 (7,4г, 3,0екв., 53,7ммоль) у сухому толуолі (90мл) нагрівають при перемішуванні до 90°C протягом 7-9год. Реакційну суміш розводять етилацетатом (300мл) та промивають водою і розсолом. Органічний шар осушають (Na2SO4), конденсують і залишок піддають хроматографії з використанням етилацетату та гексанів, одержуючи названу у заголовку сполуку у вигляді в'язкої рідини (3,4г, 44%). [α]25D:-6,5°(c1,0, MeOH). 1 H ЯМР (CDCI3, 200МГц): δ 1,26 (т, J=7,0Гц, 3H); 1,98 (квінтет, J=7,2Гц, 2H); 2,75 (т, J=7,6Гц, 2H); 2,93 (д, J=5,9Гц, 2H); 3,02-3,22 (м, 5H); 3,37 (с, 3H); 3,91 (т, J=6,4Гц, 1H); 4,20 (кв, J=7,0Гц, 2H); 6,65 (д, J=8,0Гц, 2H); 7,08 (д, J=8,3Гц, 2H); 7,15-7,3 (ароматичне ядро, 4H). ІЧ (чиста речовина) см-1: 3405, 2934, 2934, 1739, 1617, 1522, 1367. Маса m/z (Cl): 435 [M], 436 [М+1]. Приклад 2 Етил-2-етокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламіно}феніл]пропіонат Починаючи з 4-(3метансульфонілоксипропіл)фенілметансульфонату, одержаного у Синтезі 1, та етил-2-етокси-3-(4-амінофеніл)пропіонату, одержаного у Синтезі 5, одержують названу у заголовку сполуку у вигляді в'язкої рідини (вихід 40%) за процедурою Прикладу 1. 1 H ЯМР (CDCI3, 200МГц): δ 1,16 (т, J=5,8Гц, 3H); 1,21 (т, J=5,8Гц, 3H); 1,91 (квінтет, J=7,2Гц, 2Н); 2,72 (т, J=7,3Гц, 2Н); 2,88 (д, J=6,3Гц, 2Н); 3,02-3,18 (м, 5Н); 3,22-3,42 (м, 1Н); 3,42-3,62 (м, 1Н); 3,93 (т, J=6,5Гц, 1Н); 4,15 (кв, J=7,3Гц, 2Н); 6,51 (д, J=8,3Гц, 2Н); 7,10 (д, J=8,3Гц, 2Н); 7,157,24 (ароматичне ядро, 4Н). ІЧ (чиста речовина) см-1: 3400, 2978, 2934, 1738, 1616, 1502. Маса m/z (Cl): 449 [M], 450 [М+1]. Приклад 3 (S)-Етил-2-етокси-3-[4-{3-(4метансульфонілоксифеніл)пропіламідо}феніл]пропіонат 60 З 4-(3метансульфонілоксипропіл)фенілметансульфонату, одержаного у Синтезі 1, та (S)-етил-2-етокси-3-(4-амінофеніл)пропіонату, одержаного у Синтезі 26, одержують названу у заголовку сполуку за процедурою Прикладу 1. [α]25D:-6,3° (1,0, MeOH). 1 H ЯМР (CDCI3, 200МГц): δ 1,16 (т, J=5,8Гц, 3H); 1,21 (т, J=5,8Гц, 3H); 1,91 (квінтет, 7,2Гц, 2Н); 2,72 (т, J=7,3Гц, 2Н); 2,88 (д, J=6,3Гц, 2Н); 3,023,18 (м, 5Н); 3,22-3,42 (м, 1Н); 3,42-3,62 (м, 1Н); 3,93 (т, J=6,5Гц, 1Н); 4,15 (кв, J=7,3Гц, 2Н); 6,51 (д, J=8,3Гц, 2Н); 7,10 (д, J=8,3Гц, 2Н); 7,15-7,24 (ароматичне ядро, 4Н). ІЧ (чиста речовина) см-1: 3400, 2978, 2934, 1738, 1616, 1502. Маса m/z (Cl): 449 [M], 450 [М+1]. Приклад 4 Етил-2-етокси-3-[4-{3-(4метансульфонілоксифеніл)пропілоксикарбоніламіно}феніл]пропіонат Названу у заголовку сполуку одержують як побічний продукт під час синтезу за Прикладом 2 (вихід 20%). 1 H ЯМР (CDCI3, 200МГц): δ 1,14 (т, J=7Гц, 3H); 1,22 (т, J=7Гц, 3H); 1,98 (квінтет, J=7Гц, 2Н); 2J2 (т, J=8Гц, 2Н); 2,95 (д, J=6,1Гц, 2Н); 3,10 (с, 3H); 3,253,45 (м, 1Н); 3,50-3,70 (м, 1Н); 3,97 (т, J=6,4Гц, 1Н); 4,05-4,24 (м, 4Н); 6,68 (с, NH); 7,10-7,30 (ароматичне ядро,
ДивитисяДодаткова інформація
Назва патенту англійськоюb-aryl-a-oxysubstituted propionuc acid derivatives and pharmaceutical composition based thereon
Автори англійськоюBhuniya Debnath, Das Saibal Kumar, Madhavan Gurram Ranga, Iqbal Javed, Chakrabarti Ranjan, Vikramadithyan Reeba Kannimel
Назва патенту російськоюПроизводные b-арил-a-оксизамещенной пропионовой кислоты и фармацевтическая композиция на их основе
Автори російськоюБхуния Дебназ, Дас Сайбал Кумар, Мадхаван Гуррам Ранга, Икбал Джавед, Чакрабарти Ранджан, Викрамадизиан Рееба Каннимел
МПК / Мітки
МПК: C07C 311/53, A61P 25/28, A61P 9/12, A61K 31/255, A61P 1/18, A61P 3/10, A61P 3/04, A61P 15/08, A61P 17/06, A61P 3/06, A61P 21/04, A61P 35/00, C07C 303/00, A61P 1/04, C07C 279/14, A61P 29/00, A61P 13/12, C07C 309/00, A61K 45/00, A61P 9/00, A61P 27/02, A61P 19/10, A61K 31/216, A61P 9/10
Код посилання
<a href="https://ua.patents.su/42-82835-pokhidni-b-aril-a.html" target="_blank" rel="follow" title="База патентів України">Похідні b-арил-a</a>
Попередній патент: Спосіб ущільнення тонкодисперсних матеріалів
Наступний патент: Пристрій для багатоадресних передач (варіанти) та спосіб широкого мовлення для групи абонентів (варіанти)
Випадковий патент: Масообмінний контактний пристрій












