Спосіб отримання ефірів 2,4,6-заміщених хіназолініл(1,2-дигідро-4н)-оцтової-3 кислоти
Номер патенту: 12331
Опубліковано: 15.02.2006
Автори: Руденко Олег Павлович, Ганевич Віктор Миколайович, Галкин Борис Миколайович
Формула / Реферат
Спосіб отримання ефірів 2,4,6-заміщених хіназолініл(1,2-дигідро-4Н)-оцтової-3 кислоти загальної формули 1:
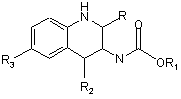 ,(1)
,(1)
де R означає (пара-бром)феніл п-ВrС6Н4, (пара-хлор)феніл п-СlС6Н4, (орто-хлор)феніл о- п-СlС6Н4, (пара-фтор)феніл п-FС6Н4, (орто-фтор)феніл o-FС6Н4, (пара-окси)феніл п-НОС6Н4, (орто-окси)феніл о-НОС6Н4, (пара-метокси)феніл п-СН3ОС6Н4, (орто-метокси)-феніл о-СН3ОС6Н4, (2,4-диметокси)феніл 2,4-(СН3О)2С6Н2, (3,4-диметокси)феніл 3,4-(СН3О)2С6Н3, (3,4,5-триметокси)феніл 3,4,5-(СН3О)3С6Н2, (2-окси-3-нітро-5-метокси)-феніл 2-НО-3-O2Н-5-СН3ОС6Н2, (пара-нітро)феніл п-O2NC6H4, (мета-нітро)феніл м-О2NC6H4, (пара-диметиламіно)феніл п-(CH3)2NC6H4, (пара-діетиламіно)феніл п-(С2Н5)2NC6H4; R1 - метил СН3, етил C2H5; R2 - феніл С6Н5, (орто-хлор)феніл о-СlС6Н4; R3 - бром, хлор або метил, яка включає ефіри формули 2 як вихідні продукти, який відрізняється тим, що до суміші ефіру формули 2:
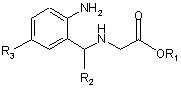 ,(2)
,(2)
де R1, R2 і R3 указані вище, з альдегідом формули RCHO (3), де R указаний вище, в співвідношенні 1:1 додають 0,017-0,019 частини, відносно ефіру формули 2, хлориду кальцію, кип’ятять в метанолі до розчинення, додають 2,5 частини, відносно метанола, безводного бензолу, упарюють при атмосферному тиску на 3/4, закінчення реакції контролюють тонкошаровою хроматографією, додають хлороформ, вільний від гідрохлориду, розчин фільтрують, упарюють на 3/4, додають метанол до розчину, кристалізують при 20-23°С, осад відфільтровують, промивають метанолом і ефіром, висушують при 20-23°С і 60-63°С.
Текст
Спосіб отримання ефірів 2,4,6-заміщених хіназолініл(1,2-дигідро-4Н)-оцтової-3 кислоти загальної формули 1: H R N O 2 (пара-нітро)феніл п-O2NC6H4, (мета-нітро)феніл мО2NC6H4, (пара-диметиламіно)феніл п(CH3)2NC6H4, (пара-діетиламіно)феніл п(С2Н5)2NC6H4; R1 - метил СН3, етил C2H5; R2 - феніл С6Н5, (орто-хлор)феніл о-СlС6Н4; R3 - бром, хлор або метил, яка включає ефіри формули 2 як вихідні продукти, який відрізняється тим, що до суміші ефіру формули 2: NH2 O H N R3 OR1 R2 де R означає (пара-бром)феніл п-ВrС6Н4, (парахлор)феніл п-СlС6Н4, (орто-хлор)феніл о-СlС6Н4, (пара-фтор)феніл п-FС6Н4, (орто-фтор)феніл 0FC6H4, (пара-окси)феніл п-НОС6Н4, (ортоокси)феніл о-НОС6Н4, (пара-метокси)феніл пСН3ОС6Н4, (орто-метокси)-феніл о-СН3ОС6Н4, (2,4діметокси)феніл 2,4-(СН3О)2С6Н3, (3,4діметокси)феніл 3,4-(СН3О)2С6Н3, (3,4,5триметокси)феніл 3,4,5-(СН3О)3С6Н2, (2-окси-3нітро-5-метокси)-феніл 2-НО-3-O2N-5-СН3ОС6Н2, (пара-нітро)феніл п-O2NC6H4, (мета-нітро)феніл м (19) Спосіб отримання відноситься до галузі біологічно активних похідних хіназоліну, конкретно до корисної моделі отримання ефірів хіназолініл(1,2дигідро-2R-4Н-4R2-6R3)оцтової-3 кислоти загальної формули 1 UA (11) ,(1) де R означає (пара-бром)феніл п-ВrС6Н4, (парахлор)феніл п-СlС6Н4, (орто-хлор)феніл о- п-СlС6Н4, (пара-фтор)феніл п-FС6Н4, (орто-фтор)феніл oFС6Н4, (пара-окси)феніл п-НОС6Н4, (ортоокси)феніл о-НОС6Н4, (пара-метокси)феніл пСН3ОС6Н4, (орто-метокси)-феніл о-СН3ОС6Н4, (2,4диметокси)феніл 2,4-(СН3О)2С6Н2, (3,4диметокси)феніл 3,4-(СН3О)2С6Н3, (3,4,5триметокси)феніл 3,4,5-(СН3О)3С6Н2, (2-окси-3нітро-5-метокси)-феніл 2-НО-3-O2Н-5-СН3ОС6Н2, (13) OR1 ,(2) де R1, R2 і R3 указані вище, з альдегідом формули RCHO (3), де R указаний вище, в співвідношенні 1:1 додають 0,017-0,019 частини, відносно ефіру формули 2, хлориду кальцію, кип’ятять в метанолі до розчинення, додають 2,5 частини, відносно метанола, безводного бензолу, упарюють при атмосферному тиску на 3/4, закінчення реакції контролюють тонкошаровою хроматографією, додають хлороформ, вільний від гідрохлориду, розчин фільтрують, упарюють на 3/4, додають метанол до розчину, кристалізують при 20-23°С, осад відфільтровують, промивають метанолом і ефіром, висушують при 20-23°С і 60-63°С. 12331 N R3 U R2 3 12331 4 O2NС6Н4, (пара-діметиламіно)феніл пЦей технічний результат досягається описува(CH3)2NC6H4, (пара-діетиламіно)феніл пною корисною моделлю отримання ефірів 2,4,6(С2Н5)2NС6Н4; R1 - метил СН3, етил С2Н5; R2 - фезаміщених хіназолініл(1,2-дигідро-4Н)оцтової-3 ніл С6Н5, (орто-хлор)феніл о-СlС6Н4; R3 - бром, кислоти загальної формули 1 хлор або метил, яка може бути використана в синтезі ноотропних лікарських засобів пролонгірованої дії. Рівень техніки в даній галузі характеризується слідуючим. Відомий спосіб отримання ефірів хіназолінон-2-(1,4-дигідро-4-феніл)оцтової-3 кислоти де R означає (пара-бром)феніл п-ВrС6Н4, (параформули 4 (схема 1), [А.с. СССР, №707191, 1979], хлор)феніл п-СlС6Н4, (орто-хлор)феніл о-СlС6Н4, де в якості вихідного продукту використовують (пара-фтор)феніл п-FС6Н4, (орто-фтор)феніл оефіри N-(2-амінобензгідрил)гліцину формули 2 і FС6Н4, (пара-окси)феніл п-НОС6Н4, (ортойого взаємодію з алкіл- або бензилхлоркарбонаокси)феніл о-НОС6Н4, (пара-метокси)феніл птом формули 5 в присутності триетиламіну СН3ОС6Н4, (орто-метокси)-феніл о-СН3ОС6Н4, (2,4діметокси)феніл 2,4-(СН3О)2С6Н3, (3,4діметокси)феніл 3,4-(СН3О)2С6Н3, (3,4,5триметокси)феніл 3,4,5-(СН3О)3С6Н2, (2-окси-3нітро-5-метокси)-феніл 2-НО-3-O2N-5-СН3ОС6Н2, (пара-нітро)феніл п-O2НС6Н4, (мета-нітро)феніл мде R1 означає метил СН3, етил СН2СН3; R2 - феніл O2NС6Н4, (пара-діметиламіно)феніл пС6Н5, R3 - бром, хлор, метил; (СН3)2NС6Н4, (пара-діетиламіно)феніл пR5 бензил С6Н5СН2 або ізобутил (C2H5)2NC6H4; R1 - метил СН3, етил С2Н5; R2 - феСН3СН2СНСН3. ніл С6Н5, (орто-хлор)феніл о-СlС6Н4; R3 - бром, Схема 1 хлор або метил, згідно якої до суміші ефіру N-(2Відомий спосіб отримання ефірів 2,4,6амінобензгідрил)гліцину формули 2, заміщених хіназолініл(1,2-дегідро-4Н)-оцтової-3 кислоти формули 6 (схема 2) [заявка України, №20031110218, поз. ріш. від 02.06.04], де як вихідні продукти використовують ефіри N-(2амінобензгідрил)гліцину формули 2, їх взаємодію з де R1, R2 і R3 указані вище, з альдегідом загальної хлорангідридами органічних кислот формули 7 і формули RCHO (3), де R указаний вище, в співвідпослідуючою каталітичною дією оцтової кислоти ношенні 1:1 додають 0,017-0,019 частин, відносно на створений проміжний продукт формули 9. ефіру 2, хлориду кальцію і кип’ятять в метанолі до розчину, додають 2,5 частини, відносно метанолу, безводного бензолу і упарюють при атмосферному тиску на % попереднього об'єму. Закінчення реакції контролюють тонкошаровою хроматографією. До залишку додають хлороформ, вільний від гідрохлориду, розчин фільтрують і упарюють на 3/4 попереднього об'єму. Додають метанол до розчину, після кристалізації при 20-23°С осад відфільтровують, промивають метанолом і ефіром, висушують при 20-23°С і 60-63°С. R означає метил СН3, етил СН2СН3, феніл Суттєва особливість заявленої корисної модеС6Н5, (пара-бром)феніл п-ВrС6H4, (ортолі заключається в тому, що в описуваних умовах бром)феніл о-ВrС6Н4, (пара-хлор)феніл п-СlС6Н4, взаємодія ефірів формули 2 (схема 3) з альдегі(орто-хлор)феніл о-СlС6Н4, (мета-хлор)феніл мдами формули 3 протікає по обом, первинній і СlС6Н4, (пара-метоксі)феніл п-ОСН3С6Н4, (3,4,5вторинній аміногрупам ефіру формули 2 з утвотриметоксі)феніл 3,4,5-ОСН3С6Н2, морфоліномеренням хіназолінового циклу і рівновага реакції тилен CH2N(CH2)4O, морфоліноетилен зсунута в бік утворення ефіру 2,4,6-заміщеного CH2CH2N(CH2)4O; R1 - метил, етил; R2 - феніл хіназолініл(1,2-дигідро-4Н)-оцтової-3 кислоти фоС6Н5, (орто-хлор)феніл о-СlС6Н4; R3 - бром, хлор рмули 1. або метил. Пояснення корисної моделі отримання з обСхема 2 ґрунтуванням граничних значень режима і параВ основу корисної моделі поставлено задачу метрів процесу: розробки корисної моделі отримання ефірів 2,4,6Ефіри формули 2 (сx.3) і альдегіди формули 3 заміщених хіназолініл(1,2-дигідро-4Н)оцтової-3 використовують в співвідношенні 1:1. Надлишок кислоти з використанням ефірів Н-(2любого реагента затрудняє очистку цільових проамінобензгідрил)гліцина як вихідних продуктів. дуктів 1, Досягаємий технічний результат - це синтез ефірів 2,4,6-заміщених хіназолініл-(1,2-дигідро4Н)оцтової-3 кислоти шляхом взаємодії ефірів N(2-амінобензгідрил)гліцину з альдегідами при нагріванні в органічних розчинниках в присутності хлориду кальцію. 5 12331 6 де R, R1, R2 і R3 указані вище. 175-176°С (метанол-хлороформ 1:1). Знайдено, %: Схема 3 С 58.54; Н 4.25; N 5.98. С23Н20ВrClN2O2. РозрахоПри взаємодії реагентів 2 і 3 хлорид кальцію вано, %: С 58.56; Н 4.27; N 5.94. каталізує внутрішньо-молекулярну дегідратацію і EE xiнaзoлiнiл[1,2-дiгiдpo-2-(41-xлop)фeнiл-4Hутворюються цільові продукти 1. Кількість хлорида 4-фeнiл-6-бpoм]oцтoвoї-3 кислоти із ЕЕ БІТ (5кальцію 0,017-0,019 частин, відносно ефіру 2, опбром) і пара-хлорбензальдегіда. Вихід 82%. Т.пл. тимальна. Використання, наприклад 0,015 частин 159-160 С (метанол). Знайдено, %: С 59.31; Н збільшує час утворення продукту 1, а 0,021 частин 4.58; N 5.79. С24Н22ВrСlN2O2. Розраховано, %: С зменшує вихід внаслідок збільшення кількості ме59.34; Н 4.56; N 5.77. танолу при їх виділенні. Реакція взаємодії реагенME хіназолініл[1,2-дигідро-2-(21-хлор)фенілтів 2 і 3 рівноважна, для зсуву рівноваги вправо 4Н-4-феніл-6-бром]оцтової-3 кислоти із ME БГГ (5приміняють азеотропну відгонку води з бензолом бром) і орто-хлорбензальдегіда. Вихід 92%. Т.пл. із реакційної суміші. Для відділення механічних 209-210°С (метанол-хлороформ 1:2). Знайдено, %: домішок залишок розчиняють в хлороформі і фільС 58.53; Н 4.24; N 5.98. С23H20BrClN2O2. Розрахотрують. Якщо в хлороформі міститься гідрохлорид, вано, %: С 58.56; Н 4.27; N 5.94. то із цільових 1 утворюються побічні продукти, які ЕЕ xiнaзoлiнiл [1,2-дiгiдpo-2-(21-xлop)фeнiл-4Hзатрудняють їх очистку. Цільові 1 добре розчинні в 4-фeнiл-6-бpoм]oцтoвoї-3 кислоти із ЕЕ БГГ (5хлороформі, тому розчин частково упарюють і добром) і орто-хлорбензальдегіда. Вихід 76%. Т.пл. дають метанол для оптимальної кристалізації. Для 147-148°С (метанол-хлороформ 2:1). Знайдено, %: запобігу спікання продукту 1 при 60-63°С його поС 59.38; Н 4.53; N 5.74. C24H22BrClN2O2. Розрахопередньо висушують при 20-23°С. вано, %: С 59.34; Н 4.56; N 5.77. Приклад ME xiнaзoлiнiл[1,2-дiгiдpo-2-(41-фтop)фeнiлМетиловий ефір хіназолініл[1,2-дигідро-2(31,414H-4-фeнiл-6-бpoм]oцтoвoї-3 кислоти із ME БГГ (5діметокси)феніл-4Н-феніл-6-бром]оцтової-3 кисбром) і пара-фторбензальдегіда. Вихід 89%. Т.пл. лоти. 189-190°С (метанол-хлороформ 1:1). Знайдено, %: До суміші 3,49г (0,01моль) метилового ефіру С 60.65; Н 4.46; N 6.18. С23Н20ВrClN2O2. РозрахоN-(2-аміно-5-бромбензгідрил)гліцину і 1,66г вано, %: С 60.67; Н 4.43; N 6.15. (0,01моль) 3,4-діметоксибензальдегіда додають ЕЕ xiнaзoлiнiл[1,2-дiгідро-2-(41-фтop)фeнiл-4H60мг (0,017 частин, відносно вихідного ефіру) хло4-фeнiл-6-бpoм]oцтoвoї-3 кислоти із ЕЕ БГГ (5риду кальцію в 20мл метанолу і кип’ятять до розбром) і пара-фторбензальдегіда. Вихід 76%. Т.пл. чину 10-15 хвилин. Додають 50мл (2,5 частини, 149-150°С (метанол-хлороформ 3:1). Знайдено, %: відносно метанолу) безводного бензолу, упарюють С 61.44; Н 4.69; N 5.98. C24H22BrFN2O2. Розраховакип’ятінням при атмосферному тиску до 18-20мл і но, %: С 61.42; Н 4.72; N 5.97. закінчення реакції контролюють тонкошаровою ME xiнaзoлiніл[1,2-дiгiдpo-2-(21-фтop)фeнiлхроматографією. До залишку додають 18-20мл 4H-4-фeнiл-6-бpoм]oцтoвoї-3 кислоти із ME БГГ(5хлороформу, вільного від гідрохлориду, нагрівабром) і орто-фторбензальдегіда. Вихід 78%. Т.пл. ють до кипіння і фільтрують через паперовий 169-170 С (метанол-хлороформ 2:1). Знайдено, %: фільтр. Розчин упарюють до 10-12мл, до залишку С 60.63; Н 4.45; N 6.16. C23H20BrFN2O2. Розраховадодають 15-20мл метанолу і нагрівають до кипінно, %: С 60.67; Н 4.43; N 6.15. ПМР-спектр ( , м. ня. Після кристалізації при 20-23°С осад відфільтд.): 6,78-7.64 (12 Н, феніл); 5.04-5.25 (2Н, СН); 6.55 ровують, його промивають 8-10мл метанолу, 5(1Н, NH); 3.50 (3Н, ОСН3); 3.04-3.31 (2Н, СН2). 6мл діетилового ефіру, висушують при 20-23°С і (ДМСО-d6-ССІ4). 60-63°С і отримують 3,8г (78%) цільового продукту. ЕЕ xiнaзoлiнiл[1,2-дiгiдpo-2-(21-фтop)фeнiл-4HТ.пл. 148-149°С. Знайдено, %: С 60.34; Н 5.03; N 4-фeнiл-6-бpoм]oцтoвoї-3 кислоти із ЕЕ БГГ (55.68. C25H25BrN2O4. Розраховано, %: С 60.37; Н бром) і орто-фторбензальдегіда. Вихід 79%. Т.пл. 164-165 °С (метанол-хлороформ 2:1). Знайдено, 5.07; N 5.63. ПМР-спектр ( , м.д.): 6,45-7,45 (11Н, %: С 61.44; Н 4.70; N 5.98. C24H22BrFN202. Розфенил); 5,01-5,23 (2Н, СН); 6,81 (1Н, NH); 3,55-3,79 раховано, %: С 61.42; Н 4.72; N 5.97. (9Н, ОСН3); 3,05-3,40 (2Н, СН2). (ДМСО-d6-ССl4). ME хіназолініл[1,2-дiгідро-2-(41-окси)феніл-4НВ аналогічних умовах отримують: 4-феніл-6-бром]оцтової-3 кислоти із ME БГГ (5Метиловий ефір (ME) хіназолініл[1,2-дигідро-2бром) і пара-оксибензальдегіду. Вихід 86%. Т.пл. (41-бром)феніл-4Н-4-феніл-6-бром]-оцтової-3 кис211-212°С (метанол). Знайдено, %: С 60.91; Н лоти із ME 2-аміно-5-бромбензгідрилгліцина (БГГ) і 4.64; N 6.21. C23H21BrN2O3. Розраховано, %: С пара-бромбензальдегіда. Вихід 91%. Т.пл. 17960.94; Н 4.67; N 6.18. 180°С (метанол-хлороформ 1:1). Знайдено, %: С ЕЕ хіназолініл[1,2-дiгідро-2-(41-окси)феніл-4Н53.49; Н 3.88; N 5.46. С23Н20Вr2N2O2. Розраховано, 4-феніл-6-бром]оцтової-3 кислоти із ЕЕ БГГ (5%: С 53.51; Н 3.91; N 5.43. бром) і пара-оксибензальдегіду. Вихід 89%. Т.пл. Етиловий ефір (ЕЕ) хіназолініл[1,2-дигідро-2185-186°С (етанол-ефір 1:3). Знайдено, %: С (41-бром)феніл-4Н-4-феніл-6-бром]-оцтової-3 кис61.66; Н 4.98; N 5.96. С24Н23ВrN2O3. Розраховано, лоти із ЕЕ 2-аміно-5-бромбензгідрилгліцина (БГГ) і %: С 61.68; Н 4.96; N 5.99. пара-бромбензальдегіда. Вихід 84%. Т.пл. 1681 ME хіназолініл[1,2-дiгідро-2-(2 -окси)феніл-4Н169 С (метанол-хлороформ 2:1). Знайдено, %: С 4-феніл-6-бром]оцтової-3 кислоти із ME БГГ (554.39; Н 4.16; N 5.31. C24H22Br2N2O2. Розраховано, бром) і саліцилового альдегіду. Вихід 84%. Т.пл. %: С 54.36; Н 4.18; N 5.28. 159-160°С (метанол-ефір 2:1). Знайдено, %: С ME xiнaзoлiнiл[1,2-дiгiдpo-2-(41-xлop)фeнiл-4H60.98; Н 4.64; N 6.21. С23Н21ВrN2O3. Розраховано, 4-фeнiл-6-бpoм]oцтoвoї-3 кислоти із ME БГГ (5%: С 60.94; Н 4.67; N 6.18. ПМР-спектр ( , м. д.): бром) і пара-хлорбензальдегіда. Вихід 88%. Т.пл. 7 12331 8 9.38 (1Н, ОН); 6,71-7,43 (12Н, феніл); 6.45-6.49 N 8.78. С25Н26ВrN3O2. Розраховано, %: С 62.50; Н (1Н, NH); 5.15-5.46 (2Н, СН); 3.58-3.64 (ЗН, ОСН3); 5.46; N 8.75. 3.12-3.38 (2Н, CH2). (ДМСО-d6). ЕЕ xiнaзoлiнiл[1,2-дiгiдpo-2-(411 ЕЕ хіназолініл[1,2-дiгідро-2-(2 -окси)феніл-4Ндiмeтилaмiнo)фeнiл-4H-4-фeнiл-6-бpoм]oцтoвoї-3 4-феніл-6-бром]оцтової-3 кислоти із ЕЕ БГГ (5кислоти із ЕЕ БГГ (5-бром) і парабром) і саліцилового альдегіду. Вихід 78%. Т.пл. діметиламінобензальдегіду. Вихід 56%. Т.пл. 99100°С (етилацетат-ефір-гексан 1:3:1). Знайдено, 129-130 С (метанол-ефір 3:1). Знайдено, %: С %: С 63.19; Н 5.74; N 8.53. С26Н28ВrN3O2. Розрахо61.65; Н 4.98; N 5.96. С24Н23ВrN2Oз. Розраховано, вано, %: С 63.16; Н 5.71; N 8.50. %: С 61.68; Н 4.96; N 5.99. ME xiнaзoлiнiл[1,2-дiгідpo-2-(41ME xiнaзoлiнiл[1,2-дiгiдpo-2-(41-мeтoкcи)фeнiлдieтилaмінo)фeнiл-4H-4-фeнiл-6-бpoм]oцтoвoї-3 4H-4-фeнiл-6-бpoм]oцтoвoї-3 кислоти із ME БГГ (5кислоти із ME БГГ (5-бром) і парабром) і анісового альдегіду. Вихід 88%. Т.пл. 174діетиламінобензальдегіду. Вихід 68%. Т.пл. 154175°С (метанол-хлороформ 3:1). Знайдено, %: С 155°С (метанол-хлороформ-ефір 3:1:1). Знайдено, 61.65; Н 4.98; N 5.66. С24Н23ВrN2O3. Розраховано, %: С 63.81; Н 5.98; N 8.29. С27Н30ВrN3O2. Розрахо%: С 61.68; Н 4.96; N 5..99. ПМР-спектр ( , м. д.): вано, %: С 63.78; Н 5.95; N 8.26. ПМР-спектр ( , м. 6.81-7.53 (12Н, феніл); 6.45(1Н, NH); 4.95-5.42 (2Н, д.): 6.58-7.41 (12Н, феніл); 6.51 (1Н, СН); 4.81-5.20 СН); 3.45-3.81 (6Н, ОСН3); 3.02-3.21 (2Н, СН2). (2Н, СН); 3.45-3.55 (ЗН, ОСН3); 2.91-3.45 (6Н, СН2); (ДМСО-d6). 1.10 (6Н, СН3); (ДМСО-d6-ССl4). ЕЕ xiнaзoлiнiл[1,2-дiгiдpo-2-(41-мeтoкcи)фeнiлME xiнaзoлiнiл[1,2-дiгiдpo-2-(41-нiтpo)фeнiл4H-4-фeнiл-6-бpoм]oцтoвoї-3 кислоти із ЕЕ БГГ (54H-4-фeнiл-6-бpoм]oцтoвoї-3 кислоти із ME БГГ (5бром) і анісового альдегіду. Вихід 82%. Т.пл. 153бром) і пара-нітробензальдегіда. Вихід 84%. Т.пл. 153°С (етилацетат-метанол 1:4). Знайдено, %: С 202-203°С (метанол-хлороформ 2:1). Знайдено, %: 62.41; Н 5.21; N 5.86. С25Н25ВrN2O3. Розраховано, С 57.31; Н 4.16; N 8.74. С23Н20ВrN3O4. Розрахова%: С 62.38; Н 5.23; N 5.82. но, %: С 57.27; Н 4.18; N 8.71. ME xiнaзoлiнiл[1,2-дiгiдpo-2-(21-мeтoкcи)фeнiлME xiнaзoлiнiл[1,2-дiгiдpo-2-(31-нiтpo)фeнiл4H-4-фeнiл-6-бpoм]oцтoвoї-3 кислоти із ME БГГ (54H-4-фeнiл-6-бpoм]oцтoвoї-3 кислоти із ME БГГ (5бром) і орто-метоксибензальдегіду. Вихід 89%. бром) і мета-нітробензальдегіду. Вихід 82%. Т.пл. Т.пл. 173-174 С (метанол-хлороформ 1:1). Знай206-207°С (метанол-хлороформ 2:1). Знайдено, %: дено, %: С 61.63; Н 4.99; N 6.01. C24H23BrN2O3. С 57.31; Н 4.22; N 8.74. С23Н20ВrN3O4. РозраховаPoзpaxoвaно, %: С 61.68; Н 4.96; N 5.99. ПМРно, %: С 57.27; Н 4.18; N 8.71. спектр ( , м. д.): 6.71-7.78 (12Н, феніл); 6.16-6.44 ME xiнaзoлiнiл[1,2-дiгiдpo-2-(21-oкcи-31-нітро(1H.NH) 4.98-5.25 (2Н, СН); 3.48-3.59 (6Н, ОСН3); 1 5 -мeтoкcи)фeніл-4Н-4-фeніл-6-бром]оцтової-3 3.06-3..36 (2Н, СН2). (ДМСО-d6). кислоти із ME БГГ (5-бром) і 2-окси-3-нітро-5ЕЕ xiнaзoлiнiл[1,2-дiгiдpo-2-(21-мeтoкcи)фeнiлметоксибензальдегіда. Вихід 78%. Т.пл. 138-139 С 4H-4-фeнiл-6-бpoм]oцтoвoї-3 кислоти із ЕЕ БГГ (5(метанол-ефір 2:1). Знайдено, %: С 54.59; Н 4.23; бром) і орто-метоксибензальдегіду. Вихід 81%. N 7.98. C24H22BrN3О6. Розраховано, %: С 54.56; Н Т.пл. 153-154°С (метанол-хлороформ 3:1). Знай4.20; N 7.95. ПМР-спектр ( , м. д.): 10.51 (1Н, ОН); дено, %: С 62.35; Н 5.26; N 5.86. С25Н25ВrN2O3. 6.70-7.41 (ЮН, феніл); 6.61 (1Н, NH); 5.15-5.21 (2Н, Розраховано, %: С 62.38; Н 5.23; N 5.82. СН); 3.60-3.85 (6Н, ОСН3); 3.11-3.32 (2H, CH2). ME хіназолініл[1,2-дигідро-2-(21,41(ДМСО-d6-ССl4). діметокси)феніл-4Н-4-феніл-6-бром]оцтової-3 кисМЕ xiнaзoлiнiл[1,2-дiгiдpo-2-(21,41,51лоти із ME БГГ (5-бром) і 2,4триметокси)феніл-4Н-4-феніл-6-бром]-оцтової-3 діметоксибензальдегіда. Вихід 73%. Т.пл. 152кислоти із ME БГГ (5-бром) і 3,4,5153°С (метанол-хлороформ 3:1). Знайдено, %: С триметоксибензальдегіда. Вихід 86%. Т.пл. 14960.39; Н 5.10; N 5.66. С25Н25ВrN2O4. Розраховано, 150°С (метанол-хлороформ 4:1). Знайдено, %: С %: С 60.37; Н 5.07; N 5.63. ПМР-спектр ( , м. д.): 59.26; Н 5.19; N 5.33. C26H27BrN2O5. Розраховано, 6.31-7.45 (11Н, феніл); 5.82 (1Н, NH); 5.01-5.22 %: С 59.21; Н 5.16; N 5.31. ПМР-спектр ( , м. д.): (2Н, СН); 3.51-3.79 (9Н, ОСН3); 3.01-3.41 (2Н, СН2). 6.65-7.44 (10Н, феніл); 6.45 (1Н, NH); 4.82-5.32 (ДМСО-d6-ССl4). (2H, CH); 3.61-3.84 (12Н, ОСН3); 3.22-3.28 (2H, ЕЕ xiнaзoлiнiл[1,2-дiгiдpo-2-(21,41СН2); (ДМСО-d6). дiмeтoкcи)фeнiл-4H-4-фeнiл-6-бpoм]oцтoвoї-3 кисME хіназолініл[1,2-дигідро-2-(31,41,51лоти із ЕЕ БГГ (5-бром) і 2,4триметокси)феніл-4Н-4-(21-хлор)феніл-6діметоксибензальдегіда. Вихід 79%. Т.пл. 143бром]оцтової-3 кислоти із ME БГГ (5-бром-21-хлор) 144°С (етилацетат-метанол 1:4). Знайдено, %: С і 3,4,5-триметоксибензальдегіда. Вихід 81%. Т.пл. 61.10; Н 5.34; N5.51. С26Н27ВrN2O4. Розраховано, 169-170°С (метанол-хлороформ 4:1). Знайдено, %: %: С 61.06; Н 5.32; N 5.48. ПМР-спектр ( , м. д.): С 55.61; Н 4.63; N 5.01. C26H26BrClN2O5. Розрахо6.35-7.45 (11Н, феніл); 5.96 (1Н, NH); 4.88-5.19 вано, %: С 55.58; Н 4.66; N 4.99. ПМР-спектр ( , м. (2Н, СН); 4.05(2Н, ОСН2); 3.51-3.86 (6Н, ОСН3); д.): 6.60-7.45 (9Н, феніл); 6.25 (1Н, NH); 5.01-5.78 3.01-3.45 (2Н, CH2); 1.21 (3Н, СН3); (ДМСО-d6(2H, CH); 3.55-3.82(12Н, ОСН3); 2.81-3.24 (2H, ССl4). СН2). (ДМСО-d6). МЕ хіназолініл[1,2-дигідро-2-(41ME хіназолініл[1,2-(21,41,51-триметокси)фенілдіметиламіно)феніл-4Н-4-феніл-6-бром]оцтової-З 4Н-4-феніл-6-метил]-оцтової-3 кислоти із ME БГГ кислоти із ME БГГ (5-бром) і пара(5-метил) і 3,4,5-триметоксибензальдегіда. Вихід діметилбензальдегіду. Вихід 83%. Т.пл. 174-175°С (метанол-ефір 4:1). Знайдено, %: С 62.54; Н 5.49; 83%. Т.пл. 136-137 С (метанол-хлороформ 6:1). 9 12331 10 Знайдено, %: С 70.13; Н 6.58; N 6.10. С27Н30N2O5. NH); 4.81-5.31 (2H, CH); 3.48-3.85 (12Н, ОСН3); Розраховано, %: С 70.11; Н 6.54; N 6.06. ПМР3.01-3.32 (2H, СН2); 2.01-2.24 (3Н, СН3). (ДМСОd6). спектр ( , м. д.): 6.71-7.52 (10Н, феніл); 6.24 (1Н, Комп’ютерна верстка А. Рябко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюA method for obtaining ethers of 2,4,6-substituted quinazolinyl (1,2-dihydro-4h)-acetic -3 acid
Автори англійськоюRudenko Oleh Pavlovych
Назва патенту російськоюСпособ получения эфиров 2,4,6-замещенных хиназолинил(1,2-дигидро-4н)-уксусной-3 кислоты
Автори російськоюРуденко Олег Павлович
МПК / Мітки
МПК: C07D 239/72, C07D 239/74
Мітки: спосіб, хіназолініл(1,2-дигідро-4н)-оцтової-3, отримання, ефірів, кислоти, 2,4,6-заміщених
Код посилання
<a href="https://ua.patents.su/5-12331-sposib-otrimannya-efiriv-246-zamishhenikh-khinazolinil12-digidro-4n-octovo-3-kisloti.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання ефірів 2,4,6-заміщених хіназолініл(1,2-дигідро-4н)-оцтової-3 кислоти</a>
Попередній патент: Ручна косарка
Наступний патент: Ламель для вертикальних жалюзі
Випадковий патент: Установка для дослідження кута повороту пружини при розтягуванні









