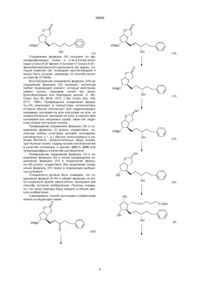
Спосіб отримання складних ефірів 13,14-дигідро-15-(r)-17-феніл-18,19,20-тринор-pgf2a
Номер патенту: 39864
Опубліковано: 16.07.2001
Автори: КОВАЧ Габорне, ДАЛМАДІ Гьюла, БАХРАМ Гезул, ІВАНІЧ Жозефне, ГЕРМЕШ Іштван, ШАБО Тібор
Формула / Реферат
1. Способ получения сложных эфиров 13,14-дигидро-15-(R)-17-фенил-18, 19, 20-тринор-PGF2a формулы (I)
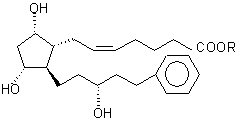 , (I)
, (I)
где R - это насыщенный или ненасыщенный прямой, разветвленный или циклический С1-7-алкил, фенильная или бензильная группа, включающий этерификацию, отличающийся тем, что сначала проводят избирательное восстановление соединения формулы (VII)
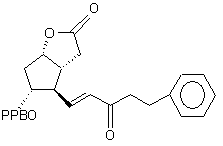 , (VII)
, (VII)
где РРВ означает 4'-фенилбензоил, посредством восстановления оксогруппы с помощью три(втор-бутил) боргидрида лития или боргидрида натрия на боковой цепи соединения формулы (VII) для получения смеси, из которой далее выделяют посредством хроматографии соединение формулы (VI)
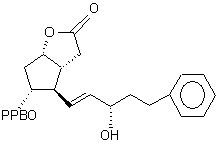 , (VI)
, (VI)
затем проводят гидрогенизацию полученного соединения формулы (VI) в присутствии катализатора и основания или натриевой соли для получения соединения формулы (V)
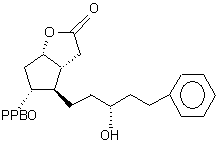 , (V)
, (V)
после чего проводят восстановление соединения формулы (V) с помощью гидрида диизобутилалюминия для получения соединения формулы (IV)
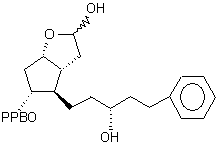 , (IV)
, (IV)
далее из соединения формулы (IV) удаляют защитную группу 4'-фенил-бензоила с помощью смеси карбоната калия и метанола для получения соединения формулы (III)
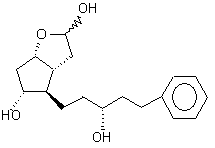 , (III)
, (III)
затем проводят реакцию соединения формулы (III) с бромидом 4-карбоксибутил-трифенил-фосфония в присутствии трет-бутоксида калия в растворителе типа эфира для получения соединения формулы (II)
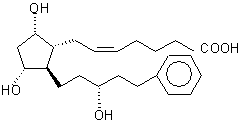 , (II)
, (II)
и этерификацию соединения формулы (II) с соединением формулы R-X, где Х означает галоген, сульфат, мезил или тозил, в присутствии карбоната калия в органическом растворителе для получения соединения формулы (I).
2. Способ по п. 1, отличающийся тем, что гидрогенизацию соединения формулы (VI) проводят в присутствии катализатора палладия на углероде.
3. Способ по п. 1, отличающийся тем, что гидрогенизацию соединения формулы (VI) проводят в присутствии солей натрия.
4. Способ по п. 1, отличающийся тем, что проводят этерификацию соединения формулы (II) с изопропилйодидом в присутствии карбоната калия в органическом растворителе.
5. Способ по п. 1, отличающийся тем, что он включает выделение соединений формулы (VI), (V) и (III) в процессе синтеза, начиная с соединения формулы (VII), и, при необходимости, очистку их путем рекристаллизации.
6.3,За,4,5,6,6а-гексагидро-2,5-дигидрокси-4-[5'-фенил-3'(К)-гидрокси-1'-пентил]-2Н-циклопента[b]фуран формулы (III):
 , (III)
, (III)
как промежуточное соединение для получения сложных эфиров.
7. 3,За,4,5,6,6а-гексагидро-2,5-гидрокси-4-[5'-фенил-3'(К)-гидрокси-1'-пентил]-5-(4-фенилбензолокси-2Н-циклопента[b]фуран формулы (IV):
 , (IV):
, (IV):
как промежуточное соединение для получения сложных эфиров.
8. 3,За,4,5,6,6а-гексагидро-2-оксо-4-[5'-фенил-3'(R)-гидрокси-1'-пентил]-5-(4-фенилбензолокси-2Н-циклопента[b]фуран формулы (V):
 , (V)
, (V)
как промежуточное соединение для получения сложных эфиров.
Текст
1. Способ получения сложных эфиров 13,14дигидро-15-(R)-17-фенил-18,19,20-тринор-PGF2α формулы (I) OH 39864 OH 6. 3,3а,4,5,6,6а-гексагидро-2,5-дигидрокси-4-[5'-фенил-3'(R)-гидрокси-1'-пентил]-2Н-циклопента[b]фуран формулы (III): OH O (III) O HO (III) OH , затем проводят реакцию соединения формулы (III) с бромидом 4-карбоксибутил-трифенилфосфония в присутствии трет-бутоксида калия в растворителе типа эфира для получения соединения формулы (II) HO OH , как промежуточное соединение для получения сложных эфиров. 7. 3,3а,4,5,6,6а-гексагидро-2,5-гидрокси-4-[5'-фенил-3'(R)-гидрокси-1'-пентил]-5-(4-фенилбензолокси -2Н-циклопента[b]фуран формулы (IV): OH OH COOH (II) O HO (IV) OH , и этерификацию соединения формулы (II) с соединением формулы R-X, где Х означает галоген, сульфат, мезил или тозил, в присутствии карбоната калия в органическом растворителе для получения соединения формулы (I). 2. Способ по п. 1, отличающийся тем, что гидрогенизацию соединения формулы (VI) проводят в присутствии катализатора палладия на углероде. 3. Способ по п. 1, отличающийся тем, что гидрогенизацию соединения формулы (VI) проводят в присутствии солей натрия. 4. Способ по п. 1, отличающийся тем, что проводят этерификацию соединения формулы (II) с изопропилйодидом в присутствии карбоната калия в органическом растворителе. 5. Способ по п. 1, отличающийся тем, что он включает выделение соединений формулы (VI), (V) и (III) в процессе синтеза, начиная с соединения формулы (VII), и, при необходимости, очистку их п утем рекристаллизации. PPBO OH , как промежуточное соединение для получения сложных эфиров. 8. 3,3а,4,5,6,6а-гексагидро-2-оксо-4-[5'-фенил3'(R)-гидрокси-1'-пентил]-5-(4-фенилбензолокси2Н-циклопента[b]фуран формулы (V): O O (V) PPBO OH , как промежуточное соединение для получения сложных эфиров. Изобретение относится к лекарственным препаратам для терапевтических целей, в частности, к лекарственным препаратам, содержащим органические активные ингредиенты, а именно – простагландины, и может быть использовано для лечения глаукомы. Известно, что многие производные простагландинов способны снижать внутриглазное давление при местном или топическом применении, т. е. и х можно применять для лечения глаукомы (опубл. Европейские патентные заявки № 0170258 и 0253094). Известен способ получения производных простагландинов, обладающих наиболее благоприятным воздействием (опубл. РСТ патентная заявка WO 90/02553, А61К31/557, 1990). Однако этот способ недостаточно эффективный, т. к. выход полученных сложных эфиров невысокий, количество - невелико, а степенью чистоты - недостаточна. В основу изобретения поставлена задача создания способа получения сложных эфиров 13,14дигидро-15-(R)-17-фенил-18,19,20-тринор-PGF2α формулы (I) с высоким выходом, в больших количествах и с н ужной степенью чистоты. Поставленная задача решается тем, что в способе получения сложных эфиров 13,14дигидро-15-(R)-17-фенил-18,19,20-тринор-PGF2α формулы (I) OH COOR HO OH , (I) где R - это насыщенный или ненасыщенный прямой, разветвленный или циклический С 1-7-алкил, фенильная или бензильная группа, включающем этерификацию; согласна изобретению сначала 2 39864 проводят избирательное восстановление соединения формулы (VII) O в присутствии трет-бутоксида калия в растворителе типа эфира для получения соединений формулы (II) OH O COOH HO PPBO OH O , (II) и этерификацию соединения формулы (II) с соединением формулы R-X, где X означает галоген, сульфат, мезил или тозил, в присутствии карбоната калия в органическом растворителе для получения соединения формулы (I). В данном способе гидрогенизацию соединения фopмулы (VI) можно проводить и присутствии катализатора палладия на углероде или в присутствии солей натрия. Согласно заявленному способу проводят этерификацию соединения формулы (II) с йодидом изопропила в присутствии карбоната калия в органическом растворителе. Способ может включать выделение соединений формулы (VI), (V) и (III) в процессе синтеза, начиная с соединения формулы (VII), и, при необходимости, очистку и х путем рекристаллизации. В основу данного изобретения поставлена также задача создания промежуточных соединений для осуществления данного способа получения сложных эфиров: 3,3а,4,5,6,6а-гексагидро-2,5-дигидрокси-4-[5'фенил-3'(R)-гидрокси-1'-пентил]-2Н-циклопента [b] фуран формулы (III) OH , (VII) где РРВ означает 4'-фенилбензойл, посредством восстановления оксо группы с помощью три(секбутил) боргидрида лития или боргидрида натрия на боковой цепи соединения формулы (VII) для получения смеси, из которой, далее выделяют посредством хроматографии соединение формулы (VI) O O PPBO OH , (VI) затем проводят гидрогенизацию полученного соединения формулы (VI) в присутствии катализатора и основания или натриевой соли для получения соединения формулы (V) O O O PPBO OH , (V) после чего проводят восстановление соединения формулы (V) с помощью гидрида диизобутилалюминия дли получения соединения формулы (IV) OH HO OH , (III) 3,3а,4,5,6,6а-гексагидро-2,5-гидрокси-4-[5'-фенил-3'(R)-гидрокси-1'-пентил]-5-(4-фенилбензолокси-2Н-циклопента [b] фуран формулы (IV) OH O O PPBO OH , (IV) далее из соединения формулы (IV) удаляют группу защиты 4'-фенил-бензойла с помощью смеси карбоната калия и метанола для получения соединения формулы (III) OH PPBO OH , (IV) 3,3а,4,5,6,6а-гексагидро-2-оксо-4-[5'-фенил-3' (R)-гидрокси-1'-пентил]-5-(4-фенилбензолокси-2Нциклопента [b] фуран формулы (V) O HO OH , (III) затем проводят реакцию соединения формулы (ІІІ) с бромидом 4-карбоксибутил-трифенил-фосфония 3 39864 O O O O PPBO PPBO OH , (V) Соединение формулы (IIІ) получают из фенилфосфониевых солей и 3,3а,4,5,6,6а-гексагидро-2-оксо-4-(5'-фенил-3-оксопент-1'-енил)-5-(4'фенилбензойлокси)-2Н-циклопента [b] фуран, который известен как посредник простагландина и может быть получен, например, по способу патента США № 3778450. Восстановление соединения формулы (VII) до соединения формулы (VI) проводят, используя любой подходящий реагент, который восстанавливает еноны, например литий три (вторбутил)боргидрид или боргидрид натрия (J. Am. Chem. Soc. 94, 8616, 1972; J. Am. Chem. Soc. 106, 6717, 1984). Превращение соединения формулы (VI) реализуют в присутствии катализатора, который обычно используют для гидрогенизации, например, палладия на угле или родия на угле, но предпочтительно палладия на угле, в присутствии основания или натриевых солей, таких как гидроксид натрия или нитрит натрия. Превращение соединения формулы (III) в соединение формулы (I) можно осуществить, используя любое сочетание условий (основание, растворитель и т. д.) обычно используемых в реакции Виттинга, предпочтительно амид натрия, трет-бутилат калия, гидрид натрия или бутиллитий в качестве основания, а диглим, ДМСО, ДМФ или тетрагидрофуран в качестве растворителя. Превращение соединения формулы (V) в соединение формулы (IV) и затем превращение соединения формулы (IV) в соединение формулы (III) можно осуществить без выделения соединения формулы (IV) также в подходящих выбранных условиях. Специалисту должно быть очевидно, что соединения формул (II-VII) и общей формулы (I) могут содержать другие заместители, пригодные для способа согласно изобретению. Поэтому очевидно, что такие реакции будут входить в объем данного изобретения. Суммировать способ настоящего изобретения можно в следующей схеме. O OH (VI) O O PPBO OH (V) OH (IV) OH O PPBO OH O OH OH (III) OH C OOH O OH OH PPBO O (VII) 4 (II) 39864 OH Пример 2 Получение 3,3а,4,5,6,6а-гексагидро-2-оксо-4/5'-фенил-3-оксо-пент-1'-енил/-5-/4'-фенилбензилокси/-2Н-циклопента-[b]-фурана (соединение формулы (VІІ)) а) К раствору 3,3а,4,5,6,6а-гексагидр-2-оксо-4гидро-ксиметил-5-/4'-фенилбензоилокси/-2Нциклопента [a] фурана (27 кг) в 165 л толуола, охлажденному до 17°С, добавляют фосфорную кислоту в диметилсульфоксиде (ДМСО) 1 М (12 л). Температуру реакционной смеси поддерживают ниже 25°С спустя 60 минут. К реакционной смеси добавляют следующие реагенты и в следующем порядке: с 60 минутными интервалами; фосфорную кислоту в ДМСО 1М (6 л), ДСС (13,5 кг), фосфорную кислоту в ДМСО 1 М (6 л). Реакционную смесь перемешивают при 20-25°С в течение дополнительных 7 часов (контроль тонкослойная хроматография). ТCX Rf=0,32 (силикагель, АсОЕт : толуол) (силикагель, толуол-АсОЕт-АсОН 30:15:2). в) Трифенил-2-оксо-4-фепилбутилфосфоний иодид (38,4 кг), гидроксид калия (5 кг) в 105 л воды, 210 л толуола в 90 л дихлорметана интенсивно перемешивают в течение 3 часов, а затем добавляют хлорид натрия (5 кг). Органический слой выделяют и промывают рассолом (3х113 л), сушат над сульфатом натрия, концентрируют в вакууме до 70 л, этот раствор добавляют к раствору полученному описанным ранее способом в части а) этого примера с такой скоростью, чтобы температура реакционной смеси не превышала 25°С. Спустя 7 часов полученный раствор охлаждают до 18°С (ТСХ контроль). Раствор концентрированной HCI (6 л) в 45 л воды добавляют, а полученную смесь перемешивают в течение часа. Осадок удаляют фильтрованием, промывают толуолом (2х45 л+2х23 л). Органический слой промывают водой (225 л) и рассолом (4х45 л), водный раствор экстрагируют толуолом (2х23+1х130 л), органические слои собирают, и сушат над сульфатом натрия (15 кг), фильтруют, промывают толуолом (2х15 л), и выпаривают в вакууме до 85 л и добавляют метанол (240 л), охлаждают до 0°С, фильтруют, промывают смесью метанол : толуол 9:1 (49 л), и метанолом (98+60 л) до получения продукта в виде белых кристаллов. Т. плавления 129130°С (выход 19,4 кг, 52,7%). (α)D20=-116° (с=1,26, CH3CN). Пример 3 Получение 3,3а,4,5,6,6а-гексагидро-2-оксо-4/5'-фенил-3' /S/-гидроксинент-1'-енил/-5-/4'-фенилбензилокси/-2Н-циклопента [b]-фурана (соединение формулы (VІ)) Смесь, содержащую 1,04M боргидрида литийтри/втор-бутила/ (418 мл, 0,434 моля) в растворе тотрагидрофурана и сухого диэтилового эфира (420 мл) охлаждают до -130°С. Соединение формулы (VII) (200 г) растворяют в тетрагидрофуране (1000 мл) и диэтиловом эфире (900 мл), охлаждают до 130°С, и добавляют к вышеуказанному раствору боргидрида в течение 1 минуты. Спустя 5 минут реакционную смесь выливают в смесь (5,5 л) 2М раствора сульфата натрия (250 мл) и физиологического раствора (500 мл) и перемешивают при комнатной температуре в течение 15 минут. Это т раствор последовательно промы COOR OH OH (I) Далее способ настоящего изобретения иллюстрируется следующими не лимитирующими примерами. Пример 1 Получение 3,3а,4,5,6,6а-гексагидро-2-оксо-4/5'-фенил-3-оксо-пент-1'-енил/-5-/4'-фенилбензолокси/-2Н-циклопента-[b] фурана (соединение формулы (VII)) Раствор, содержащий 3,3а,4,5,6,6а-гексагидро -2-окcо-4-гидроксиметил-5-/4'-фенилбензолокси/2Н-циклопента-[b] фуран (18 г, 51 ммоль) в 110 мл сухого толуола охлаждают до 18°С, затем добавляют раствор дициклогексилкарбодиимида (18 г, 83 моля) и добавляют одномолярный раствор фосфорной кислоты (8 мл, 8 ммолей) в сухом диметилсульфоксиде. Реакционную смесь поддерживаю при температуре 25°С при непрерывном охлаждении. Спустя 30 минут добавляют следующие реагенты к реакционной смеси с интервалами 30 минут. Раствор 1М фосфорной кислоты (4 мл) и диметилсульфоксиде, дициклогексилкарбодиимид (9 г, 41 ммоль) и 1М раствор фосфорной кислоты (5 мл) в диметилсульфоксиде. Затем реакционную смесь перемешивают при 20-22°С в течение 2 часов. Тем временем трифенил-/4-фенил-3-оксобутил/-фосфонийиодид (27,3 г, 50 ммолей) и 5М раствор гидроксида кальция (10 мл) в 250 мл. толуола перемешивают при 45°С в течение 90 минут, а затем полученный раствор трижды промывают 100 мл воды (каждая порция) при температуре 45-50°С до нейтрализации, а затем 45 мл толуола удаляют из раствора при пониженном давлении. Оставшийся раствор добавляют к другой реакционной смеси с такой скоростью, чтобы его температура не превышала 30°С. Спустя 2 часа раствор нагревают до 35°С, а еще час спустя добавляют концентрированную соляную кислоту (4 мл), растворенную в 30 мл воды, а затем перемешивают еще в течение часа. Осадок удаляют фильтрованием, полученный фильтрат промывают толуолом, и, после объединения, толуольный раствор промывают водой (150 мл), 4 раза физиологическим раствором (30 мл), сушат над безводным сульфатом натрия, а затем выпаривают до 350 мл. Вышеуказанный раствор переносят в колонку с силикагелем (135 г), и элюируют толуолом, используя смесь 5:1 толуола и этилацетата. После выпаривания раствора, получают темнокоричневый твердый продукт (21 г), и его растворяют в кипящем метаноле (840 мл). После охлаждения раствора до 0°С, осадок отфильтровывают и промывают холодным метанолов (30 мл), полученный продукт сушат при комнатной температуре до получения указанного в заглавии соединения формулы (VII) в виде белого вещества с вы ходом 12,0 г (48,7%), т. плавления 129-130°С, (α)D=-145° (с=1, этилацетат). 5 39864 вают водой (2 л), этилацетатом (1 л) и дважды физиологическим раствором (порциями по 200 мл), сушат над безводным сульфатом натрия, и выпаривают при пониженном давлении. Жидкий остаток получают и переносят в колонку с силикагелем (5 кг). Затем проводят элюирование смесью 7:1 метиленхлорида и этилацетата, и перекристаллизовывают продукт, полученный из смеси этилацетата (80 мл), диизопропилового эфира (160 мл) и гексана (80 мл), получают белый кристаллический порошок указанного в заглавии соединения формулы (VI) (69,7 г). Т. плавления 129130°С, (α)D=-108°С (c=1, этилацетат). Пример 4 Получение 3,3а,4,5,6,6а-гексагидро-2-оксо-4/5'-фенил-3'-/S/-гидроксипент-1'-енил/-5-/4'-фенилбензоилокси/-2Н-циклопента [b] фурана (соединение формулы (VI)) К перемешиваемой суспензии енона формулы (VII) (19,3 кг) в 4,5 кг метанола и 200 л хлороформа, охлажденного до –3…-5°С добавляют боргидрид натрия (2,38 кг) (контроль ТСХ). Реакционную смесь выливают в воду (20 л), а затем добавляют концентрированную HCI (12,6 л). Полученную смесь сушат на силикагеле (30 кг), фильтруют, промывают хлороформом (60+30 л). Органический слой концентрируют до 60 л, и хроматографируют на двух колонках. Обе колонки заполнены силикагелем (135 кг) и толуолом (300 л). В обеих колонках в качестве элюента используют последовательно смесь толуол : АсОЕт 666 л : 133л + (250 л : 150 л) и АсОЕт 250 л. Фракцию V (410 л) концентрируют в вакууме до 35 л. К остатку добавляют диизопропиловый эфир (90 л), охлаждают до 0°С…-5°С, перемешивают в течение часа. Белый кристаллический продукт фильтруют и промывают ДІРе-АсОЕт 3:1 (16 л). Выход 7,38 кг (38%). ТСХ : Rf=0,5 (силикагель; АсОЕт) (0,36/ АсОЕт : гексан 1:1) (α)D=-101,59 (с=0,69 СН3СN). Пример 5 Получение 3,3а,4,5,6,6а-гексагидро-2-оксо-4/5'-фенил-3' /R/-гидрокси-1'-пентил/-5-/4'-фенилбензоилокси/-2Н-циклопента [b] фурана (соединение формулы (V)) К раствору, содержащему 3,3а,4,5,6,6а-гексагидро-2-оксо-4-/5'-фенил-3' /S/-гидроксинент-1'енил/-5-/4'-фенил-бензилокси/-2Н-циклопента [b]фуран (70 г, 144 ммоля) в 2 л этанола при 18-20°С, добавляют катализатор - палладий на угле (7,0 г) и нитрит натрия (3,5 г, 50 ммолей) в виде суспензии в 100 мл воды. Полученную смесь перемешивают в атмосфере водорода под давлением 5 бар в течение 90 минут, затем катализатор отфильтровывают, добавляют 1М раствор соляной кислоты (100 мл), и полученную смесь перемешивают при комнатной температуре в течение 1 часа. После удаления растворителя при пониженном давлении, полученный маслянистый остаток растворяют в этилацетате (700 мл). Водную фазу дважды экстрагируют етилацетатом (по 200 мл каждая порция), и объединенный этилацетатный раствор дважды промывают физиологическим раствором (по 100 мл порция). После сушки над безводным сульфатом натрия и выпаривания растворителя получают указанное в заглавии соединение формула (V) в виде маслянистого остатка с выходом 95% при Rf=0,23 (проявляющая сис тема гексан/этилацетат 1:1) (α)D=-66° (с=1, этилацетат). ИК спектр (получен на спектрометре Цейсс Спекорд М-80) (КВг, см -1) : 3500 (ОН), 3080, 3020, (СН ароматика), 2940, 2860 (СН алифатика), 1770, 1710, (С=0), 1610, 1500 (колебания ароматического кольца), 1290, 1190, 1100 (С-О-С), 850 (пара-замещ. ароматика), 750, 700 (монозамещенная ароматика). Пример 6 Получение 3,3а,4,5,6,6а-гексагидро-2-оксо-4/5'-фенил-3'/R/-гидрокси-1'-пентил/-5-/4'-фенилбензоилокси/-2Н-циклопента [b] фурана (соединение формулы (V)) К раствору соединения формулы (VI) (7,2 кг) в абсолютированном этаноле (200 л) при 15-20°С, и добавляют суспензию 10% Pd/С (1,4 кг) и нитрит натрия (0,72 кг) в 36 л воды. Полученный раствор перемешивают в атмосфере водорода (1200 кbL) в течение 3 часов (контроль ТСХ). Добавляют 1M раствор HCI (105 л) и перемешивают при комнатной температуре в течение 1 часа. Полученный катализатор удаляют фильтрованием, промывают абсолютированным этанолом (20 л). Растворитель удаляют в вакууме до 50 л. Полученный маслянистый остаток растворяют в толуоле (140 л), промывают рассолом 15% (3х30 л). Водную фазу промывают толуолом (20 л). Объединенные органические экстракты сушат над сульфа том натрия (10 кг) и бикарбонатом натрия (0,5 кг), соответственно, и фильтруют. Осадок промывают толуолом (30 л). Растворитель удаляют в вакууме до получения остатка (90 л), который используют непосредственно на следующей стадии. Полученный остаток содержит соединение формулы (V) (7,03 кг, 96,7%). Пример 7 Получение 3,3а,4,5,6,6а-гексагидро-2-гидрокси -4-/5'-фенил-3'/R/-гидрокси-1'-пентил/-5-/4'-фенилбензоилокси/-2Н-циклопента [b] фурана (соединение формулы (IV)) После растворения 3,3а,4,5,6,6а-гексагидро-2оксо-4-/5'-фенил-3'/R/-гидрокси-1'-пентил/-5-/4'-фенилбензоилокси/-2Н-циклопента [b]фурана (65,7 г, 135 ммоля) в сухом тетрагидрофуране (330 мл), диизобутилалюминийгидрид (150 мл, 297 ммоля) в сухом гексановом растворе (150 мл) прикапывают при температуре между -65°С и -75°С. После перемешивания реакционной смеси в течение 10 минут, полученный раствор выливают в смесь воды (1 л) и 2М раствор бисульфата натрия (500 мл), и перемешивают в течение 30 минут. Этот раствор промывают этилацетатом (1л, а затем дважды по 500 мл), а затем объединенные органические фазы дважды промывают физиологическим раствором (по 200 мл каждую). После выпаривания органической фазы при пониженном давлении получают указанное в заглавии соединение в виде бесцветного маслянистого остатка, который используют без дальнейшей очистки на следующей стадии, Rf=0,25 (бензол/этилацетат 1:1). Пример 8 Получение 3,3а,4,5,6,6а-гексагидро-2-гидрокси -4-/5'-фенил-3'/R/-гидрокси-1'-пентил/-5-/4'-фенилбензоилокси/-2Н-циклопента [b] фурана (соединение формулы (IV)) 6 39864 Раствор диизобутилалюминийгидрида (ДІВАL) (9,1 кг в сухом толуоле (31 л) добавляют к перемешиваемому раствору соединения формулы (V) (6,8 кг), в толуоле (70 л) при температуре -72…-80°С, спустя час (при контроле ТСХ) добавляют этилацетат (5 л), а затем добавляют сульфат натрий 1М (240 л). Органический слой выделяют и сушат над сульфатом натрия (9 кг), фильтруют и промывают толуолом; АсОЕт (5л:5л). Водный слой промывают АсОЕт (3х35 л). Органический слой собирают и сушат над сульфатом натрия (9 кг), фильтруют, промывают толуолом: АсОЕт 1:1 (40 л). Органические слои собирают и для стабилизации триола добавляют 100 л толуола, 0,5 л триэтиламина. Раствор триола хроматографируют на силикагеле (34 кг) заполненном толуолом (60 л), используя толуол : АсОЕт (1:1) (400 л) и АсОЕт (560 л) соответственно, в качестве элюента, собирают следующие фракции в следующем порядке: фракция I (50 л), фракции II и III (по 400 л каждая), фракция IV (230 л). Фракция II содержит много целевого продукта. Растворитель удаляют в вакууме. К остатку (20 л) добавляют диизопропиловый эфир (ДІРЕ) (65 л), охлажденный до 0°С, Образующееся твердое вещество отфильтровывают и промывают смесью ДIРЕ : АсОЕт 3:1 (2х10 л) до получения белого кристаллического продукта с выходом (2,8 кг, 63,1%). Избыток ДІВАL используют для удаления РРВ, а соединение формулы (V) восстанавливают до соединения формулы (ІV). Пример 9 Получение 3,3а,4,5,6,6а-гексагидро-2,5-дигидрокси-4-/5'-фенил-3'/R/-гидрокси-1-пентил/-2Н-циклопента [b] фурана (соединение формулы (III)) Смесь, содержащую 3,3а,4,5,6,6а-гексагидро2-гидрокси-4-/5'-фенил-3'/R/-гидрокси-1'-пентил/-5/4'-фенилбензоилокси/-2Н-циклопента [b] фурана (65,2 г, 133,4 ммоля) карбонат калия (19,0 г, 133,4 ммоля) и 330 мл метанола, перемешивают при температуре 40-45°С в течение 5 часов, затем охлаждают до 0°С и рН устанавливают 7-8, медленно добавляя раствор 1н фосфорной кислоты. После отфильтровывания остатка, полученный фильтрат дважды промывают водой (70 мл каждая порция), а затем дважды смесью 2:1 метанол (30 мл) и вода. Затем добавляют к фильтрату физиологический раствор, и экстрагируют четыре раза этилацетатом (250 мл каждая порция), объединенные органические фазы промывают физиологическим раствором, сушат и выпаривают при пониженном давлении. Полученный твердый продукт растворяют в этилацетате (100 мл) при 60°С, диизопропиловый эфир (100 мл) добавляют к раствору, охлаждают до комнатной температуры, а затем медленно добавляют гексан (200 мл). После перемешивания полученной смеси при 0°С, кристаллический осадок отфильтровывают, дважды промывают смесью 2:1 диизопропилового эфира (30 мл) и этилацетата, и сушат до получения белого кристаллического вещества, указанного в заглавии соединения (35,93 г, 87,90%) формулы (III), т. плавления: 103-106°С (α)D=-47° (с=1, этилацетат). ИК спектр (получен на спектрометре Цейсс, спекорд М-80) (Квг, см -1): 3380 (ОН), 3030 (СН ароматика), 2980, 2960, 2920, 2860 (СН али фатические), 1600, 1590, 1570, 1500 (колебания ароматического кольца), 1090 (С-О-С), 1000 (С-О(Н)), 750, 700 (монозамещенная ароматика). 1 Н-ЯМР спектр (получен на спектрометре Brukeг WP-80, СДСІ3, TМС-стандарт, δ м.д, (7,23/с, 5Н, ароматич. Н), 5,64, 5,51 (д, 1Н, 3-Н), 4,63 (м, 1Н, 1-Н) 3,90 (1Н, 7-H), 3,60 (1H, 3-H). Полученный продукт является смесью 1:1 экзо и эндо изомеров. Пример 10 Получение 13,14-дигидро-15/R/-17-фенил18,19,20-тринop-PGF2α (соединение формулы (II)) 4-Карбоксибутил-трифенилфосфонийбромид (147,2 г, 3,32 ммоля) и трет.бутоксид калия (186 г, 1,66 ммоля) добавляют к раствору 3,3а,4,5,6,6агексагидро-2,5-дигидрокси-4-/5'-фенил-3'/R/-гидрокси-1'-пентил/-2Н-циклопента [b] фурана (33,9 г, 110,7 ммоля) (соединение формулы (III)) в 500 мл тетрагидрофурана, и полученный раствор охлаждают до -25°С. Полученную смесь перемешивают вначале при -20°С, а затем при 0°С, в общем 6 часов, затем рН устанавливают 8-9, добавляя 2М водный раствор бисульфата натрия, тетрагидрофуран отгоняют при пониженном давлении. После добавления к остатку воды (200 мл), полученную смесь охлаждают до комнатной температуры, осадок отфильтровывают, дважды промывают насыщенным раствором бисульфата натрия (200 мл) каждый, а затем дважды водой (по 100 мл каждый). Объединенные водные фазы промывают дважды метиленхлоридом (150 мл каждая порция), рН устанавливают 3-4, используя раствор бисульфата натрия, и полученный раствор дважды экстрагируют этилацетатом. Объединенные этилацетатные фазы дважды промывают физиологическим раствором (100 мл каждая порция) и выпаривают. Густую жидкую суспензию встряхивают с ацетоном (100 мл) в течение 10 минут, осадок отфильтровывают, промывают 6 раз порциями по 100 мл смесью 40:25 (по объему) диизопропилового эфира и ацетона, и полученный фильтрат выпаривают при пониженном давлении до получения указанного в заглавии соединения формулы (II) в виде маслянистого остатка с выходом 85%, которое можно превратить в соединение формулы (I) без дополнительной очистки. Пример 11 Получение 13,14-дигидро-17-фенил-18,19,20тринop-1-PGF2α (соединение формулы (II) К перемешиваемой суспензии 4-карбоксибутилтрифенилфосфонийбромида (5,32 кг) в 40 мл ТГФ в атмосфере азота при 0-5°С добавляют бутоксид калия (4,49 кг), и перемешивают при комнатной температуре в течение 20 минут. К полученному красно-оранжевому раствору илида при -15…-10°С, добавляют соединение формулы (III) (1,23 кг) в 8 л ТГФ, полученную смесь перемешивают в течение 4-7 часов (при контроле ТСХ). Реакционную смесь разбавляют водой (25 л), промывают толуолом (25 л) органическую фазу выделяют. Водный слой промывают хлороформом (3х6 л), подкисляют бисульфатом натрия 2М /15 л/, экстрагируют АсОЕт (18 л и 22 х6 л) последовательно. Органический слой промывают 15% раствором хлорида натрия (2х6 л), сушат над сульфатом натрия (0,4 кг), фильтруют. Осадок 7 39864 промывают дважды АсОЕт (4 л), растворитель удаляют в вакууме, суспензию встряхивают с ДIРЕ : ацетон 2:1 (18 л) до кристаллизации побочного продукта - трифенилфосфоксида, который удаляют фильтрованием, промывают смесью ДIРЕ : ацетон (4x3 л). Органический слой концентрируют в вакууме до получения соединения формулы (II), которое используют непосредственно без выделения на следующей стадий. Пример 12 Получение 13,14-дигидро-15/R/-17-фенил18,19,20-тринop-PGF2α изопропилового эфира (соединение формулы (I) После добавления безводного карбоната калия (22,95 г) и изопропилиодида (37,55 г, 221,4 ммоля) к раствору неочищенного 13,14дигидро-15/R/-17-фенил-18,19,20-тринop-PGF2α в 200 мл сухого диметилформамида (50,64 г, 110,7 моля) полученного в примере 6, полученную смесь перемешивают при 50°С в течение 5 часов, затем реакционную смесь выливают в смесь воды (900 мл), 2М раствора бисульфата натрия (120 мл) и этилацетата (500 мл). Водную фазу экстрагируют дополнительно етилацетатом (500 мл). Объединенные этилацетатные фазы последовательно промывают дважды 2% раствором литийхлорида (по 500 мл порция), насыщенным раствором бикарбоната натрия (100 мл) и дважды физиологическим раствором (по 200 мл), сушат, а этилацетат выпаривают при пониженном давлении. Маслянистый остаток очищают на хроматографической колонке с силикагелем (1 кг), содержащей силиконовый гель, используя смесь 20:1 метиленхлорида и изопропанола в качестве элюента, а затем на силикагеле (900 г), используя смесь 1:1 этилацетата и гексана в качестве элюента до получения после упаривания указанного в заглавии соединения в виде маслянистого остатка (16 г) формулы (I), Rf=0,42 (диизопропиловый эфир/ ацетон/ вода 40:25:1), (α)D=+34° (с=1, ацетонитрил). ИК спектр получен на спектрофотометре Цейсc спекорд М-80, используя слой жидкой пленки между окошками из NаСl/ (см -1); 3400 (ОН), 3060 (СН ароматические), 2990, 2930, 2860 (СН алифатические), 1730 (С=0), 1600, 1650 (колебания ароматического кольца), 1110 (С-О-C), 750, 700 (монозамещенная ароматика). Спектр 1Н-ЯМР (получен на спектрометре фирмы Брукер АС400, СДСI3, ТМС-вн утренний стандарт, δ, мд) 7,24 (с, 5Н, ароматика), 5,44 (дд, 1H, 6-Н), 5,41 (дд, 1Н, 5-Н), 4,99 (м, 1Н, -СНизопропанол), 4,17 (с, 1Н, 9-Н), 3,94 (с, 1Н, 11-Н), 3,66 (м, 1Н, 15-Н). Пример 13 Получение 13,14-дигидро-17-фенил-18,19,20тринop-PGF2α изопропилового сложного эфира (соединение общей формулы (І), где R является изопропильной группой) К неочищенному продукту формулы (II), растворенному в ДМФ (6 л), добавляют карбонат калия (1,24 кг) и изопропилиодид (1,15 л), и полученную смесь нагревают до 45-50°С за 5-6 часов, причем за это время реакция завершается (ТСХ контроль). Полученную смесь разбавляют водой (2,8 л), подкисляют до рН 2-3 бисульфатом натрия 1М (13 л). Водным слой экстрагируют смесью АсОЕт : гексан 3:2 (3х9 л), после чего органический слой промывают водой (2х4 л) и суша т над сульфатом натрия (1,5 кг), и фильтруют. Полученный осадок промывают АсОЕт (2 х1,5 л), концентрируют в вакууме, и получают целевое соединение в виде светло-коричневого масла. Неочищенное масло (2,7 кг) обрабатывают на хроматографической колонке с силикагелем дважды. Неочищенное масло растворяют в смеси ДIР : ацетон 3:1 (6 л) и хроматографируют на силикагеле (70 кг) используя смесь ДІРЕ : ацетон 3:1 (1200 л), в качестве элюента, и собирают пять фракций в следующем порядке: I (280), II (50), III (10), ІV (270) и V (70 л) соответственно. Фракция ІV содержит основное количество продукта (контроль TCХ), который концентрируют в вакууме. Полученное масло растворяют в дихлорметане (6 л) и хроматографируют на силикагеле (20 кг), используя градиентное элюирование дихлорметаном (20 л) и смесью дихлорметан : изопропанол 40:1 (61,5 л), 30:1 (20,7 л) и 5:1 (60 л), последовательно. Собирают 5 фракций в следующем порядке: I (127 л), II (0,5 л), III (0,5 л), ІV (12 л) и V (5 л), соответственно. Чистоту фракций исследуют с помощью ТСХ и высокоэффективной жидкостной хроматографии. Обнаруживают, что фракция ІV чистая. Растворитель удаляют в вакууме, полученное желтоватое масло обрабатывают активированным углем (0,11 кг) в изопропаноле (6,2 л), фильтруют, промывают изопропанолом (2х0,56 л). Растворитель удаляют в вакууме (0,2 бар) при 4050°С до получения целевого соединения в виде чистого бесцветного до слегка желтоватого масла о выходом (0,96 кг, 55,5%). Пример 14 Получение 3,3а,4,5,6,6а-гексагидро-2-гидрокси -4-/5'-фенил-3'/R/-гидрокси-1'-пентил/-2Н-циклопента [b] фурана (соединение формулы (Ill)) Раствор, содержащий 3,3а,4,5,6,6а-гексагидро -2-оксо-4-/5'-фенил-3'/R/-гидрокси-1'-пентил/-5-/4'фенилбензоилокси-2Н-циклопента [b] фурана (6,8 г, 14 ммолей), в безводном толуоле (82 мл) охлаждают до -80°С и к этому раствору при охлаждении прикапывают раствор диизобутилалюминийгидрида (9,1 г, 64 ммоля) в безводном толуоле (31 мл). Реакционную смесь перемешивают при температуре между -70°С и -80°С до завершения реакции (около 1 часа). Затем реакционную смесь выливают в 1M раствор бисульфа та натрия (204 мл), перемешивают в течение 45 минут, и после разделения фаз оставшийся в водной фазе продукт экстрагируют етилацетатом. После объединения органические фазы сушат над безводным сульфатом натрия, и затем переносят в колонку с силикагелем (34 г) и толуолом (60 мл). Целевой продукт элюируют смесью толуола и этилацетата. Фракцию, содержащую чистый продукт, выпаривают до объема 20-25 мл, и полученный продукт кристаллизуют, используя смесь диизопропилового эфира и этилацетата до получения указанного в заглавии продукта (2,8 г) формулы (III). Т. плавления 103-106°С. 8 39864 __________________________________________________________ ДП "Український інститут промислової власності" (Укрпатент) Україна, 01133, Київ-133, бульв. Лесі Українки, 26 (044) 295-81-42, 295-61-97 __________________________________________________________ Підписано до друку ________ 2001 р. Формат 60х84 1/8. Обсяг ______ обл.-вид. арк. Тираж 50 прим. Зам._______ ____________________________________________________________ УкрІНТЕІ, 03680, Київ-39 МСП, вул. Горького, 180. (044) 268-25-22 ___________________________________________________________ 9
ДивитисяДодаткова інформація
МПК / Мітки
МПК: A61K 31/557, A61P 27/02, C07B 61/00, A61K 31/5575, C07C 405/00, C07D 307/935
Мітки: 13,14-дигідро-15-(r)-17-феніл-18,19,20-тринор-pgf2a, складних, отримання, спосіб, ефірів
Код посилання
<a href="https://ua.patents.su/9-39864-sposib-otrimannya-skladnikh-efiriv-1314-digidro-15-r-17-fenil-181920-trinor-pgf2a.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання складних ефірів 13,14-дигідро-15-(r)-17-феніл-18,19,20-тринор-pgf2a</a>
Попередній патент: Вуглецева сажа /варіанти/ та композиція, що містить вуглецеву сажу
Наступний патент: Роторний вітродвигун
Випадковий патент: Спосіб усунення вестибулярно розташованого ороантрального співустя у дистальному відділі при наявності молярів з одномоментною гайморотомією