Спосіб одержання амідінів або їх фармацевтично прийнятних солей
Формула / Реферат
(57) Способ получения амидинов общей формулы I
или их фармацевтически приемлемых солей, где NR1R2 означает морфолино, пирролидинил, пиперидино тиоморфолино, метилпиперазинил, Ν,Ν-диметил-амино или N-(метоксиэтил)-N-метиламино, R3 является алкильной группой, содержащей 1-4 углеродных атомов, когда R5 и R6 являются водородом или R3 является группой NH2, когда NR5R6 означает Ν,Ν-диметиламино Ν,Ν-ди-этиламино N-бутил-N-метиламино, N,N'-бис(метоксиэтил)амино, морфолино, пирррлидинил или пиперидино, R7 представляет собой атом водорода, метил, этил, изобутид, метокси, метилтио, метилтиометил, фтор или хлор, оτличающийся тем, что нагревают соединения формулы VII:
где NR1R2 и R7 имеют значения, указанные выше с соединением формулы: R'CN, где R1 является группой R3, когда R5 и R6 являются водородом или означает группу NR5R6, когда R3 означает NH2 при температуре 90-170°С, при необходимости в присутствии безводного хлорида алюминия, когда R1 означает R3 или в присутствии m-крезола, когда R' означает NR5R6.
Текст
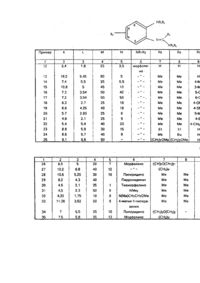
Настоящее изобретение касается способа получения новых терапевтических соединений, полезных в качестве противодиабетических средств, в частности, гипогликемических средств, способов получения таких лечебных средств и фармацевтических композиций, содержащих их. Конкретно, настоящее изобретение предусматривает способ получения соединений формулы I: и их фармацевтически приемлемых солей, где NR1R2 означает морфолино, пиперидино, пирролидинил, тиаморфолино, метилпиперазинил, Ν,Ν-диметиламино или N-{метоксиэтил)-N-метиламино. R3 является алкильной группой, содержащей 1-4 углеродных атомов, когда R5 и R6 являются водородом или R3 является группой NH2, когда NR5R6 означает Ν,Ν-диметиламино, Ν,Ν-диэтиламино, N-бутил-Nметиламино, N,N-бис(метоксиэтил)амино, морфолино, пирролидинил или пиперидино. R7 представляет собой атом водорода, метил, этил, изобутил, метокси, метилито, метилтиометил, фтор или хлор. Специфическими соединениями формулы I являются: N-{2-мopфoлинoфeнил)-aцeтaмидин; N-(5-метил-2-морфолинофенил)-ацетамидин; . N-(2-морфолинофенил)-пропионамид; N-(2-морфолинофенил)-бутирамидин; N-(2-морфолинофенил)-изобутирамидин; N-(5-мeтилтиo-2-мopфoлинoфeнил)-изoбутирамидин; N-(5-фтор-2-морфолинофенил)-изобутирамидин; 2-(2-морфолинофенил)-валерамидин; 2-(2-морфолинофенил)-пиваламидин; 2-(2-морфолинофенил}-гуанидин; 1,1-диметил-2-(5-метил-2-морфолино-фенил)-гуанидин; 1,1-диметил-2-(6-метил-2-морфолино-фенил)-гуанидин; 1,1-диметил-2-(4-хлор-2-морфолинофенил)-гуанидин; 1,1-диметил-2-(3-хлор-2-морфолинофенил)-гуанидин; 1,1-диметил-2-(5-метокси-2-морфолино-фенил)-гуанидин; 1,1-диметил-2-(5-метилтио-2-морфолинофенил)-гуанидин; 1,1-диметил-2-(4-метил-2-морфолино-фенил)-гуанидин; 1,1 -диметил-2-(5-этил-2-морфолинофенил)-гуанидин; 1,1-диметил-2-(5-метилтиометил-2-морфолинофенил)-гуанидин: 1,1-диметил-2-{2-морфолинофенил)-гуанидин; 1-(Н-бутил)-1-метил-2-(2-морфолинофенил)-гуанидин; 1,1-бис-(2-метоксиэтил)-2-(2-морфолинофенил)-гуанидин; N-(2-морфолинофенил)-морфолин-4-карбоксамидин; N-(2-мopфoлинoфeнил)-пиppoлидин-1-карбоксамидин; 1,1-диметил-2-(2-морфолинофенил)-гуанидин; 1,1-диметил-2-(2-пиперидинофенил)-гуанидин; 1,1 -диметил-2-(2-(1 -пирролидинил)-фенил)-гуанидин; 1,1-диметил-2-(2-тиаморфолинофенил)-гуанидин; 1,1-диметил-2-(2-диметиламино фенил}-гуанидин; 1,1-диметил-2-{2-/N-{2-метоксиэтил)-N-метиламино)-фенил}-гуанидин; 1,1-диметил-2-/2-(4-метил-1 -пиперазинил)-фенил)-гуанидин; N-{2-пипepидинoфeнил)-мopфoнлин-4-карбоксимидин; N-(2-пипepидинoфeнил)-пиnepидин-1-карбоксимидин; 1-1-диметил-2-(5-метокси карбонил-2-морфолинофенил)-гуанидин, и их фармацевтически приемлемые соли. Соединения формулы (I) могут существовать как соли с фармацевтически приемлемыми кислотами. Примеры таких солей включают гидрохлориды, гидробромиды, гидройодиды, сульфаты, нитраты, малеаты, ацетаты, цитраты, фумараты, тартраты, сукцинаты, бензоаты, памоаты и соли с кислыми аминокислотами, такими как глутаминовая кислота. Соединения формулы (I) и их соли могут существовать в форме сольватов (например, гидратов). Некоторые соединения формулы (I) содержат один или более асимметрических углеродных атомов и существуют в различных оптически активных формах. Если соединения формулы (I) содержат хиральный центр, то соединения существуют в двух энантиомерных формах, и настоящее изобретение включает обе энанитомерные формы и их смеси. Если соединения формулы I содержат более одного хирального центра, то соединения могут существовать в диастереоизомерных формах. Настоящее изобретение включает каждую из этих диастереоизомерных форм и их смеси. Настоящее изобретение включает также фармацевтические композиции, содержащие терапевтически эффективное количество соединения формулы I вместе с фармацевтически приемлемым разбавителем или носителем. При терапевтическом использовании активное соединение может быть введено перорально, ректально, парентерально или локально, предпочтительно перорально. Таким образом, терапевтические композиции согласно настоящему изобретению могут иметь форму любой из известных фармацевтических композиций для перорального, ректального, парентерального или локального введения. Фармацевтически приемлемые носители, пригодные для использования в таких композициях, хорошо известны в данной области. Композиции согласно настоящему изобретению могут содержать 0,1-90% вес. активного соединения. Композиции согласно, настоящему изобретению обычно получают в форме дозированных единиц. В качестве композиций для перорального введения используют предпочтительные композиции согласно настоящему изобретению в виде известных фармацевтических форм для такого введения, например таблетки, капсулы, сиропы и водные или масляные суспензий. Средой для лекарства, используемой для получения указанных композиций, являются хорошо известные в фармакологии индеферентные составные части лекарства, Таблетки могут быть получены путем смешения активного соединения с инертным разбавителем таким как фосфат кальция в присутствии десинтегрирующи х агентов, например, кукурузного крахмала, и смазывающих средств, например, стеарата магния, и таблетирования смеси известными методами. Таблетки могут быть сформованы способом, известным специалистам в данной области, чтобы получить длительное освобождение соединений согласно изобретению. Такие таблетки, если необходимо, могут иметь энтеросолюбильное покрытие, нанесенное известными способами/ например, с использованием фталата ацетата целлюлозы. Аналогично капсулы, например, жесткие или мягкие желатиновые капсулы, содержащие активное соединение с добавленными наполнителями или без таковых, могут быть получены традиционными Средствами, и, если желают, снабжены растворяющимся в кишечнике покрытием известными методами. Таблетки и капсулы могут традиционно содержать каждая по 50-500 мг активного соединения. Другие композиции для перорального введения включают, например, водные растворы содержащие активное соединение, водные суспензии, содержащие активное соединение в водной среде а присутствии нетоксичного суспендирующего средства, такого как натрий-карбоксиметилцеллюлоза. и масляные суспензии, содержащие соединение согласно изобретению в подходящем растительном масле, например, в арахисовом масле. Некоторые композиции могут быть пригодны для использования соединений согласно настоящему изобретению в форме частиц очень малого размера, например, получаемых жидким помолом. В композициях согласно настоящему изобретению активное соединение может, если желают, сочетаться с другими совместимыми фармакологически активными ингредиентами. Фармацевтические композиции, содержащие терапевтически эффективное количество соединения формулы (I) могут быть использованы для лечения гипергликемии человека. При таком лечении количество соединений формулы (I), вводимое в день, находится в пределах от 50 до 3000 мг. Предпочтительным путем введения является введение через рот, Гипогликемическую активность соединений формулы I, которые представлены в следующи х ниже примерах, подтверждали следующим тестом. Крыс, весивших 150-200 г, фиксировали на 18 часов, и затем подкожно инъецировали глюкозу (800 мг/4 мл/кг) с последующим пероральным введением дозы соединения, подлежащего испытаниям (х мг в 4 или 5 мл 2% агара /кг). Через два и четыре часа отбирали кровь из глазницы и глюкозу плазмы оценивали на анализаторе глюкозы Бекмана с использованием специфического метода окисления глюкозы (Kadish АН, Little R.L and Struberg J.G., Clim. Chem., 14,.116, 1968). Затем рассчитывали процентное снижение глюкозы плазмы в сравнении с контрольными животными, которые не получали испытываемого соединения, но получали только 2%-й гомогенат агара. Соединения считались обладающими гипогликемической активностью в этом тесте, если они показывали 15% или более снижение глюкозы плазмы при любых значениях X до 200 как на втором, так и на четвертом часах. Результаты, полученные при любом значении x в описанных выше тестах, обсуждались игипогликемическую активность каждого соединения классифицировали по следующей шкале. Если для конкретного значения x имелось более одной серии результатов, то использовали среднее значение % снижения для классификации активности соединений. А - более чем 25%-ное снижение через два и четыре часа после введения соединения. В - более чем 25-е снижение через два часа, но меньше чем 25%-ное снижение через 4 часа, С - снижение в пределах 15-25% через два часа, но более 25%-ное снижение через 4 часа. D - снижение в пределах 15-25% как через два часа, так и через 4 часа. Ε - снижение в пределах 15-25% через два часа, но меньше, чем 15%-ное снижение через 4 часа. F - менее чем 15%-ное снижение через два часа, но более чем 15%-ное снижение через 4 часа. Активности соединений, описанных в приведенных ниже примерах, представлены в таблице А. Настоящее изобретение будет проиллюстрировано следующими примерами, приведенными только в качестве примеров. Конечный продукт каждого примера будет характеризоваться элементным анализом. Пример 1. Смесь 4-(2-аминофенил)-морфолина (5,34 г), ацетонитрила (4,52 мл) и безводного хлористого алюминия (12 г) нагревали при 160-170°С в течение 4 часов и получали N-(2-морфолинофенил)-ацетамидин (т.пл. 140-141°С), который перекристаллизовывали из гексана. Пример 2. Смесь 4-{2-амино-4-метил-фенил)-морфолина (5,76 г), ацетонитрила (3,5 г) и безводного хлористого алюминия (12 г) нагревали при 160-170°С пять часов и получали N-(5-метил-2морфолинофенил)ацетамидин (точка пл. 121°С), который перекристаллизовывали из гексана. Пример 3. Смесь 4-(2-аминофенил)-морфолина (5,34 г), пропионитрила (4,7 г) и безводного хлористого алюминия (12 г) нагревали при 160-170°С в течение 6 часов и получали N-(2 морфолинофенил)пропионамидин (т.пл. 114°С), который перекристаллизовывали из гексана. Пример 4. Смесь гидрохлорида 4-{2-аминофенил)-морфолина (7,5 г) и н-бутиро-нитрила (20 мл) нагревали при 170°С в герметичном сосуде высокого давления из нержавеющей стали в течение 60 часов. Избыток н-бутиронитрила удаляли, остаток растворяли в воде, подщелачивали 10%-м раствором гидроокиси натрия до рН 12 и экстрагировали дихлорметаном. Экстракт промывали водой, затем рассолом, сушили и растворитель удаляли. Остаток очищали хроматографией на колонке с нейтральным глиноземом. Элюированием смесью дихлорметангексан в отношении 1:1 удаляли непрореагировавший исходный материал и затем элюированием смесью метанолдихлорметан в отношении 1:99 получали твердое вещество , которое растворяли в метаноле (10 мл) и обрабатывали фумаровой кислотой (0,4 г) и получали N(2-морфолинофенил)-бутирамидин, монофумарат (температура плавления 168-170°С, который перекристаллизовывали из смеси метанол-эфир в отношении 1:2. Пример 5. Измельченный в порошок безводный хлористый алюминий (12 г) по частям добавляли к перемешиваемому шламу 4-{2-аминофенил)-морфолина (5,34 т) и н-бутиронитрила (6 г) при 50-40°С. Затем смесь нагревали при 160-170°С шесть часов, охлаждали и затем вываривали с 40% водным раствором гидроокиси натрия. Раствор экстрагировали эфиром, экстракт промывали водой рассолом и сушили. После удаления растворителя получали остаток, который кристаллизовывали из смеси этилацетат-гексан в отношении 1:1 и получали N-(2-морфолинофенил)-бутирамидин (точка плавления 131 °С, который обращали в его монофумаровую соль (точка плавления 173°С), перекристаллизованную из пропан-2-ола. Пример 6. Смесь 4-(2-аминофенил)-морфолина гидрохлорида (10 г) и изобутиронитрила (60 мл) нагревали при 165°С в течение 26 часов в герметичном сосуде высокого давления из нержавеющей стали и получали N-(2-морфолинофенил)-изобутирамидин (точка плавления 140-141°C), который перекристаллизовывали из гексана. Пример 7. Смесь 4-(2-аминофенил)-морфолина гидрохлорида (5,34 г), изобутиронитрила (6 г) и безводного хлорида алюминия (12 г) нагревали при 160-170°С 6 часов и получали N-(2-морфолинофенил)изобутирамидин (точка плавления 138°С). который перекристаллизовывали из смеси этилацетат-гексан в отношений 1:1. Πример 8. Смесь 5-метилтио-2-морфолиноанилина (1,8 г), изобутиронитрила (1,66 г) и безводного хлористого алюминия (3,2 г) нагревали при 140°С два часа и получали N-(5-метилтио-2-морфолинофенил)изобутирамидин (точка плавления 155°С), который перекристаллизовывали из гексана. Пример 9. Смесь 5-фтор-2-морфолиноанилина (1,96 г), изобутиронитрила (2 г) и безводного хлористого алюминия нагревали при 150°С четыре часа и получали N-(5-фтор-2-морфолино-фенил)-изобутирамидин (точка плавления 142°С), который был перекристаллизован из гексана и обращен в его фумаратную соль (точка плавления 172°С), которая была перекристаллизована из смеси метанол-эфир в отношении 1:1. Пример 10. Смесь гидрохлорида 4-(2-аминофенил)-морфолина (6,5 г) и валеронитрила (35 мл) нагревали при 160-165°С в атмосфере азота в течение 25 часов и затем охлаждали. Смесь обрабатывали водной гидроокисью натрия и подщелочную смесь экстрагировали дихлорметаном. Растворитель удаляли выпариванием и остаток отгоняли придавлений 50 мм Η для удаления половины непрореагировавшегося валеронитрила. Твердое вещество, выделившееся при охлаждении, отделяли фильтрацией, промывали гексаном (50 мл) и перекристаллизовывали из гексана и получали N-(2-морфолинофенил)валеромидин (температура плавления (135-136°С). Пример 11. Смесь 4-(2-аминофенил)-морфолина (3,56 г), пивалонитрила (5 г) и безводного хлорида алюминия (8 г) нагревали при 160-170°С в течение шести часов и получали N-(2-морфолинофенил)пиваламидин (точка плавления 126°С), который был перекристаллизован из гексана и обращен в его монофумаратную соль (точка плавления 211°С), перекристализованную из метанола. Примеры 12-35. Взаимодействием соединения формулы УП в форме его хлористоводородной соли (К граммов) с соединением формулы NC-NR5R6 (граммов) в метакрезоле (М мл) проводили нагреванием при 9095°С в течение N часов с получением соединений, идентифицированных в таблице, причем в примечаниях дано: (32) - продукт перекристаллизован из гексана; (38) - продукт выделен в форме монофумаратной соли, которая перекристаллизована из смеси метанолэфир в о тношении 1:2; (44) - продукт перекристаллизован из этилацетата; (45) - продукт выделен в форме монофумаратной соли, которую перекристаллизовали из метанола; (65) - реакцию проводили при 110°С; (66) - продукт выделяли в форме монофумаратной соли, которую перекристаллизовывали из смеси метанол-эфир в отношении 1:1; (67) - реакцию проводили при 90-95°С в течение восьми часов и затем при 115-120°С в течение четырех часов; (68) - реакцию проводили при 120-125°С; (69) - реакционную смесь нагревали при 90-95°С в течение 9 часов и затем при 120°С в течение 21 часа; (70) - из реакционной смеси получали масло, которое экстрагировали кипящим гексаном и получали свободное основание, которое обращали в монофумаратную соль, перекристаллизованную из смеси метанол-эфир в отношении 1:3; (71) - из реакционной смеси получали масло, которое экстрагировали гексаном с получением свободного основания в форме масла, которое очищали хроматографией на колонке нейтрального: глинозема, используя последовательно следующие элементы: гексан, смесь дихлорметан-гексан в отношении 1:1, дихлорметан и смесь метанол-дихлорметан в отношении 1:99 с получением основания, перекристаллизованного из смеси метанол-эфир в отношении 2:7. Пример 36, Смесь гидрохлорида 4-(2-аминофенил)-морфолина (2,1 г) и Ν,Ν-диметилцианамида (7 мл) нагревали в атмосфере азота при 165-170°С в течение 12 часов. Реакционную смесь охлаждали до 10°С, выпавший осадок собирали фильтрацией, промывали эфиром и перемешивали с 40%-м водным раствором гидроокиси натрия. Полученную смесь экстрагировали дихлорметаном, экстракт промывали рассолом и сушили. После удаления растворителя получали остаток, который перекристаллизовывали из гексана и получали 1,2-диметил-2-(2-морфолинофенил)-гуанидин (точка плавления 144-145°С). Пример 37. Смесь 4-(2-амино-4-метоксикарбонилфенил)-морфолина (2,7 г) и Ν,Ν-диметилцианамида (1 г) и м-крезола (15 мл) нагревали при 90-95°С в течение 10 часов. Добавляли лед и реакционную смесь подкисляли до рН добавлением 2 н хлористоводородной кислоты и полученную смесь экстрагировали эфиром. Водный слой охлаждали, подщелачивали до рН 8 добавлением твердого бикарбоната натрия и затем экстрагировали дихлорметаном. Экстракт сушили, растворитель удаляли и получали масляный остаток, который очищали хроматографией на колонке нейтрального глинозема, элюированной смесью метанол-дихлорметан в отношении 1:99 и получали 1,1-диметил-2-(5-метоксикарбонил-2-морфолинофенил)гуанидин (т.пл, 152-154°С). Пример 38. Смесь гидрохлорида 5-изобутил-2-морфолиноанилина (4,1 г) Ν,Ν-диметилцианамида (1,77 г) и метакрезола (15 мл) нагревали при 90-95°С шесть часов и получали остаток, который экстрагировали горячим гексаном, обесцвечивали древесным углем и очищали хроматографией на колонке глинозема, элюируемой смесью метанол-дихлорметан в отношении 2:98. Полученный продукт кристаллизовали из смеси этилацетат-гексан в отношении 1:3. Начальный осадок удаляли фильтрацией и фильтрат выпаривали из смеси этилацетат-гексан в отношении 1:3 и получали 1,2 диметил-2-(5-изобутил-2-морфолинофенил)гуанидин. Пример 39. Смесь гидрохлорида 2-морфолиноанилина (19,2 г), метакрезола (80 мл) и диметилцианамида (9,45 г) нагревали при 100°С пять часов, охлаждали и добавляли к смеси 40% водного раствора гидроокиси натрия (300 мл) и льда (300 г). Добавляли воду (300 мл) и полученное твердое вещество выделяли фильтрацией, промывали водой и растворяли в дихлорметане. Раствор сушили, растворитель удаляли и получали остаток, который перекристаллизовывали из тексана и получали 1,1-диметил-2-(2морфолинофенил)-гуанидин (точка плавления 142-143°С). К размешанному раствору N-этил-N-(2-метоксиатил)анина (10,3 г) в безводном бензоле (80 мл), охлажденном до 5°С в ледяной бане, в течение 10 минут добавляли раствор бромистого циана (5,3 г) в безводном бензоле (20 мл), и температуру реакционной смеси доводили до комнатной температуры. После чего реакционную смесь размешивали в течение ночи. Затем растворитель удаляли при пониженном давлении, а остаток неоднократно экстрагировали безводным эфиром (4x25 мл). Органические экстракты осушали суль фатом натрия, фильтровали, растворитель удаляли, и в результате получали N-этил-N-(2метоксиэтил)цианамид в виде бледно-желтого маслянистого продукта (6,3г). Смесь N-(2-аминофенил)морфолина гидрохлорида (2 г). N-этил-N-(2-метоксиэтил)цианамида (2,5 г) и ткрезола (15 мл) нагревали при 90-95°С в течение 8 часов. Затем добавляли N-этил-N-(2-метоксиэтил) цианамид (2,5 г) и продолжали нагревать еще в течение 20 часов. После удаления растворителя получали желтоватое маслянистое вещество, которое очищали с помощью колоночной хроматографии на нейтральной окиси алюминия (80 г), элюируя сначала дихлорметаном, а затем 1% метанолом-дихлорметаном, в результате чего получали бесцветное маслянистое вещество (1 г), которое затем подвергали реакции взаимодействия с фумаровой кислотой (0,38 г) в метаноле (10 мл) и получали N-этил-N-(2-метокси-этил)-N-[2-(4-морфолино) фенил] гуанидина монофумарат в виде бесцветного твердого вещества (0,8 г, т.пл. 170-171 °С), которое перекристаллизовали из смеси метанола и эфира (1:2).
ДивитисяДодаткова інформація
Назва патенту англійськоюA process for preparation of amidines or pharmaceutically acceptable salts thereof
Назва патенту російськоюСпособ получения амидинов или их фармацевтически приемлемых солей
МПК / Мітки
МПК: C07D 295/135
Мітки: фармацевтично, спосіб, солей, одержання, амідінів, прийнятних
Код посилання
<a href="https://ua.patents.su/5-19156-sposib-oderzhannya-amidiniv-abo-kh-farmacevtichno-prijjnyatnikh-solejj.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання амідінів або їх фармацевтично прийнятних солей</a>
Попередній патент: Пристрій для визначення осадки, крену і диференту плавзасобу
Наступний патент: Тара для демонстрації та зберігання монет
Випадковий патент: Спосіб отримання напоїв на основі плодоовочевого соку