6-(r)-метилселено-2-оксо-4-(2-фурил)-3,5-диціано-1,2,3,4-тетрагідропіридини
Номер патенту: 74550
Опубліковано: 12.11.2012
Автори: Фролов Костянтин Олександрович, Кривоколиско Сергій Геннадійович
Формула / Реферат
6-(R)-метилселено-2-оксо-4-(2-фурил)-3,5-диціано-1,2,3,4-тетрагідропіридини загальної формули (І) характеризуються тим, що у четвертому положенні мають 2-фурильний замісник, а у шостому положенні піридинового циклу містять атом селену з різними алкілпохідними замісниками
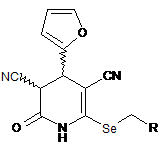 , I
, I
де, R=Н, Alk, Ar, Het, C(O)OAlk, C(O)Alk, C(O)Ar, C(O)Het, C(O)NH2, C(O)NHAlk, C(O)NHAr, C(O)NHHet;
Текст
Реферат: 6-(R)-метилселено-2-оксо-4-(2-фурил)-3,5-диціано-1,2,3,4-тетрагідропіридини загальної формули (І), які характеризуються тим, що у четвертому положенні мають 2-фурильний замісник, а у шостому положенні піридинового циклу містять атом селену з різними алкілпохідними замісниками. UA 74550 U (12) UA 74550 U UA 74550 U Корисна модель належить до галузі органічного синтезу, зокрема до нових 6-(R)метилселено-2-оксо-4-(2-фурил)-3,5-диціано-1,2,3,4-тетрагідропіридинів загальної формули (І) див.фіг. O CN NC O 5 10 15 20 25 30 N H R Se ,I де, R=Н, Alk, Ar, Het, C(O)OAlk, C(O)Alk, C(O)Ar, C(O)Het, C(O)NH2, C(O)NHAlk, C(O)NHAr, C(O)NHHet; і може бути використана як потенційно біологічно активні сполуки з направленою фармакологічною активністю та вихідні речовини для синтезу нових функціонально заміщених гетероциклічних сполук. Сполуки (І), їх отримання, властивості і використання у патентних виданнях не описані. Найбільш близькими структурними аналогами сполук, що заявляються, є 4-Аr-6-(R)метилтіо-2-оксо-3,5-диціано-1,2,3,4-тетрагідропіридини, їх властивості та методи синтезу описані у статті [1]. Спільною ознакою найближчого аналога та корисної моделі, що заявляється, є те, що вказані сполуки належать до групи 4-Аr-6-(R)-метилхалькоген-2-оксо-3,5-диціано-1,2,3,4тетрагідропіридинів. Задачею корисної моделі є створення раніше невідомих 6-(R)-метилселено-2-оксо-4-(2фурил)-3,5-диціано-1,2,3,4-тетрагідропіридинів. Поставлена задача вирішується тим, що синтезовані сполуки (І), у четвертому положенні мають 2-фурильний замісник, а у шостому положенні піридинового циклу містять атом селену з різними алкіл похідними замісниками. Синтез 6-(R)-метилселено-2-оксо-4-(2-фурил)-3,5-диціано-1,2,3,4-тетрагідропіридинів (І) здійснюють наступним чином: 0,83 мл (1 ммоль) 2-фуральдегіду (II), 1,47 г (1 ммоль) ціаноселеноацетаміду (III), 2 мл ацетону та 1 краплю відповідної органічної основи перемішують при 10 °C у атмосфері аргону 10 хв., потім додають 1,67 г (1 ммоль) 3,5-диметил-1(ціаноацетил)піразолу (IV) та (1,5 ммоль) органічної основи по краплинах. Отриману суміш перемішують 30 хв., потім додають 1 ммоль відповідного алкілгалогеніду (V), 30 мл 70 % водного етанолу та кип'ятять 1-2 хвилини у атмосфері аргону, швидко відфільтровують крізь паперовий фільтр. Розчин залишають на 24 год. при 20 °C. Осад, що утворився, відфільтровують, промивають етанолом та гексаном, отримують відповідні селенони (І), які являють собою дрібнокристалічні порошки з забарвленням від білого до коричневого кольору, добре розчиняються у ДМФА, ДМСО, ацетоні, помірно розчиняються у EtOH, AcOH. NC H3C CN O + NH2 CHO II III O N + Se N H3C O O B CN NC 10 oC HalCH2R V CN NC EtOH, O N H IV Se - + BH O N H I Se R , 35 40 де, R=H, Alk, Ar, Het, C(O)OAlk, C(O)Ar, C(O)Het, C(O)NH2, C(O)NHAlk, C(O)NHAr, C(O)NHHet; В=Et3N, N-метилморфолін, піперидин, морфолін. 1 Структура сполук, що заявляються, підтверджується спектрами ЯМР Н, знятими на приладі Bruker Avance II 400 (399,97 МГц) в ДМСО-d6 (внутрішній стандарт ТМС), ІЧ-спектри отримували на спектрофотометрі ІЧС-29 у вазелиновій олії. Елементний аналіз проводили на приладі "Perkin-Elmer С, Н, N-Analyzer". Контроль індивідуальності синтезованих сполук проводили 1 UA 74550 U 5 10 15 20 25 30 35 40 45 50 55 60 методом ТСХ на пластинках Silufol UV-254, у системі ацетон-гептан (1:1), проявлення - пари йоду, УФ-детектор. Одержані продукти мають достатню чистоту для аналізу та для подальшого використання. Отримані 6-(R)-метилселено-2-оксо-4-(2-фурил)-3,5-диціано-1,2,3,4-тетрагідропіридини за структурними та фізико-хімічними властивостями суттєво відрізняються від сполук порівняння. Корисна модель ілюструється наступними прикладами, які ілюструють, а не обмежують її об'єм. Приклад 1. Метил-([6-оксо-3,5-диціано-4-(2-фурил)-1,4,5,6-тетрагідропіридин-2-іл]селено)ацетат (співвідношення цис- та транс-ізомерів складає ≈ 2:5). Світло-коричнева дрібнокристалічна сполука, вихід 0.16 г (47 %), т. пл. 150-152 °C. ІЧ-1 1 спектр, v, см : 1710 (С=О), 2210, 2270 (2 C≡N), 3150 (NH). Спектр ЯМР Н, , м. д. (J, Гц): 3.67 (3Н, с, ОМетранс); 3.72 (3Н, с, ОМецис); 3.80-3.90 (4Н, м, накладання сигналів SeCH2цис та транс); 4.42 (1Н, м, С(4)Нцис); 4.55 (1Н, м, С(4)Нтранс); 4.64 (1Н, м, С(5)Нтранс); 4.81 (1Н, м, С(5)Нцис); 6.39-6.48 3 (4Н, м, С(3)Нфурил, С(4)Нфурил); 7.55 (1Н, пош.д, С(5)Нфурил, транс, J=5.9); 7.60 (1Н, пош.д, 3 С(5)Нфурил, цис, J=5.9); 11.12 (1Н, с, NHтpaнс); 11.14 (1Н, с, NHцис). Знайдено, %: С 45.91; Н 3.07; N 11.43. C14H11N3O4Se. Вираховано, %: С 46.17; Н 3.04; N11.54. Приклад 2. 2-Оксо-6-[(2-оксо-2-фенілетил)селено]-4-(2-фурил)-3,5-диціано-1,2,3,4-тетрагідропіридин (співвідношення цис- та трансізомерів складає ≈ 2:1). Біла дрібнокристалічна сполука, вихід 0.18 -1 г (45 %), т. пл. 197-199 °C (з АсОН). ІЧ-спектр, v, см : 1725 (С=О), 2205, 2260 (2 C≡N), 3135 (NH). 1 3 Спектр ЯМР Н, , м. д. (J, Гц): 4.38 (1Н, д, С(4)Нцис, J=6.6); 4.57 (2Н, д.д, С(3)Нтранс та С(4)Нтранс, 3 3 J=12.2); 4.79 (1Н, д, С(3)Нцис, J=6.6); 4.70-4.83 (4Н, м, SeCH2циc та транс); 6.38-7.64 (14Н, м, накладання сигналів С(3)Н-С(5)Нфеніл та С(3)Н-С(5)Нфурил); 7.99 (2Н, пош.д, С(2)Нфеніл, С(6)Нфеніл, 3 J=7.8); 11.04 (2Н, пош.с, NHцис та транс). Знайдено, %: С 55.31; Н 3.22; N 10.17. C19H13N3O3Se. Вираховано, %: С 55.62; Н 3.19; N 10.24. Приклад 3. 6-{[2-(4-Метилфеніл)-2-оксоетил]селено}-2-оксо-4-(2-фурил)-3,5-диціано-1,2,3,4тетрагідропіридин (співвідношення цис- та трансізомерів складає ≈ 2:1). Біла дрібнокристалічна -1 сполука, вихід 0.24 г (59 %), т. пл. 193-195 °C (з АсОН). ІЧ-спектр, v, см : 1712 (С=О), 2205, 2260 1 (2 C≡N), 3120 (NH). Спектр ЯМР Н, , м. д. (J, Гц): 2.44 (6Н, пош.с, 4-СН3С6Н4цис та транс); 4.37 (1Н, 3 3 д, С(4)Нцис, J=6.6); 4.55 (2Н, д.д, С(3)Нтранс та С(4)Нтранс, J=12.1); 4.67-4.80 (4Н, накладання двох 2 3 д.д, SeCH2циc та транс, J=14.4); 4.78 (1Н, д, С(3)Нцис, J=6.6); 6.39-6.48 (4Н, м, С(3)Нфурил, С(4)Нфурил); 7.29 (4Н, м, С(3)Нарил та С(5)Нарил); 7.53 (1Н, м, С(5)Нфурил, цис); 7.58 (1H, м, С(5)Нфурил, транс); 7.90 (4Н, м, С(2)Нарил та С(6)Нарил); 11.02 (2Н, пош.с, NHцис, транс). Знайдено, %: С 56.26; Н 3.59; N 9.86. С20Н15N3О3Sе. Вираховано, %: С 56.61; Н 3.56; N9.90. Приклад 4. 2-{[6-Оксо-4-(2-фурил)-3,5-диціано-1,4,5,6-тетрагідропіридин-2-іл]селено}-N-фенілацетамід (співвідношення цис- та трансізомерів складає ≈ 5:2). Світло-коричнева дрібнокристалічна -1 сполука, вихід 0.28 г (68 %), т. пл. 188-190 °C (з АсОН). ІЧ-спектр, v, см : 1725 (С=О), 2200, 2265 1 (2 C≡N), 3135, 3400 (2 NH). Спектр ЯМР Н, , м. д. (J, Гц): 3.85-4.01 (4Н, м, SeCH2циc та транс); 4.42 3 3 3 (1Н, д, С(4)Нцис, J=6.7); 4.66 (2Н, д.д, С(4)Нтранс, C(5)Hтpaнс, J=12.5); 4.87 (1Н, д, С(5)Нцис, J=6.7); 6.39 (2Н, пош.с, С(3)Нфурил, цис та С(4)Нфурил, цис); 6.43 та 6.49 (по 1Н, обидва м, С(3)Нфурил, транста С(4)Нфурил, транс); 7.59-7.04 (12Н, м, С(5)Нфурил, цис, С(5)Нфурил, транс, Phцис та транс); 10.33 (1Н, c, PhNHциc); 10.36 (1Н, с, РhNНтранс); 11.38 (1Н, с, NHцис); 11.42 (1Н, с, NHтpaнс). Знайдено, %: С 53.12; Н 3.35; N 13.06. C19H14N4O3Se. Вираховано, %: С 53.66; Н 3.32; N13.17. Приклад 5. 2-{[6-Оксо-4-(2-фурил)-3,5-диціано-1,4,5,6-тетрагідропіридин-2-іл]селено}-N-(4метилфеніл)ацетамід (співвідношення цис- та трансізомерів складає ≈ 2:1). Світло-коричнева -1 дрібнокристалічна сполука, вихід 0.25 г (60 %), т. пл. 199-201 °C. ІЧ-спектр, v, см : 1720 (С=О), 1 2205, 2260 (2 C≡N), 3165, 3375 (2 NH). Спектр ЯМР Н, , м. д. (J, Гц): 2.31 (6Н, пош.с, накладання сигналів 4-CH3C6H4цис та транс); 3.81-3.98 (4Н, м, SeCH2циc та транс); 4.39 (1Н, д, С(4)Нцис, 3 3 J=6.6); 4.60 (2Н, пош. псевдо-с, С(4)Нтранс та С(5)Нтранс); 4.84 (1Н, д, С(5)Нцис, J=6.6); 6.38 (2Н, пош.с, С(3)Нфурил, цис та С(4)Нфурил, цис); 6.42 та 6.46 (по 1Н, обидва м, С(3)Нфурил, транс та С(4)Нфурил, транс); 7.06-7.46 (8Н, м, накладання сигналів 4-СН3С6Н4цис та транс); 7.52 (1Н, пош. псевдо-с, С(5)Нфурил, цис); 7.56 (1Н, пош. псевдо-с, С(5)Нфурил, транс); 10.22 (1Н, с, 4-CH3C6H4NHцис); 10.25 (1Н, с, 4-CH3C6H4NHтранс); 11.43 (1Н, с, NHцис); 11.50 (1Н, с, NHтpaнс). Знайдено, %: С 53.92; Н 3.71; N 12.61. C20H16N4О3Se. Вираховано, %: С 54.68; Н 3.67; N 12.75. Джерело інформації: 1. Кривоколыско С.Г., Дяченко В.Д., Русанов Э.Б., Литвинов В.П. ХГС, 525, (2001). 2 UA 74550 U ФОРМУЛА КОРИСНОЇ МОДЕЛІ 5 6-(R)-метилселено-2-оксо-4-(2-фурил)-3,5-диціано-1,2,3,4-тетрагідропіридини загальної формули (І), які характеризуються тим, що у четвертому положенні мають 2-фурильний замісник, а у шостому положенні піридинового циклу містять атом селену з різними алкілпохідними замісниками O CN NC O 10 N H Se R ,I де R=Н, Alk, Ar, Het, C(O)OAlk, C(O)Alk, C(O)Ar, C(O)Het, C(O)NH2, C(O)NHAlk, C(O)NHAr, C(O)NHHet. Комп’ютерна верстка А. Крижанівський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 3
ДивитисяДодаткова інформація
Назва патенту англійською6-(r)-methylseleno-2-oxo-4-(2-furyl)-3,5-dicyano-1,2,3,4-tetrahydropyridines
Автори англійськоюKryvokolysko Serhii Hennadiiovych, Frolov Kostiantyn Oleksandrovych
Назва патенту російською6-(r)-метилселено-2-оксо-4-(2-фурил)-3,5-дициано-1,2,3,4-тетрагидропиридины
Автори російськоюКривоколиско Сергей Геннадиевич, Фролов Константин Александрович
МПК / Мітки
МПК: C07D 211/68, C07D 211/52, C07D 211/02, C07D 211/40, C07D 211/42
Мітки: 6-(r)-метилселено-2-оксо-4-(2-фурил)-3,5-диціано-1,2,3,4-тетрагідропіридини
Код посилання
<a href="https://ua.patents.su/5-74550-6-r-metilseleno-2-okso-4-2-furil-35-diciano-1234-tetragidropiridini.html" target="_blank" rel="follow" title="База патентів України">6-(r)-метилселено-2-оксо-4-(2-фурил)-3,5-диціано-1,2,3,4-тетрагідропіридини</a>
Попередній патент: 6-оксо-4-(2-фурил)-3,5-диціано-1,4,5,6-тетрагідропіридин-2-селенолати амонію
Наступний патент: Спосіб накладання біліодигестивного анастомозу з антирефлюксним захистом
Випадковий патент: Мембрана з присосами, сформованими з еластичного термопластичного матеріалу на гідрофільній та/або проникній підкладці









