Амідне похідне для інгібування росту ракових клітин
Номер патенту: 96045
Опубліковано: 26.09.2011
Автори: Парк Бум Воо, Кім Се Йоунг, Дзунг Йоунг Хеє, Лі Гван-Сун, Кім Маєнг Суп, Ахн Йоунг-Гіл, Кім Хан Кіонг, Чоі Бо Ім, Лі Кванг-Ок, Лі Чанг Гон, Ча Мі Йоунг, Чае Юн Дзунг, Банг Кеукчан, Кім Мі Ра, Ко Мі Йоунг
Формула / Реферат
1. Амідне похідне формули (І) або його фармацевтично прийнятна сіль:
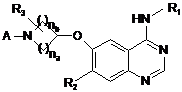 , (І)
, (І)
де
А являє собою
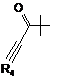 або
або 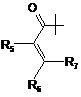 ,
,
R4, R5, R6 і R7, кожен незалежно, являють собою водень, галоген, N-С1-6алкіл або N-гідроксіамідо або оборотний С-С1-6алкіламідо(-NHCOС1-6), гідроксикарбоніл(-СООН), С1-6алкілоксикарбоніл(-СООС1-6), С1-6алкіл або С1-6алкіл, заміщений гідроксигрупою, С1-6діалкіламіном або гетероциклічною групою;
R1 являє собою арильну або гетероциклічну групу, заміщену одним-п'ятьма X, або С1-6алкіл, заміщений арилом;
R2 являє собою водень, гідрокси, С1-6алкокси або С1-6алкокси, заміщений С1-6алкокси або гетероциклічною групою;
R3 являє собою водень, -СООН, С1-6алкілоксикарбоніл або амідо, N-незаміщений або N-заміщений Y;
nа і nb, кожен, є цілим числом від 0 до 6; де:
X являє собою водень, галоген, гідрокси, ціано, нітро, (моно-, ди- або тригалоген)метил, меркапто, С1-6алкілтіо, акриламідо, С1-6алкіл, С1-6алкеніл, С1-6алкініл, С1-6алкокси, арилокси, С1-6діалкіламіно або С1-6алкіл або С1-6алкокси, заміщений Z, за умови, що, коли кількість замісників X дорівнює двом або більше, групи X можуть бути конденсовані одна з одною з утворенням циклічної структури;
Y являє собою гідрокси, С1-6алкіл або С1-6алкіл, заміщений Z, С1-6алкіл має один-чотири фрагменти, вибрані із групи, що складається з N, О, S, SO і SO2; і
Z являє собою С1-6алкіл, арильну або гетероциклічну групу, зазначений арил є С5-12 моноциклічною або біциклічною ароматичною групою, зазначена гетероциклічна група є С5-12 моноциклічною або біциклічною ароматичною або неароматичною групою, що містить один-чотири фрагменти, вибрані із групи, що складається з N, О, S, SO і SO2, і зазначена арильна і гетероциклічна група є незаміщеною або заміщена замісниками, вибраними із групи, що складається з галогену, гідроксилу, аміно, нітро, ціано, С1-6алкілу, С1-6алкенілу, С1-6алкінілу, С1-6алкокси, С1-6моноалкіламіно і С1-6діалкіламіно.
2. Сполука за п. 1, де R1 являє собою 3-хлор-4-фторфеніл, 3-хлор-2-фторфеніл, 3-хлор-2,4-дифторфеніл, 3,4-дихлор-2-фторфеніл, 4-бром-3-хлор-2-фторфеніл, 4-бром-2-фторфеніл, (R)-1-фенілетил, 3-хлор-4-(3-фторбензилокси)феніл, 3-хлор-4-(піридин-2-ілметокси)феніл, 1-(3-фторбензил)-1Н-5-індазол, 3-етинілфеніл, 4-хлор-2,5-диметоксифеніл, 4-бром-3-метилфеніл, 4-ізопропілфеніл, 3-метилфеніл, 3-бромфеніл, 3-хлорфеніл, 3,4-дихлорфеніл, 2,3,4-трифторфеніл, 4-фтор-3-метилфеніл, 3,4-диметилфеніл, 4-фенілоксифеніл, 2,3-дигідро-1H-інденіл, 4-гідрокси-3,5-дихлорфеніл, 3-гідрокси-4-хлорфеніл, 4-гідрокси-2-хлорфеніл, 2-гідрокси-4-хлорфеніл, 3-ціанофеніл, 3-трифторметилфеніл, 3-хлор-2-метоксифеніл, 4-хлор-3-метилфеніл, 4-бром-3-хлорфеніл, 4-бром-3-фторфеніл, 3-хлор-2-метилфеніл, 3-диметиламінофеніл, 2-фтор-3-трифторметилфеніл, 3-ціано-4-фторфеніл, 3-ціано-4-хлорфеніл, 3-метилтіофеніл, 2-хлорфеніл, 4-хлорфеніл, 3-хлорфенілметил, 3-вінілфеніл, 3-нітрофеніл, 3-акриламідофеніл, 3-меркаптофеніл, 3-хлорметилфеніл, 4-гідрокси-3-хлорфеніл або 4-гідрокси-3-фторфеніл;
R2 являє собою водень, гідрокси, метокси, етокси, 3-морфолінопропілокси або метоксіетокси;
R3 являє собою водень, метилоксикарбоніл, карбоксил, амідо, N-метиламідо, N-етиламідо, N-пропіламідо, N-ізопропіламідо, N-гідроксіамідо, N-2-гідроксіетиламідо, N-3-гідроксипропіламідо, N-2-метоксіетиламідо, N-2-метилтіоетиламідо, N-2-метилсульфонілетиламідо, N-2-N,N'-діетиламіноетиламідо або N-2-морфоліноетиламідо;
R4, R5, R6 і R7, кожен незалежно, являють собою водень, метил, 4-метилпіперазинілметил, 4-метилпіперазинілетил, N,N'-диметиламінометил, N,N'-діетиламінометил, морфолінометил, піролідин-1-ілметил, піперидин-1-ілметил, гідроксиметил, N-метилкарбоксамідо, ацетамідо, N-гідроксіамідо, метиловий складний ефір, хлор або карбоксил; і
na і nb, кожен незалежно, являють собою ціле число від 0 до 2.
3. Сполука за п. 1, вибрана із групи, що складається з
1) 1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2-ен-1-ону;
2) (Е)-1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)бут-2-ен-1-ону;
3) 1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)бут-2-ин-1-ону;
4) 1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)-5-(4-метилпіперазин-1-іл)пент-2-ин-1-ону;
5) 1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)-4-(диметиламіно)бут-2-ин-1-ону;
6) 1-((3S)-3-(4-(3-хлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2-ен-1-ону;
7) 1-((3S)-3-(4-(4-бром-3-хлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2-ен-1-ону;
8) 1-((3S)-3-(4-(3,4-дихлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2-ен-1-ону;
9) 1-((3S)-3-(4-(4-бром-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2-ен-1-ону;
10) 1-((3S)-3-(4-(3-хлор-4-(піридин-2-ілметокси)феніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2-ен-1-ону;
11) 1-((3S)-3-(7-метокси-4-((1R)-1-фенілетиламін)хіназолін-6-ілокси)піролідин-1-іл)проп-2-ен-1-ону;
12) 1-((3S)-3-(4-(1-(3-фторбензил)-1Н-індазол-5-іламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2-ен-1-ону;
13) 1-((3S)-3-(4-(3-хлор-4-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2-ен-1-ону;
14) 1-((3R)-3-(4-(3-хлор-4-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2-ен-1-ону;
15) 1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)хіназолін-6-ілокси)піролідин-1-іл)проп-2-ен-1-ону;
16) 1-((3S)-3-(4-(3-хлор-4-(3-фторбензилокси)феніламіно)хіназолін-6-ілокси)піролідин-1-іл)проп-2-ен-1-ону;
17) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен-1-ону;
18) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
19) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
20) 1-((3R)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2-ен-1-ону;
21) N-(2-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)етил)акриламіду;
22) 1-(3-(7-метокси-4-((1R)-1-фенілетиламіно)хіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен-1-ону;
23) 1-(3-(4-(3-хлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен-1-ону;
24) 1-(3-(4-(3,4-дихлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен-1-ону;
25) 1-(3-(4-(3-хлор-4-фторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен-1-ону;
26) 1-(3-(4-(3-хлорфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен-1-ону;
27) 3-(6-(1-акрилоїлазетидин-3-ілокси)-7-метоксихіназолін-4-іламіно)бензонітрилу;
28) (Е)-4-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-N-метил-4-оксобут-2-енаміду;
29) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-2-метилпроп-2-ен-1-ону;
30) (Z)-метил-4-(3-(4-(3-хлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-4-оксобут-2-еноату;
31) N-(3-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-3-оксопроп-1-ен-2-іл)ацетаміду;
32) (Z)-3-хлор-1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен-1-ону;
33) (Е)-3-хлор-1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен-1-ону;
34) 1-(4-(4-(3-хлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
35) 1-(4-(7-метокси-4-((1R)-1-фенілетиламіно)хіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
36) 1-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
37) 1-(4-(4-(3-етинілфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
38) 1-(4-(4-(4-хлор-2,5-диметоксифеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
39) 1-(4-(4-(4-бром-3-метилфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
40) 1-(4-(4-(4-ізопропілфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
41) 1-(4-(4-(м-толуїдино)-6-їлокси)піперидин-1-іл)проп-2-ен-1-ону;
42) 1-(4-(4-(3-бромфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
43) 1-(4-(4-(3-хлорфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
44) 1-(4-(4-(3,4-дихлорфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
45) 1-(4-(7-метокси-4-(2,3,4-трифторфеніламіно)хіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
46) 1-(4-(4-(4-фтор-3-метилфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
47) 1-(4-(4-(3,4-диметилфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
48) 1-(4-(7-метокси-4-(4-феноксифеніламіно)хіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
49) 1-(4-(4-(2,3-дигідро-1Н-інден-5-іламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
50) 1-(4-(4-(3,5-дихлор-4-гідроксифеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
51) 1-(4-(4-(4-хлор-3-гідроксифеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
52) 1-(4-(4-(2-хлор-4-гідроксифеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
53) 1-(4-(4-(4-хлор-2-гідроксифеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
54) 1-(4-(4-(3-хлор-4-(3-фторбензилокси)феніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
55) 1-(4-(4-(3-хлор-4-(піридин-2-ілметокси)феніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
56) 3-(6-(1-акрилоїлпіперидин-4-ілокси)-7-метоксихіназолін-4-іламіно)бензонітрилу;
57) 1-(4-(4-(3-хлор-4-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
58) 1-(4-(7-метокси-4-3-(трифторметил)феніламіно)хіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
59) 1-(4-(4-(3-хлор-2-метоксифеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
60) 1-(4-(4-(4-хлор-3-метилфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
61) 1-(4-(4-(4-бром-3-хлорфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
62) 1-(4-(4-(4-бром-3-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
63) 1-(4-(4-(3-хлор-2-метилфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
64) 1-(4-(4-(3-(диметиламіно)феніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
65) 1-(4-(4-(2-фтор-3-(трифторметил)феніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
66) 5-(6-(1-акрилоїлпіперидин-4-ілокси)-7-метоксихіназолін-4-іламіно)-2-фторбензонітрилу;
67) 5-(6-(1-акрилоїлпіперидин-4-ілокси)-7-метоксихіназолін-4-іламіно)-2-хлорбензонітрилу;
68) 1-(4-(7-метокси-4-(3-(метилтіо)феніламіно)хіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
69) 1-(4-(4-(2-хлорфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
70) 1-(4-(4-(4-хлорфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
71) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)хіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
72) 1-(4-(4-(3-хлорбензиламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
73) 1-(4-(7-метокси-4-(3-вінілфеніламіно)хіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
74) 1-(4-(7-метокси-4-(3-нітрофеніламіно)хіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
75) N-(3-(6-(1-акрилоїлпіперидин-4-ілокси)-7-хіназолін-4-іламіно)феніл)акриламіду;
76) 1-(4-(4-(3-меркаптофеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
77) 1-(4-(4-(3-хлорметил)феніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
78) 1-(4-(4-(3-хлор-4-гідроксифеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
79) 1-(4-(4-(3-фтор-4-гідроксифеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
80) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)бут-2-ин-1-ону;
81) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-3-метилбут-2-ен-1-ону;
82) (Е)-4-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-N-метил-4-оксобут-2-енаміду;
83) (Z)-метил-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-4-оксобут-2-еноату;
84) (Z)-метил-(4-(4-(3,4-дихлор-2-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-4-оксобут-2-еноату;
85) (Z)-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-4-оксобут-2-енової кислоти;
86) (Z)-4-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-4-оксобут-2-енової кислоти;
87) (Е)-4-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-4-оксобут-2-енової кислоти;
88) (Е)-4-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-N-гідроксі-4-оксобут-2-енаміду;
89) (Z)-3-хлор-1-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
90) (Е)-3-хлор-1-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
91) N-(3-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-3-оксопроп-1-ен-2-іл)ацетаміду;
92) (Е)-1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)-4-(диметиламіно)бут-2-ен-1-ону;
93) (Е)-1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)-4-(диметиламіно)бут-2-ен-1-ону;
94) (Е)-1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)-4-морфолінобут-2-ен-1-ону;
95) (Е)-1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)-4-(піролідин-1-іл)бут-2-ен-1-ону;
96) (Е)-1-((3S)-3-(4-(3-хлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піролідин-1-іл)-4-(диметиламіно)бут-2-ен-1-ону;
97) (E)-l-((3S)-3-(4-(3-xлop-2,4-фторфеніламіно)хіназолін-6-ілокси)піролідин-1-іл)-4-(диметиламіно)бут-2-ен-1-ону;
98) (Е)-1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-4-(диметиламіно)бут-2-ен-1-ону;
99) (Е)-1-(4-(4-(3,4-дихлор-2-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-4-(диметиламіно)бут-2-ен-1-ону;
100) (Е)-1-(4-(4-(3-хлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-4-(диметиламіно)бут-2-ен-1-ону;
101) (Е)-1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-4-(диметиламіно)бут-2-ен-1-ону;
102) (Е)-1-(3-(4-(3-хлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-4-(диметиламіно)бут-2-ен-1-ону;
103) (Е)-N-(2-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)етил)-4-(диметиламіно)бут-2-енаміду;
104) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-2-((диметиламіно)метил)проп-2-ен-1-ону;
105) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-2-(морфолінометил)проп-2-ен-1-ону;
106) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-2-((4-метилпіперазин-1-іл)метил)проп-2-ен-1-ону;
107) 1-(3-(4-(3-хлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-2-(піперидин-1-ілметил)проп-2-ен-1-ону;
108) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-2-(піперидин-1-ілметил)проп-2-ен-1-ону;
109) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-2-((диметиламіно)метил)проп-2-ен-1-ону;
110) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-2-(морфолінометил)проп-2-ен-1-ону;
111) 1-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-2-((диметиламіно)метил)проп-2-ен-1-ону;
112) (Z)-1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-4-(диметиламіно)бут-2-ен-1-ону;
113) (Z)-1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-2-(диметиламіно)бут-2-ен-1-ону;
114) 1-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-2-(гідроксиметил)проп-2-ен-1-ону;
115) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-гідроксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен-1-ону;
116) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-(2-метоксіетокси)хіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен-1-ону;
117) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-(2-метоксіетокси)хіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
118) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-(3-морфолінопропокси)хіназолін-6-ілокси)піперидин-1-іл)проп-2-ен-1-ону;
119) (2S,4S)-метил-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-2-карбоксилату;
120) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-2-карбоксаміду;
121) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)-N-метилпіперидин-2-карбоксаміду;
122) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)-N-етилпіперидин-2-карбоксаміду;
123) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)-N-пропілпіперидин-2-карбоксаміду;
124) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)-N-ізопропілпіперидин-2-карбоксаміду;
125) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)-N-гідроксипіперидин-2-карбоксаміду;
126) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)-N-(2-гідроксіетил)піперидин-2-карбоксаміду;
127) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)-N-(2-метоксіетил)піперидин-2-карбоксаміду;
128) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)-N-(2-(метилтіо)етил)піперидин-2-карбоксаміду;
129) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)-N-(2-(метилсульфоніл)етил)піперидин-2-карбоксаміду;
130) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)-N-(2-(диметиламіно)етил)піперидин-2-карбоксаміду;
131) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)-N-(3-гідроксипропіл)піперидин-2-карбоксаміду;
132) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)-N-(2-морфоліноетил)піперидин-2-карбоксаміду;
133) (2R,4R)-метил-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-2-карбоксаміду;
134) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-2-карбонової кислоти;
135) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-2-карбоксаміду;
136) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)-N-метилпіперидин-2-карбоксаміду;
137) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)-N-гідроксипіперидин-2-карбоксаміду;
138) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)-N-(2-(метилсульфоніл)етил)піперидин-2-карбоксаміду;
139) (2R,4R)-1-акрилоїл-4-(4-(3,4-дихлор-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-2-карбоксаміду і
140) (2R,4R)-1-акрилоїл-4-(4-(4-бром-2-фторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-2-карбоксаміду.
4. Фармацевтична композиція для інгібування росту ракових клітин, що містить амідне похідне або його фармацевтично прийнятну сіль за п. 1 як активний інгредієнт.
5. Фармацевтична композиція за п. 4, яку вводять у комбінації з іншим протираковим агентом, вибраним із групи, що складається з інгібіторів передачі клітинного сигналу, інгібіторів мітозу, алкілувальних агентів, антиметаболітів, антибіотиків, інгібіторів фактора росту, інгібіторів клітинного циклу, інгібіторів топоізомерази, модифікаторів біологічних реакцій, антигормональних агентів і антиандрогенів.
6. Фармацевтична композиція за п. 4, де ріст ракових клітин викликаний надекспресією EGFR, Erb-B2 або мутацією EGFR.
Текст
1. Амідне похідне формули (І) або його фармацевтично прийнятна сіль: R1 R3 HN ( )n b O A N ( )n N a C2 2 (19) 1 3 гідрокси-3,5-дихлорфеніл, 3-гідрокси-4-хлорфеніл, 4-гідрокси-2-хлорфеніл, 2-гідрокси-4-хлорфеніл, 3ціанофеніл, 3-трифторметилфеніл, 3-хлор-2метоксифеніл, 4-хлор-3-метилфеніл, 4-бром-3хлорфеніл, 4-бром-3-фторфеніл, 3-хлор-2метилфеніл, 3-диметиламінофеніл, 2-фтор-3трифторметилфеніл, 3-ціано-4-фторфеніл, 3ціано-4-хлорфеніл, 3-метилтіофеніл, 2-хлорфеніл, 4-хлорфеніл, 3-хлорфенілметил, 3-вінілфеніл, 3нітрофеніл, 3-акриламідофеніл, 3-меркаптофеніл, 3-хлорметилфеніл, 4-гідрокси-3-хлорфеніл або 4гідрокси-3-фторфеніл; R2 являє собою водень, гідрокси, метокси, етокси, 3-морфолінопропілокси або метоксіетокси; R3 являє собою водень, метилоксикарбоніл, карбоксил, амідо, N-метиламідо, N-етиламідо, Nпропіламідо, N-ізопропіламідо, N-гідроксіамідо, N2-гідроксіетиламідо, N-3-гідроксипропіламідо, N-2метоксіетиламідо, N-2-метилтіоетиламідо, N-2метилсульфонілетиламідо, N-2-N,N'діетиламіноетиламідо або N-2морфоліноетиламідо; R4, R5, R6 і R7, кожен незалежно, являють собою водень, метил, 4-метилпіперазинілметил, 4метилпіперазинілетил, N,N'-диметиламінометил, N,N'-діетиламінометил, морфолінометил, піролідин-1-ілметил, піперидин-1-ілметил, гідроксиметил, N-метилкарбоксамідо, ацетамідо, Nгідроксіамідо, метиловий складний ефір, хлор або карбоксил; і na і nb, кожен незалежно, являють собою ціле число від 0 до 2. 3. Сполука за п. 1, вибрана із групи, що складається з 1) 1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-ону; 2) (Е)-1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілокси)піролідин-1-іл)бут-2ен-1-ону; 3) 1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)бут-2-ин1-ону; 4) 1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)-5-(4метилпіперазин-1-іл)пент-2-ин-1-ону; 5) 1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)-4(диметиламіно)бут-2-ин-1-ону; 6) 1-((3S)-3-(4-(3-хлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-ону; 7) 1-((3S)-3-(4-(4-бром-3-хлор-2-фторфеніламіно)7-метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-ону; 8) 1-((3S)-3-(4-(3,4-дихлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-ону; 9) 1-((3S)-3-(4-(4-бром-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-ону; 10) 1-((3S)-3-(4-(3-хлор-4-(піридин-2ілметокси)феніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-ону; 96045 4 11) 1-((3S)-3-(7-метокси-4-((1R)-1фенілетиламін)хіназолін-6-ілокси)піролідин-1іл)проп-2-ен-1-ону; 12) 1-((3S)-3-(4-(1-(3-фторбензил)-1Н-індазол-5іламіно)-7-метоксихіназолін-6-ілокси)піролідин-1іл)проп-2-ен-1-ону; 13) 1-((3S)-3-(4-(3-хлор-4-фторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-ону; 14) 1-((3R)-3-(4-(3-хлор-4-фторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-ону; 15) 1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)хіназолін-6-ілокси)піролідин-1іл)проп-2-ен-1-ону; 16) 1-((3S)-3-(4-(3-хлор-4-(3фторбензилокси)феніламіно)хіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-ону; 17) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен1-ону; 18) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 19) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 20) 1-((3R)-3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-ону; 21) N-(2-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)етил)акриламіду; 22) 1-(3-(7-метокси-4-((1R)-1фенілетиламіно)хіназолін-6-ілоксі)азетидин-1іл)проп-2-ен-1-ону; 23) 1-(3-(4-(3-хлор-2-фторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен1-ону; 24) 1-(3-(4-(3,4-дихлор-2-фторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен1-ону; 25) 1-(3-(4-(3-хлор-4-фторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен1-ону; 26) 1-(3-(4-(3-хлорфеніламіно)-7-метоксихіназолін6-ілоксі)азетидин-1-іл)проп-2-ен-1-ону; 27) 3-(6-(1-акрилоїлазетидин-3-ілокси)-7метоксихіназолін-4-іламіно)бензонітрилу; 28) (Е)-4-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-N-метил4-оксобут-2-енаміду; 29) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-2метилпроп-2-ен-1-ону; 30) (Z)-метил-4-(3-(4-(3-хлор-2-фторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-4-оксобут2-еноату; 31) N-(3-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-3оксопроп-1-ен-2-іл)ацетаміду; 32) (Z)-3-хлор-1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)проп-2-ен-1-ону; 5 33) (Е)-3-хлор-1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)проп-2-ен-1-ону; 34) 1-(4-(4-(3-хлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 35) 1-(4-(7-метокси-4-((1R)-1фенілетиламіно)хіназолін-6-ілокси)піперидин-1іл)проп-2-ен-1-ону; 36) 1-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 37) 1-(4-(4-(3-етинілфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 38) 1-(4-(4-(4-хлор-2,5-диметоксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 39) 1-(4-(4-(4-бром-3-метилфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 40) 1-(4-(4-(4-ізопропілфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 41) 1-(4-(4-(м-толуїдино)-6-їлокси)піперидин-1іл)проп-2-ен-1-ону; 42) 1-(4-(4-(3-бромфеніламіно)-7-метоксихіназолін6-ілокси)піперидин-1-іл)проп-2-ен-1-ону; 43) 1-(4-(4-(3-хлорфеніламіно)-7-метоксихіназолін6-ілокси)піперидин-1-іл)проп-2-ен-1-ону; 44) 1-(4-(4-(3,4-дихлорфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 45) 1-(4-(7-метокси-4-(2,3,4трифторфеніламіно)хіназолін-6-ілокси)піперидин1-іл)проп-2-ен-1-ону; 46) 1-(4-(4-(4-фтор-3-метилфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 47) 1-(4-(4-(3,4-диметилфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 48) 1-(4-(7-метокси-4-(4феноксифеніламіно)хіназолін-6-ілокси)піперидин1-іл)проп-2-ен-1-ону; 49) 1-(4-(4-(2,3-дигідро-1Н-інден-5-іламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 50) 1-(4-(4-(3,5-дихлор-4-гідроксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 51) 1-(4-(4-(4-хлор-3-гідроксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 52) 1-(4-(4-(2-хлор-4-гідроксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 53) 1-(4-(4-(4-хлор-2-гідроксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 54) 1-(4-(4-(3-хлор-4-(3фторбензилокси)феніламіно)-7-метоксихіназолін6-ілокси)піперидин-1-іл)проп-2-ен-1-ону; 96045 6 55) 1-(4-(4-(3-хлор-4-(піридин-2ілметокси)феніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону; 56) 3-(6-(1-акрилоїлпіперидин-4-ілокси)-7метоксихіназолін-4-іламіно)бензонітрилу; 57) 1-(4-(4-(3-хлор-4-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 58) 1-(4-(7-метокси-4-3(трифторметил)феніламіно)хіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону; 59) 1-(4-(4-(3-хлор-2-метоксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 60) 1-(4-(4-(4-хлор-3-метилфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 61) 1-(4-(4-(4-бром-3-хлорфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 62) 1-(4-(4-(4-бром-3-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 63) 1-(4-(4-(3-хлор-2-метилфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 64) 1-(4-(4-(3-(диметиламіно)феніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 65) 1-(4-(4-(2-фтор-3-(трифторметил)феніламіно)7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 66) 5-(6-(1-акрилоїлпіперидин-4-ілокси)-7метоксихіназолін-4-іламіно)-2-фторбензонітрилу; 67) 5-(6-(1-акрилоїлпіперидин-4-ілокси)-7метоксихіназолін-4-іламіно)-2-хлорбензонітрилу; 68) 1-(4-(7-метокси-4-(3(метилтіо)феніламіно)хіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону; 69) 1-(4-(4-(2-хлорфеніламіно)-7-метоксихіназолін6-ілокси)піперидин-1-іл)проп-2-ен-1-ону; 70) 1-(4-(4-(4-хлорфеніламіно)-7-метоксихіназолін6-ілокси)піперидин-1-іл)проп-2-ен-1-ону; 71) 1-(4-(4-(3-хлор-2,4дифторфеніламіно)хіназолін-6-ілокси)піперидин-1іл)проп-2-ен-1-ону; 72) 1-(4-(4-(3-хлорбензиламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 73) 1-(4-(7-метокси-4-(3-вінілфеніламіно)хіназолін6-ілокси)піперидин-1-іл)проп-2-ен-1-ону; 74) 1-(4-(7-метокси-4-(3-нітрофеніламіно)хіназолін6-ілокси)піперидин-1-іл)проп-2-ен-1-ону; 75) N-(3-(6-(1-акрилоїлпіперидин-4-ілокси)-7хіназолін-4-іламіно)феніл)акриламіду; 76) 1-(4-(4-(3-меркаптофеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 77) 1-(4-(4-(3-хлорметил)феніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 78) 1-(4-(4-(3-хлор-4-гідроксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 7 79) 1-(4-(4-(3-фтор-4-гідроксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону; 80) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)бут-2-ин1-ону; 81) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-3метилбут-2-ен-1-ону; 82) (Е)-4-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-Nметил-4-оксобут-2-енаміду; 83) (Z)-метил-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-оксобут-2-еноату; 84) (Z)-метил-(4-(4-(3,4-дихлор-2дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-оксобут-2-еноату; 85) (Z)-4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-4оксобут-2-енової кислоти; 86) (Z)-4-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-4оксобут-2-енової кислоти; 87) (Е)-4-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-4оксобут-2-енової кислоти; 88) (Е)-4-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-Nгідроксі-4-оксобут-2-енаміду; 89) (Z)-3-хлор-1-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону; 90) (Е)-3-хлор-1-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону; 91) N-(3-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-3оксопроп-1-ен-2-іл)ацетаміду; 92) (Е)-1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілокси)піролідин-1-іл)-4(диметиламіно)бут-2-ен-1-ону; 93) (Е)-1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілокси)піролідин-1-іл)-4(диметиламіно)бут-2-ен-1-ону; 94) (Е)-1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілокси)піролідин-1-іл)-4морфолінобут-2-ен-1-ону; 95) (Е)-1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілокси)піролідин-1-іл)-4(піролідин-1-іл)бут-2-ен-1-ону; 96) (Е)-1-((3S)-3-(4-(3-хлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)-4(диметиламіно)бут-2-ен-1-ону; 97) (E)-l-((3S)-3-(4-(3-xлop-2,4фторфеніламіно)хіназолін-6-ілокси)піролідин-1-іл)4-(диметиламіно)бут-2-ен-1-ону; 98) (Е)-1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-4(диметиламіно)бут-2-ен-1-ону; 99) (Е)-1-(4-(4-(3,4-дихлор-2-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-4(диметиламіно)бут-2-ен-1-ону; 96045 8 100) (Е)-1-(4-(4-(3-хлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-4(диметиламіно)бут-2-ен-1-ону; 101) (Е)-1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-4(диметиламіно)бут-2-ен-1-ону; 102) (Е)-1-(3-(4-(3-хлор-2-фторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-4(диметиламіно)бут-2-ен-1-ону; 103) (Е)-N-(2-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)етил)-4(диметиламіно)бут-2-енаміду; 104) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-2((диметиламіно)метил)проп-2-ен-1-ону; 105) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-2(морфолінометил)проп-2-ен-1-ону; 106) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-2-((4метилпіперазин-1-іл)метил)проп-2-ен-1-ону; 107) 1-(3-(4-(3-хлор-2-фторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-2(піперидин-1-ілметил)проп-2-ен-1-ону; 108) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-2(піперидин-1-ілметил)проп-2-ен-1-ону; 109) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-2((диметиламіно)метил)проп-2-ен-1-ону; 110) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-2(морфолінометил)проп-2-ен-1-ону; 111) 1-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-2((диметиламіно)метил)проп-2-ен-1-ону; 112) (Z)-1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-4(диметиламіно)бут-2-ен-1-ону; 113) (Z)-1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-2(диметиламіно)бут-2-ен-1-ону; 114) 1-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-2(гідроксиметил)проп-2-ен-1-ону; 115) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7гідроксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен1-ону; 116) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7-(2метоксіетокси)хіназолін-6-ілоксі)азетидин-1іл)проп-2-ен-1-ону; 117) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-(2метоксіетокси)хіназолін-6-ілокси)піперидин-1іл)проп-2-ен-1-ону; 118) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-(3морфолінопропокси)хіназолін-6-ілокси)піперидин1-іл)проп-2-ен-1-ону; 119) (2S,4S)-метил-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксилату; 120) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксаміду; 9 96045 10 121) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-метилпіперидин-2-карбоксаміду; 122) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)-Nетилпіперидин-2-карбоксаміду; 123) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-пропілпіперидин-2-карбоксаміду; 124) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілоксі)-Nізопропілпіперидин-2-карбоксаміду; 125) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-гідроксипіперидин-2-карбоксаміду; 126) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-гідроксіетил)піперидин-2-карбоксаміду; 127) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-метоксіетил)піперидин-2-карбоксаміду; 128) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-(метилтіо)етил)піперидин-2-карбоксаміду; 129) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-(метилсульфоніл)етил)піперидин-2карбоксаміду; 130) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-(диметиламіно)етил)піперидин-2карбоксаміду; 131) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(3-гідроксипропіл)піперидин-2-карбоксаміду; 132) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-морфоліноетил)піперидин-2-карбоксаміду; 133) (2R,4R)-метил-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксаміду; 134) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбонової кислоти; 135) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксаміду; 136) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-метилпіперидин-2-карбоксаміду; 137) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-гідроксипіперидин-2-карбоксаміду; 138) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-(метилсульфоніл)етил)піперидин-2карбоксаміду; 139) (2R,4R)-1-акрилоїл-4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксаміду і 140) (2R,4R)-1-акрилоїл-4-(4-(4-бром-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксаміду. 4. Фармацевтична композиція для інгібування росту ракових клітин, що містить амідне похідне або його фармацевтично прийнятну сіль за п. 1 як активний інгредієнт. 5. Фармацевтична композиція за п. 4, яку вводять у комбінації з іншим протираковим агентом, вибраним із групи, що складається з інгібіторів передачі клітинного сигналу, інгібіторів мітозу, алкілувальних агентів, антиметаболітів, антибіотиків, інгібіторів фактора росту, інгібіторів клітинного циклу, інгібіторів топоізомерази, модифікаторів біологічних реакцій, антигормональних агентів і антиандрогенів. 6. Фармацевтична композиція за п. 4, де ріст ракових клітин викликаний надекспресією EGFR, ErbB2 або мутацією EGFR. Даний винахід стосується нового амідного похідного і його фармацевтично прийнятної солі, що селективно та ефективно інгібує ріст ракових клітин, викликаний надекспресією рецептора епідермального фактора росту (EGFR) і також запобігає розвитку лікарської стійкості, викликаної мутацією EGFR тирозин кінази, і фармацевтичної композиції, що включає його у ролі активного інгредієнта. У клітинах існує безліч систем передачі сигналу, які функціонально взаємопов'язані для керування проліферацією, ростом, метастазуванням і апоптозом клітин (Nature Reviews Cancer 5, 689, 2005). Відмова міжклітинної системи керування внаслідок генетичних факторів або факторів навколишнього середовища викликає аномальне посилення або руйнування системи передачі сигналу, що призводить до появи ракових клітин (Cell 100, 57, 2000). Протеїн тирозин кінази відіграють важливу роль у такому клітинному регулюванні (Nature Reviews Drug Discovery 3, 993, 2004), та їхня аномальна експресія або мутація спостерігається в ракових клітинах. Протеїн тирозин кіназа є ферментом, який каталізує транспорт фосфатних груп від АТФ до тирозинів, що знаходяться в білкових субстратах. Безліч рецепторних білків факторів росту функціонують як тирозин кінази, щоб передавати клітинні сигнали. Взаємодія між факторами росту і їхніми рецепторами у нормі керує ростом клітин, але аномальна передача сигналу, викликана мутацією або надекспресією кожного з рецепторів, часто індукує пухлинні клітини і різні види раку. Протеїн тирозин кінази були класифіковані на безліч сімейств відповідно до їхніх факторів росту, зокрема була детально вивчена тирозин кіназа (EGFR), що стосується рецептора фактора росту 11 96045 12 епітеліальних клітин (EGF) (Nature Reviews Cancer 5, 341, 2005). EGFR тирозин кіназа складається з рецептора і тирозин кінази та доставляє позаклітинні сигнали в ядро клітини через клітинну мембрану. Різні EGFR тирозин кінази класифіковані на основі їхніх структурних відмінностей на EGFR (Erb-B1), Erb-B2, Erb-В3 і Erb-B4, кожна з яких може утворювати гомодимерний або гетеродимерний комплекс доставки сигналу. Також надекспресія більше ніж одного з таких гетеродимерів часто спостерігається в злоякісних клітинах. На додаток, відомо, що як EGFR, так і Erb-B2 вносять значний вклад в утворення гетеродимерного комплексу доставки сигналу. Були розроблені деякі лікарські засоби, такі як малі молекули, для інгібування EGFR тирозин кіназ, такі як гефітиніб, ерлотиніб, лапатиніб та інші. Гефітиніб або ерлотиніб селективно та оборотно інгібують EGFR, а лапатиніб оборотно інгібує як EGFR, так і Erb-B2, у такий спосіб затримуючи ріст пухлин і в значній мірі продовжуючи термін життя пацієнта або надаючи терапевтичні переваги. Інгібітори передачі сигналу з малими молекулами, включаючи EGFR тирозин кінази, мають у ролі загальної структурної ознаки хіназоліновий фрагмент, і інгібітори тирозин кінази, що мають хіназоліновий фрагмент, розкриті в міжнародних публікаціях № WO 99/006396, WO 99/006378, WO 97/038983, WO 2000/031048, WO 98/050038, WO 99/024037, WO 2000/006555, WO 2001/098277, WO 2003/045939, WO 2003/049740 і WO 2005/012290, патентах США № 7019012 і 6225318 і патентах ЕР № 0787722, 0387063 і 1292591. У той же час добре відомо, що розвиток стійкості до конкретних використовуваних лікарських засобів викликає зниження активності лікарського засобу. Наприклад, повідомлялося, що гефітиніб або ерлотиніб породжують мутант EGFR T790M, вторинну мутацію, а також, що в половини пацієнтів, яким вводили гефітиніб або ерлотиніб, розвивається стійкість до гефітинібу або ерлотинібу, і що такі лікарські засоби не забезпечують істотного клінічного ефекту в пацієнтів із варіацією EGFR T790M (Public Library of Science Medicine, 2(3), 225, 2005, Cancer Res, 67(24), 11924,2007). У цьому зв'язку недавно було виявлено, що необоротні інгібітори мішені EGFR більш перспективні для подолання проблеми розвитку стійкості в порівнянні із загальноприйнятими необоротними інгібіторами, такими як гефітиніб або ерлотиніб (Cancer Cell 12, 81, 2007, Bioorganic & Medicinal Chemistry 16, 3482, 2008). Наприклад, необоротні інгібітори, такі як BIBW-2992 (British Journal of Cancer 98, 80, 2008), HKI-272 (Cancer Research 64, 3958, 2004) і AV-412 (Cancer Sci. 98(12), 1977, 2007), розроблені та у цей час перебувають на клінічній стадії. Структури необоротних інгібіторів показані нижче: Сполуки, показані вище, мають загальну структурну ознаку - акриламідну функціональну групу в положенні С-6 хіназолінового або ціанохінолінового залишку, яка утворює ковалентний зв'язок із цистеїном773 (Cys773), розташованим у домені АТФ EGFR, у такий спосіб необоротно блокуючи автофосфорилування EGFR і ефективно інгібуючи передачу сигналу ракових клітин (Proc. Natl. Acad. Sci. U.S.A. 95, 12022, 1998). Вони проявляють більше високі інгібуючі активності in vitro і in vivo у порівнянні із загальноприйнятими оборотними інгібіторами (J. Med. Chem. 42, 1803, 1999). Міжнародна патентна заявка WO 2008/032039, подана авторами вищезазначеної літератури, розкриває нову протиракову сполуку, що має інший акриламідний замісник у положенні С-6 хіназоліну, яка показує поліпшену інгібуючу-активність проти EGFR тирозин кіназ. Відповідно, існує постійна потреба в розробці нового лікарського засобу, що має поліпшену інгібуючу активність проти мутантів EGFR тирозин кіназ, який може ефективно інгібувати розвиток лікарської стійкості, викликаної мутантами EGFR тирозин кіназ, і одночасно не викликає небажаних побічних ефектів. Відповідно, метою даного винаходу є забезпечення нового амідного похідного або його фарма цевтично прийнятної солі, що селективно та ефективно інгібує ріст ракових клітин, викликаний надекспресією рецептора епідермального фактора росту (EGFR) і також запобігає розвитку лікарської стійкості, викликаної мутацією EGFR тирозин кінази, і фармацевтичної композиції, що включає його як активний інгредієнт. Іншою метою даного винаходу є забезпечення фармацевтичної композиції для інгібування росту ракових клітин, що включає зазначене амідне похідне як активний інгредієнт. Відповідно до одного аспекту даного винаходу забезпечується амідне похідне формули (І) або його фармацевтично прийнятна сіль: де А являє або , R4, R5, R6 і R7, кожен незалежно являє водень, галоген, N-C1-6 алкіл або N-гідроксіамідо або оборотний С-C1-6 алкіламідо (-NHCOC1-6), гідроксикарбоніл (-СООН), 13 C1-6 алкоксикарбоніл (-СООC1-6), C1-6 алкіл або C1-6 алкіл, заміщений гідроксигрупою, C1-6 діалкіламіном або гетероциклічною групою; R1 являє арильну або гетероциклічну групу, заміщену одним-п'ятьма X, або C1-6 алкіл, заміщений арилом; R2 являє водень, гідрокси, C1-6 алкокси або C16 алкокси, заміщений C1-6 алкокси або гетероциклічною групою; R3 являє водень, -СООН, C1-6 алкілоксикарбоніл або амідо, N-незаміщений або N-заміщений Y; nа і nb, кожен, є цілим числом від 0 до 6; де: X являє водень, галоген, гідрокси, ціано, нітро, (моно-, ди- або тригалоген)метил, меркапто, C1-6 алкілтіо, акриламідо, C1-6 алкіл, C1-6 алкеніл, C1-6 алкініл, C1-6 алкокси, арілокси, C1-6 діалкіламіно або C1-6 алкіл або C1-6 алкокси, заміщений Z, за умови, що коли кількість замісників X дорівнює двом або більше, групи X можуть бути конденсовані один з одним з утворенням циклічної структури; Υ являє гідрокси, C1-6 алкіл або C1-6 алкіл, заміщений Ζ, C1-6 алкіл має один-чотири фрагменти, вибрані із групи, що складається з Ν, О, S, SO і SO2; і Ζ являє C1-6 алкіл, арильну або гетероциклічну групу, зазначений арил є С5-12 моноциклічною або біциклічною ароматичною групою, зазначена гетероциклічна група є С5-12 моноциклічною або біциклічною ароматичною або неароматичною групою, що містить один-чотири фрагменти, вибрані із групи, що складається з N, О, S, SO і SO2, і зазначена арильна або гетероциклічна група є незаміщеною або заміщена замісниками, вибраними із групи, що складається з галогену, гідроксилу, аміно, нітро, ціано, C1-6 алкілу, C1-6 алкенілу, C1-6 алкінілу, C1-6 алкокси, C1-6 моноалкіламіно і C1-6 діалкіламіно. У переважному втіленні даного винаходу R1 являє 3-хлор-4-фторфеніл, 3-хлор-2-фторфеніл, 3хлор-2,4-дифторфеніл, 3,4-дихлор-2-фторфеніл, 4-бром-3-хлор-2-фторфеніл, 4-бром-2-фторфеніл, (R)-1-фенілетил, 3-хлор-4-(3фторбензилокси)феніл, 3-хлор-4-(піридин-2ілметокси)феніл, 1-(3-фторбензил)-1Н-5-індазол, 3-етинілфеніл, 4-хлор-2,5-диметоксифеніл, 4бром-3-метилфеніл, 4-ізопропілфеніл, 3метилфеніл, 3-бромфеніл, 3-хлорфеніл, 3,4дихлорфеніл, 2,3,4-трифторфеніл, 4-фтор-3метилфеніл, 3,4-диметилфеніл, 4-фенілоксифеніл, 2,3-дигідро-ІН-інденіл, 4-гідрокси-3,5-дихлорфеніл, 3-гідрокси-4-хлорфеніл, 4-гідрокси-2-хлорфеніл, 2гідрокси-4-хлорфеніл, 3-ціанофеніл, 3трифторметилфеніл, 3-хлор-2-метоксифеніл, 4хлор-3-метил феніл, 4-бром-3-хлорфеніл, 4-бром3-фторфеніл, 3-хлор-2-метилфеніл, 3диметиламінофеніл, 2-фтор-3трифторметилфеніл, 3-ціано-4-фторфеніл, 3ціано-4-хлорфеніл, 3-метилтіофеніл, 2-хлорфеніл, 4-хлорфеніл, 3-хлорфенілметил, 3-вінілфеніл, 3нітрофеніл, 3-акриламідофеніл, 3-меркаптофеніл, 3-хлорметилфеніл, 4-гідрокси-3-хлорфеніл або 4гідрокси-3-фторфеніл; R2 являє водень, гідрокси, метокси, етокси, 3-морфолінопропілокси або метоксіетокси; R3 являє водень, метилоксикарбоніл, карбоксил, амідо, N-метиламідо, N-етиламідо, N 96045 14 пропіламідо, N-ізопропіламідо, N-гідроксіамідо, N2-гідроксіетиламідо, N-3-гідроксипропіламідо, N-2метоксіетиламідо, N-2-метилтіоетиламідо, N-2метилсульфонілетиламідо, N-2-Ν,Ν'діетиламіноетиламідо, або N-2морфоліноетиламідо; R4, R5, R6 і R7 кожен незалежно являє водень, метил, 4метилпіперазинілметил, 4-метилпіперазинілетил, Ν,Ν'-диметиламінометил, Ν,Ν'-діетиламінометил, морфолінометил, піролідин-1-ілметил, піперидин1-ілметил, гідроксиметил, N-метилкарбоксамідо, ацетамідо, N-гідроксіамідо, метиловий складний ефір, хлор або карбоксил; і nа i nb, кожен незалежно, являє ціле число від 0 до 2, в амінопохідному формули (І). У даному винаході термін "галоген" стосується фтору, хлору, брому або йоду, якщо інше не зазначено. У даному винаході термін "алкіл" стосується насичених моновалентних вуглеводневих радикалів, що мають нормальний, циклічний або розгалужений ланцюг, якщо інше не зазначено. Прикладами більш переважних сполук формули (І) відповідно до даного винаходу є 1) 1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-он; 2) (Е)-1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)бут-2-ен-1-он; 3) 1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілокси)піролідин-1-іл)бут-2ин-1-он; 4) 1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілокси)піролідин-1-іл)-5-(4метилпіперазин-1-іл)пент-2-ин-1-он; 5) 1-((3S)-3-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілокси)піролідин-1-іл)-4(диметиламіно)бут-2-ин-1-он; 6) 1-((3S)-3-(4-(3-хлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-он; 7) 1-((3S)-3-(4-(4-бром-3-хлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-он; 8) 1-((3S)-3-(4-(3,4-дихлор-2-фторфеніламіно)7-метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-он; 9) 1-((3S)-3-(4-(4-бром-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-он; 10) 1-((3S)-3-(4-(3-хлор-4-(піридин-2ілметокси)феніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-он; 11) 1-((3S)-3-(7-метокси-4-((1R)-1фенілетиламін)хіназолін-6-ілокси)піролідин-1іл)проп-2-ен-1-он; 12) 1-((3S)-3-(4-(1-(3-фторбензил)-1Н-індазол5-іламіно)-7-метоксихіназолін-6-ілокси)піролідин-1іл)проп-2-ен-1-он; 13) 1-((3S)-3-(4-(3-хлор-4-фторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-он; 15 14) 1-((3R)-3-(4-(3-хлор-4-фторфеніламіно)-7метоксихіназолін-6-ілокси)піролідин-1-іл)проп-2ен-1-он; 15) 1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)хіназолін-6-ілокси)піролідин-1іл)проп-2-ен-1-он; 16) 1-((3S)-3-(4-(3-хлор-4-(3фторбензилокси)феніламіно)хіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-он; 17) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен1-он; 18) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 19) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 20) 1-((3R)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-он; 21) N-(2-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)етил)акриламід; 22) 1-(3-(7-метокси-4-((1R)-1фенілетиламіно)хіназолін-6-ілоксі)азетидин-1іл)проп-2-ен-1-он; 23) 1-(3-(4-(2-фторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен1-он; 24) 1-(3-(4-(3,4-дихлор-2-фторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен1-он; 25) 1-(3-(4-(3-хлор-4-фторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-і л)проп-2-ен1-он; 26) 1-(3-(4-(3-хлорфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен1-он; 27) 3-(6-(1-акрилоїлазетидин-3-ілокси)-7метоксихіназолін-4-іламіно)бензонітрил; 28) (Е)-4-(3-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-Nметил-4-оксобут-2-енамід; 29) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-2метилпроп-2-ен-1-он; 30) (Z)-метил-4-(3-(4-(3-хлор-2фторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-4-оксобут-2-еноат; 31) N-(3-(3-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-3оксопроп-1-ен-2-іл)ацетамід; 32) (Z)-3-хлор-1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)проп-2-ен-1-он; 33) (Е)-3-хлор-1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)проп-2-ен-1-он; 34) 1-(4-(4-(3-хлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 35) 1-(4-(7-метокси-4-((1R)-1фенілетиламіно)хіназолін-6-ілокси)піперидин-1іл)проп-2-ен-1-он; 96045 16 36) 1-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 37) 1-(4-(4-(3-етинілфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 38) 1-(4-(4-(4-хлор-2,5-диметоксифеніламіно)7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 39) 1-(4-(4-(4-бром-3-метилфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 40) 1-(4-(4-(4-ізопропілфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 41) 1-(4-(4-(м-толуїдино)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-он; 42) 1-(4-(4-(3-бромфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 43) 1-(4-(4-(3-хлорфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 44) 1-(4-(4-(3,4-дихлорфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 45) 1-(4-(7-метокси-4-(2,3,4трифторфеніламіно)хіназолін-6-ілокси)піперидин1-іл)проп-2-ен-1-он; 46) 1-(4-(4-(4-фтор-3-метилфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 47) 1-(4-(4-(3,4-диметилфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 48) 1-(4-(7-метокси-4-(4феноксифеніламіно)хіназолін-6-ілокси)піперидин1-іл)проп-2-ен-1-он; 49) 1-(4-(4-(2,3-дигідро-1H-інден-5-іламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 50) 1-(4-(4-(3,5-дихлор-4-гідроксифеніламіно)7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 51) 1-(4-(4-(4-хлор-3-гідроксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 52) 1-(4-(4-(2-хлор-4-гідроксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 53) 1-(4-(4-(4-хлор-2-гідроксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 54) 1-(4-(4-(3-хлор-4-(3фторбензилокси)феніламіно)-7-метоксихіназолін6-ілокси)піперидин-1-іл)проп-2-ен-1-он; 55) 1-(4-(4-(3-хлор-4-(піридин-2ілметокси)феніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-он; 56) 3-(6-(1-акрилоїлпіперидин-4-ілокси)-7метоксихіназолін-4-іламіно)бензонітрил; 57) 1-(4-(4-(3-хлор-4-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 17 58) 1-(4-(7-метокси-4-3(трифторметил)феніламіно)хіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-он; 59) 1-(4-(4-(3-хлор-2-метоксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 60) 1-(4-(4-(4-хлор-3-метилфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 61) 1-(4-(4-(4-бром-3-хлорфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 62) 1-(4-(4-(4-бром-3-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 63) 1-(4-(4-(3-хлор-2-метилфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 64) 1-(4-(4-(3-(диметиламіно)феніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 65) 1-(4-(4-(2-фтор-3(трифторметил)феніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-он; 66) 5-(6-(1-акрилоїлпіперидин-4-ілокси)-7метоксихіназолін-4-іламіно)-2-фторбензонітрил; 67) 5-(6-(1-акрилоїлпіперидин-4-ілокси)-7метоксихіназолін-4-іламіно)-2-хлорбензонітрил; 68) 1-(4-(7-метокси-4-(3(метилтіо)феніламіно)хіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-он; 69) 1-(4-(4-(2-хлорфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 70) 1-(4-(4-(4-хлорфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 71) 1-(4-(4-(3-хлор-2,4дифторфеніламіно)хіназолін-6-ілокси)піперидин-1іл)проп-2-ен-1-он; 72) 1-(4-(4-(3-хлорбензиламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 73) 1-(4-(7-метокси-4-(3вінілфеніламіно)хіназолін-6-ілокси)піперидин-1іл)проп-2-ен-1-он; 74) 1-(4-(7-метокси-4-(3нітрофеніламіно)хіназолін-6-ілокси)піперидин-1іл)проп-2-ен-1-он; 75) N-(3-(6-(1-акрилоїлпіперидин-4-ілокси)-7хіназолін-4-іламіно)феніл)акриламід; 76) 1-(4-(4-(3-меркаптофеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 77) 1-(4-(4-(3-хлорметил)феніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 78) 1-(4-(4-(3-хлор-4-гідроксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 79) 1-(4-(4-(3-фтор-4-гідроксифеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-он; 96045 18 80) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)бут-2-ин1-он; 81) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-3метилбут-2-ен-1-он; 82) (Е)-4-(4-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілокси)піперидин-1-іл)-Nметил-4-оксобут-2-енамід; 83) (Z)-метил-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-оксобут-2-еноат; 84) (Z)-метил-(4-(4-(3,4-дихлор-2дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-оксобут-2-еноат; 85) (Z)-4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-4оксобут-2-енова кислота; 86) (Z)-4-(4-(4-(3,4-дихлор-2-фторфеніламіно)7-метоксихіназолін-6-ілокси)піперидин-1-іл)-4оксобут-2-енова кислота; 87) (Е)-4-(4-(4-(3,4-дихлор-2-фторфеніламіно)7-метоксихіназолін-6-ілокси)піперидин-1-іл)-4оксобут-2-енова кислота; 88) (Е)-4-(4-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілокси)піперидин-1-іл)-Nгідрокси-4-оксобут-2-енамід; 89) (Z)-3-xлop-1-(4-(4-(3,4-диxлop-2фтopфeнiлaмiнo)-7-мeтoкcиxiнaзoлiн-6ілокси)піперидин-1-іл)проп-2-ен-1-он; 90) (Е)-3-хлор-1-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-он; 91) N-(3-(4-(4-(3,4-дихлор-2-фторфеніламіно)7-метоксихіназолін-6-ілокси)піперидин-1-іл)-3оксопроп-1-ен-2-іл)ацетамід; 92) (Е)-1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)-4-(диметиламіно)бут-2-ен-1он; 93) (Е)-1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)-4-(диметиламіно)бут-2-ен-1он; 94) (Е)-1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)-4-морфолінбут-2-ен-1-он; 95) (Е)-1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)-4-(піролідин-1-іл)бут-2-ен-1он; 96) (Е)-1-((3S)-3-(4-(3-хлор-2-фторфеніламіно)7-метоксихіназолін-6-ілокси)піролідин-1-іл)-4(диметиламіно)бут-2-ен-1-он; 97) (Е)-1-((3S)-3-(4-(3-хлор-2,4фторфеніламіно)хіназолін-6-ілокси)піролідин-1-іл)4-(диметиламіно)бут-2-ен-1-он; 98) (Е)-1-(4-(4-(3-хлор-2,4-дифторфеніламіно)7-метоксихіназолін-6-ілокси)піперидин-1-іл)-4(диметиламіно)бут-2-ен-1-он; 99) (Е)-1-(4-(4-(3,4-дихлор-2дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-(диметиламіно)бут-2-ен-1он; 19 100) (Е)-1-(4-(4-(3-хлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-4(диметиламіно)бут-2-ен-1-он; 101) (Е)-1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-4-(диметиламіно)бут-2-ен-1он; 102) (Е)-1-(3-(4-(3-хлор-2-фторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-4(диметиламіно)бут-2-ен-1-он; 103) (Е)-N-(2-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)етил)-4-(диметиламіно)бут-2-енамід; 104) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-2((диметиламіно)метил)проп-2-ен-1-он; 105) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-iлоксі)азетидин-1-іл)-2((морфолінометил)проп-2-ен-1-он; 106) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-2-((4метилпіперазин-1-іл)метил)проп-2-ен-1-он; 107) 1-(3-(4-(3-хлор-2-фторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-2(піперидин-1-ілметил)проп-2-ен-1-он; 108) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)-2(піперидин-1-ілметил)проп-2-ен-1-он; 109) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-2((диметиламіно)метил)проп-2-ен-1-он; 110) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-2(морфолінометил)проп-2-ен-1-он; 111) 1-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-2((диметиламіно)метил)проп-2-ен-1-он; 112) (Z)-1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-4-(диметиламіно)бут-2-ен-1он; 113) (Z)-1-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-2-(диметиламіно)бут-2-ен-1он; 114) 1-(4-(4-(3,4-дихлор-2-фторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)-2(гідроксиметил)проп-2-ен-1-он; 115) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7гідроксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен1-он; 116) 1-(3-(4-(3-хлор-2,4-дифторфеніламіно)-7(2-метоксіетокси)хіназолін-6-ілоксі)азетидин-1іл)проп-2-ен-1-он; 117) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7(2-метоксіетокси)хіназолін-6-ілокси)піперидин-1іл)проп-2-ен-1-он; 118) 1-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7(3-морфолінопропокси)хіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-он; 119) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксилат; 96045 20 120) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксамід; 121) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-метилпіперидин-2-карбоксамід; 122) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-етилпіперидин-2-карбоксамід; 123) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-пропілпіперидин-2-карбоксамід; 124) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-ізопропілпіперидин-2-карбоксамід; 125) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-гідроксипіперидин-2-карбоксамід; 126) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-гідроксіетил)піперидин-2-карбоксамід; 127) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-метоксіетил)піперидин-2-карбоксамід; 128) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-(метилтіо)етил)піперидин-2-карбоксамід; 129) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-метилсульфоніл)етил)піперидин-2карбоксамід; 130) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-(диметиламіно)етил)піперидин-2-карбоксамід; 131) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-б-ілокси)N-(З-гідроксипропіл) піперидин-2-карбоксамід; 132) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-морфоліноетил)піперидин-2-карбоксамід; 133) (2R,4R)-метил-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксамід; 134) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбонова кислота; 135) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксамід; 136) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-метилпіперидин-2-карбоксамід; 137) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-гідроксипіперидин-2-карбоксамід; 138) (2R,4R)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6-ілокси)N-(2-метилсульфоніл)етил)піперидин-2карбоксамід; 139) (2R,4R)-1-акрилоїл-4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксамід; і 140) (2R,4R)-1-акрилоїл-4-(4-(4-бром-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксамід. 21 96045 22 Сполука формули (І) даного винаходу може бути одержана, наприклад, за методикою, представленою схемою реакції (І) (див., [Bioorg. Med. Chem. Lett, 2001; 11: 1911] і міжнародну патентну публікацію WO 2003/082831): де A, R1, R2, R3, na i nb мають ті самі значення, що і визначені вище. У схемі реакцій (І) сполуку формули (X) піддають реакції конденсації з гідрохлоридом формамідину при високій температурі (наприклад, 210°С) із утворенням сполуки формули (IX) із наступною реакцією з L-метіоніном у середовищі органічної кислоти (наприклад, метансульфонової кислоти), включаючи видалення метилу з положення С-6 сполуки формули (IX), з утворенням сполуки формули (VIII). Потім сполуку формули (VIII) піддають реакції введення захисної групи в середовищі основи (наприклад, піридину) і безводної оцтової кислоти з утворенням сполуки формули (VII) із наступною реакцією з неорганічною кислотою (наприклад, тіонілхлоридом або оксихлоридом фосфору) у присутності каталітичної кількості диметилформаміду в умовах кип'ятіння зі зворотним холодильником з утворенням сполуки формули (VI) у формі гідрохлорату. Сполуку формули (VI) додають до спиртового розчину, що містить аміак (наприклад, 7н метанольного розчину, що містить аміак), який перемішують, включаючи видалення з нього ацетилу з утворенням сполуки формули (IV). Сполуку формули (IV) потім піддають реакції Міцунобу зі сполукою формули (V) і реакції заміщення з R1NH2 в органічному розчиннику (наприклад, 2-пропанол або ацетонітрил) для введення в нього R1. Одержану сполуку піддають реакції з органічною або неорганічною кислотою (наприклад, трифтороцтовою кислотою або концентрованою хлористоводневою кислотою) в органічному розчиннику (наприклад, метиленхлориді), включаючи видалення трет-бутоксикарбонілу, з утворенням сполуки фо рмули (II). У реакції Міцунобу можна використовувати діізопропілазодикарбоксилат, діетилазодикарбоксилат, ди-трет-бутилазодикарбоксилат або трифенілфосфін. Потім сполуку формули (І) даного винаходу одержують, піддаючи сполуку формули (II) реакції конденсації зі сполукою формули (III) A-C1 у суміші органічного розчинника (наприклад, тетрагідрофурану і води, або метиленхлориду) у присутності неорганічної або органічної основи (наприклад, бікарбонату натрію, піридину або триетиламіну), або піддаючи сполуку формули (II) реакції конденсації зі сполукою формули (III) A-OH в органічному розчиннику (наприклад, тетрагідрофурані або метиленхлориді) у присутності агента сполучення (наприклад, етил-3-(3диметиламінопропіл)карбодііміду (EDC) або гексафторфосфату метанамінію 2-(1Н-7азабензотриазол-1-іл)-1,1,3,3-тетраметил європію (HATU)). Сполука формули (І) даного винаходу також може застосовуватися у формі фармацевтично прийнятної солі, утвореної неорганічною або органічною кислотою, такою як хлористоводнева кислота, бромистоводнева кислота, сірчана кислота, фосфорна кислота, азотна кислота, оцтова кислота, гліколева кислота, молочна кислота, піровиноградна кислота, малонова кислота, бурштинова кислота, глутарова кислота, фумарова кислота, яблучна кислота, мигдальна кислота, винна кислота, лимонна кислота, аскорбінова кислота, пальмітинова кислота, малеїнова кислота, гідроксималеїнова кислота, бензойна кислота, гідроксибензойна кислота, фенілоцтова кислота, корична кислота, саліцилова кислота, метансульфонова кислота, бензолсульфонова кислота і толуолсульфонова кислота. 23 Сполука винаходу або її фармацевтично прийнятна сіль селективно та ефективно інгібує ріст ракових клітин, викликаний епідермальним фактором росту і його мутантами, і чинить поліпшену протиракову дію в комбінації з іншим протираковим агентом. Конкретно, сполука винаходу або її фармацевтично прийнятна сіль є корисними для поліпшення дії протиракового агента, вибраного із групи, що складається з інгібіторів передачі клітинного сигналу, інгібіторів мітозу, алкілувальних агентів, антиметаболітів, антибіотиків, інгібіторів фактора росту, інгібіторів клітинного циклу, інгібіторів топоізомерази, модифікаторів біологічних реакцій, антигормональних агентів і антиандрогенів. Тому даний винахід забезпечує фармацевтичну композицію для інгібування росту ракових клітин, що включає у ролі активного інгредієнта сполуку формули (І) або її фармацевтично прийнятну сіль. Сполука винаходу або її фармацевтично прийнятна сіль як активний інгредієнт може бути введена перорально або парентерально в ефективній кількості, що змінюється від приблизно 0,01 до 100 мг/кг, перевалено - від 0,2 до 50 мг/кг маси тіла на день у випадку ссавця, включаючи людини, у вигляді разової дози або розділених доз. Дозування активного інгредієнта може бути встановлене з урахуванням різних релевантних факторів, таких як стан пацієнта, що піддається лікуванню, тип і серйозність захворювання, швидкість введення та думка лікаря. У деяких випадках може бути придатною кількість, менша вищезазначеного дозування. Кількість, більша вищезазначеного дозування, може застосовуватися, якщо вона не викликає шкідливих побічних ефектів, і така кількість може бути введене у вигляді розділених денних доз. Фармацевтична композиція винаходу може бути складена відповідно до будь-яких загальноприйнятих способів у формі таблетки, гранули, порошку, капсули, сиропу, емульсії або мікроемульсії для перорального введення або для парентерального введення, включаючи внутрішньом'язовий, внутрішньовенний і підшкірний шляхи. Фармацевтична композиція винаходу для перорального введення може бути приготовлена змішуванням активного інгредієнта з носієм, таким як целюлоза, силікат кальцію, кукурудзяний крохмаль, лактоза, сахароза, декстроза, фосфат кальцію, стеаринова кислота, стеарат магнію, стеарат кальцію, желатин, тальк, поверхнево-активна речовина, суспендувальний агент, емульгатор і розріджувач. Прикладами носія, застосовуваного в композиції для ін'єкцій даного винаходу, є вода, розчин солі, розчин глюкози, розчин аналога глюкози, спирт, простий ефір гліколю (наприклад, поліетиленгліколь 400), олія, жирна кислота, складний ефір жирної кислоти, гліцерид, поверхневоактивна речовина, суспендувальний агент і емульгатор. Наступні приклади призначені для подальшої ілюстрації даного винаходу без обмеження його обсягу. 96045 24 Приклад 1 Одержання 1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-ону (1-1) 6,7-Диметоксихіназолін-4(3Н)-он 36,9 г 4,5-диметоксіантранілової кислоти змішують із 25,0 г гідрохлориду формамідину і суміш 30 хвилин перемішують при 210°С. Після завершення реакції одержану в такий спосіб тверду речовину охолоджують до кімнатної температури, перемішують із 200 мл (0,33 М) водного розчину гідроксиду натрію і відфільтровують при зниженому тиску. Одержану в такий спосіб тверду речовину промивають водою і сушать на повітрі, одержують зазначену в заголовку сполуку (24,6 г, 64%). 1 Н-ЯМР (300 МГц, ДМСО-d6) δ 7,99 (с, 1H), 7,44 (с, 1H), 7,13 (с, 1Н), 3,90 (с, 3H), 3,87 (с, 3H). (1-2) 6-Гідрокси-7-метоксихіназолін-4(3Н)-он 3,06 г сполуки, одержаної в (1-1), розводять 20 мл метанмульфонової кислоти. До одержаного розчину додають 2,66 г L-метіоніну і перемішують 22 години при 100°С. До реакційної суміші додають лід і нейтралізують 40% водним розчином гідроксиду натрію, викликаючи кристалізацію продукту. Тверду речовину відфільтровують при зниженому тиску, промивають водою і сушать на повітрі, одержують зазначену в заголовку сполуку (2,67 г, 94%). 1 Н-ЯМР (300 МГц, ДМСО-d6) δ 11,94 (с, 1H), 9,81 (с, 1Н), 7,92 (с, 1Н), 7,39 (с, 1Н), 7,11 (с, 1H), 3,91 (с, 3H). (1-3) 7-Метокси-4-оксо-3,4-дигідрохіназолін-6ілацетат 6,08 г сполуки, одержаної в (1-2), розчиняють у суміші 550 мл оцтової кислоти і 7 мл піридину, і одержаний розчин перемішують 3 години при 100°С. Реакційний розчин охолоджують до кімнатної температури і додають у нього лід, викликаючи кристалізацію продукту. Тверду речовину відфільтровують при зниженому тиску, промивають водою і сушать на повітрі, одержують зазначену в заголовку сполуку (4,87 г, 65%). 1 Н-ЯМР (300 МГц, ДМСО-d6) δ 12,21 (с, 1Н), 8,09 (с, 1H), 7,76 (с, 1Н), 7,28 (с, 1Н),3,91(с, 3Н),2,30(с, 3Н). (1-4) Гідрохлорид 4-хлор-7-метоксихіназолін-6ілацетату 4,87 г сполуки, одержаної в (1-3), розчиняють у суміші 33 мл тіонілхлориду і 6 мл оксихлориду фосфору. До одержаного розчину додають дві краплі диметилформаміду і перемішують 7 годин при 120°С. Реакційний розчин охолоджують до кімнатної температури і з нього при зниженому тиску видаляють розчинник з утворенням залишку. До залишку додають толуол, і одержаний розчин концентрують при зниженому тиску з видаленням розчинника, і цю процедуру повторюють ще 2 рази. Одержану в такий спосіб тверду речовину сушать при зниженому тиску, одержують зазначену в заголовку сполуку (5,16 г). 1 Н-ЯМР (300 МГц, ДМСО-d6) δ 9,01 (с, 1H), 8,02 (с, 1H), 7,64 (с, 1Н), 4,02 (с, 3H), 2,35 (с, 3H). (1-5) 4-Хлор-7-метоксихіназолін-6-ол 2 г сполуки, одержаної в (1-4), додають до 25 мл 7н розчину аміаку в метанолі. Суміш перемі 25 шують при кімнатній температурі 1 годину, утворену в реакційній суміші тверду речовину відфільтровують, промивають діетиловим ефіром і сушать, одержують зазначену в заголовку сполуку (1,43 г, 98%). 1 Н-ЯМР (300 МГц, ДМСО-d6) δ 8,78 (с, 1H), 7,41 (с, 1H), 7,37 (с, 1Н), 4,00 (с, 3H). (1-6) N-(3-хлор-2,4-дифторфеніл)-7-метокси-6((3S)-піролідин-3-ілокси)хіназолін-4-амін 1,43 г сполуки, одержаної в (1-5), 1,91 г (R)-NВос-3-піролідинолу і 1,96 г трифенілфосфіну додають до 20 мл метиленхлориду і по краплях додають туди 2,01 мл діізопропілазодикарбоксилату. Одержану суміш перемішують при кімнатній температурі 1 годину, переганяють при зниженому тиску і залишок попередньо очищають колонковою хроматографією (етилацетат:метиленхлорид:метанол = 20:20:1). Частково очищений залишок розчиняють потім у 60 мл 2пропанолу, додають туди 1,17 г хлор-2,4дифтораніліну, і суміш перемішують 3 години при 100°С. Одержану суміш переганяють при зниженому тиску для видалення розчинника і залишок розчиняють у 60 мл метиленхлориду. Додають туди 60 мл трифтороцтової кислоти, і суміш перемішують 1 годину при кімнатній температурі. Одержану суміш переганяють при зниженому тиску для видалення розчинника. До одержаного залишку додають розчин бікарбонату натрію до основної реакції з наступною екстракцією хлороформом. Органічний шар сушать над безводним сульфатом натрію, фільтрують і переганяють при зниженому тиску. Одержаний залишок піддають колонковій хроматографії (хлороформ:метанол = 1:2), одержують зазначену в заголовку сполуку (2 г, 73%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,68 (с, 1Н), 8,35 (м, 1H), 7,29 (с, 1Н), 7,09 (с, 1Н), 7,08 (м, 1H), 5,03 (ушир.м, 1Η), 4,02 (с, 3H), 3,37 (м, 1H), 3,27 (м, 1H), 3,11 (м, 1Н), 3,00 (м, 1H), 2,24 (м, 1Н), 2,12 (м, 1Н); + + MS (ESI ): m/z = 407,19 [М+Н] . (1-7) 1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-он 1,03 г сполуки, одержаної в (1-6), і 0,55 г бікарбонату натрію додають до 40 мл тетрагідрофурану і 6 мл дистильованої води, додають туди 0,18 г акрилоїлхлориду і суміш перемішують 30 хвилин при 0°С. Після завершення реакції до реакційної суміші додають насичений розчин бікарбонату натрію та одержану суміш екстрагують хлороформом. Одержаний у такий спосіб органічний шар сушать над безводним сульфатом натрію, фільтрують і переганяють. Одержаний залишок очищають колонковою хроматографією (хлороформ:метанол = 30:1), одержують зазначену в заголовку сполуку (0,7 г, 70%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,63 (с, 1Н), 8,14 (м, 1Н), 7,41 (с, 1H), 7,14 (с, 1Н), 7,02 (т, 1Н), 6,33 (м, 2Н), 5,63 (м, 1H), 5,11 (ушир.м, 1Н), 4,03 (с, 1H), 3,94 (с, 3H), 3,78 (м, 4Н), 2,46 (м, 1H), 2,28 (м, 1H); + + MS (ESI ): m/z = 461,4 [М+Н] . Приклад 2 Одержання (Е)-1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)бут-2-ен-1-ону 96045 26 Повторюють методику прикладу 1 за винятком використання транс-кротонілхлориду замість акрилоїлхлориду на стадії (1-7) з одержанням зазначеної в заголовку сполуки (35 мг, 60%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,53 (с, 1Н), 7,74 (м, 1Н), 7,37 (с, 1H), 7,14 (с, 1Н), 7,03 (м, 1H), 6,86 (м, 1Н), 5,99 (м, 1Н), 5,11 (ушир, м, 1Н), 4,09 (с, 1H), 3,94 (с, 3H), 3,81 (м, 4Н), 2,46 (м, 1Н), 2,29 (м, 1Н), 1,83 (м, 3H); + + MS (ESI ): m/z = 475,2 [М+Н] . Приклад 3 Одержання 1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)бут-2-ин-1-ону Повторюють методику прикладу 1 за винятком використання бут-2-іноїлхлориду замість акрилоїлхлориду на стадії (1-7) з одержанням зазначеної в заголовку сполуки (50 мг, 46%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,58 (с, 1H), 7,88 (м, 1Н), 7,37 (с, 1H), 7,20 (с, 1Н), 7,04 (т, 1H), 5,14 (ушир.м, 1Н), 3,98 (с, 3H), 3,82 (м, 4Н), 2,39 (м, 1Н), 2,27 (м, 1Н), 1,92 (с, 3H); + + MS (ESI ): m/z = 473,1 [М+Н] . Приклад 4 Одержання 1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)-5-(4-метилпіперазин-1іл)пент-2-ин-1-ону Повторюють методику прикладу 1 за винятком використання 5-(4-метилпшеразин-1-іл)пент-2іноїлхлориду замість акрилоїлхлориду на стадії (17) з одержанням зазначеної в заголовку сполуки (65 мг, 47%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,60 (с, 1H), 7,98 (м, 1H), 7,33 (с, 1Н), 7,23 (с, 1Н), 7,05 (т, 1Н), 5,14 (ушир.м, 1Н), 3,98 (с, 3H), 3,85 (м, 4Н), 2,52 (м, + + 14Н), 2,27 (с, 3H); MS (ESI ): m/z = 585,2 [М+Н] . Приклад 5 Одержання 1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)-4-(диметиламіно)бут-2-ин-1ону Повторюють методику прикладу 1 за винятком використання 4-(диметиламіно)бут-2-іноїлхлориду замість акрилоїлхлориду на стадії (1-7) з одержанням зазначеної в заголовку сполуки (50 мг, 41%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,59 (с, 1Н), 7,97 (м, 1H), 7,37 (с, 1Н), 7,23 (с, 1Н), 7,04 (т, 1H), 5,15 (ушир.м, 1Н), 3,98 (с, 3H), 3,87 (м, 4Н), 3,37 (с, 2Н), 2,34 (м, 2Н), 2,29 (с, 6Н); + + MS (ESI ): m/z = 516,2 [М+Н] . Приклад 6 Одержання 1-((3S)-3-(4-(3-хлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання 3-хлор-2-фтораніліну замість 3-хлор2,4-дифтораніліну на стадії (1-6) з одержанням зазначеної в заголовку сполуки (10 мг, 39%). 1 H-ЯМР (300 МГц, CDCI3) δ 9,82 (с, 1Н), 8,77 (м, 1Н), 8,64 (с, 1H), 7,11 (м, 2Н), 6,93 (с, 1H), 6,46 (м, 3H), 5,72 (м, 1Н), 4,00 (м, 7Н), 3,75 (м, 1Н), 2,50 (м, 1H); + + MS (ESI ): m/z = 443,18 [М+Н] . 27 Приклад 7 Одержання 1-((3S)-3-(4-(4-бром-3-хлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання 4-бром-3-хлор-4-фтораніліну замість 3-хлор-2,4-дифтораніліну на стадії (1-6) з одержанням зазначеної в заголовку сполуки (140 мг, 55%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,68 (с, 1Н), 8,32 (м, 1Н), 7,48 (м, 1Н), 7,27 (с, 1H), 7,19 (с, 1Н), 6,43 (м, 2Н), 5,71 (м, 1H), 5,12 (ушир.м, 1H), 4,03 (с, 1H), 3,99 (с, 3H), 3,83 (м, 4Н), 2,49 (м, 1Н), 2,31 (м, 1Н); + + MS (ESI ): m/z = 521,15 [М+Н] . Приклад 8 Одержання 1-((3S)-3-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання 3,4-дихлор-2-фтораніліну замість 3хлор-2,4-дифтораніліну на стадії (1-6) з одержанням зазначеної в заголовку сполуки (100 мг, 52%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,58 (с, 1Н), 7,94 (м, 1Н), 7,44 (с, 1Н), 7,28 (с, 1Н), 7,16 (с, 1H), 6,36 (м, 2Н), 5,63 (м, 1H), 5,10 (ушир, м, 1H), 3,99 (с, 1Н), 3,94 (с, 3H), 3,79 (м, 4Н), 2,47 (м, 1Н), 2,27 (м, 1Н); + + MS (ESI ): m/z = 477,1 [М+Н] . Приклад 9 Одержання 1-((3S)-3-(4-(4-бром-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання 4-бром-2-фтораніліну замість 3хлор-2,4-дифтораніліну на стадії (1-6) з одержанням зазначеної в заголовку сполуки (42 мг, 75%). 1 H-ЯМР (300 МГц, CDCI3+CD3OD) δ 8,33 (с, 1Н), 7,73 (д, 1H), 7,53 (т, 1Η), 7,41 (м, 2Н), 7,16 (д, 1Η), 6,60 (м, 1Н), 6,30 (дт, 1Н), 5,74 (тд, 1H), 5,19 (м, 1H), 3,90 (с, 3H), 3,83 (м, 4Н), 2,33 (м, 2Н); + + MS (ESI ): m/z = 487,1 [М+Н] . Приклад 10 Одержання 1-((3S)-3-(4-(3-хлор-4-(піридин-2ілметокси)феніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання 3-хлор-4-(піридин-2ілметокси)аніліну замість 3-хлор-2,4-дифтораніліну на стадії (1-6) з одержанням зазначеної в заголовку сполуки (42 мг, 76%). 1 H-ЯМР (300 МГц, CD3OD) δ 8,51 (д, 1Н), 8,34 (д, 1H), 7,83 (м, 2Н), 7,65 (т, 2Н), 7,51 (м, 1H), 7,35 (м, 1H), 7,05 (м, 2Н), 6,60 (м, 1H), 6,30 (дт, 1Н), 5,73 (тд, 1Н), 5,18 (с, 2Н), 4,85 (м, 1H), 3,90 (м, 4Н), 3,89 (с, 3H), 2,31 (м, 2Н); + + MS (ESI ): m/z = 532,2 [М+Н] . Приклад 11 Одержання (1-((3S)-3-(7-метокси-4-((1R)-1фенілетиламін)хіназолін-6-ілокси)піролідин-1іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання (1R)-1-фенілетанаміну замість 3хлор-2,4-дифтораніліну на стадії (1-6) з одержанням зазначеної в заголовку сполуки (44 мг, 67%). 96045 28 1 H-ЯМР (300 МГц, CDCI3) δ 8,27 (с, 1H), 7,75 (д, 1Н), 7,41 (д, 2Н), 7,28 (м, 2Н), 7,19 (д, 1H), 7,06 (с, 1Н), 6,58 (м, 1H), 6,30 (м, 1Н), 5,74 (м, 1Н), 5,58 (кв., 1H), 5,15 (ушир.м, 1Н), 3,90 (с, 3H), 3,73 (м, 4Н), 2,23 (м, 2Н); + + MS (ESI ): m/z = 419,2 [М+Н] . Приклад 12 Одержання 1-((3S)-3-(4-(1-(3-фторбензил)-1Hіндазол-5-іламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання (1-(3-фторбензил)-1Н-індазол-5аміну замість 3-хлор-2,4-дифтораніліну на стадії (1-6) з одержанням зазначеної в заголовку сполуки (11 мг, 35%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,32 (с, 1H), 8,08 (с, 1H), 8,03 (м, 1H), 7,77 (д, 1Н), 7,58 (м, 2Н), 7,30 (м, 1Н), 7,14 (д, 1H), 7,03 (м, 1Н), 6,98 (м, 1Н), 6,85 (м, 1H), 6,65 (м, 1Н), 6,28 (м, 1Н), 5,75 (м, 1H), 5,66 (с, 2Н), 5,20 (ушир.м, 1Н), 3,96 (с, 3H), 3,85 (м, 4Н), 2,34 (м, 2Н); + + MS (ESI ): m/z = 539,3 [М+Н] . Приклад 13 Одержання 1-((3S)-3-(4-(3-хлор-4фторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання 3-хлор-4-фтораніліну замість 3-хлор2,4-дифтораніліну на стадії (1-6) з одержанням зазначеної в заголовку сполуки (13 мг, 56%). 1 H-ЯМР (300 МГц, CD3OD) δ 8,34 (с, 1H), 7,89 (м, 1H), 7,67 (д, 1Н), 7,54 (м, 1Н), 7,15 (т, 1H), 7,06 (м, 1Н), 6,59 (м, 1Н), 6,47 (м, 1Н), 5,67 (м, 1Н), 5,15 (м, 1Н), 3,87 (с, 3H), 3,73 (м, 4Н), 2,23 (м, 2Н). Приклад 14 Одержання 1-((3R)-3-(4-(3-хлор-4фторфеніламіно-7-метоксихіназолін 6ілокси)піролідин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання (S)-(+)-N-Boc-3-піролідинолу замість (R)-(-)-N-Вос-3-піролідинолу на стадії (1-6) з одержанням зазначеної в заголовку сполуки (32 мг, 43%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,71 (с, 1Н), 7,96 (с, 1Н), 7,71 (м, 1H), 7,60 (м, 1Н), 7,27 (м, 1H), 7,15 (м, 1H), 6,45 (м, 2Н), 5,76 (м, 1H), 5,05 (м, 1H), 4,04 (с, 3H), 3,32 (м, 2Н), 3,12 (м, 2Н), 2,10 (м, 2Н). Приклад 15 Одержання 1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)хіназолін-6-ілокси)піролідин-1іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання 2-аміно-5-метоксибензойної кислоти замість 4,5-диметоксіантранілової кислоти на стадії (1-1) з одержанням зазначеної в заголовку сполуки (1,4 мг, 17%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,70 (с, 1Н), 8,31 (м, 1H), 7,92 (с, 1H), 7,47 (м, 1Н), 7,22 (м, 1H), 7,08 (м, 1Н), 6,44 (м, 2Н), 5,72 (м, 1Н), 5,13 (ушир.м, 1H), 3,99 (с, 1H), 3,76 (м, 4Н), 2,30 (м, 2Н); + + MS (ESI ): m/z = 431,26 [М+Н] . Приклад 16 Одержання 1-((3S)-3-(4-(3-хлор-4-(3фторбензилокси)феніламіно)хіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-ону 29 Повторюють методику прикладу 1 за винятком використання 2-аміно-5-метоксибензойної кислоти замість 4,5-диметоксіантранілової кислоти на стадії (1-1) і 3-хлор-4-(3-фторбензилокси)аніліну замість 3-хлор-2,4-дифтораніліну на стадії (1-6) з одержанням зазначеної в заголовку сполуки (42 мг, 75%). 1 H-ЯМР (300 МГц, CD3OD) δ 8,39 (д, 1H), 7,84 (т, 1H), 7,68 (м, 2Н), 7,54 (м, 1H), 7,44 (м, 1H), 7,36 (дд, 1H), 7,27 (м, 2Н), 7,06 (м, 2Н), 6,60 (м, 1H), 6,30 (дт, 1H), 5,73 (тд, 1Н), 5,19 (м, 1H), 5,14 (с, 2Н), 3,80 (м, 4Н), 2,31 (м, 2Н); + + MS (ESI ): m/z = 519,2 [М+Н] . Приклад 17 Одержання 1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання N-Boc-3-гідроксіазетидину замість (R)-(-)-N-Вос-3-піролідинолу на стадії (1-6) з одержанням зазначеної в заголовку сполуки (90 мг, 44%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,62 (с, 1H), 8,16 (с, 1H), 7,87 (м, 1H), 7,30 (с, 1Н), 7,20 (с, 1H), 7,03 (м, 1Н), 6,21 (м, 2Н), 5,65 (м, 1Н), 5,13 (м, 1H), 4,66 (м, 2Н), 4,51 (м, 1Н), 4,21 (м, 1Н), 4,03 (с, 3H); + + MS (ESI ): m/z = 447,1 [М+Н] . Приклад 18 Одержання 1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання N-Boc-3-гідроксипіперидину замість (R)-(-)-N-Вос-3-піролідинолу на стадії (1-6) з одержанням зазначеної в заголовку сполуки (110 мг, 54%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,63 (с, 1Н), 8,32 (с, 1Н), 8,07 (с, 1H), 8,00 (м, 1Н), 7,04 (м, 1H), 6,64 (м, 1Н), 6,42 (м, 1H), 5,79 (дд, 1H), 4,63 (м, 1H), 4,31 (м, 1Н), 4,02 (с, 3H), 3,84 (м, 1Н), 3,72 (м, 1Н), 3,43 (м, 1Н), 3,16 (дд, 1H), 2,17 (м, 1Н), 2,08 (м, 2Н); + + MS (ESI ): m/z = 475,2 [М+Н] . Приклад 19 Одержання 1-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання N-Boc-4-гідроксипіперидину замість (R)-(-)-N-Вос-3-піролідинолу на стадії (1-6) з одержанням зазначеної в заголовку сполуки (25 мг, 32%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,63 (с, 1Н), 8,09 (м, 1Н), 7,79 (с, 1H), 7,42 (с, 1Н), 7,29 (с, 1H), 7,04 (м, 1H), 6,58 (м, 1Н), 6,25 (м, 1Н), 5,68 (дд, 1H), 4,66 (м, 1H), 3,99 (с, 3H), 3,87 (м, 2Н), 3,53 (м, 2Н), 1,95 (м, 4Н); + + MS (ESI ): m/z = 475,2 [М+Н] . Приклад 20 Одержання 1-((3R)-3-(4-(3-хлор-2,4дифторфеніламіно-7-метоксихіназолін-6ілокси)піролідин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 1 за винятком використання (S)-(+)-N-Boc-3-піролідинолу замість (R)-(-)-N-Вос-3-піролідинолу на стадії (1-6) з одер 96045 30 жанням зазначеної в заголовку сполуки (310 мг, 51%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,62 (с, 1H), 8,02 (м, 1H), 7,28 (с, 1H), 7,10 (с, 1H), 7,07 (с, 1Н), 6,40 (м, 2Н), 5,71 (м, 1H), 5,15 (ушир.м, 1H), 4,08 (м, 1H), 3,99 (с, 3H), 3,86 (м, 3H), 2,32 (м, 2Н); + + MS (ESI ): m/z = 461,1 [М+Н] . Приклад 21 Одержання N-(2-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)етил)акриламіду Повторюють методику прикладу 1 за винятком використання трет-бутил 2-гідроксіетилкарбамату замість (R)-(-)-N-Вос-3-піролідинолу на стадії (1-6) з одержанням зазначеної в заголовку сполуки (26 мг, 23%). 1 H-ЯМР (300 МГц, CDCI3+CD3OD) δ 9,12 (с, 1H), 8,49 (с, 1Н), 7,73 (с, 1H), 7,48 (с, 1Н), 7,21 (м, 1H), 6,47 (с, 2Н), 5,71 (м, 1H), 4,48 (с, 2Н), 4,15 (с, 3H), 3,78 (с, 2Н), 3,16 (с, 2Н). Приклад 22 Одержання (R)-1-(3-(7-метокси-4-(1фенілетиламіно)хіназолін-6-ілоксі)азетидин-1іл)проп-2-ен-1-ону Повторюють методику прикладу 17 за винятком використання (R)-1-фенілетанаміну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (10 мг, 17%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,55 (с, 1H), 7,44 (м, 2Н), 7,31 (м, 4Н), 7,10 (м, 1Н), 6,50 (м, 1H), 6,25 (м, 2Н), 5,71 (м, 2Н), 5,07 (м, 1Н), 4,57 (м, 2Н), 4,52 (м, 1Н), 4,17 (м, 1Н), 3,99 (с, 3H), 1,65 (д, 3H); MS + + (ESI ): m/z = 405,2 [М+Н] . Приклад 23 Одержання 1-(3-(4-(3-хлор-2-фторфеніламіно)7-метоксихіназолін-6-ілоксі)азетидин-1-іл) проп-2ен-1-ону Повторюють методику прикладу 17 за винятком використання 3-хлор-2-фтораніліну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (20 мг, 36%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,67 (с, 1Н), 8,09 (м, 1H), 7,35 (с, 1H), 7,28 (с, 1Н), 7,16 (м, 3H), 6,23 (м, 2Н), 5,68 (м, 1H), 5,13 (м, 1Н), 4,66 (м, 2Н), 4,47 (м, 1H), 4,24 (м, 1Н), 4,04 (с, 3H); + + MS (ESI ): m/z = 429,2 [М+Н] . Приклад 24 Одержання 1-(3-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 17 за винятком використання 3,4-дихлор-2-фтораніліну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (5 мг, 8%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,68 (с, 1Н), 8,15 (м, 1Н), 7,34 (м, 2Н), 7,12 (с, 1H), 6,28 (м, 2Н), 5,69 (м, 1H), 5,17 (м, 1H), 4,67 (м, 2Н), 4,51 (м, 1H), 4,26 (м, 1H), 4,03 (с, 3H); + + MS (ESI ): m/z = 463,1 [М+Н] . Приклад 25 Одержання 1-(3-(4-(3-хлор-4-фторфеніламіно)7-метоксихіназолін-6-ілоксі)азетидин-1-іл) проп-2ен-1-ону Повторюють методику прикладу 17 за винятком використання 3-хлор-4-фтораніліну замість 3 31 хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (50 мг, 44%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,44 (с, 1H), 7,94 (м, 1Н), 7,61 (м, 1H), 7,48 (с, 1H), 7,24 (м, 2Н), 6,29 (м, 2Н), 5,74 (м, 1Н), 5,22 (ушир.м, 1Н), 4,77 (м, 1H), 4,55 (м, 1Н), 4,38 (м, 1H), 4,09 (м, 1H), 4,00 (с, 3H); + + MS (ESI ): m/z = 429,2 [М+Н] . Приклад 26 Одержання 1-(3-(4-(3-хлорфеніламіно)-7метоксихіназолін-6-ілоксі)азетидин-1-іл)проп-2-ен1-ону Повторюють методику прикладу 17 за винятком використання 3-хлораніліну замість 3-хлор2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (90 мг, 40%). 1 H-ЯМР (300 МГц, ДМСО-d6) δ 9,51 (с, 1H), 8,55 (с, 1Н), 8,00 (с, 1Н), 7,79 (д, 1H), 7,59 (с, 1Н), 7,44 (т, 1Н), 7,29 (с, 1Н), 7,19 (д, 1Н), 6,40 (м, 1H), 6,15 (д, 1Н), 5,71 (д, 1H), 5,26 (с, 1H), 4,80 (т, 1H), 4,56 (с, 1H), 4,30 (д, 1Н), 3,97 (с, 3H). Приклад 27 Одержання 3-(6-(1-акрилоїлазетидин-3ілокси)-7-метоксихіназолін-4-іламіно) бензонітрилу Повторюють методику прикладу 17 за винятком використання 3-амінобензонітрилу замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (90 мг, 40%). 1 H-ЯМР (300 МГц, ДМСО-d6) δ 9,51 (с, 1H), 8,55 (с, 1Н), 8,00 (с, 1H), 7,79 (д, 1H), 7,59 (с, 1Н), 7,44 (т, 1Н), 7,29 (с, 1H), 7,19 (д, 1H), 6,40 (м, 1H), 6,15 (д, 1H), 5,71 (д, 1Н), 5,26 (с, 1H), 4,80 (т, 1H), 4,56 (с, 1Н), 4,30 (д, 1H), 3,97 (с, 3H). Приклад 28 Одержання (Е)-4-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-N-метил-4-оксобут-2-енаміду Повторюють методику прикладу 17 за винятком використання (Е)-4-(метиламіно)-4-оксобут-2еноїлхлориду замість акрилоїлхлориду з одержанням зазначеної в заголовку сполуки (100 мг, 39%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,64 (с, 1Н), 8,11 (с, 1H), 7,97 (м, 1H), 7,28 (с, 1Н), 7,20 (с, 1Н), 7,07 (м, 1Н), 6,12 (м, 2Н), 5,18 (м, 1Н), 4,61 (м, 2Н), 4,39 (м, 1H), 4,29 (м, 1Н), 4,03 (с, 3H), 2,84 (с, 3H); + + MS (ESI ): m/z = 504,2 [М+Н] . Приклад 29 Одержання 1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихінозолін-6ілоксі)азетидин-1-іл)-2-метилпроп-2-ен-1-ону Повторюють методику прикладу 17 за винятком використання 2-метилакрилоїлхлориду замість акрилоїлхлориду з одержанням зазначеної в заголовку сполуки (58 мг, 62%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,68 (с, 1H), 8,10 (м, 1Н), 7,71 (ушир.с, 1Н), 7,35 (с, 1H), 7,07 (м, 1H), 7,05 (с, 1Н), 6,44 (д, 1H), 5,37 (с, 1Н), 5,16 (м, 1H), 4,69 (м, 2Н), 4,45 (м, 1H), 4,25 (м, 1Н), 4,07 (с, 3H), 1,94 (с, 3H); + + MS (ESI ): m/z = 461,2 [М+Н] . Приклад 30 Одержання (Z)-метил 4-(3-(4-(3-хлор-2фторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-4-оксобут--2-еноату 96045 32 Повторюють методику прикладу 17 за винятком використання 3-хлор-2-фторфеніламіну замість 3-хлор-2,4-дифтораніліну і (Z)-метил-4-хлор4-оксобут-2-еноату замість акрилоїлхлориду з одержанням зазначеної в заголовку сполуки (150мг, 23%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,58 (с, 1H), 7,91 (м, 1Н), 7,32 (с, 1H), 7,19 (м, 1H), 6,26 (д, 1Н), 6,03 (д, 1H), 5,22 (м, 1H), 4,75 (м, 1Н), 4,48 (м, 1H), 4,31 (м, 1Н), 4,24 (м, 1Н), 3,99 (с, 3Н), 3,71 (с, 3Н); + + MS (ESI ): m/z = 487,2 [М+Н] . Приклад 31 Одержання N-(3-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-3-оксопро-1-ен-2-іл)ацетаміду Повторюють методику прикладу 17 за винятком використання 2-ацетамідоакрилоїлхлориду замість акрилоїлхлориду з одержанням зазначеної в заголовку сполуки (8 мг, 12%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,67 (с, 1H), 8,12 (м, 1H), 7,93 (с, 1Н), 7,71 (с, 1H), 7,33 (с, 1Н), 7,08 (м, 1Н), 7,04 (с, 1Н), 6,44 (с, 1Н), 5,15 (м, 1H), 5,08 (с, 1H), 4,81 (м, 1Н), 4,61 (м, 2Н), 4,35 (м, 1Н), 2,10 (с, 3H); + + MS (ESI ): m/z = 504,1 [М+Н] . Приклад 32 Одержання (Z)-3-хлор-1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 17 за винятком використання (Z)-3-хлоракрилоїлхлориду замість акрилоїлхлориду з одержанням зазначеної в заголовку сполуки (20 мг, 33%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,65 (с, 1Н), 8,06 (м, 1H), 7,70 (с, 1Н), 7,32 (с, 1Н), 7,05 (м, 2Н), 6,50 (д, 1Η), 6,15 (д, 1H), 5,18 (м, 1H), 4,72 (м, 1Н), 4,60 (м, 1H), 4,47 (м, 1H), 4,26 (м, 1H), 4,04 (с, 3H); + + MS (ESI ): m/z = 481,2 [М+Н] . Приклад 33 Одержання (Е)-3-хлор-1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 17 за винятком використання (Е)-3-хлоракрилоїлхлориду замість акрилоїлхлориду з одержанням зазначеної в заголовку сполуки (18 мг, 30%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,69 (с, 1H), 8,28 (м, 1H), 7,34 (с, 1Н), 7,22 (с, 1Н), 7,08 (м, 1H), 6,91 (с, 1Н), 6,32 (д, 1H), 5,17 (м, 1Н), 4,61 (м, 2Н), 4,48 (м, 1Н), 4,29 (м, 1H), 4,05 (с, 3H); + + MS (ESI ): m/z = 481,2 [М+Н] . Приклад 34 Одержання 1-(4-(4-(3-хлор-2-фторфеніламіно)7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання 3-хлор-2-фтораніліну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (7 мг, 23%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,69 (с, 1H), 8,36 (м, 1Н), 7,32 (с, 2Н), 7,16 (м, 2Н), 6,61 (м, 1H), 6,29 (м, 1Н), 5,71 (м, 1H), 4,72 (м, 1Н), 4,01 (с, 3H), 3,90 (м, 2Н), 3,72 (м, 1H), 3,57 (м, 1Н), 1,97 (м, 4Н); + + MS (ESI ): m/z = 457,2 [М+Н] . 33 Приклад 35 Одержання (R)-(4-(7-метокси-4-(1фенілетиламіно)хіназолін-6-ілокси)піперидин-1іп)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання (R)-1-фенілетанаміну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (11 мг, 30%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,52 (с, 1Н), 7,43 (м, 2Н), 7,35 (м, 3H), 7,27 (м, 1Н), 7,23 (с, 1Н), 6,59 (м, 1H), 6,28 (м, 1Н), 5,68 (м, 2Н), 4,62 (м, 1H), 3,95 (с, 3H), 3,86 (м, 2Н), 3,67 (м, 1Н), 3,50 (м, 1H), 1,83 (м, 4Н), 1,68 (д, 3H); + + MS (ESI ): m/z = 433,3 [М+Н] . Приклад 36 Одержання 1-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 3,4-дихлор-2-фтораніліну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (3 мг, 13%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,68 (с, 1H), 8,39 (т, 3H), 7,31 (м, 3H), 6,61 (м, 1Н), 6,29 (м, 1H), 5,72 (м, 1Н), 4,75 (м, 1H), 4,02 (с, 3H), 3,89 (м, 2Н), 3,60 (м, 2Н), 1,86 (м, 4Н); + + MS (ESI ): m/z = 491,2 [М+Н] . Приклад 37 Одержання 1-(4-(4-(3-етинілфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання 3-етинілбензоламіну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (64 мг, 30%). 1 H-ЯМР (300 МГц, ДМСО-d6) δ 7,90 (с, 1H), 7,75 (с, 1H), 6,96 (с, 1H), 6,93 (с, 1H), 6,80 (м, 1H), 6,57 (с, 1Η), 6,08 (м, 1Н), 5,65 (м, 1Н), 4,63 (м, 1Н), 4,29 (м, 2Н), 3,71 (с, 3H), 3,60 (с, 3H), 2,61 (м, 2Н), 1,94 (м, 2Н), 1,61 (м, 2Н). Приклад 38 Одержання 1-(4-(4-(4-хлор-2,5диметоксифеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 4-хлор-2,5диметоксибензоламіну замість 3-хлор-2,4дифтораніліну з одержанням зазначеної в заголовку сполуки (56 мг, 25%). 1 H-ЯМР (300 МГц, ДМСО-d6) δ 7,90 (с, 1H), 7,90 (с, 1Н), 7,75 (с, 1Н), 6,96 (с, 1H), 6,93 (с, 1H), 6,93 (с, 1H), 6,80 (м, 1H), 6,57 (с, 1H), 6,08 (м, 1Н), 5,65 (м, 1Н), 4,63 (м, 1H), 4,29 (м, 2Н), 3,93 (с, 3H), 3,71 (с, 3H), 3,60 (с, 3H), 2,60 (м, 2Н), 1,93 (м, 2Н), 1,61 (м, 2Н). Приклад 39 Одержання 1-(4-(4-(4-бром-3метилфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 4-бром-3-метилбензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (70 мг, 27%). 1 H-ЯМР (300 МГц, ДМСО-d6) δ 9,41 (с, 1H), 8,46 (с, 1Н), 7,95 (с, 1H), 7,65 (м, 3H), 7,21 (с, 1H), 96045 34 6,83 (м, 1H), 6,10 (м, 1H), 5,67 (м, 1H), 4,78 (м, 1H), 3,93 (с, 3H), 3,84 (м, 2Н), 3,52 (м, 2Н), 2,36 (с, 3H), 1,95 (м, 2Н), 1,69 (м, 2Н). Приклад 40 Одержання 1-(4-(4-(4-ізопропілфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання 4-ізопропілбензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (60 мг, 32%). 1 H-ЯМР (300 МГц, ДМСО-d6) δ 9,36 (с, 1Н), 8,39 (с, 1H), 7,94 (с, 1H), 7,62 (д, 2H), 7,24 (д, 2Н), 7,19 (с, 1Н), 6,82 (м, 1H), 6,10 (м, 1Н), 5,67 (м, 1H), 4,79 (м, 1Н), 3,92 (с, 3H), 3,82 (м, 2Н), 3,43 (м, 2Н), 3,42 (м, 2Н), 2,88 (м, 1Н), 1,98 (м, 2Н), 1,69 (м,2Н), 1,21 (д, 6Н). Приклад 41 Одержання 1-(4-(4-(м-толуїдино)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання м-толуїдину замість 3-хлор-2,4дифтораніліну з одержанням зазначеної в заголовку сполуки (70 мг, 33%). 1 H-ЯМР (300 МГц, ДМСО-d6) δ 8,42 (с, 1H), 8,18 (с, 1H), 7,94 (с, 1H), 7,57 (д, 1H), 7,52 (с, 1Н), 7,24 (т, 1Н), 6,92 (д, 1H), 6,81 (м, 1H), 6,07 (м, 1H), 5,65 (м, 1Н), 4,78 (м, 1H), 3,90 (с, 3H), 3,82 (м, 2Н), 3,47 (м, 2Н), 2,31 (с, 3H), 1,97 (м, 2Н), 1,67 (м, 2Н). Приклад 42 Одержання 1-(4-(4-(3-бромфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання 3-бромбензоламіну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (31 мг, 34%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,53 (с, 1H), 7,89 (с, 1Н), 7,69 (м, 1H), 7,14 (м, 2Н), 6,61 (м, 1H), 6,21 (м, 1Н), 5,67 (м, 1H), 4,83 (м, 1Н), 3,94 (с, 3H), 3,71 (м, 1H), 3,58 (м, 2Н), 1,98 (м, 2Н), 1,85 (м, 2Н). Приклад43 Одержання 1-(4-(4-(3-хлорфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання 3-хлорбензоламіну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (19 мг, 40%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,64 (с, 1Н), 7,81 (с, 1Н), 7,62 (м, 2Н), 7,29 (м, 2Н), 7,09 (м, 1H), 6,59 (м, 1Н), 6,28 (м, 1H), 5,71 (м, 1Н), 4,68 (м, 1H), 3,94 (с, 3H), 3,88 (м, 2Н), 3,48 (м, 2Н), 2,29 (м, 2Н), 1,94 (м, 2Н). Приклад 44 Одержання 1-(4-(4-(3,4-дихлорфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання 3,4-дихлорбензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (47 мг, 46%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,51 (с, 1Н), 7,92 (м, 2Н), 7,62 (м, 1H), 7,30 (м, 2Н), 6,62 (м, 1H), 6,28 35 (м, 1Н), 5,69 (м, 1Н), 4,98 (м, 1Н), 3,97 (с, 3H), 3,86 (м, 2Н), 3,58 (м, 2Н), 1,88 (м, 4Н). Приклад 45 Одержання 1-(4-(7-метокси-4-(2,3,4трифторфеніламіно)хіназолін-6-ілокси)піперидин1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 2,3,4-трифторбензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (3,2 мг, 3%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,70 (с, 1H), 8,46 (т, 1Η), 7,34 (м, 2Н), 7,22 (с, 1H), 6,63 (м, 1H), 6,27 (м, 1Н), 5,73 (м, 1H), 4,72 (м, 1Н), 4,02 (с, 3H), 3,89 (м, 2Н), 3,71 (м, 1Н), 3,58 (м, 1H), 2,01 (м, 2Н); + + MS (ESI ): m/z = 459,3 [М+Н] . Приклад 46 Одержання 1-(4-(4-(4-фтор-3метилфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 4-фтор-3-метилбензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (57 мг, 30%). 1 H-ЯМР (300 МГц, ДМСО-d6) δ 9,50 (с, 1H), 8,43 (с, 1Н), 7,95 (с, 1Н), 7,65 (д, 2Н), 7,22 (с, 1H), 7,17 (т, 1H), 6,85 (м, 1Н), 6,13 (м, 1Н), 5,69 (м, 1Н), 4,80 (м, 1Н), 3,94 (с, 3H), 3,84 (м, 2Н), 3,52 (м, 2Н), 3,32 (с, 3H), 2,28 (с, 3H), 1,94 (м, 2Н), 1,70 (м, 2Н). Приклад 47 Одержання 1-(4-(4-(3,4-диметилфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання 3,4-диметилбензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (55 мг, 24%). 1 H-ЯМР (300 МГц, ДМСО-d6) δ 9,29 (с, 1H), 8,39 (с, 1Н), 7,94 (с, 1H), 7,48 (м, 2Н), 7,18 (с, 1H), 7,12 (д, 1H), 6,82 (м, 1Н), 6,09 (м, 1H), 5,67 (м, 1Н), 4,78 (м, 1Н), 3,92 (с, 3H), 3,84 (м, 2Н), 3,49 (м, 2Н), 2,24 (с, 3H), 2,21 (с, 3H), 1,99 (м, 2Н), 1,68 (м, 2Н). Приклад 48 Одержання 1-(4-(7-метокси-4-(4феноксифеніламіно)хіназолін-6-ілокси)піперидин1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 4-феноксибензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (81 мг, 30%). 1 H-ЯМР (300 МГц, ДМСО-d6) δ 9,43 (с, 1H), 8,42 (с, 1Н), 7,94 (с, 1Н), 7,74 (д, 1H), 7,83 (т, 2Н), 7,20 (с, 1H), 7,05 (м, 5Н), 6,83 (м, 1Н), 6,10 (м, 1Н), 5,67 (м, 1Н), 4,79 (м, 2Н), 3,93 (с, 3H), 3,85 (м, 2Н), 3,46 (м, 2Н), 2,01 (м, 2Н), 1,69 (м, 2Н). Приклад 49 Одержання 1-(4-(4-(2,3-дигідро-1H-інден-5іламіно)-7-метоксихіназолін-6-ілокси)піперидин-1іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 2,3-дигідро-1H-інден-5-аміну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (63 мг, 25%). 1 H-ЯМР (300 МГц, ДМСО-D6) δ 9,32 (с, 1H), 8,40 (с, 1H), 7,94 (с, 1H), 7,62 (с, 1H), 7,44 (д, 1H), 7,21 (д, 1Н), 7,18 (с, 1Н), 6,82 (м, 1Н), 6,10 (д, 1Н), 96045 36 5,67 (д, 1Н), 4,78 (м, 1H), 3,92 (с, 3H), 3,84 (м, 2Н), 3,48 (м, 2Н), 2,86 (кв., 4Н), 1,99 (м, 4Н), 1,69 (м, 2Н). Приклад 50 Одержання 1-(4-(4-(3,5-дихлор-4гідроксифеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 4-аміно-2,6-дихлорфенолу замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (2,1 мг, 7%). 1 H-ЯМР (300 МГц, CDCI3) δ 9,05 (с, 1Н), 8,87 (с, 1Н), 8,66 (м, 1Н), 7,83 (с, 1Н), 7,36 (м, 1H), 6,82 (м, 1H), 6,24 (μ, 1Η), 5,61 (м, 1H), 4,79 (μ, 1Η), 3,99 (с, 3H), 3,52 (м, 4Н), 2,24 (м, 2Н), 1,93 (м, 2Η). Приклад 51 Одержання 1-(4-(4-(4-хлор-3гідроксифеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 5-аміно-2-хлорфенолу замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (8 мг, 15%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,87 (с, 1Н), 8,48 (с, 1Н), 7,57 (м, 1H), 7,37 (с, 1H), 7,17 (с, 1Н), 7,07 (м, 1H), 6,80 (м, 2Н), 6,09 (м, 1H), 5,71 (м, 1Н), 4,93 (с, 1Н), 4,00 (с, 3H), 3,69 (м, 2Н), 3,28 (м, 2Н), 2,04 (м, 2Н), 1,63 (м, 2Н). Приклад 52 Одержання 1-(4-(4-(2-хлор-4гідроксифеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 4-аміно-3-хлорфенолу замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (26 мг, 40%). 1 H-ЯМР (300 МГц, ДМСО-d6) δ 9,92 (с, 1Н), 9,33 (с, 1H), 8,31 (с, 1Н), 7,87 (м, 1H), 7,27 (д, 1Н), 6,96 (с, 1Н), 6,83 (м, 1Н), 6,80 (м, 2Н), 6,09 (м, 1Н), 5,71 (м, 1H), 4,74 (м, 1H), 3,92 (с, 3H), 3,46 (м, 2Н), 3,26 (м, 2Н), 2,02 (м, 2Н), 1,67 (м, 2Н). Приклад 53 Одержання 1-(4-(4-(4-хлор-2гідроксифеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 2-аміно-5-хлорфенолу замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (7,9 мг, 17%). 1 H-ЯМР (300 МГц, CD3OD) δ 8,35 (с, 1H), 7,87 (м, 1H), 7,46 (д, 1H), 7,23 (с, 1Н), 7,00 (м, 1H), 6,83 (м, 1Н), 6,81 (м, 1Н), 6,26 (м, 1Н), 5,77 (м, 1H), 5,71 (м, 1Н), 4,02 (с, 3H), 3,66 (м, 2Н), 3,39 (м, 2Н), 2,10 (м, 2Н), 1,90 (м, 2Н); + + MS (ESI ): m/z = 455,2 [М+Н] . Приклад 54 Одержання 1-(4-(4-(3-хлор-4-(3фторбензилокси)феніламіно)-7-метоксихіназолін6-ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 3-хлор-4-(3фторбензилокси)бензоламіну замість 3-хлор-2,4дифтораніліну з одержанням зазначеної в заголовку сполуки (75 мг, 27%). 37 1 H-ЯМР (300 МГц, ДМСО-d6) δ 8,39 (с, 1H), 7,81 (д, 1Н), 7,80 (с, 1Н), 7,03-7,68 (м, 7Н), 6,80 (м, 1H), 6,23 (м, 1H), 5,76 (м, 1H), 5,20 (с, 2Н), 4,82 (м, 1H), 3,99 (с, 3H), 3,96 (м, 2Н), 3,68 (м, 2Н), 2,04 (м, 2Н), 1,92 (м, 2Н). Приклад 55 Одержання 1-(4-(4-(3-хлор-4-(піридин-2ілметокси)феніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 3-хлор-4-(піридин-2ілметокси)бензоламіну замість 3-хлор-2,4дифтораніліну з одержанням зазначеної в заголовку сполуки (75 мг, 16%). 1 Н-ЯМР (300 МГц, ДМСО-d6) δ 8,56 (д, 1H), 8,40 (с, 1H), 7,90 (м, 2Н), 7,86 (д, 1Н), 7,80 (с, 1Н), 7,72 (д, 1H), 7,55 (м, 1Н), 7,40 (т, 1H), 7,15 (м, 2Н), 6,81 (м, 1H). 6,22 (м, 1H), 5,75 (м, 1H), 5,26 (с, 2Н), 4,84 (м, 1H), 3,99 (с, 3H), 3,92 (м, 2Н), 3,49 (м, 2Н), 2,03 (м, 2Н), 2,07 (м, 2Н), 1,91 (м, 2Н). Приклад 56 Одержання 3-(6-(1-акрилоїлпіперидин-4ілокси)-7-метоксихіназолін-4-іламіно)бензонітрилу Повторюють методику прикладу 19 за винятком використання 3-амінобензонітрилу замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (27 мг, 28%). 1 H-ЯМР (300 МГц, ДМСО-d6) δ 9,71 (с, 1H), 8,58 (с, 1Н), 8,40 (с, 1Н), 8,16 (м, 1Н), 8,01 (с, 1Н), 7,59 (м, 2Н), 7,29 (с, 1H), 6,88 (м, 1H), 6,12 (м, 1Н), 5,71 (м, 1H), 4,86 (м, 1Н), 3,98 (с, 3H), 3,90 (м, 2Н), 3,55 (м, 1H), 2,08 (м, 1H), 1,76 (м, 1Н); + + MS (ESI ): m/z = 430,3 [М+Н] . Приклад 57 Одержання 1-(4-(4-(3-хлор-4-фторфеніламіно)7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання 3-хлор-4-фтораніліну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (14 мг, 31%). 1 Н-ЯМР (300 МГц, ДМСО-d6) δ 8,60 (с, 1H), 8,42 (с, 1H), 8,22 (м, 1H), 8,12 (м, 1H), 7,29 (с, 1H), 7,22 (м, 1Н), 6,88 (м, 1H), 6,24 (м, 1Н), 5,72 (м, 1H), 4,81 (м, 1H), 3,81 (с, 3H), 3,65 (м, 2Н), 3,31 (м, 2Н), 1,95 (м, 1H); + + MS (ESI ): m/z = 457,2 [М+Н] . Приклад 58 Одержання 1-(4-(7-метокси-4-(3(трифторметил)феніламіно)хіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 3-(трифторметил)бензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (18 мг, 21%). 1 H-ЯМР (300 МГц, ДМСО-d6) δ 9,66 (с, 1H), 8,63 (м, 1H), 8,41 (м, 2Н), 8,02 (м, 1H), 7,46 (м, 1Н), 7,26 (м, 1H), 7,13 (м, 1H), 6,86 (м, 1Н), 6,12 (м, 2Н), 5,79 (м, 1H), 4,95 (м, 1H), 3,96 (с, 3H), 3,87 (м, 2Н), 3,53 (м, 2Н), 2,03 (м, 2Н), 1,21 (м, 2Н); + + MS (ESI ): m/z = 473,0 [М+Н] . Приклад 59 Одержання 1-(4-(4-(3-хлор-2метоксифеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону 96045 38 Повторюють методику прикладу 19 за винятком використання 3-хлор-2-метоксибензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (11 мг, 27%). 1 Н-ЯМР (300 МГц, ДМСО-d6) δ 8,91 (с, 1H), 8,53 (с, 1Н), 7,92 (с, 1Н), 7,58 (м, 2Н), 7,37 (м, 1H), 6,88 (м, 1Н), 6,21 (м, 1H), 5,82 (м, 1H), 4,90 (м, 1H), 3,99 (с, 3H), 3,73 (с, 3H), 3,82 (м, 2Н), 3,60 (м, 2Н), 2,11 (м, 2Н), 1,25 (м, 2Н); + + MS (ESI ): m/z = 469,3 [М+Н] . Приклад 60 Одержання 1-(4-(4-(4-хлор-3метилфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 4-хлор-3-метилбензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (13 мг, 10%). 1 Н-ЯМР (300 МГц, ДМСО-d6) δ 9,50 (с, 1H), 8,43 (с, 1Н), 7,95 (с, 1H), 7,65 (д, 2Н), 7,22 (с, 1Н), 7,17 (т, 1H), 6,85 (м, 1Н), 6,13 (м, 1Н), 5,69 (м, 1H), 4,80 (м, 1H), 3,94 (с, 3H), 3,84 (м, 2Н), 3,51 (м, 2Н), 3,32 (с, 3H), 2,28 (с, 3H), 1,96 (м, 2Н), 1,70 (м, 2Н); + + MS (ESI ): m/z = 453,3 [М+Н] . Приклад 61 Одержання 1-(4-(4-(4-бром-3-хлорфеніламіно)7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання 4-бром-3-хлорбензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (14 мг, 37%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,68 (с, 1H), 7,98 (с, 1H), 7,56 (м, 2Н), 7,39 (м, 1Н), 7,28 (м, 1Н), 6,62 (м, 1Н), 6,29 (м, 1H), 5,71 (м, 1Н), 4,67 (м, 1H), 3,99 (с, 3H), 3,82 (м, 2Н), 3,60 (м, 2Н), 2,11 (м, 2Н), 1,25 (м, 2Н); + + MS (ESI ): m/z = 517,2 [М+Н] . Приклад 62 Одержання 1-(4-(4-(4-бром-3фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 4-бром-3-фторбензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (22 мг, 41%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,69 (с, 1Н), 7,90 (м, 1H), 7,51 (м, 1Н), 7,36 (м, 1H), 7,28 (м, 2Н), 6,62 (м, 1H), 6,29 (м, 1H), 5,70 (м, 1H), 4,68 (м, 1Н), 3,99 (с, 3H), 3,82 (м, 2Н), 3,67 (м, 2Н), 2,01 (м, 4Н); + + MS (ESI ): m/z = 501,2 [М+Н] . Приклад 63 Одержання 1-(4-(4-(3-хлор-2метилфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 3-хлор-2-м етилбензол аміну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (15 мг, 14%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,59 (с, 1H), 7,43 (м, 1Н), 7,34 (м, 1Н), 7,28 (м, 1H), 7,26 (м, 1H), 7,19 (м, 1H), 6,61 (м, 1Н), 6,31 (м, 1Н), 5,69 (м, 1Н), 4,54 (м, 1Н), 4,00 (с, 3H), 3,87 (м, 2Н), 3,72 (м, 2Н), 2,34 (с, 3H), 1,93 (м, 4Н). 39 Приклад 64 Одержання 1-(4-(4-(3(диметиламіно)феніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання Ν',Ν'-диметилбензол-1,3-діаміну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (8 мг, 14%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,64 (с, 1H), 7,26 (м, 3H), 6,93 (м, 1H), 6,99 (м, 1H), 6,59 (м, 1Н), 6,55 (м, 1Н), 6,31 (м, 1Н), 5,68 (м, 1Н), 4,58 (м, 1Н), 3,98 (с, 3H), 3,87 (м, 2Н), 3,48 (м, 2Н), 2,96 (с, 6Н), 1,32 (м, 4Н). Приклад 65 Одержання 1-(4-(4-(2-фтор-3(трифторметил)феніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 2-фтор-3(трифторметил)бензоламіну замість 3-хлор-2,4дифтораніліну з одержанням зазначеної в заголовку сполуки (29 мг, 23%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,87 (с, 1H), 8,63 (с, 1Н), 7,87 (с, 1H), 7,50 (м, 2Н), 7,43 (м, 1H), 6,85 (м, 1H), 6,26 (м, 1Н), 5,82 (м, 1Н), 4,90 (м, 1H), 3,99 (с, 3H), 3,82 (м, 2Н), 3,60 (м, 2Н), 2,11 (м, 2Н), 1,25 (м, 2Н). Приклад 66 Одержання 5-(6-(1-акрилоїлпіперидин-4ілокси)-7-метоксихіназолін-4-іламіно)-2фторбензонітрилу Повторюють методику прикладу 19 за винятком використання 5-аміно-2-фторбензонітрилу замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (28 мг, 28%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,69 (с, 1Н), 8,65 (с, 1Н), 8,18 (м, 1H), 8,07 (м, 1H), 7,29 (с, 1H), 7,21 (т, 1H), 6,61 (м, 1H), 6,20 (м, 1Н), 5,68 (м, 1H), 4,71 (м, 1Н), 3,92 (с, 3H), 3,71 (м, 2Н), 3,48 (м, 2Н), 1,19 (м, 4Н); + + MS (ESI ): m/z = 448,3 [М+Н] . Приклад 67 Одержання 5-(6-(1-акрилоїлпіперидин-4ілокси)-7-метоксихіназолін-4-іламіно)-2хлорбензонітрилу Повторюють методику прикладу 19 за винятком використання 5-аміно-2-хлорбензонітрилу замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (14 мг, 21%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,78 (с, 1Н), 8,64 (с, 1Н), 8,16 (м, 1Н), 8,01 (м, 1Н), 7,32 (с, 1H), 7,21 (т, 1Η), 6,61 (м, 1Н), 6,21 (м, 1Н), 5,66 (м, 1H), 4,71 (м, 1H), 3,96 (с, 3H), 3,71 (м, 2Н), 3,48 (м, 2Н), 1,19 (м, 4Н); + + MS (ESI ): m/z = 464,3 [М+Н] . Приклад 68 Одержання 1-(4-(7-метокси-4-(3(метилтіо)феніламіно)хіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 3-(метилтіо)бензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (35 мг, 15%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,66 (с, 1Н), 8,62 (с, 1Н), 7,40 (м, 2Н), 7,28 (м, 2Н), 7,05 (м, 1H), 6,62 96045 40 (м, 1H), 6,26 (м, 1H), 5,72 (м, 1H), 4,67 (м, 1H), 3,99 (с, 3H), 3,90 (м, 2Н), 3,54 (м, 2Н), 1,94 (м, 4Н). Приклад 69 Одержання 1-(4-(4-(2-хлорфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання 2-хлорбензоламіну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (93 мг, 19%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,72 (с, 1Н), 7,72 (м, 1H), 7,26 (м, 5Н), 6,63 (м, 1H), 6,27 (м, 1H), 5,72 (м, 1H), 4,93 (м, 1Н), 3,95 (с, 3H), 3,73 (м, 2Н), 3,57 (м, 2Н), 1,25 (м,4Н). Приклад 70 Одержання 1-(4-(4-(4-хлорфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання 4-хлорбензоламіну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (40 мг, 27%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,65 (с, 1Н), 8,00 (с, 1Н), 7,67 (д, 2Н), 7,36 (с, 1H), 7,33 (д, 2Н), 6,61 (м, 1Н), 6,23 (м, 1H), 5,68 (м, 1Н), 4,64 (м, 1H), 3,97 (с, 3H), 3,76 (м, 2Н), 3,65 (м, 2Н), 1,70 (м, 4Н). Приклад 71 Одержання 1-(4-(4-(3-хлор-2,4дифторфеніламіно)хіназолін-6-ілокси)піперидин-1іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 2-аміно-5-метоксибензойної кислоти замість 4,5-диметоксіантранілової кислоти з одержанням зазначеної в заголовку сполуки (10 мг, 10%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,71 (с, 1Н), 8,448,42 (с, 1Н), 7,92 (д, 1H), 7,54-7,50 (м, 1H), 7,21 (м, 1Н), 7,11-7,06 (м, 1H), 6,64 (дд, 1H), 5,74 (д, 1H), 4,77 (м, 1Н), 3,84-3,63 (м, 4Н), 2,04-1,91 (м, 4Н). Приклад 72 Одержання 1-(4-(4-(3-хлорбензиламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання (3-хлорфеніл)метанаміну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (8 мг, 29%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,58 (с, 1Н), 8,40 (с, 1Н), 8,16 (м, 1H), 8,01 (с, 1Н), 7,59 (м, 2Н), 7,29 (с, 1H), 6,59 (м, 1H), 6,28 (м, 1H), 5,68 (м, 2Н), 4,62 (м, 1H), 3,95 (с, 3H), 3,86 (м, 2Н), 3,67 (м, 2Н), 3,50 (м, 2Н), 1,83 (м, 4Н). Приклад 73 Одержання 1-(4-(7-метокси-4-(3вінілфеніламіно)хіназолін-6-ілокси)піперидин-1іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 3-вінілбензоламіну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (25 мг, 28%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,65 (с, 1H), 7,67 (с, 1Н), 7,60 (д, 1H), 7,48 (м, 1H) 7,32 (т, 3H), 7,19 (д, 1H), 6,64 (м, 2Н), 6,27 (д, 1H), 5,70 (т, 2Η), 5,26 (д, 1H), 4,56 (с, 1H), 3,99 (с, 3H), 3,85 (с, 2Н), 3,62 (с, 1Н), 3,48 (с, 1Н). 41 Приклад 74 Одержання 1-(4-(7-метокси-4-(3нітрофеніламіно)хіназолін-6-ілокси)піперидин-1іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 3-нітробензоламіну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (35 мг, 89%). 1 Н-ЯМР (300 МГц, ДМСО-d6) δ 9,84 (ушир.с, 1Н), 8,82 (с, 1H), 8,55 (с, 1Н), 8,37 (д, 1H), 8,03 (с, 1Н), 7,92 (д, 1H), 7,66 (т, 1H), 7,25 (с, 1H), 6,87-6,78 (м, 1Н), 6,13-6,07 (м, 1Н), 5,68-5,64 (м, 1H), 4,854,82 (м, 1H), 3,94 (с, 3H), 3,88-3,85 (м, 2Н), 3,51 (м, 2Н), 2,01 (м, 2Н), 1,71 (м, 2Н). Приклад 75 Одержання N-(3-(6-(1-акрилоїлпіперидин-4ілокси)-7-метоксихіназолін-4-іламіно) феніл) акриламіду 0,12 г заліза суспендують в 5 мл 50% етанолу. До суспензії додають 0,01 мл розчину хлористоводневої кислоти концентрації 35% і одержану суміш нагрівають для активування до 100°С. Додають 0,2 г сполуки, одержаної в прикладі 74, і одержану суміш кип'ятять зі зворотним холодильником. Після завершення реакції гарячий реакційний розчин фільтрують через шар целіту при зниженому тиску. Фільтрат переганяють при зниженому тиску та сушать. Одержаний залишок розчиняють в 10 мл 50% тетрагідрофурану і до одержаного розчину в зазначеному порядку додають 75 мг бікарбонату натрію і 0,05 мл акрилоїлхлориду і 30 хвилин перемішують при кімнатній температурі. Після завершення реакції до реакційної суміші додають насичений розчин бікарбонату натрію і реакційну суміш тричі екстрагують хлороформом. Одержаний у такий спосіб органічний шар промивають водою і насиченим розчином бікарбонату натрію, сушать над безводним сульфатом натрію, фільтрують і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (хлороформ:метанол = 30:1) з одержанням зазначеної в заголовку сполуки (10 мг, 21%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,62-8,54 (м, 2Н), 8,37 (ушир.с, 1H), 7,96 (с, 1H), 7,66 (с, 1Н), 7,39 (д, 1H), 7,23-7,18 (м, 3H), 6,61-6,52 (м, 1Н), 6,38-6,19 (м, 2Н), 5,69-5,65 (м, 2Н), 4,61 (с, 1Η), 3,91 (с, 3H), 3,80-3,78 (м, 2Н), 3,54-3,43 (м, 2Н), 2,05-1,85 (м, 4Н). Приклад 76 Одержання 1-(4-(4-(3-меркаптофеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону Повторюють методику прикладу 19 за винятком використання 3-амінобензотіолу замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (11 мг, 37%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,67 (с, 1H), 7,87 (м, 3H), 7,48 (с, 1H), 7,35 (м, 3H), 6,62 (м, 1H), 6,30 (д, 1Н), 5,71 (д, 1Н), 4,66 (с, 1H), 3,99 (с, 3H), 3,90 (с, 4Н), 3,65 (д, 4Н). Приклад 77 Одержання 1-(4-(4-(3-(хлорметил)феніламіно)7-метоксихіназолін-6-ілокси)піперидин-1-іл)проп-2ен-1-ону 96045 42 Повторюють методику прикладу 19 за винятком використання 3-(хлорметил)бензоламіну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (17 мг, 29%). 1 Н-ЯМP (300 МГц, CDCI3) δ 8,68 (с, 1Н), 7,71 (м, 1Н), 7,59 (с, 1H), 7,24 (м, 1H), 7,22 (м, 3H), 6,66 (м, 1Н), 6,32 (м, 1H), 5,69 (м, 1Н), 4,65 (м, 1H), 4,55 (м, 2Н), 3,91 (с, 3H), 3,78 (с, 2Н), 3,60 (м, 2Н), 1,96 (м, 4Н). Приклад 78 Одержання 1-(4-(4-(3-хлор-4гідроксифеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 4-аміно-2-хлорфенолу замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (109 мг, 28%). + + MS (ESI ): m/z = 455,3 [М+Н] . Приклад 79 Одержання 1-(4-(4-(3-фтор-4гідроксифеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 4-аміно-2-фторфенолу замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (373 мг, 67%). + + MS (ESI ): m/z = 439,2 [М+Н] . Приклад 80 Одержання 1-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)бут-2-ин-1-ону Повторюють методику прикладу 19 за винятком використання бут-2-іноїлхлориду замість акрилоїлхлориду з одержанням зазначеної в заголовку сполуки (38 мг, 33%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,34 (с, 1H), 7,78 (с, 1Н), 7,52 (м, 1Н), 7,17 (м, 2Н), 4,80 (м, 1H), 4,03 (м, 1Н), 3,99 (с, 3H), 3,83 (м, 2Н), 3,64 (м, 1Н), 2,02 (с, 3H), 2,00 (м, 4Н); + + MS (ESI ): m/z = 487,3 [М+Н] . Приклад 81 Одержання 1-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-3-метилбут-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання 2-метилакрилоїлхлориду замість акрилоїлхлориду з одержанням зазначеної в заголовку сполуки (86 мг, 36%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,67 (с, 1Н), 8,08 (с, 1Н), 7,55 (м, 1H), 7,31 (с, 1Н), 7,24 (м, 1H), 5,90 (м, 1H), 4,94 (м, 1H), 4,08 (с, 3H), 3,92 (м, 2Н), 3,58 (м, 2Н), 2,09 (м, 2Н), 1,85 (с, 3H), 1,84 (м, 2Н), 1,73 (с, 3H); + + MS (ESI ): m/z = 503,3 [М+Н] . Приклад 82 Одержання (Е)-4-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл-N-метил-4-оксобут-2-енаміду Повторюють методику прикладу 19 за винятком використання (Е)-4-(метиламіно)-4-оксобут-2еноїлхлориду замість акрилоїлхлориду з одержанням зазначеної в заголовку сполуки (60 мг, 24%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,65 (с, 1H), 8,19 (м, 1H), 7,54 (с, 1Н), 7,31 (с, 1H), 7,30 (с, 1H), 7,07 43 (м, 1H), 6,39 (д, 1H), 6,09 (д, 1H), 4,70 (м, 1Н), 4,00 (с, 3H), 3,79 (м, 3H), 3,50 (м, 1H), 2,85 (д, 3H); + + MS (ESI ): m/z = 532,3 [М+Н] . Приклад 83 Одержання (Z)-Метил 4-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-оксобут-2-еноату Повторюють методику прикладу 19 за винятком використання (Z)-Метил-4-хлор-4-оксобут-2еноату замість акрилоїлхлориду з одержанням зазначеної в заголовку сполуки (23 мг, 9%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,66 (с, 1H), 8,24 (м, 1H), 7,40 (ушир.с, 1H), 7,30 (м, 2Н), 7,06 (м, 1H), 6,58 (д, 1Н), 6,03 (д, 1H), 4,71 (м, 1Н), 4,01 (с, 3H), 3,90 (м, 1H), 3,83 (м, 1Н), 3,75 (с, 3H), 3,70 (м, 1H), 3,44 (м, 1H), 2,02 (м, 4Н); + + MS (ESI ): m/z = 533,3 [М+Н] . Приклад 84 Одержання (Z)-Метил 4-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-оксобут-2-еноату Повторюють методику прикладу 19 за винятком використання 3,4-дихлор-2-фтораніліну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (9 мг, 7%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,70 (с, 1H), 8,44 (т, 1Η), 7,42 (м, 2Н), 7,23 (с, 1Н), 6,58 (д, 1Н), 6,04 (д, 1Н), 4,73 (ушир.м, 1Н), 4,01 (с, 3H), 3,89 (м, 2Н), 3,76 (с, 3H), 3,71 (м, 1H), 3,43 (м, 1H), 2,01 (м, 4Н); + + MS (ESI ): m/z = 549,3 [М+Н] . Приклад 85 Одержання (Z)-4-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-оксобут-2-енової кислоти 0,1 г сполуки, одержаної в прикладі 83, розводять 2 мл тетрагідрофурану і при 0°С додають туди 0,1 мл 3М розчину гідроксиду літію. Одержану суміш дві години перемішують при кімнатній температурі та екстрагують хлороформом. Водний шар підкисляють 1н НСІ і тричі екстрагують хлороформом. Органічний шар сушать над безводним сульфатом натрію, фільтрують і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (метиленхлорид:метанол = 5:1) з одержанням зазначеної в заголовку сполуки (118мг, 48%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,48 (с, 1Н), 7,80 (м, 2Н), 7,22 (с, 1Н), 7,09 (т, 1Η), 6,33 (д, 1H), 6,10 (д, 1H), 4,99 (м, 1H), 4,00 (с, 3H), 3,70 (м, 4Н), 1,90 (м, 4Н); + + MS (ESI ): m/z = 519,2 [М+Н] . Приклад 86 Одержання (Z))-4-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-оксобут-2-енової кислоти Повторюють методику прикладу 85 за винятком використання 3,4-дихлор-2-фтораніліну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (100 мг, 41%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,48 (с, 1H), 7,68 (т, 1Н), 7,21 (м, 1Н), 7,20 (с, 1Н), 6,33 (д, 1Н), 5,01 (д, 1H), 4,69 (ушир.м, 1H), 3,95 (с, 3H), 3,66 (м, 3H), 3,35 (м, 1Н), 1,87 (м, 4Н); + + MS (ESI ): m/z = 535,2 [М+Н] . 96045 44 Приклад 87 Одержання (Е)-4-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-оксобут-2-енової кислоти Повторюють методику прикладу 86 за винятком використання (Е)-метил-4-хлор-4-оксобут-2еноату замість (Z)-метил-4-хлор-4-оксобут-2еноату з одержанням зазначеної в заголовку сполуки (10 мг, 20%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,49 (с, 1H), 7,74 (т, 1Н), 7,56 (с, 1H), 7,31 (м, 2Н), 7,23 (с, 1H), 6,65 (д, 1Н), 4,68 (ушир.м, 1Н), 3,95 (с, 3H), 3,79 (м, 2Н), 3,66 (м, 1Н), 3,49 (м, 1H), 1,90 (м, 4Н); + + MS (ESI ): m/z = 535,2 [М+Н] . Приклад 88 Одержання (Е)-4-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-N-гідрокси-4-оксобут-2енаміду 0,1 г (Е)-4-(4-(4-(3-хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6-ілокси)піперидин-1-іл)-4оксобут-2-енової кислоти, одержаної повторенням методики прикладу 87, за винятком використання 3-хлор-2,4-дифтораніліну замість 3,4-дихлор-2фтораніліну, розводять 1 мл тетрагідрофурану і при -15°С додають туди 0,03 мл Nметилморфоліну і 0,03 мл ізобутилхлорформіату. Одержану суміш перемішують 30 хвилин і додають до неї 0,03 мл гідроксил аміну. Одержаний розчин нагрівають при кімнатній температурі і витримують дві години. Після завершення реакції додають воду та одержаний розчин тричі екстрагують етилацетатом. Органічний шар сушать над безводним сульфатом натрію, фільтрують і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (етилацетат:метиленхлорид:метанол = 7:7:1) з одержанням зазначеної в заголовку сполуки (30 мг, 30%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,33 (с, 1H), 7,80 (с, 1Н), 7,49 (м, 1Н), 7,44 (д, 1Н), 7,22 (с, 1Н), 7,19 (м, 1H), 6,77 (д, 1Н), 4,00 (с, 3H), 3,94 (м, 1Н), 3,70 (м, 2Н), 3,06 (м, 2Н), 2,08 (м, 2Н), 1,89 (м, 2Н); + + MS (ESI ): m/z = 534,2 [М+Н] . Приклад 89 Одержання (Z)-3-хлор-1-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання (Z)-3-хлор-акрилоїлхлориду замість акрилоїлхлориду з одержанням зазначеної в заголовку сполуки (5 мг, 8%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,71 (с, 1H), 8,40 (т, 1H), 7,51 (ушир.с, 1H), 7,33 (м, 3H), 6,42 (д, 1Н), 6,36 (д, 1H), 4,73 (ушир.м, 1H), 4,03 (с, 3H), 3,93 (м, 1Н), 3,81 (м, 2Н), 3,53 (м, 1Н), 2,03 (м, 4Н); + + MS (ESI ): m/z = 525,1 [М+Н] . Приклад 90 Одержання (Е)-3-хлор-1-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 19 за винятком використання (Е)-3-хлор-акрилоїлхлориду замість акрилоїлхлориду з одержанням зазначеної в заголовку сполуки (8 мг, 13%). 45 1 Н-ЯМР (300 МГц, CDCI3) δ 8,70 (с, 1H), 8,46 (т, 1H), 7,34 (м, 4Н), 7,23 (с, 1Н), 6,74 (д, 1Н), 4,72 (ушир.м, 1H), 4,01 (с, 3H), 3,82 (м, 3H), 3,55 (м, 1Н), 1,99 (м, 4Н); + + MS (ESI ): m/z = 525,1 [М+Н] . Приклад 91 Одержання N-(3-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-3-оксопроп-1-ен-2іл)ацетаміду Повторюють методику прикладу 19 за винятком використання 2-ацетамідоакрилоїлхлориду замість акрилоїлхлориду з одержанням зазначеної в заголовку сполуки (7 мг, 3%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,66 (с, 1H), 8,22 (м, 1H), 7,80 (с, 1Н), 7,33 (м, 3H), 5,66 (с, 1Н), 4,84 (с, 1Н), 4,69 (ушир.м, 1H), 4,00 (с, 3H), 3,90 (м, 2Н), 3,69 (м, 2Н), 2,07 (с, 3H), 1,97 (м, 4Н); + + MS (ESI ): m/z = 548,3 [М+Н] . Приклад 92 Одержання (Е)-1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)-4-(диметиламіно)бут-2-ен-1ону Стадія 1) (Е)-4-бром-1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)бут-2-ен-1-он Повторюють методику прикладу 1 за винятком використання (Е)-4-бромбут-2-еноїлхлориду замість акрилоїлхлориду на стадії 7) з одержанням зазначеної в заголовку сполуки (75 мг, 58%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,63 (с, 1Н), 8,09 (м, 1Н), 7,53 (с, 1H), 7,38 (с, 1Н), 7,18 (с, 1H), 6,91 (м, 2Н), 5,20 (ушир.м, 1H), 4,08 (м, 2Н), 3,92 (с, 3H), 3,72 (м, 4Н), 2,28 (м, 2Н). Стадія 2) (Е)-1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6їлокси)піролідин-1-іл)-4-(диметиламіно)бут-2-ен-1он 580 мг сполуки, одержаної на стадії 1), розчиняють в 10 мл тетрагідрофурану при 0°С і додають туди 5 мл 1,0 Μ розчину диметиламіну в тетрагідрофурані. Одержану суміш перемішують при кімнатній температурі одну годину, додають у неї насичений розчин бікарбонату натрію та одержану суміш екстрагують хлороформом. Органічний шар сушать над безводним сульфатом натрію, фільтрують і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (хлороформ:метанол = 30:1) з одержанням зазначеної в заголовку сполуки (175 мг, 32%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,56 (с, 1H), 7,84 (м, 1Н), 7,40 (с, 1H), 7,17 (с, 1Н), 7,01 (т, 1Н), 6,85 (м, 1Н), 6,24 (м, 1H), 5,12 (ушир.м, 1H), 4,03 (с, 1H), 3,95 (с, 3H), 3,75 (м, 4Н), 3,03 (м, 2Н), 2,32 (м, 2Н), 2,22 (с, 6Н); + + MS (ESI ): m/z = 518,3 [М+Н] . Приклад 93 Одержання (Е)-1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)-4-(діетиламіно)бут-2-ен-1ону Повторюють методику прикладу 92 за винятком використання діетиламіну замість 1,0 Μ роз 96045 46 чину диметиламіну в тетрагідрофурані з одержанням зазначеної в заголовку сполуки (4 мг, 16%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,60 (с, 1H), 8,02 (м, 1H), 7,30 (с, 1H), 7,22 (с, 1Н), 7,05 (т, 1H), 6,93 (м, 1H), 6,29 (м, 1Н), 5,11 (ушир.м, 1H), 4,03 (с, 1Н), 3,98 (с, 3H), 3,82 (м, 4Н), 3,23 (д, 2Н), 2,52 (кв., 4Н), 1,01 (м, 6Н); + + MS (ESI ): m/z = 546,2 [М+Н] . Приклад 94 Одержання (Е)-1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)-1-ону Повторюють методику прикладу 92 за винятком використання морфоліну замість 1,0 Μ розчину диметиламіну в тетрагідрофурані з одержанням зазначеної в заголовку сполуки (8 мг, 26%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,61 (с, 1H), 8,05 (м, 1Н), 7,31 (с, 1Н), 7,22 (с, 1Н), 7,06 (т, 1H), 6,91 (μ, 1H), 6,29 (м, 1H), 5,12 (ушир.м, 1Н), 4,06 (с, 1H), 3,97 (с, 3H), 3,84 (м, 4Н), 3,70 (м, 4Н), 3,10 (д, 2Н), 2,44 (м, 4Н), 2,26 (м, 2Н); + + MS (ESI ): m/z = 560,2 [М+Н] . Приклад 95 Одержання (Е)-1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)-4-(піролідин-1-іл)проп-2-ен1-ону Повторюють методику прикладу 92 за винятком використання піролідина замість 1,0 Μ розчину диметиламіну в тетрагідрофурані з одержанням зазначеної в заголовку сполуки (5 мг, 18%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,61 (с, 1H), 8,02 (м, 1H), 7,28 (с, 1H), 7,22 (с, 1H), 7,05 (т, 1Н), 6,95 (м, 1H), 6,27 (м, 1Н), 5,11 (ушир.м, 1Н), 4,04 (с, 1H), 3,98 (с, 3H), 3,87 (м, 4Н), 3,23 (д, 2Н), 2,50 (м, 4Н), 2,27 (м, 2Н), 1,78 (м, 4Н); + + MS (ESI ): m/z = 544,2 [М+Н] . Приклад 96 Одержання (Е)-1-((3S)-3-(4-(3-хлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піролідин-1-іл)-4-(диметиламіно)бут-2-ен-1ону Повторюють методику прикладу 92 за винятком використання 3-хлор-2-фтораніліну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (2 мг, 5%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,70 (с, 1H), 8,38 (м, 1Н), 7,31 (с, 1H), 7,18 (м, 2Н), 6,97 (м, 1H), 6,95 (м, 1Н), 6,33 (м, 1H), 5,07 (ушир.м, 1Н), 4,00 (с, 3H), 3,82 (м, 4Н), 3,13 (м, 2Н), 2,32 (м, 2Н), 2,29 (с, 6Н); + + MS (ESI ): m/z = 500,35 [М+Н] . Приклад 97 Одержання (Е)-1-((3S)-3-(4-(3-хлор-2,4дифторфеніламіно)хіназолін-6-ілокси)піролідин-1іл)-4-(диметиламіно)бут-2-ен-1-ону Повторюють методику прикладу 92 за винятком використання 2-аміно-5-метоксибензойної кислоти замість 4,5-диметоксіантранілової кислоти з одержанням зазначеної в заголовку сполуки (26 мг, 39%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,59 (с, 1Н), 7,88 (м, 1H), 7,80 (м, 1H), 7,57 (м, 1H), 7,39 (м, 1Н), 7,02 (м, 1Н), 6,85 (м, 1H), 6,26 (м, 1Н), 5,08 (ушир.м, 1H), 3,85 (м, 4Н), 3,00 (д, 2Н), 2,43 (м, 2Н), 2,21 (с, 6Н); 47 + 96045 + MS (ESI ): m/z = 488,2 [М+Н] . Приклад 98 Одержання (Е)-1-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-(диметиламіно)бут-2-ен-1ону Повторюють методику прикладу 92 за винятком використання N-Boc-4-гідроксипіперидину замість (R)-(-)-N-Вос-3-піролідинолу з одержанням зазначеної в заголовку сполуки (50 мг, 16%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,66 (с, 1H), 8,28 (м, 1H), 7,31 (м, 2Н), 7,06 (м, 1H), 6,85 (м, 1H), 6,50 (м, 1H), 4,71 (ушир.м, 1Н), 4,02 (с, 3H), 3,89 (м, 2Н), 3,71 (м, 1Н), 3,60 (м, 1H), 3,12 (д, 2Н), 2,30 (с, 6Н), 2,00 (м, 4Н); + + MS (ESI ): m/z = 532,2 [М+Н] . Приклад 99 Одержання (Е)-1-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-(диметиламіно)бут-2-ен-1ону Повторюють методику прикладу 98 за винятком використання 3,4-дихлор-2-фтораніліну замість 3-хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (20 мг, 16%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,65 (с, 1H), 8,22 (т, 1H), 7,45 (с, 1Н), 7,30 (д, 1Н), 7,29 (с, 1Н), 6,83 (м, 1H), 6,54 (д, 1Н), 4,71 (ушир.м, 1Н), 3,99 (с, 3H), 3,85 (м, 2Н), 3,50 (м, 2Н), 3,16 (д, 2Н), 2,33 (с, 6Н), 1,98 (м, 4Н); + + MS (ESI ): m/z = 548,2 [М+Н] . Приклад 100 Одержання (Е)-1-(4-(4-(3-хлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-(диметиламіно)бут-2-ен-1ону Повторюють методику прикладу 98 за винятком використання 3-хлор-2-фтораніліну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (50 мг, 27%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,63 (с, 1H), 8,09 (т, 1H), 7,51 (с, 1Н), 7,27 (с, 1H), 7,13 (м, 2Н), 6,79 (м, 1H), 6,44 (д, 1H), 4,66 (ушир.м, 1Η), 3,96 (с, 3H), 3,84 (м, 2Н), 3,50 (м, 2Н), 3,05 (м, 2Н), 2,24 (с, 6Н), 1,93 (м, 4Н); + + MS (ESI ): m/z = 514,2 [М+Н] . Приклад 101 Одержання (Е)-1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-4-(диметиламіно)бут-2-ен-1ону Повторюють методику прикладу 92 за винятком використання N-Boc-3-гідроксіазетидину замість (R)-(-)-N-Вос-3-піролідинолу з одержанням зазначеної в заголовку сполуки (60 мг, 47%). 1 Н-ЯМР (300 МГц, CD3OD) δ 8,33 (с, 1Н), 7,53 (м, 1H), 7,37 (с, 1Н), 7,17 (м, 2Н), 6,79 (м, 1Н), 6,20 (м, 1H), 5,18 (ушир.м, 1H), 4,79 (м, 1H), 4,56 (м, 1H), 4,42 (м, 1H), 4,14 (м, 1Н), 3,99 (с, 3H), 3,12 (м, 2Н), 2,45 (с, 6Н); + + MS (ESI ): m/z = 504,3 [М+Н] . Приклад 102 Одержання (Е)-1-(3-(4-(3-хлор-2фторфеніламіно)-7-метоксихіназолін-6 48 ілоксі)азетидин-1-іл)-4-(диметиламіно)бут-2-ен-1ону Повторюють методику прикладу 101 за винятком використання 3-хлор-2-фтораніліну замість 3хлор-2,4-дифтораніліну з одержанням зазначеної в заголовку сполуки (20 мг, 21%). 1 Н-ЯМР (300 МГц, CD3OD) δ 8,36 (с, 1Н), 7,54 (т, 1H), 7,44 (с, 1H), 7,37 (м, 1Н), 7,20 (м, 2Н), 6,80 (м, 1Η), 6,23 (м, 1Н), 5,22 (ушир.м, 1H), 4,82 (м, 1H), 4,55 (м, 1H), 4,40 (м, 1H), 4,15 (м, 1Н), 4,01 (с, 3H), 3,20 (м, 2Н), 2,31 (с, 6Н); + + MS (ESI ): m/z = 486,3 [М+Н] . Приклад 103 Одержання (Е)-N-(2-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)етил)-4-(диметиламіно)бут-2-енаміду Повторюють методику прикладу 92 за винятком використання трет-бутил 2гідроксіетилкарбамату замість (R)-(-)-N-Вос-3піролідинолу з одержанням зазначеної в заголовку сполуки (46 мг, 34%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,73 (с, 1Н), 7,99 (с, 1H), 7,26 (с, 1Н), 7,19 (с, 1H), 7,01 (м, 1H), 6,81 (м, 1Н), 6,68 (м, 1H), 6,03 (д, 1Н), 4,25 (с, 2Н), 3,96 (с, 3H), 3,75 (с, 2Н), 2,93 (с, 2Н), 2,25 (с, 6Н). Приклад 104 Одержання 1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-2((диметиламіно)метил)проп-2-ен-1-ону Стадія 1) 2-((диметиламіно)метил)акрилова кислота 1 г малонової кислоти і 0,63 г параформальдегіду розводять 10 мл 1,3-діоксану і додають туди 4,8 мл 2,0 Μ розчину диметиламіну в тетрагідрофурані. Одержану суміш 1 годину перемішують при 70°С. Після припинення реакції одержаний розчин переганяють при зниженому тиску. Одержаний залишок кристалізують ацетоном і фильтуют при зниженому тиску з одержанням зазначеної в заголовку сполуки (0,4 г, 32%) у вигляді білих кристалів. 1 Н-ЯМР (300 МГц, D2O) δ 6,62 (с, 1Н), 6,11 (с, 1Н), 4,16 (с, 2Н), 2,88 (с, 6Н); + + MS (ESI ): m/z =130,0 [М+Н] . Стадія 2) 1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-2((диметиламіно)метил)проп-2-ен-1-он 50 мг 6-(азетидин-3-ілокси)-N-(3-хлор-2,4дифторфеніл)-7-метоксихіназолін-4-аміну, одержаного повторенням методики стадії 6) прикладу 1, за винятком використання N-Boc-3гідроксіазетидину замість (R)-(-)-N-Вос-3піролідинолу розводять 2 мл тетрагідрофурану і додають туди 25 мг сполуки, одержаної на стадії 1), 37 мг гідрохлориду N-(3-диметиламінопропіл)N'-етилкарбодііміду і 5 мкл піридину. Одержану суміш 2 години витримують при кімнатній температурі. Після припинення реакції додають воду та одержану суміш екстрагують хлороформом. Органічний шар сушать над безводним сульфатом натрію, фільтрують і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (хлороформ:метанол = 15:1) з 49 одержанням зазначеної в заголовку сполуки (2 мг, 4%). 1 H-ЯМР (300 МГц, CDCI3) δ 9,38 (с, 1Н), 8,54 (с, 1Н), 8,14 (с, 1Н), 7,54 (м, 1H), 6,99 (м, 1H), 6,04 (ушир.м, 1Н), 5,96 (с, 1H), 5,49 (с, 1H), 4,91 (м, 2Н), 4,03 (с, 3H), 3,96 (м, 2Н), 3,84 (с, 2Н); + + MS (ESI ): m/z = 504,3 [М+Н] . Приклад 105 Одержання 1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-2-(морфолінометил)проп-2ен-1-ону Повторюють методику прикладу 104 за винятком використання морфоліну замість 2,0 Μ розчину диметиламіну в тетрагідрофурані на стадії 1) з одержанням зазначеної в заголовку сполуки (4 мг, 6%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,64 (с, 1H), 8,04 (м, 1Н), 7,79 (с, 1H), 7,31 (с, 1H), 7,07 (с, 1H), 7,04 (м, 1H), 5,56 (с, 1Н), 5,51 (с, 1Н), 5,18 (м, 1H), 4,65 (м, 2Н), 4,50 (м, 1Н), 4,25 (м, 1Н), 4,03 (с, 3H), 3,69 (м, 4Н), 3,25 (м, 1Н), 3,11 (м, 1Н), 2,45 (м, 4Н); + + MS (ESI ): m/z = 546,3 [М+Н] . Приклад 106 Одержання 1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-2-((4-метилпіперазин-1іл)метил)проп-2-ен-1-ону Повторюють методику прикладу 104 за винятком використання 1-метилпіперазину замість 2,0 Μ розчину диметиламіну в тетрагідрофурані на стадії 1) з одержанням зазначеної в заголовку сполуки (7 мг, 3%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,61 (с, 1H), 8,43 (с, 1H), 7,84 (м, 1Н), 7,30 (с, 1H), 7,27 (с, 1H), 7,02 (м, 1H), 5,53 (с, 1H), 5,49 (с, 1Н), 5,23 (м, 1Н), 4,70 (м, 2Н), 4,23 (м, 1Н), 4,16 (м, 1Н), 4,04 (с, 3H), 3,42 (м, 1H), 3,00 (м, 1Н), 2,43 (м, 8Н), 2,27 (с, 3H); + + MS (ESI ): m/z = 559,3 [М+Н] . Приклад 107 Одержання 1-(3-(4-(3-хлор-2-фторфеніламіно)7-метоксихіназолін-6-ілоксі)азетидин-1-іл)-2(піперидин-1-ілметил)проп-2-ен-1-ону Повторюють методику прикладу 104 за винятком використання піперидину замість 2,0 Μ розчину диметиламіну в тетрагідрофурані на стадії 1) і 3-хлор-2-фтораніліну замість 3-хлор-2,4дифтораніліну на стадії 2) з одержанням зазначеної в заголовку сполуки (35 мг, 25%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,64 (с, 1H), 8,54 (ушир.с, 1H), 7,87 (м, 1H), 7,29 (с, 1H), 7,27 (с, 1H), 7,18 (м, 1H), 7,09 (м, 1H), 5,46 (с, 1H), 5,42 (с, 1H), 5,23 (м, 1Н), 4,88 (м, 1H), 4,60 (м, 1Н), 4,53 (м, 1Н), 4,19 (м, 1H), 4,03 (с, 3H), 3,29 (м, 1Н), 2,85 (м, 1Н), 2,30 (м, 4Н), 1,51 (м, 4Н), 1,40 (м, 2Н); + + MS (ESI ): m/z = 526,3 [М+Н] . Приклад 108 Одержання 1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-2-(піперидин-1-ілметил)проп2-ен-1-ону Повторюють методику прикладу 104 за винятком використання піперидину замість 2,0 Μ розчину диметиламіну в тетрагідрофурані на стадії 1) з 96045 50 одержанням зазначеної в заголовку сполуки (4 мг, 3%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,56 (с, 1Н), 7,68 (м, 1H), 7,20 (м, 2Н), 6,93 (м, 1H), 5,36 (с, 1H), 5,32 (с, 1Н), 5,17 (м, 1Н), 4,67 (м, 1H), 4,58 (м, 1Н), 4,48 (м, 1Н), 4,07 (м, 1Н), 3,94 (с, 3H), 3,31 (м, 1H), 2,70 (м, 1Н), 2,20 (м, 4Н), 1,45 (м, 4Н), 1,34 (м, 2Н); + + MS (ESI ): m/z = 544,3 [М+Н] . Приклад 109 Одержання 1-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-2((диметиламіно)метил)проп-2-ен-1-ону Повторюють методику прикладу 104 за винятком використання N-Boc-4-гідроксипіперидину замість N-Boc-3-гідроксіазетидину на стадії 2) з одержанням зазначеної в заголовку сполуки (6 мг, 3%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,54 (с, 1H), 7,87 (м, 1H), 7,46 (с, 1Н), 7,24 (с, 1Н), 7,04 (м, 1H), 5,51 (с, 1H), 5,34 (с, 1Н), 4,74 (м, 1H), 3,99 (с, 3H), 3,88 (м, 2Н), 3,62 (м, 2Н), 3,33 (с, 2Н), 2,41 (с, 6Н), 1,91 (м, 4Н); + + MS (ESI ): m/z = 532,3 [М+Н] . Приклад 110 Одержання 1-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-2-(морфолінометил)проп-2ен-1-ону Повторюють методику прикладу 104 за винятком використання морфоліну замість 2,0 Μ розчину диметиламіну в тетрагідрофурані на стадії 1) і N-Boc-4-гідроксипіперидину замість N-Boc-3гідроксіазетидину на стадії 2) з одержанням зазначеної в заголовку сполуки (180 мг, 33%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,62 (с, 1Н), 8,10 (м, 1H), 7,40 (с, 1Н), 7,29 (с, 1Н), 7,04 (м, 1H), 5,39 (с, 1H), 5,22 (с, 1Н), 4,71 (м, 1H), 3,99 (с, 3H), 3,89 (м, 2Н), 3,68 (м, 4Н), 3,59 (м, 2Н), 3,22 (с, 2Н), 2,51 (м, 4Н), 1,93 (м, 4Н); + + MS (ESI ): m/z = 574,3 [М+Н] . Приклад 111 Одержання 1-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-2((диметиламіно)метил)проп-2-ен-1-ону Повторюють методику прикладу 104 за винятком використання N-Boc-4-гідроксипіперидину замість N-Boc-3-гідроксіазетидину і 3,4-дихлор-2фтораніліну замість 3-хлор-2,4-дифтораніліну на стадії 2) з одержанням зазначеної в заголовку сполуки (10 мг, 4%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,72 (с, 1H), 8,47 (м, 1Н), 7,36 (с, 3H), 7,25 (с, 1Н), 5,40 (с, 1H), 5,24 (с, 1Н), 4,74 (м, 1Н), 4,04 (с, 3H), 3,95 (м, 2Н), 3,64 (м, 2Н), 3,17 (с, 2Н), 2,29 (с, 6Н), 2,01 (м, 4Н); + + MS (ESI ): m/z = 548,3 [М+Н] . Приклад 112 Одержання (Z)-1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-4-(диметиламіно)бут-2-ен-1ону Стадія 1) 4-(диметиламіно)бут-2-инов кислота 3,0 мл 3-диметиламінo-1-пропіну розводять 30 мл тетрагідрофурану і поступово, по краплях при 51 78°С додають туди 27 мл 1,6 Μ розчину нбутиллітію в тетрагідрофурані. Одержану суміш 30 хвилин перемішують при -78°С і нагрівають до кімнатної температури, барботуючи СО2 протягом 1 години. Після припинення реакції одержаний розчин підкисляють до рН 3-4 35% НСI, переганяють при зниженому тиску і сушать у вакуумі. Одержаний залишок розчиняють у гарячому етанолі та одержаний розчин перемішують при 0°С. Одержану тверду речовину відфільтровують при зниженому тиску з одержанням зазначеної в заголовку сполуки (2 г, 56%) у кристалічній формі. 1 H-ЯМР (300 МГц, D2O) δ 4,07 (с, 2Н), 2,89 (с, 6Н). Стадія 2) (Z)-4-(диметиламіно)бут-2-енова кислота 2 г сполуки, одержаної на стадії 1), розводять 120 мл змішаного розчинника етилацетат/метанол (1:1) і додають туди 450 мг паладію-на-карбонаті кальцію. Одержану суміш 2 години перемішують в атмосфері водню. Після припинення реакції одержаний розчин фільтрують через шар целіту і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (метиленхлорид:метанол = 2:1) з одержанням зазначеної в заголовку сполуки (800 мг, 39%). 1 H-ЯМР (300 МГц, CDCI3) δ 6,23 (д, 1H), 5,97 (м, 1Н), 3,56 (д, 2Н), 2,67 (с, 6Н). Стадія 3) (Z)-1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-іл)-4-(диметиламіно)бут-2-ен-1он Повторюють методику стадії 2) прикладу 104 за винятком використання сполуки, одержаної на стадії 2), замість 2((диметиламіно)метил)акрилової кислоти з одержанням зазначеної в заголовку сполуки (80 мг, 31%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,68 (с, 1H), 8,29 (м, 1H), 7,33 (с, 1H), 7,07 (м, 1Н), 6,89 (с, 1Н), 6,22 (м, 1Н), 5,85 (с, 1H), 5,15 (м, 1H), 4,56 (м, 2Н), 4,41 (м, 1Н), 4,26 (м, 1H), 4,04 (с, 3H), 3,57 (д, 2Н), 2,28 (с, 6Н); + + MS (ESI ): m/z = 504,2 [М+Н] . Приклад 113 Одержання (Z)-1-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-4-(диметиламіно)бут-2-ен-1ону Повторюють методику прикладу 112 за винятком використання N-Boc-4-гідроксипіперидину замість N-Boc-3-гідроксіазетидину на стадії 3) з одержанням зазначеної в заголовку сполуки (8 мг, 44%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,54 (с, 1H), 7,82 (м, 1H), 7,55 (с, 1H), 7,32 (с, 1Н), 7,06 (м, 1Н), 6,25 (д, 1H), 6,08 (м, 1H), 4,72 (м, 1Н), 4,01 (с, 3H), 3,88 (м, 2Н), 3,65 (м, 1Н), 3,49 (м, 1Н), 3,40 (д, 2Н), 2,37 (с, 6Н), 2,00 (м, 4Н); + + MS (ESI ): m/z = 532,3 [М+Н] . Приклад 114 Одержання 1-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-2-(гідроксиметил)проп-2-ен1-ону 96045 52 Стадія 1) етил 2-((третбутилдиметилсилілокси)метил)акрилат 10,8 г етил 2-(гідроксиметил)акрилату (Organic Synthesis, Coll, Vol. 8, 265, 1993) розводять 80 мл Ν,Ν'диметилформаміду і додають туди 18,8 г третбутилдиметилсилілхлориду та 11,3 г імідазолу. Одержану суміш витримують дві години при кімнатній температурі. Після припинення реакції додають воду та одержаний розчин екстрагують етилацетатом. Органічний шар п'ять разів промивають водою і насиченим водним розчином хлориду, сушать над безводним сульфатом натрію, фільтрують і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (етилацетат: н-гексан = 1:30) з одержанням зазначеної в заголовку сполуки (14,7 г, 73%). 1 Н-ЯМР (300 МГц, CDCI3) δ 6,24 (д, 1Н), 5,89 (д, 1Н), 4,36 (т, 2Η), 4,21 (м, 2Н), 1,30 (т, 3H), 0,91 (с, 9Н), 0,08 (с, 6Н). Стадія 2) 2-((третбутилдиметилсилілокси)метил)акрилова кислота 4 г сполуки зі стадії 1) розчиняють в 80 мл змішаного розчинника тетрагідрофуран/метанол (1:1) і при 0°С поступово, при перемішуванні додають туди 27 мл З Μ розчину гідроксиду літію. Одержану суміш 17 годин перемішують при кімнатній температурі, підкисляють до рН 4 3 н НСI і тричі екстрагують ефіром. Органічний шар сушать над безводним сульфатом магнію, фільтрують і переганяють при зниженому тиску з одержанням зазначеної в заголовку сполуки (0,5 г, 14%). 1 H-ЯМР (300 МГц, CDCI3) δ 6,21 (д, 1Н), 5,79 (д, 1Н), 4,26 (м, 2Н), 0,91 (с, 9Н), 0,08 (с, 6Н). Стадія 3) 2-((третбутилдиметилсилілокси)метил)-1-(4-(4-(3,4дихлор-2-фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-он Повторюють методику прикладу 104 за винятком використання сполуки зі стадії 2) замість 2((диметиламіно)метил)акрилової кислоти, N-Boc-4гідроксипіперидину замість N-Boc-3гідроксіазетидину і 3,4-дихлор-2-фтораніліну замість 3-хлор-2,4-дифтораніліну на стадії 2) з одержанням зазначеної в заголовку сполуки (160 мг, 55%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,69 (с, 1H), 8,42 (м, 1H), 7,71 (м, 1H), 7,35 (м, 2Н), 7,23 (м, 1H), 6,35 (д, 1Н), 5,95 (д, 1Н), 4,77 (м, 1Н), 4,42 (с, 1H), 4,35 (с, 1Н), 4,01 (с, 3H), 3,83 (м, 2Н), 3,65 (м, 2Н), 2,04 (м, 4Н), 0,91 (с, 9Н), 0,11 (с, 6Н); + + MS (ESI ): m/z = 635,1 [М+Н] . Стадія 4) 1-(4-(4-(3,4-дихлор-2фторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-іл)-2-(гідроксиметил)проп-2-ен1-он 140 мг сполуки, одержаної на стадії 3), розводять 3 мл тетрагідрофурану і додають туди 1,1 мл 1,0 Μ розчину фториду тетра-н-бутиламонію в тетрагідрофурані. Одержану суміш витримують три години при кімнатній температурі. Після припинення реакції додають насичений розчин гідрокарбонату натрію та одержаний розчин двічі екстрагують хлороформом. Органічний шар сушать над безводним сульфатом натрію, фільтрують і 53 переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (етилацетат:метиленхлорид:метанол = 7:7:1) з одержанням зазначеної в заголовку сполуки (58 мг, 51%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,64 (с, 1H), 8,13 (м, 1Н), 7,44 (с, 1Н), 7,30 (м, 2Н), 7,27 (м, 1Н), 5,44 (с, 1H), 5,18 (с, 1H), 4,64 (м, 1H), 4,31 (с, 2Н), 3,99 (с, 3H), 3,89 (м, 2Н), 3,59 (м, 2Н), 1,94 (м, 4Н); + + MS (ESI ): m/z = 521,3 [М+Н] . Приклад 115 Одержання 1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-гідроксихіназолін-6ілоксі)азетидин-1-іл)проп-2-ен-1-ону Стадія 1) трет-бутил (3-(4-(3-хлор-2,4дифторфеніламіно)-7-гідроксихіназолін-6ілоксі)азетидин-1-карбоксилат 1,3 г 6-(азетидин-3-ілокси)-N-(3-хлор-2,4дифторфеніл)-7-метоксихіназолін-4-аміну, одержаного повторенням методики стадії 6) прикладу 1 за винятком використання N-Boc-3гідроксіазетидину замість (R)-(-)-Вос-3-піролідину, і 0,77 г гідрохлориду піридину перемішують три години при 170°С. Додають метиленхлорид і метанол, та одержану суміш переганяють і сушать при зниженому тиску. Одержаний продукт розводять 10 мл метанолу і поступово додають 0,8 мл триетиламіну і 1,38 г дитрет-бутилдикарбоксилату, й одержану суміш три години кип'ятять зі зворотним холодильником при 60°С. Після припинення реакції додають воду та одержаний розчин тричі екстрагують змішаним розчинником хлороформ/2пропанол (3:1). Органічний шар сушать над безводним сульфатом натрію, фільтрують і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (метиленхлорид: метанол = 20:1) з одержанням зазначеної в заголовку сполуки (342 мг, 22%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,65 (с, 1H), 7,538,45 (м, 1Н), 7,41 (с, 1H), 7,31 (с, 1Н), 7,18 (ушир.с, 1Н), 7,10-7,03 (м, 1H), 4,98 (м, 1H), 4,48-4,40 (м, 2Н), 3,57-3,48 (м, 2Н), 1,47 (с, 9Н). Стадія 2) 6-(азетидин-3-ілокси)-(4-(3-хлор-2,4дифторфеніламіно)хіназолін-7-ол 100 мг сполуки, одержаної на стадії 1), розводять 2 мл метиленхлориду і додають туди 0,2 мл трифтороцтової кислоти. Одержану суміш перемішують одну годину при кімнатній температурі. Після припинення реакції одержаний розчин переганяють при зниженому тиску для видалення розчинника. Одержаний залишок підлужнюють насиченим розчином бікарбонату натрію та екстрагують змішаним розчинником хлороформ/2пропанол (3:1). Органічний шар сушать над безводним сульфатом натрію, фільтрують і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (метиленхлорид:метанол = 10:1) з одержанням зазначеної в заголовку сполуки (69 мг, 87%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,84 (с, 1Н), 8,628,54 (м, 1H), 7,48 (с, 1H), 7,41 (с, 1Н), 7,25 (ушир.с, 1H), 7,17-7,12 (м, 1Н), 4,53 (д, 1Н), 4,36-4,24 (м, 2Н), 3,21-3,16 (м, 2Н). 96045 54 Стадія 3) 1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-гідроксихіназолін-6ілоксі)азетидин-1-іл)проп-2-ен-1-он Повторюють методику стадії 7) прикладу 1 за винятком використання сполуки, одержаної на стадії 2), замість N-(3-хлор-2,5-дифторфеніл)-7метокси-6-((3S)-піролідин-3-ілокси)хіназолін-4аміну з одержанням зазначеної в заголовку сполуки (20 мг, 25%). 1 Н-ЯМР (300 МГц, CDCI3+CD3OD) δ 8,43 (с, 1Н), 7,71 (д, 2Н), 7,47 (д, 2Н), 7,32 (м, 1H), 7,12 (м, 1Н), 6,29 (дд, 1Н), 5,73 (д, 1Н), 5,38 (д, 1H), 4,91 (м, 1Н), 3,69 (д, 2Н), 3,38 (д, 2Н); + MS (ESI ): m/z = 433,2 [М+Н]. Приклад 116 Одержання 1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-(2-метоксіетокси)хіназолін-6ілоксі)азетидин-1-іл)проп-2-ен-1-ону Стадія 1) трет-бутил (3-(4-(3-хлор-2,4дифторфеніламіно)-7-(2-метоксіетокси)хіназолін-6ілоксі)азетидин-1-карбоксилат 110 мг сполуки, одержаної на стадії 1) прикладу 115, розводять 2 мл Ν,Ν'-диметилформаміду і додають туди 26 мкл 1-бром-2-метоксіетану, 38 мг карбонату калію і 1 мг йодиду калію. Одержану суміш витримують шість годин при 80°С. Після припинення реакції додають воду та одержаний розчин тричі екстрагують етилацетатом. Органічний шар п'ять разів промивають водою і насиченим водним розчином хлориду, сушать над безводним сульфатом натрію, фільтрують і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (метиленхлорид:метанол = 20:1) з одержанням зазначеної в заголовку сполуки (40 мг, 32%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,00 (с, 1Н), 7,67 (с, 1Н), 6,99-6,88 (м, 2Н), 6,68 (с, 1H), 4,97 (м, 1Н), 4,41-4,38 (м, 1Н), 4,37-4,29 (м, 1Н), 4,08-3,99 (м, 2Н), 3,65-3,62 (м, 2Н), 3,45-3,40 (м, 2Н), 3,31 (с, 3H), 1,45 (с, 9Н). Стадія 2) 6-(азетидин-3-ілокси)-N-(3-хлор-2,4дифторфеніл)-7-(2-метоксіетокси)хіназолін-4-амін Повторюють методику стадії 2) прикладу 115 за винятком використання сполуки, одержаної на стадії 1), замість трет-бутил (3-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілоксі)азетидин-1-карбоксилату з одержанням зазначеної в заголовку сполуки (37 мг, 100%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,00 (с, 1H), 7,72 (с, 1Н), 7,05-6,89 (м, 2Н), 6,73 (с, 1Н), 4,38 (м, 1Н), 4,36 (д, 1H), 4,13 (д, 1Н), 4,04 (т, 2Η), 3,66 (т, 2Η), 3,31 (с, 3H), 3,06 (м, 2Н). Стадія 3) 1-(3-(4-(3-хлор-2,4дифторфеніламіно)-7-(2-метоксіетокси)хіназолін-6ілоксі)азетидин-1-іл)проп-2-ен-1-он Повторюють методику стадії 3) прикладу 115 за винятком використання сполуки, одержаної на стадії 2), замість 6-(азетидин-3-ілокси)-4-(3-хлор2,4-дифторфеніламіно)хіназолін-7-олу з одержанням зазначеної в заголовку сполуки (21 мг, 50%). 1 Н-ЯМР (300 МГц, CDCI3) δ 7,91 (с, 1H), 7,67 (с, 1Н), 6,98-6,90 (м, 2Н), 6,56 (м, 1Н), 6,33 (д, 1H), 6,20 (дд, 1Н), 5,69 (д, 1Н), 4,41 (м, 1H), 4,31 (м, 1Н), 4,04-3,98 (м, 3H), 3,74-3,70 (м, 1Н), 3,64-3,55 (м, 2Н), 3,30 (с, 3H); 55 + 96045 + MS (ESI ): m/z = 491,3 [М+Н] . Приклад 117 Одержання 1-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-(2-метоксіетокси)хіназолін-6ілокси)піперидин-1-іл)проп-2-ен-1-ону Повторюють методику прикладу 116 за винятком використання N-Boc-4-гідроксипіперидину замість N-Boc-3-гідроксіазетидину з одержанням зазначеної в заголовку сполуки (20 мг, 22%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,67 (с, 1H), 8,16 {д, 1Н), 7,50 (с, 1Н), 7,34 (с, 1H), 6,65 (т, 1Н), 6,62 (дд, 1H), 6,31 (д, 1Н), 5,73 (д, 1Н), 4,72 (м, 1Н), 4,33 (м, 2Н), 3,89 (м, 6Н), 3,59 (с, 3H), 2,07 (м, 2Н), 1,99 (м, 2Н); + + MS (ESI ): m/z = 519,3 [М+Н] . Приклад 118 Одержання 1-(4-(4-(3-хлор-2,4дифторфеніламіно)-7-(3морфолінопропокси)хіназолін-6-ілокси)піперидин1-іл)проп-2-ен-1-ону Повторюють методику прикладу 117 за винятком використання 4-(3-хлорпропіл)морфоліну замість 1-бром-2-метоксіетану з одержанням зазначеної в заголовку сполуки (8 мг, 27%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,64 (с, 1Н), 8,258,24 (м, 1H), 7,31-7,29 (с, 2Н), 7,09-7,06 (т, 1H), 6,65-6,50 (м, 1H), 6,28 (дд, 1H), 5,70 (дд, 1H), 4,68 (м, 1H), 4,22 (т, 2Н), 3,82 (м, 3H), 3,72 (м, 5Н), 2,56 (т, 2Н), 2,48-2,47 (м, 4Н), 2,11-2,06 (м, 2Н), 1,961,94 (м, 1Н); + + MS (ESI ): m/z = 588,4 [М+Н] . Приклад 119 Одержання (2S,4S)-метил-акрилоїл-4-(4-(3хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксилату Повторюють методику прикладу 1 за винятком використання (2S,4R)-1-трет-бутил 2-метил-4гідроксипіперидин-1,2-дикарбоксилату (J. Org. Chem. 1996, 61, 2226-2231) замість (R)-(-)-N-Вос-3піролідинолу на стадії 6) з одержанням зазначеної в заголовку сполуки (45 мг, 32%). 1 H-ЯМР (300 МГц, CDCI3) δ 9,00 (с, 1Н), 8,64 (м, 1H), 8,27 (ушир.с, 1Н), 8,22 (с, 1Н), 7,04 (тд, 1Н), 6,67 (м, 1Н), 6,34 (м, 1Н), 5,82 (м, 2Н), 4,80 (м, 1H), 4,56 (м, 1H), 4,03 (с, 3H), 3,84 (с, 3H), 3,28 (м, 1Н), 3,07 (м, 1H), 2,21 (м, 2Н), 2,03 (м, 1Н), 1,69 (м, 1H); + + MS (ESI ): m/z = 533,3 [М+Н] . Приклад 120 Одержання (2S,4S)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксаміду Стадія 1) (2S,4S)-1-трет-бутил 2-метил 4-(4-(3хлор-2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1,2-дикарбоксилат Повторюють методику стадії 6) прикладу 1 за винятком використання (2S,4R)-1-трет-бутил 2метил-4-гідроксипіперидин-1,2-дикарбоксилату (J. Org. Chem. 1996, 61, 2226-2231) замість (R)-(-)-NВос-3-піролідинолу без проведення реакції видалення захисної групи з використанням трифтороцтової кислоти з одержанням у такий спосіб зазначеної в заголовку сполуки (1,7 г, 40%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,59 (с, 1H), 7,94 (м, 1Н), 7,85 (с, 1H), 7,25 (с, 1Н), 6,95 (тд, 1Н), 5,10 56 (м, 1Н), 4,41 (м, 1Н), 4,13 (м, 1H), 3,98 (с, 3H), 3,78 (с, 3H), 2,89 (м, 2Н), 2,08 (м, 1Н), 1,78 (м, 2Н), 1,47 (с, 3H). Стадія 2) (2S,4S)-1-(трет-бутоксикарбоніл)-4(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-2-карбонова кислота 1,66 г сполуки, одержаної на стадії 1), розводять 18 мл 50% тетрагідрофурану і додають туди 145 мг моногідрату гідроксиду літію. Одержану суміш перемішують три години при кімнатній температурі. Після припинення реакції одержаний розчин підкисляють оцтовою кислотою і двічі екстрагують етилацетатом. Органічний шар сушать над безводним сульфатом натрію, фільтрують і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (метиленхлорид:етилацетат:метанол = 5:5:1) з одержанням зазначеної в заголовку сполуки (1,5 г, 92%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,31 (с, 1Н), 7,74 (с, 1Н), 7,60 (м, 2Н), 7,12 (м, 2Н), 4,60 (м, 1H), 4,09 (м, 2Н), 3,94 (с, 3H), 3,29 (м, 1Н), 2,70 (м, 1H), 2,31 (м, 1Н), 2,07 (м, 1H), 1,92 (м, 1H), 1,43 (с, 9Н). Стадія З) (2S,4S)-1-трет-бутил 2-карбамоїл-4(4-(3-хлор-2,4-дифторфеніламіно)-7метоксихіназолін-6-ілокси)піперидин-1карбоксилат 1,93 г сполуки, одержаної на стадії 1), розводять 17 мл тетрагідрофурану і при -15°С додають туди 0,53 мл N-метилморфоліну і 0,58 мл ізобутилхлорформіату. Одержану суміш перемішують 10 хвилин і додають туди 1,0 мл 28% водного аміаку. При поступовому нагріванні до кімнатної температури одержану суміш витримують одну годину. Після припинення реакції додають воду і одержаний розчин екстрагують хлороформом. Органічний шар промивають водою і насиченим водним розчином хлориду, сушать над безводним сульфатом натрію, фільтрують і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (метиленхлорид:етилацетат = 1:3) з одержанням зазначеної в заголовку сполуки (1,0 г, 52%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,61 (с, 1H), 8,02 (м, 2Н), 7,05 (м, 1Н), 6,48 (с, 1Н), 5,52 (м, 1Н), 4,74 (м, 1Н), 4,33 (м, 1H), 4,02 (с, 3H), 3,06 (м, 2Н), 1,90 (м, 2Н), 1,49 (м, 1H). Стадія 4) (2S,4S)-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-1-карбоксамід Повторюють методику стадії 2) прикладу 115 за винятком використання сполуки, одержаної на стадії 3), замість трет-бутил 3-(4-(3-хлор-2,4дифторфеніламіно)-7-гідроксихіназолін-6ілоксі)азетидин-1-карбоксилату з одержанням зазначеної в заголовку сполуки (580 мг, 71%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,32 (с, 1H), 7,76 (с, 1Н), 7,53 (с, 1H), 7,19 (м, 1Н), 6,71 (с, 1Н), 4,92 (м, 2Н), 4,00 (с, 3H), 3,12 (м, 1H), 2,96 (м, 1Н), 2,23 (м, 1Н), 1,87 (м, 3H), 1,26 (с, 9Н). Стадія 5) (2S,4S)-1-акрилоїл-4-(4-(3-хлор-2,4дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксамід 57 Повторюють методику стадій 1)-7) за винятком використання сполуки, одержаної на стадії 4), замість N-(хлор-2,4-дифторфеніл)-7-метокси-6-((3S)піролідин-3-ілокси)хіназолін-4-аміну з одержанням зазначеної в заголовку сполуки (10мг,69%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,58 (с, 1Н), 8,08 (ушир.с, 1Н), 7,99 (ушир.с, 2Н), 7,24 (с, 1Н), 7,00 (тд, 1H), 6,66 (м, 2Н), 6,36 (д, 1Н), 5,82 (д, 2Н), 5,49 (м, 1Н), 4,88 (м, 1H), 4,15 (м, 1Н), 4,00 (с, 3H), 3,28 (м, 1Н), 3,01 (м, 1Н), 2,22 (м, 1H), 2,15 (м, 1Н), 2,02 (м, 1H), 1,55 (м, 1H); + + MS (ESI ): m/z = 518,2 [М+Н] . Приклад 121 Одержання (2S,4S)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)-N-метилпіперидин-2-карбоксаміду Повторюють методику прикладу 120 за винятком використання 2,0 Μ розчину метиламіну в тетрагідрофурані замість 28% водного аміаку на стадії 3) з одержанням зазначеної в заголовку сполуки (240 мг, 66%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,63 (с, 1Н), 8,34 (с, 1Н), 8,19 (с, 1Н), 8,13 (м, 1H), 7,04 (тд, 1Н), 6,70 (дд, 2Н), 6,45 (дд, 1H), 5,88 (дд, 1H), 5,50 (м, 1Н), 4,99 (м, 1H), 4,21 (м, 1H), 4,02 (с, 3H), 3,30 (т, 1H), 3,07 (д, 2Н), 2,25 (м, 1H), 2,02 (м, 1H), 1,80 (м, 3H), 1,58 (м, 1H); + + MS (ESI ): rn/z = 532,3 [М+Н] . Приклад 122 Одержання (2S,4S)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)-N-етилпіперидин-2-карбоксаміду Повторюють методику прикладу 120 за винятком використання 2,0 Μ розчину метиламіну в тетрагідрофурані замість 28% водного аміаку на стадії 3) з одержанням зазначеної в заголовку сполуки (25 мг, 60%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,63 (с, 1Н), 8,37 (с, 1Н), 8,21 (с, 1Н), 8,16 (м, 1H), 7,08 (тд, 1Н), 6,71 (дд, 2Н), 6,45 (дд, 1H), 5,88 (дд, 1H), 5,51 (м, 1H), 4,99 (м, 1Н), 4,22 (м, 1Н), 4,08 (с, 3H), 3,41 (м, 1H), 3,26 (д, 2Н), 2,26 (м, 1H), 2,02 (м, 1H), 1,57 (м, 1H), 1,25 (м, 2Н), 1,14 (м, 3H); + + MS (ESI ): m/z = 546,2 [М+Н] . Приклад 123 Одержання (2S,4S)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)-N-пропілпіперидин-2-карбоксаміду Повторюють методику прикладу 120 за винятком використання пропіламіну замість 28% водного аміаку на стадії 3) з одержанням зазначеної в заголовку сполуки (3,8 мг, 11%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,63 (с, 1H), 8,38 (с, 1Н), 8,21 (с, 1Н), 8,16 (м, 1Н), 7,06 (тд, 1H), 6,71 (дд, 2Н), 6,44 (дд, 1H), 5,88 (дд, 1H), 5,51 (м, 1H), 4,99 (м, 1Н), 4,18 (м, 1H), 4,03 (с, 3H), 3,25 (м, 3H), 3,07 (д, 1Н), 2,22 (м, 1Н), 2,04 (м, 1Н), 1,55 (м, 4Н), 1,25 (м, 2Н), 0,89 (т, 3H); + + MS (ESI ): m/z = 560,0 [М+Н] . Приклад 124 Одержання (2S,4S)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін~6ілокси)-N-ізопропілпіперидин-2-карбоксаміду Повторюють методику прикладу 120 за винятком використання ізопропіламіну замість 28% вод 96045 58 ного аміаку на стадії 3) з одержанням зазначеної в заголовку сполуки (10,6 мг, 16%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,63 (с, 1Н), 8,38 (с, 1Н), 8,21 (с, 1Н), 8,16 (м, 1H), 7,06 (тд, 1H), 6,68 (дд, 1H), 6,48 (м, 2Н), 5,87 (дц, 1Н), 5,48 (м, 1H), 4,98 (м, 1Н), 4,12 (м, 2Н), 4,02 (с, 3H), 3,23 (м, 1H), 3,07 (м, 1H), 2,24 (м, 1Н), 2,02 (м, 1Н), 1,85 (м, 2Н), 1,51 (м, 1H), 1,03 (м, 6Н); + + MS (ESI ): m/z = 560,0 [М+Н] . Приклад 125 Одержання (2S,4S)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)-№гідроксипіперидин-2-карбоксаміду Повторюють методику прикладу 120 за винятком використання гідроксиламіну замість 28% водного аміаку на стадії 3) з одержанням зазначеної в заголовку сполуки (13 мг, 18%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,32 (с, 1H), 7,79 (с, 1H), 7,52 (м, 1H), 7,18 (м, 2Н), 6,82 (м, 1H), 6,25 (д, 1Н), 5,77 (м, 1H), 5,38 (м, 1Н), 4,85 (м, 1H), 4,15 (м, 1H), 3,97 (с, 3H), 2,70 (м, 1H), 2,31 (м, 1H), 1,90 (м, 1H), 1,67 (м, 1H), 1,28 (м, 1H); + + MS (ESI ): m/z = 534,2 [М+Н] . Приклад 126 Одержання (2S,4S)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)-N-(2-гідроксіетил)піперидин-2-карбоксаміду Повторюють методику прикладу 120 за винятком використання етаноламіну замість 28% водного аміаку на стадії 3) з одержанням зазначеної в заголовку сполуки (10 мг, 25%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,32 (с, 1Н), 7,80 (с, 1Н), 7,52 (м, 1H), 7,18 (м, 2Н), 6,82 (м, 1Н), 6,25 (д, 1H), 5,80 (м, 1H), 5,40 (м, 1Н), 4,85 (м, 1Н), 4,15 (м, 1Н), 3,97 (с, 3H), 3,89 (м, 2Н), 3,26 (м, 2Н), 2,70 (м, 1H), 2,31 (м, 1H), 1,95 (м, 1H), 1,71 (м, 1H), 1,20 (м, 1Н); + + MS (ESI ): m/z = 562,3 [M+H] . Приклад 127 Одержання (2S,4S)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)-N-(2-метоксіетил)піперидин-2-карбоксаміду Повторюють методику прикладу 120 за винятком використання 2-метилоксіетиламіну замість 28% водного аміаку на стадії 3) з одержанням зазначеної в заголовку сполуки (12 мг, 25%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,46 (с, 1H), 7,87 (с, 1Н), 7,65 (м, 1H), 7,13 (с, 1Н), 6,96 (м, 1H), 6,68 (м, 1Н), 6,40 (дд, 1H), 5,85 (д, 1Н), 4,45 (м, 1H), 3,92 (м, 4Н), 3,26 (м, 7Н), 2,83 (м, 1Н), 2,59 (м, 1H), 1,91 (м, 2Н), 1,76 (м, 1Н); + + MS (ESI ): m/z = 576,2 [М+Н] . Приклад 128 Одержання (2S,4S)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)-N-(2-(метилтіо)етил)піперидин-2карбоксаміду Повторюють методику прикладу 120 за винятком використання 2-(метилтіо)етиламіну замість 28% водного аміаку на стадії 3) з одержанням зазначеної в заголовку сполуки (40 мг, 47%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,63 (с, 1Н), 8,30 (с, 1H), 8,12 (м, 2Н), 7,12 (м, 1H), 7,09 (м, 1H), 6,86 (м, 1Н), 6,54 (дд, 1H), 5,92 (д, 1H), 5,63 (м, 1H), 4,95 (м, 1H), 4,15 (м, 1H), 4,03 (с, 3H), 3,78 (м, 1H), 59 3,57 (м, 2Н), 3,15 (м, 1H), 2,87 (м, 2Н), 2,21 (м, 1H), 2,06 (с, 3H), 1,65 (м, 2Н), 1,60 (м, 1Н); + + MS (ESI ): m/z = 592,3 [М+Н] . Приклад 129 Одержання (2S,4S)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)-N-(2-(метилсульфоніл)етил)піперидин-2карбоксаміду 41 мг сполуки, одержаної в прикладі 128, розводять 1 мл тетрагідрофурану і додають туди 1 мл насиченого водного бікарбонату натрію і 34 мг 3хлорпероксибензойної кислоти. Одержану суміш дві години інкубують при кімнатній температурі. Після припинення реакції додають воду та одержаний розчин двічі екстрагують етилацетатом. Органічний шар промивають водою і насиченим водним розчином хлориду, сушать над безводним сульфатом натрію, фільтрують і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (метиленхлорид:етилацетат:метанол = 10:10:1) з одержанням зазначеної в заголовку сполуки (20 мг, 47%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,64 (с, 1H), 8,26 (м, 1H), 8,18 (с, 1Н), 8,09 (с, 1Н), 7,28 (с, 1H), 7,09 (м, 1Н), 6,68 (дд, 1Н), 6,42 (д, 1H), 5,82 (д, 1H), 5,56 (м, 1H), 4,85 (м, 1Н), 4,21 (м, 1Н), 4,02 (с, 3H), 3,98 (м, 1H), 3,75 (м, 1H), 3,37 (м, 2Н), 3,10 (м, 1Н), 2,95 (с, 3H), 2,24 (м, 1Н), 2,02 (м, 1H), 1,52 (м, 1H); + + MS (ESI ): m/z = 624,3 [М+Н] . Приклад 130 Одержання (2S,4S)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)-N-(2-(диметиламіно)етил)піперидин-2карбоксаміду Повторюють методику прикладу 120 за винятком використання Ν,Ν-диметилетилендіаміну замість 28% водного аміаку на стадії 3) з одержанням зазначеної в заголовку сполуки (39 мг, 44%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,62 (с, 1Н), 8,25 (с, 2Н), 8,12 (м, 1H), 7,30 (м, 1Н), 7,05 (тд, 1H), 6,68 (м, 1H), 6,41 (дд, 1H), 5,85 (д, 1H), 5,59 (м, 1Н), 4,83 (м, 1H), 4,15 (м, 1Н), 4,02 (с, 3H), 3,30 (м, 2Н), 3,14 (м, 1H), 2,55 (м, 3H), 2,29 (м, 8Н), 2,01 (м, 1H), 1,50 (м, 1Н); + + MS (ESI ): m/z = 589,3 [М+Н] . Приклад 131 Одержання (2S,4S)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)-N-(3-гідроксипропіл)піперидин-2карбоксаміду Повторюють методику прикладу 120 за винятком використання 3-аміно-1-пропанолу замість 28% водного аміаку на стадії 3) з одержанням зазначеної в заголовку сполуки (50 мг, 27%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,62 (с, 1H), 8,19 (с, 1Н), 8,10 (с, 1H), 7,26-7,01 (м, 2Н), 6,67 (м, 1H), 6,38 (д, 1H), 5,84 (д, 1H), 4,92 (м, 1H), 4,17 (м, 1H), 4,02 (с, 3H), 3,98 (м, 1H), 3,68 (м, 2Н), 3,46 (м, 2Η), 3,33 (м, 1Н), 3,11 (м, 2Н), 2,21 (м, 1H), 2,04 (м, 1Н), 1,60 (м, 1H); + + MS (ESI ): m/z = 576,2 [М+Н] . Приклад 132 Одержання (2S,4S)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6 96045 60 ілокси)-N-(2-морфоліноетил)піперидин-2карбоксаміду Повторюють методику прикладу 120 за винятком використання N-(2-аміноетил)морфоліну замість 28% водного аміаку на стадії 3) з одержанням зазначеної в заголовку сполуки (100 мг, 43%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,63 (с, 1H), 8,32 (с, 1Н), 8,17 (с, 1H), 7,08-7,02 (м, 2Н), 6,67-6,65 (м, 1Н), 6,45 (д, 1Н), 5,87 (д, 1H), 5,56 (м, 1Н), 4,95 (м, 1H), 4,02 (с, 3H), 3,70-3,65 (м, 4Н), 3,55-3,25 (м, 2Н), 3,02 (д, 1H), 2,49-2,41 (м, 8Н), 2,35 (м, 1Н), 2,21 (м, 1H), 1,55 (м, 1Н); + + MS (ESI ): m/z = 631,4 [М+Н] . Приклад 133 Одержання (2R,4R)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксилату Повторюють методику прикладу 1 за винятком використання (2R,4S)-1-тpeт-бутил 2-метил-4гідроксипіперидин-1,2-дикарбоксилату (J. Org. Chem. 1996, 61, 2226-2231) замість (R)-(-)-N-Вос-3піролідинолу на стадії 6) з одержанням зазначеної в заголовку сполуки (42 мг, 34%). 1 Н-ЯМР (300 МГц, CDCI3) δ 9,00 (с, 1Н), 8,64 (м, 1Н), 8,27 (ушир.с, 1Н), 8,22 (с, 1H), 7,04 (тд, 1H), 6,67 (м, 1Н), 6,34 (м, 1H), 5,82 (м, 2Н), 4,80 (м, 1H), 4,56 (м, 1Н), 4,03 (с, 3H), 3,84 (с, 3H), 3,28 (м, 1H), 3,07 (м, 1Н), 2,21 (м, 1H), 2,03 (м, 1Н), 1,69 (м, 2Н); + + MS (ESI ): m/z = 533,3 [М+Н] . Приклад 134 Одержання (2R,4R)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфеніламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбонові кислоти 15 мг сполуки, одержаної в прикладі 133, розчиняють в 0,2 мл змішаного розчинника тетрагідрофуран/метанол (1:1) і при 0°С додають туди 1,4 мг моногідрату гідроксиду літію. Одержану суміш одну годину інкубують при кімнатній температурі. Після припинення реакції одержаний розчин підкисляють до рН 4 3 н НСI і двічі екстрагують метиленхлоридом. Органічний шар сушать над безводним сульфатом магнію, фільтрують і переганяють при зниженому тиску. Одержаний залишок очищають колонковою хроматографією (метиленхлорид:етилацетат:метанол = 1:1:1) з одержанням зазначеної в заголовку сполуки (10 мг, 69%). 1 H-ЯМР (300 МГц, CDCI3) δ 8,41 (с, 1H), 7,83 (с, 1Н), 7,51 (м, 1H), 7,19 (м, 2Н), 6,81 (м, 1Н), 6,20 (м, 1Н), 5,74 (м, 1H), 4,65 (м, 1Н), 4,15 (м, 1H), 3,99 (с, 3H), 3,49 (м, 1H), 2,84 (м, 1H), 2,34 (м, 1H), 2,00 (м, 1H), 1,27 (м, 2Н); + + MS (ESI ): m/z = 519,3 [М+Н] . Приклад 135 Одержання (2R,4R)-1-акрилоїл-4-(4-(3-хлор2,4-дифторфемламіно)-7-метоксихіназолін-6ілокси)піперидин-2-карбоксаміду Повторюють методику прикладу 120 за винятком використання (2R,4S)-1-трет-бутил 2-метил-4гідроксипіперидин-1,2-дикарбоксилату замість (2S,4R)-1-трет-бутил 2-метил-4-гідроксипіперидин1,2-дикарбоксилату на стадії 1) з одержанням зазначеної в заголовку сполуки (50 мг, 45%). 1 Н-ЯМР (300 МГц, CDCI3) δ 8,63 (с, 1H), 8,36 (с, 1Н), 8,15 (м, 2Н), 7,27 (с, 1Н), 7,04 (тд, 1H), 6,70
ДивитисяДодаткова інформація
Назва патенту англійськоюAmide derivative for inhibiting the growth of cancer cells
Автори англійськоюLee, Kwang-Ok, Cha, Mi Young, Kim, Mi Ra, Jung, Young Hee, Lee, Chang Gon, Kim, Se Young, Bang, Keukchan, Park, Bum Woo, Choi, Bo Im, Chae, Yun Jung, Ko, Mi Young, Kim Han Kyong, Ahn, Young-Gil, Kim, Maeng Sup, Lee, Gwan Sun
Назва патенту російськоюАмидное производное для ингибирования роста раковых клеток
Автори російськоюЛи Кванг-Ок, Ча Ми Йоунг, Ким Ми Ра, Дзунг Йоунг Хее, Ли Чанг Гон, Ким Се Йоунг, Банг Кеукчан, Парк Бум Воо, Чои Бо Им, Чаэ Юн Дзунг, Ко Ми Йоунг, Ким Хан Кионг, Ахн Йоунг-Гил, Ким Маенг Суп, Ли Гван Сун
МПК / Мітки
МПК: C07D 403/12
Мітки: клітин, амідне, інгібування, ракових, росту, похідне
Код посилання
<a href="https://ua.patents.su/51-96045-amidne-pokhidne-dlya-ingibuvannya-rostu-rakovikh-klitin.html" target="_blank" rel="follow" title="База патентів України">Амідне похідне для інгібування росту ракових клітин</a>
Попередній патент: Курильний виріб із оновленою обгорткою
Наступний патент: Розподільна пластина ударної дробарки з вертикальним валом і спосіб заміни такої пластини
Випадковий патент: Спосіб оцінки ступеня вираженості запальних змін в біологічних об'єктах












