16a,17-циклогексилметилендіокси-11b,21-дигідроксипрегна-1,4-дієн-3,20-діон, спосіб його одержання, лікарський засіб
Номер патенту: 45311
Опубліковано: 15.04.2002
Автори: Флокерці Дітер, Амшлер Херман, Рідель Річард, Бейме Рольф, Постіус Штефан, Стоек Міхаель, Цех Карл
Формула / Реферат
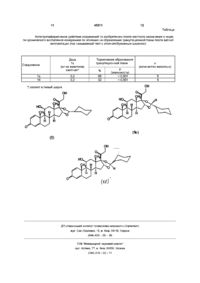
1. -циклогексилметилендиокси--дигидроксипрегна-1,4-диен-3,20-дион общей формулы І
в виде индивидуальных эпимеров или их смесей.
2. Соединение по п. 1, отличающееся тем, что эпимеры соединения формулы I характеризуются соединением -циклогексилметилендиокси--дигидроксипрегна-1,4-диен-3,20-дион формулы Іа
3. Соединение по любому из пп. 1, 2, отличающееся тем, что эпимеры
соединения формулы І характеризуются соединением -циклогексилметилендиокси--дигидроксипрегна-1,4-диен-3,20-дион формулы Іб
4. Соединение формулы І по любому из пп. 1-3, отличающееся тем, что формула І для смеси эпимеров соединения формулы Іа
и соединения формулы Іб
имеет любое соотношение компонентов смеси.
5. Соединение по одному из пп. 1-4 для применения при лечении или профилактике заболевания кожи, заболеваний дыхательных путей, воспалительных заболеваний кишечника и аллергических ринитов/конъюнктивитов.
6. Способ получения соединения формулы І по любому из пп. 1-3, отличающийся тем, что 16-гидроксипреднизолон вводят во взаимодействие с циклогексанальдегидом.
7. Лекарственное средство, содержащее соединение формулы І по любому из пп. 1-4, в виде смеси эпимеров соединений Іа и Іб в любом соотношении компонентов смеси для лечения или профилактики заболевания кожи, заболеваний дыхательных путей, воспалительных заболеваний кишечника и аллергических ринитов/конъюнктивитов.
8. Лекарственное средство, содержащее соединение формулы Іа по пункту 2, отличающееся тем, что лекарственное средство по существу свободно от соединения формулы Іб.
9. Лекарственное средство, содержащее соединение формулы Іб по пункту 3, отличающееся тем, что лекарственное средство по существу свободно от соединения формулы Іа.
Текст
1 1 ба,17 -циклогексилметилендиокси-1 ір,21 дигидроксипрегна-1,4-диен-3,20-дион общей формулы циклогексилметилендиокси- 11р,21 дигидроксипрегна-1,4-диен-3,20-дион формулы 16 4 Соединение формулы І по любому из пп 1-3, отличающееся тем, что формула I для смеси эпимеров соединения формулы la ж но о (і) в виде индивидуальных эпимеров или их смесей 2 Соединение по п 1, отличающееся тем, что эпимеры соединения формулы I характеризуются соединением 16а,17 - (22R) циклогексилметилендиокси- 11р,21 дигидроксипрегна-1,4-диен-3,20-дион формулы la но (1а) 3 Соединение по любому из пп 1, 2, отличающееся тем, что эпимеры соединения формулы I характеризуются соединением 1 ба,17 - (22S) и соединения формулы 16 го ю имеет любое соотношение компонентов смеси 5 Соединение по одному из пп 1-4 для применения при лечении или профилактике заболевания кожи, заболеваний дыхательных путей, воспалительных заболеваний кишечника и аллергических ринитов/конъюнктивитов 6 Способ получения соединения формулы I по любому из пп 1-3, отличающийся тем, что 16гидроксипреднизолон вводят во взаимодействие с циклогексанальдегидом 7 Лекарственное средство, содержащее соединение формулы I по любому из пп 1-4, в виде смеси эпимеров соединений la и Іб в любом соотношении компонентов смеси для лечения или профи 45311 лаісгики заболевания кожи, заболеваний дыхательных путей, воспалительных заболеваний кишечника и аллергических ринитов/конъюнктивитов 8 Лекарственное средство, содержащее соединение формулы la по пункту 2, отличающееся тем, что лекарственное средство по существу свободно Изобретение относится к новым производным преднизолона, которые применяют в фармацевтической промышленности для изготовления медикаментов В выложенном описании к неакцептованной заявке на патент ФРГ 41 29 535 раскрывают прегна—1,4—диен—3,20—дион—16,17—ацеталь— 21—сложные эфиры, которые несут на циклическом ацетальном кольце остаток бутила, изопропила, втор -бутила, циклогексила или фенила и С— 21—гидроксильная группа которых ацилирована остатком ацетила или изобутирила Теперь найдено, что следующие соединения согласно изобретению, которые отличаются от соединений заявки на патент ФРГ 41 29 535 отсутствующим остатком ацила на С—21 — гидроксильной группе, имеют неожиданные и выгодные свойства Предметом изобретения являются эпимеры соединения формулы 1 (см прилагаемый листок с формулами) в чистом виде и смеси этих эпимеров в любом соотношении компонентов смеси Эпимеры соединения формулы 1 можно охарактеризовать формулами 1а и 16 (см прилагаемый листок с формулами) Другим предметом изобретения является способ получения соединений согласно изобретению Способ отличается тем, что 16— гидроксипреднизолон вступает во взаимодействие с циклогексанальдегидом Взаимодействие осуществляют известным специалисту способом в подходящих растворителях, таким как простые эфиры, например, диоксан, простой диизопропиловый эфир, сложные эфиры, например, сложный этиловый эфир уксусной кислоты, галогенированные углеводороды, например, хлористый метилен, хлороформ, нитрированные углеводороды, например, нитрометан, или без растворителей, при добавке каталитических или также очень больших количеств кислоты, как минеральные кислоты, например, хлорная кислота, соляная кислота, тетрафторборная кислота, или сул ь-фо кислоты, например, метан сульфокислота, при температурах преимущественно от 0 до 60°С Преимущественно взаимодействие до смеси эпимеров (формула 1) осуществляют в диоксане или в сложном этиловом эфире уксусной кислоты с 70%-ной хлорной кислотой или с 85%-ной тетрафторборной кислотой при температуре от 0°С до комнатной температуры Реакция взаимодействия 16— гидроксипреднизолона с циклогексанальдегидом дает, как правило, смесь эпимеров, причем соот от соединения формулы 16 9 Лекарственное средство, содержащее соединение формулы 16 по пункту 3, отличающееся тем, что лекарственное средство по существу свободно от соединения формулы la ветствующим изменением условии реакции можно регулировать превращение таким образом, что образуется преимущественно определенный эпимер Для преимущественного получения R— эпимера (формула 1а) предпочитают, например, следующие условия галогенированные углеводороды или нитрометан превращают с метансульфокислотой при температуре от комнатной до 40°С, или с 35—70%-ной хлорной кислотой при температуре от 0°С до комнатной температуры Другая возможность для преимущественного получения R—эпимера заключается в обработке смеси эпимеров (формула 1) 70%-ной хлорной кислотой вподходящем растворителе, как например, хлористый метилен, при 0°С (эпимеризация) Преимущественного получения S—эпимера (формула 16) достигают при помощи газообразного хлористого водорода в растворителе, как например, диоксан при температуре от 0°С до комнатной Поскольку желательно получение эпимера в более чистой форме, как этого достигают на основании условий реакции, можно дополнительно подключать к взаимодействию стадии разделения и очистки, как например, препаративная тонкослойная хроматография (HPLC) Следующие примеры служат для более подробного пояснения изобретения Примеры 1 500мг (1,3ммол) 16—гидроксипреднизолона суспендируют в 5мл нитрометана и смешивают с ЗЗмкл (0,38ммол) 70%-ной хлорной кислоты и 195мкл (1,6ммол) циклогексанальдегида После 4,5 часа перемешивания при комнатной температуре (соотношение эпимеров в реакционной смеси R/S=55/45, препаративная тонкослойная хроматография HPLC — содержание 95%) реакционную смесь смешивают с раствором бикарбоната натрия, отсасывают осадок, промывают водой и нитрометаном и сушат при 50°С в высоком вакууме Выход 440мг (70%), соотношение эпимеров R/S = 57/43 (определение методом препаративной тонкослойной хроматографии, неподвижная фаза ODS гиперзил, подвижная фаза вода/эта н ол=60/40) 2 2,0 (5,3ммол) 16—гидроксипреднизолона суспендируют в 20мл нитрометана и смешивают с 0,88мл (10,2ммол) 70%-ной хлорной кислоты и 0,78мл (6,4ммол) циклогексанальдегида После 4,5 часов перемешивания при комнатной температуре (соотношение эпимеров в реакционной смеси R/S=73/27, препаративная тонкое 45311 лойная хроматография HPLC — содержание 95%) работают как в примере 1 Выход 1,96г (78%), соотношение эпимеров R/S=76/24 3 2,Or (5,3ммол) 16—гидроксипреднизолона суспендируют в 10мл нитрометана и 1,5мл (17,4ммол) 70%-ной хлорной кислоты и затем закапывают 0,8мл (б.бммол) циклогексанальдегида Перемешивают 2 часа при комнатной температуре (соотношение эпимеров в реакционной смеси R/S=92/8, HPLC — содержание 98%) и работают как в примере 1 Выход 2,2г (88%), соотношение эпимеров R/S=92/8 4 2,0г (5,3ммол) 16—гидроксипреднизолона суспендируют в 20мл нитрометана и смешивают с 3,52мл (4ммол) 70%-ной хлорной кислоты и 0,78мл (6,4ммол) циклогексанальдегида После 1 часа перемешивания при комнатной температуре подают на раствор бикарбоната натрия, экстрагируют хлористым метиленом, сушат органическую фазу при помощи сульфата натрия и сгущают в вакууме Остаток хроматографируют на силикагеле с хлористым метиленом/сложным этиловым эфиром уксусной кислоты =1/1 (Rf = 0,5) Выход 1,0г (40%), соотношение эпимеров R/S=89/11 5 20г (53ммол) 16—гидроксипреднизолона суспендируют в 300мл хлороформа, смешивают с 8,0мл (ббммол) циклогексанальдегида и при охлаждении в ледяной бане закапывают 17,6мл (205ммол) 70%-ной хлорной кислоты После 2,5 часов перемешивания при комнатной температуре реакционную смесь подают на содовый раствор, экстрагируют органическую фазу водой, сушат при помощи сульфата натрия и сгущают в вакууме (соотношение эпимеров в сыром продукте R/S=85/15) Остаток растворяют в теплом метаноле, смешивают до помутнения с водой, охлаждают в ледяной бане и осадок отсасывают и сушат Выход 20,2г (81%), соотношение эпимеров R/S=85/15 6 5,0г (13,3ммол) 16—гидроксипреднизолона суспендируют в 100мл хлористого метилена, смешивают с 4,4мл (51,2ммол) 70%-ной хлорной кислоты и закапывают 2,1мл (17,3ммол) циклогексанальдегида После 1,25 часа реакционную смесь подают на содовый раствор, промывают органическую фазу водой, сушат при помощи сульфата магния и сгущают в вакууме Выход сырого продукта количественный, HPLC — содержание 96%, соотношение эпимеров R/S=89/11 7 300г (797ммол 16—гидроксипреднизолона суспендируют в 3,0л сложного этилового эфира уксусной кислоты, смешивают с 120мл (991ммол) циклогексанальдегида и в течение 20 минут закапывают 150мл (1,75мол) 70%-ной хлорной кислоты После 1 часа перемешивания раствор смешивают с 250г карбоната натрия и размешивают с 1,5л воды Водную фазу экстрагируют сложным этиловым эфиром уксусной кислоты, собранные органические фазы экстрагируют насыщенным раствором хлористого натрия После сушки органической фазы сульфатом натрия медленно сгущают ее в вакууме, отсасывают образующееся твердое вещество, дополнительно промывают простым диэтиловым эфиром и сушат Выход 282г (75%), соотношение эпимеров R/S=58/42 8 10,0г (26,6ммол) 16—гидроксипреднизолона при охлаждении суспендируют в ледяной бане в 100мл диоксана, смешивают с 8,8мл (102,4ммол) 70%-ной хлорной кислоты и в течение 45 минут закапывают 3,7мл (30,5ммол) циклогексанольдегида Перемешивают 2 часа при комнатной температуре, нейтрализуют содовым раствором и экстрагируют хлористым метиленом Органическую фазу промывают водой, сушат при помощи сульфата натрия и сгущают в вакууме (соотношение эпимеров в сыром продукте R/S=49/51) Остаток поглощают в теплом этаноле и кристаллизуют добавкой воды и охлаждением в ледяной бане методом дробной кристаллизации 1-я фракция 8,5г, соотношение эпимеров R/S=60/40 2-я фракция 2,5г, соотношение эпимеров R/S=27/73 Общий выход 11 г (88%) 9 0,5г (1,3ммол) 16—гидроксипреднизолона суспендируют при комнатной температуре в 20мл простого диизопропилового эфира и смешивают с 120мкл (1,56ммол) циклогексанальдегида и 440мкл (5,1ммол) 70%-ной хлорной кислоты После 45 минут реакционную смесь перемешивают со сложным этиловым эфиром уксусной кислоты и экстрагируют раствором бикарбоната натрия и водой Органическую фазу сушат при помощи сульфата магния и сгущают в вакууме Выход сырого продукта количественный, HPLC — содержание 95%, соотношение эпимеров R/S=57/43 10 2,0г (5,3ммол) 16—гидроксипреднизолона суспендируют при комнатной температуре в 20мл нитрометана и смешивают с 1,4мл (21,5ммол) метансульфокислоты и 0,78мл (6,4ммол) циклогексанальдегида Раствор перемешивают 3 часа при 40°С и разбавляют после охлаждения хлористым метиленом Реакционную смесь экстрагируют раствором бикарбоната натрия и водой, органическую фазу сушат при помощи сульфата натрия и сгущают в вакууме Остаток подвергают хроматографии как в примере 4 Выход 1,7г (68%), соотношение эпимеров R/S=85/15 11 5,0г (13,3ммол) 16—гидроксипреднизолона суспендируют в 50мл хлористого метилена, смешивают при охлаждении в ледяной бане с 3,45мл (53,1ммол) метансульфокислоты и в течение 10 минут закапывают 1,95мл (16,1ммол) циклогексанальдегида Оставляют до получения комнатной температуры и затем перемешивают 3 часа при 40°С Раствор экстрагируют водой, сушат при помощи сульфата натрия и сгущают в вакууме Выход сырого продукта количественный, HPLC — содержание 96%, соотношение эпимеров R/S=85/15 45311 8 12 10 0г (26,6ммол) 16— си—прегна —1,4—диен—3,20—диона (соединегидроксипреднизолона при охлаждении в ледяной ние 1, соотношение эпимеров R/S=60/40) раствобане суспендируют в 60мл 70%-ной хлорной киряют при 0°С в 240мл хлористого метилена, слоты и в течение 10 минут смешивают с 3,7мл смешивают с 8,7мл (101,1ммол) 70%-ной хлорной (30,5ммол) циклогексанальдегида кислоты и после 40 минут перемешивания добавляют на раствор бикарбоната натрия ЭкстрагиПосле 30-минутного перемешивания при охруют водную фазу хлористым метиленом, собранлаждении льдом подают на охлажденный льдом ные органические фазы водой и сушат при раствор бикарбоната натрия и экстрагируют сложпомощи сульфата магния После сгущения расным этиловым эфиром уксусной кислоты Органитворителя в вакууме рекуперируют количественно ческую фазу промывают раствором бикарбоната соединение 1 с соотношением эпимеров натрия и водой, сушат при помощи сульфата наR/S=90/10 (HPLC —содержание 98%) трия и сгущают в вакууме (соотношение эпимеров в сыром продукте R/S=93/7) 17 Разделение эпимеров (исходя из любой смеси эпимеров) можно осуществлять при помоОстаток очищают как в примере 8 1-я фракщи препаративной тонкослойной хроматографии ция 2,1 г, соотношение эпимеров R/S=94, 5/5, 5, 2HPLC следующим образом я фракция 6,56г, соотношение эпимеров R/S=96/4, 3-я фракция 1,29, соотношение эпимеПриборы, HP 1084B жидкостной хроматограф, ров R/S=91,5/8,5 HP 79850BLC терминал и ультрафиолетовый детектор, материал колонки гиперзил С18, 12мкм, Общий выход 9,95г (79,5%) 250x20 мм, растворитель для элюирования вода При соответствующем взаимодействии про(59%)/этанол (41%), длина волны детектора дуктов выделения в 50%или 35%-ной хлорной 242нм, концентрация пробы 220мг в бООмкл дикислоте в сыром продукте получают соотношение метил—сульфоксид + 3800мкл этанола, загрузочэпимеров R/S=95/5 или 81/19 ный объем 200мкл=10мг смеси эпимеров, поток 13 5,0г (13,3ммол) 16—гидроксипреднизолона Юмл/мин, температура печи 40°С, достигнутая при охлаждении в ледяной бане суспендируют в чистота R—эпимер 99,6%, S-эпимер 99,4% 80мл диоксана, смешивают с 2,5мл 85%-ной тетрафторборной кислоты в простом диэтиловом Соединения согласно изобретению имеют эфире и добавляют в течение 10 минут 1,95мл ценные фармакологические свойства, которые (16,1ммол) циклогексанальдегида дают возможность применять их в промышленности Обычно соединения согласно изобретению Перемешивают 1 час при комнатной темпераприменяют для лечения таких болезненных сотуре, затем выливают на раствор бикарбоната стояний, которые можно лечить стероидальными натрия и экстрагируют сложным этиловым эфипротивовоспалительными средствами Сюда отром ускусной кислоты Органическую фазу экстраносят, в первую очередь, заболевания кожи и дыгируют водой, сушат при помощи сульфата натрия хательных путей, а также воспалительные забои сгущают в вакууме Остаток хроматографируют левания кишечника и аллергические как в примере 4 риниты/конъюнктивиты Выход 4,0г (64%), отношение эпимеров R/S=47/53 В области кожи соединения согласно изобретению на основе своих противовоспалительных, 14 100мг (0,27ммол) 16— антипролиферативных, иммуноподавляющих, ангидроксипреднизолона суспендируют в 5мл ниттизудящих и сосудосуживающих свойств подходят рометана, смешивают с 50мкл 85%-ной тетрафдля (особенно местного) лечения дерматозов разторборной кислоты в простом диэтиловом эфире личного генеза Например, следует назвать али 35мкл (0,29ммол) циклогексанальдегида и перелергическую контактную экзему, атопическую экмешивают 15 часов при комнатной температуре зему, себорейную экзему, простой лишай, псориаз Соотношение эпимеров реакционной смеси (чешуйчатый лишай), солнечный ожог, зуд в обR/S=80/20, HPLC — содержание 96% Регулироласти гениталий, гнездная алоцеция, гипертрофивания соотношения эпимеров можно достигать ческие рубцы и дисковидная красная волчанка также нагреванием реационной смеси в течение 30 минут до 60°С В области дыхательных путей соединения согласно изобретению почти подавляют все проис15 2,0г (5,3ммол) 16—гидроксипреднизолона ходящие в стенке дыхательных путей воспалисуспендируют в 40мл диоксана, смешивают при тельные реакции, причем они тормозят охлаждении в водяной бане с 760мкл (6,3 ммол) пролиферацию, дифференцирование, миграцию и циклогексанальдегида и в течение 20 минут закаактивацию воспалительных клеток и образование пывают 15мл 14,8%-ного раствора хлористоводопростагландинов, лейкотриенов и ПАФ родного газа/диоксана После 2 часов перемешивания при 0°С и 2 чаБлагодаря этому соединения согласно изосов при комнатной температуре добавляют расбретению уменьшают бронхиальную гиперрактивтвор бикарбоната натрия и экстрагируют сложным ность, сокращают образование слизи, улучшают этиловым эфиром уксусной кислоты Органичеслизистый клиренс и усиливают (частично благоскую фазу промывают водой, сушат при помощи даря повышенной экспрессии р— сульфата натрия и сгущают в вакууме Остаток адренорецепторов) действие р— хроматографируют как в примере 4 симпатомиметических средств Выход 620мг (25%), соотношение эпимеров На основании этих свойств соединения соR/S=25/75 гласно изобретению, в первую очередь, применяют (в форме местных ингаляторов) для продолжи16 12,0г (25,5ммол) 16а, 17— тельного лечения бронхиальной астмы циклогексилметиленди-окси—11р, 2 1 — дигидрок 45311 Соединения согласно изобретению отличаются небольшой токсичностью, в основном, топической эффективностью, большим терапевтическим диапазоном, длительным действием и отсутствием существенных побочных явлений Эффективность соединений согласно изобретению делает возможным их применение в гуманной и ветеринарной медицине Поэтому другим предметом изобретения является способ лечения млекопитающих, включая людей, страдающих одной из вышеназванных болезней Способ отличается тем, что заболевшему млекопитающему назначают терапевтически эффективное и фармакологически переносимое количество одного или нескольких соединений согласно изобретению Следующим предметом изобретения являются соединения согласно изобретению для применения при лечении и/или для профилактики названных заболеваний Изобретение относится также к применению соединений согласно изобретению для изготовления лекарственных средств, которые используют для лечения и/или для профилактики названных заболеваний Далее, предметом изобретения являются лекарственные средства для лечения и/или профилактики названных заболеваний, которые содержат одно или несколько соединений согласно изобретению Для лечения дерматозов соединения согласно изобретению применяют особенно в форме таких лекарственных средств, пригодных для топического применения Для изготовления лекарственных средств соединения согласно изобретению ( = активнодействующие вещества) смешивают преимущественно с подходящими фармацевтическими вспомогательными веществами и перерабатывают в соответствующие лекарственные формы В качестве подходящих лекарственных форм следует назвать, например, пудру, эмульсии, суспензии, аэрозоли, масла, мази, жирные мази, кремы, пасты, гели или растворы Какие вспомогательные вещества для желательных лекарственных форм пригодны, специалисту известно на основании его специальных знаний Наряду с растворителями, гелеобразователями, основами мазей и другими носителями активного вещества можно применять, например, антиокислители, диспергаторы, эмульгаторы, консерванты, агенты растворения или промоторы проницания Для лечения заболеваний дыхательных путей соединения согласно изобретению применяют преимущественно как ингаляторы Для этого их назначают или непосредственно как порошки (преимущественно в микронизированной форме) или распылением растворов или суспензий, которые их содержат Относительно лекарственных 10 форм и форм введения ссылаются, например, на разъяснения в европейском патенте 163 965 Лекарственные средства согласно изобретению изготовляют известными способами Дозировка активных веществ имеет обычный для сильно эффективных глюкокортикоидов порядок величины Так, топические формы применения (как например, мази) для лечения дерматозов содержат активные вещества в концентрации, например, 0,1-1% Доза для применения при ингаляции составляет обычно между 0,2 и 2мг в день Обычная (поддерживающая) доза при систематической терапии составляют около 10мг в день, причем в случае тяжелых приступов астмы и особенно при астматическом состоянии можно применять также повышенные дозы (например, 250—500мг внутривенно) Фармакологические данные Проведение опытов для определения местного и систематического действия испытываемых соединений на образование грануляционных тканей после ватной имплантации у крысы (методом с хлопчатобумажной гранулой) Sprague—Dawley—крысам мужского пола (соответственно 8-16 животных на одну дозу, вес каждого животного 180-230г) имплантируют при изофлуран-наркозе и при стерильных условиях в области лопатки с обеих сторон по 1 ватному шарику (изготовитель фирма Хартманн/Хайденхайм, ватный шарик размера 2,N4865/2) 13,0±0, мг, подкожно Перед началом опыта в предусмотренные для имплантации в левую сторону тела ватные шарики капают соответственно спиртовые растворы (0,05мл/шарик, 96%-ный спирт) испытываемых соединений К моменту имплантации шарики становятся сухими, т е вещества осаждаются на нитях ваты Шарики правой стороны тела имплантируются без обработки В течение 7 дней по причине раздражения инородным телом образуются гранулемы Последние - на 8-й день осторожно, т е при щажении соединительнотканной капсулы, полностью удаляют из умертвленных животных, сушат (15 часов при 120°С) и взвешивают Вычитанием весовой доли ватных шариков получают количество новообразованной грануляционной ткани Критерием для антипролиферативного действия соединения служит снижение в процентном отношении среднего веса гранулемы в сухом состоянии обработанной группы по сравнению с контрольной группой (= 100%) На левой гранулеме наблюдают местное, на правой - систематическое действие Для регистрации систематического действия кортикоидов определяли также сырые веса вилочковой железы и надпочечника 11 45311 12 Таблица Антипролиферативное действие соединений по изобретению после местного назначения в модели хронического воспаления измеренное по влиянию на образование грануляционной ткани после ватной имплантации (так называемый тест с хлопчатобумажным шариком) Доза 1х (мг на животное) местная* Соединение 1а 16 0,2 0,2 Торможение образования грануляционной ткани % 69 32 Р (значимость) < 0,001 < 0,001 *) капают в левый шарик (1) ДП «Український інститут промислової власності» (Укрпатент) вул Сім'ї Хохлових, 15, м Київ, 04119, Україна (044)456-20- 90 ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)216-32-71 п (количество животных) 8 8
ДивитисяДодаткова інформація
МПК / Мітки
МПК: A61P 27/02, A61P 29/00, A61P 11/00, C07J 71/00, A61P 1/04, A61K 31/58
Мітки: спосіб, 16a,17-циклогексилметилендіокси-11b,21-дигідроксипрегна-1,4-дієн-3,20-діон, одержання, засіб, лікарський
Код посилання
<a href="https://ua.patents.su/6-45311-16a17-ciklogeksilmetilendioksi-11b21-digidroksipregna-14-diehn-320-dion-sposib-jjogo-oderzhannya-likarskijj-zasib.html" target="_blank" rel="follow" title="База патентів України">16a,17-циклогексилметилендіокси-11b,21-дигідроксипрегна-1,4-дієн-3,20-діон, спосіб його одержання, лікарський засіб</a>
Попередній патент: Гідравлічний пристрій натягування болтів
Наступний патент: Спосіб виготовлення металевого магнію, спосіб виготовлення оксиду магнію (варіанти) і спосіб виготовлення вогнетривкого матеріалу на основі оксиду магнію
Випадковий патент: Спосіб обробки зубців черв'ячних коліс