Дигідрохлориди (3-карбоксамідино-2-оксо-2н-хромен-7-іл)-4-гуанідинобензоатів, які виявляють властивості блокаторів рн-чутливих іонних каналів
Номер патенту: 66987
Опубліковано: 25.01.2012
Автори: Сукач Володимир Андрійович, Кришталь Олег Олександрович, Бута Андрій Зеновійович, Максимюк Олександр Петрович, Вовк Михайло Володимирович
Формула / Реферат
Дигідрохлориди (3-карбоксамідино-2-оксо-2Н-хромен-7-іл)-4-гуанідинобензоатів загальної формули :
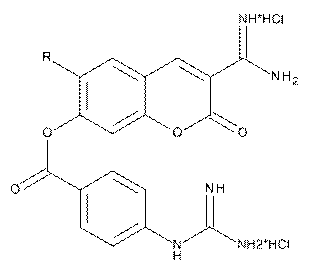 ,
,
де R=H (І), Сl (II), Et (III),
які виявляють властивості блокаторів рН-чутливих іонних каналів.
Текст
УКРАЇНА (19) UA (11) 66987 (13) U (51) МПК C07D 311/06 (2006.01) C07D 311/16 (2006.01) A61K 31/37 (2006.01) ДЕРЖАВНА СЛУЖБА ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ УКРАЇНИ видається під відповідальність власника патенту ОПИС ДО ПАТЕНТУ НА КОРИСНУ МОДЕЛЬ (54) ДИГІДРОХЛОРИДИ (3-КАРБОКСАМІДИНО-2-ОКСО-2Н-ХРОМЕН-7-ІЛ)-4-ГУАНІДИНОБЕНЗОАТІВ, ЯКІ ВИЯВЛЯЮТЬ ВЛАСТИВОСТІ БЛОКАТОРІВ рН-ЧУТЛИВИХ ІОННИХ КАНАЛІВ 1 2 NH*HCl R NH2 O O O NH O N H NH2*HCl , де R=H (І), Сl (II), Et (III), які виявляють властивості блокаторів рН-чутливих іонних каналів. O O O NH O N H NH2*HCl , де R=H (І), Сl (II), Et (III). Запропоновані нові сполуки, спосіб їх отримання, властивості і застосування в науковій літературі та патентних виданнях не описані. (11) NH2 UA R Відомо, що клітини нервової системи більш чутливі до негативного впливу ішемії, ніж клітини інших тканин. Явище ішемії при інсульті головного мозку швидко викликає нейродегенерацію і пов'язані з нею патології. Авторами дослідження [1] встановлено, що активація рН-чутливих іонних каналів (ASIC), а саме підтипу ASIC la, внаслідок ішемічного ацидозу є головною причиною ураження нейронів головного мозку. При цьому нейротоксичний ефект досягається за рахунок підвищення концентрації іонів кальцію, які здатні проникати через іонний канал даного підтипу. Раніше вважалось, що основним джерелом 2+ нагромадження внутрішньоклітинних іонів Са в таких процесах є N-метил-D-аспартат (NMDA) рецептори та потенціалкеровані кальцієві канали, однак часове терапевтичне вікно їх антагоністів становить лише 30 хв, що практично унеможливлює терапію ішемічного ураження, в зв'язку з чим виявлена роль ASIC як кальцієвих каналів набула ще більш важливого значення. Саме тому контроль над функціонуванням рН-чутливих іонних каналів в центральній нервовій системі відкриває (19) Корисна модель належить до органічної хімії, а саме до нових похідних (3-карбоксамідино-2оксо-2H-хромен-7-іл)-4-гуанідинбензоатів загальної формули: NH*HCl 66987 (13) U (21) u201108744 (22) 12.07.2011 (24) 25.01.2012 (46) 25.01.2012, Бюл.№ 2, 2012 р. (72) СУКАЧ ВОЛОДИМИР АНДРІЙОВИЧ, ВОВК МИХАЙЛО ВОЛОДИМИРОВИЧ, МАКСИМЮК ОЛЕКСАНДР ПЕТРОВИЧ, БУТА АНДРІЙ ЗЕНОВІЙОВИЧ, КРИШТАЛЬ ОЛЕГ ОЛЕКСАНДРОВИЧ (73) ІНСТИТУТ ОРГАНІЧНОЇ ХІМІЇ НАН УКРАЇНИ, ІНСТИТУТ ФІЗІОЛОГІЇ ІМ. О.О. БОГОМОЛЬЦЯ НАН УКРАЇНИ (57) Дигідрохлориди (3-карбоксамідино-2-оксо-2Нхромен-7-іл)-4-гуанідинобензоатів загальної формули : 3 66987 4 нові перспективи для лікування патологічних наслідків ішемічного інсульту. Зважаючи на вагому роль ASIC в фізіологічних та патологічних процесах, пошук їх блокаторів є актуальною проблемою як фундаментальної фізіології, так і медицини. Найближчими аналогами за фармакологічною дією сполук, які заявляються, є амілорид - відомий діуретик з широким спектром блокувальної дії на натрієві іонні канали [2]. Природний токсин РсТХ1, виділений з отрути павука-птахоїда Psalmopoeus Cambridgei, є сильним селективним блокатором ASIC la, але має складну будову та обмежену доступність [3]. В останні роки інгібуючі властивості по відношенню до ASIC рецепторів знайдені серед важкодоступних похідних 7-алкініл-2нафтиламідину виробництва компанії Merck [4]. Для антикоагулянта нафамостата виявлений побічний ефект блокування ASIC1a і ASIC3 [5]. Селективні антагоністи серед названих препаратів не відомі. O NH Cl N Амілорид NH2 O O N N H H2 N , NH NH2 NH2 , NH N NH2 H Нафамостат . Задачею корисної моделі є дизайн та синтез нових ефективних сполук з вираженими властивостями до блокування рН-чутливих іонних каналів. Вирішення поставленої задачі досягається синтезом нових похідних (3-карбоксамідино-2-оксо2H-хромен-7-іл)-4-гуанідинбензоату. Для одержання зазначених сполук нами розроблена препаративно зручна 4-стадійна схема, яка базується на використанні доступних формілрезорцинів і передбачає низку наступних послідовних перетворень: NCCH2COOEt AcONH4 EtOH, 78oC NH3 HCl діізопропілкарбодіімід ДМФА I-III де R=H (І), Сl (II), Et (III). Схема ілюструється прикладами синтезу проміжних та цільових сполук, структура яких підтверджена аналітичними даними та результатами ви1 мірів ІЧ - та ЯМР Н спектрів. Загальний спосіб одержання гідрохлоридів 7гідрокси-2-оксо-2Н-хромен-3-карбоксамідинів. До розчину 5,46 ммоль 2,4-дигідрокси-5-Rбензальдегіду в 15 мл етанолу послідовно дода -EtOH , ють 1,0 г (5,46 ммоль) етилціаноацетату та 1,26 г (16,38 ммоль) ацетат амонію, кип'ятять протягом 10 хв. та охолоджують до кімнатної температури. Отриманий осад відфільтровують, промивають етанолом, суспендують в 10 мл води, до суспензії додають 20 мл розчину хлористоводневої кислоти концентрації 1 моль/л і суміш перемішують 1 год. при кімнатній температурі. Осад відфільтровують, 5 промивають 10 мл води та висушують у вакуумі водноструменевого насосу при температурі 90 °C. Приклад 1. Гідрохлорид 7-гідрокси-2-оксо-2Н-хромен-3карбоксамідину. Вихід 72 %, т. пл. 291-295 °C. ІЧ -1 спектр, KBr, v, см : 1735 (СО), 3330-3355 (N-H), 1 -1 3440 (ОН). Спектр ЯМР Н, DMSO-d6, δ, млн : 7,50 (с, 1Н), 7,56 (с, 1Н), 8,02 (с, 1Н), 8,88 (с, 1H), 9,50 (с, 4Н), 11,20 (с, 1H). Знайдено, %: С 50,07; Н 3,63; N 11,40. С10Н9СlN2О3. Вирахувано, %: С 49,89; Н 3,77; N 11,65. Приклад 2. Гідрохлорид 7-гідрокси-2-оксо-6-хлоро-2Нхромен-3-карбоксамідину. Вихід 75 %, т. пл. -1 >300 °C. ІЧ спектр, KBr, v, см : 1730 (С=О), 33201 3350 (N-Н), 3450 (ОН). Спектр ЯМР Н, DMSO-d6, -1 δ, млн : 7,53 (с, 1H), 8,14 (с, 1Н), 8,95 (с, 1Н), 9,44 (с, 4Н), 11,25 (с, 1Н). Знайдено, %: С 43,70; Н 3,11; N 11,42. C10H8Cl2N2O3. Вирахувано, %: С 43,63; Н 2,93; N 11,65. Приклад 3. Гідрохлорид 7-гідрокси-2-оксо-6-етил-2Нхромен-3-карбоксамідину. Вихід 75 %, т. пл. 285-1 290 °C. ІЧ спектр, KBr, v, см : 1730 (С=О), 33201 3340 (N-H), 3460 (ОН). Спектр ЯМР Н, DMSO-d6, -1 δ, млн : 1,02 (т, 3Н), 2,48 (кв, 2Н), 7,53 (с, 1H), 8,14 (с, 1Н), 8,95 (с, 1Н), 9,44 (с, 4Н), 11,25 (с, 1Н). Знайдено, %: С 53,88; Н 4,75; N 10,55. С12Н13СlN2О3. Вирахувано, %: С 53,64; Н 4,88; N 10,43. Загальний спосіб одержання дигідрохлоридів (3-карбоксамідино-2-оксо-6R-2Н-хромен-7-іл)-4гуанідинбензоатів. До розчину 2,08 ммоль гідрохлориду 7гідрокси-2-оксо-2H-хромен-3-карбоксамідину в 5 мл сухого диметилформаміду при перемішуванні при 40 °C додають розчин 0,45 г (2,08 ммоль) 4гуанідинбензойної кислоти в 5 мл сухого ДМФА, а потім 1,1 мл діізопропілкарбодііміду. Суміш перемішують 24 год. при кімнатній температурі, розбавляють 2 мл сухого ацетонітрилу та перемішують додатково 6 год. Утворений осад відфільтровують, промивають сухим ДМФА, ацетонітрилом та висушують при 70 °C. Приклад 4. Дигідрохлорид (3-карбоксамідино-2-оксо-2Нхромен-7-іл)-4-гуанідин-бензоату. Вихід 67 %, т.пл. -1 235-237 °C. ІЧ спектр, KBr, v, см : 1730-1740 (ОО), 1 3350-3380 (N-H). Спектр ЯМР Н, DMSO-d6, δ, млн 1 : 7,45-7,51 (м, 3Н), 7,67 (с, 1Н), 7,94-8,05 (м, 5Н), 8,19 (д, J=8,0, 2Н), 8,90 (с, 1Н), 9,50 (с, 4Н), 10,80 (с, 1Н). Знайдено, %: С 49,62; Н 4,05; N 16,23. C18H17Cl2N5O4. Вирахувано, %: С 49,33; Н 3,91; N 15,98. Приклад 5. Дигідрохлорид (3-карбоксамідино-2-оксо-6хлоро-2Н-хромен-7-іл)-4-гуанідин-бензоату. Вихід -1 69 %, т.пл. 249-253 °C. ІЧ спектр, KBr, v, см : 17351 1740 (С=О), 3350-3390 (N-H). Спектр ЯМР Н, -1 DMSO-d6, δ, млн : 7,50-7,58 (м, 3Н), 7,90-8,17 (м, 5Н), 8,15-8,18 (м, 2Н), 8,90 (с, 1Н), 9,45-9,53 (м, 4Н), 10,73 (с, 1Н). Знайдено, %: С 45,92; Н 3,33; N 17,61. Q18H16Cl3N5O4. Вирахувано, %: С 45,74; Н 3,41; N 14,82. 66987 6 Приклад 6. Дигідрохлорид (3-карбоксамідино-2-оксо-6етил-2Н-хромен-7-іл)-4-гуанідин-бензоату. Вихід -1 65 %, т.пл. 218-220 °C. ІЧ спектр, KBr, v, см : 17401 1745 (С=О), 3345-3385 (N-H). Спектр ЯМР Н, -1 DMSO-d6, δ, млн : 1,11 (т, 3Н), 2,55 (кв, 2Н), 7,518,17 (м, 10Н), 8,90 (с, 1H), 9,56 (с, 4Н), 10,64 (с, 1Н). Знайдено, %: С 51,77; Н 4,40; N 14,83. C20H21Cl2N5O4. Вирахувано, %: С 51,49; Н 4,54; N 15,02. рН-чутливі іонні канали є так званими "рецепторами до протонів", що активуються при зниженні рН середовища та експресуються у багатьох типах клітин, зокрема у нейронах центральної (ЦНС) та периферійної (ПНС) нервових систем [7, 8]. Активація ASIC каналів спричиняє транзіентний іонний трансмембранний струм, що спадає протягом декількох секунд навіть за умов підтримання кислого середовища внаслідок процесу десенситизації рецептора. Не дивлячись на багаторічні дослідження, механізми відкриття рН-чутливого іонного каналу, його переходу в непроникний для іонів і вихідний чутливий стан наразі залишаються нез'ясованими. Всього ідентифіковано чотири гени, котрі кодують ASIC канали, формуючи загалом зі сплайсинговими варіантами шість підтипів субодиниць ASIC каналів. Залежно від підтипу, ASIC локалізуються як в периферичній, так і в центральній нервовій системі і відрізняються функціональними властивостями та виконують різну фізіологічну роль. Найбільш поширеним підтипом в ПНС є ASIC3, тоді як в ЦНС переважно експресуються ASIC1a. При дослідженні пригнічення струмів, викликаних активацією рН-чутливих іонних каналів у присутності 5 мкмоль/л дигідрохлоридів (3карбоксамідино-2-оксо-2Н-хромен-7-іл)-4гуанідинбензоатів (І-ІІІ) знайдено, що сполука (І) викликає найбільш значне оборотне зменшення інтенсивності іонного трансмембранного струму (Фіг. 1, таблиця 1). Значення концентрації половинного пригнічення (ІС50) активованих струмів ASIC la для неї становить 7,0 мкмоль/л. ІС50 блокування струмів підтипу ASIC3 становить 12,7 мкмоль/л (Фіг. 2). Для нафамастату величина ІС 50 сягає відповідно 13,5 та 2,5 мкмоль/л [5]. Таким чином блокувальна дія сполук (І-ІП) на рН-чутливі іонні канали перевищує рівень відомого аналога - нафамастату по відношенню до підтипу ASIC1a. Знайдені антагоністи можуть бути прототипами для створення принципово нових високоефективних нейропротекторних лікарських засобів. Приклад 7. Дослідження блокувальної дії дигідрохлоридів (3-карбоксамідино-2-оксо-2Н-хромен-7-іл)-4гуанідино-бензоатів (І-ІІІ) на рН-чутливі іонні канали. Вимірювання струмів проводилося за методом фіксації потенціалу в режимі відведення від цілої клітини. Протон-активовані струми викликались прикладанням розчину Рінгера (рН=5.0), а також при потребі рН активаційного розчину змінювали (з 5,0 до 6,0-6,7). Струми реєструвались за підт 7 66987 римуваного потенціалу у мінус 60 мВ. Скляні мікропіпетки (опір 2-3 мОм) заповнювались розчином, що містив (у ммоль/л): фториду калію 120; Tris-Cl 20 (рН доводився до значення 7.3 за допомогою гідроксиду калію). В ролі зовнішньоклітинного розчину використовувався фізіологічний розчин Рінгера (рН=7,35). Експерименти проводились при кімнатній температурі (20±2)°С. Усі хімічні реагенти, що використовувалися під час експериментів, вироблені компанією Sigma (США). Скринінг речовин проводився методом фіксування потенціалу у конфігурації "ціла клітина". При переході з кондиціонуючого розчину з рН=7,35 (розчин Рінгера) до активаційного розчину з рН=5,0 (кислий розчин Рінгера) (швидкість зміни розчину ~ 50 мс) при підтримуваному внутрішньоклітинному потенціалі мінус 60 мВ спостерігалась активація рН-чутливих іонних каналів у вигляді трансмембранних струмів амплітудою 400-800 (для ASIC1a) та 1000-5000 пА (для ASIC3), які швидко десенситизувались (протягом 3-5 с). Дослідження дії речовин проводилось на гомомерних ASIC1a-іонних каналах людських ембріональних ниркових клітин (НЕК-293) і на нативних ASIC3іонних каналах нейронів задньо-корінцевих гангліїв щура (DRG), котрі були підкультивовані 1-2 дні. Зовнішньоклітинний розчин містив: 130 ммоль/л хлориду натрію; 2 ммоль/л хлориду кальцію; 5 ммоль/л хлориду калію; 2 ммоль/л хлориду магнію, 10 HEPES; рН=7,5 при температурі (25±1)°С доведений розчином гідроксиду натрію з масовою часткою основної речовини 5 %. Склад активаційного розчину аналогічний кондиціонуючому, за винятком буфера (HEPES замінювався на MES), а рН=5,0 при температурі (25±1)°С доведений розчином гідроксиду натрію (при потребі до 6,0 або 6,7). Піпетки заповнювалися внутрішньоклітинним розчином наступного складу (у ммоль/л): 20 TrisCl, 120 фториду калію; рН 7,3 при температурі (25,0±0,5)°С доведений водним розчином гідрок 8 сиду калію з масовою часткою основної речовини 5 %. Джерела інформації:: [1] Xiong Z.-G., Zhu X.-M., Chu X.-P., Minami M., Hey J., Wei W.-L., MacDonald J.F., Wemmie J.A., Price M.P., Welsh M.J., Simon R.P… Neuroprotection in Ischemia: Blocking Calcium-Permeable AcidSensing Ion Channels // Cell-2004. - Vol. 118. - P. 687-698. [2] Korkushko A.O., Kryshtal O.A. Blocking of proton-activated sodium permeability of the membranes of trigeminal ganglion neurons in the rat by organic cations [//Neirofiziologiia.-1984. - Vol. 16, № 4. - P. 557-561. [3] Escoubas P., Bernard C., Lambeau, Lazdunski G.M., Darbon H. Recombinant production and solution structure of PcTx1, the specific peptide inhibitor of ASIC la proton-gated cation channels // Protein Sci.-2003. - Vol. 12, - P. 1332-1343. [4] Kuduk S.D., Di Marco С.N., BodmerNarkevitch V., Cook S.P., Cato M.J. Synthesis, Structure-Activity Relationship, and Pharmacological Profile of Analogs of The ASIC-3 Inhibitor A-317567 // ACS Chem. Neurosci.-2010. - Vol. 1, № 1. - P. 19-24. [5] Ugawa S., Ishida Y., Ueda Т., Inoue K., Nagao M., Shimada S. Nafamostat mesilate reversibly blocks acid-sensing ion channel currents // Biochem. and Biophys. Res. Commun.-2007. - Vol. 363. - P. 203-208. [6] Jasti J., Furukawa H., Gonzales E.В., Goimux E. Structure of acid-sensing ion channel 1 at 1.9 A resolution and low pH // Nature.-2007. - Vol. 449. - P. 316-323. [7] Krishtal O. The ASICs: Signaling molecules? Modulators? // TRENDS in Neurosciences.-2003. Vol. 26, № 9. - P. 477-483. [8] Xiong Z.-G., Pignataro G., Li M., Chang S.-Y., Simon R. P. Acid-sensing ion channels (ASICs) as pharmacological targets for neurodegenerative diseases // Curr. Opinion in Pharm.-2007. - Vol. 7. P. 1-8. Таблиця 1 Пригнічення струмів ASIC1a та ASIC3 типів у присутності розчину сполук (І-ІІІ) з концентрацією 5 мкмоль/л Сполука (5 мкмоль/л) І II III Залишковий струм ASIC1а (%) 48 51 53 Залишковий струм ASIC3 (%) 53 53 60 9 66987 10 11 Комп’ютерна верстка Г. Паяльніков 66987 Підписне 12 Тираж 23 прим. Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюDihydrochlorides of (3-carboxamidino-2-oxo-2h-chromen-7-yl)-4-guanidine benzoates exhibiting properties of ph-sensitive ion channel blockers
Автори англійськоюSukach Volodymyr Andriiovych, Vovk Mykhailo Volodymyrovych, Maksimiuk Oleksandr Petrovych, Buta Andrii Zenoviiovych, Kryshtal Oleh Oleksandrovych
Назва патенту російськоюДигидрохлориды (3-карбоксамидино-2-оксо-2н-хромен-7-ил)-4-гуанидинобензоатов, которые проявляют свойства блокираторов рн-чувствительных ионных каналов
Автори російськоюСукач Владимир Андреевич, Вовк Михаил Владимирович, Максимюк Александр Петрович, Бута Андрей Зеновиевич, Кришталь Олег Александрович
МПК / Мітки
МПК: A61K 31/37, C07D 311/06, C07D 311/16
Мітки: каналів, властивості, 3-карбоксамідино-2-оксо-2н-хромен-7-іл)-4-гуанідинобензоатів, іонних, блокаторів, дигідрохлориди, рн-чутливих, виявляють
Код посилання
<a href="https://ua.patents.su/6-66987-digidrokhloridi-3-karboksamidino-2-okso-2n-khromen-7-il-4-guanidinobenzoativ-yaki-viyavlyayut-vlastivosti-blokatoriv-rn-chutlivikh-ionnikh-kanaliv.html" target="_blank" rel="follow" title="База патентів України">Дигідрохлориди (3-карбоксамідино-2-оксо-2н-хромен-7-іл)-4-гуанідинобензоатів, які виявляють властивості блокаторів рн-чутливих іонних каналів</a>
Попередній патент: Пристрій для визначення дихання зерна
Наступний патент: Спосіб одержання етилових естерів 7-r-3,5-діоксо-1,2,6,7-тетрагідроімідазо[1,5-с]піримідин-8-карбонової кислоти
Випадковий патент: Композиція інгредієнтів для бальзаму "бахмут"










