Спосіб одержання похідних 5-метил-3,6-ді-(арилкарбоксамідо)-4,7-дигідропіразоло[1.5-а]піримідинів
Номер патенту: 81081
Опубліковано: 26.11.2007
Автори: Афанасіаді Людмила Михайлівна, Комихов Сергій Олександрович, Петрова Марина Генадіївна, Десенко Сергій Михайлович, Борівський Валерій Олександрович
Формула / Реферат
Спосіб одержання похідних 5-метил-3,6-ді-(арилкарбоксамідо)-4,7-дигідропіразоло[1,5-а]піримідинів загальної формули І:
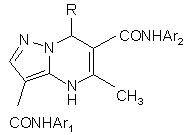 ,
,
де R - С6Н5, iзo-C4H8, iзo-C5H10, 4-Вr-С6Н4, 4-Сl-С6Н4, 4-C5H4N, 3-СН3-С6Н4, 4-СН3-С6Н4, 4-ОС2Н5-С6Н4, 4-F-С6Н4, 2-Сl-С6Н4, 2-F-С6Н4, 4-ОСН3-С6Н4, 4-NO2-С6Н4, 3-NO2-С6Н4, 2,3-діОСН3-С6Н3, 3,4-діОСН3-С6Н3, 2-F-5-Вr-С6Н3, 3-Сl-С6Н4, 2,4-дiОСН3-С6Н3, 2-СН3-С6Н4, 4-С2Н5-С6Н4, 2,5-діОСН3-С6Н3, 3-ОСН3-4-ОС2Н5-С6Н3;
Аr1 - С6Н5, 3-СН3-С6Н4, 4-СН3-СбН4, 4-ОС2Н5-С6Н4, 4-F-С6Н4, 2-СН3-С6Н4, 4-Сl-С6Н4, 2,4-диСН3-С6Н3;
Аr2 - С6Н5, 2-ОСН3-С6Н4, 4-ОСН3-С6Н4, 2,4-диСН3-С6Н3, 4-Сl-С6Н4,
що включає конденсацію 3-амінопіразолу, відповідної карбонілметиленової похідної та альдегіду в середовищі розчинника при кипінні протягом часу, необхідного для утворення продукту і його виділення, який відрізняється тим, що як 3-амінопіразол використовують 4-(N-арилкарбоксамідо)-3-аміно-1Н-піразол, як карбонілметиленову похідну - ариламіди ацетооцтової кислоти та як альдегід - відповідний заміщений аліфатичний або ароматичний альдегід, конденсацію проводять в середовищі основного розчинника – диметилформаміду, протягом 15-20 хвилин до повного зневоднення реакційної маси і утворення відповідної похідної, а виділення одержаної похідної здійснюють етиловим спиртом.
Текст
Спосіб одержання похідних 5-метил-3,6-ді(арилкарбоксамідо)-4,7-дигідропіразоло[1,5а]піримідинів загальної формули І: R N H CH3 , Винахід відноситься до області органічної хімії, а саме, до способу одержання похідних 5-метил3,6-ді-(арилкарбоксамідо)-4,7-дигідропіразоло[1,5а]піримідинів (19) UA CONHAr1 де R - С6Н5, iзo-C4H8, iзo-C5H10, 4-Вr-С6Н4, 4-СlС6Н4, 4-C5H4N, 3-СН3-С6Н4 , 4-СН3-С6Н4, 4-ОС2Н5С6Н4, 4-F-С6Н4, 2-Сl-С6Н4, 2-F-С6Н4, 4-ОСН3-С6Н4, 4-NO2-С6Н4, 3-NO2-С6Н4, 2,3-діОСН3-С6Н3, 3,4діОСН3-С6Н3, 2-F-5-Вr-С6Н3, 3-Сl-С6Н4, 2,4-дiОСН3С6Н3, 2-СН3-С6Н4, 4-С2Н5-С6Н4, 2,5-діОСН3-С6Н3, 3ОСН3-4-ОС2Н5-С6Н3; Аr1 - С6Н5, 3-СН3-С6Н4, 4-СН3-СбН4, 4-ОС2Н5-С6Н4, 4-F-С6Н4, 2-СН3-С6Н4, 4-Сl-С6Н4, 2,4-диСН3-С6Н3; Аr2 - С6Н5, 2-ОСН3-С6Н4, 4-ОСН3-С6Н4, 2,4-диСН3С6Н3, 4-Сl-С6Н4, що включає конденсацію 3-амінопіразолу, відповідної карбонілметиленової похідної та альдегіду в середовищі розчинника при кипінні протягом часу, необхідного для утворення продукту і його виділення, який відрізняється тим, що як 3-амінопіразол використовують 4-(Nарилкарбоксамідо)-3-аміно-1Н-піразол, як карбонілметиленову похідну ариламіди ацетооцтової кислоти та як альдегід - відповідний заміщений аліфатичний або ароматичний альдегід, конденсацію проводять в середовищі основного розчинника – диметилформаміду, протягом 15-20 хвилин до повного зневоднення реакційної маси і утворення відповідної похідної, а виділення одержаної похідної здійснюють етиловим спиртом. (11) CONHAr 2 N N 2 C2 ПОХІДНИХ (13) (54) СПОСІБ ОДЕРЖАННЯ ДИГІДРОПІРАЗОЛО[1.5-А]ПІРИМІДИНІВ ОПИС 81081 ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ R CONHAr 2 N N N H CONHAr1 CH3 I 3 81081 R=С6Н5, iso-C4H8, iso-C5H10, 4-Вr-С6Н4, 4-СlС6Н4, 4-C5H4N, 3-СН3-С6Н4 4СН3-С6Н4, 4-ОС2Н5-С6Н4, 4-F-С6Н4, 2-Сl-С6Н4, 2-F-С6Н4, 4-ОСН3-С6Н4, 4NO2-С6Н4, 3-NO2-С6Н4, 2,3-diОСН3-С6Н3, 3,4diОСН3-С6Н3, 2-F-5-Вr-С6Н3, 3-Сl-С6Н4, 2,4-diОСН3-С6Н3, 2-СН3-С6Н4, 4-С2Н5-С6Н4, 2,5dіОСН3-С6Н3, 3-ОСН3-4ОС2Н5-С6Н3, Аr1=С6Н5, 3-СН3-С6Н4, 4-СН3-СбН4, 4-ОС2Н5С6Н4, 4-F-С6Н4, 2-СН3-С6Н4, 4-Сl-С6Н4, 2,4-dіСН3-С6Н3 Аr2=С6Н5, 2-ОСН3-С6Н4, 4-ОСН3-С6Н4, 2,4-diСН3-С6Н3, 4-Сl-С6Н4, Ці сполуки є такими азотвмісними гетероциклічними сполуками, що виконують важливу роль в біоенергетиці людського організму, володіють різноманітними видами фізіологічної активності і можуть знайти застосування як лікарські препарати [Т. Yasuda, Т. Jwamoto, M. Ohara, S. Sato, Jap. J. Pharmacol, 79, 65(1999); G. Yang, R. Lu, X. Fei, H. Yang, Chin. J. Chem., 18, 435(2000); К. Tahir, H. Khamees, S. Bayomi, Bull. Chem.Farm., 134, 604(1995)]. Відомий спосіб одержання 5-метил-6-Rоксикарбоніл-7-(2-трифторметилфеніл)-4,7дигідропіразоло[1,5-а]піримідину [Яп. патент 62077387, 1987, CO7D 487/04]. Ці сполуки використовуються для одержання лікарських препаратів, що поліпшують загальну серцеву функцію, мозковий кровообіг, церебральну циркуляцію, надають м'яку гіпотензивну дію. Спосіб складається з трьох реакційних стадій і реалізується за наступною схемою: 4 Час реакції приблизно 10-12 годин. Одержаний продукт - R-заміщений ефір 2ацетил-3-амінопіразол-2-іл-3-[(2трифторметилфеніл)пропіонової кислоти циклізують в середовищі хлороформу протягом 6 годин при кипінні реакційної маси. Продукт хроматографують на силікагелі в суміші хлороформ:метанол; закристалізовують масло, що утворилося, за допомогою діїзопропілового ефіру і перекристалізовують із спирту. Час реакції на третій стадії складає приблизно 10-12 годин. Загальний час синтезу 5-метил-6-Rоксикарбоніл-7-(2-трифторметилфеніл)-4,7дигідропіразоло[1,5-а]піримідинів складає приблизно 38-44 години. Недоліком відомого способу є тривалий, багатостадійний, трудомісткий процес, пов'язаний з виділенням напівпродуктів на кожній технологічній стадії та їх очищенням. Крім того, використання легкозаймистих розчинників (бензол, ефір), подразників слизових оболонок, органів дихання (оцтова кислота, піридин) і шкіри (ацетооцтовий ефір) обмежує використання відомого методу в лабораторних і виробничих умовах. Вихід кінцевого продукту з урахуванням виходів на кожній технологічній стадії складає 18%. Відомий спосіб одержання 7-заміщених-5метил-6-етоксикарбоніл-4,7-дигідропіразоло-[1,5-а] піримідинів (III)[О.В. Федорова, М.С. Жидовинова, Г.Л. Русинов, И.Г. Овчинникова, Изв. РАН, сер. химическая, №8, с. 1667-1678 (2003)]. R CF3 CH3 CH2 COOR CF3 O H CH3COOH,piridine, benzol O COCH3 CF3 NH2 R1 O COCH3 NH2 OR N H OR N N CH3CN COOEt N N N N R1 CH3 III Спосіб одержання сполуки III здійснюється за схемою: CF3 COOR N N R1 N H CH3 N EtOOC На першій стадії взаємодією ацетооцтового ефіру з 2-(трифторметил)-бензальдегідом, оцтовою кислотою, піридином в середовищі бензолу одержують R-заміщений ефір 2-[(2трифторметилфеніл)ацетил-1-метилен]-3оксобутанової кислоти протягом 10 годин. З урахуванням водовідділення, промивання розчином NaCI і сушки над безводним Na2SO4 загальний час реакції на першій стадії приблизно 18-20 годин. На другій стадії R-заміщений ефір, що утворився, конденсують з 4-заміщеним 5амінопіразолом в середовищі ацетонітрилу протягом 3 годин при 50°С, а потім продукт хроматографують на силікагелі і кристалізують двічі з ізопропілового ефіру. N + R=C 2H 5, iso-C3 H7 , C4H 9; R1CN, CONH 2, NO2 H 3C H+ NH O + H O NH 2 COOEt N N H CH3 III У відомому джерелі багатокомпонентним методом одержано одну сполуку конденсацією 3амінопіразолу, ацетооцтового ефіру та бензальдегіду, узятих в рівномолярних співвідношеннях. Суміш компонентів кип'ятять в етанолі у присутності кислотного каталізатора концентрованої НСl протягом 5-7 годин, потім протягом 8-10 годин реакційну суміш витримують при -20°С до повного завершення реакції. Кінцевий продукт очищують перекристалізацією з етанолу або суміші метанол: вода (1:2). Вихід продукту складає 55%. Сполукам III притаманна різноманітна біологічна активність, зокрема, сильна антигіпертензивна дія. Недоліками відомого методу є тривалість процесу (16-20 годин з урахуванням 5 перекристалізації), використання глибокого заморожування (-20°С) із застосуванням низькотемпературних хладагентів (наприклад, CaCl2, рідкого азоту та ін.), витрата розчинників для очищення продукту. Цей спосіб являється найближчим за технічною суттю до способу, що заявляється, і прийнятий нами за прототип. Задача даного винаходу полягає в розробці простого і доступного способу одержання похідних 5-метил-3,6-ді-(арилкарбоксамідо)-4,7дигідропіразоло[1,5-а]піримідинів, в якому за рахунок зміни умов синтезу (використання вогненебезпечних і нетоксичних речовин) можна спростити процес, скоротити його тривалість, виключити використання низькотемпературних хладагентів, зменшити витрату розчинників за рахунок підвищення якості одержаних речовин, підвищити вихід кінцевих продуктів. Поставлена в основу цього винаходу задача розв'язується тим, що спосіб одержання похідних 5-метил-3,6-ді-(арилкарбоксамідо)-4,7дигідропіразоло[1,5-а]піримідинів формули І R CONHAr 2 N N N H CONHAr1 CH3 I R=С6Н5, iso-C4H8, iso-C5H10, 4-Вr-С6Н4, 4-СlС6Н4, 4-C5H4N, 3-СН3-С6Н4 4СН3-С6Н4, 4-ОС2Н5-С6Н4, 4-F-С6Н4, 2-Сl-С6Н4, 2-F-С6Н4, 4-ОСН3-С6Н4, 4NO2-С6Н4, 3-NO2-С6Н4, 2,3-diОСН3-С6Н3, 3,4diОСН3-С6Н3, 2-F-5-Вr-С6Н3, 3-Сl-С6Н4, 2,4-diОСН3-С6Н3, 2-СН3-С6Н4, 4-С2Н5-С6Н4, 2,5dіОСН3-С6Н3, 3-ОСН3-4ОС2Н5-С6Н3, Аr1=С6Н5, 3-СН3-С6Н4, 4-СН3-СбН4, 4-ОС2Н5С6Н4, 4-F-С6Н4, 2-СН3-С6Н4, 4-Сl-С6Н4, 2,4-dіСН3-С6Н3 Аr2=С6Н5, 2-ОСН3-С6Н4, 4-ОСН3-С6Н4, 2,4-diСН3-С6Н3, 4-Сl-С6Н4, що включає конденсацію 3-амінопіразолу, відповідних карбонілметиленового похідного та альдегіду в рівномолярних кількостях в середовищі розчинника при кипінні, згідно винаходу, в якості 3-амінопіразолу використовують 4-(N-арилкарбоксамідо)-3-амінопіразол, в якості карбонілметиленового похідного -ариламід ацетооцтової кислоти та відповідні заміщені аліфатичні та ароматичні альдегіди, конденсацію проводять в середовищі основного розчинникадиметилформаміду при кипінні протягом 15-20 хвилин до повного зневоднення реакційної маси та утворення цільового продукту, а виділення одержаного продукту здійснюють етиловим спиртом. У способі, що заявляється, диметилформамід виконує функцію висококиплячого розчинника, що сприяє швидкому виділенню води під час реакції, і одночасно роль агента циклізації основного 81081 6 характеру (процес циклодегідратації), що не вимагає додаткового використання інших основних та циклодегідратуючих агентів (діетиламіну, тріетиламіну та ін.). Висока температура кипіння диметилформаміду забезпечує прискорене протікання хімічної реакції, що, в свою чергу, приводить до значного скорочення часу синтезу. Крім того, виключається тривалий процес глибокого охолодження реакційної маси, очищення цільових продуктів за рахунок проведення реакції в диметилформаміді основному розчиннику (у прототипі утворюється масло, яке необхідно перевести в твердий стан з подальшою перекристалізацією), що приводить до підвищення виходів цільових продуктів. У зв'язку з вказаним, основні продукти заміщені піразолопіримідини вже в процесі синтезу одержують достатньо чистими і не вимагають додаткових перекристалізацій. Таким чином, виключаються додаткові витрати органічних розчинників для очищення основних продуктів, здешевлюється їх вартість, виключається використання легкозаймистих розчинників, таких як ефіри аліфатичних кислот (ізопропіловий ефір). За способом, що заявляється, синтез кінцевих продуктів повністю проходить за 15-20 хвилин (за прототипом -16-20 годин). Вихід кінцевих продуктів складає 75-92% (за прототипом - 55%). У заявляємому способі цільові продукти одержують одностадійним методом шляхом кип'ятіння рівномолярних кількостей заміщених 4(N-арилкарбоксамідо)-3-амінопіразолу, ариламідів ацетооцтових кислот і відповідних заміщених аліфатичних або ароматичних альдегідів в диметилформаміді протягом 15-20 хвилин до повного зневоднення. Суміш охолоджують, додають невелику кількість етилового спирту і фільтрують кінцевий продукт, що утворився. R N N DMF NH2 CONHAr1 I + RCHO + CH3 COCH2CONHAr 2 N CONHAr 2 N N H CH3 CONHAr1 Структура сполук, що заявляються, є достатньо гнучкою, що дозволяє широко варіювати замісники в піразольному та альдегідному фрагментах, в ариламідах ацетооцтових кислот. Така можливість забезпечує одержання різноманітного асортименту продуктів потенційних біологічно активних речовин. У таблиці 1 наведено порівняльні характеристики способу, що заявляється, і способу - прототипу. У таблиці 2 подано температури плавлення, виходи кінцевих продуктів і спектри ПМР 1Н сполук, одержаних за способом, що заявляється, також наведено для порівняння аналогічні характеристики сполук, одержаних за способом прототипом. Приклад 1. Одержання 5-метил-3,6-ді-(4фенілкарбоксамідо)-7-феніл-4,7 7 дигідропіразоло[1,5-а]піримідину (таблиця 2, поз. 1). Суміш 0,5г (2,5·10-ЗM) 3-аміно-4(4фенілкарбоксамідо) - 1Н-піразолу, 0,44г (2,5·10-ЗM) феніламіду ацетооцтової кислоти і 0,26г (2,5·10З M) бензальдегіду суспенгують в 0,5мл диметилформаміду, нагрівають до стану прозорого розчина і витримують при легкому кипінні протягом 15-20 хвилин до повного зневоднення. Потім розчин охолоджують, додають 2мл етанолу і фільтрують кінцевий продукт. Зовнішній вигляд - білий порошок. Вихід: 0,8г (75%). Т. пл . 262°С Структуру 5-метил-3,6-ді-(4фенілкарбоксамідо)-7-фенiл-4,7дигідропiразоло[1,5-а]піримідину підтверджено спектральними даними. Спектри ядерного магнітного резонансу (ЯМР, 1 Н) виміряно на спектрометрі VARIAN Mercury VX200 (200Мгц) в розчинах дейтеродиметилсульфоксиду (ДМСО-d6), внутрішній стандарт тетраметилсілан; d(м.д.): 6,49(СН, с, 1Н), 7,02-7,64 (Аr-Н, м, 15Н), 8,07 (СН, с, Н-піразол), 8,89 (NH, с, 1Н), 9,43 (NH, с, 1Н), 9,75 (NH, с, 1Н), 2,26 (СН3, с, 3Н). Приклад 2. Одержання 5-метил-3фенілкарбоксамідо-6-(2,4диметилфенілкарбоксамідо)-7-ізопропил-4,7дигідропіразоло[1,5-а] піримідину (таблиця 2, поз, 2). Одержують аналогічно прикладу 1, беруть 0,18г iзомасляного альдегіду. Вихідні дані: Т.пл. 235°С Вихід 81% (0,9г). Спектральні дані: 5,39 (СН, с, 1Н), 8,096 (СН, с,1Н), 8,57 (NH, с, 1Н), 9,35 (NH, с,1Н), 9,72 (NH, с,1Н), 7,27-7,72 (Аr-Н, м, 8Н), 0,716 і 0,85 (СН3, д, 6Н), 1,63 (СН, м, 1Н), 1,82(СН3, с, 3Н), 2,16(СН3, с, 3Н ), 2,24 (СН3 - 5 положення, с, 3Н). Приклад 3. Одержання 5-метил-3,6-ді-(4фенілкарбоксамідо)-7-ізобутил-4,7дигідропіразоло[1,5-а]піримідину (таблиця 2, поз. 3). Одержують аналогічно прикладу 1, беруть 0,21г ізовалеріанового альдегіду. Вихідні дані: Т.пл. 205°С Вихід 81% (0,93г). Спектральні дані: 5,45(СН, с, 1Н), 7,03-7,71(АrН, м, 10Н), 8,10(СН-піразол., с, 1Н), 8,65(NH, с, 1Н), 9,73(NH, с, 1Н), 9,89(NH, с, 1Н), 2,17(СН3, с, 3Н), 1,84(СН, м,1Н), 1,58(СН2, кв, 2H), 0,81(СН3, д, 3Н), 0,71(СН3, д, 3Н). Приклад 4. Одержання 5-метил-3-(4метилфенілкарбоксамідо)-6-(2метоксифенілкарбоксамідо)-7-(4-бромфеніл)-4,7дигідропіразоло[1,5-а] піримідину (табл. 2, поз. 4). Одержують аналогічно прикладу 1, беруть 0,46г 4-бромбензальдегиду. Вихідні дані: Т.пл. 235°С Вихід 83%,(1,1г). Спектральні характеристики: 6,44 (СН, с,1Н), 6,80-7,72 (Аr-Н, м, 12Н), 8,07 (СН, с,1Н), 8,84 (NH, с,1Н), 8,95 (NH, с, 1Н), 9,74 (NH, с, 1Н), 6,80-7,72 (Ar-H, м, 12Н), 3,73 (ОСН3, с, 3Н), 2,35 (СН3, с, СН3). Приклад 5. Одержання 5-метил-3-(4етоксифенілкарбоксамідо)-6-(4 81081 8 хлорфенілкарбоксамідо)-7-феніл-4,7дигідропіразоло[1,5-а]піримідину (табл. 2, поз. 5). Синтез проводиться аналогічно прикладу 1, беруть 0,35г 4-хлорбензальдегіду. Вихідні дані: Т.пл. 268°С Вихід 92% (1,0г). Спектральні дані: 6,51 (СН, с,1Н), 6,85-7,63 (Аr-Н, м, 13Н), 8,043 (СН, с, 1Н), 8,89 (NH, с, 1Н), 9,64 (NH, с, 1Н), 9,91 (NH, с, 1Н), 3,96 (СН2, кв, 2H), 2,26 (СН3, с, 3Н),1,29 (СН3, т, 3Н). Решта прикладів зведена в таблиці 2. Порівняльні характеристики способу, що заявляється Кількість стадій реакції Тривалість процесу, хв. Вихід основного продукту Очи осн пр 1 15-20 75-92 Не п 1 960-1200 55 Нео пере із етан с ме вод Спосіб, що заявляється Спосібпрототип Характеристики сполук І, одержаних за способом, що заявля NN п/п Сполука І Т.пл, °С R Аr1 Аr2 1 С6Н5 С6Н5 С6Н5 265 2 ізо-С4Н8 ізопропіл C6H5 2,4-діСН3-С6Н3 235 3 ізо-С5Н10 ізобутил С6Н5 С6Н5 205 4 Вr-4-С6Н4 СН3-4-С6Н4 2-ОСН3-СбН4 235 5 С6H4-Сl-4 OEt-4-С6Н4 С6Н5 268 В 9 81081 6 4-піридил C5H4N С6Н5 2,4-діСН3-С6Н3 7 СН3-3-СбН4 СН3-4-C6H4 СбН5 10 274 17 235 18 8 СН3-4-С6Н4 F-4-C6H4 СбН5 245 19 9 OC2H5-4-C6H4 СбН5 С1-4-C6H4 10 F-4-C6H4 F-4-C6H4 СбН5 11 Сl-2-C6H4 СбН5 2-ОСН3-C6H4 247 20 178 135 21 12 F-2-C6H4 СН3-4-C6H4 Сl-4-C6H4 246 22 13 Вr-4-C6H4 СбН5 2-ОСН3-C6H4 198 14 4-ОСН3-C6H4 СНз-4-C6H4 4-ОСН3-C6H4 15 4-NO2-С6Н4 С6Н5 2,4-діСН3-С6Н3 207 24 16 3-NO2-С6Н4 СН3-4-С6Н4 2-ОСН3-С6Н4 278 25 23 232 (NH, с, 1Н), 9,64(NH, c, 1H), 9,91 (NH, c, 1H), 3,96(СН2, кв, 2Н), 2,26(СН3, с, 3Н), 1,29(СН3, т, 3Н). 6,52(СН, с, 1Н), 6,82-7,83(Аr-Н, м, 12Н), 8,40(СН-піразол, c, 2,3-діОСН3- 8,95(NH, c, 1H), 9,74(NH, 1H), 77 СН3-3-С6Н4 4-ОСН3-С6Н4 С6Н3 c, 1H), 9,96(NH, c, 1Н), 2,32(СН3, с, 3Н), 2,25(СН3, с, 3Н), 2,22(СН3, с, 3Н). 6,49(СН, с, 1Н), 6,82-7,83(Аr-Н, м, 13Н), 8,10(СН-піразол, c, 1H), 8,95(NH, c, 1H), 9,54(NH, 78 c, 1H), 9,96(NH, c, 1Н), 3,4-діОСН3СН3 с, 3Н), 2,32(СН3, -3-С6Н42,25(СН3,С6Н6 с, С6Н3 3Н), 2,22 (СН3, с, 3Н). 6,45(СН, с, 1Н), 6,98-7,75(Аr-Н, м, 13Н), 8,02(СН-піразол, c, 82 1H), 8,76(NH, c, 1H), 9,73(NН, у.с, 2Н), 2,20,(СН3, с, 3Н), 2,26 (СН3, с, 3Н). 2-F-5-Br-С6Н3 4-СН3-С6 6,92-7,72(Аr-Н,3-С6Н3 2,4-діСН 6,85(СН, с, 1Н), H4 м, 13Н), 8,04(СН-піразол, c, 1H), 8,98(NH, c, 1H), 9,65(NH, 83 c, 1Н), 9,91(NH, c, 1Н), 3,95(СН2, кв, 2H), 2,26(СН3, с, 3Н), 1,29 (СН3, т, 3Н). 6,50(CH, c, 1H), 6,92-7,82(Ar-Н, С1-3-С6H4 м, 13Н), Н5-4-С6H4 ОС2 8,12(СН-піразол, c, 3-С6H4 4-ОСН 92 1H), 8,85(NH, c, 1H), 9,75(NH, y. c, 2H), 2,26(СН3, с, 3Н). 6,46(CH, c, 1Н), 6,85-7,90(Аr-Н, м, 13Н), 8,07(СН, с, 1Н), 8,83(NH, c, 1H), 8,95(NH, c, 86 2,4-діОСН3- 1H), 9,74(NH, c, 1H), СН3-3-С6H4 С6Н С6Н3 3,73(ОСН3, с, 3Н), 2,34(СН3, с, 5 3Н). 6,50(СН, с, 1Н), 6,95-7,85(Аr-Н, м, 13Н), 8,12(СН-піразол, c, 1H), 9,02(NH, c, 1H), 9,95(NH, 90 c, 1Н), 10,02(NH, c, 1Н), 2,34(СН3, с, 3Н), 2,23(СН3, с, 2,4-діОСН33Н). СН3-3-С6H4 2-ОСН3-С H С6Н3 6,44(СН, с, 1Н), 6,80-7,72(Аr-Н, 6 4 м, 13Н), 8,07(СН-піразол, c, 1H), 8,81(NH, c, 1H), 8,93(NH, 83 c, 1H), 9,70(NH, c, 1Н), 3,75(ОСН3, с, 3Н), 2,32(СН3, с, 3Н). 6,46(СН, с, 1Н), 6,75-7,60(Аr-Н, 3,4-діОСН3м, 12Н), F-4-С6H4 8,0(СН-піразол, с, 1Н),-С6H4 2-ОСН3 С6Н3 8,71 (NH, c, 1Н), 9,63(NH, c, 79 1H), 9,64(NH, c, 1Н), 3,68(ОСН3, с, 3Н), 3,60(ОСН3, с, 3Н), 2,17(СНз, с, 3Н). 6,59(СН, с, 1Н), 6,918,23(АrН, м, 12Н), 8,09(СН-піразол, с, 1H), 9,01(NH, c, 1H), 9,27(NH, 2,4-діОСН382 F-4-С6H4 c, 1H), 9,76(NH, c, 2,4-діСН3-С6Н3 1H), С6Н3 2,19(СН3, с, 3Н), 1,82(СН3, с, 3Н). 6,51(СН, с, 1H), 6,85-8,20(Ar-Н, 80 2-СН3-С6H4м, 12Н), Н5-4-С6H4 ОС2 8,02(СН-піразол, c, 3-С6H4 4-ОСН 1H), 8,09(NH, c, 1H), 9,05(NH, 138 267 268 255 197 208 212 178 250 11 81081 26 С1-4-С6H4 С6Н5 27 С1-4-С6Н4 С6Н5 28 С2Н5-4-С6Н4 F-4-С6Н4 29 2,5-діОСН3С6Н3 С1-4-С6Н4 30 3-ОСН3-4ОС2Н5-С6Н3 4-СН3-С6Н4 31 С1-4-С6Н4 3-СН3-С6Н4 32 3-СН3-С6Н4 F-4-С6Н4 33 С1-4-С6Н4 F-4-С6Н4 34 4-СН3-С6Н4 3-СН3-С6Н4 35 2-ОСН3-С6Н4 4-СН3-С6Н4 12 Н, м, 12Н), 8,01(СН-піразол, c, 1H), 9,02(NH, c, 1H), 9,95(NH, c, 1H), 9,98(NH, c, 1Н), 3,95(СН2, кв, 2Н), 3,75(ОСН3, с, 3Н), 2,32(СН3, с, 3Н), 2,26(СН3, с, 3Н), 1,29(СН3, т, 3Н). С1-4-С6Н4 36 С6Н5 С6Н5 276 6,45(СН, с, 1Н), 6,79-7,71 (АrН, м, 13Н), 8,06(СН-піразол, c, 1H), 8,83(NH, c, 1H), 8,94(NH, 2-ОСН3-С6H4 182 90 c, 1H), 9,73(NH, c, 1Н), 3,73(ОСН3, с, 3Н), 2,34(СН3, с, 37 4-ОСН3С6Н4 С6Н5 С1-4-С6Н4 224 3Н). 6,5(СН, с, 1H), 7,04-7,72(Ar-Н, м, 13Н), 8,09(СН-піразол, с, С1-4-С6Н4 207 92 1Н), 9,00(NH, с, 1Н), 9,75(NH, c, 1H), 9,93(NH, c, 1H), 2,27(СН , с, 3Н). 38 С1-4-С6Н4 2-СН3-С63 4 Н 2-ОСНз-С6Н4 215 6,49(СН, с, 1Н), 6,68-7,56(АrН, м, 13Н), 7,81(СН-піразол, c, 1H), 8,92(NH, c, 1H), 9,25(NH, С6Н5 185 89 c, 1H), 9,58(NH, c, 1Н), 3,95(СН3, кв, 2Н), 2,32(СН3, с, 3Н), 1,29(СН3, т, 3Н). 39 С6Н5 6,35(СН, с, 1Н),6Н3 2,4-діСН3-С6Н3 2,4діСН3-С 6,36-7,74(Аr236 Н, м, 12Н), 8,06(СН-піразол, c, 1H), 8,86(NH, c, 1H), 9,74(NH, С6Н5 180 86 c, 1H), 9,96(NH, c, 1Н), 3,54(ОСН3, с, 3Н), 3,57(ОСН3, с, 3Н), 2,25(СН3, с, 3Н), 2,26(СН , с, 3Н). 40 С6Н5 С1-4- С63 4 Н 2,4-діСН3- С6Н3 233 6,49(СН, с, 1Н), 6,85-7,78(АrН, м, 13Н), 8,00(СН-піразол, c, 1H), 8,82(NH, c, 1H), 9,05(NH, c, 1H), 9,28(NH, c, 1Н), за способом-прототипо Структура 4-ОСН3-С6Н4 267 80 3,9(СН2, кв, 2Н), 3,75(ОСН3, с, 3Н), 3,67(ОСН3, с, 3Н), 2,32(СН3, с, 3Н), 2,26(СН3, с, 190 3Н), 1,29(СН3, т, 3Н). 6,45(СН, с, 1Н), 6,91-7,59(АrН, м, 11H), 8,04(СН-піразол, c, Дані таблиць 1H), та 2 і c, опису винаходу 1 8,8(NH, 1H), 9,17(NH, c, 2,4-діСН3- С6Н3 показують, що спосіб, 9,63(NH, c, 1H), 2,32(СН3, 237 79 1H), що заявляється, має ряд 3Н), 2,25(СН3 способомсуттєвих переваг в с,порівнянні із , с, 3Н), 2,20(СН3, с, 3Н), 1,83(СН3, с, прототипом і дозволяє: 3Н). - значно зменшити тривалість процесу одержання до 15-206,58(СН, с, 1Н), 7,10-7,95(Arхвилин (за прототипом - 16-20 Н, м, 13Н), 8,02(СН-піразол, c, годин); С6Н5 230 82 1H), якість кінцевих продуктів - підвищити вихід і 8,98(NH, c, 1H), 9,75(НН, у.с, прототипом (55%); (до 75-92%) в порівнянні з 2Н), 2,26(СН3, с, 3Н), 2,17(СН3, с, основного - за рахунок використання 3Н). розчинника виключити процес тривалого глибокого 6,51(СН, с, 1Н), 7,01-7,85(Аrохолодження і очищення 8,12(СН-піразол, c, Н, м, 13Н), цільових продуктів С6Н5 278 92 шляхом перекристалізації; 1H), 9,01(NH, c, 1H), 9,85(NH, - забезпечити відсутність2,37(CH3, c, 3H) y.c, 2H), легкозаймистих і подразнюючих шкіру6,49(CH, c,оболонку речовин; і слизову 1H), 6,82-7,83(Ar- широко варіювати в13Н), 8,10(СН-піразол, c, Н, м, молекулі замісники різної електронної природи; 8,95(NH, c, 1H), 9,54(NH, 1H), С6Н5 198 78 - здешевити вартість кінцевих продуктів. c, 1H), 9,96(NH, c, 1Н), Спосіб одержання сполук 3Н), 2,25(СНІ, с, 2,32(СН3, с, структури 3, що заявляється, простий 3Н),технологічному плані, в 2,22(СН3, с, 3Н). здійснюється в одну стадію і 6,75-7,82(Аrб,72(СН, с, 1Н), може легко 4-ОСН3-С6Н4 відтворюватися якН, в 12Н), 8,00(СН-піразол, іс, у 240 76 м, лабораторних, так виробничих умовах. 1H), 8,70(NH, c, 1H), 9,63(NH,
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 5-methyl-3,6-di-(arylcarboxamido)-4,7-dihydropyrazolo[1,5-а]pyrimidines derivatives
Автори англійськоюBorivskyi Valerii Oleksandrovych, Komikhov Serhii Oleksandrovych, Petrova Maryna Hennadiivna, Desenko Serhii Mykhailovych, Afanasiadi Liudmyla Mykhailivna
Назва патенту російськоюСпособ получения производных 5-метил-3,6-ди-(арилкарбоксамидо)-4,7-дигидропиразоло[1.5-а]пиримидинов
Автори російськоюБоровский Валерий Александрович, Комихов Сергей Александрович, Петрова Марина Геннадиевна, Десенко Сергей Михайлович, Дэсэнко Сергей Михайлович, Афанасиади Людмила Михайловна
МПК / Мітки
МПК: C07D 487/00, C07D 487/04
Мітки: одержання, похідних, 5-метил-3,6-ді-(арилкарбоксамідо)-4,7-дигідропіразоло[1.5-а]піримідинів, спосіб
Код посилання
<a href="https://ua.patents.su/6-81081-sposib-oderzhannya-pokhidnikh-5-metil-36-di-arilkarboksamido-47-digidropirazolo15-apirimidiniv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання похідних 5-метил-3,6-ді-(арилкарбоксамідо)-4,7-дигідропіразоло[1.5-а]піримідинів</a>
Попередній патент: Пристрій регулювання витрати рідких речовин
Наступний патент: Швидкорознімне з’єднання рукавів і трубопроводів
Випадковий патент: Спосіб корекції стану макрофагальної системи у хворих з синдромом підвищеної стомлюваності