Похідні 5-арил-8,8-диметил-1,2,3,4,5,6,7,8,9,10-декагідропіримідо[4,5-в]хінолін-4,6-діону
Номер патенту: 85082
Опубліковано: 25.12.2008
Автори: Сараєв Вячеслав Євгенович, Афанасіаді Людмила Михайлівна, Чебанов Валентин Анатолійович, Десенко Сергій Михайлович
Формула / Реферат
Похідні 5-арил-8,8-диметил-5-(4-метилфеніл)-1,2,3,4,5,6,7,8,9,10-декагідропіримідо[4,5-b]хінолін-2,4,6-діону загальної формули І
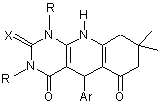 , (I)
, (I)
де при Х = О;
R = СН3;
Аr = 2-СН3О-С6Н4; 4-F-C6H4;
при Х = S, NH;
R = Н;
Аr = 4-СН3-С6Н4; 4-СН3О-С6Н4; 2-СН3О-С6Н4; 4-F-C6H4.
Текст
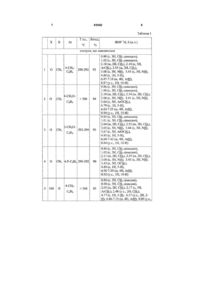
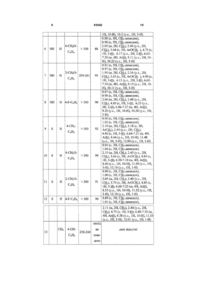
Похідні 5-арил-8,8-диметил-5-(4-метилфеніл)1,2,3,4,5,6,7,8,9,10-декагідропіримідо[4,5-b]хінолін2,4,6-діону загальної формули І R H Винахід відноситься до області хімії і являє собою нові похідні піримідохінолінів, а саме 2-Х-5арил-8,8-диметил-1,2,3,4,5,6,7,8,9,10-декагідропіримидо [4,5 -b] хінолін-4,6-діони загальної формули І важливу роль у життєдіяльності людини, так і з хімічної точки зору для дослідження зв'язку між будовою і властивостями цих сполук, у препаративному органічному синтезі. Різноманітні області біологічних активностей сполук подібної структури стимулюють підвищений інтерес до розробки нових сполук цієї структури і пошуку ефективних шляхів їх синтезу. Так, комп'ютерне моделювання за програмою PASS показало потенційну можливість використання сполук, що заявляються, як антиконвульсантів, інсулінопромоутерів (сполук, що сприяють виробленню інсуліну). Сполуки, що заявляються, не розчиняються у воді, розчинні у неполярних розчинниках (бензол, ксилол, толуол), мають підвищену розчинність у полярних і гідроксилвмісних розчинниках (спирти, диметилформамід, диметилсульфоксид), що розширює можливості використання для біологічних досліджень і медичної діагностики, у сільському N R N (I) N O Ar O (I) N O Ar O де X=0, S, NH; R1=R2=H,CH3; Ar2=4-СН3-С6Н4 ; 4-СН3О-С6H4; 2-СН3О-С6Н4; 4-F-C6H4. Сполуки, що заявляються, являють собою складні азотовмісні системи, структура яких представляє інтерес як з точки зору використання їх у якості біологічно активних речовин, що виграють (11) N UA R2 H N X (19) R1 85082 (13) , де при Х = О; R = СН3; Аr = 2-СН3О-С6Н4; 4-F-C 6H4; при Х = S, NH; R = Н; Аr = 4-СН3-С6Н4; 4-СН3О-С6Н4; 2-СН3О-С6Н4; 4-FC6H4. C2 X 3 85082 господарстві в якості хімічних засобів захисту рослин і таке інше. Указані сполуки у доступних джерелах інформації не виявлено. Серед заміщених гідрованих похідних піримідохінолінів відомі сполуки 5-арил-8,8-диметил1,2,3,4,5,6,7,8,9,10-декагідропіримідино[4,5-b] хінолін-2,4,6-тріони загальної формули П, що описані у [Э.Э. Гринштейн, Э.И. Станкевич, Г.Я. Дубур "Химия гетероциклических соединений" N1, 395 (1967)] H H H N O N (II) N O R 4 ність - у диметилформаміді і диметилсульфоксиді - навіть при кімнатній температурі. Сполуки III проявляють при відносно високих концентраціях високу протигрибкову активність, антибактеріальну активність проти грампозитивних організмів з низькою потенцією і вузьким спектром дії, протимікробну активність. Найбільш близькими за хімічною будовою до сполук, що заявляються, і прийнятими нами у якості прототипу є 1,3,8,8-тетраметил-2,4.6-тріоксо-5(R1)-1,2,3,4,5,6,7,8,9,10-декагідропіримідино[4,5b]хіноліни - сполуки IV, що описано у [A.Adarwal, P.M.S. Chanhan, Tetrahedron Letters, 4^ 1345-1348 (2005)]. O де R=H, CH3, C3H7 5-Арил-8,8-диметил-1,2,3,4,5,6,7,8,9,10декагідропіримідино-[4,5-b] хінолін-4,6-тріони проявляють підвищену стабільність до лужних середовищ: при тривалому кип'ятінні у 3%-ному розчині метилату натрію їх склад не змінюється. Відомі аналоги мало розчиняються у полярних середовищах (діоксан, спирти, диметилформамід). У лужно-спиртовому середовищі вони мають жовтувато-зелене забарвлення, у концентрованій H2SO4 - розчин жовтого кольору, у воді при нагріванні розчин має жовто-зелений відтінок. Сполуки подібної структури - піримідопіримідини знайшли використання, як біологічно активні піримідинові нуклеозіди [A.Takur, P.Saikia, J.Sandhu, Synlett, 1299 (2001)], як компоненти комбінаторної хімії. Похідні піримідохінолінів являються нестійкими продуктами, легко окислюються киснем повітря і іншими зовнішніми окислювальними агентами, потребують сушіння у вакуум-ексикаторі впродовж тривалого часу. При стоянні на повітрі такі сполуки утворюють суміш продуктів з окисленою (гетероароматичною) і неокисленою (гідрованою) структурами з непостійним складом. Оскільки у сполуках II R-замісники мають електронодонорний характер, це приводить до зниження їх стабільності до окислювачів. Відомі 1,3,5-тріарил-10-бензил1.2,3,4,5,6,7,8,9,10-декагідро-8,8-диме-тил-4,6діоксо-2-тіо-5Н,10Н-піримідо [4,5-Ь] хіноліни - сполуки III, близькі за хімічною будовою до сполук І, що заявляються, і описані у [V.K.Ahluwalia, R.Sahay, U.Das, Indian, J.Chem, 38B, 1136-1138 (1999)]. Сполуки III, як і аналогічні структурні аналоги II, мало розчинні у неполярних розчинниках, практично не розчиняються у воді. Розчинність їх підвищується при переході до полярних розчинників, добре розчиняються у спиртах. Найвища розчин Сполуки IV добре розчиняються у полярних і мало розчинні у неполярних середовищах, стійкі до лужних агентів і кисню повітря. Різноманітні області біологічних активностей сполук подібної структури - протипухлинних, антиканцерогенних, протизапальних описано в [R.Kumar, DX. Tyrrell, Y. Bioorg. Med.Chem. Lett, U, 2917 (2001)] Задача винаходу полягала у пошуку нови х сполук у низці похідних пі-римідохінолінів з підвищеною розчинністю в органічних розчинниках. Поставлена задача досягається розробкою нових похідних 5-арил-8,8-диметил1,2,3,4,5,6,7,8,9,10-декагідротримідо[4,5-b]хінолін4,6-діону формули І Видозмінення структури сполук І, що заявляються, привело до появи нових властивостей. Так, наявність метильних груп при гетероциклічних атомах азоту при введенні угруповування - NH або атому сірки замість атому кисню приводить до підвищення розчинності у розчинниках, що мають гідроксильні групи, полярних розчинниках, що для такої складної структури є несподіваним. Структури сполук IV за прототипом вміщують у 5 положенні молекули фрагменти 4-карбокси- і 4гідроксибензальдегідів. ЦІ угр уп ування приводять до утворення міжмолекулярних асоціатів - сполук з міжмолекулярним водневим зв'язком між атомом кисню у положенні 2 і протоновмісними замісниками у положенні 5. Такі асоціати знижують розчинність сполук в органічних розчинниках. Введення арильних радикалів, що не вміщують протонних замісників в положенні 5 молекули І, виключає утворення указаних асоціатів. Внаслідок цього спостерігається збільшення розчинності у органічних розчинниках. 5 85082 Так, наприклад розчинність сполуки 13 (див. табл.1 поз.13) в 1 л толуолу складає 3,5 г, в той час як розчинність сполук, що заявляється, в аналогічних умовах збільшується у 2 рази. У випадку сірковмісних сполук І (див. табл. 1, поз. 9) спостерігається подальше підвищення розчинності приблизно в 4 рази, порівняно із сполукою 13 (прототипом). У таблиці 1 дано характеристики сполук І, що заявляються і сполуки IV (прототип) та їх Я МР 1Hспектри. Спосіб сполук, що заявляються, наведено на наступних прикладах: Приклад 1. Одержання 8,8-диметил-5-(4метилфеніл)-1,2,3,4,5,6,7,8,9, 10-декагідропіримидо [4,5-b] хінолін-2,4,6-тріону (табл. 1, поз. 1) У пробірку для проведення мікрохвильового синтезу ємністю 10мл містять 0,16г (0,0013 M) 6амінопіримідин-2,4-діону, 0,18г (0,0013M) 5,5диметилциклогексан-1,3-діону (димедону) 1,0 мл етилового спирту і 0,02г (0,0013M) 4метилбензальдегіду. Після розмішування реакційної маси протягом 1 хвилини додають 0,1 мл тріетиламіну. Пробірку містять у мікрохвильовий синтетайзер (режим "High absorption" та "Hold time", 150°C, 600 секунд). Після завершення реакції продукт відфільтровують, промивають 10мл етанолу, сушать у повітрі. Вихід 0,45 г (93%). T пл =290-292°C. Спектр ЯМР 1H, 6(м.г.): 0.89 (с, ЗН, СН3димедон), 1.02 (с, 3Н, CH3-димедон),2.10 (м, 2Н, CH2), 2.18 (с, 3Н, ArCH3), 2.55 (м, 2Н, CH2), 3.08 (с, 3Н, NH), 3.43 (с, 3H5 NH), 4.84 (с, IH, 5-Н), 6.877.18 (м, 4Н, ArH), 8.87 (ул., IH, 10-Н) Приклад 2. Одержання 2-іміно-8,8-диметил-5(4-метилфеніл)-1,2,3,4,5, 6,7,8,9, 10декагідропіримидо [4,5-b] хінолін-4,6-діону (табл. 1, поз. 5). Продукт одержують аналогічно прикладу 1. Для реакції беруть: 0,15г (0,0013M) 2-іміно-6амінопіримідин-4-ону, 0,18г (0,0013M) 5,5діметилциклогексан-1,3-діону і 0,02г (0,0013 M) 4метилбенз-альдегіду. Вихід 0,42г (93%). T пл. > 300°C 6 Спектр ЯМР 1H, 6(м.г.): 0.88 (с, 3Н, СН3димедон), 0.98 (с, 3Н, CH3-димедон), 2.05 (м, 2Н, CH2), 2.17 (с, 3Н, ArCH3), 2.48 (у.с, 2Н, CH2), 4.77 (с, IH, 5-Н), 6.17 (у.с, 2Н, 2-Н), 6.86-7.15 (м, 4Н, ArH), 9.09 (у.с, IH, 10-Н), 10.2 (у.с, IH, 3-Н) Приклад 3. Одержання 2-тіо-8,8-диметил-5-(4метилфеніл)-1,2,3,4,5,6, 7,8,9,10декагідропіримидо [4,5-b] хінолін-4,6-діону (табл. 1, поз. 9). Продукт одержують аналогічно прикладу 1. Для реакції беруть: 0,19г (0,0013 M) 2-тіо-6амінопіримидин-4-ону, 0,18г (0,0013г) 5,5диметилциклогексан-1,3-діону і 0,02г (0,0013 M) 4метил-бензальдегіду Вихід 0,43г (92%). T пл. > 300°С Спектр ЯМР 1H, 6(м.г.): 0.90 (с, 3Н, СН3димедон), 1.02 (с, 3Н, CH3-димедон), 2.10 (м, 2Н, CH2), 2.18 (с, 3Н, ArCH3), 2.43 (у.с, 2Н, CH2), 4.80 (с, IH, 5-Н), 6.64-7.21 (м, 4Н, ArH), 8.44 (у.с, IH, 10Н), 11.48 (у.с, IH, 3Н), 12.00 (у.с, IH, 1-Н) Решту прикладів зведено у таблиці 1. Як видно із тексту матеріалів, що заявляються, і даних таблиці 1, технічне рішення, що пропонується у порівнянні з прототипом має наступні переваги: - структура сполук , що заявляються, забезпечує одержання широкого асортименту похідних піримідохінолінів, з покращеними характеристиками: з підвищеною розчинністю, з високим ступенем чистоти, що не потребує додаткової очистки; - підвищення розчинності сполук, що заявляються, у органічних розчинниках дозволяє створювати високу концентрацію цих речовин у розчинах, що забезпечує більш широкі концентраційні інтервали для біологічних тестів; - структура сполук забезпечує широке варіювання у молекулах похідних піримідохінолінів альдегідної компоненти - арильного радикалу (у прототипі використано тільки 2 альдегіди), дозволяє розширити асортимент нових потенційних біологічно активних речовин. Всі ці переваги нових сполук розширяють можливості їх потенційного використання в якості фізіологічно активних речовин, в препаративному органічному синтезі, в якості хімічних засобів захисту рослин в сільському господарстві і т. ін. 7 85082 8 9 85082 10 11 Комп’ютерна в ерстка В. Клюкін 85082 Підписне 12 Тираж 28 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійською5-aryl-8,8-dimethyl-5-(4-methylphenyl)-1,2,3,4,5,6,7,8,9,10-decahydropyrimido[4,5-b]quinoline-4,6-dione derivatives
Автори англійськоюSaraev Viacheslav Yevhenovych, Chebanov Valentyn Anatoliiovych, Desenko Serhii Mykhailovych, Afanasiadi Liudmyla Mykhailivna
Назва патенту російськоюПроизводные 5-арил-8,8-диметил-1,2,3,4,5,6,7,8,9,10-декагидропиримидо[4,5-в]хинолин-4,6-диона
Автори російськоюСараев Вячеслав Евгеньевич, Чебанов Валентин Анатолиевич, Дэсэнко Сергей Михайлович, Афанасиади Людмила Михайловна
МПК / Мітки
МПК: C07D 471/04
Мітки: 5-арил-8,8-диметил-1,2,3,4,5,6,7,8,9,10-декагідропіримідо[4,5-в]хінолін-4,6-діону, похідні
Код посилання
<a href="https://ua.patents.su/6-85082-pokhidni-5-aril-88-dimetil-12345678910-dekagidropirimido45-vkhinolin-46-dionu.html" target="_blank" rel="follow" title="База патентів України">Похідні 5-арил-8,8-диметил-1,2,3,4,5,6,7,8,9,10-декагідропіримідо[4,5-в]хінолін-4,6-діону</a>
Попередній патент: Універсальне колесо
Наступний патент: Спосіб аналого-цифрового перетворення та пристрій для його реалізації
Випадковий патент: Вітрова енергетична машина