Спосіб фотометричного визначення мікрокількості міді
Формула / Реферат
Спосіб фотометричного визначення мікрокількості міді, який полягає у фотометричному визначенні за допомогою фотометричного реагенту, який відрізняється тим, що як реагент використовується саліцилаль-тіосемикарбазон.
Текст
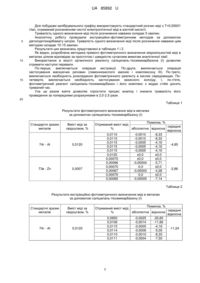
Реферат: UA 85892 U UA 85892 U 5 10 15 20 25 30 35 40 Корисна модель, що заявляється, належить до хімічної галузі, зокрема до фізико-хімічних методів визначення міді, а саме до способів прямого фотометричного визначення мікрокількостей міді в металах. Відомий спосіб фотометричного і екстракційно-фотометричного визначення мікрокількостей міді в металах, який оснований на реакціях утворення кольорових комплексних сполук міді з органічними реагентами [Труды ВНИИСО. - М.: изд. Металлургия, 1968. - Вып. ІV. - С. 5-46; Е. Сендел. Колориметрические методы определения следов металлов. - М.: изд. "Мир", 1964. - С. 393-422; Г. Шарло. Методы аналитической химии. - М.-Л.: изд. "Химия", 1965. - С. 709-715; З. Марченко. Фотометрическое определение элементов. - М.: изд. "Мир", 1971. - С. 239-255; Авт.свід. СРСР № 460243 і № 369472]. Найбільш близьким аналогом до способу, що заявляється (прототипом), і таким, що найчастіше використовується в аналітичній практиці, є екстракційно-фотометричний метод визначення мікрокількостей міді з діетилдитіокарбаматом натрію [В.В. Степин и др. Анализ цветных металлов и сплавов. - М.: изд. "Металлургия", 1974. - С. 18-19; А.Н. Грисевич, К.Б. Кладницкая. Заводская лаборатория, 1961. - Т. 27, № 11. - С. 1343-1345; Труды ВНИИСО, вып. IV. - М.: изд. "Металлургия", 1968. - С. 5-25 та інші вищенаведені]. Спосіб базується на взаємодії діетилдитіокарбамата натрію з іонами купруму (II) в аміачному розчині при рН 8,5-9,0 з утворенням колоїдного розчину діетилдитіокарбамату міді, забарвленого залежно від концентрації міді в жовтий або коричневий колір і який екстрагується хлороформом. Оптимальна концентрація міді 20 мкг в 25 мл розчину при товщині шару 50 мм. Молярний коефіцієнт погашення Е=13000 при λmах=436 нм. Визначенню міді заважають сурма (III), талій (III), телур (IV) і бісмут. Кадмій, цинк, плюмбум утворюють з діетилдитіокарбаматом натрію безбарвні комплекси. Вплив феруму, алюмінію, титану, мангану, ніколю, кобальту усувають зв'язуванням їх в комплексні сполуки лимоннокислим амонієм і динатрієвою сіллю етилендіамінтетраоцтової кислоти (комплексоном III). Загальними суттєвими ознаками найближчого аналогу і способу, що заявляється, є екстраційно-фотометричне визначення мікрокількостей міді за допомогою фотометричного реагенту. Основним недоліком відомого способу є складність і тривалість процесу. Це пояснюється тим, що для усунення впливу елементів, що заважають, при визначенні міді використовується не пряме фотометричне визначення на тлі усіх складових, а екстракційно-фотометричний метод, в якому є ряд додаткових операцій, а саме, подвійне екстрагування діетилдитіокарбамату міді, що утворюється, хлороформом, застосування маскуючих речовин (лимоннокислий амоній і комплексон III), а також необхідність користуватися спеціальними ділильними воронками для проведення екстракції. Крім цього визначення міді по цьому методу ускладнюється тим, що діетилдитіокарбамат натрію не розчинюється в органічних розчинниках і досить легко розкладається в кислих розчинах на діетиламін і сірковуглець. У дуже розбавлених розчинах утворюється колоїдна суспензія, яка може бути стабілізована добавкою захисного колоїду. Розчини його стійкі тільки впродовж 1 години при повній відсутності світла. В основу корисної моделі поставлена задача удосконалення відомого способу з метою спрощення і прискорення процесу хімічного аналізу мікрокількостей міді в металах. Поставлена задача вирішується за рахунок того, що як фотометричний реагент застосовують органічний реагент саліцилаль-тіосемікарбазон (І), 45 CH N NH C S NH2 CH C + Cu2+ OH O I 50 N N Cu II NH2 + 2H+ S , який належить до класу азометанів (основи Шиффа). Це безбарвна, кристалічна речовина, нерозчинна у воді, хлороформі, помірно розчинна в гарячих кислотах (НСl, H2SO4, СН3СООН), добре розчинна в лугах, аміаку, ацетоні. Використовуваний в способі фотометричного визначення мікрокількості міді фотометричний реагент саліцилаль-тіосемікарбазон синтезований нами уперше за загальноприйнятою методикою синтезу азометинів - кип'ятінням суміші реагуючих речовин (альдегіду і аміну) в 1 UA 85892 U 5 10 спиртовому середовищі, аналогічно методиці, використаній в роботах: [А.П. Авдеенко, А.М. Сурмий, Л.П. Атясова, Н.П. Клюшник. Новые комплексообразователи. Сообщение І. Синтез фтальальдегид-бис-оксианилов. Сб. Вопросы химии и хим. технологии. - Изд. Харьковского унта, 1980. - Вып. 60. - С. 10-14; [А.П. Авдеенко, А.М. Сурмий, Л.П. Атясова, С.И. Бурмистров. Новые комплексообразователи. Сообщение II. Синтез фтальальдегид-бис-гидразонов и диоксимов. Сб. Вопросы химии и хим. технологии. - Изд. Харьковского ун-та, 1979. - Вып. 57. С. 81-83]. Проте в даному випадку у зв'язку з малою розчинністю тіосемікарбазону в спирті реакцію проводили у водному етанолі. Синтез саліцилаль-тіосемікарбазону перебігає за наступною схемою: O C CH N H + NH 2 OH NH C NH C S NH2 NH2 + H2O OH S I 15 20 25 30 35 40 45 50 Методика синтезу саліцилаль-тіосемікарбазону (І) До 3,64 г (0,04 М) тіосемікарбазону в 30 мл гарячої суміші етанол-вода (1:1) додають 4,88 г (0,04 М) саліцилового альдегіду в 10 мл гарячого етанолу. При кип'ятінні реакційної маси впродовж 5 хвилин починає випадати осад. Кип'ятіння продовжують ще 5 хвилин, потім реакційну масу охолоджують, осад фільтрують, промивають водою і етанолом і сушать. Вихід 7,55 г (96,9 %). Безкольорові кристали (з ізобутанолу), т.пл. 222 °C. Нерозчинний у воді, хлороформі, погано розчинний в холодних спиртах, оцтовій кислоті, помірно розчинний в ацетоні, гарячому ізобутанові. Вище наведена методика свідчить про те, що синтез саліцилаль-тіосемікарбазона технологічно простий, перебігає швидко, початкові реагенти доступні є продажними реактивами. Саліцилаль-тіосемікарбазон є бідентантним аналітичним реагентом. Можливо припустити утворення незарядженого комплексу купруму (II), що підтверджується експериментальними даними. Спосіб заснований на реакції іонів купруму (II) з саліцилаль-тіосемікарбазоном (у 20 % ацетоні) при рН=2-3 з утворенням комплексної сполуки (II) жовто-зеленого кольору, розчинного у водно-ацетоновому середовищі. Оптимальна область концентрацій 5-150 мкг купруму в 25 мл розчину при товщині шару 20-30 мм. Молярний коефіцієнт погашення 20000 при довжині хвилі 364 нм. Прямому фотометричному визначенню міді не заважають іони хрому, ніколю, мангану, кобальту, цинку, алюмінію, плюмбуму, титану, ванадію, бісмуту, стибію, магнію, церію, цирконію та ін. Вплив феруму (III), що заважає, усувається аскорбіновою кислотою. Розчин саліцилаль-тіосемікарбазону стійкий впродовж декількох місяців (два і більше). Забарвлення комплексу розвивається миттєво і стійке впродовж місяця. Усі ці чинники дозволяють швидко визначити мікрокількості міді в металах і інших матеріалах металургійного виробництва на тлі усіх складових. Приклад. Визначення міді в алюмінію (С.З. 74 г зі змістом 0,012 % Сu) і в цинку (С.З. 73 в зі змістом міді 0,0007 %). 1,0 г стандартного зразку алюмінію або 2,0 г стандартного зразку цинка поміщають в склянку місткістю 300 мл, додають 20-40 мл соляної кислоти (1:1), 2 мл перекису водню (30 %-вого) і розчиняють спочатку на холоду, а потім при нагріванні до повного розчинення наважки. Для руйнування надлишку перекису водню розчин випаровують до початку кристалізації солей. Солі розчиняють в гарячій воді у присутності 2-3 крапель соляної кислоти (1:3), розчин переводять в мірну колбу на 50 мл, розбавляють дистильованою водою до мітки і перемішують. Аліквотну частину розчину, що містить 5-20 мкг міді (10 мл для стандартного зразку Аl і 20 мл для стандартного зразку Zn) поміщають в мірну колбу на 50 мл, додають 5-10 мл 5 %-ного розчину аскорбінової кислоти, створюють 2 %-ною сірчаною кислотою рН2 (за універсальним індикаторним папером), потім додають по 5 мл 0,01 %-вого розчину саліцилальтіосемикарбазона в ацетоні, перемішують, доводять до мітки дистильованою водою і фотометрують на ФЭК-56М зі світлофільтром № 2 в кюветі на 20-30 мл. Виміри роблять проти своїх "ялових", в які замість реактиву додають по 5 мл ацетону. 2 UA 85892 U 5 10 15 Для побудови калібрувального графіку використовують стандартний розчин міді з Т=0,00001 г/мл, отриманий розчиненням чистої електролітичної міді в азотній кислоті. Тривалість одного визначення міді після розчинення наважки складає 5 хвилин. Аналогічну роботу проводили екстракційно-фотометричним методом за допомогою діетилдитіокарбамату натрію. Тривалість одного визначення міді після розчинення наважки цим методом складає 10-15 хвилин. Результати цих визначень представлені в таблицях 1 і 2. Як видно, розроблена методика прямого фотометричного визначення мікрокількостей міді в металах цілком відповідає за простотою і швидкістю сучасним вимогам аналітичної хімії. Використання в якості органічного реагенту саліцилаль-тіосемикарбазона (І) дозволяє отримати наступні переваги. По-перше, виключається операція екстракції. По-друге, виключається операція застосування маскуючих речовин (лимоннокислого амонію і комплексону III). По-третє, виключається необхідність розкладання фотометричного реагенту в кислих середовищах. Почетверте, виключається необхідність застосування захисного колоїду. І, по-п'яте, фотометричний реагент саліцилаль-тіосемикарбазон і його комплекс з міддю стійкі досить тривалий час. Усе це разом взяте дозволяє спростити процес аналізу і знизити тривалість його проведення за попередніми розрахунками в 2,0-2,5 рази. 20 Таблиця 1 Результати фотометричного визначення міді в металах за допомогою салицилаль-тіосемікарбазону (І) Стандартні зразки металів Вміст міді за свідоцтвом, % 74г - Аl 0,0120 73в - Zn 0,0007 Помилка, % Отриманий вміст міді, середня % абсолютна відносна відносна 0,0110 -0,0010 -8,33 0,0110 -0,0010 -8,33 0,0115 -0,0005 -4,16 -4,85 0,0115 -0,0005 -4,16 0,0115 -0,0005 -4,16 0,0120 ±0,0 ±0,0 0,00070 ±0,0 ±0,0 0,00066 -0,00004 -5,71 0,00070 -0,0 ±0,0 -2,86 0,00067 -0,00003 -4,28 0,00070 -0,0 ±0,0 0,00065 -0,00005 -7,14 Таблиця 2 Результати екстракційно-фотометричного визначення міді в металах за допомогою саліцилаль-тіосемікарбазону (І) Стандартні зразки металів Вміст міді за свідоцтвом, % 74г - Аl 0,0120 Помилка, % Отриманий вміст міді, середня % абсолютна відносна відносна 0,0950 -0,0025 -20,83 0,0106 -0,0014 -11,66 0,0115 -0,0005 -4,16 -11,24 0,0114 -0,0006 -5,00 0,0110 -0,0010 -8,33 0,0111 -0,0004 -7,50 3 UA 85892 U Продовження таблиці 2 Стандартні зразки металів Вміст міді за свідоцтвом, % 73в - Zn 0,0007 Помилка, % Отриманий вміст міді, середня % абсолютна відносна відносна 0,00065 -0,00005 -7,14 0,00063 -0,00007 -11,00 0,00067 -0,00003 -4,28 -5,88 0,00066 -0,00004 -5,71 0,00065 -0,00005 -7,14 0,00070 ±0,0 ±0,0 ФОРМУЛА КОРИСНОЇ МОДЕЛІ 5 Спосіб фотометричного визначення мікрокількості міді, який полягає у фотометричному визначенні за допомогою фотометричного реагенту, який відрізняється тим, що як реагент використовується саліцилаль-тіосемикарбазон. Комп’ютерна верстка М. Ломалова Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 4
ДивитисяДодаткова інформація
Автори англійськоюAvdeienko Anatolii Petrovych
Автори російськоюАвдеенко Анатолий Петрович
МПК / Мітки
МПК: G01N 33/52
Мітки: спосіб, мікрокількості, фотометричного, визначення, міді
Код посилання
<a href="https://ua.patents.su/6-85892-sposib-fotometrichnogo-viznachennya-mikrokilkosti-midi.html" target="_blank" rel="follow" title="База патентів України">Спосіб фотометричного визначення мікрокількості міді</a>
Попередній патент: Спосіб лікування гіперпроліферативних станів органів малого таза
Наступний патент: Бічна рама візка залізничного вагону
Випадковий патент: Термоелектричний холодильник