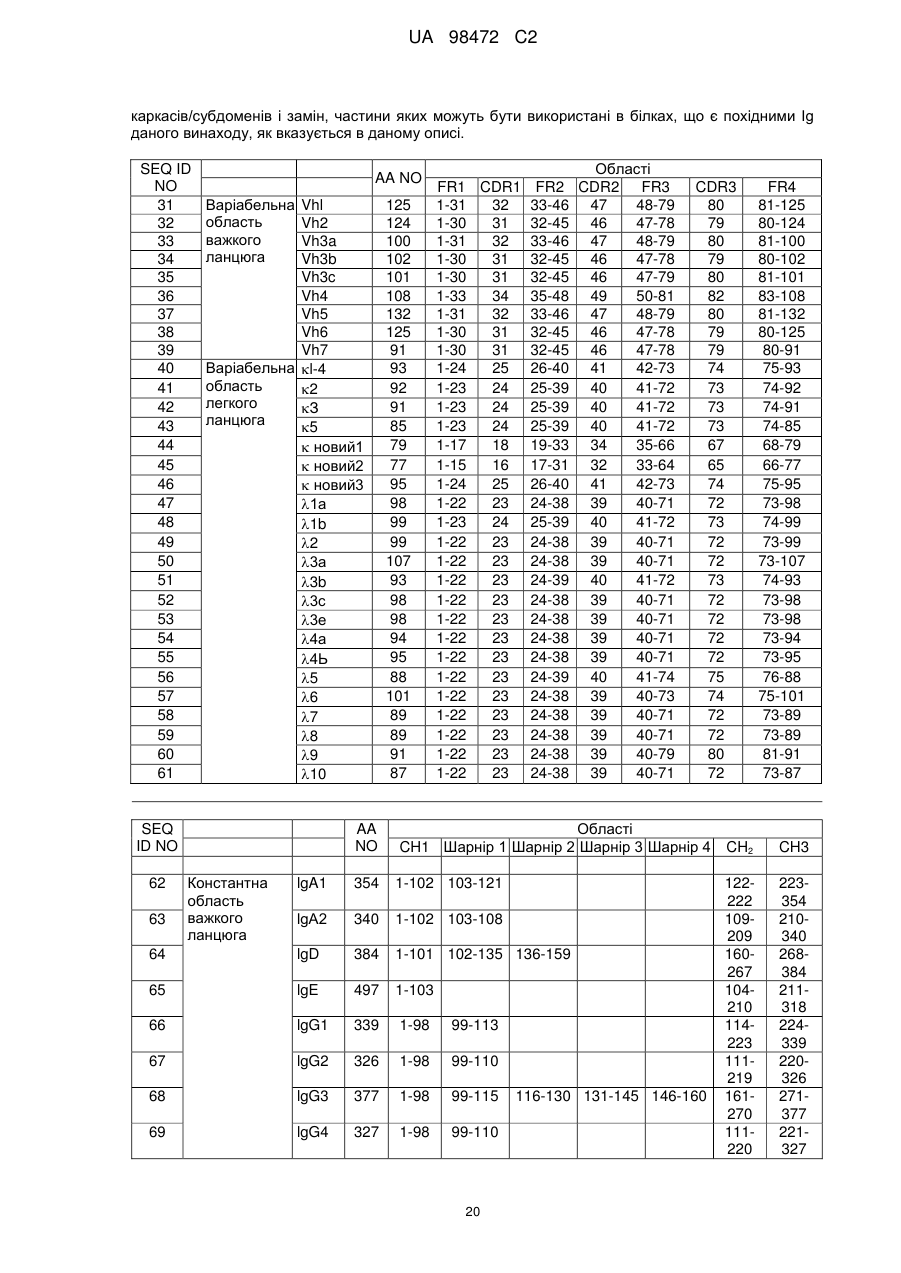
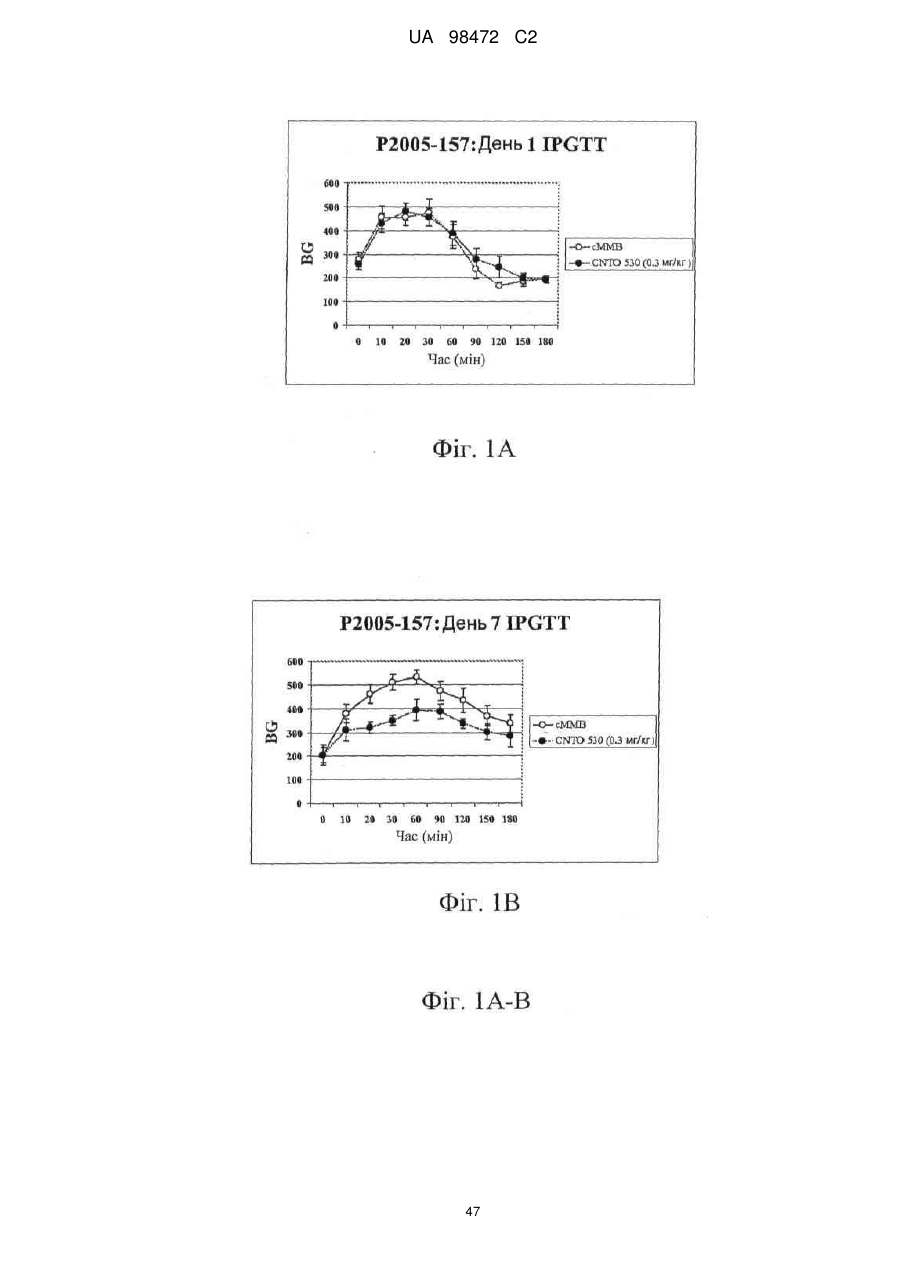
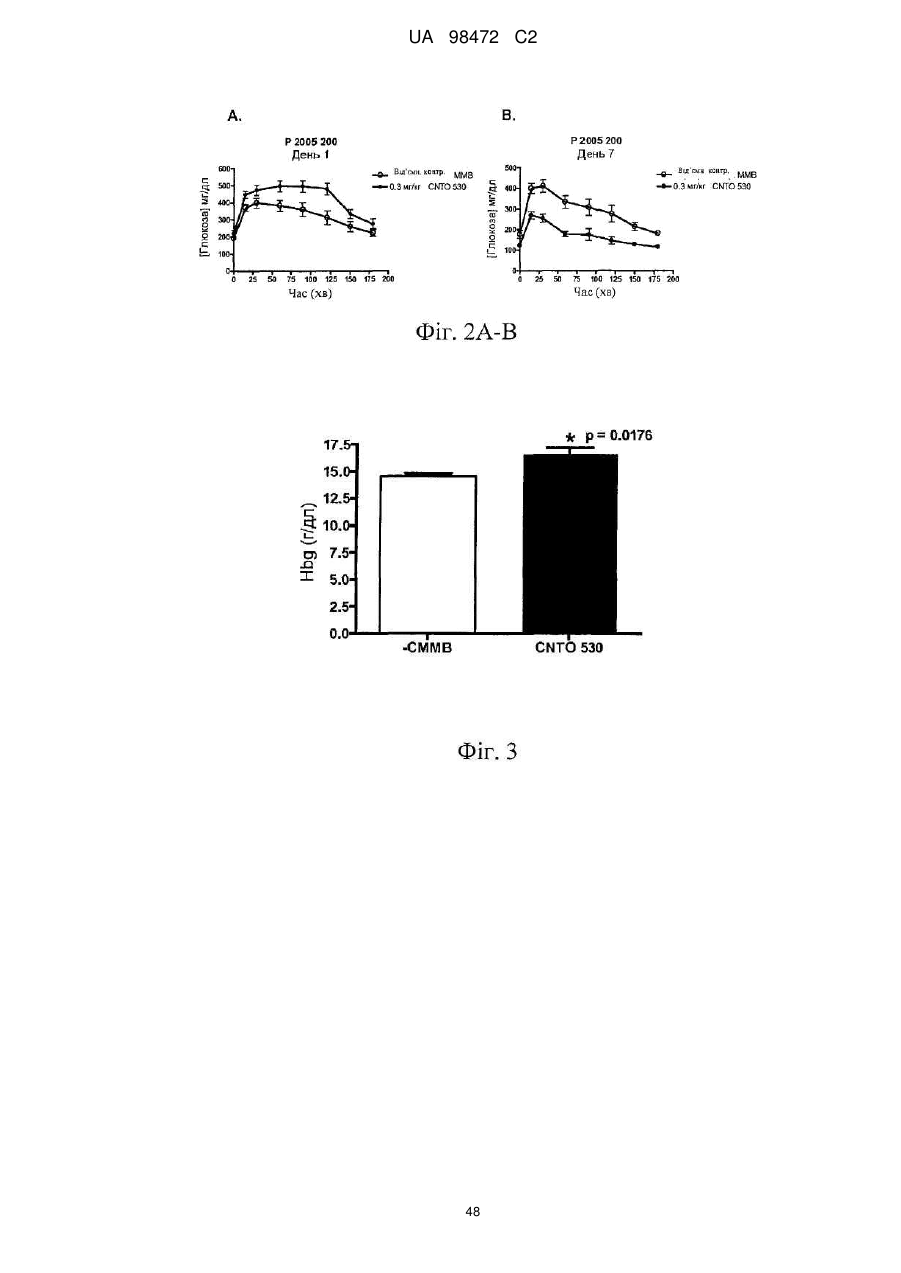
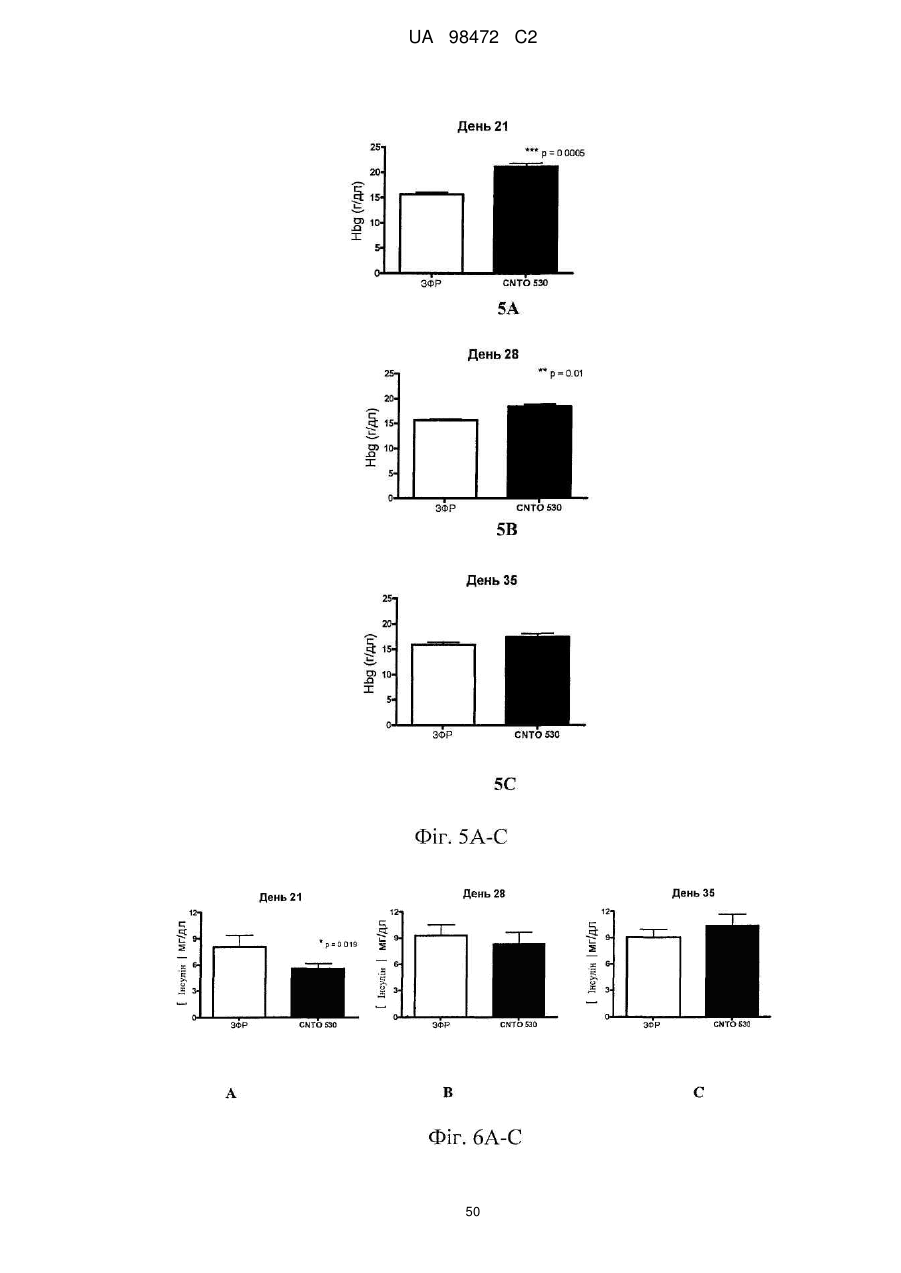
Застосування агоніста рецептора epo людини для лікування інтолерантності до глюкози
Формула / Реферат
1. Застосування агоніста рецептора еритропоетину (ЕРО) для лікування інтолерантності до глюкози в клітині, тканині, органі або у тварини.
2. Застосування за п. 1, де вказаний агоніст рецептора ЕРО вибраний з біологічної сполуки-агоніста рецептора ЕРО і з низькомолекулярної сполуки-агоніста рецептора ЕРО.
3. Застосування за п. 2, де вказана біологічна сполука-агоніст рецептора ЕРО вибрана з поліпептиду, антитіла і поліпептиду, злитого з антитілом.
4. Застосування за п. 3, де вказаний поліпептид являє собою ЕРО або природний варіант.
5. Застосування за п. 3, де вказаний поліпептид додатково включає щонайменше одну молекулу поліетиленгліколю.
6. Застосування за п. 3, де вказаний поліпептид являє собою неприродний варіант ЕРО.
7. Застосування за п. 6, де вказаний неприродний варіант ЕРО являє собою дарбепоетин-альфа.
8. Застосування за п. 3, де вказане антитіло являє собою антитіло-агоніст відносно рецептора ЕРО або ЕРО.
9. Застосування за п. 3, де вказаний поліпептид являє собою функціональний міметик ЕРО.
10. Застосування за п. 9, де вказаний функціональний міметик ЕРО являє собою щонайменше одну послідовність, вибрану з SEQ ID NOs: l-39, або білок, що містить амінокислотну послідовність SEQ ID NO: 88.
11. Застосування за п. 3, де вказаний поліпептид являє собою гематид.
12. Застосування за п. 3, де вказаний злитий з антитілом поліпептид включає щонайменше частину послідовності важкого ланцюга антитіла і щонайменше один поліпептид-агоніст рецептора ЕРО.
13. Застосування за п. 12, де вказаний поліпептид являє собою функціональний міметик ЕРО.
14. Застосування за п. 2, де вказана низькомолекулярна сполука являє собою хімічну сполуку, яка є агоністом рецептора ЕРО.
15. Застосування за п. 14, де вказана низькомолекулярна сполука вибрана з FG-2216 i FG-4592.
16. Застосування за будь-яким з пп. 1-15, де вказане лікування здійснюється за допомогою доставки фармацевтичної сполуки шляхом, вибраним з парентерального, підшкірного, внутрішньом'язового, внутрішньовенного, внутрішньосуглобового, внутрішньобронхіального, внутрішньоочеревинного, внутрішньокапсулярного, внутрішньохрящового, внутрішньопорожнинного, внутрішньочеревного, внутрішньомозочкового, всередину шлуночків мозку, всередину ободової кишки, інтрацервікального, внутрішньошлуночкового, внутрішньопечінкового, всередину міокарда, внутрішньокісткового, внутрішньотазового, всередину перикарда, інтраперитонеального, внутрішньоплеврального, внутрішньопростатного, внутрішньолегеневого, інтраректального, внутрішньониркового, всередину сітківки, внутрішньоспінального, інтрасиновіального, внутрішньогрудного, внутрішньоматкового, внутрішньоміхурового, всередину пошкодження, болюсного, піхвового, ректального, защічного, під'язикового, інтраназального або черезшкірного.
Текст
Реферат: Даний винахід стосується застосування агоніста рецептора еритропоетину (ЕРО) для лікування інтолерантності до глюкози в клітині, тканині, органі або у тварини. UA 98472 C2 (12) UA 98472 C2 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 Відомий рівень техніки Галузь техніки, до якої належить винахід Даний винахід стосується способу використання щонайменше одного агоніста рецептора EPO людини для запобігання або лікування інтолерантності до глюкози і/або анемії, пов'язаної із захворюванням нирок, включаючи терапевтичні композиції, методи і пристрої. Характеристика відомого рівня техніки Певні патологічні стани включають аномальний еритропоез. Рекомбінантний EPO людини (rHuEPO) застосовують терапевтично в ряді країн. У Сполучених Штатах Управління з контролю за продуктами і ліками США (FDA) схвалило використання rHuEPO's для лікування анемії, пов'язаної з термінальною стадією ниркового захворювання. Хворі, що знаходяться на гемодіалізі, для лікування цього порушення зазвичай страждають від важкої анемії, що викликається руйнуванням і передчасною загибеллю еритроцитів внаслідок проведення діалізу. EPO корисний при лікуванні інших типів анемії. Наприклад, анемію, індуковану хіміотерапією, анемію, пов'язану з мієлодисплазією, анемії, пов'язані з різними природженими порушеннями, анемію, пов'язану зі СНІДом, і анемію, пов'язану з передчасним розвитком, можна лікувати за допомогою EPO. Крім того, EPO може грати роль в інших галузях, таких як сприяння більш швидкому відновленню нормального гематокриту у хворих з трансплантацією кісткового мозку, у хворих, підготовлених для аутологічних трансфузій крові, і у хворих, що страждають від порушень, пов'язаних з перевантаженням залізом. Еритопоетин (EPO) являє собою глікопротеїновий гормон, що складається з 165 амінокислот і чотирьох вуглеводневих ланцюгів, який функціонує як головний регулятор еритропоезу внаслідок зв’язування зі специфічним рецептором на поверхні клітин-попередників еритроцитів. Це зв’язування є сигналом до їх проліферації і диференціації в зрілі еритроцити. Рецептор еритропоетину являє собою глікопротеїн з 484 амінокислот з високою спорідненістю до еритропоетину. Для рецептора еритропоетину індукована лігандом гомодимеризація може бути однією з ключових подій, яка управляє активацією. Еритропоетин має відносно короткий період напівжиття. Введений внутрішньовенно еритропоетин видаляється зі швидкістю, сумісною з кінетикою першого порядку, з періодом напівжиття в циркуляції в діапазоні від приблизно 3 до 4 годин у хворих CRF. У межах діапазону терапевтичної дози рівні еритропоетину, що визначаються, в плазмі підтримуються протягом щонайменше 24 годин. Після підшкірного введення еритропоетину піки рівнів в сироватці досягаються в межах 5-24 годин і потім повільно знижуються. На ринку управління анемією домінують агенти, що стимулюють еритропоез (ESAs), мішенню яких є рецептор ростового фактора еритропоетину (EPO), який стимулює продукцію еритроцитів. EPOs, епоетин-альфа (Epogen; Amgen and Procrit/Eprex; Johnson & Johnson) і епоетин-бета (NeoRecormon/Eprex; Roche) знаходяться на ринку протягом декількох років. Дарбепоетин Amgen's (Aranesp) являє собою гіперглікозильований варіант EPO (одержаний внаслідок двох амінокислотних замін), має більш тривале напівжиття в порівнянні з епоетином, що дозволяє дарбепоетину підтримувати рівні гемоглобіну-мішені при менш частих дозах (один раз кожні 3-4 тижні у випадку дарбепоетину в порівнянні з одним разом на тиждень у випадку епоетину). Пегільований епоетин Roche's CERA (тривалий активатор рецептора еритропоетину) проходить клінічні випробування і також має більш тривале напівжиття, ніж EPO. Гематид включає димерний пептид, що не має відношення за послідовністю ні до природного EPO, ні до того, що є на ринку, який зв'язується з рецептором EPO і стимулює еритропоез. Малі пептидоміметики еритропоетину ідентифіковані декількома групами шляхом скринінга бібліотек фагового дисплея випадкових пептидів на афінність до рецептору еритропоетину. Ці послідовності не мають гомології з еритропоетином. У функціональних тестах деякі з цих пептидів виявляли активність, але тільки 1/100000 від рекомбінантного еритропоетину. Хоча було зроблено декілька спроб збільшення ефективності цих пептидів шляхом одержання ковалентних димерів або мультимерів пептидоміметиків, ці сполуки можуть бути в 1000 - 10000 разів менш активними, ніж еритропоетин в молярному вираженні, і мати дуже короткі періоди напівжиття, що робить їх не придатними для використання як терапевтичних агентів. Декілька агоністів рецепторів EPO знаходяться в даний час в процесі розробки для лікування анемії, CHF і інших показів: 55 Ліки Еритропоетини Дарбепоетин-альфа (Aranesp) Компанія Покази Анемія, пов'язана з раком Amgen 1 Статус Фаза III UA 98472 C2 CERA (рецепторний активатор безперервного еритропоезу) Застійна серцева недостатність CKD Roche NE-180 (ГлікоПЕГNeose еритропоетин) EPO-Fc Syntonix AMG 114 (гіперглікозильований Amgen аналог дарбепоетину) Синтетичний агоніст рецептора еритропоетину Гематид Affymax/Take da Замісники еритропоетину FG-2216 FibroGen FG-4592 FibroGen 5 10 15 20 25 30 35 40 Фаза II CIA CKD, CIA Зареєстровани й BLA Фаза III Фаза I CKD, CIA CIA Фаза I Фаза I *CKD, CIA, анемія у хворих з PRCA Фаза II CKD, CIA Анемія, зумовлена недостатністю процесингу заліза Фаза II Фаза I (CIA, анемія, індукована хіміотерапією; CKD, хронічне захворювання нирок; ПЕГ, поліетиленгліколь; PRCA, істинна еритроцитарна аплазія). Однак існує потреба в забезпеченні новими варіантами використання агоністів EPO, які долають одну або більше з цих і інших проблем, відомих в даній галузі техніки, і в знаходженні нових показів і способів лікування. Короткий виклад суті винаходу У даному винаході пропонуються агоністи EPOR, включаючи низькомолекулярні агоністи, пептидні або білкові агоністи, антитіла-агоністи або модифіковані імуноглобуліни, продукти розщеплення і інші їх специфічні частини і варіанти, і кодуючі їх нуклеїнова кислота, вектори і клітини-хазяїни, а також композиції, склади агоністів EPOR, поєднанні способи лікування і тому подібне, кодуючі або комплементарні нуклеїнові кислоти, вектори, клітини-хазяїни, композиції, склади, пристрої і методи їх одержання і використання для запобігання або лікування інтолерантності до глюкози і споріднених станів і/або анемії, пов'язаної із захворюванням нирок, як описано і/або можливо в даному описі, в поєднанні з тим, що відомо в даній галузі техніки. У даному винаході також пропонуються композиції, методи і пристрої для запобігання або лікування інтолерантності до глюкози і/або анемії, пов'язаної із захворюванням нирок, з використанням щонайменше одного виділеного агоніста рецептора EPO (EPOR) або конкретної частини або варіанту, як описано в цьому документі, і/або відомо в даній галузі техніки. Агоністи EPOR добре відомі в даній галузі техніки і включають, але не обмежуються цим, агоніст EPO або EPOR (або агоністи, які мають ефект активації EPOR, наприклад, HIF): пептиди, білки, хімічні сполуки або низькомолекулярні сполуки і тому подібне, і нуклеїнові кислоти, вектори і клітини-хазяїни, що кодують такі пептиди або білки, такі як, але не обмежуючись цим, EPO, модифікований EPO, білок EPO і низькомолекулярні міметики, антитіла-агоністи EPO або EPOR, або їх фрагменти або їх злиття. У даному винаході також пропонується щонайменше одна композиція для запобігання або лікування інтолерантності до глюкози і/або анемії, пов'язаної із захворюванням нирок, що включає (a) щонайменше один виділеним агоніст EPOR; і (b) придатний носій або розріджувач. Носій або розріджувач можуть необов'язково бути фармацевтично прийнятними відповідно до відомих методів. Композиція може також необов'язково додатково включати щонайменше одну додаткову сполуку, білок або композицію. У даному винаході додатково пропонується щонайменше один агоніст EPOR, конкретна частина або варіант в методі або композиції при введенні в терапевтично ефективній кількості для модуляції, лікування або зниження симптомів щонайменше одного з інтолерантності до глюкози і/або анемії, пов'язаної із захворюванням нирок (дивись, наприклад, керівництво The Merck Manual, 17th ed., Merck Research Laboratories, Merck and Co., Whitehouse Station, NJ (1999), наведене в даному описі як посилання в повному обсязі), як це потрібно при багатьох різних станах, таких як, але не обмежуючись цим, перед, після або протягом захворювання, що належить до цього, або стану, що піддається лікуванню, як відомо в даній галузі техніки. У даному винаході також пропонується щонайменше одна композиція, пристрій і/або метод доставки терапевтично або профілактично ефективної кількості щонайменше одного агоніста 2 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 EPOR або конкретної частини або варіанту за даним винаходом для запобігання або лікування інтолерантності до глюкози і/або анемії, пов'язаної із захворюванням нирок. У даному винаході також пропонується щонайменше одна композиція, що включає (a) нуклеїнову кислоту, що кодує виділений агоніст EPOR і/або агоніст EPOR, як описано в цьому документі; і (b) придатний носій або розріджувач для запобігання або лікування інтолерантності до глюкози і/або анемії, пов'язаної із захворюванням нирок. Носій або розріджувач можуть необов'язково бути фармацевтично прийнятними відповідно до відомих носіїв або розріджувачів. Композиція може необов'язково додатково включати щонайменше одну додаткову сполуку, білок або композицію. Пропонується також композиція, що включає щонайменше одне виділене міметотіло, що імітує шарнірну основу EPO людини, і щонайменше один фармацевтично прийнятний носій або розріджувач. Композиція може необов'язково додатково містити ефективну кількість щонайменше однієї сполуки або білка, вибраного щонайменше з мітки, що визначається, або репортера, протиінфекційних ліків, ліків, пов'язаних з інтолерантністю до глюкози, ліків, пов'язаних з анемією внаслідок захворювання нирок, ліків для шлунково-кишкового (GI) тракту, гормональних ліків, ліків для балансу рідин і електролітів, гематологічних ліків, антагоніста TNFальфа, релаксанту м'язів, наркотику, нестероїдного протизапальних ліків (NTHE), анальгетика, анестетика, седативного агента, місцевого анестетика, блокатора нейром’язової передачі, протимікробного агента, антипсоріазного агента, кортикостероїда, анаболічного стероїду, модулятора глюкози, імунізації, імуноглобуліну, імуносупресорного агента, гормону росту, ліків гормонзамісної терапії, радіофармацевтичного агента, антидепресанту, нейролептичного агента, збуджувального агента, ліків проти астми, бета-агоніста, стероїду для інгаляції, епінефрину або його аналога, цитокіну або антагоніста цитокіну. Пропонується також метод діагностики, запобігання або лікування інтолерантності до глюкози і/або анемії, пов'язаної із захворюванням нирок, в клітині, тканині, органі або у тварини, що включає (a) піддавання клітини, тканини, органу дії або введення тварині або введення в них композиції, що включає ефективну кількість щонайменше одного агоніста EPOR. Спосіб може необов'язково додатково включати використання ефективної кількості 0,00001-500 мг/кілограм для клітин, тканини, органу або тварини. Спосіб може необов'язково додатково включати використання приведення в контакт або введення з допомогою щонайменше одного способу, вибраного з парентерального, підшкірного, внутрішньом'язового, внутрішньовенного, внутрішньосуглобового, внутрішньобронхіального, внутрішньочеревинного, внутрішньокапсульного, внутрішньохрящового, внутрішньочеревинного, внутрішньомозочкового, всередину шлуночків мозку, всередину товстої кишки, внутрішньошийкового, внутрішньошлункового, внутрішньопечінкового, внутрішньоміокардіального, внутрішньокісткового, внутрішньотазового, внутрішньоперикардіального, внутрішньоплеврального, інтроперитонеального, внутрішньоплеврального, внутрішньопростатного, внутрішньолегеневого, внутрішньоректального, внутрішньониркового, всередину сітківки, інтраспинального, інтрасиновіального, інтрадоракального, внутрішньоматкового, внутрішньоміхурного, болюсного, вагінального, ректального, защічного, під’язикового, інтраназального або черезшкірного. У даному винаході додатково пропонується будь-який описаний в цьому документі винахід. Опис фігур Фігура 1A-B. Мишам з діабетом (db/db) внутрішньовенно вводили дозу CNTO 530 (0,3 мг/кг) або негативний контроль MMB (з відсутністю пептиду). А. IPGTT здійснювали через 10 хвилин після введення дози. В. IPGTT здійснювали через 7 днів після введення дози. Фігура 2A-B. Мишам з діабетом (DIO) внутрішньовенно вводили дозу CNTO 530 (0,3 мг/кг) або негативний контроль MMB (з відсутністю пептиду). А. IPGTT здійснювали через 10 хвилин після введення дози. В. IPGTT здійснювали через 7 днів після введення дози. Фігура 3. Мишам з діабетом (DIO) внутрішньовенно вводили дозу CNTO 530 (0,3 мг/кг) або негативний контроль MMB (з відсутністю пептиду). Через сім днів після введення дози тварин забивали і збирали кров. Фігура 4A-F. Мишам з діабетом (DIO) внутрішньовенно вводили дозу CNTO 530 (0,3 мг/кг) або ЗФР. IPGTTs здійснювали через 10 хвилин (А), 7 днів (В), 14 днів (С), 21 день (D), 28 днів (Е), 35 днів (F). Фігура 5A-C. Мишам з діабетом (DIO) внутрішньовенно вводили дозу CNTO 530 (0,3 мг/кг) або ЗФР. Тварин забивали через різні проміжки часу і збирали кров для вимірювань гематологічних параметрів. Показані рівні гемоглобіну А. 21 день, В. 28 днів і С. 35 днів після введення дози. 3 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 Фігура 6A-C. Мишам з діабетом (DIO) внутрішньовенно вводили дозу CNTO 530 (0,3 мг/кг) або ЗФР. Тварин забивали через різні проміжки часу і збирали кров для вимірювань інсуліну. Показані рівні інсуліну в циркуляторному руслі А. 21 день, В. 28 днів і С. 35 днів після введення дози. Фігура 7A-B. Мишам з діабетом (DIO) внутрішньовенно вводили дози EPO (0,03, 0,1, 0,3 мг/кг) або ЗФР. IPGTTs здійснювали через 5 днів. (А) Рівні глюкози в процесі IPGTT, (В) область під кривою з А. Фігура 8A-B. Мишам з діабетом (DIO) внутрішньовенно вводили дози EPO (0,03, 0,1, 0,3 мг/кг) або ЗФР. Через п'ять днів вимірювали (А) гемоглобін і (В) ретикулоцити. Фігура 9A-B. Мишам з діабетом (DIO) внутрішньовенно вводили дози дарбепоетину (0,01, 0,03, 0,1 мг/кг) або ЗФР. IPGTTs здійснювали через 7 днів. (А) Рівні глюкози в процесі IPGTT, (В) область під кривою з А. Фігура 10. Мишам з діабетом (DIO) внутрішньовенно вводили дози дарбепоетину (0,01, 0,03, 0,1 мг/кг) або ЗФР. Через 7 днів визначали глюкозу крові натщесерце. Фігура 11A-B. Мишам з діабетом (DIO) внутрішньовенно вводили дози дарбепоетину (0,03, 0,1, 0,3 мг/кг) або ЗФР. Через сім днів вимірювали (А) гемоглобін і (В) ретикулоцити. Фігура 12. Глюкоза крові натщесерце у мишей дикого типу (миші C57B16) або трансгенних мишей (гетерозиготних або гомозиготних), гіперекспресуючих EPO людини. Фігура 13. GTT у мишей дикого типу (миші C57B16) або трансгенних мишей (гетерозиготних або гомозиготних), гіперекспресуючих EPO людини. Фігура 14A-B. Мишам з діабетом (DIO) внутрішньовенно вводили дозу CNTO 530 (0,3 мг/кг) або ЗФР. Рівні глюкози (А) і інсуліну (В) вимірювали після нічного голодування і через 20 хвилин після глюкозного навантаження. Фігура 15. Рівні глюкози і інсуліну натщесерце, представлені на фігурі 14, використовували для розрахунку HOMA. Фігура 16. Вплив введення EPO на гемоглобін у хворих з базальними рівнями HbA1C вище 6,0. Фігура 17. Вплив введення EPO на гемоглобін A1C у хворих з базальними рівнями HbA1C вище 6,0. Фігура 18. Вплив введення EPO на глюкозу крові натщесерце у хворих з базальними рівнями HbA1C вище 6,0. Фігура 19. Вплив введення EPO на рівні HbA1C на основі відмінностей в базальному рівні HbA1C вище 6. Фігура 20. Вплив введення EPO і базальних рівнів HbA1C на рівні HbA1C на 1-2 і 4-6 місяць (лонгіт’юдні дані). Фігура 21. Вплив введення EPO на рівні глюкози крові натщесерце на 1-2 і 4-6 місяці у хворих, для яких доступні дані в момент базальної лінії t (за 2 місяці перед введенням EPO) і в подальші часові інтервали (1-3 місяці і 4-6 місяців). Опис винаходу Даний винахід стосується методу використання щонайменше одного агоніста рецептора EPO людини для запобігання або лікування інтолерантності до глюкози і/або анемії, пов'язаної із захворюванням нирок, включаючи терапевтичні композиції, методи і пристрої. Агоністи EPOR добре відомі в даній галузі техніки і включають, але не обмежуються цим, агоніст EPO або EPOR (або агоністи, які мають ефект активації EPOR, наприклад, HIF): пептиди, білки, хімічні сполуки або низькомолекулярні сполуки і тому подібне, такі як, але не обмежуючись цим, EPO, модифікований EPO, білок EPO і низькомолекулярні міметики, антитіла-агоністи EPO або EPOR, або їх фрагменти або їх злиття. Необмежувальні приклади одержання і використання агоністів EPOR пропонуються за допомогою переліку публікацій, що належать до цієї PCT в наступній таблиці, причому публікації включені в даний опис в повному обсязі як посилання, оскільки вони свідчать про стан даної галузі техніки і про те, як одержати і використовувати агоністи рецептора EPO для методів і варіантів лікування даного винаходу. Необмежувальні приклади агоністів рецептора EPO, відомі в даній галузі техніки, включають EPO, його активні фрагменти і міметики, а також хімічний агоніст рецептора EPO, які також розкриваються в подальших публікаціях, які включені в даний опис в повному обсязі як посилання: 4 UA 98472 C2 Назва публікації PCT WO9818926A1 WO06017772A1 WO06017773A1 WO05025606A1 WO04022577A2 WO02062843A2 WO9533057A1 WO04033651A2 WO03053997A2 WO0243572A2 WO9928346A1 WO06055412A1 WO06014466A2 WO06002646A2 WO05121173A1 WO05070451Al WO05063808A1 WO05051327A2 WO05021579A2 WO04024761A1 WO03029291A2 WO02085940A2 WO0138342A2 WO0061164A1 WO9938890A1 WO9911781A1 WO9907401A2 WO9905268A1 WO9858660A1 WO9709996A1 WO9635718A1 WO06062685A2 WO06060148A2 WO06029094A2 WO06014349A2 WO05112998A2 WO05103076A2 WO05100403A2 WO05099773A1 WO05097167A1 WO05092369A2 WO05087804A1 Переносимі в циркуляторному руслі агоністи рецептора еритропоетину Стабільні суспензійні склади агоністів рецептора еритропоетину Стабільні частинкові склади агоністів рецептора еритропоетину Тривало діючі еритропоетини, які підтримують захисну активність відносно тканин ендогенного еритропоетину Тривало діючі еритропоетини, які підтримують захисну активність відносно тканин ендогенного еритропоетину Модифікований еритропоетин (Epo) із зниженою імуногенністю Гібридна молекула формули Gm-Csf-L-Epo або Epo-L-Gm-Csf для стимуляції гемопоезу Еритропоетин: модернізація і глікокон’югація еритропоетину Методи збільшення ендогенного еритропоетину (Epo) Експресія еритропоетину і рецептора еритропоетину при раку людини Еритропоетин з високою специфічною активністю Методи лікування стійкості до еритропоетину Новий карбамілований Epo і метод його одержання Новий карбамілований Epo і метод його одержання Метод очищення еритропоетину Фармацевтична композиція, що включає неглікозильований еритропоетин Злитий білок Fc-еритропоетин з поліпшеною фармакокінетикою Глікопегільований еритропоетин Пептидні міметики і злиті білки Epo Гакільовані поліпептиди, особливо гакільований еритропоетин Пегільований і диглікозильований еритропоетин Нові полінуклеотиди і поліпептиди гена еритропоетину Нові пептидні димери як агоністи рецептора еритропоетину (Epo) і пов'язані з цим методи синтезу і використання Модуляція функції збудливої тканини еритропоетином, що периферично вводиться Еритропоетин із зміненою біологічною активністю Рекомбінантний еритропоетин людини зі сприятливим профілем глікозилування Використання еритропоетину і препаратів заліза для одержання поєднаних фармацевтичних препаратів для лікування ревматичних захворювань Одержання еритропоетину активацією ендогенного гена Поєднані фармацевтичні препарати, що містять еритропоетин і модифікований гемоглобін Поєднані фармацевтичні препарати, що містять еритропоетин і препарати заліза Метод одержання еритропоетину, що не містить тваринних білків Нові пептиди, які зв'язуються з рецептором еритропоетину Нові пептиди, які зв'язуються з рецептором еритропоетину Похідні еритропоетину із зміненої імуногенністю Метод одержання повністю карбамільованого еритропоетину Композиції і методи запобігання гіпертензії, пов'язаної з еритрпоетином Варіанти білка еритропоетину Антитіла проти рецептора еритропоетину і їх використання Використання еритропоетину для лікування раку Поєднання режиму дозування для еритропоетину Кон’югати гідроксіетилкрохмалю і еритропоетину Рідкий склад еритропоетину 5 UA 98472 C2 WO05079232A2 WO05063809A1 WO05058347A1 WO05053745A1 WO05032460A2 WO05014025A1 WO05001136Al WO05000340A1 WO04108681A1 WO04108667A2 WO04108152A1 WO04106373A1 WO04101611A2 WO04101606A2 WO04091495A2 WO04043382A2 WO04035603A2 WO04006958A1 WO04006948A1 WO04005323A2 WO04002493A1 WO03094858A2 WO03064664A1 WO03055526A2 WO03048210A1 WO03046013A1 WO03037273A2 WO03012432A1 WO02089799A2 WO02064085A2 WO02053580A2 WO0249673A2 WO0248194Al WO0214356A2 WO0187329A1 WO0159074A1 WO0136489A2 WO0129178A2 WO0107075A2 WO0102017A2 Метод одержання злитих білків аналога еритропоетину-IgG людини з молока трансгенних ссавців Ідентичний природному еритропоетин Використання еритропоетину при лікуванні порушень розподілу заліза при хронічних запальних захворюваннях кишечнику Склад розчину еритропоетину Міметотіла, що імітують шарнірну основу Epo людини, композиції, методи і використання Склад вільного від альбуміну еритропоетину Методи і композиції для модуляції експресії еритропоетину Синергічні композиції, що включають еритропоетин і бурштинову кислоту (сіль) Гетероарильні сполуки, що містять азот, і їх використання для збільшення ендогенної продукції еритропоетину Склад нових кон’югатів еритропоетину з використанням трансглютамінази Стабільний водний розчин еритропоетину людини, що не містить сироваткового альбуміну Сполуки кон’югатів еритропоетину із збільшеними періодами напівжиття Нові пептиди, які зв'язуються з рецептором еритропоетину Нові пептиди, які зв'язуються з рецептором еритропоетину Композиції і методи, що належать до одержання еритропоетину Поліпшені варіанти еритропоетину і методи використання Антитіла, що зв'язуються з рецептором еритропоетину Стабільна фармацевтична композиція, що включає еритропоетин Стабільна фармацевтична композиція, що включає еритропоетин Малі молекули зі спорідненістю до рецептору Epo Агент, що потенціює продукцію еритропоетину Ctp-розширений еритропоетин Фізіологічно регульований експресуючий еритропоетин вектор для лікування анемії Кон'югати еритропоетину Злитий білок, що має підвищену еритропоетинову активність in vivo Злитий білок, що має підвищену активність еритропоетину in vivo Метод використання еритропоетину для лікування гострої ішемічної ниркової недостатності Поєднана терапія еритропоетином і протипухлинним фактором некрозу пухлин альфа Використання дигідропіразолів для підвищення еритропоетину і васкуляризації Лікування нейрологічної дисфункції, що включає сульфамати фруктопіранози і еритропоетин Захист, відновлення і приріст клітин, тканин і органів, що відповідають на еритропоетин Кон'югати еритропоетину Злитий білок, що має підвищену активність еритропоетину in vivo Терапевтичні методи лікування індивідуумів рекомбінантним еритропоетином, що має високу активність і знижені побічні ефекти Рідка фармацевтична композиція, що містить похідне еритропоетину Метод одержання трансгенного, продукованого у свиней еритропоетину людини і трансгенні свині Форми еритропоетину з поліпшеними властивостями Ген 1 первинної відповіді на Epo, Eprg1 Склади еритропоетину для багаторазового прийому Похідні еритропоетину 6 UA 98472 C2 WO0067776A1 WO0061637A1 WO0061169Al WO0028066A1 WO0027997A1 WO0027869A1 WO0027419A1 WO0014261A1 WO0009713A1 WO9966054A2 WO9954279A1 WO9952543A2 WO9947151A1 WO9921966A1 WO9906063A1 WO9902709A1 WO9823643A1 WO9819695A1 WO9807442A1 WO9749729A1 WO9748729A1 WO9741526A1 WO9727219A1 WO9708200A1 WO9640749A1 WO9640073A2 WO9632413A1 WO9619573A1 WO9618647A1 WO9603438A1 WO9505469A1 WO9505465A1 WO9425055A1 WO9424160A2 WO9417784A1 WO9402611A2 WO9325221A1 WO9305807A2 WO9118973A1 WO9111200A1 WO9106630A1 WO9105867A1 Фармакокінетичне і фармакодинамічне моделювання введення еритропоетину Антитіла до рецептору еритропоетину Фармацевтичні композиції еритропоетину Клітини-хазяїни, що експресують рекомбінантний еритропоетин людини Метод масивної культури клітин, що продукують рекомбінантний еритропоетин людини Методи очищення рекомбінантного еритропоетину людини з супернатантів клітинної культури Метод одержання ліофілізованих фармацевтичних композицій рекомбінантного еритропоетину людини, стабільних при кімнатній температурі Одержання еритропоетину людини Аденовірусні вектори, що кодують еритропоетин, і їх використання в генній терапії Злиття аналога еритропоетину-сироваткового альбуміну людини Міметики еритропоетину із замінами амінокислот Фармацевтичні композиції, що включають еритропоетин, для лікування раку Пептидні ліганди рецептора еритропоетину Опосередкований еритропоетином нейрогенез Ген первинної відповіді на Epo, Eprg3pt Злиті білки рекомбінантний еритропоетин/імуноглобулін Мультимерний еритропоетин з підвищеною біологічною активністю Пристрій і метод для доставки еритропоетину Препарат з постійним вивільненням, що включає еритропоетин і полілактидспівгліколід Поліпептиди-міметики активності еритропоетину людини Двовалентні молекули, які утворюють активуючий комплекс з рецептором еритропоетину Низькомолекулярні міметики еритропоетину Методи очищення і використання еритропоетинзв’язувального білка Еритропоетинзв’язувальний білок, придатний для регуляції еритропоезу, і метод його визначення Сполуки і пептиди, які зв'язуються з рецептором еритропоетину Композиція для постійного вивільнення неагрегованого еритропоетину Спосіб очищення глікопротеїнів, подібні еритропоетину Рекомбінантні молекули ДНК і експресійні вектори для еритропоетину Висушуваний при розпиленні еритропоетин Антитіла, які активують рецептор еритропоетину Фрагмент рецептора еритропоетину людини і антитіла до нього Аналоги еритропоетину Композиції аналогів еритропоетину і методи Мутантні білки еритропоетину з підвищеною активністю Легеневе введення еритропоетину Рекомбінантний еритропоетин людини із зміненою біологічною активністю Система доставки лікарського еритропоетину Агенти, що посилюють дію еритропоетину, і методи їх використання Залежні від еритропоетину еритробластоїдні клітинні лінії миші Поліпшений склад еритропоетину на основі циклодекстрину Залежна від факторів гематопоетична клітинна лінія, що демонструє Epo дозрівання еритроцитів, що індукується Ізоформи еритропоетину 7 UA 98472 C2 WO900882A1 WO8800241A1 WO8604068A1 WO8603520A1 WO8503079A1 WO8403152Al Рецептори еритропоетину Ген еритропоетину людини: високий рівень експресії в стабільно трансфікованій клітині ссавця Гомогенний еритропоетин Метод одержання еритропоетину CDA клон еритропоетину людини Atcc Hb8209 і її моноклональне антитіло до еритропоетину Деякі агоністи рецептора EPO знаходяться в даний час на стадії розробки для анемії, CHF і інших показів і можуть бути використані як агоністи рецептора EPO в методах даного винаходу: Ліки Еритропоетини Дарбепоетин-альфа (Aranesp) CERA (рецепторний активатор безперервного еритропоезу) Компанія Свідчення Анемія, пов'язана з раком Застійна серцева недостатність CKD Amgen Roche NE-180 (ГлікоПЕГNeose еритропоетин) EPO-Fc Syntonix AMG 114 Amgen (гіперглікозильований аналог дарбепоетину) Синтетичний агоніст рецептора еритропоетину Гематид Affymax/ Takeda* Замісники еритропоетину FG-2216 FibroGen FG-4592 FibroGen Статус Фаза III Фаза II CIA CKD, CIA Зареєстрован ий BLA Фаза III Фаза I CKD, CIA CIA Фаза I Фаза I *CKD, CIA, анемія у хворих з PRCA Фаза II CKD, CIA Анемія, зумовлена недостатністю процесинга заліза Фаза II Фаза I 5 10 15 20 25 30 Інші антагоністи рецептора EPO даного винаходу включають злиті білки з антитілом, які містять пептиди-агоністи рецептора EPO, будь-який з яких може бути використаний за даним винаходом. Необмежувальні приклади включають міметотіла EPO, як розкрито в патентних заявках США nos. 10/609783, зареєстрованій 30 червня 2003 р. і 10/935005, зареєстрованій 3 вересня 2004 р., кожна з яких включена в даний опис в повному обсязі як посилання. В іншому необмежувальному прикладі агоніста EPOR, який може використовуватися в методах даного винаходу, в даному винаході пропонується також щонайменше одне виділене міметотіло, що імітує шарнірну основу EPO, або конкретна частина, або варіант, як описано в цьому документі і/або відомо в даній галузі техніки. Міметотіло, що імітує шарнірну основу EPO, може необов'язково включати щонайменше одну область CH3, безопосередковано зв'язану з щонайменше однією областю CH2, безопосередковано зв'язану з щонайменше однією областю шарніра або його фрагмента (Н), безопосередковано зв'язаного з необов'язковою лінкерною послідовністю (L), безопосередковано зв'язаною з щонайменше одним терапевтичним пептидом (Р), необов'язково додатково безопосередковано зв'язаним з щонайменше частиною щонайменше однієї варіабельної (V) послідовності антитіла. У переважному здійсненні міметотіло, що імітує шарнірну основу EPO, включає формулу (I): ((V(m)-Р(n)-L(про)-Н(р)-CH2(q)-CH3(r))(s), де V являє собою щонайменше одну частину N-кінця варіабельної області імуноглобуліну, Р являє собою щонайменше один біологічно активний пептид, L являє собою поліпептид, який забезпечує структурну гнучкість, дозволяючи міметотілу мати альтернативні орієнтації і зв'язувальні властивості, Н являє собою щонайменше частину варіабельної шарнірної області імуноглобуліну, CH2 являє собою щонайменше частину константної області CH2 імуноглобуліну, CH3 являє собою щонайменше частину константної області CH3 імуноглобуліну, m, n, про, р, q, r і s можуть незалежно являти собою ціле число між 0, 1 або 2 і 10, імітуючи різні типи молекул імуноглобулінів, наприклад, але не обмежуючись цим, IgG1, 8 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 60 IgG2, IgG3, IgG4, IgA, IgM, IgD, IgE і тому подібне, або їх поєднання. Мономер, в якому m=1, може бути з’єднаний з іншими мономерами шляхом асоціації або ковалентного зв'язку, такого як, але, не обмежуючись цим, Cys-Cys дисульфідний зв'язок, або іншою послідовністю імуноглобуліну. Міметотіло даного винаходу, що імітує шарнірну основу EPO, імітує структуру антитіла із заданими властивостями і функціями, в той же час, забезпечуючи терапевтичним пептидом і його заданими або надбаними властивостями або активністю in vitro, in vivo або in situ. Різні частини антитіла і частини терапевтичного пептиду щонайменше одного міметотіла даного винаходу, що імітує шарнірну основу EPO, можуть варіюватися, як описано в цьому документі в поєднанні з тим, що відомо в даній галузі техніки. Застосовуване в даному описі «міметотіло, що імітує шарнірну основу EPO», «частину міметотіла, що імітує шарнірну основу EPO» або «фрагмент міметотіла, що імітує шарнірну основу EPO», і/або «варіант міметотіла, що імітує шарнірну основу EPO» і подібні ним міметики мають або імітують зв’язування щонайменше одного ліганду або щонайменше одну біологічну активність щонайменше одного білка, таку як зв’язування ліганду або активність in vitro, in situ і/або переважно in vivo, такі як, але не обмежуючись цим щонайменше одна з SEQ ID NOS: 130. Наприклад, придатні міметотіло, конкретна частина або варіант даного винаходу, що імітує шарнірну основу EPO, можуть зв'язувати щонайменше один білковий ліганд і включають щонайменше один білковий ліганд, рецептор, розчинний рецептор і тому подібне. Придатні міметотіло, конкретна частина або варіант, що імітує шарнірну основу EPO, можуть також модулювати, збільшувати, модифікувати, активувати щонайменше один сигнальний шлях білкового рецептора або іншу піддану вимірюванню або визначенню активність. Міметотіла, придатні в методах і композиціях даного винаходу, характеризуються відповідною спорідненістю зв’язування з білковими лігандами або рецепторами і необов'язково і переважно мають низьку токсичність. Зокрема, міметотіло, що імітує шарнірну основу EPO, в якому індивідуальні компоненти, такі як частина варіабельної області, константна область (без частини CH1) і скелет або будь-яка його частина (наприклад, частина областей J, D або V варіабельної області важкого або легкого ланцюга; щонайменше частина щонайменше однієї шарнірної області, константна область важкого ланцюга або легкого ланцюга і тому подібне) індивідуально і/або спільно необов'язково і переважно мають низьку імуногенність, використовуються в даному винаході. Міметотіла, які можуть бути придатні у винаході, необов'язково характеризуються за їх здатністю лікувати хворих протягом тривалих періодів з від хорошого до прекрасного послаблення симптомів і низькою токсичністю. Низька імуногенність і/або висока спорідненість, а також іншіневизначені властивості можуть вносити внесок в досягнуті терапевтичні результати. «Низька імуногенність» визначається в даному описі як ріст значущих відповідей HAMA, HACA або HAHA менше ніж у приблизно 75% або переважно менше ніж у приблизно 50, 45, 40, 35, 30, 35, 20, 15, 10, 9, 8, 7, 6, 5, 4, 3, 2, і/або 1% хворих, що одержували лікування, і/або індукція низьких титрів у хворих, що одержували лікування (менше приблизно 300, менше приблизно 100 при вимірюванні імуноферментним аналізом з двома антигенами) (дивись, наприклад, Elliott et al., Lancet 344:1125-1127 (1994)). Застосування Виділені нуклеїнові кислоти даного винаходу можуть бути використані для одержання щонайменше одного міметотіла, що імітує шарнірну основу EPO, його фрагмента або конкретного варіанту, які можуть бути використані (або кодуючої ДНК) для дії на клітину, тканину, орган або тварину (включаючи ссавців і людину) для модуляції, лікування, послаблення, допомоги в запобіганні захворюваності або зниженні симптомів щонайменше одного стану, вибраного з, але не обмежуючись цим, щонайменше інтолерантності до глюкози і/або захворювання нирок, пов'язаного з анемією, а також інших відомих або конкретних пов'язаних з білком станів. Такий метод може включати введення ефективної кількості композиції або фармацевтичної композиції, що включає щонайменше одне міметотіло, що імітує шарнірну основу EPO, або конкретну частину або варіант, в клітину, тканину, орган, тварині або хворому, що потребує таку модуляцію, лікування, послаблення, запобігання або зниження симптомів, ефектів або механізмів. Ефективна кількість може включати кількість від приблизно 0,0001 до 500 мг/кг на одну або множину введень, або до досягнення концентрації в сироватці 0,0001-5000 мкг/мл концентрації в сироватці на одну або множину введень, або будь-який ефективний діапазон або величину в його межах, як це робиться і визначається з використанням відомих методів, як описано в цьому документі або відомо в даній галузі техніки. Цитування Всі публікації або патенти, цитовані в даному описі, наведені в даному описі в повному обсязі як посилання, оскільки вони відображають стан рівня техніки до моменту даного 9 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 60 винаходу і/або дають право і можливість опису даного винаходу. Публікації посилаються на будь-які наукові або патентні публікації або на будь-яку іншу інформацію, доступну в будь-якому форматі носія, включаючи всі записані, електронні або друкарські формати. Наступні посилання наведені в повному об'ємі в даному описі як посилання: Ausubel, et al., ed., Current Protocols in Molecular Biology, John Wiley & Sons, Inc., NY, NY (1987-2006); Sambrook, et al., Molecular nd Cloning: А Laboratory Manual, 2 Edition, Cold Spring Harbor, NY (1989); Harlow and Lane, Antibodies, а Laboratory Manual, Cold Spring Harbor, NY (1989); Colligan, et al., eds., Current Protocols in Immunology, John Wiley & Sons, Inc., NY (1994-2006); Colligan et al., Current Protocols in Protein Science, John Wiley & Sons, NY, NY, (1997-2006). Міметотіла або агоністи рецептора EPO даного винаходу Міметотіло, що імітує шарнірну основу EPO, може необов'язково включати щонайменше одну область CH3, безопосередковано зв'язану щонайменше з однією областю CH 2, безопосередковано зв'язану з щонайменше однією частиною щонайменше одного фрагмента шарнірної області (Н), такої як така, що включає щонайменше одну область основи шарніра, безопосередковано зв'язаного з необов'язковою лінкерною послідовністю (L), безопосередковано зв'язаною з щонайменше одним терапевтичним пептидом (Р), необов'язково додатково безопосередковано зв'язаним з щонайменше частиною щонайменше однієї варіабельної (V) послідовності антитіла. У переважному варіанті здійснення пара CH3CH2-H-L-V, являє собою пару, зв'язану шляхом асоціації або ковалентного зв'язку. Таким чином, міметотіло даного винаходу, що імітує шарнірну основу EPO, імітує структуру антитіла з властивими йому властивостями і функціями, в той же час, пропонуючи терапевтичний пептид з властивими йому або надбаними властивостями або активністю in vitro, in vivo або in situ. Різні частини антитіла і частини терапевтичного пептиду щонайменше одного міметотіла даного винаходу, що імітує шарнірну основу EPO, можуть варіюватися, як описано в цьому документі в поєднанні з тим, що відомо в даній галузі техніки. Міметотіла даного винаходу, таким чином, забезпечують щонайменше однією відповідною властивістю в порівнянні з відомими білками, такою як, але не обмежуючись цим, щонайменше одна із збільшеного періоду напівжиття, підвищеної активності, більш специфічній активності, підвищеної спорідненості, підвищеної або зниженої швидкості видалення, селективного або більш придатного набору активності, меншої імуногенності, підвищеної якості або тривалості щонайменше одного бажаного терапевтичного ефекту, менших побічних ефектів і тому подібного. Фрагменти міметотіл за формулою (I) можуть бути одержані за допомогою ферментативного розщеплення, способів синтезу або рекомбінантних способів, як відомо в даній галузі техніки і/або описано в цьому документі. Міметотіла можна також одержувати у вигляді різноманітних укорочених форм з використанням генів антитіл, в які введені один або більше стоп-кодонів вище природного сайту термінації транскрипції. Різні частини міметотіл можуть бути зв’язані разом хімічно за допомогою загальноприйнятих методів або можуть бути одержані у вигляді безперервного білка з використанням методів генної інженерії. Наприклад, для одержання безперервного білка для використання в міметотілах даного винаходу можна експресувати нуклеїнову кислоту, що кодує щонайменше одну з константних областей ланцюга антитіла людини. Дивись, наприклад, Ladner et al., патент США No. 4946778 і Bird, R.E. et al., Science, 242: 423-426 (1988), відносно одноланцюжкових антитіл. Термін «міметотіло людини», що застосовується в даному описі, належить до антитіла, в якому по суті кожна частина білка (наприклад, пептид-міметик EPO, скелет, домени CL, CH (наприклад, CH2, CH3), шарнір (VL, VH)), як очікується, по суті не буде імуногенним у людини при тільки мінорних замінах або варіаціях послідовності. Такі зміни або варіації необов'язково і переважно зберігають або знижують імуногенність у людини в порівнянні з немодифікованими антитілами людини або міметотілами даного винаходу. Таким чином, антитіло людини і відповідне міметотіло, що імітує шарнірну основу EPO даного винаходу, відрізняються від химерного або гуманізованого антитіла. Підкреслюється, що антитіло людини і відповідне міметотіло, що імітує шарнірну основу EPO, можуть бути одержані у тварини, що не є людиною, або за допомогою генів. У переважному здійсненні щонайменше одному міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретну частину, або варіант даного винаходу одержують з допомогою щонайменше одній лінії клітин, змішаної лінії клітин, іморталізованої клітини або клональної популяції іморталізованих і/або культивованих клітин. Іморталізовані клітини, що продукують білок, можуть бути одержані з використанням відповідних методів. Переважно щонайменше одне міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретну частину, або варіант даного винаходу створюють шляхом 10 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 забезпечення нуклеїновою кислотою або векторами, що включає ДНК, що походить або має по суті схожу послідовність з щонайменше одним локусом імуноглобуліну людини, який функціонально реорганізують або який піддають функціональній реорганізації і який додатково включає структуру міметотіла, як описано в цьому документі, наприклад, але не обмежуючись цим, в формулі (I), де частини С- і N-кінців варіабельних областей можуть бути використані для V, шарнірні області для Н, CH2 для CH2 і CH3 для CH3, як відомо в даній галузі техніки. Молекули нуклеїнової кислоти Використовуючи інформацію, що пропонується в даному описі і відоме в даній галузі техніки, таке як нуклеотидні послідовності, що кодують різні пептидні або білкові агоністи EPO R, може бути одержана молекула нуклеїнової кислоти даного винаходу, що кодує щонайменше один агоніст EPO R, з використанням описаних в цьому документі методів або відомих в даній галузі техніки. Молекули нуклеїнової кислоти даного винаходу можуть бути в формі РНК, такій як мРНК, гяРНК, тРНК або будь-яка інша форма, або в формі ДНК, включаючи, але, не обмежуючись цим, кДНК і геномну ДНК, що одержуються за допомогою клонування або продуковані синтетично або за допомогою будь-якого їх поєднання. ДНК може бути триспіральною, двуспіральною або односпіральною або будь-яким їх поєднанням. Будь-яка частина щонайменше однієї спіралі ДНК або РНК може бути кодуючим ланцюгом, також відомим як смисловий ланцюг або вона може бути некодуючим ланцюгом, що позначається також як антисмисловий ланцюг. Виділені молекули нуклеїнової кислоти даного винаходу можуть включати молекули нуклеїнової кислоти, що включають відкриту рамку считування (ORF), необов'язково з одним або більше інтронів, молекули нуклеїнової кислоти, що включають кодуючу послідовність для міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або конкретної частини, або варіанту; і молекули нуклеїнової кислоти, які включають нуклеотидну послідовність, по суті відмінну від послідовностей, описаних вище, але яка завдяки вирожденості генетичного коду, все ще кодує щонайменше одне міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, як описано в цьому документі і/або відомо в даній галузі техніки. Зазвичай, генетичний код добре відомий в даній галузі техніки. Таким чином, для фахівця в даній галузі техніки повинно бути звичайним створення таких варіантів нуклеїнової кислоти з вирожденостістю коду, які кодують конкретне міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретну частину, або варіанти даного винаходу. Дивись, наприклад, Ausubel, et al., вище, і такі варіанти нуклеїнової кислоти включаються в даний винахід. Як вказується в даному описі, молекули нуклеїнової кислоти даного винаходу, які включають нуклеїнову кислоту, що кодує міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретну частину, або варіант, можуть включати, але не обмежуються цим, молекули, що самі кодують амінокислотну послідовність міметотіла, що імітує шарнірну основу EPO, або фрагмент іншого агоніста рецептора EPO; кодуючу послідовність для повного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або їх частини; кодуючу послідовність для міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, фрагмента або частини, а також додаткові послідовності, такі як кодуюча послідовність щонайменше одного сигнального лідируючого пептиду або злитого пептиду, з або без вказаних вище додаткових кодуючих послідовностей, таких як щонайменше один інтрон спільно з додатковими некодуючими послідовностями, включаючи, але, не обмежуючись цим, некодуючі 5'- і 3'-послідовності, такі як транскрибовані, нетрансльовані послідовності, які грають роль в транскрипції, процесинзі мРНК, включаючи сигнали сплайсингу і поліаденілування (наприклад, зв’язування з рибосомами і стабільність мРНК); додаткову кодуючу послідовність, яка кодує додаткові амінокислоти, такі як амінокислоти, що забезпечують додатковими функціями. Таким чином, послідовність, що кодує міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретну частину, або варіант, може бути з’єднана з маркерною послідовністю, такою як послідовність, що кодує пептид, який сприяє очищенню злитого міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або конкретної частини, або варіанту, що включає міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або частину. Полінуклеотиди, які селективно гібридизуються з полінуклеотидом, як описано в цьому документі У даному винаході пропонуються виділені нуклеїнові кислоти, які гібридизуються в селективних умовах гібридизації з розкритим в даному описі полінуклеотидом або іншим, розкриті в даному описі, включаючи конкретні варіанти або їх частини. Таким чином, 11 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 60 полінуклеотиди цього варіанту здійснення можуть бути використані для виділення, визначення і/або кількісної оцінки нуклеїнових кислот, що включають такі полінуклеотиди. Умови гібридизації з низькою або помірною жорсткістю є типовими, але не єдиними, що застосовуються з послідовностями, що мають редуковану ідентичність послідовності по відношенню до комплементарних послідовностей. Умови з помірною і високою жорсткістю можуть необов'язково застосовуватися для послідовностей з більш високою ідентичністю. Умови з низькою жорсткістю дозволяють селективно гібридизувати послідовності, що мають приблизно 40-99% ідентичність послідовностей, і можуть використовуватися для ідентифікації ортологічних або паралогічних послідовностей. Необов'язково полінуклеотиди цього винаходу повинні кодувати щонайменше частину міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або конкретну частину або варіант, що кодуються описаними в цьому документі полінуклеотидами. Полінуклеотиди цього винаходу охоплюють послідовності нуклеїнової кислоти, які можуть використовуватися для селективної гібридизації з полінуклеотидом, що кодує міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретну частину або варіант даного винаходу. Дивись, наприклад, Ausubel, вище; Colligan, вище, кожний з яких наведений в даному описі в повному обсязі як посилання. Конструкція нуклеїнових кислот Виділені нуклеїнові кислоти даного винаходу можуть бути створені з використанням (a) рекомбінантних методів, (b) методів синтезу, (с) методів очищення або їх поєднання, як добре відомо в даній галузі техніки. Нуклеїнові кислоти можуть відповідним чином включати послідовності в доповнення до полінуклеотиду даного винаходу. Наприклад, сайт множинного клонування, що включає один або більше сайтів рестрикції ендонуклеазами, може бути включений в нуклеїнову кислоту для сприяння виділенню полінуклеотиду. Можуть бути включені також послідовності, що транслюються для допомоги у виділенні трансльованого полінуклеотиду даного винаходу. Наприклад, гексагістидинова маркерна послідовність створює зручні умови для очищення білків даного винаходу. Нуклеїнова кислота даного винаходу, виключаючи кодуючу послідовність, являє собою необов'язково вектор, адаптер або лінкер для клонування і/або експресії полінуклеотиду даного винаходу. Додаткові послідовності можуть бути додані до таких клонуючих і/або експресійних послідовностей для оптимізації їх функції при клонуванні і/або експресії, для допомоги у виділенні полінуклеотиду або для поліпшення введення полінуклеотиду в клітину. Використання клонуючих векторів, експресійних векторів, адаптерів і лінкерів добре відоме в даній галузі техніки. Дивись, наприклад, Ausubel, вище; або Sambrook, вище. Рекомбінантні методи для створення нуклеїнових кислот Композиції виділених нуклеїнових кислот цього винаходу, такі як РНК, кДНК, геномна ДНК або будь-яке їх поєднання, можуть бути одержані з біологічних джерел з використанням будьякої кількості методів клонування, відомих фахівцям в даній галузі техніки. У деяких варіантах здійснення олігонуклеотидні зонди, які селективно гібридизуються при відповідних умовах жорсткості з полінуклеотидами даного винаходу, використовують для ідентифікації бажаної послідовності в бібліотеці кДНК або геномній ДНК. Виділення РНК і створення кДНК і геномних бібліотек добре відоме фахівцям в даній галузі техніки. (Дивись, наприклад, Ausubel, вище; або Sambrook, вище). Синтетичні методи створення нуклеїнових кислот Виділені нуклеїнові кислоти даного винаходу можуть бути також одержані за допомогою прямого хімічного синтезу шляхом відомих методів (Дивись, наприклад, Ausubel et al., вище). При хімічному синтезі звичайно одержують одноланцюжковий олігонуклеотид, який може бути перетворений на дволанцюжкову ДНК шляхом гібридизації з комплементарною послідовністю або за допомогою полімеризації з ДНК-полімеразою з використанням одного ланцюга як матриці. Фахівець в даній галузі техніки знає, що тоді як хімічний синтез ДНК може бути обмежений послідовностями з приблизно 100 або більше основ, більш довгі послідовності можуть бути одержані за допомогою лігування більш коротких послідовностей. Рекомбінантні експресійні касети У даному винаході додатково пропонуються рекомбінантні експресійні касети, що включають нуклеїнову кислоту даного винаходу. Послідовність нуклеїнової кислоти даного винаходу, наприклад, кДНК або геномна послідовність, що кодує міметотіло, імітуюче шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретну частину або варіант даного винаходу, може бути використана для створення рекомбінантної експресійної касети, яка може бути введена в щонайменше одну бажану клітину-хазяїна. Рекомбінантна експресійна касета 12 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 60 зазвичай повинна включати полінуклеотид даного винаходу, оперативно зв'язаний з регуляторними послідовностями ініціації транскрипції, які повинні управляти транскрипцією полінуклеотиду в призначеній клітині-хазяїні. Як гетерологічні, так і негетерологічні (тобто ендогенні) промотори можуть використовуватися для управління експресією нуклеїнових кислот даного винаходу. У деяких варіантах здійснення виділені нуклеїнові кислоти, які служать як промотор, енхансер або інші елементи, можуть бути введені у відповідному положенні (вище, нижче або в інтрон) негетерологічної форми полінуклеотиду даного винаходу, так щоб позитивно або негативно регулювати експресію полінуклеотиду даного винаходу. Наприклад, ендогенні промотори можуть бути змінені in vivo або in vitro за допомогою мутації, делеції і/або заміни, як відомо в даній галузі техніки. Полінуклеотид даного винаходу можна експресувати або в смисловій, або в антисмисловій орієнтації, як це бажано. Необхідно брати до уваги, що контроль експресії гена або в смисловій, або в антисмисловій орієнтації може мати прямий вплив на характеристики, що спостерігаються. Іншим методом пригнічення є смислове пригнічення. Введення нуклеїнової кислоти з конфігурацією в смисловій орієнтації, як показано, є ефективним способом блокування транскрипції генів-мішеней. Вектори і клітини-хазяїни Даний винахід також належить до векторів, які включають виділені молекули нуклеїнової кислоти даного винаходу, клітин-хазяїнів, які генетично модифіковані рекомбінантними векторами, і до продукції щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або конкретної частини або варіанту за допомогою рекомбінантних способів, як добре відомо в даній галузі техніки. Дивись, наприклад, Sambrook, et al., вище; Ausubel, et al., вище, кожна з яких наведена в даному описі в повному обсязі як посилання. Полінуклеотиди можуть бути необов'язково зв’язані з вектором, що містить маркер селекції, для розмноження в хазяїні. Зазазвичай в клітину вводять плазмідний вектор, використовуючи відповідні відомі методи, такі як електропорація і тому подібне, інші відомі методи включають використання вектора у вигляді преципітату, такого як преципітат фосфату кальцію, або в комплексі із зарядженим ліпідом. Якщо вектором є вірус, він може бути упакований in vitro з використанням відповідної упаковуючої лінії клітин і потім введений в клітини-хазяїни. Введена ДНК повинна бути оперативно зв'язана з відповідним промотором. Експресійні конструкти повинні додатково містити сайти необов'язково для щонайменше одного, з сайту ініціації транскрипції, термінації транскрипції і в транскрибованій області сайт зв’язування рибосомою для трансляції. Кодуюча частина зрілих транскриптів, експресованих конструктами, повинна переважно включати на початку сайт ініціації трансляції і кодон термінації (наприклад, UAA, UGA або UAG), відповідним чином розташований на кінці мРНК, яка буде транслюватися, з UAA і UAG, переважними для експресії в клітинах ссавців або еукаріотних клітинах. Експресійні вектори повинні переважно, але необов'язково, включати щонайменше один маркер селекції. Такі маркери включають, але не обмежуються цим, гени стійкості до метотрексату (MTX), дигідрофолатредуктази (DHFR, патенти США Nos. 4399216; 4634665; 4656134; 4956288; 5149636; 5179017, ампіциліну, неоміцину (G418), мікофенолової кислоти або глутамінсинтетази (GS, патенти США Nos. 5122464; 5770359; 5827739) для культури еукаріотних клітин і гени стійкості до тетрацикліну або ампіциліну для культивування Е. coli і інших бактерій або прокаріот (вказані вище патенти включені в даний опис в повному обсязі як посилання). Придатні культуральні середовища і умови для описаних вище клітин-хазяїнів відомі в даній галузі техніки. Придатні вектори повинні бути з легкістю ясні фахівцеві в даній галузі техніки. Введення векторної конструкції в клітину-хазяїна може бути здійснене за допомогою трансфекції з фосфатом кальцію, трансфекції, опосередкованої ДЕАЕ-декстраном, трансфекції, опосередкованої катіонним ліпідом, електропорації, трансдукції, інфікування або інших відомих методів. Такі методи описані в даній галузі техніки, такій як Sambrook, вище, розділи 1-4 і 16-18; Ausubel, вище, розділи 1, 9, 13, 15, 16. Щонайменше одне міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретна частина або варіант даного винаходу може експресуватися в модифікованій формі, такій як злитий білок, і може включати не тільки сигнали секреції, але також додаткові гетерологічні функціональні області. Наприклад, область додаткових амінокислот, особливо заряджених амінокислот, може бути додана до N-кінця міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або конкретної частини або варіанту для поліпшення стабільності і виживаності в клітині-хазяїні в процесі очищення або в процесі подальшої обробки і зберігання. До міметотіла, що імітує шарнірну основу EPO, або до іншого агоніста рецептора EPO, або до конкретної частини або варіанта даного винаходу 13 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 60 можуть бути також додані пептидні частини для полегшення очищення. Такі області можуть бути видалені перед остаточним одержанням міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або щонайменше одного його фрагмента. Такі методи описані в багатьох стандартних лабораторних керівництвах, таких як Sambrook, (2003), вище, розділи 17.29-17.42 і 18.1-18.74; Ausubel (2003), вище, розділи 16, 17 і 18. Фахівцям в даній галузі техніки відомі численні експресійні системи, доступні для експресії нуклеїнової кислоти, що кодує білок даного винаходу. Ілюстративними культурами клітин, придатними для продукції міметотіл, їх конкретних частин або варіантів, є клітини ссавців. Системи клітин ссавців часто повинні бути у вигляді моношарів клітин, хоча можуть використовуватися також суспензії клітин ссавців або біореактори. У даній галузі техніки розроблений ряд відповідних ліній клітин, здатних експресувати інтактні глікозильовані білки, і вони включають лінії клітин COS-1 (наприклад, ATCC CRL 1650), COS-7 (наприклад, ATCC CRL-1651), HEK, HEK293, BHK21 (наприклад, ATCC CRL-10), CHO (наприклад, ATCC CRL 1610, DG-44) і BSC-1 (наприклад, ATCC CRL-26), клітини hepG2, клітини P3X63Ag8.653, SP2/0-Ag14, 293, клітин HeLa і тому подібне, які легко доступні від, наприклад, американської колекції типових культур, Manassas, Va. Переважні клітинихазяїни включають клітини лімфоїдного походження, такі як клітини мієломи і лімфоми. Особливо переважними клітинами-хазяїнами є клітини P3X63Ag8.653 (номер надходження ATCC CRL-1580) і клітини SP2/0-Ag14 cells (номер надходження ATCC CRL-1851). Експресійні вектори для цих клітин можуть включати одну або більше з наступних послідовностей, контролюючих експресію, таких як, але, не обмежуючись цим, оріджин реплікації; промотор (наприклад, пізній або ранній промотори SV40, промотор CMV (наприклад, патенти США 5168062; 5385839), промотор HSV tk, промотор pgk (фосфогліцераткінази), промотор EF-1 альфа (наприклад, патент США No. 5266491) щонайменше один промотор імуноглобуліну людини; енхансер і/або сайти, що містять інформацію про процесинг, такі як сайти зв’язування рибосом, сайти сплайсингу РНК, сайти поліаденілування (наприклад, додатковий сайт полі А великого Т Ag SV40) і послідовності термінації транскрипції. Дивись, наприклад, Ausubel et al., вище; Sambrook, et al., вище. Відомі і/або доступні інші клітини, придатні для продукції нуклеїнових кислот або білків даного винаходу, наприклад, з каталогу ліній клітин і гібридом американської колекції типових культур (www.atcc.org) або інших відомих або комерційних джерел. Коли використовують клітини-хазяїни еукаріот, послідовності поліаденілування або термінації транскрипції зазвичай включають у вектор. Прикладом послідовності термінації транскрипції є послідовність поліаденілування від гена гормону росту бика. Можуть бути також включені послідовності для правильного сплайсингу транскрипту. Прикладом послідовності сплайсингу є інтрон VP1 з SV40 (Sprague, et al., J. Virol. 45:773-781 (1983)). Додатково у вектор можуть бути включені послідовності генів для контролю реплікації в клітині-хазяїні, як відомо в даній галузі техніки. Очищення міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або його конкретної частини або варіанту Міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретна частина, або варіант можуть бути виділені і очищені з рекомбінантних клітинних культур добре відомими методами, включаючи, але не обмежуючись цим, очищення за допомогою протеїну А, осадження сульфатом амонію або етанолом, екстракцію кислотою, аніоно- або катіонообмінну хроматографію, хроматографію на фосфоцелюлозі, хроматографію на основі гідрофобної взаємодії, афінну хроматографію, хроматографію на гідроксилапатиті і хроматографію на лектинах. Високоефективна рідинна хроматографія («ВЕРХ») також може бути використана для очищення. Дивись, наприклад, Colligan, Current Protocols in Immunology, or Current Protocols in Protein Science, John Wiley & Sons, NY, NY, (1997-2006), наприклад, розділи 1, 4, 6, 8, 9, 10, кожна з яких наведена в даному описі в повному обсязі як посилання. Міметотіла, або конкретні частини, або варіанти даного винаходу включають природні очищені продукти, продукти процедур хімічного синтезу і продукти, продуковані рекомбінантними способами від еукаріотного хазяїна, включаючи, наприклад, клітини дріжджів, вищих рослин, комах і ссавців. Залежно від хазяїна, що використовується в методі рекомбінантної продукції, міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретна частина, або варіант даного винаходу можуть бути глікозильованими або можуть бути неглікозильованими, причому глікозильовані переважніше. Такі методи описані в багатьох стандартному лабораторному керівництві, такому як Sambrook, вище, розділи 17.37-17.42; Ausubel, вище, розділи 10, 12, 13, 16, 18 і 20, Colligan, Protein Science, вище, розділи 12-14, всі наведені в даному описі в повному обсязі як посилання. 14 UA 98472 C2 5 10 15 20 25 30 35 40 Міметотіла, конкретні фрагменти і/або варіанти Виділені міметотіла даного винаходу включають міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретну частину, або варіант, що кодуються будьякими полінуклеотидами даного винаходу, як більш детально обговорювалося в даному описі, або будь-яке виділене або одержане міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або його конкретна частина, або варіант. Переважно, міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або лігандзв’язувальна частина, або варіант, зв'язує щонайменше один білковий ліганд EPO або рецептор і тим самим забезпечує щонайменше одну біологічну активність EPO відповідного білка або його фрагмента. Різні терапевтично або діагностічно важливі білки добре відомі в даній галузі техніки, і придатні методи або біологічна активність таких білків також добре відомі в даній галузі техніки. Необмежувальні приклади придатних пептидів-міметиків EPO для цього винаходу представлені в таблиці 1 нижче. Ці пептиди можуть бути одержані за допомогою методів, розкритих і/або відомих в даній галузі техніки. У більшості випадків використовуються однолітерні абревіатури амінокислот. X в цих послідовностях (і у всьому цьому описі, якщо не вказано інакше в конкретному прикладі) означає, що може бути присутнім будь-який з 20 природних або відомих амінокислотних залишків або їх відомих похідних, або відповідна ним будь-яка відома модифікована амінокислота. Будь-який з цих пептидів може бути з’єднаний в тандем (тобто послідовно) з або без лінкера, і декілька прикладів тандемного зв'язку представлено в таблиці. Лінкери перераховуються як «∆» і можуть являти собою будь-який з лінкерів, описаних в цьому документі. Тандемні повтори і лінкери показані окремо за допомогою тире для ясності. Будь-який пептид, що містить цистеїніловий залишок, необов'язково може бути поперечно зшитий з іншим Cys-вмісним пептидом, або один, або обидва з яких можуть бути зв’язані з носієм. Деякі приклади поперечних зшитих пептидів представлені в таблиці. Будь-який пептид, що має більше одного Cys залишку, може з успіхом утворювати внутрішньопептидний дисульфідний зв'язок; дивись, наприклад, пептиди-міметики EPO в таблиці 1. Декілка прикладів пептидів, з внутрішньопептидними дисульфідними зв'язками, описано в таблиці. Будь-який з цих пептидів може бути дериватізований, як описаний в цьому документі, і деякі приклади похідних представлені в таблиці. Для похідних, в яких карбоксильний кінець може бути кепований аміногрупою, кепуюча аміногрупа представлена як – NH2. Для похідних, в яких залишки амінокислот замінені частинами, відмінними від амінокислотних залишків, заміни позначаються як δ, що означає будь-яку з частин, відомих в даній галузі техніки, наприклад, як описано в статтях Bhatnagar et al. (1996), J. Med. Chem. 39: 3814-9 і Cuthbertson et al. (1997), J. Med. 5 Chem. 40:2876-82, які включені в повному обсязі як посилання. Замісник J і замісники Z (Z5, Z6, … Z40) являють собою визначене в патентах США Nos. 5608035, 5786331 і 5880096, які включені в даний опис в повному обсязі як посилання. Для послідовностей міметиків EPO (таблиця 1) замісники з X2 до X11 і ціле число «n» являють собою визначене в патенті WO 96/40772, який включений в повному обсязі як посилання. Залишки, виділені напівжирним шрифтом, являють собою D-амінокислоти, але можуть бути необов'язково L-амінокислотами. Всі пептиди зв'язані через пептидні зв'язки, якщо не вказано інакше. Абревіатури перераховані в кінці цього опису. У колонці «SEQ ID NO» «NR» означає, що не потрібно переліку послідовності для даної послідовності. 15 UA 98472 C2 16 UA 98472 C2 5 10 15 20 25 30 35 Біологічна активність EPO добре відома в даній галузі техніки. Дивись, наприклад, Anagnostou А et al. Erythropoietin has а mitogenic and positive chemotactic effect on endothelial cells. Proceedings of the National Academy of Science (USA) 87: 5978-82 (1990); Fandrey J and Jelkman WE Interleukin 1 and tumor necrosis factor-alpha inhibit erythropoietin production in vitro. Annals of the New York Academy of Science 628: 250-5 (1991); Geissler K et al. Recombinant human erythropoietin: А multipotential hemopoietic growth factor in vivo and in vitro. Contrib. Nephrol. 87: 110 (1990); Gregory CJ Erythropoietin sensitivity as а differentiation marker in the hemopoietic system. Studies of three erythropoietic colony responses in culture. Journal of Cellular Physiology 89: 289-301 (1976); Jelkman W et al. Monokines inhibiting erythropoietin production in human hepatoma cultures and in isolated perfused rat kidneys. Life Sci. 50: 301-8 (1992); Kimata Н et al. Human recombinant erythropoietin directly stimulates В cell immunoglobulin production and proliferation in serum-free medium. Clinical and Experimental Immunology 85: 151-6 (1991); Kimata Н et al. Erythropoietin enhances immunoglobulin production and proliferation by human plasma cells in а serum-free medium. Clin. Immunology Immunopathol. 59: 495- 501 (1991); Kimata Н et al. Effect of recombinant human erythropoietin on human IgE production in vitro Clinical and Experimental Immunology 83: 483-7 (1991); Koury MJ and Bondurant MC Erythropoietin retards DNA breakdown and prevents programmed cell death in erythroid progenitor cells. Science 248: 378-81 (1990); Lim VS et al. Effect of recombinant human erythropoietin on renal function in humans. Kidney International 37: 131-6 (1990); Mitjavila MT et al Autocrine stimulation by erythropoietin and autonomous growth of human erythroid leukemic cells in vitro. Journal of Clinical Investigation 88: 789-97 (1991); Andre M et al. Performance of an immunoradiometric assay of erythropoietin and results for specimens from anemic and polycythemic patients. Clinical Chemistry 38: 758-63 (1992); Hankins WD et al. Erythropoietindependent and erythropoietin-producing cell lines. Implications for research and for leukemia therapy. Annals of the New York Academy of Science 554: 21-8 (1989); Kendall RGT et al. Storage and preparation of samples for erythropoietin radioimmunoassay. Clin.Lab. Haematology 13: 189-96 (1991); Krumvieh D et al. Comparison of relevant biological assays for the determination of biological active erythropoietin. Dev. Biol. Stand. 69: 15-22 (1988); Ma DD et al Assessment of an EIA for measuring human serum erythropoietin as compared with RIA and an in-vitro bioassay. British Journal of Haematology 80: 431-6 (1992); Noe G et al. А sensitive sandwich ELISA for measuring erythropoietin in human serum British Journal of Haematology 80: 285-92 (1992); Pauly JU et al. Highly specific and highly sensitive enzyme immunoassays for antibodies to human interleukin 3 (IL3) and human erythropoietin (EPO) in serum. Behring Institut Mitteilungen 90: 112-25 (1991); Sakata S and Enoki Y Improved microbioassay for plasma erythropoietin based on CFU-E colony formation. 17 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 Ann. Hematology 64: 224-30 (1992); Sanengen Т et al. Immunoreactive erythropoietin and erythropoiesis stimulating factor(s) in plasma from hypertransfused neonatal and adult mice. Studies with а radioimmunoassay and а cell culture assay for erythropoietin. Acta Physiol. Scand. 135: 11-6 (1989); Widness JA et al. А sensitive and specific erythropoietin immunoprecipitation assay: application to pharmacokinetic studies. Journal of Lab. Clin. Med. 119: 285-94 (1992); для додаткової інформації дивись також індивідуальні клітинні лінії, що використовуються в індивідуальних біотестах. Кожне з представлених вище посилань наведена в даному описі в повному обсязі як посилання. EPO можна протестувати, використовуючи такі клітинні лінії, як HCD57, NFS-60, TF-1 і UT-7, які відповідають на фактор. Активність EPO може бути оцінена також в тесті утворення колоній шляхом визначення кількості CFU-E з клітин кісткового мозку. Альтернативним і повністю відмінним методом визначення є кількісне визначення цитокінів за допомогою ЗТ-ПЛР. Міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або його конкретна частина або варіант, яка частково або переважно по суті виявляють щонайменше одну біологічну активність щонайменше одного білка або фрагмента, можуть зв'язувати білковий ліганд або фрагмент і тим самим забезпечувати щонайменше одну активність, яка іншим чином опосередковується шляхом зв’язування білка з щонайменше одним білковим лігандом або рецептором, або через інший залежний від білків або опосередкований ними механізм. Термін «активність міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO», що застосовується в даному описі, належить до міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, які можуть модулювати або викликати щонайменше одну залежну від білка активність на приблизно 20-10000%, на щонайменше приблизно 60, 70, 80, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 250, 300, 350, 400, 450, 500, 550, 600, 700, 800, 900, 1000, 2000, 3000, 4000, 5000, 6000, 7000, 8000, 9000% або більше залежно від методу. Здатність міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або його конкретної частини або варіанту забезпечувати щонайменше одну залежну від білка активність переважно оцінюється за допомогою щонайменше одного відповідного білкового біологічного методу, як описано в цьому документі і/або відомо в даній галузі техніки. Міметотіло людини, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретна частина або варіант винаходу можуть схоже належати до будь-якого класу (IgG, IgA, IgM і т.д.) або ізотипу і можуть включати щонайменше частину легкого ланцюга каппа або лямбда. В одному варіанті здійснення міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретна частина або варіант включають варіабельний фрагмент важкого ланцюга IgG, шарнірну область, CH 2 і CH3, наприклад щонайменше один з ізотипів IgG1, IgG2, IgG3 або IgG4. Щонайменше одне міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретна частини або варіант винаходу зв'язує щонайменше один конкретний ліганд, специфічний у відношенні щонайменше одного білка, субодиниці, фрагмента, частини або будьякого їх поєднання. Щонайменше один пептидний міметик EPO щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або конкретної частини або варіанту даного винаходу може необов'язково зв'язуватися з щонайменше одним конкретним лігандним епітопом ліганду. Зв'язуючий епітоп може включати будь-яке поєднання щонайменше однієї амінокислотної послідовності з від щонайменше 1-3 амінокислот до повної конкретної частини прилеглих амінокислот послідовностей, вибраних з групи, що складається з білкового ліганду, такого як рецептор EPO або його частина. Такі міметотіла можуть бути одержані за допомогою з'єднання разом різних частин формули (I) міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, з використанням відомих методів, за допомогою одержання і експресії щонайменше однієї (тобто однієї або більше) молекул нуклеїнової кислоти, які кодують міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, з використанням відомих методів технології рекомбінантних ДНК або за допомогою використання будь-якого іншого придатного методу, такого як хімічний синтез. Міметотіла, які зв'язуються з лігандами або рецепторами EPO людини і які включають щонайменше одну частину, що визначає варіабельну область важкого або легкого ланцюга, можуть бути одержані з використанням придатних методів, таких як фаговий дисплей (Katsube, Y., et al., Int J Mol. Med, l(5):863-868 (1998)) або методів, в яких використовуються трансгенні тварини, як відомо в даній галузі техніки і/або описано в цьому документі. Міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, конкретна частина або варіант можуть 18 UA 98472 C2 5 10 15 20 експресуватися з використанням кодуючої нуклеїнової кислоти або її частини у придатній клітині-хазяїні. Переважно такі міметотіла або їх лігандзв’язувальні фрагменти можуть зв'язувати ліганди або рецептори EPO людини з високою спорідненістю (наприклад, з KD менш або рівної -7 приблизно 10 М). Амінокислотні послідовності, які є по суті тими ж, що і послідовності, описані в цьому документі, включають послідовності, що включають консервативні заміни амінокислот, а також делеції і/або вставки амінокислот. Консервативна заміну амінокислот належить до заміни першої амінокислоти другою амінокислотою, яка має хімічні і/або фізичні властивості (наприклад, заряд, структуру, полярність, гідрофобність/гідрофільність), які схожі з першою амінокислотою. Консервативні заміни включають заміну однієї амінокислоти іншою амінокислотою в межах наступних груп: лізин (K), аргінін (R) і гістидин (Н); аспартат (D) і глутамат (Е); аспарагін (N), глутамін (Q), серин (S), треонін (Т), тирозин (Y), K, R, Н, D і Е; аланін (А), валін (V), лейцин (L), ізолейцин (I), пролін (Р), фенілаланін (F), триптофан (W), метіонін (M), цистеїн (С) і гліцин (G); F, W і Y; С, S і Т. Коди амінокислот Амінокислоти, які входять в склад міметотіл, або конкретних частин, або варіантів даного винаходу, часто представлені абревіатурами. Назви амінокислот можуть бути вказані у вигляді позначення амінокислоти за допомогою її однолітерного коду, її трилітерного коду, назви або тринуклеотидного кодону(нів), як це добре відоме в даній галузі техніки (дивись Alberts, В., et al., Molecular Biology of The Cell, Third Ed., Garland Publishing, Inc., New York, 1994), як представлено в таблиці. Таблиця 2 Однолітерний код А С D Е 30 Glu F G Н I К L M N Р Q R S Т V w Y 25 Трилітерний код Ala Cys Asp Phe Gly His He Lys Leu Met Asn Pro Gln Arg Ser Thr Val Trp Tyr Назва Аланін Цистеїн Аспарагінова кислота Глютамінова кислота Фенілаланін Гліцин Гістідін Ізолейцин Лізін Лейцин Метіонін Аспарагін Пролін Глутамін Аргінін Серин Треонін Валін Триптофан Тирозин Тринуклеотидний(ні) кодон(и) GCA, GCC, GCG, GCU UGC, UGU GAC, GAU GAA, GAG UUC, UUU GGA, GGC, GGG, GGU CAC, CAU AUA, AUC, AUU AAA, AAG UUA, UUG, CUA, CUC, CUG, CUU AUG AAC, AAU CCA, CCC, CCG, CCU CAA, CAG AGA, AGO, CGA, CGC, CGG, CGU AGC, AGU, UCA, UCC, UCG, UCU АСА, ACC, ACG, ACU QUA, GUC, GUG, GUU UGG UAC, UAU Міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретна частина або варіант даного винаходу може включати одну або більше амінокислотних замін, делецій або добавок, в результаті або природних мутацій, або маніпуляцій людини, як описано в цьому документі. Такі або інші послідовності, які можуть бути використані в даному винаході, включають, але не обмежуються цим, наступні послідовності, представлені в таблиці 3, як далі описано в фігурах 1-42 попередньої заявки США 60/507349, зареєстрованої 30.09.2003 р, наведеної в даному описі в повному обсязі як посилання, відповідні фігурам 1-41 заявки PCT No. US04/19783, зареєстрованої 17 червня, 2004 р, наведеної в даному описі в повному обсязі як посилання, згідно з SEQ ID NOS:31-72. Ці посилання на фігури 1-42 (SEQ ID NOS:31-72) або фігури 1-41 PCT US04/19783, є прикладами послідовностей варіабельних/константних областей важких/легких ланцюгів, 19 UA 98472 C2 каркасів/субдоменів і замін, частини яких можуть бути використані в білках, що є похідними Ig даного винаходу, як вказується в даному описі. SEQ ID NO 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 AA NO Варіабельна область важкого ланцюга Vhl Vh2 Vh3a Vh3b Vh3c Vh4 Vh5 Vh6 Vh7 Варіабельна l-4 область 2 легкого З ланцюга 5 новий1 новий2 новий3 1а 1b 2 3а 3b 3с 3е 4а 4Ь 5 6 7 8 9 10 125 124 100 102 101 108 132 125 91 93 92 91 85 79 77 95 98 99 99 107 93 98 98 94 95 88 101 89 89 91 87 Області FR1 CDR1 FR2 CDR2 FR3 1-31 32 33-46 47 48-79 1-30 31 32-45 46 47-78 1-31 32 33-46 47 48-79 1-30 31 32-45 46 47-78 1-30 31 32-45 46 47-79 1-33 34 35-48 49 50-81 1-31 32 33-46 47 48-79 1-30 31 32-45 46 47-78 1-30 31 32-45 46 47-78 1-24 25 26-40 41 42-73 1-23 24 25-39 40 41-72 1-23 24 25-39 40 41-72 1-23 24 25-39 40 41-72 1-17 18 19-33 34 35-66 1-15 16 17-31 32 33-64 1-24 25 26-40 41 42-73 1-22 23 24-38 39 40-71 1-23 24 25-39 40 41-72 1-22 23 24-38 39 40-71 1-22 23 24-38 39 40-71 1-22 23 24-39 40 41-72 1-22 23 24-38 39 40-71 1-22 23 24-38 39 40-71 1-22 23 24-38 39 40-71 1-22 23 24-38 39 40-71 1-22 23 24-39 40 41-74 1-22 23 24-38 39 40-73 1-22 23 24-38 39 40-71 1-22 23 24-38 39 40-71 1-22 23 24-38 39 40-79 1-22 23 24-38 39 40-71 CDR3 80 79 80 79 80 82 80 79 79 74 73 73 73 67 65 7472 73 72 72 73 72 72 72 72 75 74 72 72 80 72 AA NO Області CH1 Шарнір 1 Шарнір 2 Шарнір 3 Шарнір 4 lgA1 354 1-102 103-121 lgА2 340 1-102 103-108 64 lgD 384 1-101 102-135 136-159 65 lgE 497 1-103 66 lgG1 339 1-98 99-113 67 lgG2 326 1-98 99-110 68 lgG3 377 1-98 99-115 69 lgG4 327 1-98 99-110 SEQ ID NO 62 63 Константна область важкого ланцюга 20 116-130 131-145 146-160 FR4 81-125 80-124 81-100 80-102 81-101 83-108 81-132 80-125 80-91 75-93 74-92 74-91 74-85 68-79 66-77 75-95 73-98 74-99 73-99 73-107 74-93 73-98 73-98 73-94 73-95 76-88 75-101 73-89 73-89 81-91 73-87 CH2 CH3 122222 109209 160267 104210 114223 111219 161270 111220 223354 210340 268384 211318 224339 220326 271377 221327 UA 98472 C2 70 71 72 5 10 15 20 25 30 35 40 45 50 lgM Константна область легкого ланцюга 476 lgс lgc 1-104 105217 218323 107 107 Зазвичай, фахівець в даній галузі техніки повинен оцінювати кількість амінокислотних замін залежно від багатьох факторів, включаючи описані вище. Взагалі кажучи, кількість амінокислотних замін, вставок або делецій для щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO повинна бути не більше 40, 30, 20, 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2, 1 амінокислот, наприклад, 1-30 або будьякий діапазон величин всередині нього, як описано в цьому документі. Подальший опис компонентів міметотіла, що імітує шарнірну основу EPO даного винаходу, заснований на використанні формули I даного винаходу ((V(m)-Р(n)-L(про)-Н(р)-CH2(q)-CH3(r))(s), де V являє собою щонайменше одну частину N-кінця варіабельної області імуноглобуліну, Р являє собою щонайменше один біологічно активний пептид, L являє собою щонайменше один лінкерний пептид, Н являє собою щонайменше одну частину щонайменше однієї шарнірної області імуноглобуліну, CH2 являє собою щонайменше частину константної області CH 2 імуноглобуліну, CH3 являє собою щонайменше частину константної області CH3 імуноглобуліну, m, n, о, р, q, r і s незалежно являють собою ціле число між 0, 1 або 2 і 10, імітуючи різні типи молекул імуноглобулінів, наприклад, але не обмежуючись цим, IgG1, IgG2, IgG3, IgG4, IgA, IgM, IgD, IgE і тому подібне, або їх підклас, або будь-яке їх поєднання. У міметотілах шарнірної основи даного винаходу необов'язкова N-кінцева частина V може включати 1-20 амінокислот щонайменше одного каркаса 1 варіабельної області важкого ланцюга (FR1), наприклад, як представлено на фігурах 1-9 (SEQ ID NOS:31-39), або щонайменше одну варіабельну область LC, наприклад, як представлено на фігурах 10-31 (SEQ ID NOS:40-61) попередньої заявки США 60/507349, зареєстрованої 30.09.2003 р, наведеної в даному описі в повному обсязі як посилання, що відповідає фігурам 1-41 заявки PCT No. US04/19783, зареєстрованої 17 червня 2004 р, наведеної в даному описі в повному обсязі як посилання, включаючи заміни, делеції або вставки, як представлено на цих фігурах, причому з тим, що фігури 5, 6 і 8 є переважними. Переважними також є варіабельні послідовності, які включають послідовність Q-X-Q. Частина Р може включати щонайменше один терапевтичний пептид, як відомо в даній галузі техніки або як описано в цьому документі, такий як, але не обмежуючись представленими в таблиці 1, SEQ ID NOS: 1-30, або як відомо в даній галузі техніки, або будь-яке їх поєднання, або їх консенсусну послідовність, або будь-який їх злитий білок. Необов'язкова лінкерна послідовність може являти собою будь-який придатний пептидний лінкер, як відомо в даній галузі техніки. Переважна послідовність включає будь-яке поєднання G і S, наприклад, Xl-X2-X3-X4-Xn, де X може являти собою G або S, і n може дорівнювати 5-30. Необмежувальні приклади включають GS, GGGS, GSGGGS, GSGGGSGG, і тому подібне. У даному винаході частина CH1 не використовується, і різна кількість амінокислот видалена з N-кінця шарнірної області, наприклад, як при посиланні на фігури 1-42 попередньої заявки США 60/507349, зареєстрованої 30.09.2003 р, наведеної в даному описі в повному обсязі як посилання, що відповідають фігурам 1-41 заявки PCT No. US04/19783, зареєстрованої 17 червня 2004 р, наведеної в даному описі в повному обсязі як посилання, і в таблиці 3. Різна кількість амінокислот, що використовується для частини шарнірної основи міметотіла даного винаходу, включає, але не обмежується цим, делецію будь-якої з 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57 або 1-3, 2-5, 2-7, 2-8, 3-9, 410, 5-9, 5-10, 5-15, 10-20, 2-30, 20-40, 10-50, або будь-якого діапазону або величини в цих межах N-кінцевих амінокислот щонайменше однієї шарнірної області, наприклад, як представлено на фігурах 32-40 попередньої заявки США 60/507349, зареєстрованої 30.09.2003 р, наведеної в даному описі в повному обсязі як посилання, що відповідають фігурам 1-41 заявки PCT No. US04/19783, зареєстрованої 17 червня 2004 р, наведеної в даному описі в повному обсязі як посилання, або в таблиці 3 вище, наприклад, але не обмежуючись цим, делецію від будь-який до всіх амінокислот від 99-101 до 105-157, амінокислот 99-105, 99-108, 99-111, 99-112, 99-113, 99-114, 99-115, 99-119, 99-125, 99-128, 99-134, 99-140, 99-143, 99-149, 99-155 і 99-158 фігур 3240 попередньої заявки США 60/507349, зареєстрованої 30.09.2003 р, наведеної в даному описі 21 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 60 в повному обсязі як посилання, що відповідають фігурам 1-41 заявки PCT No. US04/19783, зареєстрованої 17 червня 2004 р, наведеної в даному описі в повному обсязі як посилання, що відповідають SEQ ID NOS:62-70, включаючи заміни, вставки або делеції, описані на фігурах 3240 попередньої заявки США 60/507349, зареєстрованої 30.09.2003 р, наведеної в даному описі в повному обсязі як посилання, що відповідають фігурам 1-41 заявки PCT No. US04/19783, зареєстрованої 17 червня 2004 р, наведеної в даному описі в повному обсязі як посилання. У переважних варіантах здійснення області шарнірної основи даного винаходу включають делецію N-кінця шарнірної області для забезпечення області шарнірної основи, яка включає делецію до, але не включаючи, залишок Cys, або до, але не включаючи послідовність Cys-ProXaa-Cys. У додатковому переважному варіанті здійснення такі послідовності шарнірної основи, що використовуються в міметотілі шарнірної основи даного винаходу, включають амінокислоти 109-113 або 112-113 (SEQ ID NO:66) (IgG1); 105-110 або 109-110 (SEQ ID NO:67) (IgG2); 111160, 114-160, 120-160, 126-160, 129-160, 135-160, 141-160, 144-160, 150-160, 156-160 і 159-160 (SEQ ID NO:68) (IgG3); або 106-110 або 109-110 (SEQ ID NO:69) (IgG4). Послідовність CH2, CH3 і необов'язково CH4 може являти собою будь-яку придатну послідовність людини або сумісну з людиною, наприклад, як представлено на фігурах 1-42 попередньої заявки США 60/507349, зареєстрованої 30.09.2003 р, наведеної в даному описі в повному обсязі як посилання, що відповідають фігурам 1-41 заявки PCT No. US04/19783, зареєстрованої 17 червня 2004 р, наведеної в даному описі в повному обсязі як посилання в таблиці 3, або як відомо в даній галузі техніки, або їх будь-яке поєднання, або консенсусну послідовність, або будь-який їх злитий білок. Амінокислоти в міметотілі, що імітує шарнірну основу EPO, або в іншому агоністі рецептора EPO, або в конкретній частині, або у варіанті даного винаходу, які суттєві для функції, можуть бути ідентифіковані методами, відомими в даній галузі техніки, такими як сайт-направлений мутагенез або скануючий мутагенез аланіну (наприклад, Ausubel, вище, розділи 8, 15; Cunningham and Wells, Science 244:1081-1085 (1989)). В останньому методі вводяться одиничні мутації аланіну в кожний залишок молекули. Одержані мутантні молекули потім тестуються на біологічну активність, таку як, але, не обмежуючись цим щонайменше одна зв'язана з білком активність, як описано в цьому документі, або відомо в даній галузі техніки. Сайти, які є критичними для зв’язування міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або конкретної частини, або варіанту даного винаходу, можуть бути ідентифіковані за допомогою структурного аналізу, такого як кристалізація, ядерний магнітний резонанс або фотоафінна мітка (Smith, et al., J. Mol. Biol. 224:899-904 (1992) і de Vos, et al., Science 255:306-312 (1992)). Міметотіла або конкретні частини, або варіанти даного винаходу можуть включати як частину Р формули (I), але не обмежуючись цим щонайменше одну частину, послідовність або поєднання, вибрану з від 3 до всіх щонайменше однієї SEQ ID NOS:1-30. Необмежувальні варіанти, які можуть збільшувати або підтримувати щонайменше одну з перерахованої активності вказаної вище, включають, але не обмежуються цим, будь-який з вказаних вище поліпептидів, що додатково включають щонайменше одну мутацію, що відповідає щонайменше одній заміні, вставці або делеції, яка суттєво не впливає на відповідну біологічну активність або функції вказаного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO. Міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретна частина, або варіант можуть додатково необов'язково включати щонайменше одну функціональну частину щонайменше одному поліпептиду як частину Р формули (I) щонайменше однієї з 90-100% SEQ ID NOS:1-30. Міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO можуть додатково необов'язково включати амінокислотну послідовність частини Р формули (I), вибрану з однієї або більше SEQ ID NOS:1-30. В одному варіанті здійснення амінокислотна послідовність Р або її частина мають приблизно 90-100% ідентичність (тобто 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100 або будь-який діапазон або величину в цих межах) відповідної амінокислотної послідовності відповідної частини щонайменше однієї з SEQ ID NOS:1-30. Переважно 90-100% ідентичність амінокислот (тобто 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100 або будь-який діапазон або величина в цих межах) визначається при використанні відповідного комп'ютерного алгоритму, як відомо в даній галузі техніки. Міметотіла або конкретні частини, або варіанти даного винаходу можуть включати будь-яку кількість сусідніх амінокислотних залишків з міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або конкретної частини, або варіанту даного винаходу, де ця кількість вибрана з групи цілих чисел, що перебувають від 10-100% кількості сусідніх залишків в 22 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 60 міметотілі, що імітує шарнірну основу EPO, або іншому агоністі рецептора EPO. Необов'язково ця послідовність сусідніх амінокислот становить щонайменше приблизно 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 40, 50, 60, 70, 80, 90, 100, 110, 120, 130, 140, 150, 160, 170, 180, 190, 200, 210, 220, 230, 240, 250 або більше амінокислоти в довжину або будь-який діапазон або величину в цих межах. Далі, кількість таких послідовностей може являти собою будь-яке ціле число, вибране з групи, що складається з від 1 до 20, таке як щонайменше 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 або більш. Як повинно бути зрозуміло фахівцеві в даній галузі техніки, даний винахід включає щонайменше одне біологічно активне міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або конкретну частину, або варіант даного винаходу. Біологічно активні міметотіла, або конкретні частини, або варіанти мають специфічну активність щонайменше 20%, 30% або 40% і переважно щонайменше 50%, 60% або 70% і найбільш переважно щонайменше 80%, 90% або 95%-1000% від природного (несинтетичного), ендогенного або спорідненого і з відомими вставками або злитого білка, або конкретної частини або варіанту. Методи визначення і кількісного вимірювання ферментативної активності і субстратної специфічності добре відомі фахівцям в даній галузі техніки. В іншому аспекті винахід стосується міметотіл і лігандів’язувальних фрагментів людини, як описано в цьому документі, які модифіковані шляхом ковалентного приєднання органічної частини. Така модифікація може давати міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або лігандзв’язувальний фрагмент з поліпшеними фармакокінетичними властивостями (наприклад, підвищеним періодом напівжиття в сироватці in vivo). Органічна частина може бути лінійною або розгалуженою гідрофільною полімерною групою, групою жирної кислоти або групою складного ефіру жирної кислоти. У конкретних варіантах здійснення гідрофільна полімерна група може мати молекулярну масу від приблизно 800 до приблизно 120000 дальтон і може являти собою поліалкангліколь (наприклад, поліетиленгліколь (ПЕГ), поліпропіленгліколь (PPG)), полімер вуглеводів, полімер амінокислот або полівінілпіролідон, і група жирної кислоти або складного ефіру жирної кислоти може включати від приблизно восьми до приблизно сорока атомів вуглеводу. Модифіковані міметотіла і лігандзв’язувальні фрагменти винаходу можуть включати одну або більше органічних частин, які ковалентно зв'язані, прямо або опосередковано з міметотілом, що імітує шарнірну основу EPO, або з іншим агоністом рецептора EPO, або з конкретною частиною або варіантом. Кожна органічна частина, яка зв'язується з міметотілом, що імітує шарнірну основу EPO, або з іншим агоністом рецептора EPO, або з лігандзв’язувальним фрагментом винаходу, може незалежно являти собою гідрофільну полімерну групу, групу жирної кислоти або групу складного ефіру жирної кислоти. Термін « жирна кислота», що використовується в даному описі, охоплює монокарбонові кислоти і дикарбонові кислоти. «Гідрофільна полімерна група», як термін, що використовується в даному описі належить до органічного полімеру, який більш розчинний у воді, ніж октан. Наприклад, полілізин більш розчинний у воді, ніж октан. Таким чином, міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, модифікований ковалентним приєднанням полілізину, охоплюються винаходом. Гідрофільні полімери, придатні для модифікації міметотіл винаходу, можуть бути лінійними або розгалуженими і включають, наприклад, поліалкангліколі (наприклад, ПЕГ, монометоксиполіетиленгліколь (мПЕГ), PPG і тому подібне), вуглеводи (наприклад, декстран, целюлоза, олігосахариди, полісахариди і тому подібне), полімери гідрофільних амінокислот (наприклад, полілізин, поліаргінін, поліаспартат і тому подібне), поліалканоксиди (наприклад, поліетиленоксид, поліпропіленоксид і тому подібне) і полівінілпіролідон. Переважно гідрофільний полімер, який модифікує міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO винаходу має молекулярну масу від приблизно 800 до приблизно 150000 дальтон у вигляді окремої молекулярної одиниці. Наприклад, може бути використаний ПЕГ2500, ПЕГ5000, ПЕГ7500, ПЕГ9000, ПЕГ10000, ПЕГ12500, ПЕГ15000 і ПЕГ20000, де підрядковий індекс являє собою середню молекулярну масу полімеру в дальтонах. Гідрофільна полімерна група може бути заміщена від однієї до приблизно шести групами алкілів, жирної кислоти або складного ефіру жирної кислоти. Гідрофільні полімери, які заміщені групою жирної кислоти або складного ефіру жирної кислоти, можуть бути одержані шляхом використання відповідних методів. Наприклад, полімер, що включає аміногрупу, може бути з’єднаний з карбоксилатом жирної кислоти або складного ефіру жирної кислоти, і активований карбоксилат (наприклад, активований N,N-карбонілдіімідазолом) жирної кислоти або складного ефіру жирної кислоти може бути з’єднаний з гідроксильною групою полімеру. 23 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 60 Жирні кислоти і складні ефіри жирних кислот, придатні для модифікації міметотіл винаходу, можуть бути насиченими або можуть містити одну або більше ненасичених одиниць. Жирні кислоти, які підходять для модифікації міметотіл винаходу, включають, наприклад, ндодеканоат (C12, лаурат), н-тетрадеканоат (C14, міристат), н-октадеканоат (C18, стеарат), нейкозаноат (C20, арахідат), н-докозаноат (C22, бегенат), н-триаконтаноат (C30), н-тетраконтаноат (C40), цис-∆9-октадеканоат (C18, олеат), всі цис-∆5,8,11,14-ейкозатетраеноат (C20, арахідонат), октандикарбонову кислоту, тетрадекандикарбонову кислоту, октадекандикарбонову кислоту, докозандикарбонову кислоту і тому подібне. Відповідний складний ефір жирних кислот включає моноефіри дикарбонових кислот, які включають лінійну або розгалужену нижчу алкільну групу. Нижча алкільна група може включати від одного до приблизно дванадцяти, переважно від одного до шести вуглецевих атомів. Модифіковані міметотіла людини і лігандзв’язувальні фрагменти можуть бути одержані при використанні відповідних способів, таких як взаємодія з одним або більше модифікуючих агентів. «Модифікуючий агент», як термін, що використовується в даному описі, належить до відповідної органічної групи (наприклад, гідрофільного полімеру, жирної кислоти, складного ефіру жирної кислоти), яка включає активуючу групу. «Активуюча група» являє собою хімічну частину або функціональну групу, яка може при відповідних умовах взаємодіяти з другою хімічною групою, утворюючи в результаті цього ковалентний зв'язок між модифікуючим агентом і другою хімічною групою. Наприклад, взаємодіючі з аміном активуючі групи включають електрофільні групи, такі як тозилат, мезилат, галоген (хлор, бром, фтор, йод) Nгідроксисукцинімідильні ефіри (NHS) і тому подібне. Активуючі групи, які можуть взаємодіяти з тіолами, включають, наприклад, малеімід, йодацетил, акрилоліл, піридилдисульфіди, тіол 5тіол-2-нітробензоєвої кислоти (TNB-тіол) і тому подібне. Альдегідна функціональна група може бути з’єднана з молекулами, що містять амін або гідразид, і азидна група може взаємодіяти з тривалентною фосфористою групою з утворенням фосфорамідатних або фосфорімідних зв'язків. Придатні методи введення активуючих груп в молекули відомі в даній галузі техніки (дивись, наприклад, Hermanson, G.T., Bioconjugate Techniques, Academic Press: San Diego, CA (1996)). Активуюча група може бути з’єднана з органічною групою (наприклад, гідрофільним полімером, жирною кислотою, складним ефіром жирної кислоти) безопосередковано або через лінкерну частину, наприклад, двовалентну групу C 1-C12, де один або більше вуглецевих атомів можуть бути заміщені гетероатомом, таким як кисень, азот або сірка. Придатні лінкерні частини включають, наприклад, тетраетиленгліколь -(CH2)3-, -NH-(CH2)6- NH-, -(CH2)2- NH- і CH2-O-CH2CH2-O-CH-NH-. Модифікуючі агенти, які включають лінкерну частину, можуть бути одержані, наприклад, шляхом взаємодії моно-Вос-алкілдіаміну (наприклад, моно-Вос-етілендіаміну, моноВос-діаміногексану) з жирною кислотою в присутності 1-етил-3-(3-диметиламінопропіл)карбодііміду (EDC) з утворенням амідного зв'язку між вільним аміном і карбоксилатом жирної кислоти. Захисна група Boc може бути видалена з продукту шляхом обробки трифтороцтовою кислотою (ТФО) з експозицією первинного аміну, який може бути приєднаний, з іншим карбоксилатом, як описано, або він може бути введений в реакцію з малеїновим ангідридом, і одержаний продукт конденсований з одержанням активованого малеімідного похідного жирної кислоти. (Дивись, наприклад, Thompson, et al., патент WO 92/16221, вказівки якого включені в даний опис в повному обсязі як посилання). Модифіковані міметотіла винаходуможуть бути одержані шляхом взаємодії міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або лігандзв’язувального фрагмента з модифікуючим агентом. Наприклад, органічні частини можуть бути зв'язані з міметотілом, що імітує шарнірну основу EPO, або іншим агоністом рецептора EPO неспецифічним у відношенні сайта способом за допомогою використання реагуючого з аміном модифікуючого агента, наприклад, складного ефіру NHS або ПЕГ. Модифіковані міметотіла або лігандзв’язувальні фрагменти людини можуть бути також одержані шляхом відновлення дисульфідних зв'язків (наприклад, внутрішньоланцюжкових дисульфідних зв'язків) міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або лігандзв’язувального фрагмента. Відновлене міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або лігандзв’язувальний фрагмент можна потім вводити в реакцію з реагуючим з тіолом модифікуючим агентом з одержанням модифікованого міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO винаходу. Модифіковані міметотіла і лігандзв’язувальні фрагменти людини, що включають органічну частину, яка зв'язана зі специфічними сайтами міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або конкретною частиною, або варіантом даного винаходу, можуть бути одержані з використанням придатних методів, таких як зворотний протеоліз (Fisch et al., Bioconjugate Chem., 3:147-153 (1992); Werlen et al., Bioconjugate Chem., 5:411-417 (1994); 24 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 Kumaran et al., Protein Sci. 6(10):2233-2241 (1997); Itoh et al., Bioorg. Chem., 24(1): 59-68 (1996); Capellas et al., Biotechnol. Bioeng., 56(4):456-463 (1997)), і інші методи, описані в Hermanson, G.T., Bioconjugate Techniques, Academic Press: San Diego, CA (1996). Міметотіло, що імітує шарнірну основу EPO, або інші композиції агоністів рецептора EPO У даному винаході також пропонується щонайменше одне міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO або композиція з окремої частини або варіанту, що включає щонайменше одне, щонайменше два, щонайменше три, щонайменше чотири, щонайменше п'ять, щонайменше шість або більше міметотіл або їх окремих частин або варіантів, як викладено в даному описі і/або відомих в даній галузі техніки, і яке пропонується в неприродній композиції, суміші або формі. Процентний склад таких композицій виражають по масі, об'єму, концентрації, молярності або моляльності для рідких або сухих розчинів, сумішей, суспензій, емульсій або колоїдів, як відомо в даній галузі техніки або як викладено в даному описі. Такі композиції можуть включати 0,00001-99,9999 процентів по масі, об'єму, концентрації, молярності або моляльності для рідких, газоподібних або сухих розчинів, сумішей, суспензій, емульсій або колоїдів, як відомо в даній галузі техніки або як викладено в даному описі, в будьякому діапазоні або відповідно до будь-якої величини даного опису, такої як, але не обмежуючись цим, 0,00001, 0,00003, 0,00005, 0,00009, 0,0001, 0,0003, 0,0005, 0,0009, 0,001, 0,003, 0,005, 0,009, 0,01, 0,02, 0,03, 0,05, 0,09, 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1,0, 1,1, 1,2, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8, 1,9, 2,0, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9, 3,0, 3,1, 3,2, 3,3, 3,4, 3,5, 3,6, 3,7, 3,8, 3,9, 4,0, 4,3, 4,5, 4,6, 4,7, 4,8, 4,9, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 99,1, 99,2, 99,3, 99,4, 99,5, 99,6, 99,7, 99,8, 99,9 %. Такі композиції даного винаходу, таким чином, включають, але не обмежуються цим, 0,00001-100 мг/мл і/або 0,00001100 мг/м. Композиція може необов'язково додатково включати ефективну кількість щонайменше одну сполуку або білок, вибрану з щонайменше одних протиінфекційних ліків, ліків для серцевосудинної (CV) системи, ліків для центральної нервової системи (ЦНС), ліків для автономної нервової системи (АНС), ліків для дихального тракту, ліків для шлунково-кишкового (GI) тракту, гормональних ліків, ліків для балансу рідини або електролітів, гематологічних ліків, протипухлинних ліків, імуномодулюючих ліків, очних, вушних або носових ліків, ліків для місцевого застосування, дієтологічних ліків або тому подібного. Такі ліки добре відомі в даній галузі техніки, включаючи склади, покази, дозування і введення кожного з представлених в даному описі (дивись, наприклад, Nursing 2001 Handbook of Drugs, 21st edition, Springhouse Corp., Springhouse, PA, 2001; Health Professional's Drug Guide 2001, ed., Shannon, Wilson, Stang, Prentice-Hall, Inc, Upper Saddle River, NJ; Pharmcotherapy Handbook, Wells et al., ed., Appleton & Lange, Stamford, CT, кожна з яких включена в даний опис як посилання). Композиції даного винаходу імітуючого шарнірну основу EPO міметотіла або іншого агоніста рецептора EPO або окремої частини або варіанту можуть додатково включати щонайменше один з будь-яких допоміжних агентів, таких як, але не обмежуючись цим, розріджувач, зв'язуючий агент, стабілізатор, буфери, солі, ліпофільні розчинники, консервант, ад’ювант або тому подібне. Переважні фармацевтично прийнятні допоміжні агенти. Їх необмежувальні приклади і методи одержання таких стерильних розчинів добре відомі в даній галузі техніки, такі як, але не обмежуючись цим, Gennaro, Ed., Remington's Pharmaceutical Sciences, 18th Edition, Mack Publishing Co. (Easton, PA) 1990. Фармацевтично прийнятні носії зазвичай можна вибрати так, щоб вони відповідали даному способу введення, розчинності і/або стабільності композиції імітуючого шарнірну основу EPO міметотіла або іншого агоніста рецептора EPO, як добре відомо в даній галузі техніки або як викладено в даному описі. Фармацевтичні наповнювачі і добавки, придатні в даній композиції, включають, але не обмежуються цим, білки, пептиди, амінокислоти, ліпіди і вуглеводи (наприклад, цукор, включаючи моносахариди, ди-, три-, тетра- і олігосахариди; похідні цукру, такі як альдити, альдонові кислоти, етерифіковані цукри і тому подібне; і полісахариди або полімери цукру), які можуть бути присутніми окремо або в поєднанні, включаючи окремий або поєднанний вміст 199,99% по масі або об'єму. Типові білкові наповнювачі включають сироватковий альбумін, такий як людський сироватковий альбумін (ЧСА), рекомбінантний альбумін людини (rHA), желатин, казеїн і тому подібне. Репрезентативні амінокислотні компоненти імітуючого шарнірну основу EPO міметотіла або іншого агоніста рецептора EPO або окремої частини або варіанту, які можуть також брати участь у визначенні буферної ємності, включають аланін, гліцин, аргінін, бетаїн, гістидин, глутамінову кислоту, аспарагінову кислоту, цистеїн, лізин, лейцин, ізолейцин, 25 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 60 валін, метіонін, фенілаланін, аспартам і тому подібне. Однією з переважних амінокислот є гліцин. Придатні для використання у винаході вуглеводневі наповнювачі включають, наприклад, моносахариди, такі як фруктоза, мальтоза, галактоза, глюкоза, D-маноза, сорбоза і тому подібне; дисахариди, такі як лактоза, сахароза, трегалоза, целобіоза і тому подібне; полісахариди, такі як рафіноза, мелезитоза, мальтодекстрини, декстрани, крохмаль і тому подібне; і альдити, такі як маніт, ксиліт, мальтит, лактит, ксиліт, сорбіт (гліцит), міоінозит і тому подібне. Переважними вуглеводневими наповнювачами для використання в даному винаході є маніт, трегалоза і рафіноза. Композиції імітуючого шарнірну основу EPO міметотіла або іншого агоніста рецептора EPO можуть включати буфер або агента, що доводить pH; зазвичай буфер являє собою сіль, одержану з органічної кислоти або основи. Типові буфери включають солі органічних кислот, такі як солі лимонної кислоти, аскорбінової кислоти, глюконової кислоти, карбонової кислоти, винної кислоти, бурштинової кислоти, оцтової кислоти або фталевої кислоти; трис, трометаміну гідрохлорид або фосфатні буфери. Переважними буферами для використання в даних композиціях є солі органічних кислот, такі як цитрат. Крім того, композиції імітуючого шарнірну основу EPO міметотіла або іншого агоніста рецептора EPO або окремої частини або варіанту винаходу можуть включати полімерні наповнювачі/добавку, такі як полівінілпіролідони, фіколі (полімерний цукор), декстрати (наприклад, циклодекстрини, такі як 2-гідроксипропіл-β-циклодекстрин), поліетиленгліколі, віддушки, протимікробні агенти, підсолоджувачі, антиоксиданти, антистатики, поверхневоактивні речовини (наприклад, полісорбати, такі як «твін 20» і «твін 80»), ліпіди (наприклад, фосфоліпіди, жирні кислоти), стероїди (наприклад, холестерин) і хелатувальні агенти (наприклад, ЕДТА). Ці і додаткові відомі фармацевтичні наповнювачі і/або добавки, придатні для використання в композиціях міметотіла, імітуючі шарнірну основу EPO, або іншого агоніста рецептора EPO за винаходом, відомі в даній галузі техніки, наприклад, як перераховано в "Remington: The Science nd & Practice of Pharmacy", 19th ed., Williams & Williams, (1995), і в "Physician's Desk Reference", 52 ed., Medical Economics, Montvale, NJ (1998), розкриття яких повністю включене в даний опис як посилання. Переважними речовинами-носіями або наповнювачами є вуглеводи (наприклад, сахариди і альдити) і буфери (наприклад, цитрат) або полімерні агенти. Склади Як відмічалося вище, у винаході пропонуються стабільні склади, які можуть переважно включати придатний буфер з сольовим розчином або вибраною сіллю, а також необов'язкові консервовані розчини і склади, що містить консервант, а також консервовані склади багаторазового застосування, придатні для фармацевтичного або ветеринарного використання, що включають щонайменше одне міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO або окрему частину або варіант в фармацевтично прийнятному складі. Консервовані склади містять щонайменше один відомий консервант або необов'язково вибране з групи, що складається з щонайменше одного з фенолу, м-крезолу, п-крезолу, о-крезолу, хлоркрезолу, бензилового спирту, фенілртутьнітриту, феноксіетанолу, формальдегіду, хлорбутанолу, магнію хлориду (наприклад, гексагідрату), алкілпарабену (метил, етил, пропіл, бутил і тому подібне), бензалконію хлориду, бензетонію хлориду, дегідроацетату натрію і тимерозалу, або їх суміші у водному розріджувачі. Може бути використана будь-яка відповідна концентрація або суміш, як це відомо в даній галузі техніки, така як 0,001-5%, або будь-який діапазон або величина всередині нього, така як, але не обмежуючись цим, 0,001, 0,003, 0,005, 0,009, 0,01, 0,02, 0,03, 0,05, 0,09, 0,1, 0,2, 0,3, 0,4, 0,5, 0,6, 0,7, 0,8, 0,9, 1,0, 1,1, 1,2, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8, 1,9, 2,0, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9, 3,0, 3,1, 3,2, 3,3, 3,4, 3,5, 3,6, 3,7, 3,8, 3,9, 4,0, 4,3, 4,5, 4,6, 4,7, 4,8, 4,9, або будь-який діапазон або величина всередині нього. Необмежувальні приклади включають відсутність консерванту, 0,1-2% м-крезолу (наприклад, 0,2, 0,3, 0,4, 0,5, 0,9, 1,0%), 0,1-3% бензилового спирту (наприклад, 0,5, 0,9, 1,1, 1,5, 1,9, 2,0, 2,5%), 0,001-0,5% тимерозалу (наприклад, 0,005, 0,01), 0,001-2,0% фенолу (наприклад, 0,05, 0,25, 0,28, 0,5, 0,9, 1,0%), 0,0005-1,0% алкілпарабену (алкілпарабенів) (наприклад, 0,00075, 0,0009, 0,001, 0,002, 0,005, 0,0075, 0,009, 0,01, 0,02, 0,05, 0,075, 0,09, 0,1, 0,2, 0,3, 0,5, 0,75, 0,9, 1,0%) і тому подібне. Як відмічалося вище, у винаході пропонується предмет виробництва, що включає пакувальний матеріал і щонайменше один флакон, що включає розчин щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або окремої частини, або варіанту з встановленими буферами і/або консервантами необов'язково у водному розріджувачі, де вказаний пакувальний матеріал включає етикетку, на якій вказано, що такий 26 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 60 розчин може зберігатися протягом періоду 1, 2, 3, 4, 5, 6, 9, 12, 18, 20, 24, 30, 36, 40, 48, 54, 60, 66, 72 годин або більше. Винахід додатково включає предмет виробництва, що включає пакувальний матеріал, першу посудину, що включає ліофілізоване щонайменше одне міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO або окрему частину або варіант, і другий флакон, що включає водний розріджувач встановленого буфера або консерванту, де вказаний пакувальний матеріал включає етикетку з інструкцією хворому з відновлення щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або окремої частини, або варіанту у водному розріджувачі для утворення розчину, який може зберігатися протягом двадцяти чотирьох часового періоду або довше. Щонайменше одне міметотіло, що імітує шарнірну основу EPO, або інший агоніст рецептора EPO, або окрема частина, або варіант, що використовується за даним винаходом, може бути одержане рекомбінантними способами, включаючи одержання з клітин ссавців або трансгенних препаратів, або може бути очищене з інших біологічних джерел, як описано в даному описі або як відомо в даній галузі техніки. Діапазон кількостей щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або окремої частини, або варіанту, в продукті даного винаходу включає кількості, що дають після відновлення у вологій/сухій системі концентрації від приблизно 1,0 мкг/мл до приблизно 1000 мг/мл, хоча діють і більш низькі і більш високі концентрації і залежать від наміченого засобу доставки, наприклад, склади розчинів повинні відрізнятися від методів доставки з використанням черезшкірного пластиру, через легені, через слизову або осмотичні або мікронасоси. Переважно водний розріджувач необов'язково додатково включає фармацевтично прийнятний консервант. Переважні консерванти включають консерванти, вибрані з групи, що складається з фенолу, м-крезолу, п-крезолу, о-крезолу, хлоркрезолу, бензилового спирту, алкілпарабену (метил, етил, пропіл, бутил і тому подібне), бензалконію хлориду, бензетония хлориду, дегідроацетату натрію і тимерозалу, або їх суміші. Концентрація консерванту, що використовується в складі, являє собою концентрацію, достатню для надання протимікробної дії. Такі концентрації залежать від вибраного консерванту і легко визначаються досвідченим фахівцем. До розріджувача можуть бути додані необов'язково і переважно інші наповнювачі, наприклад, агенти ізотонічності, буфери, антиоксиданти, підсилювачі консервації. Агент ізотонічності, такий як гліцерин, зазвичай використовують у відомих концентраціях. Фізіологічно допустимий буфер переважно додають для забезпечення поліпшеного контролю pH. pH складів може знаходитися в широкому діапазоні, такому як від приблизно pH 4 до приблизно pH 10, і переважно в діапазонах від приблизно pH 5 до приблизно pH 9, і найбільш переважно в діапазоні від приблизно 6 до приблизно 8. Переважно склади даного винаходу мають pH між приблизно 6,8 і приблизно 7,8. Переважні буфери включають фосфатні буфери, найбільш переважно фосфат натрію, особливо забуференний фосфатом фізіологічний розчин (ЗФР). Для зниження агрегації до складів або композицій можуть бути необов'язково додані інші добавки, такі як фармацевтично прийнятні солюбілізатори, подібні твіну 20 (поліоксіетилен (20) сорбітану монолаурат), твіну 40 (поліоксіетилен (20) сорбітану монопальмітат), твіну 80 (поліоксіетилен (20) сорбітану моноолеат), Pluronic F68 (поліоксіетилен поліоксипропілен блокспівполімери) і ПЕГ (поліетиленгліколь), або неіонні поверхнево-активні речовини, такі як полісорбат 20 або 80 або полоксамер 184 або 188, Pluronic® поліли, інші блокспівполімери і хелатори, такі як ЕДТА і ЕГТА. Ці добавки особливо корисні, коли для введення складу використовують насос або пластиковий контейнер. Присутність фармацевтично прийнятної поверхнево-активної речовини знижує схильність білка до агрегації. Склади даного винаходу можуть бути одержані за допомогою методу, який включає змішування щонайменше одному міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або окремої частини, або варіанту і консерванту, вибраного з групи, що складається з фенолу, м-крезолу, п-крезолу, о-крезолу, хлоркрезолу, бензилового спирту, алкілпарабену (метил, етил, пропіл, бутил і тому подібне), бензалконію хлориду, бензетонію хлориду, дегідроацетату натрію і тимерозалу, або їх сумішей у водному розріджувачі. Змішування щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або окремої частини, або варіанту і консерванту у водному розріджувачі проводять з використанням традиційних процедур розчинення і змішування. Для одержання придатного складу, наприклад, відміряної кількості щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або окремої частини, або варіанту в забуференому розчині з'єднують з бажаним консервантом в забуференому розчині в 27 UA 98472 C2 5 10 15 20 25 30 35 40 45 50 55 60 кількостях, достатніх для забезпечення бажаних концентрацій білка і консерванту. Варіанти цього процесу повинні бути зрозумілі фахівцеві в даній галузі техніки. Наприклад, порядок додавання компонентів, використання додаткових добавок, температура і pH, при яких одержують склад всі ці фактори можуть бути оптимізовані відносно використовуваних концентрації і засобів введення. Заявлені склади можуть бути надані хворим у вигляді прозорих розчинів або у вигляді двох флаконів, що включають флакон ліофілізованого щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або окремої частини, або варіанту, яке відновлюють за допомогою другого флакона, що містить воду, консервант і/або наповнювачі, переважно фосфатний буфер і/або фізіологічний розчин і вибрану сіль, у водному розріджувачі. Або єдиний флакон з розчином, або два флакони, що потребують відновлення, можуть бути використані повторно багато разів і можуть забезпечувати один або багато циклів лікування хворого і тим самим забезпечувати більш зручний режим лікування, ніж наявний в даний час. Заявлені продукти можуть надаватися хворим опосередковано, шляхом їх надання аптекам, клінікам або іншим подібним організаціям і підприємствам по наданню послуг прозорих розчинів або двох флаконів, що включають флакон ліофілізованого щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або окремої частини, або варіанту, яке відновлюють за допомогою другого флакона, що містить водний розріджувач. У цьому випадку прозорий розчин може мати об'єм до одного літра або навіть більше, забезпечуючи великий резервуар, з якого можна відбирати однократно або багато разів менші частини щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або окремої частини, або варіанту для перенесення в менші флакони і забезпечення аптекою або клінікою своїх покупців і/або хворих. Загальновизнані пристрої, що включають ці системи з одним флаконом, включають пристрої ручки-інжектора з одним або двома флаконами для доставки розчину ліків для використання в даному винаході, а також необов'язково додатково таких, що включають систему з двома флаконами, яка включає такі системи ручки-інжектора для відновлення ліофілізованих ліків в картріджі для доставки розчину ліків, як добре відома в даній галузі техніки, такі як розкриті в патентах США nos. 6203530, 5026349, 5567160, 5954738, 5879327, 5599302, 6015438, 6461333, 6517517, 6077247, 6099504, 6428528, 6387078, 5868711, 5960797, 5176643, 5271744, 5405362, 5451210, 5137516, 5176643, 5300030, 5295965, 5425715, 5478316, 5575777, 5599309, 5681291, 5709662, 5779677, 5913843, 5843036, 5957897, 6428528, 6086562, 6099503, 6221044, 6270479, 6258068, 6391003, 6280421, 6045534, 6371939, 6090078, 5267963, 5487732, 5425715, 6575939, 6565540, 6159181, 6179812, 6544234, 6572581, 6676630, 6083197, 6203530, 6270479, 6371939, 5575777, 6090078, 6743199, 6589210, 6689093, 6783509, 6645170, 6641554, 6796967, 6645181, 6641565, 6575939, 6569115, 6673049, 6641560, 6569124, 6699220, 6638256, 6607508, 6607510, 6776777, 6767336, 6595962, 6740062, 6565553, 6746429, 6569123, 6595957, 6770056, кожний з яких повністю включений в даний опис як посилання. Заявлені в даному описі продукти включають пакувальний матеріал. Пакувальний матеріал забезпечує на додаток до інформації, необхідної органами державного регулювання, умови, за яких продукт можна використовувати. Пакувальний матеріал даного винаходу містить інструкції для хворого по відновленню щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або окремої частини, або варіанта, у водному розріджувачі з утворенням розчину і по використанню розчину протягом періоду 2-24 годин або більше для продукту з двома флаконами, сирий/сухий. У випадку продукту у вигляді розчину в одному флаконі на етикетці вказується, що такий розчин можна використовувати протягом періоду 2-24 годин або більше. Заявлені в даному описі продукти придатні для використання як фармацевтичний продукт для людини. Склади даного винаходу можуть бути одержані за допомогою методів, які включають змішування щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або окремої частини, або варіанту і вибраного буфера, переважно фосфатного буфера, що містить фізіологічний розчин, або вибраної солі. Змішування щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або окремої частини, або варіанту і буфера у водному розріджувачі проводять за допомогою традиційних процедур розчинення і змішування. Для одержання відповідного складу, наприклад, відміряну кількість щонайменше одного міметотіла, що імітує шарнірну основу EPO, або іншого агоніста рецептора EPO, або окремої частини, або варіанту у воді або буфері з'єднують з бажаним буферувальним агентом у воді в кількостях, достатніх для забезпечення бажаних концентрацій білка і буфера. Варіанти цього процесу повинні бути 28
ДивитисяДодаткова інформація
Назва патенту англійськоюUse of human epo receptor agonists for treating glucose intolerance related conditions
Автори англійськоюJames, Ian, E., Picha, Kristen
Назва патенту російськоюПрименение агониста рецептора epo человека для лечения интолерантности к глюкозе
Автори російськоюДжеймс Айан Э., Пича Кристен
МПК / Мітки
МПК: A61K 38/18, A61P 3/08
Мітки: рецептора, лікування, глюкози, агоніста, інтолерантності, людини, застосування
Код посилання
<a href="https://ua.patents.su/61-98472-zastosuvannya-agonista-receptora-epo-lyudini-dlya-likuvannya-intolerantnosti-do-glyukozi.html" target="_blank" rel="follow" title="База патентів України">Застосування агоніста рецептора epo людини для лікування інтолерантності до глюкози</a>
Попередній патент: Ґрунтообробний пристрій з великою шириною захвату
Наступний патент: Солі та кристалічні форми 2-метил-2-[4-(3-метил-2-оксо-8-хінолін-3-іл-2,3-дигідроімідазо[4,5-с]хінолін-1-іл)феніл]пропіонітрилу
Випадковий патент: Спосіб лікування післяінсультних порушень і пристрій для його реалізації