Піразолінові сполуки та їх фармацевтичне застосування, композиція на їх основі
Номер патенту: 92670
Опубліковано: 25.11.2010
Автори: Махоні Мет'ю Вілліям, Рейтс Девід Брюс, Аргансет Ґресіела Барбіері, Лонґ Скотт Аллен, Мейерс Марвін Джей, Гокерман Сюзан Ландіс, Чен Кіянґйан, Ріко Джозеф Ґерас
Формула / Реферат
1. Сполука або фармацевтично прийнятна сіль сполуки, де сполука має структуру формули І:
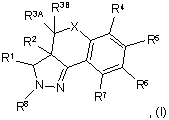
де:
X вибрано з групи: -СН2- та -О-;
R1 вибрано з групи: циклопентил, циклобутил та феніл; де R1 циклопентил, циклобутил та феніл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: хлор, флуор, метил, етил, пропіл, хлорметил, дихлорметил, трихлорметил, флуорметил, дифлуорметил та трифлуорметил;
R2 вибрано з групи: гідроген та алкіл;
R3A та R3B є незалежно вибраними з групи: гідроген та алкіл;
R4, R6 та R7 є незалежно вибраними з групи: гідроген, галоген, гідрокси, алкіл, галогеналкіл, гідроксіалкіл та алкокси;
R5 вибрано з групи: гідроген, -(CH2)mOR50, -(CH2)mC(O)R50, -(CH2)mC(O)OR50, -(CH2)mC(O)NR51R52, -(CH2)mNR51R52, -(CH2)mN(R51)C(O)R52 та -(CH2)mS(O)nR50;
m=0, 1, 2, 3, 4, 5 або 6;
n=0, 1 або 2;
R50 вибрано з групи: гідроген та алкіл;
R51 та R52 є незалежно вибраними з групи: гідроген та алкіл; або R51 та R52 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6-членний кільцевий гетероцикліл;
де R50, R51 та R52 алкіли та R51/R52 гетероцикліл можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: галоген, піролідиніл, -OR53, -C(O)R53, -C(O)OR53, -C(O)NR54R55, -NR54R55, -N(R56)C(O)R53, -S(O)pR53 та -S(O)pNR54R55;
p=0, 1 або 2;
R53 вибрано з групи: гідроген, алкіл, галогеналкіл, гідроксіалкіл та карбоксіалкіл;
R54 та R55 є незалежно вибраними з групи: гідроген, алкіл, галогеналкіл, гідроксіалкіл та карбоксіалкіл; або R54 та R55 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6-членний кільцевий гетероцикліл;
R56 вибрано з групи: гідроген та алкіл; а
R8 вибрано з групи: феніл, піридиніл та піримідиніл; де феніл, піридиніл та піримідиніл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, алкіл, галогеналкіл, ціаноалкіл, гідроксіалкіл, карбоксіалкіл, алкокси, галогеналкокси, ціаноалкокси, аміно, алкіламіно, діалкіламіно та алкоксикарбоніл.
2. Сполука або фармацевтично прийнятна сіль сполуки, де сполука має структуру формули II:
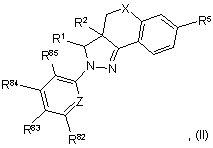
де:
X вибрано з групи: -СН2- та -О-;
Z вибрано з групи: -C(R81)- та -N-;
R1 вибрано з групи: циклопентил, циклобутил та феніл; де R1 циклопентил, циклобутил та феніл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: хлор, флуор, метил, етил, пропіл, хлорметил, дихлорметил, трихлорметил, флуорметил, дифлуорметил та трифлуорметил;
R2 вибрано з групи: гідроген або (С1-С4)-алкіл;
R5 вибрано з групи: -(CH2)mOR50, -(CH2)mC(O)OR50 та -(CH2)mC(O)NR51R52; де:
m=0, 1, 2 або 3;
R50 вибрано з групи: гідроген та (С1-С6)-алкіл;
R51 та R52 є незалежно вибраними з групи: гідроген та (С1-С6)-алкіл;
де R50, R51 та R52 (С1-С6)-алкіли можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: галоген, -OR53, -C(O)R53, -C(O)OR53, -C(O)NR54R55, -NR54R55, -N(R56)C(O)R53, -S(O)pR53 та -S(O)pNR54R55;
p=0, 1 або 2;
R53 вибрано з групи: гідроген, (С1-С6)-алкіл, галоген-(С1-С6)-алкіл, гідроксі-(С1-С6)-алкіл та карбоксі-(С1-С6)-алкіл;
R54 та R55 є незалежно вибраними з групи: гідроген, (С1-С6)-алкіл, галоген-(С1-С6)-алкіл, гідроксі-(С1-С6)-алкіл та карбоксі-(С1-С6)-алкіл; а
R81, R82, R83, R84 та R85 є незалежно вибраними з групи: гідроген, хлор, флуор, ціано, гідрокси, карбокси, метил, етил, трихлорметил, трифлуорметил, ціанометил, гідроксиметил, карбоксиметил, метокси, аміно, метиламіно та диметиламіно.
3. Сполука за п. 2, де R2 - гідроген.
4. Сполука за п. 3, де:
R5 - -(CH2)mC(O)OR50, де:
m=0, 1, 2 або 3;
R50 вибрано з групи: гідроген та (С1-С6)-алкіл;
де R50 (С1-С6)-алкіл може бути незалежно та необов'язково заміщеним одним або більше замісниками, вибраними з групи: галоген, -OR53, -C(O)R53, -C(O)OR53, -C(O)NR54R55, -NR54R55, -N(R56)C(O)R53, -S(O)pR53 та -S(O)pNR54R55;
p=0, 1 або 2;
R53 вибрано з групи: гідроген, (С1-С6)-алкіл, галоген-(С1-С6)-алкіл, гідроксі-(С1-С6)-алкіл та карбоксі-(С1-С6)-алкіл; а
R54 та R55 є незалежно вибраними з групи: гідроген, (С1-С6)-алкіл, галоген-(С1-С6)-алкіл, гідроксі-(С1-С6)-алкіл та карбоксі-(С1-С6)-алкіл.
5. Сполука за п. 3, де:
X - -СН2-;
Z - -C(R81)-;
R1 вибрано з групи: циклопентил, циклобутил та феніл, де R1 феніл може бути необов'язково заміщеним флуором; R5 - -(CH2)mC(O)OR50,
де: m=0;
R50 - гідроген;
R81, R84 та R85, кожний, - гідроген; а
R82 та R83 є незалежно вибраними з групи: хлор, ціано та метил.
6. Сполука за п. 5, де R82 - хлор, a R83 - ціано.
7. Сполука за п. 5, де R1 - циклопентил.
8. Сполука за п. 5, де R1 - феніл, де R1 феніл може бути необов'язково заміщеним флуором.
9. Сполука за п. 3, де:
X - -О-;
Z - -C(R81)-;
R1 вибрано з групи: циклопентил, циклобутил та феніл, де R1 феніл може бути необов'язково заміщеним флуором; R5 - -(CH2)mC(O)OR50, де: m=0;
R50 - гідроген;
R81, R84 та R85, кожний, - гідроген; а R82 та R83 є незалежно вибраними з групи: хлор, ціано та метил.
10. Сполука за п. 3, де:
X - -СН2-;
Z - -N-;
R1 вибрано з групи: циклопентил, циклобутил та феніл, де R1 феніл може бути необов'язково заміщеним флуором;
R5 - -(CH2)mC(O)OR50, де:
m=0;
R50 - гідроген;
R81, R84 та R85, кожний, - гідроген; а
R82 та R83 є незалежно вибраними з групи: хлор, ціано та метил.
11. Сполука за п. 3, де:
X - -О-;
Z - -N-;
R1 вибрано з групи: циклопентил, циклобутил та феніл, де R1 феніл може бути необов'язково заміщеним флуором;
R5 - -(CH2)mC(O)OR50, де:
m=0;
R50 - гідроген;
R81, R84 та R85, кожний, - гідроген; а
R82 та R83 є незалежно вибраними з групи: хлор, ціано та метил.
12. Сполука за п. 3, вибрана з групи:
2-(3-хлор-4-ціанофеніл)-3-(4-флуорфеніл)-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
3-(4-флуорфеніл)-7-гідрокси-3,3а,4,5-тетрагідробензо[g]індазол-2-іл)-2-метилбензонітрил;
3-(4-флуорфеніл)-7-гідрокси-3,3а,4,5-тетрагідробензо[g]індазол-2-іл)-2-(трифлуорметил)бензонітрил;
2-хлор-4-(3-(4-флуорфеніл)-7-гідрокси-3,3а,4,5-тетрагідробензо[g]індазол-2-іл)бензонітрил;
2-(3-хлор-4-ціанофеніл)-3-(4-флуорфеніл)-N-(2-(метилсульфоніл)етил)-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбоксамід;
2-(3-хлор-4-ціанофеніл)-3-циклопентил-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
2-(4-ціанофеніл)-3-циклопентил-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
2-(4-ціано-3-метилфеніл)-3-циклопентил-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
2-(5-ціано-6-метилпіридин-2-іл)-3-циклопентил-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
2-(4-ціано-3-метоксифеніл)-3-циклопентил-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
N-(-2-(3-хлор-4-ціанофеніл)-3-циклопентил-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-іл)ацетамід;
метил 2-(3-хлор-4-ціанофеніл)-3-циклопентил-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбоксилат;
2-(3-хлор-4-ціанофеніл)-3-циклопентил-3а-метил-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
2-(3-хлор-4-ціанофеніл)-3-циклопентил-N-(2-(метилсульфоніл)етил)-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбоксамід;
2-(3-хлор-4-ціанофеніл)-3-циклопентил-N-(2-гідроксіетил)-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбоксамід;
2-(4-ціано-3-метилфеніл)-3-циклопентил-2,3,3а,4-тетрагідрохромено[4,3-с]піразол-7-карбонова кислота;
2-(3-хлор-4-ціанофеніл)-3-циклобутил-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
2-(3-хлор-4-ціанофеніл)-3-циклопентеніл-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
2-(4-ціано-3-метилфеніл)-3-циклопентеніл-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
2-(3-хлор-4-ціанофеніл)-3-(5-метил-2-фурил)-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
2-(3-хлор-4-ціанофеніл)-3-(3-фурил)-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
2-(3-хлор-4-ціанофеніл)-3-(5-метил-2-фурил)-N-[2-(метилсульфоніл)етил]-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбоксамід;
2-(3-хлор-4-ціанофеніл)-N-[2-(метилсульфоніл)етил]-3-(2-метил-1,3-тіазол-5-іл)-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбоксамід;
2-(3-хлор-4-ціанофеніл)-3-циклопентил-2,3,3а,4-тетрагідрохромено[4,3-с]піразол-7-карбонова кислота;
2-[4-ціано-3-(трифлуорметил)феніл]-3-циклопентил-2,3,3а,4-тетрагідрохромено[4,3-с]піразол-7-карбонова кислота;
2-(4-ціано-3-метилфеніл)-3-циклопентеніл-2,3,3а,4-тетрагідрохромено[4,3-с]піразол-7-карбонова кислота та
2-(3-хлор-4-ціанофеніл)-3-циклопентеніл-2,3,3а,4-тетрагідрохромено[4,3-с]піразол-7-карбонова кислота;
або її фармацевтично прийнятні солі.
13. Сполука за п. 3, вибрана з групи:
2-(3-хлор-4-ціанофеніл)-3-циклопентил-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
2-(4-ціано-3-метилфеніл)-3-циклопентил-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота та
2-(4-ціано-3-метоксифеніл)-3-циклопентил-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота;
або її фармацевтично прийнятні солі.
14. Сполука, що має формулу
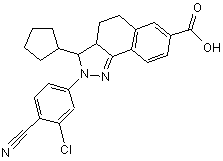 ,
,
або її фармацевтично прийнятна сіль.
15. Сполука, що має формулу
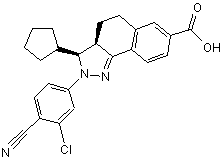 ,
,
або її фармацевтично прийнятна сіль.
16. Сполука, що має формулу
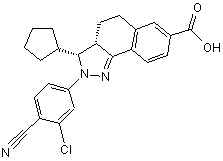 ,
,
або її фармацевтично прийнятна сіль.
17. Сполука, що має формулу
 .
.
18. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки за будь-яким пп. 1-17 або її фармацевтично прийнятної солі та фармацевтично прийнятний носій.
19. Композиція за п. 18, що додатково містить терапевтично ефективну кількість одної або більше сполук, вибраних з групи: діуретики, інгібітори ферменту перетворення ангіотензину, блокатори рецептора ангіотензину II, блокатори каналів кальцію, бета-блокатори, альфа-блокатори, альфа-бета-блокатори, антагоністи рецептора альдостерону та інгібітори реніну.
20. Спосіб лікування стану, вибраного з групи: серцево-судинні стани, ниркові стани, стани печінки, стани судин, запальні стани, біль, ретинопатія, невропатія, інсулінопатія, набряк, ендотеліальна дисфункція та барорецепторна дисфункція, при якому застосовують терапевтично ефективну кількість сполуки за будь-яким з пп. 1-17 або її фармацевтично прийнятної солі до суб'єкта, що потребує цього.
Текст
1. Сполука або фармацевтично прийнятна сіль сполуки, де сполука має структуру формули І: 2 (19) 1 3 X R2 R1 R85 N 92670 R5 N R84 Z R83 R82 , (II) де: X вибрано з групи: -СН2- та -О-; Z вибрано з групи: -C(R81)- та -N-; R1 вибрано з групи: циклопентил, циклобутил та феніл; де R1 циклопентил, циклобутил та феніл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: хлор, флуор, метил, етил, пропіл, хлорметил, дихлорметил, трихлорметил, флуорметил, дифлуорметил та трифлуорметил; R2 вибрано з групи: гідроген або (С1-С4)-алкіл; R5 вибрано з групи: -(CH2)mOR50, -(CH2)mC(O)OR50 та -(CH2)mC(O)NR51R52; де: m=0, 1, 2 або 3; R50 вибрано з групи: гідроген та (С1-С6)-алкіл; R51 та R52 є незалежно вибраними з групи: гідроген та (С1-С6)-алкіл; де R50, R51 та R52 (С1-С6)-алкіли можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: галоген, OR53, -C(O)R53, -C(O)OR53, -C(O)NR54R55, -NR54R55, -N(R56)C(O)R53, -S(O)pR53 та -S(O)pNR54R55; p=0, 1 або 2; R53 вибрано з групи: гідроген, (С1-С6)-алкіл, галоген-(С1-С6)-алкіл, гідроксі-(С1-С6)-алкіл та карбоксі(С1-С6)-алкіл; R54 та R55 є незалежно вибраними з групи: гідроген, (С1-С6)-алкіл, галоген-(С1-С6)-алкіл, гідроксі(С1-С6)-алкіл та карбоксі-(С1-С6)-алкіл; а R81, R82, R83, R84 та R85 є незалежно вибраними з групи: гідроген, хлор, флуор, ціано, гідрокси, карбокси, метил, етил, трихлорметил, трифлуорметил, ціанометил, гідроксиметил, карбоксиметил, метокси, аміно, метиламіно та диметиламіно. 3. Сполука за п.2, де R2 - гідроген. 4. Сполука за п.3, де: R5 - -(CH2)mC(O)OR50, де: m=0, 1, 2 або 3; R50 вибрано з групи: гідроген та (С1-С6)-алкіл; де R50 (С1-С6)-алкіл може бути незалежно та необов'язково заміщеним одним або більше замісниками, вибраними з групи: галоген, -OR53, -C(O)R53, -C(O)OR53, -C(O)NR54R55, -NR54R55, -N(R56)C(O)R53, -S(O)pR53 та -S(O)pNR54R55; p=0, 1 або 2; R53 вибрано з групи: гідроген, (С1-С6)-алкіл, галоген-(С1-С6)-алкіл, гідроксі-(С1-С6)-алкіл та карбоксі(С1-С6)-алкіл; а R54 та R55 є незалежно вибраними з групи: гідроген, (С1-С6)-алкіл, галоген-(С1-С6)-алкіл, гідроксі(С1-С6)-алкіл та карбоксі-(С1-С6)-алкіл. 5. Сполука за п.3, де: X - -СН2-; Z - -C(R81)-; 4 R1 вибрано з групи: циклопентил, циклобутил та феніл, де R1 феніл може бути необов'язково заміщеним флуором; R5 - -(CH2)mC(O)OR50, де: m=0; 50 R - гідроген; R81, R84 та R85, кожний, - гідроген; а R82 та R83 є незалежно вибраними з групи: хлор, ціано та метил. 6. Сполука за п.5, де R82 - хлор, a R83 - ціано. 7. Сполука за п.5, де R1 - циклопентил. 8. Сполука за п.5, де R1 - феніл, де R1 феніл може бути необов'язково заміщеним флуором. 9. Сполука за п.3, де: X - -О-; Z - -C(R81)-; R1 вибрано з групи: циклопентил, циклобутил та феніл, де R1 феніл може бути необов'язково заміщеним флуором; R5 - -(CH2)mC(O)OR50, де: m=0; R50 - гідроген; R81, R84 та R85, кожний, - гідроген; а R82 та R83 є незалежно вибраними з групи: хлор, ціано та метил. 10. Сполука за п.3, де: X - -СН2-; Z - -N-; R1 вибрано з групи: циклопентил, циклобутил та феніл, де R1 феніл може бути необов'язково заміщеним флуором; R5 - -(CH2)mC(O)OR50, де: m=0; R50 - гідроген; 81 84 85 R , R та R , кожний, - гідроген; а R82 та R83 є незалежно вибраними з групи: хлор, ціано та метил. 11. Сполука за п.3, де: X - -О-; Z - -N-; R1 вибрано з групи: циклопентил, циклобутил та феніл, де R1 феніл може бути необов'язково заміщеним флуором; 5 50 R - -(CH2)mC(O)OR , де: m=0; R50 - гідроген; R81, R84 та R85, кожний, - гідроген; а R82 та R83 є незалежно вибраними з групи: хлор, ціано та метил. 12. Сполука за п.3, вибрана з групи: 2-(3-хлор-4-ціанофеніл)-3-(4-флуорфеніл)-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота; 3-(4-флуорфеніл)-7-гідрокси-3,3а,4,5тетрагідробензо[g]індазол-2-іл)-2метилбензонітрил; 3-(4-флуорфеніл)-7-гідрокси-3,3а,4,5тетрагідробензо[g]індазол-2-іл)-2(трифлуорметил)бензонітрил; 2-хлор-4-(3-(4-флуорфеніл)-7-гідрокси-3,3а,4,5тетрагідробензо[g]індазол-2-іл)бензонітрил; 2-(3-хлор-4-ціанофеніл)-3-(4-флуорфеніл)-N-(2(метилсульфоніл)етил)-3,3а,4,5-тетрагідро-2Нбензо[g]індазол-7-карбоксамід; 2-(3-хлор-4-ціанофеніл)-3-циклопентил-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота; 5 2-(4-ціанофеніл)-3-циклопентил-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота; 2-(4-ціано-3-метилфеніл)-3-циклопентил-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота; 2-(5-ціано-6-метилпіридин-2-іл)-3-циклопентил3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота; 2-(4-ціано-3-метоксифеніл)-3-циклопентил3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота; N-(-2-(3-хлор-4-ціанофеніл)-3-циклопентил3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7іл)ацетамід; метил 2-(3-хлор-4-ціанофеніл)-3-циклопентил3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбоксилат; 2-(3-хлор-4-ціанофеніл)-3-циклопентил-3а-метил3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота; 2-(3-хлор-4-ціанофеніл)-3-циклопентил-N-(2(метилсульфоніл)етил)-3,3а,4,5-тетрагідро-2Нбензо[g]індазол-7-карбоксамід; 2-(3-хлор-4-ціанофеніл)-3-циклопентил-N-(2гідроксіетил)-3,3а,4,5-тетрагідро-2Нбензо[g]індазол-7-карбоксамід; 2-(4-ціано-3-метилфеніл)-3-циклопентил-2,3,3а,4тетрагідрохромено[4,3-с]піразол-7-карбонова кислота; 2-(3-хлор-4-ціанофеніл)-3-циклобутил-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота; 2-(3-хлор-4-ціанофеніл)-3-циклопентеніл-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота; 2-(4-ціано-3-метилфеніл)-3-циклопентеніл3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота; 2-(3-хлор-4-ціанофеніл)-3-(5-метил-2-фурил)3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота; 2-(3-хлор-4-ціанофеніл)-3-(3-фурил)-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота; 2-(3-хлор-4-ціанофеніл)-3-(5-метил-2-фурил)-N-[2(метилсульфоніл)етил]-3,3а,4,5-тетрагідро-2Нбензо[g]індазол-7-карбоксамід; 2-(3-хлор-4-ціанофеніл)-N-[2(метилсульфоніл)етил]-3-(2-метил-1,3-тіазол-5-іл)3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбоксамід; 2-(3-хлор-4-ціанофеніл)-3-циклопентил-2,3,3а,4тетрагідрохромено[4,3-с]піразол-7-карбонова кислота; 2-[4-ціано-3-(трифлуорметил)феніл]-3циклопентил-2,3,3а,4-тетрагідрохромено[4,3с]піразол-7-карбонова кислота; 2-(4-ціано-3-метилфеніл)-3-циклопентеніл2,3,3а,4-тетрагідрохромено[4,3-с]піразол-7карбонова кислота та 2-(3-хлор-4-ціанофеніл)-3-циклопентеніл-2,3,3а,4тетрагідрохромено[4,3-с]піразол-7-карбонова кислота; або її фармацевтично прийнятні солі. 92670 6 13. Сполука за п.3, вибрана з групи: 2-(3-хлор-4-ціанофеніл)-3-циклопентил-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота; 2-(4-ціано-3-метилфеніл)-3-циклопентил-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота та 2-(4-ціано-3-метоксифеніл)-3-циклопентил3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота; або її фармацевтично прийнятні солі. 14. Сполука, що має формулу O OH N N Cl N , або її фармацевтично прийнятна сіль. 15. Сполука, що має формулу O OH N N Cl N , або її фармацевтично прийнятна сіль. 16. Сполука, що має формулу O OH N N N Cl , або її фармацевтично прийнятна сіль. 17. Сполука, що має формулу O OH N N Cl N . 18. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки за будьяким пп.1-17 або її фармацевтично прийнятної солі та фармацевтично прийнятний носій. 19. Композиція за п.18, що додатково містить терапевтично ефективну кількість одної або більше сполук, вибраних з групи: діуретики, інгібітори ферменту перетворення ангіотензину, блокатори рецептора ангіотензину II, блокатори каналів ка 7 92670 8 льцію, бета-блокатори, альфа-блокатори, альфабета-блокатори, антагоністи рецептора альдостерону та інгібітори реніну. 20. Спосіб лікування стану, вибраного з групи: серцево-судинні стани, ниркові стани, стани печінки, стани судин, запальні стани, біль, ретинопатія, невропатія, інсулінопатія, набряк, ендотеліальна дисфункція та барорецепторна дисфункція, при якому застосовують терапевтично ефективну кількість сполуки за будь-яким з пп.1-17 або її фармацевтично прийнятної солі до суб'єкта, що потребує цього. Заявлений винахід стосується класу піразолінових сполук, що мають структуру формул І або II та фармацевтичних композицій, що містять сполуку формул І або II. Заявлений винахід також стосується способів лікування суб'єкту застосуванням терапевтично ефективної кількості сполуки формул І або II до суб'єкту. Заявлений винахід крім того стосується способів отримання сполук формул І або II та відповідних інтермедіатів. Гіпертензія вражає приблизно 20% популяції дорослих у розвинених країнах. У популяції дорослих віком 60 років або старше, цей відсоток збільшується до приблизно 60%-70%. Гіпертензія також є асоційованою зі збільшеним ризиком інших фізіологічних ускладнень, охоплюючи інсульт, інфаркт міокарду, мерехтіння передсердя, серцеву недостатність, хворобу периферійних судин та ниркову недостатність. Хоча ряд антигіпертензивних ліків є доступними у різних фармакологічних категоріях, ефективність та безпечність таких ліків може варіювати від пацієнта до пацієнта. Антагоністи мінералокортикоїдного рецептору є одним класом ліків, що можна застосовувати для лікування гіпертензії та/або пов'язаних фізіологічних ускладнень (Jewell, С. W., et al., Cardiovascular & Hematological Agents in Medicinal Chemistry (2006) Vol.4, pgs.129-153). Мінералокортикоїди, якто альдостерон, приймають участь у регуляції балансу солі та води у ссавців. Активація мінералокортикоїдного рецептору може збуджувати гіпертензію та викликати інші шкідливі серцево-судинні та фізіологічні ефекти. Два антагоністи мінералокортикоїдного рецептору, спіронолактон (ALDACTONE™) та еплеренон (INSPRA™), зараз доступні та показані для лікування гіпертензії та серцевої недостатності (Baxter, J. D., et al., Molecular та Cellular Endocrinology (2004) Vol.217, pgs.151-165). Ідентифікація додаткових сполук, що є антагоністами мінералокортикоїдного рецептору, є потрібною. Такі сполуки можна застосовувати для лікування суб'єктів, які потерпають від гіпертензії або сприйнятливі до неї та/або пов'язаних фізіологічних проблем, а крім того розширення меж варіантів лікування, доступного для таких суб'єктів. Спіронолактон та еплеренон мають стероїдну структуру. Заявлений винахід зокрема стосується антагоністів мінералокортикоїдного рецептору, що є нестероїдними сполуками. Застосування нестероїдного антагоністу мінералокортикоїдного рецептору потенційно дає деякі переваги над стероїдним антагоністом мінералокортикоїдного рецептору, охоплюючи, наприклад, подальше поліпшення селективності відносно рецепторів ста тевих гормонів; меншу складність та вартість хімічного синтезу; тощо. Про трициклічні піразоли повідомлено у літературі. Наприклад: WO 06/086358 (опубліковано Серпень 17, 2006) повідомляє про клас трициклічних піразолів, як інгібітори мітотичного кінезину. Про нестероїдні сполуки, корисні як антагоністи мінералокортикоїдного рецептору, повідомлено у літературі. Наприклад: WO 06/076202 (опубліковано Липень 20, 2006) повідомляє про клас імідазол-карбоксамідів як антагоністів мінералокортикоїдного рецептору. WO 06/012642 (опубліковано Лютий 2, 2006) повідомляє про клас пірол-карбоксамідів як антагоністів мінералокортикоїдного рецептору. WO 04/052847 (опубліковано Червень 24, 2004) повідомляє про клас дибензосуберанів як антагоністів мінералокортикоїдного рецептору. WO 05/066161 (опубліковано Липень 21, 2005) повідомляє про клас дибензосуберанів як антагоністів мінералокортикоїдного рецептору. WO 03/078394 (опубліковано Вересень 25, 2003) повідомляє про клас 3,3-бісарил-оксиндолів як антагоністів мінералокортикоїдного рецептору. WO 05/097118 (опубліковано Жовтень 20, 2005) повідомляє про клас 4-арил-1,4дигідропіридинів як антагоністів мінералокортикоїдного рецептору. WO 04/067529 (опубліковано Серпень 12, 2004) повідомляє про клас 3-бензил-індолів як антагоністів мінералокортикоїдного рецептору. WO 06/077821 (опубліковано Липень 27, 2006) повідомляє про класи бензоксазинтіонів та тетрагідрохінолінів як антагоністів мінералокортикоїдного рецептору. WO 06/010142 (опубліковано Січень 26, 2006) повідомляє про клас арил-бензоксазинонів/тіонів як антагоністів мінералокортикоїдного рецептору. В одному втіленні винахід стосується класу сполук, що мають структуру формули І: та їх фармацевтично прийнятні солі, де R1, R2, R , R3B, R4, R5, R6, R7, R8 та X є визначеними у детальному описі заявленого винаходу. У ще одному втіленні винахід стосується фармацевтичної композиції, що містить сполуку, що 3A 9 має структуру формули І, або її фармацевтично прийнятну сіль; та фармацевтично-прийнятний носі. У ще одному втіленні винахід стосується фармацевтичної композиції, що містить сполуку, що має структуру формули І, або її фармацевтично прийнятну сіль; одну або більше додаткових фармацевтично активних сполук; та фармацевтичноприйнятний носій. У ще одному втіленні винахід стосується способів лікування стану у суб'єкта застосуванням до суб'єкту терапевтично ефективної кількості сполуки, що має структуру формули І. Стани, що можна лікувати згідно з заявленим винаходом, охоплюють серцево-судинні стани (охоплюючи гіпертензію та серцеву недостатність), ниркові стани, стани печінки, стани судин, ретинопатію, невропатію (охоплюючи периферійну невропатію), інсулінопатію, набряк, ендотеліальну дисфункцію, барорецепторну дисфункцію, тощо. У ще одному втіленні винахід стосується способів лікування стану у суб'єкта застосуванням сполуки, що має структуру формули І у комбінації із ще одною фармацевтично активною сполукою. Стани, що можна лікувати згідно з заявленим винаходом, охоплюють серцево-судинні стани (охоплюючи гіпертензію та серцеву недостатність), ниркові стани, стани печінки, стани судин, ретинопатію, невропатію (охоплюючи периферійну невропатію), інсулінопатію, набряк, ендотеліальну дисфункцію, барорецепторну дисфункцію, тощо. У ще одному втіленні винахід стосується застосування сполук, що мають структуру формули І, або їх фармацевтично прийнятних солей для виробництва медикаменту для лікування стану у суб'єкта. Стани, що можна лікувати згідно з заявленим винаходом, охоплюють серцево-судинні стани (охоплюючи гіпертензію та серцеву недостатність), ниркові стани, стани печінки, стани судин, ретинопатію, невропатію (охоплюючи периферійну невропатію), інсулінопатію, набряк, ендотеліальну дисфункцію, барорецепторну дисфункцію, тощо. У ще одному втіленні винахід стосується способів отримання сполук, що має структуру формули І, або її фармацевтично прийнятної солі. У ще одному втіленні винахід стосується інтермедіатів, корисних при отриманні сполуки, що має структуру формули І, або її фармацевтично прийнятної солі. Цей детальний опис втілень призначено тільки для ознайомлення спеціалістів з винаходом, його принципами, та його практичним застосуванням так, щоб спеціалісти могли пристосовувати та застосовувати винаходи в їх численних формах, оскільки вони можуть бути найпідхожими для потреб певного застосування. Ці винаходи, тому, не є обмеженими втіленнями, описаними у цьому описі, та можуть бути різноманітно модифікованими. А. Скорочення та Визначення Як застосовувано стосовно 1Н ЯМР, символ "δ" стосується хімічного зсуву 1Н ЯМР. Як застосовувано стосовно 1Н ЯМР, скорочення "br" стосується широкий сигнал 1Н ЯМР. Як застосовувано стосовно 1Н ЯМР, скорочення "d" стосується дублету піку 1Н ЯМР. 92670 10 Як застосовувано стосовно 1Н ЯМР, скорочення "dd" стосується дублету дублетів піку 1Н ЯМР. Скорочення "МСВР" стосується масспектроскопії високого розділення (іонізація електророзпиленням, позитивне сканування). Скорочення "m/z" стосується піку мас-спектру. Як застосовувано стосовно 1Н ЯМР, скорочення "m" стосується мультиплету піку 1Н ЯМР. Як застосовувано стосовно 1Н ЯМР, скорочення "q" стосується квартету піку 1Н ЯМР. Як застосовувано стосовно 1Н ЯМР, скорочення "s" стосується синглету піку 1Н ЯМР. Як застосовувано стосовно 1Н ЯМР, скорочення "t" стосується триплету піку 1Н ЯМР Термін "алкіл" стосується насиченого вуглеводневого заміснику з нерозгалуженим або розгалуженим ланцюгом (тобто, заміснику з вмістом тільки карбону та гідрогену) з вмістом в одному втіленні приблизно від одного до приблизно дванадцяти атомів карбону; у ще одному втіленні приблизно від одного до приблизно дванадцяти атомів карбону; у ще одному втіленні приблизно від одного до приблизно десяти атомів карбону; у ще одному втіленні приблизно від одного до приблизно восьми атомів карбону; у ще одному втіленні приблизно від одного до приблизно шести атомів карбону; у ще одному втіленні приблизно від трьох до приблизно шести атомів карбону; у ще одному втіленні приблизно від одного до приблизно чотирьох атомів карбону; у ще одному втіленні приблизно від одного до приблизно трьох атомів карбону; та у ще одному втіленні приблизно від одного до приблизно двох атомів карбону. Приклади таких замісників охоплюють метил, етил, пропіл (охоплюючи н-пропіл та ізопропіл), бутил (охоплюючи н-бутил, ізобутил, втор-бутил та трет-бутил), пентил, ізоаміл, гексил тощо. Термін "алкеніл" стосується вуглеводневого заміснику з нерозгалуженим або розгалуженим ланцюгом з вмістом одного або більше подвійних зв'язків та приблизно від двох до приблизно дванадцяти атомів карбону; у ще одному втіленні приблизно від двох до приблизно дванадцяти атомів карбону; у ще одному втіленні приблизно від двох до приблизно шести атомів карбону; у ще одному втіленні приблизно від трьох до приблизно шести атомів карбону; та у ще одному втіленні приблизно від двох до приблизно чотирьох атомів карбону. Приклади алкенілу охоплюють етеніл (також відомий як вініл), аліл, пропеніл (охоплюючи 1-пропеніл та 2-пропеніл) та бутеніл (охоплюючи 1-бутеніл, 2-бутеніл та 3-бутеніл). Термін "алкеніл" охоплює замісники, що мають "цис" та "транс" орієнтацію, або альтернативно, "Е" та "Z" орієнтацію. Термін "бензил" стосується метилу, заміщеного фенілом. Термін "циклоалкіл" стосується насиченого карбоциклічного заміснику, що має від трьох до приблизно чотирнадцяти атомів карбону. У ще одному втіленні циклоалкіл замісник має від трьох до приблизно восьми атомів карбону. У ще одному втіленні циклоалкіл має від трьох до приблизно шести атомів карбону; у ще одному втіленні від трьох до приблизно чотирьох атомів карбону. Приклади 11 циклоалкілу охоплюють циклопропіл, циклобутил, циклопентил та циклогексил. Термін "арил" стосується карбоциклічної ароматичної системи з вмістом одного, двох або трьох кілець, де такі кільця можуть бути з’єднаними разом у підвішеному стані або можуть бути конденсованими. Термін "арил" стосується ароматичних замісників, як-то феніл, нафтил та антраценіл. Термін "арилалкіл" стосується алкілу, заміщеного арилом. У деяких випадках число атомів карбону у вуглеводневому заміснику (як-то, алкіл, алкеніл, алкініл, циклоалкіл, циклоалкеніл, арил, тощо.) є показаним префіксом "Сх-Су-,", де x є мінімальним, а у є максимальним число атомів карбону у заміснику. Тому, наприклад, "С1-С6-алкіл" стосується алкілу з вмістом від 1 до 6 атомів карбону. Крім того, С3-С6циклоалкіл стосується насиченого карбоциклілу з вмістом від 3 до 6 кільцевих атомів карбону. Терміни "гідрокси" та "гідроксил" стосуються ОН. Гідроксил можна застосовувати поодинці для позначення заміснику, як у "гідроксильній групі." При застосуванні у комбінації із ще одним терміном, префікс "гідрокси" означає, що замісник, до котрого префікс є приєднаним, є заміщеним один або більше гідроксилами. Сполуки, у котрих є один або більше гідроксилів, охоплюють, наприклад, спирти, еноли та фенол. Термін "гідроксіалкіл" стосується алкілу, що є заміщеним принаймні одним гідроксилом. Приклади гідроксіалкілу охоплюють гідроксиметил, гідроксіетил, гідроксипропіл та гідроксибутил. Термін "алкіламіно" стосується аміногрупи, де принаймні один алкіл-ланцюг є зв'язаним з амінонітрогеном замість атома гідрогену. Приклади алкіламінозамісників охоплюють моноалкіламіно, якто метиламіно (що представлено формулою NH(CH3)), та діалкіламіно, як-то диметиламіно, (що представлено формулою –N((СН3)2). Термін "амінокарбоніл" стосується -C(O)-NH2. Термін "галоген" стосується флуору, хлору, брому або йоду (що можна зображувати, як -І). В одному втіленні галогеном є хлор. У ще одному втіленні галогеном є флуор. Префікс "галоген" означає, що замісник, до котрого префікс приєднують, є заміщеним одним або більше незалежно вибраними галогенами. Наприклад, галогеналкіл стосується алкілу, що є заміщеним принаймні одним галогеном. Де більше одного гідрогену заміщено галогеном, заміщення можуть бути ідентичними або відмінними. Приклади галогеналкілів охоплюють хлорметил, дихлорметил, дифлуорхлорметил, дихлорфлуорметил, трихлорметил, 1-брометил, флуорметил, дифлуорметил, трифлуорметил, 2,2,2-трифлуоретил, дифлуоретил, пентафлуоретил, дифлуорпропіл, дихлорпропіл, та гептафлуорпропіл. Крім того, "галогеналкокси" стосується алкокси, що є заміщеним принаймні одним галогеном. Приклади галогеналкоксизамісників охоплюють хлорметокси, 1-брометокси, флуорметокси, дифлуорметокси, трифлуорметокси (також відомий, як "перфлуорметилокси"), та 2,2,2-трифлуоретокси. Слід розуміти, що якщо замісник є заміщеним більше, ніж 92670 12 одним галогеном, ці галогени можуть бути ідентичними або відмінними (якщо не вказане інше). Термін "оксо" стосується =0. Термін "окси" стосується етер-заміснику, та його можна зображувати, як -0-. Термін "алкокси" стосується алкілу, приєднаного до атому оксигену, котрий можна також репрезентувати, як -O-R, де R - алкіл. Приклади алкокси охоплюють метокси, етокси, пропокси та бутокси. Термін "алкілкарбоніл" стосується -С(О)алкілу. Наприклад, "етилкарбоніл". Приклади інших алкілкарбонілів охоплюють метилкарбоніл, пропілкарбоніл, бутилкарбоніл, пентилкарбоніл, та гексилкарбоніл. Термін "аміноалкілкарбоніл" стосується -С(О)алкіл-NН2. Наприклад, "амінометилкарбоніл". Термін "алкоксикарбоніл" стосується -С(О)-Оалкілу. Наприклад, "етоксикарбоніл". Приклади інших алкоксикарбонілів охоплюють метоксикарбоніл, етоксикарбоніл, пропоксикарбоніл, бутоксикарбоніл, пентоксикарбоніл, та гексилоксикарбоніл. У ще одному втіленні, де атом карбону карбонілу є приєднаним до атому карбону другого алкілу, утворена функціональна група є естером. Терміни "тіо" та "тіа" стосуються двовалентного атому сульфуру та такий замісник можна зображувати, як -S-. Наприклад, тіоетер репрезентує "алкіл-тіо-алкіл" або, альтернативно, алкіл-S-алкіл. Термін "тіол" стосується сульфгідрильного заміснику, та його можна зображувати, як-SH. Термін "сульфоніл" стосується -S(O)2-. Тому, наприклад, "алкіл-сульфоніл-алкіл" стосується алкіл-S(О)2-алкілу. Приклади алкілсульфонілів охоплюють метилсульфоніл, етилсульфоніл, та пропілсульфоніл. Термін "аміносульфоніл" стосується -S(O)2NH2 Термін "сульфініл" стосується -S(O)-. Тому, наприклад, "алкілсульфінілалкіл" або "алкілсульфоксидоалкіл" стосується алкіл-S(О)-алкілу. Зразкові алкілсульфініли охоплюють метилсульфініл, етилсульфініл, бутилсульфініл, та гексилсульфініл. Термін "спіросполука" стосується двох або трьох кілець, котрі мають тільки один спільний атом та два або три кільця не є приєднаними містком. Спільний кільцевий атом позначають, як спіроатом. Спіросполука може містити один або більше гетероатомів; така сполука стосується визначення гетероциклілу, дивись нижче. Термін "гетероцикліл" стосується насиченої, частково насиченої, або ненасиченої кільцевої структур з вмістом загалом 3-14 кільцевих атомів. Принаймні одним з кільцевих атомів є гетероатомом (як-то, оксиген, нітроген, або сульфур), а залишкові кільцеві атоми незалежно вибрані з групи: карбон, оксиген, нітроген та сульфур. Гетероцикліл може бути одиничним кільцем, котре звичайно містить від 3 до 7 кільцевих атомів, більш звичайно від 3 до 6 кільцевих атомів, та навіть більш звичайно від 5 до 6 кільцевих атомів. Приклади одинично-кільцевих гетероциклілів охоплюють, без обмеження, азетидиніл, фураніл, дигідрофураніл, тетрагідрофураніл, тіофураніл, дигі 13 дротіофураніл, тетрагідротіофураніл, піроліл, піролініл, піролідиніл, імідазоліл, імідазолініл, імідазолідиніл, піразоліл, піразолініл, піразолідиніл, триазоліл, тетразоліл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, тіазолініл, ізотіазолініл, тіазолідиніл, оксатіазоліл, оксадіазоліл, фуразаніл, оксатриазоліл (охоплюючи 1,2,3,4-оксатриазоліл або 1,2,3,5-оксатриазоліл), діоксазоліл (охоплюючи 1,2,3-діоксазоліл, 1,2,4-діоксазоліл, 1,3,2діоксазоліл, або 1,3,4-діоксазоліл), оксатіоланіл, піраніл (охоплюючи 1,2-піраніл або 1,4-піраніл), дигідропіраніл, піридиніл (також відомий як "піридил"), піперидиніл, піридазиніл, піримідиніл (також відомий як "піримідил"), піразиніл, піперазиніл, триазиніл, оксазиніл, оксазолідиніл, ізоксазолідиніл, оксатіазиніл, оксадіазиніл, морфолініл, азепініл, оксепініл, тієпініл, та діазепініл. Гетероцикліл може також містити 2 або 3 кільця, конденсовані разом, де принаймні одне таке кільце містить принаймні один гетероатом як кільцевий атом (наприклад, нітроген, оксиген, або сульфур). Приклади 2-конденсованих кільцевих гетероциклілів охоплюють, без обмеження, індолізиніл, 4Н-хінолізиніл, пуриніл, нафтиридиніл, птеридиніл, індоліл, ізоіндоліл, індолнініл, фталазиніл, хіноксалініл, хіназолініл, бензодіазиніл, бензопіраніл, бензотіопіраніл, бензоксазоліл, бензодіоксоліл, бензодіоксаніл, бензоксадіазоліл, бензофураніл, ізобензофураніл, бензотієніл, бензотіазоліл, бензотіадіазоліл, бензімідазоліл, бензотриазоліл, бензоксазиніл, тетрагідроізохінолініл, карбазоліл, ксантеніл, та акридиніл. Додаткові приклади конденсованих кільцевих гетероциклілів охоплюють тетрагідродіоксолопіроліл та тетрагідротриазолопіразиніл. Термін "гетероарил" стосується ароматичного гетероциклілу з вмістом від 5 до 14 кільцевих атомів. Гетероарил може бути одиничним кільцем або 2 або 3 конденсованими кільцями. Приклади гетероарилалкілів охоплюють 6-членні кільцеві замісники, як-то піридиніл (також відомий як "піридил"), піразил, піримідиніл (також відомий як "піримідил"), та піридазиніл; 5-членні кільцеві замісники, як-то триазоліл, імідазил, фураніл, тіофураніл, піразоліл, оксазоліл, ізоксазоліл, тіазоліл, оксадіазоліл та ізотіазоліл; 6/5-членні конденсовані кільцеві замісники, як-то бензотіофураніл, бензізоксазоліл, бензоксазоліл, та пуриніл; та 6/6-членні конденсовані кільця, як-то хінолініл, ізохінолініл, цинолініл, та хіназолініл. Термін "гетероциклілалкіл" стосується алкілу, заміщеного гетероциклілом. Термін "гетероциклоалкіл" стосується повністю насиченого гетероциклілу. Замісник є "здатним до заміщення" якщо він містить принаймні один карбон, сульфур, оксиген або нітроген, що є зв'язаним з одним або більше атомами гідрогену. Тому, наприклад, гідроген, галоген, та ціано не підпадають під це визначення. Якщо замісник є описаним як "заміщений," замісник є замість гідрогену на карбоні або нітрогені заміснику. Тому, наприклад, заміщений алкіл алкіл, де принаймні один замісник є замість гідрогену на алкілі. Для ілюстрації, монофлуоралкіл алкіл, заміщений флуором, та дифлуоралкіл - ал 92670 14 кіл, заміщений двома флуорами. Слід розуміти, що якщо є більше одного заміщення на заміснику, кожний замісник може бути ідентичним або відмінним (якщо не вказане інше). Якщо замісник є описаним як "необов'язково заміщений", замісник може бути (1) незаміщеним або (2) заміщеним. Якщо карбон заміснику є описаним як необов'язково заміщений одним або більше з перелічених замісників, один або більше гідрогенів на карбоні можуть окремо та/або разом бути заміщеними незалежно вибраним необов'язковим замісником. Якщо нітроген є описаний як необов'язково заміщений одним або більше з перелічених замісників, один або більше гідрогенів на нітрогені можуть бути заміщеними незалежно вибраним необов'язковим замісником. Цей опис застосовує терміни "замісник", "радикал", та "група" взаємозамінними. Якщо групу замісників описано разом як необов'язково заміщеними одним або більше з перелічених замісників, група може охоплювати: (1) нездатні до заміщення замісники, (2) здатні до заміщення замісники, що не є заміщеними необов'язковими замісниками, та/або (3) здатні до заміщення замісники, що є заміщеними одним або більше з необов'язкових замісників. Якщо замісник є описаним як необов'язково заміщений певним числом замісників, цей замісник може бути (1) незаміщеним; або (2) заміщеним певним числом замісників або максимальним числом на придатних до заміщення позиціях на заміснику. Тому, наприклад, якщо замісник є описаним як гетероарил, необов'язково заміщений замісниками числом до 3, тоді будь-як гетероарил з менше, ніж 3 здатними до заміщення позиціями може бути необов'язково заміщеним стількома замісниками, скільки гетероарил має здатних до заміщення позицій. Для ілюстрації, тетразоліл (котрий має тільки одну здатну до заміщення позицію) може бути необов'язково заміщеним одним замісником. Для ілюстрації крім того, якщо амінонітроген є описаним як необов'язково заміщений 2 замісниками, тоді нітроген може бути необов'язково заміщеним замісниками числом до 2, якщо амінонітроген є первинним нітрогеном, амінонітроген може бути необов'язково заміщеним тільки 1 замісником, якщо амінонітроген є вторинним нітрогеном. Префікс, приєднаний до багаточастинного заміснику стосується тільки першої частини. Для ілюстрації, термін "алкілциклоалкіл" містить дві частини: алкіл та циклоалкіл. Тому, префікс С1-С6на С1-С6-алкілциклоалкілі означає, що алкіл алкілциклоалкілу містить від 1 до 6 атомів карбону; С1С6- префікс не описує циклоалкіл. Для ілюстрації крім того, префікс "галоген" на галогеналкоксіалкілі означає, що тільки алкоксичастина алкоксіалкілу є заміщеною одним або більше галогенами. Якщо заміщення галогеном може альтернативно або додатково відбуватися на алкілі, замісник може бути описаним як "галоген-заміщений алкоксіалкіл" чи "галогеналкоксіалкіл." Та зрештою, якщо заміщення галогеном може відбуватися тільки на алкілі, замісник може бути описаним, як "алкоксигалогеналкіл." 15 Коли замісник складається з багатьох частин, якщо не вказане інше, він стосується кінцевої частини, як точки приєднання до залишку молекули. Наприклад, у заміснику А-В-С, частина С є приєднаною до залишку молекули. У заміснику AB-C-D, частина D є приєднаною до залишку молекули. Подібним чином у заміснику амінокарбонілметил метил є приєднаним до залишку молекули. У заміснику трифлуорметиламінокарбоніл, карбоніл є приєднаним до залишку молекули. Вставні слова можна застосовувати для опису заміснику, коли багато перших частин призначено для заміщення одиничної другої частини. У заміснику (гідроксиметил)(етил)піперидиніл, гідроксиметил та етил є безпосередньо приєднаними до піперидинілу. Альтернативно, якщо замісник не є здатним до заміщення, вставні слова не є необхідними. Наприклад, "флуорхлорметан" описує атом карбону зв'язаний безпосередньо з хлором, флуором, та двома атомами гідрогену. Якщо замісники є описаними, як "незалежно вибрані" з групи, кожний замісник є вибраним незалежно. Кожний замісник тому може бути ідентичним або відмінним від інших замісників. Термін "фармацевтично прийнятний носій" стосується носія, що є сумісним із іншими інгредієнтами композиції та не є шкідливим для суб'єкту. Такі носії можуть бути фармацевтично прийнятними матеріалом, композицією або середовищем, якто рідкий або твердий наповнювач, розріджувач, розчинник або інкапсулювальний матеріал, що приймає участь у переносі хімічного засобу. Краща композиція залежить від способу застосування. Термін "попередження" стосується попередження початку доклінічного стану або попередження початку доклінічної стадії стану у суб'єкта. Попередження охоплює, але без обмеження, профілактику суб'єкту при ризику розвитку стану. Термін "терапевтично ефективна кількість" стосується кількості ліків або фармацевтичного засобу, що виявлятиме біологічну або медичну реакцію тканини, системи або тварини, що досліджує дослідник або клініцист. Термін "лікування" охоплює пом'якшувальне, зміцнювальне та попереджувальне лікування суб'єкту. Термін "пом'якшувальне лікування" стосується лікування, що полегшує або зменшує ефект або інтенсивність стану у суб'єкта без лікування стану. Термін "попереджувальне лікування" (та відповідний термін "профілактика") стосується лікування, що попереджує появу стану у суб'єкта. Термін "зміцнювальне лікування" стосується лікування, що зупиняє прогресування, зменшує патологічні вияви, або повністю усуває стан у суб'єкта. В. Сполуки Заявлений винахід стосується класу сполук (охоплюючи фармацевтично прийнятні солі та таутомери сполук), де сполуки мають структуру формули І: 92670 16 де: X вибрано з групи: -СН2- та -О-; R1 вибрано з групи: алкіл, циклоалкіл, циклоалкеніл, феніл та гетероцикліл; де гетероциклілалкіл є 5- або 6-членним кільцевим гетероциклілом, що містить принаймні один кільцевий гетероатом, вибраний з оксигену, сульфуру та нітрогену; та де алкіл, циклоалкіл, циклоалкеніл, феніл та гетероциклілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: гідрокси, галоген, алкіл, та галогеналкіл; R2 вибрано з групи: гідроген та алкіл; R3A та R3B є незалежно вибраними з групи гідроген та алкіл; R4, R6, та R7 є незалежно вибраними з групи гідроген, галоген, гідрокси, алкіл, галогеналкіл, гідроксіалкіл, та алкокси; R5 вибрано з групи: гідроген, -(CH2)mOR50, (CH2)mC(O)R50, -(CH2)mC(O)OR50, . (CH2)mC(O)NR51R52, -(CH2)mNR51R52, (CH2)mN(R51)C(O)R52, та -(CH2)mS(O)nR50; m=0, 1, 2, 3, 4, 5, або 6; n=0, 1, або 2; R50 вибрано з групи: гідроген та алкіл; R51 та R52 є незалежно вибраними з групи: гідроген та алкіл; або R51 та R52 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6-членний кільцевий гетероцикліл; де R50, R51 та R52 алкіли та R51/R52 гетероциклілалкіл можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: галоген, піролідиніл, -OR53, -C(O)R53, -C(O)OR53, C(O)NR54R55, -NR54R55, -N(R56)C(O)R53; -S(O)pR53, та -S(O)pNR54R55; p=0, 1, або 2; R53 вибрано з групи: гідроген, алкіл, галогеналкіл, гідроксіалкіл, та карбоксіалкіл; R54 та R55 є незалежно вибраними з групи: гідроген, алкіл, галогеналкіл, гідроксіалкіл, та карбоксіалкіл; або R54 та R55 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6членний кільцевий гетероцикліл; R56 вибрано з групи: гідроген та алкіл; та R8 вибрано з групи: феніл, піридиніл та піримідиніл; де феніл, піридиніл та піримідинілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, алкіл, галогеналкіл, ціаноалкіл, гідроксіалкіл, карбоксіалкіл, алкокси, галогеналкокси, ціаноалкокси, аміно, алкіламіно, діалкіламіно, та алкоксикарбоніл. В одному втіленні сполуки формули І R3A, R3B, 4 R , R6 та R7, кожний, - гідроген. У ще одному втіленні R2, R3A, R3B, R4, R6 та R7, кожний, - гідроген. 17 У ще одному втіленні X - -СН2-; та R2, R3A, R3B, R4, R6 та R7, кожний, - гідроген. У ще одному втіленні X - -О-; та R2, R3A, R3B, R4, R6 та R7, кожний, - гідроген. 2 У ще одному втіленні сполуки формули І R , 3A 3B 4 6 7 1 R , R , R , R та R , кожний, -гідроген; та R вибрано з групи: циклоалкіл та феніл; де R1 циклоалкіл та фенілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, алкіл, та галогеналкіл. У ще одному втіленні сполуки формули І R2, 3A R , R3B, R4, R6 та R7, кожний, -гідроген; та R8 феніл; де R8 фенілалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, алкіл, галогеналкіл, ціаноалкіл, гідроксіалкіл, карбоксіалкіл, алкокси, галогеналкокси, ціаноалкокси, аміно, алкіламіно, діалкіламіно, та алкоксикарбоніл. У ще одному втіленні R8 фенілалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, та алкіл. У ще одному втіленні сполуки формули І R2, 3A R , R3B, R4, R6 та R7, кожний, - гідроген; та R8 піридиніл; де R8 піридинілалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, алкіл, галогеналкіл, ціаноалкіл, гідроксіалкіл, карбоксіалкіл, алкокси, галогеналкокси, ціаноалкокси, аміно, алкіламіно, діалкіламіно 8 та алкоксикарбоніл. У ще одному втіленні R піридинілалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, та алкіл. У ще одному втіленні сполуки формули І R2, 3A R , R3B, R4, R6 та R7, кожний, -гідроген, та R5 вибрано з групи: -(CH2)mOR50, -(CH2)mC(O)OR50, та (CH2)mC(O)NR51R52; де m=0, 1, 2, 3, 4, 5, або 6; R50 вибрано з групи: гідроген та алкіл; R51 та R52 є незалежно вибраними з групи: гідроген та алкіл; або R51 та R52 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6-членний кільцевий гетероцикліл; де R50, R51 та R52 алкіли та R51/R52 гетероциклілалкіли можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: галоген, піролідиніл, -OR53, -C(O)R53, -C(O)OR53, -C(O)NR54R55, NR54R55, -N(R56)C(O)R53; -S(O)pR53 та S(O)pNR54R55; p=0, 1 або 2; R53 вибрано з групи: гідроген, алкіл, галогеналкіл, гідроксіалкіл, та карбоксіалкіл; R54 та R55 є незалежно вибраними з групи: гідроген, алкіл, галогеналкіл, гідроксіалкіл, та карбоксіалкіл; або R54 та R55 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5або 6-членний кільцевий гетероцикліл; та R56 вибрано з групи: гідроген та алкіл. У ще одному втіленні R5 - -(CH2)mC(O)OR50; m=0; та R50 вибрано з групи: гідроген та алкіл. У ще одному втіленні R5 - (CH2)mC(O)OR50; m=0; та R50 - гідроген. У ще одному втіленні сполуки формули І R2, 3A R , R3B, R4, R6 та R7, кожний, -гідроген; R1 вибрано з групи: (С3-С7)-циклоалкіл та феніл; де замісники R1 (С3-С7)-циклоалкіл та фенілалкіл можуть бути необов'язково заміщеними одним або більше за 92670 18 місниками, незалежно вибраними з групи: галоген, (С1-C6)-алкіл, та галоген-(С1-C6)-алкіл; R5 вибрано з групи: -(CH2)mOR50, -(CH2)mC(O)OR50, та (CH2)mC(O)NR51R52; де m=0, 1, 2, 3, 4, 5, або 6; R50 51 вибрано з групи: гідроген та (С1-C6)-алкіл; R та 52 R є незалежно вибраними з групи: гідроген та (С1-C6)-алкіл; або R51 та R52 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6членний кільцевий гетероцикліл; де R50, R51 та R52 (С1-С6)-алкіли та R51/R52 гетероцикліл ал кіл и можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: галоген, піролідиніл, -OR53, -C(O)R53, C(O)OR53, -C(O)NR54R55, -NR54R55, -N(R56)C(O)R53; S(O)pR53, та -S(O)pNR54R55; p=0, 1 або 2; R53 вибрано з групи: гідроген, (С1-C6)-алкіл, галоген-(С1C6)-алкіл, гідрокси-(С1-С6)-алкіл, та карбокси-(С1C6)-алкіл; R54 та R55 є незалежно вибраними з групи: гідроген, (С1-C6-алкіл, галоген(С1-C6)-алкіл, гідрокси-(С1-C6)-алкіл, та карбокси-(С1-C6)-алкіл; або R54 та R55 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6-членний кільцевий гетероцикліл; та R56 вибрано з групи: гідроген та (С1-C6)-алкіл; та R8 вибрано з групи: феніл та піридиніл; де замісники R8 феніл та піридинілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-C6)алкіл, галоген-(С1-С6)-алкіл, ціано-(С1-C6)-алкіл, гідрокси-(С1-С6)-алкіл, карбокси-(С1-C6)-алкіл, (С1C6)-алкокси, галоген-(С1-С6)-алкокси, ціано-(С1-С6)алкокси, аміно, (С1-C6)-алкіламіно, ді-(С1-С6)алкіламіно, та -(С1-С6)-алкоксикарбоніл. У ще одному втіленні X - -СН2-. У ще одному втіленні X - О-. У ще одному втіленні сполуки формули І R2, 3A R , R3B, R4, R6 та R7, кожний, -гідроген; R1 - (С3С7)-циклоалкіл; де R1 (С3-С7)-Циклоалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: гало5 ген, (С1-C6)-алкіл, та галоген-(С1-C6)-алкіл; R виб50 50 рано з групи: -(CH2)mOR , -(CH2)mC(O)OR , та (CH2)mC(O)NR51R52; де m=0, 1, 2, 3, 4, 5, або 6; R50 вибрано з групи: гідроген та (С1-C6)-алкіл; R51 та R52 є незалежно вибраними з групи: гідроген та (С1-C6)-алкіл; або R51 та R52 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6членний кільцевий гетероцикліл; де R50, R51 та R52 (С1-C6)-алкіли та R61/R52 гетероциклілалкіли можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: галоген, піролідиніл, -OR53, -C(O)R53, C(O)OR53, -C(O)NR54R55, -NR54R55, -N(R56)C(O)R53; S(O)PR53, та -S(O)pNR54R55; p=0, 1 або 2; R53 вибрано з групи: гідроген, (С1-C6)-алкіл, галоген-(С1C6)-алкіл, гідрокси-(С1-C6)-алкіл, та карбокси-(С1C6)-алкіл; R54 та R55 є незалежно вибраними з групи: гідроген, (С1-C6)-алкіл, галоген-(С1-C6)-алкіл, гідрокси-(С1-C6)-алкіл, та карбокси-(С1-C6)-алкіл; або R54 та R55 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6-членний кільцевий гетероцикліл; та R56 вибрано з групи: гідроген та (С1-C6)-алкіл; та R8 вибрано з групи: феніл та піридиніл; де R8 феніл та піридинілалкіл можуть бути необов'язково заміщеними одним або більше 19 замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-C6)-алкіл, галоген-(С1-C6)-алкіл, ціано-(С1-С6)-алкіл, гідрокси-(С1С6)-алкіл, карбокси-(С1-C6)-алкіл, (С1-C6)-алкокси, галоген-(С1-С6)-алкокси, ціано-(С1-С6)-алкокси, аміно, (С1-С6)-алкіламіно, ді-(С1-С6)-алкіламіно, та -(С1-C6)-алкоксикарбоніл. У ще одному втіленні X -СН2-. У ще одному втіленні X - -О-. У ще одному втіленні R1 вибрано з групи: циклогексил, циклопентил, циклобутил та циклопропіл. У ще одному втіленні R1 - циклопентил. У ще одному втіленні сполуки формули І R2, 3A R , R3B, R4, R6 та R7, кожний, - гідроген; R1 - феніл; де R1 феніл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-С6)-алкіл, та галоген-(С1-С6)-алкіл; R5 вибрано з групи: -(CH2)mOR50, -(CH2)mC(O)OR50, та -(CH2)mC(O)NR51R52; де m=0, 1, 2, 3, 4, 5, або 6; R50 вибрано з групи: гідроген та (С1-C6)-алкіл; R51 та R52 є незалежно вибраними з групи: гідроген та (С1-C6)-алкіл; або R51 та R52 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6-членний кільцевий гетероцикліл; де R50, R51 та R52 (С1-C6)-алкіли та R51/R52 гетероциклілалкіли можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: галоген, піролідиніл, -OR53, -C(O)R53, -C(O)OR53, -C(O)NR54R55, NR54R55, -N(R56)C(O)R53; -S(O)pR53, та 54 55 S(O)pNR R ; p=0, 1 або 2; R53 вибрано з групи: гідроген, (С1-C6)-алкіл, галоген-(С1-С6)-алкіл, гідрокси-(С1-С6)-алкіл, та карбокси-(С1-C6)-алкіл; R54 та R55 є незалежно вибраними з групи: гідроген, (С1-С6)-алкіл, галоген-(С1-C6)-алкіл, гідрокси-(С1-C6)-алкіл, та карбокси-(С1-C6)-алкіл; або R54 та R55 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6-членний кільцевий гетероцикліл; та R56 вибрано з групи: гідроген та (С1-C6)-алкіл; та R8 вибрано з групи: феніл та піридиніл; де R8 феніл та піридинілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-C6)-алкіл, галоген(С1-C6)-алкіл, ціано-(С1-C6)-алкіл, гідрокси-(С1-С6)алкіл, карбокси-(С1-C6)-алкіл, (С1-C6)-алкокси, галоген-(С1-C6)-алкокси, ціано-(С1-C6)-алкокси, аміно, (С1-C6)-алкіламіно, ді-(С1-C6)-алкіламіно, та (С1-C6)-алкоксикарбоніл. У ще одному втіленні R1 фенілалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-C6)-алкіл та галоген-(С1С6)-алкіл. У ще одному втіленні R1 фенілалкіл є заміщеним одним або більше галогенами. У ще одному втіленні R1 фенілалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: хлор та флуор. У ще одному втіленні R1 фенілалкіл є заміщеним одним або більше флуорами. У ще одному втіленні сполуки формули І R2, R3A, R3B, R4, R6 та R7, кожний, -гідроген; R1 вибрано з групи: (С3-С7)-циклоалкіл та феніл; де R1 (С3-С7)циклоалкіл та фенілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-С6)алкіл, та галоген-(С1-С6)-алкіл; R5 вибрано з групи: 92670 20 -(CH2)mOR5t), -(CH2)mC(O)OR50, та (CH2)mC(O)NR51R52; де m=0, 1, 2, З, 4, 5, або 6; R50 вибрано з групи: гідроген та (С1-С6)-алкіл; R51 та R52 є незалежно вибраними з групи: гідроген та 51 52 (С1-С6)-алкіл; або R та R разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або бчленний кільцевий гетероцикліл; де R50, R51 та R52 (С1-C6)-алкіли та R51/R52 гетероциклілалкіли можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: галоген, піролідиніл, -OR53, -C(O)R53, C(O)OR53, -C(O)NR54R55, -NR54R55, -N(R56)C(O)R53; S(O)pR53, та -S(O)pNR54R55; p=0, 1 або 2; R53 вибрано з групи: гідроген, (С1-С6)-алкіл, галоген-(С1C6)-алкіл, гідрокси-(С1-С6)-алкіл, та карбокси-(С1C6)-алкіл; R54 та R55 є незалежно вибраними з групи: гідроген, (С1-С6)-алкіл, галоген-(С1-С6)-алкіл, гідрокси-(С1-C6)-алкіл, та карбокси-(С1-C6)-алкіл; або R54 та R55 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6-членний кільцевий гетероцикліл; та R56 вибрано з групи: гідроген та (С1-С6)-алкіл; та R8 - феніл; де R8 фенілалкіл є заміщеним одним або більше ціанозамісниками та, необов'язково, може бути крім того заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, гідрокси, карбокси, (С1-C6)-алкіл, галоген-(С1-C6)-алкіл, ціано-(С1-С6)-алкіл, гідрокси-(С1-C6)-алкіл, карбокси-(С1-C6)-алкіл, (С1-С6)-алкокси, галоген-(С1-С6)алкокси, ціано-(С1-С6)-алкокси, аміно, (С1-C6)алкіламіно, ді-(С1-С6)-алкіламіно, та (С1-C6)8 алкоксикарбоніл. У ще одному втіленні R фенілалкіл є заміщеним одним або більше ціанозамісниками та, необов'язково, може бути крім того заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-C6)-алкіл та (С1C6)-алкокси. У ще одному втіленні R8 фенілалкіл є заміщеним одним або більше ціанозамісниками та, необов'язково, може бути крім того заміщеним одним або більше галогенами. У ще одному вті8 ленні R фенілалкіл є заміщеним одним або більше ціанозамісниками та, необов'язково, може бути крім того заміщеним одним або більше замісниками, незалежно вибраними з групи: хлор та флуор. У ще одному втіленні R8 фенілалкіл є заміщеним одним або більше ціанозамісниками та, необов'язково, може бути крім того заміщеним одним або більше хлорами. У ще одному втіленні R8 фенілалкіл є заміщеним одним або більше ціанозамісниками та, необов'язково, може бути крім того заміщеним одним або більше (С1-С6)-алкілами. У ще одному втіленні R8 фенілалкіл є заміщеним одним або більше ціанозамісниками та, необов'язково, може бути крім того заміщеним одним або більше (С1-C4)-алкілами. У ще одному втіленні R8 фенілалкіл є заміщеним одним або більше ціанозамісниками та, необов'язково, може бути крім того заміщеним одним або більше метилалкілами. У ще одному втіленні сполуки формули І R2, R3A, R3B, R4, R6 та R7, кожний, - гідроген; R1 вибрано з групи: (С3-С7)-циклоалкіл та феніл; де R1 (С3С7)-циклоалкіл та фенілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, (С1С6)-алкіл, та галоген-(С1-С6)-алкіл; R5 - 21 (CH2)mC(O)OR50 де m=0, 1, 2, 3, 4, 5, або 6; R50 вибрано з групи: гідроген та (С1-C6)-алкіл; де R50 (С1-С6)-алкіл може бути незалежно та необов'язково заміщеним одним або більше замісниками, 53 53 53 вибраними з групи: -OR , -C(O)R , -C(O)OR , 54 55 54 55 56 53 C(O)NR R , -NR R , -N(R )C(O)R ; -S(O)pR53, та -S(O)pNR54R55; p=0, 1 або 2; R53 вибрано з групи: гідроген, (С1-C6)-алкіл, галоген-(С1-C6)-алкіл, гідрокси-(С1-C6)-алкіл, та карбокси-(С1-C6)-алкіл; R54 та R55 є незалежно вибраними з групи: гідроген, (С1С6)-алкіл, галоген-(С1-C6)-алкіл, гідрокси-(С1-С6)алкіл, та карбокси-(С1-C6)-алкіл; або R54 та R55 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6-членний кільцевий гетероцикліл; та R56 вибрано з групи: гідроген та (С1-C6)алкіл; та R8 вибрано з групи: феніл та піридиніл; де R8 феніл та піридинілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-C6)-алкіл, галоген-(С1С6)-алкіл, ціано-(С1-С6)-алкіл, гідрокси-(С1-C6)алкіл, карбокси-(С1-С6)-алкіл, (С1-C6)-алкокси, галоген-(С1-C6)-алкокси, ціано-(С1-C6)-алкокси, аміно, (С1-C6)-алкіламіно, ді-(С1-С6)-алкіламіно, та (С1-C6)-алкоксикарбоніл. У ще одному втіленні m=0. У ще одному втіленні R50 - гідроген. У ще одному втіленні m=0, та R50 - гідроген. У ще одному втіленні сполуки формули І R2, 3A R , R3B, R4, R6 та R7, кожний, -гідроген; R1 вибрано з групи: (С3-С7)-циклоалкіл та феніл; де R1 (С3-С7)циклоалкіл та фенілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-C6)алкіл, та галоген-(С1-C6)-алкіл; R5 51 52 (CH2)mC(O)NR R ; де m=0, 1, 2, 3, 4, 5, або 6; R51 та R52 є незалежно вибраними з групи: гідроген та (С1-C6)-алкіл; або R51 та R52 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або бчленний кільцевий гетероцикліл; де R51 та R52 (С1C6)-алкіли та R51/R52 гетероциклілалкіли можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: галоген, піролідиніл, -OR53, -C(O)R53, -C(O)OR53, C(O)NR54R55, -NR54R55, -N(R56)C(O)R53; -S(O)pR53, та -S(O)pNR54R55; p=0, 1 або 2; R53 вибрано з групи: гідроген, (С1-С6)-алкіл, галоген-(С1-C6)-алкіл, гідрокси-(С1-C6)-алкіл, та карбокси-(С1-C6)-алкіл; R54 та R55 є незалежно вибраними з групи: гідроген, (С1C6)-алкіл, галоген-(С1-С6)-алкіл, гідрокси-(С1-С6)алкіл, та карбокси-(С1-С6)-алкіл; або R54 та R55 разом з нітрогеном, до котрого вони є приєднаними, утворюють 5- або 6-членний кільцевий гетероцикліл; та R56 вибрано з групи: гідроген та (С1-С6)алкіл; та R8 вибрано з групи: феніл та піридиніл; де R8 феніл та піридинілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-С6)-алкіл, галоген-(С1C6)-алкіл, ціано-(С1-С6)-алкіл, гідрокси-(С1-С6)алкіл, карбокси-(С1-C6)-алкіл, (С1-C6)-алкокси, галоген-(С1-C6)-алкокси, ціано-(С1-С6)-алкокси, аміно, (С1-С6)-алкіламіно, ді-(С1-C6)-алкіламіно, та (С1-С6)-алкоксикарбоніл. У ще одному втіленні m=0. У ще одному втіленні R50 - гідроген. У ще одному втіленні m=0; та R51 та R52 є незалежно 92670 22 вибраними з групи: гідроген та (С1-С6)-алкіл. У ще одному втіленні m=0; та R51 та R52 є незалежно вибраними з групи: гідроген та (С1-C6)-алкіл; де R51 та R52 (С1-C6)-алкіли можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: -OR53 та -S(O)PR53; p=0, 1 або 2; та R53 вибрано з групи: гідроген та (С1-C6)-алкіл. У ще одному втіленні сполуки формули І R2, R3A, R3B, R4, R6 та R7, кожний, -гідроген; R1 вибрано з групи: циклопентил, циклобутил та феніл; де R1 циклопентил, циклобутил та фенілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-С6)-алкіл, та галоген-(С1-C6)алкіл; R5 вибрано з групи: -(CH2)mOR50, (CH2)mC(O)OR50, та -(CH2)mC(O)NR51R52; де m=0, 1,2, або 3; R50 вибрано з групи: гідроген та (С1-C6)апкіл; R51 та R52 є незалежно вибраними з групи: гідроген та (С1-С6)-алкіл; де R50, R51 та R52 (С1-С6)алкіли можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: галоген, -OR53, -C(O)R53, C(O)OR53, -C(O)NR54R55, -NR54R55, -N(R56)C(O)R53; S(O)pR53, та -S(O)pNR54R55; p=0, 1 або 2; R53 вибрано з групи: гідроген, (С1-C6)-алкіл, галоген-(С1C6)-алкіл, гідрокси-(С1-С6)-алкіл, та карбокси-(С1C6)-алкіл; R54 та R55 є незалежно вибраними з групи: гідроген, (С1-C6)-алкіл, галоген-(С1-C6)-алкіл, гідрокси-(С1-С6)-алкіл, та карбокси-(С1-C6)-алкіл; та R56 вибрано з групи: гідроген та (С1-C6)-алкіл; та R8 вибрано з групи: феніл та піридиніл; де R8 феніл та піридинілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-С6)-алкіл, галоген-(С1-C6)-алкіл, ціано-(С1-C6)-алкіл, гідрокси-(С1-С6)-алкіл, карбокси(С1-С6)-алкіл, (С1-C6)-алкокси, галоген-(С1-C6)алкокси, ціано-(С1-C6)-алкокси, аміно, (С1-С6)алкіламіно, ді-(С1-C6)-алкіламіно, та -(С1-C6)алкоксикарбоніл. У ще одному втіленні X - -СН2-. У ще одному втіленні X - -О-. У ще одному втіленні сполуки формули І R2, R3A, R3B, R4, R6 та R7, кожний, - гідроген; R1 вибрано з групи: циклопентил, циклобутил та феніл; де R1 циклопентил, циклобутил та фенілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-C6)-алкіл, та галоген-(С1-C6)-алкіл; R5 вибрано з групи: -(CH2)mOR50, -(CH2)mC(O)OR50, та (CH2)mC(O)NR51R52; де m=0, 1, 2, або 3; R50 вибрано з групи: гідроген та (С1-C6)-алкіл; R51 та R52 є незалежно вибраними з групи: гідроген та (С1-C6)алкіл; де R50, R51 та R52 (С1-C6)-алкіли можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: галоген, -OR53, -C(O)R53, -C(O)OR53, -C(O)NR54R55, NR54R55, -N(R56)C(O)R53; -S(O)pR53, та 54 55 S(O)pNR R ; p=0, 1 або 2; R53 вибрано з групи: гідроген, (С1-C6)-алкіл, галоген-(С1-C6)-алкіл, гідрокси-(С1-C6)-алкіл, та карбокси-(С1-C6)-алкіл; R54 та R55 є незалежно вибраними з групи: гідроген, (С1C6)-алкіл, галоген-(С1-C6)-алкіл, гідрокси-(С1-C6)алкіл, та карбокси-(С1-C6)-алкіл; та R56 вибрано з групи: гідроген та (С1-C6)-алкіл; та R8 вибрано з групи: феніл та піридиніл; де R8 феніл та піридині 23 лалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-C6)-алкіл, галоген-(С1-С6)-алкіл, ціано-(С1-C6)алкіл, гідрокси-(С1-С6)-алкіл, карбокси-(С1-C6)алкіл, (С1-C6)-алкокси, галоген-(С1-C6)-алкокси, ціано-(С1-C6)-алкокси, аміно, (С1-C6)-алкіламіно, ді(С1-C6)-алкіламіно, та -(С1-С6)-алкоксикарбоніл. У ще одному втіленні X - -СН2-. У ще одному втіленні X - -О-. У ще одному втіленні R1 - циклопентил; де R1 циклопентилалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-С4)-алкіл, та галоген-(С1-С4)-алкіл. У ще одному втіленні R1 феніл; де R1 феніл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-С4)-алкіл, та галоген-(С1-С4)-алкіл. У ще одному втіленні R5 - (CH2)mC(O)OR50; m=0; та R50 вибрано з групи: гідроген та алкіл. У ще одному втіленні R5 - (CH2)mC(O)OR50; m=0; та R50 - гідроген. У ще одному втіленні R8 - феніл; де R8 фенілалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-C6)-алкіл, галоген-(С1-C6)-алкіл, ціано-(С1-С6)-алкіл, гідрокси-(С1C6)-алкіл, карбокси-(С1-C6)-алкіл, (С1-C6)-алкокси, галоген-(С1-C6)-алкокси, ціано-(С1-C6)-алкокси, аміно, (С1-C6)-алкіламіно, ді-(С1-С6)-алкіламіно, та -(С1-C6)-алкоксикарбоніл. У ще одному втіленні R8 - піридиніл; де R8 піридинілалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-C6)-алкіл, галоген-(С1-C6)алкіл, ціано-(С1-C6)-алкіл, гідрокси-(С1-С6)-алкіл, карбокси-(С1-C6)-алкіл, (С1-C6)-алкокси, галоген(С1-C6)-алкокси, ціано-(С1-C6)-алкокси, аміно, (С1C6)-алкіламіно, ді-(С1-C6)-алкіламіно, та -(С1-C6)алкоксикарбоніл. У ще одному втіленні сполуки формули І R2, 3A 3B 4 6 7 1 R , R , R , R та R , кожний, -гідроген; R вибрано з групи: циклопентил, циклобутил та феніл; де R1 циклопентил, циклобутил та фенілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-C6)-алкіл, та галоген-(С1-C6)-алкіл; R5 - (CH2)mC(O)OR50; де m=0, 1,2, або 3; R50 вибрано з групи: гідроген та (С1-C6)-алкіл; де R50 (С1-C6)-алкіл може бути незалежно та необов'язково заміщеним одним або більше замісниками, вибраними з групи: галоген, -OR53, -C(O)R53, -C(O)OR53, C(O)NR54R55, -NR54R55, -N(R56)C(O)R53; -S(O)pR53, та -S(O)pNR54R55; p=0, 1 або 2; R53 вибрано з групи: гідроген, (С1-C6)-алкіл, галоген-(С1-C6)-алкіл, гідрокси-(С1-С6)-алкіл, та карбокси-(С1-C6)-алкіл; R54 та R55 є незалежно вибраними з групи: гідроген, (С1C6)-алкіл, галоген-(С1-C6)-алкіл, гідрокси-(С1-С6)алкіл, та карбокси-(С1-С6)-алкіл; та R56 вибрано з групи: гідроген та (С1-С6)-алкіл; та R8 вибрано з групи: феніл та піридиніл; де R8 феніл та піридинілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-С6)-алкіл, галоген-(С1-C6)-алкіл, ціано-(С1-C6)алкіл, гідрокси-(С1-C6)-алкіл, карбокси-(С1-C6) 92670 24 алкіл, (С1-C6)-алкокси, галоген-(С1-C6)-алкокси, ціано-(С1-С6)-алкокси, аміно, (С1-C6)-алкіламіно, та ді-(С1-С6)-алкіламіно. У ще одному втіленні X - СН2-. У ще одному втіленні X - -О-. У ще одному 1 1 втіленні R - циклопентил; де R циклопентилалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-С4)-алкіл, та галоген-(С1-C4)-алкіл. у ще одному втіленні R1 - феніл; де R1 феніл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-С4)-алкіл, та галоген-(С1-С4)-алкіл. У ще одному втіленні R5 - (CH2)mC(O)OR50; m=0; та R50 вибрано з групи: гідроген та (С1-C6)-алкіл. У ще одному втіленні R5 - -(CH2)mC(O)OR50; m=0; та R50 гідроген. У ще одному втіленні R8 - феніл; де R8 фенілалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-C6)-алкіл, галоген-(С1-C6)-алкіл, ціано-(С1-C6)алкіл, гідрокси-(С1-C6)-алкіл, карбокси-(С1-C6)алкіл, (С1-C6)-алкокси, галоген-(С1-C6)-алкокси, ціано-(С1-C6)-алкокси, аміно, (С1-С6)-алкіламіно та ді-(С1-C6)-алкіламіно. У ще одному втіленні R8 піридиніл; де R8 піридинілалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-C6)-алкіл, галоген-(С1-C6)алкіл, ціано-(С1-C6)-алкіл, гідрокси-(С1-C6)-алкіл, карбокси-(С1-C6)-алкіл, (С1-С6)-алкокси, галоген(С1-C6)-алкокси, ціано-(С1-C6)-алкокси, аміно, (С1C6)-алкіламіно та ді-(С1-C6)-алкіламіно. У ще одному втіленні сполуки формули І R2, 3A R , R3B, R4, R6 та R7, кожний, - гідроген; R1 вибрано з групи: циклопентил, циклобутил та феніл; де R1 циклопентил, циклобутил та фенілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-С4)-алкіл, та галоген-(С1-С4)-алкіл; R5 - (CH2)mC(O)OR50; де m=0, 1, або 2; R50 вибрано з 50 групи: гідроген та (С1-C4)-алкіл; де R (С1-C4)-алкіл може бути незалежно та необов'язково заміщеним одним або більше замісниками, вибраними з групи: галоген, -OR53, -C(O)R53, та -C(O)OR53; R53 вибрано з групи: гідроген та (С1-С4)-алкіл; та R8 вибрано з групи: феніл та піридиніл; де R8 феніл та піридинілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-С4)-алкіл, галоген-(С1-С4)-алкіл, ціано-(С1C4)-алкіл, гідрокси-(С1-С4)-алкіл, та карбокси-(С1С4)-алкіл. У ще одному втіленні X - -СН2-. У ще одному втіленні X - -О-. У ще одному втіленні R1 циклопентил; де R1 циклопентилалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, (С1-С4)-алкіл, та галоген-(С1-С4)-алкіл. У ще одному втіленні R1 - феніл; де R1 феніл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, (С1C4)-алкіл, та галоген-(С1-С4)-алкіл. У ще одному втіленні R5 - -(CH2)mC(O)OR50; m=0; та R50 вибрано з групи: гідроген та (С1-C4)-алкіл. У ще одному втіленні R5 - -(CH2)mC(O)OR50; m=0; та R50 - гідроген. У ще одному втіленні R8 - феніл; де R8 фенілалкіл 25 може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-С4)алкіл, галоген-(С1-С4)-алкіл, ціано-(С1-С4)-алкіл, гідрокси-(С1-С4)-алкіл та карбокси-(С1-C4)-алкіл. У ще одному втіленні R8 - піридиніл; де R8 піридинілалкіл може бути необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: галоген, ціано, гідрокси, карбокси, (С1-С4)алкіл, галоген-(С1-С4)-алкіл, ціано-(С1-С4)-алкіл, гідрокси-(С1-С4)-алкіл та карбокси-(С1-С4)-алкіл. Заявлений винахід також стосується підкласу сполук (охоплюючи фармацевтично прийнятні солі та таутомери сполук), де сполуки мають структуру формули II: де: X вибрано з групи: -СН2- та -О-; Ζ вибрано з групи: -C(R81)- та -N-; R1 вибрано з групи: циклопентил, циклобутил та феніл; де R1 циклопентил, циклобутил та фенілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: хлор, флуор, метил, етил, пропіл, хлорметил, дихлорметил, трихлорметил, флуорметил, дифлуорметил та трифлуорметил, R2 вибрано з групи: гідроген або (С1-С4)-алкіл; R5 вибрано з групи. -(CH2)mOR50, 50 (CH2)mC(O)OR , та -(CH2)mC(O)NR51R52; де: m=0, 1,2, або 3; R50 вибрано з групи: гідроген та (С1-С6)-алкіл; R51 та R52 є незалежно вибраними з групи: гідроген та (С1-С6)-алкіл; де R50, R51 та R52 (С1-С6)алкіли можуть бути незалежно та необов'язково заміщеними одним або більше замісниками, вибраними з групи: галоген, -OR53, -C(O)R53, C(O)OR53, -C(O)NR54R55, -NR54R55, -N(R56)C(O)R53; S(O)PR53, та -S(O)PNR54R55; p=0, 1 або 2; R53 вибрано з групи: гідроген, (С1-С6)-алкіл, галоген-(С1-С6)-алкіл, гідрокси-(С1-С6)-алкіл, та карбокси-(С1-С6)-алкіл; R54 та R55 є незалежно вибраними з групи- гідроген, (С1-С6)-алкіл, галоген-С1-С6)-алкіл, гідрокси(С1-С6)-алкіл, та карбокси-(С1-С6)-алкіл; та R81, R82, R83, R84, та R85 є незалежно вибраними з групи: гідроген, хлор, флуор, ціано, гідрокси, карбокси, метил, етил, трихлорметил, трифлуорметил, ціанометил, гідроксиметил, карбоксиметил, метокси, аміно, метиламіно, та диметиламіно. В одному втіленні сполуки формули II R2 - метил. У ще одному втіленні сполуки формули II R2 гідроген. 92670 26 У ще одному втіленні сполуки формули II R2 гідроген; R5 - -(CH2)mC(O)OR50; де m=0, 1,2, або 3; R50 вибрано з групи: гідроген та (С1-С6)-алкіл; де R50 (С1-С6)-алкіл може бути незалежно та необов'язково заміщеним одним або більше замісниками, вибраними з групи: галоген, -OR53, -C(O)R53, C(O)OR53, -C(O)NR54R55, -NR54R55, -N(R56)C(O)R53; S(O)pR53, та -S(O)pNR54R55; p=0, 1 або 2; R53 вибрано з групи: гідроген, (С1-С6)-алкіл, галоген-(С1С6)-алкіл, гідрокси-(С1-С6)-алкіл, та карбокси-(С1С6)-алкіл; та R54 та R55 є незалежно вибраними з групи: гідроген, (С1-С6)-алкіл, галоген-(С1-С6)-алкіл, гідрокси-(С1-С6)-алкіл, та карбокси-(С1-С6)-алкіл.У ще одному втіленні сполуки формули II R2 гідроген; R5 - -(CH2)mC(O)OR50; де m=0, 1, або 2; R50 вибрано з групи: гідроген та (С1-С4)-алкіл; де R50 (С1-С4)-алкіл може бути незалежно та необов'язково заміщеним одним або більше замісниками, вибраними з групи: галоген, -OR53, -C(O)R53, та -C(O)OR53; та R53 вибрано з групи: гідроген та (С1С4)-алкіл. У ще одному втіленні сполуки формули II R2 гідроген; Ζ вибрано з групи: -C(R81)-та -N-; R1 вибрано з групи: циклопентил, циклобутил та феніл; де R1 циклопентил, циклобутил та фенілалкіл можуть бути необов'язково заміщеними одним або більше замісниками, незалежно вибраними з групи: хлор, флуор, метил, та трифлуорметил; R5 - (CH2)mC(O)OR50; де m=0, 1, або 2; R50 вибрано з групи: гідроген та (С1-С4)-алкіл; де R50 (С1-С4)-алкіл може бути незалежно та необов'язково заміщеним одним або більше замісниками, вибраними з групи: галоген, -OR53, -C(O)R53, та -C(O)OR53; та R53 вибрано з групи: гідроген та (С1-С4)-алкіл; та R81, R82, R83, R84, та R85 є незалежно вибраними з групи: гідроген, хлор, флуор, ціано, гідрокси, карбокси, метил, етил, ціанометил, гідроксиметил, карбоксиметил, метокси, аміно, метиламіно, та диметиламіно. У ще одному втіленні сполуки формули II R2 81 1 гідроген; Ζ вибрано з групи: -C(R )-та -N-, R вибрано з групи: циклопентил, циклобутил та феніл; де R1 циклопентил, циклобутил та фенілалкіл можуть бути необов'язково заміщеними флуором; R5 - -(CH2)mC(O)OR50; де m=0; R50 вибрано з групи: гідроген та (С1-С4)-алкіл; та R81 та R85, кожний, гідроген; та R82, R83, та R84 є незалежно вибраними з групи: хлор, ціано, та метил. У ще одному втіленні сполуки формули II R2 гідроген; X - -СН2-; Ζ - -C(R81)-; R1 вибрано з групи: циклопентил, циклобутил та де R1 феніл може бути необов'язково заміщеним флуором; R5 - (CH2)mC(O)OR50; де m=0; R50 - гідроген; R81, R84 та R85, кожний, - гідроген; та R82 та R83 є незалежно вибраними з групи: хлор, ціано, та метил. У ще одному втіленні R82 вибрано з групи, хлор та метил; та R83 - ціано. У ще одному втіленні R82 - хлор та R83 - ціано. У ще одному втіленні R1 - циклопентил. У ще одному втіленні R1 - феніл; де R1 феніл може бути необов'язково заміщеним флуором. У ще одному втіленні R1 - феніл; де R1 феніл може бути необов'язково заміщеним флуором у парапозиції. У ще одному втіленні сполуки формули II R2 гідроген; X - -О-; Ζ - -C(R81)-; R1 вибрано з групи: 27 циклопентил, циклобутил та де R1 феніл може бути необов'язково заміщеним флуором; R5 - (CH2)mC(O)OR50; де m=0; R50 - гідроген; R81, R84 та R86, кожний, - гідроген; та R82 та R83 є незалежно вибраними з групи: хлор, ціано, та метил. У ще одному втіленні R82 вибрано з групи: хлор та метил; та R83 - ціано. У ще одному втіленні R82 - хлор та R83 - ціано. У ще одному втіленні R1 - циклопентил. У ще одному втіленні R1 - феніл; де R1 феніл може бути необов'язково заміщеним флуором. У ще одному втіленні R1 - феніл; де R1 феніл може бути необов'язково заміщеним флуором у парапозиції. У ще одному втіленні сполуки формули II R2 гідроген; X - -СН2-; Ζ - -Ν-; R1 вибрано з групи: циклопентил, циклобутил та де R1 феніл може бути необов'язково заміщеним флуором; R5 - (CH2)mC(O)OR50; де m=0; R50 - гідроген; R81, R84 та R85, кожний, - гідроген; та R82 та R83 є незалежно вибраними з групи: хлор, ціано, та метил. У ще одному втіленні R82 вибрано з групи: хлор та метил; та R83 - ціано. У ще одному втіленні R82 - хлор та R83 - ціано. У ще одному втіленні R1 - циклопентил. У ще одному втіленні R1 - феніл; де R1 феніл може бути необов'язково заміщеним флуором. У ще одному втіленні R1 - феніл; де R1 феніл може бути необов'язково заміщеним флуором у парапозиції. У ще одному втіленні сполуки формули II R2 гідроген; X - -О-; Ζ - -Ν-; R1 вибрано з групи: циклопентил, циклобутил, та де R1 феніл може бути 5 необов'язково заміщеним флуором; R - (CH2)mC(O)OR50; де m=0; R50 - гідроген; R81, R84 та R85, кожний, - гідроген; та R82 та R83 є незалежно вибраними з групи: хлор, ціано, та метил. У ще одному втіленні R82 вибрано з групи: хлор та метил; та R83 - ціано. У ще одному втіленні R82 - хлор та R83 - ціано. У ще одному втіленні R1 - циклопентил. У ще одному втіленні R1 - феніл; де R1 феніл може бути необов'язково заміщеним флуором. У 1 1 ще одному втіленні R - феніл; де R феніл може бути необов'язково заміщеним флуором у парапозиції. У ще одному втіленні сполуки формули II є вибраними з групи: 2-(3-хлор-4-ціанофеніл)-3-(4-флуорфеніл)3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота; 3-(4-флуорфеніл)-7-гідрокси-3,3а,4,5тетрагідробензо[g]індазол-2-іл)-2метилбензонітрил; 3-(4-флуорфеніл)-7-гідрокси-3,3а,4,5тетрагідробензо[g]індазол-2-іл)-2(трифлуорметил)бензонітрил; 2-хлор-4-(3-(4-флуорфеніл)-7-гідрокси3,3а,4,5-тетрагідробензо[g]індазол-2іл)бензонітрил; та 2-(3-хлор-4-ціанофеніл)-3-(4-флуорфеніл)-N(2-(метилсульфоніл)етил)-3,3а,4,5-тетрагідро-2Нбензо[g]індазол-7-карбоксамід. У ще одному втіленні сполуки формули II є вибраними з групи: 2-(3-хлор-4-ціанофеніл)-3-циклопентил3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота; 92670 28 2-(4-ціанофеніл)-3-циклопентил-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота; 2-(4-ціано-3-метилфеніл)-3-циклопентил3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота; 2-(5-ціано-6-метилпіридин-2-іл)-3циклопентил-3,3а,4,5-тетрагідро-2Нбензо[g]індазол-7-карбонова кислота; 2-(4-ціано-3-метоксифеніл)-3-циклопентил3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота; та N-(-2-(3-хлор-4-ціанофеніл)-3-циклопентил3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7іл)ацетамід; У ще одному втіленні сполуки формули II є вибраними з групи: метил 2-(3-хлор-4-ціанофеніл)-3-циклопентил3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбоксилат; 2-(3-хлор-4-ціанофеніл)-3-циклопентил-Заметил-3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота; 2-(3-хлор-4-ціанофеніл)-3-циклопентил-N-(2(метилсульфоніл)етил)-3,3а,4,5-тетрагідро-2Нбензо[g]індазол-7-карбоксамід; 2-(3-хлор-4-ціанофеніл)-3-циклопентил-N-(2гідроксіетил)-3,3а,4,5-тетрагідро-2Нбензо[g]індазол-7-карбоксамід; та 2-(4-ціано-3-метилфеніл)-3-циклопентил2,3,3а,4-тетрагідрохромено[4,3-с]піразол-7карбонова кислота. У ще одному втіленні сполуки формули II є вибраними з групи: 2-(3-хлор-4-ціанофеніл)-3-циклобутил-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота; 2-(3-хлор-4-ціанофеніл)-3-циклопентеніл3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота; та 2-(4-ціано-3-метилфеніл)-3-циклопентеніл3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота. У ще одному втіленні сполуки формули II є вибраними з групи: 2-(3-хлор-4-ціанофеніл)-3-(5-метил-2-фурил)3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота; 2-(3-хлор-4-ціанофеніл)-3-(3-фурил)-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбонова кислота; 2-(3-хлор-4-ціанофеніл)-3-(5-метил-2-фурил)N-[2-(метилсульфоніл)етил]-3,3а,4,5-тетрагідро2Н-бензо[g]індазол-7-карбоксамід; та 2-(3-хлор-4-ціанофеніл)-І\І-[2(метилсульфоніл)етил]-3-(2-метил-1,3-тіазол-5-іл)3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбоксамід. У ще одному втіленні сполуки формули II є вибраними з групи: 2-(3-хлор-4-ціанофеніл)-3-циклопентил2,3,3а,4-тетрагідрохромено[4,3-с]піразол-7карбонова кислота; 29 2-[4-ціано-3-(трифлуорметил)феніл]-3циклопентил-2,3,3а,4-тетрагідрохромено[4,3с]піразол-7-карбонова кислота; 2-(4-ціано-3-метилфеніл)-3-циклопентеніл2,3,3а,4-тетрагідрохромено[4,3-с]піразол-7карбонова кислота; та 2-(3-хлор-4-ціанофеніл)-3-циклопентеніл2,3,3а,4-тетрагідрохромено[4,3-с]піразол-7карбонова кислота. С. Ізомери Сполуки заявленого винаходу можуть бути стереоізомерами, як-то енантіомери та діастереомери. Наприклад, сполуки (охоплюючи сполуки формул І та II) загалом містять два або більше асиметричних атомів карбону та можуть бути у формі одного або більше стереоізомерів (як-то, індивідуальні енантіомери, діастереомери та їх суміші). Більш конкретно, сполуки заявленого винаходу можуть бути 3R,3aR стереоізомером, 3S,3aS стереоізомером, 3S,3aR стереоізомером, 3R,3aS стереоізомером, або сумішшю двох або більше цих стереоізомерів. В одному втіленні сполуки формул І або II мають 3R,3aR конфігурацію. У ще одному втіленні сполуки формул І або II мають 3S,3aS конфігурацію. У ще одному втіленні сполуки формул І або II мають 3S,3aR конфігурацію. У ще одному втіленні сполуки формул І або II мають 3R,3aS конфігурацію. У ще одному втіленні сполуки формул І або II є сумішшю двох або більше стереоізомерів, вибраних з групи: 3R,3aR стереоізомер, 3S,3aS стереоізомер, 3S,3aR стереоізомер, та 3R,3aS стереоізомер. На додаток, коли сполука заявленого винаходу містить алкеніл, можуть бути геометричні ізомери. D. Таутомерні форми Заявлений винахід стосується таутомерних форм сполук формул І та II. Де структурні ізомери є взаємоперетворюваними внаслідок низького енергетичного бар'єру, може відбуватися таутомерна ізомерія ('таутомерія'). Це може мати форму протонної таутомерії у сполуках формули І або формули II з вмістом, наприклад, іміно, кето, або оксимогрупи, або так званої валентної таутомері у сполуках, котрі містять ароматичну частину. Звідси витікає, що одинична сполука може виявляти більше одного типу ізомерії. Різні співвідношення таутомеріє у твердій та рідкій формі є залежними від різних замісників на молекулі, а також певного способу кристалізації, застосовуваного для виділення сполуки. Е. Солі Сполуки цього винаходу можна застосовувати у формі солей, похідних від неорганічних або органічних кислот. Залежно від конкретної сполуки, сіль сполуки може бути переважною внаслідок одної або більше фізичних властивостей солі, якто посилена фармацевтична стабільність при різних температурах та вологості, або потрібна роз чинність у воді або олії. У деяких випадках сіль сполуки також можна застосовувати, як допоміжну у виділенні, очистці, та/або розділенні сполуки. 92670 30 Коли сіль призначено для застосування до пацієнта (як протилежно, наприклад, застосуванню у контексті in vitro), зразкова сіль є фармацевтично прийнятною. Термін "фармацевтично прийнятна сіль", що стосується солі, отриманої комбінуванням сполуки формул І або II кислотою, або основою, загалом розглядають придатною для вживання людиною. Фармацевтично прийнятні солі є особливо корисними, як продукти способів заявленого винаходу внаслідок їх більшої водної розчинності відносно вихідної сполуки. Для застосування у медицині солі сполук цього винаходу є нетоксичними "фармацевтично прийнятними солями." Солі, охоплені у терміні "фармацевтично прийнятні солі" стосуються нетоксичних солей сполук цього винаходу, котрі загалом отримують реакцією вільної основи з придатною органічною або неорганічною кислотою. Придатні фармацевтично прийнятні кислотноадитивні солі сполук заявленого винаходу, коли можливо, охоплюють похідні від неорганічної кислоти, як-то, хлоридна, бромідна, флуоридна, боратна, флуорборатна, фосфатна, метафосфатна, нітритна, карбонова сульфонова, та сульфатна кислоти, та органічні кислоти, наприклад, оцтова, бензенсульфонова, бензойна, лимонна, яблучна, етансульфонова, фумарова, глюконова, гліколева, ізотіонова, молочна, лактобіонова, малеїнова, метансульфонова, трифлуорметансульфонова, бурштинова, толуєнсульфонова, винна та трифлуороцтова кислоти. Придатні органічні кислоти загалом охоплюють, наприклад, аліфатичні, циклоаліфатичні, ароматичні, араліфатичні, гетероциклічні, карбонові, та сульфонові органічні кислоти. Певні приклади придатних органічних кислот дають ацетат, трифлуорацетат, форміат, пропіонат, сукцинат, гліколят, глюконат, диглюконат, лактат, малат, тартрат, цитрат, аскорбат, глюкуронат, малеат, фумарат, піруват, аспартат, глютамат, бензоат, антранілат, мезилат, стеарат, саліцилат, пгідроксибензоат, фенілацетат, манделат, ембонат, метансульфонат, етансульфонат, бензенсульфонат, толуєнсульфонат, 2-гідроксіетансульфонат, циклогексиламіносульфонат, галактарат, галактуронат, адипат, альгінат, бутират, камфорат, камфорсульфонат, циклопентанпропіонат, додецилсульфат, глікогептаноат, гліцерофосфат, гептаноат, гексаноат, нікотинат, 2нафталсульфонат, оксалат, пальмоат, пектинат, 3фенілпропіонат, пікрат, півалат, тіоціанат, тозилат та ундеканоат. У ще одному втіленні приклади придатних утворених адитивних солей охоплюють ацетат, аспартат, бензоат, безилат, гідрогенкарбонат/карбонат, гідрогенсульфат/сульфат, борат, камзилат, цитрат, едизилат, езилат, форміат, фумарат, глюцептат, глюконат, глюкуронат, гексафлуорфосфат, гібензат, гідрохлорид/хлорид, гідробромід/бромід, гідройодид/йодид, ізетіонат, лактат, малат, малеат, нітрат, оротат, оксалат, пальмітат, памоат, фосфат/гідрогенфосфат/дигідрогенфосфат, сахарат, стеарат, сукцинат, тартрат, тозилат та трифлуорацетат. У ще одному втіленні репрезентативні 31 солі охоплюють бензенсульфонат, гідробромід та гідрохлорид. Крім того, де сполуки заявленого винаходу мають кислотну частину, їх придатні фармацевтично прийнятні солі можуть охоплювати солі лужного металу, як-то, натрій або калій; солі лужноземельного металу, як-то, кальцій або магній; та солі, утворені з придатними органічними лігандами, наприклад, солі четвертинного амонію. У ще одному втіленні солі утворюють з основою, котра утворює нетоксичні солі, охоплюючи алюміній, аргінін, бензатин, холін, діетиламін, діоламін, гліцин, лізин, меглумін, оламін, трометамін та цинк. Органічні солі можна робити з солей вторинних, третинних або четвертинних амінів, як-то трометамін, діетиламін, Ν,Ν'дибензилетилендіамін, хлорпрокаїн, холін, діетаноламін, етилендіамін, меглумін (Nметилглюкамін), та прокаїн. Групи з вмістом основного нітрогену можна кватернізувати засобами, як-то нижчі (С1-С6) алкілгалогеніди (наприклад, метил, етил, пропіл, та бутилхлориди, броміди, та йодиди), діалкілсульфати (наприклад, диметил, діетил, дибутил, та діамілсульфати), довголанцюгові галогеніди (наприклад, децил, лаурил, міристил та стеарилхлориди, броміди, та йодиди), арилалкілгалогеніди (наприклад, бензил та фенетилброміди), та інші. В одному втіленні гемісолі кислот та основ можуть бути утвореними також, наприклад, гемісульфат та гемісолі кальцію. F. Проліки Також у рамках заявленого винаходу є так звані "проліки" сполук формул І та II. Тому, деякі похідні сполук будь-якої з формул І або II, котрі можуть мати малу фармакологічну активність або не мати її, можуть при застосуванні для організму, перетворитися у сполуки будь-якої з формул І або II, що мають потрібну активність, наприклад, при гідролітичному розщепленні. Так похідні стосуються "проліків". Наступну інформацію про застосування проліків можна знайти у "Pro-drugs as Novel Delivery Systems, Vol.14, ACS Symposium Series (T Higuchi та W Stella) та "Bioreversible Carriers in Drug Design" Pergamon Press, 1987 (ed. Ε Β Roche, American Pharmaceutical Association). Проліки згідно з винаходом можна, наприклад, продукувати заміщенням прийнятних функціональних груп у сполуках будь-якої з формул І або II з деякими частинами, відомими спеціалістам, як "пpοчастини", які описані, наприклад, у "Design of Prodrugs" Bundgaard (Elseview, 1985). G. Способи лікування Заявлений винахід крім того стосується способів лікування стану у суб'єкта, що має або є сприйнятливим мати такий стан, застосуванням до суб'єкту терапевтично ефективної кількості одної або більше сполук формул І та II, які описані вище. В одному втіленні лікуванням є попереджувальне лікування. У ще одному втіленні лікуванням є пом'якшувальне лікування. У ще одному втіленні лікуванням є зміцнювальне лікування. 1. Стани Стани, що можна лікувати згідно з заявленим винаходом, охоплюють, але без обмеження, сер 92670 32 цево-судинні стани, ниркові стани, стани печінки, стани судин, запальні стани, біль, ретинопатію, невропатію (як-то периферійну невропатію), інсулінопатію, набряк, ендотеліальну дисфункцію, барорецепторну дисфункцію тощо. Серцево-судинні стани охоплюють, але без обмеження, гіпертензію, серцеву недостатність (як-то застійна серцева недостатність), діастолічну дисфункцію (як-то ліво-шлуночкова діастолічна дисфункція, діастолічна серцева недостатність, та порушене діастолічне наповнення), систолічну дисфункцію (як-то систолічна серцева недостатність), аритмію, ішемію, гіпертрофічну кардіоміопатію, раптову серцеву смерть, фіброз міокарду та судин, порушену артеріальну еластичність, некротичні ураження міокарду, пошкодження судин, інфаркт міокарду, ліво-шлуночкову гіпертрофію, зменшену фракцію викиду, серцеві ураження, гіпертрофію стінок судин, ендотеліальне ущільнення, фібриноїдний некроз коронарних артерій, інсульт, тощо. Ниркові стани охоплюють, але без обмеження, гломерулосклероз, кінцеву стадію ниркової хвороби, діабетичну нефропатію, зменшений потік ниркової крові, збільшену фракцію гломерулярного фільтрування, протеїнурію, зменшену швидкість гломерулярного фільтрування, зменшений кліренс креатиніну, мікроальбумінурію, ниркову артеріопатію, ішемічні ураження, тромбозні ураження, глобальний фібриноїдний некроз, фокальний тромбоз гломерулярних капілярів, набряк та проліферацію внутрішньокапілярних (ендотеліальних та мезангіальних) та/або зовнішньокапілярних клітин (півмісячних), розширення сітчастого мезангіального матриксу із або без значної гіперцелюлярності, злоякісний нефросклероз (як-то ішемічна ретракція, тромбонекроз капілярних жмутків, артеріолярний фібриноїдний некроз та тромбозні мікроангіопатичні ураження, що вражають гломерули та мікросудини), тощо. Стани печінки охоплюють, але без обмеження, цироз печінки, асцит печінки, печінкову конгестію, тощо. Стани судин охоплюють, але без обмеження, тромбозну хворобу судин (як-то муральний фібриноїдний некроз, екстравазація та фрагментація червоних клітин крові, та люмінальний та/або муральний тромбоз), проліферативну артеріопатію (як-то набряклі міоінтимальні клітини, оточені слизотвірним зовнішньоклітинним матриксом та вузлуватим ущільненням), атеросклероз, зменшену еластичність судин (як-то ригідність, зменшена шлуночкова еластичність та зменшена еластичність судин), ендотеліальну дисфункцію, тощо. Запальні стани охоплюють, але без обмеження, артрит (наприклад, остеоартрит), запальні хвороби дихальних шляхів (наприклад, хронічна обструктивна хвороба легень (COPD)), тощо. Біль охоплює, але без обмеження, гострий біль, хронічний біль (наприклад, артралгію), тощо. Набряк охоплює, але без обмеження, набряк периферійних тканин, печінкову конгестію, селезінкову конгестію, асцит печінки, респіраторну або легеневу конгестію, тощо. 33 Інсулінопатії охоплюють, але без обмеження, резистентність до інсуліну, цукровий діабет типу І, цукровий діабет типу І, чутливість до глюкози, переддіабетичний стан, синдром X, тощо. В одному втіленні стан вибрано з групи: серцево-судинні стани, ниркові стани та стани печінки. У ще одному втіленні станом є серцевосудинний стан. У ще одному втіленні станом є серцевосудинний стан, що вибрано з гіпертензії, серцевої недостатності (особливо серцевої недостатності після інфаркту міокарду), ліво-шлуночкової гіпертрофії та інсульту. У ще одному втіленні станом є гіпертензія. У ще одному втіленні станом є серцева недостатність. У ще одному втіленні станом є залишкова шлуночкова гіпертрофія. У ще одному втіленні станом є інсульт. У ще одному втіленні станом є нирковий стан. У ще одному втіленні станом є нефропатія. У ще одному втіленні станом є цукровий діабет типу І. 2. Суб'єкти Придатні суб'єкти для лікування згідно із заявленим винаходом охоплюють ссавців. Ссавці згідно із заявленим винаходом охоплюють, але без обмеження, собак, котів, корів, кіз, коней, овець, свиней, гризунів, кролів, приматів, тощо. В одному втіленні людина є придатним суб'єктом. Людина може бути будь-якої статі та у будь-якій стадії розвитку. 3. Застосування та дозування Сполуки заявленого винаходу загалом застосовують у терапевтично ефективній кількості. В одному втіленні сполуки заявленого винаходу застосовують в кількості для антагонізування мінералокортикоїдного рецептору. Сполуки заявленого винаходу можна застосовувати будь-яким придатним шляхом у формі фармацевтичної композиції, пристосованої до такого шляху, та у дозі, ефективній для призначеного лікування. Терапевтично ефективні дози сполук заявленого винаходу, потрібні для попередження або затримки прогресу, або для лікування медичного стану, легко визначити спеціалісту, застосовуючи звичайні доклінічні та клінічні підходи. Режим дозування для сполуки та/або композиції з вмістом сполуки є на основі багатьох факторів, охоплюючи тип, вік, масу, стать та медичний стан пацієнта; суворість стану; шлях застосування; та активність певної застосованої сполуки. Тому режим дозування може варіювати на основі певної ситуації. Рівні дозування приблизно від 0,001мг до 100мг сполуки заявленого винаходу на кілограм маси тіла на добу є корисними у лікуванні вищенаведених станів. В одному втіленні загальна добова доза сполуки заявленого винаходу (застосовувана в одиничній або поділених дозах) є звичайно приблизно від 0,001мг/кг до 20мг/кг (тобто, мг сполуки/кг маси тіла). У ще одному втіленні загальна добова доза сполуки заявленого винаходу є приблизно від 0,005мг/кг до 10мг/кг. У ще одному втіленні загальна добова доза є приблизно від 0,005мг/кг до 5мг/кг. У ще одному втіленні загаль 92670 34 на добова доза є приблизно від 0,01мг/кг до 1мг/кг. У ще одному втіленні загальна добова доза є приблизно від 0,8мг/кг до 15мг/кг. У ще одному втіленні загальна добова доза є приблизно від 0,2мг/кг до 4мг/кг. Ці дози є на основі середньої людини, що має масу приблизно 65кг-75кг Лікарю легко визначити дози для суб'єктів, чия маса є поза цими межами, як-то дітей. Застосування сполуки заявленого винаходу можна повторювати багато разів на добу (звичайно не більше 4 разів) для досягнення потрібної добової дози. Для зручності сполуки заявленого винаходу можна застосовувати у формі окремої дози. Якщо потрібно багато доз на добу, форми окремої дози можна застосовувати для збільшення загальної добової дози. Формою окремої дози, наприклад, може бути таблетка або капсула з вмістом приблизно 0,01, 0,05, 0,1, 0,5, 1, 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 125, 150, 175, 200, 250 або 500мг сполуки заявленого винаходу. В одному втіленні форма окремої дози містить приблизно від 0,01мг до 500мг сполуки заявленого винаходу. У ще одному втіленні форма окремої дози містить приблизно від 0,05мг до 250мг сполуки заявленого винаходу. У ще одному втіленні форма окремої дози містить приблизно від 0,1мг до 200мг сполуки заявленого винаходу. У ще одному втіленні форма окремої дози містить приблизно від 0,5мг до 150мг сполуки заявленого винаходу. Н. Застосування при отриманні медикаменту Заявлений винахід крім того стосується застосування сполуки формул І або II для застосування, як медикамент (як-то дозована таблетка або дозована капсула). У ще одному втіленні заявлений винахід стосується застосування сполуки формул І або II для виробництва медикаменту (як-то дозована таблетка або дозована капсула) для лікування одного або більше станів, ідентифікованих у вищенаведених способах лікування. В одному втіленні станом є гіпертензія. У ще одному втіленні станом є серцева недостатність. І. Фармацевтичні композиції Для лікування вищенаведених станів сполуки формул І або II можна застосовувати самі по собі. Альтернативно, фармацевтично прийнятні солі є придатними для медичного застосування внаслідок їх більшої водної розчинності відносно вихідної сполуки. На додаток, сполуки заявленого винаходу можна застосовувати у формі фармацевтичної композиції, що містить сполуку формули І або II, або її фармацевтично прийнятну сіль, та фармацевтично-прийнятний носій. Носій може бути твердим, рідким або обома, та його можна формувати зі сполукою, як композицію окремої дози, як-то, таблетка, котра може містити від 0,05% до 95мас.% активних сполук. Інші фармакологічно активні речовини можуть бути також. Активні сполуки заявленого винаходу можна застосовувати будь-яким придатним шляхом, де форму фармацевтичної композиції пристосовують до такого шляху, та у дозі, ефективній для призначеного лікування. Активні сполуки та композиції, 35 наприклад, можна застосовувати перорально, ректально, парентерально або місцево. Пероральне застосування твердої форми дози може бути, наприклад, дискретними одиницями, як-то тверді або м'які капсули, пілюлі, облатки, пастилки або таблетки, кожна з вмістом попередньо визначеної кількості принаймні одної сполуки заявленого винаходу. У ще одному втіленні перораль не застосує ання може бути у формі порошку або гранул. У ще одному втіленні пероральна форма дози є сублінгвальною, як-то, наприклад, пастилка. У таких твердих дозованих формах сполуки формул І або II звичайно комбінують із одним або більше ад'ювантами. У випадку капсул, таблеток, та пілюль, дозовані форми також можуть містити буферувальні засоби або їх можна отримувати з ентеросолюбільним покриттям. У ще одному втіленні пероральне застосування може бути у рідкій формі дози. Рідкі дозовані форми для перорального застосування охоплюють, наприклад, фармацевтично прийнятні емульсії, розчини, суспензії, сиропи та еліксири з вмістом інертних розріджувачів, звичайно застосовуваних у рівні техніки (наприклад, води). Такі композиції також можуть містити ад'юванти, як-то емульгатори, змочувальні, суспендувальні, смакові засоби (наприклад, підсолоджувальні), та/або ароматизатори. У ще одному втіленні заявлений винахід стосується парентеральної форми дози. "Парентеральне застосування" охоплює, наприклад, підшкірні ін'єкції, внутрішньовенні ін'єкції, інтраперитонеальні, внутрішньом'язові ін'єкції, інтрастернальні ін'єкції, та вливання. Придатні для ін'єкцій препарати (наприклад, стерильні придатні для ін'єкцій водні або олійні суспензії) можна формувати відомими способами, застосовуючи придатні диспергувальні, змочувальні засоби, та/або засоби суспендування. У ще одному втіленні заявлений винахід стосується місцевої форми дози. У ще одному втіленні заявлений винахід стосується форми дози для інтраназального застосування або застосування інгаляцією. У ще одному втіленні заявлений винахід стосується ректальної форми дози. Інші носії та режими застосування, відомі у фармацевтиці, можна також застосовувати. Фармацевтичні композиції заявленого винаходу можна отримувати будь-яким з добре відомих способів, як-то ефективні способи композиції та застосування. Вищенаведені міркування відносно ефективних композицій та способів застосування є добре відомими у рівні техніки та є описаними у стандартних довідниках. Композиції ліків є обговореними, наприклад, у Hoover, John E., Remington's Pharmaceutical Sciences, Mack Publishing Co., Easton, Pennsylvania, 1975; Liberman, et al., Eds., Pharmaceutical Dosage Forms, Marcel Decker, New York, N.Y., 1980; та Kibbe, et al., Eds., Handbook of Pharmaceutical Excipients (3rd Ed.), American Pharmaceutical Association, Washington, 1999. J. Комбінації та комбінаційна терапія Сполуки заявленого винаходу можна застосовувати, поодинці або у комбінації із іншими фармацевтично активними сполуками для лікування 92670 36 станів, як-то описаних вище. Сполуки заявленого винаходу та інші фармацевтично активні сполуки можна застосовувати одночасно (у будь-якій дозованій формі або у окремих дозованих формах) або послідовно. Відповідно, в одному втіленні заявлений винахід стосується способів лікування стану застосуванням до суб'єкту терапевтично ефективної кількості одної або більше сполук формул І або II та одної або більше додаткових фармацевтично активних сполук. У ще одному втіленні заявлений винахід стосується фармацевтичної композиції, що містить одну або більше сполук формул І або II, одну або більше додаткових фармацевтично активних сполук, та фармацевтично прийнятний носій. В одному втіленні одну або більше сполук формул І або II можна співзастосовувати з одним або більше діуретиками. Приклади придатних діуретиків охоплюють (а) петльові діуретики, як-то фуросемід (як-то LASIX™), торсемід (як-то DEMADEX™), беметанід (як-то BUMEX™), та етакринова кислота (як-то EDECRIN™); (b) діуретики тіазидного типу, як-то хлортіазид (як-то DIURIL™, ESIDRIX™ або HIDRODIURIL™), гідрохлортіазид (як-то MICROZIDE™ або ORETIC™), бензтіазид, гідрофлуметіазид (як-то SALURON™), бендрофлуметіазид, метилхлортіазид, політіазид, трихлорметіазид, та індапамід (як-то LOZOL™); (с) діуретики фталімідинового типу, як-то хлорталідон (якто HYGROTON™), та метолазон (як-то ZAROKCOLYN™); (d) діуретики хіназолінового типу, як-то хінетазон; та (e) калій-збережувальні діуретики, як-то тріамтерен (як-то DYRENIUM™), та амілорид (як-то ΜІDAMOR™ або MODURETIC™). Переважно співзастосовуваними діуретиком або діуретиками повинні бути калійвідхідні діуретики. Калій-відхідні діуретики є діуретиками, що можуть викликати збільшення виділення калію, що може призводити до знижених рівнів калію, охоплюючи зменшення калію у сироватці. Приклади калій-відхідних діуретиків охоплюють, але без обмеження: петльові діуретики, як-то фуросемід та торсемід; діуретики типу тіазиду, як-то хлортіазид та гідрохлортіазид; та діуретики типу фталімідину, як-то хлорталідон. У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із петльовим діуретиком. У ще одному втіленні петльовий діуретик вибрано з фуросеміду та торсеміду. У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із фуросемідом. У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із торсемідом. У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із діуретиком типу тіазиду. У ще одному втіленні діуретик типу тіазиду вибрано з групи: хлортіазид та гідрохлортіазид. У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із хлортіазидом. У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із гідрохлортіазидом. У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із діуре 37 тиком типу фталімідину. У ще одному втіленні діуретик типу фталімідину - хлорталідон. У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із одним або більше інгібіторами ферменту перетворення ангіотензину. Приклади придатних інгібіторів ферменту перетворення ангіотензину охоплюють хінаприл (як-то ACCUPRIL™), периндоприл (як-то ACEON™), каптоприл (як-то CAPOTEN™), еналаприл (як-то VASOTEC™), ENALAPRILAT™, раміприл (як-то ALTACE™), цилазаприл, делаприл, фозеноприл (як-то MOHOPRIL™), зофеноприл, індолаприл, беназеприл (як-то LOTEH3I/IH™), лізиноприл (як-то PRINIVIL™ та ZESTRIL™), спіраприл, трандолаприл (як-то MAVIK™), периндеп, пентоприл, моексиприл (як-то UNIVASC™) фазидонтрил, S-алімеркаптокаптоприл, та півоприл. У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із одним або більше блокаторами рецептору ангіотензину II. Приклади придатних блокаторів рецептору ангіотензину II охоплюють кандесартан (як-то ATACAND™), епросартан (як-то TEVETEN™), ірбесартан (як-то AVEPRO™), лосартан (як-то COZAAR™), олмесартан, олмесартан медоксоміл (як-то BENICAR™), тазосартан, телмісартан (як-то MICARDIS™), валсартан (як-то DIOVAN™), золасартан, FI-6828K, RNH-6270, UR-7198, Way126227, KRH-594, ТАК-536, BRA-657, та ТА-606. У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із одним або більше блокаторами каналів кальцію. Приклади придатних блокаторів каналів кальцію охоплюють ніфедипін (як-то ADALAT™, ADALAT СС™ та PROCARDIA™), верапаміл (як-то CALAN™, COVERA-HS™, ISOPTIN SR™ та VERELAN™), дитіазем (як-то CARDIZEM™ CARDIZEM CD™, CARDIZEM LA™, CARDIZEM SR™, DILACOR™, TIAMATE™ та ТІАЗАС™), ісрадипін (як-то DYNACIRC™ та DYNACIRC CR™), амлодипін (якто NORVASC™), фелодипін (як-то PLENDIL™), нізолдипін (як-то SULAR™), бепридил (як-то VASCOR™), нікардипін, ватанідипін, клевідипін, леркапідипін, та NNC-55-0396. У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із одним або більше бета-блокаторами. Приклади придатних бета-блокаторів охоплюють тимолол (як-то BLOCARDEN™), картеолол (як-то CARTROL™), карведилол (як-то COREG™), надолол (як-то CORGARD™), пропраналол (як-то INNOPRAN XL™), бетаксолол (як-то KERLONE™), пенбутолол (як-то LEVATOL™), метопролол (як-то LOPRESSOR™ та TOPROL-XL™), атенолол (як-то TENORMIN™), піндолол (як-то VISKEN™), ацебутолол, та бізопролол. У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із одним або більше альфа-блокаторами. Приклади придатних альфа-блокаторів охоплюють празозин, доксазозин (як-то CARDURA™), феноксибензамін (якто ДИБЕНЗИЛШЕ™), теразозин (як-то HYTRIN™), CDRI-93/478 та CR-2991. У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із одним 92670 38 або більше альфа-бета-блокаторами. Прикладом придатного альфа-бета-блокатору є лабеталол (як-то NORMODYNE™ або TRANDATE™). У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати ізодним або більше антагоністами рецептору альдостерону. Приклади придатних антагоністів рецептору альдостерону охоплюють еплеренон (як-то INSPRA™) або спіронолактон (як-то ALDACTONE™). У ще одному втіленні одну або більше сполук формул І або II можна співзастосовувати із одним або більше інгібіторами реніну. Приклади придатних інгібіторів реніну охоплюють аліскірен (SPP 100), SPP-500/600 та YS-004-39. K. Комплекти Заявлений винахід крім того стосується комплектів, що є придатними для застосування у вищенаведених способах лікування або попередження. В одному втіленні комплект містить першу дозовану форму, що містить одну або більше сполук заявленого винаходу та тару для доз, у кількості, достатній для здійснення способів заявленого винаходу. У ще одному втіленні комплект заявленого винаходу містить одну або більше сполук формул І або II та діуретик. У ще одному втіленні комплект заявленого винаходу містить одну або більше сполук формул І або II та інгібітор ферменту перетворення ангіотензину. У ще одному втіленні комплект заявленого винаходу містить одну або більше сполук формул І або II та антагоніст рецептору ангіотензину II. У ще одному втіленні комплект заявленого винаходу містить одну або більше сполук формул І або II та антагоніст рецептору альдостерону. L. Інтермедіати У ще одному втіленні винахід стосується нових інтермедіатів, корисних для отримання сполук формул І або II. У ще одному втіленні нові інтермедіати, корисні для отримання сполук формул І або II є вибраними з групи: 4-гідразиніл-2-метилбензонітрил гідрохлорид; 4-гідразиніл-2-(трифлуорметил)бензонітрил гідрохлорид; 4-гідразиніл-2-метоксибензонітрил гідрохлорид; 5-гідразинілпіколінонітрил дигідрохлорид; 6-гідразиніл-2-метилнікотинонітрил; 4-гідразиніл-2-(метоксиметил)бензонітрил гідрохлорид; 2-((диметиламіно)метил)-4гідразинілбензонітрил дигідрохлорид; та 2-(бензилокси)-4-гідразинілбензонітрил. У ще одному втіленні нові інтермедіати, корисні для отримання сполук формул І або II є вибраними з групи: етил 7-(4-флуорбензіліден)-8-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат; метил 6-(циклопентилметилен)-5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат; метил 6-(циклобутилметилен)-5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат; 39 92670 40 метил 5-оксо-6-((тетрагідрофуран-3іл)метилен)-5,6,7,8-тетрагідронафталін-2карбоксилат; метил 5-оксо-6-((тетрагідро-2Н-піран-4іл)метилен)-5,6,7,8-тетрагідронафталін-2карбоксилат, трет-бутил 4-((6-(метоксикарбоніл)-1 -оксо-3,4дигідронафталін-2(1Н)-іліден)метил)піперидин-1карбоксилат; метил 6-(5-метил-2-фурилметилен)-5-оксо5,6,7,8-тетрагідронафталін-2-карбоксилат; метил 6-(циклопент-1-ен-1-ілметилен)-5-оксо5,6,7,8-тетрагідронафталін-2-карбоксилат; метил 6-(2-фурилметилен)-5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат; метил 6-(3-фурилметилен)-5-оксо-5,б,7,8тетрагідронафталін-2-карбоксилат; метил 6-[(2-метил-1,3-тіазол-5-іл)метилен]-5оксо-5,6,7,8-тетрагідронафталін-2-карбоксилат; метил 6-(ізоксазол-5-ілметилен)-5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат; етил [3-(4-флуорбензіліден)-4-оксо-3,4дигідро-2Н-хромен-7-іл]ацетат; метил 3-(4-флуорбензіліден)-4-оксохроман-7карбоксилат; метил 3-(циклопентилметилен)-4-оксохроман7-карбоксилат; метил 3-(циклопентилметилен)-4-оксохроман7-карбоксилат; метил 3-(циклопропілметилен)-4-оксохроман7-карбоксилат; метил 3-(циклопентенілметилен)-4оксохроман-7-карбоксилат; та N-(6-(циклопентилметилен)-5-оксо-5,6,7,8тетрагідронафталін-2-іл)ацетамід. М. Загальні схеми синтезу Сполуки заявленого винаходу можна отримувати, застосовуючи способи, ілюстровані схемами синтезу та експериментальними способи детально нижче. Ці загальні схеми синтезу та експериментальні способи є для ілюстрації та не є обмежувальними. Вихідні матеріали, застосовувані для отримання сполук заявленого винаходу є комерційно доступними або можна отримувати, застосовуючи звичайні способи, відомі у рівні техніки (якто способи, розкриті у COMPENDIUM OF ORGANIC SYNTHETIC METHODS, Vol.I-VI (опубліковано Wiley-lnterscience) або інших стандартних довідниках). Схема 1 нижче ілюструє загальне отримання піразолінових сполук заявленого винаходу. Якщо не вказане інше, R1, R5, R6, R8, та X показані у Схем 1 є визначеними у різних втіленнях заявленого винаходу, розкритих раніше. Спосіб А: Отримання α,β-ненасиченого кетону го додавання утворену суміш перемішують протягом приблизно 30 хвилин. Розчин альдегіду R1CHO (1,05 еквіваленти) у тетрагідрофурані (приблизно 2,5мл/ммоль кетону 1) додають до суміші, котру тоді нагрівають до кімнатної температури при перемішуванні. Через приблизно дві години суміш гасять насиченим амоній хлоридом та екстрагують етилацетатом. Органічні шари сушать натрій сульфат та концентрують. Сирий продукт очищають флеш-хроматографією на силікагелі (етилацетат/гептан) або зворотно-фазовою ВЕРХ (ацетонітрил/вод/0,1% трифлуороцтової кислоти), отримуючи α,β-ненасичений кетон 2. Спосіб В: Конденсація піразоліну Суміш α,β-ненасиченого кетону 2 (1ммоль), гідразин (R8NHNH2) гідрохлориду (1,2-1,5ммоль), та абсолютного етанолу (приблизно 8мл/ммоль α,βненасиченого кетону 2) продувають аргоном та перемішують при приблизно 80°С протягом приблизно 4-24 годин. Суміш охолоджують до кімнатної температури та фільтрують. Утворені тверді продукти промивають етанолом, отримуючи піразолін 3. Схема 2 нижче ілюструє наступну дериватизацію піразолінових сполук, отриманих згідно зі схемою 1. Якщо не вказане інше, замісники R1, R2, R8, R50, R51, R52 та X, показані у схемі 2, є визначеними у різних втіленнях заявленого винаходу, розк 2 Спосіб А1 Піролідин (1,2 еквіваленти), або ще один циклічний вторинний амін, як-то піперидин, додають до суміші кетону 1 (1 еквівалент) та альдегіду R1CHO (2 еквіваленти) у спирті, як-то метанол (2мл/ммоль кетону 1) при кімнатній температурі. Приблизно через одну - шість годин суміш охолоджують до 0°С. Утворений осад фільтрують та промивають, наприклад холодним спиртом, як-то метанол, отримуючи α,β-ненасичений кетон 2. Спосіб А2 Суміш кетону 1 (1,0 еквівалент) та альдегіду R1CHO (1,2 еквіваленти) у концентрованій хлоридній кислоті та етанол гріють при кипінні під зворотним холодильником протягом ночі. Альтернативно, 4н гідрогенхлорид у діоксані можна застосовувати замість концентрованої хлоридної кислоти. Прогріту при кипінні під зворотним холодильником суміш тоді розбавляють водою, фільтрують та сушать, отримуючи α,β-ненасичений кетон 2. Спосіб A3 Розчин кетону 1 (1 еквівалент) у тетрагідрофурані (приблизно 2,5мл/ммоль кетону 1) додають краплями під азотом до 1Μ розчину літій гексаметилдисилазиду у тетрагідрофурані (1,05 еквіваленти) і охолоджують льодяною банею. Після повно 41 92670 42 ритих раніше. Альтернативно, піразоліни 5, 6, 7, та 8 можна отримувати, застосовуючи кетон 1 як вихідний матеріал, що має потрібні замісники R5 та R6 (та захист та тоді зняття захисту цими замісниками, якщо необхідно, застосовуючи звичайний хімічний захист). Спосіб С: Похідні піразолінової кислоти 2,5 Η натрій гідроксид (2мл/ммоль естеру піразоліну 4) додають до розчину естеру піразоліну 4 (1 еквівалент) у тетрагідрофурані (6мл/ммоль естеру піразоліну 4) та метанолі (2мл/ммоль естеру піразоліну 4). Утворену суміш перемішують при кімнатній температурі до закінчення реакції, як визначають за допомогою ВЕРХ (1-24 години). Суміш концентрують під струмом азоту до половини вихідного об'єму та підкислюють водною хлоридною кислотою для зменшення рН до менше приблизно 4. Суміш розбавляють водою та фільтрують, отримуючи піразолінову кислоту 5. Спосіб D: R2-Заміщені піразоліни Замісник R2 можна уводити обробкою естеру піразоліну 4 сильною основою, як-то літій діізопропіламід (LDA) або літій гексаметилдисилазид (LHMDS), та алкілувальним засобом, як-то алкілгалогенід R2X. Алкілований естер піразоліну можна тоді гідролізувати, як описано у способі С, отримуючи алкіловану піразолінову кислоту 6. Спосіб Е: Похідні естеру піразоліну N-(3-диметиламінопропіл)-N'-етилкарбодіімід гідрохлорид (1,2 еквіваленти) додають під азотом до суміші піразолінової кислоти 5 (1 еквівалент), спирт R50OH (1,2еквів.), та 4-(диметиламіно)піридин (1,2 еквіваленти) у безводному тетрагідрофурані (5мл/200мг піразолінової кислоти 5). Суміш перемішують протягом ночі, обробляють надлишком 1Η хлоридної кислоти та екстрагують етилацетатом. Органічний шар випарюють. Залишок розчиняють у дихлорметані та очищають хроматографією на силікагелі сумішшю етилацетат/гептан. Потрібні фракції комбінують та випарюють, отримуючи естер піразоліну 7. Якщо заміщення у позиції R2 є потрібним, піразолінову кислоту 6 можна застосовувати замість піразолінової кислоти 5. Спосіб F: Амідні похідні піразоліну 2-(1Н-бензотриазол-1-іл)-1,1,3,3тетраметилуроній гексафлуорфосфат (1,1ммоль), а потім Ν,Ν-діізопропілетиламін (1,5ммоль), додають під азотом при кімнатній температурі до роз чину піразолінової кислоти 5 (1ммоль) у 5мл безводного диметилформаміду. Суміш перемішують протягом приблизно 5 хвилин та додають амін NHR51R52 (1,5ммоль). Суміш перемішують протягом ще години. Суміш тоді фільтрують та очищають зворотно-фазовою ВЕРХ (ацетонітрил/вода/0,1% трифлуороцтової кислоти). Фракції з вмістом чистого продукту комбінують та ліофілізують, отримуючи піразолінамід 8. Якщо заміщення у позиції R2 є потрібним, піразолінову кислоту 6 можна застосовувати замість піразолінової кислоти 5. Спосіб G: Хіральне розділення Піразолінові сполуки заявленого винаходу (охоплюючи інтермедіати) можуть мата два або більше хіральних центрів. Коли синтез дає сполуку як суміш енантіомерів або діастереомерів, потрібний енантіомер або діастереомер (або потрібну енантіомерно збагачену суміш або діастереомерно збагачену суміш) можна отримувати, застосовуючи звичайні способи хірального розділення. Звичайні способи, що можна застосовувати, охоплюють хроматографію (як-то ВЕРХ) або надкритичну хроматографію на асиметричній смолі. Приклади корисних смол охоплюють, але без обмеження Chiralcel OJ-H, Chiralpak AD-H, Chiralpak ΘΑ та Chiralpak-AS-H. Концентрація елюату дає збагачену суміш. Стереоізомерно збагачений піразолін може бути крім того дериватизованим, як зображено у схемі 2 чином, аналогічним для піразолінів 4, 5 та 6. Схеми 3а, 3b, та 3с нижче ілюструють кілька альтернативних схем синтезу, що можна застосовувати для отримання R8NHNH2 гідразинового реагенту, застосованого у схемі 1. Якщо не вказане інше, замісники R81, R82, R84, та R85, показані у схемі 1, є визначеними у різних втіленнях заявленого винаходу, розкритих раніше, а Аr - арил або гетероарил. 43 92670 44 Спосіб Н: Отримання з галогенованого арилнітрилу Розчин пара-заміщеного галогеном арил/гетероарилнітрилу гріють при кипінні під зворотним холодильником з надлишком гідразин моногідрату у спирті, як-то етанол. По закінченні реакції суміш розбавляють водою та фільтрують. Арил/гетероарилгідразин можна тоді перетворити у гідрохлорид обробкою еквівалентом безводного гідрогенхлориду у діетил-етері. Утворений гідразин гідрохлорид виділяють фільтруванням. Спосіб І: Отримання з аніліну Арил- або гетероариланіліни можна перетворити у відповідний арил- або гетероарилгідразин діазотуванням та наступним відновленням. Відповідно, охолоджену льодом суміш аніліну у сильній водній кислоті, як-то концентрованій хлоридній кислоті або водній сульфатній кислоті, обробляють натрій нітритом (звичайно 1-1,1 еквіваленти). Після короткого періоду часу, звичайно 15-60 хвилин, утворену суміш додають до охолодженої льодом суспензії надлишку станум хлориду у сильній водній кислоті, як-то концентрованій хлоридній кислоті або водній сульфатній кислоті. Суміш тоді нагрівають до кімнатної температури протягом кількох годин. Суміш тоді нейтралізують водною основою та екстрагують придатним органічним розчинником, як-то етилацетат, для виділення арил/гетероарилгідразину. Арил /гетероарилгідразин можна тоді перетворити у гідрохлорид обробкою еквівалентом безводного гідрогенхлориду у діетил-етері. Утворений гідразин гідрохлорид виділяють фільтруванням. Способи J та K: Отримання з арилгалогенідів Арил- або гетероарилгідразини можна отримувати сполученням арил/гетероарилгалогеніду із бензофенон-гідразоном у присутності паладієвого каталізатору, фосфінового ліганду, та основи (Mauger та Mignani (2005) Advanced Synthesis and Catalysis 347 (6), 773-782; Haddad, et al. (2004) Tetrahedron Lett. 45, 5935-7; Haddad та Baron (2002) 43(12), 2171-2173; Wagaw et al. (1999) 121(44) 10251-10263 (Спосіб J). Сполучений продукт далі гідролізують нагріванням при кипінні під зворотним холодильником у водній кислоті та органічному співрозчиннику, як-то тетрагідрофуран, для виходу арил/гетероарилгідразину (Спосіб K). Схема 4 нижче ілюструє схему синтезу, що можна застосовувати для отримання кетону 11 (тобто, кетону 1, де R5 - метоксикарбоніл, a R6 гідроген), для застосування як реагенту у схемі 1. Способи L та М: Отримання тетрадону 11 Чином, аналогічним описаному Gerlach та Wollmann у Tetrahedron Letters (1992), 33(38), 5499-5502, кетон 11 можна отримувати з фенольного кетону 9 трифлатуванням трифлатним ангідридом та піридином у придатному органічному 45 92670 46 розчиннику, як-то метиленхлорид та гептан, з наступним каталізованим паладієм карбонілуванням карбон моноксидом у диметилформаміді та метанолі, Синтез інших кетонів, корисних при отриманні піразолінів, описаних у схемі 1, є описаним у літературі (наприклад, дивись Reiter et al., Bioorganic та Medicinal Chemistry Letters, 7, 2307-2312; Koch et al., Патент США 5,550,152 (1996); Ferraz et al. Tetrahedron (2003) 59(31) 5817-5821); Cannon et al., Journal of Medicinal Chemistry (1989) 32(9), 2210-2214; та Beugelmans, et al. Journal of Organic Chemistry (1985), 50(24), 4933-4938). Так кетони можуть бути крім того дериватизованими, застосовуючи звичайні способи, відомі у рівні техніки (якто способи, розкриті у COMPENDIUM OF ORGANIC SYNTHETIC METHODS, Vol.I-VI (опубліковано Wiley-lnterscience) або інших довідниках). Схема 5 нижче ілюструє схему синтезу, що можна застосовувати для отримання піразолінової кислоти 14 (тобто, піразолінової кислоти 5а, де X карбон, а позиція карбоксизаміснику R5 є показаною), котра може бути крім того дериватизованою, як показано у схемі 2. Спосіб Ν: Конденсація піразоліну Піразолін 13а можна отримувати конденсацією R8NHNH2 з α,β-ненасиченим кетоном 12 (отриманим, як описано у схемі 1, Спосіб А1) у киплячому спирт, як-то метанол або етанол, та одним - двома еквівалентами 4 Η гідрогенхлориду у діоксані або іншим придатним джерелом гідрогенхлориду. Через 4-24 години реакційну суміш охолоджують, а естер піразоліну 13а виділяють фільтруванням. Спосіб О: Хіральне розділення Стереоізомерно збагачені естери піразоліну 13b загалом можна отримувати, застосовуючи хроматографію, як-то ВЕРХ на асиметричній смолі з рухомою фазою, що містить вуглеводень або галогенований вуглеводень, як-то гептан, гексан, або дихлорметан, та крім того з вмістом співрозчиннику, як-то ізопропанол (приблизно від 0% до 50об.%, звичайно приблизно від 2% до 20об.%), та алкіламіну (наприклад, від 0 до 5об.%, звичайно приблизно 0,1об.% діетиламіну). Стереоізомерно збагачені сполуки загалом можна також отримувати, застосовуючи надкритичну хроматографію (SFC) на асиметричній смолі з рухомою фазою, що містить спирт (приблизно 30% - 60об.%, звичайно приблизно 50об.%) та карбон діоксид. Приклади корисних смол охоплюють, але без обмеження Chiralcel OJ-H, Chiralpak AD-H, Chiralpak ΘΑ та Chiralpak-AS-H. Концентрація елюату дає стереоізомерно збагачену суміш 13b. Спосіб Р: Гідроліз Суміш естеру піразоліну 13b у придатному органічному розчиннику, як-то тетрагідрофуран, обробляють натрій триметилсиланоатом, звичайно одним - трьома еквівалентами, в інертній атмосфері. Реакцію проводять між кімнатною температурою та 50°С. N. Приклади сполук Отримання 1 2-хлор-4-гідразинілбензонітрил гідрохлорид Суміш 2-хлор-4-флуорбензонітрил (20,0г, 129ммоль), гідразин моногідрату (9,4мл, 193ммоль), та етанолу (80мл) гріли при кипінні під зворотним холодильником протягом 4 годин (Спосіб Η та Схема 3а). Суміш розбавляли водою 47 92670 (200мл). Осад фільтрували, промивали водою, та сушили, отримуючи білуватий твердий продукт (16,8г). Твердий продукт суспендували у діетилетері (400мл) та обробляли 2Η сумішшю гідрогенхлорид/етер (50мл, 100ммоль). Осад фільтрували, промивали діетил-етером, та сушили, отримуючи 2-хлор-4-гідразинілбензонітрил гідрохлорид як білий твердий матеріал (16,3г, 79,9ммоль, 62% виходу). 1Η ЯМР (400МГц, ДМСО-d6) δ млн.-1 9,63 (br. s., 3Η), 9,17 (br. s., 1Η), 7,74 (d, J=8,9Гц, 1Η), 7,13 (d, J=2,1Гц, 1Η), 6,92 (dd, J=8,6, 2,1Гц, 1Η). EP-MC m/z 168 (M+H). Отримання 2 4-гідразиніл-2-метилбензонітрил гідрохлорид Суміш 4-флуор-2-метилбензонітрилу (20,4г, 151ммоль), гідразин моногідрату (14,6мл, 302ммоль), та етанолу (80мл) гріли при кипінні під зворотним холодильником протягом 48 годин (Спосіб Η та cхема 3а). Суміш розбавляли водою (200мл). Осад фільтрували, промивали водою, та сушили, отримуючи білуватий твердий продукт (16,1г). Твердий продукт суспендували у діетилетері (400мл) та обробляли 2Η сумішшю гідрогенхлорид/етер (55мл, 110ммоль). Осад фільтрували, промивали діетил-етером, та сушили, отримуючи 4-гідразиніл-2-метилбензонітрил гідрохлорид як білий твердий матеріал (15,6г, 85,0ммоль, 56% виходу). 1Н ЯМР (400МГц, ДМСО-d6) δ млн.-1 8,42 (br. s., 1Η), 8,33 (br. s., 3Η), 7,51 (d, J=8,6Гц, 1Η), 6,81 (d, J=1,9Гц, 1Η), 6,74 (dd, J=8,6, 2,4Гц, 1Η), 2,35 (s, 3Η). EP-MC m/z 148 (M+H). Отримання 3 4-гідразиніл-2-(трифлуорметил)бензонітрил гідрохлорид Заголовну сполуку було отримано способом при отриманні 1 з 4-флуор-2(трифлуорметил)бензонітрилу (1,89г, 10ммоль), замість 2-хлор-4-флуорбензонітрилу, при 80°С, отримуючи білуватий твердий продукт (1,89г, 8,0ммоль, 80% виходу). ЕР-МС m/z 202 (М+Н). Отримання 4 4-гідразиніл-2-метоксибензонітрил гідрохло рид Заголовну сполуку було отримано способом при отриманні 1 з 4-флуор-2-метоксибензонітрилу 48 (4,97г, 32,9ммоль), замість 2-хлор-4флуорбензонітрилу, гріючи при кипінні під зворотним холодильником протягом ночі, отримуючи 4гідразиніл-2-метоксибензонітрил гідрохлорид 1 (3,54г, 17,8ммоль. 54% виходу) Н ЯМР (400МГц, ДМСО-d6) δ млн.-1 3,82 (s, 3Η), 6,44 (dd, J=8,46, 2,01Гц, 1Η), 6,64 (d, J=2,15Гц, 1Η), 7,41 (d, J=8,32Гц, 1Η), 7,99 (s, 2Η), 8,40 (s, 1Η). EP-MC m/z 164 (M+H). Отримання 5 5-гідразинілпіколінонітрил дигідрохлорид До розчину 5-амінопіколінонітрилу (1,0г, 8,4ммоль) у 20% водній сульфатній кислоті (20мл) при 0°С, повільно додавали натрій нітрит (590мг, 9,2ммоль) у воді (3мл), тримаючи температуру нижче 10°С. Цей розчин перемішували на льодяній бані протягом 30 хвилин та тоді обробляли повільно охолодженим льодом розчином станум(ІІ) хлориду дигідрату (5,7г, 25,2ммоль) у 20% водній сульфатній кислоті (20мл) тримаючи температуру нижче 10°С. Розчин перемішували при 0°С протягом 15 хвилин та нагрівали до кімнатної температури протягом 30 хвилин. Реакційну суміш нейтралізували амоній гідроксидом, та утворені солі стануму відфільтровували. Фільтрат екстрагували тричі етилацетатом, сушили магній сульфатом, фільтрували та випарювали. Утворений твердий залишок розчиняли в етилацетаті та тетрагідрофурані та обробляли 4Η гідрогенхлоридом у діоксані (приблизно 3мл). Суміш випарювали та утворений твердий продукт розтирали у порошок з діетил-етером та сушили під високим вакуумом протягом ночі, отримуючи 2:1 суміш 5гідразинілпіколінонітрил дигідрохлориду до вихідного матеріалу (875мг). ЕР-МС m/z 135 (М+Н). Отримання 6 6-гідразиніл-2-метилнікотинонітрил До суспензії 6-хлор-2-метилнікотинонітрилу (6,2ммоль) у 6,2мл етанолу, додавали гідразин моногідрат (9,3ммоль). Утворену суміш тоді гріли до 80°С протягом ночі. Суміш охолоджували до кімнатної температури та додавали 2мл води. Це гріли до 80°С знов до прозорого розчину та тоді дозволяли охолонути до кімнатної температури та зрештою у льодяній бані. Твердий матеріал збирали фільтруванням, промивали холодним 50% етанолом, та сушили під вакуумом, отримуючи 550мг потрібного твердого продукту. 1Н ЯМР -1 (400МГц, ДМСО-d6) δ млн. 2,41 (s, З Н), 4,41 (s, 2Η), 6,60 (br. s., 1Η), 7,66 (d, J=8,59Гц, 1Η), 8,47 (s, 1Η); EP-MC m/z 149 (М+Н). 49 Отримання 7 2-(бромметил)-4-флуорбензонітрил Розчин 2-метил-4-флуор-бензонітрилу (3,5г, 25,9ммоль) у 40мл карбон тетрахлориду обробляли N-бромсукцинімідом (4,6г, 25,9ммоль) та бензоїлпероксидом (157мг, 0,65ммоль). Суміш гріли при кипінні під зворотним холодильником протягом 3 годин, охолоджували до кімнатної температури та перемішували протягом ночі. Тверді продукти відфільтровували та промивали карбон тетрахлоридом. Фільтрат конденсували та очищали нормально-фазовою флешхроматографією на колонці на 50г силікагелю (градієнт 5-50% етилацетат/гексан). Два піки розділяли. Цим визначали, що другий пік елювання є потрібним продуктом. Чисті фракції цього піку поєднували та концентрували під вакуумом, отримуючи 2-(бромметил)-4-флуорбензонітрил (1,35г, 0,63ммоль, 25% виходу) як білий твердий матеріал. 1Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 4,79 (s, 2Η), 7,44 (dt, J=8,59, 2,69Гц, 1Η), 7,68 (dd, J=9,53, 2,55Гц, 1Η), 8,01 (dd, J=8,59, 5,64Гц, 1Η). Отоимання 8 4-флуор-2-(метоксиметил)бензонітрил Розчин 2-(бромметил)-4-флуорбензонітрилу (501мг, 2,3ммоль) у метанолі (5мл) обробляли натрій метоксидом (5,6мл 0,5Μ розчин у метанолі, 2,81ммоль) та перемішували протягом 1 години при кімнатній температурі і гріли до 55°С протягом 2 годин. Суміш охолоджували до кімнатної температури, конденсували до сухого стану та безпосередньо очищали нормально-фазовою флешхроматографією на колонці на 20г силікагелю (градієнт 5-60% етилацетат/гексан). Чисті фракції поєднували та концентрували під вакуумом, отримуючи 4-флуор-2-(метоксиметил)бензонітрил (110мг, 0,66ммоль, 28% виходу) як оливу. 1Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 7,97 (dd, J=8,46, 5,50Гц, 1Η), 7,46 (dd, J=9,53, 2,55Гц, 1Η), 7,39 (td, J=8,59, 2,69Гц, 1Η), 4,58 (s, 2Η), 3,37 (s, 3Η). Отримання 9 92670 50 4-гідразиніл-2-(метоксиметил)бензонітрил гідрохлорид Суміш 4-флуор-2-(метоксиметил)бензонітрилу (110мг, 0,67ммоль), гідразину моногідрату (133мг, 0,13мл, 2,6ммоль) та етанолу (5мл) гріли при кипінні під зворотним холодильником протягом ночі. Суміш охолоджували до кімнатної температури та конденсували. Залишок розчиняли у метанолі та обробляли 2,0Η гідрогенхлоридом у діетил-етері. Розчинник видаляли та твердий продукт сушили, отримуючи 4-гідразиніл-2(метоксиметил)бензонітрил гідрохлорид як білуватий твердий продукт. Отримання 10 2-((диметиламіно)метил)-4-флуорбензонітрил Суміш 2-(бромметил)-4-флуорбензонітрилу (423мг, 1,9ммоль) та 2,0Μ диметиламіну (4мл) перемішували при кімнатній температурі протягом 30 хвилин. Суміш тоді концентрували, очищали нормально-фазовою флеш-хроматографією на колонці, на 20г силікагелю (градієнт 5-45% етилацетат/гексан), та концентрували під вакуумом, отримуючи 2-((диметиламіно)метил)-4флуорбензонітрил (241мг, 1,35ммоль, 68%). 1Н ЯМР (400МГц, ДМСО-d6) δ млн.-1 7,92 (dd, J=8,59, 5,37Гц, 1Η), 7,42 (dd, J=9,94, 2,69Гц, 1Η),7,35 (td, J=8,46, 2,69Гц, 1Η), 3,56 (s, 2Η), 2,19 (s, 6Η). Отримання 11 2-((диметиламіно)метил)-4гідразинілбензонітрил дигідрохлорид Суміш 2-((диметиламіно)метил)-4флуорбензонітрилу (241мг, 1,35ммоль), гідразин моногідрату (101мг, 0,10мл, 2,0ммоль) та етанолу (5мл) гріли протягом ночі при 90°С. Суміш охолоджували до кімнатної температури та концентрували до сухого стану. Залишок розчиняли у діетилетері та обробляли 2,0Μ гідрогенхлоридом у діетил-етері. Утворений твердий продукт фільтрували та сушили, отримуючи 2((диметиламіно)метил)-4-гідразинілбензонітрил дигідрохлорид (430мг, 1,63ммоль, >100% виходу). 1 Н ЯМР (400МГц, ДМСО-d6) δ млн.-1 9,26 (s, 1Η), 7,80 (d, J=8,59Гц, 1Η), 7,36 (d, J=2,15Гц, 1Η), 7,08 (dd, J=8,59, 2,15Гц, 1Η), 4,35 (s, 2Η), 2,78 (s, 6Η). EP-MC m/z 191 (M+H). 51 Отримання 12 2-(бензилокси)-4-флуорбензонітрил Бензиловий спирт (3,25г, 30ммоль) повільно додавали при перемішуванні до суспензії натрій гідриду (1,15г, 28,7ммоль) у толуєні (50мл) при кімнатній температурі. Суміш перемішували протягом 30 хвилин та тоді додавали 2,4дифлуорбензонітрил та перемішування продовжували протягом ночі. Суміш гасили водою, екстрагували тричі етилацетатом, промивали розсолом, сушил и магній сульфатом, фільтрували та конденсували. Сирий продукт розчиняли у гарячому етилацетаті та розтирали у порошок з гексаном, отримуючи 2-(бензилокси)-4-флуорбензонітрил (5,4г, 23,8ммоль, 88% виходу) як білий твердий матеріал. 1Н ЯМР (400МГц, ДМСО-d6) δ млн.-1 5,30 (s, 2Η), 6,99 (td, J=8,46, 2,42Гц, 1Η), 7,29-7,51 (m, 6Η), 7,86 (dd, J=8,59, 6,44Гц, 1Η). Отримання 13 2-(бензилокси)-4-гідразинілбензонітрил Розчин 2-(бензилокси)-4-флуорбензонітрилу (4,8г, 21ммоль), в етанолі (80мл) обробляли гідразин моногідратом (2,6г, 2,5мл, 53ммоль) та гріли при кипінні під зворотним холодильником протягом 3 діб. Суміш охолоджували до кімнатної температури та концентрували. Воду додавали та залишок екстрагували тричі етилацетатом, сушили магній сульфатом, фільтрували та конденсували, отримуючи 2-(бензилокси)-4-гідразинілбензонітрил (3,8г, 15,8ммоль, 75% виходу) як білуватий твердий продукт. 1Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 4,27 (s, 2Η), 5,16 (s, 2Η), 6,36 (dd, J=8,73, 1,75Гц, 1Η), 6,61 (d, J=1,61Гц, 1Η), 7,30 (d, J=8,59Гц, 1Η), 7,32-7,51 (m, 5Η), 7,78 (s, 1Η). EP-MC m/z 240 (M+H). Отримання 14 Циклопент-1-енкарбальдегід До розчину натрій перйодату (28,3г, 0,13моль) у воді (250мл) додавали етил-етерний розчин (150мл) 1,2-циклогександіолу (12,0г, 0,10моль). Розчин перемішували протягом 30 хвилин при зовнішній температурі. До цього розчину додавали 20% водний калій гідроксид (40мл) та розчин перемішували протягом години. Шари розділяли та органічний шар промивали водою та розсолом та сушили магній сульфатом. Концентрація під вакуумом дала циклопент-1-енкарбальдегід як жовту 92670 52 оливу (6,0г, 62% виходу). Зворотно-фазова ВЕРХ на 4,6 50мм колонці С-18, tR=0,825 хвилин (10 до 90% ацетонітрил/вода протягом 4 хвилин при 4мл/хвилин з визначенням при 254нМ, при 20°С); 1 Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 1,83-1,93 (m, 2Η), 2,36 (td, J=7,65, 2,15Гц, 2Η), 2,50-2,59 (m, 2Η), 7,01-7,08 (m, 1Η), 9,73 (s, 1Η). Отримання 15 Метил 5-оксо-5,6,7,8-тетрагідронафталін-2карбоксилат Розчин 5-оксо-5,6,7,8-тетрагідронафталін-2карбонової кислоти (5,14г, 27,0ммоль) (Peakdale Molecular) у 4Η хлоридній кислоті у метанолі гріли при кипінні під зворотним холодильником протягом 18 годин. Розчин повертали до зовнішньої температури та концентрували під вакуумом. Залишок розбавляли етилацетатом та промивали насиченим розчином натрій гідрогенкарбонату та насиченим розчином натрій хлориду та сушили магній сульфатом. Фільтрування, а потім концентрація під вакуумом дали метил 5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат як коричневий твердий продукт (4,76г, 86% виходу). Зворотнофазова ВЕРХ на 4,6 50мм колонці С-18, tR=1,90 хвилин (10 до 90% ацетонітрил/вода протягом 4 хвилин при 4мл/хвилин з визначенням при 254нМ, при 20°С); 1Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 1,99-2,08 (m, 2Η), 2,58-2,66 (m, 2Η), 2,99 (t, J=6,04Гц, 2Η), 3,85 (s, 3Η), 7,83-7,87 (m, 1Η), 7,91 (d, J=0,81Гц, 1Η), 7,92-7,97 (m, 1Η). Отримання 16 етил 6-(4-флуорбензіліден)-5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат Заголовну сполуку було отримано способом А2. Сирий осад був сумішшю етил 5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилату, етил 6-(4флуорбензіліден)-5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилату та 6-(4флуорбензіліден)-5-оксо-5,6,7,8тетрагідронафталін-2-карбонової кислоти. Суміш комбінували із 4-флуорбензальдегідом (0,5мл), етанолом (40мл) та сумішшю 4Η гідрогенхлорид/діоксан (10мл) та гріли при кипінні під зворотним холодильником протягом 20 годин. Розчин виливали у 200мл води, фільтрували, та сушили, отримуючи етил 6-(4-флуорбензіліден)-5-оксо5,6,7,8-тетрагідронафталін-2-карбоксилат як білуватий твердий продукт (826мг, 2,55ммоль, 49% виходу). 1Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 1,33 (t, J=7,12Гц, 3Η), 3,06 (m, 4Η), 4,34 (q, J=6,98Гц, 2Η), 7,31 (t, J=8,86Гц, 2Η), 7,62 (dd, J=8,59, 5,64Гц, 53 2Η), 7,74 (s, 1Η), 7,94 (m, 2Η), 8,06 (d, J=8,59Гц, 1Η). EP-MC m/z 325 (M+H). Отримання 17 етил 7-(4-флуорбензіліден)-8-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат Заголовну сполуку було отримано способом А2 з 8-оксо-5,6,7,8-тетрагідронафталін-2карбонової кислоти та 4-флуорбензальдегіду як білуватий твердий продукт (64% виходу). 1Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 1,34 (t, J=7,12Гц, 3Η), 3,05 (m, 4Η), 4,34 (q, J=7,25Гц, 2Η), 7,30 (m, 2Η), 7,54 (d, J=7,79Гц, 1Η), 7,61 (m, 2Η), 7,74 (s, 1Η), 8,10 (dd, J=7,92, 2,01Гц, 1Η), 8,49 (d, J=1,88Гц, 1Η). EP-MC m/z 325 (M+H). Отримання 18 метил 6-(циклопентилметилен)-5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат До розчину метил 5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилату (3,4г, 16,7ммоль) у метанолі (30мл) додавали циклопентанкарбоксальдегід (3,3г, 33,3ммоль) та піролідин (2,78мл, 33,3ммоль). Розчин перемішували протягом 20 годин при зовнішній температурі. Реакційну суміш доповнювали 0,5мл циклопентанкарбоксальдегіду. Утворений осад збирали вакуумним фільтруванням, отримуючи метил 6(циклопентилметилен)-5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат як твердий продукт(2,8г, 60% виходу). РХ/МС на 4,6 50мм колонці С-18, tR=6,71 хвилин (10 до 90% ацетонітрил/вода протягом 8 хвилин при 2мл/хвилин з визначенням при 254нМ, при 50°С); EP-MC m/z 285 (М+Н); 1Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 1,241,39 (m, 2Η), 1,52-1,74 (m, 4Η), 1,76-1,89 (rn, 2Η), 2,77 (t, J=5,77Гц, 2Η), 2,79-2,90 (m, 1Η), 2,97 (t, J=6,44Гц, 2Η), 3,85 (s, 3Η), 6,71 (d, J=9,94Гц, 1Η), 7,88 (d, J=6,44Гц, 1Η), 7,91 (s, 1Η), 7,98 (d, J=8,06Гц, 1Η). Отримання 19 метил 6-(циклобутилметилен)-5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат Розчин метил 5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилату (600мг, 2,9ммоль) у тетрагідрфурані (10мл) охолоджували льодяною банею та обробляли 1,0Μ літій гексаметилдисилазидом у тетрагідрфурані (5мл). Після перемішування протягом 20 хвилин, циклобутанкарбоксальдегід (J. Med. Chem. 1989, 32, 1001-6) (24мл 0,5Μ розчин у тетрагідрофурані) повільно 92670 54 додавали та суміш нагрівали до кімнатної температури та перемішували протягом 3 діб. Суміш виливали у воду, екстрагували тричі етилацетатом, промивали розсолом, сушили магній сульфатом, фільтрували та концентрували. Сирий продукт очищали нормально-фазовою флешхроматографією на колонці на 50г силікагелю (градієнт 5-50% етилацетат/гексан). Чисті фракції поєднували та концентрували під вакуумом, отримуючи метил 6-(циклобутилметилен)-5-оксо5,6,7,8-тетрагідронафталін-2-карбоксилат (300мг, 1,1ммоль, 38% виходу). 1Н ЯМР (400МГц, ДМСОd6) δ млн.-1 1,81-2,03 (т, 4 Н), 2,14-2,27 (т, 2 Н), 2,71 (t, J=6,58Гц, 2Η), 2,93-3,00 (т, 2Η), 3,34-3,44 (т, 1Η), 3,88 (s, 3Η), 6,91 (d, J=9,13Гц, 1Η), 7,84-7,95 (m, 2Η), 8,01 (d, J=8,06Гц, 1Η). EP-MC m/z 271 (M+H). Отримання 20 (±)-метил 5-оксо-6-((тетрагідрофуран-3іл)метилен)-5,6,7,8-тетрагідронафталін-2карбоксилат До розчину метил 5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилату (240мг, 1,2ммоль) у метанолі (3мл) додавали (±)тетрагідрофуран-3-карбоксальдегід (240мг, 2,4ммоль) та піролідин (0,20мл, 2,4ммоль). Розчин перемішували протягом 20 годин при зовнішній температурі та протягом 4 годин при 45°С. Реакційну суміш концентрували під вакуумом. Хроматографія (на силікагелі, етилацетат/гексан) дала (±)-метил 5-оксо-6-((тетрагідрофуран-3іл)метилен)-5,6,7,8-тетрагідронафталін-2карбоксилат, суміш стереоізомерів, як оранжеву оливу (200мг, 58% виходу). РХ/МС на 4,6 50мм колонці С-18, tR=2,52 хвилин (10 до 90% ацетонітрил/вода протягом 4 хвилин при 4мл/хвилину з визначенням при 254нМ, при 50°С); EP-MC m/z 287 (М+Н). Отримання 21 метил 5-оксо-6-((тетрагідро-2Н-піран-4іл)метилен)-5,6,7,8-тетрагідронафталін-2карбоксилат Розчин метил 5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилату (2,9ммоль), тетрагідро-піран-4-карбальдегіду (3,2ммоль), та піперидину (3,2ммоль) у 6мл метанолу гріли до 65°С протягом ночі. Охолоджену суміш розбавляли етилацетатом, промивали водою та розсолом, сушили натрій сульфатом, та концентрували. Залишок очищали силікагелем, елюючи етилацетатом у гексан від 10% до 40%, отримуючи 430мг потрібного продукту. ЕР-МС m/z 301 (М+Н). 55 92670 56 Отримання 22 трет-бутил 4-((6-(метоксикарбоніл)-1-оксо-3,4дигідронафталін-2(1Н)-іліден)метил)піперидин-1карбоксилат Отримано способом з отримання 21, застосовуючи трет-бутил 4-формілпіперидин-1карбоксилат, замість тетрагідро-піран-4карбальдегіду, отримуючи заголовну сполуку з 71% виходу. ЕР-МС m/z 422 (M+Na). Отримання 23 метил 6-(5-метил-2-фурилметилен)-5-оксо5,6,7,8-тетрагідронафталін-2-карбоксилат Заголовну сполуку було отримано з 5-оксо5,6,7,8-тетрагідронафталін-2-карбонової кислоти метил-естеру (396мг, 1,9ммоль) та 5-метил-2фуральдегіду способом А3. (192мг, 2,0ммоль). ЕРМС m/z 297 (М+Н). Отримання 24 Метил 6-(циклопент-1-ен-1-ілметилен)-5-оксо5,6,7,8-тетрагідронафталін-2-карбоксилат Заголовну сполуку було отримано з 5-оксо5,6,7,8-тетрагідронафталін-2-карбонової кислоти метил-естеру (396мг, 1,9ммоль) та 1циклопентенкарбальдегіду (220мг, 2,0ммоль) способом A3 з 70% виходу. ЕР-МС m/z 283 (М+Н). Отримання 25 метил 6-(2-фурилметилен)-5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат Заголовну сполуку було отримано з 5-оксо5,6,7,8-тетрагідронафталін-2-карбонової кислоти метил-естеру (396мг, 1,9ммоль) та 2-фуральдегіду (192мг, 2,0ммоль) способом A3 з 80% виходу. ЕРМС m/z 283 (М+Н). Отримання 26 метил 6-(3-фурилметилен)-5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат Заголовну сполуку було отримано з 5-оксо5,6,7,8-тетрагідронафталін-2-карбонової кислоти метил-естеру (396мг, 1,9ммоль) та 3-фуральдегіду (192мг, 2,0ммоль) способом A3 з 80% виходу. ЕРМС m/z 283 (М+Н). Отримання 27 метил 6-[(2-метил-1,3-тіазол-5-іл)метилен]-5оксо-5,6,7,8-тетрагідронафталін-2-карбоксилат Заголовну сполуку було отримано з 5-оксо5,6,7,8-тетрагідронафталін-2-карбонової кислоти метил-естеру (396мг, 1,9ммоль) та 2-метил-1,3тіазол-5-карбальдегіду (220мг, 2,0ммоль) способом A3 з 60% виходу. ЕР-МС m/z 314 (М+Н). Отримання 28 метил 6-(ізоксазол-5-ілметилен)-5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилат Заголовну сполуку було отримано з 5-оксо5,6,7,8-тетрагідронафталін-2-карбонової кислоти метил-естеру (396мг, 1,9ммоль) та ізоксазол-5карбальдегіду (200мг, 2,0ммоль) способом A3 з 55% виходу. ЕР-МС m/z 284 (М+Н). Отримання 29 етил [3-(4-флуорбензіліден)-4-оксо-3,4дигідро-2Н-хромен-7-іл]ацетат Заголовну сполуку було отримано з метил [4оксо-3,4-дигідро-2Н-хромен-7-іл]ацетату (L.A. Reiter et al. Biorganic та Medicianal Chemistry Letters, 1997, 7 2307-2312) та 4флуорбензальдегіду способом А2 з 45% виходу. ЕР-МС m/z 341 (М+Н). 57 92670 58 Отримання 30 метил 3-(4-флуорбензіліден)-4-оксохроман-7карбоксилат Заголовну сполуку було отримано з метил 4оксохроман-7-карбоксилат (Koch, K., та Biggers, M. S. J. Org. Chem. 1994, 59, 1216-1218) та 4флуорбензальдегіду способом A2, застосовуючи метанол та 4Η гідрогенхлорид/діоксан. Білуватий твердий продукт (76% виходу). 1Н ЯМР (400МГц, ДМСО-d6) δ млн.-1 3,88 (s, ЗΗ), 5,48 (s, 1Η), 7,35 (t, J=8,59Гц, 2Η), 7,50-7,61 (m, 3Η), 7,66 (d, J=7,25Гц, 1Η), 7,80 (s, 1Η), 8,01 (d, J=8,06Гц, 1Η). Отримання 31 метил 3-(циклопентилметилен)-4-оксохроман7-карбоксилат Заголовну сполуку було отримано загальним способом А1 з метил 4-оксохроман-7карбоксилату (Koch, K., та Biggers, Μ. S. J. Org. Chem. 1994, 59, 1216-1218) та циклопентанкарбоксальдегіду як білуватий твердий продукт (2,12г, 7,42ммоль, 76% виходу). ЕР-МС m/z 287 (М+Н). Отримання 32 метил 3-(2-метилпропіліден)-4-оксохроман-7карбоксилат Заголовну сполуку було отримано загальним способом А1 з метил 4-оксохроман-7карбоксилату (Koch, K., та Biggers, M. S. J. Org. Chem. 1994, 59, 1216-1218) та ізобутиральдегіду. Після перемішування протягом ночі, розчин розподіляли між 1Η гідрогенхлоридом та етилацетатом. Органічні шари промивали 1Η гідрогенхлоридом та розсолом, сушили (натрій сульфат), та концентрували. Сирий продукт очищали флешхроматографією (0 до 20% етилацетат/гексан), отримуючи метил 3-(2-метилпропіліден)-4оксохроман-7-карбоксилат як оливний твердий продукт (730мг, 2,8ммоль, 58% виходу). 1Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 7,95 (d, J=8,2Гц, 1Η), 7,62 (dd, J=8,2, 1,6Гц, 1Η), 7,53 (d, J=1,6Гц, 1Η), 6,65 (dt, J=10,3, 1,7Гц, 1Η), 5,22 (d, J=1,6Гц, 2Η), 3,88 (s, 3Η), 2,73-2,86 (m, 1Η), 1,04 (d, J=6,6Гц, 6Η). EP-MC m/z 261 (M+H). Отримання 33 метил 3-(циклопропілметилен)-4-оксохроман7-карбоксилат Заголовну сполуку було отримано способом А1 з метил 4-оксохроман-7-карбоксилату (Koch, K., та Biggers, Μ. S. J. Org. Chem. 1994, 59, 1216-1218) та циклопропанкарбоксальдегіду як білуватий твердий продукт (1,14г, 91% виходу). 1Н ЯМР (400МГц, ДМСО-d6) δ млн.-1 0,75-0,86 (m, 2Η), 1,001,11 (m, 2Η), 1,80-1,95 (m, 1Η), 3,87 (s, 3Η), 5,31 (d, J=1,56Гц, 2Η), 6,27 (d, J=11,33Гц, 1Η), 7,52 (d, J=1,56Гц, 1Η), 7,60 (dd, J=8,20, 1,56Гц, 1Η), 7,94 (d, J=8,20Гц, 1Η). EP-MC m/z 259 (M+H). Отримання 34 метил 3-(циклопентенілметилен)-4оксохроман-7-карбоксилат До розчину метил 4-оксохроман-7карбоксилату (500мг, 2,4ммоль) у метанолі (5мл) додавали циклопент-1-енкарбальдегід (465мг, 4,8ммоль) та піролідин (0,40мл, 4,8ммоль). Розчин перемішували протягом години при зовнішній температурі. Утворений коричневий осад збирали вакуумним фільтруванням та сушили, отримуючи метил 3-(циклопентенілметилен)-4-оксохроман-7карбоксилат (444мг, 64% виходу). РХ/МС на 4,6 50мм колонці С-18, tR=6,49 хвилин (10 до 90% ацетонітрил/вода протягом 8 хвилин при 2мл/хвилин з визначенням при 254нМ, при 50°С); ЕР-МС m/z 285 (М+Н). 1Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 1,88-1,99 (m, 2Η), 2,43 (d, J=13,16Гц, 2Η), 2,63 (t, J=6,98Гц, 2Η), 3,85 (s, 3Η), 5,36 (s, 2Η), 6,45 (br. s., 1Η), 7,37 (s, 1Η), 7,49 (d, J=1,34Гц, 1Η), 7,60 (dd, J=8,06, 1,61Гц, 1Η), 7,93 (d, J=8,32Гц, 1Η). Отримання 35 3-(4-флуорбензіліден)-4-оксохроман-7-іл трифлуорметансульфонат Заголовну сполуку було отримано способом А1 з 4-оксохроман-7-іл трифлуорметансульфонату (500мг, 1,7ммоль) (Патент США №5,550,152; Приклад 1, Етап С) та 4-флуорбензальдегіду (0,21мл, 2,0ммоль), отримуючи 3-(4-флуорбензіліден)-4оксохроман-7-іл трифлуорметансульфонат (260мг, 0,65ммоль, 40% виходу) як твердий продукт. 1Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 5,52 (d, J=1,88Гц, 2Η), 7,25 (dd, J=8,73, 2,28Гц, 1Η), 7,31-7,39 (m, 3Η), 7,56 (dd, J=8,73, 5,50Гц, 2Η), 7,80 (s, 1Η), 8,06 (d, J=8,86Гц, 1Η). EP-MC m/z 403 (М+Н). 59 92670 60 Отримання 36 N-(6-(циклопентилметилен)-5-оксо-5,6,7,8тетрагідронафталін-2-іл)ацетамід Суміш 6-ацетамідо-1-тетрадону (Ryan Scientific) (200мг, 0,98ммоль) та циклопентанкарбоксальдегіду (0,21мл, 1,9ммоль) у метанолі (2мл) обробляли піролідином (0,25мл, 2,9ммоль) при кімнатній температурі протягом 1 години і гріли при 55°С протягом ночі. Суміш охолоджували до кімнатної температури, обробляли 1Η гідрогенхлоридом (4мл) фільтрували, елюючи сумішшю 90% дихлорметан/10% етилацетат та конденсували фільтрат, отримуючи (Ε)-Ν-(6(циклопентилметилен)-5-оксо-5,6,7,8тетрагідронафталін-2-іл)ацетамід (200мг, 0,71ммоль, 72% виходу), як кремову пінку. 1Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 1,25-1,44 (m, 2Η), 1,521,76 (m, 4Η), 1,77-1,90 (m, 2Η), 2,08 (s, 3Η), 2,702,92 (m, 5Η), 6,63 (d, J=9,67Гц, 1Η), 7,49 (dd, J=8,59, 2,15Гц, 1Η), 7,59-7,66 (m, 1Η), 7,86 (d, J=8,59Гц, 1Η), 10,23 (s, 1Η). EP-MC m/z 284 (M+H). Приклад 1 етил 2-(3-хлор-4-ціанофеніл)-3-(4флуорфеніл)-3,3а,4,5-тетрагідро-2Нбензо[g]індазол-7-карбоксилат Заголовну сполуку було отримано з етил 6-(4флуорбензіліден)-5-оксо-5,6,7,8тетрагідронафталін-2-карбоксилату (Отримання 16; 324мг, 1,0ммоль) та 2-хлор-4гідразинілбензонітрил гідрохлориду (Отримання 1; 306мг, 1,5ммоль) способом В (жовтий твердий продукт, 394мг, 0,830ммоль, 83% виходу). Заголовна сполука головним чином представляла (±)етил (3RS,3аRS)-2-(3-хлор-4-ціанофеніл)-3-(4флуорфеніл)-3,3а,4,5-тетрагідро-2Нбензо[g]індазол-7-карбонову кислоту. 1Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 0,80 (m, 1Η), 1,31 (t, J=7,12Гц, 3Η), 1,79 (m, 1Η), 2,95 (m, 2Η), 3,97 (ddd, J=13,49, 11,21, 4,83Гц, 1Η), 4,31 (q, J=6,98Гц, 2Η), 5,94 (d, J=11,28Гц, 1Η), 7,15 (m, 6Η), 7,66 (d, J=8,86Гц, 1Η), 7,80 (s, 1Η), 7,85 (dd, J=8,19, 1,75Гц, 1Η), 8,16 (d, J=8,06Гц, 1Η). EP-MC m/z 474 (M+H). Приклад 2 2-(3-хлор-4-ціанофеніл)-3-(4-флуорфеніл)3,3а,4,5-тетрагідро-2Н-бензо[g]індазол-7карбонова кислота Заголовну сполуку було отримано з етил 2-(3хлор-4-ціанофеніл)-3-(4-флуорфеніл)-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбоксилату (Приклад 1; 330мг, 0,696ммоль) способом С (жовтий твердий продукт, 297мг, 0,666ммоль, 96% виходу). Заголовна сполука головним чином представляла (+)-(3RS,3aRS)-2-(3-хлор-4-ціанофеніл)3-(4-флуорфеніл)-3,3а,4,5-тетрагідро-2Нбензо[g]індазол-7-карбонову кислоту. 1Н ЯМР (400МГц, ДMCO-d6) δ млн.-1 0,80 (m, 1Η), 1,79 (m, 1Η), 2,93 (m, 2Η), 3,96 (m, 1Η), 5,93 (d, J=11,01Гц, 1Η), 7,15 (m, 6Η), 7,66 (d, J=8,59Гц, 1Η), 7,78 (s, 1Η), 7,83 (dd, J=8,19, 1,48Гц, 1Η), 8,14 (d, J=8,06Гц, 1Η), 13,07 (s, 1Η). EP-MC m/z 446 (M+H). Приклад 3 (3R,3аR)-2-(3-хлор-4-ціанофеніл)-3-(4флуорфеніл)-3,3а,4,5-тетрагідро-2Нбензо[g]індазол-7-карбонова кислота Заголовну сполуку було отримано з 2-(3-хлор4-ціанофеніл)-3-(4-флуорфеніл)-3,3а,4,5тетрагідро-2Н-бензо[g]індазол-7-карбонової кислоти, отриманої у прикладі 2, застосовуючи хіральне розділення (наприклад, Спосіб G) (Chiralcel OJ-H 30 250мм, 50% етанол/карбон діоксид, 70мл/хвилин). Перший пік елювання: хіральна ВЕРХ tR=2,3 хвилин (Chiralcel OJ-H 4,6 250мм; 50% етанол/карбон діоксид, 3мл/хвилин). Приклад 4 (3S,3аS)-2-(3-хлор-4-ціанофеніл)-3-(4флуорфеніл)-3,3а,4,5-тетрагідро-2Нбензо[g]індазол-7-карбонова кислота Заголовну сполуку було отримано з 2-(3-хлор4-ціанофеніл)-3-(4-флуорфеніл)-3,3а,4,5
ДивитисяДодаткова інформація
Назва патенту англійськоюPyrazoline compounds as mineralocorticoid receptor antagonists , pharmaceutical use thereof, composition based thereon
Автори англійськоюMeyers, Marvin Jay, Arhancet, Graciela Barbieri, Chen, Xiangyang, Hockerman, Susan Landis, Long, Scott, Allen, Mahoney, Matthew, William, Reitz, David, Bruce, Rico, Joseph Gerace
Назва патенту російськоюПиразолиновые соединения и их фармацевтическое применение, композиция на их основе
Автори російськоюМейэрс Марвин Джей, Аргансет Гресиэла Барбиэри, Чен Киянгйан, Гокерман Сюзан Ландис, Лонг Скотт Аллен, Махони Метью Виллиям, Рейтс Девид Брюс, Рико Джозеф Герас
МПК / Мітки
МПК: A61K 31/4162, C07D 231/54, A61K 31/416, C07D 493/04, C07D 401/04, C07D 405/04, A61P 9/12
Мітки: сполуки, застосування, піразолінові, фармацевтичне, основі, композиція
Код посилання
<a href="https://ua.patents.su/66-92670-pirazolinovi-spoluki-ta-kh-farmacevtichne-zastosuvannya-kompoziciya-na-kh-osnovi.html" target="_blank" rel="follow" title="База патентів України">Піразолінові сполуки та їх фармацевтичне застосування, композиція на їх основі</a>
Попередній патент: Вітроенергетична установка
Наступний патент: Привід круглов’язальної машини
Випадковий патент: Привід круглов'язальної машини












