Сполуки піридазинону та їх використання як інгібіторів daao
Номер патенту: 111851
Опубліковано: 24.06.2016
Автори: Фарнабі Вільям, Лівермор Девід, Кер Катріна, Філдхаус Шарлот, Мілер Девід, Хезел Кетрін, Кінсела Наташа, Мерчант Кевін
Формула / Реферат
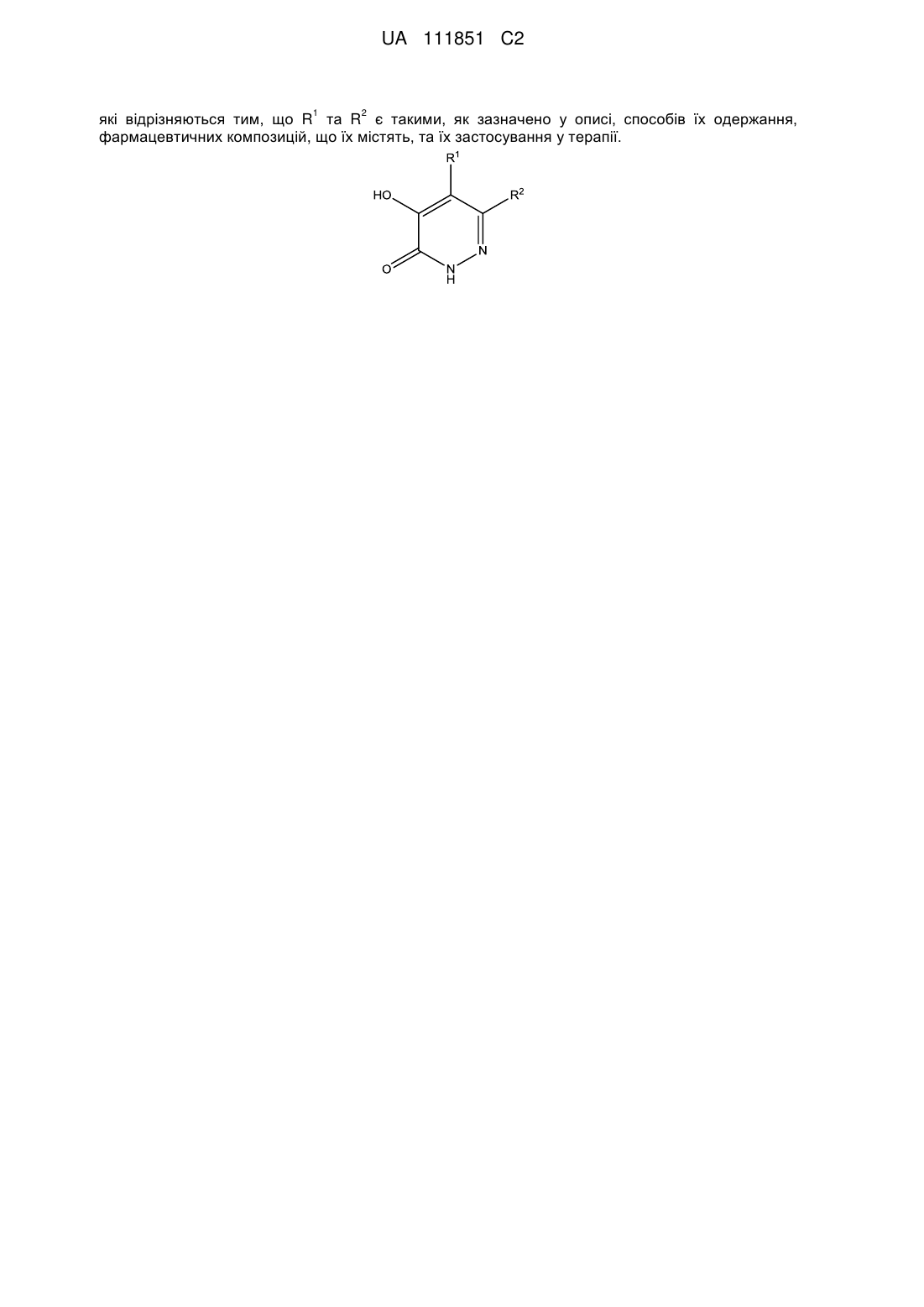
1. Сполука формули (І)
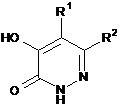 , (I)
, (I)
у якій
R1 означає атом гідрогену або фтору або трифторметильну групу;
R2 означає групу -X-Y-R3;
кожен з X та Y незалежно означає зв'язок, атом оксигену або групу -С(O), -S(O)n, -C(O)NR4, -S(O)2NR4, -NR4,
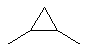 ,
, ![]() або -CR4R5-, за умови, що X та Y не можуть обидва одночасно означати зв'язок, та за умови, якщо як X, так і Y означають інше, ніж зв’язок, щонайменше один X та Y означає -CR4R5-;
або -CR4R5-, за умови, що X та Y не можуть обидва одночасно означати зв'язок, та за умови, якщо як X, так і Y означають інше, ніж зв’язок, щонайменше один X та Y означає -CR4R5-;
n являє собою 0, 1 або 2;
кожен R4 незалежно означає атом гідрогену або С1-С6алкіл, або С1-С6галоалкільну групу;
кожен R5 незалежно означає атом гідрогену, С1-С6алкіл або С1-С6галоалкільну групу, або =СН-;
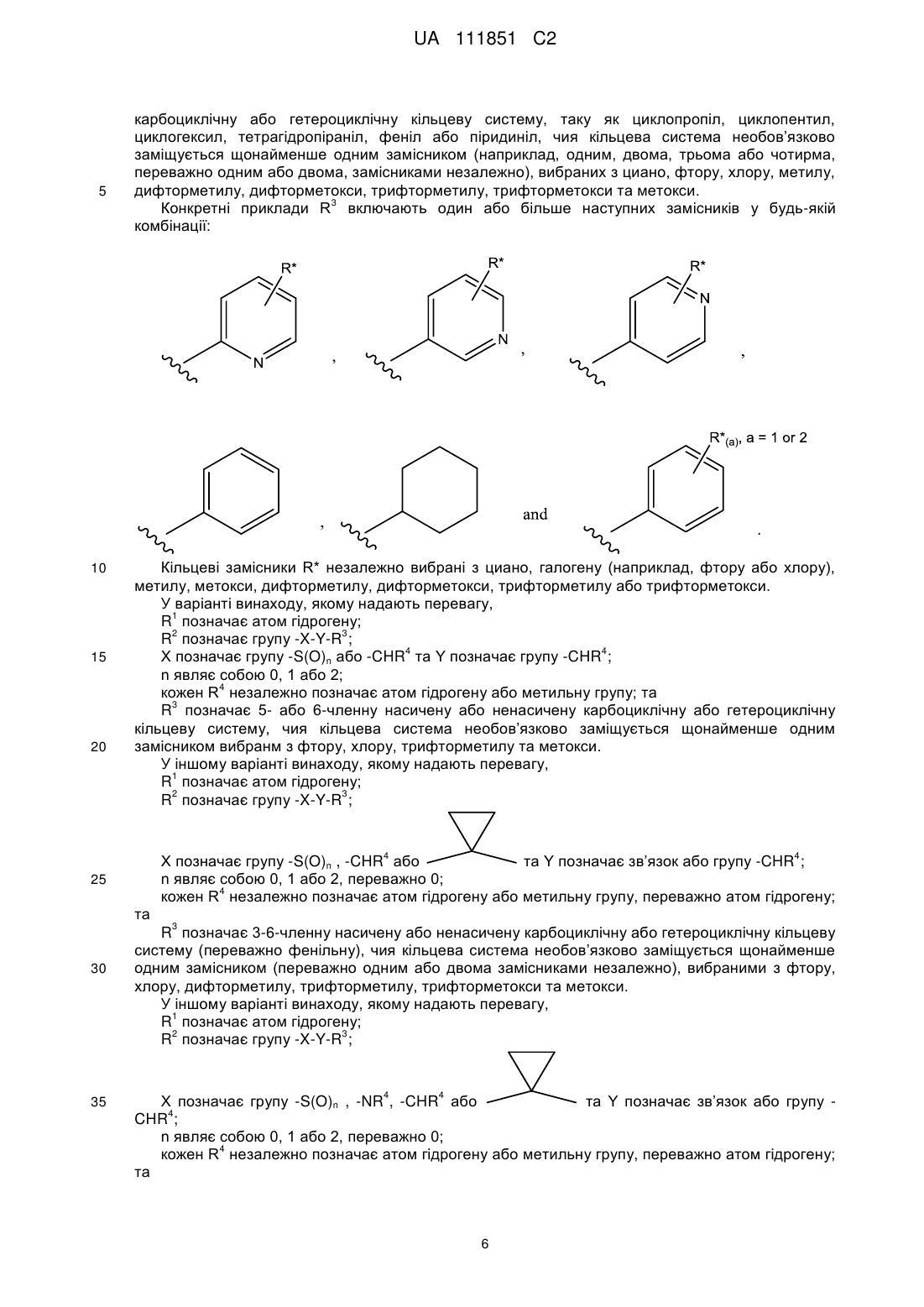
R3 означає 3-10-членну насичену або ненасичену карбоциклічну або гетероциклічну кільцеву систему, сама кільцева система необов'язково заміщена щонайменше одним замісником, вибраним з галогену, гідроксилу, ціано, оксо, С1-С6алкілу, С2-С6алкенілу, С1-С6галоалкілу, С1-С6гідроксіалкілу, С1-С6алкокси, С1-С6галоалкокси, С1-С6алкілтіо, С1-С6алкілсульфінілу, С1-С6алкілсульфонілу, С1-С6алкілкарбонілу, С1-С6алкілкарбонілокси, С1-С6алкоксикарбонілу, аміно (-NH2), -CON(R6)2, С1-С6алкіламіно, ді-(С1-С6алкіл)аміно, С3-С6циклоалкілу, С3-С6циклоалкілокси, С3-С6циклоалкілметилу, -[O]р-(СН2)q-O-R7 та 4-6-членного насиченого або ненасиченого гетероциклічного кільця (необов'язково заміщеного щонайменше одним замісником, вибраним з С1-С4алкілу та C1-C4алкокси);
кожен R6 незалежно означає атом гідрогену або С1-С6алкільну групу;
р являє собою 0 або 1;
q являє собою 1, 2, 3 або 4; та
R7 означає С1-С6алкільну групу;
або її фармацевтично прийнятна сіль.
2. Сполука за п. 1, де R1 означає атом гідрогену.
3. Сполука за п. 1 або п. 2, де X означає зв'язок, атом оксигену або групу -С(O), -S(O)n, -C(O)NR4, -S(O)2NR4, -NR4,  ,
, ![]() або -CR4R5-, та Y означає зв'язок або -CR4R5-.
або -CR4R5-, та Y означає зв'язок або -CR4R5-.
4. Сполука за п. 3, де X означає групу -S(O)n, -CHR4 або ![]() , та Y означає зв'язок або групу -CHR4.
, та Y означає зв'язок або групу -CHR4.
5. Сполука за п. 4, де кожен R4 незалежно означає атом гідрогену або метильну групу.
6. Сполука за будь-яким з пп. 1-5, де у R3 3-10-членна насичена або ненасичена карбоциклічна або гетероциклічна кільцева система вибрана з фенілу, піридинілу, оксазолілу, піразинілу, циклопропілу, циклопентилу, циклогексилу, тетрагідропіранілу, 2,3-дигідробензофуранілу, піримідинілу, імідазо[1,2-а]піридинілу, піразолілу, тіазолілу та піперидинілу.
7. Сполука за будь-яким з пп. 1-5, де R3 означає необов'язково заміщену 3-6-членну насичену або ненасичену карбоциклічну або гетероциклічну кільцеву систему.
8. Сполука за п. 7, де
R1 означає атом гідрогену;
R2 означає групу -X-Y-R3, в якій
X означає групу S(O)n, -CHR4 та Y означає групу -CHR4;
n являє собою 0, 1 або 2;
кожен R4 незалежно означає атом гідрогену або метильну групу, та
R3 означає 5- або 6-членну насичену або ненасичену карбоциклічну або гетероциклічну кільцеву систему, гетероциклічну кільцеву систему, в якій кільцева система необов'язково заміщена щонайменше замісником, вибраним з фтору, хлору, трифторметилу або метокси.
9. Сполука за п. 1, де
R1 означає атом гідрогену;
R2 означає групу -X-Y-R3, в якій
X означає групу S(O)n, -CHR4 або ![]() , та Y означає зв'язок або групу -CHR4;
, та Y означає зв'язок або групу -CHR4;
n являє собою 0, 1 або 2, переважно 0;
кожен R4 незалежно означає атом гідрогену або метильну групу, переважно атом гідрогену; та
R3 означає 3-6-членну насичену або ненасичену карбоциклічну або гетероциклічну кільцеву систему, гетероциклічну кільцеву систему, в якій кільцева система необов'язково заміщена щонайменше замісником, вибраним з фтору, хлору, дифторметилу, трифторметилу, трифторметокси або метокси.
10. Сполука формули (І) за п. 1, вибрана з групи, яка складається з:
4-гідрокси-6-(2-фенілетил)піридазин-3(2Н)-ону,
6-[2-(4-фторфеніл)етил]-4-гідроксипіридазин-3(2Н)-ону,
4-гідрокси-6-{2-[5-(трифторметил)піридин-2-іл]етил}піридазин-3(2Н)-ону,
6-[(4-xлоробензил)сульфаніл]-4-гідроксипіридазин-3(2Н)-ону,
4-гідрокси-6-{2-[6-(трифторметил)піридин-3-іл]етил}піридазин-3(2Н)-ону,
6-[2-(3-фторфеніл)етил]-4-гідроксипіридазин-3(2Н)-ону,
6-[2-(2-фторфеніл)етил]-4-гідроксипіридазин-3(2Н)-ону,
6-[2-(3,5-дифторфеніл)етил]-4-гідроксипіридазин-3(2Н)-ону,
6-[2-(3,4-дифторфеніл)етил]-4-гідроксипіридазин-3(2Н)-ону,
4-гідрокси-6-{2-[3-(трифторметокси)феніл]етил}піридазин-3(2Н)-ону,
4-гідрокси-6-{2-[3-(трифторметил)феніл]етил}піридазин-3(2Н)-ону,
4-гідрокси-6-{2-[5-(трифторметил)піридин-3-іл]етил}піридазин-3(2Н)-ону,
6-(2-циклогексилетил)-4-гідроксипіридазин-3(2Н)-ону,
6-(2-циклопропілетил)-4-гідроксипіридазин-3(2Н)-ону,
6-(2-циклопентилетил)-4-гідроксипіридазин-3(2Н)-ону,
4-гідрокси-6-[2-(4-метоксициклогексил)етил]піридазин-3(2Н)-ону,
6-[2-(2,4-дифторфеніл)етил]-4-гідроксипіридазин-3(2Н)-ону,
6-{2-[3-(дифторметил)феніл]етил}-4-гідроксипіридазин-3(2Н)-ону,
6-бензил-4-гідроксипіридазин-3(2Н)-ону,
6-[2-(3-хлорофеніл)етил]-4-гідроксипіридазин-3(2Н)-ону,
4-гідрокси-6-(1-фенілциклопропіл)піридазин-3(2Н)-ону,
4-[2-(5-гідроксі-6-оксо-1,6-дигідропіридазин-3-іл)етил]бензонітрилу,
6-[2-(3,4-диметоксифеніл)етил]-4-гідроксипіридазин-3(2Н)-ону,
6-[1-(4-фторфеніл)циклопропіл]-4-гідроксипіридазин-3(2Н)-ону,
6-[1-(4-фторфеніл)етил]-4-гідроксипіридазин-3(2Н)-ону,
4-гідрокси-6-{1-[3-(трифторметил)феніл]етил}піридазин-3(2Н)-ону,
6-((циклопропілметил)(метил)аміно)-4-гідроксипіридазин-3(2Н)-ону,
6-((циклогексилметил)(метил)аміно)-4-гідроксипіридазин-3(2Н)-ону,
6-(3-хлоробензил)-4-гідроксипіридазин-3(2Н)-ону,
6-(4-хлоробензил)-4-гідроксипіридазин-3(2Н)-ону,
6-(циклогексилметил)-4-гідроксипіридазин-3(2Н)-ону,
6-(4-фторбензил)-4-гідроксипіридазин-3(2Н)-ону,
6-(2-хлоро-6-фторбензил)-4-гідроксипіридазин-3(2Н)-ону,
6-(2-хлоробензил)-4-гідроксипіридазин-3(2Н)-ону,
6-(3-фторбензил)-4-гідроксипіридазин-3(2Н)-ону,
6-(2-фторбензил)-4-гідроксипіридазин-3(2Н)-ону,
6-(4-метилбензил)-4-гідроксипіридазин-3(2Н)-ону,
6-(3-метилбензил)-4-гідроксипіридазин-3(2Н)-ону,
4-гідрокси-6-(3-(трифторметил)бензил)піридазин-3(2Н)-ону,
4-гідрокси-6-{2-[5-(трифторметил)піридин-3-іл]етил}піридазин-3(2Н)-ону,
4-гідроксі-6-[2-(оксан-4-іл)етил]піридазин-3(2Н)-ону,
6-{[(4-фторфеніл)метил](метил)аміно}-4-гідроксипіридазин-3(2Н)-ону,
6-[2-(2-хлоро-6-фторфеніл)етил]-4-гідроксипіридазин-3(2Н)-ону,
6-{[3,5-біс(трифторметил)феніл]метил}-4-гідроксипіридазин-3(2Н)-ону,
6-(1-фенілетил)-4-гідроксипіридазин-3(2Н)-ону,
6-(циклопропілметил)-4-гідрокси-2,3-дигідропіридазин-3-ону,
4-гідрокси-6-{1-[4-(трифторметил)феніл]циклопропіл}-2,3-дигідропіридазин-3-ону,
6-{2-[2-хлоро-4-(трифторметил)феніл]етил}-4-гідрокси-2,3-дигідропіридазин-3-ону,
6-{2-[2,4-біс(трифторметил)феніл]етил}-4-гідрокси-2,3-дигідропіридазин-3-ону,
6-{2-[3,4-біс(трифторметил)феніл]етил}-4-гідрокси-2,3-дигідропіридазин-3-ону,
4-гідрокси-6-(3-метил-4-(трифторметил)фенетил)піридазин-3(2Н)-ону,
3,4-біс(бензилокси)-6-((3-хлоро-4-(трифторметил)феніл)етил)-піридазину,
4-гідрокси-6-{2-[2-метил-4-(трифторметил)феніл]етил}-2,3-дигідропіридазин-3-ону,
6-{2-[3,5-дифтор-4-(трифторметил)феніл]етил}-4-гідрокси-2,3-дигідропіридазин-3-ону,
6-{2-[3-фтор-4-(трифторметил)феніл]етил}-4-гідрокси-2,3-дигідропіридазин-3-ону,
або її фармацевтично прийнятні солі.
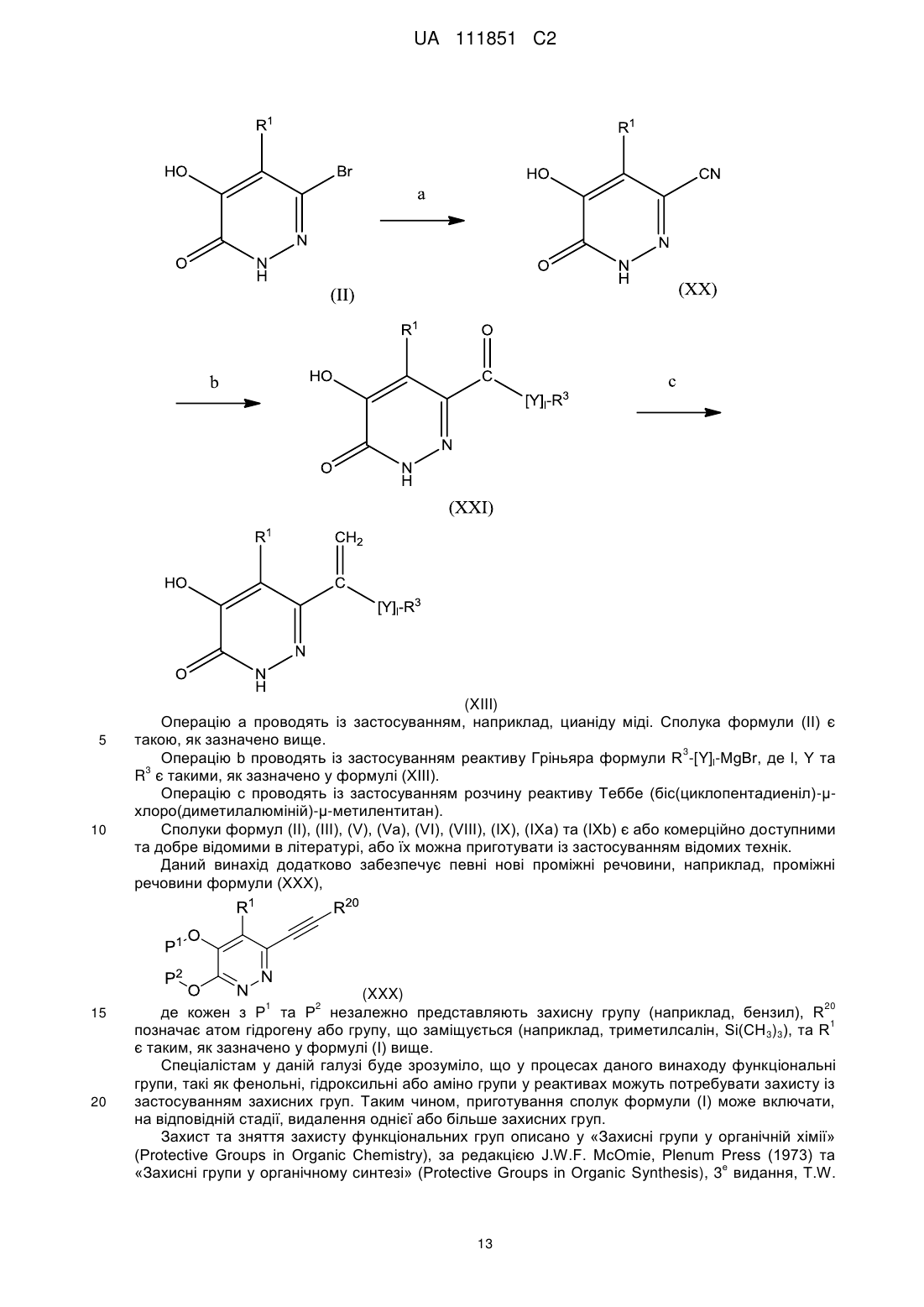
11. Спосіб одержання сполуки формули (І) або її фармацевтично прийнятної солі, як зазначено у п. 1, за яким здійснюють:
(і) коли X означає атом сірки або коли X являє собою зв'язок та Y означає атом сірки,
реакцію сполуки формули (II)
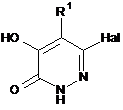 , (II)
, (II)
у якій Hal означає атом галогену, та R1 є таким, як зазначено у формулі (І), зі сполукою формули (III): HS-[Y]t-R3, де t являє собою 0 або 1, та Y та R3 є такими, як зазначено у формулі (І); або
(іі) коли X означає SO або коли X являє собою зв'язок та Y означає SO,
окислення сполуки формули (IV)
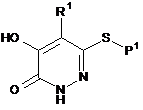 , (IV)
, (IV)
у якій Р1 означає захисну групу, та R1 є таким, як зазначено у формулі (І), відповідним окиснюючим агентом, з наступною реакцією зі сполукою формули (V): L1-[Y]w-R3, де w являє собою 0 або 1, L1 означає групу, що відходить, а Y та R3 є такими, як зазначено у формулі (І); або
(ііі) коли X означає SO2 або коли X являє собою зв'язок та Y означає SО2,
окислення сполуки формули (IV), як зазначено у п. (іі) вище, відповідним окиснюючим агентом, з наступною реакцією зі сполукою формули (V), як зазначено у п. (іі) вище; або
(iv) коли X означає атом оксигену або коли X являє собою зв'язок та Y означає атом оксигену,
реакцію сполуки формули (II), як зазначено у п. (і) вище, зі сполукою формули (VI): HO-[Y]z-R3, де z являє собою 0 або 1, та Y та R3 є такими, як зазначено у формулі (І); або
(v) коли X означає С(О) або коли X являє собою зв'язок та Y означає С(O),
реакцію сполуки формули (II), як зазначено у п. (і) вище, з відповідним окиснюючим агентом, з наступним додаванням активуючого агента та реакцією зі сполукою формули (Va): M-[Y]w-R3, де М являє собою Li або MgR20, R20 означає атом галогену, а w, Y та R3 є такими, як зазначено у формулі (V) у п. (іі) вище; або
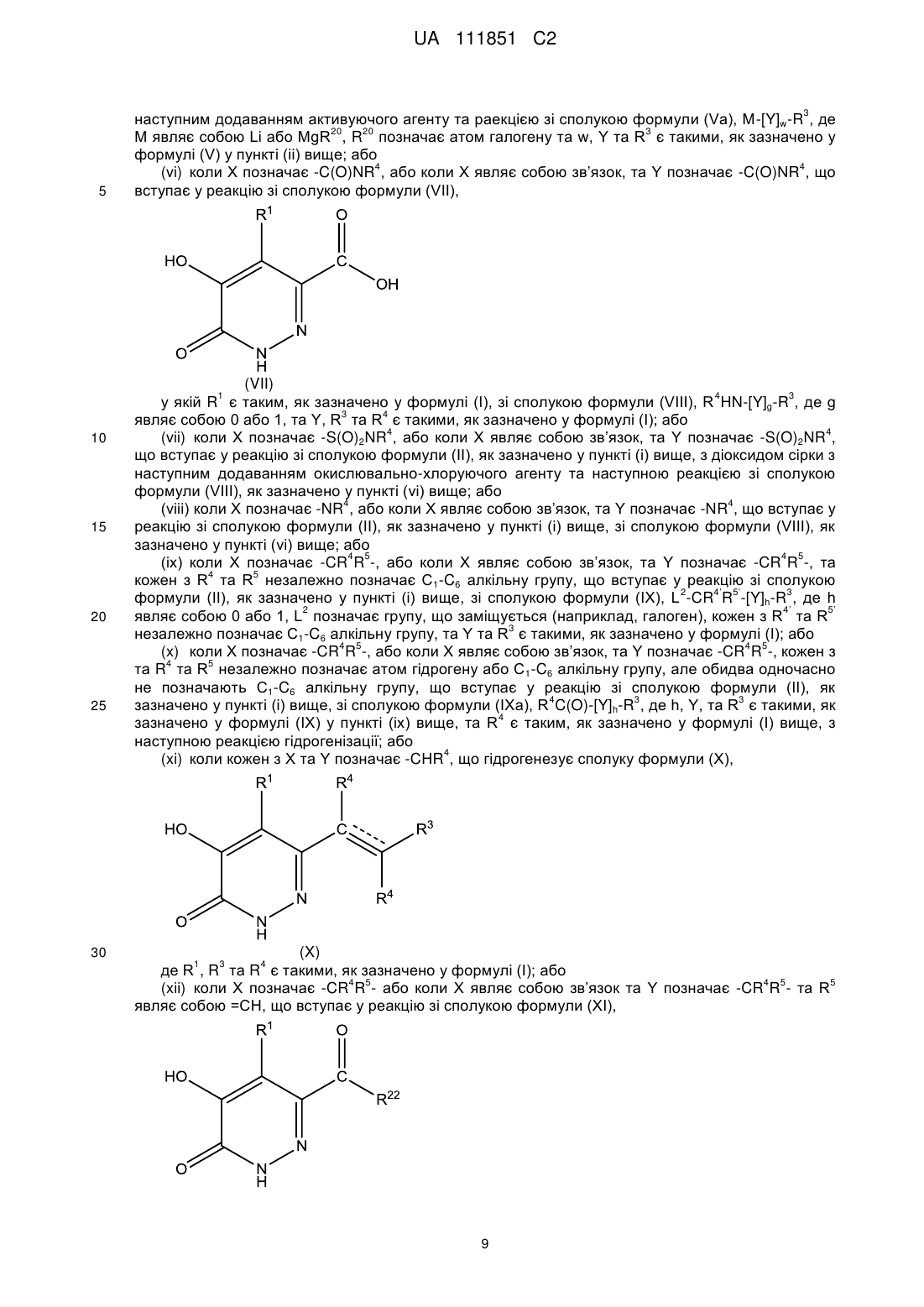
(vi) коли X означає -C(O)NR4 або коли X являє собою зв'язок та Y означає -C(O)NR4,
реакцію сполуки формули (VII)
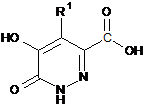 , (VII)
, (VII)
у якій R1 є таким, як зазначено у формулі (І), зі сполукою формули (VIII): R4HN-[Y]g-R3, де g являє собою 0 або 1, та Y, R3 та R4 є такими, як зазначено у формулі (І); або
(vii) коли Х означає -S(O)2NR4 або коли X являє собою зв'язок та Y означає -S(O)2NR4,
реакцію сполуки формули (II), як зазначено у п. (і) вище, з діоксидом сірки, з наступним додаванням окиснюючо-хлоруючого агента та наступною реакцією зі сполукою формули (VIII), як зазначено у п. (vi) вище; або
(viii) коли X означає -NR4 або коли X являє собою зв'язок та Y означає -NR4,
реакцію сполуки формули (II), як зазначено у п. (і) вище, зі сполукою формули (VIII), як зазначено у п. (vi) вище; або
(іх) коли X означає -CR4R5- або коли X являє собою зв'язок та Y означає -CR4R5-, та кожен R4 та R5 незалежно представляє С1-С6алкільну групу,
реакцію сполуки формули (II), як зазначено у п. (і) вище, зі сполукою формули (IX): L2-CR4'R5'-[Y]h-R3, де h являє собою 0 або 1, L2 означає групу, що відходить, кожен R4' та R5' незалежно представляє С1-С6алкільну групу, та Y та R3 є такими, як зазначено у формулі (І); або
(х) коли X означає -CR4R5- або коли X являє собою зв'язок та Y означає -CR4R5-, та кожен R4 та R5 незалежно представляє атом гідрогену або С1-С6алкільну групу, але не означають обидва одночасно С1-С6алкільну групу,
реакцію сполуки формули (II), як зазначено у п. (і) вище, зі сполукою формули (ІХа): R4C(О)-[Y]h-R3, де h, Y та R3 є такими, як зазначено у формулі (IX) у п. (іх) вище, та R4 є таким, як зазначено у формулі (І) вище, з наступною реакцією гідрогенізації; або
(хі) коли кожен X та Y представляє -CHR4,
гідрогенування сполуки формули (X)
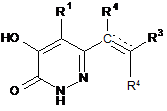 , (X)
, (X)
де R1, R3 та R4 є такими, як зазначено у формулі (І); або
(хіі) коли X означає -CR4R5- або коли X являє собою зв'язок та Y означає -CR4R5-, та R5 являє собою =СН,
реакцію сполуки формули (XI)
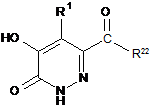 , (XI)
, (XI)
де R22 означає атом гідрогену або С1-С6алкільну групу, та R1 є таким, як зазначено у формулі (І), зі сполукою формули (IXb): R24-CH(R26)-[Y]h-R3, де R24 означає фосфонатний компонент, R26 означає атом гідрогену або С1-С6алкільну групу, та h, Y та R3 є такими, як зазначено у формулі (IX) у п. (іх) вище; або
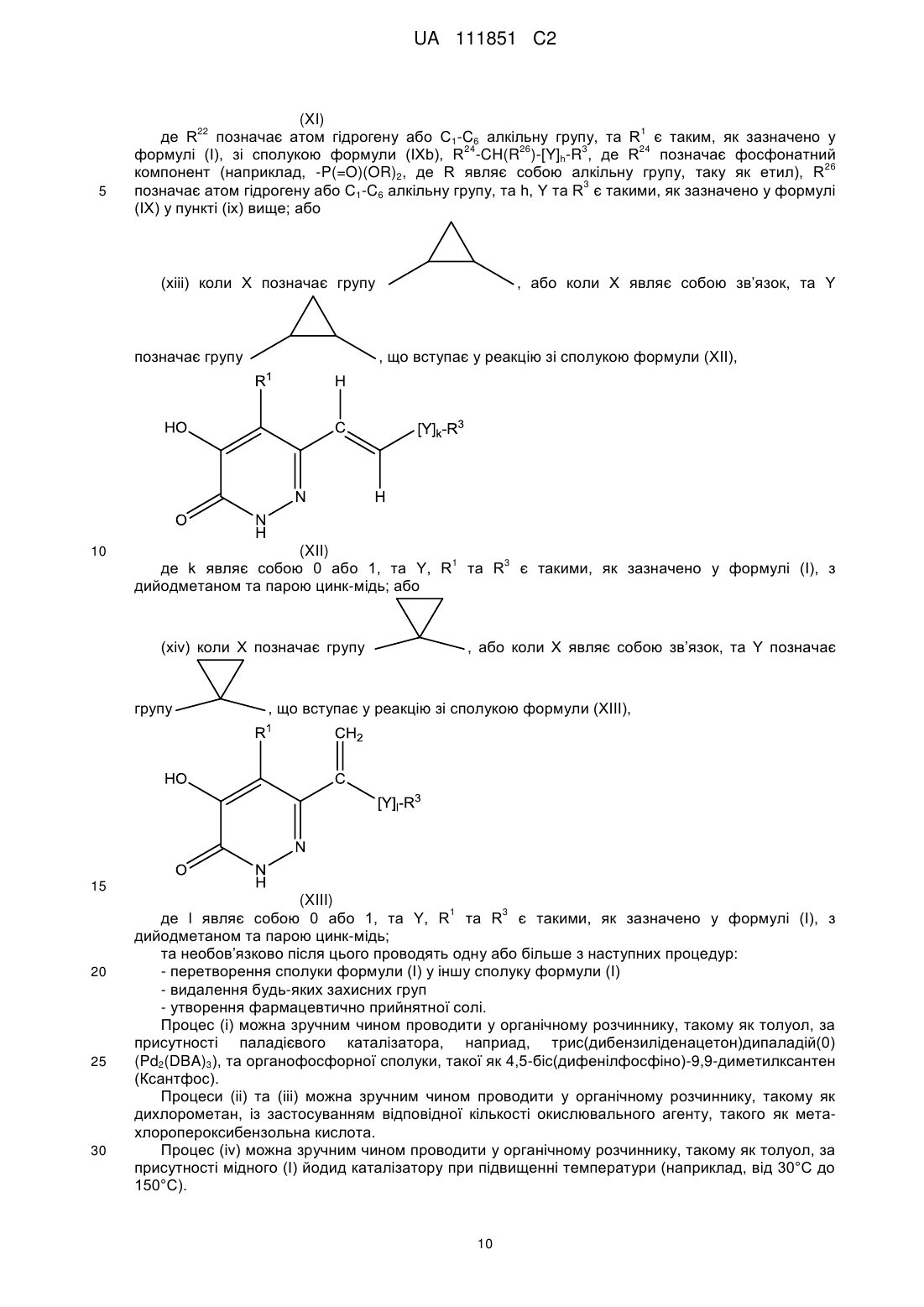
(хііі) коли X означає групу  або коли X являє собою зв'язок та Y означає групу
або коли X являє собою зв'язок та Y означає групу ![]() ,
,
реакцію сполуки формули (XII)
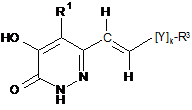 , (XII)
, (XII)
де k являє собою 0 або 1, та Y, R1 та R3 є такими, як зазначено у формулі (І), з дийодометаном та парою цинк-мідь; або
(xiv) коли X означає групу ![]() або коли X являє собою зв'язок та Y означає групу
або коли X являє собою зв'язок та Y означає групу ![]() ,
,
реакцію сполуки формули (XIII)
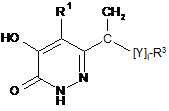 , (XIII)
, (XIII)
де 1 являє собою 0 або 1, та Y, R1 та R3 є такими, як зазначено у формулі (І), з дийодометаном та парою цинк-мідь;
та, необов'язково, наступне проведення однієї або більше наступних процедур:
перетворення сполуки формули (І) у іншу сполуку формули (І),
видалення будь-яких захисних груп,
утворення фармацевтично прийнятної солі.
12. Фармацевтична композиція, що містить сполуку формули (І) або її фармацевтично прийнятну сіль, як зазначено у будь-якому з пп. 1-10, у поєднанні з фармацевтично прийнятним ад'ювантом, розріджувачем або носієм.
13. Сполука формули (І) або її фармацевтично прийнятна сіль, як зазначено у будь-якому з пп. 1-10, для застосування у лікуванні захворювання, розвиток або симптоми якого пов'язані з активністю ферменту оксидази D-амінокислот (DAAO).
14. Сполука формули (І) або її фармацевтично прийнятна сіль, як зазначено у будь-якому з пп. 1-10, для застосування у лікування шизофренії, шизофреноморфного розладу, шизоафективного розладу, когнітивних розладів або болю.
15. Комбінація сполуки формули (І) або її фармацевтично прийнятної солі, як зазначено у будь-якому з пп. 1-10, та одного або більше агентів, вибраних з карбамазепіну, оланзепіну, кветіапіну, верапамілу, ламотриджину, окскарбамазепіну, рисперидону, арипіпразолу, зипрасидону та літію.
16. Проміжна сполука формули (XXX)
 , (XXX)
, (XXX)
в якій кожен Р1 та Р2 незалежно представляє бензильну захисну групу, R20 означає атом гідрогену або триметилсилангрупу, що відходить, та R1 є таким, як зазначено у формулі (І) п. 1.
Текст
Реферат: Даний винахід стосується сполук формули (І) та їх фармацевтично прийнятних солей R 1 HO O R N H 2 N , (I) UA 111851 C2 (12) UA 111851 C2 1 2 які відрізняються тим, що R та R є такими, як зазначено у описі, способів їх одержання, фармацевтичних композицій, що їх містять, та їх застосування у терапії. UA 111851 C2 5 10 15 20 25 30 35 40 Даний винахід стосується похідних пірідазінона, процесів їх виготовлення, фармацевтичних композицій, до складу яких вони входять, та їх застосування у терапіїі, зокрема, для лікування або попередження розвитку захворювань, що повязують з оксидазою D-амінокислот (DAAO). Гіпер-допамінергічна теорія десятиліттями була основою для пошуку лікарських засобів для лікування шизофренії та привела до створення таких значущих препаратів, як клозапін та оланзапін. Не зважаючи на те, що зазначені лікарські препарати мужуть бути високоефективними у боротьбі з позитивними симптомати шизофренії та мали значний сприятливий вплив у багатьох пацієнтів, вони не являють собою повне рішення, маючи незначний або зовсім не маючи впливу на негативні та когнітивні аспекти даного захворювання та профілі небажаних явищ у деяких випадках. Серед інших гіпотез гіпер-глутаматергічна теорія характеризується багатьма перевагами, маючи перші реальні докази застосування PCP (фенциклідину), MK801 або кетаміну, прямих антагоністів рецепторів N-метил-D-аспартату (NMDA), що можуть провокувати шизофренія-подібну симптоматику у здорових добровольців або посилювати клінічні ознаки у хворих на шизофренію. Однак, пряма модуляція рецептора NMDA за допомогою агністів не виявилась успішною у зв’язку з екситотоксичністю (надмірною стимуляцією нейротрансмітером), яка призводила до розвитку небажаних явищ. Альтернативний напрям полягає у тому, щоб зробити мішенню коагоністи, які є необхідними для активації рецептора NMDA. Такими є гліцин та серін (D-SER). Спроби підсилити активність рецептора NMDA шляхом застосування інгібіторів транспортерів гліцину привели до розробки клінічних сполук (які на сьогоднішній день не представлені на ринку в якості лікарських препаратів). D-SER є коагоністом навіть з більшою активністю у порівнянні з гліцином, і, таким чином, модуляція D-SER може являти собою альтернативну стратегію. Одним із способів підвищення рівнів D-SER є зменшення активності DAAO, ферменту, який видаляє його з синаптичної щілини. Інгібітори ферменту DAAO є відомими у даній галузі. Наприклад, Adage et al., European Neuropsychopharmacology 2008, 18, 200-214 описали AS-057278, низькомолекулярний інгібітор ферменту DAAO. Подібним чином Sparey et al., Bioorganic & Medicinal Chemistry Letters, 2008, 18, 3386-3391 показали, що молекули, які містять невеликі гетероциклічні кільця у поєзнанні з групою карбоксильної кислоти, можуть інгібувати фермент DAAO. Інгібітори DAAO, які уникають групи карбоксильної кислоти, були описані Ferraris et al., J. Med. Chem. 2008, 51, 3357-3359 та Duplantier et al., J. Med. Chem. 2009, 52, 3576-3585. Додаткові серії інгібіторів ферменту DAAO, що містять карбоксильну кислоту, компанії «Sepracore» описані у WO 2008/089453. Ми винайшли новий клас сполук, які являють собою інгібітори ферменту DAAO та мають бажані профілі активності. Сполуки даного винаходу характеризуються сприятливою активністю, селективністю та/або фармакокінетичними властивостями. Відповідно до даного винаходу, забезпечена формула винаходу (I), (I) де 1 R позначає атом гідрогену або фтору, або трифторметильну групу; 2 3 R позначає групу -X-Y-R ; 4 кожен з X та Y незалежно позначає зв'язок, атом оксигену або групу -C(O), -S(O)n, -C(O)NR , 4 45 4 4 5 -S(O)2NR , -NR , , або -CR R -, за умови, що X та Y не можуть обидва одночасно позначати зв'язок, та за умови, якщо як X, так і Y позначають дещо інше, ніж 4 5 звязок, щонайменше один X та Y позначає -CR R -; n являє собою 0, 1 або 2; 4 кожен R незалежно позначає атом гідрогену або C1-C6 алкільну або C1-C6 галоалкільну групу; 5 кожен R незалежно позначає атом гідрогену, C1-C6 алкільну або C1-C6 галоалкільну групу, 1 UA 111851 C2 5 10 15 20 25 30 35 40 45 50 55 або =CH-; 3 R позначає 3-10-членну насичену або ненасичену карбоциклічну або гетероциклічну кільцеву систему, сама кільцева система необов’язково заміщується щонайменше одним замісником, вибраним з галогену, гідроксилу, циано, оксо, C1-C6 алкілу, C2-C6 алкенілу, C1-C6 галоалкілу, C1-C6 гідроксиалкілу, C1-C6 алкокси, C1-C6 галоалкокси, C1-C6 алкілтіо, C1-C6 алкілсульфінілу, C1-C6 алкілсульфонілу, C1-C6 алкілкарбонілу, C1-C6 алкілкарбонілокси, C16 C6 алкоксикарбоніл, аміно (-NH2), -CON(R )2, C1-C6 алкіламіно, ди-(C1-C6 алкіл)аміно, C3-C6 7 циклоалкілу, C3-C6 циклоалкілокси, C3-C6 циклоалкілметилу, -[O]p-(CH2)q-O-R та 4-6-членного насиченого або ненасиченого гетероциклічного кільця (необов’язково заміщується щонайменшеодним замісником, вибраним з C1-C4 алкілу та C1-C4 алкокси); 6 кожен R незалежно позначає атом гідрогену або C1-C6 алкільну групу; p являє собою 0 або 1; q являє собою 1, 2, 3 або 4; та 7 R позначає C1-C6 алкільну групу; або їх фармацевтично прийнятну сіль. В контексті даної специфікації, якщо не зазначено інакше, алкіл, алкеніл або алкініл замісна група або алкіл, алкеніл або алкініл компонент у замісній групі може бути лінійним або розгалуженим. Приклади C1-C6 алкільних груп/компонентів включають метил, етил, пропіл, 2метил-1-пропіл, 2-метил-2-пропіл, 2-метил-1-бутил, 3-метил-1-бутил, 2-метил-3-бутил, 2,2диметил-1-пропіл, 2--метил-пентил, 3-метил-1-пентил, 4-метил-1-пентил, 2-метил-2-пентил, 3метил-2-пентил, 4-метил-2-пентил, 2,2-диметил-1-бутил, 3,3-диметил-1-бутил, 2-етил-1-бутил, n-бутил, ізобутил, трет-бутил, n-пентил, ізопентил, неопентил та n-гексил. Приклади C2-C6 алкенільних груп/компонентів включають етеніл, пропеніл, 1-бутеніл, 2-бутеніл, 1-пентелін, 1гексеніл, 1,3-бутадиеніл, 1,3-пентадиеніл, 1,4-пентадиеніл та 1-гексадиеніл. Приклади C2-C6 алкінільних груп/компонентів включають етиніл, пропініл, 1-бутиніл, 2-бутиніл, 1-пентиніл та 1гексиніл. Подібним чином, алкіленова група/компонент може бути лінійною або розгалуженою. Приклади C1-C6 алкіленових груп/компонентів включають метилен, етилен, n-пропілен, nбутилен, n-пентилен, n-гексилен, 1-метилетилен, 2-метилетилен, 1,2-диметилетилен, 1етилетилен, 2-етилетилен, 1-, 2- або 3-метилпропілен та 1-, 2- або 3-етилпропілен. C1-C6 галоалкільна або C1-C6 галоалкокси замісна група/компонент буде містити щонайменше один атом галогену, наприклад, один, два, три, чотири або п’ять атомів галогену, приклади яких включають фторметил, дифторметил, трифторметил, фторметокси, дифторметокси, трифторметокси або пентафторетил. C1-C6 гідроксиалкільна замісна група/компонент буде містити щонайменше одну гідроксильну групу, наприклад, одну, дві, три або чотири гідроксильні групи, приклади яких включають -CH2OH, -CH2CH2OH, -CH2CH2CH2OH, -CH(OH)CH2OH, -CH(CH3)OH та -CH(CH2OH)2. Алкільні групи у ди-C1-C6 алкіламіно групі/компоненті можуть бути однаковими або відрізнятися одна від одної. 3 У означенні R насичена або ненасичена 3-10-членна карбоциклічна або гетероциклічна кільцева система може мати аліциклічні або ароматичні властивості, як і замісник 4-6-членного насиченого або ненасиченого гетероциклічного кільця. Ненасичена кільцева система буде частково або повністю ненасиченою. 3 З метою уникнути сумнівів, коли R являє собою необов’язково 3-10-членну карбоциклічну або гетероциклічну кільцеву систему, слід розуміти, що винахід не охоплює жодних нестабільних кільцевих структур та жодних зв’язків O-O, O-S або S-S, а також те, що замісник, 3 за наявності, може приєднуватись до будь-якого відповідного кільцевого атому. Компонент R може приєднуватись до будь-якого гетероатому або атому карбону, що приводить до створення стабільної структури. Подвбні коментарі також застосовуються щодо замісника 4-6-членного 3 насиченого або ненасиченого гетероциклічного кільця на кільцевій системі R . Коли будь-який хімічний компонент або група у формулі (I) описуються як такі, що необов’язково заміщуються, спеціалістам у даній галузі буде зрозуміло, що компонент або група можуть можуть бути незаміщеними або заміщуватися одним або більше відомими замісниками. Спеціалістам у даній галузі буде зрозуміло, що число та природа замісників будуть обрані таким чином, щоб уникнути просторово небажаних комбінацій. 1 У одному варіанті даного винаходу R позначає атом гідрогену. 4 Кожен з X та Y незалежно позначає зв'язок, атом оксигену або групу -C(O), -S(O)n, -C(O)NR , 2 UA 111851 C2 4 5 10 4 4 5 -S(O)2NR , -NR , , або -CR R -, за умови, що X та Y не можуть обидва одночасно позначати зв'язок, та за умови, якщо як X, так і Y позначають дещо інше, ніж 4 5 звязок, щонайменше один X та Y позначає -CR R -. 4 Кожен R незалежно позначає атом гідрогену або C1-C6, або C1-C4, або C1-C2 алкільну, переважно метильну, групу або C1-C6, або C1-C4, або C1-C2 галоалкільну, переважно трифторметильну, групу. 5 Кожен R незалежно позначає атом гідрогену, C1-C6 або C1-C4, або C1-C2 алкільну, переважно метилльну, групу, C1-C6 або C1-C4, або C1-C2 галоалкільну, переважно 4 5 трифторметильну, групу або групу =CH- так, що -CR R - позначає алкеніленовий компонент, 4 4 CR =CH- або -CH=CR -. У одному варіанті даного винаходу X позначає зв'язок, атом оксигену або групу -C(O), -S(O)n, 4 4 4 4 4 4 5 15 -C(O)NR , -S(O)2NR , -NR , , або -CR R - (наприклад, CH2 або 4 5 CH(CH3)), та Y позначає зв’язок або -CR R - (наприклад, CH2 або CH(CH3)), до яких застосовується умова, зазначена вище. У іншому варіанті даного винаходу X позначає зв’язок, атом оксигену або групу -C(O), -S(O)n, 20 -C(O)NR , -S(O)2NR , , або -CR R - (наприклад, CH2 або CH(CH3)), 4 5 та Y позначає зв’язок або -CR R - (наприклад, CH2 або CH(CH3)), до яких застосовується умова, зазначена вище. 4 5 У іншому варіанті даного винаходу X позначає -CR R - (наприклад, CH2 або CH(CH3)) та Y 4 4 4 позначає зв’язок, атом оксигену або групу -C(O), -S(O)n, -C(O)NR , -S(O)2NR , -NR , 4 4 5 5 , або -CR R - (наприклад, CH2 або CH(CH3)), до яких застосовується умова, зазначена вище. 4 У наступному варіанті X позначає групу -S(O)n (наприклад, -S-), -CHR (наприклад, CH2 або 4 25 CH(CH3)) або , та Y позначає зв’язок або групу -CHR (наприклад, CH2), до яких застосовується умова, зазначена вище. 4 У наступному варіанті X позначає групу -S(O)n (наприклад, -S-), -NR (наприклад, N(CH3)), 4 4 CHR (наприклад, CH2 або CH(CH3)) або , особливо -CHR , та Y позначає зв’язок або 4 групу -CHR (наприклад, CH2), до яких застосовується умова, зазначена вище. Конкретні приклади комбінацій X та Y включають будь-який один або більше з наступних: 30 X S CH2 CH2 S SO2 CH2 O O C(O) C(O)NH S(O)2NH Y CH2 S CH2 CH(CH3) CH2 SO2 CH2 CH(CH3) CH2 CH2 CH2 3 UA 111851 C2 CH2 CH(CH3) CH2 C(CH3)2 -CH=CHзв’язок CH2 зв’язок циклопропіл зв’язок CH(CH3) зв’язок N(CH3) CH(CH3) CH2 C(CH3)2 CH2 зв’язок -CH=CHзв’язок CH2 зв’язок циклопропіл зв’язок CH(CH3) CH2 У одному варіанті даного винаходу комбінації X та Y, яким надають перевагу, включають будь-який один або більше з наступних: X S CH2 CH2 зв’язок Циклопропіл (наприклад, Y CH2 CH2 зв’язок CH2 зв’язок ) Циклопропіл (наприклад, зв’язок ) CH(CH3) зв’язок N(CH3) зв’язок CH(CH3) CH2 5 10 15 20 25 У іншому варіанті даного винаходу перевага надається тому, щоб як X, так і Y, позначають CH2. 6 Кожен R незалежно позначає атом гідрогену або C 1-C6, або C1-C4, або C1-C2 алкільну групу. Приклади алкільних груп описані вище та включають метил, етил, ізо-пропіл, n-пропіл та nбутил. 7 R позначає C1-C6 або C1-C4, або C1-C2 алкільну групу, приклади якої були описані раніше. 3 Відповідно до одного аспекту даного винаходу, R може позначати 3-10-членну (наприклад, від 3-, 4-, 5- або 6- до 7-, 8-, 9- або 10-членну) насичену або ненасичену карбоциклічну або гетероциклічну кільцеву систему, яка необов’язково заміщуються щонайменше одним замісником (наприклад, одним, двома, трьома або чотирма замісниками незалежно), вибраними з галогену (наприклад, фтору, хлору або брому), гідроксилу, циано, оксо, C 1-C6 або C1-C4, або C1-C2 алкілу, C2-C6 або C2-C4 алкенілу, C1-C6 або C1-C4, або C1-C2 галоалкілу, C1-C6 або C1-C4, або C1-C2 гідроксиалкілу, C1-C6 або C1-C4, або C1-C2 алкокси, C1-C6 або C1-C4, або C1C2 галоалкокси, C1-C6 або C1-C4, або C1-C2 алкілтіо, C1-C6 або C1-C4, або C1-C2 алкілсульфінілу, C1-C6 або C1-C4, або C1-C2 алкілсульфонілу, C1-C6 або C1-C4, або C1-C2 алкілкарбонілу, C1-C6 або C1-C4, або C1-C2 алкілкарбонілокси, C1-C6 або C1-C4, або C1-C2 алкоксикарбонілу, аміно, 6 CON(R )2, C1-C6 або C1-C4, або C1-C2 алкіламіно, ди-(C1-C6 або C1-C4, або C1-C2 алкіл)аміно, C3C6 або C3-C5 циклоалкілу, C3-C6 або C3-C5 циклоалкілокси, C3-C6 або C3-C5 циклоалкілметилу, 7 [O]p-(CH2)q-O-R та 4-6-членного насиченого або ненасиченого гетероциклічного кільця (що необов’язково заміщуються щонайменше одним замісником, наприклад, одним, двома або трьома замісниками незалежно, вибраними з C 1-C4 алкілу, такого як метил або етил, та C1-C4 алкокси, такого як метокси або етокси). 4 UA 111851 C2 5 10 15 20 25 30 35 40 45 50 55 60 Гетероциклічна кільцева система буде містити щонайменше один кільцевий гетероатом (наприклад, один, два, три або чотири кільцевих гетероатоми незалежно), вибраних з нітрогену, сірки та оксигену. Приклади насичених або ненасичених 3-10-членних карбоциклічних або гетероциклічних кільцевих систем, які можуть застосовуватися, що можуть бути моно циклічними або поліциклічними (наприклад, біциклічними), в яких два або більше кілець злиті, включають один або більше (у будь-якій комбінації) циклопропіл, циклобутил, циклопентил, циклогексил, біцикло[2.2.1]гептил, циклопентелін, циклогексеніл, феніл, піролідиніл, піперідиніл, піперазиніл, морфолініл, тіоморфолініл, оксадиазоліл (наприклад, 1,2,4-оксадиазоліл), тетрагідрофураніл, диазабіцикло[2.2.1]гепт-2-іл, нафтіл, бензофураніл, бензотіеніл, бензодіоксоліл, хінолініл, оксазоліл, тіадіазоліл (наприклад, 1,2,3-тіадіазоліл), 2,3дигідробензофураніл, тетрагідропіраніл, піразоліл, імідазо[1,2-a]піридиніл, піразиніл, тіазолідиніл, інданіл, тіеніл, ізоксазоліл, піридазиніл, піроліл, фураніл, тіазоліл, індоліл, імідазоліл, піримідиніл, бферментідазоліл, тіазоліл, тетразоліл та піридиніл. Кільцеві системи, яким надають перевагу, включають феніл, піридиніл, оксазоліл, піразиніл, циклопропіл, циклопентил, циклогексил, тетрагідропіраніл, 2,3-дигідробензофураніл, піримідиніл, імідазо[1,2-a]піридиніл, піразоліл, тіазоліл та піперідиніл. Переважно кільцева система являє собою феніл, піридиніл, циклопропіл, циклопентил, циклогексил або тетрагідропіраніл. У варіанті винаходу, якому надають перевагу, кільцева система являє собою феніл або піридиніл, зокрема, феніл. Замісник 4-6-членного насиченого або ненасиченого гетероциклічного кільця буде містити щонайменше один кільцевий геретоатом (наприклад, один, два, три або чотири кільцевих гетероатоми незалежно), вибраних з ніторогену, сірки та оксигену. Переважно кільцеві гетероатоми вибрані з нітрогену та оксигену. Приклади таких кільцевих замісників включають азетідиніл, піролідиніл та оксадиазоліл, такий як 1,2,4-оксадиазоліл. 3 У одному варіанті даного винаходу, R позначає від 3-, 4- або 5- до 6-, 7-, 8- або 9-членну, наприклад, 3-6- або 5-9-членну, насичену або ненасичену карбоциклічну або гетероциклічну кільцеву ситему, яка необов’язково заміщується щонайменше одним замісником (наприклад, одним, двома, трьома або чотирма замісниками незалежно), вибраним з галогену (наприклад, фтору, хлору або брому), гідроксилу, циано, оксо, C1-C4 алкілу (наприклад, метилу або етилу), C2-C4 алкенілу (наприклад, етенілу), C1-C2 галоалкілу (наприклад, дифторметилу або трифторметилу), C1-C2 гідроксиалкілу (наприклад, гідроксиметилу), C 1-C4 алкокси (наприклад, метокси або етокси), C1-C2 галоалкокси (наприклад, дифторметокси або трифторметокси), C 1C4 алкілтіо (наприклад, метилтіо або етилтіо), C1-C4 алкілсульфініл (наприклад, метилсульфініл або етилсульфініл), C1-C4 алкілсульфонілу (наприклад, метилсульфонілу або етилсульфонілу), C1-C4 алкілкарбонілу (наприклад, метилкарбонілу або етилкарбонілу), C 1-C4 алкілкарбонілокси (наприклад, метилкарбонілокси), C1-C4 алкоксикарбонілу (наприклад, метоксикарбонілу), аміно, 6 -CON(R )2, C1-C4 алкіламіно (наприклад, метиламіно або етиламіно), ди-(C1-C4 алкіл)аміно (наприклад, диметиламіно), C3-C6 циклоалкілу, C3-C6 циклоалкілокси, C3-C6 циклоалкілметилу, 7 [O]p-(CH2)q-O-R та 4-6-членного насиченого або ненасиченого гетероциклічного кільця, яке необов’язково заміщується метилом або метокси. 3 У іншому варіанті даного винаходу, R позначає 5- або 6-членну ненасичену карбоциклічну або гетероциклічну кільцеву систему, гетероциклічна кільцева система містить один або два кільцеві гетероатоми, незалежно вибраних з нітрогену та оксигену, чия карбоциклічна або гетероциклічна кільцева система необов’язково заміщується одним, двома, трьома або чотрима замісниками, незалежно вибраними з фтору, хлору, брому, гідроксилу, циано, оксо, C 1-C4 алкілу (наприклад, метилу або етилу), C2-C4 алкенілу (наприклад, етенілу), C1-C2 галоалкілу (наприклад, дифторметилу або трифторметилу), C 1-C2 гідроксиалкілу (наприклад, гідроксиметилу), C1-C4 алкокси (наприклад, метокси або етокси), C1-C2 галоалкокси (наприклад, дифторметокси або трифторметокси), C1-C4 алкілтіо (наприклад, метилтіо або етилтіо), C1C4 алкілсульфінілу (наприклад, метилсульфінілу або етилсульфінілу), C 1-C4 алкілсульфонілу (наприклад, метилсульфонілу або етилсульфонілу), C 1-C4 алкілкарбонілу (наприклад, метилкарбонілу або етилкарбонілу), C1-C4 алкілкарбонілокси (наприклад, метилкарбонілокси), C1-C4 алкоксикарбонілу (наприклад, метоксикарбонілу), аміно, карбоксамідо (-CONH2), C1C4 алкіламіно (наприклад, метиламіно або етиламіно), ди-(C1-C4 алкіл)аміно (наприклад, диметиламіно), C3-C6 циклоалкіл, C3-C6 циклоалкілокси, C3-C6 циклоалкілметилу, -[O]p-(CH2)q-O7 R та 4-6-членного насиченого або ненасиченого гетероциклічного кільця, яке переважно містить щонайменше один кільцтовий атом нітрогену, що необов’язково заміщується метилом або метокси. 3 У іншому варіанті R позначає 3-6-членну, переважно 5-6-членну, насичену або ненасичену 5 UA 111851 C2 5 10 15 20 карбоциклічну або гетероциклічну кільцеву систему, таку як циклопропіл, циклопентил, циклогексил, тетрагідропіраніл, феніл або піридиніл, чия кільцева система необов’язково заміщується щонайменше одним замісником (наприклад, одним, двома, трьома або чотирма, переважно одним або двома, замісниками незалежно), вибраних з циано, фтору, хлору, метилу, дифторметилу, дифторметокси, трифторметилу, трифторметокси та метокси. 3 Конкретні приклади R включають один або більше наступних замісників у будь-якій комбінації: Кільцеві замісники R* незалежно вибрані з циано, галогену (наприклад, фтору або хлору), метилу, метокси, дифторметилу, дифторметокси, трифторметилу або трифторметокси. У варіанті винаходу, якому надають перевагу, 1 R позначає атом гідрогену; 2 3 R позначає групу -X-Y-R ; 4 4 X позначає групу -S(O)n або -CHR та Y позначає групу -CHR ; n являє собою 0, 1 або 2; 4 кожен R незалежно позначає атом гідрогену або метильну групу; та 3 R позначає 5- або 6-членну насичену або ненасичену карбоциклічну або гетероциклічну кільцеву систему, чия кільцева система необов’язково заміщується щонайменше одним замісником вибранм з фтору, хлору, трифторметилу та метокси. У іншому варіанті винаходу, якому надають перевагу, 1 R позначає атом гідрогену; 2 3 R позначає групу -X-Y-R ; 4 25 та 30 35 4 X позначає групу -S(O)n , -CHR або та Y позначає зв’язок або групу -CHR ; n являє собою 0, 1 або 2, переважно 0; 4 кожен R незалежно позначає атом гідрогену або метильну групу, переважно атом гідрогену; 3 R позначає 3-6-членну насичену або ненасичену карбоциклічну або гетероциклічну кільцеву систему (переважно фенільну), чия кільцева система необов’язково заміщується щонайменше одним замісником (переважно одним або двома замісниками незалежно), вибраними з фтору, хлору, дифторметилу, трифторметилу, трифторметокси та метокси. У іншому варіанті винаходу, якому надають перевагу, 1 R позначає атом гідрогену; 2 3 R позначає групу -X-Y-R ; 4 4 X позначає групу -S(O)n , -NR , -CHR або та Y позначає зв’язок або групу 4 CHR ; n являє собою 0, 1 або 2, переважно 0; 4 кожен R незалежно позначає атом гідрогену або метильну групу, переважно атом гідрогену; та 6 UA 111851 C2 3 5 10 15 20 25 30 35 40 45 50 55 60 R позначає 3-6-членну насичену або ненасичену карбоциклічну або гетероциклічну кільцеву систему (переважно фенільну), чия кільцева система необов’язково заміщується щонайменше одним замісником (переважно одним або двома замісниками незалежно), вибраними з циано, фтору, хлору, дифторметилу, дифторметокси, трифторметилу, трифторметокси, метилу та метокси. Приклади сполук даного винаходу включають: 4-Гідрокси-6-(2-фенілетил)піридазин-3(2H)-он, 6-[2-(4-Фторфеніл)етил]-4-гідроксипіридазин-3(2H)-он, 4-Гідрокси-6-{2-[5-(трифторметил)піридин-2-іл]етил}піридазин-3(2H)-он, 6-[(4-Хлоробензіл)сульфаніл]-4-гідроксипіридазин-3(2H)-он, 4-Гідрокси-6-{2-[6-(трифторметил)піридин-3-іл]етил}піридазин-3(2H)-он, 6-[2-(3-Фторфеніл)етил]-4-гідроксипіридазин-3(2H)-он, 6-[2-(2-Фторфеніл)етил]-4-гідроксипіридазин-3(2H)-он, 6-[2-(3,5-Дифторфеніл)етил]-4-гідроксипіридазин-3(2H)-он, 6-[2-(3,4-Дифторфеніл)етил]-4-гідроксипіридазин-3(2H)-он, 4-Гідрокси-6-{2-[3-(трифторметокси)феніл]етил}піридазин-3(2H)-он, 4-Гідрокси-6-{2-[3-(трифторметил)феніл]етил}піридазин-3(2H)-он, 4-Гідрокси-6-{2-[5-(трифторметил)піридин-3-іл]етил}піридазин-3(2H)-он, 6-(2-Циклогексилетил)-4-гідроксипіридазин-3(2H)-он, 6-(2-Циклопропілетил)-4-гідроксипіридазин-3(2H)-он, 6-(2-Циклопентилетил)-4-гідроксипіридазин-3(2H)-он, 4-Гідрокси-6-[2-(4-метоксициклогексил)етил]піридазин-3(2H)-он, 6-[2-(2,4-Дифторфеніл)етил]-4-гідроксипіридазин-3(2H)-он, 6-{2-[3-(Дифторметил)феніл]етил}-4-гідроксипіридазин-3(2H)-он, 6-Бензил-4-гідроксипіридазин-3(2H)-он, 6-[2-(3-Хлорофеніл)етил]-4-гідроксипіридазин-3(2H)-он, 4-Гідрокси-6-(1-фенілциклопропіл)піридазин-3(2H)-он, 4-[2-(5-Гідрокси-6-оксо-1,6-дигідропіридазин-3-іл)етил]бензонітрил, 6-[2-(3-Фтор-4-метилфеніл)етил]-4-гідроксипіридазин-3(2H)-он, 6-[2-(4-Фтор-3-метилфеніл)етил]-4-гідроксипіридазин-3(2H)-он, 6-[2-(3,4-Диметоксифеніл)етил]-4-гідроксипіридазин-3(2H)-он, 4-Гідрокси-6-{2-[3-(трифторметокси)феніл]етил}піридазин-3(2H)-он, 6-[2-(4-Хлорофеніл)етил]-4-гідроксипіридазин-3(2H)-он, 6-[2-(2-Хлорофеніл)етил]-4-гідроксипіридазин-3(2H)-он, 4-Гідрокси-6-{2-[2-(трифторметил)феніл]етил}піридазин-3(2H)-он, 6-(4-(Дифторметокси)фентетил)-4-гідроксипіридазин-3(2H)-он, 6-(4-(Трифторметокси)фентетил)-4-гідроксипіридазин-3(2H)-он, 6-(3-(Дифторметокси)фентетил)-4-гідроксипіридазин-3(2H)-он, 6-[1-(4-Фторфеніл)циклопропіл]-4-гідроксипіридазин-3(2H)-он, 6-[1-(4-Фторфеніл)етил]-4-гідроксипіридазин-3(2H)-он, 4-Гідрокси-6-{1-[3-(трифторметил)феніл]етил}піридазин-3(2H)-он, 4-Гідрокси-6-{2-[4-(трифторметил)феніл]етил}піридазин-3(2H)-он, 6-((Циклопропілметил)(метил)аміно)-4-гідроксипіридазин-3(2H)-он, 6-((Циклогексилметил)(метил)аміно)-4-гідроксипіридазин-3(2H)-он, 6-(3-Хлоробензіл)-4-гідроксипіридазин-3(2H)-он, 6-(4-Хлоробензіл)-4-гідроксипіридазин-3(2H)-он, 6-(Циклогексилметил)-4-гідроксипіридазин-3(2H)-он, 6-(4-Фторбензил)-4-гідроксипіридазин-3(2H)-он, 6-(2-Хлоро-6-фторбензил)-4-гідроксипіридазин-3(2H)-он, 6-(2-Хлоробензіл)-4-гідроксипіридазин-3(2H)-он, 6-(3-Фторбензил)-4-гідроксипіридазин-3(2H)-он, 6-(2-Фторбензил)-4-гідроксипіридазин-3(2H)-он, 6-(4-Метилбензил)-4-гідроксипіридазин-3(2H)-он, 6-(3-Метилбензил)-4-гідроксипіридазин-3(2H)-он, 4-Гідрокси-6-(3-(трифторметил)бензил)піридазин-3(2H)-он, 4-Гідрокси-6-{2-[5-(трифторметил)піридин-3-іл]етил}піридазин-3(2H)-он, 4-Гідрокси-6-[2-(оксан-4-іл)етил]піридазин-3(2H)-он, 6-{[(4-Фторфеніл)метил](метил)аміно}-4-гідрокси-піридазин-3(2H)-он, 6-[2-(2,6-Дифторфеніл)етил]-4-гідрокси-піридазин-3(2H)-он, 6-[2-(2-Хлоро-6-фторфеніл)етил]-4-гідрокси-піридазин-3(2H)-он, 7 UA 111851 C2 5 10 15 20 6-{[3,5-біс(Трифторметил)феніл]метил}-4-гідроксипіридазин-3(2H)-он, 6-(1-Фенілетил)-4-гідроксипіридазин-3(2H)-он, 6-(Циклопропілметил)-4-гідрокси-2,3-дигідропіридазин-3-он, 4-Гідрокси-6-{1-[4-(трифторметил)феніл]циклопропіл}-2,3-дигідропіридазин-3-он, 6-{2-[2-Хлоро-4-(трифторметил)феніл]етил}-4-гідрокси-2,3-дигідропіридазин-3-он, 6-{2-[2-Фтор-4-(трифторметил)феніл]етил}-4-гідрокси-2,3-дигідропіридазин-3-он, 6-{2-[3,5-біс(Трифторметил)феніл]етил}-4-гідрокси-2,3-дигідропіридазин-3-он, 6-{2-[2,4- біс(Трифторметил)феніл]етил}-4-гідрокси-2,3-дигідро-піридазин-3-он, 6-{2-[3,4- біс(Трифторметил)феніл]етил}-4-гідрокси-2,3-дигідропіридазин-3-он, 4-Гідрокси-6-(3-метил-4-(трифторметил)фентетил) піридазин-3(2H)-он, 3,4-біс(Бензилокси)-6-((3-хлоро-4-(трифторметил)феніл) етил)-піридазин, 4-Гідрокси-6-{2-[2-метил-4-(трифторметил)феніл]етил}-2,3-дигідропіридазин-3-он, 6-{2-[3,5-Дифтор-4-(трифторметил)феніл]етил}-4-гідрокси-2,3-дигідропіридазин-3-он, 6-{2-[3-Фтор-4-(трифторметил)феніл]етил}-4-гідрокси-2,3-дигідропіридазин-3-он, та фармацевтично прийнятні солі будь-якого з них. Слід зауважити, що кожна з хімічних сполук, перелік яких наведено вище, позначає окремий та незалежний аспект даного винаходу. Даний винахід додатково забезпечує процес приготування сполуки формули (I) або її фармацевтично прийнятної солі, як зазначено вище, що включає (i) коли X позначає атом сірки, або коли X являє собою зв’язок, та Y позначає атом сірки, що вступає у реакцію зі сполукою формули (II) 1 25 30 35 40 у якій Hal позначає атом галогену, такого як хлор, та R є таким, як зазначено у формулі (I), 3 3 зі сполукою формули (III), HS-[Y]t-R , де t являє собою 0 або 1, та Y та R є такимм, як зазначено у формулі (I); або (ii) коли X позначає SO, або коли X являє собою зв’язок, та Y позначає SO, що окислює сполуку формули (IV) (IV) 1 1 у якій P позначає захисну групу (наприклад, метил пропіонат), та R є таким, як зазначено у формулі (I), з відповідним окиснюючим агентом, з наступною реакцією зі сполукою формули (V), 1 3 1 L -[Y]w-R , де w являє собою 0 або 1, L позначає групу, що заміщується (наприклад, галоген), та 3 Y та R є такими, як зазначено у формулі (I); або (iii) коли X позначає SO2, або коли X являє собою зв’язок, та Y позначає SO 2, що окислює сполуку формули (IV), як зазначено у пункті (ii) вище, з відповідним окиснюючим агентом, з наступною реакцією зі сполукою формули (V), як зазначено у пункті (ii) вище; або (iv) коли X позначає атом оксигену, або коли X являє собою зв’язок, та Y позначає атом оксигену, що вступає у реакцію зі сполукою формули (II), як зазначено у пункті (i) вище, зі 3 3 сполукою формули (VI), HO-[Y]z-R , де z являє собою 0 або 1, та Y та R є такими, як зазначено у формулі (I); або (v) коли X позначає C(O), або коли X являє собою зв’язок, та Y позначає C(O), що вступає у реакцію зі сполукою формули (II), як зазначено у пункті (i) вище, з діоксином карбону з 8 UA 111851 C2 3 5 10 15 20 25 30 наступним додаванням активуючого агенту та раекцією зі сполукою формули (Va), M-[Y]w-R , де 20 20 3 M являє собою Li або MgR , R позначає атом галогену та w, Y та R є такими, як зазначено у формулі (V) у пункті (ii) вище; або 4 4 (vi) коли X позначає -C(O)NR , або коли X являє собою зв’язок, та Y позначає -C(O)NR , що вступає у реакцію зі сполукою формули (VII), (VII) 1 4 3 у якій R є таким, як зазначено у формулі (I), зі сполукою формули (VIII), R HN-[Y]g-R , де g 3 4 являє собою 0 або 1, та Y, R та R є такими, як зазначено у формулі (I); або 4 4 (vii) коли X позначає -S(O)2NR , або коли X являє собою зв’язок, та Y позначає -S(O)2NR , що вступає у реакцію зі сполукою формули (II), як зазначено у пункті (i) вище, з діоксидом сірки з наступним додаванням окислювально-хлоруючого агенту та наступною реакцією зі сполукою формули (VIII), як зазначено у пункті (vi) вище; або 4 4 (viii) коли X позначає -NR , або коли X являє собою зв’язок, та Y позначає -NR , що вступає у реакцію зі сполукою формули (II), як зазначено у пункті (i) вище, зі сполукою формули (VIII), як зазначено у пункті (vi) вище; або 4 5 4 5 (ix) коли X позначає -CR R -, або коли X являє собою зв’язок, та Y позначає -CR R -, та 4 5 кожен з R та R незалежно позначає C1-C6 алкільну групу, що вступає у реакцію зі сполукою 2 4’ 5’ 3 формули (II), як зазначено у пункті (i) вище, зі сполукою формули (IX), L -CR R -[Y]h-R , де h 2 4’ 5’ являє собою 0 або 1, L позначає групу, що заміщується (наприклад, галоген), кожен з R та R 3 незалежно позначає C1-C6 алкільну групу, та Y та R є такими, як зазначено у формулі (I); або 4 5 4 5 (x) коли X позначає -CR R -, або коли X являє собою зв’язок, та Y позначає -CR R -, кожен з 4 5 та R та R незалежно позначає атом гідрогену або C1-C6 алкільну групу, але обидва одночасно не позначають C1-C6 алкільну групу, що вступає у реакцію зі сполукою формули (II), як 4 3 3 зазначено у пункті (i) вище, зі сполукою формули (IXa), R C(O)-[Y]h-R , де h, Y, та R є такими, як 4 зазначено у формулі (IX) у пункті (ix) вище, та R є таким, як зазначено у формулі (I) вище, з наступною реакцією гідрогенізації; або 4 (xi) коли кожен з X та Y позначає -CHR , що гідрогенезує сполуку формули (X), (X) 1 3 4 де R , R та R є такими, як зазначено у формулі (I); або 4 5 4 5 5 (xii) коли X позначає -CR R - або коли X являє собою зв’язок та Y позначає -CR R - та R являє собою =CH, що вступає у реакцію зі сполукою формули (XI), 9 UA 111851 C2 5 (XI) 22 1 де R позначає атом гідрогену або C1-C6 алкільну групу, та R є таким, як зазначено у 24 26 3 24 формулі (I), зі сполукою формули (IXb), R -CH(R )-[Y]h-R , де R позначає фосфонатний 26 компонент (наприклад, -P(=O)(OR)2, де R являє собою алкільну групу, таку як етил), R 3 позначає атом гідрогену або C1-C6 алкільну групу, та h, Y та R є такими, як зазначено у формулі (IX) у пункті (ix) вище; або (xiii) коли X позначає групу позначає групу 10 , або коли X являє собою зв’язок, та Y , що вступає у реакцію зі сполукою формули (XII), (XII) 1 3 де k являє собою 0 або 1, та Y, R та R є такими, як зазначено у формулі (I), з дийодметаном та парою цинк-мідь; або (xiv) коли X позначає групу групу , або коли X являє собою зв’язок, та Y позначає , що вступає у реакцію зі сполукою формули (XIII), 15 20 25 30 (XIII) 1 3 де l являє собою 0 або 1, та Y, R та R є такими, як зазначено у формулі (I), з дийодметаном та парою цинк-мідь; та необов’язково після цього проводять одну або більше з наступних процедур: - перетворення сполуки формули (I) у іншу сполуку формули (I) - видалення будь-яких захисних груп - утворення фармацевтично прийнятної солі. Процес (i) можна зручним чином проводити у органічному розчиннику, такому як толуол, за присутності паладієвого каталізатора, наприад, трис(дибензиліденацетон)дипаладій(0) (Pd2(DBA)3), та органофосфорної сполуки, такої як 4,5-біс(дифенілфосфіно)-9,9-диметилксантен (Ксантфос). Процеси (ii) та (iii) можна зручним чином проводити у органічному розчиннику, такому як дихлорометан, із застосуванням відповідної кількості окислювального агенту, такого як метахлоропероксибензольна кислота. Процес (iv) можна зручним чином проводити у органічному розчиннику, такому як толуол, за присутності мідного (I) йодид каталізатору при підвищенні температури (наприклад, від 30°C до 150°C). 10 UA 111851 C2 5 10 15 20 25 30 35 40 45 Першу операцію процесу (v) можна зручним чином проводити у органічному розчиннику, такому як диетиловий ефір, при низькій температурі (наприклад, -78°C) за присутності реактиву, такого як бутиллітій. Відповідним активуючим агентом, який застосовують у другій операції, буде сполука, така як N,O-диметилгідроксиламіну гідрохлорид, яка є комерційно доступною, наприклад, виробництва корпорації «Sigma-Aldrich», для утворення «аміда Вайнреба», який потім вступає в реакцію зі сполукою формули (Va) для утворення відповідної сполуки формули (I). Процес (vi) можна зручним чином проводити у органічному розчиннику із застосуванням відповідного амідного звязуючого реактиву. Різноманітні амідні звязуючі реактиви відомі спеціалістам у даній галузі, такі як дициклогексилкарбодиімід (DCC), диізопропілкарбодиімід (DIC), O-(бензотриазол-1-іл)-N,N,N’,N’-тетраметилуроній гексафторфосфат (HBTU) та O(бензотриазол-1-іл)- N,N,N’,N’-тетраметилуроній тетрафторборат (TBTU). Першу операцію процесу (vii) можна зручним чином проводити у органічному розчиннику, такому як диетиловий ефір, при низькій температурі (наприклад, -78°C) за присутності реактиву, такого як ізопропілмагнію хлорид. Відповідним окислювально-хлоруючим агентом, який застосовують у другій операції, буде сульфурил хлорид, та наступну реакцію зі сполукою формули (VIII) можна проводити відповідно до процедур зв’язування сульфонамідів, відомих у даній галузі. Реакцію амінування у процесі (viii) можна зручним чином проводити у органічному розчиннику, такому як толуол, за присутності (1) каталісту паладію, такого як трис(дибензиліденацетон)дипаладій(0) (Pd2(DBA)3), (2) основи, такої як натрій t-бутоксид, та (3) органофосфорної сполуки, такої як 4,5-біс(дифенілфосфіно)-9,9-диметилксантен (Ксантфос). Процеси (ix) та (x) можна зручним чином проводити у органічному розчиннику, такому як диетиловий ефір, при низькій температурі (наприклад, -78°C) за присутності реактиву, такого як бутиллітій. Реакцію гідрогенізації у процесі (x) та процесі (xi) можна проводити відповідно до технік, відомих у даній галузі, наприклад, за присутності органічного розчинника, такого як етанол, із застосуванням газу гідрогену та паладію на карбоновому каталізаторі при необхідних кислотнокаталітичних умовах. Процес (xii) являє собою аналог реакції Хорнера-Водсворта-Еммонса, как известно, наприклад, из Wadsworth, W. Org. React. 1977, 25, 73. Відповідні умови реакції для проведення реакцій даного типу відомі спеціалістам у даній галузі. Процеси (xiii) та (xiv) являють собою аналоги реакції циклопропанування алкенів СиммонсаСміта, наприклад, як описано Howard H. Simmons, Ronald D. Smith (1959) "A New Synthesis of Cyclopropanes" J. Am. Chem. S°C. 81 (16): 4256-4264. 1 Сполуки формули (IV), у якій P позначає захисну групу, таку як -CH2CH2C(O)°CH3, можна приготувати за допомогою реакції зі сполукою формули (II), як зазначено вище, з метил 3сульфанілпропаноатом. Сполуки формули (VII) можна приготувати за допомогою реакції зі сполукою формули (II), як зазначено вище, з діоксидом карбону у органічному розчиннику, такому як диетиловий ефір, при низькій температурі (наприклад, -78°C) за присутності реактиву, такого як бутиллітій. 4 Сполуки формули (X), у якій CR групи зв’язані карбон-карбоновим подвійним зв’язком, можна приготувати за допомогою процесів, що є аналогічними процесу (xii), описаному вище. 4 Сполуки формули (X), у якій CR групи зв’язані карбон-карбоновим потрійним зв’язком, 4 3 кожен R позначає атом гідрогену, та R позначає необов’язково заміщену гетероциклічну кільцеву систему, можна приготувати відповідно до наступної схеми реакції: 11 UA 111851 C2 5 10 15 20 25 (X) 1 Операцію 1 проводять за допомогою реакції сполуки піридазину (у якій R є таким, як зазначено вище) з етинілтриметилсиланом у органічному розчиннику, такому як тетрагідрофуран. Операцію 2 проводять із застосуванням калію карбонату у полярному розчиннику, такому як метанол. 3 3 Операцію 3 проводять із застосуванням сполуки формули R -Br, де R позначає необов’язково заміщену гетероциклічну кільцеву систему, як зазначено вище, за присутності йодиду міді(I) та відповідного каталізатора палладію. 4 Сполуки формули (X), у якій CR групи зв’язані карбон-карбоновим потрійним зв’язком, 4 3 кожен R позначає атом гідрогену, та R позначає необов’язково заміщену карбоциклічну кільцеву систему, можна приготувати відповідно до наступної схеми реакції: (II) (X) Операцію 4 проводять за допомогою реакції сполуки формули (II), як описано вище, зі 3 3 сполукою формули, HC C-R , де R позначає необов’язково заміщену карбоциклічну кільцеву систему, як зазначено вище, за присутності йодиду міді(I) та відповідного каталізатора палладію. Сполуки формули (XI) можна приготувати за допомогою реакції зі сполукою формули (II), як зазначено вище, з диметилформамідом у органічному розчиннику, такому як диетиловий ефір, при низькій температурі (наприклад, -78°C) за присутності реактиву, такого як бутиллітій, за якою необов’язково проводять реакцію алкілування. Сполуки формули (XII) можна приготувати за допомогою процесів, аналогічних тим, що використовують для приготування сполуки формули (X). Сполуки формули (XIII) можна приготувати відповідно до наступної схеми реакції: 12 UA 111851 C2 5 10 15 20 (XIII) Операцію a проводять із застосуванням, наприклад, цианіду міді. Сполука формули (II) є такою, як зазначено вище. 3 Операцію b проводять із застосуванням реактиву Гріньяра формули R -[Y]l-MgBr, де l, Y та 3 R є такими, як зазначено у формулі (XIII). Операцію c проводять із застосуванням розчину реактиву Теббе (біс(циклопентадиеніл)-μхлоро(диметилалюміній)-μ-метилентитан). Сполуки формул (II), (III), (V), (Va), (VI), (VIII), (IX), (IXa) та (IXb) є або комерційно доступними та добре відомими в літературі, або їх можна приготувати із застосуванням відомих технік. Даний винахід додатково забезпечує певні нові проміжні речовини, наприклад, проміжні речовини формули (XXX), (XXX) 1 2 20 де кожен з P та P незалежно представляють захисну групу (наприклад, бензил), R 1 позначає атом гідрогену або групу, що заміщується (наприклад, триметилсалін, Si(CH 3)3), та R є таким, як зазначено у формулі (I) вище. Спеціалістам у даній галузі буде зрозуміло, що у процесах даного винаходу функціональні групи, такі як фенольні, гідроксильні або аміно групи у реактивах можуть потребувати захисту із застосуванням захисних груп. Таким чином, приготування сполук формули (I) може включати, на відповідній стадії, видалення однієї або більше захисних груп. Захист та зняття захисту функціональних груп описано у «Захисні групи у органічній хімії» (Protective Groups in Organic Chemistry), за редакцією J.W.F. McOmie, Plenum Press (1973) та е «Захисні групи у органічному синтезі» (Protective Groups in Organic Synthesis), 3 видання, T.W. 13 UA 111851 C2 5 10 15 20 25 30 35 40 45 50 55 60 Greene та P.G.M. Wuts, Wiley-Interscience (1999). Сполуки формули (I) вище можна перетворити на їх фармацевтично прийнятні солі, переважно кислотно-адитивні солі, такі як солі гідрохлориду, гідроброміду, бензолсульфонату (бесилату), цукрину (наприклад, моноцукрину), трифторацетату, сульфату, нітрату, фосфату, ацетату, фумарату, малеату, тартрату, лактату, цитрату, пірувату, сукцинату, валерату, пропаноату, бутаноату, малонату, оксалату, 1-гідрокси-2-нафтоату (ксинафоату), метансульфонату або p-толуолсульфонату. У одному аспекті винаходу сполуки формули (I) можуть мати одну або більше радіоактивну мітку. Такі радіоактивні мітки можна вводити із застосуванням реактивів, що містять радіоактивну мітку, в синтезі сполук формули (I), або можна вводити із застосуванням зєднання сполук формули (I) з хелатоутворюючими компонентами, які мають здатність зв’язуватись з атомом радіоактивного металу. Такі радіо мічені версії сполук можна застосовувати, наприклад, у дослідженнях діагностичної візуалізації. Сполуки формули (I) та їх солі можуть бути у формі гідратів або сольватів, що утворюють один аспект даного винаходу. Такі сольвати можна створити зі звичайних органічних розчинників, включаючи, але не обмежуючись ними, спиртові розчинники, наприклад, метанол, етанол або ізопропанол. Сполуки формули (I) можуть існувати у стереоізомірних формах. Спеціалістам у даній галузі буде зрозуміло, що даний винахід охоплює застосування всіх геометричних та оптичних ізомерів (включаючи атропоізомери) сполук формули (I) та їх суміші, включаючи рацемати. Застосування таутомерів та їх сумішей також утворює аспект даного винаходу. Енантіомірно чисті форми є особливо бажаними. Сполуки формули (I) та їх фармацевтично прийнятні солі мають активність фармацевтичних препаратів, зокрема, як інгібітори ферменту оксидази D-амінокислот (DAAO), та, таким чином, їх можна застосовувати у лікуванні шизофренії та інших психотичних розладів (наприклад, психотичного розладу, психозу), деменції та інших когнітивних розладів, тривожних розладів (наприклад, генералізованого тривожного розладу), розладів настрою (наприклад, депресивних розладів, великих депресивних розладів, біполярних розладів, включаючи біполярний I та II, біполярну манію, біполярну депресію), розладів сну, розладів, які зазвичай вперше діагностують у ранньому дитячому віці, дитячому або підлітковому віці (наприклад, розладу дефіциту уваги та порушення соціальної поведінки), болю (наприклад, невропатичного болю) та нейродегенеративних розладів (наприклад, хвороби Паркінсона або хвороби Альцгеймера). Таким чином, даний винахід забеспечує сполуку формули (I) або її фармацевтично прийнятну сіль, як зазначено вище, для застосуванні у терапії, зокрема, для лікування захворювань, розвиток або симптоми яких пов’язують з активністю ферменту DAAO. Даний винахід також забеспечує застосування сполуки формули (I) або її фармацевтично прийнятної солі, як зазначено вище, для приготування лікарського препарату для лікування захворювань, розвиток або симптоми яких пов’язують з активністю ферменту DAAO. В контексті даної специфікації термін «терапія» також включає «профілактику», якщо не зазначено інакше. Терміни «терапевтичний» та «терапевтично» слід тлумачити відповідним чином. Очікують, що профілактика є релевантною, зокрема, до лікування осіб, які вже мали епізод або з інших причин належать до групи підвищеного ризику розвитку розладу або захворювання, що розглядається. До осіб, які належать до групи ризику розвитку певного розладу або захворювання, зазвичай належать особи з сімейним анамнезом розладу або захворювання, або особи, які були ідентифіковані за допомогою генетичного тестування або скринінгу, як такі, зокрема, що є чутливими до розвитку розладу або захворювання, або такі, що знаходяться у продромальній фазі розладу. Зокрема, сполуки винаходу (включаючи фармацевтично прийнятні солі) можна застосовувати у лікуванні позитивних симптомів шизофренії, шизофреноморфного розладу або шизоафективного розладу (наприклад, чуття голосів або галюцинацій), когнітивних розладів (таких як деменція та порушення здатності до навчання), а також болю (такого як невропатичний біль). Винахід також забезпечує метод лікування щонайменше одного симптому або захворювання, які пов’язують з шизофренією, шизофреноморфним розладом, шизоафективним розладом та іншими психотичними розладами (наприклад, психотичним розладом, психозом), деменцією та іншими когнітивними розладами, тривожними розладами (наприклад, генералізованим тривожним розладом), розладами настрою (наприклад, депресивними розладами, великим депресивним розладом, біполярним розладом, включаючи біполярний I та II, біполярну манію, біполярну депресію), розладами сну, розладами, які зазвичай вперше 14 UA 111851 C2 5 10 15 20 25 30 35 40 45 50 55 60 діагностують у ранньому дитячому віці, дитячому або підлітковому віці (наприклад, розлад дефіциту уваги та порушення соціальної поведінки), болем (наприклад, невропатичним болем) та нейродегенеративними розладами (наприклад, хворобою Паркінсона або хворобою Альцгеймера), що включає застосування пацієнтом, який має в цьому потребу, терапевтично еіективної кількості сполуки формули (I) або її фармацевтично прийнятної солі, як зазначено вище. Такі симптоми та захворювання включають, але не обмежуються ними, неспокій, збудженість, ворожість, паніку, порушення харчування, афективний симптом, симптом настрою, негативний та позитивний психотичний симптом, що зазвичай пов’язують з психозом та нейродегенеративним порушенням. Для терапевтичного застосування, вказаного вище, дози, звичайно, будуть відрізнятися в залежності від сполуки, що застосовується, способу введення, бажаного лікування та самого порушення. Наприклад, денна доза сполуки винаходу при застосування шляхом інгаляцій може варіюватися від 0,05 мікрограм на кілограм маси тіла (мкг/кг) до 100 мікрограм на кілограм маси тіла (мкг/кг). Однак, якщо сполуку застосовують перорально, денна доза сполуки винаходу може варіюватися від 0,01 мікрограм на кілограм маси тіла (мкг/кг) до 100 міліграм на кілограм маси тіла (мг/кг). Сполуки формули (I) та їх фармацевтично прийнятні солі можна застосовувати окремо, але зазвичай їх будуть застосовувати у вигляді фармацевтичної композиції, у якій сполука/сіль (активний інгредієнт) формули (I) зв’язується з фармацевтично прийнятним ад’ювантом, розчинником або носієм. Таким чином, даний винахід додатково забезпечує фармацевтичну композицію, яка містить сполуку формули (I) або її фармацевтично прийнятну сіль, як зазначено вище, у поєднання з фармацевтично прийнятним ад’ювантом, розчинником або носієм. Даний винахід додатково забезпечує процес приготування фармацевтичної композиції винаходу, що включає змішування сполуки формули (I) або її фармацевтично прийнятної солі, як зазначено вище з фармацевтично прийнятним ад’ювантом, розчинником або носієм. Традиційні процедури відбору та приготування відповідних фармацевтичних композицій описані у, наприклад, "Pharmaceutics - The Science of Dosage Form Design", M. E. Aulton, Churchill Livingstone, 1988. Фармацевтично прийнятні ад’юванти, розчинники або носії, які можна застосовувати у фармацевтичних композиціях даного винаходу, є такими, що традиційно застосовуються у галузі фармацевтичних композицій та включають, але не обмежуються ними, цукри, цукрові спирти, крохмалі, іонообмінники, оксид алюмінію, алюмінію стеарат, лецитин, білки сироватки крові, такі як альбумін сироватки крові людини, буферні речовини, такі як фосфати, гліцерин, сорбінова кислота, калію сорбат, суміші неповних гліцеридів насичених рослинних жирних кислот, воду, солі або електроліти, такі як протаміну сульфат, динатрію гідроген фосфат, калію гідроген фосфат, натрію хлорид, солі цинку, колоїдний діоксин кремнію, магнію трисилікат, полівінілпіролідон, речовини на основі целюлози, поліетиленгліколь, натрію карбоксиметилцелюлоза, поліакрилати, воски, поліетилен- поліоксипропілен-блок полімери, поліетиленгліколь та ланолін. Фармацевтичні композиції даного винаходу можна застосовувати перорально, парентерально, за допомогою спрію для інгалації, ректально, назально, трансбукально, інтравагінально або через імплантований резервуар. Пероральний спосіб застосування є переважним. Фармацевтичні композиції даного винаходу можуть містити будь-які традиційні нетоксичні фармацевтично прийнятні ад’юванти, розчинники або носії. Термін «парентерально» в даному контексті включає підшкірну, інтрадермальну, внутрішньовенну, внутрішньом’язову, інтраартикулярну, інтрасиновіальну, інтрастернальну, інтратекальну, інтраочагову та інтракраніальну техніку ін’єкції або інфузії. Фармацевтичні композиції можуть бути у формі стерильного препарату для ін’єкцій, наприклад, стерильної водної або маслянистої суспензії для ін’єкцій. Суспензію можна одержати відповідно до технік, відомих у даній галузі, із застосуванням відповідних дисперсійних або зволожувальних агентів (таких як, наприклад, Твін 80) та суспендуючи агентів. Стерильний препарат для ін’єкцій також може бути стерильним розчином для ін’єкцій або суспензією у нетоксичному парентерально прийнятному розріджувачі або розчиннику, наприклад, розчином у 1,3-бутандіолі. Прийнятними розріджувачами або розчинниками, що можна застосовувати, є манітол, вода, розчин Рінгера та ізотонічний розчин натрію хлориду. Окрім того, старильні, нелетючі олії традиційно застосовують як розчинник або суспендуючи середовище. З цією метою можна застосовувати будь-яку легку нелетючу оліб, включаючи синтетичні моно- або дигліцериди. Жирні кислоти, такі як олеїнова кислота та її гліцеридні 15 UA 111851 C2 5 10 15 20 25 30 35 40 45 50 55 60 похідні, є корисними у приготуванні ін’єкційних препаратів, як і природні фармацевтично прийнятні олії, такі як оливкова олія або касторова олія, особливо у їх поліоксиетилованих версіях. Ці олійні розчини або суспензії також можуть містити спиртовий розчинник з довгим ланцюгом або дисперсант, такі як описані у Фармакопеї Швейцарії, або подібний спирт. Фармацевтичні композиції даного винаходу можна застосовувати перорально у будь-якій перорально прийнятній формі дозування, включаючи, але не обмежуючись ними, капсули, таблетки, порошки, гранули та водні суспензії та розчини. Ці форми дозування готують відповідно до технік, які є добре відомими у галузі фармацевтичних композицій. У випадку таблеток для перорального застосування, носії, що традиційно використовують, включають лактозу та кукурудзяний крохмаль. Лубриканти, такі як магнію стеарат, також зазвичай додають. Для перорального застосування у формі капсул, корисні розріджувачі включають лактозу та висушений кукурудзяний крохмаль. Коли водні суспензії застосовують перорально, активний інгредієнт поєднують з емульгаторами та суспендуючи ми агентами. За бажанням можна додавати певні підсолоджувачі та/або смакові добавки, та/або барвники. Фармацевтичні композиції даного винаходу можна також застосовувати у формі ректальних супозиторій. Ці композиції можна приготувати змішуванням активного інгредієнту з відповідною неподразнюючою допоміжною речовиною, яка є твердою при кімнатній температурі і рідиною при температурі у прямій кишці, та, таким чином, буде плавитися у прямій кишці для вивільнення активного інгредієнту. Такі матеріали включають, але не обмежуються ними, масло какао, бджолиний віск та поліетиленгліколі. Фармацевтичні композиції даного винаходу можна застосовувати у вигляді назального аерозолю або інгаляції. Такі композиції готують відповідно до технік, які є добре відомими у галузі фармацевтичних композицій, та можна готувати у вигляді розчинів у фізіологічному розчині при застосуванні бензилового спирту або інших відповідних консервантів, промоторів абсорбції для збільшення біодоступності, фторкарбонів та/або інших солюбілізуючих або диспергуючих агентів, які є добре відомими у даній галузі. В залежності від шляху введення, фармацевтична композиція буде переважно містити від 0,05 до 99 %м (відсотків по масі), більш переважно від 0,05 до 80 %м, ще більш переважно від 0,10 до 70 %м та ще більш переважно від 0,10 до 50 %м активного інгредієнту, причому всі показники відсотків по масі базуються на загальній композиції. Сполуки даного винаходу (тобто сполуки формули (I) та їх фармацевтично прийнятні солі) можна також застосовувати у поєднанні з іншими сполуками, що застосовують у лікування захворювань, зазначених вище, та/або із серином. Винахід, таким чином, також стосується комбінаційних видів терапії, у яких сполука даного винаходу або фармацевтична композиція, або композиція, що містить сполуку даного винаходу, застосовується з іншим терапевтичним агентом або агентами та/або з серином для лікування одного або більше захворювань, зазначених вище. Такі терапевтичні агенти можуть бути вибрані з наступних: (i) антидепресанти, такі як, наприклад, амітриптилін, амоксапін, бупропіон, циталопрам, кломіпрамін, дезіпрамін, доксепін дулоксетін, елзасонан, есциталопрам, флувоксамін, флуоксетин, гепірон, іміпрамін, іпсапірон, мапротілін, нортриптілін, нефазодон, пароксетін, фенелзін, протриптілін, ребоксетін, робаізотан, сертралін, сібутрамін, тіонізоксетін, транілципромін, тразодон, триміпрамін, венлафаксин та їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (ii) атипові антипсихотичні засоби, включаючи, наприклад, кветіапін та його фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (iii) антипсихотичні засоби, включаючи, наприклад, амісульприд, аріпіпразол, азенапін, бензизоксиділ, біфепрунокс, карбамазепін, клозапін, хлорпромазин, дебензапін, дівалпрекс, дулоксетин, есзопіклон, галоперідол, ілоперідол, ламотриджин, локсапін, мезорідазин, оланзапрін, паліперідон, перлапін, перфеназин, фенотіазин, фенілбутліпіперідин, пімозід, прохлорперазин, рісперідон, сертіндол, сулпірид, супроклон, суріклон, тіорідазин, трифлуоперазин, триметозин, вальпроат, вальпроєва кислота, зопіклон, зотепін, ципразідон та їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (iv) анксиолітичні засоби, включаючи, наприклад, алнеспірон, азапірони, бензодіазепіни, барбітурати та їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и). Приклади анксиолітиків включають адінозолам, алпразолам, балезепам, бентазепам, бромазепам, бротізолам, буспірон, клоназепам, клоразепат, хлордіазепоксид, ципразепам, діазепам, діфенгідрамін, естазолам, фенобам, флунітразепам, флуразепам, фозазепам, лоразепам, лорметазепам, мепробамат, мідазолам, нітразепам, оксазепам, празепам, квазепам, реклазепам, траказолат, трепіпам, темазепам, триазолам, улдазепам та золазепам; 16 UA 111851 C2 5 10 15 20 25 30 35 40 45 50 55 60 та їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (v) антиконвульсанти, включаючи, наприклад, карбазепін, вальпроат, ламотриджин та габапентин, та їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (vi) препарати проти хвороби Альцгеймера, включаючи, наприклад, донепезил, мемантин, та крин та їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (vii) препарати проти хвороби Паркінсона, включаючи, наприклад, депреніл, L-допа, реквіп, мірапекс, інгібітори МАО-Б, такі як селегін та разагілін, інгібітори КОМТ, такі як тасмар, A-2 інгібітори, інгібітори зворотного захвату допаміну, агоністи NMDA, агоністик нікотину та агоністик допаміну, а також інгібітори нейрональної синтази оксиду нітрогену та їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (viii) препарати проти мігрені, включаючи, наприклад, алмотриптан, амантадин, бромокріптин, буталбітал, каберголін, діхлоралфеназон, елетриптан, фроватриптан, лізурид, наратриптан, перголід, праміпексол, різатриптан, ропінірол, суматриптан, золмітриптан та зомітриптан, а какож їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (ix) препарати проти інсульту, включаючи, наприклад, абциксимаб, актіваз, NXY-059, цитиколін, кробенетін, десмотеплаза, репінотан, траксопроділ та їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (x) препарати проти нетримання сечі, включаючи, наприклад, дарафенацин, фалвоксат, оксибутинін, пропіверін, робалзотан, соліфенацин та толтерадин, а також їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (xi) препарати проти невропатичного болю, включаючи, наприклад, габапентин, лідодерм та прегаблін, а також їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (xii) препарати проти ноцицептивного болю, такі як, наприклад, целекоксиб, еторікоксиб, луміракоксиб, рофекоксиб, валдекоксиб, діклофенак, локсопрофен, напроксен та парацетамол, а також їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (xiii) препарати проти безсоння, включаючи, наприклад, алобарбітал, алонімід, амобарбітал, бензоктамін, бутабарбітал, капурід, хлорал, клоперідон, клоретат, декскламол, етхлорвінол, етомідат, глутетімід, халазепам, гідроксизин, меклоквалон, мелатонін, мефобарбітал, метаквалон, мідафлур, нізобамат, пентобарбітал, фенобарбітал, пропофол, ролетамід, триклофос, секобарбітал, залеплон та золпідем, а також їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (xiv) стабілізатори настрою, включаючи, наприклад, карбамазепін, дівалпроекс, габапентин, ламотриджин, літій, оланзапін, кветіапін, валпроат, вальпроева кислота та верапаміл, а також їх еквіваленти та фармацевтично активний(і) ізомер(и) та/або метаболіт(и); (xv) ліганди 5HT1B такі як, наприклад, сполуки, розкриті у WO 99/05134 та WO 02/08212; (xvi) агоністи mGluR2; (xvii) альфа 7 нікотинові агоністи такі як, наприклад, сполуки, розкриті у WO 96/006098, WO 97/030998, WO 99/003859, WO 00/042044, WO 01/029034, WO 01/60821, WO 01/36417, WO 02/096912, WO 03/087102, WO 03/087103, WO 03/087104, WO 2004/016617, WO 2004/016616 та WO 2004/019947; (xviii) інгібітори хемокінового рецептора CCRl; та (xix) дельта опоїдні агоністи такі як, наприклад, сполуки, розкриті у WO 97/23466 та WO 02/094794. У зазначених комбінаціях продуктів застосовують сполуки даного винаходу в межах діапазону доз, описаному у даній заявці, та інший фармацевтично активний агент в межах ухваленого діапазону доз та/або у доуванні, такому як описано у публікації посилання. Інший аспект даного винаходу забеспечує комбінацію (наприклад, для лікування шизофренії, когнітивних порушень або болю) сполуки формули (I) або її фармацевтично прийнятної солі, як зазначено вище, та одного або більше агентів, вибраних з карбамазепіну, оланзепіну, кветіапіну, верапамілу, ламотриджину, окскарбамазепіну, рисперідону, аріпіпразолу, зіпрасідону та літію. Винахід також забезпечує фармацевтичний продукт, що включає, у комбінації, препарат першого активного інгредієнту, який являє собою сполуку формули (I) або її фармацевтично прийнятну сіль, як зазначено вище, та препарат другого активного інгредієнту, який являє собою карбамазепін, оланзепін, кветіапін, верапаміл, ламотриджин, окскарбамазепін, рисперідон, аріпіпразол, зіпрасідон або літій, для одночасного, полідовного або окремого застосування у терапії. У іншому аспекті винахід забезпечує набір, який включає препарат першого активного інгредієнту, який являє собою сполуку формули (I) або її фармацевтично прийнятну сіль, як зазначено вище, та препарат другого активного інгредієнту, який являє собою карбамазепін, 17 UA 111851 C2 5 10 15 20 25 30 35 оланзепін, кветіапін, верапаміл, ламотриджин, окскарбамазепін, рисперідон, аріпіпразол, зіпрасідон або літій, а також інструкції для одночасного, полідовного або окремого застосування препаратів у пацієнта, який цього потребує. Даний винахід буде додатково пояснено шляхом посилання на наступні ілюстративні приклади. Методи, які застосовують для синтеза сполук даного винаходу проілюстровані за допомогою загальних схем, наведених нижче, та препаративних прикладів, що йдуть за ними. Вихідні матеріали та реактиви, що застосовують при приготуванні зазначених сполук є доступними через комерційних постачальників. Ці загальні схеми мають винятково ілюстративний характер щодо методів, із застосуванням яких сполуки даного винаходу можна синтезувати, та різні модифікації зазначених схем можуть бути розроблені та будуть запропоновані спеціалісту у даній галузі з посиланням на дане розкриття. Спектри ядерного магнітного резонансу (ЯМР) реєструють на 400М Гц; хімічні зсуви () представлені у частинах на мільон. Спектри реєстрували при застосуванні інструменту Bruker 400 Avance Bruker 400 з 5мм датчиком BBFO або датчиком DUL. Інструментальний контроль проводили за допомогою програмного забеспечення Bruker TopSpin 2.1, якщо інакше не зазначено. Чистоту оцінювали із застосуванням НПРХ з УФ (фотодіодна матриця) детектором у широкому діапазоні довжини хвилі, зазвичай 220-450нм, із застосуванням системи Waters Acquity для НПРХ, обладнаної колонками BEH або HSS C18 Acquity для НПРХ (2,1мм у діаметрі x 50мм у довжину), температура 50 або 60°C. Рухомі фази типово складалися з суміші ацетонітрилу або метанолу з водою, що містила 0,05% мурашиної кислоти або 0,025% амонію. Мас-спектри реєстрували за допомогою одноквадрупольного мас-спектрометра Waters SQD із застосуванням іонізації атмосферного тиску, якщо інакше не зазначено. Сполуки очищували із застосуванням хроматографії з нормальними фазами на кварці або оксиді алюмінію або за допомогою зворотно-фазових методів хроматографії з картриджем Biotage або Isolute KPNH, картриджем SCX та картриджами твердофазної екстракції SCX-2. Препаративну високоефективну рідинну хроматографію (ВЕРХ) проводили із застосуванням системи Agilent Technologies 1100 Series, типово використовували колонки C18 Waters 19мм у діаметрі x 100мм у довжину, такі як XBridge або SunFire 5мкм матеріали при 20 мл/хвил. Рухомі фази типово складалися з суміші ацетонітрилу або метанолу з водою, що містила 0,1% мурашиної кислоти або 0,1% амонію, якщо інакше не зазначено. У описах, наведених нижче, термін «кімнатна температура» позначає температуру від 20°C до 25°C. Скорочення, які застосовано у специфічних прикладах, мають наступні значення: ДМСО Диметилсульфоксид ДМСО-d6 Дейтерований диметилсульфоксид MeOH-d Дейтерований метанол MeOH Метанол МС мас-спектр ЯМР Ядерний магнітний резонанс Pd2(DBA)3 Трис(дибензиліденацетон)дипаладій(0) MgSO4 Магнію сульфат КСАНТФОС 4,5-Біс(дифенілфосфіно)-9,9-диметилксантен ДБУ 2,3,4,6,7,8,9,10-Октагідропіримідо[1,2-a]азепін CHCl3 Трихлорометан CDCl3 Дейтерований трихлорометан CD2Cl2 Дейтерований дихлорметан МТБЕ Метил трет-бутиловий ефір ТГФ Тетрагідрофуран CO2 Діоксид карбону 1. Проміжні продукти Схема 1: Проміжний продукт 1: 3,4-біс(Бензилоксі)-6-хлоропіридазин 18 UA 111851 C2 5 10 15 20 25 30 35 Фенілметанол (6,72 г, 62,2 ммоль) покрапельно додають до суспензії натрію гідриду (60 % суспензія у мінеральній олії; 2,486 г, 62,2 ммоль) у тетрагідрофурані (загальний об’єм: 100 мл) при кімнатній температурі. Одержану суміш перемішують протягом 1 години та потім охолоджують до температури 0°C перед додаванням 3,4,6-трихлоропіридазину (5,7 г, 31,1 ммоль) кількома порціями протягом 10 хвилин. Ракції потім дають нагрітися до кімнатної температури та перемішують протягом 16 годин перед тим, як виливають у воду та екстрагують за допомогою етилацетату (двічі). Органічний шар промивають розсолом, сушать (магнію сульфат) та випарюють. Залишок очищують за допомогою кварцової хроматографії (елюювання із застосуванням 5-20 % етилацетату у бензині, що містить 5 % тетрагідрофурану) для одержання 3,4-біс(Бензилоксі)-6-хлоропіридазину (4,0 г, 12,24 ммоль, 39,4 % вихід) як основного продукту. 1 H ЯМР (400 МГц, ДМСО-d6): ppm 7,31-7,52 (m, 11 H) 5,51 (s, 2 H) та 5,31 (s, 2 H). Проміжний продукт 2: 3,4-біс(Бензилоксі)-6-(фенілетиніл)піридазин Мікрохвильову віалу ємністю 20 мл наповнюють 3,4-біс(Бензилоксі)-6-хлоропіридазином (Проміжний продукт 1; 440 мг, 1,35 ммоль), ДБУ (1230 мг, 8,08 ммоль) та етинілбензолом (413 мг, 4,04 ммоль) у тетрагідрофурані (5 мл) для одержання розчину оранжевого кольору. Суміш продувають нітрогеном та додають дихлоробіс(трифенілфосфін)паладій(II) (47,3 мг, 0,067 ммоль) та йодид міді(I) (25,6 мг, 0,135 ммоль), після чого всю суміш піддіють дії мікрохвильового випромінення протягом 1 години при температурі 80°C. Після охолодження одержану суміш розводять етилацетатом та промивають розсолом, а органічний шар очищують за допомогою кварцової хроматографії (елюювання із застосуванням 0-30 % етилацетат-бензину) для одержання 3,4-біс(Бензилоксі)-6-(фенілетиніл)піридазину (320 мг, 0,815 ммоль, 61 % вихід). 1 H ЯМР (400 МГц, ДМСО-d6): 7,34 - 7,58 (m, 15 H), 7,06 (s, 1 H), 5,56 (s, 2 H) та 5,34 (s, 2 H). + MS ES : 393. Проміжний продукт 3: 3,4-біс(Бензилоксі)-6-[(4-фторфеніл)етиніл]піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-(фенілетиніл)піридазину (Проміжний продукт 2), з 3,4-біс(Бензилоксі)-6-хлоропіридазином (Проміжний продукт 1) та 1-етиніл-4-фторбензолом на виході 72 %. 1 H ЯМР (400 МГц, ДМСО-d6): 7,67-7,76 (m, 2 H), 7,57 (s, 1 H), 7,29-7,53 (m, 12 H), 5,58 (s, 2 H) та 5,31 (s, 2 H). + MS ES : 410. Схема 2: Проміжний продукт 4: 3,4-біс(Бензилоксі)-6-[(триметилсиліл)етиніл]піридазин 40 Мікрохвильову віалу ємністю 20 мл наповнюють 3,4-біс(Бензилоксі)-6-хлоропіридазином (Проміжний продукт 1, 3,06 ммоль) та етинілтриметилсаліном (902 мг, 9,18 ммоль) у тетрагідрофурані (5 мл) для одержання розчину оранжевого кольору. Реакційну суміш продувають нітрогеном та додають ДБУ (2,77 мл, 18,36 ммоль), 19 UA 111851 C2 5 10 15 20 дихлоробіс(трифенілфосфін)паладій(II) (107 мг, 0,153 ммоль) та йодид міді(I) (58,3 мг, 0,306 ммоль), після чого всю суміш піддіють дії мікрохвильового випромінення протягом 1 години при температурі 80°C. Після охолодження одержану суміш розводять етилацетатом та промивають розсолом. Органічний шар очищують за допомогою кварцової хроматографії (елюювання із застосуванням 0-30 % етилацетату у бензині) для одержання 3,4-біс(Бензилоксі)-6((триметилсиліл)етиніл)піридазину (838 мг, 2,16 ммоль, 70 % вихід) 1 H ЯМР (400 МГц, ДМСО-d6): 7,08-7,28 (m, 11 H), 5,32 (s, 2 H), 5,06 (s, 2 H) та 0,08 (s, 9 H) + MS ES : 389. Проміжний продукт 5: 3,4-біс(Бензилоксі)-6-етинілпіридазин Калію карбонат (295 мг, 2,136 ммоль), 3,4-біс(Бензилоксі)-6-((триметилсиліл)етиніл) піридазин (Проміжний продукт 4; 830 мг, 2,14 ммоль) та метанол (10 мл) додають до тетрагідрофурану (5 мл) для одержання суспензії оранжевого кольору. Суміш перемішують протягом 1 години та після цього ділять між розсолом та етилацетатом. Органічний шар промивають розсолом та випарюють, після чого залишок очищують за допомогою кварцової хроматографії (елюювання із застосуванням 10-50 % етилацетату у бензині) для одержання 3,4біс(Бензилоксі)-6-етинілпіридазину (530 мг, 1,68 ммоль, 78 % вихід). 1 H ЯМР (400 МГц, ДМСО-d6): 7,31-7,53 (m, 11 H), 5,59 (s, 2 H), 5,30 (s, 2 H) та 4,53 (s, 1 H). + MS ES : 317. Схема 3: Проміжний продукт 6: 3,4-біс(Бензилоксі)-6-{[5-(трифторметил)піридин-2-іл]етиніл}піридазин 25 30 35 3,4-біс(Бензилоксі)-6-етинілпіридазин (Проміжний продукт 5; 530 мг, 1,68 ммоль) та 2-бромо5-(трифторметил)піридин (379 мг, 1,68 ммоль) розчиняють у тетрагідрофурані (5 мл) для одержання розчину оранжевого кольору. Реакційну суміш продувають нітрогеном та додають триетиламін (1,40 мл, 10,05 ммоль), дихлорбіс(трифенілфосфін)паладій(II) (58,8 мг, 0,08 ммоль) та йодид міді(I) (31,9 мг, 0,17 ммоль), після чого всю суміш піддіють дії мікрохвильового випромінення протягом 1 години при температурі 80°C. Після охолодження одержану суміш розводять етилацетатом та промивають розсолом. Органічний шар концентрують in vacuo, після чого неочищений залишок очищують за допомогою кварцової хроматографії (елюювання із застосуванням 0-50 % етилацетату у бензині) для одержання 3,4-біс(Бензилоксі)-6-{[5(трифторметил)піридин-2-іл]етиніл}піридазину (460 мг, 0.10 ммоль, 60 % вихід). 1 H ЯМР (400 МГц, ДМСО-d6): 9,08 (s, 1 H), 8,34-8,38 (m, 1 H), 7,96-8,01 (m, 1 H), 7,70 (s 1 H), 7,33-7,53 (m, 10 H), 5,61 (s, 2 H) та 5,33 (s, 2 H). + MS ES : 462. Схема 4: Проміжний продукт 7: 6-Хлоро-3,4-біс[(4-метоксибензил) оксі]піридазин 20 UA 111851 C2 5 10 15 20 25 30 35 40 До розчину (4-метоксифеніл)метанолу (1,88 г, 13,63 ммоль) у тетрагідрофурані (7,89 мл) додають розчин калію трет-бутоксиду у тетрагідрофурані (13,63 мл, 13,63 ммоль). Після перемішування при кімнатній температурі протягом 1,5 годин суміш охолоджують до температури 0°C та додають трихлоропіридазин (1,0 г, 5.45 ммоль) порціями протягом приблизно 5-10 хвилин. Одержану в результаті суміш залишають, перемішуючи та нагріваючи до кімнатної температури, на 16 годин, апотім виливають у воду, екстрагують у етилацетаті, та об’єднані органічні речовини висушують (магнію сульфат). Після цього розчин випарюють in vacuo та очищують за допомогою кварцової хроматографії (елюювання із застосуванням 0-40 % етилацетату у бензині) для одержання 6-хлоро-3,4-біс[(4-метоксибензил)oxy]піридазину (550 мг, 1,420 ммоль, 26 % вихід). 1 H ЯМР (400 МГц, MeOH-d): 7,51 (s, 1 H), 7,38-7,45 (m, 4 H), 6,91-6,99 (m, 4 H), 5,39 (s, 2 H), 5,19 (s, 2 H) та 3,76 (s, 6 H). Проміжний продукт 8: 6-[(4-Хлоробензіл)сульфаніл]-3,4-біс[(4-метоксибензил)оксі]піридазин Суміш 6-хлоро-3,4-біс[(4-метоксибензил)оксі]піридазину (Проміжний продукт 7; 550 мг, 1,42 ммоль), (4-хлорофеніл)метантіолу (248 мг, 1,56 ммоль), Pd2(DBA)3 (52,1 мг, 0.057 ммоль), КСАНТФОС (65,8 мг, 0,114 ммоль) та лугу Хуніга (етил диізопропіламін; 404 мг, 3,13 ммоль) піддають дії мікрохвильового випромінення протягом 1 години при температурі 120°C. Одержану в результаті суміш виливають у воду та екстрагують у етилацетаті, після чого об’єднані органічні речовини промивають розсолом та висушують (магнію сульфат). Одержаний в результаті розчин випарюють in vacuo та очищують за допомогою кварцової хроматографії (елюювання із застосуванням 0-40 % дихлорметану у бензині) для одержання 6-[(4хлоробензіл)сульфаніл]-3,4-біс[(4-метоксибензил)оксі] піридазину (201 мг, 1,42 ммоль, 28 % вихід). 1 H ЯМР (400 МГц, MeOH-d): 7,25-7,48 (m, 8 H), 6,88-6,95 (m, 4 H), 5,42 (s, 2 H), 5,08 (s, 2 H), 4,41 (s, 2 H) та 3,83 (s, 6 H). + MS ES : 509. Проміжний продукт 9: 3,4-біс(Бензилоксі)-6-{[6-(трифторметил)піридин-3-іл]етиніл}піридазин Мікрохвильову віалу наповнюють 5-йодо-2-(трифторметил)піридином (617 мг, 2,260 ммоль), йодидом міді(I) (39,1 мг, 0,205 ммоль), біс(трифенілфосфін)паладій(II) хлоридом (72,1 мг, 0,103 ммоль), 1,8-діазабіциклоундец-7-ене (ДБУ; 1858 мкл, 12,33 ммоль) та тетрагідрофураном (6849 мкл). Реакційну суміш потім продувають та обкачують нітрогеном та потім додають 3,4біс(Бензилоксі)-6-етинілпіридазин (Проміжний продукт 5: 650 мг, 2,1 ммоль). Реакційну суміш нагрівають до температури 80°C, при цьому піддають дії мікрохвильового випромінення протягом 1 години. Після охолодження реакційну суміш розділяють між етилацетатом та водою, при чому утворюється тверда речовина, яку фільтрують та відкидають. Органічні речовини промивають водою та розсолом, висушують (MgSO 4), фільтрують та концентрують для одержання олії коричневого кольору. Її очищують за допомогою кварцової хроматографії (елюювання із застосуванням 0-100 % етилацетату у бензині) для одержання 3,4 21 UA 111851 C2 біс(Бензилоксі)-6-{[6-(трифторметил)піридин-3-іл]етиніл}піридазину у вигляді аморфної твердої речовини жовтого кольору (вихід = 10 %) + MS ES : 462. Проміжний продукт 10: 3,4-біс(Бензилоксі)-6-[(3-фторфеніл)етиніл]піридазин 5 10 15 20 25 30 Готують, як описано для 3,4-біс(Бензилоксі)-6-(фенілетиніл)піридазину (Проміжний продукт 2), з 3,4-біс(Бензилоксі)-6-хлоропіридазином (Проміжний продукт 1) та 1-етиніл-3фторбензолом. 1 H ЯМР (400 МГц, ДМСО-d6): 7,32-7,64 (m, 15 H), 5,56 (s, 2 H) та 5,30 (s, 2 H). + MS ES : 411. Проміжний продукт 11: 3,4-біс(Бензилоксі)-6-[(2-фторфеніл)етиніл]піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-(фенілетиніл)піридазину (Проміжний продукт 2), з 3,4-біс(Бензилоксі)-6-хлоропіридазином (Проміжний продукт 1) та 1-етиніл-2фторбензолом. 1 H ЯМР (400 МГц, ДМСО-d6): 7,63-7,76 (m, 1 H), 7,58 (s, 2 H), 7,30-7,50 (m, 12 H), 5,59 (s, 2 H) та 5,32 (s, 2 H). + MS ES : 411. Проміжний продукт 12: 3,4-біс(Бензилоксі)-6-[(3,5-дифторфеніл)етиніл]піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-(фенілетиніл)піридазину (Проміжний продукт 2), з 3,4-біс(Бензилоксі)-6-хлоропіридазином (Проміжний продукт 1) та 1-етиніл-3,5дифторбензолом. 1 H ЯМР (400 МГц, ДМСО-d6): 7,63 (s, 1 H), 7,32-7,52 (s, 13 H), 5,59 (s, 2 H) та 5,30 (s, 2 H). + MS ES : 429. Проміжний продукт 13: 3,4-біс(Бензилоксі)-6-[2-(3,4-дифторфеніл)етиніл]піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-(фенілетиніл)піридазину (Проміжний продукт 2), з 3,4-біс(Бензилоксі)-6-хлоропіридазином (Проміжний продукт 1) та 1-етиніл-3,4дифторбензолом. 1 H ЯМР (400 МГц, ДМСО-d6): 7,52-7,67 (s, 1 H), 7,36-7,59 (s, 13 H), 5,58 (s, 2 H) та 5,31 (s, 2 22 UA 111851 C2 H). + MS ES : 429. Проміжний продукт 14: 3,4-біс(Бензилоксі)-6-{2-[3-(трифторметокси)феніл]етиніл}піридазин 5 10 15 20 25 30 Готують, як описано для 3,4-біс(Бензилоксі)-6-(фенілетиніл)піридазину (Проміжний продукт 2), з 3,4-біс(Бензилоксі)-6-хлоропіридазином (Проміжний продукт 1) та 1-етиніл-3трифторметоксибензолом (Готують, як описано у опублікованій міжнародній патентній заявці № WO 2005/94822, див. Препарат 28). 1 H ЯМР (400 МГц, ДМСО-d6): 7,60-7,75 (m, 3 H), 7,31-7,57 (s, 12 H), 5,58 (s, 2 H) та 5,28 (s, 2 H). + MS ES : 477. Проміжний продукт 15: 3,4-біс(Бензилоксі)-6-{2-[3-(трифторметил)феніл]етиніл}піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-{[6-(трифторметил)піридин-3іл]етиніл}піридазину (Проміжний продукт 9), з 3,4-біс(Бензилоксі)-6-етинілпіридазином (Проміжний продукт 5) та 1-йодо-3-(трифторметил)бензолом. 1 H ЯМР (400 МГц, ДМСО-d6): 8,01 (s, br, 1 H), 7,96 (d, J=7,83 Hz, 1 H), 7,87 (d, J=7,83 Hz, 1 H), 7,70-7,77 (m, 1 H), 7,64 (s, 1 H), 7,29-7,52 (m, 10 H), 5,59 (s, 2 H), 5,31 (s, 2 H). + MS ES : 461. Проміжний продукт 16: 3,4-біс(Бензилоксі)-6-{2-[5-(трифторметил)піридин-3іл]етиніл}піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-{[6-(трифторметил)піридин-3іл]етиніл}піридазину (Проміжний продукт 9), з 3,4-біс(Бензилоксі)-6-етинілпіридазином (Проміжний продукт 5) та 3-бромо-5-трифторметилпіридином. + MS ES : 462. Проміжний продукт 17: 3,4-біс(Бензилоксі)-6-(циклогексилетиніл)піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-(фенілетиніл)піридазину (Проміжний продукт 2), з 3,4-біс(Бензилоксі)-6-хлоропіридазином (Проміжний продукт 1) та етинілциклогексаном. 1 H ЯМР (400 МГц, CD2Cl2) 7,54-7,56 (m, 2 H), 7,33-7,48 (m, 8 H), 6,92 (s, 1 H), 5,63 (s, 2 H), 5,17 (s, 2 H), 2,61-2,73 (m, 1H), 1,90-2,00 (m, 2 H), 1,75-1,84 (m, 2 H), 1,52-1,67 (m, 4 H), 1,35-1,46 (m, 2 H). 23 UA 111851 C2 + MS ES : 399. Проміжний продукт 18: 3,4-біс(Бензилоксі)-6-(циклопропілетиніл)піридазин 5 10 15 20 25 30 Готують, як описано для 3,4-біс(Бензилоксі)-6-(фенілетиніл)піридазину (Проміжний продукт 2), з 3,4-біс(Бензилоксі)-6-хлоропіридазином (Проміжний продукт 1) та етинілциклопропаном. 1 H ЯМР (400 МГц, ДМСО-d6) 7,14-7,55 (m, 11 H), 5,53 (s, 2 H), 5,25 (s, 2 H), 1,57-1,67 (m, 1 H), 0,92-0,99 (m, 2 H), 0,77-0,84 (m, 2 H). + MS ES : 357. Проміжний продукт 19: 3,4-біс(Бензилоксі)-6-(циклопентилетиніл)піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-(фенілетиніл)піридазину (Проміжний продукт 2), з 3,4-біс(Бензилоксі)-6-хлоропіридазином (Проміжний продукт 1) та етинілциклопентаном. 1 H ЯМР (400 МГц, CD2Cl2) 7,28-7,55 (m, 10 H), 6,82-6,90 (m, 1 H), 5,57 (s, 2 H), 5,14 (s, 2 H), 2,79-2,94 (m, 1 H), 1,97-2,13 (m, 2 H), 1,49-1,86 (m, 6 H) + MS ES : 385. Проміжний продукт 20: 3,4-біс(Бензилоксі)-6-[(4-метоксициклогекс-1-ен-1-іл)етиніл]піридазин Мікрохвильову реакційну віалу наповнюють 4-метоксициклогекс-1-еніл трифторметансульфонатом (1069 мг, 4,11 ммоль), йодидом міді(I) (16,83 мг, 0,09 ммоль), тетракіс(трифенілфосфін)паладієм(0) (54,6 мг, 0,05 ммоль), триетиламіном (1432 мкл, 10,27 ммоль) та сухим N,N-диметилформамідом (6849 мкл). Реакційну суміш відкачують та продувають нітрогеном, додають розчин 3,4-біс(Бензилоксі)-6-етинілпіридазину (Проміжний продукт 5; 650 мг, 2,06 ммоль) у сухому тетрагідрофурані (3 мл), після чого все перемішують у мікрохвильовій пічі при температурі 70°C протягом 1 години. Після охолодження одержану суміш розділяють між етилацетатом та водою, органічні екстракти промивають водою та розсолом, сушать (MgSO4), фільтрують та концентрують для одержання олії коричневого кольору. Ії очищують за допомогою хроматографії на кварці, вимиваючи 0-75 % етилацетатом у бензині для одержання 3,4-біс(Бензилоксі)-6-[(4-метоксициклогекс-1-ен-1-іл)етиніл]піридазину (Проміжний продукт 20) у вигляді олії коричневого кольору (860 мг, 85 %). 1 H ЯМР (400 МГц, CD2Cl2) 7,28-7,57 (m, 10 H), 6,90 (s, 1 H), 6,22 (br s, 1 H), 5,60 (s, 2 H), 5,14 (s, 2 H), 3,45-3,55 (m, 1 H), 3,31-3,38 (m, 3 H), 2,10-2,56 (m, 4 H), 1,88-1,97 (m, 1 H), 1,64-1,78 (m, 1 H) + MS ES : 427. Проміжний продукт 21: 3,4-біс(Бензилоксі)-6-[(2,4-дифторфеніл)етиніл]піридазин 24 UA 111851 C2 5 10 15 20 25 30 Готують, як описано для 3,4-біс(Бензилоксі)-6-(фенілетиніл)піридазину (Проміжний продукт 2), з 3,4-біс(Бензилоксі)-6-хлоропіридазином (Проміжний продукт 1) та 1-етиніл-2,4дифторбензолом. 1 H ЯМР (400 МГц, CD2Cl2) 7,49-7,67 (m, 3 H), 7,31-7,51 (m, 8 H), 6,85-7,07 (m, 3 H), 5,70 (s, 2 H), 5,23 (s, 2 H). + MS ES : 429. Проміжний продукт 22: 3,4-біс(Бензилоксі)-6-{[3-(дифторметил)феніл]етиніл}піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-{[6-(трифторметил)піридин-3іл]етиніл}піридазину (Проміжний продукт 9), з 3,4-біс(Бензилоксі)-6-етинілпіридазином (Проміжний продукт 5) та 3-бромо-5-дифторметилпіридином. 1 H ЯМР (400 МГц, CDCl3) 7,65-7,85 (m, 2 H), 7,21-7,65 (m, 12 H), 6,99 (s, 1 H), 6,40-6,90 (m, 1 H, CHF2), 5,70 (s, 2 H), 5,24 (s, 2 H). + MS ES : 443. Проміжний продукт 23: 6-Бензил-3,4-біс(Бензилоксі)піридазин До розчину 3,4-біс(Бензилоксі)-6-хлоропіридазину (Проміжний продукт 1: 0,22 г, 0,67 ммоль) у тетрагідрофурані (6 мл) та воді (0,6 мл) додають цезію карбонат (0,66 г, 2,01 ммоль) та [1,1’біс(дифенілфосфіно)ферроцен]дихлоропаладій (II) (0,049 г, 0,067 ммоль). Реакційну суміш продувають та відкачують нітрогеном декілька разів, після чого додають 9-бензил-9борабіцикло[3.3.1]нонан (9-BBN; 4,02 мл, 2.01 ммоль). Після цього реакційну судину укупорюють та нагрівають до температури 60°C протягом 1 години. Після охолодження одержану суміш розводять етилацетатом та промивають 5 разів сумішшю 1:1 води та насиченого водного розсолу. Органічну частину висушують (MgSO4), фільтрують та концентрують для одержання олії оранжевого колоьру. Неочищену олію очищують за допомогою кварцової хроматографії (елюювання із застосуванням 0-80 % етилацетату у бензині) для одержання 6-бензил-3,4-біс (Бензилоксі)піридазину у вигляді безбарвної олії (вихід = 64 %). 1 H ЯМР (400 МГц, CDCl3) 7,56 (d, J = 7,33 Hz, 2 H), 7,12-7,48 (m, 13 H), 6,55 (s, 1 H), 5,64 (s, 2 H), 5,08 (s, 2 H), 4,17 (s, 2 H). + MS ES : 383. Проміжний продукт 24: 3,4-біс(Бензилоксі)-6-((3-хлорофеніл)етиніл)піридазин До розчину 1-хлоро-3-йодобензолу (0,862 г, 3,62 ммоль) у сухому тетрагідрофурані (11 мл) 25 UA 111851 C2 5 10 15 20 25 30 35 40 45 додають йодид міді(I) (0,063 г, 0,33 ммоль), біс(трифенілфосфін)паладій(II) хлорид (0,115 г, 0,16 ммоль) та 1,8-діазабіциклоундец-7-ен та (ДБУ; 2,97 мл, 19,72 ммоль). Реакційну суміш продувають та відкачують нітрогеном декілька разів, після чого додають 3,4-біс(Бензилоксі)-6етинілпіридазин (Проміжний продукт 5; 1,04 г, 3,29 ммоль). Після цього реакційну судину укупорюють та нагрівають до температури 80°C протягом 1 години. Після охолодження одержану суміш розділяють між етилацетатом та водою. Об’єднані органічні частини промивають водою (x 2) та розсолом, сушать (MgSO4), фільтрують та концентрують для одержання олії коричневого кольору. Неочищену олію очищують за допомогою кварцової хроматографії (елюювання із застосуванням 0-20 % етилацетату у бензині) для одержання 3,4біс(Бензилоксі)-6-((3-хлорофеніл)етиніл)піридазину у вигляді твердої речовини жовтого кольору (вихід = 30 %). 1 H ЯМР (400 МГц, CDCl3) 7,21-7,65 (m, 14 H), 6,97 (s, 1 H), 5,70 (s, 2 H), 5,23 (s, 2 H). + MS ES : 427/429. Проміжний продукт 25: 3,4-біс(Бензилоксі)-6-(1-фенілетеніл)піридазин Суміш 3,4-біс(Бензилоксі)-6-хлоропіридазину (Проміжний продукт 1: 3 г, 9,18 ммоль), диоксану (32,1 мл) та води (9,64 мл) дегазують та додають до неї моно(біс(ди-трет-бутил(4(диметиламіно)феніл)фосфоніо)паладій(IV)) дихлорид (0,195 г, 0,275 ммоль), цезію карбонат (10,14 г, 31,1 ммоль) та 4,4,5,5-тетраметил-2-(1-фенілетеніл)-1,3,2-диоксоборолан (3 г, 13,04 ммоль). Суміш нагрівають до температури 80°C протягом 6 годин та після охолодження розділяють між дихлорметаном та водою. Органічну частину висушують (MgSO4), фільтрують та концентрують для одержання олії оранжевого кольору. Неочищену олію очищують за допомогою кварцової хроматографії з елююванням за допомогою 0-60 % етилацетату у бензині для одержання 3,4-біс(Бензилоксі)-6-(1-фенілетеніл)піридазину у вигляді олії коричневого кольору (вихід = 91 %). 1 H ЯМР (400 МГц, CHCl3-d) 7,54-7,66 (m, 2 H), 7,24-7,44 (m, 13 H), 6,72 (s, 1H), 6,02 (s, 1H), 5,70 (s, 2H), 5,63 (s, 1H), 5,11 (s, 2H). + MS ES : 395. Проміжний продукт 26: 3,4-біс(Бензилоксі)-6-(1-фенілциклопропіл)піридазин До суспензії натрію гідриду (0,487 г, 12,17 ммоль, 60% у мінеральній олії) у ДМСО (33,8 мл) при помішуванні під нітрогеном додають триметил сульфоксоніум йодид (2,68 г, 12,17 ммоль) 4 порціями протягом 20 хвилин. Додають розчин 3,4-біс(Бензилоксі)-6-(1-фенілетеніл)піридазину (Проміжний продукт 25; 3,2 г, 8,11 ммоль) у тетрагідрофурані (50,7 мл) через крапельну воронку протягом 90 хвилин, після чого реакційну суміш залишають стояти, перемішуючи, при кімнатній температурі протягом 18 годин. Одержану суміш концентрують, виливають у крижану воду та екстрагують з етилацетатом (x3). Органічну частину висушують (MgSO 4), фільтрують та концентрують для одержання олії коричневого кольору. Неочищену олію очищують за допомогою кварцової хроматографії (елюювання із застосуванням 0-50 % етилацетату у бензині) для одержання 3,4-біс(Бензилоксі)-6-(1-фенілциклопропіл)піридазину у вигляді олії жовтого кольору (вихід = 23 %). 1 H ЯМР (400 МГц, CHCl3-d) 7,47-7,63 (m, 2 H), 7,22-7,46 (m, 11 H), 7,10-7,25 (m, 2 H), 6,40 (s, 1 H), 5,62 (s, 2 H), 4,97 (s, 2 H), 1,71-1,85 (m, 2 H), 1,25-1,38 (m, 2 H). + MS ES : 409. Схема 5a: 26 UA 111851 C2 'Hal' позначає галоген Проміжний продукт 27: 4-{2-[5,6-біс(Бензилоксі) піридазин-3-іл]етиніл}бензонітрил 5 10 15 20 25 30 Готують, як описано для 3,4-біс(Бензилоксі)-6-{[5-(трифторметил)піридин-2іл]етиніл}піридазину (Проміжний продукт 6), з 3,4-біс(Бензилоксі)-6-етинілпіридазином (Проміжний продукт 5) та 4-йодобензонітрилом на виході 73 %. 1 H ЯМР (400 МГц, CD2Cl2) 7,67-7,81 (m, 4 H), 7,32-7,65 (m, 10 H), 7,08 (s, 1 H), 5,68 (s, 2 H) та 5,23 (s, 2 H). + MS ES : 418. Проміжний продукт 28: 3,4-біс(Бензилоксі)-6-[2-(3-фтор-4-метилфеніл)етиніл]піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-{[5-(трифторметил)піридин-2іл]етиніл}піридазину (Проміжний продукт 6), з 3,4-біс(Бензилоксі)-6-етинілпіридазином (Проміжний продукт 5) та 2-фтор-4-йодо-1-метилбензолом на виході 67 %. Проміжний продукт 29: 3,4-біс(Бензилоксі)-6-[2-(4-фтор-3-метилфеніл)етиніл]піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-{[5-(трифторметил)піридин-2іл]етиніл}піридазину (Проміжний продукт 6), з 3,4-біс(Бензилоксі)-6-етинілпіридазином (Проміжний продукт 5) та 1-фтор-4-йодо-2-метилбензолом на виході 67 %. 1 H ЯМР (400 МГц, CD2Cl2) 7,29-7,58 (m, 12 H), 6,99-7,08 (m, 2 H), 5,62 (s, 2 H), 5,17 (s, 2 H) та 2,29 (s, 3 H). + MS ES : 425. Проміжний продукт 30: 3,4-біс(Бензилоксі)-6-[2-(3,4-диметоксифеніл)етиніл]піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-{[5-(трифторметил)піридин-2іл]етиніл}піридазину (Проміжний продукт 6), з 3,4-біс(Бензилоксі)-6-етинілпіридазином (Проміжний продукт 5) та 4-йодо-1,2-диметоксибензолом на виході 17 %. 1 H ЯМР (400 МГц, CDCl3) 7,52-7,61 (m, 2 H), 7,33-7,47 (m, 8 H), 7,18-7,26 (m, 1 H), 7,09-7,15 (m, 1 H), 6,97 (s, 1 H), 6,87 (m, 1 H),5,69 (s, 2 H), 5,22 (s, 2 H) та 3,89-3,96 (m, 6 H). + MS ES : 453. Проміжний продукт 31: 3,4-біс(Бензилоксі)-6-{2-[5-(трифторметил)піридин-3іл]етиніл}піридазин 27 UA 111851 C2 5 10 15 20 25 Готують, як описано для 3,4-біс(Бензилоксі)-6-{[5-(трифторметил)піридин-2іл]етиніл}піридазину (Проміжний продукт 6), з 3,4-біс(Бензилоксі)-6-етинілпіридазином (Проміжний продукт 5) та 3-бромо-5-(трифторметил)піридином на виході 31%. + MS ES : 462. Проміжний продукт 32: 3,4-біс(Бензилоксі)-6-[2-(2-хлоро-6-фторфеніл)етиніл]піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-{[5-(трифторметил)піридин-2іл]етиніл}піридазину (Проміжний продукт 6), з 3,4-біс(Бензилоксі)-6-етинілпіридазином (Проміжний продукт 5) та 1-хлоро-3-фтор-2-йодобензолом. + MS ES : 445. Проміжний продукт 33: 3,4-біс(Бензилоксі)-6-[2-(2,6-ди фторфеніл)етиніл]піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-{[5-(трифторметил)піридин-2іл]етиніл}піридазину (Проміжний продукт 6), з 3,4-біс(Бензилоксі)-6-етинілпіридазином (Проміжний продукт 5) та 2-бромо-1,3-дифторбензолом. + MS ES : 429. Проміжний продукт 34: 3,4-біс(Бензилоксі)-6-[2-(4-хлорофеніл)етиніл]піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-{[5-(трифторметил)піридин-2іл]етиніл}піридазину (Проміжний продукт 6), з 3,4-біс(Бензилоксі)-6-етинілпіридазином (Проміжний продукт 5) та 1-хлоро-4-йодобензолом на виході 70%. 1 H ЯМР (400 МГц, ДМСО-d6) 7,22-7,75 (m, 15 H), 5,45-5,68 (m, 2 H) та 5,30 (s, 2 H). + MS ES : 427. Проміжний продукт 35: 3,4-біс(Бензилоксі)-6-[2-(2-хлорофеніл)етиніл]піридазин Готують, як описано для 3,4-біс(Бензилоксі)-6-{[5-(трифторметил)піридин-2іл]етиніл}піридазину (Проміжний продукт 6), з 3,4-біс(Бензилоксі)-6-етинілпіридазином (Проміжний продукт 5) та 1-хлоро-2-йодобензолом на виході 59%. 28
ДивитисяДодаткова інформація
Назва патенту англійськоюPyridazinone compounds and their use as daao inhibitors
Автори англійськоюFarnaby, William, Fieldhouse, Charlotte, Hazel, Katherine, Kerr, Catrina, Kinsella, Natasha, Livermore, David, Merchant, Kevin, Miller, David
Автори російськоюФарнаби Вильям, Филдхаус Шарлот, Хэзел Кэтрин, Кер Катрина, Кинсела Наташа, Ливермор Дэвид, Мерчант Кевин, Милер Дэвид
МПК / Мітки
МПК: A61K 31/50, A61P 29/00, C07D 407/10, A61P 25/28, A61P 25/18, A61K 31/501, C07D 401/10, C07D 237/16
Мітки: сполуки, інгібіторів, піридазинону, використання
Код посилання
<a href="https://ua.patents.su/69-111851-spoluki-piridazinonu-ta-kh-vikoristannya-yak-ingibitoriv-daao.html" target="_blank" rel="follow" title="База патентів України">Сполуки піридазинону та їх використання як інгібіторів daao</a>
Попередній патент: Кристалічні частинки, покриті міцелами
Наступний патент: Системи і способи для бездротових сигналів-маяків з невеликою кількістю службової інформації, які мають стиснені мережеві ідентифікатори
Випадковий патент: Багатогранна різальна пластина