Спосіб і проміжні сполуки для одержання ненуклеозидних інгібіторів ревертази вірусу віл-1
Номер патенту: 80141
Опубліковано: 27.08.2007
Автори: Ерікссон Магнус С., Кім Джі-Юонг, Басакка Карл А.
Формула / Реферат
1. Спосіб одержання сполуки формули І
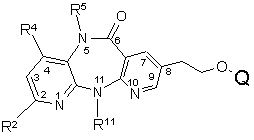 , (I)
, (I)
у якій R2 вибраний із групи, яка включає Н, F, Сl, С1-С4алкіл, С3-С4циклоалкіл і СF3,
R4 означає Н або Me,
R5 означає Н, Me або Et, за умови, що обидва R4 і R5 одночасно не означають Me і, якщо R4 означає Me, то R5 не може означати Et,
R11 означає Me, Et, циклопропіл, пропіл, ізопропіл або циклобутил, і
Q вибраний із групи, яка включає
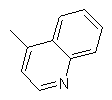 ,
, 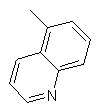 ,
, 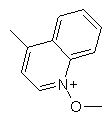 і
і 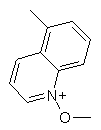 ,
,
який полягає в тому, що
(а) вихідну сполуку формули II
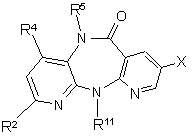 , (ІІ)
, (ІІ)
у якій R2, R4, R5 і R11 мають вказані вище для сполуки формули І значення, а Х означає хлор, йод або бром, або фторсульфонатний залишок, вибраний із групи, яка включає -OSO2F і -OSO2(СF2)nСF3, де n являє собою ціле число в інтервалі від 0 і 10,
піддають в органічному розчиннику в присутності паладієвого каталізатора, прийнятного ліганду і сильної основи взаємодії з малонатом або його "замінником" формули III
![]() , (III)
, (III)
у якій
R12 означає ціаногрупу або групу формули -COOR14, де R14 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил, та
R13 означає ціаногрупу, групу формули -COOR15 (де R15 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил), групу формули -SO2R16 (де R16 являє собою С1-С4алкільну групу, феніл, фурил, піридил або бензил), групу формули -P(O)(OR17)2 (де R17 являє собою феніл, фурил або піридил) або групу формули -SOR18 (де R18 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил),
з одержанням проміжної сполуки формули IV
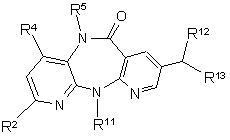 , (IV)
, (IV)
у якій R2, R4, R5, R11, R12 і R13 мають вказані вище в цьому пункті значення,
(б) при наявності в проміжній сполуці формули IV сірко- або фосфорвмісної групи її відщеплюють під дією відновника,
(в) проміжну сполуку формули IV піддають гідролізу з одержанням наступної проміжної сполуки формули V
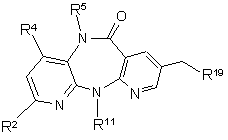 , (V)
, (V)
у якій R2, R4, R5 і R11 мають вказані вище в цьому пункті значення, a R19 означає -СООН або при використанні як реагенту формули III малонату і м'яких умов гідролізу R19 додатково може означати групу формули -COOR14, де R14 має вказані вище в цьому пункті значення,
(г) проміжну карбонову кислоту або її проміжний ефір формули V відновлюють до спирту формули VI
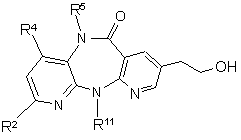 , (VI)
, (VI)
у якій R2, R4, R5 і R11 мають вказані вище в цьому пункті значення, і
(д) спирт формули VI піддають конденсації з реагентом формули
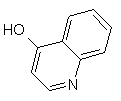 ,
, 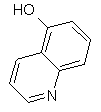 ,
, 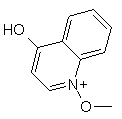 або
або 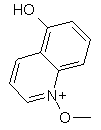 ,
,
з одержанням кінцевого продукту формули І.
2. Спосіб одержання сполуки формули IV
 , (IV)
, (IV)
у якій
R2 вибраний із групи, яка включає Н, F, Сl, С1-С4алкіл, С3-С4циклоалкіл і СF3,
R4 означає Н або Me,
R5 означає Н, Me або Et, за умови, що обидва R4 і R5 одночасно не означають Me і, якщо R4 означає Me, то R5 не може означати Et,
R11 означає Me, Et, циклопропіл, пропіл, ізопропіл або циклобутил,
R12 означає ціаногрупу або групу формули -COOR14, де R14 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил, і
R13 означає ціаногрупу, групу формули -COOR15 (де R15 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил), групу формули -SO2R16 (де R16 являє собою С1-С4алкільну групу, феніл, фурил, піридил або бензил), групу формули -P(O)(OR17)2 (де R17 являє собою феніл, фурил або піридил) або групу формули -SOR18 (де R18 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил),
який полягає в тому, що
(а) вихідну сполуку формули II
 , (II)
, (II)
у якій R2, R4, R5 і R11 мають вказані вище в цьому пункті значення, а Х означає хлор, йод, або бром, або фторсульфонатний залишок, вибраний із групи, яка включає -OSO2F і -OSO2(CF2)nCF3, де n являє собою ціле число в інтервалі від 0 і 10, піддають в органічному розчиннику в присутності паладієвого каталізатора, прийнятного ліганду і сильної основи взаємодії з малонатом або його "замінником" формули III
![]() , (III)
, (III)
у якій
R12 означає ціаногрупу або групу формули -COOR14, де R14 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил, та
R13 означає ціаногрупу, групу формули -COOR15 (де R15 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил), групу формули -SO2R16 (де R16 являє собою С1-С4алкільну групу, феніл, фурил, піридил або бензил), групу формули -P(O)(OR17)2 (де R17 являє собою феніл, фурил або піридил) або групу формули -SOR18 (де R18 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил),
з одержанням сполуки формули IV.
3. Спосіб одержання сполуки формули V
 , (V)
, (V)
у якій R2 вибраний із групи, яка включає Н, F, Сl, С1-С4алкіл, С3-С4циклоалкіл і СF3,
R4 означає Н або Me,
R5 означає Н, Me або Et, за умови, що обидва R4 і R5 одночасно не означають Me і, якщо R4 означає Me, то R5 не може означати Et,
R11 означає Me, Et, циклопропіл, пропіл, ізопропіл або циклобутил, і
R19 означає -СООН або групу формули -COOR14, де R14 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил,
який полягає в тому, що
(а) вихідну сполуку формули II
 , (ІІ)
, (ІІ)
у якій R2, R4, R5 і R11 мають вказані вище в цьому пункті значення, а Х означає хлор, йод або бром або фторсульфонатний залишок, вибраний із групи, яка включає -OSO2F і -OSO2(СF2)nСF3, де n являє собою ціле число в інтервалі від 0 і 10, піддають в органічному розчиннику в присутності паладієвого каталізатора, прийнятного ліганду і сильної основи взаємодії з малонатом або його "замінником" формули III
![]() , (III)
, (III)
у якій
R12 означає ціаногрупу або групу формули -COOR14, де R14 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил, та
R13 означає ціаногрупу, групу формули -COOR15 (де R15 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил), групу формули -SO2R16 (де R16 являє собою С1-С4алкільну групу, феніл, фурил, піридил або бензил), групу формули -P(O)(OR17)2 (де R17 являє собою феніл, фурил або піридил) або групу формули -SOR18 (де R18 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил),
з одержанням проміжної сполуки формули IV
 , (IV)
, (IV)
у якій R2, R4, R5, R11, R12 і R13 мають вказані вище в цьому пункті значення,
(б) при наявності в проміжній сполуці формули IV сірко- або фосфорвмісної групи (коли R13 у сполуці формули III являє собою групу формули -SO2R16 або Р(O)(OR17)2) її відщеплюють під дією відновника, і
(в) проміжну сполуку формули IV піддають гідролізу з одержанням сполуки формули V.
4. Спосіб за п. 3, у якому як реагент формули III використовують малонат, а як ліганд використовують трет-Вu3Р або фероценілфосфін.
5. Спосіб за п. 3, у якому як реагент формули III використовують "замінник" малонату, а як ліганд використовують трет-Вu3Р, фероценілфосфін або триарилфосфін.
6. Спосіб за п. 5, у якому як ліганд використовують РРh3, о-Тol3Р, n-Tol3Р або о-Fur3Р.
7. Сполука формули IV
 , (IV)
, (IV)
у якій
R2 вибраний із групи, яка включає Н, F, Сl, С1-С4алкіл, С3-С4циклоалкіл і СF3,
R4 означає Н або Me,
R5 означає Н, Me або Et, за умови, що обидва R4 і R5 одночасно не означають Me і, якщо R4 означає Me, то R5 не може означати Et,
R11 означає Me, Et, циклопропіл, пропіл, ізопропіл або циклобутил,
R12 означає ціаногрупу або групу формули -COOR14, де R14 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил, і
R13 означає ціаногрупу, групу формули -COOR15 (де R15 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил), групу формули -SO2R16 (де R16 являє собою С1-С4алкільну групу, феніл, фурил, піридил або бензил), групу формули -P(O)(OR17)2 (де R17 являє собою феніл, фурил або піридил) або групу формули -SOR18 (де R18 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил).
8. Сполука формули V
, (V)
у якій R2 вибраний із групи, яка включає Н, F, Сl, С1-С4алкіл, С3-С4циклоалкіл і СF3,
R4 означає Н або Me,
R5 означає Н, Me або Et, за умови, що обидва R4 і R5 одночасно не означають Me і, якщо R4 означає Me, то R5 не може означати Et,
R11 означає Me, Et, циклопропіл, пропіл, ізопропіл або циклобутил, і
R19 означає -СООН або групу формули -COOR14, де R14 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил.
Текст
1. Спосіб одержання сполуки формули І R5 O 4 R N 6 3 R5 R4 80141 O R12 N N N R13 N R11 R2 , (IV) у якій R , R , R5, R 11, R12 і R13 мають вказані вище в цьому пункті значення, (б) при наявності в проміжній сполуці формули IV сірко- або фосфорвмісної групи її відщеплюють під дією відновника, (в) проміжну сполуку формули IV піддають гідролізу з одержанням наступної проміжної сполуки формули V 2 4 R5 R4 O N R19 N N R11 означає Me, Et, циклопропіл, пропіл, ізопропіл або циклобутил, R12 означає ціаногрупу або груп у формули COOR14, де R14 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С 1-С4алкільну груп у, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил, і R13 означає ціаногрупу, груп у формули -COOR15 (де R15 являє собою С 1-С4алкільну гр упу, С1С4алкілоксі-С 1-С4алкільну гр упу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил), груп у формули -SO2R16 (де R16 являє собою С 1С4алкільну групу, феніл, фурил, піридил або бензил), групу формули -P(O)(OR17) 2 (де R17 являє собою феніл, фурил або піридил) або групу формули -SOR18 (де R18 являє собою С 1-С4алкільну груп у, С1-С4алкілоксі-С 1-С4алкільну груп у, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил), який полягає в тому, що (а) вихідну сполуку формули II N R5 R4 R11 R2 , (V) у якій R2, R4, R5 і R11 мають вказані вище в цьому пункті значення, a R19 означає -СООН або при використанні як реагенту формули III малонату і м'яких умов гідролізу R19 додатково може означати груп у формули -COOR 14, де R14 має вказані вище в цьому пункті значення, (г) проміжну карбонову кислоту або її проміжний ефір формули V відновлюють до спирту формули VI R5 R4 O N OH N N N R1 1 R2 , (VI) у якій R2, R4, R5 і R11 мають вказані вище в цьому пункті значення, і (д) спирт формули VI піддають конденсації з реагентом формули HO HO HO HO N+ N N N+ O O , , або з одержанням кінцевого продукту формули І. 2. Спосіб одержання сполуки формули IV R5 R4 , O R12 N N R2 4 N R 11 N R 13 , (IV) у якій R2 вибраний із групи, яка включає Н, F, Сl, С1С4алкіл, С3-С4циклоалкіл і СF3, R4 означає Н або Me, R5 означає Н, Me або Et, за умови, що обидва R 4 і R5 одночасно не означають Me і, якщо R 4 означає Me, то R5 не може означати Et, O N X N N N R 11 R2 , (II) у якій R , R4, R5 і R11 мають вказані вище в цьому пункті значення, а Х означає хлор, йод, або бром, або фторсульфонатний залишок, вибраний із групи, яка включає -OSO2F і -OSO2(CF 2)nCF 3, де n являє собою ціле число в інтервалі від 0 і 10, піддають в органічному розчиннику в присутності паладієвого каталізатора, прийнятного ліганду і сильної основи взаємодії з малонатом або його "замінником" формули III R 12 R 13 , (III) у якій R12 означає ціаногрупу або груп у формули COOR14, де R14 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С 1-С4алкільну груп у, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил, та R13 означає ціаногрупу, груп у формули -COOR15 (де R15 являє собою С 1-С4алкільну гр упу, С1С4алкілоксі-С 1-С4алкільну гр упу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил), груп у формули -SO2R16 (де R16 являє собою С 1С4алкільну групу, феніл, фурил, піридил або бензил), групу формули -P(O)(OR17) 2 (де R17 являє собою феніл, фурил або піридил) або групу формули -SOR18 (де R18 являє собою С 1-С4алкільну груп у, С1-С4алкілоксі-С 1-С4алкільну груп у, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил), з одержанням сполуки формули IV. 3. Спосіб одержання сполуки формули V 2 R5 R4 O N R19 N R2 N R11 N , (V) 5 80141 у якій R2 вибраний із групи, яка включає Н, F, Сl, С1-С4алкіл, С3-С4циклоалкіл і СF3, R4 означає Н або Me, R5 означає Н, Me або Et, за умови, що обидва R 4 і R5 одночасно не означають Me і, якщо R 4 означає Me, то R5 не може означати Et, R11 означає Me, Et, циклопропіл, пропіл, ізопропіл або циклобутил, і R19 означає -СООН або групу формули -COOR 14, де R14 являє собою С1-С4алкільну груп у, С1С4алкілоксі-С 1-С4алкільну гр упу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил, який полягає в тому, що (а) вихідну сполуку формули II R5 O 4 R N X N N R4 N R13 N , (IV) у якій R , R , R5, R 11, R12 і R13 мають вказані вище в цьому пункті значення, (б) при наявності в проміжній сполуці формули IV сірко- або фосфорвмісної групи (коли R13 у сполуці формули III являє собою групу формули -SO2R16 2 4 R13 R11 R2 , (IV) у якій R2 вибраний із групи, яка включає Н, F, Сl, С1С4алкіл, С3-С4циклоалкіл і СF3, R4 означає Н або Me, R5 означає Н, Me або Et, за умови, що обидва R 4 і R5 одночасно не означають Me і, якщо R 4 означає Me, то R5 не може означати Et, R11 означає Me, Et, циклопропіл, пропіл, ізопропіл або циклобутил, R12 означає ціаногрупу або груп у формули COOR14, де R14 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С 1-С4алкільну груп у, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил, і R13 означає ціаногрупу, груп у формули -COOR15 (де R15 являє собою С 1-С4алкільну гр упу, С1С4алкілоксі-С 1-С4алкільну гр упу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил), груп у формули -SO2R16 (де R16 являє собою С 1С4алкільну групу, феніл, фурил, піридил або бензил), групу формули -P(O)(OR17) 2 (де R17 являє собою феніл, фурил або піридил) або групу формули -SOR18 (де R18 являє собою С 1-С4алкільну груп у, С1-С4алкілоксі-С 1-С4алкільну груп у, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил). 8. Сполука формули V R5 R4 R 12 R 11 R2 N O N O N N N N , (ІІ) у якій R2, R4, R5 і R11 мають вказані вище в цьому пункті значення, а Х означає хлор, йод або бром або фторсульфонатний залишок, вибраний із групи, яка включає -OSO2F і -OSO2(СF 2)nСF 3, де n являє собою ціле число в інтервалі від 0 і 10, піддають в органічному розчиннику в присутності паладієвого каталізатора, прийнятного ліганду і сильної основи взаємодії з малонатом або його "замінником" формули III R 12 R 13 , (III) у якій R12 означає ціаногрупу або груп у формули COOR14, де R14 являє собою С1-С4алкільну групу, С1-С4алкілоксі-С 1-С4алкільну груп у, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил, та R13 означає ціаногрупу, груп у формули -COOR15 (де R15 являє собою С1-С4алкільну гр упу, С1С4алкілоксі-С 1-С4алкільну гр упу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил), груп у формули -SO2R16 (де R16 являє собою С1С4алкільну групу, феніл, фурил, піридил або бензил), групу формули -P(O)(OR17) 2 (де R17 являє собою феніл, фурил або піридил) або групу формули -SOR18 (де R18 являє собою С 1-С4алкільну груп у, С1-С4алкілоксі-С 1-С4алкільну груп у, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил), з одержанням проміжної сполуки формули IV R5 або Р(O)(OR17)2) її відщеплюють під дією відновника, і (в) проміжну сполуку формули IV піддають гідролізу з одержанням сполуки формули V. 4. Спосіб за п. 3, у якому як реагент формули III використовують малонат, а як ліганд використовують трет-Вu3Р або фероценілфосфін. 5. Спосіб за п. 3, у якому як реагент формули III використовують "замінник" малонату, а як ліганд використовують трет-Вu3Р, фероценілфосфін або триарилфосфін. 6. Спосіб за п. 5, у якому як ліганд використовують РРh3, о-Тol3Р, n-Tol3Р або о-Fur3Р. 7. Сполука формули IV R5 O 4 R R12 N N R11 R2 6 N R2 N R11 R1 9 N , (V) у якій R2 вибраний із групи, яка включає Н, F, Сl, С1-С4алкіл, С3-С4циклоалкіл і СF3, R4 означає Н або Me, R5 означає Н, Me або Et, за умови, що обидва R 4 і R5 одночасно не означають Me і, якщо R 4 означає Me, то R5 не може означати Et, R11 означає Me, Et, циклопропіл, пропіл, ізопропіл або циклобутил, і 7 80141 8 R19 означає -СООН або групу формули -COOR 14, де R14 являє собою С1-С4алкільну груп у, С1 С4алкілоксі-С 1-С4алкільну гр упу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил. Даний винахід стосується нового способу одержання деяких ненуклеозидних інгібіторів ревертази і нових проміжних сполук для їх синтезу. Захворювання, відоме як синдром набутого імунодефіциту (СНІД), викликається вірусом імунодефіциту людини (ВІЛ), зокрема штамом, відомим як ВІЛ-1. Необхідною умовою реплікації ВІЛ клітиною-хазяїном є вбудовування інформації, яка міститься у вірусному геномі, у ДНК клітинухазяїна. Однак ВІЛ є ретровірусом, і тому його генетична інформація представлена у вигляді РНК. З цієї причини в циклі реплікації ВІЛ потрібна стадія транскрипції вірусного геному (РНК) у ДНК. Транскрипція вірусної РНК у ДНК каталізується ферментом, який відповідно одержав назву "зворотна транскриптаза" ("ревертаза"). Віріон ВІЛ разом з вірусною РНК містить також копію ревертази. Ревертаза виконує три відомі ферментативні функції. Так, зокрема, ревертаза виконує функцію РНК-залежної ДНК-полімерази, рибонуклеази і ДНК-залежної ДНК-полімерази. Виконуючи функцію РНК-залежної ДНК-полімерази, ревертаза забезпечує транскрипцію вірусної РНК з одержанням її копії у вигляді однониткової ДНК. Виконуючи функцію рибонуклеази, ревертаза каталізує розщеплення вихідної вірусної РНК і забезпечує відділення ДНК відразу ж після її синтезу від вихідної РНК. І, нарешті, виконуючи функцію ДНК-залежної ДНК-полімерази, ревертаза каталізує утворення другої, комплементарної нитки ДНК із використанням як матриці першої нитки ДНК. Обидві ці нитки або ланцюги утворюють двониткову ДНК, яка вбудовується в геном клітини-хазяїна за допомогою іншого ферменту, який називається інтегразою. Сполуки, які інгібують ферментативні функції ревертази ВІЛ-1, пригнічують реплікацію ВІЛ-1 в інфікованих ними клітинах. Подібні сполуки можуть використовува тися для профілактики або лікування викликаної ВІЛ-1 інфекції в людини, про що свідчать дані досліджень відомих інгібіторів ревертази, як приклад яких можна назвати 3'-азидо-3'дезокситимідин (AZT), 2',3'-дидезоксіінозин (ddl), 2',3'-дидезоксицитидин (ddC), d4T, 3TC, невірапін, делавірдин, ефавіренц і абакавір і які тим самим добре зарекомендували себе як придатні для лікування ВІЛ-інфекції лікарських речовин. При застосуванні інгібіторів ревертази при лікуванні ВІЛ-інфекції вірус, як і при будь-якій противірусній терапії, в остаточному підсумку стає менш чутливим до відповідної лікарської речовини. Така резистентність (знижена чутливість) до подібних лікарських речовин є результатом мутацій, які відбуваються в ревертазній одиниці гена роl. Дотепер охарактеризовано декілька подібних мутантних штамів ВІЛ, резистентність яких до відомих терапевтичних засобів обумовлена мутаціями в гені, який кодує ревертазу. До переліку деяких мутан тів, які найбільш часто зустрічаються в клінічній практиці, належать мутант Y181C, у якого тирозин Y у положенні ко дону 181 замінений у результаті мутації на залишок цистеіну С, і мутант K103N, у якого лізин К у положенні 103 замінений на аспаргін N. До інших мутантів, які з'являються зі зростаючою частотою при лікуванні відомими противірусними засобами, належать мутанти з одиничними замінами V106A, G190A, Y188C і P236L і мутанти з подвійними замінами K103N/Y181C, K013N/P225H, K103N/V108I і K103N/L100I. Очікується, що при триваючому застосуванні противірусних засобів для терапії ВІЛ-інфекції кількість резистентних штамів, які знову з'являються, буде зростати. З цієї причини зберігається необхідність у нових інгібіторах ревертази, які мають інші механізми дії, спрямовані проти різних мутантних штамів ВІЛ. Особливе значення в контексті даного винаходу мають інгібітори ревертази ВІЛ, описані в [патенті US 6420359]. Усі ці сполуки, які належать до сімейства дипіридо[3,2-b:2',3'-е] [1,4]діазепін-6онів, які несуть 2-(хінолініл)оксіетильну або 2-(1оксидохінолініл)оксіетильну групу в положенні 8, мають більш високу активність у відношенні деяких клінічно важливих мутантних штамів ВІЛ-1. Відповідно до цього в основу даного винаходу була покладена задача розробити альтернативний спосіб одержання сполук, описаних у [патенті US 6420359]. У даному винаході пропонується удосконалений спосіб одержання сполук загальної формули І у якій R2 вибраний із групи, яка включає Н, F, СІ, С1С4алкіл, С3-С4циклоалкіл і CF3, R4 означає Н або Me, R5 означає Н, Me або Et, за умови, що обидва 4 R і R5 одночасно не означають Me і, якщо R4 означає Me, то R5 не може означати Et, R11 означає Me, Et, циклопропіл, пропіл, ізопропіл або циклобутил і Q вибраний із групи, яка включає а також їх фармацевтично прийнятних солей. 9 80141 При здійсненні запропонованого у винаході способу синтезу як вихідну використовують сполуку формули II у якій R2, R4, R5 і R11 мають вказані вище для сполуки формули І значення, а X означає хлор, йод або бром або фторсульфонатний залишок, вибраний із групи, яка включає -OSO2F і OSO2(CF 2)nCF3 , де n являє собою ціле число в інтервалі від 0 і 10. Методи одержання вихідних сполук формули II, у якій X означає бром, описані в [US 6420359]. Сполуки, у яких X має відмінні від брому значення, можна одержувати аналогічними методами, очевидними для фахівців у даній галузі. Відповідно до винаходу переважно використовувати сполуку формули II, у якій X означає бром. Вихідну сполук у формули II спочатку піддають реакції сполучення, яка каталізується паладієм, шляхом арилування малонату або його "замінника" формули III у якій R12 означає ціаногрупу або гр уп у формули COOR14, де R14 являє собою С1-С4алкільну групу, С1-С4алкілокси-С 1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил, а R13 означає ціаногрупу, гр упу формули COOR15 (де R15 являє собою С1-С4алкільну групу, С1-С4алкілокси-С 1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил), групу формули -SO2R16 (де R16 являє собою С1-С4алкільну груп у, феніл, фурил, піридил або бензил), групу формули -P(O)(OR17) 2 (де R17 являє собою феніл, фурил або піридил) або групу формули -SOR18 (де R18 являє собою С 1-С4алкільну груп у, С1-С4алкілокси- С1-С4алкільну груп у, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил). При здійсненні запропонованого у винаході способу переважно використовувати "замінник" малонату формули III у якій R12 означає ціаногрупу або гр уп у формули COOR14, де R14 являє собою С1-С4алкільну групу, С1-С4алкілокси- С1-С4алкільну груп у, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил, а R13 означає ціаногрупу, гр упу формули SO2R16 (де R16 являє собою С1-С4алкільну групу, феніл, фурил, піридил або бензил), груп у формули -P(O)(OR17)2 (де R17 являє собою феніл, фурил або піридил) або групу формули -SOR18 (де R18 являє собою С 1-С4алкільну гр упу, С1-С4алкілокси 10 С1-С4алкільну групу, феніл, нафтил, тіофеніл, фурил, піридил, імідазол або бензил). Реакцію між сполуками формул II і III проводять в органічному розчиннику, у присутності паладієвого каталізатора, прийнятного ліганду і сильної основи. Як приклад придатних для застосування в цих цілях розчинників можна назвати, але не обмежуючи тільки ними, толуол, етилбензол, ксилол, диметилформамід (ДМФ), N,N-диметилацетамід (ДМА), N-метилпіролідон (NМП), діоксан і тетрагідрофуран (ТГФ), серед яких переважний толуол. Як паладієвий каталізатор фактично можна використовувати будь-який паладієвий каталізатор, такий, наприклад, як Pd(OAc)2, PdCl2, Pd2dba3 і Pd на вугіллі, серед яких переважний Pd(OAc)2 . Як приклад придатних для застосування в вказаних вище цілях основ можна назвати гідриди металів, такі, наприклад, як NaH, алкоксиди металів, такі, наприклад, як mpem-ВиОК, mpemBuONa і Na-mpem-амілат, карбонати металів, такі, наприклад, як Na2CO3, К2СО3 і Cs 2CO3, серед яких переважний NaH, і фосфати металів, такі, наприклад, як К3РО4. Якщо реагентом формули III служить малонат (сполуки, у яких R12 і R13 обидва означають карбоксилатні групи), то як відповідні ліганди можуть використовуватися mpem-Bu3P, один з лігандів, описаних у [патенті US 6307087], або фероценілфосфін, такий як описаний у [US 6057456] і [US 6072073]. Якщо ж реагент формули III не є малонатом, а являє собою його "замінник" (сполуку, у якій R12 і R13 обидва не означають карбоксилатні групи), то в цьому випадку крім згаданих ви ще лігандів додатково можна також використовувати триарилфосфін, як такі приклади, які не обмежують, можна назвати PPh3, o-T0I3P, n-Т0І3Р і o-Fur3P. Серед таких лігандів переважний PPh3. Реакцію переважно проводити при підвищеній температурі, більш переважно при температурі в інтервалі від приблизно 50 до 150°С. У результаті описаної вище реакції сполучення сполук формул II і III одержують проміжну сполуку формули IV у якій R2, R4, R5, R 11, R12 і R13 мають вказані вище значення. Виділення проміжної сполуки формули IV перед її використанням на наступній стадії процесу в принципі є не обов'язковою стадією. Відповідно до винаходу було встановлено, що цілком прийнятно проводити реакцію за методом синтезу в одній реакційній посудині без виділення проміжної сполуки формули IV. Якщо проміжну сполуку формули IV не виділяють, а як сильну основу використовують гідрид металу, такий як NaH, деяка кількість якого залишається невитраченим у реакційній суміші, то подібну основу перед переходом до наступного стадії доцільно швидко "гасити" додаванням такого агента, як ізопропіловий спирт. 11 80141 Якщо проміжна сполука формули IV містить сірку або фосфор (коли в реагенті формули III, що використовувався, R13 являє собою груп у формули -SO2R15 -або P(O)(OR16)2), то на наступній стадії процесу сірко- або фосфорвмісну гр упу відщеплюють під дією відновника. Методи такого відновного відщеплення відомі фахівцям у даній галузі. Так, наприклад, відщеплювати сірко- або фосфорвмісну групу можна за рахунок використання нікелю Ренея або за рахунок реакції з розчинними сполуками металів. Потім проміжну сполуку формули IV або після попереднього відновного відщеплення сірко- або фосфорвмісної групи, або безпосередньо, якщо ця проміжна сполука формули IV не містить сірки або фосфор у, піддають гідролізу з одержанням наступної проміжної сполуки формули V у якій R2, R4, R5 і R11 мають вказані вище значення, a R19 означає -СООН або при використанні як реагенту формули III малонату і м'яких умов гідролізу R19 додатково може означати групу формули -COOR 14, де R14 має вказані вище 5 значення. Гідроліз можна проводити відповідно до традиційної методики, добре відомої фахівцям у даній галузі. Так, наприклад, гідроліз можна проводити з використанням водної основи, такої як NaOH, переважно при кімнатній або більш високій температурі. Проміжні сполуки формул IV і V є новими і відповідно до цього 10 становлять ще один об'єкт даного винаходу. Перед проведенням наступної стадії спочатку переважно виділяти проміжну сполуку формули V. Після цього проміжну карбонову кислоту або її проміжний ефір формули V відновлюють до спирту формули VI у якій R2, R4, R5 і R11 мають вказані вище значення. Подібне відновлення проводять традиційним методом, добре відомим фахівцям у даній галузі. Незалежно від того, чи є проміжна сполука формули V кислотою або її ефіром, відновлення можна проводити з використанням боранів, боргідридів або ) інших гідридів металів або розчинних сполук металів як відновників, при цьому у випадку кислот переважно використовувати борани, а у випадку ефірів переважно використовувати боргідриди. При використанні борану його переважно одержувати in situ з боргідриду, такого як боргідрид натрію, і електрофільного реагенту, такого, наприклад, як НСl. 12 На завершальній стадії спирт формули VI перетворюють у кінцевий продукт формули І шляхом конденсації з реагентом формули Подібну конденсацію можна проводити за методом, описаним в [US 6420359]. Нижче винахід більш докладно розглянутий на прикладах. Приклад 1: Арилування малононітрилу з одержанням сполуки формули IV, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, a R12 і R13 означають CN У колбу завантажували 10,0г трициклічного броміду (сполуки формули II, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, а X означає Вr; 30ммолів, 1екв.), 0,95г трифенілфосфіну (3,6ммоля, 0,12екв.), 0,55г Pd2dba3 (0,6ммоля, 0,04екв.) і 40мл 1,4-діоксану. До цієї суміші потім протягом 15хв порціями додавали 2,16г гідриду натрію (90ммолів, 3екв.), а потім 40мл 1,4діоксану. Після цього додавали розчин 2,57г малононітрилу (39ммолів, 1,3екв.) у 5мл 1,4-діоксану і суміш нагрівали до 90°С. Після закінчення 18год суміш охолоджували до кімнатної температури і реакцію припиняли обережним додаванням 100 мл насиченого розчину хлориду амонію. Після цього значення рН реакційної суміші встановлювали на 6 за допомогою 1н. НСl і суміш екстрагували дихлорметаном. Органічний розчин сушили (сульфат магнію) і розчинники видаляли у вакуумі з одержанням 7,03г (73%) продукту у вигляді коричневого масла. Дані ЯМР- і МС-аналізу підтверджували одержання цільового продукту (сполуки формули IV, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, a R12 і R13 означають CN). Приклад 2: Арилування діетилмалонату з одержанням сполуки формули IV, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, a R12 і R13 означають CCbEt 500-мілілітрову двогорлу круглодонну колбу, обладнану механічною мішалкою, парціальним конденсатором гарячого зрошення і термопарою, протягом 20хв продували аргоном, після чого в неї завантажували 404мг Pd(OAc) 2 (1,80ммоля, 0.03екв.), 1,08г 2-(диmpemбутилфосфіно)біфенілу (3,60ммоля, 0,06екв.) і 20,0г трициклічного броміду (сполуки формули И, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, а X означає Вr; 60,0ммолів, 1екв.). До цієї суміші в інетризованій (продутій інертним газом) колбі потім додавали 25,5г К3РО4 (120ммолів, 2екв.), 100мл PhMe і 13,8мл діетилмалонату (90,0ммолів, 1,5екв.). Перемішувану суспензію після цього поміщали в масляну баню і протягом 24год кип'ятили зі зворотним холодильником в атмосфері азоту до витрачання броміду за даними РХВР. Далі реакційну суміш о холоджували до кімнатної температури, розбавляли водою (150мл) і додавали толуол (50мл). Після цього суміш перемішували протягом 1год при кімнатній температурі до розчинення усієї твердої речовини. Потім дво 13 80141 фазний розчин переносили в ділильну лійку і шари розділяли. Водний шар екстрагували толуолом (50мл). Об'єднані органічні шари фільтрували через шар целіту і концентрували у вакуумі з одержанням в'язкого масла, яке упарювали досуха, одержуючи жовтогарячу тверду речовину. Після хроматографії на силікагелі (з використанням суміші EtOAc/гексан у співвідношенні 1:1) одержали 20,5г чистого аддукту малонату (сполуки формули IV, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, a R12 і R13 означають CO2Et) (83%) у вигляді безбарвної твердої речовини. tm 122-123°C. 1 Н-ЯМР (400МГц, CDCl3): d = 8,38 (d, J - 2,5 Гц, 1Н), 8,19 (dd, J = 1,5, 4,6 Гц, 1Н), 8,16 (d, J = 2,4 Гц, 1Н), 7,47 (dd, J = 1,5, 8,0 Гц, 1Н), 7,09 (dd, J = 4,7, 8,0 Гц, 1H), 4,56 (s, 1H), 4,20 (m, 6H), 3,49 (s, 3H), 1,25 (t, J = 7,1 Гц, 9Н). 13 С-ЯМР (100МГц, CDCl3): d = 167,30 (s), 167,23 (s), 159,31 (s), 154,50 (s), 151,18 (d), 144,34 (d), 141,93 (d), 131,63 (s), 130,74 (d), 123,52 (s), 120,57 (s), 119,78 (d), 62,17 (t), 54,80 (d), 41,24 (t), 37,30 (q), 13,96 (q), 13,58 (q). Елементний аналіз: розрахований для C21H24N4 O5: С 61,15, Н 5,87, N 13,58; виявлено: С 61,14, Н 5,66, N 13,51. Приклад 3: Арилування ізопропілціаноацетату з одержанням сполуки формули V, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, a R19 означає СO2Н У продутий інертним газом реактор об'ємом 800л завантажували 12,0кг 60%-ного NaH в маслі (300молів, 2,5екв.), 0,27кг Pd(OAc)2 (1,2моля, 0,01екв.), 1,26кг РРh3 (4,8моля, 0,04екв.) і 40кг трициклічного броміду (сполуки формули II, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, а X означає Вr; 120молів, 1екв.). Потім реактор знову продували інертним газом, після чого в нього завантажували 70кг PhMe і суміш нагрівали до 60°С. До цієї суміші потім протягом 2год за допомогою дозувальної помпи з постійною витратою додавали розчин 17,4л ціаноізопропілацетату (138молів, 1,15екв.) у 20л PhMe (при здійсненні цієї операції слід дотримуватися обережності в зв'язку з виділенням газоподібного Н 2). Далі вміст реактора нагрівали до 100°С і витримували при цій температурі протягом 1,5 год. Після закінчення цього проміжку часу РХВР-аналіз аліквотної кількості показав завершення процесу арилування до сполуки формули IV, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, R12 означає CN, a R13 означає СО2-ізо-Рr. Потім суміш охолоджували до 35°С і реакцію припиняли додаванням 19кг ізопропанолу (308молів, 2,6екв.) протягом 20хв (при здійсненні цієї операції слід дотримуватися обережності в зв'язку з виділенням газоподібного Н 2). Після цього додавали 438кг 1-молярного розчину NaOH (417молів, 3,5екв.), суміш нагрівали до 80°С і витримували при цій температурі протягом 8 год. Після закінчення цього проміжку часу РХВР-аналіз аліквотної кількості показав завершення процесу гідролізу до необхідної карбонової кислоти. Далі суміш охолоджували до 25°С і фази розділяли. Верхню фазу направляли у відхід, а нижню водну фазу повертали в реактор. Потім у реактор заван 14 тажували 218кг EtOAc і суміш перемішували протягом 15хв, після чого фазам давали розділитися. Нижню водну фазу знову повертали в реактор і охолоджували до 10°С. До цієї суміші потім повільно додавали 6н. H2SO4, безперервно контролюючи значення рН до досягнення ним кінцевої величини, яка дорівнювала 3,3, для чого потрібно було витрати ти 1,33кг розчину H2SO 4. Утворену суспензію потім нагрівали до 25°С і витримували при цій температурі протягом 1 год. Після цього вміст реактора центрифугували і двічі промивали 40кг Н2О. Тверду речовину потім сушили в повному вакуумі при 40°С до залишкового вологовмісту, що досягав межі чутливості вимірювальної апаратури менше 1% з одержанням 36,0кг карбонової кислоти (сполуки формули V, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, a R19 означає СО2Н; 96%) у вигляді білуватої твердої речовини. tm 226-228°C. 1 Н-ЯМР (500МГц, ДМСО): d = 12,47 (s, 1H), 8,32 (d, J = 2,0 Гц, 1Н), 8,20 (dd, J = 4,6, 1,5 Гц, 1Н), 7,96 (d, J = 2,3 Гц, 1Н), 7,81 (dd, J = 8,0, 1,6 Гц, 1Н), 7,24 (m, J = 4,6, 8,0 Гц, 1H), 4,08 (q, J = 7,0 Гц, 2H), 3,63 (s, 3H), 3,43 (s, 3H), 1,17 (t,J = 7,0 Гц, 3Н). 13 С-ЯМР (125МГц, ДМСО): d = 172,22 (s), 166,26 (s), 157,47 (s), 153,96 (s), 151,32 (d), 144,06 (d), 141,59 (d), 131,72 (d), 131,14 (s), 126,01 (s), 120,28 (d), 120,12 (s), 40,45 (t), 36,74 (q), 36,34 (t), 13,42 (q). Елементний аналіз: розрахований для C16H16N4 O3: С 61,53, Н 5,16, N 17,94; виявлено: С 61,28, Н 4,94, N 17,56. Приклад 4: Арилування метилфенілсульфонилацетату з одержанням сполуки формули IV, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, R12 означає СO2 Ме, a R13 означає SO2Ph У колбу завантажували 165мг Pd2dba3 (0,18ммоля, 0,02екв.), 577мг трифенілфосфіну (2,2ммоля, 0,12екв.) і 45мл 1,4-діоксану. Після 15хвилинного перемішування в атмосфері інертного газу порціями додавали 647мг NaH (27ммолів, 3екв.). Далі до цієї суміші додавали 3,00г трициклічного броміду (сполуки формули II, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, а X означає Вr; 9,00ммолів, 1екв.), а потім 2,50г (11,7ммоля, 1.3екв.) метилфенілсульфонилацетату. Після цього суміш нагрівали до 60°С і витримували при цій температурі протягом 18год, після чого охолоджували до кімнатної температури і реакцію припиняли додаванням 0,5мл Н 2О. Діоксан видаляли у вакуумі з одержанням сирого продукту у вигляді сірої твердої речовини з виходом 3,5г (близько 90%). Дані ЯМР- і МС-аналізу підтверджували одержання цільового продукту арилування (сполуки формули IV, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, R12 означає СО2Ме, a R 13 означає SO2Ph). Приклад 5: Арилування діетилфосфонілацетонітрилу з одержанням сполуки формули IV, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, R12 означає CN, a R 13 означає P(O)(OEt)2 У колбу завантажували 1,00г трициклічного броміду (сполуки формули II, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, а X озна 15 80141 чає Вr; 3,00ммоля, 1екв.), 55мг Pd2dba3 (0,06ммоля, 0,02екв.), 95мг трифенілфосфіну (0,36ммоля, 0,12екв.) і 0,69г діетилфосфонілацетонітрилу (3,90ммоля, 1,3екв.). Далі до цієї суміші додавали 15мл 1,4-діоксану, а потім 216мг NaH (9,00ммолів, 3екв.). Отриману суміш після цього нагрівали до 70°С і витримували при цій температурі протягом трьох годин. Потім суміш охолоджували до кімнатної температури, реакцію припиняли обережним додаванням 25мл Н2О і потім додавали 20мл дихлорметану. Після цього значення рН встановлювали на 2,5 за допомогою 1н. водної НСl і розбавляли додаванням додаткової Комп’ютерна в ерстка В. Клюкін 16 кількості Н 2О (25мл) і дихлорметану (25мл). Після завершення цієї операції фази розділяли й органічну фазу концентрували з одержанням коричневого масла. Це масло потім розтирали з 10мл mpemбутилметилового ефіру з одержанням продукту, що випав в осад, який відфільтровували, одержуючи 0,95 г продукту у вигляді білуватої твердої речовини. Дані ЯМР- і МС-аналізу підтверджували одержання цільового продукту арилування (сполуки формули IV, у якій R2 і R4 означають Н, R5 означає Me, R11 означає етил, R12 означає CN, a R13 означає P(O)(OEt)2). Підписне Тираж 26 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess and intermediates for making non-nucleoside hiv-1 reverse transcriptase inhibitors
Назва патенту російськоюСпособ и промежуточные соединения для получения ненуклеозидных ингибиторов ревертазы вируса вич-1
МПК / Мітки
МПК: C07D 471/04, C07F 9/6524, C07D 471/14, C07B 61/00
Мітки: сполуки, проміжні, віл-1, спосіб, ненуклеозидних, вірусу, одержання, ревертази, інгібіторів
Код посилання
<a href="https://ua.patents.su/8-80141-sposib-i-promizhni-spoluki-dlya-oderzhannya-nenukleozidnikh-ingibitoriv-revertazi-virusu-vil-1.html" target="_blank" rel="follow" title="База патентів України">Спосіб і проміжні сполуки для одержання ненуклеозидних інгібіторів ревертази вірусу віл-1</a>
Попередній патент: Спосіб одержання невірапіну, проміжна сполука (варіанти)
Наступний патент: Застосування похідної бензофенону для боротьби з pseudocercosporella herpotrichoides
Випадковий патент: Пристрій для аеропневмовивантажування бункерного вагону












