Похідні сульфінової кислоти та суміш і композиція з ними
Формула / Реферат
1. Сполука сульфінової кислоти формули (І)
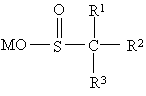 , (I)
, (I)
де
М означає атом водню, іон амонію, іон одновалентного металу або еквівалент іону двовалентного металу з групи Іа, ІІа, IІb, IVa або VІІІb Періодичної системи елементів,
R1 означає ОН або NR4R5, де незалежні один від одного R4 або R5 являють собою Н або С1-С6алкіл,
R2 означає Н або алкіл, алкеніл, циклоалкіл або арильну групу, причому для цих груп можливо мати 1, 2 або 3 замісники, які відібрані незалежно один від одного з ряду С1-С6алкілу, ОН, О-С1-С6алкілу, галогену і СF3 та
R3 означає СООМ, SО3М, COR4, CONR4R5 або COOR4, де М, R4 і R5 визначені вище, та її сіль.
2. Сполука сульфінової кислоти формули (І) за п. 1, де М являє собою іон амонію або лужного металу чи еквівалент іону лужноземельного металу або іон цинку.
3. Сполука сульфінової кислоти формули (І) за п. 1 або п. 2, де R1 являє собою ОН або NH2.
4. Сполука сульфінової кислоти формули (І) за п. 1, де R2 являє собою атом водню або алкільну чи арильну групу, яка може мати одну або дві гідроксил- чи алкоксикомпоненти.
5. Сполука сульфінової кислоти формули (І) за п. 1, де R3 являє собою СООМ або COOR4, де М і R4 є такими, як зазначено в п. 1.
6. Сполука сульфінової кислоти формули (І) за п. 1, де М означає іон лужного металу або еквівалент іону лужного металу чи іон цинку,
R1 означає ОН або NH2,
R2 означає Н або алкіл,
R3 означає СООМ або COOR4, причому М визначено вище, а
R4 означає Н або С1-С6алкіл.
7. Сполука сульфінової кислоти формули (І) за п. 1, де M є іоном Na, К, Mg, Ca, Zn, вибрана однією з групи сполук, яка включає
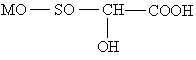 ,
,
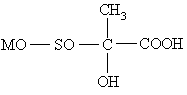 ,
,
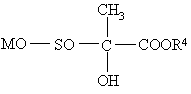 ,
,
де R4 = CH3, C2H5.
8. Суміш, яка містить сполуку сульфінової кислоти за пп. 1-7 із сульфокислотою, що відповідає сполуці цієї сульфінової кислоти чи її солі, і вибірково з відповідним сульфітом.
9. Суміш за п. 8, що має наступний склад:
сполука формули (І)
20-99 мас. %
сульфокислота, що відповідає сполуці формули (І)
не більше 60 мас. %
М2SO3
0-40 мас. %.
10. Суміш за п. 9, що має наступний склад:
2-гідрокси-2-сульфінатоцтова кислота, двонатрієва сіль
40-73 мас. %
2-гідрокси-2-сульфонатоцтова кислота, двонатрієва сіль
2-7 мас. %
сульфіт натрію
0-33 мас. %
вода
5-30 мас. %.
11. Суміш за п. 9, що має наступний склад:
2-гідрокси-2-сульфінатоцтова кислота, сіль цинку
20-70 мас. %
2-гідрокси-2-сульфонатоцтова кислота, сіль цинку
5-60 мас. %
вода
5-30 мас. %.
12. Суміш за п. 9, що має наступний склад:
2-гідрокси-2-сульфінатопропіонової кислоти двонатрієва сіль
38-70 мас. %
2-гідрокси-2-сульфонатопропіонової кислоти двонатрієва сіль
5-30 мас. %
сульфіт натрію
0-33 мас. %
вода
5-30 мас. %.
13. Суміш за п. 12, що має наступний склад:
етил 2-гідрокси-2-сульфінатоетилпропіонат, нітрат
60-80 мас. %
етил 2-гідрокси-2-сульфонатетилпропіонат, нітрат
0-5 мас. %
сульфіт натрію
0-5 мас. %
вода
5-20 мас. %.
14. Композиція, що містить щонайменше одну сполуку сульфінової кислоти відповідно до пп. 1-7 або щонайменше одну суміш відповідно до пп. 8-13, разом із звичайними добавками і наповнювачами.
15. Сполука сульфонової кислоти відповідно до пп. 1-7, що є відновником.
16. Сполука за п. 15, що є відновною компонентою для друку на текстилі, текстильного вибілювання або кубового фарбування чи призначена для відновного вибілювання при обробці мінералів або волокон.
17. Сполука за п. 15, що є співкаталізатором в емульсійній полімеризації або системі окислювально-відновного каталізатора при виробництві пластиків.
Текст
Винахід відноситься до похідних сульфінової кислоти, їх одержання і використання в різних галузях. Як відомо, сульфінова кислота, H2SO2, є одним з найсильніших відновників. Вільна сульфінова кислота є нестабільною. Тому вона і відповідно її похідні технічно реалізуються тільки в їхніх стійких формах. До цього часу економічно значущими є наступні похідні сульфінової кислоти: 1. Дитіоніт натрію (вибілювання волокон, виробництво паперу, кубове фарбування і вибілювання текстилю, вибілювання мінералів, вилучення важких металів з промислових стічних вод). 2. Дигідрат формальдегід-сульфоксилат натрію (витравний друк на текстилі, вибілювання текстилю, спільний каталізатор в емульсійній полімеризації, зниження важких металів у фармацевтиці). 3. Формамідинсульфінова кислота (вибілювання волокон у виробництві паперу, вибілювання текстилю). 4. Формальдегід-сульфоксилат цинку (друк на текстилі і вибілювання текстилю). Усі вищезгадані похідні сульфінової кислоти використовуються у вигляді водних розчинів або дисперсій. У водному середовищі дитіоніт натрію і формамідинсульфінат лужних металів (вільна формамідинсульфінова кислота практично нерозчинна у воді, у кислотному вираженні тільки має надто слабку відновну дію) стабільні тільки протягом короткого відрізку часу. В результаті навіть при кімнатній температурі вони показують чудову відновну здатність і прекрасний вибілювальний ефект на волокнах. Водні препарати формальдегід-сульфоксилату натрію і формальдегід-сульфоксилату цинку є стабільними при кімнатній температурі протягом місяців. Обидва формальдегід-сульфоксилати виявляють свою справжню відновну дію при температурі, що перевищує 90°С. У сильному лужному чи кислотному середовищі або за присутності придатних окисників обидва формальдегід-сульфоксилати чинять, звичайно, відновний ефект при температурі нижче 90°С. Ця особливість формальдегід-сульфоксилатів, а саме, демонструвати дуже однорідний і легко контрольований відновний ефект при температурах від 5°С до 90°С, використовується звичайно в емульсійній полімеризації вільнорадикальної ініціалізації. Тут формальдегід-сульфоксилати використовуються у різноманітних емульсійно-полімеризаційних системах. У випадку холодного одержання SBR (стиролбутадієновий каучук), полімеризація ініціюється за допомогою органічних пероксидів. При низьких температурах полімеризації (біля 5°С) органічні пероксиди, проте, не розпадаються на необхідні вільні радикали. Розщеплення пероксиду повинне бути ініційоване каталітичною кількістю солей заліза(И). Залізо на другій стадії окислювання переходить у третю стадію окислювання, не роблячи її довше тієї, яка потрібна для розщеплення пероксиду. За допомогою сульфоксилату формальдегіду іони заліза (III) знову відновлюються до іонів заліза (ІІ) - розщеплення пероксиду та ініціалізація вільних радикалів продовжуються. В інших емульсійно-полімеризаційних системах сполуки пероксиду, такі, як перекис водню або пероксидисульфати, використовують як джерела вільних радикалів. Для того, щоб збільшити швидкість утворення вільних радикалів, знову використовують відновники. За приклади можна навести формальдегід-сульфоксилати, бісульфіти, аскорбінову кислоту, ізоаскорбінову кислоту і еритробат натрію. Формальдегід-сульфоксилати, зокрема формальдегід-сульфоксилат натрію, довели, що можуть бути особливо ефективними і високозначущими відновниками. Однак під час процесу відновлення формальдегід-сульфоксилати виділяють формальдегід. Дисперсії пластиків чи полімерів, які не повинні містити формальдегід, полімеризуються або при використанні бісульфітів, аскорбінової кислоти, ізоаскорбінової кислоти, або еритробату натрію. Оскільки формальдегід-невмісні відновники є більш слабкими відновниками, недоліки від менш закінченої полімеризації у порівнянні з формальдегідсульфоксилатами повинні бути прийнятними. Крім того, використання аскорбінової кислоти, ізоаскорбінової кислоти і еритробату натрію призводить до небажаного пожовтіння полімеру. Об'єктом даного винаходу є одержання нових похідних сульфінової кислоти, у яких хімічні властивості є, за можливості, подібними властивостям формальдегід-сульфоксилату, але які не виділяють формальдегід у процесі або після використання. Виявилося, що ця мета досягається за допомогою похідних сульфінової кислоти того типу, який більш докладно описаний нижче. Таким чином, даний винахід охоплює сполуки сульфінової кислоти формули (І) де Μ означає атом водню, іон амонію, іон одновалентного металу чи іон еквівалентного двовалентного металу з групи Іа, IIа, IIb, IVa або Vlllb Періодичної системи елементів; R1 означає ОН або NR4R5, де R4 чи R5 незалежно один від одного являють собою Η або Сі- Сеалкіл; R2 означає Η або алкіл, алкеніл, циклоалкіл чи арильну групу, причому для цих груп можливо мати 1, 2 або 3 замісника, які відібрані незалежно один від одного з ряду С1-С6- алкілу, ОН, О - С1-С6алкілу, галогену і CF3; R3 означає СООМ, SO3M, COR4, CONR4R5 або COOR4, де Μ, R4 і R5 визначені вище, або, якщо R2 являє собою арил, який може бути незаміщеним або заміщеним, як зазначено вище, R3 означає також Н, та їхні солі. Для даного винаходу вираження, перелічені нижче, мають наступні значення: алкіл являє собою нормальну або розгалужену алкільну групу, яка переважно має 1-6, зокрема 1-4, атомів вуглецю. Приклади алкільних груп - це метил, етил, н-пропіл, ізопропіл, н-бутил, трет-бутил, н-гексил тощо. Подібне застосування властиве алкільній групі О-алкілу. Алкеніл являє собою алкенільну нормальну або розгалужену групу, яка переважно має 3-8 атомів вуглецю, зокрема 3-6 атомів карбону. Більш прийнятною алкенільною групою є алільна група. Особливо прийнятний циклоалкіл - це зокрема С3-С6циклоалкіл, циклопентил і циклогексил. Арил (також аралкіл) є переважно фенілом або нафтилом. Якщо арильний радикал є фенільною групою і заміщується, він переважно має два замісники. Вони знаходяться зокрема у другому і/або четвертому положенні. Галоген являє собою F, СІ, Вг і І, більш прийнятно СІ і Вг. Μ - переважно іон амонію, іон лужного металу або еквівалент іона лужноземельного металу чи іон цинку. Придатними іонами лужного металу є зокрема іони натрію і поташу. Придатні іони лужно-земельного металу - це зокрема іони магнезії і кальцію. R1 - переважно гідроксил- або аміногрупа. R2 - переважно атом водню або алкільна чи арильна група, яка може бути заміщена як зазначено вище. Він переважно має один або два гідрокси- і/або алкокси-замісника. R3 - переважно або СООМ, або COOR4 (M і R4 такі, як зазначено вище), або, якщо R2 є арилом, який може бути заміщений як зазначено вище, може бути також атомом водню. Більш прийнятне втілення описується складом формули (І), у якій Μ - іон лужного металу або еквівалент іона лужно-земельного металу чи іон цинку; R1 - гідроксил- або аміногрупа, R2 - Η або алкіл; R3 - СООМ або COOR4, де Μ це Н, іон лужного металу або еквівалент іона лужноземельного металу, а R4 - це Сі-Сбалкіл. Подальше більш прийнятне втілення описується формулою (І), у якій Μ - іон лужного металу або еквівалент іона лужно-земельного металу чи іон цинку; R1 - гідроксил- або аміногрупа; R2 - незаміщений арил або арил, заміщений як зазначено вище, зокрема гідроксифеніл або С1С4алкоксифеніл; R3 - атом водню. Нові сполуки одержують із солей дитіоніту. Добре, якщо це сіль, що має катіон, який є також необхідним у сполуках сульфінової кислоти. Солі дитіоніту вступають у реакцію при одержанні таких сполук, у яких R2 є незаміщеним або заміщеним ариловим радикалом, a R3 - атомом водню, відповідно до ароматичного альдегіду. Цю реакцію можна ілюструвати при використанні дитіоніту натрію і 2-оксибензальдегіду як прикладу та нижченаведеного рівняння реакції: Усі інші сполуки формули Μ одержують взаємодією солей дитіоніту з відповідною 1, 2-дикарбонілсполукою або еквівалентом сульфокислоти. Використовувана 1,2-дикарбоніл-сполука - це, зокрема, гліоксилова кислота або відповідні кето-сполуки та їхні ефіри. Ця взаємодія може бути проілюстрована шляхом використання, наприклад, дитіоніту натрію і гліоксилової кислоти і нижченаведеного рівняння реакції: Взаємодію, як правило, проводять у водному середовищі за присутності основи. Водне середовище може також включати водорозчинні органічні розчинники, такі як метанол, етанол, ізопропанол і т.п. Основи, які можна використовувати, - це, зокрема, гідроокис лужних металів і гідроокис рідко-земельних металів. Реакції, як правило, проводять при температурі оточуючого середовища; нагрівання взаємодіючої суміші, як правило, не потрібне, тому що реакція є екзотеричною. Бажаний продукт звичайно випадає в осад із взаємодіючої суміші або може бути осаджений шляхом доповнення полярними, водорозчинними органічними розчинниками, такими, як метанол, етанол, ізопропанол, ацетон тощо. Результуючий продукт утворюється у вигляді солі, яка може, якщо потрібно, бути перетворена у вільну сульфінову кислоту шляхом підкислення або хроматографії на іонообмінному наповнювачі. Крім того, цей продукт звичайно одержують у суміші з відповідним сульфітом металів. У багатьох випадкахсуміш також містить відповідну сульфокислоту і кристалізаційну воду. Нові сполуки можуть бути відділені від супутніх компонентів звичайним способом, наприклад, шляхом перекристалізації з води або з розведеного спирту. На практиці не потрібно виділяти супутні компоненти. Навпаки, виявлено, що дія нових сполук навіть посилюється завдяки цим супутнім компонентам. Даний винахід, таким чином, також охоплює відповідні суміші зі згаданими компонентами. Тому металосульфіт може бути присутнім у кількості до 40%, а сульфокислота - у кількості до 60%. Вміст води може бути до 30%. Нові сполуки є відновниками, чия відновна дія порівнянна з дією формальдегід-сульфоксилату. Проте вони мають перевагу не внаслідок виключення формальдегіду перед, протягом або після використання. Нові сполуки є, таким чином, більш прийнятними для використання в таких галузях, де виділення формальдегіду небажане. Наприклад, вони можуть використовуватися як відновники при фарбуванні текстилю, зокрема знебарвленні текстилю, при вибілюванні або кубовому фарбуванні текстилю або як відновники для мінеральних вибілювачів, таких як каолін і т.д., а також волокон, наприклад, целюлозних. Вони, проте, використовуються як спільний каталізатор в емульсійній полімеризації разом з ініціаторами окиснення для проведення полімеризації при більш низькій температурі. З цією метою сульфінові кислоти можуть також, якщо потрібно, використовуватися разом з іонами окислюваних металів, таких як Fe0+, Mn2+ і т.д. Іони таких металів потім переважно використовуються як протиіони стосовно даних сполук сульфінової кислоти, тобто M=Fe2+, Mn2+ і т.д. При використанні нові сполуки звичайно виражаються формулою разом із звичайними добавками і наповнювачами. У цьому відношенні не існує приватних обмежень; можуть використовуватися не тільки дані відновні сполуки. Нижченаведені приклади ілюструють даний винахід, але не обмежують його. Чисті сполуки, дані в прикладах, відносяться до продукту, який містить одержувану кристалізаційну воду, тобто чистота значно вище, коли вміст такої води береться до уваги. Приклад 1 2-гідроксифенілгідроксиметилсульфінової кислоти нітрат 50мл 2-гідроксибензальдегіду і 45г 50% розчину гідроксиду натрію додавали у водний розчин до 90г технічного гідросульфіту натрію (дитіоніт натрію). По закінченні екзотеричної реакції кінцевий сирий продукт був відділений при використанні метанолу і перекристалізований із метанол/етанол/водної суміші. Нітрат 2гідроксифенілгідроксиметил-сульфінової кислоти був отриманий із чистотою, що досягає 75,8%. Вміст сульфінової кислоти визначався за допомогою йодометрії. Нижче наведені дані ІЧ- спектроскопічних досліджень (Т=пропускання): 3551.97см-1 (28.51 %Т); 3175.96см-1 (19.45%Т); 2915.51см-1 (29.95%Т); 2747.10см-1 (34.58%Т); 1899.95см1 (61.96%Т); 1682.34см-1 (44.77%Т); 1641.40см-1 (38.98%Т); 1594.46см-1 (32.49 %Т); 1505.02см-1 (42.21%Т); 1455.65см-1 (17.74%Т); 1387.05см-1 (27.73%Т); 1330.41см-1 (40.37%Т); 1280.09см-1 (30.89%Т); 1244.74 см-1 (23.14%Т); 1200.40 см-1 (31.90%Т); 1155.73 см-1 (30.12%Т); 1111.53см-1 (29.83%Т); 1098.58см-1 (32.10%Т); 1072.68см-1 (28.14%Т); 1030.15см-1 (16.57%Т); 995.68см-1 (16.40%Т); 957.46см-1 (16.83%Т); 872.69см-1 (43.53%Т); 846.84см-1 (42.51%Т); 801.62см-1 (40.51%Т); 762.15см-1 (28.82%Т); 744.61см-1 (21.25%Т); 659.92см-1 (26.13%Т); 629.31см-1 (30.85%Т); 588.96см-1 (26.78%Т); 561.45см-1(41.13%Т); 496.95см-1 (30.36%Т). Приклад 2 4-метоксифенілгідроксиметилсульфінової кислоти нітрат 63г 4-метоксибензальдегіду і 45г 50% водного розчину гідроокису натрію додавали до 90г технічного гідросульфіту натрію у водному розчині. Випарюванням з отриманого розчину осаджували сирий продукт. Дані солі натрію сульфінової кислоти були отримані шляхом кристалізації з метанол/етанол/водної суміші, що мала чистоту біля 68%. Солі натрію відповідної сульфокислоти були представлені як вторинний компонент. Приклад 3 2-гідрокси-2-сульфінатооцтової кислоти двонатрієва сіль. Взаємодія 358 г технічного гідросульфіту натрію у 800імл води з 268г 50%-ною гліоксиловою кислотою і 285г 50%-ним розчином гідроксиду натрію давала 2-гідрокси-2-сульфінооцтової кислоти двонатрієву сіль з виходом до 95%. Твердий сирий продукт містив 43% сульфінової кислоти (без води від гідратації). Кристалізація від метанол/етанол/водної суміші давала гідрат сульфінової кислоти з добрими кристалами. Сірковмісні компоненти були відокремлені за допомогою йодометрії. Сульфінова кислота показувала реакцію з індантреновим папером при 75°С. ІЧ-спектральні дослідження показують наступні пікові значення: 3588.57см-1 (6.21%Т); 3485.05см-1 (1.37%Т); 3339.44см-1 (1.75%Т); 2905.13см-1 (38.46%Т); 2794.17см-1 (42.39%Т); 2189.93см-1 (54.06%Т); 1662.54см-1 (7.35%Т); 1613.92см-1 (0.67%Т); 1417.54см-1 (7.34%Т); 1388.03см-1 (8.65%Т); 1248.31см-1 (3.95%Т); 1185.34см-1 (30.75%Т); 1153.96см-1 (20.95%Т); 1103.16см-1 (5.58%Т); 1027.04см-1 (2.61%Т); 968.33см-1 (1.77%Т); 938.07см-1 (26.60%Т); 847.72см-1 (23.10%Т); 717.14см-1 (10.46%Т); 645.46см-1 (14.88%Т); 541.36см-1 (9-25%Т); 491.77 см-1 (11.95 %Т); 445.88см-1 (19.23%Т). * Спектр С-магнітно-ядерного резонансу (63МГц): δ(м.ч.): 93,8 (s); 177,7 (s). Приклад 4 2-гідрокси-2-сульфінатооцтової кислоти сіль цинку Взаємодія 33 г цинкового порошку у водному середовищі з двоокисом сірки давала дитіоніт цинку. Він взаємодіяв in situ із 136г 50%-ної гліоксилової кислоти. По закінченні екзотеричної реакції додавали 75 ZnO. Сирий продукт у фільтраті осаджували, використовуючи метиловий спирт, при цьому він містив 20% сульфінової кислоти і 48% сульфокислоти (йодометричне визначення). Приклад 5 2-гідрокси-2-сульфінатопропіонової кислоти двонатрієва сіль Брали 89г технічного гідросульфіту натрію у воді, і сирий продукт одержували шляхом взаємодії з 40г піровиноградної кислоти та приблизно 78г 50%-ним розчином гідроксиду натрію. Сирий продукт містив 40% сульфінової кислоти і був перекристалізований із метанол/етанол/водної суміші. Цей вміст визначався йодометрично. Двонатрієва сіль відповідної сульфокислоти була представлена як вторинний компонент. Нижче наведені результати ІЧ-спектроскопічних досліджень: 3484.66см-1 (6.25%Т); 2995.53см-1 (26.51%Т); 2758.93см-1 (32.54%Т); 1592.63см-1 (0.62%Т); 1456.02см-1 (16.06%Т); 1436.19см-1 (17.02%Т); 1397.00см-1 (4.77%Т); 1367.01см-1 (7.14%Т); 1190.80см-1 (2.49%Т); 1038.50см-1 (0.70%Т); 981.07см-1 (1.42%Т); 943.83см-1 (7.90%Т); 857.07см-1 (20.25%Т); 804.64см-1 (32.86%Т); 790.68см-1 (34.62%Т); 710,08см-1 (30.79%Т); 659.00см-1 (11.96%Т); 628.53см-1 (9.93%Т); 558.19 см-1 (26.14%Т); 522.56см-1 (16.21%Т); 497.03см-1 (15.70%Т); 431.34см-1 (28.83%Т). Приклад 6 2-гідрокси-2-сульфінатоетилпропіонату, нітрат Після того, як 90г технічно активного гідросульфіту натрію у водному розчині прореагували з 60г етилового ефіру піровиноградної кислоти і 39г 50%-го розчину гідроксиду натрію, нітрат 2-гідрокси-2сульфінатопропіонату етилу випадав в осад під час екзотеричної реакції як гідрат. Вилучений і висушений сирий продукт містив 79% сульфінової кислоти (розрахунок без кристалізаційної води). Склади визначали шляхом йодометрії. ІЧ-спектроскопічні сигнали підсумовані і представлені нижче: 3501.08см-1 (12.01%Т); 3328.38см-1 (16.14%Т); 3003.23см-1 (51.87%Т); 2986.52см-1 (45.03%Т); 2940.61см1 (54.87%Т); 1733.45см-1 (7.42%Т); 1663.31см-1 (48.05%Т); 1469.00см-1 (32.01%Т); 1402.22см-1 (42.89%Т); 1367.58см-1 (40.81%Т); 1298.47см-1 (43.49%Т); 1262.97см-1 (26.65%Т); 1190.27см-1 (10.52%Т); 1105.86см-1 (10.94%Т); 1038.98см-1 (6.62%Т); 1012.00см-1 (30.53%Т); 985.42см-1 (9.37%Т); 948.69см-1 (28.55%Т); 860.86см-1 (56.24%Т); 801.55см-1 (61.53%Т); 685.30см-1 (51.65%Т); 658.49см-1 (51.18%Т); 590.17см-1 (34.18Т); 523.55см-1 (34.88%Т); 471.89 см-1 (41.25%Т); 425.61см-1 (59.75%Т). Приклад 7 Для розрахунку витрати фарби для текстилю на чорній текстурі була обрана фарбувальна паста, що мала наступний склад. Основний склад фарбувальної пасти: 434г води 100г поташу 6г згущувального агента KL-100 (карбоксиметилований крохмаль) 40г Lameprint IND8 (гуар-ефір + крохмаль-ефір) 14г гліцерину 6г принтогену ( мінеральне масло, що самостабілізується) ---------------------------------------------------------------------------------600г основного складу Формальдегід-вільний відновник, що відповідає прикладу 3, або формальдегід-сульфоксилат натрію для порівняльної суміші потім додавали до основного складу. Суміш 1 Порівняльна суміш 600 г основного складу 600 г основного складу 213 г 2-гідрокси-2-сульфінатооцтової кислоти 107г формальдегід-сульфоксилату натрію двонатрієва сіль, що відповідає прикладу 3 (сирий продукт) Результуючі суміші були потім застосовані на чорній текстурі одна за одною і висушені у сушильній шафі. Текстура потім піддавалася старінню при 102°С протягом 10 хвилин, впродовж яких даний барвник відновлювався. Текстуру ретельно обполіскували для вилучення залишків згущувального агента та інших хімікатів, і незабарвлена текстура ставала явною у тих місцях, де попередньо був застосований відновник. Очевидним є те, що витравний друк має добрі характеристики. Промивка складів не становить ніяких проблем. Двонатрієва сіль 2-гідрокси-2-сульфінатооцтової кислоти, таким чином, може бути використана у витравному друку текстилю згідно з даною технологією. Результати витравного друку наведені в табл. 1. Таблиця 1 Білизна R457 1-й вимір 2-й вимір 1-й показник жовтизни 2-й показник жовтизни Суміш 1 69,55 70,24 9,83 9,51 Порівняльна суміш 71,40 70,73 8,91 9,05 Приклад 8 Вибілювання каоліну Початкова концентрація каоліну була 250г/л. Завись містила рН- 6,5. Після того, як завись каоліну була гомогенізована у змішувачі протягом 30 хвилин, рН доводили до 2,5, використовуючи частково концентровану сірчану кислоту. Двонатрієва сіль 2-гідрокси-2-сульфінатооцтової кислоти, що відповідає прикладу 3, і формальдегідсульфоксилату натрію були уведені як 10%-ні розчини і були засновані на твердому вмісті каолінової зависі (див. Табл. 2). Умови реакції: температура: кімнатна рН: 2,5 час взаємодії: 2 години. Таблиця 2 Тип каоліну Кількість сировини (%, абсолютно сухої речовини) Початкова білизна (%) R457 Кінцева білизна (%) R457 0,45 двонатріевої солі 2-гідрокси2-сульфінатс оцтової кислоти, що 73,4 > 76,8 відповідає прикладу 3 0,3 формальдегід-сульфоксилату А 73,4 74,5 натрію 0,3 двонатрієвої солі 2-гідроксиВ* 2-сульфінато-оцтової кислоти, 79,5 82,5 що відповідає прикладу 3 0,3 формальдегід-сульфоксилату В 79,5 79,7 натрію * Пірофосфат натрію додавали як комплексоутворюючий агент. А Тон R457 Насиченість R457 1,51 0,46 1,59 0,61 1,02 0,34 1,34 0,46 Композиція, що містить двонатрієву сіль 2-гідрокси-2-сульфінооцтової кислоти, приводить до добрих результатів у вибілюванні каоліну. Композиція, що містить двонатрієву сіль гідроксіацетилсульфінової кислоти, взаємодіяла у 3-4 рази швидше, ніж формальдегід-сульфоксилат натрію. Таку технологію можна використовувати у вибілюванні мінералів і, зокрема, каоліну. Приклад 9 (порівняльний приклад) 400г води, 286г 10%-го водного розчину Airvol 205 (полівініловий гідролізний спирт 88%, DP (точка роси) =500, що випускається Air Products and Chemicals, Inc.), 286г 10%-го водного розчину Airvol 107 (полівініловий спирт 98%, DP (точка роси) =500, що випускається Air Products and Chemicals, Inc.) і 47г Igepal CO-887 (неіонна поверхнево-активна речовина, що випускається Rhone - Poulenc , Inc.; 70%-ий водний розчин Igepal СО-880, що містить приблизно 30 молей етилен-оксиду) завантажували у герметичну реакційну камеру об'ємом 3,8л і перемішували з 4,8г 1%-го водного розчину сульфату заліза(ІІ). Взаємодіючу суміш доводили до рН 3,3, використовуючи 1,75г 50%-го розчину фосфорної кислоти, потім дозували 1710г мономер - вініл-ацетату. Взаємодіючу суміш перемішували зі швидкістю 900об/хв. і нагрівали до 35°С. Потім 200г газоподібного етилену уводили під тиском до 20,4атм. Далі додавали 5,7г 10%-го водного розчину ізоаскорбінової кислоти (рН=4), що мала наступний склад: 270г води 30г ізоаскорбінової кислоти 0,8г 29%-го розчину гідроксиду амонію. Полімеризацію починали, використовуючи в сумі 10г 0,65%-го водного розчину перекису водню, що мав наступний склад: 589г деіонізованої води 11,1г 35%-го перекису водню. Після початку полімеризації залишок 295,1г розчину ізоаскорбату/ ізоаскорбінової кислоти дозували через кожних 4 години. Додавання 590,1г 65%-го розчину перекису водню проводили при контролі полімеризації так, що взаємодіюча суміш нагрівалася від 35°С до 55°С за 1 годину, і температура 55°С потім могла підтримуватися протягом 3 годин. Після повного періоду полімеризації тривалістю 4 години вміст вільного мономер-вінілацетату залишався 1,5%. Взаємодіюча суміш охолоджувалася до 35°С і надходила у вакуумний реактор для дегазації надлишку етилену. Вільний мономер-вініл-ацетат, що залишався в емульсії, ефективно полімеризувався шляхом додавання 20г 10%-го водного розчину ізоаскорбінової кислоти і 3,5%-го розчину перекису водню, що в результаті приводило до зменшення кінцевого вмісту вільного мономер-вініл-ацетату, який не перевищував 0,5%. РН полімер-емульсії доводили до необхідної рН (див. Табл. 3), використовуючи 14%-ий водний розчин гідроксиду амонію. Фізичні властивості полімер-емульсії (латексу) наведені в таблиці 3. Приклад 10 (порівняльний приклад) Емульсійна полімеризація відповідно до прикладу 9 була повторена і замість ізоаскорбату амонію (ізоаскорбінової кислоти) використовувався водний розчин, що складався з 270г води і 22,1г формальдегідсульфоксилату натрію. Результати наведені в таблиці 3. Приклад 11 (співкаталізатор в емульсійній полімеризації) Емульсійна полімеризація відповідно до прикладу 9 була повторена і замість ізоаскорбату амонію (ізоаскорбінової кислоти) використовувався водний розчин, що складався з 270г води і 33г відновника згідно з прикладом 3 (сирий продукт). Результати наведені в таблиці 3. Таблиця 3 Результуючі параметри Зовнішній вигляд Вміст твердої речовини [%] рН В'язкість [Ра·s] (60об/хв; 25°С) Tg (полімер) [°С] Вільний формальдегід [об/хв] ледь жовтуватий 62,1 6,5 440 молочно-білий 63,4 6,0 380 Приклад 11 (порівняння) молочно-білий 63,2 6,2 560 +5 +4 +7 130 Приклад 9 (порівняння) Приклад 10 (порівняння) Приклад 12 Вибілювання деревного борошна Умови вибілювання: вміст сировини: 5,4% температура 75°С вибілювання: 0,2/0,4/0,6/0,8/1,0 % вибілювальні вибілювача, абсолютно добавки: сухого (стосовно сухої ваги) час вибілювання: 30 хвилин. Для вибілювання по 100г деревного борошна в кожному випадку розважували у поліетиленові пакети. Для уведення вибілювача були приготовлені водні розчини (1мл цих розчинів містив 0,2% кожного з абсолютно сухих вибілювачів). Після того, як розчин вибілювача був уведений, пакети відразу зав'язували і вміст ретельно перемішували шляхом розминання у закритих пакетах. Температуру вибілювання регулювали за допомогою термостата (водяної бані). Після досягнення необхідної температури вибілювання суспензію целюлози поміщали у вимірювальні колби і після вибілювання вимірювали рН. Об'єм доводили потім до 300мл за допомогою бюретки і суміш гомогенізували шляхом перемішування суспензії целюлози. Плівки формували, використовуючи звичайний екструдер і чисту пульпу. Отримані плівки піддавали вакуум-сушінню у плівкоформувачі протягом 12 хвилин. Ступінь білизни R 457 усіх сформованих плівок визначали за допомогою пристрою, що вимірює білизну (Elrepho 2000 від Datacolor). Результати наведені в таблиці 4. Таблиця 4 Кількість вибілювача % від абсолютно сухої ваги) 0,0 Формальдегід0,2 сульфоксил 0,4 натрію 0,6 0,8 1,0 Двонатрієва 0,0 сіль 0,2 2-гідрокси-2-суль0,4 фінатооцтової 0,6 кислоти, відповідно 0,8 Вибілювання ( Початкова рН Кінцева рн Білизна Ступінь білизни1) 6,4 6,4 6,4 6,4 6,4 6,4 6,5 6,5 6,5 6,5 6,5 6,3 6,2 6,2 6,2 6,2 6,2 6,4 6,4 6,5 6,6 6,6 65,1 66.6 66,9 67,0 67,3 67,7 65,7 66,7 67,2 67,6 68,0 1,5 1,8 1,9 2,2 2,6 _ 1,0 1,5 1,9 2,3 до прикладу 3 1,0 6,5 *) У порівнянні з необробленим деревним борошном. 6,7 68,1 2,4 Приклад 13 Вибілювальна пульпа Умови вибілювання вибілювальною пульпою: в'язкість отверджувача: 7,4% температура вибілювання: 75°С відносна кількість вибілювача: 0,2/0,4/0,6/0,8/1,0% (абсолютно сухого) час вибілювання: 60 хвилин. Для вибілювання по 70г пульпи розважували у поліетиленові пакети. Для уведення вибілювача приготовляли водні розчини (1мл таких розчинів містив 0,2% кожного з абсолютно сухих вибілювачів). Після того, як розчин вибілювача крапельно уводили, пакети відразу запаювали, і їхній вміст ретельно перемішували шляхом розминання в закритих пакетах. Температуру вибілювання регулювали шляхом використання термостата (водяної бані). Після витримки необхідного часу вибілювання суспензію целюлози відмірювали у вимірювальні колби і після вибілювання заміряли рН. Об'єм потім доводили до 300мл за допомогою бюретки і суміш гомогенізували шляхом перемішування суспензії целюлози. Плівки формували за допомогою звичайного екструдера, використовуючи чисту суспензію целюлози. Отримані плівки піддавали вакуум-сушінню у плівкоформувачі протягом 15 хвилин. Білизну R 457 усіх сформованих плівок визначали за допомогою вимірювача білизни (Elrepho 2000 від Datacolor). Результати наведені в табл. 5. Таблиця 5 Кількість вибілювача % від абсолютно Початкова рН сухої ваги) 0,0 7,2 Формальдегід0,2 7,2 сульфоксилат 0,4 7,2 натрію 0,6 7,2 0,8 7,2 1,0 7,2 Двонатрієва 0,0 7,2 сіль 0,2 7,2 2-гідрокси-2-суль0,4 7,2 фінатооцтової 0,6 7,2 кислоти, відповідно 0,8 7,2 до прикладу 3 1,0 7,2 У порівнянні з необробленим деревним борошном. Вибілювання ( Кінцева рн Білизна Ступінь білизни1) 7,2 7,2 7,3 7,3 7,3 7,4 7,2 7,4 7,4 7,4 7,5 7,5 64,5 65,9 66,3 66,9 66,9 67,0 64,5 64,9 66,0 66,2 66,5 66,3 _ 1,4 1,8 2,4 2,4 2,5 _ 0,4 1,5 1,7 2,0 1,8
ДивитисяДодаткова інформація
Назва патенту англійськоюSulphinic acid derivatives, preparation and use thereof
Назва патенту російськоюПроизводные сульфиновой кислоты, их получение и применение
МПК / Мітки
МПК: C07B 31/00, C09D 9/00, C07C 313/00, C08F 2/12, D06L 3/00, D21C 9/10
Мітки: сульфінової, кислоти, суміш, похідні, ними, композиція
Код посилання
<a href="https://ua.patents.su/7-64730-pokhidni-sulfinovo-kisloti-ta-sumish-i-kompoziciya-z-nimi.html" target="_blank" rel="follow" title="База патентів України">Похідні сульфінової кислоти та суміш і композиція з ними</a>
Попередній патент: Спосіб десублімації фталевого ангідриду із фталевоповітряної суміші
Наступний патент: Спосіб одержання талої води та установка для його здійснення
Випадковий патент: Іконниця-покутник











