Похідні хроманону та спосіб їх одержання
Номер патенту: 75892
Опубліковано: 15.06.2006
Автори: Шмід Уші, Бокел Гейнз-Германн, Мюрманн Крістоф
Формула / Реферат
1. (R)-2-амінометил-4-хроманону формули І
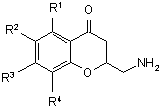 , І
, І
в якій
R1-R4 означає Н
та його солі.
2. Сполуки формули І за п. 1, які застосовують як проміжні сполуки для синтезу медичних препаратів.
3. Сполуки формули І за п. 1, які застосовують як проміжні сполуки для синтезу медичних препаратів, які впливають на центральну нервову систему.
4. Спосіб одержання (R)-2-амінометил-4-хроманону формули І за п. 1 та його солей, який відрізняється тим, що за допомогою нерацемічного хірального каталізатора, яким є комплекс перехідного металу, здійснюють гідрогенізацію сполуки формули II
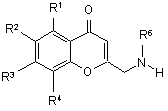 , II
, II
в якій R1, R2, R3 і R4 відповідають значенням, наведеним у п. 1, і
R6 означає ацил, що містить від 1 до 6 атомів вуглецю, -СО-Аr або амінозахисну групу,
щоб одержати сполуки формули III
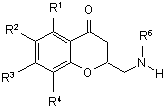 , III
, III
в якій радикали R1-R6 відповідають наведеним вище значенням, і радикал R6 відщеплюють за умов кислотного середовища.
5. Спосіб одержання (R)-2-амінометил-4-хроманону формули І за п. 4, який відрізняється тим, що каталізатором є комплекс перехідного металу, що містить метал, вибраний з групи, що складається з родію, іридію, рутенію й паладію.
6. Спосіб одержання (R)-2-амінометил-4-хроманону формули І за п. 4, який відрізняється тим, що каталізатором є комплекс перехідного металу, в якому перехідний метал утворює комплекс з лігандом хірального дифосфіну.
7. Спосіб одержання (R)-2-[5-(4-фторфеніл)-3-піридилметиламінометил]-хроману та його солей, який відрізняється тим, що
а) сполуку формули
 , II
, II
в якій R1, R2, R3 і R4 означають Н, а R6 відповідає наведеним у п. 4 значенням, гідрогенізують за допомогою нерацемічного хірального каталізатора, щоб одержати сполуку формули III
 , III
, III
в якій R1-R6 відповідають наведеним вище значенням,
b) енантіомерично чисту (R)-сполуку формули IIIа
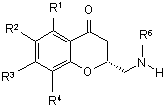 , IIIa
, IIIa
одержують кристалізацією з отриманої енантіомерично збагаченої суміші (R)- і (S)- сполук формули III, в якій R1-R6 відповідають наведеним вище значенням,
c) радикал R6 видаляють з отриманої (R)- сполуки формули ІІІа за умов кислотного середовища, в якій R1-R6 відповідають наведеним вище значенням, щоб одержати енантіомерично чисту (R)- сполуку формули І
 , I
, I
в якій R1, R2, R3 і R4 означають Н, або сіль цієї сполуки,
d) енантіомерично чисту (R)-сполуку формули І, в якій R1-R4 означає Н, відновлюють за звичайною методикою, щоб одержати (R)-амінометилхроман,
e) отриманий (R)-(хроман-2-ілметил)амін перетворюють на його сіль з кислотним залишком, а останню перетворюють за відомою методикою на (R)-2-[5-(4-фторфеніл)-3-піридилметиламінометил]хроман і, можливо, - на його сіль з кислотним залишком, крім того можна здійснювати виділення (R)-енантіомера з енантіомерично збагаченої (R,S)-суміші кристалізацією після етапу с) або після етапу d).
Текст
1. (R)-2-амінометил-4-хроманону формули І R1 O 3 R1 75892 4 ням, щоб одержати енантіомерично чисту (R)сполуку формули І R1 O O R2 R6 O R3 N R2 H R4 , III в якій R1-R6 відповідають наведеним вище значенням, b) енантіомерично чисту (R)-сполуку формули IIIа R1 O R2 R6 O R3 N H R4 , IIIa одержують кристалізацією з отриманої енантіомерично збагаченої суміші (R)- і (S)- сполук формули III, в якій R1-R6 відповідають наведеним вище значенням, c) радикал R6 видаляють з отриманої (R)- сполуки формули ІІІа за умов кислотного середовища, в якій R1-R6 відповідають наведеним вище значен Винахід відноситься до похідних хроманону формули l у якій R1-R4 кожний, незалежно один від одного означає, Н, А, СN, Hal, OR5, COOR5, CF3, OCF3, NO2, Аr, OAr, N(R5)2 або CON(R5)2, R5 означає Η або А, А означає алкіл, що містить від 1 до 6 атомів вуглецю, Аr означає феніл, що може бути незаміщеним або заміщеним А, OR5, CN, Hal, CF3, OCF3, NO2 або N(R5)2 , Hal означає F, СІ, Вr або І, і їх солям. Винахід відноситься також до оптично активних форм, рацематів, енантіомерів, гідратів і сольватів, наприклад, алкоголятів їх сполук. Аналогічні сполуки розкриті в ЕР 0707007. Предмет винаходу полягає у виявленні нових сполук, що можна застосовувати, зокрема, у якості проміжних сполук у синтезі медичних препаратів. Було виявлено, що сполуки формули І і їх солі є важливими проміжними сполуками для приготування медичних препаратів, в особливості - таких які впливають на центральну нервову систему. O R3 NH2 R4 ,I в якій R1, R2, R3 і R4 означають Н, або сіль цієї сполуки, d) енантіомерично чисту (R)-сполуку формули І, в якій R1-R4 означає Н, відновлюють за звичайною методикою, щоб одержати (R)-амінометилхроман, e) отриманий (R)-(хроман-2-ілметил)амін перетворюють на його сіль з кислотним залишком, а останню перетворюють за відомою методикою на (R)-2-[5-(4-фторфеніл)-3піридилметиламінометил]хроман і, можливо, - на його сіль з кислотним залишком, крім того можна здійснювати виділення (R)-енантіомера з енантіомерично збагаченої (R,S)-суміші кристалізацією після етапу с) або після етапу d). Винахід відноситься до похідних хроманону формули І і їх солям. Вище і нижче, радикали R1, R2, R3, R4, R5 і R6 приймають значення, зазначені в описі формул ІIII, якщо спеціально не обумовлено інше. В приведених вище формулах А означає алкіл, що може бути лінійним або розгалуженим, і містить від 1 до 6, переважно 1, 2, 3, 4, 5 або 6 атомів вуглецю. А означає переважно метил, крім того, етил, п-пропіл, ізопропіл, n-бутил, сек-бутил або тер-бутил, крім того, також пентил, 1-, 2- або 3-метилбутил, 1,1-, 1,2- або 2,2-диметилпропіл, 1етилпропіл, гексил, 1-, 2-, 3- або 4-метилпентил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- або 3,3-диметилбутил, 1або 2-етилбутил, 1-етил-1-метилпропіл, 1-етил-2метилпропіл, 1,1,2- або 1,2,2-триметилпропіл. А означає особливо переважно метил. Ацил містить від 1 до 6 атомів вуглецю, переважно 1, 2, 3 або 4 атомів вуглецю. Ацил являє собою, зокрема, ацетил, пропіоніл або бутирил. Аr означає феніл, що може бути не заміщеним або монозаміщеним, бізаміщеним або тризаміщеним A, CF3, OR5, OCF3, CN, NO2, Hal або N(R5)2, де R5 означає Н або А, і А відповідає приведеному вище визначенню. Аr являє собою переважно феніл. Hal являє собою переважно F, СІ або Вr. R1, R2, R3 і R4 кожний незалежно один від одного, означає, Н, A, CN, Hal, OR5, COOR5, CF3, OCF3, NO2, Аr, OAr, N(R5)2 або CON(R5)2, де А, Hal, Аr і R5 відповідають приведеним вище значенням. R1 переважно означає Н. R2 особливо переважно означає Н. R3 переважно означає Н. R4 переважно означає Н. 5 75892 6 R6 означає ацил, що містить від 1 до 6 атомів R1, R2, R3 і R4 відповідають значенням, привевуглецю, -СО-Ar або амінозахисну групу, де ацил і деним в пункті 1, і Аr відповідають приведеним раніше значенням. R6 R6 означає ацил, що містить від 1 до 6 атомів являє собою особливо переважно ацил. вуглецю, -СО-Аr або аміно-захисну групу, щоб Термін "амінозахисна група" у загальному виодержати сполуку формули III падку, відомий, і відноситься до груп, які придатні для захисту (блокування) аміногрупи від хімічних реакцій. Типовими прикладами таких груп є, зокрема, незаміщена або заміщена ацильна, арильна, аралкоксиметильна або аралкильна групи. Оскільки амінозахисні групи видаляють після проведення потрібної реакції (або послідовності реакцій), їх тип і розмір не мають істотного значення, однак, перевага віддається таким групам, що містять 1-20 атомів вуглецю, особливо 1-8 атомів в якій радикали R1-R6 відповідають приведевуглецю. У зв'язку з даним способом термін "ациним вище значенням, і радикал R6 відщеплюють. льна група" варто розуміти в самому широкому Зокрема, було виявлено, що гідрогенізація (2змісті. Він охоплює ацильні групи, добуті з аліфаацетиламінометил)хромeн-4-ону з різноманітними тичних, араліфатичних, аліциклічних, ароматичних нерацемічними хіральними комплексами роабо гетероциклічних карбонових кислот або сульдій/дифосфін дає енантіомерично збагачений (2фонових кислот і, зокрема, алкоксикарбонільну, ацетиламінометил)-хроман-4-он, і в той ж час ацеалкенілоксикарбонільну, арилоксикарбонільну і тилову групу можна відщепити для попереджання особливо - аралкоксикарбонільну групи. Прикларацемізації. дами ацильних груп цього типу є алканоїл, такий, Винахід відноситься також до способу одеряк ацетил, пропіоніл і бутирил; аралканоїл, такий, жання похідних хроманону формули І, що відрізяк фенілацетил, ароїл, такий, як бензоїл або толуняється тим, що нерацемічним хіральним каталіїл, арилокси-алканоїл, такий, як феноксиацетил; затором є комплекс перехідного металу. алкоксикарбоніл, такий, як метоксикарбоніл, етокКаталізатором є особливо переважно комсикарбоніл, 2,2,2-трихлоретоксикарбоніл, ВОС або плекс перехідного металу, що містить метал, об2-іод-етоксикарбоніл, алкенілоксикарбоніл, такий, раний із групи, що складає родій, іридій, рутеній і як алілоксикарбоніл (Aloс), аралкоксикарбоніл, паладій. такий, як CBZ (синонімічний Z), 4Винахід відноситься, крім того, до способу метоксибензилоксикарбоніл (MOZ), 4одержання похідних хроманону формули І, що нітробензилоксикарбоніл або 9відрізняється тим, що каталізатором є комплекс фторенілметоксикарбоніл (Fmoc), 2перехідного металу, у якому перехідний метал (фенілсульфоніл)-етоксикарбоніл; триметилсиліутворює комплекс із лігандом хірального дифосфілетоксикарбоніл (Теос), або арилсульфоніл, такий, ну. як 4-метокси-2,3,6-триметилфенілсульфоніл (Mtr). Як приклад, можна вказати наступні ліганди: Переважними амінозахисними групами є ВОС, (S)-EtDuphos: Fmoc і Aloс, крім того, CBZ, бензил і ацетил. Особливо переважними захисними групами є ВОС і Fmoc. Сполуки формули І можуть мати один або більше хоральних центрів, і, відповідно, можуть зустрічатися в різноманітних стеріоізомерних формах. Формула І може охоплювати усі ці форми. Особливо переважними сполуками формули І є такі: (S)-BINAP: a) 2-амінометил-4-хроманон, b) (R)-2-амінометил-4-хроманон, c) (S)-2-амінометил-4-хроманон, і їх солі. Винахід відноситься, крім того, до способу одержання похідних хроманону формули I за пунктом 1 і їх солей, який відрізняється тим, що за допомогою нерацемічного хірального каталізатора здійснює гідрогенізацію сполуки формули II (S)-ToIBINAP: в якій 7 75892 8 (S,R)-PFctBu: де ТоІ означає (S, S)-Chiraphos: (S, S)-DIOP: (S, S)-Skewphos (BDPP): (S,S)-BPPM (R,R)-Norphos: (S,R)-BPPFOH: У залежності від вибору (R) або (S)енантіомера ліганда в каталізаторі, з надлишком одержують (R)- або (S)-енантіомери. Попередниками хіральних лігандів є такі сполуки, як, наприклад, Rh(COD)2OTf (циклооктадієнілродію трифлат, [Rh(COD)Cl]2, Rh(COD)2BF4, [Ir(COD)Cl]2, Ir(COD)2BF4 або [Ru(COD)Cl2]x. Сполуки формули І, а також первісні матеріали для їх одержання, можливо, крім того, приготувати за допомогою відомих хімічних реакцій, що описані в літературі (наприклад, в класичних роботах, таких, як Houben-Weyl, Methoden der organischen Chemie [Methods of Organic Chemistry], GeorgThieme-Verlag, Stuttgart), при суворому дотриманні реакційних умов, що відомі і придатні для проведення згаданих реакцій. З цією метою можливо також використовувати їх варіанти, що самі по собі відомі, але тут конкретно не зазначені. Якщо це бажано, вихідні матеріали можна одержати безпосередньо в реакторі таким чином, щоб, не виділяючи їх із реакційної суміші відразу проводити їх наступне перетворення в сполуки формули І. Деякі з сполук формули II відомі; невідомі сполуки можна легко приготувати за аналогією з методиками одержання відомих сполук. Перетворення сполук формули II у сполуки формули І здійснюють у відповідністю зі способом за даним винаходом, із використанням газоподібного водню і за допомогою нерацемічного хірального каталізатора в інертному розчиннику, такому, як, наприклад, метанол або етанол, з наступним видаленням радикала R6 без рацемізації, як зазначено вище. Прикладами придатних інертних розчинників є вуглеводні, такі, як гексан, петролейний ефір, бензол, толуол або ксилол, хлоровані вуглеводні, такі, як трихлоретилен, 1,2-дихлоретан, тетрахлорметан, хлороформ або дихлорметан; спирти, такі, як ізопропанол, n-пропанол, n-бутанол або третбутанол; ефіри, такі, як діетиловий ефір, диізопропіловий ефір, тетрагідрофуран (THF) або діоксан; гліколеві ефіри, такі, як етиленгліколь монометиловий або моноетиловий ефір або етиленгліколь диметиловий ефір (диглим); кетони, такі, як ацетон або бутанон; аміди, такі, як ацетамід, диметилацетамід або диметилформамід (DMF); нітрили, такі, як ацетонітрил; ефіри, такі, як етилацетат і, якщо це бажано, також суміші зазначених розчинників 9 75892 10 один з одним або їх суміші з водою. Винахід, крім того, відноситься до застосуванЧас реакції в енантіоселективній гідрогенізації ня сполук формули І у якості проміжних сполук для складає від декількох хвилин до 14 днів, в залежсинтезу медичних препаратів. Відповідні медичні ності від використовуваних умов, а температуру препарати, які переважно роблять вплив на реакції вибирають з інтервалу між 0 і 150°, звичайцентральну нервову систему, описані, наприклад, но між 20 і 130°. в EР 0707007. Відношення каталізатор/носій звичайно знахоОтже, винахід відноситься, зокрема, до спосодиться в діапазоні від 1:100000 до 1:10, особливо бу застосування сполук формули І по пункту І у переважно від 1:10000 до 1:100. У цих випадках синтезі (R)-2-[5-(4-фторфеніл)-3час реакції складає, наприклад, від 3 до 20 годин. піридилметиламінометил]хроману і його солей, Гідрогенізацію проводять при тиску водню 1-200 який відрізняється тим, що бар, переважно при 3-100 бар. а) за допомогою нерацемічного хірального каВидалення радикала R6 без рацемізації, якщо талізатора проводять гідрогенізацію сполуки форR6 представляє собою ацил, здійснюють, напримули II клад, із використанням NaOH або КОН в воді, сумішах вода/діоксан або з використанням водного розчину соляної кислоти при температурах між 0 і 100°. Вивільнення сполук формули І із їх функціональних похідних, тобто видалення радикала R6, коли R6 являє собою амінозахисну групу, здійснюють за методиками, які описані в літературі для відповідних захисних груп [наприклад, T.W. Greene, R.G.M. Wuts, Protective Groups in Organic у якій R1, R2, R3 і R4 означають Н, a R6 відповіChemistry, 2nd Edn., Wiley, New York, 1991 або P.J. дає визначенню, приведеному в пункті 4, щоб одеKocienski, Protecting Groups, 1st Edn., Georg ржати сполуку формули III Thieme Verlag, Stuttgart - New-York, 1994]. Крім того, можна використовувати їх варіанти, що самі по собі відомі, але тут докладніше не згадані. Основу формули І можна перетворити в асоційовану сіль із кислотним залишком, наприклад, в реакції еквівалентних кількостей основи і кислоти в інертному розчиннику, такому, як етанол, із наступним випарюванням. Придатними кислотами для цієї реакції є, зокрема, такі, що дають фізіологічно прийнятні солі. Отже, можливо використовувати в якій радикали R1-R6 відповідають приведенеорганічні кислоти, наприклад, сірчану кислоту, ним вище значенням. азотну кислоту, гідрогалогенідні кислоти, такі, як тим, що соляна кислота або бромистоводнева кислота, b) енантіомерично чисту (R)-сполуку формули фосфорні кислоти, такі, як ортофосфорна кислота, lllа або сульфамінова кислота, крім того, органічні кислоти, особливо аліфатичні, аліциклічні, араліфатичні, ароматичні або гетероциклічні моноосновні або поліосновні карбонові, сульфонові або сірчані кислоти, наприклад, мурашину кислоту, оцтову кислоту, пропіонову кислоту, триметилоцтову кислоту, діетилоцтову кислоту, малонову кислоту, бурштинову кислоту, пімелинову кислоту, фумарову кислоту, малеїнову кислоту, молочну кислоту, винну кислоту, яблучну кислоту, лимонну одержують кристалізацією з отриманої енантікислоту, глюконову кислоту, аскорбінову кислоту, омерично збагаченої суміші (R)- і (S)- сполук форнікотинову кислоту, ізонікотинову кислоту, метанмули III, у якій R1-R6 відповідають приведеним виабо етансульфонову кислоту, етандисульфонову ще значенням, кислоту, 2-гідроксиетансульфонову кислоту, бентим, що золсульфонову кислоту, р-толуолсульфонову кисс) радикал R6 видаляють з отриманої (R)лоту, нафталінмоно- і -дисульфонові кислоти, і сполуки формули lllа, у котрої R1-R6 відповідає лаурилсульфонову кислоту. Солі з фізіологічно приведеним вище значенням, щоб одержати енаннеприйнятними кислотами, наприклад, пікрати, тіомерично чисту (R)-сполуку формули І можна використовувати для виділення і/або очищення сполук формули І. З іншого боку, сполуки формули І можна перетворювати у відповідні солі металів, зокрема - у солі лужних або лужноземельних металів, або у відповідні солі амонію, за допомогою основ (наприклад, гідроксиду натрію, гідроксиду калію, карбонату натрію або карбонату калію). 11 75892 12 в якій R1, R2, R3 і R4 означають Н, або сіль цієї ілметил)ацетамід І, карбонільну групу гідрогенізусполуки, ють до гідроксильної групи з використанням кататим, що d) енантіомерично чисту (R)-сполуку лізатора із благородного металу, наприклад, із формули І, у якій R1-R4 означають Н, відновлюють використанням Pd на вугіллі (вологість 50%), щоб за звичайною методикою, щоб одержати (R)одержати сполуку N-(4-гідроксихроман-2амінометилхроман, ілметил)ацетамід 2. Ацетилову групу відщеплюють тому, що e) отриманий (R)-xpoмaн-2-ілметил за допомогою основи, наприклад, гідроксиду на)амін перетворюють у його сіль із кислотним затрію. Додавання кислоти призводить до одержанлишком, а останню перетворюють за відомою меня солі з кислотним залишком 3 2тодикою в (R)-2-[5-(4-фторфеніл)-3амінометилхроман-4-олу. Подальша гідрогенізація піридилметиламінометил]-хроман і можливо - у з використанням каталізатора з благородного мейого сіль із кислотним залишком, крім того, можна талу дозволяє одержати сіль із кислотним залишздійснювати виділення (R)-енантіомеру з енантіоком 4 2-амінометилхроману. мерично збагаченої [R,S]-суміші кристалізацією Реакція енантіомерично чистих сполук, тобто після етапу с) або після етапу d). реакція (R)-N-(-4-оксохроман-2-ілметил)ацетаміду, Винахід відноситься, крім того, до застосуваніз воднем при каталізаторі з благородного металу ня сполук формули І у якості проміжних сполук для дає (R)-N-(4-гідроксихроман-2-ілметил)ацетамід. синтезу медичних препаратів, що впливають на Наступне видалення ацетилової групи дає (R)-2центральну нервову систему. амінометилхроман-4-ол і, у залежності від обробКарбонільну групу сполук формули І за даним ки, його солі. Відновлення у присутності каталізавинаходом можна відновлювати для одержання тора із благородного металу дає (R)-2відповідних похідних хроманону формули І реакціамінометилхроман, і, в залежності від обробки, єю відновлення Wolff-Kishner [наприклад, його солі. Аналогічними проміжними сполуками в Paradkar, Μ. V. і ін. у J. Chem. Res., Synop. 1998, 6, реакції (S)-N-(4-оксохроман-2-ілметил)ацетаміду є 318-319] при стандартних реакційних умовах або (S)-N-(4-гідроксихроман-2-ілметил)-ацетамід і (S)гідрогенізацією із використанням каталізатора з 2-амінометилхроман-4-ол. благородного металу [наприклад, R.M. Rylander, Крім того, винахід відноситься до сполук Hydrogenation Methods, Best Synthetic Methods, а) N-(4-гідроксихроман-2-ілметил)ацетамід, Academic Press, 1985] при стандартних реакційних b) 2-амінометилхроман-4-ол, умовах. c) (R)-N-(4-гідроксихроман-2-ілметил)ацетамід, (R)-(хроман-2-ілметил)амін, синтезований із d) (R)-2-амінометилхроман-4-ол, сполуки формули І за даним винаходом, у якому e) (S)-N-(4-гідроксихроман-2-ілметил)ацетамід 1 4 R -R означають Н, в реакції відновлення Wolffі Kishner або гідрогенізацією з використанням, катаf) (S)-2-амінометилхроман-4-ол. лізатора з благородного металу, перетворюють у Винахід відноситься, крім того, до застосуванйого сіль із кислотним залишком за описаною виня описаних вище сполук від ) а) до f) в синтезі (R)ще методикою, а цю сіль можна за відомою мето2-[5-(4-фторфеніл)-3-піридилметиламінометил] дикою перетворити в (R)-2-[5-(4-фторфеніл)-3хроману та його солей. піридил-метиламінометил]хроман [літ.: ЕР Крім того, можна одержувати (R/S)-20707007]. амінометилхроман і його солі в енантіомерично Аналогічним чином, (Хроман-2-ілметил)амін чистому вигляді або у вигляді рацемата, безпосеможна одержувати із сполуки формули III, у якій редньо в одній реакційній судині, із N-(4R1-R4 означають Н, відповідно до послідовності оксохроман-2-ілметил)ацетаміду, за допомогою реакцій 1: відщеплення аміду з наступним відновленням. Послідовність реакцій 1: Вище і нижче всі температури зазначені в С°. У представлених нижче прикладах, термін "звичайна обробка" означає, що, при необхідності, додають воду, якщо буде потрібно, та доводять рН до значень від 2 до 10, у залежності від складу кінцевого продукту, суміш екстрагують етилацетатом або дихлорметаном, розділяють фази, органічну фазу висушують над сульфатом натрію і випарюють, а продукт очищають хроматографією на силікагелі і/або кристалізацією. Значення Rf дані на силікагелі. Приклад 1: (1) 35,1г N-(4-оксохромeн-2-ілметил)ацетаміду суспендували у 90мл толуолу, і в інертних умовах додали 1,6мл 10 мілімолярного розчину, що складає з [Rh((S)-ToIBINAP)(COD)Cl] у толуолі. Цю суспензію гідрогенізували в автоклаві при тиску водню 100 бар і температурі 100°С. Через 12 годин одержали енантіомерично чистий (>99% її) (R)-N-(4-оксохроман-ілметил)ацетамід шляхом його кристалізації в результаті охолодження до кімнатної температури. Потім висушування одерПочинаючи від сполуки N-(4-оксохроман-2 13 75892 14 жали 31,04г (R)-N-(4-оксохроман-2гідрогенізацію протягом 15 годин при 70°С і тиску ілметил)ацетаміду. водню 3 бар в присутності 2г 5% Pd/вугілля (воло2) 3,7г гідроксиду натрію розчинили в 80мол гість 50%). Теплий гідрогенізований розчин відфіводи. Після додавання 10,13г (R)-N-(4-оксохроманльтрували, і при -10°С кристалізували сполуку (R)2-шметил)ацетамiду, суміш дефлегмували протяN-(4-гідроксихроман-2-ілметил)ацетаміду. Висугом 20 годин. Після охолодження, водяну фазу шування дало 19г (R)-N-(4-гідроксихроман-2тричі екстрагували ефіром МТВ (метил третілметил)ацетаміду. бутиловий ефір), і зробили відгін розчинника при (2) 18,99г (R)-N-(4-гідроксихроман-2зниженому тиску. Осад помістили у 50мл етанолу і ілметил)ацетаміду і 7,5г гідроксиду натрію витридодали 4,7мл 37% НСl. Випавший осад (R)-2мували при температурі дефлегмації протягом 15 амінометилхроман-4-ону гідрохлориду відфільтругодин у 150мл води. Потім продукт екстрагували вали і висушили. Вихід 9,55г. ефіром МТВ, розчин випарили й осад помістили в Приклад 2: 80мл етанолу. Після додавання 10мл 37% НСІ, Одержання (R)-2-амінометилхроману з (R)-2гідрохлорид (R)-2-амінометилхроман-4-олу випав амінометил-хроман-4-ону гідрохлориду для настув осад. Висушування забезпечує вихід 19,26г. пного синтезу (R)-2-[5-(4-фторфеніл)-3(3) 19,2г (R)-2-амінометилхроман-4-олу гідрохпіридилметиламінометил]хроману і його солей лориду розчинили в 300мл метанолу, і гідрогенізуздійснювали за методикою, описаною в ЕР вали при 50°С і 7 бар в присутності 2г 5% 0707007: Pd/вугілля (вологість 50%). Після фільтрації і ви9,55г (R)-2-амінометилхроман-4-ону гідрохлопарювання фільтрату, кристалізується (R)-2риду гідрогенізували при 50°С і тиску водню 7 бар амінометилхроман (вихід 15,5г). а присутності 950мг 5% Pd/вугілля (вологість 50%) Приклад 4: в 100мл метанолу, щоб одержати (R)-2Синтез в одному реакторі для одержання (R)амінометилхроман. Гарячий відфільтрований роз2-амінометилхроману з N-(4-оксохроман-2чин випарили до 50мл і охолодили, продукт (R)-2ілметил)ацетаміду для наступного синтезу (R)-2амінометилхроман, що випав в осад, відфільтру[5-(4-фторфеніл)-3вали і висушили (вихід: 8,04г). піридилметиламінометил]хроману і його солей Приклад 3: здійснювали за методикою, описаною в ЕР Альтернативний синтез для одержання (R)-20707007: амінометилхроману з N-(4-оксохроман-2100мл 5,8Μ НСІ додали до 7,85г N-(4ілметил)ацетаміду для наступного синтезу (R)-2оксохроман-2-ілметил)ацетаміду і 1,0г 5% [5-(4-фторфеніл)-3Pd/вугілля (вологість 50%), і суміш витримували в піридилметиламінометил]хроману і його солей автоклаві при температурі 110°С на протязі 24 здійснювали за методикою, описаною в ЕР годин. Потім суміш остудили до 50°С, і інжектува0707007: ли водень до 3 бар. Гідрогенізація була завершена (1) 20,9г N-(4-оксохроман-2-ілметил)ацетаміду через 16 годин, і, після фільтрації і кристалізації, розчинили в 70мл толуолу при 70°С і проводили виділили 4,1г (R)-2-амінометилхроману. Комп’ютерна верстка О. Гапоненко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюChromanone derivatives and a method for the preparation thereof
Назва патенту російськоюПроизводные хроманона и способ их получения
МПК / Мітки
МПК: C07D 311/22, C07C 209/10
Мітки: одержання, спосіб, хроманону, похідні
Код посилання
<a href="https://ua.patents.su/7-75892-pokhidni-khromanonu-ta-sposib-kh-oderzhannya.html" target="_blank" rel="follow" title="База патентів України">Похідні хроманону та спосіб їх одержання</a>
Попередній патент: Футляр дихального апарата
Наступний патент: Спосіб очищення грунту від радіонуклідів
Випадковий патент: Біопрепарат для рослинництва











