Спосіб отримання похідних (((2-r-1,3-тіазол-4-іл)метил)сульфаніл)-азолів
Номер патенту: 79385
Опубліковано: 25.04.2013
Автори: Цапко Магдаліна Дмитрівна, Коваленко Наталія Володимирівна, Воловенко Юліан Михайлович
Формула / Реферат
Спосіб отримання сполуки формули (І) або її фармацевтично прийнятної солі
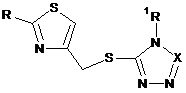 , (I)
, (I)
де 1R - СН3 або феніл, X - С або N,
R є феніл, ціанометильна група або група
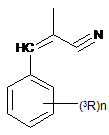 ,
,
де 3R є водень, OR4;
N(R4)2;
де R4 є водень або С1-С6алкіл; n=0-2,
за яким сполуку формули VI алкілують сполукою формули V або VII в органічному розчиннику,
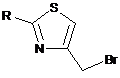
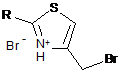
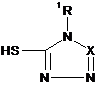
(V)
(VII)
(VI)
де 1R - СН3 або феніл, X - С або N,
R є феніл, ціанометильна група або група
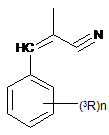 ,
,
де 3R є водень, OR4;
N(R4)2;
де R4 є водень або С1-С6алкіл; n=0-2.
Текст
Реферат: Спосіб отримання сполуки формули (І) або її фармацевтично прийнятної солі, S R 1 R N N S X N N , (I) де R - СН3 або феніл, X - С або N. R є феніл, ціанометильна група або група 1 HC N (3R)n , 3 4 де R є водень, OR ; 4 N(R )2; 4 де R є водень або С1-С6алкіл; n=0-2. UA 79385 U (54) СПОСІБ ОТРИМАННЯ ПОХІДНИХ (((2-R-1,3-ТІАЗОЛ-4-ІЛ)МЕТИЛ)СУЛЬФАНІЛ)-АЗОЛІВ UA 79385 U UA 79385 U Корисна модель належить до галузі органічної хімії, зокрема хімії гетероциклічних сполук, а саме способу отримання похідних (((2-R-1,3-тіазол-4-іл)метил)сульфаніл)-азолів (І). S R 1 R N N S X N N , (I) де R-CH3 або феніл, X - С або N. R є феніл, ціанометильна група або група 1 5 N HC (3R)n 10 15 20 , 3 4 де R є водень, OR ; 4 N(R )2; 4 де R є водень або С1-С6алкіл; n=0-2. Тіазольне кільце зустрічається в сполуках, розповсюджених у природі, які стоять в перших рядах важливості для живих систем, наприклад вітамін В1 і пеніцилін. Похідними тіазолу є аналітичний засіб аміфеназол, феноклозинова кислота, яка є активним антиперетиком з анальгітичними характеристиками; препарат клометіазол має седативну, гіпнотичну і антиконвульсативні дії, а також лікарські препарати фамотидин, цефалоспорин та інші. Різноманітні області біологічних активностей стимулюють підвищений інтерес до розробки нових сполук цієї структури. В літературі [1] описано близький спосіб, за яким сполуку IV одержано взаємодією гідроброміду 4-(хлорметил)-2-метил-1,3-тіазолу II з метил 4-(2-аміно-3,5-діциано-6-сульфаніл-4піридил)фенілкарбоматом III в диметилформаміді у присутності натрію гідрогенкарбомату. Недоліком цього способу є: 1) низький вихід цільового продукту реакції, а саме 36 %; S NH2 S N NH Cl + N HS N N N H 25 N S N N (II) NH2 O N H O (III) O O (IV) В основу корисної моделі поставлена задача створення простого способу отримання похідних (((2-R-1,3-тіазол-4-іл)метил)сульфаніл)-азолів (І) з більш високим виходом, які можуть мати фізіологічну активність, і можуть бути застосовані в медицині. Поставлена задача вирішується при здійсненні способу отримання похідних (((2-R-1,3тіазол-4-іл)метил)сульфаніл)-азолів (І) взаємодією похідних 4-бромометил-1,3-тіазолу [2-4] формули V (схема І) або гідробромідів похідних 4-бромометил-1,3-тіазолу [2-4] формули VII (схема II), 30 1 UA 79385 U Схема І 1 S R N + N R HS Br N S R X 1 N N S N R X N (V) (VI) N I(a-j) Схема II 5 1 S R Br S R N+ H 1 + N Br (VII) R R N HS Br N (V) S R X N 1 (VI) N S N R N X N I(a-j) 1 де R-CH3 або феніл, X - С або N. R є феніл, ціанометильна група або група, HC N (3R)n 10 15 20 25 30 35 , 3 4 де R є водень, OR ; 4 N(R )2; 4 де R є водень або С1-С6 алкіл; n=0-2. Одержані продукти мають достатню чистоту для подальшого використання. Корисна модель підтверджується наступними прикладами. Синтез 4-метил-3-(((2-феніл-1,3-тіазол-4-іл)метил)сульфаніл)-1H-1,2,4-триазол-1-ум броміду (Іа). Приклад 1 До 0,001 моль гідроброміду 4-бромометил-2-феніл-1,3-тіазолу формули (VIIa) додають 0,001 1 моль 4-метил-1,2,4-триазол-2-тіолу формули (VI), де R - СН3, X - С у 15 мл ацетонітрилу, додають 0,002 моль основи, розчиняють і залишають до повного виділення продукту реакції. Після охолодження осад фільтрують, промивають 1 мл ацетонітрилу і 20-30 мл води. Осад екстрагують органічним розчинником (3×25 мл). Органічну фазу відокремлюють, залишать над осушником (СаСl2) - і пропускають через тонкий шар силікагелю, до розчинника додають надлишок бромоводневої кислоти. Осад, що утворився відфільтровують. В результаті 1 виділяють 3,2 г (86 %), сполуки (Іа). Спектр ЯМР Н (ДМСО-d6), δ, м. д.: 10,13 с (1Н, СНтриазолу), 7,87 д (2Н, J 8,0 Гц, орто-протони фенілу); 7,68 с (1Н, СН-тіазолу), 7,46 м (3Н, метата пара-протони фенілу); 4,70 с (2Н, СН2), 3,84 с (3Н, СН3). Знайдено, %: С 42,26; Н 3,49; Вr 21,59; N 15,14; S 17,32. С13Н13ВrN4S2. Вирахувано, %: С 42,286; Н 3,55; Вr 21,64; N 15,17; S 17,37. Приклад 2 До 0,001 моль 0,001 моль 4-бромометил-2-феніл-1,3-тіазолу формули (Va) додають 0,001 моль 4-метил-1,2,4-триазол-2-тіолу формули (VI) де R - СН3, X - С у 15 мл ацетонітрилу, додають 0,001 моль основи, розчиняють і залишають до повного виділення продукту реакції. Після охолодження осад фільтрують, промивають 1 мл ацетонітрилу і 20-30 мл води. Осад екстрагують (3×25 мл). Органічну фазу відокремлюють, залишають над осушником (СаСl2) - і пропускають через тонкий шар силікагелю, до розчинника додають надлишок бромоводневої кислоти. Осад, що утворився, відфільтровують. В результаті виділяють 3,2 г (86 %), сполуки (Іа). 2 UA 79385 U 1 5 10 15 20 25 30 35 40 45 50 Спектр ЯМР Н (ДМСО-d6), δ, м. д.: 10,13 с (1H, СН-триазолу), 7,87 д (2Н, J 8.0 Гц, СН-фенілу); 7,67 с (1Н, СН-тіазолу), 7,32 м (3Н, -фенілу); 4,70 с (2Н, СH2), 3,84 с (3Н, СH3). Знайдено, %: С 42,26; Н 3,49; Вr 21,59; N 15,14; S 17,32. C13H13BrN4S2. Вирахувано, %: С 42,286; Н 3,55; Вr 21,64; N 15,17; S 17,37. Синтез 2-(4-(((4-феніл-4H-1,2,4-триазол-3-іл)сульфаніл)метил)-1,3-тіазол-2-іл)ацетонітрил (Іb). До 0,001 моль гідроброміду 4-бромометил-2-ціанометил-1,3-тіазолу формули (VIIb) додають 1 0,001 моль 4-феніл-1,2,4-триазол-2-тіолу формули (VI), де R - феніл, X - С у 15 мл ацетонітрилу додають 0,002 моль основи, розчиняють і залишають до повного виділення продукту реакції. Після охолодження осад фільтрують, промивають 1 мл ацетонітрилу і 20-30 мл води. Осад екстрагують (3×25 мл) бензену або (3×40 мл) хлороформу. Органічну фазу відокремлюють, залишають над осушником (СаСl2) - і пропускають через тонкий шар силікагелю, розчинник упарюють. В результаті виділяють 3,1 г (92 %), сполуки (Іb). Спектр ЯМР 1 Н (ДМСО-d6), δ, м.д.: 8,63 с (1H, СН-триазолу), 7,52-7,46 м (4Н, мета + пара-протони фенілу, С1 тіазолу); 7,40-7,38 м (2Н, орто-протони фенілу), 4,48 с (2Н, S-СH2); (), 4,34 с (2Н, CN-СH2). Знайдено, %: С 53,68; Н 3,59; N 22,39; S 20,48. С14Н11N5S2. Вирахувано, %: С 53,65; Н 3,54; N 22,35; S 20,46. Синтез 2-(4-(((1-феніл-4H-1,2,3,4-тетразол-5-іл)сульфаніл)метил1)-1,3-тіазол-2іл)ацетонітрилу (Іс). До 0,001 моль гідроброміду 4-бромометил-2-ціанометил-1,3-тіазолу формули (VIIb) додають 1 0,001 моль 4-феніл-1,2,3,4-тетразол-2-тіолу формули (VI), де R - феніл, X-N у 15 мл ацетонітрилу додають 0,002 моль основи, розчиняють і залишають до повного виділення продукту реакції. Після охолодження осад фільтрують, промивають 1 мл ацетонітрилу і 20-30 мл води. Осад екстрагують (3×25 мл) бензену або (3×40 мл) хлороформу. Органічну фазу відокремлюють, залишать над осушником (СаСl2) - і пропускають через тонкий шар силікагелю, 1 розчинник упарюють. В результаті виділяють 2,8 г (90 %), сполуки (Іс). Спектр ЯМР Н (ДМСОd6), δ, м.д.: 7,58 с (6Н, 5Н-фенілу і 1Н-тіазолу), 4,70 с (2Н, S-CH2); 4,37 с (2Н, CN- СH2). Знайдено, %: С 49,81; Н 3,29; N 26,85; S 20,61. С13Н10N6S2. Вирахувано, %: С 49,66; Н 3,21; N 26,73; S 20,40. Синтез 2-феніл-4-(((1-феніл-1H-1,2,3,4-тетразол-5-іл)сульфаніл)метил)-1,3-тіазол-3-іум броміду (Id). 1 Реакцію проводять по методу Іа. Вихід 3,5 г (81 %). Спектр ЯМР Н (ДМСО-d6), δ, м. д.: 7,88 с (2Н, орто-протони фенілу), 7,61 с (1H, тіазолу), 7,58 с (5Н, фенілу), 7.42 с (3Н, мета- та парапротони фенілу), 4,75 с (2Н, СH2). Знайдено, %: С 49,81; Н 3,29; N 26,85; S 20,61. C13H10N6S2. Вирахувано, %: С 49,66; Н 3,21; N 26,73; S 20,40. Синтез 3-(4-гідрокси-3-метоксифеніл)-2-(4-(((1-феніл-1H-1,2,3,4-тетразол-5-іл) сульфаніл)метил)-1,3-тіазол-2-іл)ацетонітрил (Іе). 1 Реакцію проводять по методу Іb. Вихід 3,5 г (81 %). Спектр ЯМР Н (ДМСО-d6), δ, м. д.: 9,96 уш. с. (1Н-ОН), 7,96 с (1Н, CH-C-CN), 7,66 с (2Н, СН 4-гідрокси-3-метоксифенілу та 1Н-тіазолу), 7,60 с (5Н, 5Н-фенілу), 7,42 д (1Н, J 8,0 Гц, орто-протон 4-гідрокси-3-метоксифенілу), 6,89 д (1Н, J 8,0 Гц мета-протон 4-гідрокси-3-метоксифенілу), 4,72 с (2Н, СH2), 3,87 с (3Н, СH2). Знайдено, %: %: С 56,34; Н 3,69; N 18,85; S 14,48. C21H16N6O2S2. Вирахувано, %: С 56,23; Н 3,60; N 18,74; S 14,30. Комп'ютерне моделювання за програмою PASS показало потенційну активність сполук, що заявляються такими, що можуть мати антибактеріальну дію, а саме проти Helicobacter, та інші біологічні властивості, наприклад, проти подразнення шкіри. У таблиці представлена потенційна біоактивність заявлених похідних тіазолу з показниками активності. Таким чином, одержано сполуки ряду похідних (((2-R-1,3-тіазол-4-іл)метил)сульфаніл)азолів формули (І), які, згідно розрахунку за програмою PASS, можуть мати широкий спектр направленостей фізіологічної активності. Потенційна можливість використання заявлених сполук дозволить розширити асортимент речовин, які можуть бути застосовані в медицині. 3 UA 79385 U Таблиця Сполука 4-метил-3-(((2-феніл-1,3-тіазол-4іл)метил)сульфаніл)-1H-1,2,4-триазол-1-ум бромід (Іа). 2-(4-(((4-феніл-4H-1,2,4-триазол-3іл)сульфаніл)метил)-1,3-тіазол-2-іл)ацетонітрил (Іb). 2-(4-(((1-феніл-4H-1,2,3,4-тетразол-5іл)сульфаніл)метил)-1,3-тіазол-2-іл)ацетонітрил (Іс). Потенційна активність властивості Helicobacter pylori Anti властивості AntiHelicobacter проти подразнення шкіри pylori проти подразнення шкіри властивості AntiHelicobacter pylori проти подразнення шкіри 2-феніл-4-(((1-феніл-1H-1,2,3,4-тетразол-5властивості Antiіл)сульфаніл)метил)-1,3-тіазол-3-іум бромід (Id). Helicobacter pylori 3-(4-гідрокси-3-метоксифеніл)-2-(4-(((1-феніл-1H- проти подразнення 1,2,3,4-тетразол-5-іл)сульфаніл)метил)-1,3-тіазол- властивості Anti2-іл)ацетонітрил (Іе). Helicobacter шкіри pylori 3-(4-диметиламіно)феніл)-2-(4-(((1-феніл-1Hпроти подразнення шкіри 1,2,3,4-тетразол-5-іл) сульфаніл)метил)-1,3властивості Antiтіазол-2-іл)ацетонітрил (If). Helicobacter pylori 6-нітро-2-(((2-амін-1,3-тіазол-4властивості Antiіл)метил)сульфаніл)-1H-бензімідазолу (Ih). Helicobacter pylori Pa* Pi* 0,620 0,004 0,620 0,004 0,291 0,106 0,941 0,004 0,620 0,004 0,966 0,554 0.205 0,667 0,003 0,028 0,093 0,013 0,172 0,158 0,737 0,010 0,375 0,014 0,487 0,006 Pa* показник активності Рі* показник неактивності Джерело інформації 1. ЕР 1 417 173 В1 5 ФОРМУЛА КОРИСНОЇ МОДЕЛІ Спосіб отримання сполуки формули (І) або її фармацевтично прийнятної солі S R 1 N N S X N 10 R N , (I) де R - СН3 або феніл, X - С або N, R є феніл, ціанометильна група або група 1 HC N (3R)n 15 , 3 4 де R є водень, OR ; 4 N(R )2; 4 де R є водень або С1-С6алкіл; n=0-2, за яким сполуку формули VI алкілують сполукою формули V або VII в органічному розчиннику, 4 UA 79385 U S R R Br N Br 1 S - N+ H N HCHS Br , , (V) 1 де R - СН3 або феніл, X - С або N, R є феніл, ціанометильна група або група R (VII) N (VI) N (3R)n 5 , 3 4 де R є водень, OR ; 4 N(R )2; 4 де R є водень або С1-С6алкіл; n=0-2. Комп’ютерна верстка І. Мироненко Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 5 X N,
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of (((2-r-1,3-thiazole-4-yl)methyl)sulfanyl)-azole derivatives
Автори англійськоюKovalenko Natalia Volodymyrivna, Volovenko Yulian Mykhailovych, Tsapko Mahdalyna Dmytrivna
Назва патенту російськоюСпособ получения производных (((2-r-1,3-тиазол- 4-ил)метил)сульфанил)-азолов
Автори російськоюКоваленко Наталия Владимировна, Воловенко Юлиан Михайлович, Цапко Магдалина Дмитриевна
МПК / Мітки
МПК: C07D 277/22
Мітки: отримання, похідних, 2-r-1,3-тіазол-4-іл)метил)сульфаніл)-азолів, спосіб
Код посилання
<a href="https://ua.patents.su/7-79385-sposib-otrimannya-pokhidnikh-2-r-13-tiazol-4-ilmetilsulfanil-azoliv.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання похідних (((2-r-1,3-тіазол-4-іл)метил)сульфаніл)-азолів</a>
Попередній патент: Спосіб переобладнання колісного трактора у землерийно-навантажувальну машину
Наступний патент: Спосіб отримання похідних 2-(((5-1r-2-r-1,3-тіазол-4-іл)метил)сульфаніл)-1,3-бензімідазолу-2r
Випадковий патент: Спосіб обробки привибійної зони пласта











