Аерозольна композиція, що містить b2-адренергічний агоніст тривалої дії, дозуючий інгалятор під тиском та спосіб його заповнення
Номер патенту: 73986
Опубліковано: 17.10.2005
Автори: Льюіс Дейвід, андертон Дейвід, Ферраріс Алессандра, Брамбілла Гаетано, Мікін Брайан
Формула / Реферат
1. Аерозольна композиція, що містить як активний інгредієнт β2-адренергічний агоніст тривалої дії, що належить до класу фенілалкіламінопохідних, вибраних з сальбутамолу, формотеролу, сальметеролу, ТА-2005 та їхніх солей, у розчині зрідженого газу-витиснювача гідрофлуоралканового (HFA) ряду, співрозчинник, вибраний з фармацевтично прийнятних спиртів, причому відносний рівень рH-розчину встановлено в межах 2,5 і 5,0 додаванням малих кількостей мінеральної кислоти.
2. Композиція за п. 1, в якій мінеральну кислоту вибрано з хлороводневої, нітратної або фосфорної кислот.
3. Композиція за п. 1, в якій газ-витиснювач містить один чи більше гідрофлуоралканів, вибраних з групи, що складається з HFA134а і HFA 227.
4. Композиція за будь-яким з пп. 1-3, в якій співрозчинником є етанол.
5. Композиція за будь-яким з пп. 1-4, в якій розчин містить малолеткий компонент з тиском пари при 25 °С не більше 0,1 кПа, переважно не більше 0,05 кПа.
6. Композиція за будь-яким з попередніх пунктів, де розчин містить щонайменше 0,2 мас.%, але не більше 10 мас.% малолеткого компонента.
7. Композиція за будь-яким з попередніх пунктів, в якій малолеткий компонент вибрано з гліколю або естеру.
8. Композиція за п. 7, в якій малолетким компонентом є ізопропілміристат.
9. Композиція за будь-яким з попередніх пунктів, в якій активний інгредієнт містить β2-агоніст, вибраний з сальбутамолу, формотеролу, сальметеролу, ТА-2005 та їх солей у комбінації з стероїдом, вибраним з беклометазону дипропіонату, флутиказону пропіонату, будезоніду та його 22R-епімеру.
10. Композиція за будь-яким з попередніх пунктів, в якій активним інгредієнтом є формотерол, а рН-розчину встановлюють в межах від 3,0 до 3,5.
11. Дозуючий інгалятор під тиском для введення аерозолю, який має контейнер, частина або всі внутрішні металеві поверхні якого виконано із неіржавіючої сталі, анодованого алюмінію чи вкриті інертним органічним покриттям, і містить композицію за будь-яким з пп. 1-10.
12. Спосіб заповнення інгалятора за п. 11, який полягає в тому, що
а) готують розчин одного або більше ніж одного активного інгредієнта в одному або більше ніж одному співрозчиннику, що містить як варіант прийнятну кількість малолеткого компонента;
б) заповнюють пристрій зазначеним розчином;
в) додають мінеральну кислоту у такій кількості, що в кінці заповнення рН-розчину було встановлено в межах 2,5-5,0;
г) додають газ-витиснювач, який містить гідрофлуоралкан;
д) обтискають клапани і перевіряють на герметичність.
Текст
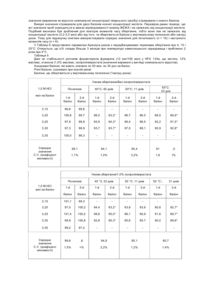
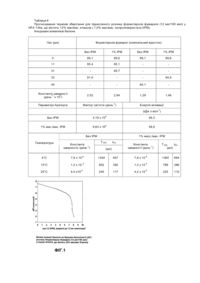
Винахід стосується стабільного фармацевтичного розчину для застосування в дозованих інгаляторах під тиском (ДІ), який підходить для аерозольного введення. Зокрема, винахід стосується розчину для застосування в дозованих інгаляторах під тиском (ДІ), який підходить для аерозольного введення, який містить р2-агоністи і який стабільний при кімнатній температурі протягом фармацевтично прийнятного терміну зберігання. Дозовані інгалятори під тиском є добре відомими пристроями для введення фармацевтичних продуктів у дихальні шляхи за допомогою інгаляції. Лікарські засоби, які звичайно доставляються за допомогою інгаляції, включають бронходілятатори, такі як р2-агоністи та антихолінергічні агенти, кортикостероїди, антилейкотріени, антиалергічні агенти та інші речовини, які можуть ефективно вводитися за допомогою інгаляції, у такий спосіб збільшуючи терапевтичний індекс і знижуючи побічні ефекти активної речовини. ДІ використовує пропелент, щоб виштовхнути краплі, що містять фармацевтичний продукт, у дихальні шляхи у виді аерозолю. Препарати для аерозольного введення за допомогою ДІ можуть бути розчинами або суспензіями. Препарати у виді розчинів дають перевагу, тому що є гомогенними, з активним інгредієнтом та ексципіентами цілком розчиненими в носії пропеленті або його суміші з придатними співрозчинниками, такими як етанол. Препарати у виді розчинів також усувають проблеми фізичної стабільності, пов'язані з препаратами у виді суспензій, у . такий спосіб забезпечуючи введення більш сумісних однорідних доз. Протягом багатьох років бажаними пропелентами^ які використовують в аерозолях для фармацевтичного застосування, є група хлорфторвуглеводів, які звичайно називають фреонами або CFCs, таких як CCI 3F (фреон 11 або CFC-11), CCI 2F2 (фреон 12 або CFC-12) та CCIF2-CCIF2 (фреон 114 або CFC-114). Останнім часом хлорфторвуглеродні пропеленти (CFC), такі як фреон 11 і фреон 12, пов'язують з руйнуванням озонового шару, і їхнє виробництво поступове припиняється. Гірофторалкани [(HFAs), відомі також як гідрофторвуглероди (HFCs)] не містять хлор і вважаються менш пагубними для озону, та їх пропонують як замінники CFCs. Було визнано, що HFAs і, зокрема, 1,1,1,2-тетрафторетан (HFA 134а) і 1,1,1,2,3,3,3-гептафторпропан (HFA 227), є кращими варіантами для пропелентів, які не містять CFC, і описаний ряд медичних аерозольних препаратів, що використовують такі · HFA пропелентні системи. Завдяки більш високій полярності HFA пропелентів, зокрема, HFA 134а (діелектрична постійна D>9,5) стосовно CFC носіїв (D0,95). У відносно апротоних розчинниках, таких як носії HFA-етанол, які використовують у цих дослідженнях, протони негідратовани; їхні коефіцієнти активності значно відрізняються від коефіцієнтів активності у водних розчинах. Хоча рівняння Нернста застосовне стосовно едс (електрорушійна сила), і система скляних електродів рНметру буде генерувати перемінний вихідний сигнал у мілівольтах відповідно до протонної концентрації і полярністю носія, показання рН-метра не представляють дійсного значення рН. Показаннями приладу є уявний рН або функція кислотності (РН')· При титруванні активного інгредієнта сильною кислотою в модельній системі носіїв, що випускається серійно (HFA43-10MEE, Vertel XF, Dupont) профіль рН’ виявляє невелике відхилення до приблизно рН' = 5,5; відповідно, функція кислотності різко знижується. Несподівано відповідні HFA препарати виявилися набагато більш стабільними при рН' нижче 5,5. З іншого боку, застосування інертних контейнерів дозволяє уникнути вимивання іонів металів або лугу як наслідок дії кислоти, яка міститься в препараті, на внутрішні стінки балонів. Іони металів, такі як АІ 3+, або луг, які відповідно витягаються шляхом заміщення зі стандартних алюмінієвих або скляних балонів, можуть, у свою чергу, каталізувати радикальні окисні або інші хімічні реакції активних інгредієнтів, які призводять до утворення продуктів деструкції. Відповідно до особливого втілення винаходу також запропонована фармацевтична композиція, що додатково містить низьколетючий компонент, таким чином, крім збільшення масового серединного аеродинамічного діаметра (MMAD) часток аерозолю при натисканні на інгалятор, як пояснюється надалі, додатково підвищувальна стабільність препарату. Фактично, додавання низьколетючого компонента зі зниженою полярністю стосовно співрозчинника, такого як складний ефір, дозволяє або скоротити кількість кислоти, що додають для регулювання рН, або зменшити полярність середовища, у такий спосіб обмежуючи можливе поглинання води з навколишнього середовища. У випадку активного інгредієнта, такого як формотерол, добре відомо, що остання (наприклад, вологість) може бути шкідлива для стабільності активного інгредієнта під час зберігання. Тому також запропонований ДІ під тиском для введення фармацевтичних доз, який складається з контейнера з анодованого алюмінію, наповненого фармацевтичною композицією, що містить розчин формотерола фумарата в HFA 134а як пропелент, який у свою чергу містить 12% мас/мас, етанолу як співрозчинника і 1,0% мас./мас. ізопропілміристату як низьколетючего компонента, причому уявний рН зазначеного розчину відрегульований між 3,0 і 3,5 за допомогою додавання невеликої кількості соляної кислоти. Вираження «% мас./мас.» означає масову процентну концентрацію компонента до загальної маси композиції. Можна припустити, що термін зберігання препарату, який поміщено в пристрій за винаходом, складе більше двох років при температурі холодильника (4 - 10°С) і три місяці при кімнатній температурі. Фахівець у даній галузі техніки може легко застосувати теорію за цим винаходом для отримання препаратів у виді HFA розчинів, які містять інші активні інгредієнти, що несуть функціональні групи, чуттєві до гідролітичних і/або окисних реакцій, такі як формамід і катехол відповідно. WO 97/47286, ЕР 513127, ЕР 504112, WO 93/11747, WO 94/21228, WO 94/21229, WO 96/18384, WO 96/19198, WO 96/19968, WO 98/05302, WO 98/34595 І WO 00/07567 описують HFA препарати у виді суспензій, у яких р2-агоністи, такі як формотерол і сальбутамол, або наведені як приклади, і/або заявлені. WO 99/65464 стосується HFA препаратів, які містять два або більш ніж два активних інгредієнти, у яких щонайменше один знаходиться в суспензії. Бажані препарати містять сальбутамола сульфат у суспензії. У WO 98/34596 заявник описав композиції у виді розчинів для застосування в аерозольному інгаляторі, які включають активну речовину, пропелент, який містить гідрофторалкан (HFA), співрозчинник і, крім того, включають низьколетючий компонент для збільшення масового серединного аеродинамічного діаметра (MMAD) аерозольних часток при натисканні на інгалятор. Зазначена заявка не стосується технічних проблем хімічної стабільності активного інгредієнта, але в значній мірі стосується доставки лікарського засобу в легені. У міжнародній заявці № РСТ/ЕР99/09002, поданої 23/11/99, заявник описує ДІ під тиском для дозування розчину активного інгредієнта в гідрофторвуглероднім пропеленті, співрозчинника і можливо низьколетючего компонента, який відрізняється тим, що вся внутрішня поверхня або її частина зазначених інгаляторів складається з нержавіючої сталі, анодованого алюмінію або футерована інертним органічним покриттям. Приклади стосуються лише стероїдів і антихолінергічних агентів, і не представлені ніякі підкислені розчини. Як показано в прикладі 1 цієї заявки, застосування контейнерів з покриттям навіть у присутності органічної кислоти недостатньо для забезпечення стабільних препаратів похідного фенілалкіламінів, такого як сальбутамол, у виді розчинів. ЕР 673240 пропонує застосування кислот як стабілізаторів, що запобігають хімічній деструкції активного інгредієнта в аерозольних препаратах у виді розчинів, що мають HFAs. Більшість прикладів стосується іпратропію броміду, антіхолінергічному лікарському засобу, і тільки один приклад представлений для b 2агоніста, тобто фенотерола. Ніяких прикладів препаратів для сальбутамола не запропоновано. З даних, наведених у прикладі 1 цієї заявки, очевидно, що сальбутамол взагалі не може бути стабілізований за допомогою додавання органічних кислот, навіть коли зберігається в балонах з покриттям. Більш того, крім іпратропії броміду в ЕР 673240 не дано ніякого розпорядження стосовно кількості кислоти, яку потрібно додавати, для . того щоб стабілізувати ліки, не ставлячи під загрозу стабільність усієї композиції в балоні. Єдину вказівку можна знайти на сторінці 5, рядка з 15 по 16, де сказано, що треба додавати деяку кількість неорганічної кислоти, щоб отримати значення рН у межах від 1 до 7, у такій дуже широкій і загальній області. WO 98/34596 стосується препаратів у виді розчинів, що містять пропелент і фізіологічно прийнятний полімер, що сприяє розчиненню і стабільності, а також активний інгредієнт. WO 00/06121 стосується сумішей пропелентів закису азоту і гідрофторалкана при отриманні аерозолей у виді суспензій і розчинів. Використання закису азоту може підвищити стабільність при збереженні чуттєвих до окислювання активних інгредієнтів. Що стосується Рг-агоніста, такого як левосальбутамола сульфат, формотерола фумарат і сальметерола ксинафоат, повідомлялося тільки про приклади, що відносяться до суспензій. У WO 99/65460 заявлені ДІ під тиском, що містять стабільні препарати β2- -агоністичного лікарського засобу в суспензії або розчині. Приклади стосуються розчинів формотерола фумарата, що містять HFA пропеллент і етанол як співрозчинник, які поміщається в стандартні скляні балони, покриті алюмінієм або пластиком. Зразки, що зберігаються в прискорених умовах (40°С, 75% відносної вологості) протягом дуже короткого періоду часу в один місяць, демонстрували близько 10% втрати лікарського засобу. Відповідно до фармацевтичних норм стабільності, втрата 10% активного інгредієнта не відповідає критеріям прийнятності. Більш того, як випливає з даних, представлених у прикладі 2 цієї заявки, дотримуючись вказівок WO 99/65460, не можна забезпечити стабільні препарати у виді розчинів формотерола. Заявник дійсно продемонстрував, що присутність низьколетючих компонентів істотно не впливає на хімічну стабільність композицій. У деяких випадках вони можуть навіть підвищувати її. Згідно ще одному аспектові винаходу запропонований спосіб заповнення аерозольного інгалятора композицією за винаходом, при якому: а) Готують розчин одного або більш ніж одного активного інгредієнта в одному або більш ніж одному співрозчиннику, можливо таким що містить відповідну кількість низьколетючего компонента. б) Заповнюють пристрій зазначеним розчином. в) Додають раніше визначену кількість сильної неорганічної кислоти. г) Додають пропеллент, який містить гідрофторалкан (HFA). д) Завальцовують клапани і проводять газування. Активними інгредієнтами, які можна застосовувати в аерозольних композиціях за винаходом, є b2адренергичні агоністи короткої і тривалої дії, такі як сальбутамол формотерол, сальметерол, ТА 2005, їхні солі і їхні комбінації зі стероїдами, такими як беклометазона діпропіонат, флутиказона пропіонат, будезонід та його 22R-eпiмep. Можна використовувати інші лікарські засоби групи амінів, які несуть функціональні групи, чуттєві до окисних і/або гідролітичних реакцій. Бажано композиція буде утримуватися в балонах з анодованого алюмінію. Можна також використовувати підходящий пристрій з покриттям. Дозуючі клапани, постачені прокладками, зробленими з каучуків на . хлоропреновій основі, можна бажано використовувати для зменшення попадання вологи, яка, як згадано вище, може несприятливо впливати на стабільність лікарського засобу під час зберігання. Можливо, додатковий захист може бути забезпечений за допомогою упакування продукту в герметичний алюмінієвий пакет. Гідрофторвуглеродний пропелент бажано вибраний із групи HFA 134a, HFA 227 і їхніх сумішей. Співрозчинник звичайно є спиртом, бажано етанол. Низьколетючий компонент, коли він присутній, має тиск пар при 25°С нижче ніж 0,1 кПа, бажано нижче ніж 0,05 кПа. Він може бути вибраний із групи гліколей, особливо пропіленгліколя, поліетиленгліколя і гліцерину, складних ефірів, наприклад, аскорбілпальмітата, ізопропілміристата та ефірів токоферолу. Композиції за винаходом можуть містити від 0,2 до 10% мас/мас, зазначеного низьколетючего компонента, бажано між 0,5 і 2,0% мас./мас. Пропіленгліколь, поліетиленгліколь, гліцерин і складні ефіри є бажаними низьколетючими компонентами. Функція низьколетючого компоненту полягає в тому, щоб регулювати MMAD (масовий серединноаеродинамічний діаметр) часток аерозолю, і бажано в тім, щоб додатково підвищувати стабільність препарату. Стосовно останнього аспекту, найбільш бажаним є застосування ізопропілміристата. Область уявного рН бажано знаходиться в межах між 2,5 і 5,0, бажано між 3,0 і 4,5, навіть більш бажано між 3,0 і 3,5. Сильні неорганічні кислоти, такі як соляна, азотна, фосфорна, бажано використовуються для регулювання уявного рН. Кількість кислоти, яку додають для досягнення бажаного уявного рН, буде заздалегідь визначено в модельному носії, представленому раніше, і буде залежати від виду і концентрації активного інгредієнта. У випадку формотерола, варто бажано додавати кількість 1,0 Μ соляної кислоти, що знаходиться в межах між 3 і 3,5 мкл. Нижченаведені приклади ілюструють винахід. Приклад 1 Стабільність розчину сальбутамол (100мкг на дозу) - HFA 134а як такого та у присутності різних органічних кислот Композиції, яка містять 24 мг сальбутамола (100мкг на дозу), 10-20% (мас./мас.) етанола в HFA 134а, які поміщені в лаковані епоксифенольною смолою балони по 12 мол, з додаванням або без додавання різних органічних кислот, зберігали при 40-50°С. Результати по стабільності, виражені у виді процентної концентрації залишкового лікарського засобу, визначені за допомогою ВЕЖХ, представлені в таблиці 1. Таблиця 1 % САЛЬБУТАМОЛА t = 42 дня t = 1,5 місяця при 4°3 69% 69-70% 70% Лимонна (0,41 мас/мас.) 40,0 Лимонна (0,02 мас/мас.) 55,1 49,6 73,8 Кислота Без кислоти Олеїнова Ксинафоева (Xinafoic) 30%-на оцтова кислота (0,4% мас/мас.) 30%-на оцтова кислота (0,14% мас/мас.) Результати показують, що додавання органічних кислот не підвищує стабільність сальбутамола, навіть коли використовують балони з покриттям. Приклад 2 Стабільність композицій сальбутамол (12мкг/100іикл) - HFA 134а в лакованих епоксифенольною смолою балонах Препарати у виді розчинів отримували за допомогою розчинення 1,44 мг формотерола фумарата в HFA 134а, у свою чергу утримуючому 15% мас./мас. етанола і 1,3% мас./мас. гліцерину. ДІ зберігали у вертикальному положенні в діапазоні 4-50°С протягом проміжку часу до 28 днів. Вміст формотерола визначали за допомогою ВЕЖХ, а відсоток залишкової концентрації підраховували відносно 12мкг на номінальну дозу, що впорскується. Відсоток залишкової концентрації формотерола представлений у таблиці 2. Похідні параметрів Ареніуса використовували для оцінки констант швидкості при температурі навколишнього середовища (18-25°С), і розчини зберігали в побутовому холодильнику (4-10°С); ці константи швидкості використовували для підрахунку прогнозованого терміну зберігання для 5% і 10% деструкції формотерола (таблиця 3). Підраховані дані про термін зберігання в Таблиці 3 показують, що формотерол не стабільний в цьому НРА-134а-етанол-гліцериновому носії. Таблиця 2 Дані швидкості деструкції розчинів формотерол - HFA 134а для ДІ (12мкг/100мкл). Носій: HFA 134а з 1,3% мас/мас, гліцерину, 15,0% мас/мас, етанола. Лаковані епоксифенольною смолою балони, що зберігаються у вертикальному положенні. Відсоток залишкової концентрації формотерола Час (дні) 50°С 43°С 40°С 25°С 4°С Початковий момент 99,7 99,7 99,7 99,7 99,7 2 92,5 4 87,2 89,4 6 80,6 7 89,0 10 74,9 12 72,1 79,4 14 67,0 81,7 92,0 16 64,4 75,7 18 59,5 20 59,5 74,5 24 54,6 68,6 28 47,2 63,3 71,3 86,6 96,7 0,995 0,989 0,993 0,997 2,53 1,49 1,17 0,51 0,11 r Константа швидкості -1 2 (день х 10 ) Параметри кривої Ареніуса: К = AeE/RT A = 2,28 х 106 днів-1; Ε = 49,4 кдж х моль -1; r = 0,9985 Таблиця 3 Дані про прогнозований термін зберігання для розчинів формотерол - HFA 134а для ДІ (12мкг/100мкл). Носій: HFA 134а з 1,3% мас/мас, гліцерину, 15,0% мас/мас, етанола. Лаковані епоксифенольною смолою балони, що зберігаються у вертикальному положенні. Термін зберігання (дні) Температура Константа швидкості (день -1 х 103) T10% 4°С 1,10 T5% 95 47 10°С 1,74 60 29 20°С 3,51 30 15 25°С 4,93 21 10 Приклад 3 Вплив соляної кислоти на рН' розчину (функцію кислотності) а) 1,0 Μ соляну кислоту додавали по зростаючий до 50 мол HFA 43 - 10МЕЕ (Vertel XF), що містить 20% мас./мас. етанола, і вимірювали рН' після додавання кожної аліквоти кислоти. Фігура 1 показує підсумкову криву титрування, нормовану на звичайний об'єм заповнення балона ДІ (12мол). Профіль рН' виявляє невелике відхилення до приблизно рН' = 5,5; відповідно, функція кислотності різко знижується. б) Експеримент (а) повторювали з препаратами формотерола, який містять більш низьку концентрацію етанола (12% мас./мас.), і з додаванням 1,0% ізопропілміристату. Підсумковий профіль рН для основної маси додаткових розчинів, представлений на Фігурі 2, подібний за формою з різким падінням рН' на одиничний приріст кислоти, яке знову починається приблизно при рН' = 5,5. Однак, потрібно тільки лише приблизно половина кислоти для досягнення такого ж зниження рН'. Це пояснюється головним чином зниженням вмісту етанола; Фігура 2 також показує подібність у профілях, отриманих з ізопропілміристату або без нього. Приклад 4 Вплив рН' на стабільність розчинів формотерола в HFA 43-1ОМЕЕ, які містять 20% мас/мас, етанола Аліквоти 1,0 Μ соляної кислоти додавали до 12 мол розчину формотерола в скляних флаконах. Після виміру рН клапани завальцовували, і флакони зберігали у вертикальному положенні при 50°С. Зразки з флаконів, які містять різні концентрації кислоти, аналізували на залишковий формотерол після 10 і 20 днів зберігання. рН' третього флакона визначали після 40 днів зберігання. Результати представлені в Таблиці 4. Таблиця 4 показує зміни рН при зберіганні; це можливо головним чином пов'язано з вимиванням лугу з легкоплавкого скла флаконів. Однак, загальний аналіз рН' і дані по вмісту формотерола означають, що стабільність препарату у виді розчину лікарського засобу в HFA можна підвищити за допомогою додавання неорганічної кислоти для забезпечення препарату зі значенням рН' між 2,5 - 5,0. Таблиця 4 рН1 і вміст формотерола в розчинах формотерол-Vertrel XF/HFA (12 мкг/100 мкл). Носій: Vertrel XF/HFA з 20% етанола і соляної кислоти. Скляні флакони St Gobain, що зберігаються у вертикальному положенні. Функція кислотності (рН') Відсоток залишкової концентрації формотерола Початкова 40 днів Початковий 10 днів 20 днів 1,8 2,8 100 4,8 Відомостей немає 2,1 4,4 100 75,1 70,7 2,6 4,2 100 97,2 86,7 3,3 4,2 100 97,1 89,9 5,6 6,6 100 95,8 92,1 7,4 6,7 100 85,4 67,2 Приклад 5 Стабільність підкислених розчинів формотерол - HFA 134а в анодованих балонах Препарати формотерола (12 мкг/100 мкл) отримували за допомогою розчинення 1,44 мг формотерола фумарата в HFA 134а, який містить 12% мас/мас, етанола, з 1,0% мас/мас, ізопропілміристата і без нього. Останній включали як нелетучий ексципіент з можливістю збільшення MMAD, якщо таке необхідно. Він також підвищує стабільність формотерола в носії і зменшує полярність носія в порівнянні з додаванням гліцерину. Балони ДІ, які містять 3,1-3,4 мкл 1,0 Μ соляної кислоти, поміщали на зберігання у вертикальному положенні і нагору дном при температурі від 4°С до 50°С, і зразки брали на аналіз вмісту формотерола з відповідними інтервалами. Дані по стабільності, отримані після 70 днів зберігання, приведені в Таблиці 5. Матрицю препаратів, що містять 1,44 мг (12 мкг/100 мкл) формотерола фумарата отримували в HFA 134а, що містить 12% мас/мас, етанола з 1,0% мас/мас, ізопропілміристату як нелетучого ексципіента або без нього. Аліквоти концентрату лікарського засобу переносили в анодовані балони, і додавали 3,15-3,35 мкл 1,0 Μ соляної кислоти перед завальцюванням клапанів на 50 мкл і газуванням; отримували від 22 до 28 повторів при кожній концентрації кислоти. Для того, щоб визначити залишковий формотерол, 30x50 мкл впорскувань випускали в трубки DUSA. Очікували, що обраний діапазон кислоти дасть значення рН' 3,0-3,5 і визначить чутливість препарату до невеликих змін концентрації кислоти. Балони поміщали на зберігання у вертикальному положенні і нагору дном (клапаном нагору і униз відповідно) при 25 - 50°С. Таблиця 5 представляє результати, отримані при 40°С і 50°С після 11 - 40 днів зберігання. Кожне значення (виражене як відсоток номінальної концентрації лікарського засобу) отримували з нового балона. Вихідні значення отримували для двох балонів кожної концентрації кислоти. Перевірка даних показує, що всі значення проб знаходяться в межах відтворюваності аналізу ВЕЖХ і не залежать від концентрації кислоти. Подібний висновок був зроблений для повторів моментів часу зберігання, тобто вони теж не залежать від концентрації кислоти (3,2-3,3 мкл) або від того, чи зберігаються балони у вертикальному положенні або нагору дном. Тому для підрахунку кінетики використовували середнє значення для початкового (п = 10) і наступного моментів часу (n = 6). У Таблиці 6 представлені параметри Ареніуса разом з передбачуваними термінами зберігання при 4, 10 і 25°С. Очікується, що t5% складе більше 3 місяців при температурі навколишнього середовища і приблизно 2 роки при 4°С. Таблиця 5 Дані по стабільності розчинів формотерола фумарата (12 мкг/100 мкл) у HFA 134а, що містить 12% мас/мас, етанола (1,0% мас/мас, ізопропілміристата (значення виражені у вигляді номінального відсотка). Анодовані балони, які мають клапани по 50 мкл, по 30 доз на балон. Різні балони, оцінювані при кожній умові. Балони, що зберігаються у вертикальному положенні ("нагору дном). Умови зберігання/Без ізопропілміристата 1,0 Μ НСІ мкл на балон Початкові 40°С; 40 днів 50°С; 33 дня 50°С; 11 днів 1-й балон 2-й балон 1-й балон 2-й балон 1-й балон 2-й балон 1-й балон 2-й балон 3,15 99,8 99,6 3,20 100,8 99,7 96,0 93,2* 96,7 96,5 88,5 89,9* 3,25 97,9 98,8 93,9 94,3* 96,4 96,5 92,2 91,5* 3,30 97,3 98,9 93,7 93,7* 97,0 89,1 90,9 92,8* 3,35 100,0 98,3 Середнє значення C.V. (коефіцієнт мінливості) 99,1 94,1 95,4 91 ,0 1,1% 1,0% 3,2% 1,6 І% 50 °С;: 31 днів Умови зберігання/1,0% ізопропілміристата Початкові 1,0 Μ НСІ мкл на балон 40 °3; 33 днів 50 °С; 11 днів 1-й 2-й 1-й 2-й 1-й 2-й 1-й 2-й балон балон балон балон балон балон балон балон 3,15 101,1 99,3 3,20 97,0 100,2 94,4 93,2* 93,8 93,6 90,6 92,7* 3,25 101,4 100,2 98,6 95,0* 96,1 95,9 91,6 89,7* 3,30 99,9 100,8 92,8 95,3* 95,6 95,7 90,0 89,6* 3,35 99,2 97,2 Середнє значення C.V. (коефіцієнт мінливості) 99,6 ,6 94,9 95,1 90,7 1,5% >% 2,2% 1,2% 1,4% Таблиця 6 Прогнозування термінів зберігання для підкисленого розчину формотерола фумарата (12 мкг/100 мкл) у HFA 134а, що містить 12% мас/мас, етанола ( 1,0% мас/мас, ізопропілміристата (ІРМ). Анодовані алюмінієві балони. Час (дні) Формотерола фумарат (номінальний відсоток) Без ІРМ 1% ІРМ Без ІРМ 1% ІРМ 0 99,1 99,6 99,1 99,6 11 95,4 95,1 31 90,7 33 91,0 94,9 40 94,1 Константа швидкості (день -1 х 103) 2,52 2,94 1,29 1,46 Фактор частоти (день -1) Параметри Ареніуса Енергія активації (кДж х мол-1) Без ІРМ 3,19 х 106 56,3 1% мас./мас. ІРМ 9,63 x 106 58,9 Без ІРМ Температура Константа швидкость (день -1) 1% масс./мас. ІРМ T10% t5% (дні) Константа швидкості (день -1) T10% t5% (дні) 4°С 7,8 х 10-5 1344 657 7,8 x 10-5 1360 664 10°С 1,3 х 10-4 802 392 1,3 х 10-4 789 386 25°С 4,4 х10-4 240 117 4,4 x 10-4 225 110
ДивитисяДодаткова інформація
Назва патенту англійськоюAerosol solution composition containing beta-2 adrenergic agonist of prolonged action, dosing pressurized inhaler and method for its filling
Автори англійськоюBrambilla Gaetano, Ferraris Alessandra
Назва патенту російськоюАэрозольная композиция, содержащая в2-адренэргический агонист длительного действия, дозирующий ингалятор под давлением и способ его заполнения
Автори російськоюБрамбилла Гаэтано, Феррарис Алессандра
МПК / Мітки
МПК: A61K 31/135, A61K 9/72, A61K 9/12
Мітки: композиція, містить, дозуючий, дії, спосіб, заповнення, тривалої, b2-адренергічний, агоніст, аерозольна, тиском, інгалятор
Код посилання
<a href="https://ua.patents.su/8-73986-aerozolna-kompoziciya-shho-mistit-b2-adrenergichnijj-agonist-trivalo-di-dozuyuchijj-ingalyator-pid-tiskom-ta-sposib-jjogo-zapovnennya.html" target="_blank" rel="follow" title="База патентів України">Аерозольна композиція, що містить b2-адренергічний агоніст тривалої дії, дозуючий інгалятор під тиском та спосіб його заповнення</a>
Попередній патент: Кришка, що повторно закривається і що легко відкривається, і банка (варіанти)
Наступний патент: Колісний хід борони дискової важкої
Випадковий патент: Дзеркально-щілинний світильник на основі над'яскравих світлодіодів